Предлагаемый способ относится к области медико-биологических наук (патофизиология, интенсивная терапия, эндокринология) и может быть использован для оценки активности липолиза, а также интенсивности катаболических процессов в организме у пациентов.
Многие патологические состояния сопровождаются истощением функциональных резервов организма в связи с ростом катаболических реакций, в число которых входит активация липолиза в жировых депо. Количественная оценка активности липолиза позволяет косвенно судить об интенсивности катаболических процессов в организме у пациентов, что необходимо для определения объема нутритивной поддержки. Примерами заболеваний, связанных с повышенным липолизом, являются сахарный диабет 1 типа и синдром полиорганной недостаточности (СПОН) [1, 2].
Существующие методы оценки активности липолиза основаны на определении веществ, содержание которых в кровотоке или образование в организме повышается при интенсификации липолиза.
Предложен способ определения активности липолиза в организме [3] путем измерения содержания продуктов липолиза при котором в качестве биологической пробы используют выдыхаемый воздух, регистрируют содержание ацетона, для чего пробу отбирают в камеру с размещенным в ней чувствительным к ацетону полупроводниковым резистором, нагретым до 495-505°С, измеряют электропроводность резистора, а активность липолиза рассчитывают по формуле:
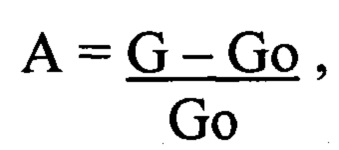
где G - электропроводность резистора в исследуемой пробе;
Go - величина, равная Cr+(0,1-0,3) Cr, где Cr - электропроводность резистора в стандартной атмосфере.
Недостатком данного способа является то, что для его применения нужно специально изготавливаемое оборудование. Кроме того, на величину образования ацетона существенно влияет не только интенсивность липолиза, но также уровень инсулина и глюкозы в крови [1]. Поэтому предложенный способ не может использоваться для оценки липолиза при различных по патофизиологическим механизмам заболеваниях, таких как сахарный диабет и СПОН.
Известен также метод, основанный на измерении концентрации меченых радиоактивными [4] или стабильными [5] изотопами жирных кислот или глицерина, высвобождающихся в процессе липолиза. Его недостатками являются необходимость наличия высокотехнологичного и дорогостоящего оборудования, большая техническая сложность, трудоемкость и длительность исследования, ионизационное воздействие на организм при использовании радиоизотопов. В связи с этим метод применяется лишь для решения научных задач.
На сегодняшний день наиболее широко применяемым методом оценки активности липолитических процессов является определение концентрации свободных жирных кислот в плазме крови. При этом чаще всего используют метод фотометрического измерения оптической плотности окрашенного раствора, образующегося в ходе ряда ферментативных реакций с участием свободных жирных кислот. Оптическая плотность образующегося раствора пропорциональна концентрации свободных жирных кислот в образце крови.
Недостатками данного метода является высокая стоимость наборов реагентов и стандартов заводского изготовления и ограниченные сроки их хранения. Точность метода снижается при повышенном содержании в крови ряда веществ (билирубин, липиды, гемоглобин). Наличие в образцах липазной активности может приводить к завышению истинной концентрации свободных жирных кислот. В связи, с чем рекомендуется проводить измерение сразу же после забора крови. Измерения приводят к недостоверным результатам при потере качества реагентов и изменении условий измерения, так как изменяется градуировочная зависимость между концентрацией свободных жирных кислот в образце и его оптической плотностью после образования окрашенного соединения [6, 7, 8].
В качестве прототипа выбран хроматографический анализ состава жирных кислот плазмы крови [11] по следующей методике: забор крови проводится натощак из периферической вены. Плазма крови отделяется от ее клеточного компонента путем центрифугирования. Затем из фиксированных объемов плазмы путем кислотного этанолиза с последующей экстракцией гексаном получают растворы производных жирных кислот. Далее жирные кислоты, присутствующие в виде этиловых эфиров в экстракте, анализируются методом капиллярной газо-жидкостной хроматографии. Определения состава жирных кислот проводятся на хроматографах ГХ-1000 и ЦВЕТ-800 (РФ). Идентификация жирных кислот осуществляется с помощью метода хромато-масс-спектрометрии с использованием прибора Thermo Scientific DSQ II (США).
При этом необходимо отметить, что определение свободных жирных кислот плазмы крови не в полной мере подходит для объективной оценки активности липолиза, так как их концентрация в плазме крови динамично изменяется под действием эмоциональных, диетических, гормональных факторов. Кроме того, свободные жирные кислоты, поступающие в кровоток, в результате липолиза, быстро захватываются клетками печени и реэтерифицируется с образованием триглицеридов [2, 5, 8, 9].
Для устранения указанных недостатков нами предложено определять долю мононенасыщенных жирных кислот (пальмитолеиновой и олеиновой жирных кислот) в общей сумме жирных кислот плазмы крови, так как эти кислоты количественно преобладают в жировой ткани и в большем количестве, нежели иные жирные кислоты поступают в кровоток при липолизе. В результате чего их процентное содержание в липидах плазмы крови возрастает [9, 10].
Технической задачей, для решения которой направлено настоящее изобретение является создание способа оценки активности липолиза по составу жирных кислот плазмы крови, что позволит повысить объективность оценки, производить измерения с высокой точностью и экономичностью, а также может применяться у пациентов с любой патологией и не требует специально изготавливаемого оборудования.
Указанная задача достигается тем, что в способе оценки активности липолиза по составу жирных кислот плазмы крови у пациента хроматографически определяют состав жирных кислот плазмы крови и, согласно изобретению, в данном составе измеряют суммарную долю пальмитолеиновой и олеиновой жирных кислот и при ее увеличении более 21,1% устанавливают повышенный уровень липолиза.
Для решения поставленной задачи проведено исследование состава жирных кислот плазмы крови 19 пациентов отделения анестезиологии и реанимации с наличием СПОН (37,6±8,3 лет). Контролем служила плазма крови 17 практически здоровых взрослых людей (38,4±3,3 лет). Критерии СПОН у пациентов устанавливали в соответствии с согласительной конференцией SCCM/ACCP 2016 г. и включали два или более баллов по шкале SOFA. Также было проведен анализ состава жирных кислот плазмы крови у 16 подростков с декомпенсированым сахарным диабетом 1 типа (14,5±1,28 лет) и 10 практически здоровых школьников (16,8±1,1 лет). Определение доли отдельных жирных кислот производилось методом внутренней нормализации при помощи системы регистрации спектрометрической информации Unichrom-97.
Полученные данные представлены в виде средних для сравниваемых групп и соответствующих значений доверительного интервала с доверительной вероятностью 95%. Оценка статистической значимости различий между выборками осуществлялась с использованием U-критерия Манна-Уитни. Изменения считались значимыми при р<0,05. Определяли точность метода (ее отражает площадь под кривой AUROC), чувствительность и специфичность.
В ходе работы обнаружено, что в сравнении со здоровыми школьниками у подростков с декомпенсированным сахарным диабетом 1 типа доля мононенасыщенных жирных кислот возрастает с 17,92±2,44% до 21,74±1,04% (р<0,001). Также если у здоровых взрослых доля мононенасыщенных жирных кислот составляет в плазме крови 18,10±1,36%, то соответствующее значение у пациентов СПОН составляет 27,71±2,32% (р<0,001).
Произведено построение и анализ характеристической кривой для разработанного нами способа. Установлено, что площадь под кривой AUROC составляет 0,915 при 95% доверительном интервале от 0,844 до 0,987 (р<0,0001), чувствительность 82,9%, специфичность 92,6%, оптимальный порог суммарной доли пальмитолеиновой и олеиновой жирных кислот 21,1%.
Предложенный способ позволяет повысить объективность оценки активности липолиза при патологии, производить измерения с высокой точностью, не требует специально изготавливаемого оборудования, является малозатратным, безопасен для обследуемых пациентов, может применяться у пациентов независимо от патологии.
Использование данного способа подтверждается конкретными примерами:
Пример 1.
Здоровый подросток Н., 15 лет. При анализе состава жирных кислот плазмы крови доля мононенасыщенных жирных кислот составила 16,3%. Заключение: активность липолиза в норме.
Пример 2.
Подросток пациент К., 16 лет. Клинический диагноз: сахарный диабет, 1 тип, состояние клинико-метаболической декомпенсации. Диабетическая нефропатия. Диабетическая полинейропатия. При анализе состава жирных кислот плазмы крови доля мононенасыщенных жирных кислот составила 22,5%. Заключение: активность липолиза повышена.
Пример 3.
Здоровый взрослый А., 39 лет. При анализе состава жирных кислот плазмы крови доля мононенасыщенных жирных кислот составила 18,2%. Заключение: активность липолиза в норме.
Пример 4.
Взрослый пациент К., 61 год. Клинический диагноз: Фибринозно-гнойный перитонит. Синдром полиорганной недостаточности. При анализе состава жирных кислот плазмы крови доля мононенасыщенных жирных кислот составила 33,7%. Заключение: активность липолиза повышена.
Источники информации:
1. Патофизиология углеводного обмена. Сахарный диабет / сост. Ю. В. Шарпань, Н.Л. Богуш; под ред. Г.В. Порядина, Ж.М. Салмаси. - М.: ИНФРА-М, 2013.-38 с.
2. Саенко, В.Ф. Сепсис и полиорганная недостаточность. Монография / В.Ф. Саенко, В.И. Десятерик, Т.А. Перцева, В.В. Шаповалюк. - Кривой Рог: Минерал, 2005. - 466 с.
3. Патент 1735785 Союза Советских Социалистических Республик, МПК G01N 33/92, опубликовано: 23.05.1992. Способ определения активности липолиза в организме / Ляшенко В.А., Коляденко В.Г. Земсков В.С, Храпач В.В., Боднар П.Н., Белецкий В.И.; Патентообладатель: Киевский медицинский институт им. акад. А.А. Богомольца - №4776967/14, заявл. 02.01.1990 // Бюллетень изобретения №19/1992.
4. Sidney, S. Instrumental methods of organic functional group analysis / S. Sidney - New York: Wiley-Interscience, 1972. - 428 p.
5. Magkos, F. Stable isotope-labeled tracers for the investigation of fatty acid and triglyceride metabolism in humans in vivo / F. Magkos, B. Mittendorfer // Clin. Lipidol. - 2009. - Vol. 4, №2. - P. 215-230.
6. Камышников, B.C. Клинико-биохимическая лабораторная диагностика: Справочник: в 2 т./ B.C. Камышников. - 2-е изд. - Мн.: Интерпрессервис, 2003. - Т. 1. - 495 с.
7. Лабораторные методы исследования в клинике: справочник / В.В. Меньшиков, Л.Н. Делекторская, Р.П. Золотницкая и др.; под ред. В.В. Меньшикова. - М.: Медицина, 1987. - 368 с.
8. Diagnostic reagent for quantitative in vitro determination of non-esterified fatty acids (NEFA) in serum or plasma on photometric systems: Reagent information. October 2016 [Electronic resource]. - Holzheim, Germany: DiaSys Diagnostic Systems, 2007. - Mode of access: https://vvww.diasys-diagnostics.com/misc/download/?_=1464860879&tx_vierwddiasysproducts_down load[file]=downloads%2FPackage%20inserts%20reagents%20general%2FNEFA%2FPI-e-NEFA-11.pdf&tx_vierwddiasysproducts_download[msds]=&cHash=7340537a19c4716719874be4703e4d58. - Date of access: 15.08.2019.
9. Insulin response and changes in composition of non-esterified fatty acids in blood plasma of middle-aged men following isoenergetic fatty and carbohydrate breakfasts / D.L. Frape [et al.] // Br. J. Nutr. - 2000. - Vol.84, №5. - P. 737-745.
10. Fatty acid composition of adipose tissue in humans: differences between subcutaneous sites / G.T. Malcom [et al.] // Am. J. Clin. Nutr. - 1989. - Vol. 50, №2.-P. 288-291.
11. Кейтс, M. Техника липидологии. Выделение, анализ и идентификация липидов: пер. с англ. / М. Кейтс.- М.: «Мир», 1975. - 322 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ диагностики инсулинорезистентности у больных сахарным диабетом 1 типа | 2024 |
|
RU2825046C1 |
| Рогалик с оптимизированным жирно-кислотным составом | 2019 |
|
RU2723621C1 |
| Способ включения в группу риска по развитию сахарного диабета типа 2 у больных хроническим пародонтитом | 2017 |
|
RU2671569C1 |
| ПОЛУЧЕНИЕ ЖИРНЫХ КИСЛОТ ИЗ ЛИЧИНОК НАСЕКОМЫХ | 2010 |
|
RU2505592C2 |
| ПИЩЕВОЙ ПРОДУКТ ДЛЯ ДИАБЕТИКОВ | 2005 |
|
RU2380983C2 |
| Способ профилактики дислипидемии | 2016 |
|
RU2621152C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ МЕТАБОЛИЗМА В ОРГАНИЗМЕ В УСЛОВИЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2010 |
|
RU2436101C1 |
| Способ дифференциальной диагностики стеатоза печени и неалкогольного стеатогепатита у мужчин | 2020 |
|
RU2753455C1 |
| Способ получения купажа растительных масел для женщин старше 75 лет с уровнем физической активности КФА-1,7 | 2023 |
|
RU2802942C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 2013 |
|
RU2545740C1 |
Изобретение относится к медицине и касается способа оценки активности липолиза по составу жирных кислот плазмы крови, при котором у пациента хроматографически определяют состав жирных кислот плазмы крови, где в данном составе измеряют суммарную долю пальмитолеиновой и олеиновой жирных кислот в общей сумме жирных кислот и при ее увеличении более 21,1% устанавливают повышенный уровень липолиза. Изобретение обеспечивает повышение объективности оценки и точности измерения активности липолиза. 4 пр.
Способ оценки активности липолиза по составу жирных кислот плазмы крови, при котором у пациента хроматографически определяют состав жирных кислот плазмы крови, отличающийся тем, что в данном составе измеряют суммарную долю пальмитолеиновой и олеиновой жирных кислот в общей сумме жирных кислот и при ее увеличении более 21,1% устанавливают повышенный уровень липолиза.
| Способ определения активности липолиза в организме | 1990 |
|
SU1735785A1 |
| WO 2014143080 A1, 18.09.2014 | |||
| ОРЛОВА Т.И | |||
| Совершенствование двухстадийной методики хроматомасс-спектрометрического определения свободных и этерифицированных жирных кислот в биологических образцах | |||
| Дисс | |||
| на соиск | |||
| уч | |||
| ст | |||
| к.х.н | |||
| СПб., 2016 | |||
| FRAPE D.L | |||
| ET AL | |||
| Insulin response and changes in composition of non-esterified | |||
Авторы
Даты
2020-06-29—Публикация
2019-10-23—Подача