Изобретение относится к области медицины, в частности к стоматологии, и может быть использовано для стимуляции регенерации костной ткани челюстно-лицевой области при введении - биокомплекса в костные дефекты.
Дефекты костной ткани могут возникать после стоматологических оперативных вмешательств и их осложнений, а также в результате хронических деструктивных процессов.
Оптимизация процессов регенерации костной ткани в челюстно-лицевой области имеет ключевое значение, и актуальным остается поиск новых материалов, способствующих созданию наиболее оптимальных условий для формирования костной ткани после оперативных вмешательств в области челюсти.
Актуальным является поиск методов малоинвазивной, эффективной терапии процессов регенерации костных дефектов в челюстно-лицевой области. Таким методом на сегодняшний день является инъекционный метод с использованием плазмы, полученной из собственной крови пациента, - тромбоцитарной аутологичной плазмы (ТАП), являющейся высокоактивным биологическим стимулятором процессов регенерации за счет содержащихся в альфа гранулах тромбоцитов различных факторов роста, действующих на все структурные единицы окружающих тканей и стимулирующих процессы регенерации.
Перспективным для лечения различных видов костных дефектов является использование обогащенной тромбоцитами аутологичной плазмы в виде фибринового сгустка, содержащего большое количество хорошо изученных разнообразных факторов роста.
Причиной применения аутологичной плазмы с богатым содержанием тромбоцитов стало открытие того факта, что тромбоциты содержат белковые факторы (PRP-factors), инициализирующие клеточный регенеративный процесс.
Для получения ТАП используется собственная венозная кровь пациента, забор которой проводится по стандартной технологии в специальные оригинальные вакуумные пробирки Plasmolifting, содержащие антикоагулянт гепарин натрия высокой степени очистки и специальный разделительный гель, позволяющий проводить фильтрацию плазмы и фиксацию эритроцитарного сгустка. После забора крови пробирка помещается в центрифугу ЕВА 20 (Германия) и центрифугируется в режиме 3200 об/мин в течение 5 мин, в результате чего в каждой пробирке получается 3,05±1,5 мл тромбоцитарной плазмы, которая располагается в верхней части пробирки, затем идет разделительный гель, отделяющий эритроцитарный сгусток.
В результате проведенного патентно-информационного поиска были отобраны для последующего анализа следующие источники.
Известен композиционный материал для замещения костной ткани (Патент РФ 2122437), содержащий фосфаты кальция и биополимеры. Материал дополнительно содержит хондроитинсульфат (ХС), при этом в качестве фосфатов кальция используются гидроксилапатит кальция (ГА) в виде гранул с диаметром 1.5-2.0 мм и порошок бетатрикальций фосфата (ТКФ) с диаметром частиц не выше 50 мкм, в качестве биополимеров используются порошки хондроитинсульфата и коллагена с диаметром частиц, не превышающим 50 мкм, и 2% раствор коллагена в количестве 1 об.ч. раствора на 2 об.ч. смеси используемых порошков и гранул.
Известен способ направленной регенерации костной ткани при цистэктомии (РФ №2311181) с использованием остеопластического материала, содержащего 2% аскорбата хитозана с молекулярной массой 100÷700 кДа и степенью деацетилирования 95-98%, включающего в себя на 1 г сухого аскорбата хитозана 5÷100 мг хондроитинсерной кислоты, 10÷100 мг гиалуроновой кислоты, 2.5÷5 мг гепарина, 11÷220 мкг сывороточного фактора роста крупного рогатого скота, 4% альгината натрия в соотношении хитозан : альгинат натрия 1:1. Недостатком данного способа является недостаточная барьерная функция материалов, которая препятствовала бы прорастанию эпителия слизистой оболочки в область костного дефекта.
В патенте (Патент РФ 2653480), вместо твердого трансплантата использовали пастообразный композиционный остеопластический материал. В частности в композиции для стимуляции регенерации костной ткани челюстей, содержится гидроксид кальция, сульфат бария и нанокристаллический диоксид церия в изотоническом растворе. Соотношение компонентов в композиции составляет 40-42 мас. % гидроксида кальция; не менее 8 мас. % сульфата бария; 0,3-2 мас. % нанокристаллического диоксида церия; остальное до 100 мас. % - изотонический раствор. Недостатком предложенной композиции является отсутствие в ее составе биологически активных веществ, существенно ускоряющих процесс регенерации.
В качестве прототипа выбран материал для восстановления костных структур (патент РФ №2399387), который содержит обогащенную тромбоцитами аутоплазму пациента, порошок никелида титана с размерами частиц до 100 нм, коллоидное 2,5% наноструктурированное серебро с размерами частиц до 20 нм. Способ получения известного материала заключается в том, что кровь пациента центрифугируют, отделяют плазму от сгустка крови, выделенный сгусток гомогенизируют, добавляют к нему коллоидное наноструктурированное серебро, порошок никелида и полученную после центрифугирования плазму, затем компоненты смешивают с помощью ультразвука и получают однородную композицию зеленого цвета с перламутровым переливом, которую используют в течение 1-2 часов. Изобретение обеспечивает восстановление костной и соединительной ткани.
Перечисленные выше материалы обладают рядом недостатков:
- композиционные материалы устойчивы к резорбции, содержат соединения неясного состава и биологического воздействия;
- материалы не обеспечивают стабильности физико-химических условий в области раны, что делает возможным резкие изменения скорости и направления течения процессов резорбции и регенерации;
- не обеспечивают выраженного остеогенетического эффекта на ранних стадиях регенерации костной ткани.
При этом наименее травматичной методикой введения остеопластической комбинации является инъекционная. Кроме этого, она позволяет точнее дозировать вводимые препараты и осуществлять процесс аугментации альвеолярного отростка в несколько этапов. До настоящего времени такая методика не разработана в стоматологии, что позволяет говорить об актуальности возникающего технического решения.
Одной из причин замедления регенерации костной ткани является воздействие супероксидных радикалов и ферментов, разрушающих ее структурные компоненты. В качестве средства, предотвращающего воздействие таких негативных факторов, перспективным является использование нанокристаллического диоксида церия. Нанокристаллический диоксид церия - неорганический антиоксидант [Ivanov, V.K., Shcherbakov, А.В., Usatenko, A.V. Structure-sensitive properties and biomedical applications of nanodispersed cerium dioxide // Russian chemical reviews, 2009, 78(9), 855].
Предлагаемый биокомплекс для регенерации костной ткани челюсти может быть использован в хирургической стоматологии, клинике общей и челюстно-лицевой хирургии, а также в травматологии и ортопедии для восстановления пародонтальных дефектов, десневой рецессии, а также при заполнении двух- или многостеночных внутрикостных дефектов, альвеолярной регенерации, аугментации верхнечелюстного синуса.
Технической задачей изобретения является использование аутоплазмы пациента, обогащенной тромбоцитами, содержащей нанодисперсный диоксид церия.
Технический результат полученный от использования предлагаемого биокомплекса: сокращения сроков восстановления целостности костных структур (микроархитектоники костной ткани челюстей) за счет оптимизации репаративного остеогенеза, создание композиции в виде геля, удобного для применения.
Технический результат достигается за счет использования биокомплекса для стимуляции регенерации костной ткани челюстно-лицевой области, содержащей обогащенную тромбоцитами аутоплазму пациента, наноструктурированный биостимулятор, наполнитель. При этом в качестве наноструктурированного биостимулятора используют нанокристаллический диоксид церия концентрации 1-5% в изотоническом растворе, дополнительно композиция содержит активатор ренампластин, при следующем соотношении компонентов, мас. %:
Сущность изобретения заключается в том, что в предложенном биокомплексе используют обогащенную тромбоцитами аутоплазму пациента для заполнения дефекта кости биологически активным материалом, насыщенной факторами дифференцировки и роста клеточного матрикса, а также нанодисперсный диоксид церия, введение которого способствует активизации практически всех внутриклеточных структур, энзимов и других факторов роста, имеющих дополнительные механизмы стимулирования остеогенеза и влияющих на внутриклеточный и внеклеточный метаболизм костной ткани. Такая комбинация факторов воздействия на различные механизмы регенерации создает эффект стимуляции регенерации и ускорения процесса созревания костной ткани, что приводит не только к сокращению сроков восстановления целостности кости при проведении хирургических вмешательств, но и полноценному восстановлению структуры костной ткани (микроархитектоники), как при замещении деструктивных дефектов костной ткани, так и при проведении направленной костной регенерации.
Наличие в биокомплексе нанокристаллического диоксида церия и обогащенной тромбоцитами плазмы крови обеспечивают улучшенную пролиферацию клеток, антибактериальный и противовирусный эффект, значительное улучшение терапевтического эффекта. Диоксид церия является уникальным неорганическим материалом, проявляющим высокую степень кислородной нестехиометрии в нанокристаллическом состоянии. В свою очередь, изменение кислородной нестехиометрии и частичное восстановление церия в поверхностном слое влечет за собой изменение электронных и электрофизических свойств нанодисперсного диоксида церия. Указанный эффект обусловливает уникальную биологическую активность этого материала. Перспективы и особенности его применения определяются двумя основными факторами: низкой токсичностью и высокой кислородной нестехиометрией. Первый фактор обеспечивает сравнительную безопасность применения наночастиц диоксида церия in vivo. Второй обусловливает активность нанодисперсного СеО2 в окислительно-восстановительных процессах в живой клетке, особенно при инактивировании активных форм кислорода. К специфическим свойствам СеО2 следует отнести и способность к регенерации кислородной нестехиометрии, которая выражается в том, что наночастицы диоксида церия после участия в окислительно-восстановительном процессе за сравнительно небольшой промежуток времени способны возвращаться к исходному состоянию, что обеспечивает возможность их многократного использования.
Специфическая способность нанокристаллического СеО2 к регенерации - крайне важное свойство данного материала. Традиционные антиоксиданты (аскорбиновая кислота, токоферол, метионин и пр.) способны участвовать только в одном редокс-цикле, после чего инактивируются. CeO2 имеет преимущество перед существующими антиоксидантами, в ряде случаев и превосходит их по своей активности.
Антиоксидантная активность нанокристаллического СеО2 обеспечивает его способность оказывать защитное действие живых систем (к которым относится плазма крови) от активных форм кислорода (далее АФК), уровень которого в организме регулируют ферменты; в случае дисбаланса между продукцией АФК и концентрацией ферментов возникает окислительный стресс.
Так, наночастицы диоксида церия ускоряют заживление ран за счет снижения окислительного повреждения мембран и белков.
Заданное по настоящему изобретению количественное содержание диоксида церия оптимально по условиям блокирования свободных радикалов, пероксидов, образующихся при окислительных процессах в ранах. При уменьшении содержания данного компонента в составе снижается его активность по отношению к свободным радикалам, пероксидам.
Ренампластин - водносолевой экстракт высушенной ацетоном ткани головного мозга кролика, стабилизированный и лиофилизированный в присутствии хлорида кальция. Производителем, осуществляющим выпуск препарата «Ренампластин» является научно-производственное объединение «Ренам». Выбор этого препарата обусловлен тем, что его введение в обогащенную тромбоцитами плазму крови способствуют формированию фибринового сгустка, увеличивая тем самым вязкость полученной гелевой композиции. Границы используемых соотношений объемов плазмы крови и препарата выбраны из тех соображений, что использование большего соотношения приводит к уменьшению скорости формирования фибринового сгустка и его низкой плотности. В то же время использование меньшего соотношения приводит к снижению лечебного эффекта в связи с относительным уменьшением доли активных веществ в продукте.
Сущность изобретения поясняется приведенными ниже рисунками и примерами реализации заявляемых способов. Примеры иллюстрируют, но не ограничивают предложенные способы.
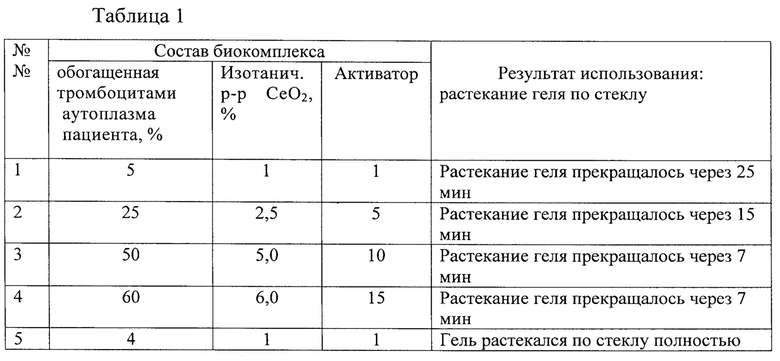
Фиг 1. Результаты морфологического исследования регенерации костной ткани а) композиция по прототипу на 15 сутки исследования, б) композиция по прототипу на 55 сутки исследования, в) предлагаемый биокомплекс, содержащий нанодисперсный диоксид церия на 15 сутки исследования г) предлагаемый биокомплекс, содержащий нанодисперсный диоксид церия, на 55 сутки исследования.
Таблица 1. Приведены составы предлагаемого биокомплекса в заявляемых интервалах. Полученный гель в количестве 5 мл капали на стекло и фиксировали в течение 2 минут время прекращения растекания.
Пример 1. Приготовление биокомплекса, обогащенной тромбоцитами аутоплазмы пациента
По известной методике осуществляли отбор 4 мл крови из боковой вены уха кролика при помощи шприца в пробирку, содержащую 3.8% цитрата натрия. Стабилизированную цитратом кровь центрифугировали при 1000 rpm 10 минут (центрифуга Eppendorf MiniSpin). После центрифугирования отделяли надосадочную фракцию и повторно ее центрифугировали при 1500 rpm 10 мин. После второго центрифугирования аккуратно удаляли плазму без тромбоцитов, получали 0.5 мл обогащенной тромбоцитами плазмы (далее ОТП). К 500 мкл ОТП добавляли 50 мкл нанодисперсный диоксид церия в изотоническом растворе с концентрацией (1-5)%, аккуратно перемешивали. Затем к полученному составу добавляли Ренампластин в качестве активатора в количестве (1-10)%. Формирование сгустка происходило в течение 1 минуты, его контракция еще в течение 1 минуты.
Пример 2 Биологические испытания
Эксперименты проводили на кроликах породы шиншилла. На правой стороне челюсти кролика в диастеме между резцами и молярами в отпрепарированное отверстие вводили композицию по прототипу, с левой стороны вводили полученную в соответствии с формулой изобретения предлагаемый биокомплекс, обогащенный нанодисперсным диоксидом церия и содержащий Ренампластин.
Для получения достоверных данных проводили комплексный морфометрический анализ на этапах регенерации костной ткани. Показано, что после регенерации костной ткани с использованием композиции по прототипу формируется очаг соединительной ткани более крупного размера с базофильными массами и мелкими фрагментами некротизированных костных балок (секвестрами). Последние сохраняются до 35-45 сут., причем на 45-е сут. на их месте остаются гранулемо-подобные структуры. Пик пролиферации остеобластов приходится на 25 - 35 сутки. К 45 суткам преобладают процессы остеосинтеза и ремоделирования костной ткани. На 55 сутки образуется костная ткань, близкая по строению к компактной кости кортикальной пластинки (рубец). Полученные результаты продемонстрированы на Фиг. 1а-б.
После регенерации костной ткани с использованием предлагаемого биокомплекса, обогащенную нанодисперсным диоксидом церия объем новообразованной соединительной ткани значительно меньше, костные секвестры и базофильный материал не встречаются. Раньше, уже с 15-х суток, отмечается выраженная пролиферация остеобластов, пик которой приходится на 15-25 сутки, но она растягивается до 45 суток. Процессы остеосинтеза и ремоделирования костной ткани не завершаются к 55 суткам. В итоге образуются участки кости по строению близкие как к компактной, так и губчатой костной ткани (полноценная морфологическая регенерация костной ткани). Полученные результаты продемонстрированы на Фиг. 1в-г, Таким образом, предложенный способ позволяет получить обогащенный тромбоцитами фибриновый сгусток, который способствует пролонгированию регенеративных процессов в костной ткани и формированию морфологически идентичной костной ткани вне поражения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ регенерации костной ткани челюстей | 2019 |
|
RU2709723C1 |
| Нанодисперсная пластическая биоинженерная композиция на основе диоксида церия для восполнения объема костной ткани | 2021 |
|
RU2793324C1 |
| Тканеинженерная конструкция для восполнения объема костной ткани челюстно-лицевой области | 2019 |
|
RU2729365C1 |
| Биокомплекс для стимуляции регенерации и ремоделирования тканей | 2021 |
|
RU2794464C1 |
| СПОСОБ РЕГЕНЕРАЦИИ КОСТНОГО ДЕФЕКТА ЧЕЛЮСТЕЙ В ЭКСПЕРИМЕНТЕ | 2023 |
|
RU2836678C1 |
| Композиция для стимуляции регенерации при дефектах костной ткани челюстей | 2017 |
|
RU2653480C1 |
| Тканебиоинженерная конструкция для восполнения объема костной ткани челюстных костей | 2022 |
|
RU2809154C1 |
| Нанодисперсный керамический биодеградируемый материал для замещения дефектов костной ткани челюстей | 2022 |
|
RU2824854C2 |
| Способ лечения хронических периодонтитов с применением технологии трансканальной лазерной беспигментной фотоабляции | 2021 |
|
RU2753794C1 |
| ЛАЗЕРНЫЙ ИМПУЛЬСНЫЙ МОДУЛЬ ДЛЯ КОМПЛЕКСНОЙ ТЕРАПИИ, ГИПЕРТЕРМИИ И ХИРУРГИИ ЗАБОЛЕВАНИЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ (ВАРИАНТ) | 2016 |
|
RU2635773C1 |
Изобретение относится к области медицины, в частности к стоматологии, и может быть использовано для стимуляции регенерации костной ткани в челюстно-лицевой области при введении предложенной композиции в дефекты костной ткани. Биокомплекс для стимуляции восстановления микроархитектоники костной ткани челюстно-лицевой области содержит обогащенную тромбоцитами аутоплазму пациента, наноструктурированный биостимулятор, наполнитель и активатор Ренампластин, причем в качестве наноструктурированного биостимулятора используют нанокристаллический диоксид церия, при следующем соотношении компонентов, мас. %: обогащенная тромбоцитами аутоплазма - 5-50; нанокристаллический диоксид церия - 1-5; активатор - 1-10; изотонический раствор - остальное до 100%. Изобретение обеспечивает сокращение сроков восстановления целостности костных структур за счет оптимизации репаративного остеогенеза, а также повышение удобства применения биокомплекса за счет создания композиции в виде геля, удобного для применения. 1 ил., 1 табл., 2 пр.
Биокомплекс для стимуляции восстановления микроархитектоники костной ткани челюстно-лицевой области, содержащий обогащенную тромбоцитами аутоплазму пациента, наноструктурированный биостимулятор, наполнитель, отличающийся тем, что в качестве наноструктурированного биостимулятора используют нанокристаллический диоксид церия, дополнительно биокомплекс содержит активатор Ренампластин, при следующем соотношении компонентов, мас.%:
| МАТЕРИАЛ ДЛЯ ИМПЛАНТАЦИИ И ПЛАСТИКИ ПАРОДОНТА И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2008 |
|
RU2399387C2 |
| Композиция для стимуляции регенерации при дефектах костной ткани челюстей | 2017 |
|
RU2653480C1 |
| СПОСОБ АУГМЕНТАЦИИ АЛЬВЕОЛЯРНОГО ОТРОСТКА ПУТЕМ ИНЪЕКЦИОННОГО ПОДНАДКОСТНИЧНОГО ВВЕДЕНИЯ ОСТЕОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ | 2014 |
|
RU2574115C1 |
| US 9427469 B2, 30.08.2016 | |||
| WO 2019076484 A1, 25.04.2019 | |||
| ЩЕРБАКОВ А.Б., ЖОЛОБАК Н.М | |||
| и др | |||
| Наноматериалы на основе диоксида церия: свойства и перспективы использования в биологии и медицине | |||
| Biotechnologia Acta, т.4, N1, 2011, с.9-28 | |||
| АЧКАСОВ Е.Е., БЕЗУГЛОВ Э.Н | |||
| и | |||
Авторы
Даты
2020-07-15—Публикация
2019-05-21—Подача