Изобретение относится к каталитическим методам обезвреживания дымовых газов электростанций и, более конкретно, к катализаторам для удаления оксидов серы из дымовых газов электростанций. Помимо природного газа, электростанции широко используют в качестве топлива мазут и каменные угли. Общее содержание сернистых соединений в негидроочищенном мазуте достигает 2-4%, в Донецком и Ростовском антрацитах - 2-6%, а в каменных углях Кузнецкого и Канско-Ачинского бассейнов - до 0.6%. При сжигании сера переходит в сернистый (SO2) и серный (SO3) ангидриды, которые, попадая в атмосферу, образуют серную кислоту. В конечном итоге, последняя выпадает в виде кислых дождей, нанося ущерб здоровью населения и окружающей среде. Таким образом, обезвреживание газовых выбросов электростанций является актуальной проблемой народного хозяйства.
Известен каталитический способ удаления оксида серы SO2 путем его окисления в серный ангидрид с получением серной кислоты (патент США 4963520, 1990), в котором использует для этой цели биметаллическую шпинель в качестве катализатора. Основные достоинства этого процесса подробно изложены в брошюре датской компании (Haldor Topsoe: "SNOX™- Эффективное и экономичное удаление сернистых газов из дымовых газов", 1981 г.). Главный недостаток процесса состоит в необходимости сбора, хранения и реализации значительных объемов разбавленной серной кислоты. Так, при установленной мощности ГРЭС 2200 Мвт она должна сжигать ~4 млн. тонн топлива в год, что даже при содержании серы на уровне 0.5% масс, сопровождается выпуском ~200 тыс. т/год 33%-ной серной кислоты.
Более предпочтительны в этом отношении катализаторы, позволяющие восстанавливать оксиды серы в элементную серу. Особенности таких катализаторов описаны в различных источниках, например, (D.C. Moody et al, "Catalytic Reduction of Sulfur Dioxide", Journal of Catalysis, v. 70 (1), 1981), (патент США 5213779, 1993), где предлагаются в качестве катализатора лантаниды металлов, либо смесь оксида лантана в комбинации с сульфидами кобальта и стронция (патент США 5853684, 1998). Недостатком предложенных катализаторов является высокая стоимость редких металлов, их сравнительно низкая стойкость к сульфатированию и требование высоких температур (300-800°С) при эксплуатации. Все это существенным образом сказывается на росте себестоимости выработки электроэнергии.
Целый ряд изобретений используют в качестве носителей высококремнистые цеолиты USY, ZSM, SSZ-13 и др. Так, например, в качестве катализатора использованы ванадий-церий обменные формы ультрастабильного фожазита (USY) (патент США 6974787, 2005), либо оксиды ванадия, титана, вольфрама и молибдена, нанесенные на высококремнистый цеолит в качестве носителя (патент США 7572414, 2009). К недостаткам предложенных катализаторов надо отнести высокое содержание в их составе оксидов металлов IV-VI групп Периодической системы и их высокую стоимость, ограничивающие возможности практического применения катализаторов.
Наиболее близким к настоящему изобретению является катализатор, представляющий собой Zn-, Mn-, Cu- и Ni-обменные формы цеолитов USY BETA, ZSM, характеризующихся высоким соотношением оксидов SiO2:AbO3 выше 10.0, с нанесенными на них ванадатами металлов. К недостаткам прототипа следует отнести узкую практическую доступность высококремнистых цеолитов в их составе, сложность процесса приготовления, а также низкую активность катализатора в реакции восстановления оксидов серы при температурах ниже 300°С (патент США 7960307, 2011).
Задачей настоящего изобретения является разработка катализатора, проявляющего высокую активность в широкой области низких температур, начиная с 240°С, на основе доступных, дешевых по стоимости компонентов с использованием простого, технологически осуществимого способа приготовления.
Поставленная задача достигается предлагаемым катализатором для удаления оксидов серы из дымовых газов электростанций на основе низкокремнистого фожазита - цеолита LSX, характеризующегося молярным соотношением оксидов кремния и алюминия SiO2:Al2O3=2.0-2.2 и содержащего бинарные поликатионные кластеры переходных металлов -меди и цинка или меди и марганца при их мольном соотношении Cu:Zn и Cu:Mn в пределах 2:1÷4:1.
Катализатор представляет собой цеолит с нанесенными поликатионами переходных металлов формулы (Cu)p(Zn)pCaLSX-r, где р - поликатионная форма, r - соотношение меди к цинку 2 или 4.
С целью уменьшения гидравлического сопротивления по ходу дымовых газов, предлагаемый катализатор выполнен в виде сферических или цилиндрических гранул большого диаметра (10-12 мм) или ячеистой структуры монолитов.
Настоящим изобретением предлагается эффективный катализатор для удаления сернистых соединений из дымовых газов электростанций путем их восстановления моноксидом углерода в элементную серу. Отличительной особенностью способа приготовления катализатора является проведение операции ионного обмена низкокремнистого цеолита LSX (SiO2:Al2O3~2.0-2.2) с растворами частично гидролизованных солей переходных металлов при рН 5.2+5.8, и включает предварительную конверсию натрий-калиевой формы цеолита в кальциевую форму с последующим синтезом поликатионных кластеров меди и цинка или меди и марганца. Таким образом, способ включает несколько стадий: а) стадию обмена щелочных катионов на катионы Са2+, б) стадию обмена катионов Са2+ на катионы Cu2+, в) стадию обмена на катионы Zn2+ или Mn2+. Метод синтеза исходного низкокремнистого цеолита LSX предложен Г. Кюлем (G.H. 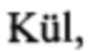 , "Crystallization of Low-Silica Faujasite (SiO2:Al2O3~2.0-2.2)", Zeolites, 1987, 7, 451), и его производство осуществлено в промышленном масштабе. Простая технология получения поликатионных форм цеолитов предложена авторами настоящего изобретения, которая наряду с активностью цеолитов с поликатионными кластерами переходных металлов в реакциях окисления моноксида углерода и сернистых соединений описана в публикациях О.Р. Tkachenko, А.А. Greish, A.V. Kucherov, K.С.Weston, A.M. Tsybulevski, L.M. Kustov "Low-temperature CO oxidation by transition metal polycation exchanged low-silica faujasites", Applied Catalysis B: Environmental, 2015, 179, 521 и A.M. Tsybulevski, O.P. Tkachenko, E.J. Rode, K.C. Weston, L.M. Kustov, E.M. Sulman, V.Y.Doluda, A.A. Greish "Reactive Adsorption of sulfur compounds on transition metal polycation-exchanged zeolites for desulfurization of hydrocarbon streams", Energy Technology, 2017, 5, 1627.
, "Crystallization of Low-Silica Faujasite (SiO2:Al2O3~2.0-2.2)", Zeolites, 1987, 7, 451), и его производство осуществлено в промышленном масштабе. Простая технология получения поликатионных форм цеолитов предложена авторами настоящего изобретения, которая наряду с активностью цеолитов с поликатионными кластерами переходных металлов в реакциях окисления моноксида углерода и сернистых соединений описана в публикациях О.Р. Tkachenko, А.А. Greish, A.V. Kucherov, K.С.Weston, A.M. Tsybulevski, L.M. Kustov "Low-temperature CO oxidation by transition metal polycation exchanged low-silica faujasites", Applied Catalysis B: Environmental, 2015, 179, 521 и A.M. Tsybulevski, O.P. Tkachenko, E.J. Rode, K.C. Weston, L.M. Kustov, E.M. Sulman, V.Y.Doluda, A.A. Greish "Reactive Adsorption of sulfur compounds on transition metal polycation-exchanged zeolites for desulfurization of hydrocarbon streams", Energy Technology, 2017, 5, 1627.
Эта активность в окислительных реакциях объясняется способностью поликатионных кластеров переходных металлов отдавать реактантам свои избыточные атомы кислорода. Активность же в восстановительных реакциях, в частности в восстановлении оксидов серы, способность отрывать атом кислорода от реактантов, оксидов серы неизвестна, абсолютно неожиданна, и впервые обнаружена авторами изобретения. Не менее неожиданна и активность предлагаемого катализатора в области низких температур, его способность полностью удалять из потока газа диоксид серы уже при 240°С, что, в свою очередь, открывает новые пути обессеривания дымовых газов электростанций.
Приготовление катализатора, его химический состав и доказательства его преимуществ в удалении оксидов серы продемонстрированы в нижеследующих примерах. Эти примеры носят иллюстративный характер и не ограничивают сферу применения изобретения.
Примеры 1-3 - Приготовление образцов катализаторов Нижеприведенные примеры приготовления образцов рассчитаны на получение 140 г конечного продукта. Все образцы катализаторов приготовлены на основе натрий-калиевой формы цеолита NaKLSX производства компании М Chemical.
Хотя катионы щелочных и щелочно-земельных металлов играют роль катионов, компенсирующих отрицательный заряд решетки в структуре низкокремнистого фожазита LSX, предварительная конверсия натрий-калиевой формы в кальциевую форму цеолита необходима для последующего синтеза поликатионных кластеров меди и цинка или меди и марганца. Таким образом, процедура приготовления включает несколько стадий.
Пример 1. Приготовление катализатора (Cu)p(Zn)pCaLSX-4.
а). Стадия обмена щелочных катионов на катионы Са2+:
приготовили 1 литр 1 N раствора хлорида кальция путем растворения 73.5 г CaCl2⋅(H2O) в деионизированной воде (ДИВ);
100 г гранул исходного цеолита обработали в 1 литре 1 N раствора CaCl2 при комнатной температуре и постоянном перемешивании. рН раствора поддерживали в пределах 6.5-7.0, чтобы получить степень ионного обмена ~55-60% с получением формы CaLSX;
промыли гранулы в ~10 л деионизированной воды.
б). Стадия обмена катионов Са2+ на катионы Cu2+:
приготовили буферный раствор - 0.05 М дигидрофосфата натрия (NaH2PO4) путем растворения 6 г безводного NaH2PO4 в 1 литре деионизированной воды;
приготовили 1 литр 1 N раствора хлорида меди CuCl2 путем растворения 85.6 г CuCl2⋅H2O в 1 литре деионизированной воды и снизили рН раствора добавкой 35 мл буферного раствора, чтобы избежать спонтанного осаждения гидроксида меди;
обработали промытые гранулы CaLSX 1 литром 1 N раствора CuCl2 при комнатной температуре и непрерывном перемешивании в течение 4 часов. Поддерживали рН обменного раствора в процессе ионного обмена на уровне 5.0-5.4, используя натрий-дигидрофосфатный буфер. Достигнутая степень ионного обмена должна быть равна ~50% Cu, 40% Са;
промыли продукт 10 л деионизированной воды.
в). Стадия обмена на катионы Zn2+:
приготовили буферный раствор - 0.03 М гидрофосфата калия (K2HPO4).
Растворили 5.25 г K2HPO4 в 1 литре деионизированной воды.
Приготовили 1 литр 1.5 N раствора хлорида цинка ZnCl2. Растворили 102 г безводного ZnCl2 в 1 литре деионизированной воды и снизили рН раствора добавлением 60 мл буфера, чтобы избежать интенсивного осаждения гидроксида цинка.
Обработали ранее полученный цеолит CuCaLSF 1 литром 1.5 N раствора ZnCl2 в течение 4 часов, поддерживая рН обменного раствора на уровне 5.6-6.0 при помощи буфера - 0.03 М раствора K2HPO4. Достигнутые степени обмена катионов в образце катализатора составили: Са - 15%, Cu - 50%, Zn - 12.5% экв.
Промыли продукт деионизированной водой, чтобы достичь отрицательной реакции на хлорид-ион с 0.028 N раствором AgNO3.
Пример 2. Приготовление катализатора (Cu)p(Zn)pCaLSX-2.
Повторили стадии а) обмена щелочных катионов на катионы Са2+ и б) обмена катионов Са2+ на катионы Cu2+ синтеза катализатора как в примере 1;
в) стадия обмена на катионы Zn2+:
приготовили 1 литр 2.5 N раствора хлорида цинка. Растворили 170 г безводного ZnCl2 в 1 литре деионизированной воды и снизили рН раствора добавлением 75 мл буфера, чтобы избежать осаждения гидроксида цинка. Использовали в качестве буфера 0.03 М раствор K2HPO4;
обработали полученный на стадии б) образец CuCaLSF 1 литром 2.5 N раствора хлорида цинка в течение 4 часов, поддерживая рН обменного раствора на уровне 5.2-5.6, используя буферный раствор K2HPO4. Достигнутые степени обмена в конечном продукте составили: Са - 12%, Cu - 45%, Zn - 22% экв.
Пример 3. Приготовление катализатора (Cu)p(Mn)pLSX-2.
Повторили стадии а) обмена щелочных катионов на катионы Са2+ и б) обмена катионов Са2+ на катионы Cu2+ синтеза катализатора как в примере 1;
в) стадия обмена на катионы Mn2+:
приготовили 1 литр 2 N раствора хлорида марганца путем растворения 198 г MnCl2⋅4H2O в 1 литре деионизированной воды с добавлением 100 мл буферного раствора гидрофосфата калия для предупреждения выпадения осадка гидроксида марганца.
Обработали в течение 4 часов полученный на стадии б) образец (Cu)pCaLSF 1 литром 2 N раствора хлорида марганца, поддерживая рН обменного раствора на уровне 5.1-5.4 при помощи буферного раствора K2HPO4. Достигнутые степени ионного обмена составили: Са - 15%, Cu - 50%, Mn - 25% экв.
Пример 4. Изучение и подтверждение поликатионной структуры катализатора на примере (Cu)p(Zn)pCaLSX-2 с помощью метода EXAFS.
EXAFS-спектры образца катализатора (Cu)p(Zn)pCaLSX-2 были сняты на БМ23 станции Европейского Центра Синхротронного Излучения (ESRF, Гренобль, Франция). Для сопоставления были записаны одновременно спектры металлической фольги. Измеренные параметры катионов меди и цинка приведены в Таблице 1.


Результаты спектральных измерений однозначно подтверждают наличие поликатионных кластеров меди и цинка в катализаторе (Cu)p(Zn)pCaLSX-2. Измеренный радиус катионов существенно превышает стандартную длину связи в монокатионных формах (1.97; 2.05 против 1.95), среднее содержание кислорода выше стехиометрического, а площадка, занимаемая поликатионами Cu и Zn в 2-3 раза больше размера монокатионов.
Пример 5. Испытание активности катализаторов
Образцы катализаторов, полученные в примерах 1-3, наряду с образцом используемого в промышленности катализатора La2O3⋅TiO2 (анатаз), являющегося аналогом известного катализатора очистки от диоксида серы (патент США 5213779, 1993) испытывали в реакции восстановления диоксида серы моноксидом углерода на лабораторной установке с металлическим реактором, имеющим внутренний диаметр 9 мм, длину - 40 см. Навеску катализатора с зернением 1.6-2.0 мм загружали в центральную часть реактора. Образцы предварительно тренировали при 250°С в течение 2 часов. Исходная газовая смесь содержала: SO2 - 0.5%, СО - 1.5%, Не - 98%, объемная скорость подачи газа в реактор - 120-160 см3/мин. Температуру реакции варьировали в интервале 220-380°С.
Анализ продуктов реакции проводили хроматографически на приборе ЛХМ-8 с детектором по теплопроводности с использованием трех набивных колонок: колонка 1 - длина -1,5 м, неподвижная фаза - цеолит 5А; колонка 2 - длина 1,5 м, неподвижная фаза - Порапак; колонка 3 - длина 2 м, неподвижная фаза - Хромосорб SE-54.
Результаты испытаний активности образцов сопоставлены в Таблице 2.
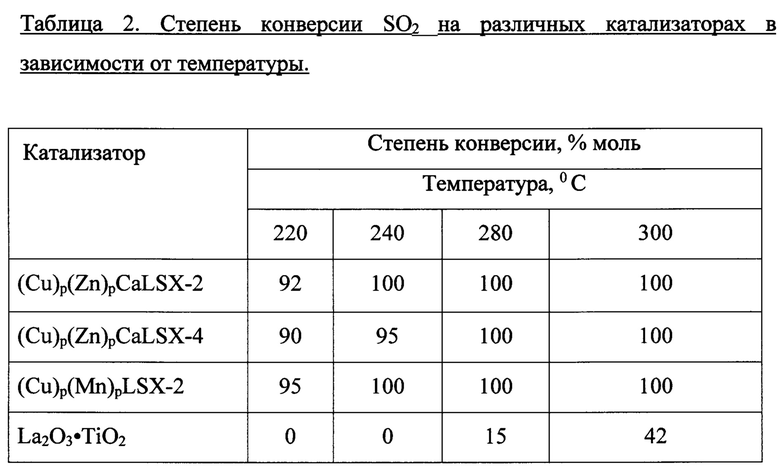
Результаты испытаний наглядно демонстрируют преимущества предложенных катализаторов, их способность полностью удалять оксиды серы в диапазоне температур, недоступном другим известным катализаторам очистки дымовых газов.
Технический результат - предложен эффективный катализатор, способный осуществлять полное удаление оксида серы при низких температурах процесса в диапазоне 240-280°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МОЛЕКУЛЯРНЫХ СИТ | 1997 |
|
RU2217233C2 |
| СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДОВ АЗОТА | 1995 |
|
RU2088316C1 |
| АДСОРБЕНТ И СПОСОБ ДЛЯ ОТДЕЛЕНИЯ МЕТАНОЛА И ОКСИГЕНАТОВ | 2019 |
|
RU2748661C2 |
| КАТАЛИЗАТОР ДЛЯ ОСУЩЕСТВЛЕНИЯ РЕАКЦИЙ МЕЖМОЛЕКУЛЯРНОГО ПЕРЕНОСА ВОДОРОДА И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2015 |
|
RU2599720C1 |
| КАТАЛИЗАТОР, УМЕНЬШАЮЩИЙ УРОВЕНЬ СОДЕРЖАНИЯ СЕРЫ В БЕНЗИНЕ, ДЛЯ СПОСОБА КАТАЛИТИЧЕСКОГО КРЕКИНГА В ПСЕВДООЖИЖЕННОМ СЛОЕ КАТАЛИЗАТОРА | 2008 |
|
RU2442649C2 |
| КАТАЛИЗАТОР УМЕНЬШЕНИЯ СОДЕРЖАНИЯ СЕРЫ В БЕНЗИНЕ ДЛЯ СПОСОБА КАТАЛИТИЧЕСКОГО КРЕКИНГА С ПСЕВДООЖИЖЕННЫМ КАТАЛИЗАТОРОМ | 2002 |
|
RU2266782C2 |
| НЕЛЕКАРСТВЕННАЯ КОРМОВАЯ ДОБАВКА, ПРЕМИКС, КОРМ, СОДЕРЖАЩИЕ НЕЛЕКАРСТВЕННУЮ КОРМОВУЮ ДОБАВКУ, И СПОСОБ ПОВЫШЕНИЯ РОСТА ЖИВОТНЫХ | 2006 |
|
RU2417624C2 |
| КАТАЛИЗАТОР УМЕНЬШЕНИЯ СОДЕРЖАНИЯ СЕРЫ В БЕНЗИНЕ ДЛЯ ПРОЦЕССА КАТАЛИТИЧЕСКОГО КРЕКИНГА В ЖИДКОЙ ФАЗЕ | 2005 |
|
RU2396304C2 |
| КАТАЛИЗАТОР И СПОСОБ КАТАЛИТИЧЕСКОЙ БЕЗВОДОРОДНОЙ ДЕПАРАФИНИЗАЦИИ УГЛЕВОДОРОДНОГО СЫРЬЯ | 2021 |
|
RU2782791C1 |
| КАТАЛИЗАТОРЫ СКВ: ПЕРЕХОДНЫЙ МЕТАЛЛ/ЦЕОЛИТ | 2008 |
|
RU2506989C2 |
Изобретение относится к катализатору для удаления оксидов серы из дымовых газов электростанций, содержащему цеолит типа фожазит и катионы переходных металлов, при этом в качестве цеолита он содержит низкокремнистый фожазит (LSX), а в качестве катионов переходных металлов - бинарные поликатионные кластеры меди и цинка либо меди и марганца при мольном соотношении Cu:Zn или Cu:Mn в пределах 2:1÷4:1. Технический результат заключается в получении эффективного катализатора, способного осуществлять полное удаление оксида серы при низких температурах процесса в диапазоне 240-280°С. 2 з.п. ф-лы, 2 табл., 5 пр.
1. Катализатор для удаления оксидов серы из дымовых газов электростанций, содержащий цеолит типа фожазит и катионы переходных металлов, отличающийся тем, что в качестве цеолита он содержит низкокремнистый фожазит (LSX), а в качестве катионов переходных металлов - бинарные поликатионные кластеры меди и цинка либо меди и марганца при мольном соотношении Cu:Zn или Cu:Mn в пределах 2:1÷4:1.
2. Катализатор по п. 1, отличающийся тем, что он содержит низкокремнистый фожазит при мольном соотношении оксидов кремния и алюминия SiO2:Al2O3 = 2.0-2.2.
3. Катализатор по пп. 1, 2, отличающийся тем, что он имеет форму сферических или цилиндрических гранул или ячеистой структуры монолитов.
| US 7960307 B2, 14.06.2011 | |||
| О.Р | |||
| Tkachenko, А.А | |||
| Greish, A.V | |||
| Kucherov, К.С | |||
| Weston, A.M | |||
| Tsybulevski, L.M | |||
| Kustov "Low-temperature CO oxidation by transition metal polycation exchanged low-silica faujasites", Applied Catalysis B: Environmental, 2015, 179, 521-529 | |||
| A.M | |||
| Tsybulevski, O.P | |||
| Tkachenko, E.J | |||
| Rode, K.C | |||
| Weston, L.M | |||
| Kustov, E.M | |||
| Sulman, |
Авторы
Даты
2020-08-06—Публикация
2019-10-24—Подача