Изобретение относится к органической химии, в частности, касается кристаллической модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (пиранокумарина), способа ее получения, и может быть использовано в химической промышленности и медицине.
Пиранокумарин является антикоагулянтом непрямого действия и используется в области медицинской и ветеринарной дератизации для борьбы с грызунами в сельском хозяйстве [The Agrochemicals Handbook (2nd Edition), by D. Hartley and H. Kidd (Editors). The Royal Society of Chemistry Information Services, 1987, approx. 1200 pages, ISBN: 0-85186-416-3]. Титульное соединение является метиловым эфиром закрытоцепочечной формы менее активного антикоагулянта «Варфарина» (3-(1-фенил-3-оксобутил)-4-гидроксихромен-2-она) (I). В зависимости от выбранного способа метилирования и последующей стадии выделения может быть получен продукт с заданным набором свойств, обладающий большей эффективностью по сравнению с исходным соединением.
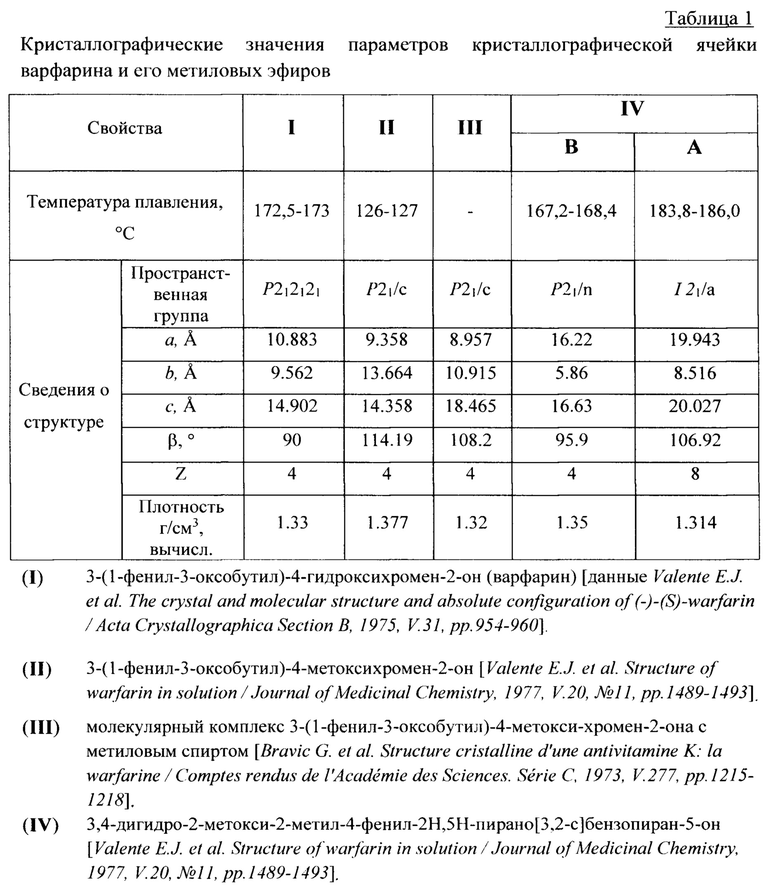
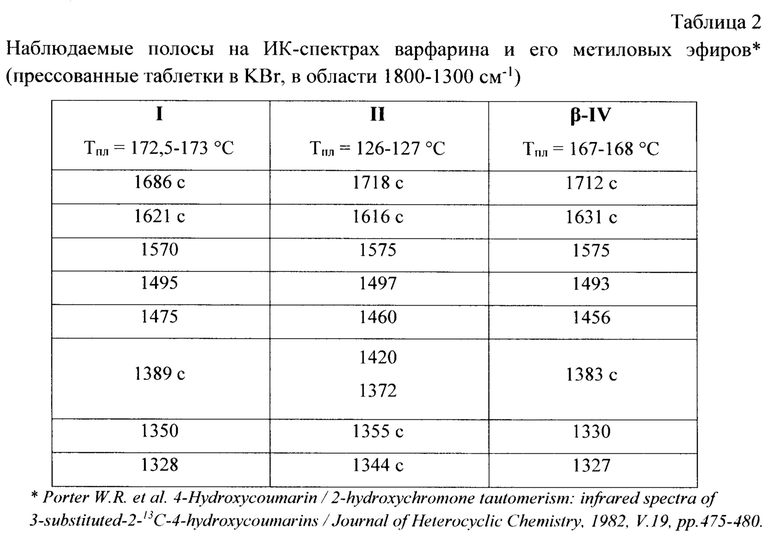
Из уровня техники известно, что метилирование варфарина (I) диазометаном [Ikawa М. et al. Studies on 4-Hydroxycoumarins. V. The condensation of α,β-unsaturated ketones with 4-hydroxycoumarin / Journal of the American Chemical Society, 1944, V. 66, №6, pp. 902-906] и с помощью метилиодида в ацетоне приводит к одному и тому же продукту: метиловому эфиру открытоцепочечной формы [Valente E.J. et al. Structure of warfarin in solution / Journal of Medicinal Chemistry, 1977, V. 20, №11, pp. 1489-1493]. Физико-химические свойства данного соединения (3-(1-фенил-3-оксобутил)-4-метоксихромен-2-он) (II) представлены в таблицах 1 и 2.
В случае кристаллизации варфарина (I) из метилового спирта (МеОН) образование метилированных производных не протекает, однако была получена сольватированная форма, содержащая МеОН в соотношении 1:1 [Bravic G. et al. Structure cristalline d'une antivitamine K: la warfarine / Comptes rendus de  des Sciences.
des Sciences.  C, 1973, V. 277, pp. 1215-1218]. Сведения о кристаллической структуре этого сольвата, являющегося молекулярным комплексом 3-(1-фенил-3-оксобутил)-4-метоксихромен-2-она с метиловым спиртом (III), представлены в таблице 1.
C, 1973, V. 277, pp. 1215-1218]. Сведения о кристаллической структуре этого сольвата, являющегося молекулярным комплексом 3-(1-фенил-3-оксобутил)-4-метоксихромен-2-она с метиловым спиртом (III), представлены в таблице 1.
Титульное соединение, являющееся метиловым эфиром гемикетальной формы варфарина (3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (IV)), может быть получено метилированием варфарина (I) кипячением раствора в метиловом спирте в присутствии смолы Dowex 50 (Н+ форма) с использованием аппарата Сокслета, заполненного молекулярными ситами 3 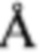 ; продукт кристаллизуют из этилового спирта [Valente E.J. et al. Structure of warfarin in solution / Journal of Medicinal Chemistry, 1977, V. 20, №11, pp. 1489-1493]. Дробная кристаллизация полученного таким способом соединения из этилового спирта приводит к двум различным β (выход 75%) и α полиморфным формам 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (IV), характеризующимся различными температурами плавления (Тпл) и параметрами кристаллографических ячеек. Сведения о физико-химических свойствах этих полиморфных форм представлены в таблицах 1 и 2, однако сведения об их биологической активности не приведены.
; продукт кристаллизуют из этилового спирта [Valente E.J. et al. Structure of warfarin in solution / Journal of Medicinal Chemistry, 1977, V. 20, №11, pp. 1489-1493]. Дробная кристаллизация полученного таким способом соединения из этилового спирта приводит к двум различным β (выход 75%) и α полиморфным формам 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (IV), характеризующимся различными температурами плавления (Тпл) и параметрами кристаллографических ячеек. Сведения о физико-химических свойствах этих полиморфных форм представлены в таблицах 1 и 2, однако сведения об их биологической активности не приведены.
Общий ход реализации получения циклических продуктов с использованием метанола и соляной кислоты ранее был показан в литературе [Ikawa М. et al. Studies on 4-Hydroxycoumarins. V. The condensation of α,β-unsaturated ketones with 4-hydroxycoumarin / Journal of the American Chemical Society, 1944, V. 66, №6, pp. 902-906], однако для титульного продукта в данном источнике информации использовали абсолютизированный метанол, в котором был растворен 4% HCl, при этом вода использовалась, по-видимому, как высаливатель для получения с высоким выходом (83%) кристаллического продукта (Тпл=166°С). Данные по эффективности не приводятся.
Техническая задача настоящего изобретения состояла в расширении арсенала родентицидных средств.
Технический результат заявленного изобретения заключается в получении новой кристаллической модификации пиранокумарина.
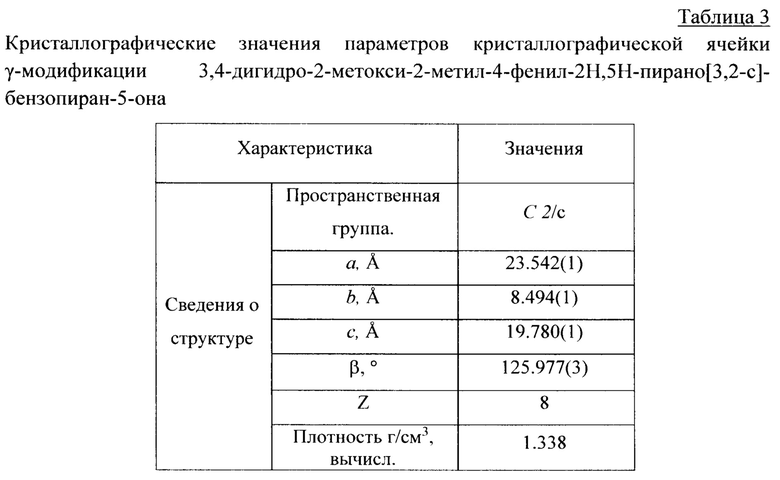
Техническая задача решается и технический результат достигается за счет того, что получена новая кристаллическая γ-модификация 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (γ-IV), характеризующаяся температурой плавления 161-164°С и следующими значениями параметров кристаллографической ячейки: пространственная группа С2/с, а=23.542(1) 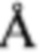 , b=8.494(1)
, b=8.494(1) 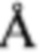 , с=19.780(1)
, с=19.780(1) 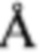 , β=125.977(3)°, Z=8.
, β=125.977(3)°, Z=8.
Техническая задача решается и технический результат достигается также способом получения указанной кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (γ-IV), согласно которому проводят реакцию варфарина с метиловым спиртом в присутствии сильной минеральной кислоты и далее осуществляют направленную кристаллизацию. Проведение направленной кристаллизации позволяет выделить (получить) заявленную полиморфную форму пирокумарина.
В примерах осуществления изобретения в качестве сильной минеральной (неорганической) кислоты использовали соляную и серную кислоты. Однако в рамках заявленного способа возможно использование и других сильных минеральных кислот.
Кроме того, техническая задача решается и технический результат достигается применением указанной кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (γ-IV) в качестве родентицидного средства.
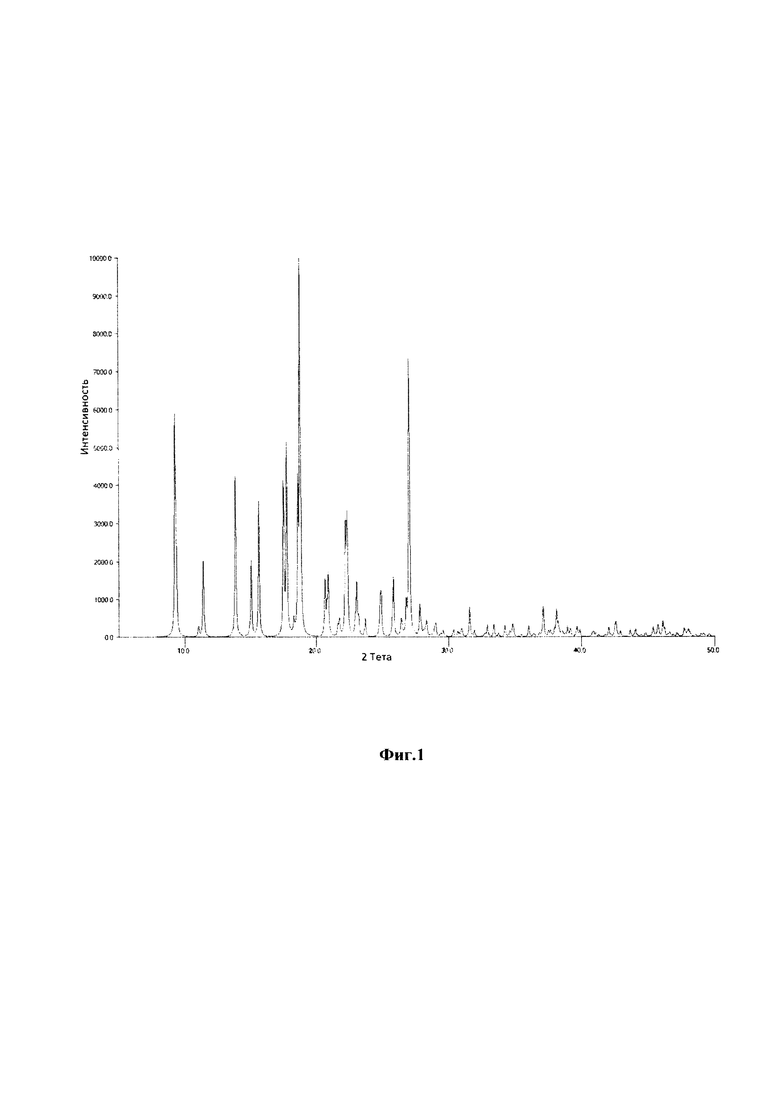
На фиг. 1 представлена рентгенограмма полученной в настоящем изобретении кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она (γ-IV); область сканирования по θ от 5 до 50 град.
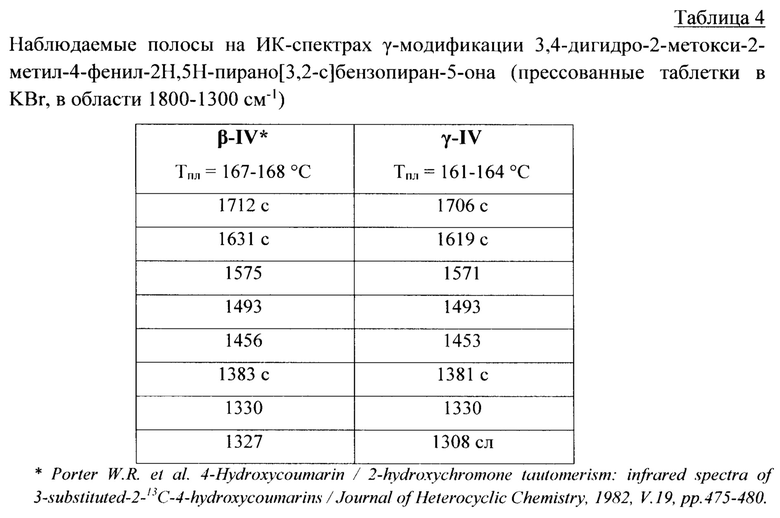
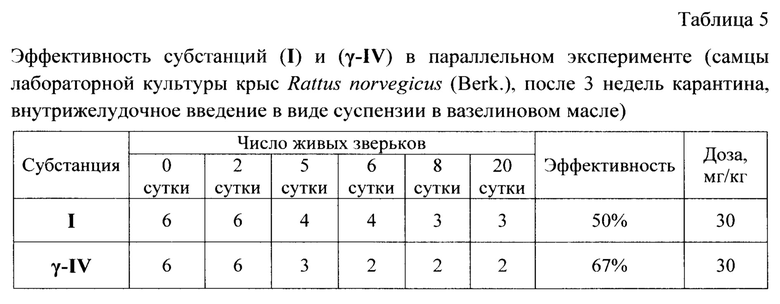
В таблице 3 представлены значения параметров кристаллографической ячейки полученной γ-модификации (γ-IV), а в таблице 4 приведены сведения по характеристическим ИК-частотам. Данные о токсикологических характеристиках (эффективности в отношении серых крыс Rattus norvegicus (Berk.)) показаны в таблице 5.
Сопоставление данных, представленных в таблицах 1-4 показывает, что полученное в настоящем изобретении вещество (γ-IV) является кристаллической γ-модификацией пиранокумарина с указанным набором характеристик, обладающей более высокой эффективностью при внутрижелудочном введении серым крысам (таблица 5) по сравнению с исходной субстанцией «Варфарин» (I).
Получение новой γ-модификации позволяет решить важную задачу - расширить ассортимент использующихся на территории Российской Федерации субстанций [Махнева Т.В. и др. Вклад отечественных производителей средств дезинфекции, дезинсекции и дератизации в развитие дезинфекционного дела в Российской Федерации / Дезинфекционное дело, 2006, №3, с. 17-22]. Внедрение в практику дератизации новой субстанции позволит косвенно решить задачу по предотвращению развития резистентности (устойчивости) грызунов к использующемуся арсеналу средств, отмеченному в литературе [Кочетов А.Н. и др. Пути создания новых антикоагулянтных родентицидов / Дезинфекционное дело, 2009, №2, с. 68-77; Смирнов A.M. и др. К проблеме образования устойчивых к родентицидам популяций грызунов / Ветеринария, Зоотехния и Биотехнология, 2018, №4, 6-12], в том числе по отношению к стартовому прекурсору «Варфарин» [Кочетов А.Н. и др. Пути создания новых антикоагулянтных родентицидов / Дезинфекционное дело, 2009, №2, с. 68-77].
Идентичность химической формулы пиранокумарина, полученного в примерах, подтверждена методами ВЭЖХ, РСА, РФА и элементным анализом. Количественный анализ показывает, что содержание пиранокумарина в полученном продукте составляет 97,0±1,0%.
Способы получения заявленной кристаллической γ-модификации пиранокумарина иллюстрируются следующими примерами.
Пример 1
К 0,5 г варфарина (3-(1-фенил-3-оксобутил)-4-гидроксихромен-2-она) (I), полученного в соответствии с известным методом [патент RU 2224739 С2, опубл. 27.02.2004], в 70 см3 метанола добавляют 0,25 мл 37-% соляной кислоты и кипятят полученный раствор в колбе с обратным холодильником в течение 1 часа. После остывания до комнатной температуры полученный бесцветный раствор был оставлен на кристаллизацию без доступа воздуха. После выдерживания в течение 5 часов выпавшие хорошо образованные пластинчатые кристаллы отделяют от маточного раствора любым общепринятым способом, двукратно промывают небольшими порциями метанола (по 5 мл) и сушат при температуре 20-50°С. Выход составляет не менее 60%. Маточный раствор может быть в дальнейшем регенерирован или вторично использован.
Полученное вещество имеет характеристики, соответствующие описанной выше кристаллической γ-модификации пиранокумарина (таблицы 3-4).
Пример 2
Способ осуществляют в соответствии с примером 1, за исключением в том, что используют 20%-ную серную кислоту (того же объема). Выход составляет 30%. Полученное вещество имеет те же характеристики, что и полученное в примере 1.
Приведенные способы получения новой кристаллической модификации эффективны и промышленно применимы.
Изобретение относится к кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она, характеризующейся температурой плавления 161-164°С и значениями параметров кристаллографической ячейки: пространственная группа С2/с, а=23.542(1) 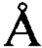 , b=8.494(1)
, b=8.494(1) 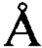 , с=19.780(1)
, с=19.780(1) 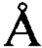 , β=125.977(3)°, Z=8. Изобретение также относится к способу получения кристаллической γ-модификации и к применению в качестве родентицидного средства. Технический результат: получена новая кристаллическая модификация 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она, которая может найти применение в качестве родентицидного средства и обладающая более высокой биологической эффективностью по сравнению с варфарином. 3 н.п. ф-лы, 1 ил., 5 табл., 2 пр.
, β=125.977(3)°, Z=8. Изобретение также относится к способу получения кристаллической γ-модификации и к применению в качестве родентицидного средства. Технический результат: получена новая кристаллическая модификация 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она, которая может найти применение в качестве родентицидного средства и обладающая более высокой биологической эффективностью по сравнению с варфарином. 3 н.п. ф-лы, 1 ил., 5 табл., 2 пр.
1. Кристаллическая γ-модификация 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она, характеризующаяся температурой плавления 161-164°С и следующими значениями параметров кристаллографической ячейки: пространственная группа С2/с, а=23.542(1) 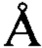 , b=8.494(1)
, b=8.494(1) 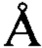 , с=19.780(1)
, с=19.780(1) 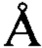 , β=125.977(3)°, Z=8.
, β=125.977(3)°, Z=8.
2. Способ получения кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она по п. 1, характеризующийся тем, что проводят реакцию варфарина с метиловым спиртом в присутствии соляной или серной кислоты при кипячении раствора, затем после остывания до комнатной температуры полученный раствор оставляют на кристаллизацию без доступа воздуха.
3. Применение кристаллической γ-модификации 3,4-дигидро-2-метокси-2-метил-4-фенил-2Н,5Н-пирано[3,2-с]бензопиран-5-она по п. 1 в качестве родентицидного средства.
| ВРЕМЕННОЕ СОГЛАСОВАНИЕ ДАННЫХ ОБРАБОТКИ НА ОСНОВЕ КВАДРАТУРНОГО ЗЕРКАЛЬНОГО ФИЛЬТРА | 2014 |
|
RU2665281C2 |
| СПОСОБ ЛИНЕЙНОГО ОПТИЧЕСКОГО ПРЕОБРАЗОВАНИЯ СИГНАЛОВ И ИНТЕРФЕРОМЕТР, РЕАЛИЗУЮЩИЙ ТАКОЕ ПРЕОБРАЗОВАНИЕ | 2018 |
|
RU2702806C1 |
| III | |||
| E | |||
| J | |||
| Valente et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| S | |||
| Shahzadi et al | |||
| "The Mechanism and Crystal | |||
Авторы
Даты
2020-09-10—Публикация
2019-12-17—Подача