Область техники
Изобретение относится к медицине, а именно к нейрохирургии и касается способа лечения нейрохирургической патологии - мальформации Киари I типа у взрослых, а также костного аутотрансплантата для применения в способе лечения.
Уровень техники
Мальформация Киари представляет собой сложный порок развития центральной нервной системы, характеризующийся патологией краниовертебральной области. В основе данного диагноза лежит, как правило, каудальная дистопия миндалин мозжечка ниже уровня большого затылочного отверстия, что приводит к хроническому сдавлению структур кранио- вертебрального перехода и нарушению ликвор о динамики и кровообращения в данной области (Хачатрян В.А. и др. Клинические рекомендации по диагностике и лечению Мальформации Киари у детей. Ассоциация нейрохирургов России. Санкт-Петербург, 2015, Каххаров Р.А. и др. Опыт использования различных вариантов пластики твердой мозговой оболочки (ТМО) в лечении больных с аномалией (мальформацией) Киари I типа. Вестник РГМУ, 4, 2016).
Согласно различным теориям причины возникновения Мальформации Киари носят как врожденный, так и приобретенный характер.
Так, Gardner (Gardner W.J. Anatomic features common to the Arnold-Chiari and the Dandy-Walker malformations suggest a common origin. Cleve Clin Q, 1959, 26) предположил, что нарушение проницаемости крыши четвертого желудочка в процессе фетального развития приводит к растяжению мозгового и спинального отдела невральной трубки, что в свою очередь о ведет к увеличению зачатков желудочковой системы и каудальному смещению задних отделов ствола.
Sahuquillo (Sahuquillo J. et al. Posterior fossa reconstruction: a surgical technique for the treatment of Chiari I malformation and Chiari I/syringomyelia complex - preliminary results and magnetic resonance imaging quantitative assessment of hindbrain migration. Neurosurgery, 1994, 35) и Peach (Peach B. The Arnold-Chiari Malformation; Morphogenesis. Arch Neurol, 1965, 12) утверждал, что нарушение правильного генеза приводит к формированию аномального изгиба в области моста. Следствием этого, по их мнению, является значительное удлинение задних отделов ствола, IV желудочка и нижних отделов червя.
По мнению Roessmann и Friede (Friede R.L., Roessmann, U. Chronic tonsillar herniation: an attempt at classifying chronic hernitations at the foramen magnum. Acta Neuropathol, 1976, 34), все случаи с грыжевым выпячиванием миндаликов мозжечка связаны с воздействием на ствол или мозжечок на уровне большого затылочного отверстия.
В зависимости от вариантов сочетания изменений и степени их выраженности различают четыре основных типа заболевания.
Мальформация Киари I типа (MKI) - грыжевое выпячивание растянутых миндаликов мозжечка в спинномозговой канал через большое затылочное отверстие. В редких случаях возможно минимальное опущение продолговатого мозга, которое объясняется не аномалией развития этого отдела мозга, а гипоплазией костных структур этой области. Такие структуры, как червь мозжечка и IV желудочек, как правило, не повреждаются и остаются в пределах физиологической нормы (Крупина Н.Е. Мальформация Киари I типа и сирингомиелия. Журнал неврологии и психиатрии им С С Корсакова, 2003, 103).
Мальформация Киари II типа - смещение миндаликов нижней части червя мозжечка, моста и продолговатого мозга, а также растянутого четвертого желудочка ниже плоскости большого затылочного отверстия (БЗО) в направлении спинномозгового канала. Возможна деформация покрышки среднего мозга, окклюзия отверстия Мажанди арахноидальной мембраной, расширение центрального канала спинного мозга, утолщение massa intermedia. Верхние шейные корешки спинномозговых нервов имеют восходящее, ростральное направление. Мальформация Киари часто сочетается со spina bifida, менингоцеле, стенозом водопровода и гидроцефалией (Chiari Н. Concerning alterations in the cerebellum resulting from cerebral hydrocephalus. Pediatr Neurosci, 1987, 13).
Мальформация Киари III типа - выраженное каудальное смещение всех структур задней черепной ямки с образованием субокципитального или высокого шейного энцефаломенингоцеле (Caldarelli М. et al. Chiari type III malformation. Childs Nerv Syst 2002, 18).
Мальформация Киари IV типа проявляется гипоплазией мозжечка без его смещения. Так как данный вид патологии не сопровождается грыжевым выпячиванием структур центральной нервной системы, он зачастую не включается в общепринятую классификацию Pillay P.K. et al. Symptomatic Chiari malformation in adults: a new classification based on magnetic resonance imaging with clinical and prognostic significance. Neurosurgery, 1991, 28).
С недавнего времени к четырем основным типам мальформации Киари, добавлены еще два редко используемых определения.
Мальформация Киари 0 типа - состояние при котором низко расположенные миндалики мозжечка заполняют всю большую затылочную цистерну, но не выходят за ее пределы. Характеризуется «переполненной задней черепной ямкой» и часто сочетается с анатомическими аберрациями области ствола головного мозга и протяженными сирингомиелическими кистами (Kyoshima K. et al. Syringomyelia without hindbrain herniation: tight cisterna magna. Report of four cases and a review of the literature. J Neurosurg, 2002, 96).
Мальформация Киари 1.5 типа проявляется дистопией миндаликов мозжечка, незначительным растяжением IV желудочка и ствола головного мозга минимальными изменениями со стороны оральных отделов спинного мозга. Согласно существующим определениям, МК 1.5 является переходной, «пограничной» формой между первым и вторым типом, сочетающей в себе признаки обоих типов патологии или эмбриологически незавершенным вариантом второго типа без сопутствующей миелодисплазии (Kim I.K. et al. Chiari 1.5 malformation: an advanced form of Chiari I malformation. J Korean Neurosurg Soc, 2010, 48).
В настоящее время диапазон хирургических манипуляций, направленных на устранение мальформации Киари, представлен примерно 20 видами различных оперативных вмешательств. Основным способом лечения взрослых пациентов с MKI является хирургическая коррекция диспропорций на уровне краниовертебрального перехода.
Краниовертебральная декомпрессия (КВД) как способ лечения MKI впервые была описана Penfield и Coburn в 1938 году (Penfield W., Coburn, D. F. Arnold-Chiari malformation and its operative treatment. Archives of Neurology & Psychiatry (Chicago), 1938, 40).
При этом разброс по степени хирургической «агрессивности» может варьировать от методов, сопровождающихся резекцией миндаликов (Penfield W, Coburn DF. Arnold-Chiari malformation and its operative treatment. Arch Neurol Psychiatry. 1938, 40), до малоинвазивных эндоскопических методик костной декомпрессии (Greenberg M.S., Arredondo N. Handbook of Neurosurgery. 6th ed. Lakeland, FL, New York: Greenberg Graphics, Thieme Medical Publishers, 2006).
На сегодняшний день отмечается тенденция к использованию КВД с последующей реконструкцией твердой мозговой оболочки и участков черепа, подвергаемых трепанации.
Takayasu (Takayasu М. et al. A simple technique for expansive suboccipital cranioplasty following foramen magnum decompression for the treatment of syringomyelia associated with Chiari I malformation. Neurosurg Rev, 2004, 27) был одним из первых, кто предложил фиксировать выпиленный в ходе проведения операции костный лоскут определенным способом с целью предотвращения дальнейшего опущения мозжечка и формирования псевдоменигоцеле. Предложенный им способ включает субокципитальную краниотомию с резекцией задней дуги С1 до открытия ее максимального диаметра, вскрытие твердой мозговой оболочки с помощью «Y-образного» разреза, пытаясь сохранить большую часть арахноидальной оболочки неповрежденной. Закрытие твердой мозговой оболочки производят трансплантатом, который герметизируют фибриновым клеем. Костный лоскут накладывают на каудальную часть зоны краниотомии и фиксируют.
Применение краниовертебральной декомпрессии с последующей пластикой твердой мозговой оболочки и реконструкцией подвергаемых воздействию участков черепа, таких как задняя черепная ямка, позволяет избежать ряда осложнений, присущих иным методикам.
Наиболее распространенные побочные эффекты, сопровождающие хирургическое лечение MKI, связаны с инфекционными процессами, длительным заживлением раны и нарушением ликвороциркуляции. Количество и частота данных осложнений нередко коррелирует с особенностями хирургической техники, в частности, с протяженностью вскрытия арахноидальной оболочки и манипуляциями в субарахноидальном пространстве и с миндаликами мозжечка (Guyotat J. et al. Syringomyelia associated with type I Chiari malformation. A 21-year retrospective study on 75 cases treated by foramen magnum decompression with a special emphasis on the value of tonsils resection. Acta Neurochir (Wien), 1998, 140). Ликвородинамические нарушения связывают с западением кожно-апоневротического лоскута в области костного дефекта, что в свою очередь, ведет к снижению перфузии мозга и нарушению венозного оттока, приводя к усугублению неврологического дефицита (Ахундов Э.М. и др. Современные методы декомпрессивной трепанации черепа (Аналитический обзор), Волгоградский научно-медицинский журнал 1, 2016).
Краниовертебральная декомпрессия с пластикой твердой мозговой оболочки и закрытием костного дефекта позволяет избежать в большей или меньшей степени вышеуказанных недостатков в зависимости от выполняемых приемов (Реутов А.А. Принципы диагностики и тактика хирургического лечения больных с мальформацией Киари I типа. Диссертация на соискание ученой степени кандидата медицинских наук, 2017).
Однако использование костных лоскутов, несмотря на их очевидное преимущество перед искусственными материалами (естественность, отсутствие ряда побочных эффектов, отсутствие дополнительной стоимости материала), не нашло активного применения при лечении мальформации Киари I типа ввиду их хрупкости, сложности обработки и установки. Как правило, в случае проведения реконструкции используются титановые или синтетические имплантаты.
Что касается пластики твердой мозговой оболочки, здесь используются самые разнообразные материалы. Наиболее часто используют фрагменты надкостницы. Однако ее использование сопровождается длительным заживлением образовавшейся операционной раны. Так, выделение надкостницы требует более протяженного разреза и, следовательно, более выраженного болевого синдрома и проблемного заживления раны.
С этой целью также могут применяться собственная широкая фасция бедра, мышечный лоскут ременной мышцы головы, фрагмент атланто-затылочной мембраны, трупная твердая мозговая оболочка (ТМО), бесклеточный аллотрансплантант из человеческой кожи дермы, политетрафторэтилен, бычий перикард или синтетические материалы на его основе и подслизистая тонкой кишки свиньи. Каждый из названных материалов имеет ряд ограничений, связанных либо с особенностью самого материала, либо технологии его использования.
Авторами патента РФ 2578544 в 2014 г. представлен способ лечения аномалии Арнольда-Кари I типа, подразумевающий использование титановой пластины: больного оперируют в положении сидя, срединный разрез в шейно-затылочной области выполняют с применением скобы трехточечной фиксации. После рассечения кожи, подкожного жирового слоя и апоневроза, рассекают мышцы и скелетируют чешую затылочной кости и край большого затылочного отверстия. Производят декомпрессивную трепанацию задней черепной ямки с пластикой твердой мозговой оболочки. После проведения основного этапа оперативного вмешательства костный дефект закрывают специально смоделированной титановой пластиной. Длину пластины подбирают по размерам трепанационного окна таким образом, чтобы окно, по горизонтальной оси, было перекрыто полностью и латеральные края пластины перекрывали края костного дефекта на величину, достаточную для проведения фиксирующих шурупов с обеих сторон. При этом по вертикальной оси формируют наружную выпуклость пластины и узкую z-образную полоску для плотного прилегания и фиксации пластины к краям дефекта. Высоту пластины подбирают так, чтобы она располагалась выше уровня заднего края большого затылочного отверстия в нижней части трепанационного окна и перекрывала как минимум на один миллиметр костный дефект в верхней части трепанационного окна. Послойно накладывают швы на рану.
Наиболее близким по сути к заявленному способу лечения мальформации Киари I типа является способ, известный из источника Р. Missori et al. Neurosurgical Techniques. Reconstruction of Suboccipital Craniectomy with Autologous Bone Chips. Acta Neurochir, 2002, 144. Методика включает проведение субокципитальной краниэктомии с выполнением нескольких отверстий на поверхности черепа, сбор полученных при сверлении измельченных костных фрагментов, сбор и помещение крупных фрагментов в раствор рифамицина, закрытие твердой мозговой оболочки водонепроницаемым материалом, последующее закрытие задней черепной ямки фрагментами аутокости.
Названный способ является сравнительно простым и безопасным по сравнению с указанными выше методиками, однако на сегодняшний день остаются нерешенными проблемы, в частности, связанные с риском западения костных лоскутов, отсутствием их подвижности в послеоперационном периоде. Неверно выбранные способ извлечения и обработки, форма, размер и расположение костного лоскута могут привести к невозможности его дальнейшего использования в качестве аутотрансплантата, например, за счет его хрупкости или наличия на нем неровностей, приводящих к травмированию сосудов.
Не менее важным является и способ установки и крепления костного лоскута, поскольку эти факторы определяют объем формируемой затылочной цистерны. Ее недостаточный объем может привести к необходимости повторного проведения операции в следствие недостижения необходимого эффекта. Избыточный же объем резекции может спровоцировать опущение мозжечка в послеоперационном периоде.
Наиболее часто встречающимися осложнениями при осуществлении существующих техники, включающих использование чужеродных материалов для закрытия твердой мозговой оболочки являются инфекционные осложнения, возможность спаечного процесса, увеличение риска ликвореи, плохого заживления вследствие иммунной реакции организма. Использование чужеродных элементов зачастую требует дополнительной герметизации зоны пластики с применением ресурсоемких (дорогих) клеевых композиций.
Другими возможными осложнениями КВД являются формирование нестабильности шейного отдела позвоночника (до 7%), опущение мозжечка вследствие избыточной краниоэктомии и, в единичных случаях, перелом переднего полукольца С1.
В основу настоящего изобретения положена техническая задача разработки способа лечения редкой нейрохирургической патологии - мальформации Киари I типа у взрослых пациентов путем модификации существующей методики задней декомпрессии краниовертебрального перехода, также дополнением ее стадиями реконструкции ТМО и задней черепной ямки аутотрансплантатами.
Для решения данной технической задачи авторами предложен новый способ хирургического лечения мальформации Киари 1 типа у взрослых, характеризующийся проведением декомпрессии криниовертебрального перехода с задним срединным доступом и выполнением следующих действий: диссекцией мягких тканей, выполняемой по белой линии аваскулярной зоны, формированием лоскута из фрагмента апоневроза и/или выйной связки, проведением субпериостальной диссекции чешуи затылочной кости и задней дуги С1, резекцией области vermian fossa по направлению от задней губы большого затылочного отверстия на расстояние до 1 см, выполнением субокципитальной краниотомии с размерами костного лоскута 2.5-3.5 см × 3.5-4.5 см, проведением резекции задней дуги С1, иссечением утолщенной атланто-затылочной мембраны, вскрытием твердой мозговой оболочки с сохранением целостности арахноидальной оболочки, наложением аутофасции на место дефекта и ее фиксацией, реконструкцией задней черепной ямки костным аутотрансплантатом, включающей получение костного аутотрансплантата путем модификации костного лоскута, подразумевающей устранение неровностей на его поверхности, придание аутотрансплантату уплощенной прямоугольной формы со скругленными углами, при этом длина его боковых противоположных сторон составляет от 3,5 до 4,5 см, длина одной из прилегающих к ним сторон составляет от 2,5 до 3,5 см, а другая прилегающая к ним сторона имеет больший радиус закругления, при этом его боковые противоположные стороны имеют прямой или вогнутый контур, выполнение по меньшей мере двух отверстий по боковым сторонам костного лоскута и/или на верхней стороне костного лоскута, укладкой на место дефекта, фиксацией полученного аутотрансплантата угловыми пластинами, при этом происходит выдвижение нижнего края костного лоскута на толщину кости относительно исходной плоскости, герметичным зашиванием мышечно-апоневротического слоя.
Для решения поставленной технической задачи и преодоления недостатков известных методик может быть использован костный аутотрансплантат, также являющийся объектом настоящего изобретения.
Предлагаемый костный аутотрансплантат выполнен из костного лоскута, полученного непосредственно у пациента при выполнении предшествующих этапов оперативного хирургического вмешательства. При помощи бора, например, высокоскоростного, предлагаемому костному аутотрансплатату предается следующая форма: выполненный в виде уплощенного объема прямоугольной формы со скругленными углами. При этом длина боковых противоположных сторон указанного лоскута составляет от 3,5 до 4,5 см, длина одной из прилегающей к ним стороны составляет от 2,5 до 3,5 см, а другая прилегающая к ним сторона имеет больший радиус закругления. При этом боковые противоположные стороны указанного лоскута имеют прямой или вогнутый контур.
Костный аутотрансплантат характеризуется тем, что он включает фрагмент нижнего отдела затылочной кости. В конкретном варианте реализации костный аутотрансплатат включает фрагмент чешуи затылочной кости ниже наружнего затылочного выступа (инион).
В аутотрансплатате сверлом выполняются отверстия. В результате чего он характеризуется наличием по меньшей мере двух отверстий, расположенных на боковых сторонах трансплантата и/или на верхней стороне аутотрансплантата и предназначенных для его фиксации пластинами в зоне дефекта задней черепной ямки, при этом отверстия на боковых сторонах располагаются на противоположных боковых сторонах.
Количество отверстий на противоположных сторонах, как правило, одинаковое. Расстояние, на котором размещены отверстия от края трансплантата, составляет 1-5 мм. Предпочтительное расстояние отверстий от края составляет 2-4 мм. Еще более предпочтительным расстояние около 3 мм.
Отверстия также могут быть выполнены путем вкручивания в аутотрансплантат соответствующего количества саморезов. Предпочтительная длина самоедов составляет 3 мм и менее.
Технические эффекты, объективно проявляющиеся при использовании данного изобретения (технический результат), заключаются в его универсальности: предлагаемые изобретения могут быть использованы при любых видах задней краниовертебральной декомпрессии у пациентов с Мальформацией Киари взрослого возраста. Использование аутотрансплантатов при закрытии твердой мозговой оболочки и задней черепной ямки (ЗЧЯ) позволяет минимизировать последствия, связанные с их отторжением, и ускорить заживление. Немаловажным является и то, что предлагаемая методика позволяет производить пластику ТМО фрагментом апоневроза и/или выйной связки, что позволяет избежать дополнительных хирургических вмешательств, например, связанных с забором материала из широкой фасции бедра или надкостницы. Более того, предлагаемая форма лоскута является оптимальной с точки зрения восстановления конструкции и формы черепа, что обеспечивает необходимую прочность и устраняет возможные побочные эффекты и болевые ощущения пациента за счет отсутствия раздражения твердой мозговой оболочки, содержащей большое количество болевых рецепторов, в том числе спустя длительный период после проведения операции, что присуще пациентам, получившим лечение по ранее используемым методиками.
Предлагаемое изобретение также приводит к закрытию косметического дефекта на фоне достаточного увеличения объема ЗЧЯ. В ходе проведения операции создается объем, достаточный для устранения болевых ощущений, без рецидива и осложнений, не приводящий при этом к опущению мозжечка в отсроченном периоде.
К дополнительным техническим эффектам от использования изобретения можно отнести повышение эффективности (безопасности) хирургического лечения взрослых пациентов с Мальформацией Киари 1 типа; снижение временных затрат на лечение за счет уменьшения количества послеоперационных осложнений и сроков пребывания в стационаре; снижение финансовых затрат на лечение ввиду отсутствия необходимости применения дорогостоящих имплантатов, а соответственно снижение стоимости данного вида операции.
Изображения, поясняющие сущность изобретения
Рис. 1. Краниовертебральный переход, вид сзади;
Рис. 2. Костный аутотрансплантат;
Рис. 3. Вариант фиксации костного аутотрансплантата.
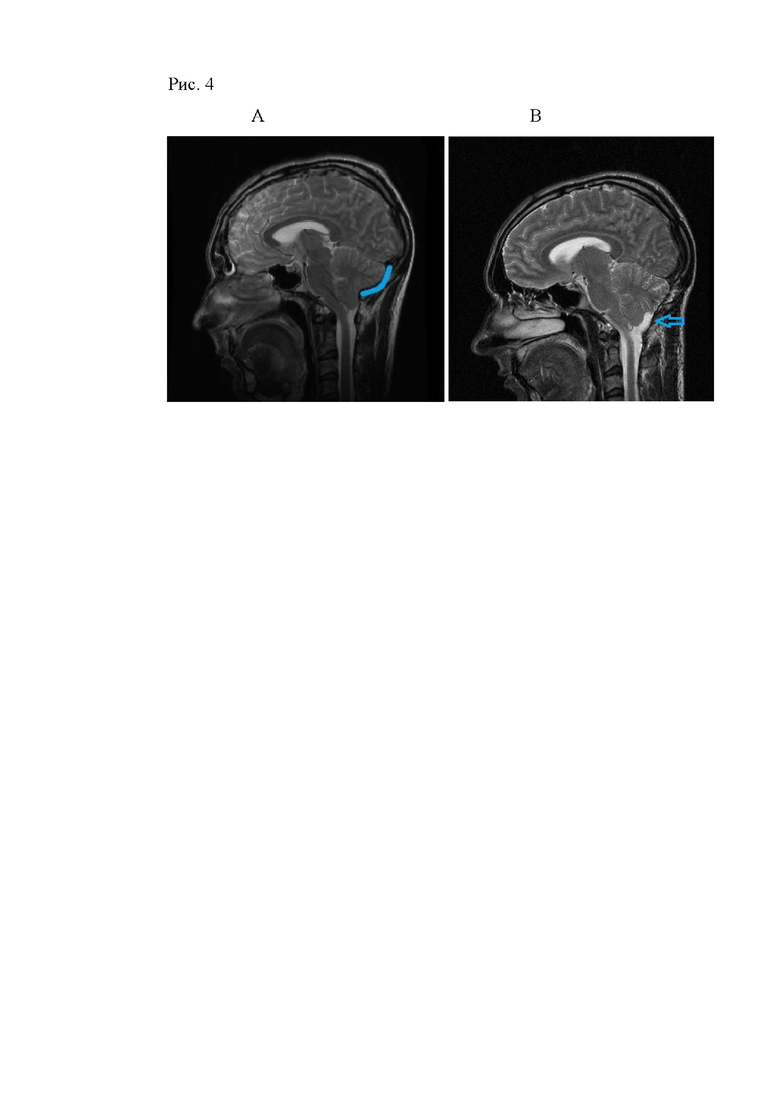
Рис. 4. Снимок магнитно-резонансной томографии пациента до оперативного вмешательства (А), после оперативного вмешательства (В).
Осуществление изобретения
Для задней декомпрессии краниовертебрального перехода можно использовать разные положения больного на операционном столе: «лежа на животе» - «concorde», «лежа на боку» и положение «полусидя». При операции в положении на животе возможно использование специальной поролоновой рамы или рамы Вилсона. Использование рамы способствует достижению необходимой экскурсии грудной клетки пациента во время аппаратного дыхания. Для обеспечения физиологичного сгибания шеи, при отсутствии рамы Вилсона, можно уложить дополнительный валик под грудь пациента. Голова пациента фиксируется строго по средней линии с помощью скобы трехточечной фиксации типа «Mayfield» с обязательным соблюдением продольной оси тела. Позиция шипов при этом должна быть таковой, чтобы обеспечить достаточный обзор операционного поля и возможность для скелетирования затылочной кости в достаточном объеме. Для обеспечения адекватного оттока венозной крови по яремным венам, при сгибании шеи пациента, расстояние между подбородком и грудью составляет не менее 3 см. Декомпрессия краниовертебрального перехода осуществляется задним срединным доступом. Разрез кожи по Наффцигеру-Тауну производится в шейно-затылочной области по средней линии. Данный разрез обеспечивает доступ к необходимым структурам ЗЧЯ на фоне небольшой травматичности. Верхняя граница разреза ~ 1 см выше наружного затылочного бугра (Inion), нижняя ~ проекция остистого отростка С-2.
Диссекцию мягких тканей предпочтительно выполнять по ходу белой линии (Linea Alba) в аваскулярной зоне. Затылочные артерии и большие затылочные нервы при этом остаются неповрежденными в отличие от стандартного разреза через все слои мягких тканей до чешуи затылочной кости и остистых отростков верхних шейных позвонков, при использовании настоящей методики следует ограничиться рассечением подкожной клетчатки с целью выкраивания лоскута для последующей пластики ТМО.
Лоскут формируется из фрагмента апоневроза и/или выйной связки. При этом следует обратить внимание, что чрезмерное иссечение апоневроза в стороны от средней линии затрудняет герметичное закрытие операционной раны и усугубляет выраженность косметического дефекта за счет формирования очевидного «углубления» мягких тканей. С целью исключения данных осложнений, забор аутофасции для последующей пластики, осуществляется из средних отделов выйной связки вдоль сагиттальной оси. Из указанных собственных тканей пациента выкраивается лоскут в форме ромба, вытянутого по вертикальной оси. Предпочтительный размер большей диагонали ромба составляет 2.5-4.5 см, длина ребра ромба 1.5-2.5 см. Более предпочтительный размер большей диагонали ромба составляет 3.5 см, длина ребра ромба 2 см.
После препаровки мягких тканей осуществляется субпериостальная диссекция чешуи затылочной кости, задней дуги С1 и остистого отростка С2. Пласт, состоящий из глубоких мышц шеи и собственно мышц затылка с помощью распатора или монополярного тока отделяется от верхней выйной линии вниз и в стороны с целью обнажить все необходимые анатомические ориентиры.
При скелетировании чешуи затылочной кости, возможно, венозное кровотечение и/или развитие воздушно-венозной эмболии из гипертрофированных костных выпускников, особенно в проекции наружного затылочного гребня. В этих случаях необходимо своевременное их закрытие с помощью медицинского воска.
С целью тупой диссекции можно использовать небольшой распатор или ложку Фолькмана. Возможное кровотечение из венозных сплетений вертебральных артерии останавливается применением гемостатической марли.
После скелетирования костных структур, область vermian fossa резецируют по направлению от задней губы большого затылочного отверстия на расстояние до 1 см с помощью костных кусачек и/или при помощи высокоскоростного бора, стремясь увеличить размер планируемого трепанационного окна в поперечном направлении в нижних его отделах. После выполнения данного этапа, начиная с нижнего края резецированного участка затылочной кости с помощью высокоскоростной дрели, выполняется субокципитальная краниотомия с размерами костного лоскута приблизительно 2.5-3.5 см × 3.5-4.5 см. Предпочтительные размеры костного лоскута составляют 2.5 × 3.5 см, 3×4 см, 3.5×4.5 см.
Предпочтительной формой лоскута является прямоугольник с закругленной верхней гранью.
Учитывая измененную анатомию костных элементов задней черепной ямки (горизонтальное положение затылочной кости, ее утолщение или асимметрию) у пациентов с Мальформацией Киари I типа, при невозможности резекции со стороны задней губы большого затылочного отверстия в качестве начального этапа выполнения декомпрессии, краниотомия может быть выполнена из фрезевого отверстия, наложенного электротрепаном под точкой Inion по верхней выйной линии. В этом случае, рекомендовано собрать костную «стружку» с целью дальнейшего тампонирования фрезевого отверстия.
С помощью пистолетных кусачек по типу Керрисона производится резекция задней дуги С1. Резекция проводят предпочтительно в стороны на протяжении не более 1.5 см от заднего бугорка. На этапе резекции задней дуги С1 следует помнить о высоком риске повреждения острыми костными отломками вертебральных артерии, расположенных в непосредственной близости от зоны хирургических манипуляций. Остистый отросток С2 играет важную роль в биомеханике и является местом прикрепления нижней косой мышцы головы - единственной мышцы, соединяющей два верхних шейных позвонка. К его резекции прибегают только в случаях измененной анатомии, ограничивающей адекватный обзор и доступ подлежащей твердой мозговой оболочки.
Далее проводят иссечение утолщенной атланто-затылочной мембраны, оказывающей прямую компрессию на опущенные миндалики мозжечка. Вскрытие твердой мозговой оболочки, обычно, сначала производится на верхнешейном уровне. По мере рассечения оболочки тупоконечными ножницами свободные края ее постоянно подтягиваются, чтобы минимизировать риск повреждения церебелло-медуллярной цистерны. Необходимым является сохранение целостности арахноидальной оболочки в ходе оперативного вмешательства, с целью минимизирования рисков перфорации, арахноидальная оболочка поэтапно отграничивается увлаженными хирургическими полосками, малого размера. Разрез твердой мозговой оболочки продолжается вверх с латерализацией на правую или левую гемисферу мозжечка до средних ее отделов.
После рассечения ТМО возможно растягивание и подшивание ее краев к окружающим мышцам временными узловыми швами. Лоскут аутофасции укладывается на место дефекта и фиксируется четырьмя единичными узловыми швами в углах ромба. Прокол иглой производят по направлению «от мозга» с целью уменьшения возможности перфорации арахноидальной оболочки. После этого атравматичной иглой с рассасывающимся материалом накладывается обвивной шов по всему периметру дефекта. Герметичность зашивания проверяется пробой Вальсавы.
Этап реконструкции начинают с моделирования костного лоскута. С помощью бора лоскуту предается необходимая для наиболее плотного прилегания форма: при необходимости стачиваются анатомические (внутренний затылочный гребень) или патологические костные утолщения в рамках измененной анатомии, устраняются неровности и/или зазубрины. В случае общей гипертрофии затылочной кости или асимметричной ее толщины, производится истончение и/или устранение данной диспропорции. При этом следят за минимальным уменьшением толщины пластины, в противном случае она становится хрупкой и непригодной для использования, увеличивается риск аутолизирования.
После этого в костном лоскуте просверливают отверстия, необходимые для его последующей фиксации. Количество отверстий составляет одно и более. Предпочтительное количество отверстий составляет 2-4. Отверстия могут располагаться по боковым сторонам лоскута в нижних их третях. Данные отверстия предназначены для фиксации лоскута пластиной. Расстояние отверстия от края лоскута составляет 2-5 мм. Предпочтительное расстояние отверстий от края составляет 2, 3 мм, еще более предпочтительно - около 3 мм.
Фиксация пластин к боковым поверхностям костного лоскута производится предпочтительно в нижней его трети и также желательно провести фиксацию одной пластины под открытым углом в средней трети верхнего края лоскута. С целью фиксации используются винты или саморезы, соответствующего размера (в зависимость от толщины лоскута 2-4 мм).
При использовании саморезов необходимые раскрытые выше отверстия в костном лоскуте образуются при вкручивании саморезов.
Вторым этапом костный лоскут укладывается на место дефекта и фиксируется к интактной затылочной кости винтами или саморезами соответствующего размера. Затем осуществляется фиксация верхней пластины к затылочной кости под точкой Inion с помощью винта или самореза.
Обязательным условием, является выдвижение нижнего края костного лоскута на толщину кости относительно исходной плоскости. Расстояние, на которое выдвигается кость, является индивидуальным и может составлять 1-4 мм, более предпочтительно на 2, 3 мм. Далее осуществляется жесткая фиксация аутотрансплантата по бокам в нижней трети бокового пропила. После этого осуществляется жесткая фиксация верхнего края лоскута пластиной.
В способе может быть использована прямая, изогнутая или L-образная пластина. Прямая пластина при необходимости может быть согнута под углом 70-120 градусов, предпочтительно, 90 градусов. Предпочтительно использование L-образных пластин или прямых пластин, согнутых под углом 90 градусов. Наличие двух прямых углов у пластины увеличивает запас прочности на изгиб в отличие от прямых пластин
Герметичное зашивание мышечно-апоневротического слоя является важным завершающим этапом операции в связи с повышенным риском развития ликвореи ввиду заведомо нарушенной ликвородинамики на этом уровне у пациентов с Мальформацией Киари I типа. Послойные узловые швы накладываются на все слои мышц, апоневроз и кожу.
Дополнительно изобретение иллюстрируют следующие неограничивающие примеры его реализации. Реализация настоящего изобретения возможна и другими способами.
Примеры
В период с 2017 по 2019 гг. прооперировано 30 взрослых пациентов с применением описываемой методики. Каких-либо осложнений связанных с особенностями используемой методики не отмечено. Клинический исход представленного примера не отличался от такого в общей группе оперированных взрослых пациентов с Мальформацией Киари 1 типа. Конкретный клинический пример приведен ниже.
Пациент 27 лет
Жалобы на упорную головную боль в шейно-затылочной области, нарушение координации.
По данным МРТ исследования выявлена картина Мальформации Киари; дистопия - опущение, заостренных миндаликов мозжечка ниже уровня большого затылочного отверстия, признаки их компрессии нижними отделами уплощенной затылочной кости с нарушением ликвороциркуляции на уровне краниовертебрального перехода.
Пациенту выполнено оперативное вмешательство - задняя декомпрессия краниовертебрального перехода с пластикой твердой мозговой оболочки аутоафасцией и реконструкцией задней черепной ямки аутокостью.
По данным контрольной компьютерной томограммы, выполненной непосредственно после операции, отчетливо видно адекватное положение фиксированного лоскута, обеспечивающее необходимый объем декомпрессии краниовертебрального перехода и восстановление ликворотока на этом уровне. Пациент отметил исчезновение имеющихся жалоб и был выписан из отделения на шестые сутки после операции. По данным контрольной МРТ через 4 месяца очевидная положительная динамика в виде нормализации, краниовертебральных диспропорций, подтягивания и «закругления» миндаликов мозжечка, формирования «новой» затылочной цистерны.
Таким образом, в результате лечения у пациента достигнут положительный клинико-рентгенологический результат в виде исчезновения имеющихся жалоб и нормализации краниовертебральных соотношений. При этом, отсутствует косметический дефект в виде характерного западения мягких тканей в шейно-затылочной области. Каких-либо осложнений, обусловленных применением данной методики не отмечено. Заживление раны первичным натяжением. Отторжения костного аутотрансплантата нет.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЛАСТИКИ КОСТНОГО ДЕФЕКТА ПОСЛЕ ДЕКОМПРЕССИОННОЙ ТРЕПАНАЦИИ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ У ПАЦИЕНТОВ С АНОМАЛИЕЙ АРНОЛЬДА-КИАРИ I ТИПА | 2014 |
|
RU2578544C2 |
| Способ хирургического лечения больных с аномалией Арнольда-Киари | 2016 |
|
RU2635862C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ МАЛЬФОРМАЦИИ КИАРИ I ТИПА И ИМПЛАНТАТ ДЛЯ ПЛАСТИКИ ДЕФЕКТОВ ОСНОВАНИЯ ЧЕРЕПА | 2019 |
|
RU2715454C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АНОМАЛИИ КИАРИ 1 ТИПА | 2001 |
|
RU2194459C1 |
| Способ декомпрессии задней черепной ямки при аномалии Киари 1 типа | 2023 |
|
RU2812752C1 |
| СПОСОБ ПЛАСТИКИ ДУРАЛЬНОЙ ВОРОНКИ ПРИ ФОРМИРОВАНИИ БОЛЬШОЙ ЗАТЫЛОЧНОЙ ЦИСТЕРНЫ У БОЛЬНЫХ С МАЛЬФОРМАЦИЕЙ КИАРИ I-ГО ТИПА | 2005 |
|
RU2290097C2 |
| Способ хирургического лечения мальформации Киари I типа у детей | 2023 |
|
RU2813420C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ СИНДРОМА ВЕРТЕБРО-БАЗИЛЯРНОЙ НЕДОСТАТОЧНОСТИ | 2008 |
|
RU2380042C1 |
| СПОСОБ СОКРАЩЕНИЯ ДЛИТЕЛЬНОСТИ ОПЕРАТИВНОГО ВМЕШАТЕЛЬСТВА ПРИ ПРОВЕДЕНИИ ДЕКОМПРЕССИИ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ | 2014 |
|
RU2594443C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНВАГИНИРОВАННОГО ЗУБОВИДНОГО ОТРОСТКА С2 ПОЗВОНКА, СОЧЕТАЮЩЕГОСЯ С МАЛЬФОРМАЦИЕЙ КИАРИ I ТИПА | 2016 |
|
RU2620888C1 |


Группа изобретений относится к медицине, а именно к нейрохирургии, и может быть использована для лечения мальформации Киари I типа у взрослых. Проводят декомпрессию криниовертебрального перехода с задним срединным доступом, диссекцию мягких тканей, формирование лоскута, субпериостальную диссекцию чешуи затылочной кости и задней дуги С1, резекцию области vermian fossa. Выполняют субокципитальную краниотомию, резекцию задней дуги С1, иссечение утолщенной атланто-затылочной мембраны. Вскрывают твердую мозговую оболочку с сохранением целостности арахноидальной оболочки. Накладывают аутофасцию на место дефекта и фиксируют её. Костный аутотрансплантат для реконструкции задней черепной ямки получают путем модификации костного лоскута, подразумевающей устранение неровностей на его поверхности, придание аутотрансплантату уплощенной прямоугольной формы со скругленными углами. При этом длина боковых противоположных сторон аутотрансплантата составляет от 3,5 до 4,5 см, длина одной из прилегающих к ним сторон составляет от 2,5 до 3,5 см, а другая прилегающая к ним сторона имеет больший радиус закругления. При этом его боковые противоположные стороны имеют прямой или вогнутый контур. Просверливают отверстия по боковым сторонам костного лоскута и/или на верхней стороне костного лоскута, укладывают на место дефекта. Фиксируют полученный аутотрансплантат. При этом происходит выдвижение нижнего края костного лоскута на толщину кости относительно исходной плоскости. Герметично зашивают мышечно-апоневротический слой и кожу. Группа изобретений обеспечивает простоту и минимизацию побочных эффектов за счет использования аутотрансплантатов при закрытии твердой мозговой оболочки и задней черепной ямки. 2 н. и 13 з.п. ф-лы, 4 ил., 1 пр.
1. Способ хирургического лечения мальформации Киари 1 типа у взрослых, характеризующийся проведением декомпрессии криниовертебрального перехода с задним срединным доступом и выполнением следующих действий: диссекцией мягких тканей, выполняемой по белой линии аваскулярной зоны, формированием лоскута из фрагмента апоневроза и/или выйной связки, проведением субпериостальной диссекции чешуи затылочной кости и задней дуги С1, резекцией области vermian fossa по направлению от задней губы большого затылочного отверстия на расстояние до 1 см, выполнением субокципитальной краниотомии с размерами костного лоскута 2.5-3.5 см × 3.5-4.5 см, проведением резекции задней дуги С1, иссечением утолщенной атланто-затылочной мембраны, вскрытием твердой мозговой оболочки с сохранением целостности арахноидальной оболочки, наложением аутофасции на место дефекта и ее фиксацией, реконструкцией задней черепной ямки костным аутотрансплантатом, включающей получение костного аутотрансплантата путем модификации костного лоскута, подразумевающей устранение неровностей на его поверхности, придание аутотрансплантату уплощенной прямоугольной формы со скругленными углами, при этом длина его боковых противоположных сторон составляет от 3,5 до 4,5 см, длина одной из прилегающих к ним сторон составляет от 2,5 до 3,5 см, а другая прилегающая к ним сторона имеет больший радиус закругления, при этом его боковые противоположные стороны имеют прямой или вогнутый контур, выполнение по меньшей мере двух отверстий по боковым сторонам костного лоскута и/или на верхней стороне костного лоскута, укладкой на место дефекта, фиксацией полученного аутотрансплантата угловыми пластинами, при этом происходит выдвижение нижнего края костного лоскута на толщину кости относительно исходной плоскости, герметичным зашиванием мышечно-апоневротического слоя.
2. Способ по п.1, в котором размер костного лоскута составляет 3×4 см.
3. Способ по п.1, в котором резекция задней дуги С1 проводится в стороны на протяжении не более 1,5 см от заднего бугорка.
4. Способ по п.1, в котором модификация костного лоскута включает стачивание внутреннего затылочного гребня и/или патологических костных утолщений на поверхности костного лоскута и/или устранение неровностей и/ или зазубрин по краям костного лоскута.
5. Способ по п.1, в котором выдвижение нижнего края костного лоскута происходит на 1-4 мм относительно исходной плоскости.
6. Способ по п.1, в котором жесткая фиксация аутотрансплантата осуществляется по бокам в нижних отделах краниотомии угловыми пластинами.
7. Способ по п.1, в котором осуществляется жесткая фиксация верхнего края лоскута по меньшей мере одной изогнутой пластиной.
8. Способ по п.7, в котором жесткая фиксация осуществляется по меньшей мере одним саморезом.
9. Костный аутотрансплантат для лечения Мальформации Киари I типа у взрослых пациентов согласно п.1, содержащий фрагмент нижнего отдела затылочной кости и характеризующийся формой в виде уплощенного объема прямоугольной формы со скругленными углами, при этом длина его боковых противоположных сторон составляет от 3,5 до 4,5 см, длина одной из прилегающей к ним стороны составляет от 2,5 до 3,5 см, а другая прилегающая к ним сторона имеет больший радиус закругления, при этом его боковые противоположные стороны имеют прямой или вогнутый контур, также характеризуется равномерной толщиной и наличием по меньшей мере двух отверстий, расположенных на противоположных боковых сторонах трансплантата и/или на верхней стороне трансплантата и предназначенных для его фиксации угловыми пластинами при его установке в зоне дефекта задней черепной ямки.
10. Аутотрансплантат по п.9, приспособленный для крепления по меньшей мере одним винтом или саморезом.
11. Аутотрансплантат по п.9, содержащий одинаковое количество отверстий на противоположных боковых сторонах.
12. Аутотрансплантат по п.9, содержащий по меньшей мере одно отверстие в верхней части.
13. Аутотрансплантат по п. 12, в котором расстояние отверстий от края трансплантата составляет 1-5 мм.
14. Аутотрансплантат по пп. 11, 12, в котором расстояние отверстий от края трансплантата составляет от 2,5 до 3,0 мм.
15. Аутотрансплантат по п.9, содержащий фрагмент чешуи затылочной кости ниже наружнего затылочного выступа.
| Missori P., Rastelli E., Polli F | |||
| et al | |||
| Reconstruction of Suboccipital Craniectomy with Autologous Bone Chips | |||
| Аппарат для электрической передачи изображений без проводов | 1920 |
|
SU144A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ хирургического лечения больных с аномалией Арнольда-Киари | 2016 |
|
RU2635862C1 |
| СПОСОБ ПЛАСТИКИ КОСТНОГО ДЕФЕКТА ПОСЛЕ ДЕКОМПРЕССИОННОЙ ТРЕПАНАЦИИ ЗАДНЕЙ ЧЕРЕПНОЙ ЯМКИ У ПАЦИЕНТОВ С АНОМАЛИЕЙ АРНОЛЬДА-КИАРИ I ТИПА | 2014 |
|
RU2578544C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АНОМАЛИИ КИАРИ 1 ТИПА | 2001 |
|
RU2194459C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ МАЛЬФОРМАЦИИ КИАРИ I ТИПА И ИМПЛАНТАТ ДЛЯ ПЛАСТИКИ ДЕФЕКТОВ ОСНОВАНИЯ ЧЕРЕПА | 2019 |
|
RU2715454C1 |
| Минимально инвазивный способ хирургического лечения мальформации Киари | 2016 |
|
RU2619492C1 |
| Реутов А | |||
| А | |||
Авторы
Даты
2020-09-29—Публикация
2019-12-13—Подача