Область техники, к которой относится изобретение
Настоящее изобретение относится к стерильным сшиваемым in situ полисахаридным композициям для восстановления объема, заполнения или замещения мягких тканей в различных косметических и терапевтических сферах применения. Композиция содержит первое производное полисахарида, функционализированное нуклеофильной группой, и второе производное полисахарида, функционализированное электрофильной группой. Указанные нуклеофильные и электрофильные функциональные группы после совместной инъекции в тело пациента спонтанно образуют in situ ковалентные связи, что приводит к формированию сшитого гидрогеля в месте совместной инъекции.
Уровень техники
В настоящее время инъекционные филлеры применяются во многих терапевтических и косметических сферах для придания объема мягким тканям. В эстетической медицине дермальные филлеры все больше применяются для омоложения лица и выбранных областей тела. Они позволяют улучшить внешний вид элементов лица (например, щек и губ), уменьшить морщины (например, носогубные складки) и борозды и могут в некоторой степени восстановить потерю объема и эластичности кожи и нижележащих тканей, происходящую при старении. В результате кожа выглядит более гладкой и наполненной и, следовательно, моложе.
Известно широкое разнообразие материалов, применяемых в наполнителях мягких тканей. Большинство из этих материалов оказывают временный эффект (от приблизительно трех до восемнадцати месяцев) из-за того, что они рассасываются в теле (например, коллаген, гиалуроновая кислота (ГК), гидроксилапатит кальция (СаНА) и поли-L-молочная кислота (PLLA)). Также существуют несколько постоянных (т.е. нерассасывающихся) наполнителей, таких как утвержденный Федеральным агентством по контролю за продуктами и лекарственными средствами США (FDA) материал-наполнитель на основе полиметилметакрилатных микросфер (ПММА-микросферы). Некоторые наполнители мягких тканей также содержат лидокаин (агент для местной анестезии), который предназначен для уменьшения боли или дискомфорта, связанных с инъекцией.
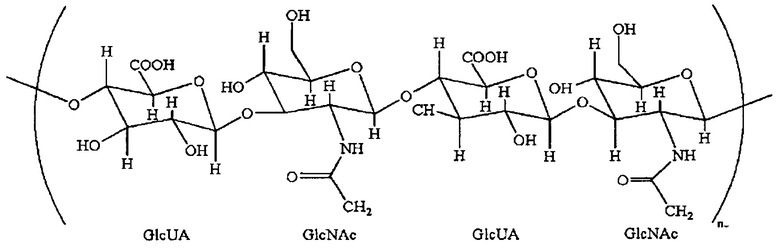
В настоящее время материалом, наиболее часто используемым в мире в качестве наполнителя мягких тканей, является гиалуроновая кислота (ГК). Это обусловлено ее исключительной способностью создавать объем и благоприятным профилем безопасности. ГК представляет собой гликозаминогликан природного происхождения, присутствующий в экстраклеточном матриксе, например дерме, и образованный из чередующихся остатков β-D-(1→3)-глюкуроновой кислоты (GlcUA) и β-D-(1→4)-N-ацетилглюкозамина (GlcNAc). ГК может соединяться с водой и набухать в гелеобразной форме, что создает эффект гладкости/наполненности. В большинстве случаев ГК, применяемая в дермальных филлерах, является сшитой, что продлевает срок ее действия в теле (от приблизительно шести до восемнадцати месяцев).
В данной области известны различные подходы к сшиванию для ковалентного связывания полимерных цепей молекул полисахаридов (например, ГК) друг с другом для формирования матрикса материала-наполнителя при помощи внутримолекулярных и межмолекулярных сшивок. Широко применяемым подходом является химическое сшивание при помощи химических агентов. Эти агенты обычно взаимодействуют с гидроксильными и/или карбоксильными функциональными группами полисахарида. К обычно применяемым сшивающим агентам относятся, без ограничений, DVS (дивинилсульфон), двух- или многофункциональные эпоксиды (например, 1,4-бутандиола диглицидиловый эфир (BDDE)), 1,2-бис(2,3-эпоксипропокси)этилен (EGDGE) и 1,2,7,8-диэпоксиоктан (DEO)), сшивающие агенты на основе ПЭГ (например, пентаэритритолтетраглицидиловый эфир (PETGE)), бискарбодиимиды (BCDI) (например, фениленбис-(этил)-карбодиимид и 1,6-гексаметиленбис-(этилкарбодиимид)), диаминовые или мультиаминовые сшивающие агенты (например, гексаметилендиамин (HMDA) и 3-[3-(3-аминопропокси)-2,2-бис(3-аминопропоксиметил)-пропокси]-пропиламин (4АА)), бис(сульфосукцинимидил)суберат (BS), 1-(2,3-эпоксипропил)-2,3-эпоксициклогексан, эпихлоргидрин, альдегиды (например, формальдегид и глутаральдегид) и гидразиды (бис-, трис- и поливалентные гидразидные соединения, например адипиновый дигидразид (ADH)).
К другим способам, применяемым для сшивания инъекционных полисахаридных гидрогелей, относятся фотохимическое сшивание метакрилированных полимеров (Moller et al., Int. J. Artif. Organs 2011, 34:93-102), сшивание посредством реакции присоединения Михаэля (Shu et al., Biomacromolecules 2002, 3:1304-1311), сшивание посредством реакции с основаниями Шиффа (Tan et ah, Biomaterials 2009, 30:2499-2506), подходы клик-химии с применением таких реакций, как тиоленовая реакция или азид-алкиновое циклическое присоединение (Hoyle et al., Chem. Soc. Rev. 2010, 39:1355-1387; van Dijk et al., Bioconjug. Chem. 2009, 20:2001-2016). В данной области также известны фотосшитые наполнители на основе полисахаридов для восстановления объема мягких тканей (см., например, WO 2011/069475). Кроме того, в данной области была изучена эстерификация карбоксильных функциональных групп кислых полисахаридов с гидроксильными группами той же или другой молекулы полисахарида, что, таким образом, приводит к образованию «внутренних» межмолекулярных и/или внутримолекулярных сложноэфирных сшивок (называется «самосшитым полимером» или «АСР»). Более того, в US 2006/0084759 описан модифицированный тирамином и сшитый ГК-гидрогелевый материал, причем сшивание осуществляется посредством опосредуемых пероксидазой дитираминовых связей, которые можно осуществить in vivo.
Однако традиционные подготовленные гидрогели часто имеют недостаток - они слишком вязкие, чтобы их можно было вводить тонкими иглами. Поэтому было приложено много усилий для разработки загустевающих in situ гидрогелевых композиций, подходящих для разных областей применения. Эти композиции вводят в ткань в жидком виде, а не в виде предварительно подготовленного геля. Например, в WO 95/15168 описан синтез гидразидных производных ГК с использованием реакций связывания с EDC (1-этил-3-(3-диметиламинопропил)карбодиимидом). Гидразид-ГК можно сшивать при помощи гомо- или гетеробифункциональных сшивающих агентов или сшивающих агентов Трота с образованием гидрогеля для доставки лекарственного средства. В WO 00/016818 раскрыто образование гидрогеля in situ посредством сшивания функционализированного альдегидом или амином производного ГК (например, адипиновой дигидразидо-ГК) при помощи гомо- или гетеробифункционального сшивающего агента (например, бифункционального сшивающего агента на основе сложного эфира N-гидроксисукцинимида, такого как (SPA)1-ПЭГ).
Более того, в WO 01/40314 раскрыта гидрогелевая композиция, содержащая окисленный полисахарид, например альгинатный полимер с альдегидными группами (PAG), и по меньшей мере один сшивающий агент, имеющий две или более функциональных групп, способных обратимо сшивать полисахарид в гидрогелевую систему, такой как сшивающий агент дигидразид адипиновой кислоты (ADH). Дополнительно в WO 2011/100469 раскрыт сшитый ГК-гидрогель, предназначенный для применения в качестве биоматериала протеза стекловидного тела глаза, полученный взаимодействием окисленной ГК, несущей альдегидные функциональные группы (окси-ГК), с дигидразидным сшивающим агентом, например дигидразидом адипиновой кислоты (ADH).
Кроме того, в WO 2009/108100 раскрыт гидрогель на основе ГК, получаемый in situ посредством смешивания модифицированной альдегидом ГК и сшивающего реагента (модифицированного гидразидом поливинилового спирта (PVAH)) с формированием сшитой структуры, имеющей множество гидроксильных групп. В WO 2011/069475 раскрыты способ получения альдегидного производного ГК, содержащего альдегидную группу, путем окисления первичной гидроксильной группы у С6 глюкозаминового повторяющегося звена с применением системы TEMPO (2,2,6,6-тетраметилпиперидинилокси)/соокислитель и применение указанного альдегидного производного ГК для получения сшитых ГК-гидрогелей путем взаимодействия с диаминовым соединением (например, гександиамином) или амин-ГК (например, с гександиамин-замещенной ГК).
Dahlmann et al. (Biomaterials 2013, 34:940-951) описывают полностью сформированные сшиваемые in situ альгинатные и ГК-гидрогели для миокардиальной тканевой инженерии. Гидрогели получают взаимодействием функционализированного альдегидом и гидразидом альгината с ГК в присутствии человеческого коллагена типа I и неонатальных клеток сердца крысы (NRHC) с получением сшитой гидразоном биосинтетической сердечной ткани на основе гидрогеля.
Ossipov et al. (Biomacromolecules 2010, 11:2247-2254) описывают синтез функционализированной гидразидом ГК с применением конкретного симметричного двухфункционального реагента, имеющего центральную двухвалентную защитную группу, который может вступать в реакцию амидного типа с карбоксилатным остатком ГК в водном растворе. Функционализированную гидразидом ГК можно применять для формирования in situ гидразонового ГК-гидрогеля путем смешивания с альдегидным производным ГК. Полученный гидрогель подходит для применения в тканевой инженерии в качестве средства доставки факторов роста.
Varghese et al. (J. Am. Chem. Soc. 2009, 131:8781-8783) сообщают о производном ГК, имеющем двойную функционализацию гидразидной группой и аминометиленбисфосфонатной группой и способном ковалентно связываться с бисфосфонатом (БФ; антиостеокластическое и антинеопластическое низкомолекулярное лекарственное средство). Смешивание указанной двойной функционализированной ГК с функционализированной альдегидом ГК приводит к формированию in situ инъекционного ГК-гидрогеля для контролируемого высвобождения лекарственного средства БФ в месте имплантации.
Oommen et al. (Adv. Funct. Mater 2013, 323:1273-1280) описывают ГК-гидрогель, получаемый смешиванием альдегидного производного ГК с функционализированным карбодигидразидом (CDH) производным ГК с получением ГК-гидрогеля с гидразоновыми связями. Дополнительно описано, что формирование ГК-гидрогеля in situ в присутствии терапевтического белка (например, рекомбинантного человеческого фактора роста ВМР-2) позволяло получить гидрогель для сфер применения in vivo, способный обеспечивать доставку факторов роста для регенерации костной ткани.
Во многих клинических вариантах применения желательными являются сшиваемые in situ полисахаридные гидрогели, поскольку их можно легко вводить даже тонкими иглами, что помогает лучше контролировать скорость инъекции и упрощает манипуляции со шприцем. Кроме того, из сшиваемых in situ полисахаридных гидрогелей можно сформировать любые сложные формы, а затем, после сшивания, они легко смешиваются с биологическими агентами и/или клетками и связываются с заданной тканью в процессе формирования геля.
Однако существующие сшиваемые in situ гидрогелевые композиции являются неудовлетворительными, поскольку не демонстрируют одного или более свойств, желаемых или необходимых для предполагаемого применения. По существу, сшиваемая in situ гидрогелевая композиция должна быть биологически совместимой, неиммуногенной, не вызывающей воспаления и безопасной. Она не должна взаимодействовать с биологическими компонентами в окружающих тканях, не должна генерировать вредных побочных продуктов и должна эффективно сшиваться in situ после введения. Также она должна быть биоразлагаемой, но одновременно обеспечивать достаточно длительное существование in vivo. Более того, важно, чтобы сшиваемые in situ гидрогели можно было вводить через тонкую иглу, однако для этого требуется, чтобы вязкость вводимой сшиваемой in situ гидрогелевой композиции была достаточно низкой.
Раскрытие изобретения
В свете вышеизложенного целью настоящего изобретения является получение сшиваемой in situ композиции, которая может легко экструдироваться через тонкие иглы и которая после введения формирует in situ сшитый гидрогель с желаемыми свойствами (например, механическими, химическими, реологическими, биологическими и иммунологическими свойствами) для восстановления объема, заполнения или замещения мягких тканей в различных косметических и терапевтических сферах применения.
Вышеуказанная цель достигается путем получения двух функционализированных производных полисахарида, которые спонтанно образуют ковалентные сшивки после введения в тело пациента (т.е. в условиях in vivo). Сформированная таким образом сшитая in situ полисахаридная сеть в виде гидрогеля действует в качестве наполнителя мягких тканей, например дермального филлера. Сшиваемая in situ полисахаридная композиция настоящего изобретения имеет преимущество, заключающееся в том, что два функционализированных производных полисахарида можно совместно вводить в жидком виде, таким образом обеспечивая совместную инъекцию с малыми силами экструзии даже через тонкие иглы. Желательно, чтобы при формировании геля in situ не образовывались никакие вредные побочные продукты. Единственным побочным продуктом является вода, которая легко поглощается сформированным гидрогелем и/или окружающими тканями. Кроме того, сформированный in situ гидрогель обладает желаемыми свойствами с точки зрения обеспечения целостности ткани, улучшения кожи, способности формировать ткань и способности создавать объем.
В первом аспекте настоящее изобретение относится к применению первого производного полисахарида и второго производного полисахарида для формирования in situ сшитого гидрогеля в косметических сферах применения, причем первое производное полисахарида функционализировано нуклеофильной группой, а второе производное полисахарида функционализировано электрофильной группой, и как первое, так и второе производные полисахарида являются стерилизованными, и при этом нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области.
В другом аспекте в соответствии с настоящим изобретением предложено первое производное полисахарида, предпочтительно в виде первого раствора-предшественника, и второе производное полисахарида, предпочтительно в виде второго раствора-предшественника, как определено в настоящем документе, для формирования in situ сшитого гидрогеля в терапевтических сферах применения. К терапевтическим сферам применения или показаниям относятся, без ограничений, недержание мочи при напряжении, вагинальная сухость, пузырно-мочеточниковый рефлюкс, недостаточность голосовой складки и медиализация голосовой складки.
В дополнительном аспекте в соответствии с настоящим изобретением предложена комбинация первого производного гиалуроновой кислоты (ГК) и второго производного гиалуроновой кислоты (ГК), как определено в настоящем документе, предпочтительно в виде первого раствора-предшественника, содержащего первое производное гиалуроновой кислоты (ГК), и второго раствора-предшественника, содержащего второе производное гиалуроновой кислоты (ГК).
В еще одном аспекте в соответствии с настоящим изобретением предложена многоцилиндровая шприцевая система, предварительно заполненная по меньшей мере (а) первым раствором-предшественником, содержащим первое производное полисахарида, как определено в настоящем документе, в одном цилиндре и (b) вторым раствором-предшественником, содержащим второе производное полисахарида, как определено в настоящем документе, в другом цилиндре.
В еще одном аспекте в соответствии с настоящим изобретением предложен набор для формирования in situ сшитого полисахаридного гидрогеля, содержащий (i) первый контейнер, содержащий первый раствор-предшественник первого производного полисахарида, как определено в настоящем документе, и (ii) второй контейнер, содержащий второй раствор-предшественник второго производного полисахарида, как определено в настоящем документе, и необязательно (iii) инструкции по применению.
В еще одном аспекте в соответствии с настоящим изобретением предложен способ формирования in situ сшитого полисахаридного гидрогеля в косметических или терапевтических сферах применения, включающий в себя этапы:
(а) получения первого раствора-предшественника первого производного полисахарида и отдельно от него второго раствора-предшественника второго производного полисахарида, причем первое производное полисахарида функционализировано нуклеофильной группой, а второе производное полисахарида функционализировано электрофильной группой, и как первый, так и второй растворы-предшественники являются стерилизованными,
(b) смешивания первого раствора-предшественника и второго раствора-предшественника с получением сшиваемого in situ смешанного раствора, и
(c) инъекции смешанного раствора в целевую область тела пациента, при этом нуклеофильная группа первого производного полисахарида и электрофильная группа второго производного полисахарида образуют in situ ковалентную связь, что приводит к формированию сшитого гидрогеля в целевой области.
Конкретные варианты осуществления настоящего изобретения представлены в прилагаемой формуле изобретения.
Краткое описание чертежей
Для более полного понимания настоящего изобретения дана ссылка на следующее описание и прилагаемые чертежи, где:
на ФИГ. 1 представлено изображение трапециевидного объемного заполнения в коже исследуемого кролика 1, сформированного загустевшим in vivo исследуемым препаратом 1 в момент времени t=0 ч после внутрикожной инъекции 200 мкл в виде одного туннеля (область D; слева вверху), двух туннелей (область I; справа вверху) и четырех болюсов (область J; справа внизу). Контрольный раствор PBS (200 мкл) введен в область Е (слева внизу); и
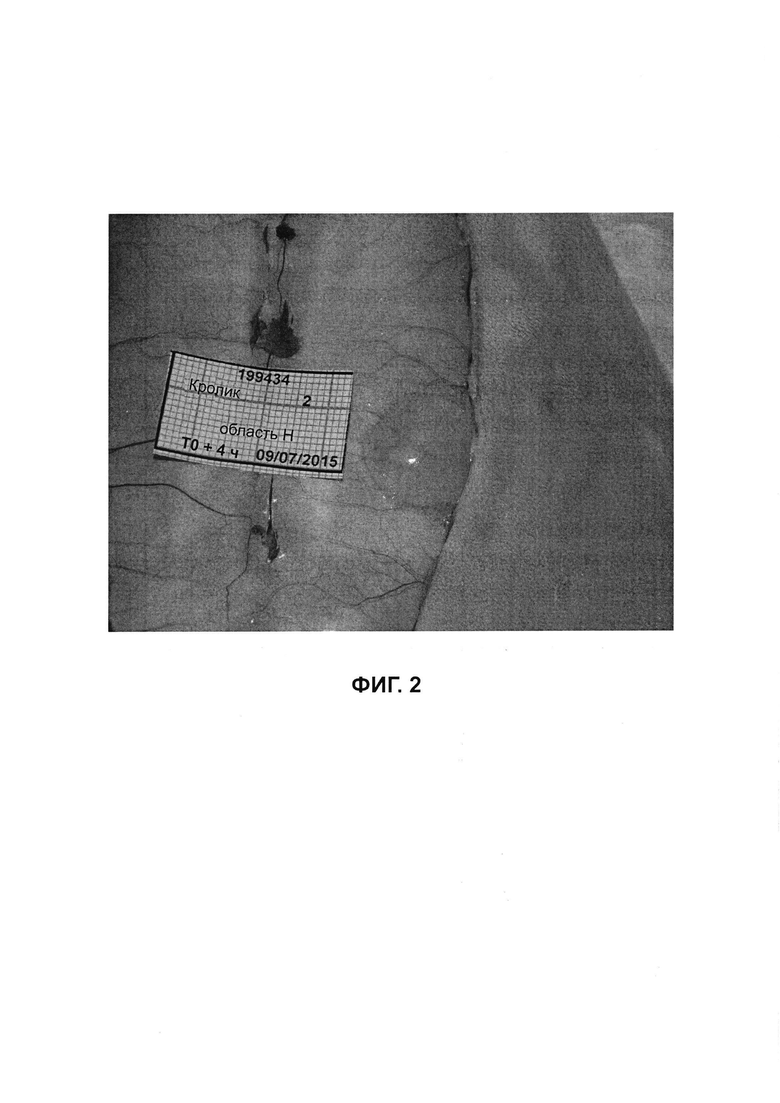
на ФИГ. 2 представлено макроскопическое изображение просматриваемой после вскрытия кожи выпуклости, образованной исследуемым препаратом 2 в момент времени t=4 ч после субдермальной инъекции 1000 мкл кролику 2.
Осуществление изобретения
Стерильную сшиваемую in situ полисахаридную композицию настоящего изобретения можно легко вводить через тонкие иглы с небольшим усилием при инъекции, и она обеспечивает улучшение кожи, формирование кожи или способствует восстановлению объема. В частности, сшиваемую in situ композицию можно удобно наносить на целевую ткань путем инъекции в виде стерильной жидкой смеси с низкой вязкостью, полученной одновременно с инъекцией путем простого физического смешивания двух стерильных растворов-предшественников, каждый из которых содержит разные функционализированные производные полисахарида. Преимуществом является возможность применения тонких игл, что, в свою очередь, представляет больший комфорт для пациента (уменьшение боли при инъекции, снижение противодействующего давления) и дополнительно позволяет пользователю точно и безопасно (без закупорки сосудов) вводить гидрогель в желаемые целевые области, например различные слои кожи.
Более того, введенная смесь растворов-предшественников быстро и эффективно сшивается in situ с формированием сшитого ковалентными связями гидрогеля в целевой области тела. Для индукции реакции сшивания не требуются добавки, катализаторы, изменение рН, УФ-излучение или любые другие внешние стимулы (или «триггеры»). В частности, не применяется и не требуется никакой сшивающий агент. Единственным побочным продуктом реакции сшивания обычно является вода, которая легко поглощается гидрогелем и/или окружающими тканями. Более того, функционализированные производные полисахаридов настоящего изобретения можно относительно легко синтезировать, обычно в ходе одноэтапной реакции, а также преимуществом является то, что их можно легко стерилизовать влажным паром (например, путем паровой стерилизации, предпочтительно автоклавированием).
Более того, сформированный in situ сшитый гидрогель демонстрирует благоприятные механические, химические и реологические свойства для применения в качестве наполнителя мягких тканей. В частности, он высокоэффективен для создания объема. Кроме того, сшитый in situ гидрогель настоящего изобретения имеет длительный (пролонгированный) период удерживания in vivo, хотя и сохраняет способность к биоразложению. Кроме того, при необходимости он может содержать анестетики (например, лидокаин) и различные другие компоненты (например, клетки, включая стволовые клетки и адипоциты, жир, липиды, факторы роста и витамины). Следовательно, сшиваемая in situ композиция настоящего изобретения особенно хорошо подходит для применения в качестве дермального филлера для косметических (эстетических) целей.
В первом аспекте настоящее изобретение относится к применению первого производного полисахарида и второго производного полисахарида для формирования in situ сшитого гидрогеля в косметических сферах применения. Первое производное полисахарида функционализировано нуклеофильной группой, а второе производное полисахарида функционализировано электрофильной группой. Кроме того, как первое, так и второе производное полисахарида являются стерилизованными. Нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию в целевой области сшитого гидрогеля.
При использовании в настоящем документе термин «in situ» означает место введения. Таким образом, чтобы сформировать гидрогель в месте введения, первое и второе производные полисахарида по существу вводят путем совместной инъекции или иным образом наносят вместе в конкретную область (целевую область) внутри тела пациента, например в область, по эстетическим причинам нуждающуюся в восстановлении объема ткани, и допускают их ковалентную сшивку в области совместной инъекции. В рамках настоящего изобретения термины «in situ» и «in vivo» могут применяться взаимозаменяемо. «Пациент» в рамках настоящего изобретения может представлять собой любого индивида или субъекта, например млекопитающего, а предпочтительно человека, нуждающегося в лечении конкретного расстройства, состояния или заболевания, например в косметических (эстетических) или терапевтических целях.
В контексте настоящего изобретения термин «совместная инъекция» по существу означает, что первое производное полисахарида и второе производное полисахарида вводят совместно в виде единой жидкой композиции, например раствора, в целевую область тела пациента. Термин «инъекционный» или «инъекция» при применении в настоящем документе означает, что композиция, формирующая in situ гидрогель, может подаваться из шприца или шприцевой системы. В частности, термин «совместная инъекция» предпочтительно означает, что первое производное полисахарида и второе производное полисахарида смешивают, в частности смешивают гомогенно, до выхода из кончика иглы и попадания в целевую область тела пациента, а затем вводят в целевую область тела пациента в виде смеси. В рамках настоящего изобретения термины «инъекция» или «совместная инъекция» могут означать внутрикожную, междермальную или субдермальную инъекцию или подкожную инъекцию. Кроме того, термин «игла» при применении в настоящем документе должен включать в себя или должен быть синонимом термина «канюля» или любых других иглообразных объектов, подходящих для инъекции.
Термин «гидрогель» при применении в настоящем документе означает набухающую в воде трехмерную сеть, состоящую из ковалентно сшитых полимерных цепей. Сшитый in situ (или «загустевший») гидрогель предпочтительно является когезивным. Термин «когезивный» или «когезивность» в контексте настоящего изобретения определяется как способность материала (например, гидрогеля) не диссоциировать вследствие аффинности его молекул друг к другу. Когезивность является ключевой характеристикой гелевых имплантатов (например, загустевших in situ гидрогелей согласно настоящему описанию) и считается необходимой для того, чтобы твердая и жидкая фазы геля оставались неизменными, и, следовательно, для целостности геля. В контексте настоящего изобретения когезивность полисахаридного гидрогеля, в частности гидрогеля на основе ГК, можно определить по шкале когезивности Гаварда - Сундарама (Sundaram et al., Plast. Reconstr. Surg. 136:678-686, 2015).
Термин «спонтанный» или «спонтанно» при применении в настоящем документе должен означать тот факт, что нуклеофильная группа первого производного полисахарида и электрофильная группа второго производного полисахарида образуют ковалентную связь в условиях in vivo, т.е. после совместной инъекции в целевую область тела пациента без каких-либо внешних стимулов (также называемых «триггерами»), таких как нагрев или УФ-излучение, что приводит к формированию in situ сшитого полисахаридного гидрогеля в целевой области.
В контексте настоящего изобретения сформированный in situ (или in vivo) гидрогель по существу подходит для применения и применяется в качестве и/или функционирует в качестве наполнителя (филлера) мягких тканей. Термин «наполнитель (филлер) мягких тканей» при применении в настоящем документе по существу означает материал, выполненный с возможностью увеличения объема в областях с недостатком мягкой ткани. Имеется в виду, например, восстановление объема, наполнение или замещение мягких тканей. В настоящем документе термин «мягкие ткани» по существу относится к тканям, которые соединяют, поддерживают или окружают другие структуры и органы тела. К мягким тканям относятся, например, мышцы, сухожилия (группы волокон, которые соединяют мышцы с костями), волокнистые ткани, жир, кровеносные сосуды, нервы и синовиальные ткани (ткани вокруг суставов). В контексте настоящего изобретения наполнитель мягких тканей предпочтительно представляет собой дермальный филлер.
Термин «производное» при применении в настоящем документе предпочтительно относится к полисахариду, функционализированному нуклеофильной группой или электрофильной группой и подходящему для формирования in situ (или in vivo) сшитого полисахаридного гидрогеля в области введения в тело пациента. Функционализированные производные полисахарида в соответствии с настоящим изобретением предпочтительно не содержат никаких других химических модификаций, кроме нуклеофильной группы или электрофильной группы.
Как первое, так и второе производное полисахарида обычно являются стерилизованными. Термин «стерилизованный» или «стерильный» при применении в настоящем документе должен означать тепловую стерилизацию, в частности стерилизацию влажным паром (например, паровую стерилизацию), а предпочтительно относится к автоклавированию. Автоклавирование можно проводить при температуре от 120°С до 132°С в течение 0,3-20 мин или при температуре от 121°С до 130°С в течение 0,5-10 мин, например при 121°С в течение 0,5-2 мин.
Первое производное полисахарида предпочтительно присутствует в виде первого стерильного раствора-предшественника, а второе производное полисахарида предпочтительно присутствует в виде второго стерильного раствора-предшественника.
Первый и второй стерильные растворы-предшественники обычно имеют низкую комплексную вязкость от 0,001 Па⋅с до 5,0 Па⋅с, в частности от 0,005 Па⋅с до 3,0 Па⋅с, предпочтительно от 0,001 Па⋅с до 1,0 Па⋅с, более предпочтительно от 0,001 Па⋅с до 0,1 Па⋅с по данным колебательных реологических измерений при 1 Гц и 25°С. Более того, первый и второй раствор-предшественник могут оба характеризоваться низкой силой экструзии от 0,01 Н до 15 Н, предпочтительно от 0,1 Н до 10 Н, более предпочтительно от 0,5 Н до 7,5 Н, а наиболее предпочтительно от 0,01 Н до 50 Н или от 1,0 Н до 5,0 Н по данным измерений через иглу 30G (TSK Laboratory) при скорости экструзии приблизительно 0,21 мм/с при использовании стандартного стеклянного шприца объемом 1,0 мл (BD Нурак SCF, 1 мл, длинный RF-PRTC, ISO 11040, внутренний диаметр 6,35 мм).
В соответствии с настоящим изобретением первое и второе производные полисахарида смешиваются в ходе совместной инъекции с формированием жидкой сшиваемой in situ композиции, содержащей смесь первого и второго производных полисахарида. Как правило, как первое производное полисахарида, так и второе производное полисахарида представлены отдельно в виде первого раствора-предшественника и второго раствора-предшественника, соответственно. Смешивание этих двух растворов-предшественников в процессе инъекции (или «совместной инъекции») позволяет получить жидкую сшиваемую in situ композицию, которая в итоге выходит из иглы и вживляется (имплантируется) в тело.
Жидкая сшиваемая in situ композиция предпочтительно имеет комплексную вязкость от 0,1 Па⋅c до 100 Па⋅c, или от 0,1 Па⋅с до 75 Па⋅c, или от 1,0 Па⋅c до 75 Па⋅с, более предпочтительно от 1 Па⋅с до 50 Па⋅c или от 5 Па⋅с до 50 Па⋅с при измерении так, как описано выше. Более того, усилие при инъекции для композиции предпочтительно составляет от 0,01 Н до 20 Н или от 0,01 до 10 Н, более предпочтительно от 0,1 Н до 10 Н и наиболее предпочтительно от 1,0 Н до 5,0 Н при измерении так, как описано выше.
Смешивание и инъекцию (или «совместную инъекцию») можно осуществлять с применением двухцилиндрового шприца, как описано ниже в настоящем документе, или любой другой подходящей шприцевой системы, в которой первое и второе производные полисахарида физически разделены до момента одновременной экструзии, сопутствующего перемешивания и совместной инъекции смешанных первого и второго производных полисахарида с помощью иглы (канюли) в тело пациента. Таким образом, совместная инъекция должна быть настолько быстрой, чтобы избежать предварительного сшивания до попадания первого и второго производных полисахарида в целевую область тела. С другой стороны, время загустевания должно быть целесообразно коротким, чтобы предотвратить распространение введенного при совместной инъекции материала в окружающие ткани.
Количество первого производного полисахарида, присутствующего в первом растворе-предшественнике, может составлять от 0,1 мас. % до 5,0 мас. %, предпочтительно от 0,5 мас. % до 4,0 мас. %, более предпочтительно от 1,0 мас. % до 3,0 мас. % и наиболее предпочтительно от 1,5 мас. % до 2,5 мас. %, а количество второго производного полисахарида, присутствующего во втором растворе-предшественнике, может составлять от 0,1 мас. % до 5,0 мас. %, предпочтительно от 0,5 мас. % до 4,0 мас. %, более предпочтительно от 1,0 мас. % до 3,0 мас. % и наиболее предпочтительно от 1,5 мас. % до 2,5 мас. %. Более того, массовое соотношение совместно вводимых первого и второго производных полисахарида составляет предпочтительно от 15:85 до 85:15, более предпочтительно от 30:70 до 70:30 и наиболее предпочтительно от 40:60 до 60:40 или 50:50 (первое производное ко второму производному).
Более того, первый и/или второй раствор-предшественник может (могут) содержать дополнительные вещества, например клетки, включая стволовые клетки, и адипоциты, жир, липиды, факторы роста, цитокины, лекарственные средства и биологически активные вещества. Более конкретно, первый и/или второй раствор-предшественник может (могут) содержать агенты для местной анестезии, многоатомные спирты, витамины, соли щелочных и щелочноземельных металлов, металлы, антиоксиданты, аминокислоты и керамические частицы.
В контексте настоящего изобретения добавление местного анестетика является особенно желательным в свете его способности уменьшать боль при инъекции. Примеры агентов для местной анестезии включают в себя, без ограничений, амбукаин, амоланон, амилокаин, беноксинат, бензокаин, бетоксикаин, бифенамин, бупивакаин, бутакаин, бутамбен, бутаниликаин, бутетамин, бутоксикаин, картикаин, хлоропрокаин, кокаэтилен, кокаин, циклометикаин, дибукаин, диметизоквин, диметокаин, диперодон, дицикломин, экгонидин, экгонин, этилхлорид, этидокаин, бета-эукаин, эупроцин, феналкомин, формокаин, гексилкаин, гидрокситетракаин, изобутила п-аминобензоат, лейцинокаина мезилат, левоксадрол, лидокаин, мепивакаин, меприлкаин, метабутоксикаин, метилхлорид, миртекаин, наепаин, октокаин, ортокаин, оксетазаин, парэтоксикаин, фенакаин, фенол, пиперокаин, пиридокаин, полидоканол, прамоксин, прилокаин, прокаин, пропанокаин, пропаракаин, пропипокаин, пропоксикаин, псевдококаин, пиррокаин, ропивакаин, салициловый спирт, тетракаин, толикаин, тримекаин, золамин и их соли.
Анестезирующим агентом предпочтительно является лидокаин, например, в виде лидокаина HCl. Первый и/или второй раствор-предшественник может (могут) иметь концентрацию лидокаина, например, от 0,05 мас. % до 8,0 мас. %, от 0,1 мас. % до 4,0 мас. %, от 0,2 мас. % до 3,0 мас. %, от 0,3 мас. % до 2,0 мас. % или от 0,4 мас. % до 1,0 мас. %.
К подходящим многоатомным спиртам для применения в настоящем изобретении относятся, без ограничений, глицерин, маннит, сорбит, пропиленгликоль, эритрит, ксилит, мальтит и лактит.Особенно подходящими для применения в настоящем изобретении являются маннит и глицерин. Кроме того, многоатомный спирт предпочтительно представляет собой гликоль, необязательно в комбинации с одним или более из перечисленных выше соединений многоатомных спиртов, в частности маннитом. К подходящим витаминам относятся витамин С, витамин Е и витамины группы В, т.е. один или более из витаминов В1 В2, В3, В5, В6, В7, В9 и В12. Витамины можно вводить для стимуляции и поддержания клеточного метаболизма и, таким образом, для повышения выработки коллагена. Особенно предпочтительным в данном случае является применение витамина С, витамина Е и витамина В6. Предпочтительной солью для применения в композиции наполнителя мягких тканей является соль цинка. Керамические частицы предпочтительно представляют собой частицы гидроксиапатита, например, частицы гидроксиапатита кальция (СаНА).
В рамках настоящего изобретения электрофильная группа предпочтительно представляет собой альдегидный остаток, а нуклеофильная группа может быть выбрана из амино, аминоокси, карбазата или гидразидного остатка и предпочтительно представляет собой гидразидный остаток. Термин «альдегидный остаток» при применении в настоящем документе включает в себя альдегидную функциональную группу (т.е. -СНО представляет собой «формил») или любую группу или остаток, имеющий боковую функциональную группу -СНО, в частности альдегидную (т.е. -СНО) концевую группу (например, линейную или разветвленную C1-C6 алкильную или алкенильную группу с концевой группой -СНО).
Функционализированное альдегидом производное полисахарида для применения в настоящем изобретении содержит предпочтительно интактные циклические полисахаридные кольца. Это означает, что функционализированное альдегидом производное полисахарида не содержит окисленных открытых колец сахаридных звеньев (также называемых «линеаризованными» сахаридными звеньями). Таким образом, в соответствии с этим предпочтительным вариантом осуществления в настоящем документе можно применять любой способ получения функционализированного альдегидом производного полисахарида, при условии что он не вызовет открытия колец циклических сахаридных звеньев полисахаридов. Соответственно, часто используемый на предшествующем уровне техники способ введения альдегидных групп в полисахариды путем окисления соседних диолов в мономерных сахаридных звеньях с помощью периодата (например, NaIO4) предпочтительно не применяется и предпочтительно исключается из настоящего изобретения.
Термин «гидразидный остаток» при применении в настоящем документе включает в себя гидразидную функциональную группу и гидразидные концевые группы или остатки, обычно имеющие общее число углеродных атомов не более 15, 10, 5, 4, 3 или 2. Гидразидный остаток предпочтительно представляет собой гидразидный (т.е. [полисахарид]-С(O)-NH-NH2) или дигидразидный остаток, в особенности дигидразидный остаток общей формулы
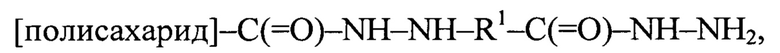
где R1 = ковалентная связь, С(=O), C(=O)-O-R2, (C=O)-R2, причем R2 = линейная или разветвленная C1, C2, С3, С4, С5 или C6 алкильная или алкенильная группа. Особенно предпочтительным для применения в настоящем документе является карбодигидразид (CDH). Если в качестве гидразидного остатка применяется CDH, соединенный с карбоксильной группой полисахарида, полученный модифицированный полисахарид имеет следующий боковой остаток с гидразидом на конце: полисахарид-С(=O)-R, где R представляет собой NH-NH-C(=O)-NH-NH2.
Полисахарид в первом и втором производных полисахарида может быть выбран из природных полисахаридов и полусинтетических полисахаридов. К конкретным примерам подходящих карбоксильных полисахаридов относятся карбоксилированная целлюлоза и производные карбоксилированной целлюлозы (например, карбоксиметилцеллюлоза, карбоксиэтилцеллюлоза, карбоксиметилэтилцеллюлоза), карбоксиметилдекстран, карбоксиметилкрахмал, альгинат, гиалуроновая кислота, пектин, хитин, хондроитинсульфат, дерматансульфат, гепарин, гепаринсульфат, гепаросан и т.п.
Первое производное полисахарида предпочтительно основано на гиалуроновой кислоте, альгинате, гепаросане, гепарине или гепаринсульфате, а второй функционализированный полисахарид предпочтительно основан на гиалуроновой кислоте, целлюлозе, хитозане, хитине или гепаросане. Особо предпочтительно, если как первое производное полисахарида, так и второе производное полисахарида основаны на гиалуроновой кислоте или альтернативно основаны на гепаросане, или первое производное полисахарида основано на гепаросане, а второе производное полисахарида основано на гиалуроновой кислоте, или первое производное полисахарида основано на гиалуроновой кислоте, а второе производное полисахарида основано на гепаросане.
В соответствии с предпочтительным аспектом настоящего изобретения первое производное полисахарида представляет собой (первое) функционализированное гидразидом производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой (второе) функционализированное альдегидом производное гиалуроновой кислоты (ГК). При сшивании in situ функционализированное гидразидом производное ГК и функционализированное альдегидом производное ГК формируют сшитый гидразоном гидрогель гиалуроновой кислоты (ГК).
Все определения, объяснения и описания, приведенные выше относительно применения первого и второго производных полисахарида, также применимы к первому и второму производным гиалуроновой кислоты (ГК), если особо не указано иное. Более того, любая конкретная ссылка на гиалуроновую кислоту или ГК также может включать в себя гепаросан. Иными словами, в тексте настоящей заявки термин «гиалуроновая кислота» или «ГК» может включать в себя «гепаросан» или может быть заменен на «гепаросан».
Гидразидный остаток функционализированного гидразидом производного гиалуроновой кислоты (ГК) и альдегидный остаток функционализированного альдегидом производного гиалуроновой кислоты (ГК) предпочтительно определены так, как приведено выше в настоящем документе. Следовательно, гидразидный остаток предпочтительно представляет собой гидразидную или дигидразидную группу или остаток, в частности карбодигидразид (CDH), как определено выше. Первое производное ГК предпочтительно функционализировано гидразидным остатком по карбоксильной группе сахаридного звена ГК.
Модификацию карбоксильных групп можно выполнять любым способом, известным в данной области, с применением водорастворимого связующего реагента. Например, подходящий способ включает в себя применение стандартных карбодиимидных химических веществ, таких как EDC (1-этил-3-(3-диметиламинопропил)карбодиимид), в качестве связующего реагента для соединения гидразидным концевым остатком с карбоксильной группой с образованием соответствующих ацилгидразидов ГК (см., например, WO 95/15168). Другими подходящими для применения связующими реагентами являются триазиновые соединения, такие как DMTMM (4-(4,6-диметокси-1,3,5-триазин-2-ил)-4-метилморфолинхлорид; см., например, WO 2016/097211), активные сложные эфиры, такие как N,N'-дисукцинимидилкарбонат, и соли тетраметиламиния (например, HATU).
Второе производное ГК предпочтительно функционализируют альдегидным остатком без разрыва циклических сахаридных колец, например, без линеаризации каркаса ГК. Такие линеаризованные сахаридные звенья создаются, например, при классическом окислении периодатом, что приводит к введению альдегидных групп в циклическую кольцевую структуру сахаридных звеньев ГК и, следовательно, одновременно приводит к разрыву и «линеаризации» каркаса ГК. Дополнительная информация представлена в соответствующих пояснениях, изложенных выше, которые в равной мере применимы к настоящему изобретению.
Второе производное ГК предпочтительно получают превращением группы -СН2ОН в группу -СНО, и в особенности функционализированное альдегидом производное ГК предпочтительно модифицировано таким образом, что гидроксильная группа у атома С6 в N-ацетилглюкозаминовом звене ГК окисляется до получения формильной (-СНО) функциональной группы. Подходящий способ последующей модификации описан, например, в WO 2011/069475 с использованием TEMPO (2,2,6,6-тетраметил-1-пиперидинилокси) в качестве окислителя для превращения первичной спиртовой группы в альдегид.
Жидкая сшиваемая in situ композиция ГК, попадающая в тело пациента, т.е. смесь двух растворов-предшественников, предпочтительно содержит общее количество функционализированных гидразидом и альдегидом производных ГК от 0,1 мас. % до 5,0 мас. % и/или массовое соотношение функционализированного гидразидом производного ГК и функционализированного альдегидом производного ГК находится предпочтительно в диапазоне от 15:85 до 85:15. В отношении предпочтительных диапазонов указанного общего количества и указанного массового соотношения следует обратиться к приведенным выше комментариям, относящимся к полисахаридам, которые в равной мере применимы к гиалуроновой кислоте в качестве предпочтительного полисахарида.
В соответствии с настоящим изобретением общее количество функционализированных гидразидом и альдегидом производных ГК, присутствующих в жидкой композиции, предпочтительно составляет от 0,1 мас. % до 5,0 мас. %, в частности от 0,5 мас. % до 4,0 мас. %, более предпочтительно от 1,0 мас. % до 3,0 мас. % и наиболее предпочтительно от 1,5 мас. % до 2,5 мас. %. Кроме того, массовое соотношение функционализированного гидразидом производного ГК и функционализированного альдегидом производного ГК предпочтительно составляет от 15:85 до 75:25, более предпочтительно от 25:75 до 60:40, особенно предпочтительно от 40:60 до 60:40 и наиболее предпочтительно 50:50.
Функционализированное гидразидом производное ГК и функционализированное альдегидом производное ГК независимо друг от друга выполнены из исходного материала ГК, имеющего среднюю молекулярную массу от 3,0×104 до 5,0×106 Да, более предпочтительно от 0,1×106 до 4,0×106 Да и наиболее предпочтительно от 0,3×106 до 3,0×106 Да или от 0,5×106 до 2,0×106 Да, или основаны на нем. При применении в настоящем документе термин «гиалуроновая кислота», или «ГК», включает в себя гиалуроновую кислоту, гиалуронат и любую соль гиалуроновой кислоты, такую как гиалуронат натрия.
Первый и/или второй растворы-предшественники могут дополнительно содержать несшитую ГК, причем несшитая ГК преимущественно имеет молекулярную массу от 5,0×105 до 4,0×106 Да, предпочтительно от 1,0×106 Да до 3,0×106 Да. Массовое соотношение сшитой ГК и несшитой ГК может составлять от 1:1 до 1:0,001, в частности от 1:0,5 до 1:0,005 или от 1:0,1 до 1:0,01.
Степень модификации функционализированного гидразидом производного ГК и функционализированного альдегидом производного ГК, выраженная в виде соотношения суммы гидразидных остатков или альдегидных остатков и суммы дисахаридных звеньев ГК, может независимо находиться в диапазоне от 0,1% до 50%, предпочтительно от 0,5% до 25%, от 0,5% до 15% или от 0,5% до 5,0%. Степень модификации может быть определена, помимо прочего, методами спектрометрического и/или спектроскопического анализа, например, анализом ЯМР-спектров, спектров в ультрафиолетовой, видимой и инфракрасной областях спектра, титрованием, ВЭЖХ, эксклюзионной хроматографией и анализом вязкости. Степень модификации удобно определять при помощи 1Н-ЯМР.
Все числовые значения, которые в настоящем документе выражают «молекулярный вес», «молекулярную массу», «средний молекулярный вес» или «среднюю молекулярную массу» полисахаридов (например, ГК), следует понимать как обозначения среднемассовой молярной массы (или среднемассовой молекулярной массы), или Mw (w означает вес; также используется термин средневесовая молекулярная масса (WAMW)) в Дальтонах (Да). Среднемассовая молярная масса (Mw) определяется следующим образом: Mw=ΣiNiMi2/ΣiNiMi, где Ni - число молекул с молекулярной массой Mi.
В настоящем документе могут применяться различные способы определения молекулярной массы ГК, например измерения характеристической вязкости (например, в соответствии с Европейской фармакопеей, версия 7.0, статья «Гиалуроновая кислота» №1472, 01/2011 г.), капиллярный электрофорез (СЕ) (например, в соответствии с Kinoshita et al., Biomed. Chromatogr., 2002, 16:141-45), гель-проникающая хроматография (ГПХ) (например, в соответствии с Kim et al., Food Chem., 2008, 109:63-770) или многоугловое рассеяние лазерного света в комбинации с гель-фильтрацией (SEC-MALLS) (например, в соответствии с Hokputsa et al., Eur. Biophys. J. Biophys. Lett., 2003, 32:450-456).
В рамках настоящего изобретения среднемассовую молярную массу (Mw) полимеров ГК предпочтительно определяют гель-проникающей хроматографией (ГПХ) или вискозиметрией посредством уравнения Марка - Хаувинка. Методика ГПХ включает в себя пропускание раствора полимера через матрицу из частиц сшитого полимера под давлением несколько сотен Паскаль (до семи сотен бар). Как известно специалисту в данной области, применение низкодисперсионных стандартов позволяет провести корреляцию между временем удержания и молекулярной массой.
Среднемассовую молярную массу (Mw), определенную посредством уравнения Марка - Хаувинка, также можно назвать вязкостной средней молярной массой, или Mv. Уравнение Марка - Хаувинка дает соотношение характеристической вязкости (η) и молекулярной массы М и позволяет определять молекулярную массу полимера по данным характеристической вязкости и наоборот. В контексте настоящего изобретения характеристическую вязкость предпочтительно измеряют в соответствии с процедурой, описанной в Европейской фармакопее 7.0 (статья «Гиалуроновая кислота» №1472, 01/2011 г.). Для вычисления молекулярной массы ГК по данным характеристической вязкости в настоящем документе применяется следующее уравнение Марка - Хаувинка:
[η]=K×Ma,
где [η] = характеристическая вязкость в м3/кг, М = молекулярная масса, K=2,26×10-5 и а=0,796.
В соответствии с настоящим изобретением к косметическим сферам применения могут относиться, без ограничений, коррекция крупных и мелких морщин, межбровных морщин, носогубных складок, морщин на подбородке, морщин «марионеток», контура нижней челюсти, морщин на щеках, периоральных морщин, «гусиных лапок», кожных углублений, рубцов, морщин в височной области, подкожный лифтинг бровей, коррекция объема скул и щек, слезных борозд, носа, губ, щек, подбородка, периоральной области, подглазничной области и коррекция асимметрии лица.
К терапевтическим сферам применения, на которые нацелено настоящее изобретение, относятся, без ограничений, недержание мочи при напряжении, вагинальная сухость, пузырно-мочеточниковый рефлюкс, недостаточность голосовой складки или медиализация голосовой складки.
В дополнительном аспекте настоящее изобретение относится к комбинации первого производного гиалуроновой кислоты (ГК) и второго производного гиалуроновой кислоты (ГК), как определено в настоящем документе, причем первое производное ГК функционализировано гидразидным остатком, а второе производное ГК функционализировано альдегидным остатком, и при этом указанный гидразиновый остаток и указанный альдегидный остаток способны образовывать ковалентную связь in situ, например, в условиях in vivo.
Предпочтительно первое производное гиалуроновой кислоты (ГК) имеет вид первого раствора-предшественника, а второе производное гиалуроновой кислоты (ГК) имеет вид второго раствора-предшественника.
Функционализированное гидразидом производное ГК, функционализированная альдегидом ГК, первый и второй стерильные растворы-предшественники и формирование in situ сшитого гидразоновыми связями гидрогеля гиалуроновой кислоты (ГК) можно дополнительно определить так, как определено выше в настоящем документе.
В еще одном аспекте настоящее изобретение относится к многоцилиндровой шприцевой системе для формирования in situ сшитого полисахаридного гидрогеля, причем многоцилиндровый шприц предварительно заполнен по меньшей мере (а) первым раствором-предшественником первого производного полисахарида, функционализированного нуклеофильной группой, как описано в настоящем документе, в одном цилиндре и (b) вторым раствором-предшественником второго производного полисахарида, функционализированного электрофильной группой, как описано в настоящем документе, в другом (т.е. отдельном) цилиндре. Как первый, так и второй растворы-предшественники, как описано выше, являются стерильными.
В частности, настоящее изобретение относится к многоцилиндровой шприцевой системе, предпочтительно двухцилиндровой или трехцилиндровой системе, предварительно заполненной по меньшей мере (а) первым (стерильным) раствором-предшественником первого производного полисахарида, функционализированного нуклеофильной группой, как определено в настоящем документе, в одном цилиндре, и (b) вторым (стерильным) раствором-предшественником второго производного полисахарида, функционализированного электрофильной группой, как определено в настоящем документе, в другом (отдельном) цилиндре, и необязательно раствором с дополнительными компонентами (например, жиром, жирными кислотами, стволовыми клетками, витаминами, многоатомными спиртами, минеральными солями, анестезирующими агентами, такими как лидокаин, антиоксидантами, аминокислотами, солями щелочных и щелочноземельных металлов), присутствующим в необязательно имеющемся третьем цилиндре. Шприцевая система представляет предпочтительно собой двухцилиндровую шприцевую систему, предварительно заполненную (а) первым раствором-предшественником, как определено в настоящем документе, и (b) вторым раствором-предшественником, как определено в настоящем документе, в другом цилиндре.
Первое и второе производные полисахаридов, нуклеофильная и электрофильная группы, первый и второй стерильные растворы-предшественники и сформированный in situ сшитый полисахаридный гидрогель могут быть дополнительно определены так, как определено выше в настоящем документе. Более того, многоцилиндровая шприцевая система, включая двухцилиндровую шприцевую систему, подходит для применения в косметических или терапевтических сферах применения, в частности при замещении или наполнении биологической ткани или при увеличении объема биологической ткани для цели косметических или терапевтических сфер применения, как определено в настоящем документе, или особенно предпочтительно для применения в качестве дермального филлера в эстетических вариантах применения.
Термин «многоцилиндровая система» при применении в настоящем документе означает любую систему или устройство, обычно шприц, который содержит по меньшей мере два отдельных цилиндра и может содержать два или более поршней. Термин «двухцилиндровая шприцевая система» при применении в настоящем документе означает любую систему или устройство, обычно шприц, который содержит два отдельных цилиндра и может содержать один или два поршня. Кроме того, многоцилиндровая, например двухцилиндровая, шприцевая система по существу содержит колпачок-наконечник, или иглу, или канюлю с защитной крышкой для иглы или без нее для герметизации конца (-ов) шприцевой системы. Цилиндры по существу имеют емкость, достаточную для хранения первого и второго растворов-предшественников. Цилиндры могут быть изготовлены из стекла, пластика или любого другого подходящего материала и могут иметь разные геометрические формы, внутренние диаметры, составы материалов, прозрачность и т.д. Кроме того, многоцилиндровая шприцевая система может представлять собой двухцилиндровую шприцевую систему в виде шприца из двух соединенных в единое целое шприцев, т.е. двух соединенных в единое целое цилиндров, с однопоршневым или двухпоршневым узлом для подачи содержимого из цилиндров. Кроме того, шприцевая система может включать в себя два разъемно соединенных цилиндра и один или два разъемно соединенных поршня.
Более того, шприцевая система может также включать в себя средство (например, наконечник-аппликатор) для тщательного перемешивания компонентов, содержащихся в цилиндрах, до их подачи через наконечник-аппликатор. Таким образом, цилиндры по существу соединены, а поршневой узел по существу выполнен с возможностью одновременной подачи содержимого из цилиндров, так чтобы сохранялись соответствующие соотношения смешивания растворов-предшественников.
Многоцилиндровая шприцевая система, включая двухцилиндровую шприцевую систему, предпочтительно предназначена для формирования in situ сшитого гидразоновыми связями гидрогеля гиалуроновой кислоты (ГК), причем двухцилиндровый шприц предварительно заполнен (а) первым раствором-предшественником функционализированного гидразидом производного гиалуроновой кислоты (ГК) в одном цилиндре и (b) вторым раствором-предшественником функционализированного альдегидом производного ГК в другом (отдельном) цилиндре. Функционализированное гидразидом производное ГК, функционализированное альдегидом производное ГК, первый и второй стерильные растворы-предшественники и формирование in situ сшитого гидразоновыми связями гидрогеля гиалуроновой кислоты (ГК) предпочтительно соответствуют описанию, приведенному выше в настоящем документе.
В еще одном аспекте настоящее изобретение относится к набору для формирования in situ сшитого полисахаридного гидрогеля, содержащему (i) первый контейнер, содержащий первый стерильный раствор-предшественник первого производного полисахарида, как определено в настоящем документе, функционализированного нуклеофильной группой, и (ii) второй контейнер, содержащий второй стерильный раствор-предшественник второго производного полисахарида, как определено в настоящем документе, функционализированного электрофильной группой, и необязательно (iii) инструкции по применению.
Первое и второе производные полисахаридов, нуклеофильная и электрофильная группы, первый и второй стерильные растворы-предшественники и сформированный in situ сшитый полисахаридный гидрогель могут быть дополнительно определены так, как определено выше в настоящем документе. Термин «контейнер» при применении в настоящем документе не имеет конкретных ограничений и включает в себя, например, стеклянные или пластиковые бутыли, флаконы, карпулы или любой другой герметичный контейнер.
Инструкции по применению предпочтительно представляют собой инструкции по применению в косметических или терапевтических сферах применения, в частности при замещении или наполнении биологической ткани или при увеличении объема биологической ткани для цели косметических или терапевтических сфер применения, как определено в настоящем документе, или особенно предпочтительно в качестве дермального филлера в эстетических вариантах применения.
Набор предпочтительно предназначен для формирования in situ сшитого гидразоновыми связями гидрогеля гиалуроновой кислоты (ГК) и содержит (i) первый контейнер, содержащий первый стерильный раствор-предшественник функционализированного гидразидом производного ГК, и (ii) второй контейнер, содержащий второй стерильный раствор-предшественник функционализированного альдегидом производного ГК, и необязательно (iii) инструкции по применению. Функционализированное гидразидом производное ГК, функционализированное альдегидом производное ГК, первый и второй стерильные растворы-предшественники и формирование in situ сшитого гидразоновыми связями гидрогеля гиалуроновой кислоты (ГК) можно дополнительно определить так, как определено выше в настоящем документе, в особенности как определено применительно к первому аспекту настоящего изобретения. Необязательно комплект может содержать третий стерильный раствор, содержащий дополнительные компоненты, такие как упомянутые применительно к многоцилиндровой шприцевой системе.
В еще одном аспекте в соответствии с настоящим изобретением предложен способ формирования in situ сшитого гидрогеля в косметических или терапевтических сферах применения, включающий в себя этапы:
(a) получения первого раствора-предшественника первого производного полисахарида и отдельно от него второго раствора-предшественника второго производного полисахарида, причем первое производное полисахарида функционализировано нуклеофильной группой, а второе производное полисахарида функционализировано электрофильной группой, и как первый, так и второй растворы-предшественники являются стерилизованными,
(b) смешивания первого раствора-предшественника и второго раствора-предшественника с получением сшиваемого in situ смешанного раствора, и
(c) инъекции смешанного раствора в целевую область тела пациента, при этом нуклеофильная группа первого производного полисахарида и электрофильная группа второго производного полисахарида образуют in situ ковалентную связь, что приводит к формированию сшитого гидрогеля в целевой области.
Смешивание и инъекцию можно выполнять, используя шприцевую систему, как определено в настоящем документе, которая обычно обеспечивает предпочтительно гомогенное физическое смешивание обоих компонентов (т.е. первой и второй композиций-предшественников) перед подачей из иглы (канюли). Термин «гомогенный» при применении в настоящем документе означает равномерно перемешанный, диспергированный или разбавленный по всей смеси, дисперсии или раствору или означает материал с однородной структурой и/или композицией на всем протяжении.
Настоящее изобретение будет дополнительно проиллюстрировано ниже с помощью следующих не имеющих ограничительного характера примеров.
ПРИМЕРЫ
Приведенные ниже примеры иллюстрируют получение сшиваемого in situ гидрогеля гиалуроновой кислоты (ГК) и демонстрируют во время исследований на животных, что гидрогель является перспективным материалом-наполнителем для различных косметических и терапевтических сфер применения. Кроме того, примеры демонстрируют, что сшиваемую in situ композицию ГК можно легко вводить через тонкие иглы, не прилагая чрезмерного усилия, но при этом обеспечивая желательные механические и реологические свойства (т.е. комплексную вязкость (η*), динамический модуль упругости (G'), модуль потерь (G'') и тангенс угла потерь (tanδ)) для восстановления объема биологических тканей.
Измерение силы экструзии
Силу экструзии (усилие при инъекции) измеряли при помощи анализатора текстур (TA.XTPlus, Texture Technologies, Corp.), оснащенного стеклянным шприцем объемом 1,0 мл (BD Hypak SCF, 1 мл, длинный RF-PRTC, ISO 11040, внутренний диаметр 6,35 мм) и иглой 30G (TSK Laboratory). Силу экструзии измеряли на скорости исследования 0,21 мм/с на расстоянии 25 мм (целевой режим: расстояние; сила: 0,98 Н (100,0 гс)). Скорости до и после исследования составляли 0,21 мм/с и 10,0 мм/с, соответственно. Триггерная сила составляла 0,02 Н (2,0 гс) (тип триггера: авто (сила)), а натяжение составляло 10,0%. За силу экструзии принимали усредненную силу после достижения плато.
Измерение комплексной вязкости (η*), динамического модуля упругости и модуля потерь (G' и G'')
Комплексную вязкость (η*), динамический модуль упругости и модуль потерь (G' и G'') измеряли при 25°С с применением реометра (Anton Paar Physica MCR 302 Rheometer, Anton Paar GmbH), оснащенного конической пластиной (диаметр 50 мм, угол 0,1°, СР50-1, величина зазора 0,1 мм). Образцы колебались с нагрузкой 1 Па, и частота колебаний варьировалась от 0,1 до 10 Гц.
В примерах ниже термин «эквивалент» или «экв.» при применении в настоящем документе относится к дисахаридным повторяющимся звеньям гиалуроновой кислоты, если особо не указано иное. Процентные значения в отсутствие особых указаний представляют собой процентное содержание по массе.
ПРИМЕР 1
Синтез альдегидного производного ГК (НА-Ald)
Функционализированное альдегидом производное ГК получали путем избирательного окисления первичной гидроксильной группы С6 в N-ацетилглюкозаминовом (GlcNAc) звене ГК в соответствии со способом, описанным в WO 2011/069475 (см., например, пример 1). Вкратце гиалуроновую кислоту (ГК) (Mw=1,0×106 Да) окисляли, применяя систему ТЕМРО/соокислитель (TEMPO, 2,2,6,6-тетраметил-1-пиперидинилокси). После диализа раствор лиофилизировали с получением функционализированной альдегидом ГК (далее называется «HA-Ald»).
ПРИМЕР 2
Синтез гидразидного производного ГК (HA-Hyd)
ГК (6000,0 мг, 14,9 ммоль дисахаридных повторяющихся звеньев) растворяли в 700,0 мл деионизированной воды при комнатной температуре в течение 12 ч. Добавляли HOBt (2289,3 мг, 14,9 ммоль), а затем добавляли твердый EDC (1-этил-3-(3-диметиламинопропил)карбодиимид (1428,9 мг, 7,84 ммоль). Значение рН доводили до 5,5-6,5 и раствор перемешивали в течение 1 ч. Далее добавляли карбогидразид (CDH; 4043,5 мг, 44,88 ммоль) и перемешивание продолжали в течение 10 ч при комнатной температуре.
Затем раствор осаждали в 5,0 л изопропанола, осадок собирали, солюбилизировали в солевом растворе и помещали в диализный мешок (Spectra Por-6, MWCO 3500). Осадок диализировали относительно дистиллированной воды, содержащей 0,1 М NaCl (2×2 л, 48 ч), после чего диализировали относительно солевого раствора (2×2 л, 24 ч). Наконец, раствор лиофилизировали с получением 5000-5500 мг гидразидного производного ГК (далее называется «HA-Hyd»).
ПРИМЕР 3
Формирование и определение характеристик ГК-гидрогеля ГК-гидрогели получали при комнатной температуре (приблизительно 25°С), смешивая равные количества стерилизованного паром (131°С, 0,7 мин) альдегидного производного ГК из примера 1 (HA-Ald) и стерилизованного паром (131°С, 0,7 мин) гидразинового производного ГК из примера 2 (HA-Hyd). HA-Ald и HA-Hyd по отдельности разводили в стерильном PBS, рН 6,5-7,5, каждый в концентрации 15 мг/мл и 24,5 мг/мл соответственно. Затем по 1,0 мл каждого из растворов-предшественников HA-Ald и HA-Hyd (отдельно для каждого с концентрациями 15 мг/мл и 24,5 мг/мл) помещали в шприц объемом 1 мл с фиксатором Люэра в объемном соотношении 1:1. Применяемые два шприца были соединены с каждого конца с Y-образным коннектором для обеспечения эффективного смешивания двух растворов-предшественников одновременно с экструзией через иглу.
Измеренные средние значения силы экструзии и реологические свойства (η*, G', G'' и tan(δ)) стерильных растворов-предшественников и смесей стерильных растворов-предшественников представлены в таблице 1.
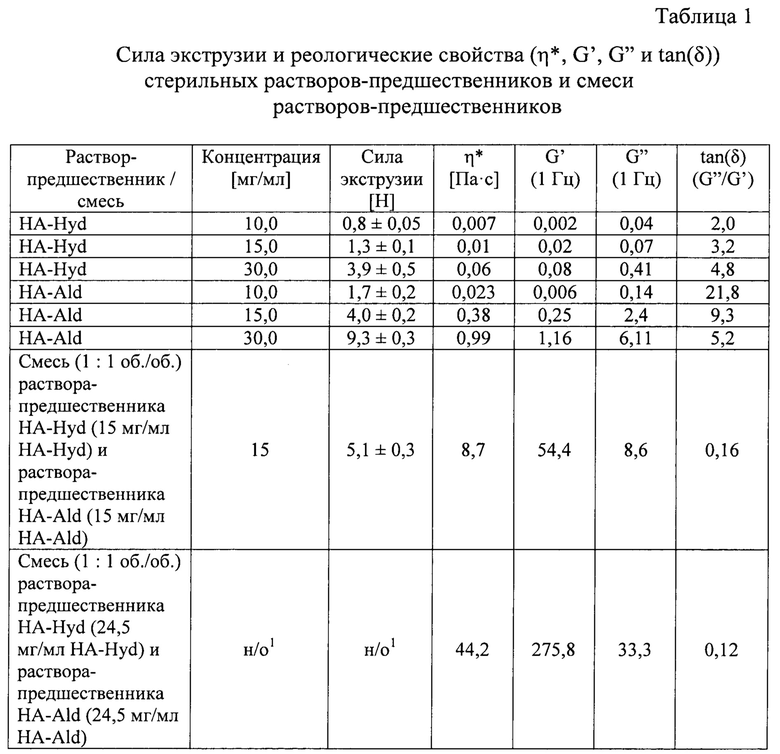
Как видно из таблицы 1, значения силы экструзии и комплексной вязкости как раствора-предшественника HA-Hyd, так и раствора-предшественника HA-Ald являются очень низкими, что указывает на жидкое (негелеобразное) состояние растворов-предшественников. Более того, было обнаружено, что смесь двух растворов-предшественников имеет значение силы экструзии лишь приблизительно 5 Н, что составляет приблизительно сумму каждого раствора-предшественника (15 мг/мл) сразу же после экструзии из отдельных шприцев через тонкую иглу 30G. Соответственно, смешанный раствор-предшественник гораздо легче вводить посредством инъекции, чем композицию дермального филлера в виде предварительно подготовленного гидрогеля.
Сшитые in situ ГК-гидрогели получали в чашках Петри из растворов-предшественников 15 мг/мл и 24,5 мг/мл соответственно, указанных в таблице 1. По данным реологии определяли адекватный и достаточный срок сшивания для получения итогового гелеобразного состояния, который составляет приблизительно 30 минут. Таким образом, реологические свойства (η*, G', G'' и tan(δ)) гидрогелей оценивали через 30 мин после смешивания двух растворов-предшественников с применением реометра Anton Paar, как описано выше. Результаты представлены в таблице 2.
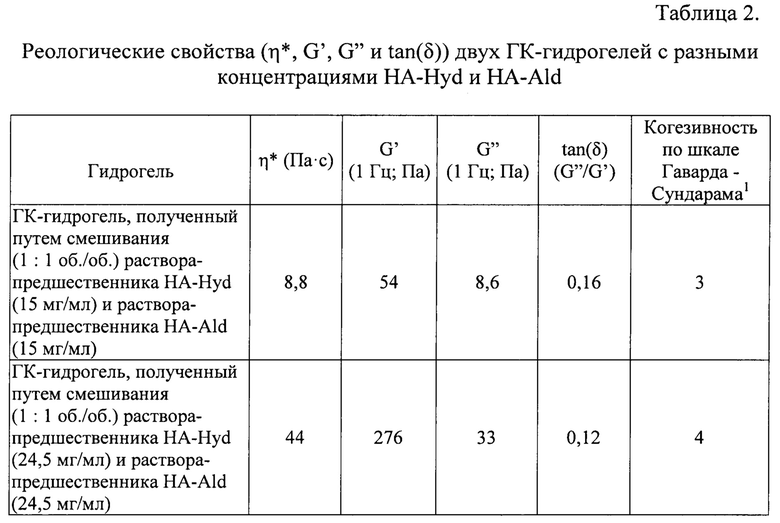
1 Sundaram et al., Cohesivity of Hyaluronic Acid Fillers: Development and Clinical Implications of a Novel Assay, Pilot Validation with a Five-Point Grading Scale, and Evaluation of Six U.S. Food and Drag Administration-Approved Fillers, Plast. Reconstr. Surg. 136:678-686, 2015.
Как показано в таблице 2, сшиваемые in situ гидрогели проявляют реологические свойства, сопоставимые с другими коммерчески доступными наполнителями, которые готовят предварительно и затем вводятся пациенту посредством инъекции. Кроме того, оба исследуемых сшиваемых in situ гидрогеля являются когезивными, на что указывает оценка в баллах 3 и выше по шкале когезивности Гаварда - Сундарама.
ПРИМЕР 4
Исследования на животных для формирования доказательства концепции
Предварительное исследование на животных
Для формирования гидрогелей in vivo у кроликов применяли два состава, приведенные в таблице 2. Первый гидрогель («исследуемый препарат 1») получали посредством совместной инъекции (1:1 об./об.) раствора-предшественника HA-Hyd (15 мг/мл) и раствора-предшественника HA-Ald (15 мг/мл) в кожу кроликов. Второй гидрогель («исследуемый препарат 2») получали посредством совместной инъекции (1:1 об./об.) раствора-предшественника HA-Hyd (24,5 мг/мл) и раствора-предшественника HA-Ald (24,5 мг/мл) в кожу кроликов.
В зависимости от глубины инъекции вводили объем от 100 мкл до 1000 мкл в разные слои кожи кроликов посредством внутрикожной (ID) и субдермальной (SD) инъекций и сравнивали с двумя коммерческими дермальными филлерами (контрольный препарат 1: Belotero Balance; контрольный препарат 2: Belotero Volume). В качестве отрицательного контроля применяли фосфатно-солевой буфер (PBS). Результаты представлены на ФИГ. 1 и 2.
Как показано на ФИГ. 1, после внутрикожной инъекции исследуемый препарат 1 выглядел приблизительно как трапециевидная масса в дерме, что является классическим результатом для филлеров на основе ГК. Кроме того, также видно, что тип инъекции (т.е. болюсная, однотуннельная и двухтуннельная инъекции) не давал никаких морфологических отличий. По существу такие же результаты были получены для исследуемого препарата 2. Более того, дополнительные исследования показали, что внутрикожная инъекция разных объемов исследуемых препаратов 1 и 2 не приводит к существенным различиям в распределении исследуемого препарата (результаты не показаны).
На ФИГ. 2 представлено макроскопическое изображение «выпуклости», или «пузыря», сформированного сшитым in vivo исследуемым препаратом 2 в момент времени t=4 ч. Как видно, исследуемый препарат 2 обеспечивает подтягивающий эффект через несколько часов после инъекции. Для сравнения солевой раствор за это время полностью исчез. Это же наблюдается и в случае исследуемого препарата 1. Пузырь, полученный после сшивания in vivo, аналогичен пузырю, полученному после инъекции наполнителей, имеющих реологические профили, аналогичные предварительно подготовленным коммерческим наполнителям (например, серии наполнителей Belotero® (Merz Aesthetics)).
В заключение внутрикожные и субдермальные инъекции разных количеств исследуемых препаратов 1 и 2 обеспечивали желаемый подтягивающий эффект и не ассоциировались ни с какими неблагоприятными гистопатологическими эффектами в коже кролика.
12-недельное исследование на животных с последующим наблюдением
На кроликах было проведено 12-недельное исследование для определения тяжести кожных реакций после внутрикожной инъекции (ID) вышеупомянутого исследуемого препарата 1 и субдермальной инъекции (SC) вышеупомянутого исследуемого препарата 2. Реакции сравнивали с внутрикожной инъекцией (ID) контрольного препарата 1 (Belotero Balance) и субдермальной инъекцией (SC) контрольного препарата 2 (Belotero Volume Lidocaine). Через четыре недели после инъекций области исследовали макроскопически и проводили гистопатологический анализ для оценки кожных реакций на каждый препарат. Все области макроскопически исследовали после инъекции, затем ежедневно в течение пяти дней, после чего еженедельно до завершения.
Неожиданно было обнаружено, что два исследуемых препарата (сшитый in vivo ГК-филлер) сформировали очень маленькие гранулы и спикулы, которые проникали между волокнами коллагена в дерме. Контрольные препараты (Belotero Balance и Belotero Balance Lidocaine) сформировали более крупные гранулы и скопления жидкости, заполнявшие в дерме большие пространства и не проникающие в коллаген дермы. Иными словами, сшитый in vivo ГК-филлер обеспечивал гораздо лучшую инфильтрацию в ткань, чем Belotero Balance (полную тканевую интеграцию в сравнении с локальным наполнением), хотя Belotero Balance известен прекрасной способностью к интеграции в ткань (Flynn et al., Comparative histology of intradermal implantation of mono and biphasic hyaluronic acid fillers, Dermatol Surg. 2011, 37:637-643 и Micheels et al., Superficial dermal injection of hyaluronic acid soft tissue fillers: comparative ultrasound study, Dermatol Surg. 2012, 38:1162-1169).
В заключение 12-недельное исследование на кроликах продемонстрировало сопоставимость in vivo ГК-филлера настоящего изобретения с коммерческими дермальными филлерами. Дополнительно было показано, что in vivo ГК-филлер обеспечивает уникальные характеристики, такие как улучшение проникновения в ткань, приводящее к полной тканевой интеграции, а не к локальному наполнению. Эти результаты отчетливо предполагают потенциал in vivo ГК-филлера настоящего изобретения для восстановления объема, наполнения или замены мягких тканей в различных косметических и терапевтических сферах применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДИФИЦИРОВАННАЯ АЛЬДЕГИДОМ ГИАЛУРОНОВАЯ КИСЛОТА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2810057C2 |
| БЫСТРОДЕЙСТВУЮЩИЙ ГЕРМЕТИК И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ И ИЗГОТОВЛЕНИЯ | 2007 |
|
RU2442612C2 |
| ПОЛИМЕРНЫЕ КОМПОЗИЦИИ МОДИФИЦИРОВАННОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2539395C2 |
| ВЫСОКОМОЛЕКУЛЯРНЫЕ КОСМЕТОЛОГИЧЕСКИЕ КОМПОЗИЦИИ | 2020 |
|
RU2839279C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛИЗОВАННЫХ ПРОИЗВОДНЫХ ГИАЛУРОНОВОЙ КИСЛОТЫ И ОБРАЗОВАНИЯ ИХ ГИДРОГЕЛЕЙ | 2009 |
|
RU2523182C2 |
| ПОПЕРЕЧНОСШИТАЯ ГИАЛУРОНОВАЯ КИСЛОТА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2007 |
|
RU2456299C2 |
| УГЛЕВОДНЫЙ СШИВАЮЩИЙ АГЕНТ | 2016 |
|
RU2733145C2 |
| СПОСОБ ДЕАЦЕТИЛИРОВАНИЯ БИОПОЛИМЕРОВ | 2016 |
|
RU2748235C2 |
| ИНЪЕКЦИОННЫЙ ГЕЛЕВЫЙ ПРОДУКТ | 2018 |
|
RU2783125C2 |
| СШИТЫЕ ПОЛИМЕРЫ И ИМПЛАНТАТЫ, ПРОИЗВЕДЕННЫЕ ИЗ ЭЛЕКТРОФИЛЬНО АКТИВИРОВАННОГО ПОЛИОКСАЗОЛИНА | 2012 |
|
RU2593755C2 |

Группа изобретений относится к косметической промышленности и медицине, в частности к применению первого и второго производных полисахарида для формирования in situ сшитого гидрогеля, используемого в косметических или терапевтических сферах применения, где первое производное представляет собой гиалуроновую кислоту (ГК), функционализированную нуклеофильной группой – гидразидом, а вторым производным является ГК, функционализированная электрофильной группой – альдегидом, причем нуклеофильная и электрофильная группы образуют in situ ковалентную связь после совместной инъекции указанных производных, при этом первое и второе производные находятся в виде соответственно первого и второго стерильных растворов с концентрацией каждого в растворе 0,1-5 мас.%, и массовое соотношение этих производных в вводимой пациенту композиции составляет 15:85-85:15. Также предложены: комбинация указанных производных ГК, многоцилиндровая шприцевая система, набор и способ для формирования in situ сшитого гидрогеля. Группа изобретений обеспечивает получение композиции, легко экструдируемой через тонкие иглы и которая после введения формирует in situ сшитый гидрогель с желаемыми свойствами для восстановления объема, заполнения или замещения мягких тканей. 6 н. и 7 з.п. ф-лы, 4 пр., 2 табл., 2 ил.
1. Применение первого производного полисахарида и второго производного полисахарида для формирования in situ сшитого гидрогеля в косметических сферах применения, в котором первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, и как первое, так и второе производные полисахарида являются стерилизованными, и при этом нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области,
причем первое производное полисахарида присутствует в виде первого стерильного раствора, а второе производное полисахарида присутствует в виде второго стерильного раствора,
при этом концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%,
причем массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
причем первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
2. Применение по п. 1, в котором образование in situ ковалентной связи происходит спонтанно при совместной инъекции.
3. Применение по п. 1 или 2, в котором каждый из первого и второго стерильного раствора имеет комплексную вязкость от 0,001 Па⋅с до 5,0 Па⋅с по данным колебательных реологических измерений при 1 Гц и 25°С или каждый из этих растворов имеет усилие при инъекции от 0,01 Н до 15 Н по данным измерений через иглу 30G при скорости экструзии 0,21 мм/с при применении стеклянного шприца объемом 1,0 мл, или оба эти варианта.
4. Применение по любому из пп. 1-3, в котором первый стерильный раствор и второй стерильный раствор смешивают во время совместной инъекции, но до попадания в тело пациента с формированием жидкой сшиваемой in situ композиции, и при этом указанная жидкая сшиваемая in situ композиция предпочтительно имеет комплексную вязкость от 0,1 Па⋅с до 100 Па⋅с по данным колебательных реологических измерений при 1 Гц и 25°С или имеет усилие при инъекции от 0,01 Н до 20 Н по данным измерений через иглу 30G при скорости экструзии 0,21 мм/с при применении стеклянного шприца объемом 1,0 мл, или оба эти варианта.
5. Применение по любому из пп. 1-4, в котором альдегидный остаток вводят в полисахарид без разрыва циклических сахаридных колец полисахаридного каркаса.
6. Применение по любому из пп. 1-5, в котором первое производное ГК является ГК, функционализированной гидразидным остатком по карбоксильной группе сахаридного звена ГК, или второе производное ГК является ГК, предпочтительно функционализированной альдегидным остатком, полученным путем превращения группы -CH2OH в группу -СНО, или оба эти варианта.
7. Применение по любому из пп. 1-6, в котором косметические сферы применения включают коррекцию крупных и мелких морщин, межбровных морщин, носогубных складок, морщин на подбородке, морщин «марионеток», контура нижней челюсти, морщин на щеках, периоральных морщин, «гусиных лапок», кожных углублений, рубцов, морщин в височной области, подкожный лифтинг бровей, коррекцию объема скул и щек, слезных борозд, носа, губ, щек, подбородка, периоральной области, подглазничной области и коррекцию асимметрии лица.
8. Применение первого производного полисахарида и второго производного полисахарида для формирования in situ сшитого гидрогеля в терапевтических сферах применения для лечения недержания мочи при напряжении, вагинальной сухости, пузырно-мочеточникового рефлюкса, недостаточности голосовой складки или медиализации голосовой складки,
в котором первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, причем нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области, и
в котором первое производное полисахарида присутствует в виде первого стерильного раствора, а второе производное полисахарида присутствует в виде второго стерильного раствора,
при этом концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%,
причем массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
причем первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
9. Комбинация первого производного гиалуроновой кислоты (ГК) и второго производного гиалуроновой кислоты (ГК) для применения в косметических сферах применения, в которой первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, причем нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области,
при этом нуклеофильная группа представляет собой гидразидный остаток, а электрофильная группа представляет собой альдегидный остаток, и
в которой первое производное полисахарида присутствует в виде первого стерильного раствора, а второе производное полисахарида присутствует в виде второго стерильного раствора,
при этом концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%,
причем массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
при этом первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
10. Многоцилиндровая шприцевая система для формирования in situ сшитого полисахаридного гидрогеля, используемого в косметических или терапевтических сферах применения для лечения недержания мочи при напряжении, вагинальной сухости, пузырно-мочеточникового рефлюкса, недостаточности голосовой складки или медиализации голосовой складки, предварительно заполненная по меньшей мере (а) первым стерильным раствором в одном цилиндре и (b) вторым стерильным раствором в другом цилиндре,
в которой первый стерильный раствор содержит первое производное полисахарида, а второй стерильный раствор содержит второе производное полисахарида,
причем первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, и как первое, так и второе производные полисахарида являются стерилизованными, и при этом нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области,
при этом концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%,
причем массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
причем первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
11. Набор для формирования in situ сшитого полисахаридного гидрогеля, содержащий (i) первый контейнер, содержащий первый стерильный раствор, и (ii) второй контейнер, содержащий второй стерильный раствор, при этом первый стерильный раствор содержит первое производное полисахарида, а второй стерильный раствор содержит второе производное полисахарида,
причем первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, и как первое, так и второе производные полисахарида являются стерилизованными, и при этом нуклеофильная группа и электрофильная группа образуют in situ ковалентную связь после совместной инъекции первого и второго производных полисахарида в целевую область тела пациента, что приводит к формированию сшитого гидрогеля в целевой области,
при этом концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%,
причем массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
причем первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
12. Набор по п. 11, дополнительно включающий (iii) инструкции по применению.
13. Способ формирования in situ сшитого гидрогеля, используемого в косметических или терапевтических сферах применения для лечения недержания мочи при напряжении, вагинальной сухости, пузырно-мочеточникового рефлюкса, недостаточности голосовой складки или медиализации голосовой складки, включающий в себя этапы, на которых:
(a) получают первый стерильный раствор первого производного полисахарида и отдельно от него второй стерильный раствор второго производного полисахарида, причем первое производное полисахарида представляет собой полисахарид, функционализированный нуклеофильной группой, а второе производное полисахарида представляет собой полисахарид, функционализированный электрофильной группой, и как первый, так и второй стерильные растворы являются стерилизованными,
(b) смешивают первый стерильный раствор и второй стерильный раствор с получением жидкой сшиваемой in situ композиции, и
(c) осуществляют инъекцию жидкой сшиваемой in situ композиции в целевую область тела пациента, при этом нуклеофильная группа первого производного полисахарида и электрофильная группа второго производного полисахарида образуют in situ ковалентную связь, что приводит к формированию сшитого гидрогеля в целевой области,
d) причем концентрация первого производного полисахарида в первом стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, а концентрация второго производного полисахарида во втором стерильном растворе составляет от 0,1 мас.% до 5,0 мас.%, при этом массовое соотношение первого производного полисахарида и второго производного полисахарида, содержащихся в жидкой сшиваемой in situ композиции, вводимой в целевую область тела пациента, составляет от 15:85 до 85:15, и
причем первое производное полисахарида представляет собой функционализированное гидразидом первое производное гиалуроновой кислоты (ГК), а второе производное полисахарида представляет собой функционализированное альдегидом второе производное гиалуроновой кислоты (ГК).
| Способ разработки труднопромывистых и валунистых россыпных месторождений полезных ископаемых | 2019 |
|
RU2716662C1 |
| WO 2012113529 A1, 30.08.2012 | |||
| WO 2011069475 A2, 16.06.2011 | |||
| СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛИЗОВАННЫХ ПРОИЗВОДНЫХ ГИАЛУРОНОВОЙ КИСЛОТЫ И ОБРАЗОВАНИЯ ИХ ГИДРОГЕЛЕЙ | 2009 |
|
RU2523182C2 |
| Oliveira J.T | |||
| et al | |||
| Hydrogels from polysaccharide-based materials: Fundamentals and applications in regenerative medicine / Natural-Based Polymers for Biomedical Applications - Woodhead Publishing Series in Biomaterials, 2008, | |||
Авторы
Даты
2020-10-16—Публикация
2016-10-14—Подача