Изобретение относится к области гальванотехники и может быть использовано в машиностроении, приборостроении и других отраслях промышленности для нанесения защитно-декоративных покрытий на металлы и сплавы.
Известен способ электрохимического нанесения хромовых покрытий при рН 1,1-2,1, температуре 35-40°С и плотности тока 20-50 А/дм2 из электролита, который содержит, г/л: сульфат хрома (III) - 100-150, оксалат натрия - 20-30, сульфат алюминия - 100, сульфат натрия - 80.
(Ю.Д. Гамбург. Гальванические покрытия. Справочник по применению / М., Техносфера. - 2006. - С. 148).
К достоинствам электролитов на основе солей хрома (III) можно отнести меньшую токсичность, высокий электрохимический эквивалент, позволяющий снизить расход электроэнергии на нанесение покрытий, и больший выход по току, по сравнению с электролитами на основе хрома (VI), а также значительное улучшение условий труда и упрощение процесса очистки сточных вод. Вместе с тем эти растворы по стабильности в работе и качеству получаемых покрытий уступают стандартному электролиту хромирования на основе CrO3.
Наиболее близким по технической сущности является способ электрохимического нанесения хромовых покрытий из электролита, содержащего, моль/л: хлорид хрома (III) - 0,3-0,6, муравьиную кислоту - 0,56-0,78, борную кислоту - 0,9-1,0, хлорид калия - 2,7-4,1, бромид калия - 0,04-0,25, при рН 1,5-4, температуре 25-40°С и плотности тока 8-12 А/дм2.
(Пат. 5294326 США МКИ С25Д 3/06, НКИ 205/287 / Shahin G.E.; Elf Atochem North America, Inc. - № 960564; Заявл. 13.10.92; Опубл. 15.03.94).
Известный способ позволяет получать хромовые покрытия высокого качества с катодным выходом по току 22-28%. Однако предложенный электролит недостаточно стабилен по содержанию ионов хрома (III) и формиат-ионам, что приводит к ухудшению качества покрытий при его длительном использовании.
Задачей изобретения и его техническим результатом является повышение стабильности состава электролита при длительной эксплуатации и расширение диапазона рабочих плотностей тока.
Технический результат достигается тем, что способ электрохимического нанесения хромовых покрытий включает электролиз при рН, температуре и катодной плотности тока в электролите, содержащем хлорид хрома (III), муравьиную и борную кислоты, хлорид и бромид аммония или щелочного металла и гидроксоформиат хрома (III) при следующем соотношении компонентов, моль/л:
хлорид хрома (III) - 0,25-0,3,
муравьиную кислоту - 0,6-0,8,
борную кислоту - 0,7-0,9,
хлорид аммония или щелочного металла - 3-4,
бромид аммония или щелочного металла - 0,4-0,6,
гидроксоформиат хрома (III) - 0,4-0,6.
Технический результат также достигается тем, что комплексное соединение вводят в электролит в виде порошка, находящегося в нетканых мешках из полипропилена или в специальном контейнере, через который осуществляется циркуляция раствора. Указанный прием позволяет избежать взмучивания малорастворимого порошка при перемешивании раствора и уноса его с деталями.
Технический результат также достигается тем, что содержание ионов калия (натрия) в электролите по отношению к суммарной концентрации ионов щелочных металлов и аммония составляет 0,08-0,13, что обеспечивается концентрацией ионов калия (натрия) 0,32-0,5 моль/л при суммарной концентрации ионов щелочных металлов и аммония 3,75-4 моль/л.
В указанных условиях получают блестящие декоративные хромовые покрытия с выходом по току 10-15% при сохранении стабильности раствора по ионам хрома и формиат-ионам и стабильности качества покрытий при длительной эксплуатации.
Для приготовления растворов заданного состава в рабочей ванне, заполненной на 1/3 дистиллированной водой, подогретой до 70°С, растворяют навеску KBr (NaBr, NH4Br). Затем добавляют HCOOH. После этого, при постоянном перемешивании, в раствор добавляют расчетный объем предварительно приготовленного концентрата хлорида хрома (1,0 М раствор CrCl3⋅6H2O, выдержанный 2 недели после приготовления) и навески H3BO3, NH4Cl (NaCl, KCl). Температуру поддерживают на уровне 50°С для увеличения скорости образования комплекса. Затем раствор доводят дистиллированной водой до заданного объема и перемешивают до полного растворения солей. Раствор выдерживают до изменения окрашивания из зеленого в синий цвет. После приготовления раствора заданного состава проводят корректировку рН раствора при помощи концентрированного раствора КОН (NaOH, NH4OH) до рН=2,5. Электролит прорабатывают при ik=15 A/дм2 (катод - медная пластина, анод - графит) без разделения анодного и катодного пространств. Количество пропущенного электричества составляет около 1А⋅ч/л. При этом рН может снизиться с 2,5 до 2,0.
Отдельно готовят комплексное соединение хрома. В 500 мл теплой (30-40 С) дистиллированной воды при перемешивании растворяют 240 г (0,9 моль) CrCl3×6H2O (раствор А). В 400 мл теплой (30-40 С) дистиллированной воды при перемешивании растворяют 82 г (1,2 моль) формиата натрия (HCOONa) (раствор Б). При непрерывном перемешивании в раствор А добавляют Раствор Б и с помощью 10%-го раствора NaOH устанавливают рН, равный 2,6-2,8. Полученный раствор нагревают до 50-60°С и выдерживают при этой температуре 1 час. После такой обработки раствор охлаждают, еще раз устанавливают рН 2,6-2,8 и оставляют на 1-2 суток для завершения реакции комплексообразования и формирования осадка хлорида дигидроксогексаформиатотрихрома. Выпавший осадок отфильтровывают, промывают холодной 10-15°С дистиллированной водой, снимают с фильтра и сушат на воздухе. Полученный осадок в соответствии с результатами элементного анализа соответствует кристаллогидрату комплексного соединения [Cr3(OH)2(HCOO)6]Cl, которое в дальнейшем используют для приготовления электролита и нанесения хромовых покрытий.
Малорастворимое комплексное соединение [Cr3(OH)2(HCOO)6]Cl участвует в поддержании равновесия между твердой фазой и раствором по реакции
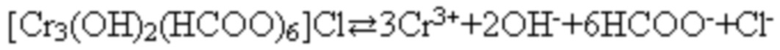
что обеспечивает поддержание постоянной концентрации основных компонентов раствора и рН в процессе длительного электролиза.
Диапазон допустимых плотностей тока, обеспечивающих получение высококачественных хромовых покрытий, существенно зависит от соотношения между ионами калия (натрия) и аммония. Наибольший диапазон плотностей тока, приводящий к повышению кроющей способности электролита и формированию блестящих декоративных покрытий на изделиях сложной конфигурации, соответствует содержанию ионов калия (натрия) 0,32-0,5 моль/л при суммарном содержании ионов щелочных металлов и аммония 3,75-4 моль/л, что соответствует отношению концентраций ионов калия (натрия) к суммарной концентрации ионов щелочных металлов и аммония равной 0,08-0,13.
Изобретение может быть проиллюстрировано следующими примерами.
Пример 1. По вышеуказанной методике приготовлены растворы хромирования без комплекса (прототип) и с добавкой комплекса (состав приведен в таблице 1). Хромирование проводили при комнатной температуре в ячейках объемом 100 мл с графитовыми анодами площадью 3 см2, катоды медные. Плотность тока на аноде 8 А/дм2, рН=1-2,5, количество электричества, прошедшее через единицу объема, составляло 10 А ч/л. Затем анализировали содержание в растворах ионов хрома Cr3+ и муравьиной кислоты НСООН. Данные таблицы 1 показывают, что ведение малорастворимого комплекса способствует сохранению начальной концентрации ионов хрома и муравьиной кислоты.
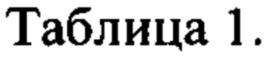
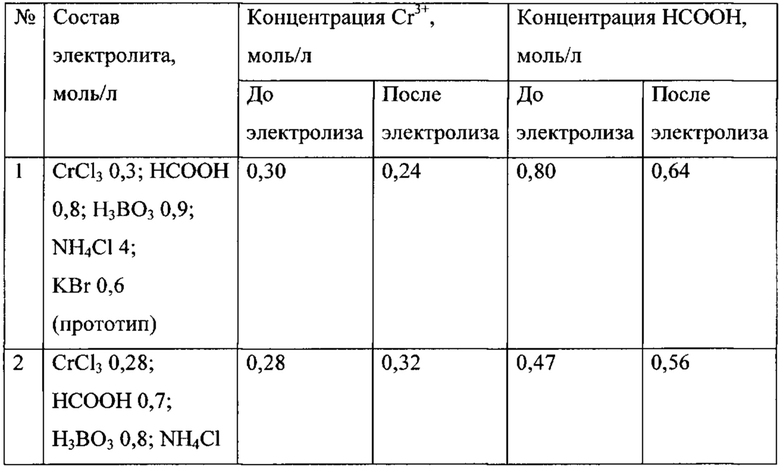
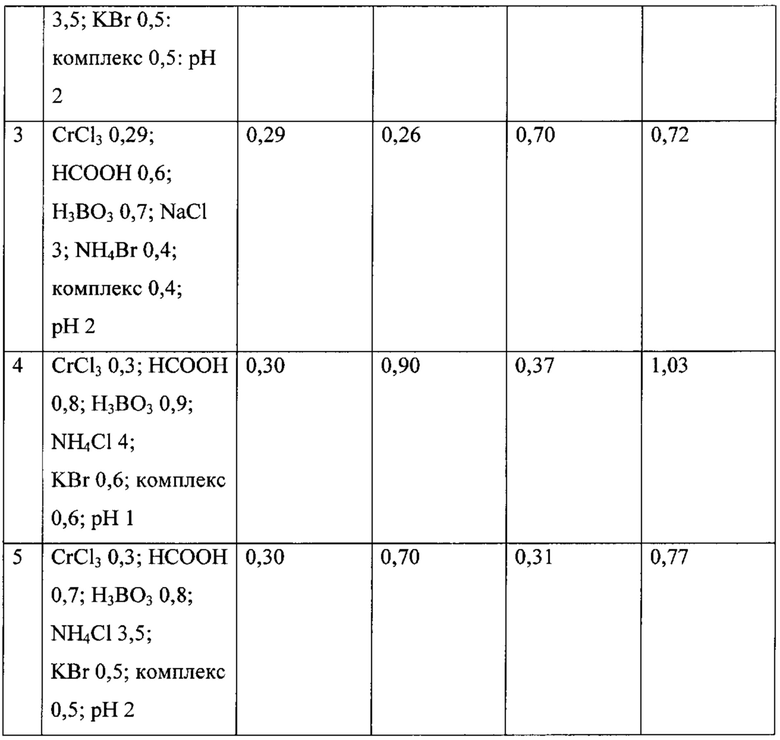
Пример 2. По вышеуказанной методике приготовлены растворы хромирования без комплекса (прототип) и с добавкой комплекса (состав приведен в таблице 1). Комплекс вводили в раствор в пластиковом контейнере с тканевым фильтром. Хромирование проводили при комнатной температуре в ячейках объемом 1000 мл с графитовыми анодами площадью 3 см2, катоды медные. Плотность тока на аноде 8 А/дм2, рН=1-2,5. Время электролиза при нанесении покрытия на один образец составляло 15 мин, рабочая плотность тока от 5 до 50 А/дм2. Температура раствора составляла 20-22°С. Содержание в растворах ионов хрома Cr3+ и муравьиной кислоты НСООН оценивали в условиях длительного электролиза - при пропускании от 10 до 35 А.ч/л. Результаты исследований влияния количества пропущенного электричества на отношение концентраций муравьиной кислоты и хрома и концентрации этих веществ в отсутствии (раствор 1) и в присутствии малорастворимого гидроксоформиата хрома (раствор 2) приведены в таблице 2.
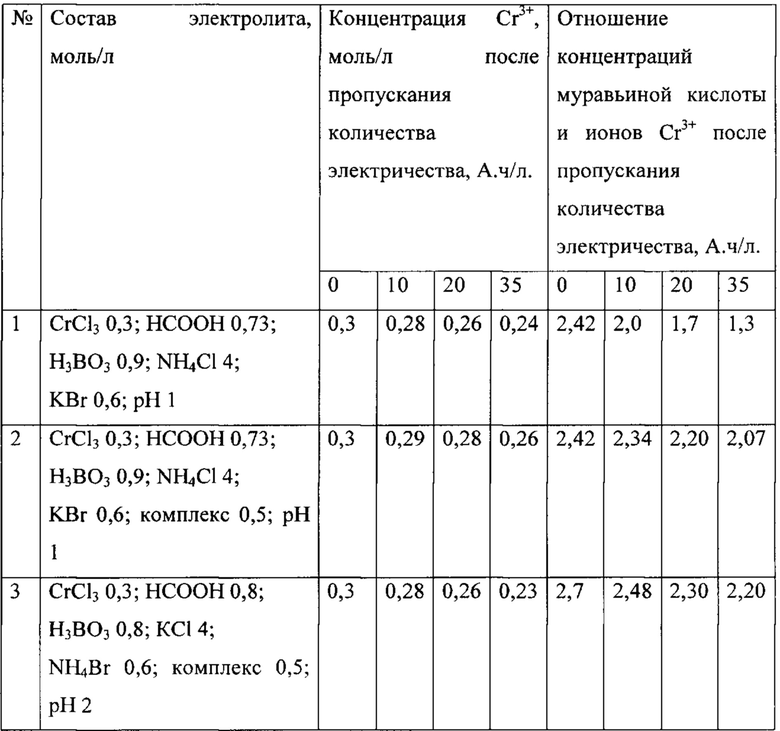
Проведенные эксперименты показывают, что концентрация хрома и муравьиной кислоты в растворе без добавления малорастворимой соли уменьшается пропорционально количеству пропущенного электричества). При насыщении электролита хромирования гидроксоформиатом хрома концентрации муравьиной кислоты и хрома несколько снижаются за счет установления ионного равновесия между раствором и малорастворимой солью, но при дальнейшем увеличении количества пропущенного электричества изменение концентраций НСООН и Cr3+ незначительно.
Пример 3. По вышеуказанной методике приготовлены растворы хромирования с добавкой комплекса (состав приведен в таблице 1) и с различным отношением (XK+) концентраций ионов калия (натрия) в электролите к суммарной концентрации ионов щелочных металлов и аммония в диапазоне от 0 до 0,2, что обеспечивалось изменением концентрации ионов калия (натрия) от 0 до 0,77 моль/л при изменении суммарной концентрации ионов щелочных металлов и аммония от 3,15 до 4,25 моль/л. Комплекс вводили в раствор в пластиковом контейнере с тканевым фильтром. Хромирование проводили при комнатной температуре в ячейках объемом 1000 мл с графитовыми анодами площадью 3 см2, катоды медные. Плотность тока на аноде 8 А/дм2, рН=1-2,5. Время электролиза при нанесении покрытия на один образец составляло 15 мин, рабочая плотность тока от 5 до 50 А/дм2. Температура раствора составляла 20-22°С.
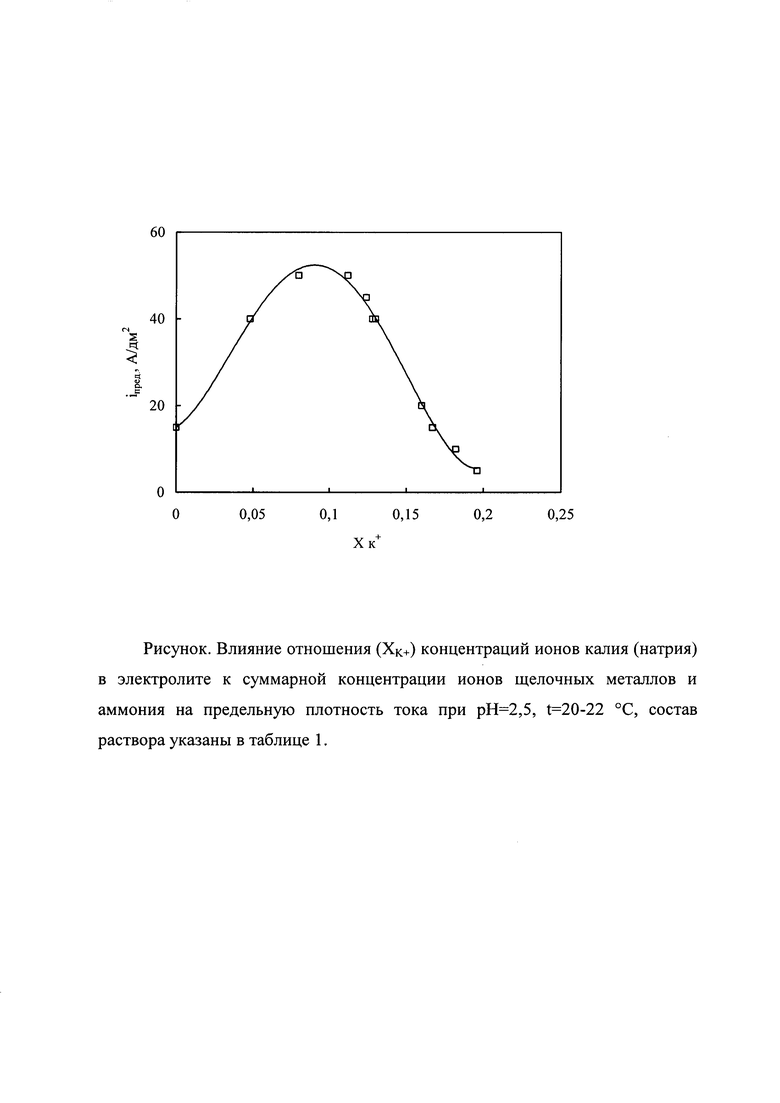
На рисунке показано влияние отношения (XK+) концентраций ионов калия (натрия) в электролите к суммарной концентрации ионов щелочных металлов и аммония на предельную плотность тока при рН=2,5, t=20-22°С, составы раствора указаны в таблице 1.
Рисунок иллюстрирует зависимость максимально допустимой плотности тока от XK+ в растворах. Как следует из рисунка с повышением XK+ значение предельной плотности тока возрастает до 50 А/дм2 и проходит через максимум при XK+ равном 0,08-0,13.
Исходя из результатов исследований, можно сделать вывод, что для получения качественных покрытий с наибольшим выходом по току хрома в широком интервале рабочих плотностей тока в составе электролита необходимо, чтобы отношения (XK+) концентраций ионов калия (натрия) в электролите к суммарной концентрации ионов щелочных металлов и аммония находилось в интервале 0,08-0,13, при этом допустимая концентрация К+ в растворе равна 0,32-0,5 моль/л, а суммарная концентрация солей щелочных металлов и аммония составляет 3,75-4 моль/л.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ электроосаждения хромовых покрытий из электролита на основе гексагидрата сульфата хрома (III) и формиата натрия | 2023 |
|
RU2814771C1 |
| ЭЛЕКТРОЛИТ ХРОМИРОВАНИЯ | 2009 |
|
RU2409707C1 |
| Способ получения композиционного металл-алмазного покрытия на поверхности медицинского изделия, дисперсная система для осаждения металл-алмазного покрытия и способ ее получения | 2020 |
|
RU2746730C1 |
| Композиционное металл-алмазное покрытие, способ его получения, дисперсная система для осаждения композиционного металл-алмазного покрытия и способ ее получения | 2019 |
|
RU2706931C1 |
| ЭЛЕКТРОЛИТ И СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЯ СПЛАВОМ ОЛОВО-КОБАЛЬТ | 2008 |
|
RU2377344C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО НАНЕСЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ НА МЕТАЛЛЫ И СПЛАВЫ | 1999 |
|
RU2139369C1 |
| Композиционное металл-алмазное покрытие, способ его получения, алмазосодержащая добавка электролита и способ ее получения | 2018 |
|
RU2699699C1 |
| Способ получения композиционного металл-дисперсного покрытия, дисперсная система для осаждения композиционного металл-дисперсного покрытия и способ ее получения | 2020 |
|
RU2746863C1 |
| Способ получения композиционного металл-дисперсного покрытия, дисперсная система для осаждения композиционного металл-дисперсного покрытия и способ ее получения | 2020 |
|
RU2746861C1 |
| Электролит для осаждения хромового покрытия, легированного молибденом | 2022 |
|
RU2778529C1 |
Изобретение относится к области гальванотехники и может быть использовано в машиностроении, приборостроении и других отраслях промышленности для нанесения защитно-декоративных покрытий на металлы и сплавы. Способ электрохимического нанесения хромовых покрытий на металлы и сплавы включает электролиз в водном растворе, содержащем, моль/л: хлорид хрома (III) 0,25-0,3, муравьиную кислоту 0,6-0,8, борную кислоту 0,7-0,9, хлорид аммония или щелочного металла 3-4, бромид аммония или щелочного металла 0,4-0,6, хлорид дигидроксогексаформиатотрихрома (III) 0,4-0,6. Электролиз проводят при температуре электролита 20-22°С, рН 1-2,5 и при рабочей плотности тока от 5 до 50 А/дм2. Изобретение обеспечивает повышение стабильности состава электролита при длительной эксплуатации и расширение диапазона рабочих плотностей тока. 2 з.п. ф-лы, 2 табл., 3 пр., 1 ил.
1. Способ электрохимического нанесения хромовых покрытий на металлы и сплавы, включающий электролиз в водном электролите, содержащем хлорид хрома (III), муравьиную и борную кислоты, хлорид и бромид аммония или щелочного металла, отличающийся тем, что электролит дополнительно содержит хлорид дигидроксогексаформиатотрихрома (III) при следующем соотношении компонентов, моль/л:
а электролиз проводят при температуре электролита 20-22°С, рН 1-2,5 и при рабочей плотности тока от 5 до 50 А/дм2.
2. Способ по п.1, отличающийся тем, что хлорид дигидроксогексаформиатотрихрома (III) вводят в электролит в виде порошка, находящегося в нетканых мешках из полипропилена или в контейнере, через который осуществляют циркуляцию электролита.
3. Способ по п. 1, отличающийся тем, что содержание ионов калия или натрия в электролите по отношению к суммарной концентрации ионов щелочных металлов и аммония составляет 0,08-0,13, что обеспечивают концентрацией ионов калия или натрия 0,32-0,5 моль/л при суммарной концентрации ионов щелочных металлов и аммония 3,75-4 моль/л.
| US 5294326 A1, 15.03.1994 | |||
| RU 2016135556 A, 15.03.2018 | |||
| ЭЛЕКТРОЛИТ ДЛЯ ОСАЖДЕНИЯ ХРОМОВЫХ ПОКРЫТИЙ НА МЕТАЛЛЫ И СПЛАВЫ | 1999 |
|
RU2146309C1 |
| EP 2899299 A1, 29.07.2015. | |||
Авторы
Даты
2020-10-27—Публикация
2020-03-23—Подача