Предполагаемое изобретение относится к медицине, а именно к хирургии и онкологии, может быть использовано при восстановлении непрерывности пищеварительного тракта после гастрэктомии.
Гастрэктомия - хирургическая операция, заключающаяся в полном удалении желудка, применяется в основном при распространенных злокачественных новообразованиях этого органа. Первую успешную гастрэктомию с соединением пищевода с тощей кишкой при помощи анастомоза конец-в-бок, выполнил швейцарский хирург Schlatter в 1897 г. (Wangensteen ОН, Wangensteen SD, Dennis С. In Westell С, Nyhus LM, Donahue РЕ, editors. Surgery of the esophagus, stomach and small intestine. Boston: Little Brown and Company; 1994; 354-85).
В последующий более чем столетний период техника операции интенсивно совершенствовалась, изучались отдаленные результаты. И в настоящее время это оперативное вмешательство в сочетании с расширенной лимфодиссекцией (D2-D3) является стандартным при хирургическом лечении рака желудка и выполняется ежегодно тысячами во всем мире.
С улучшением непосредственных и отдаленных послеоперационных результатов осталась нерешенной проблема функциональных нарушений пищеварения, обусловленных грубыми изменениями нормальных анатомо-физиологических соотношений при полном удалении желудка. В результате тяжелых функциональных нарушений, вызванных утратой желудка, у таких больных отмечается значительное ухудшение питательного статуса и снижение качеств.а жизни (Ishizuka М, Oyama Y, Abe A. Prognostic nutritional index is associated with survival after total gastrectomy for patients with gastric cancer. Anticancer Res. 2014; 34: 4223-4229)
Для устранения клинических проявлений постгастрэктомических синдромов предложено более 70 методов реконструкции и, к сожалению, идеального способа восстановления пищеварительной системы до сих пор не создано. Наиболее часто реконструкцию пищеварительного тракта после гастрэктомии выполняют при помощи петлевого анастомоза, на «отключенной» петле тощей кишки по Roux или тощекишечно-пластическим замещением утраченного желудка с редуоденизацией.
Широко используемые в клинической практике различные способы петлевых пищеводно-кишечных анастомозов с межкишечным брауновским соустьем, при высокой надежности и простоте имеют недостаток в виде проявлений рефлюкс-эзофагита, встречающихся по данным разных авторов в 7-18% случаев (Dikic S, Randjelovic Т, Dragojevic S. Early dumping syndrome and reflux esophagitis prevention with pouch reconstruction. J Surg Res. 2012; 175(1): 56-61). Это связано с утратой кардиального, пилорического сфинктеров и появлением пищеводно-кишечного соустья, располагающего к рефлюксу желчных кислот и панкретических ферментов из тощей кишки в пищевод (Шаназаров Н.А. Современные подходы к хирургическому лечению рака желудка // Фундаментальные исследования. - 2011. - №10-1. - С.204-211; Chen Xetal., 2014).
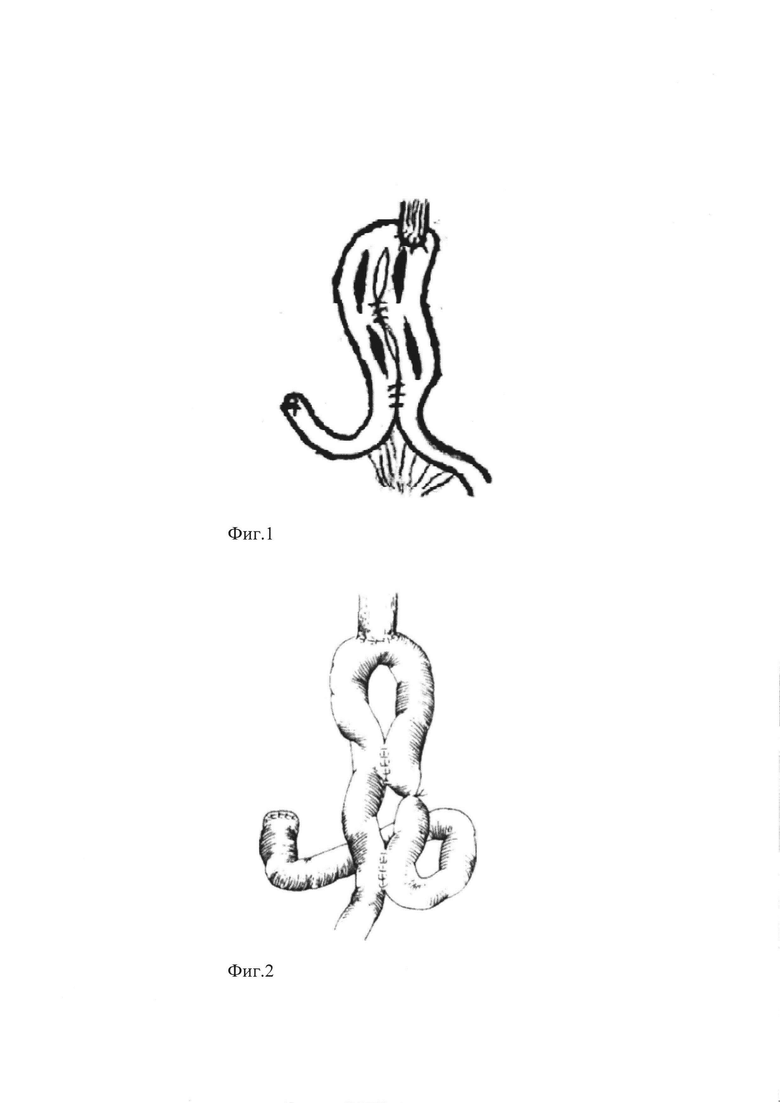
Известен способ петлевого пищеводно-кишечного анастомоза, предложенный Дэем и Куном, в 1953 году (Day В.М. Cunha F.A. Method of increasing the gastric reserveoiz following total gastrectomy // The Review of gastroenterology - 1953. - №10. P. 705-713). При этом способе формируют «искусственный желудок» путем наложения двух межкишечных анастомозов по Брауну между приводящим и отводящим коленами петли тощей кишки на расстоянии 8 см. друг от друга (Фиг. 1 - Реконструкция пищеварительного тракта способом Дэя-Куна).
Способ является сравнительно простым в исполнении и незначительно удлиняет время проведения основного этапа операции. Второй межкишечный анастомоз по Брауну призван предупредить регургитацию желчи и панкреатического сока в пищевод с развитием рефлюкс-эзофагита, однако на практике показывает низкую эффективность в этом отношении.
Наиболее близким аналогом предлагаемого варианта создания эзофагоеюноанастомоза является модификация способа Бильрот II (Нао X., Li Q., Yin J. The application of FJI and its comparison with different alimentary reconstructions after total gastrectomy for cancer // The Chinese-German Journal of Clinical Oncology - 2002, T1. - №3. P. 123-125).
В отличие от предыдущего способа, он с арефлюксной целью дополняется перевязкой приводящего колена петли тонкой кишки между двумя брауновскими межкишечными соустьями. Таким образом удается разобщить поступление желчи и панкреатического сока от эзофагоеюноанастомоза в приводящем колене петли тонкой кишки. (Фиг. 2 - Реконструкция пищеварительного тракта эзофагоеюноанастамозом в модификации Бильрот II).
Достоинствами способа является:
- профилактика энтеро-эзофагеального рефлюкса и возникновения рефлюкс-эзофагита;
- сравнительная простота исполнения;
- незначительное удлинение времени проведения основного этапа операции.
Недостатками данного способа являются:
- вероятность возникновения некротических изменений и нарушение нервной регуляции в тонкой кишке, в связи с лигированием;
- отсутствие физиологической порционности пассажа пищи для более эффективного взаимодействия с пищеварительными ферментами,
- отсутствие возможности прохождения пищи по второй петле кишки, в случае, когда развивается локальный рецидив опухоли и затруднено прохождение пищи по основной петле, идущей к пищеводу.
Задачи:
- предупредить развитие энтеро-эзофагеального рефлюкса, рефлюкс-эзофагита, риск некротических изменений и нарушений нервной регуляции в тонкой кишке;
- замедлить пассаж и обеспечить физиологическую порционность пассажа пищи и улучшение условий пищеварения.
Сущностью способа является формирование петлевого пищеводно-тонкокишечного анастомоза, отличающегося тем, что после расширенной гастрэктомии через бессосудистое окно в брыжейке поперечно-ободочной кишки проводят начальную петлю тонкой кишки длиной 30 см от связки Трейца, между задней стенкой культи пищевода и приводящей петлей кишки поперечно накладывают непрерывные обвивные серозно-мышечно-подслизистые швы в два ряда, боковые нити после завязывания со свободной нитью, пропущенной через последний стежок обвивного шва, берут на держалки, затем в соответствии с диаметром пищевода поперечно рассекают стенку кишки и анастомозируют пищевод в бок приводящей кишки обвивным прецизионным серозно-мышечно-подслизистым швом, погружают передний ряд внутренних швов анастомоза в приводящую кишку, поочередно при помощи четырех полукисетных швов, - за счет дистальных и проксимальных боковых нитей, взятых ранее на держалки с двух сторон и трех «салазочных» швов между дистальными полукисетными швами, поперечное плечо которых проходит через стенку пищевода с захватом подслизистого слоя, завязывают «салазочные» швы, наворачивают стенку приводящей кишки, тем самым инвагинируют в нее пищевод, затем на расстоянии 12 см от анастомоза поперечно прошивают приводящую петлю тонкой кишки механическим двухрядным скрепочным швом, который укрывают обвивным серозно-мышечно-подслизистым швом, этой же нитью сшивают между собой брыжеечные края приводящей и отводящей петель кишки выше на 5,0 см и ниже на 3,0 см от механического шва, после чего формируют два межкишечных анастомоза по Брауну, - проксимальный анастомоз для прохождения пищи из приводящей в отводящую петлю кишки длиной 4,0 см и дистальный длиной 1,5 см - для прохождения желчи и панкреатического сока.
Технический результат: применение данного способа восстановления непрерывности пищеварительного тракта после гастрэктомии позволило практически исключить такие послеоперационные осложнения как: развитие энтеро-эзофагеального рефлюкса, рефлюкс-эзофагита, пептические осложнения со стороны пищевода и анастомоза за счет наличия аппаратного шва, разобщающего в приводящем колене петли тонкой кишки прохождение желчи и пищеварительных ферментов от пищеводно-тонкокишечного анастомоза, без риска некротических изменений в кишке и нарушения ее нервной регуляции. Также за счет изоперистальтического эффекта при анастамозировании пищевода с приводящей петлей тощей кишки и наличия ее изгиба в обход линии аппаратного шва, обеспечивается более физиологичное порционное поступление пищи. Предложенный способ ускоряет восстановление обменных процессов и гомеостаз, обеспечивая раннюю социальную адаптацию пациентов, перенесших гастрэктомию.
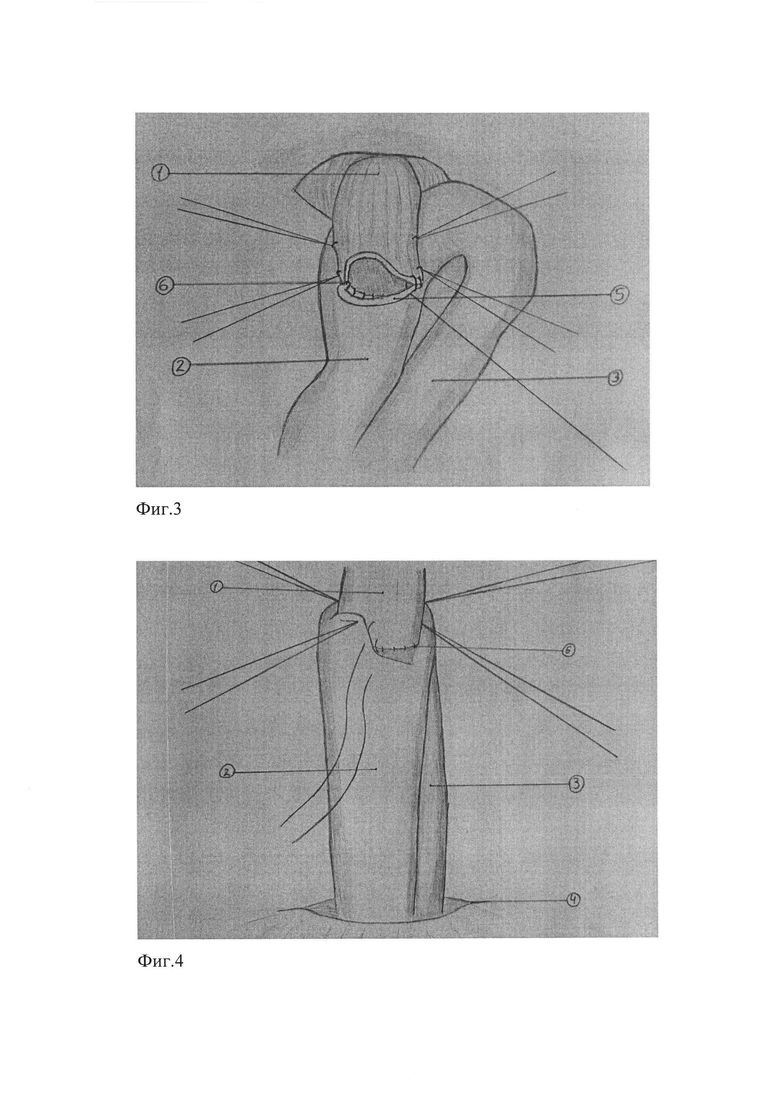
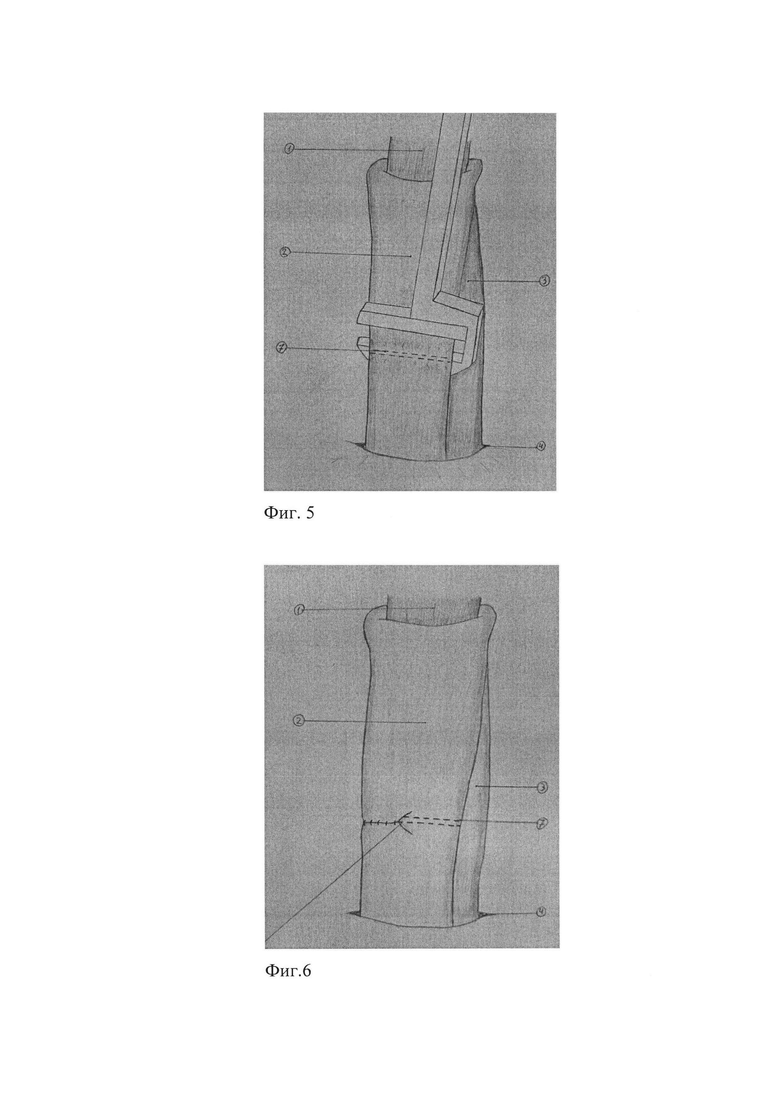
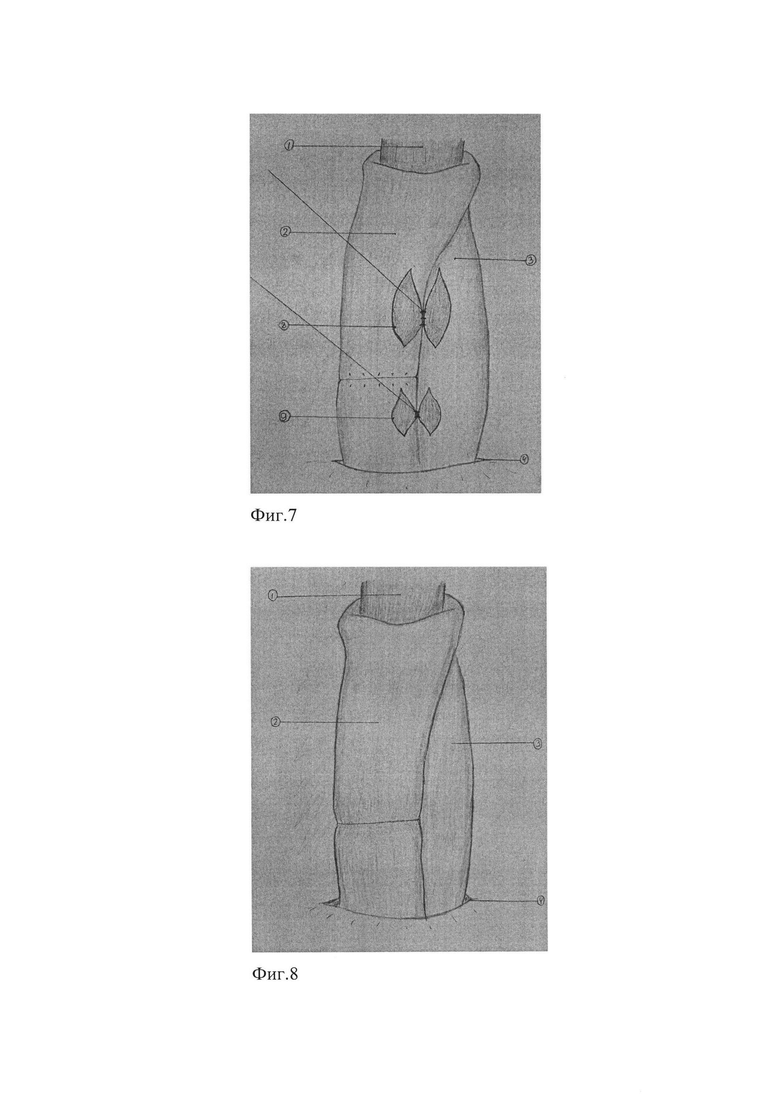
Для лучшего понимания, способ поясняется в примерах на фиг. 3 - формирование эзофагоеюноанастомоза способом конец пищевода в бок приводящей петли тощей кишки, фиг. 4 - пищеводно-кишечный анастомоз инвагинированный в кишку подтянутой и навернутой на него стенкой отводящей петли, фиг. 5 - поперечное прошивание механическим двухрядным скрепочным швом приводящей петли кишки, фиг. 6 - укрытие механического скрепочного шва обвивным серозно-мышечно-подслизистым швом, фиг. 7 - формирование двух межкишечных анастомозов по Брауну, фиг. 8 - заключительный вид реконструкции пищеварительного тракта после гастрэктомии предложенным способом, на которых: п. 1 - пищевод, п. 2 - приводящая петля тощей кишки, п. 3 - отводящая петля тощей кишки, п. 4 - бессосудистое окно в брыжейке поперечно-ободочной кишки, п. 5 - поперечный разрез тощей кишки, п. 6 - пищеводно-кишечный анастомоз, п. 7 - поперечный механический скрепочный шов, п. 8 - проксимальный межкишечный анастамоз, п. 9 - дистальный межкишечный анастамоз.
Способ осуществляют следующим образом.
Производят верхнесрединную лапаротомию, с обходом пупка влево и вниз на 3 см. Выполняют гастрэктомию по стандартной методике с расширенной D2-D3 лимфодиссекцией. Двенадцатиперстную кишку прошивают аппаратом УО-60, механический шов укрывают двумя полукисетами и Z-образным швом. Перед отсечением пищевода надсекают его мышечный слой до подслизистого. Затем, отступя 0,5 см от края сократившихся мышц, накладывают Г-образный зажим, по краю которого отсекают пищевод. После смены перчаток и инструментов, через бессосудистое окно в брыжейке поперечно-ободочной кишки (фиг. 4, п. 4) проводят без натяжения к культе пищевода (фиг. 3, п. 1) начальную петлю тощей кишки длиной 30 см от связки Трейца. Между задней стенкой культи пищевода и свободным краем приводящей петли тонкой кишки поперечно накладывают непрерывные обвивные серозно-мышечно-подслизистые швы в два ряда нерассасывающейся атравматичной нитью 3/0, завязывают нити на диаметрально противоположных краях при помощи свободной нити, пропущенной через последний стежок обвивного шва, берут на держалки. Ножницами поперечно длиннику рассекают стенку кишки (фиг. 3, п. 5) до подслизистого слоя на протяжении 2,0-3,0 см, ориентируются на диаметр пищевода, затем электроножом досекают подслизистый слой и слизистую, после чего анастомозируют конец пищевода в бок приводящей кишки (фиг. 3 п. 6) при помощи обвивного прецизионного серозно-мышечно-подслизистого шва рассасывающейся нитью. Инвагинируют передний ряд швов эзофагоеюноанастомоза (фиг. 4, п. 6) в приводящую кишку при помощи четырех полукисетных серозно-мышечных швов, которые формируют последовательно при помощи дистальных и проксимальных боковых нитей, взятых ранее на держалки с двух сторон и трех «салазочных» швов между дистальными нитями, завязанных полукисетных швов, поперечное плечо которых, проходит через стенку пищевода с захватом подслизистого слоя. Завязывают «салазочные» швы, наворачивают стенку приводящей кишки (фиг. 4, п. 2) проксимально, инвагинируют в нее пищевод (фиг. 4, п. 1), формируя вокруг линии швов «перитонеальное кольцо». Затем на расстоянии 12 см от анастомоза поперечно прошивают механическим двухрядным скрепочным швом (фиг. 5, п. 7) приводящую петлю тонкой кишки (фиг. 5, п. 2), разобщая, таким образом, в приводящем колене прохождение желчи и панкреатического сока от пищеводно-тонкокишечного анастомоза. Механический шов укрывают (фиг. 6, п. 7) обвивным серозно-мышечно-подслизистым швом нерассасывающейся атравматичной нитью 3/0, этой же нитью сшивают брыжеечные края приводящей и отводящей кишки (фиг. 6, п. 3) на расстоянии 5,0 см. выше и на 3,0 см. ниже от механического шва. Далее формируют два межкишечных анастомоза по Брауну, - проксимальный (фиг. 7, п. 8) для прохождения пищи из приводящей в отводящую петлю кишки длиной 4,0 см и дистальный (фиг. 7, п. 9) длиной 1,5 см - для прохождения желчи и панкреатического сока. Завершают операцию (фиг. 8) установкой силиконового дренажа через контрапертуру в правом подреберье, через Винслово отверстие под нижним краем печени, проведя его к зоне лимфодиссекции, концом к эзофагоэнтероанастомозу и послойным ушиванием лапаратомной раны. Дренаж удаляют на 4-е сутки после рентгенологического контроля состоятельности анастомоза и прекращения лимфореи после расширенной лимфодиссекции.
Способ апробирован у двенадцати пациентов, как реконструктивный этап, при выполнении гастрэктомии по поводу рака желудка. При сравнительном анализе с простым петлевым пищеводно-тонкокишечным анастомозом, выполненным в эти же сроки, разработанный нами способ анастомоза показал существенные функциональные преимущества, такие как отсутствие рефлюкс-эзофагита и пептических осложнений со стороны пищевода, порционный пассаж пищи, раннее восстановление обменных процессов и обеспечение субъективно более высокого качества жизни.
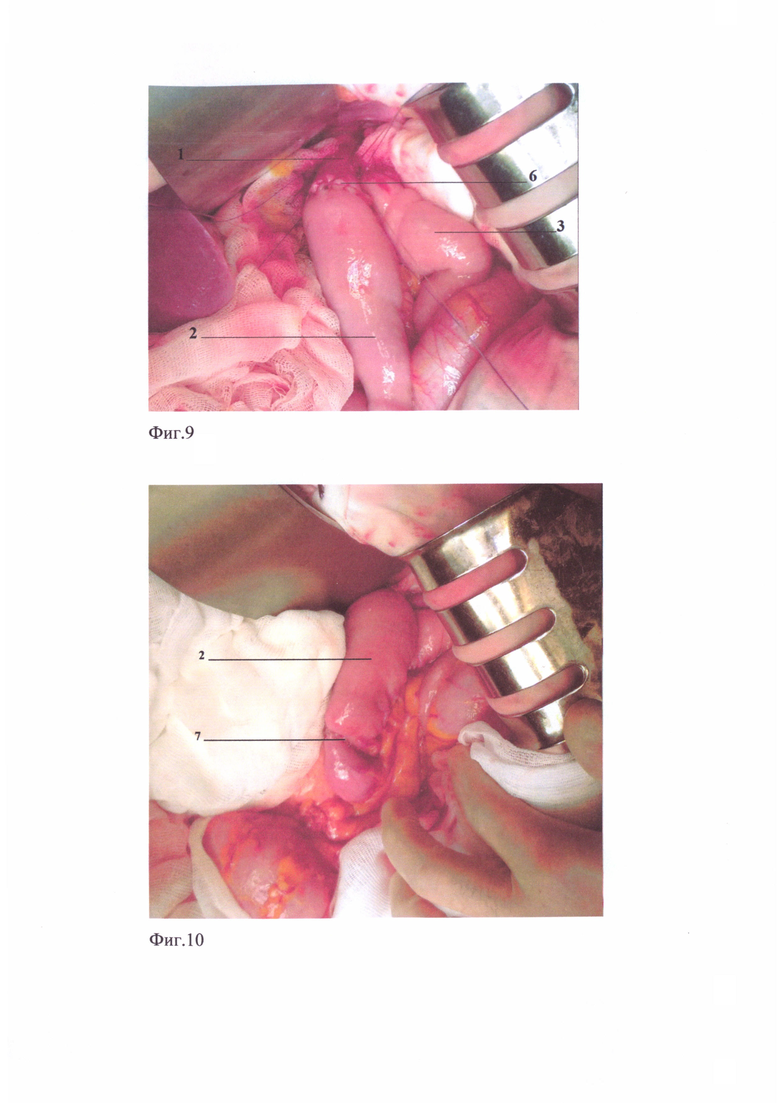
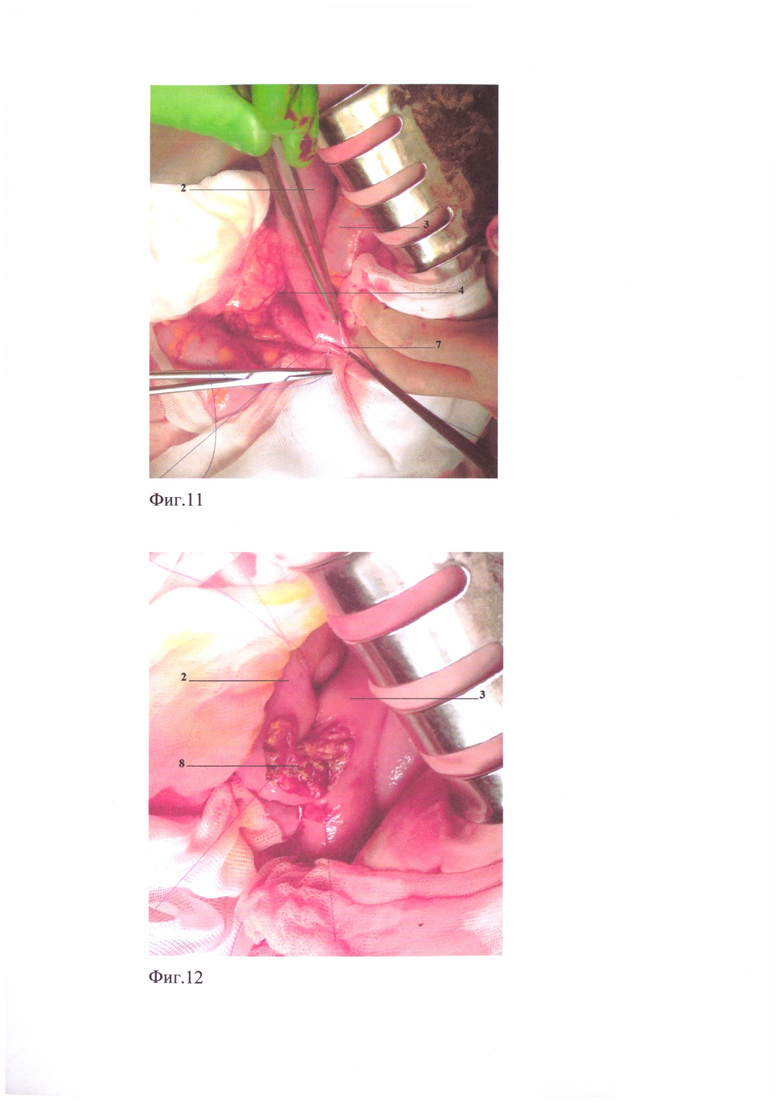
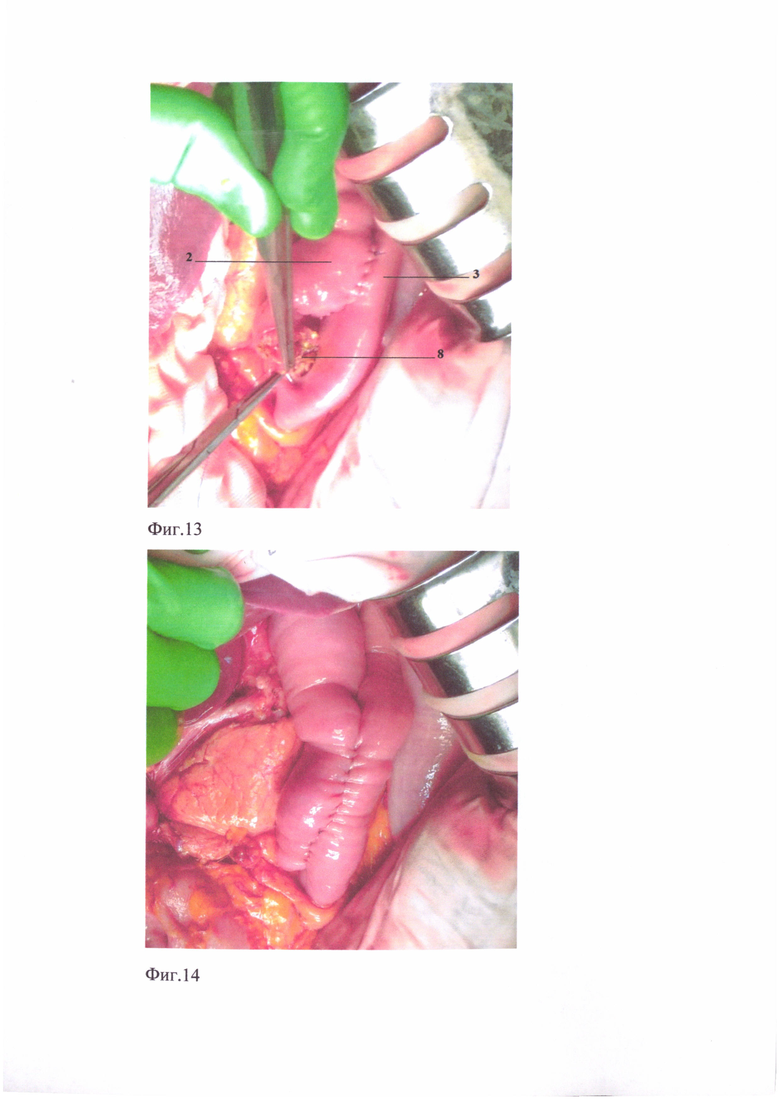
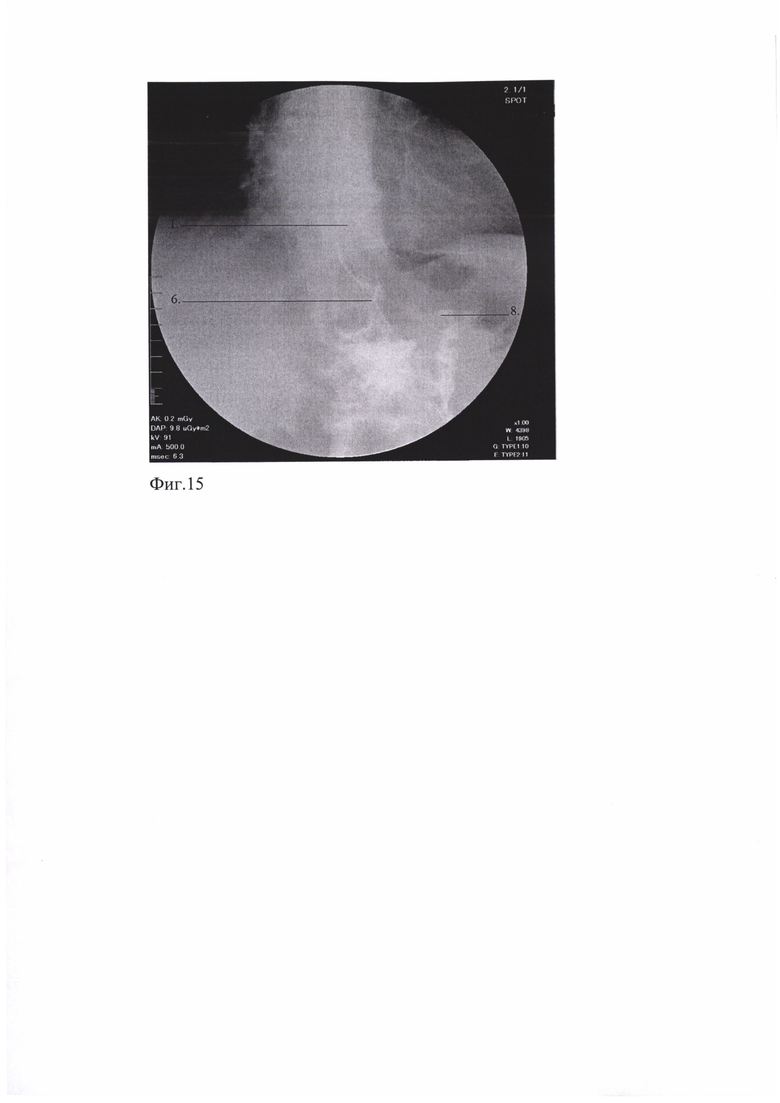
Клинический пример дополнительно иллюстрируется на: фиг. 9 - интраоперационный вид формирования пищеводно-кишечного анастомоза конец в бок приводящей петли тонкой кишки, фиг. 10 - интраоперационный вид поперечного механического ушивания приводящей петли тонкой кишки, фиг. 11 - интраоперационный вид укрытия механического двухрядного скрепочного шва приводящей петли тонкой кишки обвивным серозно-мышечно-подслизистым швом, фиг. 12 - интраоперационный вид формирования проксимального межкишечного анастомоза по Брауну, фиг. 13 - интраоперационный вид формирования дистального межкишечного анастомоза по Брауну, фиг. 14 - интраоперационный конечный вид реконструкции пищеварительного тракта после гастрэктомии предложенным способом, фиг. 15 - рентгенография анастомоза с контрастированием.
Пример 1. Больной Е., 52 года, поступил в хирургическое отделение №2 ГБУЗ «НИИ-ККБ №1 им. проф. С.В. Очаповского» с диагнозом с-г желудка T3NxM0, 2 кл. гр. Болен около 4 месяцев, жалобы на плохой аппетит, потерю в весе до 5 кг за последний месяц. При фиброэзофагогастродуоденоскопии: пищевод свободно проходим, в теле желудка определяется инфильтративная опухоль без четких границ с изъявлениями в центре до 6 см в диаметре. Гистологический диагноз - низкодифференцированная аденокарцинома с наличием перстневидных клеток прорастает всю толщу стенки желудка. Больному под эндотрахеальным наркозом проведена операция лапаротомия, гастрэктомия с расширенной (D-2) лимфодиссекцией. При ревизии: инфильтративный рак тела желудка, вдоль левой желудочной артерии определяются увеличенные лимфоузлы, печень, селезенка, серозная оболочка кишок и париетальная брюшина не изменены. Желудок мобилизовали со всеми связками, большим и малым сальниками, провели лимфодиссекцию в объеме D-2. Двенадцатиперстную кишку прошили аппаратом УО-60, механический шов укрыли двумя полукисетами и Z-образным швом. Перед отсечением пищевода предварительно надсекли его мышечный слой до подслизистого. Затем, отступив 0,5 см от края сократившихся мышц, наложили Г-образный зажим, по нижнему краю которого отсекли пищевод. Произвели смену перчаток и инструментов, обработку операционного поля водным раствором хлоргексидина (0,05%). Реконструктивный этап выполнили по описанному способу. Через бессосудистое окно в брыжейке поперечно-ободочной кишки провели без натяжения к культе пищевода начальную петлю тощей кишки длиной 30 см от связки Трейца. Между задней стенкой культи пищевода и свободным краем приводящей петли тонкой кишки поперечно наложили непрерывные обвивные серозно-мышечно-подслизистые швы в два ряда, боковые нити которых, после завязывания с отдельной нитью, пропущенной в последний стежок, взяли на держалки. Ножницами поперечно длиннику кишки рассекли серозную оболочку и мышечный слой - до подслизистого слоя, затем электроножом - подслизистый и слизистый слои на 2,5 см, - в соответствии с диаметром пищевода и анастамозировали конец пищевода в бок приводящей кишки (фиг. 9, п. 6) обвивным прецизионным серозно-мышечно-подслизистым швом нитью «Биосин» (3/0). После постановки назоинтестинального зонда предназначенного для питания за анастомоз, смены перчаток и инструмента начали формирование наружного ряда швов. Укрытие переднего ряда швов анастомоза выполнили при помощи четырех полукисетных серозно-мышечных швов за счет дистальных и проксимальных боковых нитей, взятых ранее на держалки с каждой стороны и трех «салазочных» швов между ними, поперечное плечо которых прошло через стенку пищевода с захватом подслизистого слоя. Завязали «салазочные» швы, при этом навернув стенку приводящей кишки, инвагинировали в ее просвет пищевод. На расстоянии 12 см от анастомоза поперечно прошили механическим двухрядным скрепочным швом (фиг. 10., п. 7) приводящую петлю тонкой кишки, разобщая, таким образом, в приводящей кишке прохождение желчи и панкреатического сока от пищеводно-тонкокишечного анастомоза. Контролировали зонд, - во избежание его прошивания аппаратом. Механический шов укрыли обвивным серозно-мышечно-подслизистым швом (фиг. 11, п. 7) нерассасывающейся атравматичной нитью 3/0, этой же нитью сшили брыжеечные края приводящей и отводящей кишки на расстоянии 5,0 см. выше и на 2,0 см. ниже от механического шва. Затем сформировали два межкишечных анастомоза по Брауну, - проксимальный для прохождения пищи из приводящей в отводящую петлю кишки длиной 4,0 см (фиг. 12, п. 8) и дистальный длиной 1,5 см (фиг. 13, п. 9) - для прохождения желчи и панкреатического сока. Питательный зонд провели через мижкишечное соустье для пиши и опустили его на 15,0 см ниже второго межкишечного анастомоза. Завершили операцию (фиг. 14) установкой силиконового дренажа через контрапертуру в правом подреберье, через Винслово отверстие под нижним краем печени, проведя его к зоне лимфодиссекции, концом к эзофагоэнтероанастомозу и последующим послойным ушиванием лапаратомной раны отдельными узловыми швами.
Послеоперационный период протекал без осложнений. По дренажу за сутки выходило менее 150 мл серозно-геморрагического отделяемого. Через 12 часов после операции было начато кормление по назоинтестинальному зонду энтеральной питательной смесью, - в 1-е сутки по 10 мл в час - круглосуточно. К 4-м суткам объем кормления был постепенно увеличен - до 25 мл в час. На вторые сутки больному было разрешено пить воду небольшими глотками до 250,0 мл в сутки. На 4-е сутки проведена контрастная рентгеноскопия зоны анастомоза: функционирует удовлетворительно, бариевая взвесь поступает в приводящую петлю тощей кишки и через проксимальный межкишечный анастомоз (фиг. 15, п. 8) порционно поступает в отводящую петлю, был удален дренаж из брюшной полости и питательный зонд. На 5-е сутки начато кормление по столу 0/1, на 7-е сутки - назначена щадящая диета. Пациент выписан из стационара на 11 сутки после операции в удовлетворительном состоянии под наблюдение хирурга, онколога по месту жительства. В послеоперационном периоде вес не снижался, отмечалось хорошее усвоение пищи. Контрольное обследование через 3 месяца: жалоб не предъявляет, поправился на 2,5 кг. ФЭГС, УЗИ брюшной полости: слизистая пищевода на всем протяжении физиологической окраски, без признаков воспаления, определена линия анастомоза, отмечается незначительный отек. Пищеводно-кишечное и межкишечное соустье проходимы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЗАМЕЩЕНИЯ ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ | 2011 |
|
RU2474392C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПОПЕРЕЧНОГО ГАСТРОЕЮНОАНАСТОМОЗА ПОСЛЕ СУБТОТАЛЬНОЙ ДИСТАЛЬНОЙ РЕЗЕКЦИИ ЖЕЛУДКА | 2015 |
|
RU2585740C1 |
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ КАРДИОЭЗОФАГЕАЛЬНОГО РАКА | 2008 |
|
RU2391055C2 |
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА ПОСЛЕ ГАСТРЭКТОМИИ ПО ПОВОДУ РАКА ЖЕЛУДКА | 1999 |
|
RU2146499C1 |
| Способ формирования пищеводно-желудочного анастомоза | 2024 |
|
RU2826391C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА ПОСЛЕ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ И ЭКСТИРПАЦИИ ЖЕЛУДКА С ВОССТАНОВЛЕНИЕМ ФИЗИОЛОГИЧЕСКОЙ И АНАТОМИЧЕСКОЙ ЦЕЛОСТНОСТИ | 2016 |
|
RU2636881C1 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ПИЩЕВОДНО-КИШЕЧНОГО АНАСТОМОЗА ПОСЛЕ ГАСТРЭКТОМИИ | 2006 |
|
RU2327426C1 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА | 2009 |
|
RU2437623C2 |
| СПОСОБ ФОРМИРОВАНИЯ ИСКУССТВЕННОГО ЖЕЛУДКА | 2010 |
|
RU2445018C2 |
| СПОСОБ ПЕРВИЧНОЙ ЕЮНОГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 1999 |
|
RU2189789C2 |
Изобретение относится к медицине, а именно к хирургии и онкологии. Через бессосудистое окно в брыжейке поперечно-ободочной кишки проводят начальную петлю тонкой кишки длиной 30 см от связки Трейца. Между задней стенкой культи пищевода и приводящей петлей кишки поперечно накладывают непрерывные обвивные серозно-мышечно-подслизистые швы в два ряда, боковые нити после завязывания со свободной нитью, пропущенной через последний стежок обвивного шва, берут на держалки. Затем в соответствии с диаметром пищевода поперечно рассекают стенку кишки и анастомозируют пищевод в бок приводящей кишки обвивным прецизионным серозно-мышечно-подслизистым швом. Погружают передний ряд внутренних швов анастомоза в приводящую кишку, поочередно при помощи четырех полукисетных швов - за счет дистальных и проксимальных боковых нитей, взятых ранее на держалки с двух сторон, и трех «салазочных» швов между дистальными полукисетными швами, поперечное плечо которых проходит через стенку пищевода с захватом подслизистого слоя. Завязывают «салазочные» швы, наворачивают стенку приводящей кишки, инвагинируя в нее пищевод. Затем на расстоянии 12 см от анастомоза поперечно прошивают приводящую петлю тонкой кишки механическим двухрядным скрепочным швом, который укрывают обвивным серозно-мышечно-подслизистым швом, этой же нитью сшивают между собой брыжеечные края приводящей и отводящей петель кишки выше на 5,0 см и ниже на 3,0 см от механического шва. Формируют два межкишечных анастомоза по Брауну, - проксимальный анастомоз для прохождения пищи из приводящей в отводящую петлю кишки длиной 4,0 см и дистальный длиной 1,5 см - для прохождения желчи и панкреатического сока. Способ предотвращает энтеро-эзофагеальный рефлюкс, рефлюкс-эзофагит, пептические осложнения со стороны пищевода и анастомоза, обеспечивает более физиологичное дробное поступление пищи. 15 ил., 1 пр.
Способ восстановления непрерывности пищеварительного тракта после гастрэктомии, включающий формирование петлевого пищеводно-тонкокишечного анастомоза, отличающийся тем, что после расширенной гастрэктомии через бессосудистое окно в брыжейке поперечно-ободочной кишки проводят начальную петлю тонкой кишки длиной 30 см от связки Трейца, между задней стенкой культи пищевода и приводящей петлей кишки поперечно накладывают непрерывные обвивные серозно-мышечно-подслизистые швы в два ряда, боковые нити после завязывания со свободной нитью, пропущенной через последний стежок обвивного шва, берут на держалки, затем в соответствии с диаметром пищевода поперечно рассекают стенку кишки и анастомозируют пищевод в бок приводящей кишки обвивным прецизионным серозно-мышечно-подслизистым швом, погружают передний ряд внутренних швов анастомоза в приводящую кишку, поочередно при помощи четырех полукисетных швов за счет дистальных и проксимальных боковых нитей, взятых ранее на держалки с двух сторон, и трех «салазочных» швов между дистальными полукисетными швами, поперечное плечо которых проходит через стенку пищевода с захватом подслизистого слоя, завязывают «салазочные» швы, наворачивают стенку приводящей кишки, тем самым инвагинируют в нее пищевод, затем на расстоянии 12 см от анастомоза поперечно прошивают приводящую петлю тонкой кишки механическим двухрядным скрепочным швом, который укрывают обвивным серозно-мышечно-подслизистым швом, этой же нитью сшивают между собой брыжеечные края приводящей и отводящей петель кишки выше на 5,0 см и ниже на 3,0 см от механического шва, после чего формируют два межкишечных анастомоза по Брауну, - проксимальный анастомоз для прохождения пищи из приводящей в отводящую петлю кишки длиной 4,0 см и дистальный длиной 1,5 см - для прохождения желчи и панкреатического сока.
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ТОНКОКИШЕЧНОГО АНАСТОМОЗА ПОСЛЕ ГАСТРЭКТОМИИ ПО ПОВОДУ РАКА ЖЕЛУДКА | 1999 |
|
RU2146499C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ НЕПРЕРЫВНОСТИ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА ПОСЛЕ ГАСТРЭКТОМИИ | 2016 |
|
RU2655980C1 |
| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОГО ВЫКЛЮЧЕНИЯ ЭЛЕКТРОДВИГАТЕЛЯ ПРИ СНЯТИИ ОГРАЖДЕНИЯ СТАНКА ИЛИ МАШИНЫ, ПРИВОДИМОЙ ИМ В ДЕЙСТВИЕ | 1930 |
|
SU22130A1 |
| Артиллерийский снаряд | 1930 |
|
SU21733A1 |
| US 20100081864 A1, 01.04.2010 | |||
| ОСМОНАЛИЕВ Б.К | |||
| Сравнительная оценка лигатурного и компрессионных способов формирования пищеводно-кишечных анастомозов при гастрэктомии | |||
| Автореф.диссерт | |||
| на соиск.уч.ст.к.м.н., Тюмень, 2010 | |||
| LACERDA CF et al | |||
Авторы
Даты
2020-11-09—Публикация
2020-03-03—Подача