Область техники, к которой относится изобретение
Изобретение относится к области медицины и медико-технических технологий, а именно к интраоперационной диагностике и функциональной диагностике, и предназначено для обнаружения и распознавания локальных неоднородностей, отличающихся по оптическим свойствам от окружающих биологических тканей в области исследования. Возможно применение способа для различных видов оперативного вмешательства или инвазивных манипуляций, а также для зондирования через интактные кожные покровы. В частности, изобретение может быть использовано в нейрохирургии для обнаружения и распознавания нейроваскулярных структур, артериальных и венозных сосудов и нервов, в объеме биологической ткани во время проведения операций по удалению опухоли головного мозга, в том числе эндоскопическим трансназальным методом.
Уровень техники
Задача по обнаружению и распознаванию нейроваскулярных структур особенно актуальна в нейрохирургии при выполнении операций по удалению новообразований. Проблематика текущих способов резекции опухолей основания черепа эндоскопическим трансназальным методом заключается в сложности проведения самой операции. Патологическая ткань удаляется эндоскопическим инструментарием через пазухи носа кусочно, по несколько миллиметров. В процессе операции высок риск повреждения нейроваскулярных структур, находящихся в объеме опухолевой ткани. Повреждение черепно-мозгового нерва приводит к утрате функциональных возможностей мышц, связанных с травмированным нервом, утрате важных физиологических функций, существенному ухудшению качества жизни; повреждение артериального сосуда - к мгновенному летальному исходу.
Для минимизации повреждения нейроваскулярных структур, а также для повышения степени радикальности резекции опухолевой ткани применимы современные способы диагностики и визуализации, такие как магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография (КТ), позитронно-эмиссионная томография (ПЭТ), магнитно-резонансная спектроскопия, однофотонная эмиссионная компьютерная томография (ОЭКТ), рентгенография и ангиография. Перечисленные способы и соответствующие технические средства позволяют проводить предоперационную диагностику, предоставляя информацию об индивидуальных анатомических (васкуляризация), физиологических (скорость кровотока, перфузия) и метаболических особенностях тканей и органов пациента. Для предоперационного определения расположения нервов в опухоли также применяют способ диффузионной тензорной трактографии [1]. Существенным недостатком указанных предоперационных способов диагностики является невозможность их применения для локальной нейронавигации в ходе операционных вмешательств. Для дифференцирования тканей и клеток, оценки их функциональной активности и локальной гемодинамики применимы такие оптические методы, как Рамановская спектроскопия in vivo [2], широкополосная [3] и узкополосная [4] спектроскопия, мультиспектральная визуализация [5], флуоресцентная спектроскопия и визуализация [6-8], метод оптоакустической (фотоакустической) визуализации [9] и мультимодальные сочетанные решения. Однако указанные оптические методы имеют ряд ограничений, таких как малая глубина зондирования (до 1,5 мм), отсутствие стандартных методик применения в клинической практике, либо технических решений, применимых in situ для нейрохирургии с эндоскопическим трансназальным доступом.
Известно использование для идентификации кровеносного сосуда интраоперационной ультразвуковой допплерографии (УЗДГ) [10]. Этот способ дает информацию о наличии сосуда в объеме биоткани по скорости и направлению кровотока в сосуде. Для сканирования операционного поля применяют комбинированное устройство с подвижной рабочей частью, что позволяет лоцировать сосуды в различных направлениях. Наличие артериального сосуда, глубину его залегания относительно поверхности опухоли оценивают по монитору в окне М-режима (M-Mode). Недостаток УЗДГ связан со сложностью обнаружения нервных структур в объеме ткани. Ультразвуковая визуализация нервов и сосудов, представленная в [11], не предназначена для малого операционного поля с ограниченным доступом, например, эндоназальной нейрохирургии. Идентификацию данных структур проводят путем анализа получаемых трудно интерпретируемых изображений.
Для идентификации черепных нервов известно использование триггерной электромиографии (т-ЭМГ, t-EMG) и спонтанной электромиографии (free run ЭМГ, f-EMG) [12,13]. Нейрофизиологическая идентификация черепных нервов в несколько раз снижает частоту их поражения, и как следствие, повышает качество жизни пациентов. Однако способ на основе т-ЭМГ позволяет идентифицировать только двигательные и смешанные нервы. К основным недостаткам т-ЭМГ также относятся широкая зона распространения тока по электропроводящим тканям, что может привести к возбуждению отдаленных нервных структур и к ложному ответу на стимуляцию, и необходимость регистрации отклика дополнительными измерительными средствами вне области локализации нерва. Современной альтернативой электрической стимуляции нервов является оптическая инфракрасная (ИК) стимуляция [14,15], не требующая непосредственного контакта со стимулируемым нервом и оказывающая локальное воздействие. Однако существенным ограничением данного способа является возможность обнаружения нерва при его поверхностном залегании и необходимость использования дополнительных средств для регистрации отклика. Оптическая отражательная спектроскопия [16] позволяет интраоперационно дифференцировать ткани по составу, например по концентрации гемоглобина и липидов. Однако данный способ может быть использован для идентификации поверхностно расположенных нервов и не применим для анализа глубинных слоев ткани.
Наиболее близким к заявляемому является способ интраоперационного обнаружения и распознавания нейроваскулярных структур в объеме биологической ткани [17, 18], согласно которому линейным оптоволоконным датчиком для отражательной диффузионной спектроскопии с расстояниями между источниками и приемниками 6 мм и 9 мм осуществляют подповерхностное зондирование исследуемого объема биологической ткани на глубину 2-5 мм, первой длиной волны (λ1 < 806 нм, λ1 = 692 нм) и второй длиной волны (λ2 > 806 нм, λ2 = 834 нм) из красного и/или ближнего инфракрасного (КБИК) диапазона на основе фазово-модуляционного или иначе частотного подхода (FD - frequency domain) спектроскопического метода с временным разрешением. Определяют значения оптических параметров: коэффициентов поглощения для первой длины волны μa(λ1) и для второй длины волны μa(λ2), с поправкой на содержание воды в единице объема биологической ткани, и коэффициентов транспортного рассеяния μs'(λ1) для первой длины волны и μs'(λ2) для второй длины волны. По указанным оптическим параметрам оценивают производные параметры в виде отношений 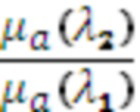 ,
, 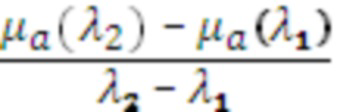 и
и 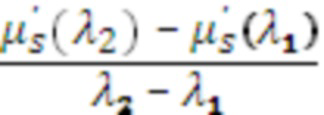 и/или физиологические параметры, такие как тканевая сатурация (StO2), концентрация общего гемоглобина ([tHb]) в единице исследуемого объема биологической ткани и индекс пульсовых гемодинамических колебаний этого объема. Применяют критерии сравнения получаемых производных и физиологических параметров с пороговыми значениями для обнаружения и распознавания нейроваскулярных структур, нервов, артериальных и венозных сосудов, с учетом предоперационной и диагностической информации об особенностях микроциркуляторного кровенаполнения исследуемого объема и его морфологической структуры на клеточном уровне.
и/или физиологические параметры, такие как тканевая сатурация (StO2), концентрация общего гемоглобина ([tHb]) в единице исследуемого объема биологической ткани и индекс пульсовых гемодинамических колебаний этого объема. Применяют критерии сравнения получаемых производных и физиологических параметров с пороговыми значениями для обнаружения и распознавания нейроваскулярных структур, нервов, артериальных и венозных сосудов, с учетом предоперационной и диагностической информации об особенностях микроциркуляторного кровенаполнения исследуемого объема и его морфологической структуры на клеточном уровне.
Однако данный способ характеризуется ограниченностью поля зрения в связи с использованием узконаправленного зондирования, реализуемого оптоволоконным датчиком линейной конфигурации, не инвариантностью к расположению нейроваскулярных структур при их наличии в исследуемом объеме биологический ткани и, как следствие, неравномерной чувствительностью к нейроваскулярным структурам при незначительных смещениях оптоволоконного датчика. Кроме того, известный способ при обнаружении и распознавании нейроваскулярных структур не учитывает информативные пульсовую и дыхательную составляющие гемодинамических процессов, протекающих в исследуемом объеме биологической ткани. Существенным недостатком известного способа является неконтролируемое позиционирование и/или неконтролируемая сила прижатия оптоволоконного датчика к поверхности исследуемого объема биологической ткани, что приводит к наличию двигательных артефактов в измерениях, вызванных тремором руки, и/или неконтролируемому пережатию биологической ткани в момент контактного зондирования исследуемого объема и, как следствие, к искажению полученных данных за счет изменения структурных и оптических параметров и снижению эффективности обнаружения и распознавания нейроваскулярных структур. Недостатком является также отсутствие оценок, качественных и/или количественных, типа артериального или венозного сосуда при его выявлении в исследуемом объеме биологической ткани. Кроме того, указанный способ не позволяет контролировать наличие возможного спазмирования артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии и степень ишемизации кровоснабжаемых ими тканей в процессе операции, что может приводить к значительному снижению эффективности и качества выполненной операции.
Технической проблемой является разработка способа, устраняющего перечисленные выше недостатки.
Раскрытие изобретения
Технический результат изобретения заключается в получении достоверных данных о наличии нервов, крупных и малых артерий и вен в объеме биологической ткани на глубине, как минимум, до 5 мм во время проведения операций.
Заявляемый способ является универсальным, может быть применен как для нейрохирургических операций открытого или эндоскопического, в том числе трансназального доступа, так и других видов оперативного вмешательства по удалению опухоли, а также в пластической и реконструктивной хирургии и, кроме того, для определения и распознавания нейроваскулярных структур через интактные кожные покровы, например при венепункции или лоцировании периферических нервов.
Использование заявляемого способа повышает эффективность интраоперационного обнаружения и распознавания нейроваскулярных структур, что снижает риски их случайного повреждения в процессе проведения хирургического вмешательства, и как следствие, повышает качество оказываемой медицинской помощи.
Указанный технический результат достигается тем, что в способе интраоперационного обнаружения и распознавания нейроваскулярных структур в объеме биологической ткани, осуществляют
контактное подповерхностное зондирование исследуемого объема биологической ткани оптическим излучением с использованием оптоволоконного датчика для отражательной диффузионной спектроскопии, включающего приемник и излучатели, по меньшей мере, на двух длинах волн, (λ1) и (λ2), где λ2 > λ1, выбранных из диапазона 650 нм - 950 нм на максимальную глубину не менее 5 мм, регистрацию методом спектроскопии с временным разрешением для каждой длины волны параметров обратнорассеянного излучения, оптических параметров, включая коэффициент поглощения μa(λi) и транспортный коэффициент рассеяния μs'(λi), по которым определяют концентрацию общего гемоглобина ([tHb]) в единице исследуемого объема биологической ткани и тканевую сатурацию (StO2), а также тангенс угла наклона транспортного коэффициента рассеяния от длины волны (Ds), с последующим обнаружением и распознаванием нейроваскулярных структур: нервов, артериальных и венозных сосудов, по итогам сравнения полученных параметров с их пороговыми значениями, полученными на основе оценки предоперационных и интраоперационных диагностических данных.
При этом зондирование исследуемого объема биологической ткани осуществляют с использованием, по меньшей мере, двух групп излучателей и, по меньшей мере, одного приемника, где группы излучателей располагают соосно с приемником каждая, причем на отдельных несовпадающих полуосях (с началом полуоси в центре фотоприемника). Каждая группа состоит, как минимум, из двух подгрупп, каждая из которых содержит излучатели, по меньшей мере, двух длин волн из указанного диапазона значений, расположенные друг от друга на расстоянии не более 1 мм, и каждая подгруппа - на определенном расстоянии (rj, j=1..M, M≥2) от приемника вдоль соответствующей полуоси, что обеспечивает указанную глубину зондирования по каждому направлению вдоль полуоси.
По полученным значениям интенсивности обратнорассеянного излучения в исследуемом объеме биологической ткани для каждой длины волны и каждого каждого rj дополнительно определяют:
амплитуды пульсовых (Aп) и дыхательных (Aд) колебаний, и их отношение Ап/д= Ап/ Ад, вектор формы ( ), представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду
), представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду 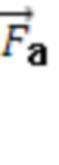 , крупному венозному сосуду
, крупному венозному сосуду 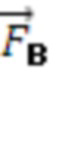 , или функциональной тканевой единице в размерах исследуемого объема биологической ткани , -
, или функциональной тканевой единице в размерах исследуемого объема биологической ткани , -
а для каждой подгруппы источников, по меньшей мере, для двух длин волн из указанного диапазона определяют локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п).
Перечисленные выше параметры измеряют в статическом режиме, при котором давление оптоволоконного датчика P на поверхность исследуемого объема биологической ткани составляет P ≤ 0,2 мм рт. ст.
Выводы о наличии определенных нейроваскулярных структур делают по получению следующих совокупностей измеренных параметров:
- при {Ds > 0; [tHb] > [tHb]0; StO2 > (StO2)0; Ап/д > (Ап/д)0;  =; Δ[tHb]п > (Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
=; Δ[tHb]п > (Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
- при {Ds > 0; [tHb] > [tHb]0; StO2 ≤ (StO2)0 или StO2 > (StO2)0; Ап/д < (Ап/д)0;  =; Δ[tHb]п ≤ (Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
=; Δ[tHb]п ≤ (Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
- при {Ds0 < Ds < 0; [tHb] ≤ [tHb]0; StO2 ≤ (StO2)0; Ап/д ≤ (Ап/д)0;  =; Δ[tHb]п < (Δ[tHb]п)0} (3) – о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
=; Δ[tHb]п < (Δ[tHb]п)0} (3) – о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
- при {Ds ≤ Ds0; [tHb] ≥ [tHb]0; StO2 ≥ (StO2)0; Ап/д ≥ (Ап/д)0;  =; Δ[tHb]п ≥ (Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой артерии;
=; Δ[tHb]п ≥ (Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой артерии;
- при {Ds0 < Ds < 0; [tHb] > [tHb]0; StO2 ≥ (StO2)0; Ап/д > (Ап/д)0;  =; Δ[tHb]п > (Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs'(λ) > 0;
=; Δ[tHb]п > (Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs'(λ) > 0;
- при {Ds0 ≤ Ds < 0; [tHb] ≥ [tHb]0; StO2 ≤ (StO2)0; Ап/д ≤ (Ап/д)0;  =; Δ[tHb]п ≤ (Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой вены,
=; Δ[tHb]п ≤ (Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой вены,
где [tHb]0, Ds0, (StO2)0, (Ап/д)0, (Δ[tHb]п)0 - пороговые значения упомянутых параметров, измеренные для функциональной тканевой единицы в размерах исследуемого объема биологической ткани,
причем значения параметров Ds, [tHb] и StO2 определяют для каждой группы излучателей и соответствующего приемника.
Для распознавания нейроваскулярной структуры в исследуемом объеме биологической ткани необходимо и достаточно выполнения критериев для Ds, [tHb] и StO2 хотя бы для одной группы излучателей и соответствующего приемника и выполнения критериев для Ап/д,  и Δ[tHb]п хотя бы для одной подгруппы излучателей этой группы.
и Δ[tHb]п хотя бы для одной подгруппы излучателей этой группы.
В одном из вариантов осуществления изобретения по получению следующих совокупностей измеренных параметров: {Ds0 ≤ Ds < 0; [tHb] < [tHb]0; StO2 < (StO2)0; Ап/д = 0 (при отсутствии пульсовых колебаний)} (7), делают вывод о спазмировании артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии.
Кроме того, в одном из вариантов осуществления изобретения параметры μa(λi), μs'(λi), [tHb], StO2 и Ds дополнительно регистрируют при осуществлении динамического режима, характеризующегося вдавливанием оптоволоконного датчика в исследуемый объем биологической ткани с заданной постоянной скоростью VL ≤ 10 мм/мин при изменении силы от 0 до Fmax, соответствующей максимально допустимому для исследуемой биологической ткани уровню давления Pmax = Fmax/S, с учетом площади контакта S оптоволоконного датчика с поверхностью исследуемого объема биологической ткани, где Pmax принимает значения от 70 мм рт.ст. для тканей головного мозга до 200 мм рт.ст. для тканей нижних конечностей, или при двухэтапном изменении давления Р от 0 до 20 мм рт.ст. и от 20 мм рт.ст. до Pmax.
Возможно измерение параметров в статическом и динамическом режимах с использованием автоматизированного контроля позиционирования и силы прижатия оптоволоконного датчика к поверхности исследуемого объема биологической ткани, реализуемого с помощью устройства позиционирования, оснащенного датчиком перемещения и датчиком силы или силомоментным датчиком с пределом измерений не более 100 Н.
При измерении параметров в динамическом режиме одномоментно регистрируют зависимости силы прижатия (F) от перемещения оптоволоконного датчика (x) и силы прижатия (F) от времени (t) с частотой дискретизации не менее 20 Гц, на основании которых выявляют наличие артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме и оценивают величину сосуда по значению давления в сосуде. При этом вывод о наличии артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме, делают при выявлении пульсовых колебаний силы F(t) с максимумом в диапазоне частот сердечных сокращений от 0,7 до 3,5 Гц с использованием методов кратно-масштабного анализа дискретных сигналов в реальном времени, включая метод оконного преобразования Фурье и вейвлет-преобразование. Значение давления (P) артериального сосуда определяют по формуле P = F/S , где F - значение силы прижатия оптоволоконного датчика в момент времени tк, соответствующий концу пульсовых колебаний, S - площадь контакта оптоволоконного датчика с поверхностью исследуемого объема биологической ткани; и при получении значения 70≤ Pt ≤90 мм рт.ст. делают вывод о наличии малой артерии на глубине, большей максимальной глубины зондирования в статическом режиме; при получении P > 90 мм рт.ст. делают вывод о наличии крупной артерии на глубине, большей максимальной глубины зондирования в статическом режиме.
Возможен вариант реализации изобретения, согласно которому на первом этапе двухэтапного динамического режима, как минимум, для одной группы источников, при уменьшении параметров μa(λi) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, более чем на 25 % по сравнению со значениями, полученными в статическом режиме, и прекращении дыхательных колебаний в соответствующих регистрируемых сигналах обратнорассеянного излучения, дополнительно подтверждают наличие крупного венозного сосуда в исследуемом объеме биологической ткани. При уменьшении на первом и втором этапах двухэтапного динамического режима параметров μa(λi) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, менее чем на 25% по сравнению со значениями, полученными в статическом режиме, для всех групп источников, дополнительно подтверждают отсутствие в исследуемой области биологической ткани крупных сосудов.
Зондирование оптическим излучением исследуемого объема биологической ткани осуществляют равномерно при помощи секторного или матричного оптоволоконного датчика, не менее 15 с с последующим усреднением измеренных параметров Ds, [tHb] и StO2 для каждой группы источников.
В одном из вариантов осуществления изобретения для λi и rj вектор формы пульсовых колебаний  определяют тремя переменными {N, AvCork, DIm}i,j , где
определяют тремя переменными {N, AvCork, DIm}i,j , где
N - количество компонент фурье-спектра автокорреляционной функции пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения, амплитуда которых не менее 0,2 отн.ед.;
AvCork, k = 1…N - амплитуды этих компонент фурье-спектра автокорреляционной функции;
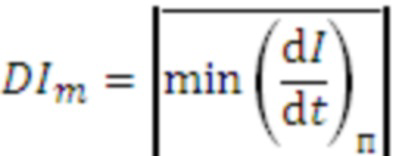 - среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратно-рассеянного излучения по времени с шагом 0,2±0,003 с.
- среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратно-рассеянного излучения по времени с шагом 0,2±0,003 с.
При этом форму пульсовой волны определяют как соответствующую функциональной тканевой единице в размерах исследуемого объема биологической ткани при получении следующих значений вектора формы:
 = : N = 1; 0,6 ≤ AvCor1 ≤ 1;
= : N = 1; 0,6 ≤ AvCor1 ≤ 1; 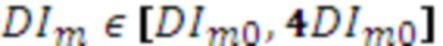 , -
, -
как соответствующую крупной артерии в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
 = : N = 1; 0,8 ≤ AvCor1 ≤ 1; DIm > 4DIm0, -
= : N = 1; 0,8 ≤ AvCor1 ≤ 1; DIm > 4DIm0, -
как соответствующую крупной вене в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
 = : N = 1 или N = 2; AvCork < 0,6, k = 1…N; DIm < DIm0, -
= : N = 1 или N = 2; AvCork < 0,6, k = 1…N; DIm < DIm0, -
где DIm0 - пороговое значение DIm, определяемое для функциональной тканевой единицы в размерах исследуемого объема биологической ткани.
В одном из вариантов осуществления изобретения локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п) для каждой подгруппы источников и соответствующего расстояния от приемника, как минимум, по двум длинам волн из указанного диапазона определяют по регистрируемым сигналам интенсивности обратно-рассеянного излучения I(λi) с учетом модифицированного закона Бугера-Ламберта-Бера [23], выражения для суммарного коэффициента поглощения на каждой длине волны с учетом соответствующего количества анализируемых хромофоров, расчетной формулы для дифференциального фактора длины на основе измеряемых в статическом режиме для соответствующей группы излучателей оптических параметров μa(λi) и μs'(λi) [21] и формул для определения концентраций оксигенированного и дезоксигенированного гемоглобина по μa(λi).
Пороговые значения параметров Ds0, [tHb]0, (StO2)0, (Ап/д)0, DIm0 и (Δ[tHb]п)0 для функциональной тканевой единицы в размерах исследуемого объема биологической ткани могут быть определены, исходя из соответствия типу исследуемой биологической ткани по клеточному составу, структуре и характеру кровоснабжения без подлежащих распознаванию нейроваскулярных включений, с использованием спектроскопических измерений с временным разрешением путем измерений в статическом режиме интраоперационно перед основными хирургическими манипуляциями с исследуемой биологической тканью, подлежащей иссечению, и/или с привлечением априорной/предоперационной диагностической информации об исследуемой биологической ткани.
Таким образом, заявляемый способ позволяет устранить следующие недостатки, присущие наиболее близкому решению, известному из уровня техники:
- неиспользование или неполное использование информативной пульсовой и дыхательной составляющих гемодинамических процессов, протекающих в исследуемом объеме биологической ткани, для обнаружения и распознавания нейроваскулярных структур;
- неконтролируемое позиционирование и/или неконтролируемая сила прижатия оптоволоконного датчика к поверхности исследуемого объема биологической ткани, что приводит к наличию двигательных артефактов в измерениях, вызванных тремором руки, и/или неконтролируемому пережатию биологической ткани в момент контактного зондирования исследуемого объема и, как следствие, к искажению полученных данных за счет изменения структурных и оптических параметров и снижению эффективности обнаружения и распознавания нейроваскулярных структур;
- отсутствие оценок, качественных и/или количественных, типа артериального или венозного сосуда при его выявлении в исследуемом объеме биологической ткани;
- ограниченность поля зрения используемого в прототипе оптоволоконного датчика, неинвариантность к расположению нейроваскулярных структур при их наличии в исследуемом объеме биологический ткани и, как следствие, неравномерная чувствительность к нейроваскулярным структурам при незначительных смещениях оптоволоконного датчика;
- отсутствие контроля за возможным спазмированием артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии и степенью ишемизации кровоснабжаемых ими тканей, особенно нервных, гипоксия и повреждение которых в процессе операции приводят к необратимым для пациента последствиям, что не позволяет говорить об эффективности и качестве выполненной операции,
- ограниченные функциональные возможности способа, низкая эффективность обнаружения и распознавания нейроваскулярных структур.
В отличие от наиболее близкого решения заявляемый способ включает:
- применение методов кратно-масштабного анализа регистрируемой интенсивности обратно-рассеянного излучения и формирование комплексной характеристики пульсовых и дыхательных колебаний, определяющей наличие или отсутствие выраженных пульсовых колебаний, наличие или отсутствие дыхательных колебаний в исследуемом объеме биологической ткани, форму пульсовой волны, соответствующую крупной артерии, малой артерии, вынужденным пульсовым колебаниям венозного объема или функциональной тканевой единице;
- расширение набора критериев обнаружения и распознавания нейроваскулярных структур: крупных и малых артериальных и венозных сосудов и нервов, - с учетом предоперационной и интраоперационной диагностической информации и с учетом априорной физиологической информации;
- осуществление возможности реализации способа в условиях автоматизированного контроля позиционирования и/или силы прижатия используемого оптоволоконного датчика к поверхности исследуемого объема биологической ткани, с помощью устройства позиционирования, оснащенного датчиками силы и перемещения, в двух режимах: статическом и динамическом;
- формирование и применение расширенного набора критериев для обнаружения и распознавания нейроваскулярных структур на основании спектроскопических измерений в статическом режиме автоматизированного контроля позиционирования и/или силы прижатия;
- возможность проведения двухэтапного динамического режима для подтверждения или обнаружения: на первом этапе - наличия венозного сосуда в исследуемом объеме биологической ткани; на втором этапе - дополнительного подтверждения наличия уже обнаруженного в статическом режиме артериального сосуда или обнаружения и распознавания артериального сосуда более глубинного залегания, не обнаруженного в статическом режиме, оценки калибра артериального сосуда по величине давления в сосуде;
- возможность дополнительного подтверждения, что исследуемая область биологической ткани является участком с микроциркуляторным руслом без нейроваскулярных включений: сосудов, типа артерий и вен, и нервов;
- обеспечение равномерности зондирования исследуемого объема биологической ткани и инвариантности способа к расположению нейроваскулярных структур, при их наличии в исследуемом объеме, за счет применения не менее двух групп излучателей и применения методов кратно-масштабного анализа к регистрируемой для каждого источника интенсивности обратно-рассеянного излучения для выделения и анализа дыхательных и пульсовых колебаний;
- обеспечение контроля наличия возможного спазмирования артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии и степени ишемизации кровоснабжаемых ими биологических тканей по отклонениям контролируемых физиологических параметров от их начальных значений, регистрируемых интраоперационно, в сторону выраженной гипоксии тканей.
Перечисленные выше отличительные признаки заявляемого способа приводят к достижению следующих преимуществ по сравнению с наиболее близким техническим решением:
- к повышению эффективности распознавания нейроваскулярных структур за счет анализа комплекса значимых параметров в статическом и, при необходимости, в динамическом режимах, и получения более широкого спектра критериев, обеспечивающих определение в т.ч. типа структуры; автоматизированного контроля позиционирования и/или силы прижатия используемого оптоволоконного датчика к поверхности исследуемого объема биологической ткани, что обеспечивает отсутствие неинформативных двигательных артефактов и искажений оптических параметров, обеспечивает стабильность и воспроизводимость параметров, по которым на основании соответствующих критериев принимается решение; повышения или обеспечения равномерности зондирования исследуемого объема биологической ткани и инвариантности способа к расположению нейроваскулярных структур;
- к повышению универсальности способа за счет: повышения глубины обнаружения и распознавания артериальных сосудов при контролируемом автоматизированном вдавливании оптоволоконного датчика в исследуемую ткань без увеличения его габаритов и размеров исследуемой области; обеспечения инвариантности способа к расположению нейроваскулярных структур в исследуемом объеме биологической ткани путем применения не менее двух групп излучателей оптоволоконного датчика и анализа интенсивности обратнорассеянного излучения для каждого источника;
- к расширению функциональных возможностей способа на единой методологической основе за счет контроля возможного спазмирования артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии и степени ишемизации кровоснабжаемых ими биологических тканей с помощью предложенного вектора признаков и соответствующих критериев оценки спазмирования и ишемизации;
- повышению качества оказываемой медицинской помощи ввиду снижения или предотвращения нередких в нейрохирургической практике случаев повреждения нейроваскулярных структур и внезапного неконтролируемого спазмирования крупных артерий при случайном резком механическом воздействии на них; на эффективное предупреждение такого рода ситуаций направлен данный способ.
Предлагаемый способ не имеет ограничений, если пространственное разрешение и минимальный зондируемый объем согласованы с характерными размерами нейроваскулярных структур, подлежащих обнаружению и распознаванию, и изменения оптических параметров, значимые для обнаружения и распознавания нейроваскулярных структур, минимум в 2 раза превосходят соответствующую шумовую характеристику.
Краткое описание чертежей
Изобретение поясняется иллюстративным материалом, где на фиг. 1 представлена структурная схема устройства для реализации предложенного способа; на фиг. 2 представлен малогабаритный секторный оптоволоконный датчик: а) в сомкнутом состоянии с минимальными габаритами; б) в рабочем состоянии с разомкнутыми браншами; в) вид торцевой поверхности с приемником и излучателями; на фиг. 3 представлены варианты конструкций рабочего торца оптоволоконного датчика, где равномерность зондирования обеспечивается увеличением количества точечных источников (а) и/или приемников (б), наличием линейки приемников (в) или увеличением количества раздвижных браншей (г); на фиг. 4 представлены примеры схем расположения в оптоволоконном датчике групп/подгрупп излучателей относительно приемника; на фиг. 5 представлен один из вариантов секторного датчика (ООО «НТЦ Волоконно-оптических устройств», г. Москва, РФ), который может быть использован при осуществлении заявляемого способа; на фиг. 6 представлена верификация лучевой артерии в процессе совместных ультразвуковых (УЗИ) и спектроскопических (СФИ) исследований магистральных сосудов запястья; на фиг. 7 представлены (а) испытательная машина Instron 8801 и (б) объект in vivo исследований ткани руки человека - при вдавливании оптоволоконного датчика с автоматизированным контролем усилия прижатия и перемещений с помощью силомоментного датчика испытательной машины; на фиг. 8 представлены примеры выделения пульсовых колебаний регистрируемого среднего уровня интенсивности (DC) обратнорассеянного в исследуемом объеме биологической ткани излучения; на фиг. 9 представлены результаты анализа формы пульсовых колебаний и определение вектора формы; на фиг. 10 представлена зависимость оптических свойств исследуемого объема биологической ткани от силы прижатия оптоволоконного датчика, подтверждение наличия вены и обнаружение крупной артерии на глубине, большей глубины зондирования в статическом режиме; на фиг. 11 представлены результаты экспериментальной проверки чувствительности секторного датчика к неоднородным включениям.
В таблице 1 представлены примеры распознавания нейроваскулярных структур предлагаемым способом и по параметрам прототипа на основе критериальных значений параметров, соответствующих функциональной тканевой единице.
Осуществление изобретения
Для более однозначного понимания сущности заявленного изобретения ниже представлены основные термины и определения, используемые в рамках настоящего описания.
Функциональная тканевая единица (ФТЕ) в размере исследуемого объема биологической ткани представляет собой комплекс специализированных клеток ткани, клеток и неклеточного компонента соединительной ткани, кровеносных и лимфатических микрососудов, окончаний нервных волокон и мельчайших артериальных и венозных сосудов диаметрами менее 0,5 мм. Основой ФТЕ определенного органа или ткани является микроциркуляторно-тканевая система, морфофункциональные особенности которой подробно рассматривают авторы работы [19]. Функциональные тканевые единицы разных органов имеют различия на структурном и функциональном уровнях: гистологические различия на уровне клеток разных тканей, различия в соединительнотканной структуре, в строении микрососудистой сети и на уровне кровеносных сосудов крупнее (диаметром более 250 мкм) сосудов микроциркуляторного уровня (диаметром 3 мкм - 250мкм). В следствие указанных различий, ФТЕ имеют разные физические свойства: оптические, акустические, электрические. Оптические параметры определяемой таким образом ФТЕ, коэффициенты поглощения и транспортные коэффициенты рассеяния на разных длинах волн, характеризуются высокой биологической вариабельностью. Поэтому разработка способов обнаружения и распознавания в объеме ФТЕ таких структур, как нервы и цельная кровь в сосудах, имеющих значительно меньшую биологическую вариабельность морфофункциональных и физических свойств, требует предварительной оценки и учета измеряемых параметров ФТЕ в применяемых критериях.
С учетом функциональных возможностей применяемого метода спектроскопии с временным разрешением для ФТЕ в размерах относительно малого исследуемого объема биологической ткани с указанной максимальной глубиной зондирования не менее 5 мм соотношение между калибром сосуда и его размером принято следующим:
- крупный сосуд, артерия или вена определяется как сосуд с диаметром 2,0 мм и выше;
- малый сосуд, артерия или вена, имеет диаметр от 0,5 мм до 2,0 мм;
- распознаваемые нервы - диаметром 1,5 - 5 мм и выше.
В рамках настоящего изобретения исследования проведены для руки человека от кисти до середины предплечья. Функциональной тканевой единицей являлся объем ткани на внешней стороне середины предплечья, полученные значения параметров Ds0, [tHb]0, (StO2)0, (Ап/д)0, DIm0 и (Δ[tHb]п)0 рассматривались как пороговые.
Возможность осуществления заявляемого способа продемонстрирована с помощью устройства, обобщенная структурная схема которого представлена на фиг. 1. Схема включает в себя следующие конструктивные единицы (устройства, блоки и элементы):
1 - спектрометр с временным разрешением на основе частотного подхода (FD, frequency domain) или временнóго подхода (TD, time domain);
2 - оптоволоконный датчик для отражательной диффузионной спектроскопии, с помощью которого осуществляют подповерхностное картирование исследуемого объема биологической ткани необходимым количеством длин волн указанного красного и ближнего инфракрасного (КБИК) диапазона на необходимую глубину с необходимым пространственным разрешением, имеющий необходимый вариант технического исполнения;
3 - устройство позиционирования оптоволоконного датчика относительно исследуемой биологической ткани, оснащенное датчиком силы (3.1) и датчиком перемещения (3.2) и имеющее узел крепления оптоволоконного датчика (3.3).
4 - блок управления структурными элементами 1 и 3 устройства для реализации способа на основе персонального компьютера со специализированным программным обеспечением (4.1) и блоком отображения и хранения информации (4.2);
5 - исследуемая биологическая ткань;
6 - видеорегистратор для освещения и регистрации изображения операционного пространства, поверхности исследуемого объема биологической ткани.
Конструкция оптоволоконного датчика (2) определяется медицинской задачей, типом доступа к исследуемому объему биологической ткани (5), размером операционного поля доступного для проведения зондирования, свойствами исследуемого объема биологической ткани (размерами, формой поверхности, биомеханическими и оптическими свойствами), необходимым количеством зондирующих длин волн КБИК диапазона, необходимой глубиной зондирования, необходимой чувствительностью и необходимым пространственным разрешением. Примеры конструкций оптоволоконных датчиков для отражательной диффузионной спектроскопии, которые могут быть использованы при реализации заявляемого способа, представлены в публикации [20].
Для интраоперационного обнаружения и распознавания нейроваскулярных структур в объеме биологической ткани оптоволоконным датчиком (2) для отражательной диффузионной спектроскопии осуществляют подповерхностное зондирование исследуемого объема биологической ткани (5), например, опухолевой.
Подповерхностное зондирование исследуемого объема биологической ткани (5) осуществляют на основе спектроскопического метода с временным разрешением на максимальную глубину не менее 5 мм, как минимум, первой длиной волны (λ1) и второй длиной волны (λ2), λ1 < λ2, из КБИК диапазона от 650 нм до 950 нм, таких, что обеспечиваются стандартные требования к выбору длин волн для отражательной диффузионной спектроскопии:
- глубина зондирования биоткани z при одинаковых расстояниях r между источниками и приемником на разных длинах волн не должна существенно различаться:
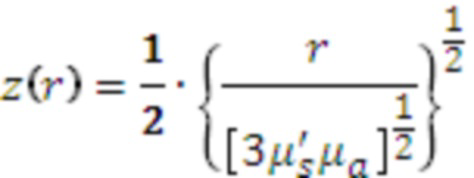 [21];
[21];
- физиологически значимые минимальные изменения [HbO2] и [HHb] должны быть различимы при измерениях, и погрешности определения [HbO2] и [HHb] должны быть минимальны при выбранных длинах волн с учетом шумовых характеристик используемого средства измерения. Рекомендуемые комбинации длин волн, применяемые в спектроскопии биотканей для диапазона 650-950 нм, приведены в [22].
Указанным критериям при выборе двух длин волн, например, соответствуют 690±10 нм и 830±10 нм.
Подробно спектроскопический метод с временным разрешением и варианты его технической реализации в виде частотного (FD) или временного (TD) подходов рассмотрены, соответственно, в [23-27] (FD) и [23,24,28,29] (TD).
Перед применением оптоволоконного датчика, в зависимости от технической реализации способа, может потребоваться калибровка датчика в соответствии с инструкцией по эксплуатации спектрометра в условиях необходимого уровня засветки операционного поля, допустимого для реализации предлагаемого способа, и на блоках с известными оптическими свойствами, близкими к оптическим свойствам исследуемого объема биологической ткани, как, например, для тканей головного мозга, μa ~ 0,1 (см-1) и μs' ~ 10 (см-1). Допустимый уровень засветки зависит от конструкции оптоволоконного датчика, условий калибровки, типа приемника диффузно рассеянного в обратном направлении излучения, аппаратно-программной реализации способа.
В процессе зондирования исследуемого объема биологической ткани (5) регистрируют параметры обратнорассеянного излучения, соответствующие спектроскопическому методу с временным разрешением, с частотой дискретизации не менее 20 Гц. Для частотного подхода такими параметрами являются средний уровень интенсивности, амплитуда модуляции и сдвиг фаз регистрируемого модулированного сигнала по отношению к опорному сигналу [23-27]. Определяют значения оптических параметров, как минимум, для двух длин волн КБИК диапазона: коэффициентов поглощения для первой длины волны μa(λ1) и для второй длины волны μa(λ2), λ1 < λ2, с поправкой на содержание воды в единице объема биологической ткани (5), и коэффициентов транспортного рассеяния μs'(λ1) для первой длины волны и μs'(λ2) для второй длины волны, допуская, что основными поглотителями излучения КБИК диапазона в исследуемом объеме биологической ткани являются вода, оксигенированный и дезоксигенированный гемоглобин. Определение оптических параметров осуществляют спектрометром (1) с временным разрешением, например, с фазово-модуляционным частотным режимом (frequency domain, FD), как в ”OxiplexTS“ (ISS, Inc., США), со специализированным программным обеспечением, как, например, “OxiTS”, реализующим расчет оптических параметров, коэффициентов поглощения μa(λ1) и μa(λ2) и транспортных коэффициентов рассеяния μs'(λ1) и μs'(λ2), по параметрам обратнорассеянного излучения и известным из литературы уравнениям [23,25-27]. Дополнительные примеры спектрометров, реализующих подход с временным разрешением, приведены в [23,24,28,30]. Перечень спектрометров, обеспечивающих измерение абсолютных значений оптических параметров μa и μs', как минимум, на двух длинах волн, представлен в [24].
Далее оценивают производный параметр (Ds) в виде отношения 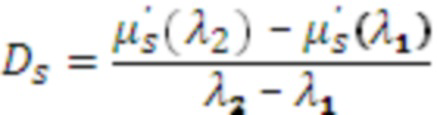 и по известным соотношениям, представленным в [17,23], рассчитывают физиологические параметры, такие как концентрации оксигенированного гемоглобина ([HbO2]), дезоксигенированного гемоглобина ([HHb]) и общего гемоглобина ([tHb] = [HbO2] + [HHb]) в единице исследуемого объема биологической ткани и тканевая сатурация (StO2 = 100*[HbO2] / [tHb]).
и по известным соотношениям, представленным в [17,23], рассчитывают физиологические параметры, такие как концентрации оксигенированного гемоглобина ([HbO2]), дезоксигенированного гемоглобина ([HHb]) и общего гемоглобина ([tHb] = [HbO2] + [HHb]) в единице исследуемого объема биологической ткани и тканевая сатурация (StO2 = 100*[HbO2] / [tHb]).
Регистрацию и расчет параметров выполняют в автоматизированном режиме посредством программного обеспечения (4.1), установленного на персональном компьютере (4), как, например, “OxiTS” для спектрометра ”OxiplexTS“.
В общем случае применения не менее двух длин зондирующих волн λi, i=1,2,…,n, физиологические параметры оценивают по измеренным коэффициентам поглощения:
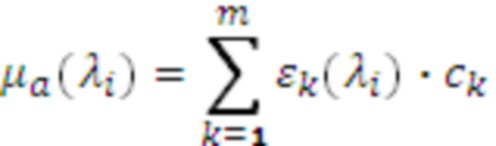 , (1)
, (1)
где 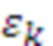 - молярные коэффициенты экстинкции, мкМ-1⋅ см-1;
- молярные коэффициенты экстинкции, мкМ-1⋅ см-1; 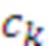 - соответствующие концентрации, мкМ=мкмоль/л, основных учитываемых биологических хромофоров: воды, оксигенированного (HbO2) и дезоксигенированного (HHb) гемоглобина, липидов и др. В случае двух зондирующих длин волн λ1 и λ2, λ1 < λ2, предполагают процент водонасыщения исследуемого объема биологической ткани (70-80%), пренебрегают вкладом липидов, если λ2 < 900 нм, и на основании соотношения (1) по измеренным значениям μa с поправкой на содержание воды оценивают [HbO2] и [HHb], [tHb]=[HbO2]+[HHb] и StO2=([HbO2]/[tHb])⋅100%. Применение трех и более зондирующих длин волн позволяет повысить точность оценки физиологических параметров [tHb] и StO2, но существенно повышает сложность и стоимость технической реализации. Ошибка при учете концентрации воды в диапазоне водонасыщения ткани от 70 до 80% не превышает десятых долей процента, в широком диапазоне водонасыщения от 50 до 90% максимальная ошибка - менее 2%.
- соответствующие концентрации, мкМ=мкмоль/л, основных учитываемых биологических хромофоров: воды, оксигенированного (HbO2) и дезоксигенированного (HHb) гемоглобина, липидов и др. В случае двух зондирующих длин волн λ1 и λ2, λ1 < λ2, предполагают процент водонасыщения исследуемого объема биологической ткани (70-80%), пренебрегают вкладом липидов, если λ2 < 900 нм, и на основании соотношения (1) по измеренным значениям μa с поправкой на содержание воды оценивают [HbO2] и [HHb], [tHb]=[HbO2]+[HHb] и StO2=([HbO2]/[tHb])⋅100%. Применение трех и более зондирующих длин волн позволяет повысить точность оценки физиологических параметров [tHb] и StO2, но существенно повышает сложность и стоимость технической реализации. Ошибка при учете концентрации воды в диапазоне водонасыщения ткани от 70 до 80% не превышает десятых долей процента, в широком диапазоне водонасыщения от 50 до 90% максимальная ошибка - менее 2%.
Производный параметр Ds, см-1/мкм, 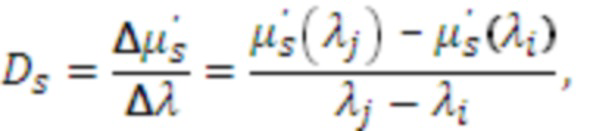 играет ключевую роль в обнаружении крупных сосудов и нервов. При наличии измеренных значений μs' на трех и более длинах волн Ds оценивают как тангенс угла линейного наклона аппроксимирующей зависимости μs'(λ) в силу специфики уменьшения μs' биологических тканей с увеличением λ [23,31].
играет ключевую роль в обнаружении крупных сосудов и нервов. При наличии измеренных значений μs' на трех и более длинах волн Ds оценивают как тангенс угла линейного наклона аппроксимирующей зависимости μs'(λ) в силу специфики уменьшения μs' биологических тканей с увеличением λ [23,31].
Для крупного кровеносного сосуда в исследуемом объеме биологической ткани Δμs' > 0 или Ds > 0, что определяется существенным отличием значений фактора анизотропии большинства мягких биологических тканей (мышечной, тканей мозга и др.), находящихся в диапазоне от 0,7 до 0,95 от значений фактора анизотропии для цельной крови 0,997 - 0,999, и изменением характера распространения зондирующего излучения в исследуемом объеме биологической ткани [23].
Используемые для обнаружения и распознавания нейроваскулярных структур по соответствующим критериям значения параметров Ds, StO2 и [tHb] определяют усреднением за период регистрации не менее 15 с.
Методы кратно-масштабного анализа применяют к регистрируемому сигналу интенсивности обратно-рассеянного излучения, например, к среднему уровню или амплитуде модуляции в случае применения спектроскопии с частотным режимом, ко всем реализуемым с помощью оптоволоконного датчика длинам волн и расстояниям от излучателей до приемника. Выполняют вейвлет-декомпозицию сигнала и последующий Фурье-анализ выделенных частотных составляющих [19 c. 167-229] с выделением максимальных пиков, соответствующих пульсовому (0,8 - 3,0 Гц) и дыхательному (0,2 - 0,4 Гц) диапазонам.
Таким образом формируют характеристику наличия или отсутствия выраженных пульсовых колебаний, наличия или отсутствия дыхательных колебаний в исследуемом объеме биологической ткани и определяют амплитуды пульсовых (Aп) и дыхательных (Aд) колебаний, и их отношение Ап/д = Ап / Ад. Определяют вектор формы ( ), представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду
), представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду 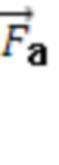 , крупному венозному сосуду
, крупному венозному сосуду 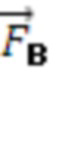 , или функциональной тканевой единице в размерах исследуемого объема биологической ткани . В одном из вариантов осуществления изобретения вектор формы пульсовых колебаний
, или функциональной тканевой единице в размерах исследуемого объема биологической ткани . В одном из вариантов осуществления изобретения вектор формы пульсовых колебаний 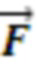 определяют тремя переменными {N, AvCork, DIm}i,j , где
определяют тремя переменными {N, AvCork, DIm}i,j , где
N - количество компонент фурье-спектра автокорреляционной функции пульсовой составляющей регистрируемой интенсивности обратно-рассеянного излучения, амплитуда которых не менее 0,2 отн.ед.;
AvCork, k = 1…N - амплитуды этих компонент фурье-спектра автокорреляционной функции;
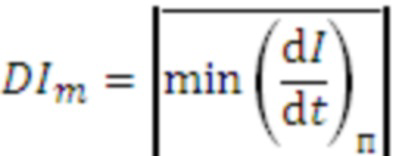 - среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения по времени с шагом 0,2±0,003 с.
- среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения по времени с шагом 0,2±0,003 с.
При этом форму пульсовой волны определяют как соответствующую функциональной тканевой единице исследуемой биологической ткани в размерах исследуемого объема при получении следующих значений вектора формы:
 = : N = 1; 0,6 ≤ AvCor1 ≤ 1;
= : N = 1; 0,6 ≤ AvCor1 ≤ 1; 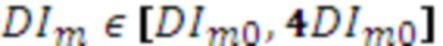 ;
;
- как соответствующую крупной артерии в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
 = : N = 1; 0,6 ≤ AvCor1 ≤ 1; DIm > 4DIm0;
= : N = 1; 0,6 ≤ AvCor1 ≤ 1; DIm > 4DIm0;
- как соответствующую крупной вене в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
 = : N = 1 или N = 2; AvCork < 0,6, k = 1…N; DIm < DIm0,
= : N = 1 или N = 2; AvCork < 0,6, k = 1…N; DIm < DIm0,
где DIm0 - пороговое значение DIm, определяемое для функциональной тканевой единицы в размерах исследуемого объема биологической ткани.
Формы пульсовой волны, соответствующие крупной артерии, малой артерии и вынужденным пульсовым колебаниям венозного объема крови при выраженной дикротической фазе и удвоении частоты колебаний или слабо выраженным вынужденным пульсовым колебаниям микроциркуляторного объема крови, могут быть определены качественно в соответствии с публикациями [32, 33].
В одном из вариантов осуществления изобретения определяют локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п) для каждой подгруппы источников и соответствующего расстояния (r) от приемника, как минимум, по двум длинам волн из указанного диапазона. При этом Δ[tHb]п определяют по регистрируемым сигналам интенсивности обратно-рассеянного излучения I(λi) с использованием известных соотношений: модифицированного закона Бугера-Ламберта-Бера [23], выражения для суммарного коэффициента поглощения на каждой длине волны с учетом соответствующего количества анализируемых хромофоров, расчетной формулы для дифференциального фактора длины (DPF) на основе измеряемых в статическом режиме для соответствующей группы излучателей оптических параметров μa(λi) и μs’(λi) [21] и формул для определения концентраций оксигенированного и дезоксигенированного гемоглобина по μa(λi):
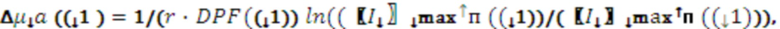
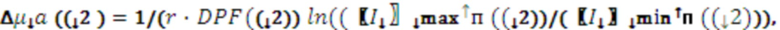
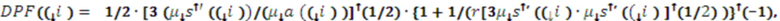
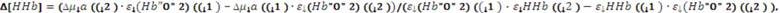
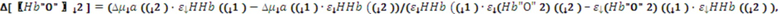
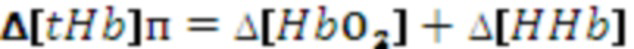 ,
,
где 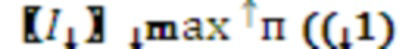 и
и 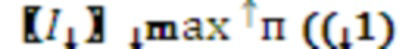 соответственно максимальное и минимальное значение интенсивности излучения, соответствующее пульсовому изменению.
соответственно максимальное и минимальное значение интенсивности излучения, соответствующее пульсовому изменению.
При этом перечисленные параметры измеряют в статическом режиме, при котором давление оптоволоконного датчика P на поверхность исследуемого объема биологической ткани составляет P ≤ 0,2 мм рт. ст.
Вывод о наличии определенных нейроваскулярных структур делают по получению следующих совокупностей измеренных параметров:
- при {Ds > 0; [tHb] > [tHb]0; StO2 > (StO2)0; Ап/д > (Ап/д)0;  =; Δ[tHb]п > (Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
=; Δ[tHb]п > (Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
- при {Ds > 0; [tHb] > [tHb]0; StO2 ≤ (StO2)0 или StO2 > (StO2)0; Ап/д < (Ап/д)0;  =; Δ[tHb]п ≤ (Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
=; Δ[tHb]п ≤ (Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
- при {Ds0 < Ds < 0; [tHb] ≤ [tHb]0; StO2 ≤ (StO2)0; Ап/д ≤ (Ап/д)0;  =; Δ[tHb]п < (Δ[tHb]п)0} (3) - о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
=; Δ[tHb]п < (Δ[tHb]п)0} (3) - о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
- при {Ds ≤ Ds0; [tHb] ≥ [tHb]0; StO2 ≥ (StO2)0; Ап/д ≥ (Ап/д)0;  =; Δ[tHb]п ≥ (Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой артерии;
=; Δ[tHb]п ≥ (Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой артерии;
- при { Ds0 < Ds < 0; [tHb] > [tHb]0; StO2 ≥ (StO2)0; Ап/д > (Ап/д)0;  =; Δ[tHb]п > (Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs’(λ) > 0;
=; Δ[tHb]п > (Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs’(λ) > 0;
- при { Ds0 ≤ Ds < 0; [tHb] > [tHb]0; StO2 ≤ (StO2)0; Ап/д ≤ (Ап/д)0;  =; Δ[tHb]п ≤ (Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой вены,
=; Δ[tHb]п ≤ (Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани, по меньшей мере, одной малой вены,
где [tHb]0, Ds0, (StO2)0, (Ап/д)0, (Δ[tHb]п)0 - пороговые значения упомянутых параметров, измеренные для функциональной тканевой единицы в размерах исследуемого объема биологической ткани,
причем значения параметров Ds, [tHb] и StO2 определяют для каждой группы излучателей и соответствующего приемника.
Для распознавания нейроваскулярной структуры в исследуемом объеме биологической ткани необходимо и достаточно выполнения критериев для Ds, [tHb] и StO2 хотя бы для одной группы излучателей и соответствующего приемника и выполнения критериев для Ап/д,  и Δ[tHb]п хотя бы для одной подгруппы излучателей этой группы.
и Δ[tHb]п хотя бы для одной подгруппы излучателей этой группы.
Величина Ds0 зависит от типа, состава и строения исследуемой биологической ткани, например, типа, состава и строения опухолевой ткани. Пороговое значение [tHb]0 для исследуемой ткани без нервов и крупных сосудов, оценивают по известным зависимостям [17, 23 стр. 468] через кровенаполнение или объемный кровоток, соответствующие физиологической норме или с учетом увеличенной перфузии биологической ткани, например, опухолевой, что выявляется на этапе предоперационной диагностики, например, с помощью рентгеновской компьютерной томографии. Значения параметров [tHb]0 и Ds0 < 0, соответствующие типу исследуемой биологической ткани по клеточному составу и структуре и характеру кровоснабжения на микроциркуляторном уровне, но без нейроваскулярных включений, можно оценивать по данным спектроскопических измерений с временным разрешением непосредственно в начале операции на исследуемой биологической ткани, например, подлежащей иссечению, и/или с привлечением априорной/предоперационной диагностической информации об исследуемой биологической ткани.
Наличие нерва в исследуемом объеме биологической ткани будет характеризоваться меньшими значениями [tHb] и StO2 по сравнению с аналогичными значениями типового объема ткани без нервов и крупных сосудов, что определяется характерным строением и молекулярным составом нерва, с высоким содержанием липидов (порядка 70%). При наличии нерва, Ds принимает значения Ds0 < Ds < 0 по сравнению с величиной Ds0 для исследуемой ткани, например, аденомы гипофиза, опухолевой ткани, структура жировой ткани характеризуется значениями Ds0 < 0, близкими к нулю.
Предлагаемые критерии обнаружения и распознавания нейроваскулярных структур в исследуемом объеме биологической ткани инвариантны к выбору подхода (временного или частотного) спектроскопического метода с временным разрешением и доступны для интерпретации и анализа, т.к. отражают физиологические процессы в исследуемом объеме биологической ткани.
Способ осуществляют в условиях автоматизированного контроля позиционирования и/или силы прижатия используемого оптоволоконного датчика (2) к поверхности исследуемого объема - биологической ткани (5), с помощью устройства позиционирования (3), оснащенного датчиками силы (3.1) и перемещения (3.2) и узлом крепления датчика (3.3). Это происходит следующим образом. Оптоволоконный датчик вставляют и жестко закрепляют в узле крепления (3.3) устройства позиционирования (3), в котором встроены датчики силы (3.1) и перемещения (3.2). Регистрация и отображение текущих значений силы и перемещения происходит с помощью ПК (4) и специализированного ПО (4.1) [34]. Примерами устройства позиционирования являются используемые в нейрохирургии устройства [35] или универсальные коллаборативные роботы типа настольных миниманипуляторов [36]. Датчики силы и перемещений (силомоментные датчики), используемые в подобных устройствах позиционирования [37] применимы для реализации предлагаемого способа.
При этом определяют и контролируют зависимости силы прижатия (F) от перемещения оптоволоконного датчика (x) и силы прижатия от времени (t) с частотой дискретизации не менее 20 Гц в двух режимах:
1) статическом, когда сила прижатия соответствует нулевому или минимальному давлению (P ≤ 0,2 мм рт.ст.) датчика на поверхность исследуемого объема биологической ткани с учетом площади поверхности контакта (S), или
2) динамическом, когда реализуют метод вдавливания оптоволоконного датчика в исследуемый объем биологической ткани с заданной постоянной скоростью (VL ≤ 10 мм/мин) при изменении силы от 0 до Fmax, соответствующей максимально допустимому для исследуемой биологической ткани уровню давления (Pmax = Fmax/S, мм рт.ст.), или при двухэтапном изменении давления от 0 до 20 мм рт.ст. и от 20 мм рт.ст. до Pmax.
В статическом режиме на основании спектроскопических измерений формируют и применяют расширенный набор критериев обнаружения и распознавания нейроваскулярных структур на основе параметров Ds, [tHb], StO2, Ап/д, DIm и Δ[tHb]п.
Затем выполняют двухэтапные измерения в динамическом режиме. На первом этапе осуществляют начальное нагружение, увеличивая силу прижатия оптоволоконного датчика к поверхности исследуемого объема биологической ткани от 0 до 20 мм рт.ст. с заданной постоянной скоростью VL. При этом при выполнении критериев обнаружения венозного сосуда в статическом режиме и при наличии на первом этапе нагружения относительно резкого, более 25 %, уменьшения параметров μa(λi) и [tHb], отражающего снижение кровенаполнения исследуемого объема биологической ткани, и при прекращении дыхательных колебаний в регистрируемых сигналах дополнительно подтверждают наличие крупного венозного сосуда в исследуемом объеме биологической ткани.
На втором этапе динамического режима проводят дальнейшее нагружение с заданной постоянной скоростью VL до максимально допустимого для исследуемой биологической ткани давления Pmax, где Pmax принимает значения от 70 мм рт.ст. для тканей головного мозга до 200 мм рт.ст. для тканей нижних конечностей, что определяется локализацией артериальных сосудов исследуемого объема биологической ткани по отношению к сердцу и величиной давления в них с учетом гидростатического давления [33].
Проводят регистрацию зависимостей силы прижатия (F) от перемещения оптоволоконного датчика (x) и силы прижатия (F) от времени (t) с частотой дискретизации не менее 20 Гц, на основании которых выявляют наличие артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме, а также оценивают величину сосуда по значению давления в сосуде. Вывод о наличии артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме, делают при выявлении пульсовых колебаний силы F(t) с максимумом в диапазоне частот сердечных сокращений от 0,8 до 3,0 Гц с использованием методов кратно-масштабного анализа дискретных сигналов в реальном времени, включая метод оконного преобразования Фурье и вейвлет-преобразование. Значение давления (P) артериального сосуда определяют по формуле P = F/S , где F - значение силы прижатия оптоволоконного датчика в момент времени tк, соответствующий концу пульсовых колебаний или Fmax, если пульсовые колебания не прекратились, S - площадь контакта оптоволоконного датчика с поверхностью исследуемого объема биологической ткани. При получении значения 70≤ P ≤90 мм рт.ст. делают вывод о наличии малой артерии на глубине, большей максимальной глубины зондирования в статическом режиме; при получении P > 90 мм рт.ст. делают вывод о наличии крупной артерии на глубине, большей максимальной глубины зондирования в статическом режиме.
При уменьшении на первом и втором этапах двухэтапного динамического режима параметров μa(λi) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, менее чем на 25% по сравнению со значениями, полученными в статическом режиме, для всех групп источников, дополнительно подтверждают отсутствие в исследуемой области биологической ткани крупных сосудов.
Одной из наиболее простых конструкций рабочего торца оптоволоконного датчика (Фиг. 2), удовлетворяющей условию повышения равномерности зондирования по сравнению с прототипом, является секторный вариант с одним приемником и восемью источниками (Фиг. 2, в), реализующий два линейных варианта минимальной конфигурации - по два расстояния от приемника до подгрупп излучателей и по две длины волны из КБИК диапазона в каждой подгруппе. В сомкнутом состоянии датчик имеет минимальные габариты для ввода в операционное поле (Фиг. 2, а), в рабочем состоянии с разведенными браншами (Фиг. 2, б) обеспечивает необходимую глубину зондирования исследуемого объема. Допустимый диапазон углов раскрытия браншей определяется конструкцией оптоволоконного датчика с требуемым доступом к операционному полю с учетом размеров операционного пространства. Угол раскрытия определяет величину зондируемого объема биологической ткани.
Отдельный линейный вариант размещения приемников и источника на торце оптоволоконного датчика, соответствующий прототипу [17, 18], не обеспечивает равномерности зондирования исследуемого объема и не реализуем для эндоскопической трансназальной нейрохирургии ввиду использования датчика с большими габаритными размерами, в два с половиной раза превышающими допустимые, например, для эндоназальной нейрохирургии, где максимальный поперечный диаметр не превышает 6 мм, и отсутствием возможности использования раздвижных браншей с источниками и приемниками оптического излучения.
Более сложные варианты конструкций рабочего торца оптоволоконного датчика представлены на Фиг. 3, где равномерность зондирования обеспечивается увеличением количества источников (Фиг. 3, а) и/или приемников (Фиг. 3, б), наличием линейки приемников (Фиг. 3, в) или увеличением количества раздвижных браншей (Фиг. 3, г). Распределенные, а не точечные, источники с равномерной засветкой исследуемого объема не обеспечивают пространственного разрешения и пространственной чувствительности к нейроваскулярным структурам в исследуемом объеме.
Инвариантность способа к расположению нейроваскулярных структур при их наличии в исследуемом объеме биологический ткани обеспечивают за счет подповерхностного картирования исследуемого объема, предполагающего распределение по поверхности рабочего торца оптоволоконного датчика (2) источников зондирующего излучения используемых длин волн КБИК диапазона и приемников обратнорассеянного в биологической ткани излучения для повышения или обеспечения равномерности зондирования исследуемого объема и пространственной чувствительности к нейроваскулярным структурам, максимально возможными для используемой технической реализации метода КБИК спектроскопии с временным разрешением с определенным количеством источников длин волн λi , i=1..N, N≥2 и требуемым количеством подгрупп излучателей с расстояниями rj, j=1..M, M≥2, от приемника, обеспечивающими максимальную глубину зондирования, не менее 5 мм, для каждой группы излучателей.
Примеры схем расположения в оптоволоконном датчике групп и подгрупп излучателей относительно приемника приведены на фиг. 4.
Пространственное разрешение и чувствительность способа определяются величиной минимально необходимого для реализации спектроскопического метода с временным разрешением [23 Гл.3, Гл.7] исследуемого объема биологической ткани, обеспечиваемого при расстояниях от излучателей до приемника не менее 5 мм, и количеством каналов измерения спектрометра.
Кроме того, заявляемый способ позволяет контролировать наличие возможного спазмирования крупных артерий и степень ишемизации кровоснабжаемых ими биологических тканей по отклонениям контролируемых физиологических параметров от их начальных значений, регистрируемых интраоперационно, в сторону выраженной гипоксии тканей, StO2 < (StO2)0, и сниженного кровотока [tHb] < [tHb]0. Для этого тем же оптоволоконным датчиком (2) для отражательной диффузионной спектроскопии с необходимой периодичностью мониторируют в статическом режиме участки органа или ткани, подлежащие контролю на предмет возможной ишемизации вследствие спазмирования артериальных сосудов исследуемого объема или кровоснабжающей их магистральной артерии, снижения локального кровотока и тканевой сатурации до критического уровня и ниже. Регистрируемые значения StO2 и [tHb] не должны быть меньше критических для биологических тканей значений: StO2≤ 55%, что определяется соотношением между поставкой кислорода кровью, адекватной потреблению кислорода в тканях [32]; критическое значение [tHb] определяется допустимым для исследуемой ткани уровнем кровотока, для оценки можно использовать известные соотношения [23, 32].
При реализации способа с количеством длин волн больше двух предпочтитетльно выполнение следующих условий: 1) как минимум две из применяемых длин волн должны соответствовать критерию λ1 < 806 нм и λ2 > 806 нм при выполнении указанных выше требований к глубине зондирования и точности оценки определяемых концентраций биологических хромофоров; 2) λ3 = (930±5) нм, что соответствует спектральному пику поглощения липидов, оценка концентрации которых будет дополнительным критерием для обнаружения и распознавания нервов; 3) одна из длин волн может быть выбрана из диапазона 900-950 нм, дополнительно к λ3~930 нм, что позволит количественно оценивать концентрацию воды в исследуемом объеме биологической ткани, повысить точность определения концентраций оксигенированного и дезоксигенированного гемоглобина, липидов, воды и других определяемых хромофоров (например, цитохром-оксидазы, коллагена, миоглобина и др.) в зависимости от практического применения способа и общего количества используемых длин волн, отличных от указанных; 4) остальные длины волн могут быть выбираны из диапазона 650 - 950 отличными от уже выбранных.
Возможность использования разработанного способа, а также достижение технического результата, продемонстрировано на представленных ниже данных.
Исследования нейроваскулярных структур проводились с помощью спектрофотометрического прибора «OxiplexTS» (ISS, Inc., USA) с двухволновым (692 нм и 834 нм) фазово-модуляционным режимом измерений (FD-режим) с использованием минимальной секторной конфигурации оптоволоконного датчика диаметром 12 мм и рабочими расстояниями от излучателей до приемника 6 мм и 9 мм (Фиг. 4), изготовленного ООО «НТЦ Волоконно-оптических устройств» (г. Москва, РФ).
С целью обнаружения и распознавания крупных венозных и артериальных сосудов исследовались in vivo области с различной анатомией сосудистого русла и нервов на руке и предплечье добровольцев (Фиг. 6, 7). Для кожных покровов и мягких мышечных тканей руки максимальная сила прижатия Fmax не превышает 10 Н, что при цилиндрической контактной поверхности диаметром 12 мм соответствует Pmax = 166 мм рт.ст.
Для верификации полученных результатов при распознавании крупных сосудов одновременно со спектроскопией применялся метод ультразвуковой допплерографии сосудов (Фиг. 6). Верификация наличия нерва в исследуемом объеме применялась ультразвуковая визуализация исследуемой конечности.
Автоматизированный контроль перемещений оптоволоконного датчика и силы прижатия осуществлялся с помощью силомоментной установки «Инстрон» (Фиг. 7) при одномоментной регистрации данных спектроскопии с помощью «OxiplexTS» на руке и предплечье испытуемого.
Применение кратно-масштабного анализа, вейвлет преобразования и спектрального фурье-анализа для выделения и анализа пульсовой и дыхательной компонент в сигналах интенсивности обратнорассеянного излучения, регистрируемых для всех источников представлено на примере пульсовой компоненты для разных сосудистых включений в исследуемом объеме биологической ткани (Фиг. 8).
Примеры анализа формы пульсовых колебаний и определения соответствующих векторов формы представлены на Фиг. 9.
Работоспособность, значимость и эффективность введенного комплекса показателей и критериев обнаружения и распознавания артерий, вен и нервов подтверждают результаты исследований, представленные в Таблице 1. Примеры распознавания приведены для предлагаемого способа в сравнении с прототипом. Пороговые значения соответствуют функциональной тканевой единице исследуемого объема ткани наружной поверхности середины предплечья. Расширение вектора признаков параметрами , 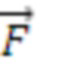 и Δ[tHb]п позволяет, в отличие от прототипа, распознавать малые артерии и вены и наличие малого объема крови крупной артерии в исследуемом объеме биологической ткани, а также состояние спазмирования артерий в исследуемом объеме или спазмирования питающей магистральной артерии.
и Δ[tHb]п позволяет, в отличие от прототипа, распознавать малые артерии и вены и наличие малого объема крови крупной артерии в исследуемом объеме биологической ткани, а также состояние спазмирования артерий в исследуемом объеме или спазмирования питающей магистральной артерии.
Эффективность контроля перемещений и силы прижатия в процессе динамического режима измерений демонстрируют результаты, представленные на Фиг. 10. Для исследуемой области с крупным венозным сосудом, локтевой веной (диаметром более 2 мм) на этапе статических измерений условие Ds < 0 не выполнялось. На первом этапе динамического режима измерений, при нагружении от 0 до 20 мм рт.ст. обнаруживается наличие крупной вены с малым давлением в сосуде (менее 20 мм рт.ст.), о чем свидетельствует и уменьшение параметров μa(692), μa(834) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, более чем на 25% от значений в статическом режиме измерений. На втором этапе нагружения в динамическом режиме обнаруживается наличие крупной артерии - локтевой - в исследуемой области, что подтверждается появлением пульсаций силы прижатия F(t), сохраняющихся до Fmax, что соответствует давлению в сосуде более 90 мм рт.ст. При этом изменения μs'(834) и μs'(692) соответствовали Ds > 0.
Повышение чувствительности секторного оптоволоконного датчика (Фиг. 5) к локальным неоднородностям исследуемого объема биологической ткани по сравнению с линейным датчиком прототипа подтверждается разной локальной динамикой (пульсовой и дыхательной) для излучателей разных подгрупп и результатами измерений, проводимых на неоднородных фантомах биологических тканей с включениями, имитирующими крупные сосуды по оптическим параметрам (Фиг. 11).
Таким образом, проведенные исследования продемонстрировали возможность осуществления изобретения с достижением заявляемого результата.
ЛИТЕРАТУРА
1. Yoshino M., Kin T., Ito A., Saito T., Nakagawa D., Ino K., Saito N. Feasibility of diffusion tensor tractography for preoperative prediction of the location of the facial and vestibulocochlear nerves in relation to vestibular schwannoma // Acta Neurochirurgica. - 2015. - 157(6), Р. 939-946.
2. E. Cordero, I. Latka, Ch. Matthus, I. W. Schie, J. Popp, "In-vivo Raman Spectroscopy: from basics to applications," J. Biomed. Opt. 23(7), 071210-1-23 (2018), doi: 10.1117/1.JBO.23.7.071210.
3. Eric Larry Wisotzky, Florian Cornelius Uecker, Philipp Arens, Steffen Dommerich, Anna Hilsmann, Peter Eisert, "Intraoperative hyperspectral determination of human tissue properties," J. Biomed. Opt. 23(9), 091409-(1-8) (September, 2018), doi: 10.1117/1.JBO.23.9.091409.
4. Kazuhiro Gono, Takashi Obi, Masahiro Yamaguchi, Nagaaki Ohyama, Hirohisa Machida, Yasushi Sano, Shigeaki Yoshida, YasuoHamamoto, Takao Endo, "Appearance of enhanced tissue features in narrow-band endoscopic imaging" // Journal of Biomedical Optics 9(3), 568-577 (May/June 2004).
5. Frank J. Bolton, Amir S. Bernat, Kfir Bar-Am, David Levitz, and Steven Jacques, "Portable, low-cost multispectral imaging system: design, development, validation, and utilization" J. Biomed. Opt. 23(12), 121612 (2018), doi: 10.1117/1.JBO.23.12.121612. (Journal of Biomedical Optics).
6. Luciano Bachmann, Denise Maria Zezell, Adriana da Costa Ribeiro, and Laercio Gomes, AmandoSiuiti, "Fluorescence Spectroscopy of Biological Tissues-A Review" Applied Spectroscopy Reviews, 41: 575-590, 2006 DOI: 10.1080/05704920600929498.
7. Yinghua Sun, NisaHatami, Matthew Yee, Jennifer Phipps, Daniel S. Elson, Fredric Gorin, Rudolph J. Schrot, Laura Marcu, "Fluorescence lifetime imaging microscopy for brain tumor image-guided surgery" // Journal of Biomedical Optics 15(5), 056022 (September/October 2010).
8. Brian W. Pogue, Summer L. Gibbs-Strauss, Pablo A. Valdes, Kimberley S. Samkoe, David W. Roberts, and Keith D. Paulsen, "Review of Neurosurgical Fluorescence Imaging Methodologies" // IEEE JOURNAL OF SELECTED TOPICS IN QUANTUM ELECTRONICS, VOL. 16, NO. 3, MAY/JUNE 2010DOI10.1109/JSTQE.2009.2034541.
9. Ovsepian, S.V., Olefir, I., Westmeyer, G., Razansky, D., and Ntziachristos, V. Pushing the boundaries of neuroimaging with optoacoustics // Neuron 96, December 6, 2017, р.966-988.
10. Шарипов О. И. и др. Опыт применения интраоперационной ультразвуковой допплерографии в эндоскопической транссфеноидальной хирургии //Журнал "Вопросы нейрохирургии" имени НН Бурденко. - 2016. - Т. 80. - №. 2. - С. 15-20.
11. Smistad E., Johansen K.F., Iversen D.H., Reinertsen I. Highlighting nerves and blood vessels for ultrasound-guided axillary nerve block procedures using neural networks // J. Med. Imag. 2018. V. 5. N 4. P. 044004.
12. Parthasarathy D. Thirumala, Santhosh Kumar Mohanraj, Miguel Habeych, Kelley Wichman, Yue Fang Chang, Paul Gardner, Carl Snyderman, Donald J. Crammond, Jeffrey Balzer. Value of Free-Run Electromyographic Monitoring of Extraocular Cranial Nerves during Expanded Endonasal Surgery (EES) of t7he Skull Base. Journal of Neurological Surgery Reports. 2013;74:R1. http://dx.doi.org/10.1055/s-0033-1346975.
13. Шкарубо А. Н. и др. Нейрофизиологическая идентификация черепных нервов в эндоскопической эндоназальной хирургии опухолей основания черепа //Журнал "Вопросы нейрохирургии" имени НН Бурденко. - 2016. - Т. 80. - №. 3. - С. 35-49.
14. Infrared neural stimulation of human spinal nerve roots in vivo / J. M. Cayce, J. D. Wells, J. D. Malphrus et al. // Neurophotonics. 2015. - 2(1). - Р. 015007.
15. Pulsed laser versus electrical energy for peripheral nerve stimulation / J. Wells, P. Konrad, C. Kao et al. // Journal of Neuroscience Methods. 2007. - 163(2). - P. 326-337.
16. Balthasar A., Desjardins A. E., M. van der Voort, et al. Optical Detection of Peripheral Nerves: An in Vivo Human Study // Regional anesthesia and pain medicine, 2012, Vol. 37, No.3, p. 277-82.
17. Сафонова, Л.П. Исследование нейроваскулярных структур с помощью фазово-модуляционной спектрофотометрии [Электронный ресурс]/ Л.П. Сафонова, В.Г. Орлова, А.Н. Шкарубо //Оптика и спектроскопия. - 2019. -том 126.№6. -С. 822-833. (DOI: 10.21883/ОS.2019.06.47778.58-19). Проверено 14.12.2019.
Версия на английском языке:
Safonova, L.P.The neurovascular structures research by phase modulation spectrophotometry [Электронный ресурс]/ Safonova, L.P., Orlova, V.G., Shkarubo, A.N. // Optics and Spectroscopy, 2019, Vol. 126, No. 6, pp. 745-757(https://rdcu.be/bM7sz). Проверено 14.12.2019.
18. Возможности спектрофотометрии для обнаружения и распознавания нейроваскулярных структур / Л.П. Сафонова, А.Н. Шкарубо, В.Г.Орлова В.Г., А.Д.Лесничая, И.В.Чернов// Медицинская техника. - 2018. - Том 52. - №6.- С. 28-31.
Версия на английском языке:
The Potential of the Spectrophotometric Method for Detection
and Identification of Neurovascular Structures [Электронный ресурс]/L.P. Safonova, A. N. Shkarubo, V. G. Orlova, A. D. Lesnichaia, and I. V. Chernov// Biomedical Engineering. -2019. -Vol. 52.- No. 6.- Р. 402-406. (DOI: 10.1007/s10527-019-09856-6). Проверено 14.12.2019.
19. Крупаткин А.И., Сидоров В.В. Функциональная диагностика состояния микроциркуляторно-тканевых систем: Колебания, информация, нелинейность. Изд.2-е. - М.: ЛЕНАНД, 2016. - 496 с.
20. Utzinger U., Richards-Kortum R. R. Fiber optic probes for biomedical optical spectroscopy // Journal of Biomedical Optics. - 2003. - Vol. 8. - No. 1. - P. 121-147.
21. Choi J.H., Wolf M., Toronov V., et al. Noninvasive determination of the optical properties of adult brain: near-infrared spectroscopy approach // Journal of Biomedical Optics. - 2004, vol. 9, No. 1, p. 221-229.
22. Scholkmann F., Kleiser S., Metz A. J., Zimmermann R., Pavia J. M., Wolf U., Wolf M. A review on continuous wave functional near-infrared spectroscopy and imaging instrumentation and methodology // NeuroImage. - 2014, vol. 85, Part 1, p. 6-27.
23. Оптическая биомедицинская диагностика. В 2 т. Т. 1 / Пер. с англ. под ред. В. В. Тучина. - М.: Физматлит, 2007. - 560 с.
24. Wolf, M., Ferrari, M., Quaresima, V. Progress of near-infrared spectroscopy and topography for brain and muscle clinical applications // Journal of Biomedical Optics. - 2007, vol. 12, N 6, p.062104 (1-14).
25. Fantini S., Franceschini M. A., and Gratton E. Semi-infinite-geometry boundary problem for light migration in highly scattering media: a frequency-domain study in the diffusion approximation // Journal of Optical Society of America. - 1994. Vol. 11. N 10. p. 2128.
26. Fantini, S., Franceschini, M.A., Maier, J. S., et.al. Frequency-domain multichannel optical detector for non-invasive tissue spectroscopy and oximetry // Optical engineering. - 1995, Vol. 34, No. 1, p.32-42.
27. Franceschini, M.A.,Fantini, S., Gratton, E. Method for measuring absolute saturation of time-varying and other hemoglobin compartments / US Patent No US 6,216,021 B1. - 2001.
28. Torricelli, A. ,Contini, D., Pifferi, A., et al. Time domain functional NIRS imaging for human brain mapping // NeuroImage. - 2014, Vol. 85, p. 28-50.
29. Martelli F., Sassaroli A., Bianco S. D. and Zaccanti G. Solution of the time-dependent diffusion equation for a three-layer medium: application to study photon migration through a simplified adult head model // Phys. Med. Biol. 52 (2007) 2827-2843.
30. Spichtig S., Hornung R., Brown D. W., Haensse D., and Wolf M. Multifrequency frequency-domain spectrometer for tissue analysis // Review of scientific instruments. - 2009, Vol. 80, p. 024301(1-7).
31. Jacques S. L. Topical Review. Optical properties of biological tissues: a review // Phys. Med. Biol. - 2013, Vol. 58, p. R37-R61.
32. Физиология человека. В 3-х томах. Т.2. Пер. с англ./ Под ред. Р. Шмидта и Г. Тевса. - М.: Мир, 1996. - С. 556-559, 626-639.
33. Лелюк В.Г., Лелюк С.Э. Церебральное кровообращение и артериальное давление. - М.: Реальное время, 2004. - 304 с.
34. Программное обеспечение для испытания материалов [Электронный ресурс] Режим доступа: https://www.instron.ru/ru-ru/products/materials-testing-software.
35. Chan S., Conti F., Salisbury K., Blevins N. H. Virtual Reality Simulation in Neurosurgery: Technologies and Evolution // Neurosurgery, 2013, Vol. 72: A154-A164.
36. Каталог промышленных роботов. Настольные минироботы [Электронный ресурс] Режим доступа: http://robotforum.ru/promyishlennyie-robotyi.html.
37. Силомоментные датчики. ForceKit от Weiss-Robotics. [Электронный ресурс] Режим доступа: http://ant-company.ru/catalog/forcesensor/forcekit/
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА ДЛЯ ИНТРАОПЕРАЦИОННОГО ОБНАРУЖЕНИЯ И РАСПОЗНАВАНИЯ НЕЙРОВАСКУЛЯРНЫХ СТРУКТУР В ОБЪЁМЕ БИОЛОГИЧЕСКОЙ ТКАНИ | 2021 |
|
RU2758868C1 |
| ОПТИКО-ХИРУРГИЧЕСКОЕ УСТРОЙСТВО ДЛЯ ОБНАРУЖЕНИЯ И РАСПОЗНАВАНИЯ НЕЙРОВАСКУЛЯРНЫХ СТРУКТУР В ОБЪЁМЕ БИОЛОГИЧЕСКОЙ ТКАНИ | 2021 |
|
RU2767895C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЦЕНКИ СОСТОЯНИЯ АРТЕРИАЛЬНОГО РУСЛА | 2019 |
|
RU2731414C1 |
| СПОСОБ ОЦЕНКИ КОРРЕКТНОСТИ УСТАНОВКИ ПОТОКОНАПРАВЛЯЮЩЕГО СТЕНТА | 2024 |
|
RU2834685C1 |
| СПОСОБ НЕИНВАЗИВНОЙ ПУЛЬСОВОЙ ДИАГНОСТИКИ СЕРДЕЧНОЙ ДЕЯТЕЛЬНОСТИ ПАЦИЕНТА И ИЗМЕРЕНИЯ СКОРОСТИ ПУЛЬСОВОЙ ВОЛНЫ И УСТРОЙСТВО ДЛЯ РЕАЛИЗАЦИИ ЭТОГО СПОСОБА | 2009 |
|
RU2393759C1 |
| НАКОЖНЫЙ ЗОНД, УСТРОЙСТВО И СПОСОБ ДЛЯ НЕИНВАЗИВНОГО ОПРЕДЕЛЕНИЯ СОСТОЯНИЯ ЗДОРОВЬЯ | 2003 |
|
RU2302196C2 |
| СПОСОБ ОЦЕНКИ ВОЗРАСТНЫХ ИЗМЕНЕНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ЧЕЛОВЕКА | 2012 |
|
RU2485886C1 |
| НОСИМОЕ УСТРОЙСТВО, СПОСОБ И СИСТЕМА ДЛЯ ИЗМЕРЕНИЯ ПАРАМЕТРОВ КРОВИ | 2023 |
|
RU2821143C1 |
| Способ определения ударного объема сердца человека | 2022 |
|
RU2790766C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИЙ ПРОИЗВОДНЫХ ГЕМОГЛОБИНА В БИОЛОГИЧЕСКИХ ТКАНЯХ | 2013 |
|
RU2517155C1 |
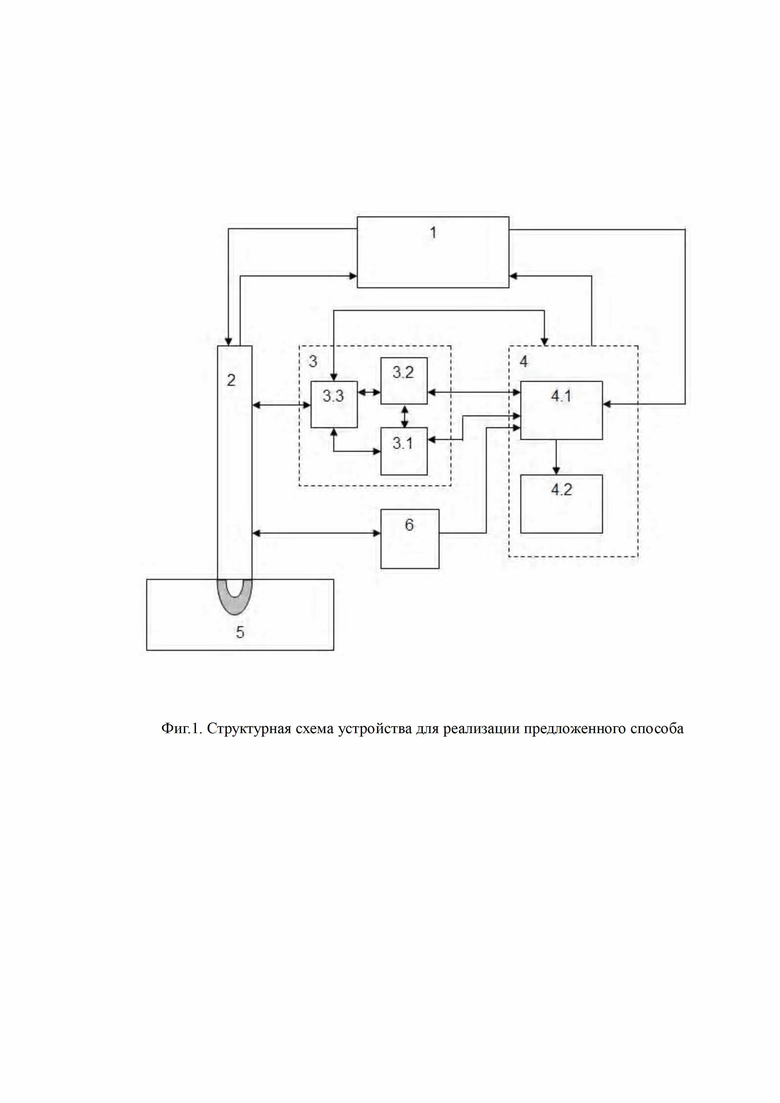



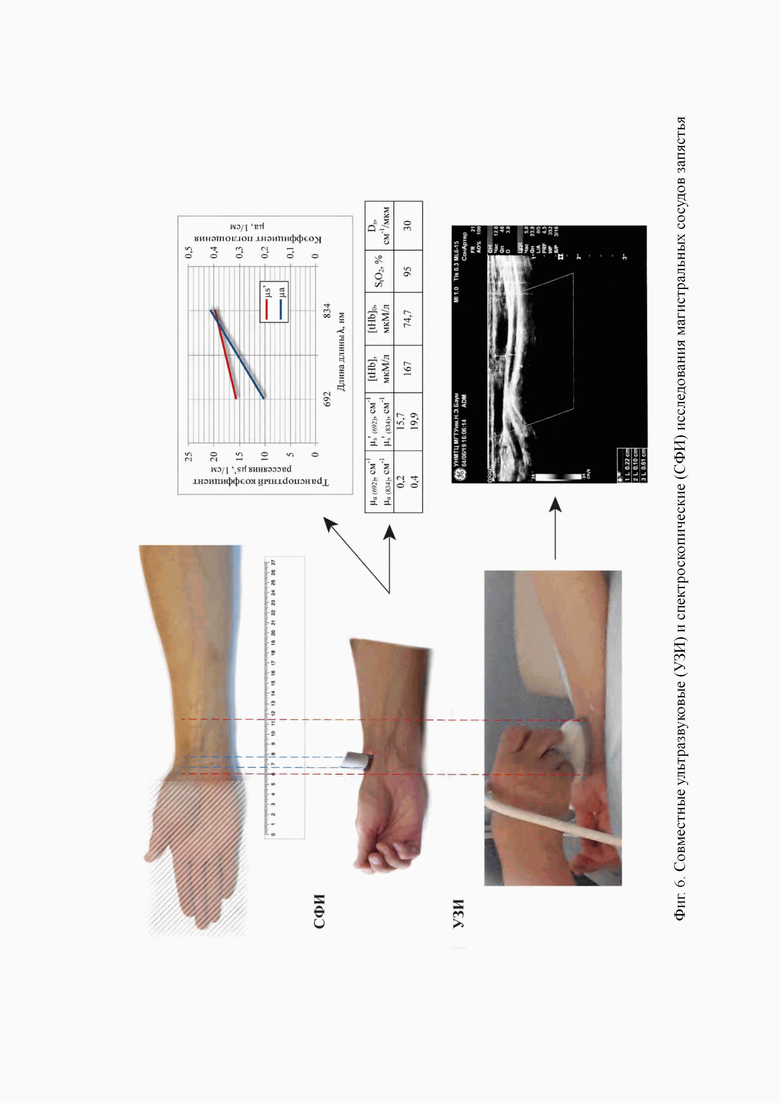
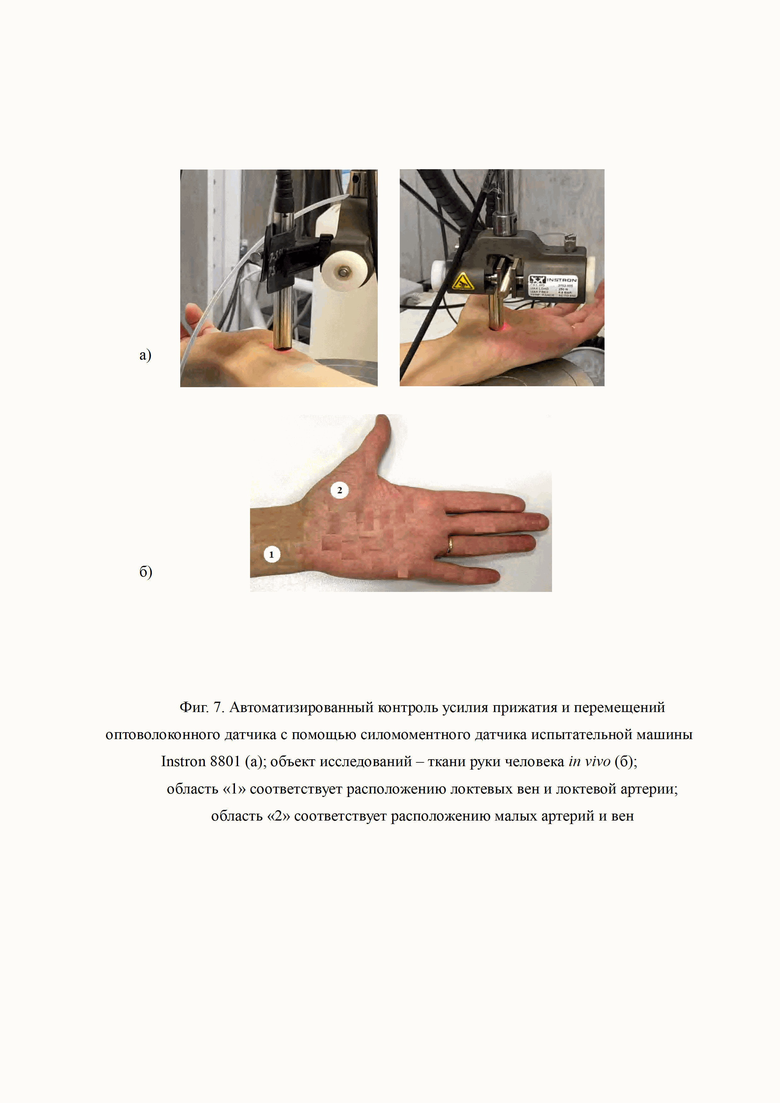
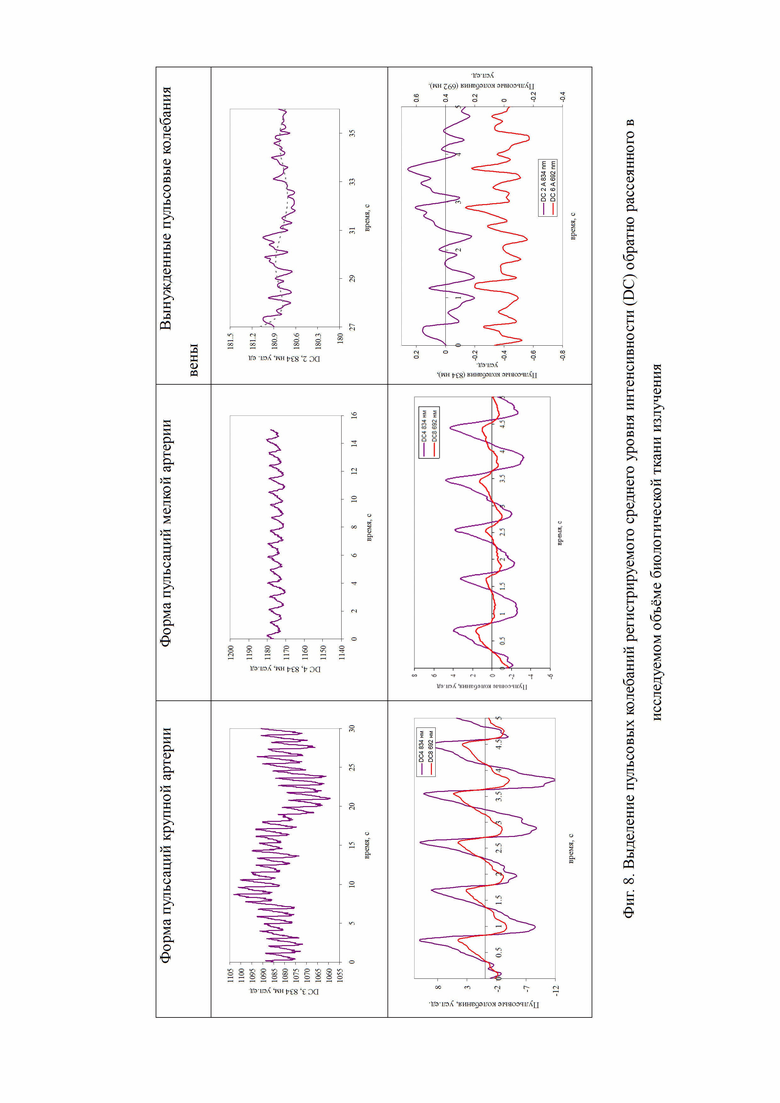
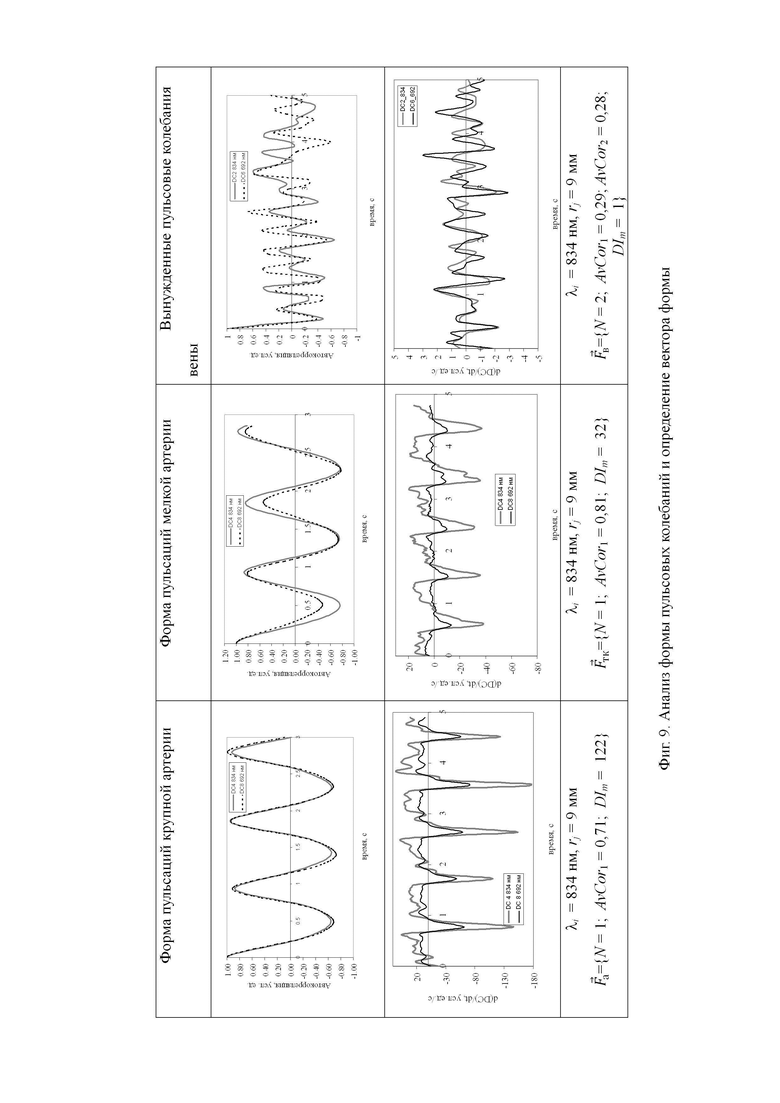
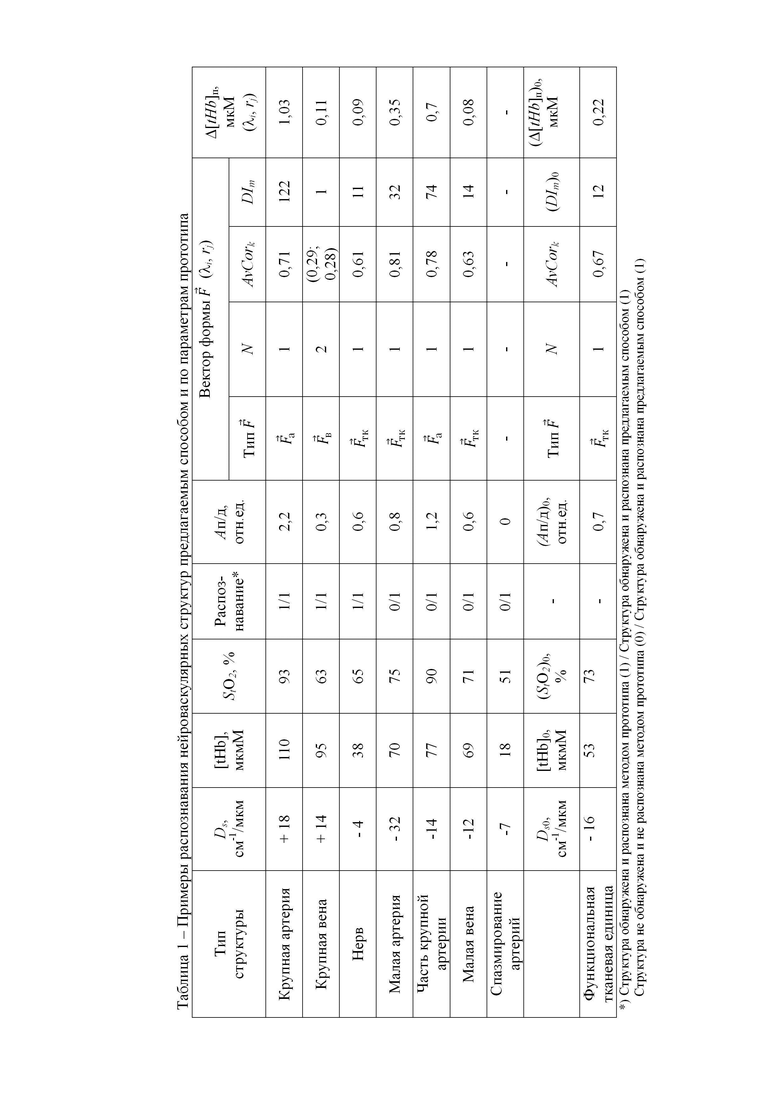
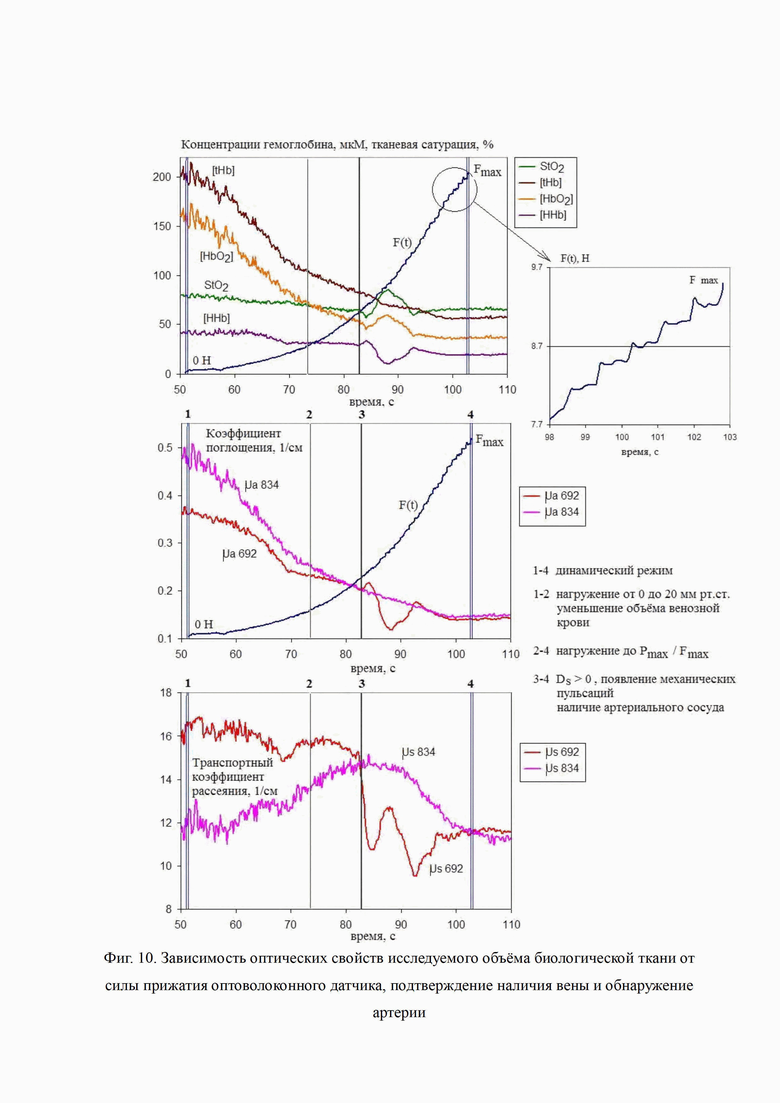
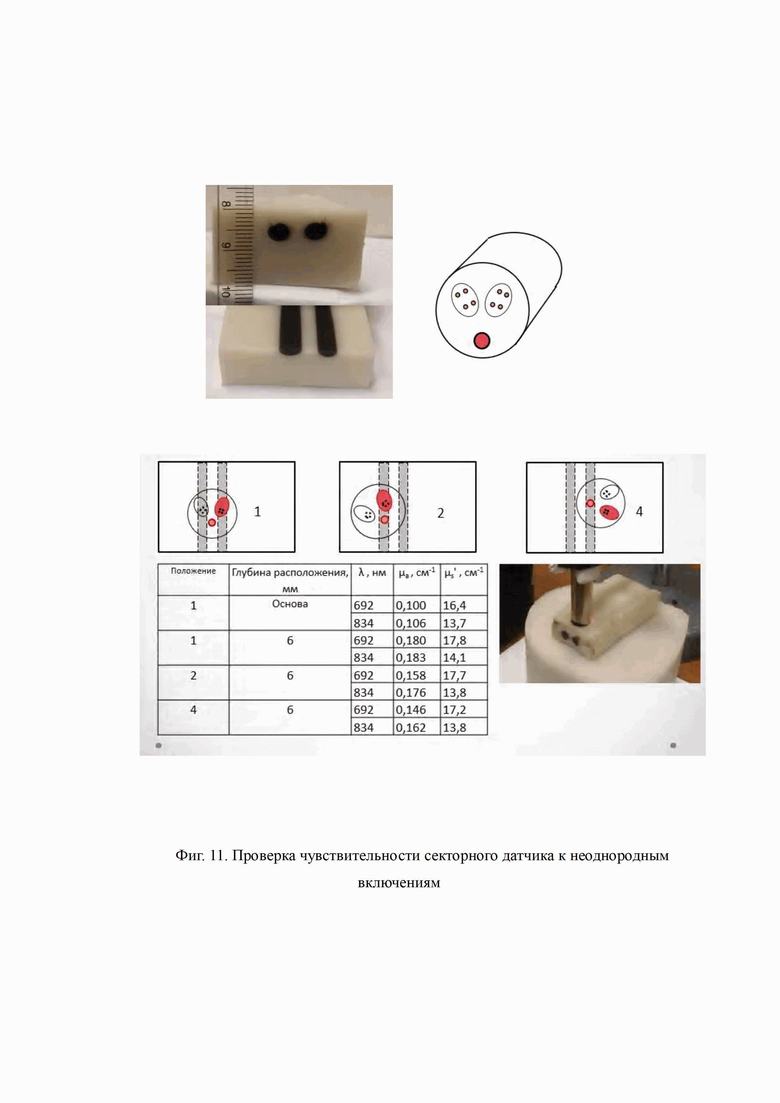
Изобретение относится к области медицины, а именно к интраоперационной диагностике и функциональной диагностике, и предназначено для интраоперационного обнаружения и распознавания нейроваскулярных структур в объеме биологической ткани. Проводят контактное подповерхностное зондирование исследуемого объема биологической ткани оптическим излучением с использованием оптоволоконного датчика для отражательной диффузионной спектроскопии, включающего приемник и излучатели по меньшей мере на двух длинах волн, (λ1) и (λ2), где λ2>λ1, выбранных из диапазона 650 - 950 нм на максимальную глубину не менее 5 мм. Регистрируют в режиме с временным разрешением для каждой длины волны параметры обратнорассеянного излучения, оптические параметры, включая коэффициент поглощения μa(λi) и транспортный коэффициент рассеяния μs'(λi), по которым определяют концентрацию общего гемоглобина ([tHb]) в единице исследуемого объема биологической ткани и тканевую сатурацию (StO2), а также тангенс угла наклона транспортного коэффициента рассеяния от длины волны (Ds). Производят последующее обнаружение и распознавание нейроваскулярных структур: нервов, артериальных и венозных сосудов по итогам сравнения полученных параметров с их пороговыми значениями, полученными на основе оценки предоперационных и интраоперационных диагностических данных. При этом зондирование исследуемого объема биологической ткани осуществляют по меньшей мере двумя группами излучателей и, по меньшей мере, одним приемником, где каждая из групп излучателей включает по меньшей мере две подгруппы, каждая из которых содержит излучатели по меньшей мере двух длин волн из указанного диапазона значений и расположена на отдельном расстоянии от приемника rj, j=1..М, М≥2. При этом по интенсивности обратнорассеянного излучения в исследуемом объеме биологической ткани для каждой длины волны и каждого rj дополнительно определяют: амплитуды пульсовых (Ап) и дыхательных (Ад) колебаний и их отношение Ап/д=Ап/Ад, вектор формы 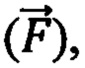 представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду
представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду 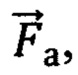 крупному венозному сосуду
крупному венозному сосуду 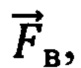 или функциональной тканевой единице в размерах исследуемого объема биологической ткани
или функциональной тканевой единице в размерах исследуемого объема биологической ткани 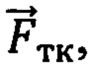 . Для каждой подгруппы источников по меньшей мере для двух длин волн из указанного диапазона определяют локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п). При этом перечисленные параметры измеряют в статическом режиме, при котором давление оптоволоконного датчика Р на поверхность исследуемого объема биологической ткани составляет Р≤0,2 мм рт.ст. Вывод о наличии определенных нейроваскулярных структур делают по получению совокупностей измеренных параметров. Способ обеспечивает получение достоверных данных о наличии нервов, крупных и малых артерий и вен в объеме биологической ткани на глубине, как минимум, до 5 мм во время проведения операций за счет расширения набора критериев обнаружения и распознавания нейроваскулярных структур, применения методов кратно-масштабного анализа регистрируемой интенсивности обратнорассеянного излучения и формирования комплексной характеристики пульсовых и дыхательных колебаний. 13 з.п. ф-лы, 1 табл., 11 ил.
. Для каждой подгруппы источников по меньшей мере для двух длин волн из указанного диапазона определяют локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п). При этом перечисленные параметры измеряют в статическом режиме, при котором давление оптоволоконного датчика Р на поверхность исследуемого объема биологической ткани составляет Р≤0,2 мм рт.ст. Вывод о наличии определенных нейроваскулярных структур делают по получению совокупностей измеренных параметров. Способ обеспечивает получение достоверных данных о наличии нервов, крупных и малых артерий и вен в объеме биологической ткани на глубине, как минимум, до 5 мм во время проведения операций за счет расширения набора критериев обнаружения и распознавания нейроваскулярных структур, применения методов кратно-масштабного анализа регистрируемой интенсивности обратнорассеянного излучения и формирования комплексной характеристики пульсовых и дыхательных колебаний. 13 з.п. ф-лы, 1 табл., 11 ил.
1. Способ интраоперационного обнаружения и распознавания нейроваскулярных структур в объеме биологической ткани, включающий:
контактное подповерхностное зондирование исследуемого объема биологической ткани оптическим излучением с использованием оптоволоконного датчика для отражательной диффузионной спектроскопии, включающего приемник и излучатели по меньшей мер на двух длинах волн, (λ1) и (λ2), где λ2>λ1, выбранных из диапазона 650 - 950 нм на максимальную глубину не менее 5 мм,
регистрацию в режиме с временным разрешением для каждой длины волны параметров обратнорассеянного излучения, оптических параметров, включая коэффициент поглощения μa(λi) и транспортный коэффициент рассеяния μs'(λi), по которым определяют концентрацию общего гемоглобина ([tHb]) в единице исследуемого объема биологической ткани и тканевую сатурацию (StO2), а также тангенс угла наклона транспортного коэффициента рассеяния от длины волны (Ds),
с последующим обнаружением и распознаванием нейроваскулярных структур: нервов, артериальных и венозных сосудов по итогам сравнения полученных параметров с их пороговыми значениями, полученными на основе оценки предоперационных и интраоперационных диагностических данных,
отличающийся тем, что
зондирование исследуемого объема биологической ткани осуществляют по меньшей мере двумя группами излучателей и по меньшей мере одним приемником, где каждая из групп излучателей включает по меньшей мере две подгруппы, каждая из которых содержит излучатели по меньшей мере двух длин волн из указанного диапазона значений и расположена на отдельном расстоянии от приемника rj, j=1..М, М≥2,
при этом по интенсивности обратнорассеянного излучения в исследуемом объеме биологической ткани для каждой длины волны и каждого rj дополнительно определяют:
амплитуды пульсовых (Ап) и дыхательных (Ад) колебаний и их отношение Ап/д=Ап/Ад,
вектор формы 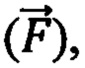 представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду
представляющий собой набор значений, характеризующих форму пульсовой волны, соответствующую крупному или малому артериальному сосуду 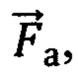 крупному венозному сосуду
крупному венозному сосуду 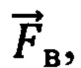 или функциональной тканевой единице в размерах исследуемого объема биологической ткани
или функциональной тканевой единице в размерах исследуемого объема биологической ткани 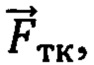
а для каждой подгруппы источников по меньшей мере для двух длин волн из указанного диапазона определяют локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п),
при этом перечисленные параметры измеряют в статическом режиме, при котором давление оптоволоконного датчика Р на поверхность исследуемого объема биологической ткани составляет Р≤0,2 мм рт.ст.,
а вывод о наличии определенных нейроваскулярных структур делают по получению следующих совокупностей измеренных параметров:
- при {Ds>0; [tHb]>[tHb]0; StO2>(StO2)0; Ап/д>(Ап/д)0; 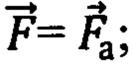 Δ[tHb]п>(Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
Δ[tHb]п>(Δ[tHb]п)0} (1) - о наличии в исследуемом объеме биологической ткани крупной артерии;
- при {Ds>0; [tHb]>[tHb]0; StO2≤(StO2)0 или StO2>(StO2)0; Ап/д<(Ап/д)0; 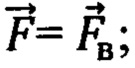 Δ[tHb]п≤(Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
Δ[tHb]п≤(Δ[tHb]п)0} (2) - о наличии в исследуемом объеме биологической ткани крупной вены;
- при {Ds0<Ds<0; [tHb]≤[tHb]0; StO2≤(StO2)0; Ап/д≤(Ап/д)0; 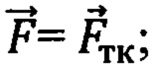 Δ[tHb]п<(Δ[tHb]п)0} (3) - о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
Δ[tHb]п<(Δ[tHb]п)0} (3) - о наличии в исследуемом объеме биологической ткани нерва диаметром от 1,5 мм и более;
- при {Ds≤Ds0; [tHb]≥[tHb]0; StO2≥(StO2)0; Ап/д≥(Ап/д)0; 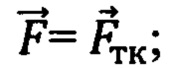 Δ[tHb]п≥(Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани по меньшей мере одной малой артерии;
Δ[tHb]п≥(Δ[tHb]п)0} (4) - о наличии в исследуемом объеме биологической ткани по меньшей мере одной малой артерии;
- при {Ds0<Ds<0; [tHb]>[tHb]0; StO2≥(StO2)0; Ап/д>(Ап/д)0; 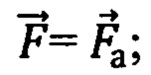 Δ[tHb]п>(Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs'(λ)>0;
Δ[tHb]п>(Δ[tHb]п)0} (5) - о наличии в исследуемом объеме биологической ткани части крупной артерии, когда объем цельной крови сосуда в исследуемом объеме биологической ткани не приводит к изменениям Δμs'(λ)>0;
- при {Ds0≤Ds<0; [tHb]>[tHb]0; StO2≤(StO2)0; Ап/д<(Ап/д)0; 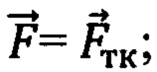 Δ[tHb]п≤(Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани по меньшей мере одной малой вены,
Δ[tHb]п≤(Δ[tHb]п)0} (6) - о наличии в исследуемом объеме биологической ткани по меньшей мере одной малой вены,
где [tHb]0, Ds0, (StO2)0, (Ап/д)0, (Δ[tHb]п)0 - пороговые значения упомянутых параметров, измеренные для функциональной тканевой единицы в размерах исследуемого объема биологической ткани,
причем значения параметров Ds, [tHb] и StO2 определяют по меньшей мере для одной группы излучателей и соответствующего приемника, а Ап/д, 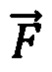 и Δ[tHb]п - по меньшей мере для одной подгруппы излучателей этой группы.
и Δ[tHb]п - по меньшей мере для одной подгруппы излучателей этой группы.
2. Способ по п. 1, характеризующийся тем, по получению следующих совокупностей измеренных параметров {Ds0≤Ds<0; [tHb]<[tHb]0; StO2<(StO2)0; Ап/д=0 (при отсутствии пульсовых колебаний)} (7) - делают вывод о спазмировании артериальных сосудов исследуемого объема биологической ткани или питающей крупной артерии.
3. Способ по п. 1, характеризующийся тем, что параметры обратнорассеянного излучения дополнительно регистрируют при осуществлении динамического режима, характеризующегося вдавливанием оптоволоконного датчика в исследуемый объем биологической ткани с заданной постоянной скоростью VL≤10 мм/мин при изменении силы от 0 до Fmax, соответствующей максимально допустимому для исследуемой биологической ткани уровню давления Pmax = Fmax/S, с учетом площади контакта S оптоволоконного датчика с поверхностью исследуемого объема биологической ткани, где Pmax принимает значения от 70 мм рт.ст. для тканей головного мозга до 200 мм рт.ст. для тканей нижних конечностей, или при двухэтапном изменении давления Р от 0 до 20 мм рт.ст. и от 20 мм рт.ст. до Pmax.
4. Способ по п. 3, характеризующийся тем, что измерение параметров в статическом и динамическом режимах проводят с использованием автоматизированного контроля позиционирования и силы прижатия оптоволоконного датчика к поверхности исследуемого объема биологической ткани, реализуемого с помощью устройства позиционирования, оснащенного датчиком перемещения и датчиком силы или силомоментным датчиком с пределом измерений не более 100 Н.
5. Способ по п. 4, характеризующийся тем, что при измерении параметров в динамическом режиме одномоментно регистрируют зависимости силы прижатия (F) от перемещения оптоволоконного датчика (х) и силы прижатия (F) от времени (t) с частотой дискретизации не менее 20 Гц, на основании которых выявляют наличие артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме, а также оценивают величину сосуда по значению давления в сосуде.
6. Способ по п. 5, характеризующийся тем, что вывод о наличии артериального сосуда на глубине, большей максимальной глубины зондирования в статическом режиме, делают при выявлении пульсовых колебаний силы F(t) с максимумом в диапазоне частот сердечных сокращений от 0,8 до 3,0 Гц с использованием методов кратно-масштабного анализа дискретных сигналов в реальном времени, включая метод оконного преобразования Фурье и вейвлет-преобразование.
7. Способ по п. 5, характеризующийся тем, что значение давления (Р) артериального сосуда определяют по формуле Р=F/S, где F - значение силы прижатия оптоволоконного датчика в момент времени tк, соответствующий концу пульсовых колебаний или Fmax, если пульсовые колебания не прекратились, S - площадь контакта оптоволоконного датчика с поверхностью исследуемого объема биологической ткани; и при получении значения 70≤Р≤90 мм рт.ст. делают вывод о наличии малой артерии на глубине, большей максимальной глубины зондирования в статическом режиме; при получении Р>90 мм рт.ст. делают вывод о наличии крупной артерии на глубине, большей максимальной глубины зондирования в статическом режиме.
8. Способ по п. 3, характеризующийся тем, что при уменьшении на первом этапе двухэтапного динамического режима, как минимум, для одной группы источников, при уменьшении параметров μа(λi) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, более чем на 25% по сравнению со значениями, полученными в статическом режиме, и прекращении дыхательных колебаний в соответствующих регистрируемых сигналах обратнорассеянного излучения, дополнительно подтверждают наличие крупного венозного сосуда в исследуемом объеме биологической ткани.
9. Способ по п. 3, характеризующийся тем, что при уменьшении на первом и втором этапах двухэтапного динамического режима параметров μа(λi) и [tHb], характеризующих кровенаполнение исследуемого объема биологической ткани, менее чем на 25% по сравнению со значениями, полученными в статическом режиме, для всех групп источников, дополнительно подтверждают отсутствие в исследуемой области биологической ткани крупных сосудов.
10. Способ по п. 1, характеризующийся тем, что зондирование оптическим излучением исследуемого объема биологической ткани осуществляют равномерно при помощи секторного или матричного оптоволоконного датчика.
11. Способ по п. 1, характеризующийся тем, что зондирование оптическим излучением осуществляют не менее 15 с с последующим усреднением измеренных параметров Ds, [tHb] и StO2 для каждой группы источников.
Способ по п. 1, характеризующийся тем, что вектор формы пульсовых колебаний 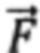 определяют тремя переменными {N, AνCork, DIm}ij, где:
определяют тремя переменными {N, AνCork, DIm}ij, где:
N - количество компонент фурье-спектра автокорреляционной функции пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения, амплитуда которых не менее 0,2 отн.ед.;
AνCork, k=1…N - амплитуды этих компонент фурье-спектра автокорреляционной функции;
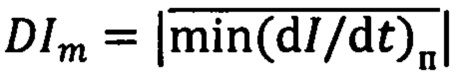 - среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения по времени с шагом 0,2±0,003 с;
- среднее за период регистрации абсолютное значение локальных минимумов производной пульсовой составляющей регистрируемой интенсивности обратнорассеянного излучения по времени с шагом 0,2±0,003 с;
при этом форму пульсовой волны определяют как соответствующую функциональной тканевой единице в размерах исследуемого объема биологической ткани при получении следующих значений вектора формы:
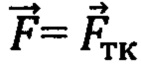 : N=1; 0,6≤AνCor1; DIm∈ [DIm0, 4DIm0], -
: N=1; 0,6≤AνCor1; DIm∈ [DIm0, 4DIm0], -
как соответствующую крупной артерии в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
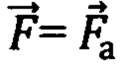 : N=1; 0,6≤AνCor1≤1; DIm>4DIm0, -
: N=1; 0,6≤AνCor1≤1; DIm>4DIm0, -
как соответствующую крупной вене в исследуемом объеме биологической ткани при получении следующих значений вектора формы:
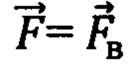 : N=1 или N=2; AνCork<0,6, k=1…N; DIm<DIm0, -
: N=1 или N=2; AνCork<0,6, k=1…N; DIm<DIm0, -
где DIm0 - пороговое значение DIm, определяемое для функциональной тканевой единицы в размерах исследуемого объема биологической ткани.
13. Способ по п. 1, характеризующийся тем, что локальную амплитуду пульсовых колебаний концентрации общего гемоглобина (Δ[tHb]п) для каждой подгруппы источников и соответствующего расстояния от приемника, как минимум, по двум длинам волн из указанного диапазона, определяют по регистрируемым сигналам интенсивности обратнорассеянного излучения I(λi) с использованием модифицированного закона Бугера-Ламберта-Бера, выражения для суммарного коэффициента поглощения на каждой длине волны с учетом соответствующего количества анализируемых хромофоров, расчетной формулы для дифференциального фактора длины на основе измеряемых в статическом режиме для соответствующей группы излучателей оптических параметров и μa(λi) и μs'(λi) и формул для определения концентраций оксигенированного и дезоксигенированного гемоглобина по μа(λi).
14. Способ по п. 1, характеризующийся тем, что пороговые значения параметров Ds0, [tHb]0, (StO2)0, (Ап/д)0, DIm0 и (Δ[tHb]п)0 для функциональной тканевой единицы в размерах исследуемого объема биологической ткани определяют, исходя из соответствия типу исследуемой биологической ткани по клеточному составу, структуре и характеру кровоснабжения без подлежащих распознаванию нейроваскулярных включений, с использованием спектроскопических измерений с временным разрешением путем измерений в статическом режиме интраоперационно перед основными хирургическими манипуляциями с исследуемой биологической тканью, подлежащей иссечению, и/или с привлечением априорной/предоперационной диагностической информации об исследуемой биологической ткани.
| УСТРОЙСТВО ДЛЯ ФЛУОРЕСЦЕНТНОЙ НАВИГАЦИИ В НЕЙРОХИРУРГИИ | 2017 |
|
RU2661029C1 |
| WO 2019023584 A1, 31.01.2019 | |||
| US 20100063523 A1, 11.03.2010 | |||
| Трансформатор тока | 1973 |
|
SU504254A1 |
| САФОНОВА Л.П | |||
| Исследование нейроваскулярных структур с помощью фазово-модуляционной спектрофотометрии | |||
| Оптика и спектроскопия | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Улей | 1923 |
|
SU822A1 |
| VALDES P | |||
| A | |||
| et al | |||
| Optical technologies for intraoperative | |||
Авторы
Даты
2020-11-13—Публикация
2020-06-29—Подача