Изобретение относится к медицине, в частности, стоматологии и челюстно-лицевой хирургии, и может быть использовано при операциях по восстановлению утраченного объема костной ткани после удаления одонтогенных кист челюстей.
Известно, что в целом ряде патологических состояний организма, связанных с нарушением репаративного остеогенеза, таких, как, переломов челюстных костей, осложненных остеопорозом, инфицированием и ослаблением иммунитета, ложных суставах и послеоперационных дефектах верхней и нижней челюстей после операции по удалению кист челюстей (цистэктомий и цистотомий) требуется направленная стимуляция костеобразования, которая выполняется хирургом путем проведения операции остеопластики. Для ускорения репаративного процесса активно используют остеопластические биоматериалы, которым присущи остеоиндуктивные и/или остеокондуктивные свойства.
Истинным остеоиндуктивным костным биоматериалом является собственная кость пациента, однако ее дефицит и сложности по забору и хранению привели к более широкому использованию аналогов - аллогенной кости, где донором является другой индивидуум, однако, данный аллогенный биоматериал требует дорогостоящей антигенной обработки. Поэтому сегодня очень широко используют модификации остеопластических материалов на основе гидроксида кальция, например, в виде пористой гидроксиапатитной керамики и трикальцийфосфата (Tanaka, Т., Komaki, Н., Chazono, М., Kitasato, S., Kakuta, A., Akiyama, S., Marumo, K. Basic research and clinical application of beta-tricalcium phosphate (β-TCP). Morphologie. 2017; 101(334):164-172. https://doi.org/10.1016/j.morpho.2017.03.002), а также костезамещающие биоматериалы на основе костного коллагена и морфогенетических белков (Song, Y., Wan, L., Zhang, S., Du, Y. Biological response to recombinant human bone morphogenetic protein-2 on bone-implant osseointegration in ovariectomized experimental design. Journal of Craniofacial Surgery. 2019; 30(1):141-144. https://doi.org/10.1097/SCS. 0000000000004992). Перечисленным выше биоматериалам присущи только остеокондуктивные свойства, в это понятие включается способность материала служить матрицей, основой для роста новообразованной костной ткани. Для проявления остеоиндуктивных свойств в составе таких биоматериалов должны присутствовать факторы роста и другие стимулирующие остеогенез вещества, например, сульфатированные или несульфатированные гликозаминогликаны (гиалуроновая кислота).
В этой связи проблема ускорения репаративного остеогенеза имеет большую актуальность и разработка способа ускорения репаративного остеогенеза с использованием остеопластических материалов, представляет большую практическую значимость.
В аспекте ускорения репаративного остеогенеза в костных полостях после удаления пораженных участков костной ткани челюсти наиболее близким предлагаемому способу по технической сути и достигаемому результату является использование полисахарида животного происхождения хонсурида для заполнения послеоперационных костных полостей (RU 2112550 С1, заявка на изобретение RU №94027755/14 от 20.07.1994, МПК А61К 6/097).
Установлено, что использование хонсурида ускоряет течение репаративного остеогенеза в послеоперационных костных полостях челюстей при достаточном кровоостанавливающем и противовоспалительном эффекте, а также хорошей биосовместимости и простой методике применения.
Вместе с этим, при использовании хонсурида скорость репаративного остеогенеза невелика, поскольку формирование костного регенерата в послеоперационной костной полости происходит не ранее 6 месяцев после хирургического вмешательства. Сам регенерат к этому сроку еще не является полноценной костью, сходной с нативной (неповрежденной) костной тканью и не пригоден для опорной функциональной нагрузки, такой, какую выполняют дентальные имплантаты или межзубные костные перегородки.
Кроме этого, в послеоперационном периоде у больных с одонтогенными кистами челюстей нередко наблюдаются явления интоксикации организма из-за длительного периода сенсибилизации микроорганизмами и продуктами их жизнедеятельности, ставшими причиной развития заболеваний твердых и мягких тканей зуба, а также тканей пародонта.
Поскольку возникновению и развитию большинства одонтогенных кист челюстей предшествует проникновение в периапикальные ткани патогенных микроорганизмов (деятельность которых ранее уже привела к воспалению тканей зуба и пародонта), необходимо обеспечение противовоспалительного и антибактериального воздействия.
Поставлена задача: ускорить формирование костного регенерата, с трабекулярной структурой, идентичной неповрежденной кости, с обеспечением сорбционного, детоксикационного и антибактериального эффекта.
Поставленная задача решена путем использования смеси хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП при температуре 38°С, активированных после помещения в рану ультрафиолетовыми лучами мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд.
Хонсурид использован в виде стерильного деминерализованного и лиофилизированного (лишенного антигенной активности) порошка, представляющего собой полисахарид животного происхождения, способствующий формированию новых коллагеновых микрофибрилл, необходимых для восстановления трабекулярной структуры костной ткани в процессе репаративного остеогенеза в костных полостях челюстей в послеоперационном периоде.
Рибофлавин (витамин В2) ускоряет рост и регенерацию клеток, участвует в обезвреживании токсинов и других вредных веществ, оказывает антиоксидантное действие, регулирует окислительно-восстановительные процессы. Известно, что рибофлавин разрушается на свету (поэтому его рекомендуют хранить в темном месте), однако, при воздействии ультрафиолетовых лучей высокой интенсивности происходит активизация рибофлавина, в результате которой он оказывается способным сшивать коллагеновые волокна (https://www.vesti.ru/doc.html?id=3248406; https://news.cornell.edu/stories/2020/03/two-step-method-patches-herniated-discs).
Гиалуроновая кислота является активным хондропротекторным средством, оказывает стимулирующее влияние на репаративные процессы в структурах соединительнотканного происхождения, а также способствует ингибированию в них дистрофических посттравматических процессов. Механизмом репаративного действия гиалуроновой кислоты выступает стимулирование синтеза гликозаминогликанов и коллагена.
Полисорб МП - неорганический, неселективный, полифункциональный энтеросорбент на основе высокодисперсного кремнезема. Иммобилизацией хонсурида и гиалуроновой кислоты на Полисорбе МП решается ряд задач, среди которых главной является обеспечение длительного депонирования синтезируемых гликозаминогликанов и коллагена в ране, достаточного для обеспечения стимуляции дифференцировки плюрипотентных клеток на протяжении от 7 до 14 суток.
При выполнении опытно-конструкторских работ, направленных на решение поставленной цели, установлено, что особенно эффективным показало себя использование смеси хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП при температуре 38°С, при которой происходит иммобилизация максимального объема смеси на Полисорбе МП. Выбранный температурный параметр определялся опытным путем, в частности, установлено, что смесь хонсурида, рибофлавина и 2% гиалуроновой кислоты, охлажденная до температуры ниже 38°С, например, до 32-35°С, плохо иммобилизуется на Полисорбе МП, образуя нерастворимые хлопья, сгустки и комки. При температуре выше 38°С, например, при 40-42°С смесь хонсурида, рибофлавина и 2% гиалуроновой кислоты теряет свои остеоиндуктивные свойства из-за денатурации костных морфогенетических протеинов.
Смесь хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованная на Полисорбе МП при температуре 38°С, помимо выраженных остеоиндуктивных свойств, обладает высокими сорбционными и детоксикационными свойствами.
После помещения в рану смеси хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованной на Полисорбе МП производится ее активация ультрафиолетовыми лучами мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд, за счет чего обеспечивается антибактериальный эффект, а также в дальнейшем - интенсивное образование коллагеновых волокон.
Суть лечебного воздействия разработанного способа заключается в следующем. Воздействие ультрафиолетовых лучей мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд дает высокий антибактериальный эффект. В результате воздействия лучей происходит активация хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП, в результате чего хонсурид из смеси и коллагеновые волокна из раны образуют прочное соединение. Под стимулирующем влиянии 2% гиалуроновой кислоты в рану начинают мигрировать плюрипотентные клетки из неповрежденных участков костной ткани, способствуя ускорению репаративного остеогенеза и формированию трабекулярной структуры новообразованной кости, которая завершается построением прочного костного регенерата через 2-3 месяца.
Способ осуществляют следующим образом. Производят разведение 60 мг хонсурида в 30 мг рибофлавина и 60 мг 2% гиалуроновой кислоты. Иммобилизацию полученной смеси на Полисорбе МП производят при температуре 38°С путем ее добавления к энтеросорбенту из расчета 60 мг хонсурида на 30 мг рибофлавина, 60 мг 2% гиалуроновой кислоты и 30 мг Полисорба МП.
Полученную смесь вносят в рану и активируют с помощью стоматологической фотополимеризационной лампы ультрафиолетовыми лучами мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд. Операцию завершают наложением нерезорбируемой мембраны для изоляции раны, которую ушивают с использованием лоскута из местных тканей.
Опыт использования разработанного способа показал, что во всех 35 случаях его клинического применения отмечается ускорение репаративного остеогенеза без воспалительных осложнений и рецидивов заболевания, подтвержденное клиническими примерами, которые приводим ниже.
Пример 1. Больная П., 40 лет, обратилась с жалобами на неприятные ощущения в области центральной части верхней челюсти, в районе центральных резцов, неприятный запах изо рта, периодическое появление гноя в полости рта из свищевого хода.
Из анамнеза установлено, что больная ранее лечила у стоматолога корневые каналы 12, 11, 21, 22 зубов.
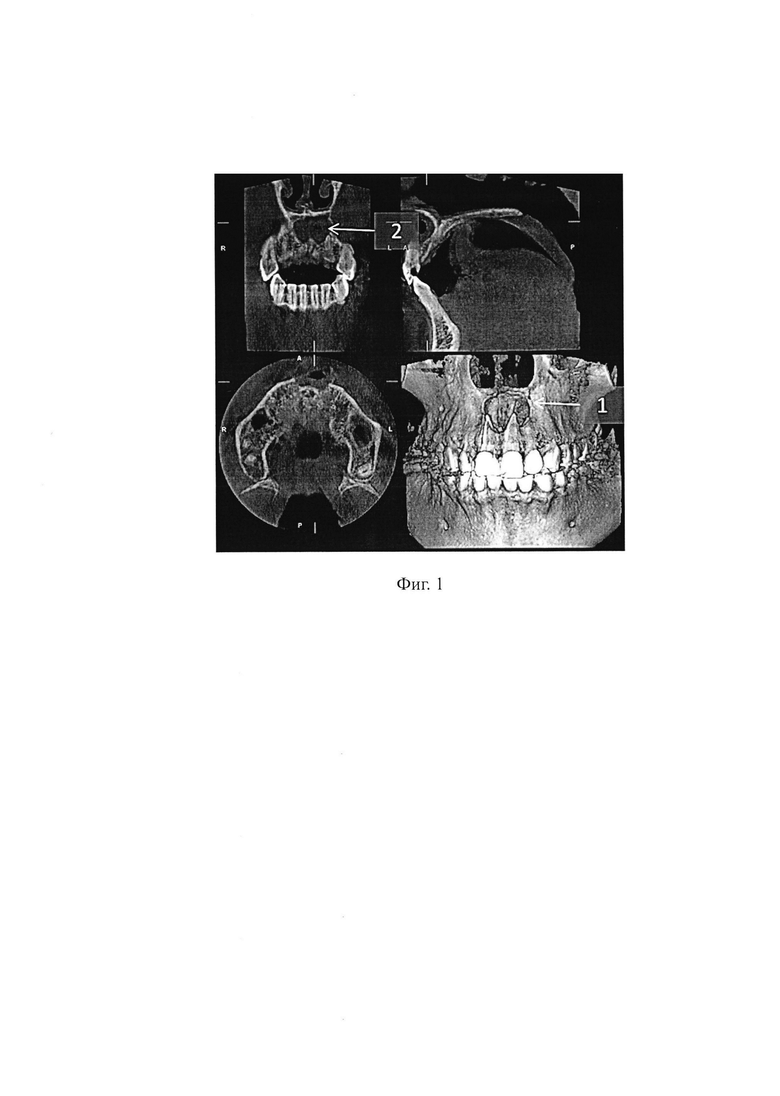
Объективно: при осмотре полости рта в области проекции корней 12, 11, 21, 22 зубов слизистая оболочка гиперемирована, отечна, имеется свищевой ход в проекции корня 21 зуба, при пальпации передняя кортикальная пластинка податливая, легкое нажатие сопровождается характерным пергаментным хрустом (симптом Дюпюитрена), при сильном нажатии - флюктуация. При рентгенологическом обследовании (компьютерная томография) установлено наличие очага деструкции костной ткани в области верхушек корней 12, 11, 21, 22 зубов (фиг. 1).
Диагноз: одонтогенная киста верхней челюсти в области верхушек корней 12, 11, 21, 22 зубов.
Лечение. Под инфильтрационной и проводниковой анестезией Sol.Ultracaini 4% с адреналином 1:100000 выполнена операция цистэктомии с кюретажем раны и удалением оболочки кисты. Вместе с инфицированной костной тканью удалены (резецированы) верхушки корней 12, 11, 21, 22 зубов.
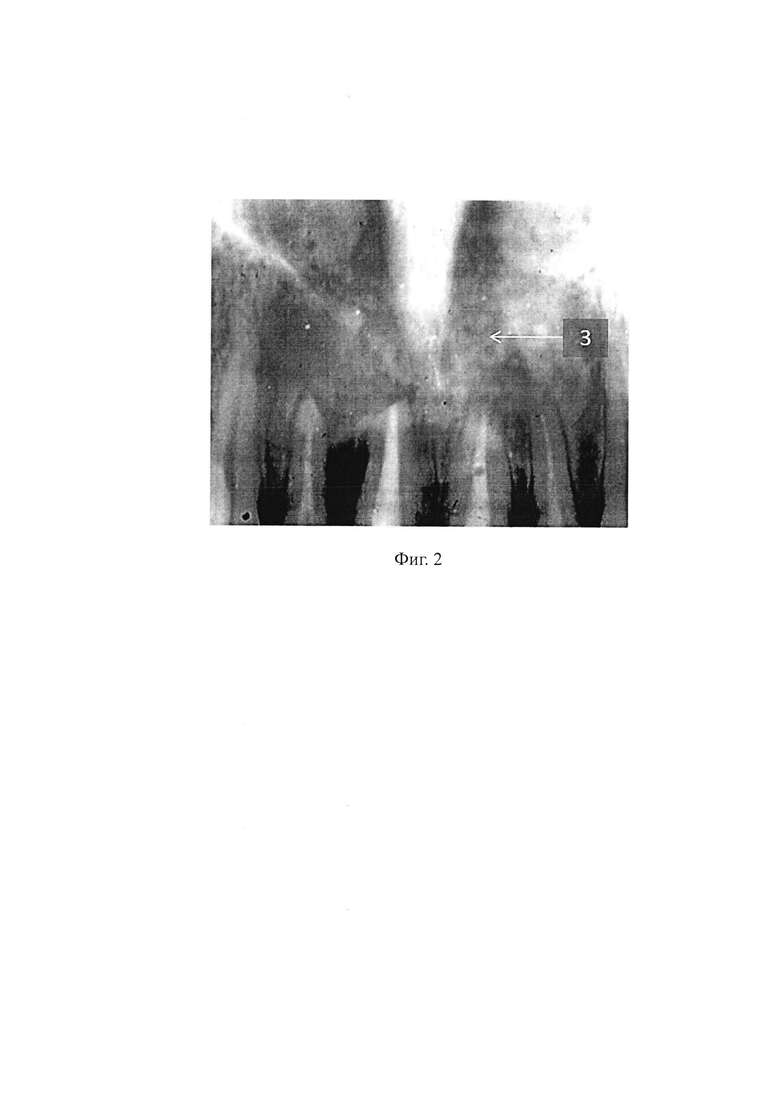
Послеоперационная костная полость диаметром 36 мм во время операции заполнена смесью хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП при температуре 38°С из расчета 60 мг хонсурида на 30 мг рибофлавина, 60 мг 2% гиалуроновой кислоты и 30 мг Полисорба МП, активированных после помещения в рану ультрафиолетовыми лучами мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд (фиг. 2). Операция завершена наложением нерезорбируемой мембраны, рана ушита узловыми швами с использованием лоскута из местных тканей.
В результате проведенной операции обеспечены сорбционный, детоксикационный и антибактериальный эффекты, ускорение репаративного остеогенеза, что подтверждено результатами дальнейшего клинического наблюдения. Наблюдение в раннем послеоперационном периоде (до 7 суток) показало, что у больной отсутствовали болевой синдром, гноетечение и отек околочелюстных мягких тканей.
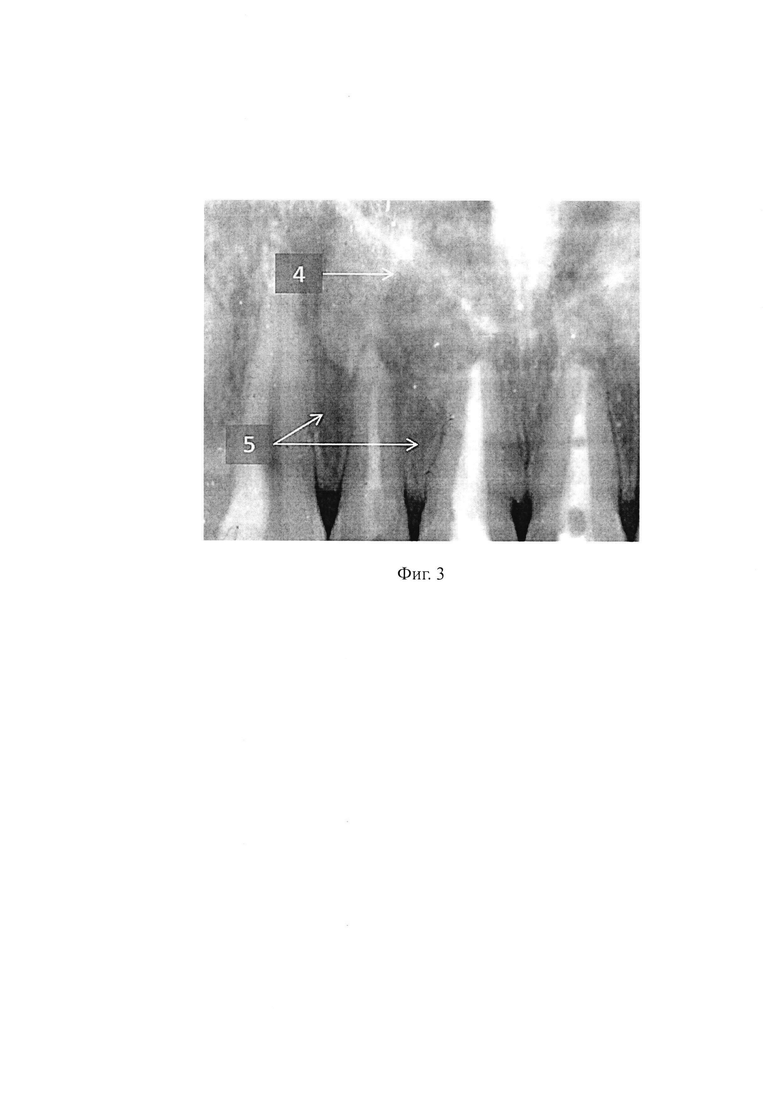
При рентгенологическом обследовании в позднем послеоперационном периоде (через 3 месяца) установлено, что заживление послеоперационного костного дефекта верхней челюсти завершилось формированием полноценного костного регенерата со средней плотностью 490 ЕД Хаунсфилда, к этому же сроку сформировались полноценные костные межзубные перегородки (фиг 3).
На фиг. 1 изображена компьютерная томограмма больной П. с очагом деструкции костной ткани верхней челюсти в области верхушек корней 12, 11, 21, 22 зубов (1) диаметром 36 мм (2) до операции.
На фиг. 2 изображен фрагмент рентгенограммы больной П. с оперированной областью верхней челюсти, заполненной смесью хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП сразу после операции (3).
На фиг. 3 изображен фрагмент рентгенограммы больной П. с оперированной областью верхней челюсти (4), заполненной смесью хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП и сформированные межкорневые костные перегородки (5) в области 21, 11 зубов через 3 месяца после операции.
Пример 2. Больной В., 38 лет, обратился с жалобами на боли в области зубов нижней челюсти слева, общую слабость, гноетечение из свищевого хода в районе 37 зуба.
Из анамнеза установлено, что больной около 2 лет назад лечил у стоматолога корневые каналы 36 и 37 зубов.
Объективно: при осмотре полости рта в области проекции корней 36 и 37 зубов слизистая оболочка гиперемирована, отечна, имеется свищевой ход в проекции корня 37 зуба, при нажатии на который выделяется гной. При пальпации наружной кортикальной пластинки не обнаружено, имеется выпячивание и флюктуация под слизистой оболочкой в проекции верхушек корней 36 и 37 зубов.
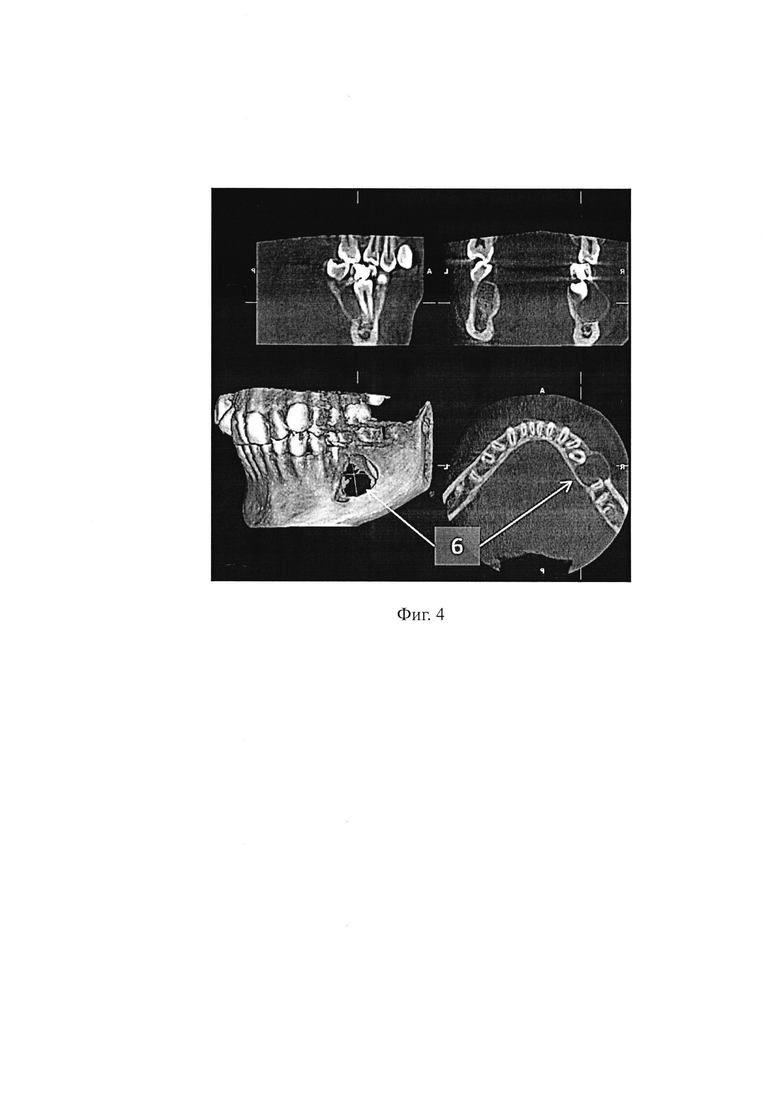
При рентгенологическом обследовании (компьютерная томография) установлено наличие очага деструкции костной ткани в области верхушек корней 36 и 37 зубов (фиг. 4).
Диагноз: одонтогенная киста нижней челюсти в области верхушек корней 36 и 37 зубов.
Лечение. Под инфильтрационной и проводниковой анестезией Sol.Ultracaini 4% с адреналином 1:100000 выполнена операция цистэктомии с кюретажем раны и удалением оболочки кисты в области 36-37 зубов.
Послеоперационная костная полость диаметром 18 мм во время операции заполнена смесью хонсурида, рибофлавина и 2% гиалуроновой кислоты, иммобилизованных на Полисорбе МП при температуре 38°С из расчета 60 мг хонсурида на 30 мг рибофлавина, 60 мг 2% гиалуроновой кислоты и 30 мг Полисорба МП, активированных после помещения в рану ультрафиолетовыми лучами мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд.
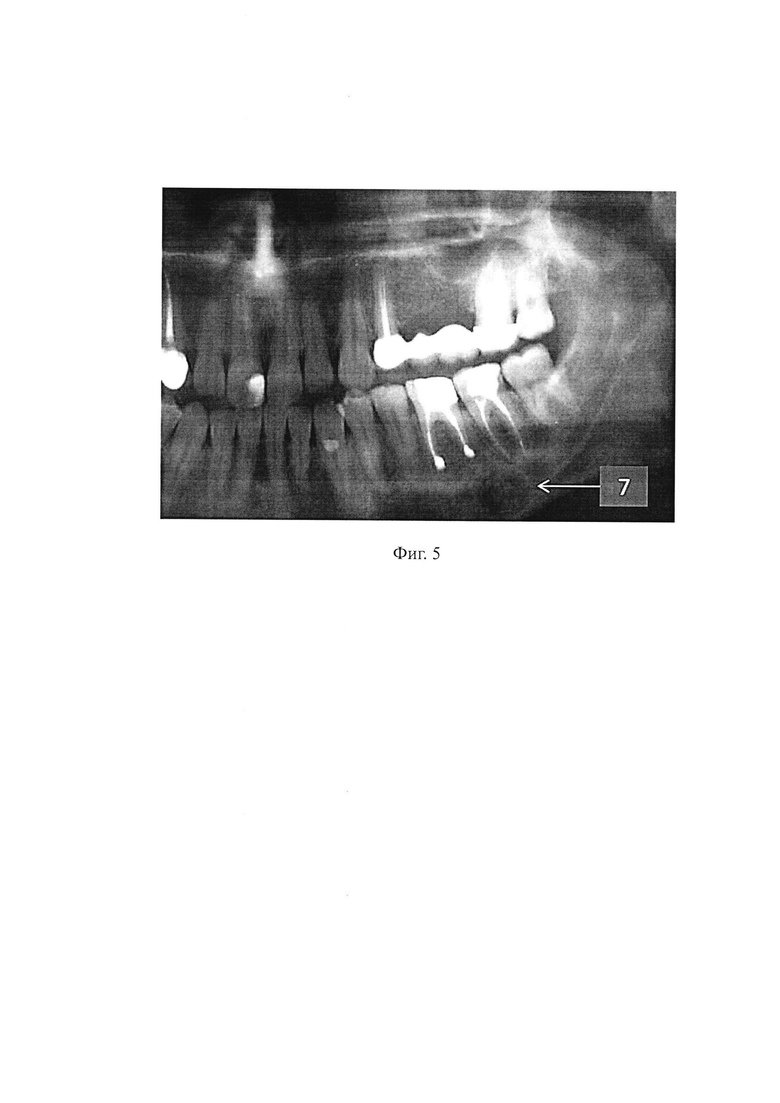
В результате проведенной операции обеспечены сорбционный, детоксикационный и антибактериальный эффекты, ускорение репаративного остеогенеза, что подтверждено результатами дальнейшего клинического наблюдения. Наблюдение в раннем послеоперационном периоде (до 7 суток) показало, что у больного отсутствовал болевой синдром, гноетечение и отек околочелюстных мягких тканей. При рентгенологическом обследовании в позднем послеоперационном периоде (через 4 месяца) установлено, что заживление послеоперационного костного дефекта нижней челюсти завершилось формированием полноценного костного регенерата со средней плотностью 645 ЕД Хаунсфилда (фиг. 5).
На фиг. 4 изображена компьютерная томограмма больного В., выполненная до операции, на которой отчетливо виден очаг деструкции костной ткани в области 36 и 37 зубов нижней челюсти слева (6).
На фиг. 5 изображена ортопантомограмма больного В., выполненная через 4 месяца после операции цистэктомии, на которой видно восстановление плотности костной ткани в области 36 и 37 зубов нижней челюсти слева (7).
Таким образом, в результате применения заявляемого способа обеспечивается сорбционный, детоксикационный и антибактериальный эффекты, ускорение репаративной регенерации кости, причем восстановление костной ткани происходит с образованием полноценного трабекулярной структуры, полностью идентичной неповрежденной (нативной) кости, что может служить основанием для широкого внедрения данного способа в практику.
Предлагаемый способ может быть использован в хирургической стоматологии и челюстно-лицевой хирургии, в клинической работе частных и государственных стоматологических учреждений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УСКОРЕНИЯ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА ПРИ БИСФОСФОНАТНОМ ОСТЕОНЕКРОЗЕ | 2020 |
|
RU2745584C1 |
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2020 |
|
RU2738406C1 |
| ОСТЕОПЛАСТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ СУБАНТРАЛЬНОЙ АУГМЕНТАЦИИ | 2019 |
|
RU2729651C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРОДОНТИТА И ПЕРИИМПЛАНТИТА | 2023 |
|
RU2830655C1 |
| СПОСОБ НЕПОСРЕДСТВЕННОЙ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ У ПАЦИЕНТОВ С ВКЛЮЧЕННЫМИ ДЕФЕКТАМИ ЗУБНЫХ РЯДОВ | 2010 |
|
RU2447859C1 |
| СПОСОБ ЛЕЧЕНИЯ ВЕРХНЕЧЕЛЮСТНОГО СИНУСИТА | 2008 |
|
RU2373873C2 |
| СПОСОБ ЦИСТОТОМИИ ЧЕЛЮСТНОЙ КИСТЫ | 2010 |
|
RU2442544C1 |
| СПОСОБ УСКОРЕНИЯ ПРОЦЕССА РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2014 |
|
RU2582976C1 |
| СПОСОБ СУБАНТРАЛЬНОЙ АУГМЕНТАЦИИ КОСТИ ДЛЯ УСТАНОВКИ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ ПРИ АТРОФИИ АЛЬВЕОЛЯРНОГО ОТРОСТКА ВЕРХНЕЙ ЧЕЛЮСТИ | 2011 |
|
RU2469675C1 |
| ЛЕЧЕБНЫЙ ЭЛИКСИР ДЛЯ ОРОШЕНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ ВЕРХНЕЧЕЛЮСТНОГО СИНУСА ПРИ ПЛАСТИКЕ ОРОАНТРАЛЬНОГО СОУСТЬЯ | 2016 |
|
RU2679919C2 |
Изобретение относится к медицине, в частности к стоматологии и челюстно-лицевой хирургии, и может быть использовано при операциях по восстановлению утраченного объема костной ткани после удаления одонтогенных кист челюстей. Способ ускорения репаративной регенерации костной ткани заключается в разведении хонсурида в рибофлавине и 2% гиалуроновой кислоте, иммобилизации полученной смеси на Полисорбе МП при температуре 38°С из расчета 60 мг хонсурида на 30 мг рибофлавина, 60 мг 2% гиалуроновой кислоты и 30 мг Полисорба МП, которые после внесения в рану активируют с помощью фотополимеризационной лампы мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд. Технический результат – обеспечение ускорения репаративного остеогенеза, высокий сорбционный, детоксикационный и антибактериальный эффекты. 5 ил., 2 пр.
Способ ускорения репаративной регенерации костной ткани, включающий хонсурид, отличающийся тем, что производят разведение хонсурида в рибофлавине и 2% гиалуроновой кислоте, иммобилизуют полученную смесь на Полисорбе МП при температуре 38°С из расчета 60 мг хонсурида на 30 мг рибофлавина, 60 мг 2% гиалуроновой кислоты и 30 мг Полисорба МП, которые после внесения в рану активируют с помощью фотополимеризационной лампы мощностью 450 мВт с длиной волны 470 нм в течение 120 секунд.
| ХОНСУРИД КАК ПРЕПАРАТ ДЛЯ ЗАПОЛНЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ КОСТНЫХ ПОЛОСТЕЙ | 1994 |
|
RU2112550C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ СУСТАВОВ (ВАРИАНТЫ), СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ СУСТАВОВ (ВАРИАНТЫ) И УСТРОЙСТВО ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННОГО СРЕДСТВА К ПОРАЖЕННОМУ УЧАСТКУ | 2004 |
|
RU2268052C2 |
| КОМПОЗИЦИЯ ДЛЯ КОСТНОЙ ПЛАСТИКИ (ВАРИАНТЫ) | 2013 |
|
RU2516921C1 |
| РАСТВОР ДЛЯ ПОЛУЧЕНИЯ ПОКРЫТИЯ НА ИМПЛАНТАТАХ И БИОМАТЕРИАЛАХ | 2012 |
|
RU2509554C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОЙ РИБОФЛАВИНОМ СШИТОЙ СОЛИ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2386640C2 |
| СПОСОБ УСКОРЕНИЯ ПРОЦЕССА РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2014 |
|
RU2582976C1 |
| WO 2018213795 A1, 22.11.2018. | |||
Авторы
Даты
2020-12-07—Публикация
2020-04-03—Подача