Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано при лечении термического, химического поражения роговицы и конъюнктивы, послеоперационного отека роговицы после факоэмульсификации катаракты, травматических эрозий роговицы, а также для повышения регенерации роговицы.
В лечении и профилактике заболеваний глаз используют различные методы введения лекарственных веществ в ткани глаза. Наиболее широкое применение нашли глазные капли, мази, гели, подконъюнктивальные, парабульбарные и внутрикамерные инъекции. Инстилляционная методика имеет ряд недостатков, такие как частые закапывания в зависимости от выраженности заболевания, закапывание антибиотиков не сопровождается достижением во влаге передней камеры глаза необходимой концентрации для подавления роста микроорганизмов [Барри П., Руководство ESCRS по профилактике и лечению эндофтальмита после операции по удалению катаракты: данные, дилеммы и выводы / П. Барри, Кордовес Л., Гарднер С.; пер. с анг. Б.Э. Малюгина. Temple house, Ирландия 2013. - 30 с.]. Эффективность лечения часто зависит от состава лекарства, а также от лекарственной формы. При повреждении структуры роговицы декспантенол активирует митоз эпителиальных клеток и ускоряет их миграцию в зону раневого дефекта. Кроме того, декспантенол предотвращает образование рубцов стромы роговицы, влияя на формирование нормальной структуры фибробластов и активизируя их пролиферацию. При использовании декспантенола в регенерированных участках происходит восстановление правильной многослойной структуры коллагеновых волокон, что положительно сказывается на восстановлении прозрачности роговицы [Ventura А.С., Walti R., Bohnke М. Corneal thickness and endothelial density before and after cataract surgery // Br. J. Ophthalmol. 2001. Vol. 85. №1. P. 18-20].
Пленки - твердая дозированная лекарственная форма, представляющая собой одно или многослойные тонкие пластинки подходящего для применения размера, содержащие одно или несколько действующих веществ и вспомогательные, в том числе пленкообразующие, вещества. Пленки как лекарственная форма впервые появились в 1970 году в офтальмологии. Глазные лекарственные пленки (ГЛП) имеют пролонгированное действие, это позволяет поддерживать необходимую концентрацию лекарства в лечебной зоне длительное время, применяются один раз в сутки, их применение исключает частые лечебные процедуры, тем самым освобождая медицинский персонал. Вследствие постепенного выделения действующего вещества ГЛП легко переносятся пациентами и с минимальными побочными и токсичными действиями [Майчук Ю.Ф. Глазные лекарственные пленки / Ю.Ф Майчук, В.И. Поздняков, Г.Л. Хромов, Е.Б. Конева, Л.Н. Старукова // Вестник офтальмологии. - 1974. - №6. - стр. 419-423.]. Заболевания роговицы и травматические повреждения, как одни из важных причин снижения зрения, - представляют собой актуальную проблему в офтальмологии и ставят задачу поиска новых форм лекарственных средств для лечения патологий органа зрения [Waring G.O. 3rd, Bourne W.M., Edelhauser H.F. et al. The corneal endothelium. Normal and pathologic structure and function // Ophthalmology. 1982. Vol. 89. №6. P. 531-590.].
Известна глазная лекарственная пленка, содержащая следующее соотношение компонентов, мас. %: поливиниловый спирт 82,5, арабиногалактан - 16,5 и левофлоксацин - 1 [патент RU 2404779, 2010 г.].
Известна глазная пленка, содержащая поливиниловый спирт, дигидрокверцетин в качестве активного вещества растительного происхождения, моксифлоксацин в качестве антибиотика. Глазные лекарственные пленки с моксифлоксацином удобны в применении, обладают продолжительным антимикробным, антиоксидантным, иммуномодулирующим, противовоспалительным свойствами [патент RU 2581025, 2016 г.].
Наиболее близким аналогом изобретения является глазная пленка, которая содержит измельченную нативную роговицу глаз крупного рогатого скота 0,25 г, поливиниловый спирт 99,25 г, гамма-глобулин 0,25 г, гентамицин 0,25 г. Глазная пленка может быть использована при лечении травматических ожоговых и дистрофических повреждений роговой оболочки и конъюнктивы [патент RU 2173178, 2001 г.]. Недостатками данной пленки являются сложность химического состава и трудоемкий затратный технологический процесс ее получения, кроме этого, эффективность данной пленки не проверена при химических ожогах роговицы.
Задачей предлагаемого изобретения является расширение арсенала лекарственных средств для лечения патологий роговицы.
Технический результат при использовании изобретения -повышение регенерации роговичной ткани.
Заявляемая ГЛП содержит в качестве пленкообразующей основы поливиниловый спирт, а в качестве биологически активного вещества содержит 6-метил-3-(тиетан-3-ил)урацил при следующем содержании компонентов, в г на 100,0 мл очищенной воды:
поливиниловый спирт - 3,3
6-метил-3-(тиетан-3-ил)урацил - 0,12
Известно, что 6-метил-3-(тиетан-3-ил)урацил стимулирует защитную активность фагоцитов, [патент РФ 2485118] и обладает антиоксидантным эффектом, противомикробной активностью, улучшает трофику, стимулирует процесс регенерации в поврежденных тканях [Мещерякова С.А., Катаев В.А., Фаттахова И.Я. и др. Синтез и противомикробная активность ацетанилидов и ацетилгидразонов тиетанилпиримидин-2,4(1H,3H)-дионового ряда // Химико-фармацевтический журнал, 2015. - Т. 49. №9. - С. 28-31].
Изобретение иллюстрируется фигурами 1-5, на которых представлены гистологические препараты глаз экспериментальных кроликов №№1-4, которые окрашены гематоксилин-эозином и исследованы методом световой микроскопии.
Предлагаемую глазную пленку получают следующим образом. На первом этапе технологии приготовления ГЛП подготавливали помещения и вспомогательные вещества, получали в асептических условиях водный раствор 6-метил-3-(тиетан-3-ил)урацила.
Глазные лекарственные пленки с 6-метил-3-(тиетан-3-ил)урацилом получали следующим образом: в асептических условиях герметично закрывающуюся емкость помещали поливиниловый спирт и заливали заранее приготовленным водным раствором 6-метил-3-(тиетан-3-ил)урацила. Оставляли при комнатной температуре в течение 12 часов для полного набухания поливинилового спирта. Затем раствор полимера термостатировали при температуре 80-90°С до его полного растворения. Полученный раствор фильтровали через стерилизующий фильтр и разливали в простерилизованные формы с ячейками стерильной пипеткой. Подложку с ячейками помещали в термостат и высушивали в температуре 45°С до остаточной влажности 5%. Полученные пленки вынимали из ячеек и помещали в стерильные флаконы по 10 мл и герметично укупоривали под обкатку.
Для экспериментальной проверки заявляемого лекарства были приготовлены образцы пленок, с использованием следующих пленкообразователей: поливиниловый спирт (ПВС),
поливинилпирролидон (ПВП), метилцеллюлоза (МЦ), натрий карбоксиметилцеллюлоза (Na-КМЦ), желатин. В качестве пластификатора во все составы, кроме состава с ПВС, вводили глицерин (таблица 1). Полимеры заливаются водой (может быть нагревание, в зависимости от свойств полимера). Масса тщательно перемешивается ручной или механической мешалкой. Смесь выдерживается при комнатной температуре и периодическом перемешивании до полного растворения полимера, затем добавляется глицерин, проводится дополнительное смешивание. Критериями для отбора наиболее подходящего состава пленок служили следующие показатели качества: органолептические свойства, рН водного раствора, толщина, влажность, время растворения. Результаты исследования показателей качества пленок различного состава представлены в таблице 2.
Все растворы пленок имеют нейтральную реакцию. На основании анализа всех показателей выбрали пленки состава №1 с пленкообразователем ПВС.У данного состава по сравнению с другими составами оптимальные органолептические показатели, влажность, толщина и время растворения (пролонгирование).
Готовая лекарственная пленка бесцветная, прозрачная, обладает высокой эластичностью и хорошей адгезией. ГЛП удобна в применении, хорошо совместима с глазной жидкостью, что способствует постепенному высвобождению действующего вещества, обеспечивая пролонгированное действие. Пленку рекомендуется хранить защищенном от света месте, при температуре от 8 до 15°С.
Предлагаемая ГЛП закладывается в конъюнктивальную полость 1 раз в день в течение 7-21 дней.
Применение ГЛП улучшает функциональные исходы, сокращает сроки лечения, пленка хорошо переносится, экономична и удобна в использовании. Показателем клинического выздоровления считается восстановление эпителиально-стромального пласта роговицы.
Предлагаемая ГЛП апробирована на переносимость тканями глаза в эксперименте на 5 кроликах породы шиншилла. Экспериментально вызвали химический ожог роговицы (по методу Обенбергера) аппликацией диска фильтровальной бумаги диаметром 8 мм, смоченной 3% уксусной кислотой, экспозицией 5 секунд. Затем промывали конъюнктивальную полость 0,9% физиологическим раствором в течение 10 минут. После этого в правые глаза кроликов №№1,2,3,4 (4 глаза) закладывали ГЛП с 6-метил-3-(тиетан-3-ил)урацилом 1 раз в день вес период эксперимента. В левый глаз кролика №5 закладывали гель декспантенола 5% (корнерегель) 2 раза в день, а правый глаз оставляли без лечения для наблюдения в условиях отсутствии лечения. Для профилактики бактериальной инфекции всем кроликам закапывали глазные капли тобрамицин 0,3% 4 раза в день. Терапевтическую эффективность лечения оценивали по следующим признакам: рассасывания отека роговицы, уменьшения светобоязни, инъекции, раздражения и отека конъюнктивы, уменьшения сроков лечения.
Гистологическая картина роговицы кролика на вторые сутки наблюдения: в центральной зоне роговицы выявлялась десквамация эпителия от основного вещества роговицы, повреждение Боуменова мембраны. Имеющиеся эпителиоциты обнаруживались со сморщенными, пикнотичными ядрами, клетки располагались в один ряд. Строма отечная, воспалительно-клеточная инфильтрация отсутствовала (фиг. 1).
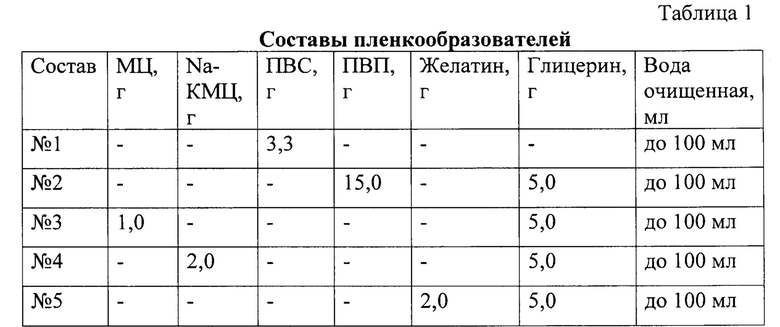
На 7-е сутки наблюдения после кислотного ожога в центральной зоне десквамация переднего эпителия роговицы сохранялась. Однако, под слущенным эпителием выявлялись признаки «наползания» новообразованного эпителиального однорядного эпителия на поверхность коллагеновых волокон основного вещества. Миграция новообразованного эпителия происходило от периферии к центру - центростремительно. Данные камбиальные клетки имели уплощенные ядра, вектор которых был направлен вдоль длинной оси поверхности роговицы (фиг. 2). При окраске по Ван-Гизону коллагеновые волокна не изменяли свои тинкториальные свойства, что говорит о сохранности их фибриллярной структуры (фиг. 3).
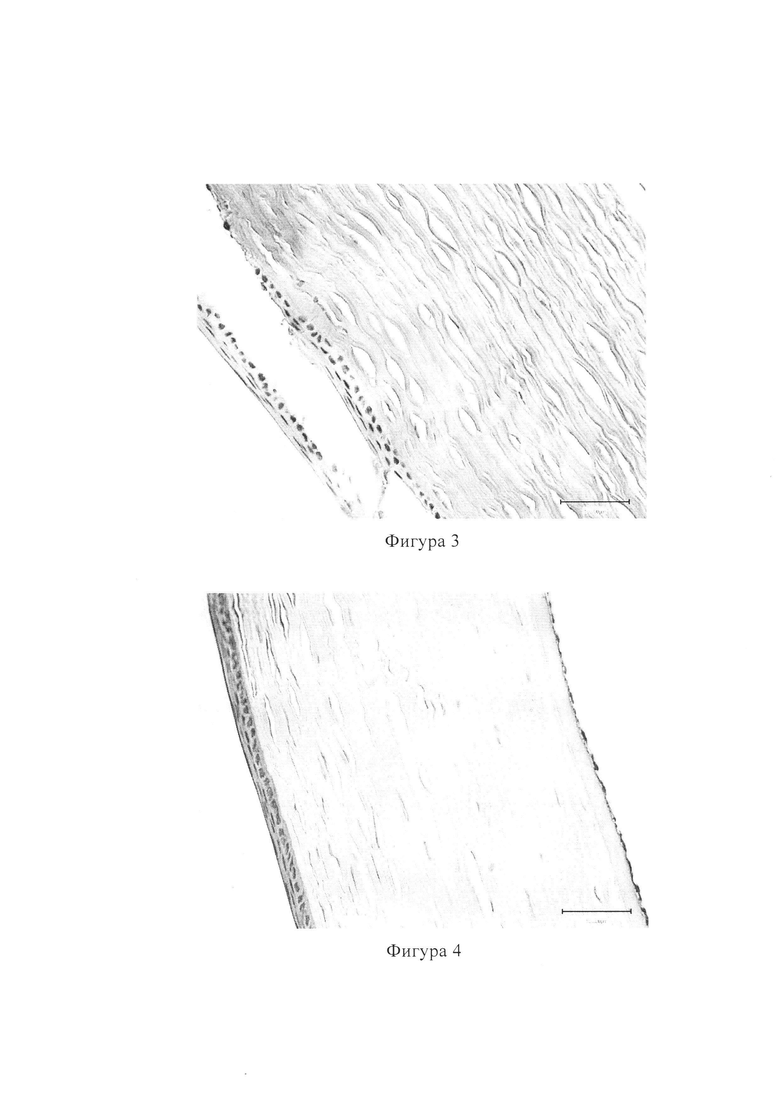
В центральной зоне роговицы спустя 14 суток многослойный плоский эпителий был представлен слоем базальных клеток, ядра их были ориентированы перпендикулярно вектору длины роговицы. Форма цилиндрическая, ядра проявляли интенсивную базофилию, свидетельствующую о высокой синтетической активности. Клетки поверхностного слоя эпителия были уплощены, составляли 2-3 ряда. Признаков десквамации эпителия или эрозивных явлений стромы не наблюдалось. В строме отечные явления уменьшались со временем. Коллагеновые волокна имели параллельно-ориентированные пучки коллагеновых волокон, без явлений набухания и разволокнения фибрилл. Боуменова мембрана определялась в виде тонкой плотной соединительнотканной пластинки, прилежащей к переднему эпителию (фиг. 4).
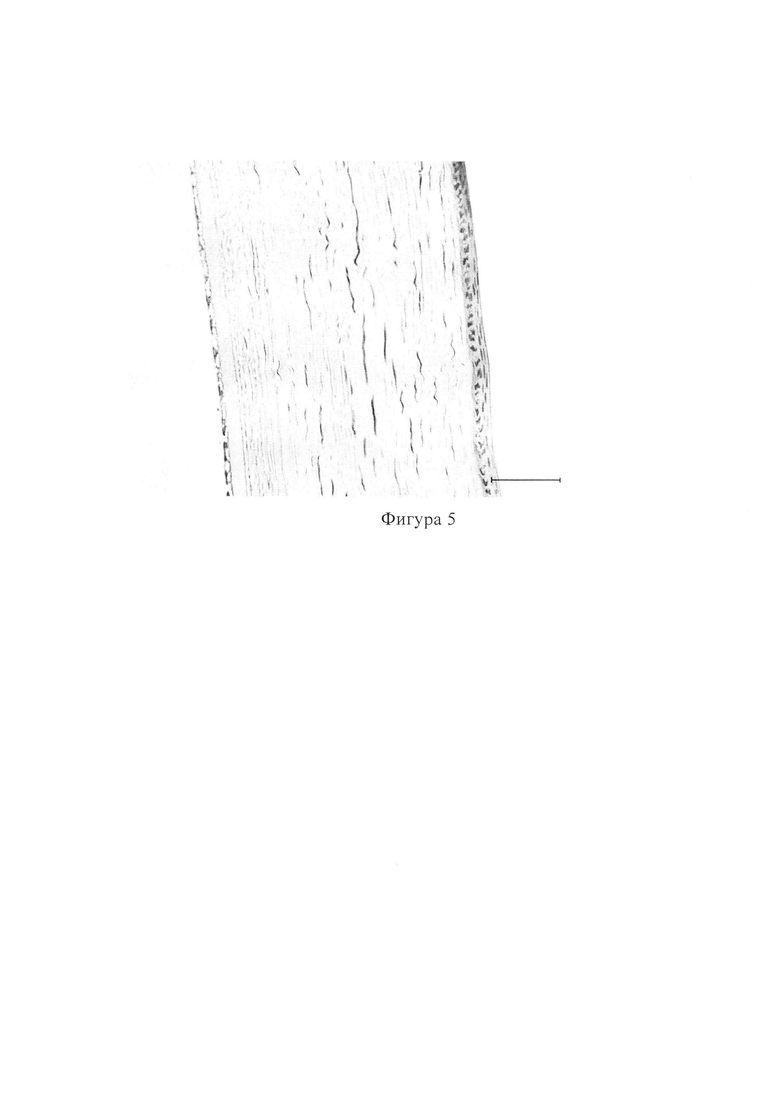
На 21-е сутки наблюдения в центральной зоне многослойный плоский неороговевающий эпителий составлял 4-5 слоев. Базальный слой составлял 1 ряд клеток с гиперхромными ядрами. Клетки переднего эпителия содержали уплощенные вытянутые клетки. В строме основного вещества явлений отека не выявлено, воспалительные явления отсутствовали (фиг. 5).
В контрольном левом глазу 5-го кролика тоже наблюдались вышеперечисленные изменения, за исключением некоторых участков, где наблюдалось относительно запоздалое закрытие дефекта, что подтверждается данными экспериментальных работ других авторов [Пронкин И.А. Разработка метода терапии рецидивирующих эпителиальных дефектов роговицы на основе «Протектора эпителия роговицы гелевого»: дис. … канд. мед. наук. - Москва, 2017. - 119 с.]. На глазу с моделью ожога без лечения дефект эпителия сохранялся 21 -е сутки наблюдения.

| название | год | авторы | номер документа |
|---|---|---|---|
| Глазная лекарственная пленка с метилурацилом, обладающая ранозаживляющим эффектом | 2020 |
|
RU2740924C1 |
| Глазная мазь на основе 6-метил-3-(тиетан-3-ил)урацила с ранозаживляющим эффектом | 2019 |
|
RU2705392C1 |
| Способ консервативного лечения адаптированных проникающих ранений роговицы | 2016 |
|
RU2644701C1 |
| Способ лечения ожогов глаз | 1990 |
|
SU1827225A1 |
| ПРИМЕНЕНИЕ НОВЫХ ОЛИГОПЕПТИДНЫХ ФРАГМЕНТОВ БЕЛКА S100b В КАЧЕСТВЕ СТИМУЛЯТОРОВ И МОДУЛЯТОРОВ РЕГЕНЕРАТОРНЫХ ПРОЦЕССОВ В РОГОВИЦЕ ГЛАЗА | 2011 |
|
RU2496454C2 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВ РОГОВИЦЫ | 2021 |
|
RU2766298C2 |
| ГЛАЗНАЯ ПЛЕНКА | 1997 |
|
RU2173178C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ КЕРАТОКОНУСА И ДРУГИХ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ РОГОВИЦЫ И ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ НА ЕГО ОСНОВЕ | 2013 |
|
RU2683651C2 |
| ГЛАЗНАЯ ПЛЕНКА | 2005 |
|
RU2286170C1 |
| ГЛАЗНАЯ ЛЕКАРСТВЕННАЯ ПЛЕНКА | 2009 |
|
RU2404779C1 |

Изобретение относится к области медицины, в частности к офтальмологии, и представляет собой глазную пленку. Пленка содержит в качестве биологически активного вещества 0,12 г 6-метил-3-(тиетан-3-ил)урацила, а в качестве пленкообразующей основы - 3,3 г поливинилового спирта в расчете на 100,0 мл воды. Использование изобретения позволяет повысить регенерацию роговичной ткани. 2 табл., 5 ил.
Глазная лекарственная пленка для повышения регенерации роговичной ткани, содержащая поливиниловый спирт в качестве пленкообразующей основы и биологически активное вещество, отличающаяся тем, что в качестве биологически активного вещества содержит 6-метил-3-(тиетан-3-ил)урацил при следующем содержании компонентов, г на 100,0 мл очищенной воды:
| ГЛАЗНАЯ ПЛЕНКА | 1997 |
|
RU2173178C2 |
| Глазная мазь на основе 6-метил-3-(тиетан-3-ил)урацила с ранозаживляющим эффектом | 2019 |
|
RU2705392C1 |
| ГЛАЗНАЯ МАЗЬ | 1994 |
|
RU2082434C1 |
| Мунасипова Д.А | |||
| "Синтез, свойства и биологическая активность тиетанпроизводных 6-метилурацила", Автореферат диссертации на соискание ученой степени кандидата химических наук, Уфа, 2014, 24 с. | |||
Авторы
Даты
2021-01-21—Публикация
2020-06-09—Подача