РОДСТВЕННАЯ ЗАЯВКА
[0001] Настоящая заявка испрашивает приоритет предварительной патентной заявки США 62/190350, поданной 9 июля 2015, содержание которой включено во всей полноте посредством ссылки.
Область техники, к которой относится настоящее изобретение
[0002] Настоящее изобретение относится к пиримидиновым соединениям, которые являются пригодными в качестве ингибиторов тирозинкиназы Брутона (BTK). Настоящее изобретение также относится к фармацевтически приемлемым композициям, содержащим соединения настоящего изобретения, и способам применения указанных композиций в лечении различных заболеваний.
Уровень техники настоящего изобретения
[0003] Протеинкиназы образуют одно из самых больших семейств человеческих ферментов и регулируют многие различные сигнальные процессы присоединением фосфатных групп к белкам (T. Hunter, Cell 1987 50:823-829). В частности, тирозинкиназы фосфорилируют белки по фенольному фрагменту остатков тирозина. Семейство тирозинкиназ включает члены, которые контролируют клеточный рост, миграцию и дифференциацию. Нарушенная киназная активность влечет за собой ряд заболеваний человека, включая рак, аутоиммунные и воспалительные заболевания. Поскольку протеинкиназы являются одними из ключевых регуляторов клеточной сигнализации, они обеспечивают мишень для регулирования клеточной функции низкомолекулярными ингибиторами киназ и, таким образом, обеспечивают хорошие лекарственные мишени. В добавление к лечению заболеваний, опосредованных киназами, селективные и эффективные ингибиторы киназной активности являются также пригодными для исследования процессов клеточной сигнализации и обнаружения других клеточных мишеней, представляющих терапевтический интерес.
[0004] Существует надежное доказательство того, что B-клетки играют ключевую роль в патогенезе аутоиммунного и/или воспалительного заболевания. Белковые терапевтические средства, которые снижают количество B клеток, такие как ритуксан, являются эффективными против воспалительных заболеваний, стимулируемых аутоантителами, таких как ревматоидный артрит (Rastetter et al. Annu Rev Med 2004 55:477). Следовательно, ингибиторы протеинкиназ, которые играют определенную роль в активации B-клеток, должны быть пригодными в качестве терапевтических средств для болезненных патологий, опосредованных B-клетками, таких как продуцирование аутоантител.
[0005] Передача сигнала через B-клеточный рецептор (BCR) контролирует ряд B-клеточных ответов, включая пролиферацию и дифференциацию клеток, продуцирующих зрелые антитела. BCR представляет собой ключевую регуляторную точку для B-клеточной активности, и нарушенная передача сигналов может вызывать разрегулированную B-клеточную пролиферацию и образование патогенных аутоантител, которые приводят к множеству аутоиммунных и/или воспалительных заболеваний. Тирозинкиназа Брутона (BTK) представляет собой не связанную с BCR киназу, которая близко расположена к мембране и сразу же ниже от BCR. Показано, что отсутствие BTK блокирует BCR передачу сигнала и, следовательно, ингибирование BTK может представлять собой пригодный терапевтический подход для блокировки болезненных процессов, опосредованных B-клетками. Кроме того, сообщалось, что BTK играет определенную роль в апоптозе (Islam and Smith Immunol. Rev. 2000, 178:49) и, таким образом, BTK ингибиторы могли бы быть полезными для лечения определенных B-клеточных лимфом и лейкемий (Feldhahn et al. J. Exp. Med. 2005 201:1837).
[0006] BTK представляет собой член Tec семейства тирозинкиназ, и показано, что она является важным регулятором раннего B-клеточного развития и активации и выживаемости зрелых B-клеток (Khan et al. Immunity, 1995. 3:283; Ellmeier et al. J. Exp. Med. 2000, 192:1611). Мутация BTK у людей приводит к агаммаглобулинемии, сцепленной с Х-хромосомой (XLA) (рассмотрена в Rosen et al. New Eng. J. Med. 1995 333:431 и Lindvall et al. Immunol. Rev. 2005, 203:200). Данные пациенты являются иммунокомпрометированными и проявляют нарушенное созревание B-клеток, сниженные концентрации иммуноглобулина и периферических B-клеток, ослабленные иммунные реакции, независящие от T-клеток, а также ослабленную мобилизацию кальция после BCR стимуляции.
[0007] Доказательства роли BTK в аутоиммунных и воспалительных заболеваниях также обеспечиваются моделями с BTK-дефицитными мышами. В предклинических мышиных моделях системной красной волчанки (SLE), BTK-дефицитные мыши показывают заметное облегчение прогрессирования заболевания. Кроме того, BTK-дефицитные мыши являются устойчивыми к коллаген-индуцированному артриту (Jansson and Holmdahl Clin. Exp. Immunol. 1993, 94:459). Селективный BTK ингибитор показывает зависящую от дозы эффективность в мышиных моделях артрита (Z. Pan et al., Chem. Med Chem. 2007, 2:58-61).
[0008] BTK также экспрессируется клетками, отличными от B-клеток, которые могут быть вовлечены в болезненные процессы. BTK представляет собой ключевой компонент Fc-гамма передачи сигналов в миелоидных клетках. Например, BTK экспрессируется тучными клетками, и BTK-дефицитные тучные клетки костного мозга показывают нарушенную антиген-зависимую дегрануляцию (Iwaki et al. J. Biol. Chem. 2005, 280:40261). Это показывает, что BTK может быть пригодным в лечении патологических реакций тучных клеток, таких как аллергия и астма. Также моноциты XLA пациентов, у которых отсутствует BTK активность, показывают ослабленное продуцирование TNF альфа после стимуляции (Horwood et al. J Exp Med 197:1603, 2003). Следовательно, воспаление, опосредованное TNF альфа, можно регулировать низкомолекулярными BTK ингибиторами.
Сущность настоящего изобретения
[0009] В настоящее время обнаружено, что соединения настоящего изобретения и их фармацевтически приемлемые композиции, являются эффективными в качестве ингибиторов BTK. Данные соединения имеют общую формулу I:
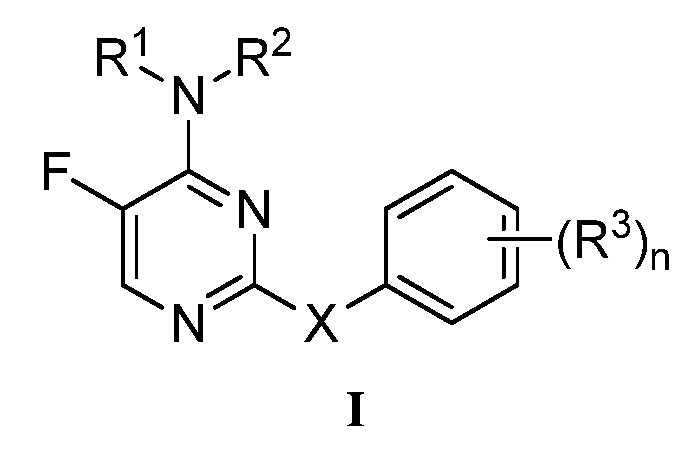
или их фармацевтически приемлемая соль, где каждый из R1, R2, R3, X, и n представляет собой, как определено и описано в вариантах осуществления настоящего изобретения.
[0010] Соединения настоящего изобретения и их фармацевтически приемлемые композиции являются пригодными для лечения ряда заболеваний, расстройств или состояний, связанных с BTK. Данные заболевания, расстройства или состояния включают заболевания, расстройства или состояния, описанные в настоящем изобретении.
Подробное описание определенных вариантов осуществления
1. Общее описание соединений настоящего изобретения
[0011] В определенных аспектах, настоящее изобретение обеспечивает ингибиторы BTK. В некоторых вариантах осуществления, данные соединения включают соединения формул, описанных в настоящем изобретении, или их фармацевтически приемлемые соли, где каждая переменная представляет собой, как определено и описано в настоящем изобретении.
2. Соединения и определения
[0012] Соединения настоящего изобретения включают соединения, описанные в общем выше, и они дополнительно проиллюстрированы классами, подклассами и типами, описанными в настоящем изобретении. Как применяют в настоящем изобретении, следующие определения следует применять, если не указано иначе. Для целей настоящего изобретения, химические элементы приводят согласно периодической таблице элементов, CAS версия, Handbook of Chemistry and Physics, 75th Ed. Кроме того, общие принципы органической химии описаны в ʺOrganic Chemistryʺ, Thomas Sorrell, University Science Books, Sausalito: 1999, и ʺMarch's Advanced Organic Chemistryʺ, 5th Ed., Ed.: Smith, M.B. и March, J., John Wiley & Sons, New York: 2001, полное содержание которых включено в настоящее изобретение с помощью ссылки.
[0013] Термин ʺалифатическийʺ или ʺалифатическая группаʺ, как применяют в настоящем изобретении, обозначает нормальную (т.е. неразветвленную) или разветвленную, замещенную или незамещенную углеводородную цепь, которая является полностью насыщенной или которая содержит один или более элементов ненасыщенности, или моноциклический углеводород или бициклический углеводород, который является полностью насыщенным или который содержит один или более элементов ненасыщенности, но который не является ароматическим (также называют ʺкарбоциклʺ ʺциклоалифатическийʺ или ʺциклоалкилʺ), который имеет одну точку присоединения к остатку молекулы. Если не указано иначе, алифатические группы содержат 1-6 алифатических атомов углерода. В некоторых вариантах осуществления, алифатические группы содержат 1-5 алифатических атомов углерода. В других вариантах осуществления, алифатические группы содержат 1-4 алифатических атомов углерода. В еще других вариантах осуществления, алифатические группы содержат 1-3 алифатических атомов углерода, и в еще других вариантах осуществления, алифатические группы содержат 1-2 алифатических атомов углерода. В некоторых вариантах осуществления, ʺциклоалифатическийʺ (или ʺкарбоциклʺ или ʺциклоалкилʺ) относится к моноциклическому C3-C6 углеводороду, который является полностью насыщенным или который содержит один или более элементов ненасыщенности, но который не является ароматическим, который имеет одну точку присоединения к остатку молекулы. Примерные алифатические группы представляют собой линейные или разветвленные, замещенные или незамещенные C1-C8 алкильные, C2-C8 алкенильные, C2-C8 алкинильные группы и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил.
[0014] Термин ʺнизший алкилʺ относится к C1-4 нормальной или разветвленной алкильной группе. Примеры низших алкильных групп представляют собой метил, этил, пропил, изопропил, бутил, изобутил, и трет-бутил.
[0015] Термин ʺнизший галогеналкилʺ относится к C1-4 нормальной или разветвленной алкильной группе, которая замещена одним или более атомами галогена.
[0016] Термин ʺгетероатомʺ обозначает один или более из кислорода, серы, азота или фосфора (включая любую окисленную форму азота, серы или фосфора; кватернизированную форму основного азота или; замещаемый азот гетероциклического кольца, например N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле)).
[0017] Термин ʺненасыщенныйʺ, как применяют в настоящем изобретении, обозначает то, что фрагмент содержит один или более элементов ненасыщенности.
[0018] Как применяют в настоящем изобретении, термин ʺдвухвалентная C1-8 (или C1-6) насыщенная или ненасыщенная, нормальная или разветвленная, углеводородная цепьʺ относится к двухвалентным алкиленовым, алкениленовым и алкиниленовым цепям, которые являются нормальными или разветвленными, как определено в настоящем изобретении.
[0019] Термин ʺалкиленʺ относится к двухвалентной алкильной группе. ʺАлкиленовая цепьʺ представляет собой полиметиленовую группу, т.е. -(CH2)n-, где n представляет собой положительное целое, предпочтительно 1-6, 1-4, 1-3, 1-2 или 2-3. Замещенная алкиленовая цепь представляет собой полиметиленовую группу, в которой один или более метиленовых атома водорода замещены заместителем. Подходящие заместители включают заместители, описанные ниже для замещенной алифатической группы.
[0020] Термин ʺалкениленʺ относится к двухвалентной алкенильной группе. Замещенная алкениленовая цепь представляет собой полиметиленовую группу, содержащую, по меньшей мере, одну двойную связь, в которой один или более атомов водорода замещены заместителем. Подходящие заместители включают заместители, описанные ниже для замещенной алифатической группы.
[0021] Термин ʺгалогенʺ обозначает F, Cl, Br или I.
[0022] Термин ʺарилʺ, применяемый отдельно или как часть большего фрагмента, как в ʺаралкилʺ, ʺаралкоксиʺ или ʺарилоксиалкилʺ, относится к моноциклическим и бициклическим кольцевым системам, содержащим в сумме от пяти до четырнадцати кольцевых члена, где, по меньшей мере, одно кольцо в системе является ароматическим, и где каждое кольцо в системе содержит 3-7 кольцевых члена. Термин ʺарилʺ применяют взаимозаменяемо с термином ʺарильное кольцоʺ. В определенных вариантах осуществления настоящего изобретения, ʺарилʺ относится к ароматической кольцевой системе. Примеры арильных групп представляют собой фенил, бифенил, нафтил, антрацил и подобные, которые необязательно содержат один или более заместителей. Также включенной в объем термина ʺарилʺ, как его применяют в настоящем изобретении, является группа, в которой ароматическое кольцо конденсировано с одним или более неароматическими кольцами, такими как инданил, фталимидил, нафтимидил, фенантридинил или тетрагидронафтил, и подобными.
[0023] Термины ʺгетероарилʺ и ʺгетероар-ʺ, применяемые отдельно или как часть большего фрагмента, напримернапример, ʺгетероаралкилʺ или ʺгетероаралкоксиʺ, относятся к группам, содержащим 5-10 кольцевых атомов, предпочтительно 5, 6 или 9 кольцевых атомов; содержащим 6, 10 или 14 π электронов, распределенных в циклической группе; и содержащим, в добавление к атомам углерода, от одного до пяти гетероатомов. Термин ʺгетероатомʺ относится к азоту, кислороду или сере, и включает любую окисленную форму азота или серы, и любую кватернизированную форму основного азота. Гетероарильные группы включают, без ограничения, тиенил, фуранил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил, изотиазолил, тиадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, индолизинил, пуринил, нафтиридинил и птеридинил. Термины ʺгетероарилʺ и ʺгетероар-ʺ, как применяют в настоящем изобретении, также включают группы, в которых гетероароматическое кольцо конденсировано с одним или более арильными, циклоалифатическими или гетероциклильными кольцами, где радикал или место присоединения находятся в гетероароматическом кольце. Неограничивающие примеры включают индолил, изоиндолил, бензотиенил, бензофуранил, дибензофуранил, индазолил, бензимидазолил, бензтиазолил, хинолил, изохинолил, циннолинил, фталазинил, хиназолинил, хиноксалинил, 4H-хинолизинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, тетрагидрохинолинил, тетрагидроизохинолинил и пиридо[2,3-b]- 1,4-оксазин-3(4H)-он. Гетероарильная группа необязательно является моно- или бициклической. Термин ʺгетероарилʺ применяют взаимозаменяемо с терминами ʺгетероарильное кольцоʺ, ʺгетероарильная группаʺ или ʺгетероароматическийʺ, причем любой из данных терминов включает кольца, которые являются необязательно замещенными. Термин ʺгетероаралкилʺ относится к алкильной группе, замещенной гетероарилом, где алкильная и гетероарильная части независимо являются необязательно замещенными.
[0024] Как применяют в настоящем изобретении, термины ʺгетероциклʺ, ʺгетероциклилʺ, ʺгетероциклический радикалʺ и ʺгетероциклическое кольцоʺ применяют взаимозаменяемо, и они относятся к стабильной 5-7-членной моноциклической или 7-10-членной бициклической гетероциклической группе, которая является или насыщенной или частично ненасыщенной, и содержащей, в добавление к атомам углерода, один или более, предпочтительно от одного до четырех, гетероатомов, как определено выше. При применении со ссылкой на кольцевой атом гетероцикла, термин ʺазотʺ включает замещенный азот. В качестве примера, в насыщенном или частично ненасыщенном кольце, содержащем 0-3 гетероатома, выбранные из кислорода, серы или азота, азот представляет собой N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или +NR (как в N-замещенном пирролидиниле).
[0025] Гетероциклическое кольцо может быть соединено с его боковой группой по любому гетероатому или атому углерода, что приводит в результате к стабильной структуре, и любой из кольцевых атомов может необязательно быть замещенным. Примеры данных насыщенных или частично ненасыщенных гетероциклических радикалов включают, без ограничения, тетрагидрофуранил, тетрагидротиофенил, пирролидинил, пиперидинил, пирролинил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, оксазолидинил, пиперазинил, диоксанил, диоксоланил, диазепенил, оксазепинил, тиазепенил, морфолинил и хинуклидинил. Термины ʺгетероциклʺ, ʺгетероциклилʺ, ʺгетероциклильное кольцоʺ, ʺгетероциклическая группаʺ, ʺгетероциклический фрагментʺ и ʺгетероциклический радикалʺ применяют взаимозаменяемо в настоящем изобретении, и они также включают группы, в которых гетероциклильное кольцо конденсировано с одним или более арильным, гетероарильным или циклоалифатическим кольцами, такие как индолинил, 3H-индолил, хроманил, фенантридинил или тетрагидрохинолинил, где радикал или место присоединения находится в гетероциклильном кольце. Гетероциклильная группа необязательно является моно- или бициклической. Термин ʺгетероциклилалкилʺ относится к алкильной группе, замещенной гетероциклилом, где алкильная и гетероциклильная части независимо являются необязательно замещенными.
[0026] Как применяют в настоящем изобретении, термин ʺчастично ненасыщенныйʺ относится к кольцевой группе, которая содержит, по меньшей мере, одну двойную или тройную связь. Предполагается, что термин ʺчастично ненасыщенныйʺ включает кольца, содержащие множество центров ненасыщенности, но не предполагается, что он включает арильные или гетероарильные группы, как определено в настоящем изобретении.
[0027] Как описано в настоящем изобретении, определенные соединения настоящего изобретения содержат ʺнеобязательно замещенныеʺ группы. В общем, термин ʺзамещенныйʺ, предшествует ли ему термин ʺнеобязательноʺ или нет, обозначает то, что один или более водородов обозначенной группы замещены подходящим заместителем. ʺЗамещенныйʺ применяют к одному или более водородам, которые явно выражены или подразумеваются из структуры (например, 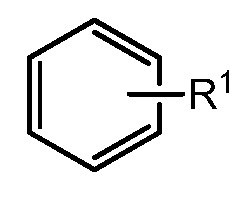 относится, по меньшей мере, к
относится, по меньшей мере, к 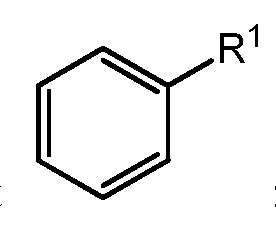 ; и
; и 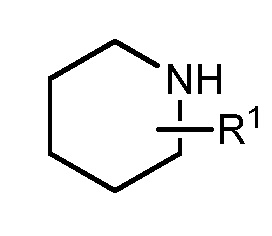 относится, по меньшей мере, к
относится, по меньшей мере, к 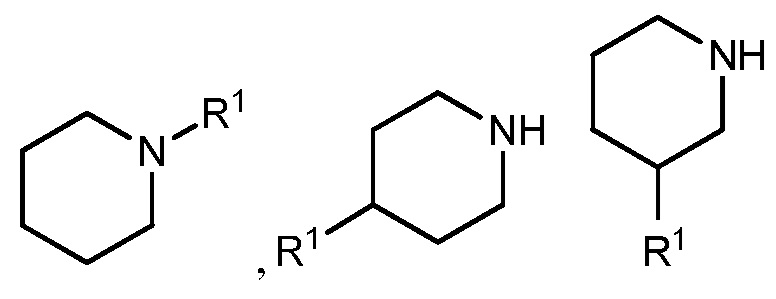 или
или 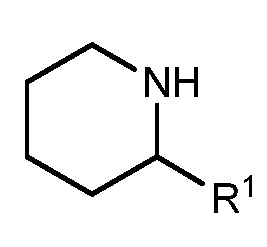 . Если не указано иначе, ʺнеобязательно замещеннаяʺ группа содержит подходящий заместитель при каждом замещаемом положении группы, и когда более одного положения в любой указанной структуре замещают более чем одним заместителем, выбранным из указанной группы, заместитель является или одинаковым или отличным в каждом положении. Комбинации заместителей, предусмотренные настоящим изобретением, предпочтительно являются комбинациями, которые приводят в результате к образованию стабильных или химически возможных соединений. Термин ʺстабильныйʺ, как применяют в настоящем изобретении, относится к соединениям, которые по существу не изменяются при воздействии условий, обеспечивающих их получение, обнаружение, и, в определенных вариантах осуществления, их извлечение, очистку и применение для одной или более из целей, описанных в настоящем изобретении.
. Если не указано иначе, ʺнеобязательно замещеннаяʺ группа содержит подходящий заместитель при каждом замещаемом положении группы, и когда более одного положения в любой указанной структуре замещают более чем одним заместителем, выбранным из указанной группы, заместитель является или одинаковым или отличным в каждом положении. Комбинации заместителей, предусмотренные настоящим изобретением, предпочтительно являются комбинациями, которые приводят в результате к образованию стабильных или химически возможных соединений. Термин ʺстабильныйʺ, как применяют в настоящем изобретении, относится к соединениям, которые по существу не изменяются при воздействии условий, обеспечивающих их получение, обнаружение, и, в определенных вариантах осуществления, их извлечение, очистку и применение для одной или более из целей, описанных в настоящем изобретении.
[0028] Подходящие моновалентные заместители по замещаемому атому углерода ʺнеобязательно замещеннойʺ группы независимо представляют собой дейтерий; галоген; -(CH2)0-4R°; -(CH2)0-4OR°; -O(CH2)0-4R°, -O- (CH2)0-4C(O)OR°; -(CH2)0-4CH(OR°)2; -(CH2)0-4SR°; -(CH2)0-4Ph, которые необязательно замещены R°; -(CH2)0-4O(CH2)0-1Ph, который необязательно замещен R°; -CH=CHPh, который необязательно замещен R°; -(CH2)0-4O(CH2)0-1-пиридил, который необязательно замещен R°; -NO2; -CN; -N3; (CH2)0-4N(R°)2; -(CH2)0-4N(R°)C(O)R°; -N(R°)C(S)R°; -(CH2)0-4N(R°)C(O)NR°2; N(R°)C(S)NR°2; -(CH2)0-4N(R°)C(O)OR°; -N(R°)N(R°)C(O)R°; N(R°)N(R°)C(O)NR°2; N(R°)N(R°)C(O)OR°; -(CH2)0-4C(O)R°; -C(S)R°; -(CH2)0-4C(O)OR°; -(CH2)0-4C(O)SR°; (CH2)0-4C(O)OSiR°3; -(CH2)0-4OC(O)R°; -OC(O)(CH2)0-4SR°, SC(S)SR°; -(CH2)0-4SC(O)R°; -(CH2)0-4C(O)NR°2; -C(S)NR°2; -C(S)SR°; -SC(S)SR°, (CH2)0-4OC(O)NR°2; C(O)N(OR°)R°; -C(O)C(O)R°; -C(O)CH2C(O)R°; -C(NOR°)R°; (CH2)0-4SSR°; -(CH2)0-4S(O)2R°; -(CH2)0-4S(O)2OR°; -(CH2)0-4OS(O)2R°; -S(O)2NR°2; (CH2)0-4S(O)R°; N(R°)S(O)2NR°2; -N(R°)S(O)2R°; -N(OR°)R°; -C(NH)NR°2; -P(O)2R°; P(O)R°2; OP(O)R°2; -OP(O)(OR°)2; SiR°3; -(C1-4 нормальный или разветвленный алкилен)O-N(R°)2; или -(C1-4 нормальный или разветвленный алкилен)C(O)O-N(R°)2, где каждый R° необязательно замещен, как определено ниже, и независимо представляет собой водород, C1-6 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph, -CH2-(5-6 членное гетероарильное кольцо), или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы, или, несмотря на определение выше, два независимых возникновения R°, взятые вместе с их промежуточным атомом (атомами), образуют 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы, которое является необязательно замещенным, как определено ниже.
[0029] Подходящие моновалентные заместители по R° (или кольцо, образованное взятием двух независимых появлений R° вместе с промежуточными атомами) независимо представляют собой дейтерий, галоген, -(CH2)0-2Rλ, -(галогенRλ), -(CH2)0-2OH, -(CH2)0-2ORλ, -(CH2)0-2CH(ORλ)2; O(галогенRλ), -CN, -N3, -(CH2)0-2C(O)Rλ, -(CH2)0-2C(O)OH, -(CH2)0-2C(O)ORλ, -(CH2)0-2SRλ, -(CH2)0-2SH, -(CH2)0-2NH2, -(CH2)0-2NHRλ, -(CH2)0-2NRλ2, -NO2, -SiRλ3, -OSiRλ3, C(O)SRλ, -(C1-4 нормальный или разветвленный алкилен)C(O)ORλ или -SSRλ где каждый Rλ является незамещенным или, когда ему предшествует ʺгалогенʺ, замещенным только одним или более галогенами, и независимо выбран из C1-4 алифатической группы, -CH2Ph, -O(CH2)0-1Ph или 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатома, независимо выбранные из азота, кислорода или серы. Подходящие двухвалентные заместители по насыщенному атому углерода R° включают =O и =S.
[0030] Подходящие двухвалентные заместители при насыщенном атоме углерода ʺнеобязательно замещеннойʺ группы включают следующие: =O, =S, =NNR*2, =NNHC(O)R*, =NNHC(O)OR*, =NNHS(O)2R*, =NR*, =NOR*, -O(C(R*2))2-3O- или -S(C(R*2))2-3S-, где каждое независимое появление R* выбирают из водорода, C1-6 алифатической группы, которая замещена, как определено ниже, или незамещенного 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатома, независимо выбранные из азота, кислорода или серы. Подходящие двухвалентные заместители, которые соединены с вицинальными замещаемыми углеродами ʺнеобязательно замещеннойʺ группы включают: -O(CR*2)2-3O-, где каждое независимое появление R* выбирают из водорода, C1-6 алифатической группы, которая необязательно замещена, как определено ниже, или незамещенного 5-6-членного насыщенного, частично ненасыщенного или арильного кольца, содержащего 0-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0031] Подходящие заместители по алифатической группе R* включают галоген, -Rλ, (галогенRλ), OH, -ORλ, -O(галогенRλ), -CN, -C(O)OH, -C(O)ORλ, -NH2, -NHRλ, -NRλ2, или -NO2, где каждый Rλ является незамещенным или, когда ему предшествует ʺгалогенʺ, является замещенным только одним или более галогенами, и независимо представляет собой C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph, или 5-6-членной насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0032] Подходящие заместители по замещаемому азоту ʺнеобязательно замещеннойʺ группы включают -R†, -NR†2, -C(O)R†, -C(O)OR†, -C(O)C(O)R†, -C(O)CH2C(O)R†, -S(O)2R†, S(O)2NR†2, -C(S)NR†2, -C(NH)NR†2, или -N(R†)S(O)2R†; где каждый R† независимо представляет собой водород, C1-6 алифатическую группу, которая является необязательно замещенной, как определено ниже, незамещенный -OPh, или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы, или, несмотря на определение выше, два независимых появления R†, взятые вместе с их промежуточным атомом (атомами), образуют незамещенное 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0033] Подходящие заместители по алифатической группе R† независимо представляют собой галоген, -Rλ, (галогенRλ), -OH, -ORλ, -O(галогенRλ), -CN, -C(O)OH, -C(O)ORλ, -NH2, -NHRλ, -NRλ2, или NO2, где каждый Rλ является незамещенным или, когда ему предшествует ʺгалогенʺ, является замещенным только одним или более галогенами, и независимо представляет собой C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0034] В определенных вариантах осуществления, термины ʺнеобязательно замещенныйʺ, ʺнеобязательно замещенный алкил,ʺ ʺнеобязательно замещенный алкенил,ʺ ʺнеобязательно замещенный алкинилʺ, ʺнеобязательно замещенный карбоциклил,ʺ ʺнеобязательно замещенный арилʺ, "необязательно замещенный гетероарил", ʺнеобязательно замещенный гетероциклилʺ и любая другая необязательно замещенная группа, как применяют в настоящем изобретении, относятся к группам, которые являются замещенными или незамещенными независимыми замещениями одного, двух, или трех или более атомов водорода в них стандартными заместителями, включая, но не ограничиваясь:
-F, -Cl, -Br, -I, дейтерий,
-OH, защищенный гидрокси, алкокси, оксо, тиооксо,
-NO2, -CN, CF3, N3,
-NH2, защищенный амино, -NH алкил, -NH алкенил, -NH алкинил, -NH циклоалкил, -NH -арил, -NH -гетероарил, -NH -гетероциклил, -диалкиламино, -диариламино, -дигетероариламино,
-O-алкил, -O-алкенил, -O-алкинил, -O-циклоалкил, -O-арил, -O-гетероарил, -O-гетероциклил,
-C(O)-алкил, -C(O)-алкенил, -C(O)- алкинил, -C(O)-карбоциклил, -C(O)-арил, -C(O)-гетероарил, -C(O)-гетероциклил,
-CONH2, -CONH-алкил, -CONH-алкенил, -CONH-алкинил, -CONH-карбоциклил, -CONH-арил, -CONH-гетероарил, -CONH-гетероциклил,
-OCO2-алкил, -OCO2-алкенил, -OCO2-алкинил, -OCO2-карбоциклил, -OCO2-арил, -OCO2-гетероарил, -OCO2-гетероциклил, -OCONH2, -OCONH-алкил, -OCONH-алкенил, -OCONH-алкинил, -OCONH-карбоциклил, -OCONH-арил, -OCONH-гетероарил, -OCONH-гетероциклил,
-NHC(O)-алкил, -NHC(O)-алкенил, -NHC(O)-алкинил, -NHC(O)-карбоциклил, -NHC(O)-арил, -NHC(O)-гетероарил, -NHC(O)-гетероциклил, -NHCO2-алкил, -NHCO2-алкенил, -NHCO2-алкинил, -NHCO2-карбоциклил, -NHCO2-арил, -NHCO2-гетероарил, -NHCO2-гетероциклил, -NHC(O)NH2, -NHC(O)NH-алкил, -NHC(O)NH-алкенил, -NHC(O)NH-алкенил, -NHC(O)NH-карбоциклил, -NHC(O)NH-арил, -NHC(O)NH-гетероарил, -NHC(O)NH-гетероциклил, NHC(S)NH2, -NHC(S)NH-алкил, -NHC(S)NH-алкенил, -NHC(S)NH-алкинил, -NHC(S)NH-карбоциклил, -NHC(S)NH-арил, -NHC(S)NH-гетероарил, -NHC(S)NH-гетероциклил, -NHC(NH)NH2, -NHC(NH)NH-алкил, -NHC(NH)NH-алкенил, -NHC(NH)NH-алкенил, -NHC(NH)NH-карбоциклил, -NHC(NH)NH-арил, -NHC(NH)NH-гетероарил, -NHC(NH)NH-гетероциклил, -NHC(NH)-алкил, -NHC(NH)-алкенил, -NHC(NH)- алкенил, -NHC(NH)-карбоциклил, -NHC(NH)-арил, -NHC(NH)-гетероарил, -NHC(NH)-гетероциклил,
-C(NH)NH-алкил, -C(NH)NH-алкенил, -C(NH)NH-алкинил, -C(NH)NH-карбоциклил, -C(NH)NH-арил, -C(NH)NH-гетероарил, -C(NH)NH-гетероциклил,
-S(O)-алкил, -S(O)-алкенил, -S(O)-алкинил, -S(O)-карбоциклил,-S(O)-арил,-S(O)-гетероарил,-S(O)-гетероциклил -SO2NH2, -SO2NH-алкил, -SO2NH-алкенил, -SO2NH-алкинил, -SO2NH-карбоциклил, -SO2NH-арил, -SO2NH-гетероарил, -SO2NH-гетероциклил,
-NHSO2-алкил, -NHSO2-алкенил,-NHSO2-алкинил, -NHSO2-карбоциклил, -NHSO2-арил, -NHSO2-гетероарил, -NHSO2-гетероциклил,
-CH2NH2, -CH2SO2CH3,
-моно-, ди- или триалкилсилил,
-алкил, -алкенил, -алкинил, -арил, -арилалкил, -гетероарил, -гетероарилалкил, -гетероциклоалкил, -циклоалкил, -карбоциклил, -гетероциклил, полиалкоксиалкил, полиалкокси, -метоксиметокси, -метоксиэтокси, -SH, -S-алкил, -S-алкенил, -S-алкинил, -S-карбоциклил, -S-арил, -S-гетероарил, -S-гетероциклил или метилтиометил.
[0035] Как применяют в настоящем изобретении, термин ʺфармацевтически приемлемая сольʺ относится к солям, которые являются, по результатам тщательной медицинской оценки, подходящими для применения в контакте с тканями человека и низших животных без неспецифической токсичности, раздражения, аллергической реакции и подобных, и обладают соразмерным соотношением риск/польза. Фармацевтически приемлемые соли являются хорошо известными в данной области техники. Например, S. M. Berge et al., подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1977, 66, 1-19, включенной в настоящее изобретение с помощью ссылки. Фармацевтически приемлемые соли соединений настоящего изобретения включают соли, полученные из подходящих неорганических и органических кислот и оснований. Примеры фармацевтически приемлемых нетоксичных солей присоединения кислоты представляют собой соли аминогруппы, образованные с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с применением других способов, используемых в данной области, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипатную, альгинатную, аскорбатную, аспартатную, бензолсульфонатную, бензоатную, бисульфатную, боратную, бутиратную, камфаратную, камфорсульфонатную, цитратную, циклопентанпропионатную, диглюконатную, додецилсульфатную, этансульфонатную, формиатную, фумаратную, глюкогептонатную, глицерофосфатную, глюконатную, гемисульфатную, гептаноатную, гексаноатную, гидроиодидную, 2-гидроксиэтансульфонатную, лактобионатную, лактатную, лауратную, лаурилсульфатную, малатную, малеатную, малонатную, метансульфонатную, 2-нафталинсульфонатную, никотинатную, нитратную, олеатную, оксалатную, пальмитатную, памоатную, пектинатную, персульфатную, 3-фенилпропионатную, фосфатную, пивалатную, пропионатную, стеаратную, сукцинатную, сульфатную, тартратную, тиоцианатную, п-толуолсульфонатную, ундеканоатную, валератную соли и подобные.
[0036] Соли, полученные из подходящих оснований, включают соли щелочных металлов, щелочноземельных металлов, аммония и N+(C1-4алкильные)4 соли. Типичные примеры солей щелочных и щелочноземельных металлов включают натриевую, литиевую, калиевую, кальциевую, магниевую и подобные. Дополнительные фармацевтически приемлемые соли содержат, при необходимости, нетоксичные аммониевые, четвертичные аммониевые и аминовые катионы, образованные, применяя противоионы, такие как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
[0037] Если не указано иначе, также предполагается, что структуры, показанные в настоящем изобретении, включают все изомерные (например, энантиомерные, диастереомерные и геометрические (или конформационные)) формы структуры; например, R и S конфигурации для каждого асимметрического центра, Z и E изомеры по двойной связи, и Z и E конформационные изомеры. Следовательно, единичные стереохимические изомеры, а также энантиомерные, диастереомерные и геометрические (или конформационные) смеси настоящих соединений включены в объем настоящего изобретения. Если не указано иначе, все таутомерные формы соединений настоящего изобретения включены в объем настоящего изобретения.
[0038] Кроме того, если не указано иначе, также предполагается, что структуры, показанные в настоящем изобретении, включают соединения, которые отличаются только наличием одного или более изотопно обогащенных атомов. Например, соединения, имеющие настоящие структуры, содержащие замену водорода дейтерием или тритием или замену углерода 13C- или 14C-обогащенным углеродом, включены в объем настоящего изобретения. В некоторых вариантах осуществления, группа содержит один или более атомов дейтерия.
[0039] Более того, предполагается, что соединение формулы I включает его изотопно-меченные формы. Изотопно-меченная форма соединения формулы I является идентичной данному соединению, помимо того, что один или более атомов соединения замещены атомом или атомами, имеющими атомную массу или массовое число, которое отличается от атомной массы или атомного числа атома, который обычно встречается в природе. Примеры изотопов, которые имеются в продаже и которые можно ввести в соединение формулы I хорошо известными способами, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, например, 2H, 3H, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F и 36Cl, соответственно. Соединение формулы I, его пролекарство или фармацевтически приемлемая соль любого из них содержит один или более приведенных выше изотопов, и/или другие изотопы других атомов предполагаются частью настоящего изобретения. Изотопно-меченное соединение формулы I можно применять рядом полезных способов. Например, изотопно-меченное соединение формулы I, в которое введен, например, радиоизотоп, такой как 3H или 14C, является пригодным для анализов распределения лекарственного средства и/или субстрата в тканях. Данные радиоизотопы, т.е. тритий (3H) и углерод-14 (14C), являются особенно предпочтительными, благодаря простоте получения и превосходной детектируемости. Введение более тяжелых изотопов, например, дейтерия (2H), в соединение формулы I обладает терапевтическими преимуществами, благодаря большей метаболической стабильности данного изотопно-меченного соединения. Большая метаболическая стабильность непосредственно обуславливает повышенное время полужизни in vivo или меньшие дозы, которые, в большинстве обстоятельств, могло бы представлять предпочтительный вариант настоящего изобретения. Изотопно-меченное соединение формулы I можно обычно получить осуществлением способов, описанных на схемах получения и родственном описании, в части с примерами и в части получения в настоящем тексте, заменяя изотопно-немеченый реагент легко доступным изотопно-меченным реагентом.
[0040] Дейтерий (2H) можно также вводить в соединение формулы I с целью изменения окислительного метаболизма соединения посредством первичного кинетического изотопного эффекта. Первичный кинетический изотопный эффект представляет собой изменение скорости химической реакции, которое является результатом замены изотопного ядра, что, в свою очередь, вызывается изменением энергий основного состояния, необходимых для образования водородных связей после данного изотопного обмена. Обмен на более тяжелый изотоп обычно приводит в результате к снижению энергии основного состояния для химической связи и, таким образом, вызывает снижение скорости ограничивающего скорость разрушения связи. Если разрушение связи протекает в или вблизи области седловой точки вдоль координаты реакции со многими продуктами, соотношения распределения продуктов можно существенно изменять. Разъяснение: если дейтерий соединен с атомом углерода в необмениваемом положении, разница в скоростях kM/kD=2-7 является типичной. Если данную разницу в скоростях успешно применить для соединения формулы I, которое подвержено окислению, профиль данного соединения in vivo можно резко изменить и получить в результате улучшенные фармакокинетические свойства.
[0041] При обнаружении и разработке терапевтических агентов, специалист в данной области техники способен оптимизировать фармакокинетические параметры, сохраняя требуемые in vitro свойства. Имеются основания полагать, что многие соединения с плохими фармакокинетическими профилями подвержены окислительному метаболизму. Доступные в настоящее время in vitro анализы микросомы печени дают ценную информацию о протекании окислительного метаболизма данного типа, что, в свою очередь, обеспечивает рациональный дизайн дейтерированных соединений формулы I с повышенной стабильностью за счет устойчивости к данному окислительному метаболизму. Посредством этого получают заметное улучшение фармакокинетических профилей соединений формулы I, и его можно выразить количество по величине увеличения времени полужизни in vivo (t/2), концентрации при максимальном терапевтическом эффекте (Cmax), площади под кривой зависимости эффекта от дозы (AUC), и F; и в терминах сниженного клиренса, дозы и стоимости материалов.
[0042] Последующее предназначено для иллюстрации приведенного выше: соединение формулы I, которое имеет большое количество потенциальных мест атаки для окислительного метаболизма, например, бензиловые атомы водорода и атомы водорода, соединенные с атомом азота, получают в виде серии аналогов, в которых различные комбинации атомов водорода заменяют на атомы дейтерия, так что некоторые, большинство или все из данных атомов водорода замещены атомами дейтерия. Определение полужизни обеспечивает подходящее и точное определение степени, в которой достигается увеличение устойчивости к окислительному метаболизму. Таким образом, определили, что время полужизни исходного соединения можно увеличить вплоть до 100% в результате обмена водорода на дейтерий данного типа.
[0043] Обмен водорода на дейтерий в соединении формулы I можно также применять для получения подходящей модификации спектра метаболитов исходного соединения для того, чтобы снизить или устранить нежелательные токсичные метаболиты. Например, если токсичный метаболит возникает за счет окислительного расщепления связи углерод-водород (C-H), разумно предположить, что дейтерированный аналог будет значительно снижать или устранять продуцирование нежелательного метаболита, даже если частичное окисление не является определяющей скорость стадией. Дополнительную информацию об уровне техники относительно обмена водорода на дейтерий можно найти, например, в Hanzlik et al., J. Org. Chem. 55, 3992-3997, 1990, Reider et al., J. Org. Chem. 52, 3326-3334, 1987, Foster, Adv. Drug Res. 14, 1-40, 1985, Gillette et al, Biochemistry 33(10) 2927-2937, 1994, и Jarman et al. Carcinogenesis 16(4), 683-688, 1993.
[0044] Как применяют в настоящем изобретении, термин ʺмодуляторʺ определяют как соединение, которое связывается с и/или ингибирует мишень с измеримым сродством. В определенных вариантах осуществления, модулятор имеет IC50 и/или константу связывания меньше приблизительно 50 мкМ, меньше чем приблизительно 5 мкМ, меньше чем приблизительно 1 мкМ, меньше чем приблизительно 500 нМ, меньше чем приблизительно 100 нМ или меньше чем приблизительно 10 нМ.
[0045] Термины ʺизмеримое сродствоʺ и ʺизмеримо ингибируетʺ, как применяют в настоящем изобретении, обозначает измеримое изменение BTK активности между образцом, содержащим соединение настоящего изобретения или его композицию, и BTK, и эквивалентным образцом, содержащим BTK, в отсутствии указанного соединения или его комбинации.
[0046] Комбинации заместителей и переменных, предполагаемые настоящим изобретением, представляют собой только те заместители и переменные, которые приводят в результате к образованию стабильных соединений. Термин ʺстабильныйʺ, как применяют в настоящем изобретении, относится к соединениям, которые обладают стабильностью, достаточной для обеспечения получения и которые сохраняют цельность соединения в течение достаточного периода времени, чтобы они были пригодными для целей, подробно приведенных в настоящем изобретении (например, терапевтического или профилактического введения субъекту).
[0047] Перечисление списка химических групп в любом определении переменной в настоящем изобретении включает определения данной переменной в виде любой одной группы или комбинации перечисленных групп. Перечисление варианта осуществления для переменной в настоящем изобретении включает данный вариант осуществления как любой один вариант осуществления или в комбинации с любыми другими вариантами осуществления или их частями.
3. Описание примерных соединений
[0048] Согласно одному аспекту, настоящее изобретение обеспечивает соединение формулы I,
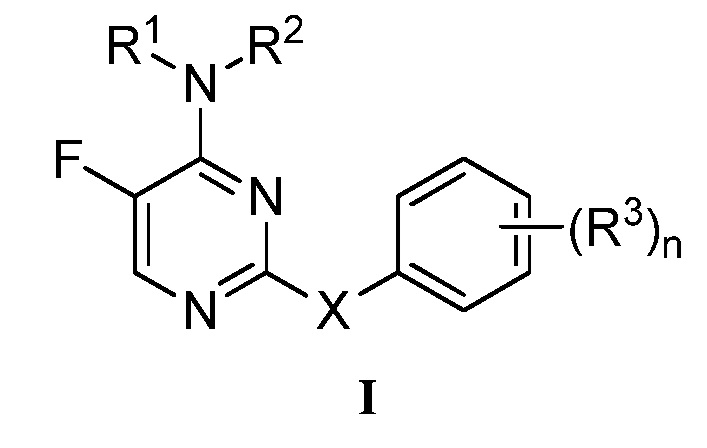
или его фармацевтически приемлемую соль, где:
R1 представляет собой C1-6 алифатическую группу, C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным;
R2 представляет собой водород, C1-6 алифатическую группу, C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным; или
R1 и R2, взятые вместе с атомом, с которым они соединены, образуют 3-7 членное гетероциклическое кольцо, содержащее 1 азот и 0-3 других гетероатома, независимо выбранные из азота, кислорода или серы; или 6-10 членное конденсированное или спиро бициклическое гетероциклическое кольцо, содержащее 1 азот и 0-3 других гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным;
где R1 или кольцо, образованное R1 и R2, замещено
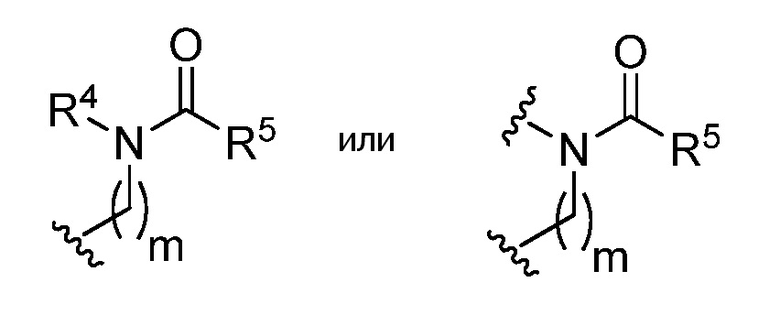
R4 представляет собой водород, C1-6 алифатическую группу, C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным;
каждый R5 независимо представляет собой C1-6 алкил, C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным;
m равен 0 или 1;
X представляет собой O, S, SO2, SO, -NRC(O), -NRSO2 или N(R);
каждый R3 независимо представляет собой -R, галоген, -OR, -SR, -CN, -NO2, SO2R, SOR, C(O)R, CO2R, C(O)N(R)2, -NRC(O)R, NRC(O)N(R)2, -NRSO2R или -N(R)2;
каждый R независимо представляет собой водород, C1-6 алифатическую группу, C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным; или
две R группы при одном атоме берут вместе с атомом, с которым они соединены, получая C5-10 арил, 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо, 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы, или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным; и
n равен 1, 2 или 3.
[0049] В определенных вариантах осуществления, R1 представляет собой необязательно замещенную C1-6 алифатическую группу. В определенных вариантах осуществления, R1 представляет собой необязательно замещенный C5-10 арил. В определенных вариантах осуществления, R1 представляет собой необязательно замещенное 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо. В определенных вариантах осуществления, R1 представляет собой необязательно замещенное 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы. В определенных вариантах осуществления, R1 представляет собой необязательно замещенное 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0050] В определенных вариантах осуществления, R1 представляет собой метил, этил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, нормальный или разветвленный пентил, или нормальный или разветвленный гексил; каждый из которых является необязательно замещенным. В определенных вариантах осуществления, R1 представляет собой замещенный метил.
[0051] В определенных вариантах осуществления, R1 представляет собой 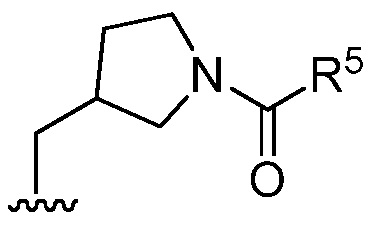 .
.
[0052] В определенных вариантах осуществления, R1 представляет собой фенил, нафтил, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, адамантил, циклооктил, [3.3.0]бициклооктанил, [4.3.0]бициклононанил, [4.4.0]бициклодеканил, [2.2.2]бициклооктанил, флуоренил, инданил, тетрагидронафтил, акридинил, азоцинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, бензимидазолинил, карбазолил, NH-карбазолил, карболинил, хроманил, хроменил, циннолинил, декагидрохинолинил, 2H,6H 1,5,2-дитиазинил, дигидрофуро[2,3-b] тетрагидрофуран, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1H-индазолил, индоленил, индолинил, индолизинил, индолил, 3H-индолил, изоиндолинил, изоиндоленил, изобензофуранил, изохроманил, изоиндазолил, изоиндолинил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил; 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, оксазолидинил, оксазолил, оксазолидинил, пиримидинил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатиинил, феноксазинил, фталазинил, пиперазинил, пиперидинил, птеридинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазол, пиридоимидазол, пиридотиазол, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, 2H-пирролил, пирролил, хиназолинил, хинолинил, 4H-хинолизинил, хиноксалинил, хинуклидинил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, 6H-1,2,5-тиадиазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, тиазолил, тиенил, тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиофенил, триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил, оксетанил, азетидинил или ксантенил; каждый из которых является необязательно замещенным.
[0053] В определенных вариантах осуществления, R1 представляет собой фенил, циклопентил или циклогексил.
[0054] В определенных вариантах осуществления, R1 представляет собой
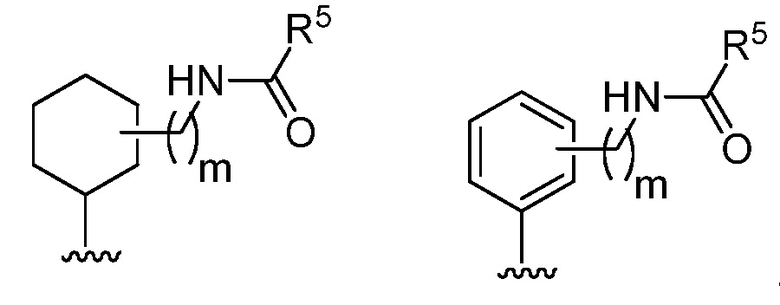
[0055] В определенных вариантах осуществления, R1 представляет собой
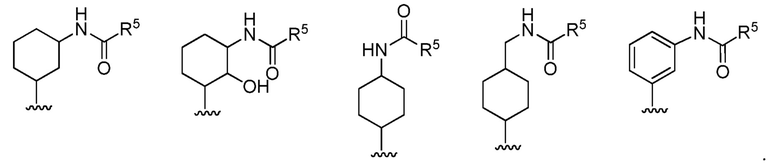
[0056] В определенных вариантах осуществления, R2 представляет собой водород.
[0057] В определенных вариантах осуществления, R2 представляет собой необязательно замещенную C1-6 алифатическую группу. В определенных вариантах осуществления, R2 представляет собой необязательно замещенный C3-10 арил. В определенных вариантах осуществления, R2 представляет собой необязательно замещенное 3-8 членное насыщенное или частично ненасыщенное карбоциклическое кольцо. В определенных вариантах осуществления, R2 представляет собой необязательно замещенное 3-7 членное гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы. В определенных вариантах осуществления, R2 представляет собой необязательно замещенное 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы.
[0058] В определенных вариантах осуществления, R2 представляет собой водород.
[0059] В определенных вариантах осуществления, R2 представляет собой метил, этил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, нормальный или разветвленный пентил, или нормальный или разветвленный гексил; каждый из которых является необязательно замещенным.
[0060] В определенных вариантах осуществления, R2 представляет собой фенил, нафтил, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, адамантил, циклооктил, [3.3.0]бициклооктанил, [4.3.0]бициклононанил, [4.4.0]бициклодеканил, [2.2.2]бициклооктанил, флуоренил, инданил, тетрагидронафтил, акридинил, азоцинил, бензимидазолил, бензофуранил, бензотиофуранил, бензотиофенил, бензоксазолил, бензтиазолил, бензтриазолил, бензтетразолил, бензизоксазолил, бензизотиазолил, бензимидазолинил, карбазолил, NH-карбазолил, карболинил, хроманил, хроменил, циннолинил, декагидрохинолинил, 2H,6H-1,5,2-дитиазинил, дигидрофуро[2,3-b]тетрагидрофуран, фуранил, фуразанил, имидазолидинил, имидазолинил, имидазолил, 1H индазолил, индоленил, индолинил, индолизинил, индолил, 3H-индолил, изоиндолинил, изоиндоленил, изобензофуранил, изохроманил, изоиндазолил, изоиндолинил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, морфолинил, нафтиридинил, октагидроизохинолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил; 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, оксазолидинил, оксазолил, оксазолидинил, пиримидинил, фенантридинил, фенантролинил, феназинил, фенотиазинил, феноксатиинил, феноксазинил, фталазинил, пиперазинил, пиперидинил, птеридинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридооксазол, пиридомиидазол, пиридотиазол, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, 2H-пирролил, пирролил, хиназолинил, хинолинил, 4H-хинолизинил, хиноксалинил, хинуклидинил, тетрагидрофуранил, тетрагидроизохинолинил, тетрагидрохинолинил, 6H-1,2,5-тиадиазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, тиантренил, тиазолил, тиенил, тиенотиазолил, тиенооксазолил, тиеноимидазолил, тиофенил, триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил, оксетанил, азетидинил, или ксантенил; каждый из которых является необязательно замещенным.
[0061] В определенных вариантах осуществления, R1 и R2, взятые вместе с атомом, с которым они соединены, образуют 3-7 членное гетероциклическое кольцо, содержащее 1 азот и 0-3 других гетероатома, независимо выбранные из азота, кислорода или серы; или 6-10 членное конденсированное или спиро бициклическое гетероциклическое кольцо, содержащее 1 азот и 0-3 других гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным.
[0062] В определенных вариантах осуществления, кольцо, образованное R1 и R2, представляет собой моноциклический пирролидин, бициклической конденсированный пирролидин или бициклический спиро-пирролидин; или кольцо, образованное R1 и R2, представляет собой моноциклический пиперидин, бициклический конденсированный пиперидин или бициклический спиро-пиперидин.
[0063] В определенных вариантах осуществления, кольцо, образованное R1 и R2, представляет собой
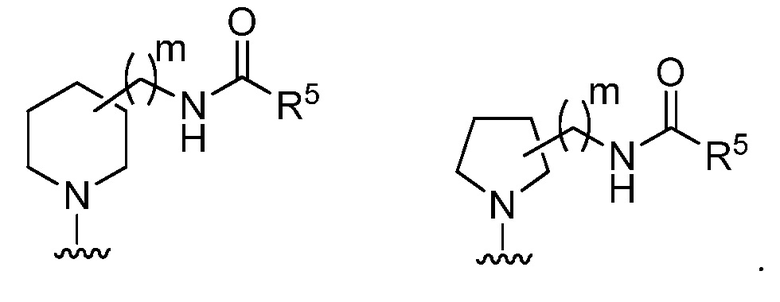
[0064] В определенных вариантах осуществления, кольцо, образованное R1 и R2, представляет собой
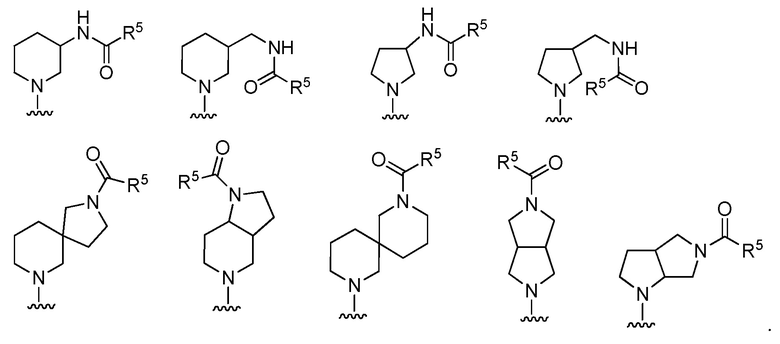
[0065] В определенных вариантах осуществления, X представляет собой N(R). В определенных вариантах осуществления, X представляет собой NH.
[0066] В определенных вариантах осуществления, каждый R3 независимо представляет собой H.
[0067] В определенных вариантах осуществления, каждый R3 независимо представляет собой -R, галоген, -OR, -SR, -CN, -NO2, SO2R, SOR, C(O)R, CO2R, C(O)N(R)2, -NRC(O)R, NRC(O)N(R)2, -NRSO2R или -N(R)2.
[0068] В определенных вариантах осуществления, каждый R3 независимо представляет собой -OR или C1-6 алифатическую группу.
[0069] В определенных вариантах осуществления, каждый R3 независимо представляет собой 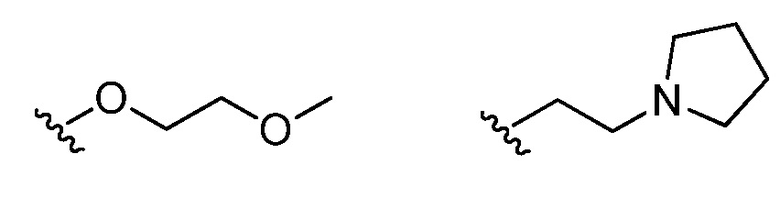 .
.
[0070] В определенных вариантах осуществления, каждый R5 независимо представляет собой C1-6 алкил, C5-10 арил или 5-6 членное моноциклическое гетероарильное кольцо, содержащее 1-4 гетероатома, независимо выбранные из азота, кислорода или серы; каждое из которых является необязательно замещенным.
[0071] В определенных вариантах осуществления, каждый R5 независимо представляет собой
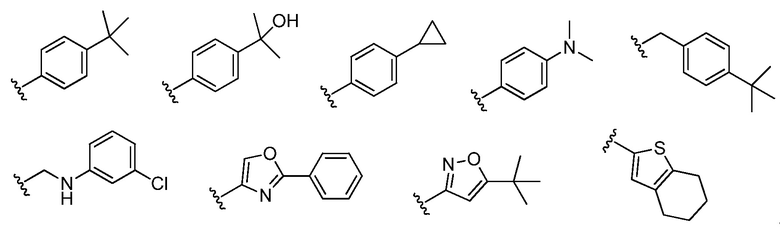
[0072] В определенных вариантах осуществления, каждый из R1, R2, R3, R4, R5, X, m и n, представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0073] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-a,
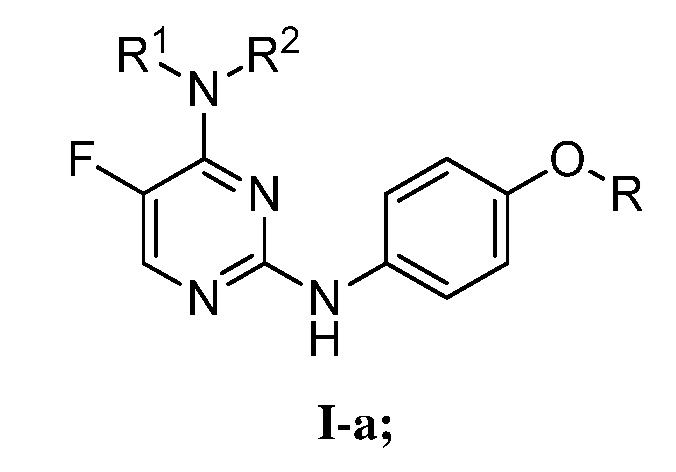
Или его фармацевтически приемлемую соль, где каждый из R, R1 и R2 представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0074] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-b,
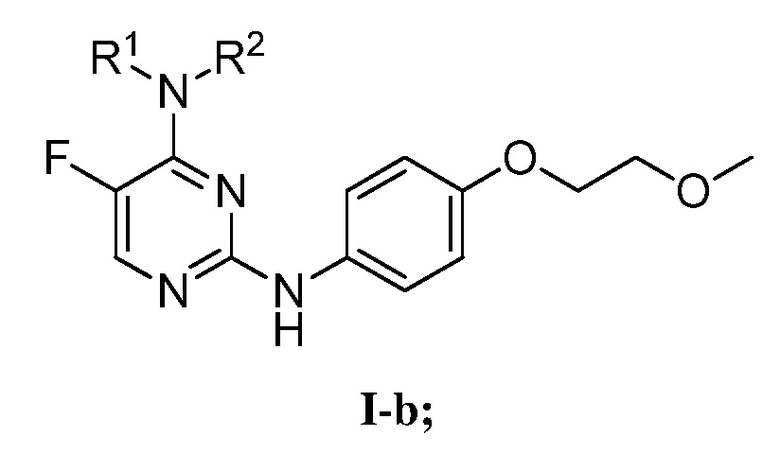
или его фармацевтически приемлемую соль, где каждый из R1 и R2 представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0075] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-c,
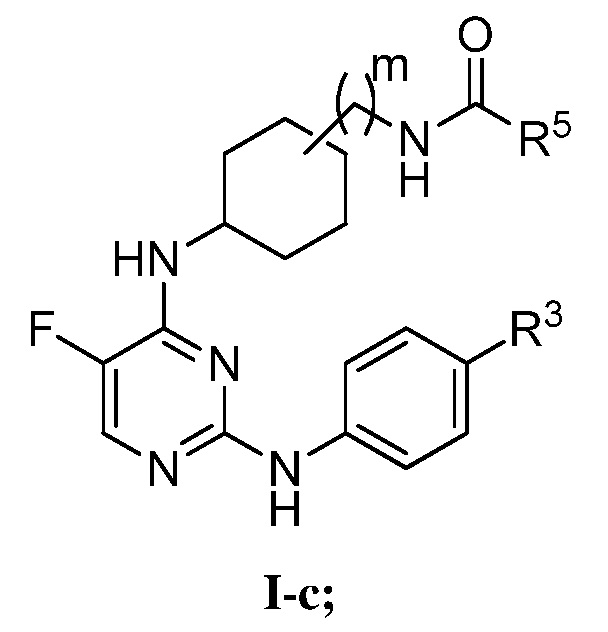
Или его фармацевтически приемлемую соль, где каждый из R3, R5 и m представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0076] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-d,
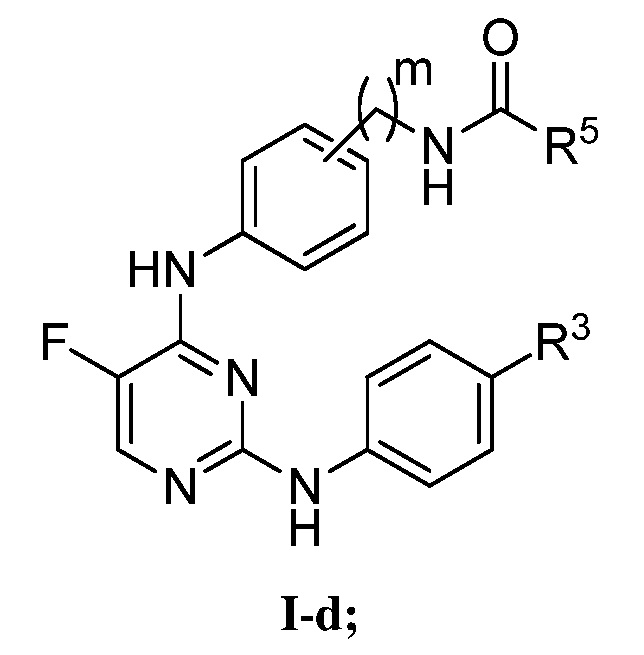
Или его фармацевтически приемлемую соль, где каждый из R3, R5 и m представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0077] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-e,
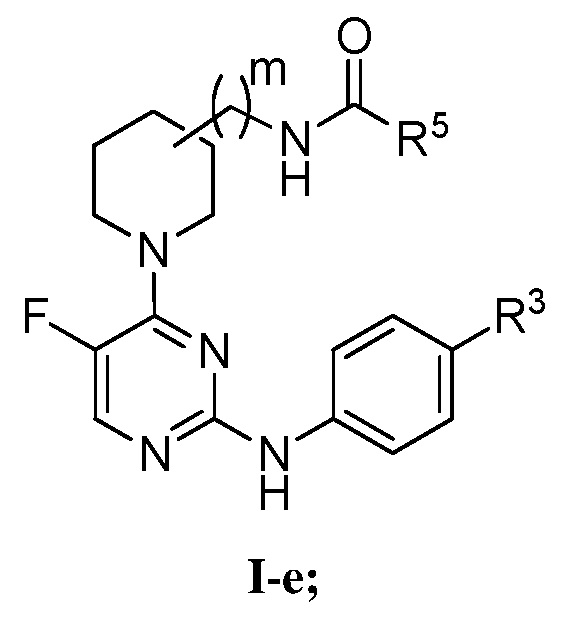
Или его фармацевтически приемлемую соль, где каждый из R3, R5 и m представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0078] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-f,
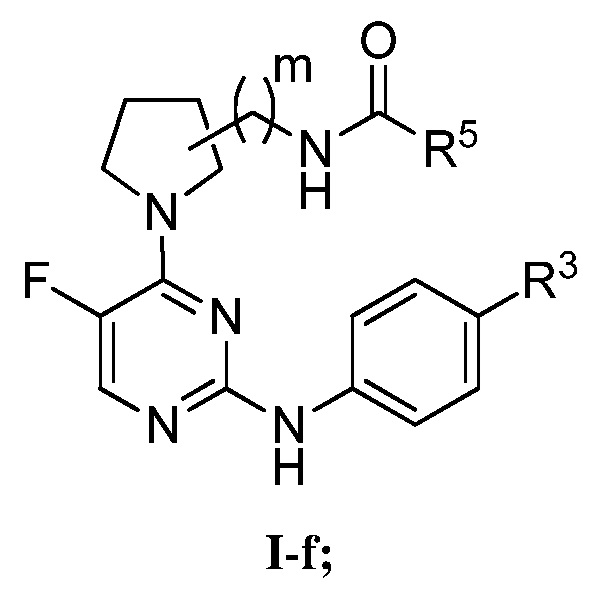
Или его фармацевтически приемлемую соль, где каждый из R3, R5, и m представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации.
[0079] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение формулы I-a,
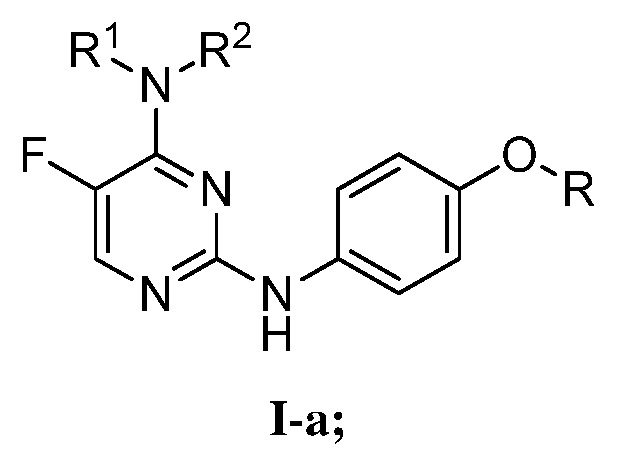
Или его фармацевтически приемлемую соль, где каждый из R представляет собой, как определено выше и описано в вариантах осуществления, классах и подклассах выше и в настоящем изобретении, отдельно или в комбинации; где кольцо, образованное N, R1 и R2, представляет собой
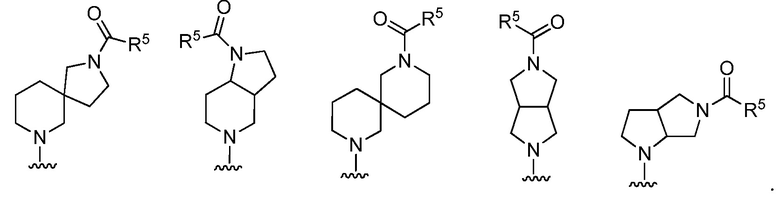
[0080] В определенных вариантах осуществления, настоящее изобретение обеспечивает соединение, выбранное из таблицы 1:
Таблица 1
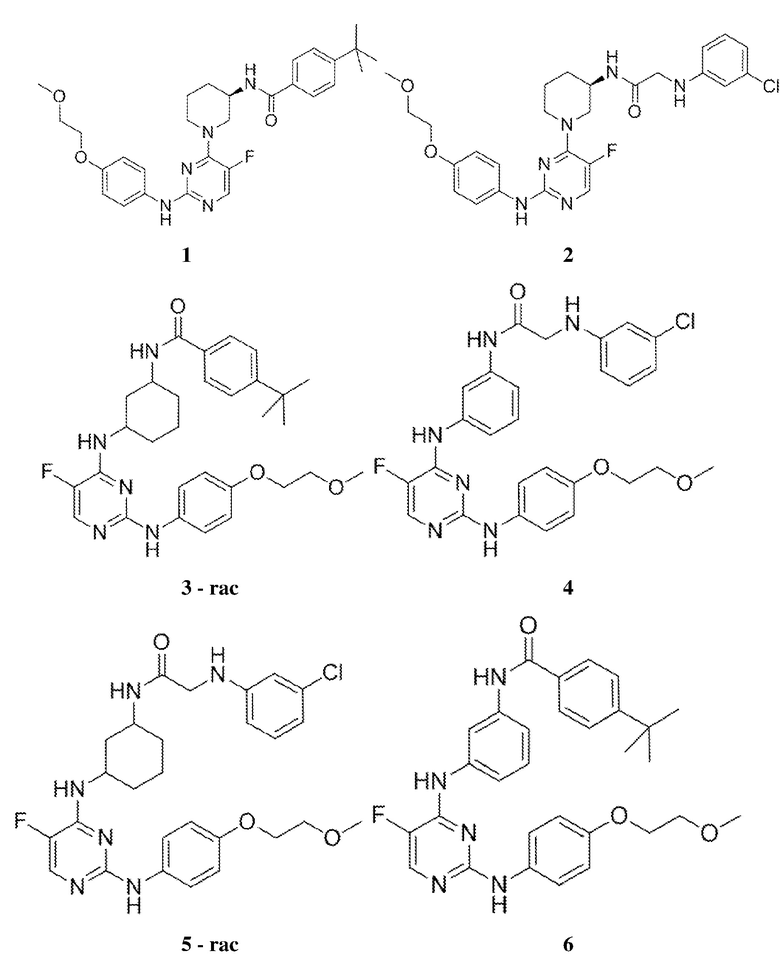
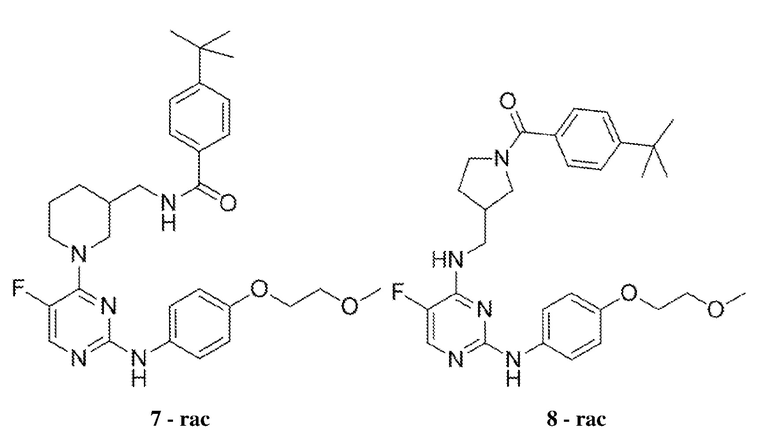
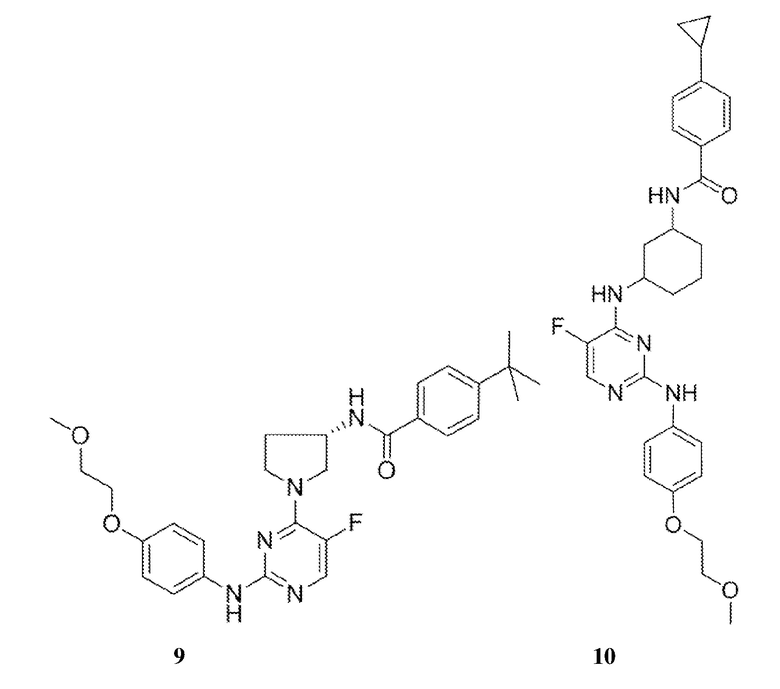
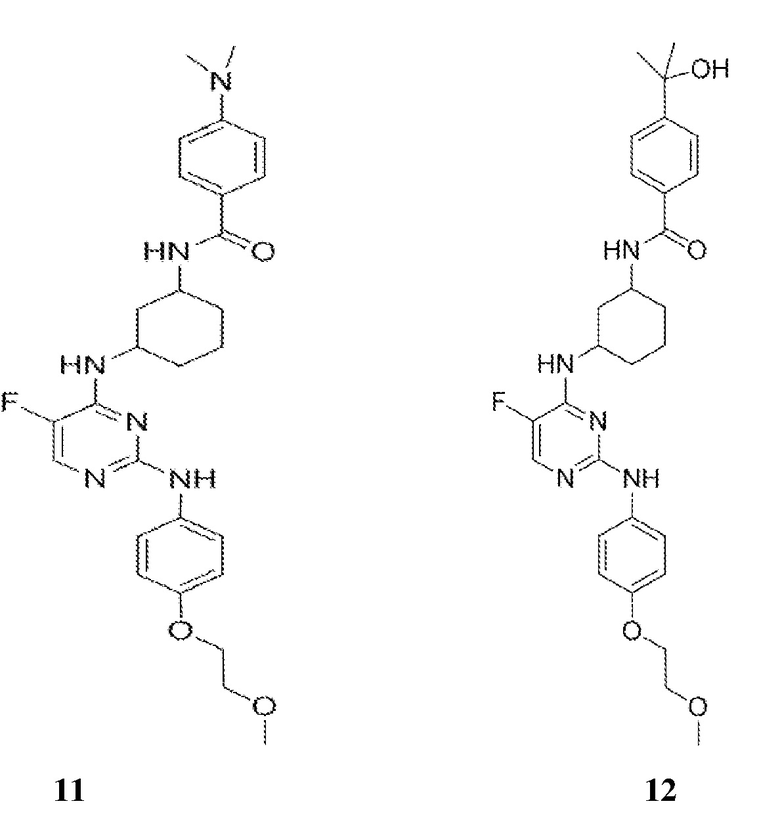
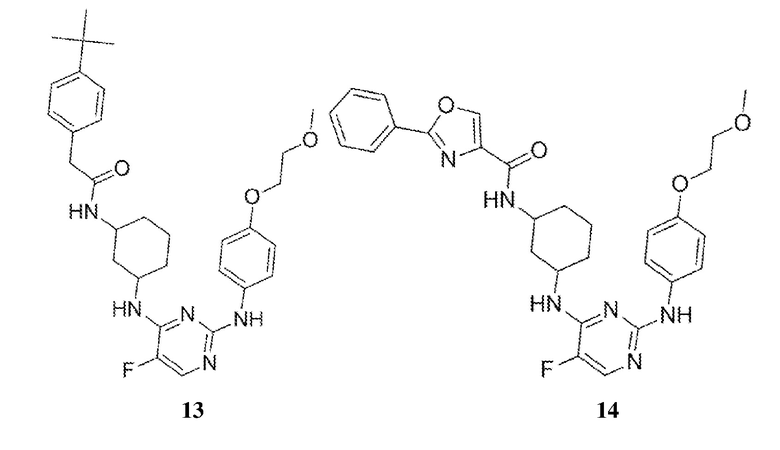
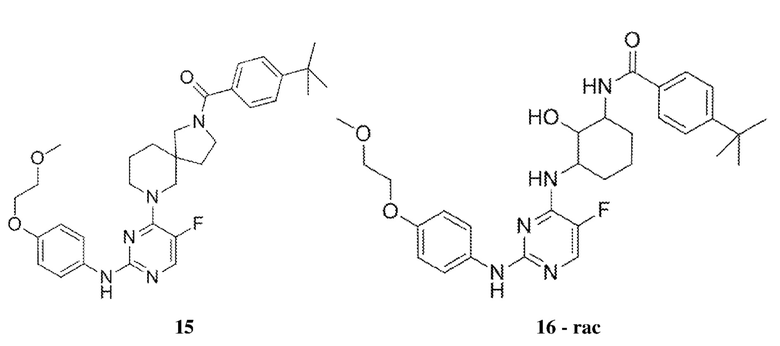
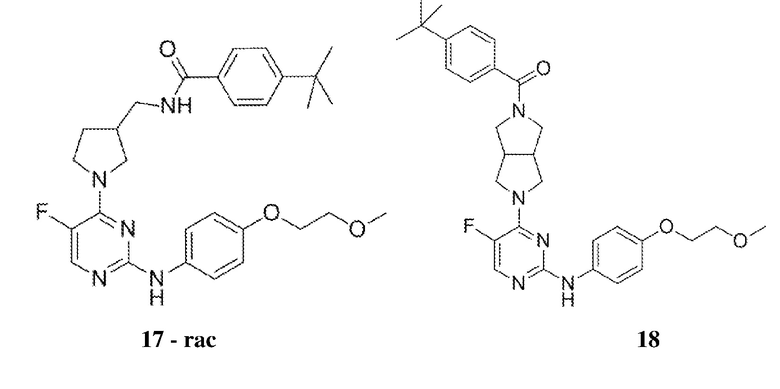
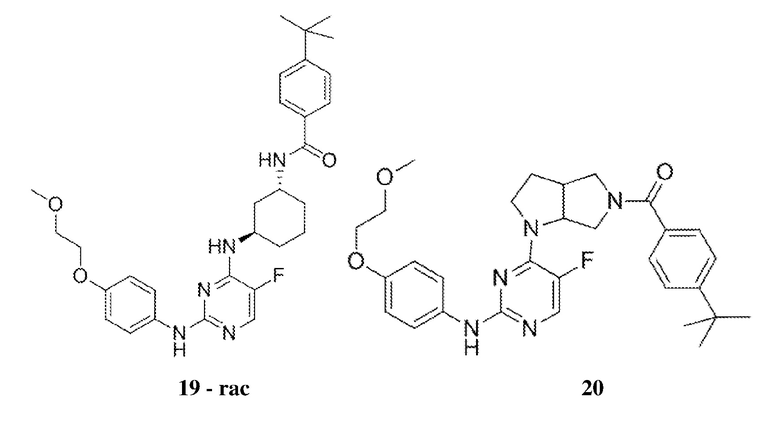
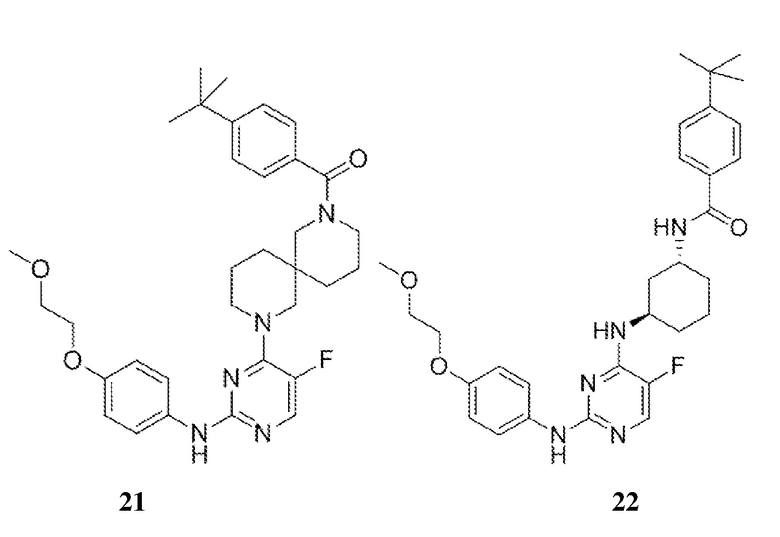
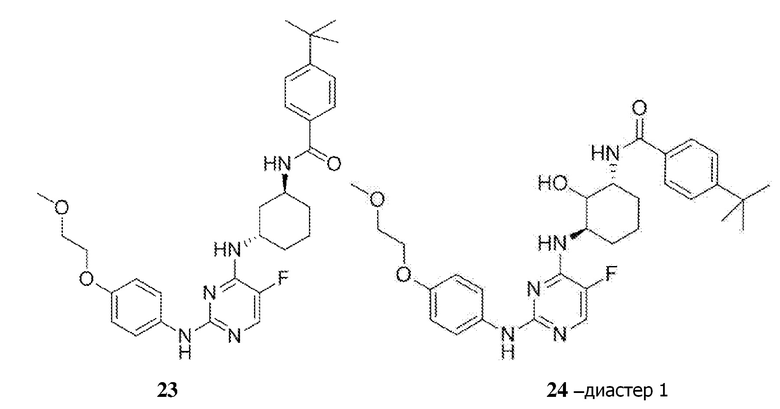
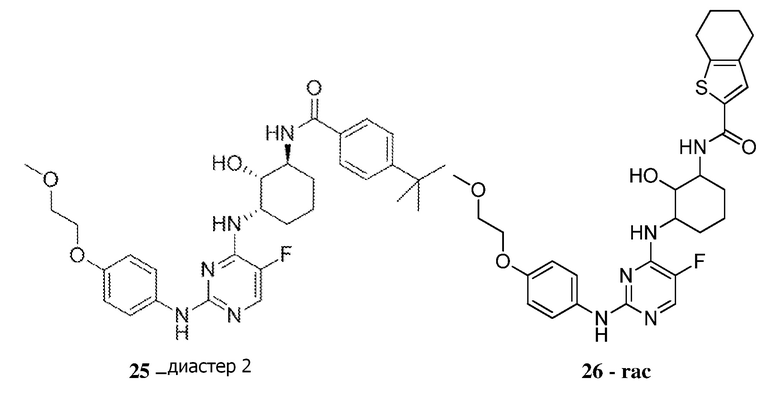
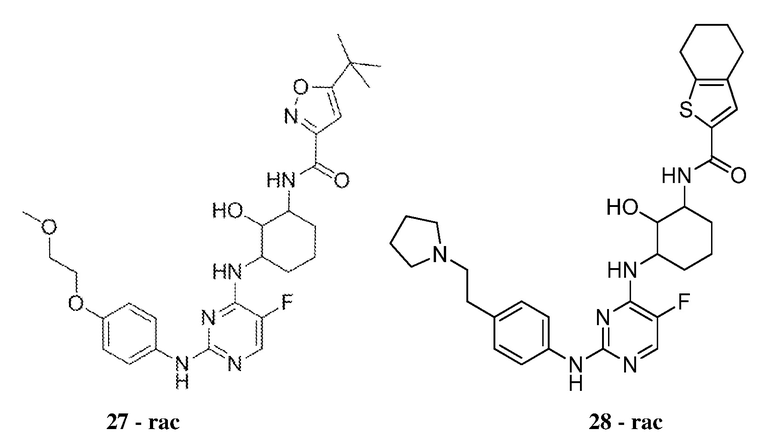
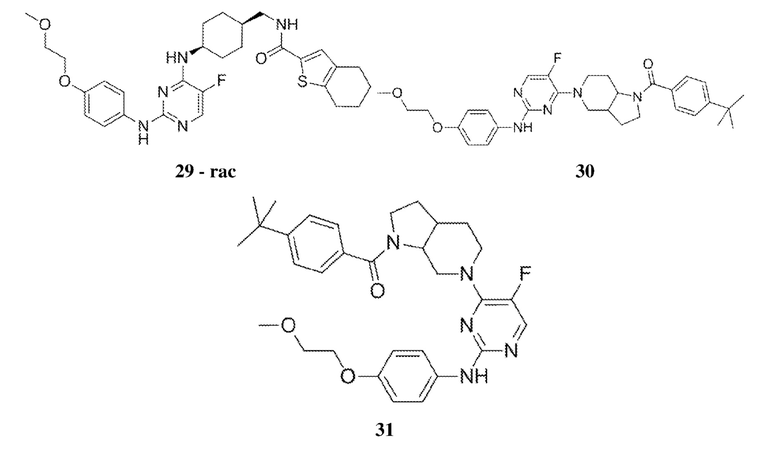
[0081] В некоторых вариантах осуществления, настоящее изобретение обеспечивает соединение, выбранное из соединений, показанных выше, или его фармацевтически приемлемую соль.
[0082] Различные структурные изображения могут показывать гетероатом без присоединенной группы, радикала, заряда или противоиона. Специалисту в данной области техники ясно, что данные изображения предназначены для обозначения того, что гетероатом соединен с водородом (например, 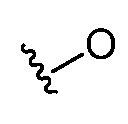 следует понимать как
следует понимать как 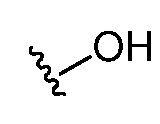 ).
).
[0083] В определенных вариантах осуществления, соединения настоящего изобретения получали согласно схемам, приведенным в примерах ниже.
4. Применение, состав и введение
Фармацевтически приемлемые композиции
[0084] Согласно другому варианту осуществления, настоящее изобретение обеспечивает композицию, содержащую соединение настоящего изобретения или его фармацевтически приемлемое производное и фармацевтически приемлемый носитель, адъювант или среду. Количество соединения в композициях настоящего изобретения является таким, что оно является эффективным для измеримого ингибирования BTK или ее мутанта в биологическом образце или у пациента. В определенных вариантах осуществления, количество соединения в композициях настоящего изобретения является таким, что оно является эффективным для измеримого ингибирования BTK или ее мутанта в биологическом образце или у пациента. В определенных вариантах осуществления, композицию настоящего изобретения формулируют для введения пациенту, нуждающемуся в данной композиции.
[0085] Термин ʺпациентʺ или ʺсубъектʺ, как применяют в настоящем изобретении, обозначает животное, предпочтительно млекопитающее, и самое предпочтительное человека.
[0086] Термин ʺфармацевтически приемлемый носитель, адъювант или средаʺ относится к нетоксичному носителю, адъюванту, или среде, которые не нарушают фармакологическую активность соединения, с которым их формулируют. Фармацевтически приемлемые носители, адъюванты или среды, которые применяют в композициях настоящего изобретения, включают, но не ограничиваются, ионообменники, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, буферные вещества, такие как фосфаты, глицин, сорбиновую кислоту, сорбат калия, частичные глицеридные смеси насыщенных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтилтенгликоль, карбоксиметилцеллюлозу натрия, полиакрилаты, воски, полиэтиленовые полиоксипропиленовые блочные полимеры, полиэтилтенгликоль и шерстяной жир.
[0087] ʺФармацевтически приемлемое производноеʺ обозначает любую нетоксичную соль, эфир, соль эфира или другое производное соединения настоящего изобретения, которое, после введения реципиенту, способно обеспечивать, или непосредственно или опосредованно, соединение настоящего изобретения или его ингибирующий активный метаболит или остаток.
[0088] Композиции настоящего изобретения вводят перорально, парентерально, впрыскиванием, местно, ректально, назально, буккально, вагинально или через имплантированный резервуар. Термин "парентеральный", как применяют в настоящем изобретении, включает подкожный, внутривенный, внутримышечный, внутрисуставной, внутрисинеальный, внутристернальный, интратекальный, внутрипеченочный, внутриочаговый и внутричерепной способ инъекции или способы вливания. Предпочтительно, композиции вводят перорально, интраперитонеально или внутривенно. Стерильные инъецируемые формы композиций настоящего изобретения включают водную или маслянистую суспензию. Данные суспензии формулируют согласно способам, известным в данной области техники, применяя подходящие диспергирующие или увлажняющие агенты и суспендирующие агенты. Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых сред и растворителей, которые можно применять, есть вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла общепринято применяют в качестве растворителя или суспендирующей среды.
[0089] Для данной цели, любое применяемое безвкусное нелетучее масло включает синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, являются пригодными в получении инъецируемых препаратов, как являются пригодными и природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных вариантах. Данные масляные растворы или суспензии также содержат длинноцепочечные спиртовые разбавители или диспергаторы, такие как карбоксиметилцеллюлоза, или аналогичные диспергаторы, которые обычно применяют в формулировании фармацевтически приемлемых лекарственных форм, включая эмульсии и суспензии. Другие общепринятые поверхностно-активные вещества, такие как Tweens, Spans и другие эмульгаторы или усилители биодоступности, которые обычно применяют в получении фармацевтически приемлемых твердых, жидких или других лекарственных форм, также применяют для целей формулирования.
[0090] Фармацевтически приемлемые композиции настоящего изобретения вводят перорально в любой перорально приемлемой лекарственной форме. Примеры пероральных лекарственных форм представляют собой капсулы, таблетки, водные суспензии или растворы. В случае таблеток для перорального применения, обычно применяемые носители включают лактозу и кукурузный крахмал. Также обычно добавляют смазывающие агенты, такие как стеарат магния. Для перорального введения в виде капсул, подходящие разбавители включают лактозу и высушенный кукурузный крахмал. Когда водные суспензии требуются для перорального применения, активный ингредиент смешивают с эмульгаторами и суспендирующими агентами. При желании, необязательно также добавляют определенные подсластители, ароматизаторы или красители.
[0091] Альтернативно, фармацевтически приемлемые композиции настоящего изобретения вводят в виде суппозиториев для ректального введения. Их можно получить смешением агента с подходящим нераздражающим вспомогательным веществом, которое является твердым при комнатной температуре, но жидким при температуре прямой кишки и, следовательно, будет плавиться в прямой кишке, высвобождая лекарственное средство. Данные материалы включают масло какао, пчелиный воск и полиэтиленгликоли.
[0092] Фармацевтически приемлемые композиции настоящего изобретения также вводят местно, особенно когда мишень лечения включает поверхности или органы, легкодоступные местным нанесением, включая заболевания глаз, кожи или нижней части кишечника. Подходящие местные составы легко получить для каждой из данных поверхностей или органов.
[0093] Местное нанесение для нижней части кишечника можно осуществлять в виде ректального суппозитория (смотри выше) или в виде подходящей клизмы. Также применяют местные трансдермальные пластыри.
[0094] Для местного нанесения, обеспечиваемые фармацевтически приемлемые композиции формулируют в виде подходящей мази, содержащей активные компоненты, суспендированные или растворенные в одном или более носителях. Примерные носители для местного введения соединений представляют собой минеральное масло, жидкий вазелин, белый вазелин, пропиленгликоль, полиоксиэтилен, полиоксипропиленовое соединение, неионный эмульгированный воск и воду. Альтернативно, обеспечиваемые фармацевтически приемлемые композиции можно формулировать в виде подходящего лосьона или крема, содержащего активные компоненты, суспендированные или растворенные в одном или более фармацевтически приемлемых носителях. Подходящие носители включают, но не ограничиваются, минеральное масло, моностеарат сорбитана, полисорбат 60, воск цетиловых эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
[0095] Фармацевтически приемлемые композиции настоящего изобретения необязательно вводят назальным аэрозолем или ингаляцией. Данные композиции получают согласно способам, хорошо известным в данной области техники фармацевтического состава, и получают в виде растворов в соляном растворе, применяя бензиловый спирт или другие подходящие консерванты, агенты, способствующие поглощению, увеличивающие биодоступность, фторуглероды, и/или другие общепринятые солюбилизирующие агенты или диспергаторы.
[0096] Самое предпочтительное, фармацевтически приемлемые композиции настоящего изобретения формулируют для перорального введения. Данные составы можно вводить с или без пищи. В некоторых вариантах осуществления, фармацевтически приемлемые композиции настоящего изобретения вводят без пищи. В других вариантах осуществления, фармацевтически приемлемые композиции настоящего изобретения вводят с пищей.
[0097] Количество соединений настоящего изобретения, которое необязательно смешивают с материалами носителя, получая композицию в виде единичной лекарственной форме, будут изменяться в зависимости от реципиента, подвергаемого лечению, конкретного пути введения. Предпочтительно, обеспечиваемые композиции следует формулировать так, чтобы дозу 0,01-100 мг/кг веса тела/день соединения можно было вводить пациенту, получающему данные композиции.
[0098] Также должно быть ясно, что конкретная доза и режим лечения для любого конкретного пациента будет зависеть от ряда факторов, включая активность конкретного применяемого соединения, возраста, веса тела, общего состояния здоровья, пола, рациона, времени введения, скорости выведения, комбинации лекарственных средств и решения лечащего врача и тяжести конкретного заболевания, которое подвергают лечению. Количество соединения настоящего изобретения в композиции будет также зависеть от конкретного соединения в композиции.
Применение соединений и фармацевтически приемлемых композиций
[0099] В определенных вариантах осуществления, настоящее изобретение обеспечивает способ ингибирования BTK или ее мутанта у пациента или в биологическом образце, включающий стадию введения указанному пациенту или контакта указанного биологического образца с соединением согласно настоящему изобретению.
[00100] В определенных вариантах осуществления, настоящее изобретение относится к применению соединений настоящего изобретения и/или его физиологически приемлемых солей для модулирования или ингибирования BTK фермента. Термин ʺмодулированиеʺ обозначает любое изменение в опосредованной BTK-передаче сигнала, которое основано на действии конкретных соединений настоящего изобретения, способных взаимодействовать с BTK мишенью таким способом, которое делает возможным узнавание, связывание и активацию. Соединения характеризуются данным высоким сродством к BTK, которое обеспечивает надежное связывание BTK. В определенных вариантах осуществления, вещества являются высокоселективными по отношению к BTK по сравнению с большинством других киназ для того, чтобы гарантировать эксклюзивное направленное узнавание одной BTK мишени. В контексте настоящего изобретения, термин ʺузнаванияʺ, не ограничиваясь им, относится к любому типу взаимодействия между конкретными соединениями и мишенью, особенно ковалентному или нековалентному связыванию или ассоциации, такой как ковалентная связь, гидрофобные/гидрофильные взаимодействия, Ван-дер-Вальсовы силы, ионные пары, водородные связи, взаимодействия лиганд-рецептор (фермент-ингибитор) и подобные. Данная ассоциация может также включать присутствие других молекул, таких как пептиды, белки или нуклеотидные последовательности. Настоящее взаимодействие белок/лиганд (фермент-ингибитор) характеризуется высоким сродством, высокой селективностью и минимальной или даже отсутствующей перекрестной реактивностью с другими молекулами, являющимися мишенями, исключая пагубные и вредные воздействия на субъекта, подвергаемого лечению.
[00101] В определенных вариантах осуществления, настоящее изобретение относится к способу ингибирования BTK фермента, по меньшей мере, одним соединением формулы (I) согласно настоящему изобретению и/или его физиологически приемлемыми солями, в таких условиях, что указанный BTK фермент ингибируется. В определенных вариантах осуществления, система представляет собой клеточную систему. В других вариантах осуществления, система представляет собой in-vitro трансляцию, которая основана на синтезе белка вне живых клеток. Клеточную систему определяют как любого субъекта, при условии, что субъект содержит клетки. Следовательно, клеточную систему можно выбрать из группы отдельных клеток, клеточных культур, тканей, органов и животных. В определенных вариантах осуществления, способ модулирования BTK фермента осуществляют in-vitro. Предшествующая идея настоящего изобретения, касающаяся соединений формулы (I), включая их любые варианты осуществления, является обоснованной и применимой без ограничений на соединениях формулы (I) и их солях при применении в способе ингибирования BTK. Предшествующая идея настоящего изобретения, касающаяся соединений формулы (I), включая их любые варианты осуществления, является обоснованной и применимой без ограничений на соединениях формулы (I) и их солях при применении в способе ингибирования BTK.
[00102] Пациенты с мутациями в BTK обладают выраженной блокировкой развития B-клеток, приводя в результате к практически полному отсутствию зрелых B-лимфоцитов и плазмоцитов, существенно сниженным концентрациям Ig и выраженному ингибированию гуморального ответа на сенсибилизирующие антигены (освящено в Vihinen et al., Frontiers in Bioscience 5: d917-928). Мыши с дефицитом BTK также имеют сниженное количество периферических B-клеток и значительно сниженные концентрации в сыворотке IgM и IgG3. BTK делеция у мышей обладает выраженным влиянием на пролиферацию B-клеток, вызванную анти-IgM, и ингибирует иммунные ответы на тимус-независимые антигены II типа (Ellmeier et al., J Exp Med 192: 1611-1623 (2000)). BTK также играет важную роль в активации тучных клеток через высокоаффинный IgE рецептор (Fc эпсилон RI). Тучные клетки дефицитных по BTK мышей обладают сниженной дегрануляцией и сниженным продуцированием провоспалительных цитокинов после перекрестного сшивания Fc эпсилон RI (Kawakami et al., Journal of Leukocyte Biology 65: 286-290).
[00103] Соединения настоящего изобретения являются ингибиторами BTK и, следовательно, являются пригодными для лечения одного или более заболеваний, связанных с активностью BTK. Таким образом, в некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения опосредованного BTK заболевания, включающий стадию введения нуждающемуся пациенту соединения настоящего изобретения или его фармацевтически приемлемой композиции.
[00104] Как применяют в настоящем изобретении, термин "опосредованные BTK" заболевания или состояния, как применяют в настоящем изобретении, обозначают любое заболевание или другое вредное состояние, при котором известно, что BTK или ее мутант играют определенную роль. Соответственно, другой вариант осуществления настоящего изобретения относится к лечению или снижению тяжести одного или более заболеваний, при которых известно, что BTK или ее мутант играют определенную роль. Конкретно, настоящее изобретение относится к способу лечения или снижения тяжести заболевания или состояния, выбранного из пролиферативного заболевания или аутоиммунного заболевания, где указанный способ включает введение нуждающемуся пациенту соединений или композиций согласно настоящему изобретению.
[00105] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK. В некоторых вариантах осуществления, заболевание или состояние представляет собой аутоиммунное заболевание, например, воспалительное заболевание кишечника, артрит, системную красную волчанку (СКВ или волчанку), волчаночный нефрит, васкулит, идиопатическую тромбоцитопеническую пурпуру (ITP), ревматоидный артрит, псориатический артрит, остеоартрит, болезнь Стилла, ювенильный артрит, диабет, миастению, тиреоидит Хашимото, тиреоидит Орда, болезнь Грейвса, аутоиммунный тиреоидит, синдром Шегрена, рассеянный склероз, системный склероз, нейроборрелиоз Лайма, синдром Гийена-Барре, острый диссеминированный энцефаломиелит, болезнь Аддисона, опсо-миоклональный синдром, анкилозирующий спондилез, синдром антифосфолипидных антител, апластическую анемию, аутоиммунные гепатиты, аутоиммунные гастриты, пернициозную анемию, целиакию, синдром Гудпасчера, идиопатическую тромбоцитопеническую пурпуру, неврит зрительного нерва, склеродермию, первичный билиарный цирроз, синдром Рейтера, артериит Такаясу, височный артериит, аутоиммунную гемолитическую анемию тепловых агглютининов, гранулематоз Вегенера, псориаз, универсальную алопецию, болезнь Бехчета, хроническую усталость, вегетативную дистонию, мембранную гломерулонефлопатию, эндометриоз, интерстициальный цистит, вульгарный пемфигус, буллезный пемфигоид, нейромиотонию, склеродермию или вульводинию. В определенных вариантах осуществления, заболевание или состояние представляет собой системную красную волчанку (SLE или волчанку) или волчаночный нефрит.
[00106] В некоторых вариантах осуществления, заболевание или состояние представляет собой гиперпролиферативное заболевание или опосредованные иммунитетом заболевания, включая отторжение трансплантируемых органов или тканей и синдром приобретенного иммунодефицита (СПИД, также известный как ВИЧ).
[00107] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, где заболевание или состояние выбирают из гетероиммунных состояний или заболеваний, которые включают, но не ограничиваются, реакцию "трансплантат против хозяина", трансплантацию, переливание крови, анафилаксию, аллергию (например, аллергию на пыльцу растений, латекс, лекарственные средства, продукты питания, яды насекомых, волосы животных, шерсть животных, пылевые клещи или чешуйки тараканов), гиперчувствительность I типа, аллергический конъюнктивит, аллергический ринит и атопический дерматит.
[00108] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, где заболевание или состояние выбирают из воспалительного заболевания, например, астмы, аппендицита, атопического дерматита, астмы, аллергии, блефарита, бронхиолита, бронхита, бурсита, цервицита, холангита, холецистита, хронического отторжения трансплантата, колита, конъюнктивита, болезни Крона, цистита, дакриоаденита, дерматита, дерматомиозита, энцефалита, эндокардита, эндометрита, энтерита, энтероколита, эпикондилита, эпидидимита, фасцита, фиброзита, гастрита, гастроэнтерита, пурпуры Хенох-Шонлейн, гепатита, гнойного гидраденита, IgA-нефропатии, интерстициальной болезни легких, ларингита, мастита, менингита, миелита, миокардита, миозита, нефрита, оофорита, орхита, остита, отита, панкреатита, паротита, перикардита, перитонита, фарингита, плеврита, флебита, пневмонита, пневмонии, полимиозита, проктита, простатита, пиелонефрита, ринита, сальпингита, синусита, стоматита, синовита, тендинита, тонзиллита, язвенного колита, увеита, вагинита, васкулита или вульвита.
[00109] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, где заболевание или состояние выбирают из рака. В одном варианте осуществления, рак представляет собой расстройство пролиферации B-клеток, например, диффузную В-крупноклеточную лимфому, фолликулярную лимфому, хроническую лимфоцитарную лимфому, хроническую лимфоцитарную лейкемию, острый лимфоцитарный лейкоз, В-клеточный пролимфоцитарный лейкоз, лимфоплазматическую лимфому/макроглобулинемию Вальденстрема, лимфому маргинальной зоны селезенки, множественную миелому (также известную как плазмоклеточная миелома), неходжкинскую лимфому, лимфому Ходжкина, плазмоцитому, экстранодальную B-клеточную лимфому из клеток маргинальной зоны, узловую B-клеточную лимфому из клеток краевой зоны, лимфому из клеток мантийной зоны, медиастинальную (тимусную) В-крупноклеточную лимфому, внутрисосудистую В-крупноклеточную лимфому, первичную эффузионную лимфому, лимфому/лейкемию Беркитта или лимфоматоидный гранулематоз. В некоторых вариантах осуществления, рак представляет собой рак молочной железы, рак предстательной железы или рак тучных клеток (например, мастоцитому, лейкемию тучных клеток, саркому тучных клеток, системный мастоцитоз). В одном варианте осуществления, рак представляет собой рак кости. В другом варианте осуществления, рак имеет другое исходное происхождение и метастазирует в кость. В определенных вариантах осуществления, рак представляет собой рак толстой и прямой кишок или рак поджелудочной железы.
[00110] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний или состояний, связанных с BTK, включая заболевания костей и суставов, включая, без ограничения, ревматоидный артрит, серонегативные спондилоартропатии (включая анкилозирующий спондилит, псориатический артрит и болезнь Рейтера), болезнь Бехчета, синдром Шегрена, системный склероз, остеопороз, рак кости и метастазы в кости.
[00111] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ для лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, где заболевание или состояние выбирают из тромбоэмболического расстройства или сердечнососудистого расстройства, например, инфаркта миокарда, стенокардии, реокклюзии после ангиопластики, рестеноза после ангиопластики, реокклюзии после аортокоронарного шунтирования, рестеноза после аортокоронарного шунтирования, инсульта, транзиторной ишемии, периферического артериального окклюзионного заболевания, эмболии легких или тромбоза глубоких вен. В отдельных вариантах осуществления настоящее изобретение обеспечивает антитромботический агент, поскольку BTK также участвует в активации тромбоцитов.
[00112] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ для лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, включая инфекционные и неинфекционные воспалительные осложнения и аутоиммунные и другие воспалительные заболевания. Данные аутоиммунные и воспалительные заболевания, расстройства и синдромы включают воспалительное заболевание таза, уретрит, солнечный ожог кожи, синусит, пневмонит, энцефалит, менингит, миокардит, нефрит, остеомиелит, миозит, гепатит, гастрит, энтерит, дерматит, гингивит, аппендицит, панкреатит, холецистит, агаммаглобулинемию, псориаз, аллергия, болезнь Крона, синдром раздраженной толстой кишки, язвенный колит, болезнь Шегрена, отторжение тканевого трансплантата, сверхострое отторжение трансплантированных органов, астму, аллергический ринит, хроническое обструктивное заболевание легких (ХОБЛ), аутоиммунное плюригландулярное заболевание (также известные как аутоиммунный плюригландулярный синдром), аутоиммунную алопецию, персистирующую анемию, гломерулонефрит, дерматомиозит, рассеянный склероз, склеродермию, васкулит, аутоиммунные гемолитические и тромбоцитопенические состояния, синдром Гудпасчера, атеросклероз, болезнь Аддисона, болезнь Паркинсона, болезнь Альцгеймера, диабет, септический шок, системную красную волчанку (СКВ), ревматоидный артрит, псориатический артрит, ювенильный артрит, остеоартрит, хроническую идиопатическую тромбоцитопеническую пурпуру, макроглобулинемию Вальденстрема, миастению, тиреоидит Хашимото, атопический дерматит, дегенеративное заболевание суставов, витилиго, аутоиммунный гипопитуитаризм, синдром Гийена-Барре, болезнь Бехчета, склерадерму, грибковые микозы, острые воспалительные реакции (такие как острый респираторный дистресс-синдром и ишемия/реперфузионное повреждение) и болезнь Грейвза. В определенных вариантах осуществления, диабет представляет собой диабет I типа.
[00113] В некоторых вариантах осуществления, настоящее изобретение обеспечивает способ лечения или снижения тяжести одного или более заболеваний и состояний, связанных с BTK, выбранных из ревматоидного артрита, рассеянного склероза, В-клеточного хронического лимфоцитарного лейкоза, острого лимфоцитарного лейкоза, лейкоза ворсистых клеток, неходжкинской лимфомы, лимфомы Ходжкина, множественной миеломы, рака кости, метастаза в кости, остеопороза, диабета (например, диабета типа I), синдрома раздраженного кишечника, болезни Крона, волчанки и почечной трансплантации.
[00114] Другая цель настоящего изобретения заключается в обеспечении способа лечения заболевания, которое вызвано, опосредовано и/или прогрессирует за счет BTK активности, где, по меньшей мере, одно соединение формулы (I) согласно настоящему изобретению и/или его физиологически приемлемые соли вводят нуждающемуся в данном лечении млекопитающему. В определенных вариантах осуществления, настоящее изобретение обеспечивает способ для лечения волчанки, где, по меньшей мере, одно соединение формулы (I) согласно настоящему изобретению и/или его физиологически приемлемые соли вводят нуждающемуся в данном лечении млекопитающему. В определенных вариантах осуществления, соединение вводят в эффективном количестве, как определено выше. В определенных вариантах осуществления, лечение представляет собой пероральное введение.
[00115] Способ настоящего изобретения модно осуществлять или in-vitro или in-vivo. Восприимчивость конкретной клетки к обработке соединениями согласно настоящему изобретению можно в частности определить in-vitro испытаниями, в процессе исследования или клинического применения. Обычно, культуру клеток смешивают с соединением согласно настоящему изобретению при различных концентрациях в течение периода времени, который является достаточным для обеспечения ингибирования BTK активности активными агентами, обычно от приблизительно одного часа до одной недели. In-vitro обработку можно осуществлять, применяя культивируемые клетки из образца биопсии или клеточной линии.
[00116] Реципиент или пациент может принадлежать к любому виду млекопитающих, например, видам приматов, в частности людям; гразунам, включая мышей, крыс и хомячков; кроликам; лошадям, коровам, собакам, кошкам и т.д. Животные модели представляют интерес для экспериментальных исследований, обеспечивая модель для лечения заболевания человека.
[00117] Для обнаружения пути передачи сигналов и для обнаружения взаимодействий между различными путями передачи сигналов, различные ученые обнаружили подходящие модели или модельные системы, например, модели клеточных структур и модели трансгенных животных. Для определения стадий в каскаде передачи сигналов, взаимодействующие соединения можно применять для того, чтобы модулировать сигнал. Соединения согласно настоящему изобретению можно также применять в качестве реагентов для исследования зависящих от BTK путей передачи сигналов в животных моделях и/или моделях клеточных культур или при клинических заболеваниях, приведенных в настоящей заявке.
[00118] Более того, следующую идею настоящего изобретения, касающуюся применения соединений формулы (I) и их производных для получения лекарственного средства для профилактического или терапевтического лечения, и/или мониторинга, считают действенной и применимой, без ограничений, для применения соединения для ингибирования BTK активности, если целесообразно.
[00119] Настоящее изобретение также относится к применению соединений формулы (I) и/или их физиологически приемлемых солей для профилактического или терапевтического лечения и/или мониторинга заболевания, которое вызвано, опосредовано и/или прогрессирует за счет BTK активности. Более того, настоящее изобретение относится к применению соединений формулы (I) и/или их физиологически приемлемых солей в получении лекарственного средства для профилактического или терапевтического лечения и/или мониторинга заболевания, которое вызвано, опосредовано и/или прогрессирует за счет BTK активности. В определенных вариантах осуществления, настоящее изобретение относится к применению соединений формулы I или их физиологически приемлемых солей в получении лекарственного средства для профилактического или терапевтического лечения опосредованного BTK заболевания.
[00120] Кроме того, соединения формулы (I) и/или их физиологически приемлемую соль можно применять в качестве промежуточного соединения для получения дополнительных лекарственных активных ингредиентов. Лекарственное средство предпочтительно получают нехимическим способом, например, смешением активного ингредиента, по меньшей мере, с одним твердым, жидким и/или полужидким носителем или вспомогательным веществом, и необязательно в сочетании с одним или более другими активными веществами в виде подходящей лекарственной формы.
[00121] Другой предмет настоящего изобретения представляет собой соединения формулы (I) согласно настоящему изобретению и/или их физиологически приемлемые соли для применения в профилактическом или терапевтическом лечении и/или мониторинге заболевания, которое вызвано, опосредовано и/или прогрессирует за счет BTK активности. Другая предпочтительная цель настоящего изобретения относится к соединениям формулы (I) согласно настоящему изобретению и/или их физиологически приемлемым солям для применения в профилактическом или терапевтическом лечении и/или мониторинге волчанки. Предшествующая идея настоящего изобретения, касающаяся соединений формулы (I), включая их любой предпочтительный вариант осуществления, является действенной и применимой без ограничений для соединений формулы (I) и их солей для применения в профилактическом или терапевтическом лечении и/или мониторинге волчанки.
[00122] Соединения формулы (I) согласно настоящему изобретению можно вводить перед или после возникновения заболевания, один или несколько раз действуя в качестве терапии. Приведенные выше соединения и медицинские продукты применения настоящего изобретения в частности применяют для терапевтического лечения. Терапевтически релевантный эффект облегчает, до некоторой степени, один или более симптомов заболевания, или возвращает в нормальное состояние, или частично или полностью, один или более физиологических или биохимических параметров, связанных с или вызывающих заболевание или патологическое состояние. Мониторинг считают вариантом лечения при условии, что соединения вводят через определенные интервалы, например, для того, чтобы простимулировать реакцию и полностью устранить патогены и/или симптомы заболевания. Можно применять или идентичное соединение или различные соединения. Способы настоящего изобретения можно также применять для снижения вероятности развития заболевания или даже предотвращать возникновение заболеваний, связанных с BTK активностью, заранее или лечить возникающие и непрекращающиеся симптомы.
[00123] В контексте настоящего изобретения, профилактическое лечение является рекомендованным, если субъект обладает любыми предпосылками для приведенных выше физиологических или патологических состояний, таких как семейная предрасположенность, генетический дефект или ранее перенесенное заболевание.
[00124] Кроме того, настоящее изобретение относится к лекарственному средству, содержащему, по меньшей мере, одно соединение согласно настоящему изобретению и/или его фармацевтически приемлемые производные, соли, сольваты и стереоизомеры, включая их смеси во всех соотношениях. В определенных вариантах осуществления, настоящее изобретение относится к лекарственному средству, содержащему, по меньшей мере, одно соединение согласно настоящему изобретению и/или его физиологически приемлемые соли.
[00125] ʺЛекарственное средствоʺ в контексте настоящего изобретения представляет собой любой агент в области медицины, который содержит один или более соединений формулы (I) или их препараты (например, фармацевтическую композицию или фармацевтический состав), и его можно применять в профилактике, терапии, последующем врачебном наблюдении или медицинской реабилитации пациентов, которые страдают от заболеваний, которые связаны с BTK активностью, таким способом, что можно облегчать, по меньшей мере, временно патогенное изменение их общего состояния или состояния конкретных областей организма.
[00126] В различных вариантах осуществления, активный ингредиент можно вводить отдельно или в комбинации с другими терапиями. Синергический эффект можно достигать применением более чем одного соединения в фармацевтической композиции, т.е. соединение формулы (I) комбинируют, по меньшей мере, с другим агентом в качестве активного ингредиента, который является или другим соединением формулы (I) или соединением отличного структурного остова. Активные ингредиенты можно применять или одновременно или последовательно.
[00127] Включенными в настоящее изобретение являются способы лечения, в которых, по меньшей мере, одно химические соединение, относящееся к настоящему изобретению, вводят в комбинации с противовоспалительным агентом. Противовоспалительные агенты включают, но не ограничиваются, НПВП, неспецифические и COX-2 специфические ингибиторы циклооксигеназы, соединения золота, кортикостероиды, метотрексат, антагонисты фактора некроза опухолей (TNF), иммуносупрессанты и метотрексат.
[00128] Примеры НПВП включают, но не ограничиваются, ибупрофен, флурбипрофен, напроксен и напроксен натрия, диклофенак, комбинации диклофенака натрия и мизопростола, сулиндак, оксапрозин, дифлуниаз, пироксикам, индометацин, этодолак, фенопрофен кальций, кетопрофен, набуметон натрия, сульфасалазин, тольметин натрия и гидроксихлорохин. Примеры НПВП также включают COX-2 специфические ингибиторы, такие как целекоксиб, вальдекоксиб, лумиракоксиб и/или эторикоксиб.
[00129] В некоторых вариантах осуществления, противовоспалительный агент представляет собой салицилат. Салицилаты включают, но не ограничиваются, ацетилсалициловую кислоту или аспирин, салицилат натрия, и салицилаты холина и магния.
[00130] Противовоспалительный агент может также представлять собой кортикостероид. Например, кортикостероид может представлять собой кортизон, дексаметазон, метилпреднизолон, преднизолон, преднизолонфосфат натрия или преднизон.
[00131] В дополнительных вариантах осуществления противовоспалительный агент представляет собой соединение золота, такое как тиомалат золота натрия или ауранофин.
[00132] Настоящее изобретение также включает варианты осуществления, в которых противовоспалительный агент представляет собой метаболический ингибитор, такой как ингибитор дигидрофолатредуктазы, такой как метотрексат, или ингибитор дигидрооротатдегидрогеназы, такой как лефлуномид.
[00133] Другие варианты осуществления настоящего изобретения относятся к комбинациям, в которых, по меньшей мере, одно противовоспалительное соединение представляет собой анти-моноклональное антитело (такое как экулизумаб или пекселизумаб), TNF антагонист, такой как энтанерцепт, или инфликсимаб, который представляет собой анти-TNF альфа моноклональное антитело.
[00134] Еще другие варианты осуществления настоящего изобретения относятся к композициям, в которых, по меньшей мере, один активный агент представляет собой иммуносупрессант, такой как иммуносупрессант, выбранный из метотрексата, лефлуномида, циклоспорина, такролимуса, азатиоприна и микофенолята мофетила.
[00135] B-клетки и B-клеточные предшественники, экспрессирующие BTK, вовлечены в патологию B-клеточных злокачественных образований, включая, но не ограничиваясь, B-клеточную лимфому, лимфому (включая ходжкинскую и неходжскинскую лимфому), волосатоклеточную лимфому, множественную миелому, хроническую и острую миелогенную лейкемию и хроническую и острую лимфоцитарную лейкемию.
[00136] Показано, что BTK является ингибитором Fas/APO-1 (CD-95) сигнального комплекса, индуцирующего смерть клетки (DISC) в B-лимфоцитах. Смерть лейкозных/лимфотических клеток может находиться в балансе между противоположными проапоптозными эффектами каспаз, активируемых DISC, и вышерасположенным антиапоптозным регуляторным механизмом, включающим BTK и/или ее субстраты (Vassilev et al., J. Biol. Chem. 1998, 274, 1646-1656).
[00137] Также было обнаружено, что BTK ингибиторы являются пригодными в качестве хемосенсибилизаторов, и, таким образом, являются пригодными в комбинации с другими химиотерапевтическим агентами, в частности, лекарственными средствами, которые вызывают апоптоз. Примеры химиотерапевтических лекарственных средств, которые можно применять в комбинации с хемосенсибилизирующими BTK ингибиторами, включают ингибиторы топоизомеразы I (камфотецин или топотекан), ингибиторы топоизомеразы II (например, дауномицин и этопозид), алкилирующие агенты (например, циклофосфамид, мелфалан и BCNU), агенты, мишенью которых является тубулин (например, таксол и винбластин), и биологические агенты (например, антитела, такие как анти CD20 антитело, IDEC 8, иммунотоксины и цитокины).
[00138] Описанные соединения формулы I можно вводить в комбинации с другими известными терапевтическими агентами, включая противораковые агенты. Как применяют в настоящем изобретении, термин "противораковый агент" относится к любому агенту, который вводят пациенту с раком для целей лечения рака.
[00139] Противораковую терапию, определенную выше, можно применять в качестве монотерапии, или она может включать, в добавление к описанным в настоящем изобретении соединениям формулы I, традиционную хирургическую операцию или радиотерапию или медицинскую терапию. Данная медицинская терапия, например, химиотерапия или таргетная терапия, может включать один или более, но предпочтительно один, из следующих противораковых агентов:
Алкилирующие агенты: такие как альтретамин, бендамустин, бусульфан, кармустин, хлорамбуцил, хлорметин, циклофосфамид, дакарбазин, ифосфамид, импросульфан, тосилат, ломустин, мелфалан, митобронитол, митолактол, нимустин, ранимустин, темозоломид, тиотепа, треосульфан, мехлорэтамин, карбоквон; апазиквон, фотемустин, глуфосфамид, палифосфамид, пипоброман, трофосфамид, урамустин, TH-3024, VAL-0834;
Платиновые соединения: такие как карбоплатин, цисплатин, эптаплатин, гидрат мириплатина, оксалиплатин, лобаплатин, недаплатин, пикоплатин, сатраплатин; лобаплатин, недаплатин, пикоплатин, сатраплатин;
Агенты, изменяющие ДНК: такие как амрубицин, бизантрен, децитабин, митоксантрон, прокарбазин, трабектедин, клофарабин; амсакрин, бросталлицин, пиксантрон, ларомустин1,3;
Ингибиторы топоизомеразы: такие как этопозид, иринотекан, разоксан, собузоксан, тенипозид, топотекан; амонафид, белотекан, ацетат эллиптиния, ворелоксин;
Модификаторы микротрубочек: такие как кабазитаксел, доцетаксел, эрибулин, иксабепилон, паклитаксел, винбластин, винкристин, винорелбин, виндезин, винфлунин; фосбретабулин, тезетаксел;
Антиметаболиты: такие как аспарагиназа3, азацитидин, левофолинат кальция, капецитабин, кладрибин, цитарабин, эноцитабин, флоксуридин, флударабин, фторурацил, гемцитабин, меркаптопурин, метотрексат, неларабин, пеметрексед, пралатрексат, азатиоприн, тиогуанин, кармофур; доксифлуридин, элецитарабин, ралтитрекс, сапацитабин, тегафур2,3, триметрексат;
Противораковые антибиотики: такие как блеомицин, дактиномицин, доксорубицин, эпирубицин, идарубицин, левамизол, милтефозин, митомицин С, ромидепсин, стрептозоцин, валрубицин, циностатин, зорубицин, даунуробицин, плекамицин; акларубицин, пепломицин, пирарубицин;
Гормоны/антагонисты: такие как абареликс, абиратерон, бикалутамид, бузерелин, калустерон, хлортрианизин, дегареликс, дексаметазон, эстрадиол, флуокортолон, флуоксиместерон, флутамид, фульвестрант, гозерелин, гистрелин, лейпрорелин, мегестрол, митотан, нафалерин, нандролон, нилутамид, октреотид, преднизолон, ралоксифен, тамоксифен, тиротропин альфа, торемифен, трилостан, трипторелин, диэтилстилбестрол; аколбифен, даназол, деслорелин, эпитиосталон, ортеролен, энзалутамид1,3;
Ингибиторы ароматазы: такие как аминоглютетимид, анастрозол, эксеместан, фадрозол, летрозол, тестолактон; форместан;
Низкомолекуляные ингибиторы киназ: такие как кризотиниб, дасатиниб, эрлотиниб, иматиниб, лапатиниб, нилотиниб, пазопаниб, регорафениб, руксолитиниб, сорафениб, сунитиниб, вандетаниб, вемурафениб, босутиниб, гефитиниб, акситиниб; афатиниб, алисертиб, дабрафениб, дакомитиниб, динациклиб, довитиниб, энзастаурин, нинтеданиб, ленватиниб, линифаниб, линзитиниб, мазитиниб, мидостаурин, мотезаниб, нератиниб, орантиниб, перифозин, понатиниб, радотиниб, ригосертиб, типифарниб, тивантиниб, тивозаниб, траметиниб, пимасертиб, бриваниб аланинат, цедираниб, апатиниб4, S-малат кабозантиниба1,3, ибрутиниб1,3, икотиниб4, бупарлизиб2, ципатиниб4, кобиметиниб1,3, иделализиб1,3, федратиниб1, XL-6474;
Фотосенсибилизаторы: такие как метоксален3; порфимер натрия, талапорфин, темопорфин;
Антитела: такие как алемтузумаб, безилезомаб, брентуксимаб ведотин, ceтуксимаб, денозумаб, ипилимумаб, офатумумаб, панитумумаб, ритуксимаб, тозитумомаб, трастузумаб, бевацизумаб, пертузумаб2,3; катумаксомаб, элотузумаб, эпратузумаб, фарлетузумаб, могамулизумаб, нецитумумаб, нимотузумаб, обинутузумаб, окаратузумаб, ореговомаб, рамицирумаб, рилотумумаб, силтуксимаб, тоцилизумаб, залутумумаб, занолимумаб, матузумаб, далотузумаб1,2,3, онартузумаб1,3, ракотумомаб1, табалумаб1,3, EMD-5257974, ниволумаб1,3;
Цитокины: такие как альдеслейкин, интерферон альфа2, интерферон альфа2a3, интерферон альфа2b2,3; целмолейкин, тазонермин, тецелейкин, опрелвекин1,3, рекобминантный интерферон бета-1a4;
Конъюгаты лекарственных средств: такие как денилейкин дифтитокс, ибритумомаб тиуксетан, йобенгуан I123, преднимустин, трасттузумаб эмтанзин, эстрамустин, гемтузумаб, озогамистин, афлиберцепт; цинтредекин безудотокс, эдотреотид, инотузумаб озогамицин, наптумомаб эстафенатокс, опортузумаб монатокс, рацитумомаб технеция (99mTc)1,3, винтафолид1,3;
Вакцины: такие как сипулейцел 3; витеспен3, эмепепимут -S3, онкоVAX4, риндопепимут3, троVax4, MGN-16014, MGN-17034; и
Разное: алитретиноин, бексаротен, бортезомиб, эверолимус, ибандроновая кислота, имиквимод, леналидомид, лентинан, метирозин, мифамуртид, памидроновая кислота, пегаспаргаза, пентостатин, сипулеуцел3, сизофиран, тамибаротен, темсиролимус, талидомид, третиноин, висмодегиб, золедроновая кислота, вориностат; целекоксиб, циленгитид, энтиностат, этанидазол, ганетеспиб, идроноксил, инипариб, иксазомиб, лонидамин, ниморазол, панобиностат, перетиноин, плитидепсин, помалидомид, прокодазол, ридафоролимус, тасквинимод, телотристат, тималфазин, тирапазамин, тоседостат, трабедерсен, убенимекс, валсподар, гендицин4, пицибанил4, реолизин4, гидрохлорид ретаспимицина1,3, требананиб2,3, вирулизин4, карфилзомиб1,3, эндостатин4, иммукотел4, белиностат3, MGN-17034.
(1 предл. INN (предложенное международное непатентованное наименование); 2 реком. INN (рекомендованные международные непатентованные наименования); 3 USAN (наименование, принятое в Соединенных Штатах); 4 без INN).
[00140] В другом аспекте, настоящее изобретение обеспечивает набор, содержащий отдельные пакеты эффективного количества соединения согласно настоящему изобретению и/или его фармацевтически приемлемых солей, производных, сольватов и стереоизомеров, включая их смеси во всех соотношениях, и необязательно, эффективного количества дополнительного активного ингредиента. Набор содержит подходящие контейнеры, такие как коробки, отдельные флаконы, мешки или ампулы. Набор может, например, содержать отдельные ампулы, причем каждая содержит эффективное количество соединения согласно настоящему изобретению и/или его фармацевтически приемлемых солей, производных, сольватов и стереоизомеров, включая их смеси во всех соотношениях, и эффективное количество дополнительного активного ингредиента в растворенной или лиофилизированной форме.
[00141] Как применяют в настоящем изобретении, термины ʺлечениеʺ, ʺлечитьʺ и ʺлечениеʺ относятся к обращению, облегчению, задержке возникновения или ингибированию развития заболевания или расстройства, или одного или более его симптомов, как описано в настоящем изобретении. В некоторых вариантах осуществления, лечение осуществляют после развития одного или более симптомов. В других вариантах осуществления, лечение осуществляют в отсутствии симптомов. Например, лечение осуществляют на предрасположенном индивиде перед возникновением симптомов (например, с учетом истории симптомов и/или с учетом генетических или других факторов подверженности). Лечение также продолжают после устранения симптомов, например, предотвращая или откладывая их повторное проявление.
[00142] Соединения и композиции согласно способу настоящего изобретения вводят, применяя любое количество и любой путь введения, эффективные для лечения или снижения тяжести заболевания, приведенного выше. Точное требуемое количество будет изменяться от субъекта к субъекту, в зависимости от вида, возраста и общего состояния субъекта, тяжести инфекции, конкретного агента, пути его введения, и подобных. Соединения настоящего изобретения предпочтительно формулируют в виде единичной дозированной формы для простоты введения и однородности дозирования. Выражение "единичная дозированная форма", как применяют в настоящем изобретении, относится к физически дискретной единице агента, подходящего для пациента, которого будут лечить. Однако ясно, что суммарное дневное применение соединений и композиции настоящего изобретения будет определяться лечащим врачом по результатом тщательной медицинской оценки. Конкретная эффективная величина дозы для любого конкретного пациента или организма будет зависеть от ряда факторов, включая заболевание, которое лечат, и тяжесть заболевания; активность конкретного применяемого соединения; конкретную применяемую композицию; возраст, вес тела, общее состояние здоровья, пол и рацион пациента; время введения, путь введения и скорость выведения конкретного применяемого соединения; продолжительность лечения; лекарственные средства, применяемые в комбинации или совместно с конкретным применяемым соединением, и подобные факторы, хорошо известные в медицинской области техники.
[00143] Фармацевтически приемлемые композиции настоящего изобретения можно вводить людям и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, интраперитонеально, местно (в виде порошков, мазей или капель), буккально, в виде перорального или назального спрея, или подобными, в зависимости от тяжести инфекции, которую лечат. В определенных вариантах осуществления, соединения настоящего изобретения вводят перорально или парентерально при уровнях доз приблизительно от 0,01 мг/кг до приблизительно 100 мг/кг и предпочтительно от приблизительно 1 мг/кг до приблизительно 50 мг/кг, веса тела субъекта в день, один или более раз в день, получая требуемый терапевтический эффект.
[00144] Жидкие лекарственные формы для перорального введения включают, но не ограничиваются, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В добавление к активному соединению, жидкие лекарственные формы необязательно содержат инертные разбавители, обычно применяемые в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и эфиры жирных кислот и сорбитана, и их смеси. Помимо инертных разбавителей, пероральные композиции могут также содержать адъюванты, такие как смачивающие агенты, эмульгаторы и суспендирующие агенты, подсластители, ароматизаторы и ароматизирующие добавки.
[00145] Инъецируемые препараты, например, стерильные инъецируемые водные или масляные суспензии формулируют согласно известному уровню техники, применяя подходящие диспергирующие или смачивающие агенты и суспендирующие агенты. Стерильный инъецируемый препарат также представляет собой стерильный инъецируемый раствор, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых сред и растворителей, которые можно применять, есть вода, раствор Рингера, раствор, соответствующий Фармакопеи США, и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла общепринято применяют в качестве растворителя или суспендирующей среды. Для этой цели можно применять любое безвкусное нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, применяют в получении инъецируемых препаратов.
[00146] Инъецируемые составы можно стерилизовать, например, фильтрованием через удерживающий бактерии фильтр, или введением стерилизующих агентов в стерильные твердые композиции, которые можно растворять или диспергировать в стерильной воде или другой стерильной инъецируемой среде перед применением.
[00147] Для того чтобы продлить эффект соединений настоящего изобретения, часто желательно замедлить поглощение соединения после подкожной или внутримышечной инъекции. Это осуществляют применением жидкой суспензии кристаллического или аморфного материала с низкой растворимостью в воде. Далее, скорость поглощения вещества будет зависеть от скорости его растворения, которая, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. Альтернативно, замедленное поглощение парентерально введенного соединения достигают растворением или суспендированием соединения в масляной среде. Инъецируемые депо-формы получают образованием микроинкапсулированного матрикса соединения в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от отношения соединения к полимеру и свойств конкретного применяемого полимера, можно контролировать скорость высвобождения соединения. Примеры других биоразлагаемых соединений включают поли(ортоэфиры) и поли(ангидриды). Депо инъецируемые составы также получают захватом соединения в липосомы или микроэмульсии, которые являются совместимыми с тканями тела.
[00148] Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые можно получить смешением соединений настоящего изобретения с подходящими нераздражающими вспомогательными веществами или носителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при комнатной температуре, но жидкими при температуре тела и, следовательно, плавятся в прямой кишке или вагинальной полости и высвобождают активное соединение.
[00149] Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В данных твердых лекарственных формах, активное соединение смешивают, по меньшей мере, с одним инертным, фармацевтически приемлемым вспомогательным веществом или носителем, таким как цитрат натрия или фосфат дикальция, и/или a) наполнителями или сухими разбавителями, такими как крахмалы, лактоза, сахароза, глюкоза, маннитол и кремниевая кислота, b) связующими, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и аравийская камедь, c) увлажняющими агентами, такими как глицерин, d) разрыхлителями, таким как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, определенные силикаты и карбонат натрия, e) агентами, замедляющими растворение, такими как парафин, f) агентами, ускоряющими поглощение, такими как четвертичные аммониевые соединения, g) смачивающими агентами, такими как, например, цетиловый спирт и моностеарат глицерина, h) абсорбентами, такими как каолин и бентонитовая глина, и i) смазывающими агентами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и их смесями. В случае капсул, таблеток и пилюль, лекарственная форма также необязательно содержит буферы.
[00150] Твердые композиции аналогичного типа можно также применять в качестве наполнителей в мягких и твердых желатиновых капсулах, применяя такие вспомогательные вещества, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и подобные. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул можно получить с покрытиями и оболочками, такими как кишечнорастворимые покрытия, и другими покрытиями, хорошо известными в области фармацевтического формулирования. Они необязательно содержат замутняющие агенты и могут быть такой композиции, что они высвобождают активный ингредиент (ингредиенты) только или предпочтительно в определенной части желудочно-кишечного тракта, необязательно, замедленным способом. Примеры заливочных композиций, которые можно применять, включают полимерные вещества и воски. Твердые композиции аналогичного типа также применяют в качестве наполнителей в мягких и твердых желатиновых капсулах, применяя такие вспомогательные вещества, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и подобные.
[00151] Активные соединения могут быть в микроинкапсулированной форме с одним или более вспомогательными веществами, как отмечалось выше. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул можно получить с покрытиями и оболочками, такими как кишечнорастворимые покрытия, покрытия с контролируемым высвобождением, и другими покрытиями, хорошо известными в области фармацевтического формулирования. В данных твердых лекарственных формах активное соединение можно смешивать, по меньшей мере, с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Данные лекарственные формы также содержат, как в нормальной практике, дополнительные вещества, отличные от инертных разбавителей, например, смазывающие агенты для таблетирования и другие агенты, способствующие таблетированию, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль, лекарственные форы необязательно также содержат буферы. Они необязательно содержат замутняющие агенты и могут также быть такой композиции, что они высвобождают активный ингредиент (ингредиенты) только или предпочтительно в определенной части желудочно-кишечного тракта, необязательно, замедленным способом. Примеры заливочных композиций, которые можно применять, включают полимерные вещества и воски.
[00152] Лекарственные формы для местного или трансдермального введения соединения настоящего изобретения включают мази, пасты, крема, лосьоны, гели, порошки, растворы, спреи, лекарственные формы для ингаляции или пластыри. Активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми требуемыми консервантами или буферами, при необходимости. Офтальмический состав, ушные капли и глазные капли также предполагаются включенными в объем настоящего изобретения. Кроме того, настоящее изобретение предполагает применение трансдермальных пластырей, которые обладают дополнительным преимуществом обеспечения контролируемой доставки соединения в тело. Данные лекарственные формы можно получить растворением или диспергированием соединения в подходящей среде. Агенты, улучшающие поглощение, также применяют для увеличения проницаемости соединения через кожу. Скорость можно контролировать или обеспечением мембраны, контролирующей скорость, или диспергированием соединения в полимерном матриксе или геле.
[00153] Согласно одному варианту осуществления, настоящее изобретение относится к способу ингибирования BTK активности в биологическом образце, включающему стадию контакта указанного биологического образца с соединением настоящего изобретения или композицией, содержащей указанное соединение.
[00154] Согласно другому варианту осуществления, настоящее изобретение относится к способу ингибирования активности BTK или ее мутанта в биологическом образце положительным способом, включающему стадию контакта указанного биологического образца с соединением настоящего изобретения или композицией, содержащей указанное соединение.
[00155] Соединения настоящего изобретения являются пригодными in-vitro в качестве уникального инструмента для понимания биологической роли BTK, включая оценку многих факторов, предполагаемых влияющими и на которые влияет продуцирование BTK и взаимодействие BTK. Настоящие соединения являются также пригодными в разработке других соединений, которые взаимодействуют с BTK, поскольку настоящие соединения дают важную информацию о связи структура-активность (SAR), которая облегчает данную разработку. Соединения настоящего изобретения, которые связываются с BTK, можно применять в качестве реагентов для детекции BTK в живых клетках, фиксированных клетках, в биологических жидкостях, в гомогенатах тканей, в очищенных, природных биологических материалах и т.д. Например, пометив данные соединения, можно обнаружить клетки, экспрессирующие BTK. Кроме того, на основе их способности связываться с BTK, соединения настоящего изобретения можно применять в in-situ окрашивании, FACS (сортировка клеток с активированной флуоресценцией), электрофорезе в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE), ELISA (твердофазный иммуноферментный анализ) и т.д., очистке ферментов, или в очистке клеток, экспрессирующих BTK внутри пермеабилизированных клеток. Соединения настоящего изобретения можно также применять в качестве коммерческих реагентов для различных медицинских исследований и диагностических применений. Данные применения включают, но не ограничиваются: применение в качестве калибровочного стандарта для количественного определения активностей потенциальных BTK ингибиторов в ряде функциональных анализов; применение в качестве блокирующих реагентов в случайном поиске соединений, т.е. в поиске новых семейств BTK лигандов можно применять соединения для блокировки улавливания заявленных в настоящем изобретении BTK соединений; применение в совместной кристаллизации с BTK ферментом, т.е. соединения настоящего изобретения будут обеспечивать образование кристаллов соединений, связанных с BTK, делая возможным определение структуры фермент/соединение рентгеноструктурным анализом; другие исследования и диагностические применения, в которых BTK предпочтительно активируется или данную активацию удобно калибровать известным количеством BTK ингибитора и т.д.; применение в анализах в качестве проб для определения экспрессии BTK в клетках; и в разработке анализов для определения соединений, которые связываются с тем же сайтом, как BTK связывающие лиганды.
[00156] Соединения настоящего изобретения можно применять или сами и/или в комбинации с физическими измерениями для диагностики эффективности лечения. Фармацевтические композиции, содержащие указанные соединения, и применение указанных соединений для лечения заболеваний, опосредованных BTK, представляет собой перспективный новых подход для широкого спектра терапий, вызывающих прямое и немедленное улучшение состояния здоровья у людей или животных. Перорально биодоступные и активные новые химические соединения настоящего изобретения повышают удобство для пациента и комплаентность для лечащего врача.
[00157] Соединения формулы (I), их соли, изомеры, таутомеры, энантиомерные формы, диастереомеры, рацематы, производные, пролекарства и/или метаболиты характеризуются высокой специфичностью и стабильностью, низкой стоимостью производства и удобным обращением. Данные признаки образуют основу для воспроизводимого действия, где включено отсутствие перекрестной реактивности, и для надежного и безопасного взаимодействия с целевой структурой.
[00158] Термин ʺбиологический образецʺ, как применяют в настоящем изобретении, включает, без ограничения, клеточные культуры или их экстракты; материал, полученный биопсией у млекопитающего или его экстрактов; и кровь, слюну, мочу, кал, сперму, слезы или другие жидкости тела или их экстракты.
[00159] Модулирование активности BTK или ее мутанта в биологическом образце является пригодным для ряда целей, которые являются известными специалисту в данной области техники. Примеры данных целей включают, но не ограничиваются, переливание крови, трансплантацию органов, хранение биологических образцов и биологические анализы.
Примеры
[00160] Как показано в примерах ниже, в определенных примерных вариантах осуществления, соединения получают согласно следующим общим способам. Ясно, что хотя общие способы показывают получение определенных соединений настоящего изобретения, следующие общие способы и другие способы, известные специалисту в данной области техники, можно применять для всех соединений и подклассов и типов каждого из данных соединений, как описано в настоящем изобретении.
[00161] Символы и допущения, применяемые в следующем описании способов, схем и примеров, соответствуют тем, что применяют в современной научной литературе, например, в the Journal of the American Chemical Society или the Journal of Biological Chemistry.
[00162] Если не указано иначе, все температуры выражены в °C (градусы Цельсия).
[00163] Все реакции проводили при комнатной температуре, если не указано иначе. Все соединения настоящего изобретения получали способами, разработанными изобретателями настоящего изобретения.
1H-ЯМР спектры регистрировали на Bruker Avance III 400. Химические сдвиги выражали в миллионных долях (м.д., δ единицы). Константы взаимодействия приведены в герцах (Гц). Структура расщепления описывает видимые мультиплетности и обозначена как с (синглет), д (дублет), т (триплет), кв (квартет), м (мультиплет) или уш (уширенный).
[00164] Масс-спектры получали на Agilent 1200 Series масс-спектрометрах от Agilent Technologies, применяя или химическую ионизацию при атмосферном давлении (APCI) или ионизацию электроспреем (ESI). Колонка: XBridge C8, 3,5 мкм, 4,6×50 мм; растворитель A: вода+0,1% TFA; растворитель B: ACN+0,1% TFA; поток: 2 мл/мин; градиент: 0 мин: 5% B, 8 мин: 100% B, 8,1 мин: 100% B, 8,5 мин: 5% B, 10 мин 5% B.
[00165] ВЭЖХ данные получали, применяя Agilent 1100 series ВЭЖХ от Agilent technologies, применяя колонку (XBridge C8, 3,5 мкм, 4,6×50 мм) и две подвижные фазы (подвижная фаза A: вода+0,1% TFA; подвижная фаза B: ACN+0,1% TFA). Скорость потока составляла 2 мл/мин. Градиентный способ представлял собой: 0 мин: 5% B; 8 мин: 100% B; 8,1 мин: 100% B; 8,5 мин: 5% B; 10 мин 5% B.
[00166] Микроволновые реакции проводили, применяя Biotage Initiator Microwave Synthesizer, применяя стандартные протоколы, которые являются известными в данной области техники.
[00167] Некоторые сокращения, которые могут появляться в данной заявке, являются следующими:
[00168] Номера соединений, применяемые в примерах ниже, соответствуют номерам соединений, приведенным выше.
[00169] Общая схема
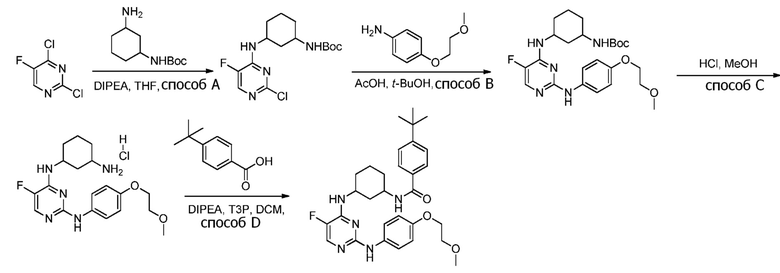
Пример 1. 4-(трет-бутил)-N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (3)
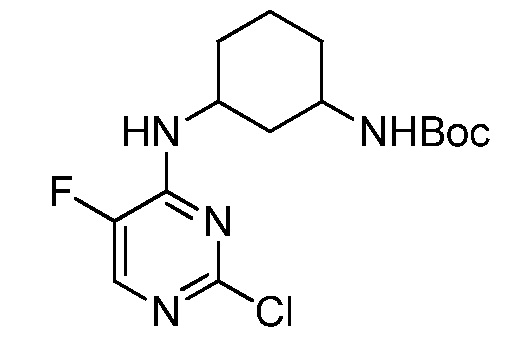
(Способ A) трет-бутил (3-((2-хлор-5-фторпиримидин-4-ил)амино)циклогексил)карбамат
[00170] В микроволновую пробирку, содержащую 2,4-дихлор-5-фторпиримидин (170,00 мг; 1,02 ммоль; 1,00 экв.) и трет-бутиловый эфир (3-аминоциклогексил)карбаминовой кислоты (218,19 мг; 1,02 ммоль; 1,00 экв.) в THF (2,00 мл; 24,69 ммоль; 24,25 экв.) добавляли DIPEA (0,37 мл; 2,24 ммоль; 2,20 экв.). Реакцию перемешивали при 60°C в течение 16 часов перед концентрированием и применением в следующую стадию без дополнительной очистки. MS: m/z=345 [M+H]+, RT= 2,80 мин.

(Способ B) трет-бутил (3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)карбамат
[00171] В микроволновую пробирку, содержащую трет-бутиловый эфир [3-(2-Хлор-5-фторпиримидин-4-иламино)циклогексил]карбаминовой кислоты (344,81 мг; 1,00 ммоль; 1,00 экв.) и 4-(2-метоксиэтокси)анилин (183,93 мг; 1,10 ммоль; 1,10 экв.) в 2-метил-бутан-2-оле (4,00 мл; 35,67 ммоль; 35,67 экв.) добавляли уксусную кислоту (6,01 мг; 0,10 ммоль; 0,10 экв.). Реакцию перемешивали при 85°C в течение 16 часов перед концентрированием и применением в следующей стадии без дополнительной очистки. MS: m/z=476 [M+H]+, RT= 3,17 мин.
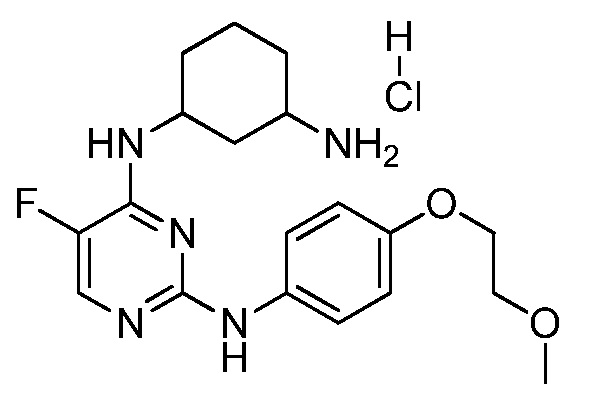
(Способ C) гидрохлорид N 4-(3-аминоциклогексил)-5-фтор- N 2-(4-(2-метоксиэтокси)фенил)пиримидин-2,4-диамина
[00172] В круглодонную колбу, содержащую трет-бутиловый эфир 3-{5-фтор-2-[4-(2-метоксиэтокси)фениламино]пиримидин-4-иламино}циклогексил)карбаминовой кислоты (475,56 мг; 1,00 ммоль; 1,00 экв.) в метаноле (6,00 мл), добавляли хлористоводородную кислоту (2,50 мл; 10,00 ммоль; 10,00 экв.). Реакцию перемешивали при комнатной температуре в течение 3 часов перед концентрированием и применением в следующей стадии без дополнительной очистки. MS: m/z=376 [M+H]+, RT= 2,01 мин
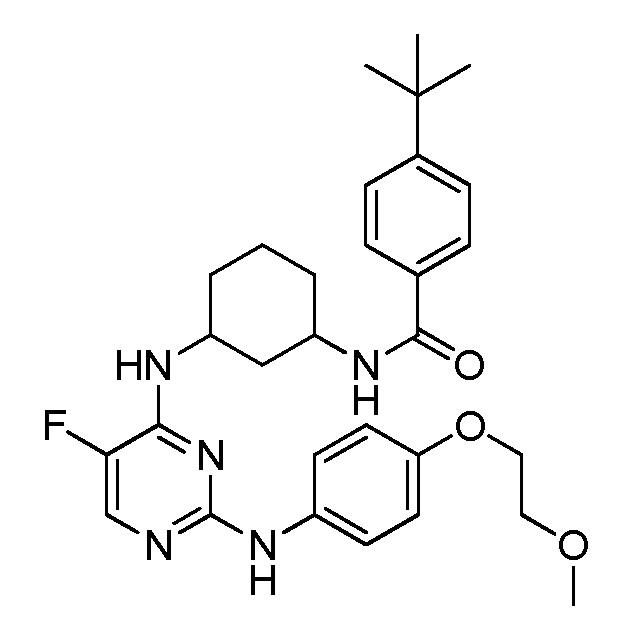
(Способ D) 4-( трет-бутил )-N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (3)
[00173] В 10 мл реакционную пробирку добавляли гидрохлорид N-(3-амино-циклогексил)-5-фтор-N2-[4-(2-метоксиэтокси)фенил]пиримидин-2,4-диамина (120,00 мг; 0,29 ммоль; 1,00 экв.), 4-трет-бутилбензойную кислоту (50,41 мкл; 0,29 ммоль; 1,00 экв.) и этилдиизопропиламин (0,31 мл; 1,75 ммоль; 6,00 экв.) в дихлорметане (4,00 мл; 58,87 ммоль; 202,07 экв.), с последующим добавлением 2,4,6-трипропил[1,3,5,2,4,6]триоксатрифосфинан 2,4,6-триоксида (233,00 мкл; 0,58 ммоль; 2,00 экв.). Реакцию перемешивали при комнатной температуре в течение 15 минут перед концентрированием и очисткой основной препаративной ВЭЖХ. Собранные фракции сушили лиофилизацией, получая белый твердый остаток (18,9 мг, 9,5%). ВЭЖХ: 95%, RT= 4,29 мин. MS: m/z=536 [M+H]+, RT= 3,54 мин. 1H-ЯМР (DMSO-D6) δ 9,66 (с, 1H), 8,25 (с, 1H), 8,04 (д, 1H), 8,00 (д, 1H), 7,77 (д, 2H), 7,50 (д, 2H), 7,84 (д, 2H), 6,92 (д, 2H), 4,30 (с, 1H), 4,22 (с, 1H), 4,43 (м, 2H),1,50-1,93 (м, 8H), 1,25 (с, 9H). Некоторые протонные пики перекрываются с пиками растворителя.
Пример 2. 4-( трет-бутил )- N -((1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)метил)бензамид (7)
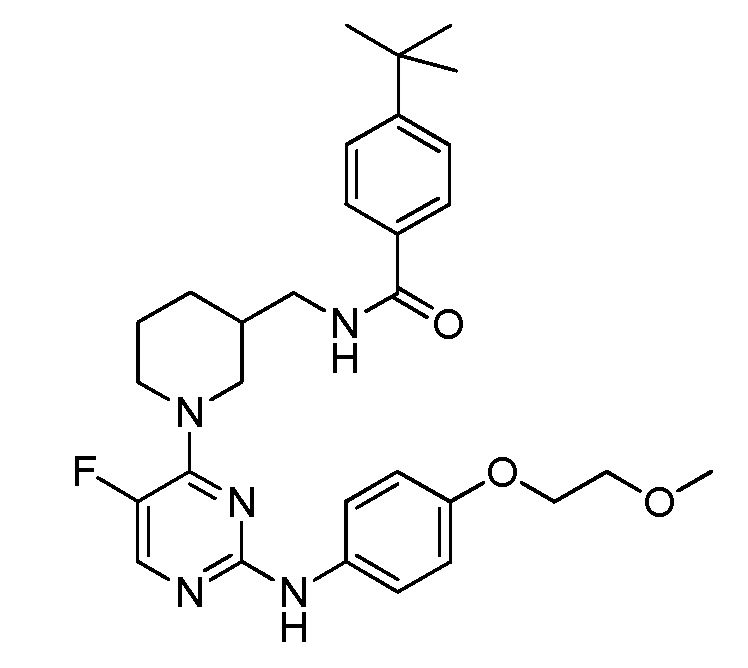
[00174] 4-(трет-бутил)-N-((1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)метил)бензамид получали из 2,4-дихлор-5-фторпиримидина, трет-бутил (пиперидин-3-илметил)карбамата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,88 мин. MS: m/z=536 [M+H]+, RT= 3,53 мин. 1H-ЯМР (DMSO-D6) δ 9,70 (с, 1H), 8,49 (м, 1H), 8,04 (д, 2H), 7,75 (д, 2H), 7,44 (м,4H) 6,82 (д, 2H), 4,26 (м, 2H), 4,02 (м, 2H), 3,61 (м, 2H), 3,30 (с, 3H), 3,25 (м, 3H), 3,01 (т, 1H), 1,81 (м, 1H), 1,74 (м, 2H), 1,52(м, 1H), 1,41 (м, 1H), 1,25 (с, 9H).
Пример 3. ( S )-4-( трет-бутил )- N -(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пирролидин-3-ил)бензамид (9)
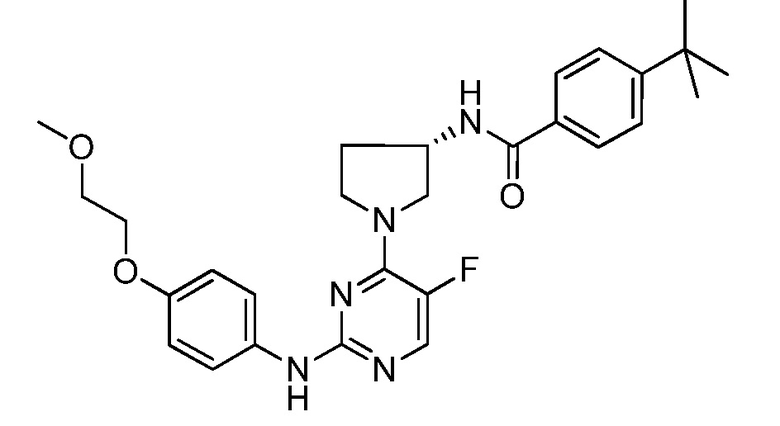
[00175] (S)-4-(трет-бутил)-N-(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пирролидин-3-ил)бензамид получали из 2,4-дихлор-5-фторпиримидина, (S)-трет-бутил пирролидин-3-илкарбамата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,77 мин. MS: m/z=508 [M+H]+, RT= 3,49 мин. 1H-ЯМР (DMSO-D6) δ 9,81 (с, 1H), 8,53 (д, 1H), 8,10 (д, 1H), 7,74 (д, 2H), 7,50 (м, 4H), 6,92(д, 2H), 4,53 (с,1H), 4,04 (м, 2H), 3,75-4,0 (м, 4H), 3,63(м, 2H), 3,25 (с, 3H), 2,25 (м, 1H), 2,08 (м, 1H), 1,25 (с, 9H).
Пример 4. (4-( трет-бутил )фенил)(5-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)гексагидропирролo[3,4-c]пиррол-2(1H)-ил)метанон (18)
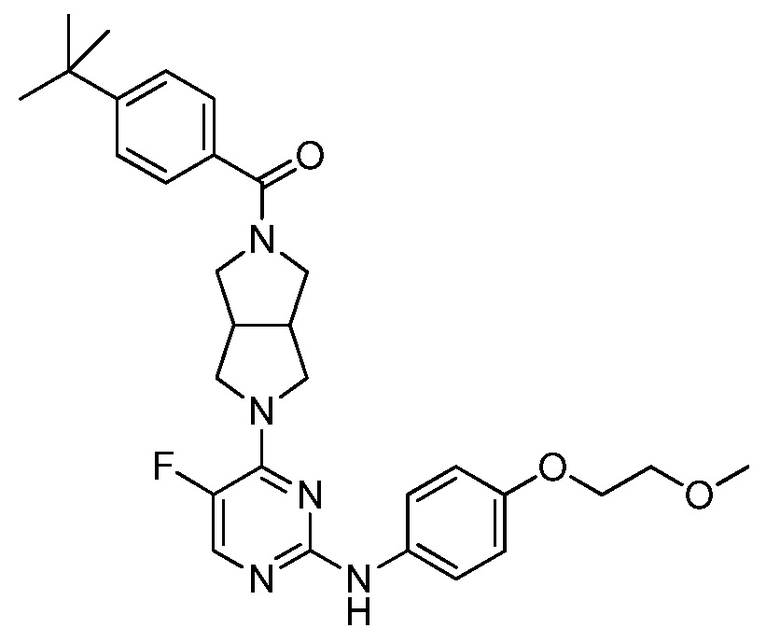
[00176] (4-(трет-бутил)фенил)(5-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)гексагидропирролo[3,4-c]пиррол-2(1H)-ил)метанон получали из 2,4-дихлор-5-фторпиримидина, трет-бутил гексагидропирролo[3,4-c]пиррол-2(1H)-карбоксилата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 97%, RT= 3,65 мин. MS: m/z=534 [M+H]+, RT= 3,38 мин. 1H-ЯМР (DMSO-D6) δ 9,52 (с, 1H), 8,01 (д, 1H), 7,48 (м, 6H), 6,89 (д, 2H), 4,02 (м, 2H), 3,26 (с, 3H), 3,0 (с, 2H), 1,25 (с, 9H). Некоторые протонные пики перекрываются с пиком растворителя.
Пример 5. 2-((3-хлорфенил)амино)- N -(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)фенил)ацетамид (4)
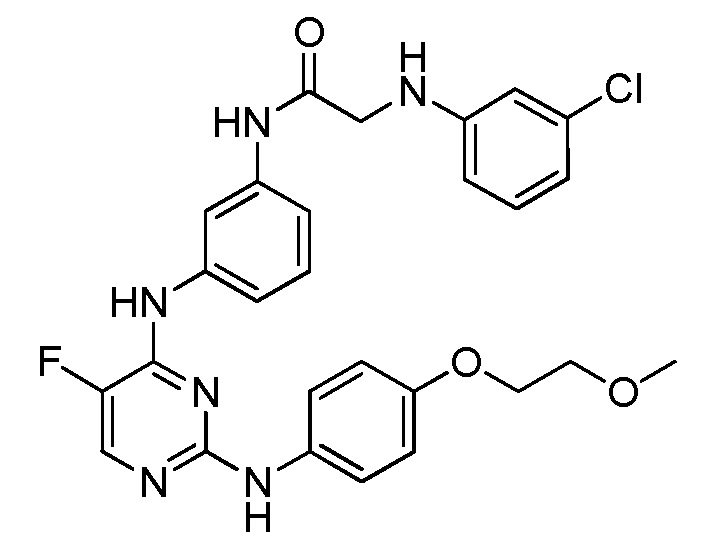
[00177] 2-((3-хлорфенил)амино)-N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)фенил)ацетамид получали из 2,4-дихлор-5-фторпиримидина, трет-бутил (3-аминофенил)карбамата, 4-(2-метоксиэтокси)анилина и 2-((3-хлорфенил)амино)уксусной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 95%, RT= 3,95 мин. MS: m/z=538[M+H]+, RT= 3,31 мин. 1H-ЯМР (DMSO-D6) δ 10,07 (с, 1H), 9,94 (с, 1H), 9,47 (с, 1H), 8,22 (м, 1H), 7,85 (м, 1H), 7,50 (м, 3H), 7,25 (м, 2H), 7,10 (т, 1H), 6,77 (д, 2H), 6,65 (м, 3H), 4,02 (м, 2H), 3,80 (с, 2H), 3,61 (м, 2H), 3,25 (с, 3H).
Пример 6. 4-( трет-бутил )- N -((1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пирролидин-3-ил)метил)бензамид (17)
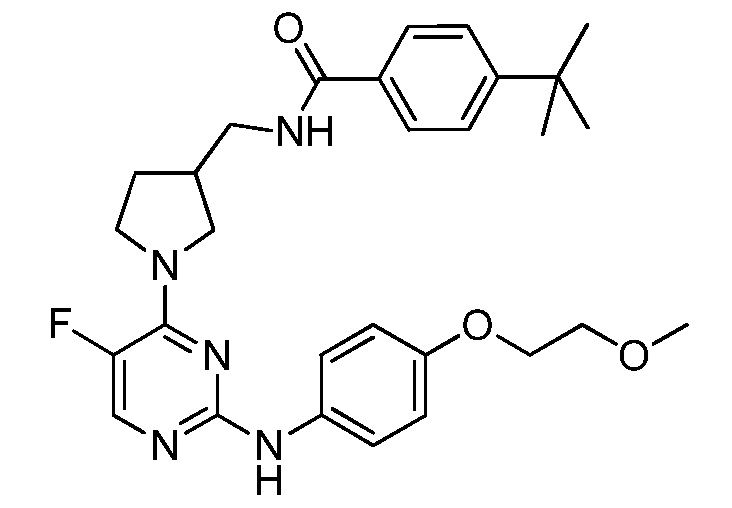
[00178] 4-(трет-бутил)-N-((1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пирролидин-3-ил)метил)бензамид получали из 2,4-дихлор-5-фторпиримидина, трет-бутил (пирролидин-3-илметил)карбамата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,75 мин. MS: m/z=522[M+H]+, RT= 3,48 мин. 1H-ЯМР (DMSO-D6) δ 9,74 (с, 1H), 8,58 (м, 1H), 9,01 (д, 1H), 7,77 (д, 2H), 7,48 (м, 4H), 6,81 (д, 2H), 4,02 (м, 2H), 3,77 (м, 2H), 3,45 (м, 4H), 3,30 (м, 2H), 3,25 (с, 3H), 2,57 (м, 1H), 2,03 (м, 1H), 1,75 (м, 1H), 1,25 (с, 9H).
Пример 7. (4-(трет-бутил)фенил)(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)гексагидропирролo[3,4-b]пиррол-5(1H)-ил)метанон (20)
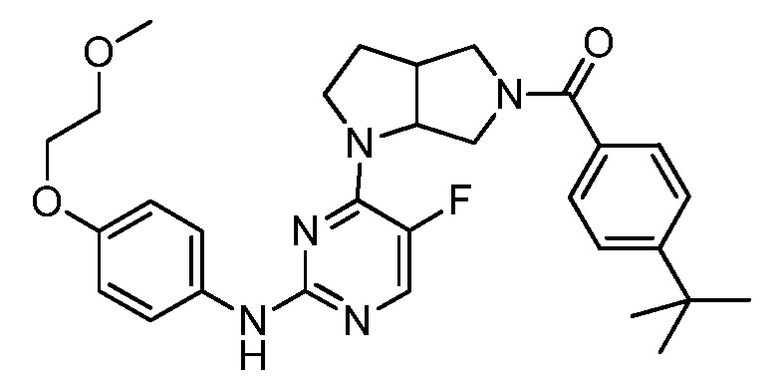
[00179] (4-(трет-бутил)фенил)(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)гексагидропирролo[3,4-b]пиррол-5(1H)-ил)метанон получали из 22,4-дихлор-5-фторпиримидина, трет-бутил гексагидропирролo[3,4-b]пиррол-5(1H)-карбоксилата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,33 мин. MS: m/z=534[M+H]+, RT= 3,77 мин. 1H-ЯМР (DMSO-D6) δ 8,77 (д, 1H), 7,90 (д, 1H), 7,50 (м, 6H),6,75 (м, 2H), 4,53 (д, 1H), 4,01 (м, 2H), 3,5-3,77 (м, 8H), 3,25 (с, 3H), 3,0 (м, 1H), 2,04 (м, 1H), 1,75 (м, 1H), 1,25 (м, 9H).
Пример 8. 4-(трет-бутил)-N-(транс-3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (19); 4-(трет-бутил)-N-((1R,3R)-3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (22); 4-(трет-бутил)-N-((1S,3S)-3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (23)
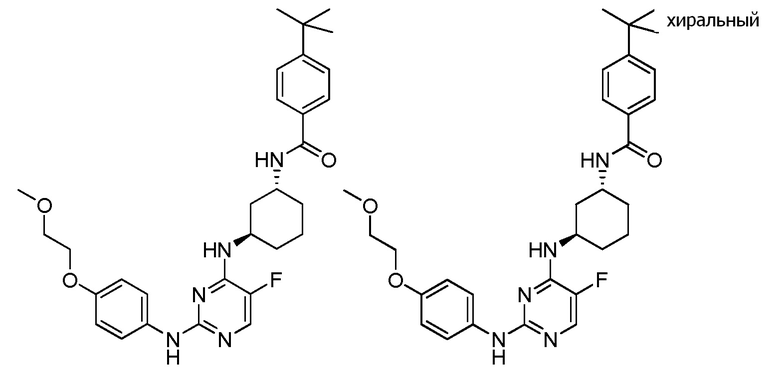
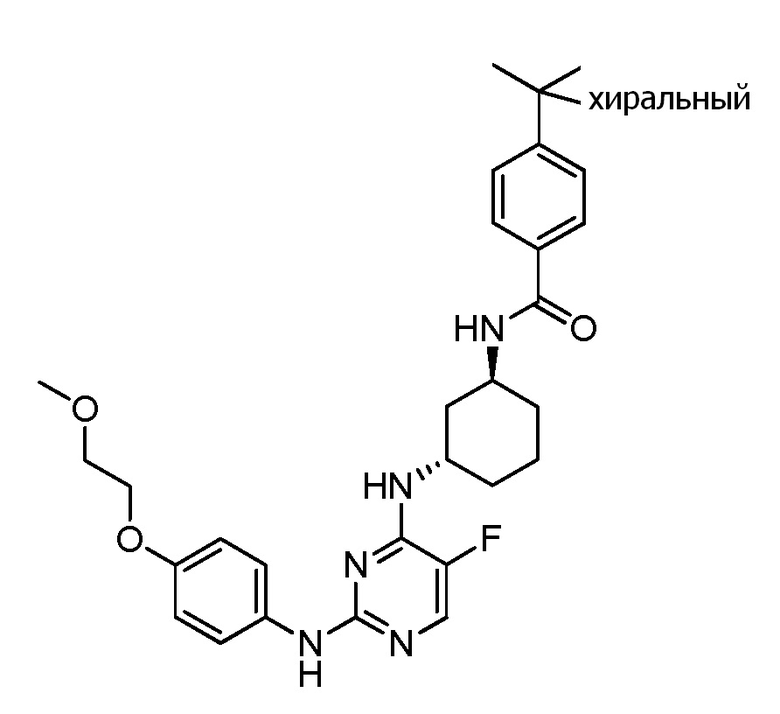
Соединения 19, 22 и 23 выделяли из реакционной смеси, полученной в примере 1. Данные хиральной ВЭЖХ получали AC_SEMIPREP-SFC системой, применяя колонку (IF колонку) и две подвижные фазы (подвижная фаза A: вода+0,1% NH4OH, подвижная фаза B: EtOH). Разделение осуществляли при 55% изократической системе со скоростью потока 8 мл/мин. (1R, 3R) хиральная ВЭЖХ: чистота 99%, RT=6,24 мин. (1S, 3S) хиральная ВЭЖХ: чистота 99%, RT=6,94 мин.
Пример 9. (4-( трет-бутил )фенил)(8-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)-2,8-диазаспиро[5.5]ундекан-2-ил)метанон (21)
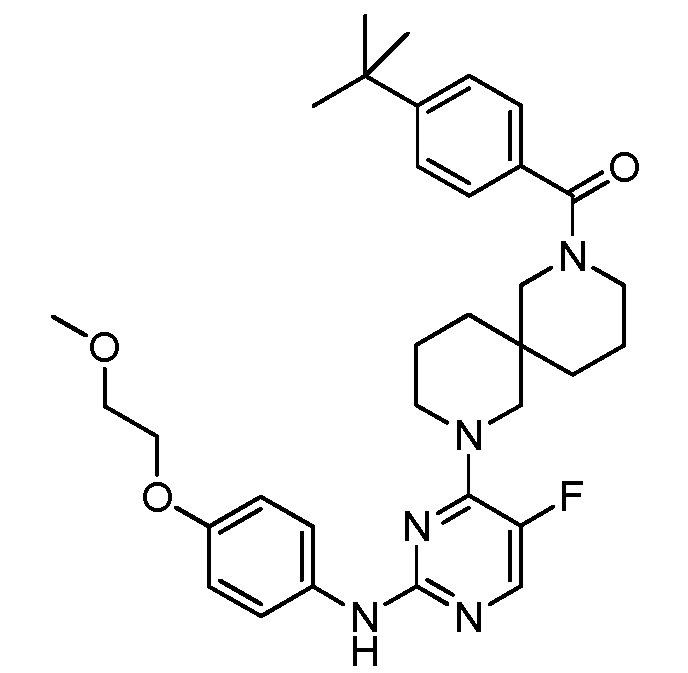
[00180] (4-(трет-бутил)фенил)(8-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)-2,8-диазаспиро[5.5]ундекан-2-ил)метанон получали из 2,4-дихлор-5-фторпиримидина, трет-бутил 2,8-диазаспиро[5.5]ундекан-2-карбоксилата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,77 мин. MS: m/z=576[M+H]+, RT= 3,66 мин. 1H-ЯМР (DMSO-D6) δ 8,87 (с, 1H), 7,82 (д, 1H), 7,57 (д, 2H), 7,34 (м, 4H), 6,65 (д, 2H), 4,0 (м, 2H), 3,75 (м, 2H), 3,59 (м, 2H), 3,25 (с, 3H), 1,5 (м, 8H), 1,25 (с, 9H). Некоторые протонные пики перекрываются с пиком растворителя.
Пример 10. (4-( трет-бутил )фенил)(3-(((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)метил)пирролидин-1-ил)метанон (8)
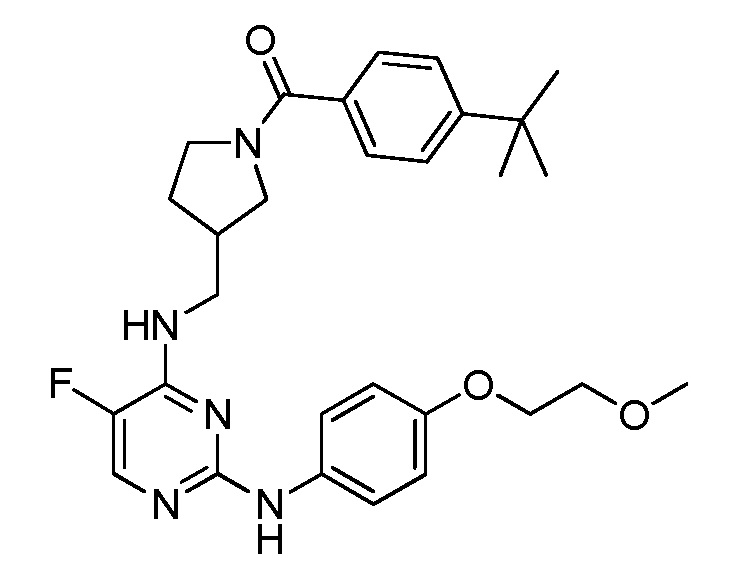
[00181] (4-(трет-бутил)фенил)(3-(((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)метил)пирролидин-1-ил)метанон получали из 2,4-дихлор-5-фторпиримидина, трет-бутил 3-(аминометил)пирролидин-1-карбоксилата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,52 мин. MS: m/z=522[M+H]+, RT= 3,28 мин. 1H-ЯМР (DMSO-D6) δ 9,75 (м, 1H), 8,75 (м, 1H), 8,01 (м, 1H), 7,50 (м, 7H), 6,91 (м, 2H), 4,05 (м, 2H), 3,57 (м, 2H), 3,25 (с, 1H), 2,0 (м, 1H), 1,62 (м, 1H), 1,25 (с, 9H). Некоторые протонные пики перекрываются с пиком растворителя.
Пример 11. (4-( трет-бутил )фенил)(7-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино) пиримидин-4-ил)-2,7-диазаспиро[4.5]декан-2-ил)метанон (15)
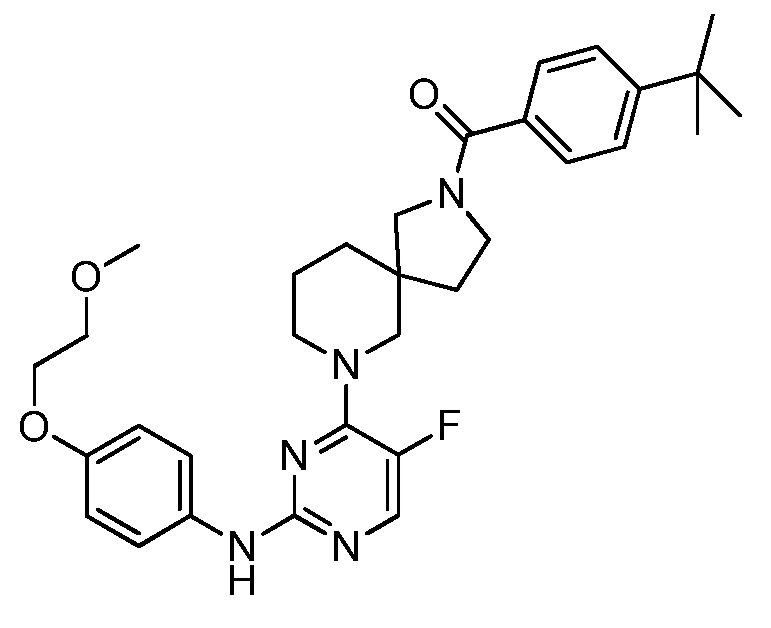
[00182] (4-(трет-бутил)фенил)(7-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)-2,7-диазаспиро[4.5]декан-2-ил)метанон получали из 2,4-дихлор-5-фторпиримидина, трет-бутил 2,7-диазаспиро[4.5]деканe-2-карбоксилата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 3,78 мин. MS: m/z=562[M+H]+, RT= 3,47 мин. 1H-ЯМР (DMSO-D6) δ 8,91 (д, 1H), 7,90 (дд, 1H), 7,52 (дд, 2H), 7,37 (м, 4H), 6,81 (д, 2H), 4,0 (м, 2H), 3,50-3,75 (м, 9H), 3,25 (м, 3H), 3,20 (м, 1H), 1,56-1,80 (м, 6H), 1,25 (м, 9H).
Пример 12. 4-( трет-бутил )- N -(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)-2-гидроксициклогексил)бензамид (16)
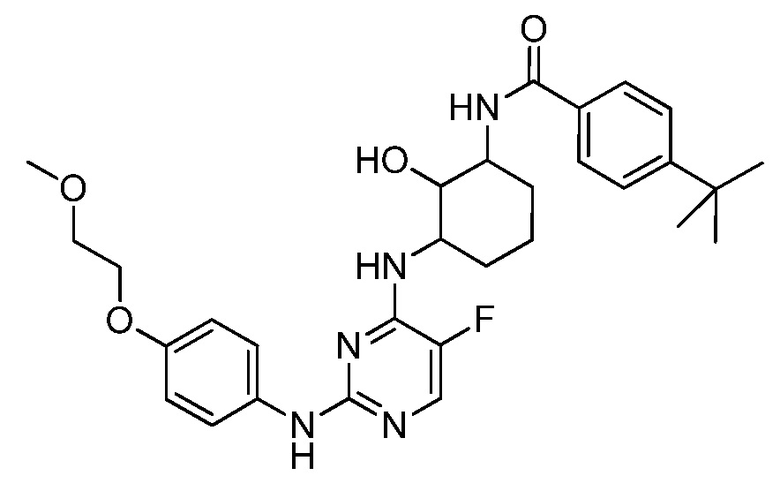
[00183] 4-(трет-бутил)-N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)-2-гидроксициклогексил)бензамид получали из 2,4-дихлор-5-фторпиримидина, трет-бутил (3-амино-2-гидроксициклогексил)карбамата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 98%, RT= 3,57 мин. MS: m/z=552[M+H]+, RT= 1,67 мин. 1H-ЯМР (DMSO-D6) δ 9,77 (с, 1H), 8,79 (с, 1H), 8,01 (д, 1H), 7,76 (д, 2H), 7,61 (д, 1H), 7,50 (д, 2H), 7,47(д, 2H), 6,88 (д, 2H), 4,25 (м, 2H), 4,01 (м, 2H), 3,81 (м, 1H), 3,61 (м, 2H), 3,24 (с, 3H), 1,81 (м, 2H), 1,50-1,75 (м, 4H), 1,25 (с, 9H).
Пример 13. ( R )-4-( трет-бутил )- N -(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)бензамид (1)
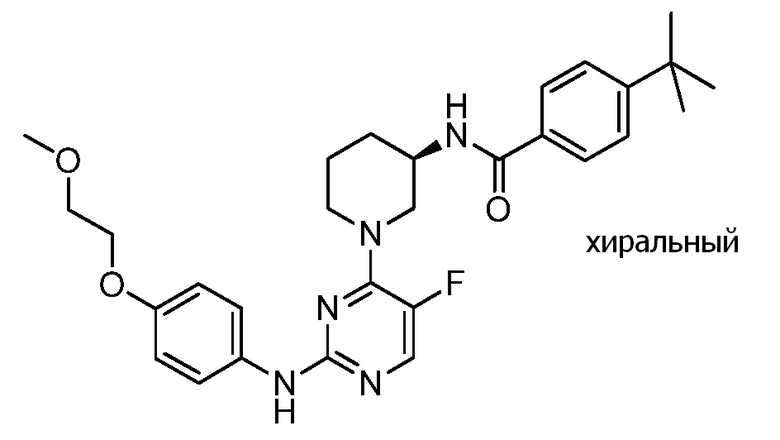
[00184] (R)-4-(трет-бутил)-N-(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)бензамид получали из 2,4-дихлор-5-фторпиримидина, (R)-трет-бутил пиперидин-3-илкарбамата, 4-(2-метоксиэтокси)анилина и 4-(трет-бутил)бензойной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 100%, RT= 4,30 мин. MS: m/z=522[M+H]+, RT= 3,52 мин. 1H-ЯМР (DMSO-D6) δ 9,39 (с, 1H), 8,30 (д, 1H), 8,03 (д, 1H), 7,76 (д, 2H), 7,46 (м, 4H), 6,79 (д, 2H), 3,53 (м, 2H), 3,14 (м, 1H), 1,92 (м, 2H), 1,62 (м, 2H), 1,25 (с, 9H). Некоторые протонные пики перекрываются с пиком растворителя.
Пример 14. ( R )-2-((3-хлорфенил)амино)- N -(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)ацетамид (2)
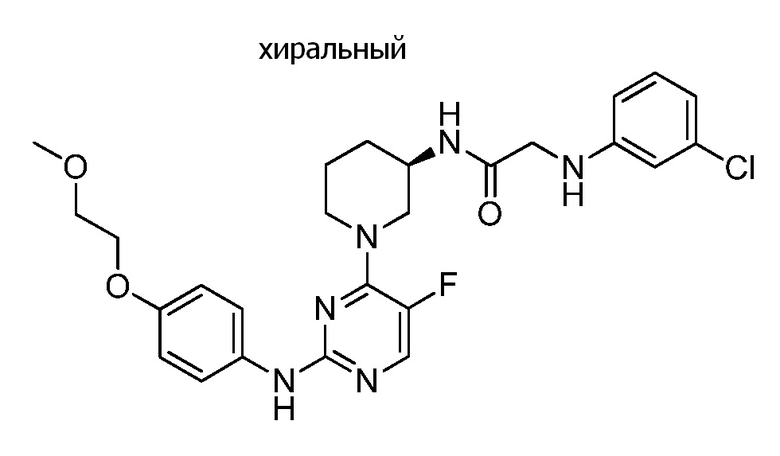
[00185] (R)-2-((3-хлорфенил)амино)-N-(1-(5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)пиперидин-3-ил)ацетамид получали из 2,4-дихлор-5-фторпиримидина, (R)-трет-бутил пиперидин-3-илкарбамата, 4-(2-метоксиэтокси)анилина и 2-((3-хлорфенил)амино)уксусной кислоты, применяя способы, описанные в способах A, B, C и D. ВЭЖХ: 98%, RT= 3,66 мин. MS: m/z=530[M+H]+, RT= 3,14 мин. 1H-ЯМР (DMSO-D6) δ 9,44 (с, 1H), 8,0 (м, 2H), 7,46 (д, 2H), 7,11 (м, 1H), 6,70 (д, 2H), 6,51 (м, 3H), 4,13 (д, 1H), 4,0 (м, 4H), 3,63 (м, 4H), 3,34 (м, 1H), 3,25 (с, 3H), 3,21 (м, 1H), 1,75 (м, 2H), 1,52 (м, 2H).
Пример 15. 4-циклопропил-N-(3-((5-фтор-2-((4-(2-метоксиэтокси)фенил)амино)пиримидин-4-ил)амино)циклогексил)бензамид (10)
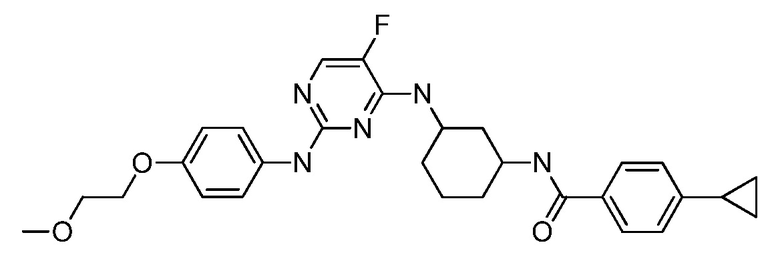
[00186] Заявленное в заголовке соединение получали способом, аналогичным способу, описанному выше, применяя гидрохлорид 4-(3-аминоциклогексил)-5-фтор-N2-[4-(2-метокси-этокси)фенил]пиримидин-2,4-диамина (0,24 ммоль; 1,00 экв.; 100,00 мг) и 4-циклопропилбензойную кислоту (0,27 ммоль; 1,10 экв.; 43,31 мг), получая 42 мг (32%) MS: m/z=520 [M+H]+, 1H ЯМР (400 МГц, хлороформ-d) δ 7,78 (д, J=3,2 Гц, 1H), 7,66 (д, J=8,0 Гц, 2H), 7,56-7,28 (м, 2H), 7,12 (д, J=8,1 Гц, 2H), 6,99-6,83 (м, 2H), 6,63 (с, 1H), 6,07 (д, J=7,5 Гц, 1H), 5,01 (д, J=7,1 Гц, 1H), 4,49-4,32 (м, 2H), 4,07 (дд, J=5,5, 4,0 Гц, 2H), 3,74 (дд, J=5,4, 4,1 Гц, 2H), 3,47 (с, 2H), 2,12-1,87 (м, 6H), 1,16-0,93 (м, 2H), 0,89-0,59 (м, 2H).
Пример 16. 4-диметиламино-N-(3-{5-фтор-2-[4-(2-метокси-этокси)фениламино]пиримидин-4-иламино}циклогексил)бензамид (11)
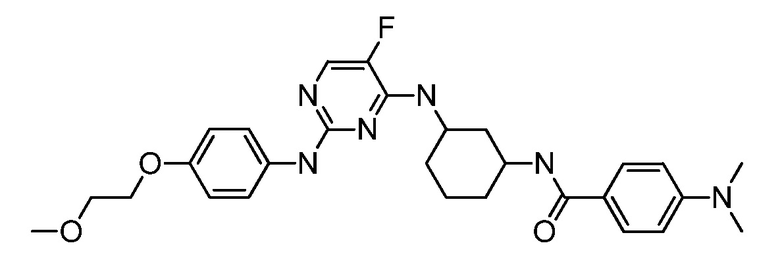
[00187] Заявленное в заголовке соединение получали способом, аналогичным способу, описанному выше, применяя гидрохлорид N4-(3-амино-циклогексил)-5-фтор-N2-[4-(2-метоксиэтокси)фенил]пиримидин-2,4-диамина (0,24 ммоль; 1,00 экв.; 100,00 мг) и 4--диметиламинобензойную кислоту (0,27 ммоль; 44,11 мг, 1,10 экв.), получая 40 мг (30%). %) MS: m/z=523 [M+H]+, 1H ЯМР (400 МГц, хлороформ-d) δ 7,77 (д, J=3,2 Гц, 1H), 7,73-7,62 (м, 2H), 7,52-7,37 (м, 2H), 6,96-6,80 (м, 2H), 6,79-6,62 (м, 3H), 6,00 (д, J=7,5 Гц, 1H), 5,19-4,89 (м, 1H), 4,37 (дт, J=12,9, 6,2 Гц, 2H), 4,19-3,97 (м, 2H), 3,73 (дд, J=5,6, 4,0 Гц, 2H), 3,46 (д, J=0,9 Гц, 3H), 3,04 (с, 5H), 2,10-1,88 (м, 2H), 1,83-1,44 (м, 7H).
Пример 17. N-(3-{5-Фтор-2-[4-(2-метоксиэтокси)фениламино]пиримидин-4-иламино}циклогексил)-4-(1-гидрокси-1-метилэтил)бензамид (12)
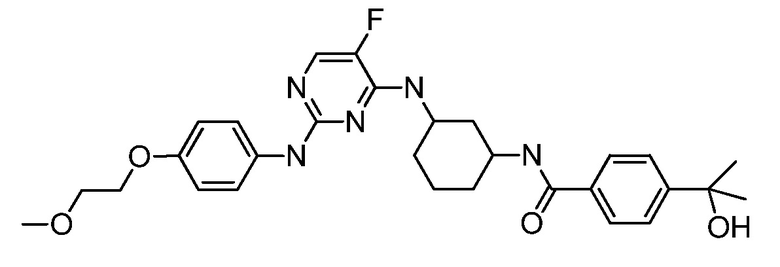
[00188] Заявленное в заголовке соединение получали способом, аналогичным способу, описанному выше, применяя гидрохлорид N4-(3-аминоциклогексил)-5-фтор-N2-[4-(2-метоксиэтокси)фенил]пиримидин-2,4-диамина (0,24 ммоль; 1,00 экв.; 100,00 мг) и 4-(1-гидрокси-1-метилэтил)бензойную кислоту (0,27 ммоль; 1,10 экв.; 48,12 мг), получая 36,00 мг (27%). MS: m/z=538 [M+H]+, 1H ЯМР (400 МГц, хлороформ-d) δ 7,87-7,68 (м, 3H), 7,55 (д, J=8,0 Гц, 2H), 7,43 (д, J=8,7 Гц, 2H), 7,29 (д, J=1,1 Гц, 1H), 6,65 (с, 1H), 6,14 (д, J=7,5 Гц, 1H), 4,98 (д, J=7,4 Гц, 1H), 4,58-4,29 (м, 2H), 4,03 (дд, J=5,7, 3,9 Гц, 2H), 3,87-3,63 (м, 2H), 3,46 (д, J=1,1 Гц, 3H), 2,24-1,87 (м, 4H), 1,60 (д, J=6,1 Гц, 18H).
Пример 18. 2-(4-трет-бутилфенил)-N-(3-{5-фтор-2-[4-(2-метоксиэтокси)фениламино]пиримидин-4-иламино}циклогексил)ацетамид (13)
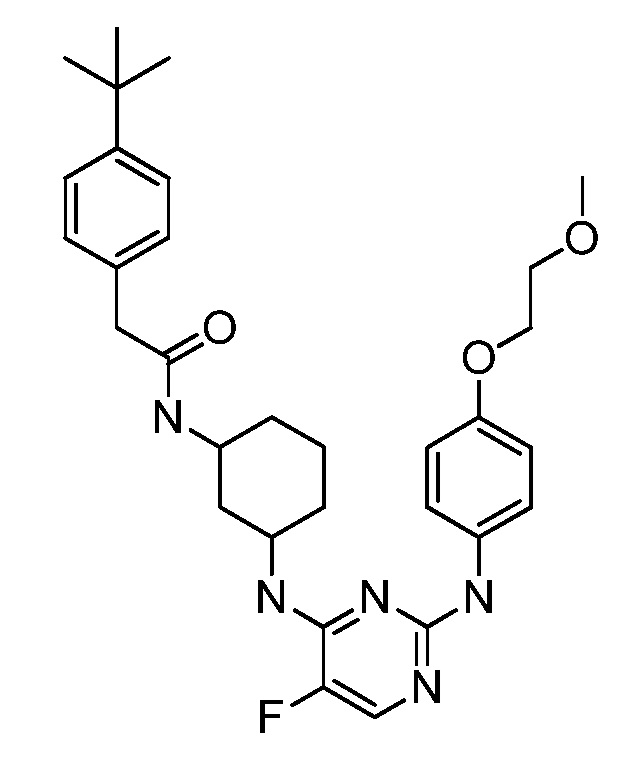
[00189] Заявленное в заголовке соединение получали способом, аналогичным способу, описанному выше, применяя гидрохлорид N4-(3-аминоциклогексил)-5-фтор-N2-[4-(2-метоксиэтокси)фенил]пиримидин-2,4-диамина (0,24 ммоль; 1,00 экв.; 100,00 мг) и (4-трет-бутилфенил)уксусную кислоту (0,27 ммоль; 1,10 экв.; 51,34 мг), получая 36,00 мг (25%). MS: m/z=538 [M+H]+, 1H ЯМР (400 МГц, хлороформ-d) δ 7,77 (д, J=3,3 Гц, 1H), 7,50-7,36 (м, 4H), 7,19 (д, J=7,9 Гц, 2H), 7,06-6,86 (м, 2H), 6,63 (с, 1H), 5,39 (д, J=7,7 Гц, 1H), 4,95 (д, J=7,2 Гц, 1H), 4,25-4,03 (м, 4H), 3,93-3,73 (м, 2H), 3,47 (д, J=0,9 Гц, 3H), 2,04-1,62 (м, 3H), 1,40-1,20 (м, 11H).
Пример 19. (3-{5-фтор-2-[4-(2-метоксиэтокси)фениламино]пиримидин-4-иламино}циклогексил)амид 2-Фенилоксазол-4-карбоновой кислоты (14)
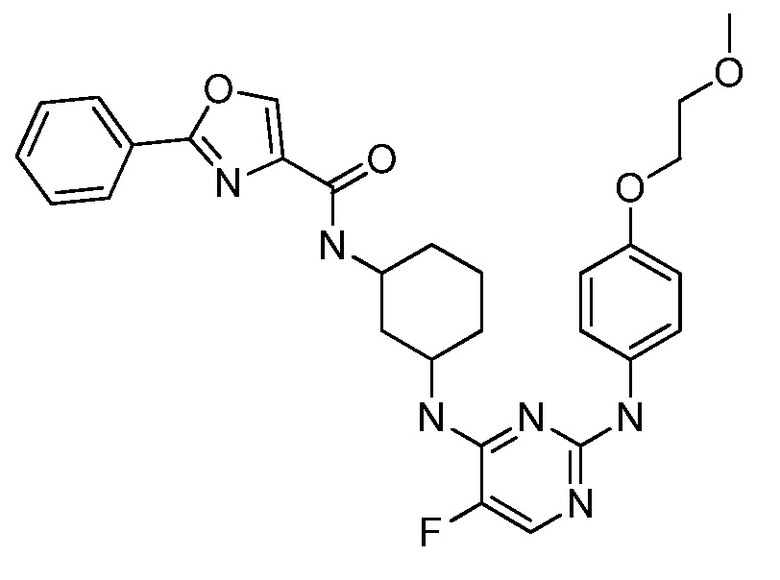
[00190] Заявленное в заголовке соединение получали способом, аналогичным способу, описанному выше, применяя гидрохлорид N4-(3-аминоциклогексил)-5-фтор-N2-[4-(2-метоксиэтокси)фенил]пиримидин-2,4-диамина (0,24 ммоль; 1,00 экв.; 100,00 мг) и 2--фенилоксазол-4-карбоновую кислоту (0,27 ммоль; 1,10 экв.; 50,52 мг), получая 31,00 мг (23%). MS: m/z=547 [M+H]+, 1H ЯМР (400 МГц, хлороформ-d) δ 8,26 (д, J=1,0 Гц, 1H), 8,19-8,01 (м, 2H), 7,79 (дд, J=3,4, 1,0 Гц, 1H), 7,63-7,38 (м, 6H), 7,12 (д, J=8,0 Гц, 1H), 7,01-6,76 (м, 2H), 6,66 (с, 1H), 5,02 (д, J=7,1 Гц, 1H), 4,42-4,33 (м, 2H), 4,06 (дд, J=5,8, 3,9 Гц, 2H), 3,84-3,60 (м, 2H), 3,45 (д, J=1,0 Гц, 3H), 2,00 (ддт, J=24,4, 11,0, 6,1 Гц, 3H), 1,88-1,43 (м, 10H).
Пример 20
Анализ A: протокол микрофлюидного внешнего анализа изменения подвижности для оценки активности относительно BTK фермента
[00191] Протокол ниже описывает микрофлюидный внешний анализ изменения подвижности для измерения специфической активности соединений относительно BTK фермента. Принцип способа исследования лучше всего описан поставщиком (Caliper Life Sciences, a PerkinElmer Company, Hopkinton, MA) на его веб-сайте по следующему адресу:
http://caliperls.com/ или http://caliperls.com/apps/drug-discovery-and-pre-clinical-development/target-id-validation.htm.
[00192] Вкратце, 2,5X исходные растворы полноразмерной человеческой BTK (08-080) от CarnaBio USA, Inc., Natick, MA, 1,6X АТФ и подходящего kinKDR пептидного субстрата (FITC-AHA-EEPLYWSFPAKKK-NH2; разработанный для внутреннего пользования) получали в буфере для киназной реакции, состоящем из 25 мМ MgCl2, 0,015% Brij-35 (30%), 100 мМ Hepes, pH 7,5 и 10 мМ DTT.
[00193] 5 мкл буфера фермента и 7,5 мкл смеси АТФ/kinKDR пептидного субстрата добавляли в Matrix (#115304) 384-луночные, стерильные, полипропиленовые планшеты (Thermo Fisher Scientific, Hudson, NH) с 125 нл последовательно разбавленных соединений, полученных в 100% DMSO, и выдерживали в течение 90 мин при 27°C. После периода выдерживания, реакции останавливали добавлением 60 мкл останавливающего буфера, состоящего из 100 мМ Hepes, pH 7,5, 0,015% Brij-35 (30%), 0,277% покрывающего реагента #3 (Caliper Life Sciences, Mountain View, CA), 5% DMSO. Остановленные реакции отслеживали при -2 PSI, -3000 В/-700 В в LabChip 3000 планшет-ридере от Caliper Life Sciences, PerkinElmer Company (Hopkinton, MA), и активность измеряли внешним анализом изменения подвижности, измеряя разницу заряд/масса между субстратом и продуктом, являющимся результатом фосфорилирования пептида. IC50 и эффективность определяли построением графика log [ингибитор] относительно % активности в GeneData Screener (Basel, Switzerland).
Анализ B: протокол микрофлюидного внешнего анализа изменения подвижности для оценки активности относительно BTK C481S фермента
[00194] Протокол ниже описывает микрофлюидный внешний анализ изменения подвижности для измерения специфической активности соединений относительно BTK C481S фермента. Принцип способа исследования лучше всего описан поставщиком (PerkinElmer, Hopkinton, MA) на его веб-сайте по следующему адресу: http://caliperls.com.
[00195] Вкратце, 2,5X исходные растворы His-TEV-hsBTK(328-659)(C481S) от the Merck Serono Protein Purification Laboratory in Darmstadt, Germany (PCS, Q27/234), 1,6X АТФ и подходящего KinKDR пептидного субстрата (FITC-AHA-EEPLYWSFPAKKK-NH2; Tufts University Core Facility заказной синтез) получали в буфере для киназной реакции, состоящем из 25 мМ MgCl2, 0,015% Brij-35 (30%), 100 мМ HEPES, pH 7,5 и 10 мМ DTT.
5 мкл буфера для фермента и 7,5 мкл смеси АТФ/KinKDR пептидный субстрат добавляли в Matrix (#4315) 384-луночные, стерильные, плоскодонные полипропиленовые планшеты (Thermo Fisher Scientific, Hudson, NH) с 125 нл последовательно разбавленными соединениями, полученными в 100% DMSO, и выдерживали в течение 90 мин при 25°C. После периода выдерживания, реакции прекращали добавлением 65 мкл останавливающего буфера, состоящего из 100 мМ HEPES, pH 7,5, 0,015% Brij-35 (30%), 0,277% покрывающего реагента #3 (PerkinElmer, Mountain View, CA), 5% DMSO. Остановленные реакции отслеживали при -2 PSI, -3000 В/-700 В в LabChip 3000 планшет-ридере от Caliper Life Sciences, a PerkinElmer Company (Hopkinton, MA), и активность количественно определяли индуцированной лазером флуоресценцией, измеряя разницу заряд/масса между субстратом и продуктом, являющимся результатом фосфорилирования пептида. IC50 и эффективность определяли построением графика log [ингибитор] относительно % активности в GeneData Screener (Basel, Switzerland).
Анализ C: зависящий от времени PMBC IC50 анализ
[00196] Btk является важным для посредничества передачи сигнала B-клеточным антигенным рецептором (BCR) после анти-IgM стимуляции. На основе данного принципа, функциональный клеточный анализ разрабатывали для определения эффективности соединений по ингибированию экспрессии, вызванной анти-IgM, CD69, последующего BCR сигнального события, в свежевыделенных мононуклеарных клетках периферической крови человека (PBMC). В данном анализе, 90 мкл суспензии PBMC, содержащей 2,5x105 клеток, предварительно обрабатывали 10 мкл испытуемого соединения при различных концентрациях в течение одного часа, и затем выдерживали в течение ночи (приблизительно 16-18 часов) с 5 мкл 420 мкл/мл affiniPure F(ab´)2 фрагмента козьего антитела к IgM Fc фрагменту человека на лунку (Dianova, Cat.No.: 109-006-129). После выдерживания, клетки промывали и иммуноокрашивали APC-меченным мышиным анти-человеческим CD69 (BD Biosciences; клон: FN50), PerCP-Cy5,5 меченным мышиным анти-человеческим CD19 (BD Biosciences; клон: SJ25C1) и FITC-меченным мышиным анти-человеческим CD3 (BD Biosciences; клон: HIT3a), и фиксировали для проточного цитометрического анализа CD69 экспрессии на CD19 положительных клетках (B клетки). Процент CD19 положительных клеток, экспрессирующих CD69, наносили на график относительно концентраций испытуемых соединений, получая кривую зависимости эффекта от концентрации, и рассчитывали IC50 величину в качестве меры активности испытуемых соединений в данном анализе.
[00197] Данные интерпретируются согласно следующему:
+ > 5 мкМ;
++ >1-5 мкМ;
+++ > 100 нМ-1 мкМ;
++++ < 100 нМ.
Пример 21. Фармацевтические препараты
[00198] (A) Инъекционные флаконы: раствор 100 г активного ингредиента согласно настоящему изобретению и 5 г гидрофосфата динатрия в 3 л бидистиллированной воды доводили до pH 6,5, применяя 2 N хлористоводородную кислоту, стерильно фильтровали, переносили в инъекционные флаконы, лиофилизировали в стерильных условиях и герметично закрывали в стерильных условиях. Каждый инъекционный флакон содержал 5 мг активного ингредиента.
[00199] (B) Суппозитории: смесь 20 г активного ингредиента согласно настоящему изобретению плавили с 100 г соевого лецитина и 1400 г масла какао, выливали в формы и охлаждали. Каждый суппозиторий содержал 20 мг активного ингредиента.
[00200] (C) Раствор: раствор получали из 1 г активного ингредиента согласно настоящему изобретению, 9,38 г NaH2PO4⋅2H2O, 28,48 г Na2HPO4⋅12H2O и 0,1 г хлорида бензалкония в 940 мл бидлистиллированной воды. pH доводили до 6,8, и раствор доводили до 1 л и стерилизовали облучением. Данный раствор можно применять в качестве глазных капель.
[00201] (D) мазь: 500 мг активного ингредиента согласно настоящему изобретению смешивали с 99,5 г вазелина в асептических условиях.
[00202] (E) таблетки: смесь 1 кг активного ингредиента согласно настоящему изобретению, 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния прессовали, получая таблетки общепринятым способом так, что каждая таблетка содержала 10 мг активного ингредиента.
[00203] (F) таблетки с покрытием: таблетки прессовали аналогично примеру E, и затем наносили покрытие общепринятым способом с покрытием из сахарозы, картофельного крахмала, талька, трагаканта и красителя.
[00204] (G) капсулы: 2 кг активного ингредиента согласно настоящему изобретению вводили в твердые желатиновые капсулы общепринятым способом так, что каждая капсула содержала 20 мг активного ингредиента.
[00205] (H) Ампулы: раствор 1 кг активного ингредиента согласно настоящему изобретению в 60 л бидистиллированной воды стерильно фильтровали, переносили в ампулы, лиофилизировали в стерильных условиях и герметично закрывали в стерильных условиях. Каждая ампула содержала 10 мг активного ингредиента.
[00206] (I) спрей для ингаляции: 14 г активного ингредиента согласно настоящему изобретению растворяли в 10 л изотонического NaCl раствора, и раствор переносили в имеющиеся в продаже контейнеры для спрея с насосным механизмом. Раствор можно распылять во рту или носу. Одно впрыскивание спрея (приблизительно 0,1 мл) соответствовал дозе приблизительно 0,14 мг.
Тогда как ряд вариантов осуществления настоящего изобретения описан в настоящем изобретении, ясно, что основные примеры можно изменять, получая другие варианты осуществления, в которых применяют соединения и способы настоящего изобретения. Следовательно, ясно, что объем настоящего изобретения должен определяться прилагаемой формулой изобретения, а не конкретными вариантами осуществления, которые представлены в качестве примера.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРИДИНЫ, ПИРИМИДИНЫ И ПИРАЗИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ БРУТОНА И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2712220C2 |
| ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ IRAK II ТИПА И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2810338C2 |
| ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2636584C2 |
| ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2734822C2 |
| ПИРАЗОЛО[1,5-a]ПИРИМИДИНЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2005 |
|
RU2417996C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ ЭНДОСОМАЛЬНЫХ TOLL-ПОДОБНЫХ РЕЦЕПТОРОВ | 2017 |
|
RU2759678C2 |
| СОЕДИНЕНИЯ ПУРИНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2013 |
|
RU2655388C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЙ ПИРИМИДИНА И ПИРИДИНА С BTK ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 2016 |
|
RU2779287C2 |
| МАКРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ IRAK1/4 ИНГИБИТОРОВ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2730016C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЙ ПИРИМИДИНА И ПИРИДИНА С BTK ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 2016 |
|
RU2765154C2 |
Изобретениие относится к соединению формулы I-b или его фармацевтически приемлемой соли, обладающим свойствами ингибитора активности ВТК, фармацевтической комозиции на их основе, способу ингибирования активности BTK, способу для лечения заболевания, опосредованного BTK, способу получения соединения формулы I-b. В общей формуле I-b R1 выбран из 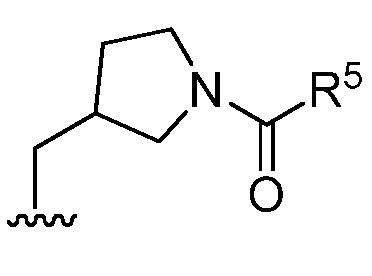
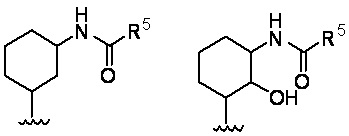 ; R2 представляет собой водород; или R1 и R2, взятые вместе с атомом, с которым они соединены, образуют 5-6 членное гетероциклическое кольцо, содержащее 1 азот и 0 других гетероатомов; или 8-10 членное конденсированное или спиро бициклическое гетероциклическое кольцо, содержащее 1 азот и 1 другой гетероатом азота; где кольцо, образованное R1 и R2, замещено
; R2 представляет собой водород; или R1 и R2, взятые вместе с атомом, с которым они соединены, образуют 5-6 членное гетероциклическое кольцо, содержащее 1 азот и 0 других гетероатомов; или 8-10 членное конденсированное или спиро бициклическое гетероциклическое кольцо, содержащее 1 азот и 1 другой гетероатом азота; где кольцо, образованное R1 и R2, замещено 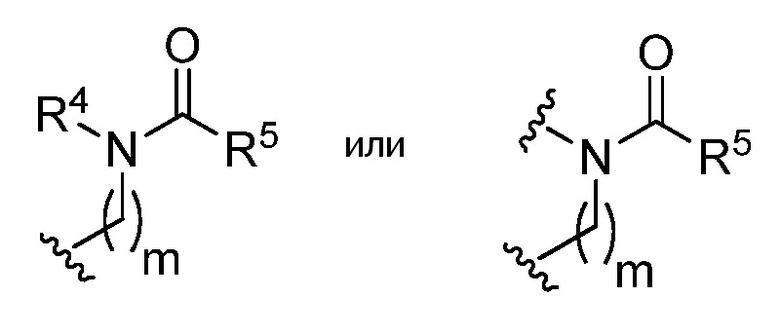 R4 представляет собой водород; каждый R5 независимо представляет собой C1-6 алкил, замещенный (2-гидроксиизопропил)фенилом, трет-бутилфенилом или -NH-фенил-Cl; фенил, замещенный трет-бутилом, циклопропилом, гидроксипропанилом или -N(CH3)2; или 5-членное моноциклическое гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранные из азота и кислорода, замещенные фенилом или трет-бутилом; и m равен 0 или 1. 5 н. и 5 з.п. ф-лы, 21 пр., 1 табл.
R4 представляет собой водород; каждый R5 независимо представляет собой C1-6 алкил, замещенный (2-гидроксиизопропил)фенилом, трет-бутилфенилом или -NH-фенил-Cl; фенил, замещенный трет-бутилом, циклопропилом, гидроксипропанилом или -N(CH3)2; или 5-членное моноциклическое гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранные из азота и кислорода, замещенные фенилом или трет-бутилом; и m равен 0 или 1. 5 н. и 5 з.п. ф-лы, 21 пр., 1 табл.
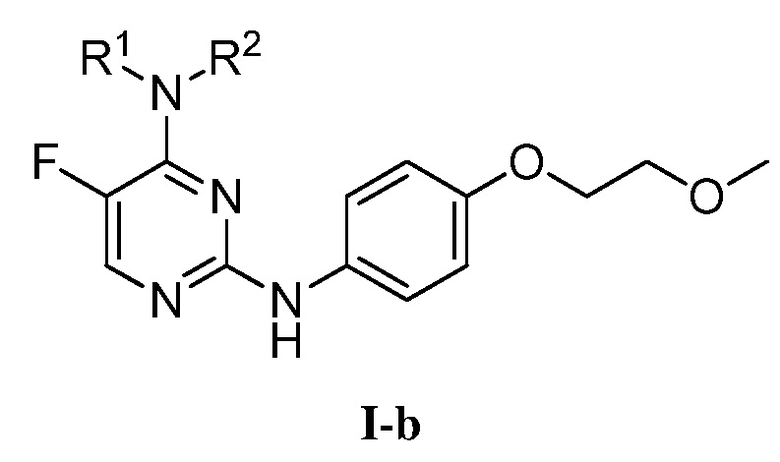
1. Соединение формулы I-b,
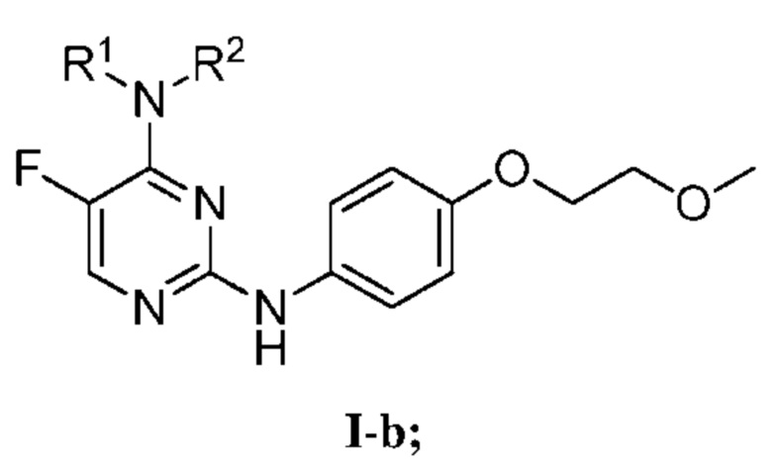
или его фармацевтически приемлемая соль, где:
R1 выбран из
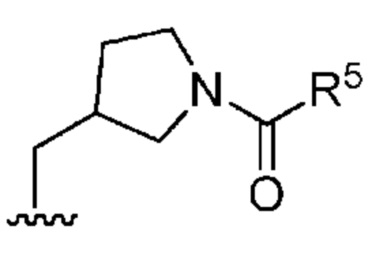
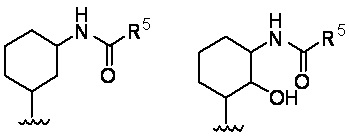 ;
;
R2 представляет собой водород; или
R1 и R2, взятые вместе с атомом, с которым они соединены, образуют 5-6 членное гетероциклическое кольцо, содержащее 1 азот и 0 других гетероатомов; или 8-10 членное конденсированное или спиро бициклическое гетероциклическое кольцо, содержащее 1 азот и 1 другой гетероатом азота;
где кольцо, образованное R1 и R2, замещено
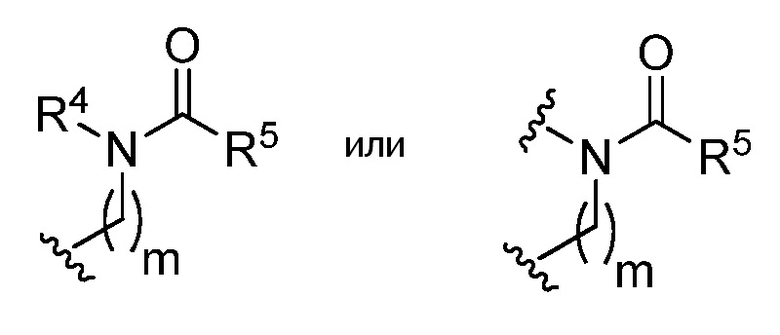
R4 представляет собой водород;
каждый R5 независимо представляет собой C1-6 алкил, замещенный (2-гидроксиизопропил)фенилом, трет-бутилфенилом или -NH-фенил-Cl; фенил, замещенный трет-бутилом, циклопропилом, гидроксипропанилом или -N(CH3)2; или 5-членное моноциклическое гетероарильное кольцо, содержащее 2 гетероатома, независимо выбранные из азота и кислорода, замещенные фенилом или трет-бутилом; и
m равен 0 или 1.
2. Соединение по п. 1, где кольцо, образованное R1 и R2, представляет собой
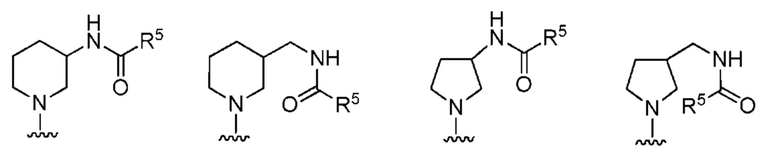
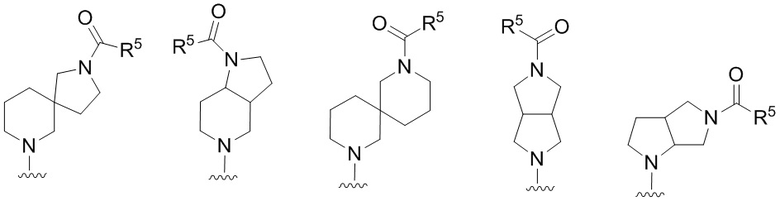 .
.
3. Соединение по п. 1, где каждый R5 независимо представляет собой
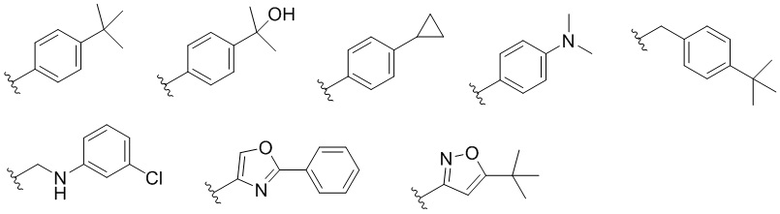 .
.
4. Соединение по п. 1, формулы I-e,
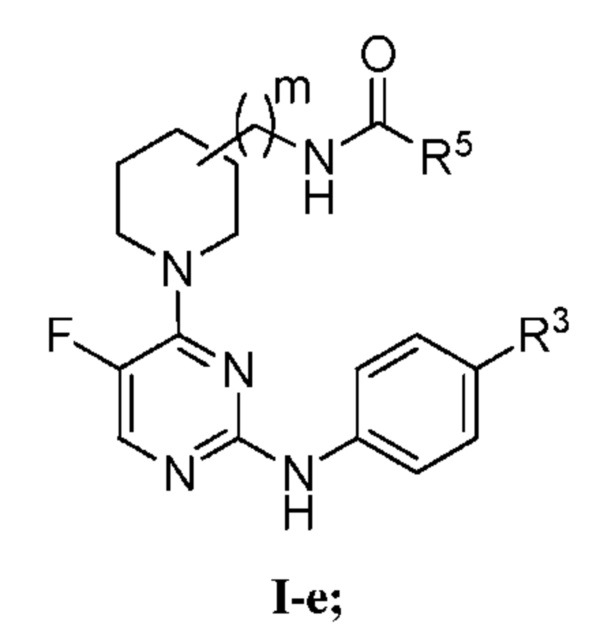
или его фармацевтически приемлемая соль; где R3 представляет -O(CH2)2OCH3, и где m и R5 такие, как определено в п.1.
5. Соединение по п. 1, формулы I-a,
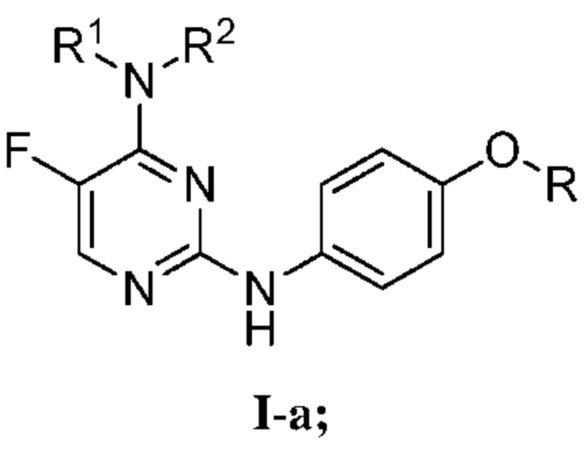
или его фармацевтически приемлемая соль; где R представляет -(CH2)2OCH3; где кольцо, образованное N, R1 и R2, представляет собой
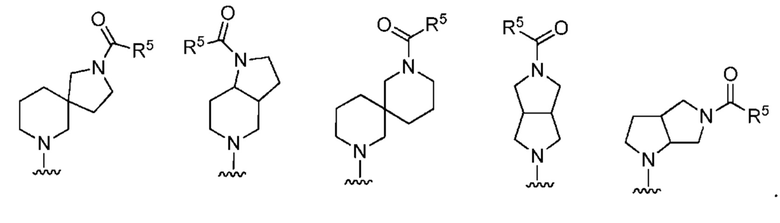 .
.
6. Соединение по п. 1, выбранное из группы, состоящей из
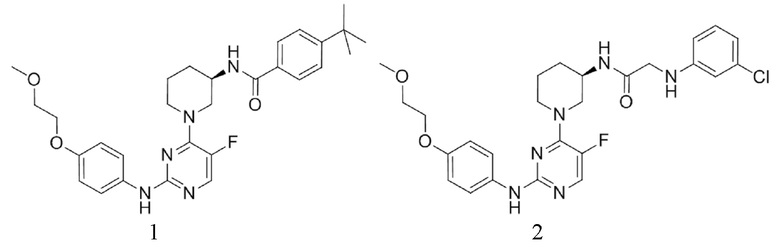
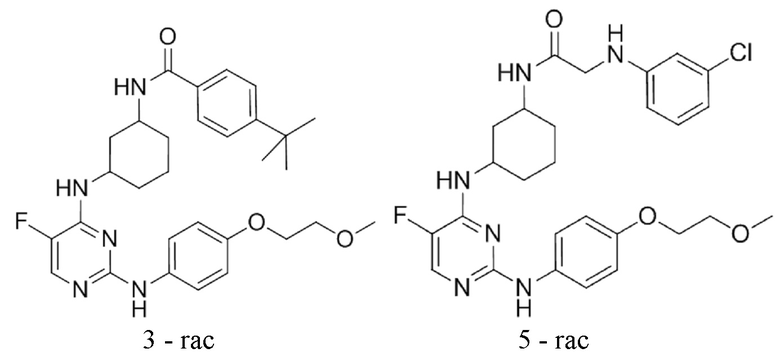
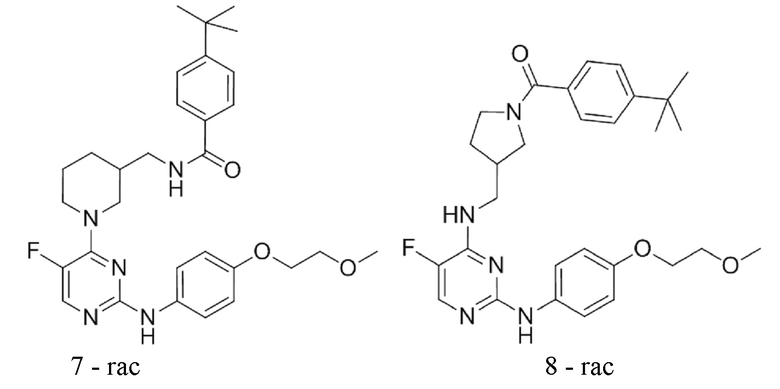
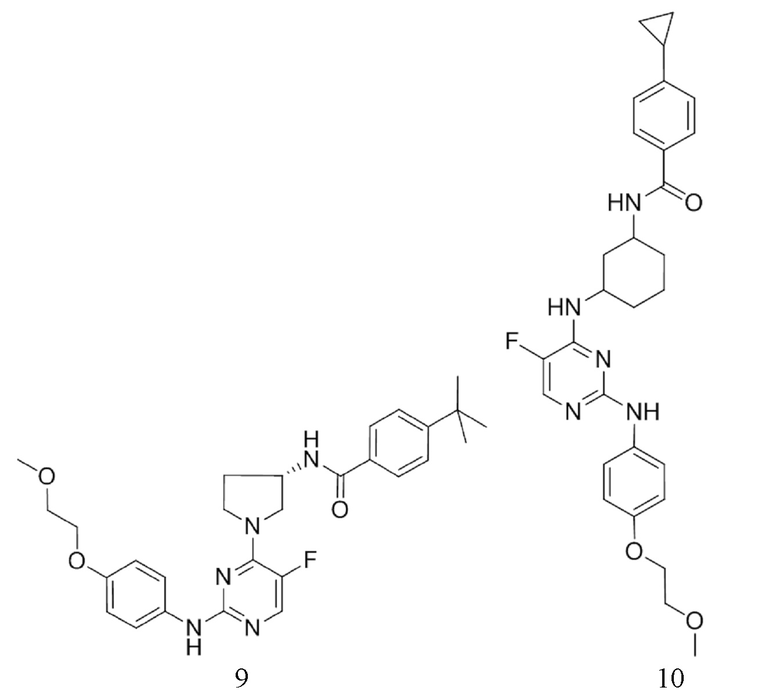
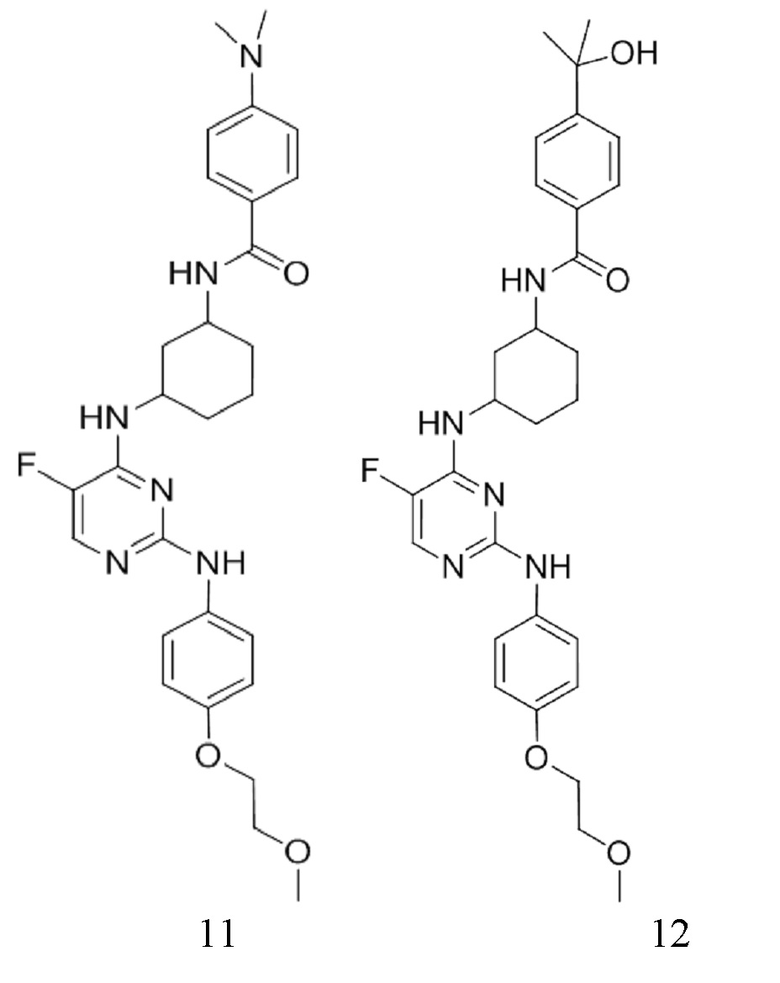
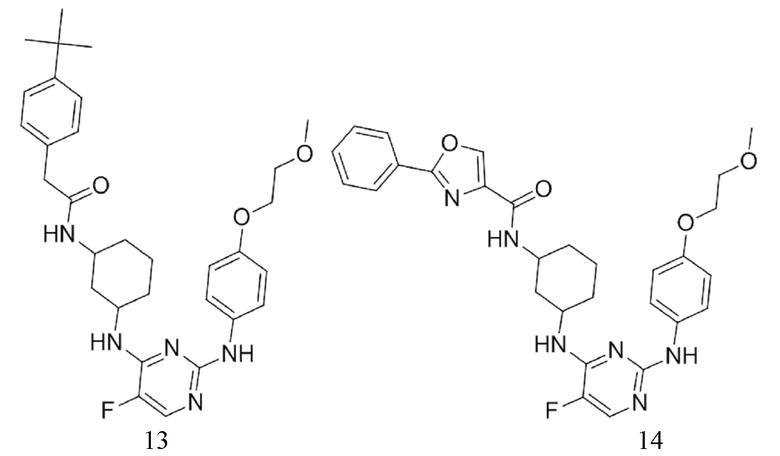
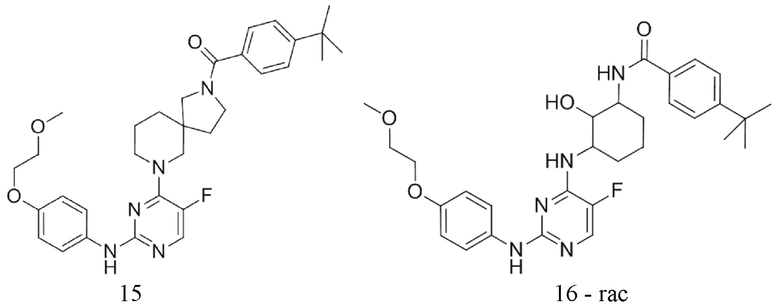
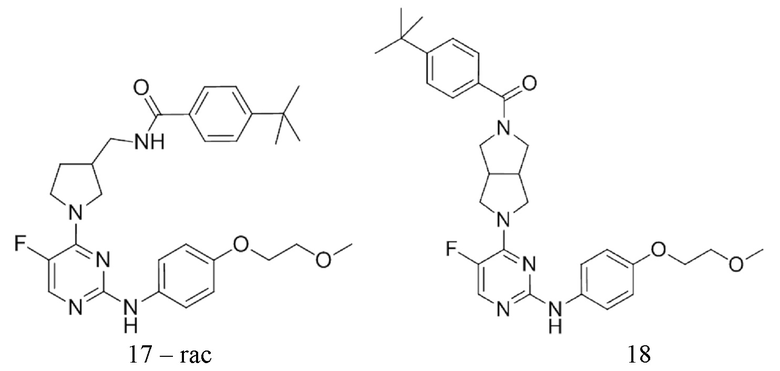
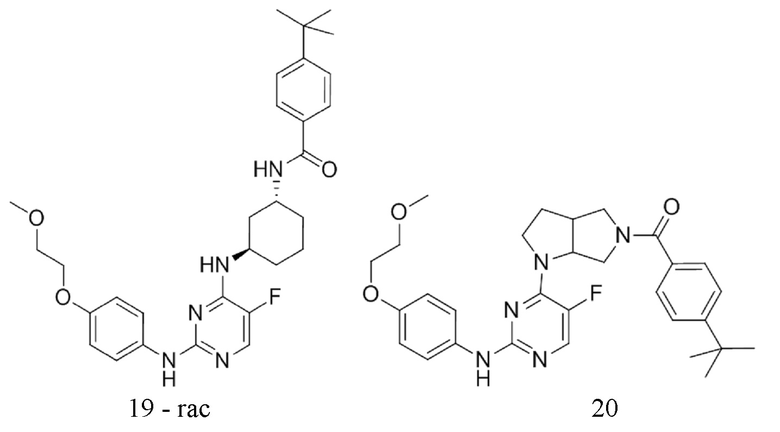
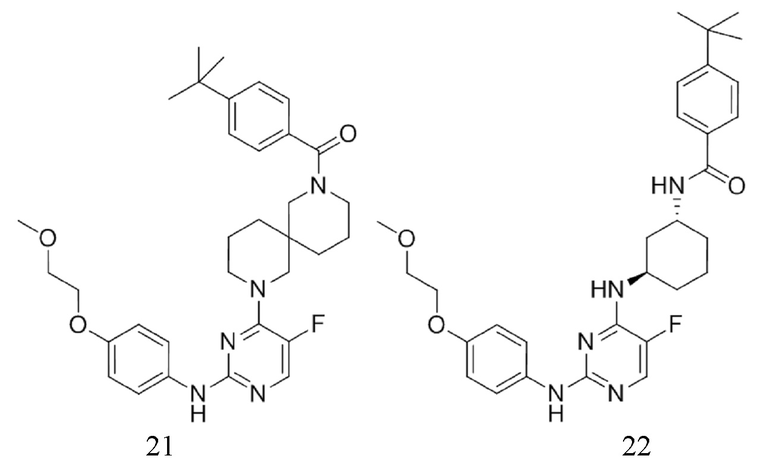
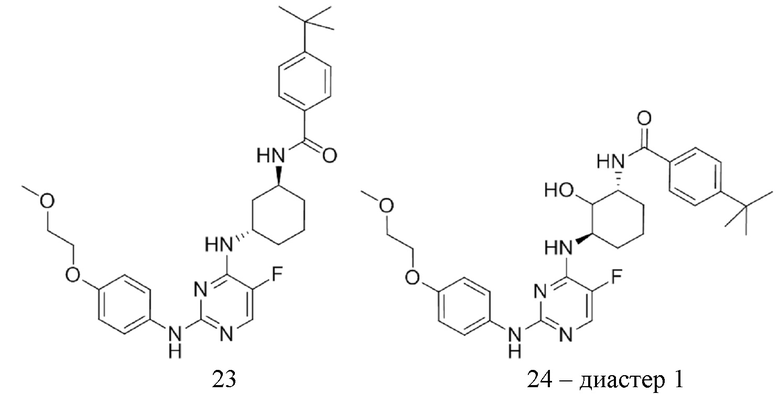
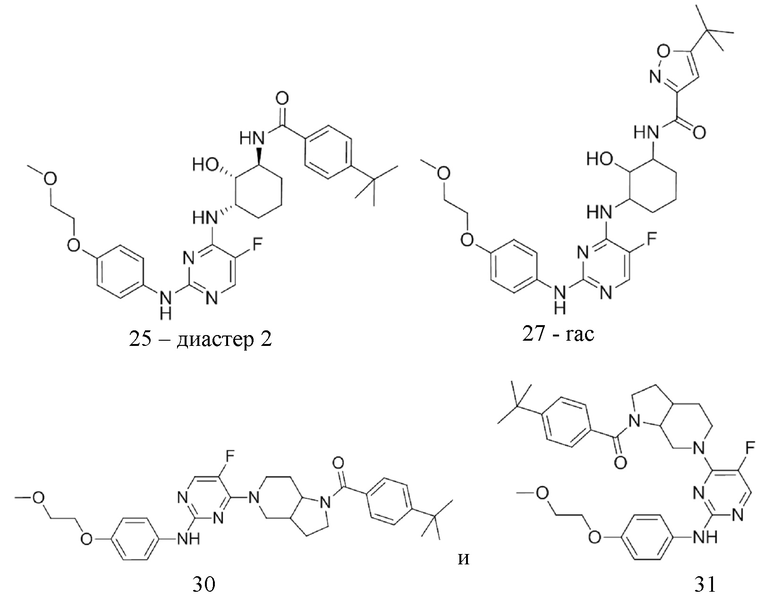
или его фармацевтически приемлемая соль.
7. Фармацевтическая композиция для лечения заболевания, опосредованного BTK, у пациента, нуждающегося в этом, содержащая эффективное количество соединения по п. 1 или его фармацевтически приемлемой соли, и фармацевтически приемлемый адъювант, носитель или среду.
8. Способ ингибирования активности BTK в биологическом образце введением в него или контактированием указанного биологического образца с эффективным количеством соединения по п. 1.
9. Способ для лечения заболевания, опосредованного BTK, включающий введение эффективного количества соединения по п. 1.
10. Способ получения соединения формулы I-b по п. 1, включающий стадии:
взаимодействия соединения формулы (A):
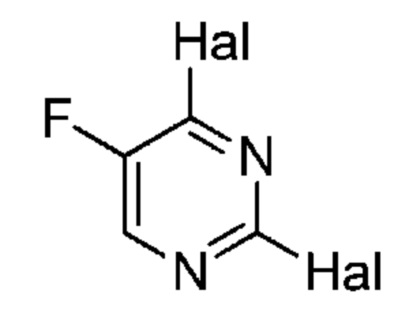
A;
с NH(R1)(R2);
где R1 и R2 представляют собой, как определено по п. 1;
с получением соединения формулы (B):
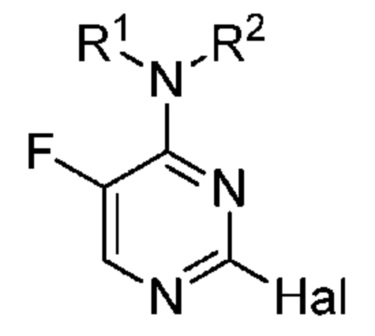
B;
и взаимодействия соединения формулы (B) с
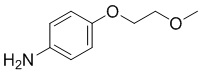 ;
;
с получением соединения формулы I-b:

где R1 и R2 представляют собой, как определено по п. 1.
| WO 2013173518 A1, 21.11.2013 | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| US 20150174128 A1, 25.06.2015 | |||
| WO 2015006754 A2, 15.01.2015 | |||
| ПРОИЗВОДНЫЕ ПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ | 2014 |
|
RU2677653C2 |
Авторы
Даты
2021-02-12—Публикация
2016-07-08—Подача