ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к новым устройствам для ингаляции, которые позволяют доставлять пользователю поставляемое вещество, такое как активное фармацевтическое вещество, в виде аэрозоля или пара с помощью пористого материала-носителя. Указанные устройства могут быть полезны для осуществления доставки пользователю регулируемых количеств поставляемого вещества.
УРОВЕНЬ ТЕХНИКИ
Указание или обсуждение ранее опубликованного документа в этом описании не следует обязательно расценивать как подтверждение того, что данный документ принадлежит к существующему уровню техники или содержит общеизвестную информацию.
Активно действующие вещества могут доставляться получателям с помощью ингаляционных устройств, которые испаряют активно действующее вещество во время использования и позволяют его вдыхать. Такие системы все чаще используются в виде электронных сигарет для доставки пользователям испаренного никотина. См., например, международную патентную заявку WO 99/44448, заявки на патент США 2014/0202477 и 2014/0014126, а также Callahan-Lyon Р. Tob Control; 2014; 23:ii36-ii40.
Испарительные устройства обычно содержат отсек, содержащий активно действующие вещества в растворенной или жидкой форме, а также нагревательное устройство для испарения жидкости. Нагревательное устройство, которое может быть нагревательным элементом, обычно расположено внутри устройства для ингаляции, чтобы оно могло непосредственно нагревать испарительный носитель, содержащий часть активно действующего вещества, а не резервуар с активно действующим веществом. Испарительный носитель частично погружен в резервуар и вытягивает жидкость из резервуара путем впитывания (капиллярное действие) в направлении нагревательного элемента, где она испаряется для вдыхания.
В заявке на патент США №2015/0209530 описано ингаляционное устройство, в котором вещество для доставки (либо активный фармацевтический ингредиент, либо никотин) предоставляется в виде пастообразной массы, которую затем наносят на материал-носитель и высушивают. Затем высушенная пастообразная масса и материал-носитель нагреваются внутри устройства для испарения активного фармацевтического ингредиента или никотина, и после этого пользователь может его вдыхать. Патент США №4303083 также раскрывает устройство для испарения летучего соединения путем нагревания соединения в жидком состоянии.
Известные устройства для ингаляции, в том числе так называемые электронные сигареты («е-cigarette»), часто имеют ряд проблем, включая неприятный вкус для пользователя, если устройство нагревается в сухом состоянии (то есть, когда летучее вещество закончилось). Кроме того, многие из добавок, содержащихся в жидкостях, используемых в них, являются вредными и могут вызвать проблемы со здоровьем. Например, известно, что в определенных условиях пропиленгликоль, растительный глицерин и полиэтилгликоль образуют такие соединения, как формальдегид и ацетальдегид, и такие остаточные вещества могут вдыхаться в результате процесса нагревания. Также трудно контролировать дозирование, что может привести к чрезмерному или неточному дозированию для пациентов.
Обработка больших количеств чистого или концентрированного никотина представляет на практике множество трудностей, в частности, для конечных пользователей. Устройства, в том числе электронные сигареты, которые содержат резервуар с жидкостью или которые должны быть заполнены посредством подсоединения к внешнему резервуару, также могут иметь проблемы, связанные с утечкой и проливом содержимых жидкостей во время использования и/или наполнения. Поэтому существует необходимостьв устройствах, в которых такие трудности сведены к минимуму.
Опиоиды широко используются в медицине как анальгетики, например, при лечении пациентов с сильной болью, хронической болью или для устранения боли после операции. Действительно, в настоящее время принято считать, что для ослабления более сильной боли не существует более эффективных терапевтических средств.
Термин «опиоид» обычно используется для описания лекарственного средства, которое активирует опиоидные рецепторы, которые находятся в головном мозге, спинном мозге и желудочно-кишечном тракте (ЖКТ). Существуют три класса опиоидов:
a) встречающиеся в природе алкалоиды опия. К ним относятся морфин и кодеин;
b) соединения, сходные по своей химической структуре с встречающимися в природе алкалоидами. Эти так называемые полусинтетические вещества производятся путем химической модификации последних и включают такие вещества, как диаморфин (героин), оксикодон и гидрокодон; а также
c) действительно синтетические соединения, такие как фентанил и метадон. Такие соединения могут быть совершенно отличаться с точки зрения своей химической структуры от встречающихся в природе соединений.
Из трех основных классов опиоидных рецепторов (μ, κ и δ) анальгетические и седативные свойства опиоидов в основном происходят из-за агонизма в μ-рецепторе.
Опиоидные анальгетики используются для лечения тяжелой, хронической боли при раке, часто в сочетании с нестероидными противовоспалительными препаратами (НПВП), а также острой боли (например, во время восстановления после операции и прорыва боли). Кроме того, их использование увеличивается при контроле хронической боли, не обусловленной раком.
При разработке композиций, содержащих исключительно сильнодействующие лекарственные средства, такие как опиаты, дозирование должно быть точным и должен быть устранен риск «сброса дозы» с учетом риска тяжелых и, в некоторых случаях, смертельных побочных эффектов. Во-вторых, в некоторых случаях пациенты могут злоупотреблять своими опиоидными препаратами, например, путем преднамеренного (а иногда и непреднамеренного) вмешательства в состав и лекарственную форму препарата, чтобы достичь более непосредственного поглощения опиоидов и более быстрого обезболивающего эффекта. В-третьих, многолетняя проблема, связанная с применением мощных опиоидных анальгетиков, таких как фентанил, является одним из злоупотреблений со стороны лиц, привычно потребляющих наркотики. Лица, привычно потребляющие наркотики, часто применяют инновационные методы при злоупотреблении фармацевтическими препаратами, например, посредством одного или более из следующих способов:
a) экстрагирование большого количества активного вещества из этого препарата с использованием подходящего элюента, такого как кислота и/или спирт, с образованием раствора, который затем вводится внутривенно. В случае большинства коммерчески доступных фармацевтических препаратов это может быть сделано относительно легко, что делает их небезопасными или «доступными для злоупотребления»;
b) нагревание (а затем курение);
c) дробление таблеток (а затем втягивание их носом); и/или
d) в случае пластыря, приготовление чая (а затем его выпивание).
Таким образом, существует явная неудовлетворенная клиническая потребность в эффективном фармацевтическом препарате, который способен лечить, например, сильную боль путем доставки контролируемого количества активных ингредиентов (таких как опиоидные анальгетики) простым способом пациентам, которые испытывают трудности с глотанием, в то же время сводя к минимуму возможность сброса дозы, злоупотребления пациентами, проходившими лечение опиоидами, и/или злоупотребления со стороны лиц, привычно потребляющих наркотики.
Одним из решений этих проблем, которое было предложено, является включение активного вещества в полимерную матрицу (см., например, US 2003/0118641 и US 2005/0163856), что обеспечивает медленное высвобождение активного вещества. Однако этот раствор не является адекватным, поскольку лицо, привычно потребляющее наркотики, могло бы в любом случае высвобождать активное вещество из полимерной матрицы путем ее смешивания с растворителем (либо до приема внутрь, либо путем принятия растворителя внутрь вместе с полимерной матрицей/активным веществом) либо путем измельчения полимерной матрицы.
Доставка некоторых опиоидов пациентам посредством ингаляции также желательна, однако очень трудно предоставить препарат в медицинской форме, предупреждающей злоупотребление, которая была бы способна хранить и высвобождать опиоид только тогда, когда того требует конечный пользователь.
Керамические материалы становятся все более полезными в области медицины, в частности, ввиду того, что они прочны и достаточно стабильны, чтобы выдерживать коррозионное воздействие биологических жидкостей.
Известно, что керамические материалы также могут использоваться в качестве наполнителей или носителей в фармацевтических препаратах с контролируемым высвобождением. См., например, ЕР 947489 A, US 5318779, WO 2008/118096, Lasserre and Bajpai, Critical Reviews in Therapeutic Drug Carrier Systems, 15, 1 (1998), Byrne and Deasy, Journal of Microencapsulation, 22, 423 (2005) and Levis and Deasy, Int. J. Pharm., 253, 145 (2003).
В частности, Rimoli et al, J. Biomed. Mater. Res., 87A, 156 (2008), заявка на патент США 2006/0165787 и международные патентные заявки WO 2006/096544, WO 2006/017336 и WO 2008/142572 раскрывают различные керамические вещества для контролируемого высвобождения активных ингредиентов, причем последние два документа относятся целиком или частично к опиоидным анальгетикам, при этом злоупотреблению препятствует механическая прочность керамических структур.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Согласно первому аспекту изобретения предлагается устройство для доставки пользователю доставляемого вещества в виде аэрозоля или пара, содержащего твердый, пористый материал-носитель и доставляемое вещество, расположенное в порах материала-носителя. Пористость материала-носителя должна составлять по меньшей мере 10%. Устройство дополнительно выполнено с возможностью нагрева материала-носителя для испарения доставляемого вещества.
Устройства, обладающие такими характерными признаками, в дальнейшем упоминаются совместно как «устройства по данному изобретению». Они также могут упоминаться в данном документе как «устройства для ингаляции».
Нами было обнаружено преимущество, состоящее в том, что устройства по данному изобретению обеспечивают высвобождение доставляемого вещества (например, активного фармацевтического вещества) в виде аэрозоля или пара (то есть газа), с тем, чтобы обеспечить контролируемое количество доставляемого вещества, которое должен принимать субъект путем ингаляции. Доставляемое вещество представляет собой вещество (или смесь веществ), которое может быть доставлено индивидууму, чтобы обеспечить терапевтический эффект. В вариантах реализации данного изобретения доставляемое вещество обычно является активным фармацевтическим веществом.
Размер пор в материале-носителе должен быть выбран таким образом, чтобы материал-носитель мог эффективно сохранять достаточное количество доставляемого вещества в течение длительного периода времени с минимальными потерями в условиях окружающей среды. Этого обычно можно достичь с помощью материала-носителя с пористостью по меньшей мере 10%.
Обычно для материалов-носителей, которые используются в устройствах для ингаляции согласно данному изобретению, требуется высокая пористость. Минимальная пористость около 10% (по объему) является предпочтительной для материала-носителя, используемого в данном изобретении. В конкретном варианте реализации изобретения материал-носитель имеет пористость от около 10% до около 90%, например от около 20% до около 70% (более предпочтительно от около 30% до около 60%). Более прочные материалы могут быть пригодны для того, чтобы иметь более высокую пористость. Например, металлы могут быть особенно пригодны для использования с пористостью, которая составляет от около 10% до около 90%, или более предпочтительно, от около 30% до около 80%. В вариантах реализации изобретения, в которых материал-носитель выполнен из керамического материала или геополимерного материала, пористость может составлять от около 10% до около 90%, или предпочтительно, от около 30% до около 70%, или более предпочтительно, от около 30% до около 60%. Контроль за пористостью материала-носителя играет важную роль, поскольку обеспечивает достижение контролируемой доставки пользователю доставляемого вещества.
Также желательно контролировать размер пор в материале-носителе, чтобы улучшить характеристики контролируемого высвобождения устройств согласно изобретению. Размер пор (например, средний внутренний размер) материала-носителя должен быть достаточно малым, чтобы избежать чрезмерного ослабления материала-носителя, и достаточно большим, чтобы обеспечить принятие порами доставляемого вещества. В одном варианте реализации изобретения средний размер пор составляет не более чем около 500 мкм, или предпочтительно, менее чем около 200 мкм. Средний размер пор может составлять всего лишь 0,5 нм (для так называемых «микропор», как описано в Science of Concrete (http://iti.northwestern.edu/cement/monograph/Monograph7_2.html). Пустоты с меньшими размерами обычно классифицируются как межслоевые пространства. Типичное распределение размеров пор в случае затвердевшего цемента охватывает широкий диапазон от всего лишь 0,5 нм (или, возможно, меньше) до около 10 мкм в диаметре. Поры большего размера от 10 нм до 10 мкм представляют собой остаточные незаполненные пространства между частицами цемента, а также могут быть определены как капиллярные поры. Мельчайшие поры варьируются от около 0,5 нм до 10 нм. Они часто называются гелевыми порами, поскольку они составляют внутреннюю пористость (например) гелевой фазы гидросиликата кальция. В одном варианте реализации изобретения минимальный средний размер пор может составлять около 0,5 нм, хотя он может составлять около 10 нм и предпочтительно составляет около 0,1 мкм. Однако в некоторых вариантах реализации изобретения минимальный размер пор может составлять около 0,2 мкм, например около 0,25 мкм. Таким образом, в одном из предпочтительных вариантов реализации изобретения средний размер пор в твердом пористом материале составляет от около 0,1 мкм до около 500 мкм, или более предпочтительно, от около 0,2 мкм до около 200 мкм. Средние размеры пор могут быть измерены способами, известными специалисту в данной области техники, например, способом внедрения ртути, методом БЭТ (Брунауэра, Эммета и Теллера) и методами адсорбции N2.
Не обязательно, чтобы материал-носитель мог пропускать воздух по всей пористой структуре. В предпочтительных вариантах реализации изобретения пористость материала-носителя и/или средний размер пор в материале-носителе таковы, что пользователь не может втянуть значительное количество воздуха через поры материала-носителя во время ингаляции.
Аналогичным образом, в конкретных вариантах реализации изобретения размер пор может быть таким, чтобы поток воздуха внутри пор материала-носителя значительно уменьшался. Доставляемое вещество высвобождается из материала-носителя за счет его испарения с последующим проникновением из внутренних зон материала-носителя в окружающий воздух. Окружающий воздух втягивается обтекая при этом внешнюю поверхность материала-носителя, над которой он смешивается с испаренным доставляемым веществом и поступает к пользователю. Использование термина «внешняя поверхность» в этом контексте относится к самой внешней поверхности твердого материала, например к внешней поверхности гранулы, блока или диска материала-носителя. Такие механизмы переноса особенно важны для материалов-носителей, имеющих небольшие средние размеры пор, например, не более чем около 100 мкм (например, не более чем около 25 мкм).
В одном из предпочтительных вариантов реализации изобретения материал-носитель имеет пористость от около 10% до около 90% (например, от около 10% до около 70%), а средний размер пор в материале-носителе составляет от около 0,1 мкм до около 500 мкм. В еще одном предпочтительном варианте реализации изобретения материал-носитель имеет пористость от около 20% до около 70%, а средний размер пор в материале-носителе составляет от около 0,2 мкм до около 200 мкм.
В еще одном предпочтительном варианте реализации изобретения материал-носитель имеет высокую механическую прочность (например, прочность на сжатие). В этом отношении, по материалам с «высокой механической прочностью», следует также учитывать, что структура этой системы пор материала-носителя сохраняет свою общую целостность (например, форму, размер, пористость и т.д.), когда прилагается усилие около 1 килограмма-силы на квадратный сантиметр (кгс/см2) (0,098 МПа), например около 5 кгс/см2 (0,49 МПа), например около 7,5 кгс/см2, например около 10,0 кгс/см2, или предпочтительно, около 15 кгс/см2, или более предпочтительно, около 20 кгс/см2, например, около 50 кгс/см2, особенно около 100 кгс/см2 или даже около 125 кгс/см2 (12,25 МПа), с использованием обычных методов испытания на механическую прочность, известных специалисту в данной области техники (например, с использованием так называемого «испытания на сжатие» или «испытания на раскалывание» с использованием подходящего инструмента, такого как, например, инструмент, производимый компанией Instron («Испытание на разрыв машиной марки Instron»), в котором образец сжимают, регистрируют деформацию при различных нагрузках, сжимающие напряжения и деформацию рассчитывают и отображают в виде диаграммы зависимости деформации от напряжения, которую используют для определения предела упругости, предела пропорциональности, предела текучести, предела текучести при растяжении и (для некоторых материалов) прочности на сжатие)). Механическая прочность также обычно не составляет более чем около 2040 кгс/см2 (200 МПа), так как материалы с очень высокой механической прочностью могут иметь недостаточную пористость, чтобы обеспечить включение в них достаточного количества доставляемого вещества. Поэтому в вариантах реализации изобретения механическая прочность составляет менее чем около 200 МПа, предпочтительно менее чем около 100 МПа.
Особенно предпочтительным материалом-носителем является материал, в котором размер и взаимосвязанность пор такова, что передача значительных количеств воздуха через поры материала-носителя не может быть достигнута посредством вдыхания пользователем. Под этим следует понимать, что здоровый взрослый индивидуум не способен вдыхать количество, соответствующее приблизительно емкости вдоха среднестатистического человека (например, около 3 литров) через материал-носитель в течение около 20 секунд. Такой материал-носитель, как правило, имел бы пористость не более чем 50% и/или средний размер пор, не превышающий 100 мкм, хотя такие материалы могли бы иметь более высокую пористость, если бы средний размер пор был меньше, и наоборот. Таким образом, в конкретном варианте реализации изобретения материал-носитель имеет пористость вплоть до 50% (например, от около 10% до около 50%) и средний размер пор вплоть до около 100 мкм (например, от около 0,1 мкм до около 100 мкм). В дальнейшем варианте реализации изобретения материал-носитель имеет пористость вплоть до 50% (например, от около 10% до около 50%) и средний размер пор вплоть до около 50 мкм (например, от около 0,1 мкм до около 50 мкм). Во всех вариантах реализации изобретения, описанных в данном документе, поры предпочтительно взаимосвязаны, чтобы позволить высвобождаемому веществу высвобождаться из внутренних зон материала-носителя (то есть зон, которые расположены вдали от внешней поверхности материала-носителя). Однако материал-носитель должен иметь достаточную пористость, по меньшей мере во внешних зонах, чтобы обеспечить достаточное количество (например, количество никотина, эквивалентное количеству никотина, которое курильщик получает из одной сигареты) доставляемого вещества, которое должно содержаться в этих порах до использования
В одном из вариантов реализации изобретения доставляемое вещество находится преимущественно внутри пор материала-носителя. При использовании фразы «преимущественно внутри пор материала-носителя» подразумевается, что по меньшей мере 50 мас. % доставляемого вещества в устройстве находится внутри пор материала-носителя. В конкретных вариантах реализации изобретения по меньшей мере 75 мас. % (или для газа по меньшей мере 75% по объему) доставляемого вещества в устройстве находится внутри пор материала-носителя. В предпочтительных вариантах реализации изобретения по меньшей мере 90 мас. % (или по меньшей мере 90% по объему) доставляемого вещества в устройстве находится внутри пор материала-носителя. Располагая доставляемое вещество преимущественно или, по существу, полностью внутри пор материала-носителя, можно добиться лучшего контроля над количеством доставляемого вещества, которое испаряется и доставляется пользователю во время использования. В конкретном варианте реализации изобретения устройство не содержит отдельный резервуар с доставляемым веществом, который отделен от материала-носителя. То есть, по существу, все доставляемое вещество находится в связи с материалом-носителем, или предпочтительно, по существу, все доставляемое вещество расположено внутри пор материала-носителя.
Значительное или полное содержание доставляемого вещества в порах материала-носителя также уменьшает возможность преднамеренных экстракций лекарственного средства ex vivo для предполагаемого злоупотребления (например, путем экстракции с помощью кислоты или спирта с последующей инъекцией).
Особенно предпочтительно, чтобы доставляемое вещество находилось преимущественно внутри пор материала-носителя, когда доставляемое вещество является одним или более терапевтическими веществами (т.е. активными фармацевтическими ингредиентами), которыми вполне можно злоупотреблять. Это является преимуществом, поскольку препятствует высвобождению доставляемого вещества из устройства и тем самым снижает риск того, что устройство, содержащее доставляемое вещество, будет использоваться в качестве незаконного источника этого доставляемого вещества.
Также предпочтительно, чтобы материалы-носители, используемые в устройствах по данному изобретению, были выполнены с возможностью хранить и высвобождать достаточное количество доставляемого вещества во время использования, так чтобы не было необходимости в том, чтобы устройство содержало дополнительный резервуар с доставляемым веществом. То есть в предпочтительных вариантах реализации изобретения устройство не содержит хранилища с доставляемым веществом, отличным от того, которое связано с (то есть преимущественно расположено в порах) материалом-носителем перед использованием.
Пористые носители обычно содержат как открытые поры, так и закрытые поры. Термин «открытые поры» относится к порам (например, пустотам внутри материала), которые сообщаются с внешней средой, так что, когда эти поры в противном случае пусты, находящиеся в окружающей среде газы могут проходить через эти поры и из этих пор. Такие поры обычно расположены на или близко к поверхности отдельных частиц материала-носителя. Термин «закрытые поры» относится к порам, которые расположены внутри частиц материала-носителя вдали от внешних поверхностей и которые могут содержать материал (например, газы), который не может свободно сообщаться с внешней средой.
В одном из вариантов реализации изобретения поры пористого материала-носителя насыщены доставляемым веществом. В устройствах, в которых доставляемое вещество присутствует в составе смеси, содержащей одно или более дополнительных веществ, упомянутых в различных частях данного документа (например, вещества, усиливающие испарение, ароматизаторы, усилители вкуса и т.д.), тогда поры пористого материала-носителя могут быть насыщенны указанной смесью. В этом контексте поры, которые насыщены доставляемым веществом (или смесью, содержащей доставляемое вещество), включают по меньшей мере открытые поры. Закрытые поры, присутствующие в материале-носителе, также могут содержать или не содержать доставляемое вещество (или смесь, содержащую доставляемое вещество). Не обязательно, чтобы закрытые поры были насыщены доставляемым веществом (или смесью, содержащей доставляемое вещество). При использовании термина «насыщенный» предполагается, что поры (например, по меньшей мере открытые поры) преимущественно заполнены (например, по существу, полностью заполнены) доставляемым веществом (или смесью, содержащей доставляемое вещество), и предпочтительно, чтобы поры содержали, по существу, только доставляемое вещество (или смесь, содержащую доставляемое вещество). Эти поры должны содержать минимальное количество свободного пространства (например, пространства, занятого атмосферными газами или материалами, отличными от доставляемого вещества). Во избежание сомнений, устройства по данному изобретению могут содержать множество доставляемых веществ, а ссылки в данном документе на поры, которые содержат, по существу, только доставляемое вещество, также относятся к порам, которые содержат, по существу, только множество доставляемых веществ.
В одном из предпочтительных вариантов реализации изобретения по меньшей мере около 70% объема полости открытых пор пористого материала-носителя заполняется доставляемым веществом (или смесью, содержащей доставляемое вещество). В еще одном варианте реализации изобретения по меньшей мере около 90% (например, по меньшей мере около 95%) объема открытых пор пористого материала-носителя заполняется доставляемым веществом (или смесью, содержащей доставляемое вещество).
Устройства по данному изобретению содержат твердый, пористый материал-носитель, имеющий пористость по меньшей мере 10%, причем по меньшей мере часть доставляемого вещества расположена внутри пор указанного материала-носителя. Устройство дополнительно выполнено с возможностью нагрева материала-носителя с последующим испарением доставляемого вещества. Материалы-носители и доставляемые вещества, описанные в данном документе, могут быть использованы в любом обычном ингаляционном устройстве, которое выполнено с возможностью доставки одного или более веществ пользователю в виде аэрозоля или пара (то есть газа). Такие устройства будут известны специалисту в данной области техники и включают электронные сигареты, известные как «е-Cigs», например, как описано в US 2014/0014126, и другие устройства для ингаляции, например, как описано в патенте US 4303083.
Устройства для ингаляции также могут быть выполнены таким образом, чтобы они могли использоваться только с материалами-носителями и доставляемыми веществами, описанными в данном документе. Это может быть достигнуто несколькими способами, например, путем обеспечения того, чтобы для сменных стаканов (например, описанных в другом месте в данном документе) нужна была определенная трехмерная форма, чтобы материал-носитель нагревался устройством, или путем включения проводящего материала (например частиц железа) в материале-носителе для целей индукционного нагрева. Специалисту в данной области техники будут известны дополнительные способы. Такие устройства особенно полезны, поскольку лицам, привычно потребляющим наркотики, было бы очень сложно использовать эти устройства для злоупотребления другими лекарственными средствами.
В одном из вариантов реализации изобретения материал-носитель, содержащий вещество, которое будет вдыхаться (то есть доставляемое вещество), расположен внутри устройства в газообразном сообщении с отверстием (например, мундштуком), расположенным на внешней поверхности устройства. При использовании доставляемое вещество в материале-носителя испаряется, после чего пар течет к отверстию и принимается пользователем (например, через мундштук).
Движение пара внутри устройства обычно достигается за счет того, что пользователь делает вдох через мундштук и тем самым вытягивает газы из устройства для ингаляции. Устройство может также содержать второе отверстие, которое находится в газообразном сообщении как с материалом-носителем, содержащим доставляемое вещество, так и с первым отверстием (например, мундштуком), упомянутым выше. Эта конфигурация позволяет пользователю втягивать воздух через внутренние зоны устройства для ингаляции и тем самым облегчить доставку пользователю испаренного материала после его образования в устройстве.
В устройствах по данному изобретению вещество, подлежащее вдыханию (т.е. доставляемое вещество), обычно представляет собой твердое вещество, жидкость или газ в условиях окружающей среды. Устройство для ингаляции содержит запас вещества, подлежащего вдыханию (например, в твердом или жидком состоянии или в виде растворенного или взвешенного газа) вместе со средствами, посредством которых указанное вещество может улетучиться. Подходящие средства включают любой источник тепла, который выполнен с возможностью подавать тепловую энергию непосредственно на материал-носитель, чтобы испарить доставляемое вещество, которое также присутствует. Таким образом, доставляемое вещество высвобождается в виде аэрозоля или газа (т.е. пара). Затем испаренный материал доставляется пользователю, как правило, пользователем, вдыхающим указанные пары. Специалисту в данной области техники будут известны подходящие нагревательные устройства, которые могут быть использованы для нагрева материала-носителя.
В одном варианте реализации изобретения материал-носитель может быть непосредственно нагрет пламенем. В таком варианте реализации изобретения устройство содержит источник воспламеняющегося газа, который способен воспламеняться для нагрева материала-носителя.
В одном из предпочтительных вариантов реализации изобретения устройство содержит нагревательный элемент (например, электрический нагревательный элемент), который выполнен с возможностью нагревать материал-носитель и, тем самым, испарять по меньшей мере часть доставляемого вещества, которое расположено в порах материала-носителя. Например, нагревательный элемент может быть резистивным нагревателем (например, в виде проводящего провода или нагревательной пластины), который высвобождает эффективное количество тепла при прохождении через него тока. Нагрев также может происходить индукционным путем. Это может быть достигнуто путем размещения материала-носителя в непосредственной близости от нагревательного элемента (например, металлического объекта или другой проводящей структуры), который, в свою очередь, может нагреваться индукцией с использованием электромагнита.
В еще одном варианте реализации изобретения нагревательный элемент расположен проксимально с (т.е. находится в непосредственной близости или предпочтительно непосредственно рядом с) материалом-носителем. Под этим подразумевается, что нагревательный элемент расположен достаточно близко к материалу-носителю, чтобы нагревательный элемент мог непосредственно нагревать материал-носитель и испарять доставляемое вещество. Нагревательный элемент может находиться в непосредственном контакте с материалом-носителем и, кроме того, может быть непосредственно введен в материал-носитель. Примером такого нагревательного элемента является нагревательная катушка. Указанная катушка может быть намотана вокруг наружной стенки блока или гранулы материала-носителя или может быть внедрена в массу материала-носителя. Внедрение обычно достигается путем введения нагревательного элемента в смесь веществ-предшественников материала-носителя до отверждения или упрочнения этой смеси, как описано в различных частях данного документа. Материалы-носители, используемые в устройствах по данному изобретению, выполнены с возможностью непосредственно нагрева (то есть не за счет потока горячего газа, производимого нагревательным элементом) без ухудшения качества и без образования неприятного вкуса для пользователя. В другом варианте реализации изобретения нагревательный элемент не смешивается с материалом-носителем, а расположен рядом с материалом-носителем или на расстоянии от материала-носителя. В таких вариантах реализации изобретения нагревательный элемент может использоваться для нагрева воздуха, который затем может подаваться для прохождения по поверхности материала-носителя и/или через материал-носитель, содержащий доставляемое вещество, для испарения по меньшей мере части доставляемого вещества, которое расположено внутри пор материала-носителя.
Системы, в которых индукционный нагрев используют для нагревания материала-носителя, и доставляемого вещества, обычно требуют наличия металлического объекта или другой электропроводящей структуры в качестве нагревательного элемента, находящегося в тесном контакте с материалом-носителем и доставляемым веществом. Дискретные частицы (например, шарики или гранулы) подходящего проводящего материала (например, железа или меди) могут быть распределены по всему материалу-носителю для содействия процессу нагрева. Использование таких систем позволяет устройству очень быстро и равномерно нагреть весь объем материала-носителя и тем самым обеспечить более контролируемое и более прогнозируемое высвобождение объема доставляемого вещества. Подходящий проводящий материал также может быть предусмотрен в других подходящих формах и с другими геометрическими параметрами, например, он может быть предусмотрен в виде ряда стержней, дисков или пластин или в виде сетки или трехмерной сетки, внутри которой могут располагаться материал-носитель и доставляемое вещество. Если проводящий материал диспергирован по всему носителю (например, в виде мелких частиц, стержней или сетки), то обычно количество присутствующего проводящего материала должно быть достаточным для обеспечения быстрого и тщательного нагрева всего материала-носителя и это количество должно быть достаточно низким, чтобы не влиять на эффективность воздействия керамического носителя и его содержимого. Как правило, количество проводящего материала (то есть нагревательного элемента), присутствующего в материале-носителе, может составлять вплоть до 40 мас. % относительно общей массы проводящего материала и материала-носителя без существенного уменьшения механических свойств отвержденного цемента. Предпочтительно, чтобы количество проводящего материала, присутствующего в материале-носителе, составляло не более 20 мас. % по отношению к общей массе проводящего материала и материала-носителя. Когда материал-носитель формируется в контакте лишь с небольшим числом (например, менее пяти, предпочтительно одной) больших проводящих масс, то относительное количество проводящего материала, присутствующего в качестве нагревательного элемента, может быть намного выше, потенциально вплоть до 70 мас. % (например, вплоть до 50 мас. %) по отношению к общей массе проводящего материала и материала-носителя. В этом отношении трехмерные сетки могут быть получены любым обычным способом, известным специалисту в данном области техники, включая трехмерную печать или образование вспененного металла, как описано в различных частях данного документа.
Проводящий материал может также содержать или состоять из ферромагнитного (или ферримагнитного) материала, такого как железо. Наличие таких магнитных материалов может дополнительно улучшить эффекты нагрева, достигаемые с помощью индукционного нагрева, поскольку дополнительное тепло генерируется за счет потерь от магнитного гистерезиса в магнитном материале. Индукционный нагрев, как правило, способен обеспечить более быстрый нагрев материалов по сравнению с резистивными нагревателями.
Проводящий материал (например, в виде частиц) также можно смешивать с материалом-носителем даже в системах, которые не предназначены для индукционного нагрева. Независимо от способа, с помощью которого материал-носитель нагревается, проводящий материал помогает увеличить темп и однородность распространения тепла по всему материалу-носителю, чтобы тем самым увеличить скорость и прогнозируемость испарения доставляемого вещества.
Материал-носитель может быть размещен внутри внешней защитной оболочки, расположенной внутри устройства для ингаляции. Например, материал-носитель может быть размещен внутри защитной оболочки, которая образована из теплопроводного материала (например, металла, такого как алюминий или сталь), которая способна сохранять материал-носитель и доставляемое вещество, когда устройство не используется. В таком варианте реализации изобретения нагревательный элемент может также находиться в непосредственном тепловом контакте с внешней поверхностью защитной оболочки.
В качестве альтернативного варианта, защитная оболочка может представлять собой керамический или геополимерный материал, например, как описано ниже. Предпочтительно защитная оболочка представляет собой керамический материал (такой же, как керамический носитель, или отличающийся от керамического носителя, описанного в данном документе), который не содержит какого-либо доставляемого вещества в своих порах. Такая керамическая защитная оболочка обеспечивает теплоизоляцию материала-носителя и содержащегося в нем доставляемого вещества. Керамические защитные оболочки особенно полезны в устройствах по данному изобретению, в которых материалы-носители нагреваются с использованием индукционного нагрева. В этих системах защитная оболочка может выступать в качестве хранилища для материала-носителя, содержащего нагревательный элемент (например, частицы проводящего материала), и отделять его от источника переменного магнитного поля (например, проводящей катушки) и от других компонентов устройства для ингаляции, которые могут быть чувствительны к высоким температурам.
В еще одном варианте реализации изобретения часть нагревательного элемента может быть расположена внутри материала-носителя. Например, некоторые или все нагревательные элементы могут быть по меньшей мере частично окружены материалом-носителем. В таких устройствах материал-носитель дополнительно имеет форму, согласующуюся с формой нагревательного элемента; то есть форма материала-носителя подходит к форме нагревательного элемента, чтобы облегчить тесный контакт между нагревательным элементом и материалом-носителем. Благодаря этому существует относительно большая площадь контакта между нагревательным элементом и материалом-носителем. Конструкция устройства таким образом обеспечивает более быструю и эффективную теплопередачу от нагревательного элемента к материалу-носителю для дальнейшего содействия контролю за высвобождением доставляемого вещества. «Контроль за высвобождением» может относиться к контролю за общим количеством и/или скоростью высвобождения доставляемого вещества из устройства во время использования.
Материал-носитель может быть изготовлен in situ, то есть в присутствии нагревательного элемента, для того, чтобы форма материала-носителя дополняла форму нагревательного элемента. Формирование материала-носителя таким образом может быть достигнуто в случаях, когда материал-носитель сформирован из пастообразной массы. Указанную пастообразную массу наносят на нагревательный элемент (который может, например, быть сформирован в виде катушки, сетки или прямой проволоки), а затем дают ей затвердеть. В качестве альтернативного варианта, материал-носитель может быть выполнен в виде твердого материала, который предварительно сформирован так, чтобы соответствовать конкретной конструкции нагревательного элемента. Например, материал-носитель может быть выполнен в виде блока материала, который при необходимости содержит одну полость или более (например, цилиндрическое отверстие), в которых может быть расположен нагревательный элемент после сборки устройства для ингаляции. В качестве альтернативного варианта, материал-носитель может быть сформирован из пастообразной массы, которую наносят на форму, дают затвердеть и затем удаляют с формы, чтобы позже его можно было включить в устройство для ингаляции. Форма сформирована так, что материал-носитель затвердевает в виде форме (то есть профиля), которая дополняет конкретную конструкцию нагревательного элемента. В вариантах реализации изобретения, в которых материал-носитель выполнен в качестве компонента в сменном элементе (как описано ниже), в этих элементах могут использоваться предварительно сформированные блоки материала-носителя, имеющие стандартизованную форму. Материалы-носители, которые могут быть сформированы при относительно низких температурах (например, ниже 400°С), такие как химически связанные керамические материалы и геополимеры, особенно подходят для изготовления предварительно сформированных блоков благодаря своим поддающимся формованию свойствам незатвердевших смесей материалов-носителей.
Материалы-носители, которые могут быть сформированы при относительно низких температурах (например, ниже 400°С), такие как химически связанные керамические материалы и геополимеры, также особенно подходят для использования с системами индукционного нагрева. Проводящий материал (будь то в виде дискретных частиц или любой другой структуры (структур)) может быть перемешан со всей смесью материала-носителя и доставляемого вещества путем введения проводящего материала до того, как материал-носитель затвердеет или будет отвержден. Композитная смесь, содержащая материал-носитель (или его предшественники), доставляемое вещество и проводящий материал, обычно представляет собой пастообразную массу, которая может быть отлита в любую требуемую форму после добавления проводящего материала. Затем композит может быть отвержден без использования высоких температур, которые могли бы расплавить проводящий материал. С другой стороны, обычные способы спекания могут включать температуры, которые превышают 1000°С и которые могут расплавить многие металлы.
Проводящий материал может в качестве альтернативного варианта представлять собой трехмерную сетку металла, которую можно получить с помощью способов, включающих трехмерную печать. Композитная смесь, содержащая материал-носитель (или его предшественники), доставляемое вещество и проводящий материал, может быть получена путем предварительной подготовки трехмерной сетки металла и последующего включения формовочной пасты из предшественника керамического кристаллоносителя, содержащей как предшественник(и) керамического кристаллоносителя, так и доставляемое вещество.
В некоторых вариантах реализации изобретения устройство является устройством многоразового использования. В одном примере после использования, т.е. когда доставляемое вещество в хранилище устройства частично или полностью исчерпано, в поры материала-носителя может быть добавлен дополнительный запас доставляемого вещества для пополнения устройства. Это может быть достигнуто путем приведения в течение определенного периода времени полностью или частично израсходованного материала-носителя в гидравлическое сообщение с внешним резервуаром, содержащим доставляемое вещество. Такой внешний резервуар предпочтительно предоставляется в виде запаса доставляемого вещества (или материала, содержащего доставляемое вещество), которое хранится отдельно от устройства между последующими заполнениями.
Материал-носитель и доставляемое вещество могут в качестве альтернативного варианта быть объединены вместе в сменном контейнере. Такой контейнер должен быть подходящим для использования в ингаляционных устройствах по данному изобретению, как описано в данном документе. В такой системе хранилище доставляемого вещества в устройстве может быть легко пополнено путем удаления отработанного контейнера из ингаляционного устройства и замены ее на полный контейнер (то есть контейнер, который содержит требуемое количество доставляемого вещества). Ингаляционные устройства, которые позволяют заменять контейнеры, содержащие доставляемое вещество, также являются многоразовыми устройствами.
Таким образом, в соответствии со вторым аспектом данного изобретения, предложен контейнер, подходящий для использования в устройстве для ингаляции, как описано в данном документе, причем указанный контейнер содержит:
(i) твердый, пористый материал-носитель, имеющий пористость по меньшей мере 10%; и
(ii) доставляемое вещество, как определено выше, находящееся внутри пор материала-носителя.
Поскольку устройства по данному изобретению предназначены для использования в доставке активных фармацевтических веществ, отдельные блоки (например, в виде сменных контейнеров, как описано выше, или в виде блоков, гранул, таблеток, дисков или палочек, как описано ниже), которые содержат одно или более активных фармацевтических веществ и которые пригодны для использования с этими устройствами, могут быть предоставлены конечному пользователю. Таким образом, эти отдельные единицы препаратов представляют собой вариант реализации «контейнера», который является вторым аспектом изобретения.
Отдельные единицы препаратов могут поставляться конечному пользователю отдельно или вместе с устройством для ингаляции. Каждая отдельная единица препарата содержит достаточное количество активного фармацевтического вещества для обеспечения требуемого количества доз (например, не более одной или двух доз для злоупотребляемых веществ, таких как опиоидные анальгетики) для пользователя, и поэтому может быть описана как «препарат с разовой дозой» или «препарат с контролируемой дозой». Когда пациенту назначают режим лечения, предусматривающий множество доз лекарственного средства, это лекарственное средство (предпочтительно лекарственное средство, не подлежащее злоупотреблению) может доставляться в препарате с контролируемой дозой, в котором каждая единица (т.е. каждая гранула, таблетка и т.д.) содержит достаточное количество лекарственного средства для обеспечения множества доз (например, по меньшей мере 5, по меньшей мере 20 или по меньшей мере 100 доз) при использовании в устройстве по данному изобретению. В случае препаратов с контролируемой дозой, которые содержат множество доз, эти препараты могут нагреваться в устройствах несколько раз в ходе лечения, причем с каждым событием нагрева облегчается доставка пациенту отдельной дозы.
В дополнительном варианте реализации изобретения предусмотрен модуль (например, сменный контейнер, препарат с разовой дозой или препарат с контролируемой дозой), содержащий:
(i) твердый пористый материал-носитель, имеющий пористость по меньшей мере 10%;
(ii) доставляемое вещество, как определено выше, находящееся внутри пор материала-носителя; и
(iii) частицы проводящего материала (например, металла), распределенные по всему материалу-носителю.
В таком варианте реализации изобретения модуль может быть использован в качестве замены отработанного контейнера в устройстве для ингаляции, как описано в данном документе. Каждый из материала-носителя, доставляемого вещества и проводящего материала может быть таким, как описано в другом месте в данном документе. Такие единичные продукты могут содержать определенное количество доставляемого вещества, например достаточное количество доставляемого вещества, что позволяет доставлять получателю контролируемую дозу (например, не более чем около одной разовой дозы) посредством ингаляции перед тем, как данный модуль эффективно исчерпается.
В вариантах реализации изобретения, в которых материал-носитель и доставляемое вещество предоставляются вместе в сменном контейнере, препарате с разовой дозой, препарате с контролируемой дозой или тому подобном, контейнер или препарат может быть выполнен таким образом, что он может быть легко удален пользователем из устройства для его замены запасным контейнером или препаратом (например, пополненным контейнером или препаратом).
В одном варианте реализации изобретения сменный контейнер, препарат с разовой дозой, препарат с контролируемой дозой или тому подобное может быть выполнен так, что носитель и доставляемое вещество находятся в непосредственной близости от нагревательного элемента в устройстве после вставки контейнера, причем они в то же время выполнены таким образом, что пользователь не может войти в физический контакт с доставляемым веществом в любое время до активации устройства. Это может помочь снизить риск непреднамеренного воздействия доставляемого вещества на пользователя при пополнении устройства. В качестве альтернативного или дополнительного варианта, сменный контейнер, препарат с разовой дозой, препарат с контролируемой дозой или тому подобное может содержать композитный материал-носитель, то есть материал, который содержит материал-носитель (например, химически связанный керамический или геополимерный материал) доставляемое вещество и частицы проводящего материала.
Запасные контейнеры могут содержать материал-носитель и доставляемое вещество вместе внутри защитной оболочки, как описано выше (например, оболочки, выполненной из иного материала, чем материал-носитель, предпочтительно из металла, сплава, керамики или геополимера), чтобы уменьшить воздействие доставляемого вещества на пользователя или свести к минимуму непреднамеренную потерю доставляемого вещества при хранении или установке в устройство.
В альтернативном варианте реализации изобретения контейнер или препарат может состоять, по существу, из материала-носителя и доставляемого вещества, необязательно вместе с частицами проводящего материала и/или одного или более дополнительных веществ, упомянутых в другом месте в данном документе, которые могут присутствовать (например, усиливающие испарение вещества, ароматизирующие вещества, вкусо-ароматические вещества, наполнители, и т.д., как должно быть известно специалисту в данной области техники). Например, контейнер может не содержать какие-либо другие элементы (кроме материала-носителя и доставляемого вещества), которые необходимы для функционирования устройства.
Варианты реализации изобретения, в которых контейнер или препарат состоит в основном из материала-носителя и доставляемого вещества (необязательно вместе с частицами проводящего материала и/или одного или более дополнительных веществ, упомянутых в других частях данного документа), могут быть, в частности, упомянуты в контексте доставки активного фармацевтического вещества. Такие контейнеры или препараты могут быть удобно предоставлены врачу, фармацевту или пациенту в виде модулей с разовой дозой или несколькими дозами препаратов, причем каждый модуль содержит определенное количество активного фармацевтического ингредиента. Благодаря предоставлению препаратов конечным пользователям в виде модулей с разовой дозой, лицам, привычно потребляющим наркотики, будет труднее получить большие количества доступного для злоупотребления лекарственного средства из таких препаратов.
Устройство для ингаляции может быть выполнено таким образом, что после использования пользователю просто необходимо удалить из устройства отработанный материал-носитель и вставить сменный модуль материала-носителя, содержащий полный запас доставляемого вещества (например, лекарственного средства). Такие сменные модули могут быть выполнены в виде блоков, дисков, таблеток, палочек или гранул материала-носителя, содержащих доставляемое вещество.
Такие сменные модули могут быть выполнены в широко используемой упаковке, коммерчески известной как «блистерная упаковка», в которой каждый модуль содержится в вакуумной упаковке, герметично запакован и извлекается по отдельности для вставки в устройство. Предоставление таких сменных модулей позволило бы свести к минимуму потери и гарантировать, что запасные контейнеры будут небольшими, и пользователю будет удобно их хранить.
Использование системы с контейнером может обеспечить лучший контроль количества доставляемого вещества, которое доставляется пользователю. Например, каждый контейнер может содержать достаточное количество доставляемого вещества (например, активного фармацевтического вещества) для предоставления пользователю определенного количества (например, не более одной фармацевтической дозы) этого доставляемого вещества.
В вариантах реализации изобретения, в которых ингаляционные устройства предназначены для использования для доставки одного или более активных фармацевтических ингредиентов, каждое отдельное устройство может содержать достаточное количество (или каждого из) активного фармацевтического ингредиента для обеспечения ограниченного, но определенного количества активного фармацевтического ингредиента для пользователя. В одном из предпочтительных вариантов реализации изобретения указанное количество может быть единственной (то есть не более чем одной) терапевтической дозировкой. В таких вариантах реализации изобретения устройство не может доставлять дополнительные количества активного фармацевтического ингредиента после того, как вышеупомянутое ограниченное количество было исчерпано. Такие устройства могут быть повторно заправлены (например, через систему контейнеров, как указано выше) или они могут быть предназначены только для ограниченного числа применений, после которых они должны быть утилизированы.
Преимущественно устройства для ингаляции по данному изобретению могут содержать более одного материала-носителя или материал-носитель, в котором разные зоны имеют разные средние размеры пор. Это позволяет сконфигурировать устройства для ингаляции таким образом, чтобы высвобождать один или более доставляемых веществ с разной скоростью. Например, такое устройство может обеспечивать первоначальное быстрое высвобождение контролируемого количества лекарственного средства с последующим замедленным высвобождением контролируемого количества либо того же, либо иного лекарственного средства, в зависимости от потребностей пользователя.
В одном из предпочтительных вариантов реализации изобретения материал-носитель выбран из одного или более керамических материалов, одного или более геополимерных материалов или одного или более металлов. Особенно предпочтительно, чтобы материал-носитель был выбран из одного или более химически связанных керамических материалов или одного или более геополимерных материалов.
Например, материал-носитель может быть выбран из одного или более спеченных керамических материалов.
Как следует понимать, термин «керамический» подразумевает включение соединений, образованных из металлических и неметаллических элементов, часто оксидов, нитридов и карбидов, которые образуются и/или обрабатываются некоторым типом процесса отверждения, который часто включает в себя воздействие теплом. В связи с этим глинистые материалы, цемент и вулканическое стекло включены в определение керамических материалов (Callister, «Material Science and Engineering, An Introduction» John Wiley & Sons, 7th edition (2007)).
Керамика может включать спеченные керамические материалы (например, каолин, метакаолин, оксид алюминия, нитрид кремния, оксид циркония, карбид кремния или их смесь).
Предпочтительно, чтобы используемый керамический материал был основан на оксиде металла (таком как оксид алюминия или оксид циркония) или особенно полезны керамические материалы на основе оксидов металлов (или металлоидов или неметаллов), поскольку они неспособны подвергаться дальнейшему окислению и, следовательно, демонстрируют хорошую стабильность при высоких температурах.
Керамический материал может также представлять собой оксид и/или двойной оксид и/или нитрид и/или карбид любого из элементов скандия, церия, иттрия, бора или, предпочтительно, кремния, алюминия, углерода, титана, циркония или тантала, или их комбинаций.
В одном из предпочтительных вариантов реализации изобретения керамический материал представляет собой оксид, нитрид и/или карбид любого из элементов кремния, алюминия, углерода, титана, циркония или тантала или их комбинаций. Конкретные материалы, которые могут быть упомянуты, включают оксид алюминия, диоксид циркония, карбид кремния, нитрид кремния и их комбинации.
Специалисту в данной области техники хорошо известны спеченные керамические материалы (включая материалы, которые образуются из оксида алюминия, оксида циркония, карбида кремния и/или нитрида кремния). Такие спеченные керамические материалы особенно полезны в качестве материалов-носителей в ингаляционных устройствах, в которых доставляемое вещество является терапевтическим веществом, которое не открыто для злоупотреблений со стороны получателя.
После спекания и формирования керамического материала в спеченные изделия может быть введено доставляемое вещество. Загрузка обычно достигается замачиванием материала-носителя в жидкости, содержащей доставляемое вещество. Эффективность загрузки, связанной с пропиткой, может быть улучшена с использованием методов вакуумной загрузки. Могут также использоваться другие способы, облегчающие формирование доставляемого вещества в поры материала-носителя с помощью капиллярных сил. Например, доставляемое вещество может быть нанесено на керамику путем распыления, фибриллирования, прокатки, нанесения покрытия методом погружения, нанесения порошкового покрытия, разбрызгивания электролита.
Размеры пор в материале-носителе могут контролироваться различными методами, известными специалисту в данной области техники. Для керамических материалов (и геополимеров) регулирование размера пор обычно достигается в процессе получения сетчатой структуры материала-носителя. Примеры способов, известных в отношении изготовления пористых подложек, описаны в Subia В. et al. (2010) Biomaterial Scaffold Fabrication Techniques for Potential Tissue Engineering Applications, Tissue Engineering, Daniel Eberli (Ed.).
Конкретным способом, который подходит для использования с керамическими материалами-носителями, используемыми в данном изобретении, является способ выщелачивания порообразующего агента, который включает использование временной фазы во время образования материала-носителя. Порообразующий материал может быть включен как часть реакционной смеси во время образования материала-носителя, чтобы способствовать образованию пор в сетчатой структуре конечного материала-носителя. Порообразующие материалы включают, например, масла, жидкости (например, воду), сахара, маннит и т.д. Затем порообразующий материал может быть удален из материала-носителя, например, путем его выжигания, когда материал-носитель нагревается во время процесса отверждения или спекания, или путем его растворения с использованием подходящего растворителя, например воды.
В керамических материалах, которые обычно изготавливаются в процессе спекания, конечная пористость также может контролироваться путем частичного завершения процесса спекания. Спекание определяется в широком смысле как отверждение при нагревании свободной массы частиц, которые находятся в контакте друг с другом, до более плотной массы. Это приводит к уменьшению удельной поверхности и пористости и к увеличению плотности. Как правило, спекание происходит в три этапа. На начальном этапе участки контакта между отдельными частицами образуются путем контактного спекания и уплотнительного спекания. На промежуточном этапе участки контакта между соседними частицами растут в размерах, а большое количество мелких частиц заменяется меньшим количеством крупных зерен. Между границами зерен происходит интенсивная усадка открытых пор, что связано с изменением геометрии пор. На заключительном этапе спекания диффузия по границам зерен и в кристаллической решетке являются преобладающими механизмами переноса вещества. Образуются изолированные закрытые поры, размеры которых уменьшаются по мере того, как происходит уплотнение.
Для достижения требуемого уровня пористости предшественник спеченного керамического материала может быть нагрет до более низкой температуры, под более низким давлением или в течение более короткого периода времени, чем это обычно имеет место в процессе нормального спекания, тем самым обеспечивая гораздо больший размер пор, который нужно сохранить. Другой способ управления пористостью конечного продукта включает в себя обеспечение полуфабриката (т.е. материала, который должен быть спечен), имеющего определенную начальную пористость. Следующий способ включает добавление контролируемого количества расходуемого материала, который теряется во время процесса спекания. Подходящие способы контроля за пористостью спеченного керамического материала раскрыты в Journal of the European Ceramic Society, Vol. 29, No. 13, 2009, 2867-2872.
В качестве альтернативного варианта, материал-носитель может быть основан на одном или более химически связанных керамических материалах. Один или оба из них могут быть представлены в виде гранул.
Подходящие химически связанные керамические материалы включают негидратированные, частично гидратированные или полностью гидратированные керамические материалы или их комбинации.
Неограничивающие примеры химически связанных керамических систем включают фосфаты кальция, сульфаты кальция, карбонаты кальция, силикаты кальция, алюминаты кальция, карбонаты магния и их комбинации. Предпочтительные химические составы включают составы, которые основаны на химически связанных керамических материалах, которые после гидратации одного или более подходящих веществ-предшественников потребляют контролируемое количество воды для образования сетки.
Другими доступными системами являются системы, которые основаны на алюминатах и силикатах, причем и те, и другие потребляют большое количество воды. Могут быть использованы фазы, такие как СА2, СА, СА3 и С12А7, а также C2CA3S и C3S в кристаллическом или аморфном состоянии (С=СаО, А=Al2O3, SiO2=S, в соответствии с общей терминологией цемента), которые легко доступны. Фазы алюмината кальция и/или силиката кальция могут использоваться в виде отдельной фазы или в виде смесей фаз. Вышеупомянутые фазы, все в негидратированной форме, действуют как связующая фаза (цемент) в материале-носителе при гидратации. Массовое отношение жидкости (воды) к цементу обычно находится в диапазоне от 0,2 до 0,5, или предпочтительно, в диапазоне от 0,3 до 0,4.
Другие материалы, которые могут быть упомянуты в этом отношении, включают глинистые минералы, такие как силикат алюминия и/или гидрат силиката алюминия (кристаллический или аморфный). Неограничивающие примеры включают каолин, дикит, галлуазит, накрит, цеолит, иллит или их комбинации, предпочтительно галлуазит.
В других вариантах реализации изобретения пористый твердый материал основан на керамическом материале, который образован из самонастраивающегося керамического материала. Неограничивающие примеры самонастраивающихся керамических материалов включают сульфат кальция, фосфат кальция, силикат кальция и материалы на основе алюмината кальция. Конкретные керамические материалы, которые могут быть упомянуты в этом отношении, включают альфа-трикальцийфосфат, полугидрат сульфата кальция, CaOAl2O3, СаО(SiO2)3, CaO(SiO2)2 и тому подобное.
Другие керамические материалы, которые могут быть использованы, включают материалы, которые основаны на сульфате, таком как сульфат кальция, или фосфате, таком как фосфат кальция. Конкретные примеры таких веществ включают альфа- или бета-фазу полугидрата сульфата кальция (конечный продукт дигидрата сульфата кальция), щелочный или нейтральный фосфат кальция (апатит) и кислый фосфат кальция (брушит). Как и в случае спеченных керамических материалов, химически связанные керамические материалы могут быть загружены путем пропитывания керамического материала жидкостью, содержащей доставляемое вещество, или любым другим способом, который облегчает включение доставляемого вещества в поры керамического материала посредством капиллярных сил (включая распыление, фибриллирование, прокатку, нанесение покрытия методом погружения, порошковое покрытие или разбрызгивание).
Размер зерен керамического материала (например, силиката алюминия) может быть меньше чем около 500 мкм, или предпочтительно, меньше чем около 100 мкм, или более предпочтительно, меньше чем около 50 мкм и, в частности, меньше чем около 20 мкм по результатам измерений с помощью лазерной дифракции усредненного по объему диаметра частиц (например, с помощью системы Malvern Mastersizer). Использование керамического материала с более крупными размерами зерен может приводить к менее оптимальной установке и снижению прочности конечного твердого вещества, хотя и может обеспечить более удобную работу с цементом. Зерна могут иметь любую форму (например, сферическую, закругленную, игольчатую, пластинчатую и т.д.). В устройствах по данному изобретению могут быть использованы материалы-носители с размерами зерен менее 1 мкм, но предпочтительные размеры зерен составляют по меньшей мере 1 мкм для облегчения процесса изготовления (чтобы избежать образования очень вязких пастообразных масс при смачивании) и предпочтительно в диапазоне около 10 мкм. Эти размеры зерен подходят для всех керамических материалов в контексте устройств по данному изобретению, включая, но не ограничиваясь как спеченными, так и химически связанными керамическими материалами, описанными в данном документе. Зерна могут иметь любую форму (например, сферическую, закругленную, иглообразную, пластинчатую и т.д.). Во избежание сомнений, когда материал-носитель сформирован из геополимеров, размер зерен материала может также быть менее чем около 100 мкм, или более предпочтительно, менее чем около 50 мкм и, в частности, меньше чем около 20 мкм.
Средний размер зерен любых частиц порошкообразного керамического предшественника может быть менее чем около 500 мкм, например, менее чем около 100 мкм, или предпочтительно, от около 1 мкм до около 30 мкм. Это усиливает гидратацию. Такой материал-предшественник может быть преобразован в наноразмерную микроструктуру во время гидратации. Эта реакция включает растворение материала-предшественника и повторное последующее осаждение гидратов с наноразмерной структурой в воде (растворе) и на оставшемся негидратированном материале-предшественнике. Эта реакция благоприятно продолжается до тех пор, пока материалы-предшественники не будут преобразованы и/или пока не будет измерена предварительно выбранная пористость, определяемая частичной гидратацией с помощью времени и температуры, а также количества H2O в жидкости и/или влажности.
Химически связанные керамические материалы особенно подходят для использования в качестве материалов-носителей для активных фармацевтических веществ. Эти материалы-носители относительно дешевы и просты в изготовлении и обеспечивают адекватное высвобождение летучего доставляемого вещества под воздействием тепла.
Во избежание сомнений пористый твердый материал может содержать более одного керамического материала, например, включая смесь спеченных и химически связанных керамических материалов.
Размеры пор в химически связанных керамических материалах могут контролироваться различными методами в процессе получения сетчатой структуры материала-носителя. Конкретным способом, который подходит для использования с химически связанными керамическими материалами-носителями, используемыми в данном изобретении, является способ выщелачивания порообразующего вещества, который включает использование расходной фазы во время образования материала-носителя. Порообразующий материал может быть включен как часть реакционной смеси во время образования материала-носителя, чтобы способствовать образованию пор в сетчатой структуре конечного материала-носителя. Порообразующие материалы включают, например, масла, жидкости (например, воду), сахара, маннит и т.д. Затем порообразующий материал может быть удален из материала-носителя, например, путем его выжигания, когда материал-носитель нагревается во время процесса отверждения, или путем его растворения с использованием подходящего растворителя. Растворение обычно достигается с помощью воды, чтобы избежать образования остаточного количества вещества, которое может оказывать вредное воздействие на работу устройства или неблагоприятное воздействие на пользователя.
Способы вспенивания также могут быть использованы для увеличения размеров пор в химически связанных керамических материалах, а также других материалов-носителей, упомянутых в данном документе. Такие способы будут известны специалисту в данной области техники и особенно полезны для формирования материалов-носителей с большими размерами пор.
В качестве альтернативного варианта, материал-носитель может быть основан на одном или более геополимерных материалах.
Специалисту в данной области техники должно быть понятно, что термин «геополимер» будет включать или подразумевать любой материал, выбранный из класса синтетических или природных алюмосиликатных материалов, который может быть образован путем вступления материала-предшественника алюмосиликата (предпочтительно в виде порошка) в реакцию с водной щелочной жидкостью (например, раствором), предпочтительно в присутствии источника диоксида кремния.
Под термином «источник диоксида кремния» подразумевается любая форма оксида кремния, такая как SiO2, включая силикат Специалист в данной области техники поймет, что диоксид кремния может быть изготовлен в нескольких формах, включая стекло, кристалл, гель, аэрогель, аэрозольный диоксид кремния (или пирогенный диоксид кремния) и коллоидный диоксид кремния (например, аэросил).
Подходящие материалы-предшественники алюмосиликата обычно (но не обязательно) являются кристаллическими по своей природе и включают каолин, дикит, галлуазит, накрит, цеолиты, иллит, предпочтительно дегидроксилированный цеолит, галлуазит или каолин и, более предпочтительно, метакаолин (т.е. дегидроксилированный каолин). Дегидроксилирование (например, каолина) предпочтительно осуществляют путем прокаливания (т.е. нагревания) гидроксилированных алюмосиликатов при температурах выше 400°С. Например, метакаолин может быть приготовлен, как описано Stevenson and Sagoe-Crentsil в J. Mater. Sci., 40, 2023 (2005) и Zoulgami et al в Eur. Phys J. AP, 19, 173 (2002), и/или как описано ниже. Дегидроксилированный алюмосиликат может быть также изготовлен путем конденсации источника диоксида кремния и пара, содержащего источник оксида алюминия (например, Al2O3).
Таким образом, в следующем варианте реализации изобретения материал-носитель может быть материалом, получаемым в процессе взаимодействия материала-предшественника алюмосиликата, такого как материал, выбранный из группы, состоящей из каолина, дикита, галлуазита, накрита, цеолитов, иллитов, дегидроксилированного цеолита, дегидроксилированного галлуазита и метакаолина, с водной щелочной жидкостью, необязательно в присутствии источника диоксида кремния.
Вещества-предшественники также могут быть получены с использованием золь-гель методов, обычно приводящих к образованию аморфного порошкообразного (или частично кристаллического) предшественника алюмосиликата нанометрового размера, как описано Zheng et al в J. Materials Science, 44, 3991-3996 (2009). Это приводит к более мелкой микроструктуре отвержденного материала. (Такие способы, как золь-гель методы, также могут быть использованы при изготовлении веществ-предшественников для химически связанных керамических материалов, описанных выше).
При использовании в виде порошка, средний размер зерен частиц предшественника алюмосиликата составляет менее чем около 500 мкм, предпочтительно менее чем около 100 мкм, или более предпочтительно, менее чем около 30 мкм.
При формировании геополимерных материалов такие вещества-предшественники могут быть растворены в водном щелочном растворе, например, со значением рН по меньшей мере около 12, или например, по меньшей мере около 13. Подходящие источники ионов гидроксида включают сильные неорганические основания, такие как гидроксиды (например, гидроксид натрия) щелочного или щелочноземельного металла (например, Ва, Mg или, более предпочтительно, Са или особенно Na или K, или их комбинации). Молярное отношение катиона металла к воде может варьироваться от около 1:100 до около 10:1, или предпочтительно, от около 1:20 до около 1:2.
Источник диоксида кремния (например, силикат, такой как SiO2) предпочтительно добавляют к реакционной смеси с помощью некоторых средств. Например, водная щелочная жидкость может содержать SiO2, образуя то, что часто называют растворимым стеклом, то есть раствор силиката натрия. В таких случаях соотношение SiO2 к воде в жидкости составляет предпочтительно вплоть до около 2:1, более предпочтительно вплоть до около 1:1, и наиболее предпочтительно вплоть до около 1:2. Водная жидкость может также при необходимости содержать алюминат натрия.
В альтернативном варианте силикат (и/или оксид алюминия) можно добавлять к необязательно порошкообразному предшественнику алюмосиликата, предпочтительно в виде пирогенного диоксида кремния (микросилика, диоксида кремния AEROSIL®). Количество, которое может быть добавлено, предпочтительно составляет вплоть до около 30 мас. %, или более предпочтительно, вплоть до около 5 мас. % алюмосиликатного предшественника.
Присутствие свободных гидроксидных ионов в этой промежуточной щелочной смеси приводит к растворению атомов алюминия и кремния из исходного материала (материалов). Затем геополимерные материалы могут быть образованы за счет того, что может быть установлена (отвердиться или затвердеть) полученная смесь, причем в ходе этого процесса атомы алюминия и кремния из исходных материалов переориентируются с образованием твердого (и по меньшей мере в значительной степени) аморфного геополимерного материала. Отверждение может быть проведено при комнатной температуре, при повышенной температуре или при пониженной температуре, например, при температуре около или чуть выше температуры окружающей среды (например, от около 20°С до около 90°С, например около 40°С). Затвердевание может также выполняться в любой атмосфере, при любой влажности или давлении (например, в вакууме или иной среде). Полученная в результате неорганическая полимерная сетка представляет собой в общем высококоординированный 3-мерный алюмосиликатный гель, причем отрицательные заряды на тетраэдрических позициях Al3+ уравновешиваются в плане зарядов катионами щелочных металлов.
В этом отношении материал-носитель на основе геополимера может быть образован путем смешивания порошка, содержащего предшественник алюмосиликата, и водосодержащей жидкости (например, раствора), источника ионов гидроксида, как описано выше, и источника диоксида кремния (например, силиката) для образования пастообразной массы. Отношение жидкости к порошку предпочтительно составляет от около 0,2 до около 20 (в весовом отношении), или более предпочтительно, от около 0,3 до около 10 (в весовом отношении). Силикат кальция и алюминат кальция также могут быть добавлены к компоненту-предшественнику алюмосиликата.
В одном из предпочтительных вариантов реализации изобретения доставляемое вещество совместно вкрапливается в поры в сети материала-носителя. Это означает, что, независимо от процесса, который используется для образования материала-носителя, он также должен обязательно образовывать поры, внутрь которых вкрапливается доставляемое вещество. Материал-носитель, который основан на одном или более химически связанных керамических материалах или одном или более геополимерных материалах, особенно подходит для использования в таких вариантах реализации изобретения, как способ, с помощью которого образуется материал-носитель и его пористая сеть, так как это не требует очень высоких температур, в отличие от спеченных керамических материалов.
Таким образом, доставляемое вещество (или смесь, содержащая доставляемое вещество) может быть смешано с материалом-носителем (например, керамическим, геополимерным или металлическим) или к ним может быть добавлен предшественник (предшественники), посредством различных методов, таких как введение в виде золь-гель метода, в виде раствора или в виде суспензии, пасты или пластичного вещества, например, частиц, гранул или крупиц его материала-носителя или предшественника (предшественников) в присутствии соответствующей жидкости (например, водного или органического растворителя). Затем следует определенный способ «отверждения», чтобы образовать композицию с замедленным высвобождением, которая содержит указанные поры, в которых находится доставляемое вещество. Можно сказать, что материалы-носители, которые сформированы таким образом, являются предварительно заполненными доставляемым веществом (например, никотином).
Такие поры сами по себе представляют трехмерную сетку каналов или пустот внутри твердой сетчатой структуры, содержащей (например, частицы) доставляемого вещества.
Таким образом, такие поры могут быть, по существу, «вторичными порами», образованными за счет химических взаимодействий (например, «связывание») между поверхностями первичных частиц материала-носителя (которые могут быть пористыми по своей природе (т.е. содержат «первичные» поры), например керамические материалы или геополимеры. Такие поры могут, например, быть результатом воздействия на такие материалы одного или более химических реагентов, которые вызывают физическое и/или химическое преобразование (например, частичное растворение) при последующем физическом и/или химическом связывании этих поверхностей между собой (что само по себе может быть результатом какого-либо другого физико-химического процесса, такого как сушка, отверждение и т.д.), приводя к возникновению указанных пор/пустот.
В таких случаях подобные химические реагенты могут быть смешаны вместе с доставляемым веществом (или смесью, содержащей доставляемое вещество) во время приготовления материала-носителя. Однако такие вторичные поры не обязательно образуются таким образом, и связывание первичных частиц материалов-носителей между собой также может быть физическим и/или механическим или может быть образовано во время производства трехмерной, химически связанной керамической сети, как описано выше, в присутствии доставляемого вещества.
Таким образом, предусмотрено устройство для доставки доставляемого вещества в виде аэрозоля или пара, содержащее материал-носитель, который представляет собой твердую непрерывную трехмерную сетчатую структуру, содержащую частицы керамического материала, причем частицы связываются друг с другом с образованием вторичных пор или пустот, а доставляемое вещество находится в указанных вторичных порах или пустотах.
В качестве альтернативного варианта, если сетка образована посредством химической реакции (например, полимеризации или как описано выше для геополимеров), доставляемое вещество может быть смешано со смесью предшественника, содержащей соответствующие реагенты, и после этого размещено в порах или пустотах, которые образуются во время образования самой трехмерной сетки материала-носителя.
Особенно предпочтительно, чтобы керамический материал был основан на химически связанном керамическом материале или геополимере, поскольку эти материалы особенно подходят для облегчения загрузки никотина до того, как в носителе сформируется сетка пор. Это, в свою очередь, предлагает эффективный способ для надежного контроля за количеством никотина, которое загружается в носитель во время производства. Такие устройства, в частности устройства, которые основаны на геополимерах, являются предпочтительными, когда устройство для ингаляции содержит активный фармацевтический ингредиент, которым можно злоупотреблять.
Для геополимеров контроль за размером пор обычно осуществляется в процессе изготовления сетчатой структуры материала-носителя. Примеры известных способов изготовления пористых подложек описаны в Subia В. et al. (2010) Biomaterial Scaffold Fabrication Techniques for Potential Tissue Engineering Applications, Tissue Engineering, Daniel Eberli (Ed.).
Конкретным способом, который подходит для использования с геополимерными материалами-носителями, используемыми в данном изобретении, является способ порообразующего выщелачивания, описанный выше в отношении керамических материалов-носителей. Порообразующие материалы, которые могут быть использованы при образовании пористого геополимерного материала, включают, например, масла, жидкости (например, воду), сахара, маннит ит.д.
В другом альтернативном варианте материал-носитель может быть основан на одном или более металлах.
Термин «металл» подразумевает как чистые металлы, так и сплавы (т.е. смеси двух или более металлов). Подходящие металлы, которые могут быть использованы в качестве материалов-носителей, включают металлы, которые остаются твердыми вплоть до температуры нагрева или выше температуры нагрева, используемой в устройствах по данному изобретению, например, выше 400°С или предпочтительно выше 500°С. Конкретные металлические материалы-носители включают материалы, которые основаны на титане, никеле, хроме, меди, железе, алюминии, цинке, марганце, молибдене, платине и сплавах, содержащих эти металлы. Так называемые тугоплавкие металлы могут также использоваться с учетом их высокой устойчивости к нагреву и износу.
Специфические чистые металлы и сплавы, которые могут быть использованы в этом контексте, включают латунь, марганец, молибден, никель, платину, цинк и, в частности, включают титан, титановые сплавы, никель-хромовые сплавы, медно-никелевые сплавы, железо, сталь (например, нержавеющая сталь), алюминий, сплавы железа, хрома и алюминия.
Размеры пор в металлических материалах-носителях могут контролироваться различными методами, известными специалисту в данной области техники. Примеры подходящих способов, которые могут быть использованы для образования металлической подложки, имеющей требуемую пористость, включают трехмерную печать и сверление. Трехмерная печать пористых твердых материалов может быть достигнута с помощью обычного устройства для трехмерной печати, а размеры пор, составляющие всего лишь 10 мкм, могут быть получены с помощью этой технологии изготовления. Специалисту в данной области техники известны способы сверления для создания пористости или повышения уровня пористости в материалах. Такие способы могут быть особенно полезны, поскольку они обеспечивают более высокую степень контроля за размерами пор и общим уровнем пористости в материале. Такие способы сверления могут быть использованы для образования пор, имеющих средний размер, равный всего лишь около 100 мкм и, возможно, меньше.
Внутренняя пористость также может быть образована в металлических структурах (особенно в случаях, когда металлическая структура присутствует в качестве проводящей части системы индукционного нагрева) посредством способа расширения газа (или вспенивания) на основе горячего изостатического прессования (HIPing). В результате этих процессов образуются пористые тела, как правило, с 20-40%-й изолированной пористостью. Пористость может формироваться гораздо быстрее при вспенивании в высокореактивных многокомпонентных порошковых системах, таких как системы, которые подвергаются самораспространяющемуся высокотемпературному синтезу (SHS). Высокоэкзотермические реакции, инициированные либо локальным, либо общим нагревом прессованных порошковых смесей до температуры реакции воспламенения, приводят к испарению гидратированных оксидов на поверхностях порошка и выделению газов, растворенных в порошке. Реакционная порошковая смесь нагревается быстро, чтобы образовать жидкость, содержащую (в основном водород) пузырьки газа и, когда реакция завершена, она быстро охлаждается, захватывая газ для образования пены. Газообразование и расширение пены могут быть усилены добавлением парообразующих фаз, таких как углерод (который горит в воздухе для получения СО) или пенообразователи, которые взаимодействуют друг с другом для повышения температуры реакции и получения мелких частиц, которые стабилизируют пену. Другие подходящие способы, известные специалисту в данной области техники, описаны в работе Andrew Kennedy (2012). Porous Metals and Metal Foams Made from Powders, Powder Metallurgy, Dr. Katsuyoshi Kondoh (Ed.).
Любой из материалов-носителей, описанных в данном документе, может быть использован в устройствах по данному изобретению. Таким образом, в следующем варианте реализации изобретения данное изобретение относится к устройству, описанному выше, в котором керамический материал выбирается из группы, включающей:
(i) оксид, нитрид и/или карбид любого из элементов: кремния, алюминия, углерода, титана, циркония или тантала и их комбинаций;
(ii) материал, получаемый в процессе взаимодействия материала-предшественника алюмосиликата с водной щелочной жидкостью;
(iii) фосфат кальция, сульфат кальция, карбонат кальция, силикат кальция, алюминат кальция, карбонат магния, силикат алюминия и их комбинации; а также
(iv) латунь, марганец, молибден, никель, платину, цинк, титан, титановые сплавы, никель-хромовые сплавы, медно-никелевые сплавы, железо, сталь, алюминий и сплавы железа, хрома, алюминия.
Особенно предпочтительными являются материалы, перечисленные в пунктах (ii) и (iii) выше.
Нами было обнаружено преимущество, состоящее в том, что устройства согласно данному изобретению обеспечивают высвобождение доставляемого вещества в виде аэрозоля или пара, так что доставляемое вещество может вводиться пользователю посредством ингаляции. При использовании устройство для ингаляции позволяет пользователю вдыхать доставляемое вещество, как правило, для использования в рекреационных целях. В вариантах реализации изобретения, в которых доставляемое вещество является никотином, устройство для ингаляции может использоваться для терапевтических целей, например, для снижения частоты курения.
Доставляемое вещество может быть предусмотрено в устройстве в составе смеси, содержащей один или более дополнительных компонентов. Один или более указанных дополнительных компонентов могут присутствовать, чтобы облегчить улетучивание доставляемого вещества при нагреве материала-носителя. В устройствах для ингаляции по данному изобретению материал-носитель имеет определенную пористость, и это помогает контролировать количество и/или скорость доставки доставляемого вещества, получаемого пользователем.
Таким образом, доставляемое вещество может быть предоставлено в смеси, содержащей один или более агентов, повышающих испарение, то есть агентов, которые усиливают парообразование пара доставляемого вещества. Подходящие средства, повышающие испарение, включают глицерин, растительный глицерин (VG), пропиленгликоль, полиэтиленгликоль или их смеси.
Однако устройства по данному изобретению могут преимущественно обеспечивать реализацию способа, с помощью которого доставляемое вещество может доставляться пользователю без необходимости использования агентов, повышающих испарение, таких как агенты, указанные выше, которые могут потенциально быть токсичными или свойства которых могут ухудшаться в процессе нагрева с образованием токсичных побочных продуктов. Таким образом, в одном из предпочтительных вариантов реализации изобретения доставляемое вещество предоставляется (в материале-носителе) либо отдельно, либо в смеси, которая не содержит никаких из вышеупомянутых агентов, повышающих испарение.
В другом варианте реализации изобретения доставляемое вещество может быть предоставлен в смеси, содержащей одно или более дополнительных веществ, которые не предназначены для предоставления пользователю какой-либо терапевтической пользы. В качестве примера указанные дополнительные вещества могут присутствовать, чтобы помочь в изготовлении продукта, помочь в испарении доставляемого вещества или повысить качество услуги для пользователя.
Аэрозоль или пар, который доставляется пользователю, по существу, состоит из воздуха, доставляемого вещества (например, никотина) и потенциально одного или более необязательных дополнительных веществ (например, агента, повышающего испарение), которые могут присутствовать в смеси с доставляемым веществом. Например, аэрозоль или пар может также содержать любой требуемый ароматизатор (например, ароматизатор или подсластитель, как описано в данном документе) или инертную добавку для улучшения вкуса, консистенции или текстуры аэрозоля или пара, тем самым делая терапию ингаляцией более приемлемой для пользователя (то есть пациента).
В одном варианте реализации изобретения доставляемое вещество представляет собой никотин. Никотин обычно получают из табачных изделий, например табачного масла и других экстрактов, и он обычно присутствует в таких продуктах, как никотин-битартрат. Как никотин, так и никотин-битартрат могут использоваться в описанных в данном документе устройствах для ингаляции.
Устройства для ингаляции, содержащие никотин, могут быть использованы для лечения зависимости от никотина (например, никотиновая зависимость) с целью оказания помощи индивидууму в сокращении курения или его полном прекращении.
Устройства для ингаляции, которые содержат устройство, которое выполнено с возможностью контроля за использованием устройства и, возможно, ограничения его использования пользователем, также могут быть особенно полезны для использования при лечении никотиновой зависимости. Такие устройства могут помочь пользователю вести учет характера их использования и тем самым более точно контролировать их использование с течением времени.
В более широком смысле доставляемое вещество может быть активным фармацевтическим ингредиентом. Активным фармацевтическим ингредиентом является фармацевтическое вещество, которое предназначено для введения пациенту, нуждающемуся в этом, для обеспечения терапевтической пользы или эффекта. Например, активный фармацевтический ингредиент может быть никотином и может быть предназначен для использования в терапевтических процедурах, как описано выше. В одном из предпочтительных вариантов реализации изобретения активный фармацевтический ингредиент не является никотином (или его фармацевтически приемлемой солью). Устройства по данному изобретению также могут быть выполнены с возможностью доставки пользователю множества активных фармацевтических ингредиентов. Таким образом, в следующем варианте реализации изобретения ингаляция устройств по данному изобретению включает множество активных фармацевтических ингредиентов.
Активные фармацевтические ингредиенты, которые могут быть использованы в устройствах по данному изобретению, предпочтительно включают вещества из различных фармакологических классов, например антибактериальные агенты, антигистаминные средства и противоотечные средства, противовоспалительные средства, противопаразитарные средства, противовирусные средства, местные анестетики, противогрибковые средства, амебицидалы или трихомоноцидные средства, анальгетики, анксиолитические средства, противосвертывающиеся средства, противоартритные средства, антиастматические средства, антикоагулянты, противосудорожные средства, антидепрессанты, антидиабетические средства, антиглаукомные средства, противомалярийные средства, противомикробные средства, противоопухолевые средства, средства против ожирения, антипсихотические средства, антигипертензивные средства, агенты для борьбы с аутоиммунными расстройствами, средства против импотенции, средства, препятствующие развитию болезни Паркинсона, агенты для борьбы с болезнью Альцгеймера, жаропонижающие средства, антихолинергические средства, антиязвенные средства, агенты, снижающие уровень глюкозы в крови, бронходилататоры, средства для поддержки центральной нервной системы, сердечно-сосудистые средства, когнитивные энхансеры, противозачаточные средства, средства, снижающие содержание холестерина, агенты, действующие против дислипидермии, цитостатики, диуретики, антимикробные идиодиалы, блокаторы Н2, ингибиторы протонного насоса, гормональные средства, антигемонические агенты, снотворные средства, инотропы, миорелаксанты, мышечные контрактанты, физиотерапевтические средства, седативные средства, симпатомиметики, вазодилататоры, вазоконтрикторы, транквилизаторы, электролитные добавки, витамины, урикозурические средства, сердечные гликозиды, ингибиторы мембранного оттока, ингибиторы мембранного транспортирования белка, отхаркивающие, слабительные, контрастные вещества, радиофармацевтические, визуализирующие агенты, опиоиды, пептиды, ферменты, факторы роста, вакцины, минеральные микроэлементы. Конкретные классы активных фармацевтических ингредиентов, которые могут быть упомянуты, включают в себя антигипертензивные средства, седативные средства, снотворные средства, опиоиды (в том числе используемые в качестве анальгетиков, седативных средств или для лечения кашля), а также неопиоидные анальгетики.
Активными фармацевтическими ингредиентами, которые могут быть использованы в устройствах по данному изобретению, могут быть вещества, которые являются твердыми веществами, жидкостями или газами в условиях окружающей среды. Во избежание сомнений, когда в устройствах по данному изобретению используется более одного активного фармацевтического ингредиента, эти ингредиенты могут быть предоставлены в том же или в другом физическом состоянии (например, один может быть твердым, а другой может быть жидким). В вариантах реализации изобретения, в которых один или более активных фармацевтических ингредиентов, присутствующих в устройстве, представляют собой газ в условиях окружающей среды, указанный газ может быть представлен в виде, в котором он содержится (например, растворен или суспендирован) во втором веществе, в котором смесь газа и второго вещества затем могут быть включены в материал-носитель.
Активные ингредиенты, которые могут быть использованы в устройствах по данному изобретению, предпочтительно включают любые ингредиенты, которыми могли бы злоупотребить, такие как ингредиенты, которые полезны при лечении острой или хронической боли, нарушений гиперактивности дефицита внимания (ADHD), беспокойства и нарушений сна, а также гормоны роста (например, эритропоэтин), анаболические стероиды и т.д. При использовании активных ингредиентов, которыми могли бы злоупотребить, особенно предпочтительно, чтобы керамический материал был основан на химически связанном керамическом материале или геополимере, как описано выше. Специалисты могут легко найти полный список потенциально опасных веществ, например, см. активные ингредиенты, перечисленные в следующей ссылке: http://www.deadiversion.usdoj.gov/schedules/alpha/alphabetical.htm.
Неопиоидные лекарственные вещества, которые могут быть конкретно упомянуты, включают не-опиоидные анальгетики, такие как суматриптан (и другие антагонисты 5-НТ 1); салицилаты, такие как аспирин, алоксиприн, метилсалицилат, салицилат магния, этилсалицилат, субсалицилат висмута, салицилат натрия, салициламид, салицин, бенорилат, сальсалат, этхензамид, дфлунизал, троламин салицилат, гомосалат, салицилметилэггонин, октилсалицилат, алинон, бензил салицилат, медный аспиринат и салицилат калия; психостимуляторы, такие как модафинил, амфетамин, декстроамфетамин, метамфетамин и гидроксилампатхамин и, более предпочтительно, метилфенид; бензодиазепины, такие как бромазепам, камезепам, хлордиазепоксид, клотазепам, клоксазепам, дезоразепам, эстазолам, флуазепам, флуразепам, галазепам, галоксазепам, кетазолам, лорметазепам, медазепам, ниметазепам, нордиазепам, оксазолам, пиназепам, празепам, темазепам, тетразепам и, более предпочтительно, альпразолам, клоназепам, диазепам, флунитразепам, лоразепам, мидазолам, нитразепам, оксазепам и триазолам; и другие, не бензодиазепиновые седативные средства (например, снотворные средства снотворного действия), такие как залеплон, золпидем, зопиклон и эзопикл.
Другие неопиоидные анальгетики, которые могут быть упомянуты, включают анальгетики, полученные из каннабиса, в частности, каннабиноидные вещества, и в особенности каннабиноидные вещества, происходящие из растений каннабиса. Каннабиноидные вещества, имеющие обезболивающие свойства, которые могут быть упомянуты, включают тетрагидроканнабинол, каннабидиол и каннабинол. Таким образом, ингаляционные устройства, содержащие одно или более каннабиноидных веществ, могут также использоваться в медицине, особенно при лечении боли.
В вариантах реализации изобретения, в которых доставляемое вещество представляет собой активный фармацевтический ингредиент, доставляемое вещество должно быть термически устойчивым фармацевтическим веществом, предпочтительно веществом, которое устойчиво при температурах вплоть до, по меньшей мере, около 400°С, более предпочтительно вплоть до по меньшей мере около 600°С. Использование термина «термостойкий» подразумевает, что доставляемое вещество является достаточно устойчивым при этой температуре, чтобы гарантировать, что оно не подвергнется значительному химическому распаду во время использования. Например, когда доставляемое вещество является термостойким фармацевтическим веществом, то термин «термостойкий» относится к фармацевтическим веществам, которые не демонстрируют более чем 5%-ый распад при нагреве до 200°С в течение 30 секунд.
Устройства по данному изобретению могут быть использованы для доставки активных фармацевтических веществ, температура кипения которых составляет вплоть до, по меньшей мере, 600°С. Предпочтительно, чтобы фармацевтическое вещество имело температуру кипения, которая находится на уровне или ниже приблизительно 400°С, например, на уровне или ниже приблизительно 300°С, или предпочтительно, на уровне или ниже приблизительно 200°С.
Устройства по данному изобретению могут также найти применение в составлении фармацевтических препаратов, когда дробление таблетки может подвергнуть пациента риску или может увеличить риск неблагоприятных эффектов и/или неприятного вкуса. То есть, речь идет о таких активных ингредиентах, которые можно использовать когда желательно избежать одно или более из следующего:
(i) разжевывание таблетки перед проглатыванием;
(ii) случайное разрушение при прохождении через желудочно-кишечный тракт; и/или
(iii) вмешательство ex vivo, т.е. дробление для последующего злоупотребления (см. ниже), или для удобства последующего глотания, что может привести к разрушению функциональных свойств препарата.
Такие лекарственные средства будут хорошо известны специалисту в данной области техники, а также могут быть найдены, например, по веб-ссылке http://www.ismp.org/Tools/DoNotCrush.pdf.
Однако предпочтительные фармацевтически активные ингредиенты, которые могут быть использованы в устройствах по данному изобретению, включают опиоидные анальгетики. Особенно предпочтительно, чтобы керамический материал был основан на химически связанном керамическом материале или, наиболее предпочтительно, геополимере, когда ингаляционное устройство содержит опиоидный анальгетик. Специалист в данной области техники должен понимать, что термин «опиоидный анальгетик» должен включать любое вещество, имеющееся в природе или синтетическое вещество, с опиоидными или морфиноподобными свойствами и/или которое связывается с опиоидными рецепторами, особенно с μ-опиоидным рецептором, имеющим при меньшей мере частичную агонистическую активность, таким образом оказывая обезболивающий эффект. Проблемы, связанные с потенциальным вмешательством в состав препарата и извлечение наркотиков лицами, привычно потребляющими наркотики, особенно заметны в случае опиоидов.
Опиоидные анальгетики, которые можно упомянуть, включают производные опия и опиаты, включая природные фенантрены в опиуме (такие как морфин, кодеин, тебаин и их аддукты Дильса-Альдера) и полусинтетические производные опийных соединений (таких как диаморфин, гидроморфон, оксиморфон, гидрокодон, оксикодон, этарфин, никоморфин, гидрокодиин, дигидрокодеин, метопон, норморфин и N-(2-фенилэтил)норморфин). Другие опиоидные анальгетики, которые могут быть упомянуты, включают полностью синтетические соединения с опиоидными или морфиноподобными свойствами, включая производные морфинана (такие как рацемерафан, леворфанол, декстрометорфан, леваллофан, циклофан, буторфанол и налбуфин); производные бензоморфана (такие как циклозацин, пентазоцин и феназоцин); фенилпиперидины (такие как петидин (меперидин), фентанил, альфентанил, суфентанил, ремифентанил, кетобемидон, карфентанил, анилидин, пиминодин, этогептазин, альфапродин, бетапродин, 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МРТР), дифеноксилат и лоперамид), фенилгептамины или соединения с «открытой цепью» (такие как метадон, изометадон, пропоксифен и левометадилацетат гидрохлорид (LAAM)); производные дифенилпропиламина (такие как декстрорамид, пирирамид, безитрамид и декстропропоксифен); смешанные агонисты/антагонисты (такие как бупренорфин, налорфин и оксилорфан) и другие опиоиды (такие как тилидин, трамадол и дезоцин). Другие опиоидные анальгетики, которые могут быть упомянуты, включают аллилпродин, бензилморфин, клонизазин, дезоморфин, диампромид, дигидроморфин, дименоксадол, димефетаптанол, диметилэтамбутен, диоксафетилбутират, дипипанон, эттазоцин, этинтитазен, гидроксипитидин, левофенацилморфан, лофентанил, мептазинол, метазоцин, мирофин, нарциин, норпипанон, павврет, фенадоксон, феноморф, феноперидин и пропирам.
Более предпочтительные опиоидные анальгетики включают морфин, оксикодон, бупренорфин, альфентанил, суфентанил, ремифентанил и, в частности, фентанил.
Активные ингредиенты, перечисленные выше, могут быть составлены в устройствах по данному изобретению в любой конкретной комбинации.
Устройства по данному изобретению могут быть использованы практически с любым активным фармацевтическим ингредиентом или комбинацией ингредиентов, и полезность не ограничивается исключительно активным фармацевтическим ингредиентом, описанным или приведенным в качестве примера в данном изобретении.
Активные вещества могут дополнительно использоваться в виде соли или в любой другой подходящей форме, такой как, например, комплекс, сольват или пролекарство или в любой физической форме, такой как, например, аморфное состояние, в виде кристаллического или частично кристаллического материала, в виде сокристаллов или в полиморфной форме или, если необходимо, в любой стереоизомерной форме, включая любую энантиомерную, диастереомерную или рацемическую форму, или комбинацию любого из вышеуказанного.
Фармацевтически приемлемые соли никотина, которые могут быть упомянуты, включают соли присоединения кислот и соли присоединения основания. Такие соли могут быть образованы с помощью обычных способов, например, путем реакции свободной кислоты или формы свободной основы с одним или более эквивалентами пригодной кислоты или основы, необязательно в растворителе или в среде, в которой соль нерастворима, с последующим удалением указанного растворителя или указанной среды с помощью стандартных методов (например, в вакууме, путем сушки вымораживанием или путем фильтрации). Соли также могут быть получены путем замены противоиона активного вещества в форме соли на другой противоион, например, с применением пригодной ионообменной смолы.
Примеры фармацевтически приемлемых солей присоединения включают соли присоединения, полученные из минеральных кислот, таких как хлористоводородная, бромистоводородная, фосфорная, метафосфорная, азотная и серная кислоты; из органических кислот, таких как янтарная кислота и особенно винная, уксусная, лимонная, яблочная, молочная, фумаровая, бензойная, гликолевая, глюконовая, янтарная, арилсульфоновая кислоты; и из металлов, таких как натрий, магний или предпочтительно калий и кальций. В вариантах реализации изобретения, в которых доставляемое вещество является никотином, конкретная соль, которая может быть упомянута, представляет собой никотин-битартрат. Ссылки в данном случае на «никотин» включают ссылки на фармацевтически приемлемые соли никотина, такие как никотин-битартрат, если не указано иное.
Устройства по данному изобретению также могут быть выполнены с возможностью позволять пользователю контролировать и/или вести учет использования им устройства в течение неопределенного периода времени. Это может помочь пользователям и медицинским специалистам точно учитывать количество и частоту, с которой пользователь вводит (то есть один или несколько активных фармацевтических веществ) пользователю.
В еще одном варианте реализации изобретения устройства по данному изобретению могут содержать устройство для записи истории использования устройства в течение определенного периода времени. Такое устройство может содержать электронное устройство, которое регистрирует соответствующие события, такие как общее количество применений устройства, количество раз, когда устройство было пополнено (например, количество раз, когда был заменен контейнер), периоды времени, в которые устройство используется или пополняется, количество активного вещества, которое было доставлено пользователю, и тому подобное. Такие данные могут храниться в устройстве, так что они могут быть загружены в отдельное устройство обработки данных пользователем или медицинским специалистом, или устройство может дополнительно содержать устройство отображения, чтобы данные можно было визуально отображать.
В еще одном варианте реализации изобретения устройство может содержать интерфейс или блок передачи данных, позволяющие извлекать записанные данные из устройства для отдельного анализа. Подходящий интерфейс содержит универсальную последовательную шину (USB) или другой аналогичный компонент, позволяющий использовать электрическое соединение для передачи данных. В устройствах, которые содержат блок передачи данных, указанные данные могут передаваться устройством, например, через Bluetooth или подобным образом, на отдельное устройство. В каждом случае отдельным устройством может быть устройство электронной обработки данных, которое содержит подходящее программное обеспечение (например, приложение) для обработки данных, полученных от устройства для ингаляции.
В еще одном варианте реализации изобретения устройство может быть выполнено с возможностью контроля использования устройства пользователем и необязательно контроля за степенью, в которой доставляемое вещество может быть введено пользователю. Например, устройство может быть выполнено таким образом, что количество раз, которое оно может использоваться за конкретный период, может быть ограничено. Это особенно полезно, когда нежелательно, чтобы пользователь мог получать большое количество доставляемого вещества (например, активного фармацевтического вещества) в течение определенного периода времени, например, если доставляемое вещество вызывает привыкание или является токсичным или если устройство предназначено для использования детьми или умственно отсталыми лицами. Таким образом, такие устройства позволяют измерять количество доставляемого вещества, которое вводится пользователю.
Защитные покрытия могут также использоваться в сочетании с материалами-носителями описанных в данном документе устройств.
Защитные покрытия могут использоваться для контроля за скоростью испарения доставляемого вещества во время использования. Одно или несколько покрытий могут быть нанесены на внешнюю поверхность материала-носителя. Когда материал-носитель нагревается во время использования, покрытие может помочь контролировать температуру, при которой происходит испарение. Это, в свою очередь, может дополнительно способствовать контролю за доставкой доставляемого вещества, например, путем обеспечения того, что пользователь получает испаренный материал за короткий промежуток времени, и тем самым уменьшается вероятность того, что пользователь может прекратить вдыхание, прежде чем получить всю предполагаемую дозу.
Защитные покрытия также могут быть полезны для улучшения устойчивости доставляемых веществ внутри устройства. Например, покрытие может защищать одно или более доставляемых веществ от воздействий внешней среды или может выступать в качестве барьера между доставляемыми веществами, тем самым уменьшая степень их смешивания и химического взаимодействия друг с другом.
В качестве альтернативного варианта, защитное покрытие может содержать второе активный фармацевтический ингредиент, который обладает дополнительными полезными свойствами (например, второй активный фармацевтический ингредиент может быть антидотом для первого активного фармацевтического ингредиента). В иллюстративном примере первым активным фармацевтическим ингредиентом может быть терапевтический агент, которым можно злоупотреблять. Затем выбирают подходящий антидот (например, фармацевтический антагонист) с более высокой температурой кипения, чем первый активный фармацевтический ингредиент. Когда такая смесь используется в устройствах по данному изобретению, нагревание материала-носителя может контролироваться, чтобы гарантировать, что пользователь получает достаточное количество первого активного фармацевтического ингредиента, получая только минимальное количество антидота. Указанные смеси могут быть устойчивыми к злоупотреблениям, поскольку использование плохо контролируемого источника тепла, например открытого пламени, приведет к одновременному высвобождению первого активного фармацевтического ингредиента и антидота.
Материал-носитель, который используется в устройствах по данному изобретению, может быть спроектирован так, чтобы проявлять инертность за счет:
1. общей физико-химической устойчивости при нормальных условиях хранения, в том числе при температурах от около минус 80 до около плюс 50°С (предпочтительно, от около 0 до около 40°С, и более предпочтительно, в диапазоне комнатных температур, например, от около 15 до около 30°С), давлении от около 0,1 до около 2 бар (предпочтительно при атмосферном давлении), относительной влажности от около 5 до около 95% (предпочтительно от около 10 до около 75%), и/или воздействии от около 460 люкс УФ/видимого света, в течение длительных периодов времени (т.е. больше или равно шести месяцам). В таких условиях сетки материалов-носителей, как описано в данном документе, могут демонстрировать менее чем около 5%, или например менее чем около 1% химический распад /разложение, как указано выше;
2. общей физико-химической устойчивости в кислотных, щелочных и/или алкогольных (например, этанольных) условиях, при комнатной температуре и/или при повышенных температурах (например, вплоть до около 200°С), что особенно важно, когда активный ингредиент, который используется, представляет собой опиоидный анальгетик. Это может привести к менее чем около 15%-му распаду, что позволяет избегажать возможности преднамеренной экстракции ex vivo лекарственного средства для возможного злоупотребления (например, путем экстракции с помощью кислоты или спирта с последующей инъекцией, или путем нагрева керамической составляющей устройства по данному изобретению с последующим вдыханием опиоидным наркоманом выделяемого пара или дыма); а также
3. общей физической устойчивости, что опять-таки особенно важно, когда используемый активный ингредиент представляет собой опиоидный анальгетик. При этом уменьшается возможность механического измельчения или размалывания с целью извлечения активного ингредиента, как описано в пункте 2 выше, или непосредственного втягивания через нос опиоидным наркоманом полученного порошка.
Со ссылкой на приведенный выше пункт 3, в этом отношении предпочтительно, чтобы сетка имела прочность на сжатие более чем около 1 МПа, например, более чем около 5 МПа, или например, около 10 МПа на уровне микро- и наноструктур, которая достаточно высока, чтобы выдерживать разрушение материала на уровне микроструктуры, т.е. менее чем около 200 мкм.
Керамический материал, содержащий доставляемое вещество, может быть получен с помощью множества обычных методов и с использованием стандартного оборудования, известного специалисту в данной области техники, в том числе путем смешивания доставляемого вещества и материала-носителя или его предшественников.
Стандартное смешивающее оборудование может быть использовано для смешивания компонентов композиций по данному изобретению. Время смешивания, вероятно, будет варьироваться в зависимости от используемого оборудования, и специалисту в данной области техники не составит труда определить путем обычного экспериментирования подходящее время смешивания для данной комбинации ингредиента (ингредиентов).
Доставляемое вещество можно смешивать с материалом-носителем (например, керамическим материалом) с помощью множества методов, таких как введение посредством золь-гель процесса, в виде раствора, суспензии, пасты или пластичного вещества. Введение смеси, содержащей доставляемое вещество и материал-носитель (или его предшественника (предшественников)), может сопровождаться определенным «отверждением» для образования пор, в которых находится доставляемое вещество. Во время выполнения этого способа может быть образована сетчатая структура пористого материала-носителя.
Предпочтительный способ получения материала-носителя для использования в устройствах по данному изобретению включает смешивание между собой материала-носителя (например, керамического материала или его предшественника(ов)) и доставляемого вещества, а затем добавление жидкости, такой как водный растворитель (например, вода), что обеспечивает влажный гранулят.
Другой предпочтительный способ получения материала-носителя для использования в устройствах по данному изобретению включает смешивание доставляемого вещества с водным растворителем (например, водой) перед смешиванием этой смеси с материалом-носителем (например, керамическим материалом или его предшественником(ами)).
Методы влажной грануляции хорошо известны специалистам в данной области техники и включают в себя любой метод, включающий перемешивание смеси сухих частиц первичного порошка с использованием гранулирующей жидкости, причем жидкость содержит летучий инертный растворитель, такой как вода, необязательно в присутствии материала для гранулирования.
Продукт, полученный вышеуказанным способом, может быть дополнительно адаптирован за счет:
(I) экструзии гранулята (в случаях, когда происходит гранулирование);
(II) сферонизации (выдавливания влажной массы через сито для получения гранул);
(III); сушки и/или
(IV) (при необходимости) отверждения путем нагревания, с использованием обычных методов во всех случаях.
В процессе формирования материалов-носителей, содержащих геополимеры для использования в устройствах по данному изобретению, предварительно сформированный геополимер может вступить в реакцию с дополнительным предшественником алюмосиликата и водной щелочной жидкостью (например, раствором), предпочтительно в присутствии источника диоксида кремния (как описано выше), а также в присутствии доставляемого вещества, как описано выше. Для композиций по данному изобретению, содержащих геополимеры, отверждение может быть выполнено за счет того, что полученная смесь затвердевает в любой заданной форме, например, в виде блоков, пеллет, гранул или порошка. В этом отношении смесь может быть перенесена в заливочные формы и оставлена для загустения в виде пеллет/гранул или альтернативно (например, предпочтительно) пеллеты/гранулы могут быть изготовлены с использованием соответствующего метода экструзии-сферонизации. В этом случае сформированная паста (порошок и жидкая смесь) может быть выдавлена через отверстие. Размер отверстия может составлять от около 10 мкм вплоть до около 30 мм, предпочтительно от около 100 мкм до около 1 мм. Если требуются большие пеллеты/гранулы, размер отверстия может быть больше, например, от около 1 мм вплоть до около 30 мм или предпочтительно от около 1 мм вплоть до около 10 мм. Затем образовавшийся экструдат может быть помещен в сферонизатор, который обычно представляет собой вертикальный полый цилиндр с горизонтальным вращающимся диском, расположенным внутри. Когда диск вращается, экструдат разбивается на равномерную длину и постепенно превращается в сферические гранулы, которые затем могут быть отверждены, как описано выше.
В описанных выше способах первичные частицы доставляемого вещества могут быть обработаны методами, такими как шлифование, сухое измельчение, влажное измельчение, осаждение и т.д., перед гранулированием.
Во всех случаях пригодные размеры пеллет/гранул находятся в диапазоне от около 0,05 мм до около 3,0 мм (например, около 2,0 мм, например, около 1,7 мм), и предпочтительно от около 0,1 мм (например, около 0,2 мм) до около 1,6 мм (например, около 1,5 мм), например около 1,0 мм.
Материалы-носители для использования в устройствах по данному изобретению могут дополнительно содержать один или более других обычно используемых фармацевтических вспомогательных веществ. Подходящие вспомогательные вещества включают неактивные вещества, которые обычно используются в качестве носителя для активных ингредиентов в медикаментах. Подходящие вспомогательные вещества также включают вещества, которые используются в фармацевтической области, для составления фармацевтических композиций, в которых используются очень сильнодействующие, активные ингредиенты, чтобы обеспечить удобное и точное дозирование. В качестве альтернативного варианта, вспомогательные вещества также могут быть использованы в способах получения композиций по данному изобретению, чтобы помочь в обращении с необходимым активным ингредиентом.
В этом отношении фармацевтически приемлемые вспомогательные вещества включают частицы наполнителя, посредством которых включаются частицы материала, которые не участвуют химически в способе, при выполнении которого образуется материал-носитель, который используется в устройствах по данному изобретению. Такие частицы наполнителя могут быть добавлены в качестве балласта и/или могут обеспечить композицию функциональными возможностями. Неограничивающие примеры включают: диоксид циркония и сульфат бария для увеличения радионепроницаемости, которые могут быть добавлены к более мелким частицам (например, измельченным) материала-носителя, используемого в устройствах по данному изобретению. Количество добавленных частиц наполнителя может составлять вплоть до около 80 мас. %, предпочтительно вплоть до около 40 мас. % в расчете на массу материала-носителя. Предпочтительно общий объем наполнителя относительно невелик (например, менее чем около 50% по объему всей структуры материала-носителя (включая поры)), чтобы обеспечить сохранение материалом-носителем достаточной механической прочности.
Дополнительные фармацевтически приемлемые вспомогательные вещества включают углеводы и неорганические соли, такие как хлорид натрия, фосфаты кальция и карбонат кальция.
Материал-носитель можно альтернативно измельчать до состояния мелкого порошка, предпочтительно с размером частиц порошка менее чем около 100 мкм и более предпочтительно менее чем около 20 мкм. Материалы-носители с размерами зерен менее 1 мкм могут использоваться в устройствах по данному изобретению, но предпочтительные размеры зерен находятся в диапазоне около 10 мкм. Измельчение необязательно выполняется с использованием шарового помола, планетарного шарового помола, размола на струйной мельнице или их комбинации.
В вышеупомянутых вариантах реализации изобретения материал-носитель может дополнительно включать вспомогательный материал для гранулирования. Вспомогательный материал для гранулирования может быть определен как материал, который выполнен с возможностью контроля за распределением гранулирующей жидкости по всей массе влажного порошка во время гранулирования и модификации реологических свойств в смеси. Подходящие вспомогательные материалы для гранулирования включают гидроксипропилметилцеллюлозу (НРМС), гидроксиэтилцеллюлозу (НЕС) и предпочтительно микрокристаллическую целлюлозу. В случае присутствия вспомогательного материала для гранулирования его предпочтительно используют в количестве от 0,5 до 50 мас. % в расчете на общий вес препарата-таблетки. Предпочтительный диапазон составляет от 1 до 20%, например от около 2,0 до около 12 мас. % (например, около 10 мас. %).
Материал-носитель, используемый в устройствах по данному изобретению, может также необязательно содержать наполнители, порогены, дисперсионные агенты или гелеобразующие агенты для контроля за реологией и пористостью. Общее количество таких вспомогательных веществ ограничено до около 20 мас. % от общей массы материала-носителя (то есть керамического или геополимерного материала), включая любые другие компоненты, которые могут присутствовать (например, активные фармацевтические вещества, наполнители и т.д.). Неограничивающие примеры таких вспомогательных веществ включают поликарбоновые кислоты, целлюлозу, поливинилалхол, поливинилпирролидон, крахмал, нитрилотриуксусную кислоту (NTA), полиакриловые кислоты, ПЭГ, сорбит, маннит, глицерин, фармацевтически приемлемые масла (включая растительные масла (оливковое масло, масло кукурузы, масло кукурузы, арахисовое масло, подсолнечное масло, льняное масло, пальмовое масло, касторовое масло, соевое масло и т.д.), эфирные масла (например, масло примулы вечерней), масла омега-3 (например, рыбий жир), парафиновое масло, липидные масла, полученные с животных веществ, силиконовые масла и т.д.) и их комбинации.
Материал-носитель может также содержать одно или более связующих веществ. Связующее вещество может быть определено как материал, который выполнен с возможностью действовать в качестве усилителя образования связи, способствуя включению доставляемого вещества в материал-носитель. Подходящие связующие вещества включают целлюлозную смолу и микрокристаллическую целлюлозу. В случае присутствия связующего вещества его предпочтительно используют в количестве от 0,5 до 20 мас. % в расчете на общую массу материала-носителя и содержащихся в нем материалов. Предпочтительный диапазон составляет от 1 до 15%, например от около 2,0 до около 12 мас. % (например, около 10 мас. %).
Материал-носитель может также содержать одно или более веществ, исправляющих вкус лекарственного средства, ароматизаторов (например, лимона, порошка мяты перечной или, предпочтительно, ментола) или подсластителей (например, неохесперидин, ацесульфам K или, предпочтительно, сукралоза).
Материалы-носители могут также содержать один или несколько красителей (например, оксид железа для красного, кобальт для синего, оксид титана для белого и т.д.). Эти красители обычно предоставляются в виде частиц указанного окрашенного материала с соответствующим размером, чтобы можно было видеть цвет, без оказания существенного влияния на способность материала-носителя хранить доставляемое вещество и выделять его при нагревании. Как и в случае со всеми описанными выше добавками, частицы красителя могут быть добавлены к смеси керамических материалов-предшественников до того, как эта смесь будет отверждена или затвердеет.
Устройства по данному изобретению могут использоваться для доставки пользователю одного или более доставляемых веществ. Таким образом, в третьем аспекте изобретения предлагается способ доставки пользователю доставляемого вещества в виде пара или аэрозоля, который включает: обеспечение изделия, содержащего:
(i) твердый пористый материал-носитель, как определено в данном документе, имеющий пористость по меньшей мере 10%; и
(ii) доставляемое вещество, определенное в данном документе, расположенное внутри поры материала-носителя; и
нагрев материала-носителя для испарения доставляемого вещества
В одном варианте реализации изобретения изделие представляет собой устройство для ингаляции, как определено в данном документе. В альтернативном варианте реализации изобретения изделие представляет собой контейнер или модуль, который подходит для использования в устройстве для ингаляции, как определено в данном документе. Таким образом, в четвертом аспекте изобретения предлагается изделие, как определено в данном документе. В вариантах реализации изобретения, в которых изделие представляет собой контейнер, который подходит для использования в устройстве для ингаляции, как определено в данном документе, в котором содержится нагревательный элемент, предпочтительно, чтобы контейнер был сформирован так, чтобы его форма соответствовала нагревательному элементу.
В следующем варианте реализации изобретения предлагается использование изделия, как определено выше, при доставке доставляемого вещества пользователю в виде пара или аэрозоля. Аналогичным образом указанное использование будет включать этап нагрева материала-носителя для испарения доставляемого агента, чтобы его мог вдыхать пользователь.
В других конкретных вариантах реализации третьего аспекта изобретения, в частности, в вариантах реализации изобретения, в которых устройство выполнено с возможностью контроля за использованием пользователем устройства и необязательно контроля за степенью, в которой доставляемое вещество может быть введено пользователю, способ может включать введение пользователю контролируемой дозы доставляемого вещества. Это особенно полезно в тех случаях, когда доставляемое вещество вызывает привыкание или является токсичным, если устройство предназначено для использования детьми или умственно отсталыми лицами. Конкретные примеры включают способы, в которых доставляемое вещество является опиоидным анальгетиком.
Когда получаемый агент является активным терапевтическим агентом, доставка этого агента пользователю может быть предназначена для лечения заболевания или болезненного состояния. Во избежание сомнений, «лечение» подразумевает терапевтическое лечение, а также симптоматическое лечение, профилактику или диагноз состояния.
Таким образом, в пятом аспекте изобретения предлагается способ лечения или профилактики заболевания, включающий использование ингаляционного устройства, описанного выше (например, когда доставляемое вещество является активным фармацевтическим ингредиентом) для доставки активного фармацевтического ингредиента в форме аэрозоля или пара субъекту при его потребности в нем (то есть лицу, страдающему от указанного заболевания или восприимчивому к указанному заболеванию), причем указанный активный фармацевтический ингредиент лечит или предотвращает указанное заболевание.
Ингаляционные устройства по данному изобретению могут быть эффективными для использования при анестезии. В таких вариантах реализации изобретения устройства по данному изобретению могут использоваться для доставки пациенту контролируемого количества одного или более анестетиков, чтобы дать желаемый терапевтический эффект, будь то аналгезию, расслабление мышц, гипноз или любую их комбинацию.
Ингаляционные устройства по данному изобретению, содержащие опиоидные анальгетики, полезны при лечении боли, особенно острой и/или хронической боли. В соответствии с еще одним вариантом реализации изобретения предлагается способ лечения боли, который включает в себя использование ингаляционного устройства, описанного выше, для доставки одного или более опиоидных анальгетиков в виде аэрозоля или пара лицу, страдающему от боли или восприимчивому к боли.
Ингаляционные устройства по данному изобретению, содержащие неопиоидные анальгетики, также могут быть полезны при лечении боли. В вариантах реализации изобретения, в которых активный фармацевтический ингредиент представляет собой сукцинат суматриптана, устройство может быть полезным при лечении мигрени. Доставка анальгетика путем ингаляции особенно эффективна для быстрого облегчения боли, особенно у страдающих мигренью. В противоположность этому, пероральная доставка анальгетиков обычно не может обеспечить такое быстрое облегчение.
В следующем аспекте изобретения предлагается способ лечения боли, причем способ включает использование ингаляционного устройства по данному изобретению, при котором доставляемое вещество является анальгетиком, полученным из каннабиса, таким как любое из каннабиноидных веществ, упомянутых в данном документе.
В следующем аспекте изобретения предлагается способ лечения зависимости от никотина (например, никотиновой зависимости), причем способ включает использование ингаляционного устройства по данному изобретению, при котором доставляемым веществом является никотин (или его фармацевтически приемлемая соль) для доставки никотина в виде аэрозоля или пара лицу, страдающему от симптомов никотиновой зависимости. Аналогично, устройства по данному изобретению могут быть полезны в способе лечения (например, облегчения) симптомов никотиновой зависимости (включая никотиновую привязанность или никотиновую зависимость). Такие симптомы могут включать тягу к никотину, гнев/раздражительность, тревогу, депрессию, нетерпение, проблемы со сном, беспокойство, голод или увеличение веса и/или трудности с концентрацией внимания.
Никотин также могут быть использован для снижения симптомов, связанных с различными заболеваниями, в том числе деменцией, болезнью Альцгеймера, болезнью Паркинсона, болезнью Хантингтона и депрессией. Таким образом, в еще одном аспекте изобретения предлагается способ снижения симптомов, связанных с деменцией, болезнью Альцгеймера, болезнью Паркинсона, болезнью Хантингтона и депрессией, при этом способ включает использование ингаляционного устройства по данному изобретению, в котором доставляемым веществом является никотин (или его фармацевтически приемлемая соль) для доставки никотина в виде аэрозоля или пара лицу, страдающему от указанных симптомов.
Устройства для ингаляции по данному изобретению, которые содержат активный фармацевтический ингредиент, выполнены с возможностью высвобождать фармакологически эффективное количество активного ингредиента во время нормального использования. Под «фармакологически эффективным количеством» подразумевается количество активного ингредиента, которое способно дать требуемый терапевтический эффект находящемуся на лечении пациенту, независимо от того, вводится ли оно отдельно или в комбинации с другим активным ингредиентом. Эффект может быть объективным (т.е. измеряемым каким-либо анализом или маркером) или субъективным (т.е. оцениваемым по результатам опроса жалоб или ощущений субъекта относительно эффекта).
Более предпочтительные композиции по данному изобретению могут быть адаптированы (например, как описано в данном документе) для обеспечения достаточной дозы лекарственного средства через интервалы дозирования (независимо от количества доз за единицу времени) для получения требуемого терапевтического эффекта.
Таким образом, количество активных ингредиентов, которые могут быть использованы в устройствах по данному изобретению, может быть определено врачом или специалистом в данной области техники применительно к тому, что будет наиболее подходящим для отдельного пациента. Это может варьироваться в зависимости от типа и тяжести состояния, которое необходимо лечить, а также от возраста, веса, пола, функции почек, функции печени и реакции конкретного пациента, подлежащего лечению.
В одном из вариантов реализации данного изобретения устройство предназначено для разового использования и содержит достаточное количество активных фармацевтических ингредиентов, чтобы доставить не более чем одну разовую дозу того ингредиента, который должен быть доставлен получателю через ингаляцию. Альтернативно, в вариантах реализации изобретения, в которых материал-носитель и активный фармацевтический ингредиент доставляются вместе в контейнере или блоке, каждый контейнер или блок может содержать достаточное количество активных фармацевтических ингредиентов, чтобы доставлять не более чем одну дозу этого ингредиента для доставки получателю через ингаляцию.
Подходящие дозы активного ингредиента в одном блоке доставки ингаляции (например, один контейнер, содержащий материал-носитель и активный ингредиент) могут быть ниже 1 г, предпочтительно ниже 100 мг и выше 1 мкг. Когда доставляемое вещество представляет собой опиоидный анальгетик (например, фентанил) или другое лекарственное вещество, которым могут злоупотребить, устройства, контейнеры и единицы препарата, описанные в данном документе, могут преимущественно содержать только разовую единицу доставляемого вещества. Использование химически связанных керамических веществ и геополимеров в качестве материалов-носителей значительно улучшает способность контролировать количество лекарственного средства, которое хранится в устройстве (или контейнере и т.д.), и/или которое доставляется пациенту, по сравнению с препаратами, в которых лекарственное средство хранится в виде жидкости. Кроме того, такие разовые составы (особенно те, в которых материал-носитель основывается на геополимере) также гораздо менее подвержены злоупотреблениям.
В вариантах реализации изобретения, в которых доставляемое вещество представляет собой никотин, подходящие суточные дозы могут составлять от около 1 до около 100 мг/сутки. Обычные сигареты обычно содержат от около 8 до 20 мг никотина. Предпочтительно, чтобы описанные в данном документе устройства и контейнеры содержали такое количество никотина, которое, по меньшей мере, эквивалентно одной сигарете. Когда никотин подается пользователю в виде сменных контейнеров (например, таблеток, гранул или палочек), то каждый контейнер может содержать от около 8 мг до около 20 мг никотина. Поскольку устройства могут быть выполнены с возможностью доставки пациенту, по существу, всего никотина, удерживаемого в материале-носителя, каждый контейнер или устройство могут преимущественно содержать меньшее количество никотина (например, от около 100 мкг до около 5 мг или предпочтительно от около 1 мг до около 3 мг), в то же время он выполнен с возможностью доставки пациенту такого количества никотина, которое приблизительно эквивалентно количеству никотина, которое вдыхается при курении одной сигареты. Большие количества никотина также могут храниться в одном устройстве или контейнере, например в размере вплоть до 100 мг, вплоть до 500 мг или вплоть до 1 г. Такие устройства и контейнеры предназначены для многократного использования, либо в течение одного дня, либо нескольких дней, прежде чем устройство необходимо будет пополнить или контейнер необходимо будет пополнить или заменить. Такие количества никотина могут использоваться в устройствах, контейнерах и единицах препаратов, которые используются в медицине, например, при лечении зависимости от никотина (например, никотиновой зависимости), лечении (или смягчении) симптомов зависимости от никотина (включая никотиновую зависимость или отвыкание от никотина), деменции, болезни Альцгеймера, болезни Паркинсона, болезни Хантингтона и депрессии. Подходящие дозы для лечения таких заболеваний (обычно с помощью назального спрея) могут составлять от 5 до 15 мг/сутки. Следовательно, устройство или контейнер согласно изобретению могут содержать достаточное количество для одной суточной дозы или ее долю (например, половину, одну третью или одну четвертую).
Когда композиции по данному изобретению содержат опиоидные анальгетики, подходящими фармакологически эффективными количествами таких опиоидных анальгетических соединений являются количества, которые способны вызывать (например, постоянное) облегчение боли при использовании устройства, и тогда лекарственное средство вводят путем ингаляции. Таким образом, общее количество активного ингредиента опиоидного анальгетика, которое может быть использовано в устройстве по данному изобретению, будет зависеть от характера соответствующего активного ингредиента, который используется, но может находиться в диапазоне около 0,0005%, например от около 0,1% (например, около 1%, например около 2%) до около 20%, например около 10%, например, около 7% по массе в расчете на общую массу материала-носителя. Количество этого активного ингредиента также может быть выражено как количество в стандартной дозе. В таком случае количество активного ингредиента опиоидного анальгетика, которое может присутствовать, может быть достаточным для обеспечения стандартной дозы, которая составляет от около 1 мкг (например, около 5 мкг) до около 50 мг (например, около 15 мг, например около 10 мг).
Вышеуказанные дозы являются типовыми для усредненного случая; конечно, могут быть отдельные случаи, когда возможно применение больших или меньших диапазонов доз, при этом такие диапазоны включены в объем данного изобретения.
Устройства по данному изобретению, содержащие опиоидные анальгетики, полезны при лечении боли, особенно острой и/или хронической боли. Они могут быть особенно эффективными, поскольку они обеспечивают преимущественно быстрое начало действия (например, с большей скоростью, чем в случае многих других путей введения, особенно при пероральном введении). В соответствии с еще одним аспектом изобретения предлагается способ лечения боли, который включает в себя использование устройства по данному изобретению для введения опиоидного анальгетика посредством ингаляции лицу, страдающему от такого состояния или восприимчивому к нему.
Во избежание сомнений, «лечение» подразумевает терапевтическое лечение, а также симптоматическое лечение, профилактику или диагноз состояния.
Устройства согласно данному изобретению, содержащие несколько единиц доз обладают тем преимуществом избегания и/или снижения риска либо сброса дозы (т.е. непроизвольного высвобождения), либо, что не менее важно, преднамеренной экстракции ex vivo ее большей части (например, больше чем около 50%, например, около 60%, или например, около 70%, и, в частности, около 80%) дозы активного ингредиента (ингредиентов), который первоначально находится внутри материала-носителя в устройстве по данному изобретению, либо in vivo (т.е. когда композиция по данному изобретению вводится пациенту) либо ex vivo (т.е. в другую среду за пределами тела) в течение периода времени, который может вызвать нежелательные последствия, такие как неблагоприятные фармакологические эффекты (например, когда такое высвобождение происходит in vivo в непроизвольном смысле) или потенциальное злоупотребление этим активным ингредиентом (например, когда такое высвобождение преднамеренно осуществляется индивидуумом ex vivo). Такое высвобождение со сбросом дозы может, например, иметь место либо in vivo, либо ex vivo в течение около 3 часов, например, в течение около 2 часов, например, в течение около 1 часа, и, в частности, в течение около 30 минут.
Устройства по данному изобретению могут обеспечивать защиту от преднамеренного механического разрушения материала-носителя, например, обычными способами, такими как дробление, толчение и образование раствора, расплющивание и т.д., благодаря тому, что материал-носитель имеет высокий уровень прочности на сжатие на микроуровне материала.
Устройства по данному изобретению и, в частности, используемые в них материалы-носители также могут обладать преимуществом, заключающимся в том, что они могут быть получены с использованием установленных фармацевтических способов обработки и могут использовать материалы, которые одобрены для использования в пищевых продуктах или фармацевтических препаратах или могут иметь аналогичный нормативный статус.
Материалы-носители, которые используются в устройствах по данному изобретению, могут иметь преимущество, заключающееся в том, что они могут быть более эффективными; быть менее токсичными; отличаться более длительным действием; быть более активными; вызывать меньше побочных эффектов; более легко абсорбироваться; и/или отличаться лучшей фармакокинетикой и/или иметь другие пригодные фармакологические, физические или химические свойства по сравнению с фармацевтическими композициями, известными в предшествующем уровне техники, независимо от того, применяют ли их согласно указанным выше показаниям или иным образом. Это особенно относится к вариантам реализации изобретения, в которых устройство по данному изобретению или материал-носитель (например, в случае сменных контейнеров) не содержит обычный агент, повышающий испарение, такой как пропиленгликоль, глицерин или полиэтиленгликоль.
Использование описанных в данном документе материалов-носителей (в частности, химически связанных керамических материалов и геополимеров) позволяет обеспечить съемные и сменные блоки, которые будут использоваться в сочетании с нагревательными устройствами для достижения приемлемых уровней высвобождения доставляемого вещества при нагревании, при этом минимизируя риск подверженности влиянию хранящихся внутри их материалов, например, через утечку. Материалы-носители также легко изготавливаются без необходимости в высокотемпературном спекании, и поэтому дополнительные элементы, такие как проводники и магниты, могут быть включены в материал-носитель для содействия процессу нагрева. Способность включать доставляемое вещество в материал-носитель в качестве структуры материала-носителя также обеспечивает лучший контроль над количеством присутствующего доставляемого вещества.
Везде, где в данном документе используется слово «около» в контексте измерений (например, значений, температуры, давления (прилагаемых сил), относительной влажности, размеров и веса, размеров частиц или зерен, размеров пор, временных рамок и т.д.), количеств (например, относительных количеств (например, чисел или процентных отношений) частиц, отдельных составляющих в композиции или компоненте композиции и абсолютных количеств, таких как дозы активных ингредиентов, количеств частиц и т.д.), отклонений (от постоянных величин, степеней ухудшения параметров и т.д.) будет понятно, что такие переменные являются приблизительными и как таковые могут варьироваться на ± 10%, например ± 5%, и, предпочтительно, на ± 2% (например, ± 1%) от указанных в данном документе чисел.
Изобретение проиллюстрировано следующими примерами, в которых:
На фиг. 1 показано количество ибупрофена в керамических дисках перед (контролем) и после термообработки (АН; n=1). Планки погрешностей показывают максимальные и минимальные значения;
На фиг. 2 показано количество никотина в керамических дисках перед (контролем; n=1) и после термообработки (АН; n=2). Планки погрешностей показывают максимальные и минимальные значения;
На фиг. 3 показано количество никотина в стержнях из оксида алюминия до и после термообработки в печи (n=3);
На фиг. 4 показано количество никотина в стержнях из сульфата кальция до и после термообработки в печи (n=3);
На фиг. 5 показано количество никотина в пуансонах из сульфата кальция до и после термообработки в печи (n=3);
На фиг. 6 показано количество никотина в пуансонах из геополимеров до и после термообработки в печи (n=3);
На фиг. 7 показана экспериментальная установка для устройства электронной сигареты;
На фиг. 8 показано количество никотина в стержнях из сульфатов кальция до и после термообработки в устройстве электронной сигареты (n=3);
На фиг. 9 показано количество никотина в стержнях из оксида алюминия до и после термообработки в устройстве электронной сигареты (n=3);
На фиг. 10 показана экспериментальная установка для индукционных испытаний;
На фиг. 11 показано количество никотина в пуансонах из сульфата кальция до и после термообработки с использованием индукционного нагрева (n=3); а также
На фиг. 12 показано количество никотина в пуансонах из сульфата кальция до и после термообработки с использованием индукционного нагрева на предварительно нагретой пластине (n=3);
На фиг. 13 показано количество сукцината суматриптана в стержнях из Al2O3 до и после термообработки с использованием нагрева печи;
На фиг. 14 показано количество гидрохлорида клонидина в пуансонах из сульфата кальция до и после термообработки в печи (n=2);
На фиг. 15 показано количество гидрохлорида клонидина в пуансонах из сульфата кальция до и после термообработки в печи (n=2);
На фиг. 16 показано количество никотина в пуансонах из сульфата кальция до и после термообработки в печи (n=2); а также
На фиг. 17 показано количество сукцината суматриптана в пуансонах из сульфата кальция до и после термообработки в печи (n=2).
ПРИМЕРЫ
Пример 1 - нагрев в печи
Керамические диски, содержащие ибупрофен (IOL Chemicals and Pharmaceuticals Ltd, Индия) были изготовлены с использованием оксида алюминия (Al2O3; Keranova, Швеция) следующим образом.
Керамические диски (Al2O3) с разными размерами пор (0,25, 1, 6, 15 и 30 мкм) были изготовлены в двух размерах: i) диаметром 63 мм и толщиной 6,3 мм (размеры пор 0,25, 1 и 6 мкм); и ii) диаметром 48 мм и толщиной 6,3 мм (размеры пор 15 и 30 мкм). Пористость составляла около 40 об.%, а плотность составляла 3,75 г/см3 для всех дисков в соответствии со спецификацией продукта.
Диски (размеры пор 0,25, 1, 6, 15 и 30 мкм) были пропитаны 400 мл фосфатного буфера с рН 7,4 (одна фосфатно-буферная соляная таблетка (Sigma-Aldrich, США), растворенная в 200 мл деионизированной воды) с концентрацией 408,5 мкг/мл ибупрофена в течение 24 часов. Диски сушили при комнатной температуре в течение 24 часов. Диски нагревали в печи при температуре 250°С в течение 15 минут, контрольные диски не нагревали. Все диски были измерены на предмет концентрации ибупрофена в 400 мл фосфатного буфера с рН 7,4 при 37°С (способ с использованием лопастной мешалки по фармакопеи США (USP) (скорость лопастной мешалки 50 об/мин), VanKel 7025, Varian Inc., США), и концентрацию ибупрофена измеряли с помощью УФ спектрофотометра Shimadzu 1800, Япония, на длине волны 220 нм для определения количества ибупрофена в керамических дисках. Количество ибупрофена в контрольных дисках измеряли через 15 часов (т.е. после максимального высвобождения лекарственного средства) и в термообработанных дисках через 1,5 часа (т.е. в этот момент времени было высвобождено максимальное количество лекарственного средства).
Количество ибупрофена, оставшегося после термообработки, было равно нулю для всех образцов. Никаких существенных изменений в поглощении на других длинах волн не было обнаружено, что указывает на то, что не произошло значительного распада ибупрофена.
Пример 2 - нагрев в печи
Керамические диски, содержащие никотин (раствор никотина (24 мг/мл), Ritch Group Ltd, Соединенное Королевство) были изготовлены с использованием оксида алюминия (Al2O3, Keranova, Швеция) следующим образом.
Керамические диски (Al2O3) с разными размерами пор (0,25, 1, 6, 15 и 30 мкм) были изготовлены в двух размерах: i) диаметром 63 мм и толщиной 6,3 мм (размеры пор 0,25,1 и 6 мкм); и ii) диаметром 48 мм и толщиной 6,3 мм (размеры пор 15 и 30 мкм). Пористость составляла около 40 об.%, а плотность составляла 3,75 г/см3 для всех дисков в соответствии со спецификацией продукта.
На поверхности керамических дисков (размеры пор 0,25, 6, 15 и 30 мкм) распределяли раствор никотина (0,25 мл; соответствующий 6 мг никотина). Диски сушили при комнатной температуре в течение 24 часов. Диски нагревали в печи при температуре 188°С в течение 15 минут, контрольные диски не нагревали. Все диски были измерены на предмет количества никотина в 400 мл фосфатного буфера с рН 7,4 при 37°С (способ с использованием лопастной мешалки по USP (скорость лопастной мешалки 50 об/мин), VanKel 7025, Varian Inc., США), и концентрацию никотина измеряли с помощью УФ спектрофотометра Shimadzu 1800, Япония, на длине волны 252,8 нм для определения количества никотина в керамических дисках. Количество никотина в контрольных дисках измеряли через 15 часов (т.е. после максимального высвобождения никотина) и в термообработанных дисках через 1,5 часа (то в этот момент времени было высвобождено максимальное количество никотина).
Количество никотина, оставшегося после термообработки, очень значительно уменьшилось для всех образцов по сравнению с контрольными образцами предварительной термообработки. Никаких существенных изменений в поглощении на других длинах волн не было обнаружено, что указывает на то, что не произошло значительной распадаемости никотина.
Пример 3 - нагрев в печи
Стержни из оксида алюминия
Керамические стержни из оксида алюминия были получены от Ceramtech (Швеция): цилиндрические стержни из Al2O3 диаметром 3 мм и длиной 10 мм, содержащие 4 отверстия (ориентированные в осевом направлении) диаметром 0,8 мм.
Стержни и пуансоны из сульфата кальция
Стержни из альфа-полугидрата сульфата кальция (CaS) были получены от Во Ehrlander АВ (Швеция). Формованный силиконовый каучук был использован в качестве форм как для стержней (диаметр: 6 мм, длина 12 мм), так и для пуансонов (диаметр: 12 мм, толщина: 2 мм). Сульфат кальция смешивали с деионизированной водой (соотношение жидкость/порошок составило 0,4 (в весовом отношении)) для образования гомогенной пасты, которая была залита в каучуковые формы. После заполнения формы сушили в течение по меньшей мере 12 ч в условиях окружающей среды.
Геополимерные пуансоны
Чистый для анализа каолинит, коллоидальный диоксид кремния (размер частиц 7 нм) и чистый для анализа гидроксид натрия были получены от Sigma-Aldrich (Швеция). Раствор силиката натрия был изготовлен путем растворения гидроксида натрия (NaOH) и коллоидального диоксида кремния (SiO2) в деионизированной воде. Метакаолин был образован путем нагревания каолинита в течение 2 ч при 800°С.
Геополимер синтезировали путем смешивания раствора силиката натрия с метакаолином с использованием раствора и пестика до образования однородной пасты. Состав геополимера получил следующие молярные соотношения: Si/Al=1,94, H2O/Al2O3=12,24 и Na2/Al2O3=1,23. Паста была залита в формы из силиконового каучука в форме пуансона и отверждена при 100%-й влажности в течение 48 часов, при атмосферном давлении при 37°С. После отверждения геополимер высушивали при температуре окружающей среды и влажности в течение 24 часов.
Никотин
Чистый никотин по USP/EP был получен от BGP Healthcare pvt. Ltd. (Индия). Жидкость (E-juice) для электронных сигарет (LIQUA) 18 мг/мл и 24 мг/мл получили от Cigoteket (Швеция). Жидкость e-juice представляет собой раствор никотина в пропиленгликоле. Концентрации ниже 18 мг/мл достигались добавлением соответствующего количества деионизированной воды в e-juice.
Нанесение никотина
Нанесение никотина было достигнуто либо пропитыванием, либо нанесением никотина или раствора никотина в диапазоне концентраций на поверхность керамического стержня/пуансона.
(i) Нанесение никотина
Чистый никотин (в жидком состоянии), чистая жидкость для электронных сигарет (E-juice) или жидкость для электронных сигарет, разбавленная водой, наносилась и распределялась по поверхности стержней или пуансонов. После нанесения никотина образцы высушивали в течение 24 часов при комнатной температуре перед термообработкой и/или анализом.
(ii) Пропитывание никотином
Стержни были пропитаны чистым никотином или раствором никотина (точный объем не измерялся, а стержень был просто покрыт жидкостью, около 100 мкл). Образцы пропитывали в течение 24 часов при комнатной температуре, после чего сушили в течение 24 часов перед термообработкой и/или анализом.
Способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температуру установили приблизительно на 200°С. Температуру измеряли с помощью ИК термометра производства Mastech.
Обнаружение высвобождения никотина
Все испытания на высвобождение никотина проводили в соответствии с тем же аналитическим способом. Образец погружали в химический стакан, содержащий 50 мл деионизированной воды. Через 24 часа образец вынимали и фильтровали (размер пор: 0,2 мкм). Характеристики образца определяли с помощью УФ спектрофотометра на длине волны 219 нм. Затем подсчитывали количество никотина в образцах. Оценивали разницу испаренного количества в контрольном образце и термообработанном образце.
Контрольные образцы представляют количество никотина, которое было загружено до термообработки. Разница в количестве никотина, обнаруженного в термообработанных образцах и контрольном образце, представляет собой количество никотина, который испарился во время термообработки.
Результаты - оксид алюминия
Стержни из оксида алюминия пропитывали в 6 мг/мл раствора никотина (разбавленной жидкости для электронных сигарет) в течение 24 часов. Измеряли количество никотина, оставшегося в стержнях до и после термообработки, как показано на фиг. 3.
При нагревании почти весь никотин высвобождался в течение первых 5-10 мин, поскольку количество никотина, оставшегося в образцах после термообработки, было незначительным. Стержни были способны поглощать приблизительно 135 мкг никотина/стержень.
Результаты - сульфат кальция
Стержни из сульфата кальция пропитывали чистым никотином в течение 24 часов. Стержни были способны поглощать приблизительно 20 мг никотина/стержень. Измеряли количество никотина, оставшегося в стержнях после и до термообработки, как показано на фиг. 4.
Большая часть никотина высвобождалась при нагреве. Было отмечено, что в течение 5 мин нагревания высвобождалось большее количество никотина по сравнению с 1 мин нагрева.
Чистый никотин (20 мг) распределяли по пуансонам из сульфата кальция. Измеряли количество никотина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 5.
Никотин является летучим веществом, и поэтому количество никотина, обнаруженного в контрольном образце, было меньше 20 мг. Также в этом случае после нагревания было обнаружено более низкое высвобождение никотина.
Результаты - геополимер
Чистый никотин (20 мг) наносили и распределяли по поверхности пуансонов из геополимера. Измеряли количество никотина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 6.
Никотин является летучим веществом, и поэтому количество никотина, обнаруженного в контрольном образце (около 16 мг), было меньше, чем первоначально применялось. Также в этом случае после нагрева было обнаружено более низкое высвобождение никотина.
Пример 4 - термическая обработка с использованием устройства электронной сигареты
Материалы
Керамические стержни из оксида алюминия и стержни из сульфата кальция получали, как описано в примере 3. Были доставлены и применены никотин и никотиновые растворы, и уровни никотина были обнаружены, как описано в примере 3.
Нагревательные приборы
Образцы нагревали с использованием прототипа устройства электронной сигареты (X-Cube II, Smoke), полученного от Devex Mekatronik АВ (Швеция). Устройство получено из коммерчески доступной электронной сигареты X-Cube.
Способ
Образец в устройстве нагревали катушкой, намотанной вокруг образца. Настройки для электронной сигареты приведены в таблице ниже.

Конец устройства был подключен к флакону через силиконовый шланг. Во флаконе содержался 1 мл деионизированной воды. Чтобы моделировать курение, в устройство помещали стержень и выполняли пыхтение. Пыхтение включает последовательность из 5 затяжек, каждая из которых длится 10 секунд. После пыхтения шланг убирали и промывали водой. Воду анализировали на концентрацию никотина.
Результаты - сульфат кальция
Стержни из сульфата кальция пропитывали в течение 24 часов чистым никотином и нагревали (5*10 с) в устройстве электронной сигареты. Измеряли количество никотина, оставшегося в стержнях до и после термообработки, как показано на фиг. 8.
Результаты показывают, что термообработка в устройстве приведет к высвобождению никотина. Результаты - оксид алюминия
Стержни из оксида алюминия (Al2O3) пропитывали в течение 24 часов в растворе никотина (18 мг/мл) и нагревали (5*10 с) в устройстве. Измеряли количество никотина, оставшегося в стержнях до и после термообработки, как показано на фиг. 9.
Пример 5 - термическая обработка с использованием индукционного нагрева
Материалы
Пуансоны из сульфата кальция были получены, как описано в примере 3. Для непрямого индукционного в пуансон был введен магнит. Были получены и нанесены никотин и никотиновые растворы, а уровни никотина определялись, как описано в примере 3.
Нагревательный прибор
Металлическая пластина для индукционной плиты была получена от  (Швеция). Индукционная плита Wilfa ICP-2000 была получена от Media Markt (Швеция). Магниты (10*1 мм, магниты Samarium Cobalt, сила притягивания 0,4 кг) были получены от first4magnets (Великобритания). ИК термометр (MS6520A) был получен от Mastech (США).
(Швеция). Индукционная плита Wilfa ICP-2000 была получена от Media Markt (Швеция). Магниты (10*1 мм, магниты Samarium Cobalt, сила притягивания 0,4 кг) были получены от first4magnets (Великобритания). ИК термометр (MS6520A) был получен от Mastech (США).
Способ нагрева
Термическую обработку посредством непрямой индукции проводили путем размещения металлической пластины на индукционной плите. Керамические пуансоны, содержащие магнит, наносили на металлическую пластину и нагревали с максимальным эффектом (точная температура не измерялась, см. фиг. 10).
Результаты - ненагретая пластина
Раствор никотина (50 мкл, 18 мг/мл) распределяли по поверхности пуансонов из сульфата кальция и нагревали на индукционной пластине в течение приблизительно 1 минуты или приблизительно 5 минут. Было измерено количество никотина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 11. Большая часть никотина была высвобождена в течение первой минуты.
Результаты - предварительно нагретая пластина
Никотиновый раствор (50 мкл, 18 мг/мл) был распределен по поверхности пуансонов из сульфата кальция. Пластину предварительно нагревали в течение приблизительно 10 секунд, чтобы получить высокую температуру (по меньшей мере 150°С). Пуансоны нагревали в течение 5 секунд на пластине перед снятием. Пуансонам давали остыть в течение приблизительно 15 минут, прежде чем вводить их в экстракционную ванну. Было измерено количество никотина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 12.
Измерения показывают, что значительное количество никотина было высвобождено в результате термообработки.
Пример 6 - сукцинат суматриптана
Материалы
Керамические стержни из оксида алюминия были получены от Ceramtech (Швеция): цилиндрические стержни из Al2O3 диаметром 3 мм и длиной 10 мм, содержащие 4 отверстия (ориентированные в осевом направлении)диаметром 0,8 мм. Сукцинат суматриптана был получен от SMS Pharmaceuticals Limited, Индия.
Нанесение сукцината суматриптана
Нанесение сукцината суматриптана было достигнуто путем пропитывания стержней из Al2O3 раствором сукцината суматриптана с концентрацией 20 мг/мл. Объем раствора составлял около 100 мкл, но точно не измерялся; объем был достаточным для полного погружения стержней. Образцы пропитывали в течение 24 часов при комнатной температуре, после чего образцы высушивали в течение 24 часов перед термообработкой и/или анализом.
Прибор и способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температуру устанавливали приблизительно на 300°С. Температуру измеряли с помощью ИК термометра производства Mastech, США. Стержни нагревали в печи в течение периода времени в диапазоне от 0 до 15 минут.
Определение сукцината суматриптана
Все испытания по высвобождению суматриптана проводились в соответствии с тем же аналитическим способом. Стержни погружали в химический стакан, содержащий 50 мл деионизированной воды. Через 24 часа образец воды вынимали и фильтровали (размер пор: 0,2 мкм). Характеристики образца определяли с помощью УФ спектрофотометрии на длине волны 282 нм. Затем рассчитывали количество сукцината суматриптана в образцах. Контрольные образцы представляют собой количество сукцината суматриптана, которое было загружено до термообработки. Разница между количеством сукцината суматриптана, обнаруженным в термообработанных образцах и контрольном образце, представляет собой количество сукцината суматриптана, которое испаряется во время термообработки.
Результаты
Измеряли количество сукцината суматриптана, оставшегося в стержнях до и после термообработки, как показано на фиг. 13.
При нагревании почти весь сукцинат суматриптана высвобождался в течение первых 5-15 минут, так как количество сукцината суматриптана, оставшегося в образцах после термообработки, было незначительным. Стержни были способны поглощать приблизительно 1 мг сукцината суматриптана/стержень.
Пример 7 - нагрев пуансонов из сульфата кальция предварительно заполненных гидрохлоридом клонидина
Подготовка образца
Альфа-полугидрат сульфат кальция (CaS) был получен от Во Ehrlander АВ (Швеция). Гидрохлорид клонидина получили от PCAS (Финляндия). Формованный силиконовый каучук использовали в качестве форм для получения пуансонов (диаметр: 12 мм, толщина: 2 мм). Сульфат кальция смешивали с порошком гидрохлорида клонидина (0,07 г гидрохлорида клонидина/г сульфата кальция) и деионизированной водой (соотношение жидкость/порошок 0,4 (в весовом отношении)) с образованием гомогенной пасты, которая использовалась для заполнения каучуковых форм. После заполнения пастой, формы подвергали сушке в течение по меньшей мере 12 часов в условиях окружающей среды.
Способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температуру печи установили приблизительно на 250°С. Температуру измеряли с помощью ИК термометра производства Mastech (США). Пуансоны нагревали в печи в течение периода времени в диапазоне от 0 до 15 минут.
Обнаружение высвобождения гидрохлорида клонидина
Каждый пуансон взвешивали и погружали в химический стакан, содержащий 200 мл деионизированной воды. Через 24 часа образец жидкости вынимали и фильтровали (размер пор: 0,2 мкм). Образец характеризовали системой ЖХВД Shimadzu LC-2030 (Германия) с аналитической колонкой Genesis С18 4 мкм (100 × 2,1 мм внутр. диаметр) с подвижной фазой ацетонитрила/фосфорной кислоты, рН 3(11/89). Длина волны была установлена на 220 нм.
Контрольные образцы представляют собой количество гидрохлорида клонидина, мг/г сульфата кальция, которое загружали до термообработки. Разница в количестве гидрохлорида клонидина, обнаруженная в термообработанных образцах и контрольном образце, представляет собой количество гидрохлорида клонидина, которое испаряется во время термообработки.
Результаты - сульфат кальция
Гидрохлорид клонидина смешивали с сульфатом кальция (0,07 г гидрохлорида клонидина/г сульфата кальция) с образованием пуансонов. Пуансоны содержали около 17 мг гидрохлорида клонидина (1 пуансон весила около 0,3 г). Пуансоны нагревали, как описано выше (или не нагревали в случае контрольного образца). Измеряли количество гидрохлорида клонидина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 14. При нагреве почти весь гидрохлорид клонидина высвобождался в течение первых 15 мин, так как количество оставшегося в образцах гидрохлорида клонидина после термообработки было незначительным.
Пример 8 - нагрев пуансонов из сульфата кальция, заполненных гидрохлоридом клонидина
Подготовка образца
Альфа-полугидрат сульфат кальция (CaS) был получен от Во Ehrlander АВ (Швеция). Гидрохлорид клонидина получили от PCAS (Финляндия). Формованный силиконовый каучук использовали в качестве форм для получения пуансонов (диаметр: 12 мм, толщина: 2 мм). Сульфат кальция смешивали с деионизированной водой (соотношение жидкость/порошок 0,4 (в весовом отношении)) с образованием гомогенной пасты, которую использовали для заполнения каучуковых форм. После заполнения пастой, формы подвергали сушке в течение по меньшей мере 12 ч в условиях окружающей среды.
Раствор гидрохлорида клонидина (50 мкл, 5 мг/мл) распределяли по пуансонам из сульфата кальция. Когда раствор был нанесен, пуансоны подвергали сушке в течение, по меньшей мере, 12 часов в условиях окружающей среды.
Способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температура была установлена приблизительно на 250°С. Температуру измеряли с помощью ИК термометра производства Mastech (США). Пуансоны нагревали в печи в течение периода времени в диапазоне от 0 до 15 минут.
Обнаружение высвобождения гидрохлорида клонидина
Каждый пуансон взвешивали и погружали в химический стакан, содержащий 200 мл деионизированной воды. Через 24 часа образец воды вынимали и фильтровали (размер пор: 0,2 мкм). Образец характеризовали системой ЖХВД Shimadzu LC-2030 (Германия) с аналитической колонкой Genesis С18 4 мкм (100 × 2,1 мм внутр. диаметр) с подвижной фазой ацетонитрила/фосфорной кислоты, рН 3(11/89). Длина волны была установлена на 220 нм.
Контрольные образцы представляют собой количество гидрохлорида клонидина, которое было загружено до термообработки. Разница в количестве гидрохлорида клонидина, обнаруженная в термообработанных образцах и контрольном образце, представляет собой количество гидрохлорида клонидина, которое испаряется во время термообработки.
Результаты - сульфат кальция
Раствор гидрохлорида клонидина (50 мкл, 5 мг/мл) распределяли по поверхности пуансонов из сульфата кальция. Пуансоны нагревали, как описано выше (или не нагревали в случае контрольного образца). Измеряли количество гидрохлорида клонидина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 15. Во время нагрева количество гидрохлорида клонидина, присутствующего в пуансонах, со временем значительно уменьшалось.
Пример 9 - нагрев пуансонов из сульфата кальция, предварительно заполненных никотином
Подготовка образца
Альфа-полугидрат сульфат кальция (CaS) был получен от Во Ehrlander АВ (Швеция). Формованный силиконовый каучук использовали в качестве форм для получения пуансонов (диаметр: 12 мм, толщина: 2 мм). Сульфат кальция смешивали с раствором никотина с концентрацией 5 или 20 мг/мл никотина (соотношение жидкость/порошок 0,4 (в весовом отношении)) с образованием гомогенной пасты, которой заполняли каучуковые формы. После заполнения пастой формы подвергали сушке в течение по меньшей мере 12 ч в условиях окружающей среды.
Способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температуру установили приблизительно на 200°С. Температуру измеряли с помощью ИК термометра производства Mastech (США). Пуансоны нагревали в печи в течение периода времени в диапазоне от 0 до 15 минут.
Обнаружение высвобождения никотина
Каждый пуансон погружали в химический стакан, содержащий 50 мл деионизированной воды. Через 24 часа образец вынимали и фильтровали (размер пор: 0,2 мкм). Характеристики образца определяли с помощью УФ спектрофотометра на длине волны 219 нм. Затем подсчитывали количество никотина в образцах. Разница в количествах в контрольном образце и термообработанном образце представляет собой количество никотина, который испаряется во время термообработки.
Контрольные образцы представляют собой количество никотина мкг/г сульфата кальция, которое загружали до термообработки. Разница в количестве никотина, обнаруженного в термообработанных образцах и контрольном образце, представляет собой количество никотина, который испарился во время термообработки.
Результаты
Для изготовления пуансонов использовались два разных раствора никотина; 5 мг/мл и 20 мг/мл. В обеих партиях использовали одинаковое соотношение жидкость/порошок 0,4 (в весовом отношении). Пуансоны содержали около 180 мкг (для пуансонов, смешанных с раствором никотина 5 мг/мл) и 390 мкг (для пуансонов, смешанных с раствором никотина 20 мг/мл). Измеряли количество никотина, оставшегося в пуансонах до и после термообработки, как показано на фиг. 16.
Пример 10 - нагрев пуансонов из сульфата кальция, предварительно заполненных сукцинатом суматриптана
Подготовка образца
Альфа-полугидрат сульфата кальция (CaS) был получен от Во Ehrlander АВ (Швеция). Сукцинат суматриптана был получен от SMS Pharmaceuticals Limited, Индия. Формованный силиконовый каучук использовали в качестве форм для получения пуансонов (диаметр: 12 мм, толщина: 2 мм). Сульфат кальция смешивали с сукцинатом суматриптана (0,07 г сукцината суматриптана/г сульфата кальция) и деионизированной водой (соотношение жидкость/порошок 0,4 (в весовом отношении)) с образованием гомогенной пасты, которой заполняли каучуковые формы. После заполнения пастой, формы подвергали сушке в течение по меньшей мере 12 ч в условиях окружающей среды.
Способ нагрева
Печь Wilfa EMK 218 была получена от Wilfa (Норвегия). Температура была установлена приблизительно на 250°С. Температуру измеряли с помощью ИК термометра производства Mastech (США). Пуансоны нагревали в печи в течение периода времени в диапазоне от 0 до 15 минут.
Определение сукцината суматриптана
Пуансоны погружали в химический стакан, содержащий 50 мл деионизированной воды. Через 24 часа образец воды вынимали и фильтровали (размер пор: 0,2 мкм). Характеристики образца определяли с помощью УФ спектрофотометрии на длине волны 282 нм. Затем рассчитывали количество сукцината суматриптана в образцах.
Контрольные образцы представляют собой количество сукцината суматриптана, которое было загружено до термообработки. Разница между количеством сукцината суматриптана, обнаруженным в термообработанных образцах и контрольном образце, представляет собой количество сукцината суматриптана, которое испаряется во время термообработки.
Результаты
Измеряли количество сукцината суматриптана, оставшегося в пуансонах до и после термообработки, как показано на фиг. 17 При нагревании почти весь сукцинат суматриптана высвобождался в течение первых 15 мин, поскольку количество сукцината суматриптана, оставшегося в образцах после термообработки, было незначительным.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВА ДЛЯ ИСПАРЕНИЯ И ИНГАЛЯЦИИ НИКОТИНА | 2017 |
|
RU2743447C2 |
| ИНГАЛЯТОР АРОМАТИЗИРОВАННОГО НИКОТИНОВОГО ПОРОШКА | 2015 |
|
RU2680422C2 |
| ИНГАЛЯТОР НИКОТИНОВОГО ПОРОШКА | 2015 |
|
RU2696570C2 |
| АРОМАТИЗИРОВАННЫЙ НИКОТИНОВЫЙ ПОРОШОК | 2016 |
|
RU2762084C2 |
| УСТРОЙСТВО ДЛЯ ПУЛЬМОНАЛЬНОГО ВВЕДЕНИЯ | 2018 |
|
RU2766733C2 |
| НОВЫЕ ЧАСТИЦЫ НОСИТЕЛИ ДЛЯ СУХИХ ПОРОШКОВЫХ КОМПОЗИЦИЙ ДЛЯ ИНГАЛЯЦИИ | 2018 |
|
RU2745045C1 |
| ЗАБУФЕРЕННАЯ ЖИДКАЯ НИКОТИНОВАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕГОЧНОГО ВВЕДЕНИЯ | 2003 |
|
RU2283111C2 |
| СИСТЕМА И СПОСОБ РЕГУЛИРОВАНИЯ РЕЗКОГО ПРИВКУСА СУХИХ ПОРОШКОВЫХ СОСТАВОВ НА ОСНОВЕ НИКОТИНА | 2016 |
|
RU2707104C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ 5,8,14-ТРИАЗАТЕТРАЦИКЛО[10.3.1.0(2,11).0(4,9)]ГЕКСАДЕКА-2( 11),3,5,7,9-ПЕНТАЕНА | 2002 |
|
RU2272629C2 |
| ИНГАЛЯТОР С ВИХРЕВОЙ ПОЛОСТЬЮ ДЛЯ КАПСУЛЫ | 2019 |
|
RU2783884C2 |




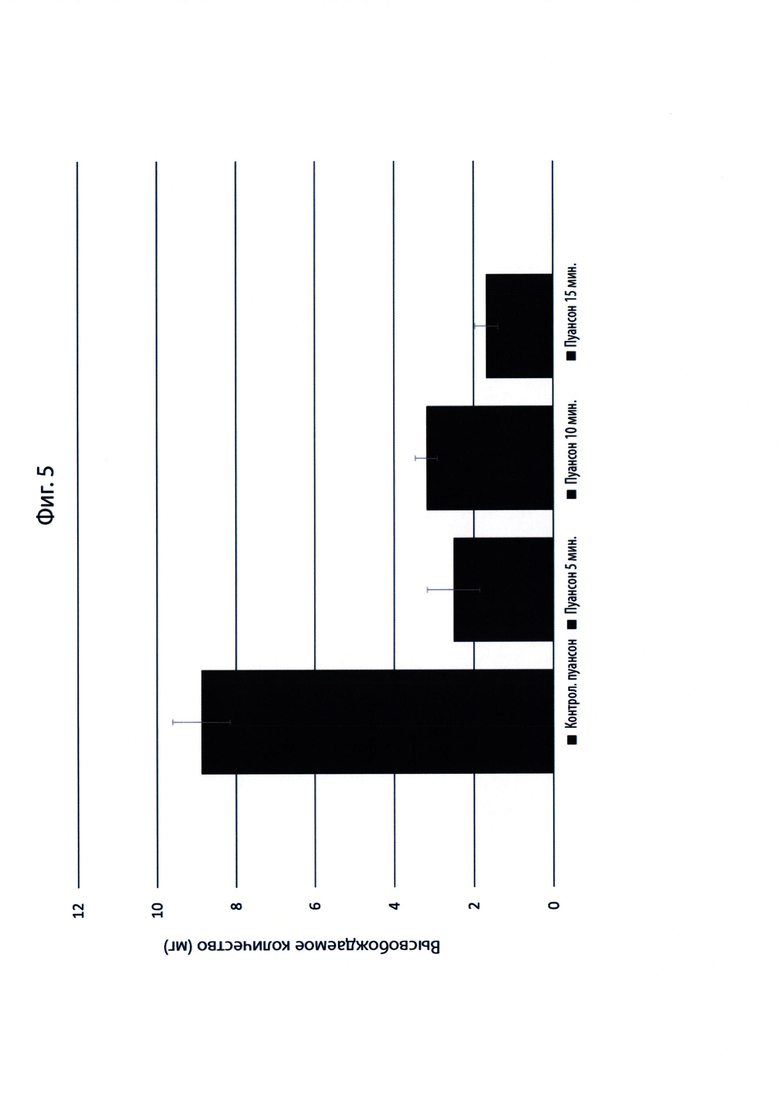




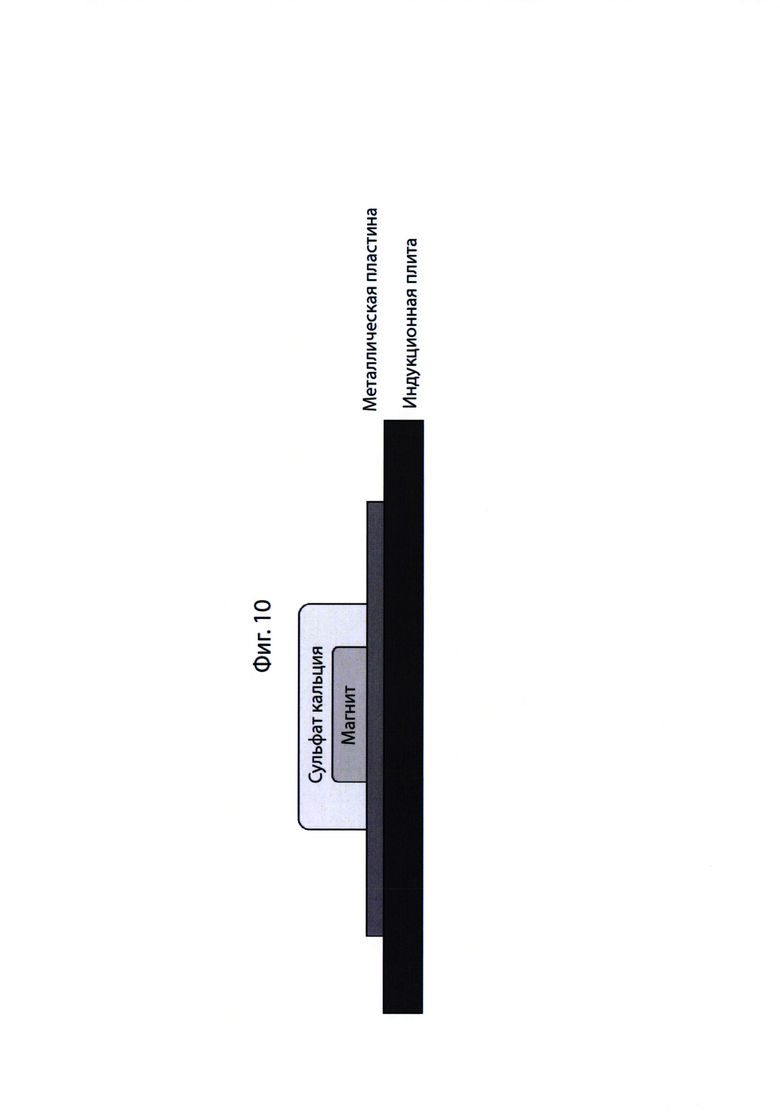

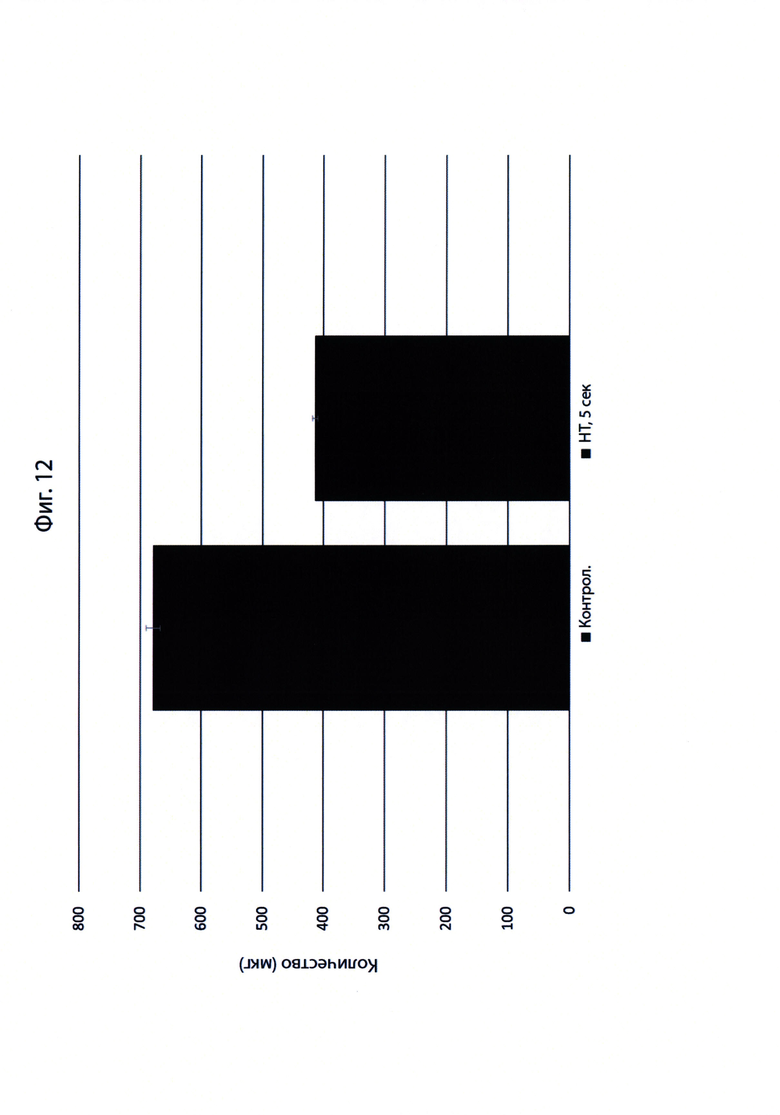



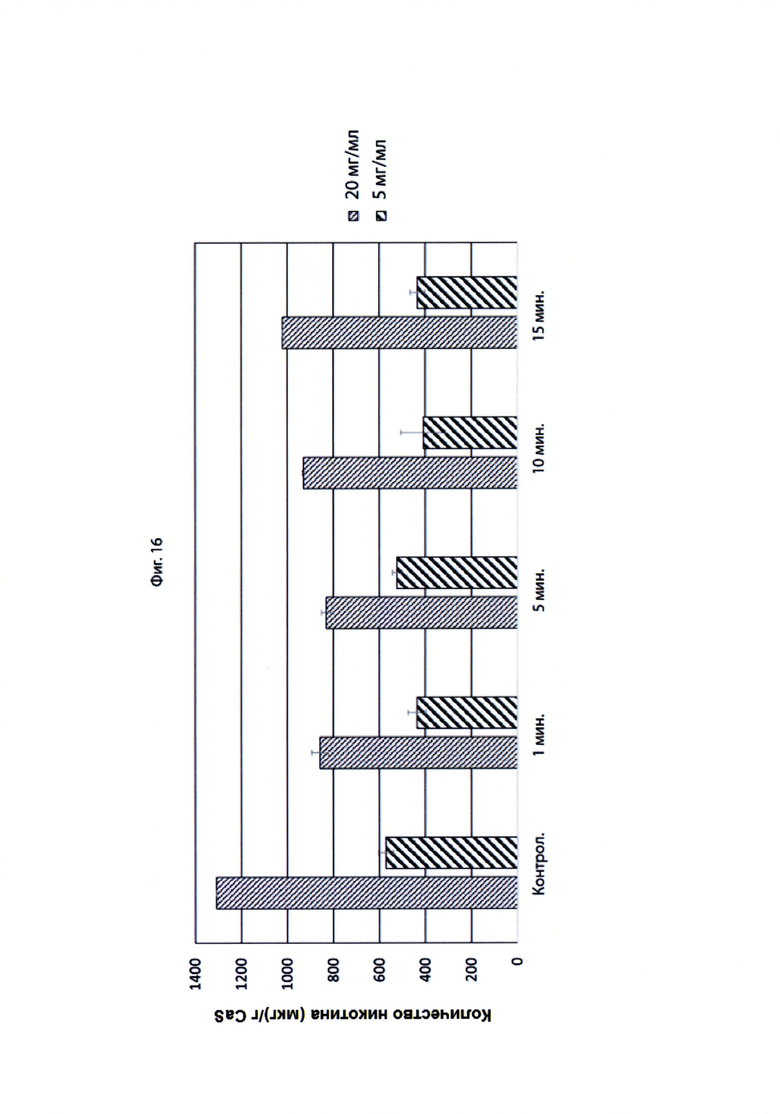
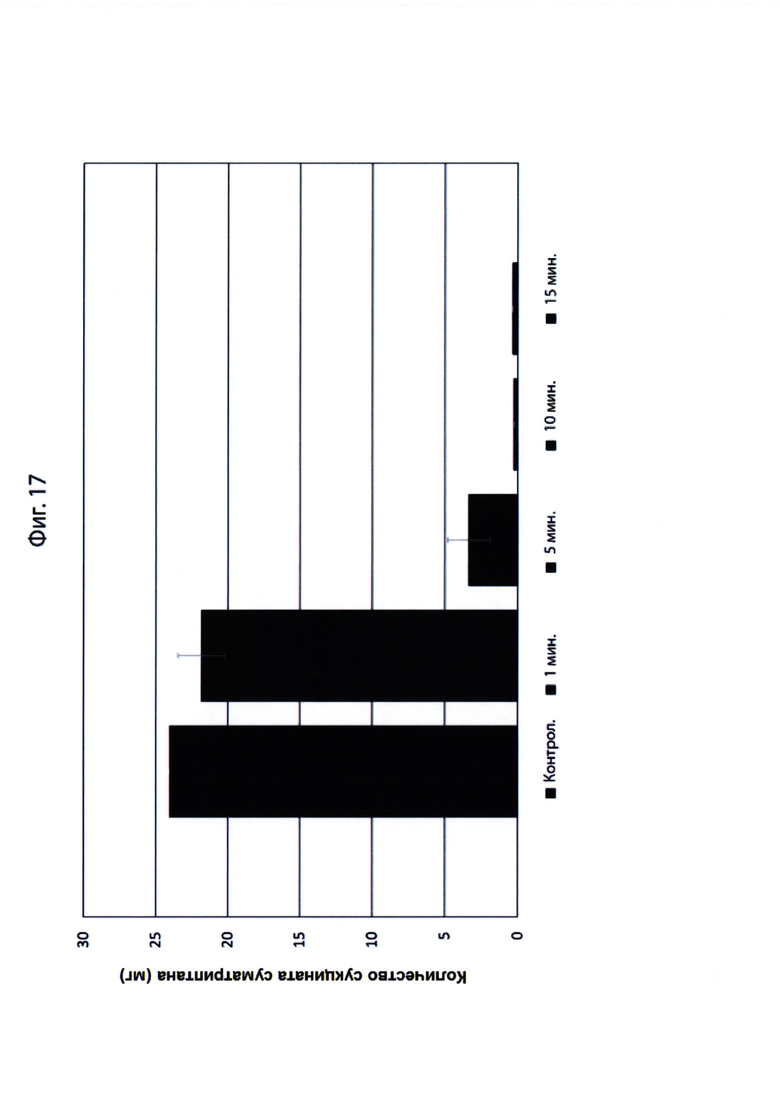
Группа изобретений относится к медицинской технике. Устройство для доставки пользователю доставляемого вещества в виде аэрозоля или пара. Устройство содержит твердый пористый материал-носитель, имеющий пористость по меньшей мере 10%, и доставляемое вещество. Часть доставляемого вещества расположена в порах материала-носителя, причем устройство выполнено с возможностью нагрева материала-носителя и испарения доставляемого вещества. Материал-носитель основан на одном или более химически связанных керамических материалах, одном или более геополимерных материалах. Раскрыты контейнер для использования в устройстве и препарат с разовой дозой. Технический результат состоит в обеспечении контролируемого высвобождения активных ингредиентов. 8 н. и 22 з.п. ф-лы, 17 ил.
1. Устройство для доставки пользователю доставляемого вещества в виде аэрозоля или пара, причем указанное устройство содержит твердый пористый материал-носитель, имеющий пористость по меньшей мере 10%, и доставляемое вещество, причем по меньшей мере часть доставляемого вещества расположена в порах материала-носителя, причем устройство выполнено с возможностью нагрева материала-носителя и испарения доставляемого вещества; причем материал-носитель основан на одном или более химически связанных керамических материалах, одном или более геополимерных материалах.
2. Устройство по п. 1, отличающееся тем, что твердый пористый материал-носитель имеет пористость от около 20% до около 70%.
3. Устройство по п. 1 или 2, отличающееся тем, что средний размер пор в материале-носителе составляет от около 0,1 мкм до около 500 мкм, и предпочтительно, от около 0,2 мкм до около 200 мкм.
4. Устройство по любому из предшествующих пунктов, отличающееся тем, что доставляемое вещество расположено преимущественно в порах материала-носителя.
5. Устройство по любому из предшествующих пунктов, отличающееся тем, что материал-носитель выбирается из группы, состоящей из:
i) материала, получаемого в процессе вступления в реакцию материала-предшественника алюмосиликата с водной щелочной жидкостью; и
ii) фосфата кальция, сульфата кальция, карбоната кальция, силиката кальция, алюмината кальция, карбоната магния, силиката алюминия и их комбинаций.
6. Устройство по любому из предшествующих пунктов, отличающееся тем, что материал-носитель i) выбирается из группы, состоящей из сульфата кальция, фосфата кальция, силиката кальция, карбоната кальция, алюмината кальция, карбоната магния, или их комбинации или ii) является материалом, получаемым в процессе вступления в реакцию материала-предшественника алюмосиликата, выбранного из группы, состоящей из каолина, дикита, галлуазита, накрита, цеолитов, иллитов, дегидроксилированного цеолита, дегидроксилированного галлуазита и метакаолина с водной щелочной жидкостью.
7. Устройство по п. 6, причем процесс вступления в реакцию материала-предшественника алюмосиликата с водной щелочной жидкостью осуществляют в присутствии источника диоксида кремния.
8. Устройство по любому из предшествующих пунктов, отличающееся тем, что доставляемое вещество представляет собой активный фармацевтический ингредиент.
9. Устройство по п. 8, отличающееся тем, что активный фармацевтический ингредиент выбирается из группы, состоящей из антигипертензивных, седативных, снотворных и болеутоляющих веществ.
10. Устройство по п. 8 или 9, отличающееся тем, что активный фармацевтический ингредиент представляет собой опиоидный анальгетик.
11. Устройство по п. 10, отличающееся тем, что опиоидный анальгетик выбирается из морфина, оксикодона, бупренорфина, альфентанила, суфентанила, ремифентанила и фентанила.
12. Устройство по п. 8 или 9, отличающееся тем, что активный фармацевтический ингредиент представляет собой никотин или его фармацевтически приемлемую соль.
13. Устройство по любому из предшествующих пунктов, отличающееся тем, что материал-носитель и доставляемое вещество совместно находятся в сменном контейнере.
14. Устройство по п. 13, отличающееся тем, что сменный контейнер, по существу, состоит из материала-носителя и доставляемого вещества.
15. Устройство по п. 14, отличающееся тем, что сменный контейнер дополнительно содержит частицы проводящего материала и/или одно или более веществ, выбранных из группы, состоящей из веществ, повышающих испарение, ароматизаторов и усилителей вкуса.
16. Устройство по любому из предшествующих пунктов, дополнительно содержащее нагревательный элемент, выполненный с возможностью нагрева материала-носителя.
17. Устройство по п. 16, отличающееся тем, что нагревательный элемент расположен в непосредственной близости к материалу-носителю.
18. Контейнер для использования в устройстве для ингаляции, причем контейнер с разовой дозой содержит:
i) твердый пористый материал-носитель, имеющий пористость по меньшей мере 10%; и
ii) доставляемое вещество по любому из пп. 1 или 8-12, расположенное в порах материала-носителя.
19. Контейнер по п. 18, причем твердый пористый материал-носитель выполнен из одного или более химически связанных керамических материалов или одного или более геополимерных материалов, как определено в любом из пп. 1-7.
20. Контейнер по п. 18 или 19, дополнительно содержащий частицы проводящего материала.
21. Препарат с разовой дозой для использования в устройстве для ингаляции, причем препарат с разовой дозой содержит:
i) твердый пористый материал-носитель, имеющий пористость по меньшей мере 10%; и
ii) доставляемое вещество по любому из пп. 1 или 8-12, расположенное в порах материала-носителя.
22. Препарат с разовой дозой по п. 21, причем твердый пористый материал-носитель выполнен из одного или более химически связанных керамических материалов или одного или более геополимерных материалов, как определено в любом из пп. 1-7.
23. Препарат с разовой дозой по п. 21 или 22, дополнительно содержащий частицы проводящего материала.
24. Устройство по любому из пп. 1-17, отличающееся тем, что доставляемое вещество является активным фармацевтическим ингредиентом, и устройство содержит достаточное количество активного фармацевтического ингредиента, чтобы обеспечить пользователю не более одной разовой дозы активного фармацевтического ингредиента.
25. Контейнер по п. 18, отличающийся тем, что доставляемое вещество является активным фармацевтическим ингредиентом, и контейнер содержит достаточное количество активного фармацевтического ингредиента, чтобы обеспечить пользователю не более одной разовой дозы активного фармацевтического ингредиента.
26. Разовая доза по п. 21, отличающаяся тем, что доставляемое вещество является активным фармацевтическим ингредиентом и препарат с разовой дозой содержит достаточное количество активного фармацевтического ингредиента, чтобы обеспечить пользователю не более одной разовой дозы активного фармацевтического ингредиента.
27. Способ доставки пользователю доставляемого вещества в виде пара или аэрозоля, включающий:
a) наличие изделия, содержащего:
i) твердый, пористый материал-носитель, имеющий пористость по меньшей мере 10%, как определено в любом из пп. 1-7; и
ii) доставляемое вещество по любому из пп. 1 или 8-12, причем доставляемое вещество расположено внутри пор материала-носителя; и
b) нагрев материала-носителя для испарения доставляемого вещества.
28. Способ лечения или профилактики заболевания, включающий использование устройства для ингаляции, как определено в п. 8 или 9, для доставки активного фармацевтического ингредиента в виде аэрозоля или пара лицу, страдающему от указанного заболевания или восприимчивого к указанному заболеванию, причем указанный активный фармацевтический ингредиент лечит или предотвращает указанное заболевание.
29. Способ устранения боли, включающий использование устройства для ингаляции, как определено в п. 10, для доставки одного или более опиоидных анальгетиков в виде аэрозоля или пара лицу, страдающего от боли или восприимчивого к боли.
30. Способ лечения никотиновой зависимости, включающий использование устройства для ингаляции, как определенно в п. 12, для доставки никотина в виде аэрозоля или паров лицу, страдающему от симптомов никотиновой зависимости.
| US 2013220314 A1, 29.08.2013 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Многосекционный винт и способ его сборки | 1980 |
|
SU947489A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| УСТРОЙСТВО ДЛЯ ИНГАЛЯЦИИ И СПОСОБ ИНГАЛЯЦИИ | 1998 |
|
RU2207886C2 |
Авторы
Даты
2021-02-18—Публикация
2017-02-28—Подача