Изобретение относится к биотехнологии и фармацевтике, а именно к получению капсулированной формы антимикробного препарата на основе биомассы бактерий, выделенных из сапропеля, для терапии инфекционных заболеваний желудочно-кишечного тракта.
Антибиотикорезистентность (нечувствительность или устойчивость возбудителей инфекционных болезней к назначаемым для борьбы с ними антибиотикам) - тема, волнующая сегодня все человечество [1]. Антибиотикорезистентность определена ВОЗ как глобальная проблема, требующая незамедлительного решения [2]. Европейская сеть по эпиднадзору за устойчивостью к антимикробным препаратам («EARS-Net») ежегодно регистрирует до 400000 случаев развития полирезистентных инфекций, селекция которых вызвана, прежде всего, нерациональным использованием антибиотиков и антисептиков. Многие исследователи отмечают, что если существующие негативные тенденции не изменятся, то медицина столкнется с проблемой полувековой давности, когда еще отсутствовали антибиотики [3-7].
Согласно «Toronto declaration to combat antimicrobial resistance)) (Toronto, 2000) и «Глобальной стратегии ВОЗ по сдерживанию резистентности к антимикробным препаратам» (Женева, 2001) одним из путей преодоления лекарственной устойчивости выступает разработка и внедрение в практику новых противомикробных средств.
В поисках решения этой задачи возрос интерес к изучению нового класса антимикробных пептидов, продуцируемых эукариотическими клетками, а также к исследованиям большого числа антимикробных субстанций бактериального происхождения. Среди последних особое место занимают бактериоцины - рибосомально синтезируемые клеткой низкомолекулярные (<10,0 кДа), термоустойчивые, чаще всего катионной природы гидрофобные пептиды [8-9].
В настоящее время в научной литературе имеется значительное количество публикаций, посвященных вопросам изучения и биотехнологического производства различных видов биологически активных веществ, продуцируемых преимущественно спорообразующими микроорганизмами вида Bacillus subtilis, а также рядом штаммов молочнокислых бактерий [10].
Из уровня техники известна фармацевтическая композиция антибиотиков и пребиотиков для профилактики и лечения дисбиозов в процессе антибактериальной терапии (патент РФ №2325187, опубл. 27.05.2008), содержащая (по первому варианту) антибиотик и пребиотик -олигосахарид, выбранный из группы: фруктоолигосахариды, галактоолигосахариды, ксилоолигосахариды, мальтоолигосахариды и изомальтоолигосахариды со степенью полимеризации от 2 до 10, с размером частиц до 0,3 мм и чистотой не менее 95%, а антибиотик - с размерами частиц от 20 до 200 мкм; антибиотик и олигосахарид включены в массовом соотношении от 1:1 до 1:100 соответственно; по второму варианту фармацевтическая композиция содержит антибиотик в виде порошка с размерами частиц от 20 до 200 мкм, выбранный из группы: бета-лактамы, включая комбинации бета-лактамов с ингибиторами бактериальных беталактамаз; азалиды, фторхинолоны, амфениколы, гликопептиды, ансамицины, нитрофураны, производные фосфоновой кислоты, циклосерин, триметоприм, а в качестве пребиотика - олигосахарид в виде порошка со степенью полимеризации от 2 до 10, с размером частиц до 0,3 мм, чистотой не менее 95%; при этом антибиотик и олигосахарид включены в состав композиции в массовом соотношении от 1:1 до 1:100, соответственно.
Недостатком известного способа получения фармацевтической композиции является отсутствие процесса помола действующих веществ с целью повышения их антибактериальной активности после высушивания, так как процесс подсушки композиции до 2-3% влажности обязательно приведет к агрегации частиц антибиотика и олигосахарида с соответствующей потерей их дисперсности, а, следовательно, и активности.
Также известно средство, обладающее антибактериальной активностью (патент РФ №1779377, опубл. 07.12.1992), содержащее живую культуру ацидофильных лактобактерий в сочетании с комплексом сывороточных иммуноглобулинов, взятых в одинаковых весовых частях, при концентрации жизнеспособных микробных клеток 107-108 на массу 0,1 г и процентном соотношении компонентов в комплексе иммуноглобулина G:M:A, равном (55-60):(20-25):(15-20), для получения которого сухую микробную массу соединяют с сухой биомассой КИП в соотношении 1:1 и используют для приготовления оральной или ректальной формы.
В качестве недостатка известного изобретения следует признать низкую антибактериальную активность препарата.
Описана метабиотическая композиция для обеспечения колонизационной резистентности микробиоценоза кишечника человека (патент РФ №2589818, опубл. 10.07.2016), выполненная в твердой дозированной форме в виде капсул, количество ингредиентов в одной капсуле составляет, масс. %: стерилизованная высушенная культуральная жидкость, содержащая метаболиты пробиотического штамма бактерий Bacillus subtilis ВКНМ. № В-2335 - 1,9; стерилизованная высушенная культуральная жидкость, содержащая метаболиты пробиотического штамма бактерий Enterococcus faecium L-3 - 4,5; стерилизованная высушенная культуральная жидкость, содержащая метаболиты пробиотического штамма бактерий Lactobacillus delbrueckii TS1-06 - 4,5; стерилизованная высушенная культуральная жидкость, содержащая метаболиты пробиотического штамма бактерий Lactobacillus fermentum TS3-06 - 4,5; цеолит - 64,3; овсяные хлопья - 20,0; стеарат кальция или аэросил - 0,3.
В качестве основного недостатка описанной композиции следует отметить многокомпонентный состав.
В ходе патентного поиска не выявлено техническое решение, принятое в качестве ближайшего аналога.
Технической задачей предлагаемого изобретения является расширение ассортимента антимикробных препаратов, нормализующих микробиоценоз кишечника, для терапии заболеваний желудочно-кишечного тракта, имеющих микробиологическую природу.
Технический результат, достигаемый при реализации заявленного изобретения, состоит в разработке нового способа производства капсулированной формы антимикробного препарата на основе биомассы бактерий, изолированных из сапропеля, для терапии заболеваний ЖКТ, имеющих микробиологическую природу.
Для достижения указанного технического результата предложено использовать разработанный способ. Согласно разработанному способу производства капсулированной формы антимикробного препарата для терапии заболеваний ЖКТ осуществляют культивирование бактерий, выделенных из сапропеля, до достижения концентрации бактерий 2,0⋅106 КОЕ/мл, после чего биомассу отделяют от питательной среды центрифугированием, полученную надосадочную жидкость сублимационно высушивают и заключают в капсулы, оболочка которых состоит из растительных полисахаридов - каррагинана и агар-агара.
В предпочтительном варианте реализации способа отбирают образцы сапропеля. Для выделения колоний бактерий отобранные образцы сапропеля измельчают в стерильных условиях и небольшой кусочек растирают на поверхности чашки Петри с агаризованной питательной средой, либо 5 г образца вносят в 5 мл жидкой питательной среды. Инкубируют чашки Петри и пробирки при температуре 37°С стационарно в течение 3 суток.
Для первичного выделения бактерий используют жидкие питательные среды. Из пробирок с видимым ростом бактерий (помутнение) и с суммарных газонов на чашках проводят истощающие рассевы. Выделенные бактерии культивируют на агаризованных питательных средах.
Культуры бактерий, выделенных из сапропеля, хранят в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не более 24 месяцев.
Согласно изобретению, капсулированную форму антимикробного препарата для терапии заболеваний ЖКТ получают следующим образом. Лиофилизированные культуры бактерий, выделенных из сапропеля, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток инкапсулируют в оболочки, состоящие из растительных полисахаридов, при следующем соотношении компонентов, масс. %:
Изобретение иллюстрируется следующими примерами.
Пример 1
Отбирают образцы сапропеля. Для отбора проб сапропеля используют бур с пробоотборочным челноком ТБ-5, длиной 0,5 м. Пробы сапропеля отбирают послойно по 0,25 м до минерального дна. При отборе проб челнок бура погружают в залежь в открытом состоянии первоначально на 0,5 м. Поворотом ручки по часовой стрелке на 180° челнок закрывают и извлекают из залежи. Затем приводят его в горизонтальное положение, вытирают снаружи, открывают, разделяют содержимое челнока на две равные части по 0,25 м и переносят каждую часть отдельно в тару. Полость челнока после удаления пробы тщательно вытирают. Затем процесс отбора проб возобновляют с последовательным погружением бура на глубину 1,0, 1,5 м и т.д.
Для выделения колоний бактерий отобранные образцы сапропеля измельчают в стерильных условиях и небольшой кусочек (приблизительно 5 г) растирают на поверхности чашки Петри с агаризованной питательной средой состава (г/л): пептический перевар животной ткани - 6,0, гидролизат казеина - 4,0, дрожжевой экстракт - 3,0, мясной экстракт - 1,5, глюкоза - 1,0, агар-агар - 15,0; либо 5 г образца вносят в 5 мл жидкой питательной среды состава (г/л): пептический перевар животной ткани - 6,0, гидролизат казеина - 4,0, дрожжевой экстракт - 3,0, мясной экстракт - 1,5, глюкоза - 1,0. Инкубируют чашки Петри и пробирки при температуре 37°С стационарно в течение 3 суток.
Для первичного выделения бактерий используют жидкую питательную среду аналогичного состава. Из пробирок с видимым ростом бактерий (помутнение) и с суммарных газонов на чашках проводят истощающие рассевы. Выделенные бактерии культивируют на агаризованной питательной среде. Культуры бактерий, выделенных из сапропеля, хранят в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не более 24 месяцев.
Лиофилизированные культуры бактерий, выделенных из сапропеля, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток заключают в капсулы на основе растительных полисахаридов, которые получают следующим образом. Готовят смесь растительных полисахаридов (каррагинан, агар-агар), воды, а также вспомогательного компонента - пластификатора глицерина, при следующем соотношении компонентов, масс. %:
В отмеренный объем воды комнатной температуры при постоянном перемешивании постепенно добавляют каррагинан и агар-агар, нагревают смесь до 75°С и продолжают перемешивание в течение 1 ч. После растворения полисахаридов в смесь добавляют глицерин, продолжая перемешивание в течение 30 мин.
После отключения мешалки и обогрева смесь оставляют в реакторе в течение 1,5-2 ч с подключением вакуума для удаления из массы пузырьков воздуха. Приготовленную массу передают для стабилизации в термостатирующую емкость с контролируемой температурой и выдерживают при температуре 50°С в течение 2,5 ч. Далее смесь подают на стадию капсулирования, которую осуществляют с помощью машины для изготовления капсул.
Емкость со смесью для капсулирования подключают к машине, через шланги раствор подается в боксы (температура боксов 60°С), из боксов раствор попадает на барабаны, температура которых от 18 до 22°С, где смесь желируется и формируется лента определенной толщины. Далее лента проходит через смазочные ролики, где на всю поверхность ленты наносится вазелиновое масло, затем она проходит через пресс-формы, где происходит вырубка капсул и спайка шва капсулы. Сверху через нагревательный элемент в формирующуюся капсулу подается наполнитель - лиофилизированные культуры бактерий, изолированных из донных отложений водоемов. Температура наполнителя не должна быть более 28°С.
Сформованные капсулы подаются в сушильные барабаны, где происходит первичная сушка капсул при температуре 25°С в течение 20 ч и удаление с поверхности капсул остатков вазелинового масла. Готовые капсулы сортируют на установке для сортировки капсул. Полученные капсулы раскладывают на специальные поддоны, поддоны составляют в стеки. Стеки закатываются в сушильные тоннели. Температура в тоннелях от 20 до 25°С, относительная влажность воздуха должна быть от 20 до 30%.
Сушка капсул происходит от 2 до 5 суток на барабанной установке для досушивания капсул фирмы «Sigma» (США) до достижения капсулами необходимых параметров по твердости, эластичности, весу и влажности оболочки. Высушенные капсулы передаются на стадию контроля качества и участок фасовки.
Результаты определения антагонистических свойств полученной согласно примеру 1 капсулированной формы препарата по отношению к бактериям, вызывающим заболевания ЖКТ, представлены в таблице 1.
Пример 2
Отбор образцов сапропеля и выделение из них бактерий осуществляют согласно примеру 1.
Лиофилизированные культуры бактерий, выделенных из сапропеля, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток заключают в капсулы на основе растительных полисахаридов, которые получают следующим образом. Готовят смесь растительных полисахаридов (каррагинан, агар-агар), воды, а также вспомогательного компонента - глицерина, при следующем соотношении компонентов, масс. %:
В отмеренный объем воды комнатной температуры при постоянном перемешивании постепенно добавляют каррагинан и агар-агар, нагревают смесь до 75°С и продолжают перемешивание в течение 1 ч. После растворения полисахаридов в смесь добавляют глицерин, продолжая перемешивание в течение 30 мин.
После отключения мешалки и обогрева смесь оставляют в реакторе в течение 1,5-2 ч с подключением вакуума для удаления из массы пузырьков воздуха. Приготовленную массу передают для стабилизации в термостатирующую емкость с контролируемой температурой и выдерживают при температуре 50°С в течение 2,5 ч. Далее смесь подают на стадию капсулирования, которую осуществляют с помощью машины для изготовления капсул.
Емкость со смесью для капсулирования подключают к машине, через шланги раствор подается в боксы (температура боксов 60°С), из боксов раствор попадает на барабаны, температура которых от 18 до 22°С, где смесь желируется и формируется лента определенной толщины. Далее лента проходит через смазочные ролики, где на всю поверхность ленты наносится вазелиновое масло, затем она проходит через пресс-формы, где происходит вырубка капсул и спайка шва капсулы. Сверху через нагревательный элемент в формирующуюся капсулу подается наполнитель - лиофилизированные культуры бактерий, изолированных из донных отложений водоемов. Температура наполнителя не должна быть более 28°С.
Сформованные капсулы подаются в сушильные барабаны, где происходит первичная сушка капсул при температуре 25°С в течение 20 ч и удаление с поверхности капсул остатков вазелинового масла. Готовые капсулы сортируют на установке для сортировки капсул. Полученные капсулы раскладывают на специальные поддоны, поддоны составляют в стеки. Стеки закатываются в сушильные тоннели. Температура в тоннелях от 20 до 25°С, относительная влажность воздуха должна быть от 20 до 30%.
Сушка капсул происходит от 2 до 5 суток на барабанной установке для досушивания капсул фирмы «Sigma» (США) до достижения капсулами необходимых параметров по твердости, эластичности, весу и влажности оболочки. Высушенные капсулы передаются на стадию контроля качества и участок фасовки.
Результаты определения антагонистических свойств полученной согласно примеру 2 капсулированной формы препарата по отношению к бактериям, вызывающим заболевания ЖКТ, представлены в таблице 1.
Пример 3
Отбор образцов сапропеля и выделение из них бактерий осуществляют согласно примеру 1.
Лиофилизированные культуры бактерий, выделенных из сапропеля, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток заключают в капсулы на основе растительных полисахаридов, которые получают следующим образом. Готовят смесь растительных полисахаридов (каррагинан, агар-агар), воды, а также вспомогательного компонента - глицерина, при следующем соотношении компонентов, масс. %:
В отмеренный объем воды комнатной температуры при постоянном перемешивании постепенно добавляют каррагинан и агар-агар, нагревают смесь до 75°С и продолжают перемешивание в течение 1 ч. После растворения полисахаридов в смесь добавляют глицерин, продолжая перемешивание в течение 30 мин.
После отключения мешалки и обогрева смесь оставляют в реакторе в течение 1,5-2 ч с подключением вакуума для удаления из массы пузырьков воздуха. Приготовленную массу передают для стабилизации в термостатирующую емкость с контролируемой температурой и выдерживают при температуре 50°С в течение 2,5 ч. Далее смесь подают на стадию капсулирования, которую осуществляют с помощью машины для изготовления капсул.
Емкость со смесью для капсулирования подключают к машине, через шланги раствор подается в боксы (температура боксов 60°С), из боксов раствор попадает на барабаны, температура которых от 18 до 22°С, где смесь желируется и формируется лента определенной толщины. Далее лента проходит через смазочные ролики, где на всю поверхность ленты наносится вазелиновое масло, затем она проходит через пресс-формы, где происходит вырубка капсул и спайка шва капсулы. Сверху через нагревательный элемент в формирующуюся капсулу подается наполнитель - лиофилизированные культуры бактерий, изолированных из донных отложений водоемов. Температура наполнителя не должна быть более 28°С.
Сформованные капсулы подаются в сушильные барабаны, где происходит первичная сушка капсул при температуре 25С в течение 20 ч и удаление с поверхности капсул остатков вазелинового масла. Готовые капсулы сортируют на установке для сортировки капсул. Полученные капсулы раскладывают на специальные поддоны, поддоны составляют в стеки. Стеки закатываются в сушильные тоннели. Температура в тоннелях от 20 до 25°С, относительная влажность воздуха должна быть от 20 до 30%.
Сушка капсул происходит от 2 до 5 суток на барабанной установке для досушивания капсул фирмы «Sigma» (США) до достижения капсулами необходимых параметров по твердости, эластичности, весу и влажности оболочки. Высушенные капсулы передаются на стадию контроля качества и участок фасовки.
Результаты определения антагонистических свойств полученной согласно примеру 3 капсулированной формы препарата по отношению к бактериям, вызывающим заболевания ЖКТ, представлены в таблице 1.
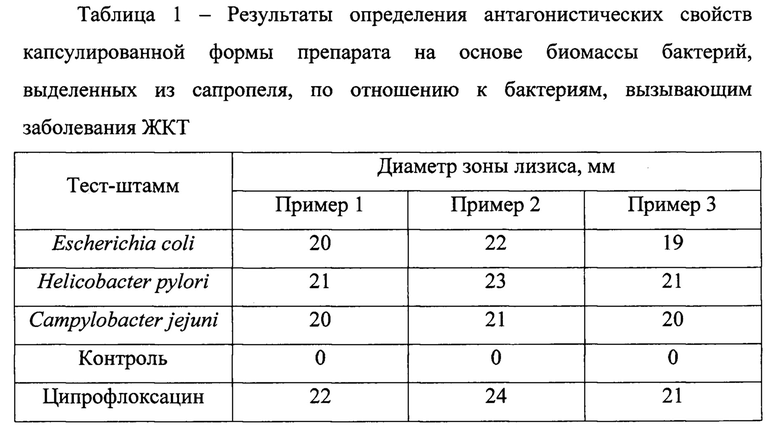
Из таблицы 1 следует, что капсулированные формы препарата на основе биомассы бактерий, выделенных из сапропеля, полученные согласно трем примерам, проявляют высокую антимикробную активность по отношению к бактериям - возбудителям заболеваний ЖКТ (Escherichia coli, Helicobacterpylori, Campylobacterjejuni), что позволяет использовать их для терапии таких заболеваний, как диарея, гастроэнтериты, гастриты, дуодениты, кампилобактериоз.
Таким образом, техническим результатом заявленного способа является разработка нового способа производства капсулированной формы антимикробного препарата на основе биомассы бактерий, изолированных из сапропеля, для терапии заболеваний ЖКТ, имеющих микробиологическую природу.
Источники информации:
1. Намазанова-Баранова, Л.С. Антибиотикорезистентность в современном мире / Л.С. Намазанова-Баранова, А.А. Баранов // Педиатрическая фармакология. 2017. Т. 14. №5. С. 341-354.
2. The WHO policy package to combat antimicrobial resistance // Bulletin of the World Health Organization. 2011. №89. P. 390-392.
3. Козлов, P.C. Клиническое значение резистентности грамположительных бактерий / P.C. Козлов // Инфекции в хирургии. 2009. Т. 7. С. 3-10.
4. Политика применения антибиотиков в хирургии / под ред. Л.С. Страчунского, Ж.К. Пешере, П.Э. Дедлинджер // Клиническая микробиология и антимикробная химиотерапия. 2003. Т. 5. №4. С.302-317.
5. Kapil, A. The challenge of antibiotic resistance: need to contemplate / A. Kapil // Indian J. Med. Res. 2005. Vol. 121. №2. P. 83-91.
6. Антибиотики в хирургии и интенсивной терапии / Б.З. Белоцерковский и др. // Инфекции в хирургии. 2009. Т. 7. №2. С. 70-76.
7. Бархатова, Н.А. Динамика резистентности возбудителей локальных и генерализованных форм инфекций мягких тканей / Н.А. Бархатова // Казанский медицинский журнал. 2009. Т. 90. №3. С. 385-390.
8. Ennahar, S. Class IIa bacteriocins: biosynthesis, structure and activity / S. Ennahar, T. Sashihara, K. Sonomoto, A. Ishizaki // FEMS Microbiology Reviews. 2000. Vol.24. Issue 1. P. 85-106.
9. Popaganni, M. Ribosomally synthezed peptides with antimicrobial properties: biosynthesis, structure, function, and applications / M. Popaganni // Biotechnol. Adv. 2003. Vol.21. №6. P. 465-499.
10. Забокрицкий, Н.А. Биологически активные вещества, синтезируемые пробиотическими микроорганизмами родов Bacillus и Lactobacillus // Журнал научных статей «Здоровье и образование в XXI веке. 2015. Т. 17. №3.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА КАПСУЛИРОВАННОЙ ФОРМЫ ПРОБИОТИЧЕСКОЙ ПИЩЕВОЙ ДОБАВКИ | 2021 |
|
RU2795965C1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОЦИНСОДЕРЖАЩЕЙ КОМПОЗИЦИИ | 2020 |
|
RU2773131C2 |
| МЕТАБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ОБЕСПЕЧЕНИЯ КОЛОНИЗАЦИОННОЙ РЕЗИСТЕНТНОСТИ МИКРОБИОЦЕНОЗА КИШЕЧНИКА ЧЕЛОВЕКА | 2015 |
|
RU2589818C1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ПРЕПАРАТА С ПРОБИОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2605626C2 |
| Штамм Meyerozyma (Pichia) guilliermondii (варианты), используемый для изготовления пре-, про- и аутопробиотических препаратов и продуктов для человека и животных, лечебно-профилактическое средство на его основе и способ его получения (варианты) | 2021 |
|
RU2771136C1 |
| Штамм бактерии Pasteurella multocida "РМ - В" для изготовления биопрепаратов для специфической профилактики пастереллеза (геморрагической септицемии) крупного рогатого скота, вызванного пастереллой серогруппы В | 2023 |
|
RU2818959C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ИНГИБИТОР РОСТА HELICOBACTER PYLORI И СПОСОБ ПРОВЕДЕНИЯ АНТИХЕЛИКОБАКТЕРНОЙ ТЕРАПИИ | 2007 |
|
RU2367458C1 |
| МОРОЖЕНОЕ, СОДЕРЖАЩЕЕ ТРЕГАЛОЗУ, АГАРОЗУ И ЭРИТРУЛОЗУ | 2012 |
|
RU2515381C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСФОРМИРОВАННЫХ РАСТИТЕЛЬНЫХ КЛЕТОК, СОДЕРЖАЩИХ РЕКОМБИНАНТНУЮ ЩЕЛОЧНУЮ ФОСФАТАЗУ ЧЕЛОВЕКА, И ПРИМЕНЕНИЕ ТРАНСФОРМИРОВАННЫХ РАСТИТЕЛЬНЫХ КЛЕТОК, СОДЕРЖАЩИХ РЕКОМБИНАНТНУЮ ЩЕЛОЧНУЮ ФОСФАТАЗУ ЧЕЛОВЕКА | 2018 |
|
RU2698397C2 |
| Способ получения биологически активной добавки на основе молочной сыворотки и растительного экстракта | 2022 |
|
RU2792775C1 |
Настоящее изобретение относится к способу производства капсулированной формы антимикробного препарата для терапии заболеваний желудочно-кишечного тракта, характеризующемуся тем, что проводят культивирование бактерий, выделенных из сапропеля, на агаризованной питательной среде состава (г/л): пептический перевар животной ткани - 6,0, гидролизат казеина - 4,0, дрожжевой экстракт - 3,0, мясной экстракт - 1,5, глюкоза - 1,0, агар-агар - 15,0, при температуре 37°С до достижения концентрации бактерий 2,0⋅106 КОЕ/мл, отделение биомассы от питательной среды центрифугированием, сублимационную сушку надосадочной жидкости и последующее инкапсулирование полученного сухого остатка в оболочку на основе растительных полисахаридов, причем центрифугирование осуществляют при 3900 об/мин в течение 20 мин, сублимационную сушку надосадочной жидкости - при вакууме 0,05 мБар и температуре -20°С, а используемая оболочка капсулы содержит каррагинан, агар-агар, глицерин и воду. Настоящее изобретение обеспечивает разработку нового способа производства капсулированной формы антимикробного препарата на основе биомассы бактерий, изолированных из сапропеля, для терапии заболеваний желудочно-кишечного тракта, имеющих микробиологическую природу. 3 з.п. ф-лы, 1 табл., 3 пр.
1. Способ производства капсулированной формы антимикробного препарата для терапии заболеваний желудочно-кишечного тракта, характеризующийся тем, что проводят культивирование бактерий, выделенных из сапропеля, на агаризованной питательной среде состава (г/л): пептический перевар животной ткани - 6,0, гидролизат казеина - 4,0, дрожжевой экстракт - 3,0, мясной экстракт - 1,5, глюкоза - 1,0, агар-агар - 15,0, при температуре 37°С до достижения концентрации бактерий 2,0⋅106 КОЕ/мл, отделение биомассы от питательной среды центрифугированием, сублимационную сушку надосадочной жидкости и последующее инкапсулирование полученного сухого остатка в оболочку на основе растительных полисахаридов, причем центрифугирование осуществляют при 3900 об/мин в течение 20 мин, сублимационную сушку надосадочной жидкости - при вакууме 0,05 мБар и температуре -20°С, а используемая оболочка капсулы содержит каррагинан, агар-агар, глицерин и воду.
2. Способ по п. 1, отличающийся тем, что в состав оболочки капсулы входят растительные полисахариды и пластификатор глицерин при следующем соотношении компонентов, мас.%:
3. Способ по п. 1, отличающийся тем, что в состав оболочки капсулы входят растительные полисахариды и пластификатор глицерин при следующем соотношении компонентов, мас.%:
4. Способ по п. 1, отличающийся тем, что в состав оболочки капсул входят растительные полисахариды и пластификатор глицерин при следующем соотношении компонентов, мас.%:
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ПРЕПАРАТА С ПРОБИОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2605626C2 |
| СПОСОБ ПРОФИЛАКТИКИ ЯЗВООБРАЗОВАНИЯ НА СЛИЗИСТОЙ ОБОЛОЧКЕ ЖЕЛУДКА | 2011 |
|
RU2481111C1 |
| WO 2015077794 A1, 28.05.2015 | |||
| Платонов В.В и др., БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ САПРОПЕЛЯ / ФУНДАМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ, 2014, N.9, стр.2474-2480. | |||
Авторы
Даты
2021-02-24—Публикация
2020-03-03—Подача