Изобретение относится к биотехнологии, фармацевтике и медицине, а именно к получению фармацевтической композиции для лечения заболеваний, имеющих микробиологическую природу.
По оценкам Всемирной организации здравоохранения, половина всех производимых в мире антибиотиков используется не только для лечения людей, но и животных и птиц, продукцию от которых человек употребляет в пишу. Неудивительно, что количество штаммов возбудителей, резистентных даже к резервной группе, неуклонно возрастает. Так, распространенность штаммов S. aureus, резистентных к оксациллину, к 2012 г.в США составляла 25-75%, штаммов Acinetobacter baumannii, устойчивых к карбапенемам, - до 80% в отдельных штатах. В Европе ситуация немногим лучше: распространенность возбудителей, резистентных к карбапенемам, в 2013 г.достигала 25%, а в Италии и Греции превышала 52%[1].
Неуклонный рост антибиотикорезистентности - одна из острейших глобальных медицинских и социальных проблем. Следствием этого является увеличение заболеваемости, сроков стационарного лечения и уровня смертности. Сегодня человечество вплотную подошло к тому рубежу, за которым устойчивость к антибиотикам станет серьезной угрозой для общественного здравоохранения. Разработка новых антибиотиков -сложный, длительный и крайне дорогостоящий процесс. Антибиотики теряют свою эффективность так быстро, что фармацевтические компании не успевают создавать новые [1].
В поисках решения этой задачи возрос интерес к разработке эффективных пробиотических препаратов на основе безопасных для человека бактерий-антагонистов; к изучению нового класса антимикробных пептидов, продуцируемых эукариотическими клетками, а также к исследованиям большого числа антимикробных субстанций бактериального происхождения. Среди последних особое место занимают бактериоцины - рибосомально синтезируемые клеткой низкомолекулярные (<10,0 кДа), термоустойчивые, чаще всего катионной природы гидрофобные пептиды [2-3].
В настоящее время в научной литературе имеется значительное количество публикаций, посвященных вопросам изучения и биотехнологического производства различных видов биологически активных веществ, продуцируемых преимущественно спорообразующими микроорганизмами вида Bacillussubtilis, а также рядом штаммов молочнокислых бактерий [4].
Из уровня техники известно средство, обладающее антибактериальной активностью (патент РФ №1779377, опубл. 07.12.1992), содержащее живую культуру ацидофильных лактобактерий в сочетании с комплексом сывороточных иммуноглобулинов, взятых в одинаковых весовых частях, при концентрации жизнеспособных микробных клеток 107-108 на массу 0,1 г и процентном соотношении компонентов в комплексе иммуноглобулина G:M:A, равном (55-60):(20-25):(15-20), для получения которого сухую микробную массу соединяют с сухой биомассой КИП в соотношении 1:1 и используют для приготовления оральной или ректальной формы.
В качестве недостатка известного изобретения следует признать низкую антибактериальную активность препарата.
Также известна фармацевтическая композиция антибиотиков и пребиотиков для профилактики и лечения дисбиозов в процессе антибактериальной терапии (патент РФ №2325187, опубл. 27.05.2008), содержащая (по первому варианту) антибиотик и пребиотик - олигосахарид, выбранный из группы: фруктоолигосахариды, галактоолигосахариды, ксилоолигосахариды, мальтоолигосахариды и изомальтоолигосахариды со степенью полимеризации от 2 до 10, с размером частиц до 0,3 мм и чистотой не менее 95%, а антибиотик - с размерами частиц от 20 до 200 мкм; антибиотик и олигосахарид включены в массовом соотношении от 1:1 до 1:100 соответственно; по второму варианту фармацевтическая композиция содержит антибиотик в виде порошка с размерами частиц от 20 до 200 мкм, выбранный из группы: бета-лактамы, включая комбинации бета-лактамов с ингибиторами бактериальных беталактамаз; азалиды, фторхинолоны, амфениколы, гликопептиды, ансамицины, нитрофураны, производные фосфоновой кислоты, циклосерин, триметоприм, а в качестве пребиотика - олигосахарид в виде порошка со степенью полимеризации от 2 до 10, с размером частиц до 0,3 мм, чистотой не менее 95%; при этом антибиотик и олигосахарид включены в состав композиции в массовом соотношении от 1:1 до 1:100, соответственно.
Недостатком известного способа получения фармацевтической композиции является отсутствие процесса помола действующих веществ с целью повышения ихантибактериальной активности после высушивания, так как процесс подсушки композиции до 2-3% влажности обязательно приведет к агрегации частиц антибиотика и олигосахарида с соответствующей потерей их дисперсности, а, следовательно, и активности.
Известен комплексный бактериальный препарат для лечения и профилактики желудочно-кишечных заболеваний животных энтерацид П, содержащий штаммы Lactobacillusacidophilus ВКПМ В-6535 и Enterococcusfaecium ВКПМ В-2990 (патент РФ №2091075, опубл. 27.09.1997), получение которого включает следующие этапы: приготовление питательной среды для раздельного выращивания составляющих его культур, получение инокулята, приготовление посевного материала, накопление бактериальной массы, отделение бактериальной массы от культуральной жидкости, приготовление защитной среды, смешиваниебактериальной массы с защитной средой, замораживание, сушка суспензии сублимацией, измельчение сухих порошков биомассы, смешивание культур-компонентов, стандартизация, упаковка, маркировка.
Основным недостатком данного способа является низкая антибактериальная активность.
Известна фармацевтическая бактериоциновая композиция, отличающаяся тем, что содержит эффективное количество лантионинсодержащего бактериоцина (выбранного из группы, состоящей из низина, субтилина, эпидермина, Пен 5, анковенина, таллидермина, дуромицина или циннамицина) и фармацевтически приемлемый носитель - цитрат, ЭДТК, кислотный носитель (заявка на изобретение №94037764, опубл. 27.07.1996).
Известная фармацевтическая бактериоциновая композиция характеризуется недостатком - недостаточно широкий спектр антимикробной активности (Escherichiacoli, Helicobacterpylori, Campylobacterjejuni).
В ходе патентного поиска не выявлено техническое решение, принятое в качестве ближайшего аналога.
Технической задачей предлагаемого изобретения является расширение ассортимента фармацевтических композиций для терапии заболеваний микробиологической природы.
Технический результат, достигаемый при реализации заявленного изобретения, состоит в разработке нового способа получения фармацевтической композиции с широким спектром антимикробного действия, содержащей бактериоцины, для лечения заболеваний, имеющих микробиологическую природу.
Для достижения указанного технического результата предложено использовать разработанный способ. Согласно разработанному способу получения бактериоцинсодержащей фармацевтической композиции осуществляют культивирование бактерий, выделенных из почвы, до достижения концентрации бактерий 2,0⋅106 КОЕ/мл, после чего биомассу отделяют от питательной среды центрифугированием, полученную надосадочную жидкость сублимационно высушивают. Из полученной сухой массы надосадочной жидкости, которую предварительно растворяют в 0,25 M фосфатном буфере, путем осаждения сульфатом аммония выделяют общий белок, который разделяют методом гель-проникающей ВЭЖХ. Полученные пептидные фракции (бактериоцины) подвергают хроматографической очистке и сублимационной сушке. Бактериоцинсодержащие фармацевтические композиции получают путем смешивания бактериоцинов в соответствии с рецептурами.
В предпочтительном варианте реализации способа отбирают образцы почвы. Для выделения колоний бактерий отобранные образцы почвы измельчают в стерильных условиях и небольшой кусочек растирают на поверхности чашки Петри с агаризованной питательной средой, либо 5 г образца вносят в 5 мл жидкой питательной среды. Инкубируют чашки Петри и пробирки при температуре 37°С стационарно в течение 3 суток.
Для первичного выделения бактерий используют жидкие питательные среды. Из пробирок с видимым ростом бактерий (помутнение) и с суммарных газонов на чашках проводят истощающие рассевы. Выделенные бактерии культивируют на агаризованных питательных средах.
Культуры бактерий, выделенных из почвы, хранят в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не более24 месяцев.
Согласно изобретению, бактериоцинсодержащие фармацевтические композиции получают следующим образом. Лиофилизированные культуры бактерий, выделенных из почвы, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток растворяют в 0,25 M фосфатном буфере, после чего осаждают общий белок добавлением концентрированного раствора сульфата аммония. Полученную взвесь белков отделяют от раствора центрифугированием при 8000 об/мин.
Далее общий белок разделяют на фракции методом гель-проникающей ВЭЖХ с использованием хроматографа Biorad (США). Отобранные фракции, содержащие индивидуальные белки, исследуют методом ПААГ-электрофореза и МАЛДИ-ТОФ спектрометрии с использованием стандартных протоколов производителя.
Дополнительно каждую фракцию очищают с использованием хроматографии на гидрофобных смолах Amberlite XAD Х-6.
Сублимационную сушку бактериоцинов осуществляют на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -30°С.
Готовят бактериоцинсодержащие фармацевтические композиции путем смешивания бактериоцинов в порционном смесителе при скорости вращения мешалки 50 об/мин в соответствии с рецептурами.
Изобретение иллюстрируется следующими примерами.
Пример 1
Отбирают образцы почвы. Пробы отбирают в шахматном порядке, по диагонали, методом конверта на определенной глубине или по горизонтам. Для отбора проб почвы используют лопату, совок, нож и почвенный бур. Каждый предмет перед взятием отдельной пробы тщательно очищают, протирают ватным тампоном со спиртом и обжигают. Образцы почвы отбирают в стерильную бумагу Крафта.
Для выделения колоний бактерий отобранные образцы почвы измельчают в стерильных условиях и небольшой кусочек (приблизительно 5 г) растирают на поверхности чашки Петри с агаризованной питательной средой состава (г/л): бактопептон - 10, аммоний лимоннокислый - 2, мясной экстракт - 10, натрий уксуснокислый - 5, дрожжевой экстракт - 5, MgSO4⋅7H2O - 0,1, глюкоза - 20, MnSO4⋅5H2O - 0,05, твин 80 - 1, Na2HP04 -2. pH готовой среды доводят до 6,5. Инкубируют чашки Петри и пробирки при температуре 37°С стационарно в течение 3 суток.
Для первичного выделения бактерий используют жидкую питательную среду аналогичного состава. Из пробирок с видимым ростом бактерий (помутнение) и с суммарных газонов на чашках проводят истощающие рассевы. Выделенные бактерии культивируют на агаризованной питательной среде. Культуры бактерий, выделенных из почвы, хранят в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не более 24 месяцев.
Лиофилизированные культуры бактерий, выделенных из почвы, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток растворяют в 0,25 M фосфатном буфере, после чего осаждают общий белок добавлением концентрированного раствора сульфата аммония. Полученную взвесь белков отделяют от раствора центрифугированием при 8000 об/мин.
Далее общий белок разделяют на фракции методом гель-проникающей ВЭЖХ с использованием хроматографа Biorad (США). Для этого осадок белка растворяют в 1 мл 0,025 M Трис буферного раствора с рН 4,5. Осадок наносят на колонку для гель-проникающей ВЭЖХ, используя систему прямого ввода. В качестве колонки для гель-проникающей хроматографии используют колонку Enrich 650 10 mm X 300 mm производства Biorad (США). Детектирование проводят при длине волны 280 нм.
Фракционирование осуществляют с использованием коллектора фракций NGC Biorad (США).
Отобранные фракции, содержащие индивидуальные белки, исследуют методом ПААГ-электрофореза и МАЛДИ-ТОФ спектрометрии с использованием стандартных протоколов производителя. Состав полученных пептидных фракций приведен в таблице 1.

Дополнительно каждую фракцию очищают с использованием хроматографии на гидрофобных смолах Amberlite XAD Х-6. Стеклянную колонку заполняют 10 г смолы Amberlite XAD-2, смолу уравновешивают 10 мл 20 мМ раствором трифторуксусной кислоты в воде. На колонку наносят подготовленный раствор белка в ацетатном буферном растворе и элюируют в градиенте метанола от 0% до 15%, подъем градиента 5% на каждые 10 фракций. Фракции, содержащие белки, определяют, отбирая от каждой фракции по 50 мкл, смешивают с раствором реактива Брэдфорда в соотношении 1:1. Полученный раствор измеряют на спектрофотометре BioradSmartSpecPlus Spectrophotometer (США). Фракции, имеющие оптическое поглощение 0,06 и более, отбирают для дальнейшей сушки.
Сублимационную сушку пептидов осуществляют на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -30°С.
Результаты определения антибактериальных свойств выделенных пептидов представлены в таблице 2, фунгицидных свойств - в таблице 3.
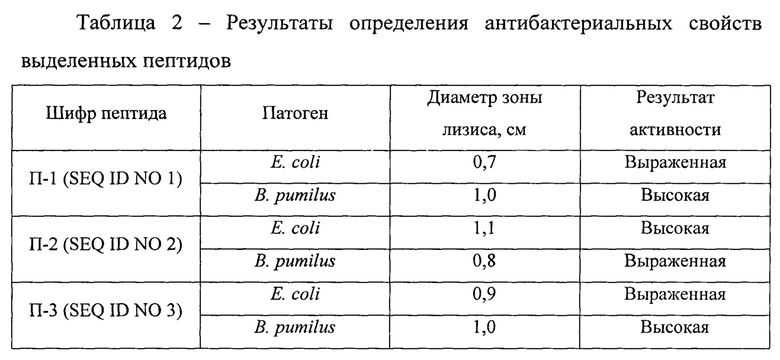

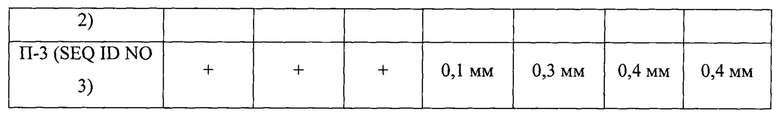
Согласно таблице 2, все три изученные пептидные фракции демонстрируют высокую антагонистическую активность по отношению к Е. coli и В. pumilus. Из таблицы 3 следует, что выделенные пептиды способны ингибировать рост и размножение микроскопических грибов Aspergillus niger и Aspergillus flavus. Наличие у пептидов, выделенных из биомассы бактерий, изолированных из почвы, антибактериальных и фунгицидных свойств позволяет отнести их к бактериоцинам.
Далее готовят бактериоцинсодержащую фармацевтическую композицию путем смешивания бактериоцинов в порционном смесителе при скорости вращения мешалки 50 об/мин при следующем массовом соотношении компонентов, масс. %:
П-1 (SEQ ID NO 1) - 30,0
П-2 (SEQ ID NO 2) - 35,0
П-3 (SEQ ID NO 3) - 35,0.
Результаты определения антибактериальных и фунгицидных свойств фармацевтической композиции представлены в таблицах 7 и 8, соответственно.
Пример 2
Отбирают образцы почвы согласно примеру 1.
Для выделения колоний бактерий отобранные образцы почвы измельчают в стерильных условиях и небольшой кусочек (приблизительно 5 г) растирают на поверхности чашки Петри с агаризованной питательной средой состава (г/л): триптон - 10, дрожжевой экстракт - 5, NaCl - 10. Инкубируют чашки Петри и пробирки при температуре 37°С стационарно в течение 3 суток.
Для первичного выделения бактерий используют жидкую питательную среду аналогичного состава. Из пробирок с видимым ростом бактерий (помутнение) и с суммарных газонов на чашках проводят истощающие рассевы. Выделенные бактерии культивируют на агаризованной питательной среде. Культуры бактерий, выделенных из почвы, хранят в сублимационно-высушенном состоянии в ампулах при температуре 4±2°С не более 24 месяцев.
Лиофилизированные культуры бактерий, выделенных из почвы, восстанавливают путем переноса содержимого ампул в пробирки с жидкой питательной средой. Далее осуществляют процесс ферментации при температуре 37°С в течение 16-24 ч до достижения концентрации бактерий 2,0⋅106 КОЕ/мл.
По окончании культивирования удаляют клеточный дебрис, после чего культуры центрифугируют при 3900 об/мин в течение 20 мин. Надосадочную жидкость переносят в сосуды для лиофилизации и упаривают досуха на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -20°С. Сухой остаток растворяют в 0,25 M фосфатном буфере, после чего осаждают общий белок добавлением концентрированного раствора сульфата аммония. Полученную взвесь белков отделяют от раствора центрифугированием при 8000 об/мин.
Далее общий белок разделяют на фракции методом гель-проникающей ВЭЖХ с использованием хроматографа Biorad (США). Для этого осадок белка растворяют в 1 мл 0,025 M Трис буферного раствора с рН 4,5. Осадок наносят на колонку для гель-проникающей ВЭЖХ, используя систему прямого ввода. В качестве колонки для гель-проникающей хроматографии используют колонку Enrich 650 10 mm X 300 mm производства Biorad (США). Детектирование проводят при длине волны 280 нм. Фракционирование осуществляют с использованием коллектора фракций NGC Biorad (США).Отобранные фракции, содержащие индивидуальные белки, исследуют методом ПААГ-электрофореза и МАЛДИ-ТОФ спектрометрии с использованием стандартных протоколов производителя. Состав полученных пептидных фракций приведен в таблице 4.

Дополнительно каждую фракцию очищают с использованием хроматографии на гидрофобных смолах Amberlite XAD Х-6. Стеклянную колонку заполняют 10 г смолы Amberlite XAD-2, смолу уравновешивают 10 мл 20 мМ раствором трифторуксусной кислоты в воде. На колонку наносят подготовленный раствор белка в ацетатном буферном растворе и элюируют в градиенте метанола от 0% до 15%, подъем градиента 5% на каждые 10 фракций. Фракции, содержащие белки, определяют, отбирая от каждой фракции по 50 мкл, смешивают с раствором реактива Брэдфорда в соотношении 1:1. Полученный раствор измеряют на спектрофотометре BioradSmartSpecPlus Spectrophotometer (США). Фракции, имеющие оптическое поглощение 0,06 и более, отбирают для дальнейшей сушки.
Сублимационную сушку пептидов осуществляют на сублимационной сушилке Labconco "Triad" при вакууме 0,05 мБар и температуре -30°С.
Результаты определения антибактериальных свойств выделенных пептидов представлены в таблице 5, фунгицидных свойств - в таблице 6.
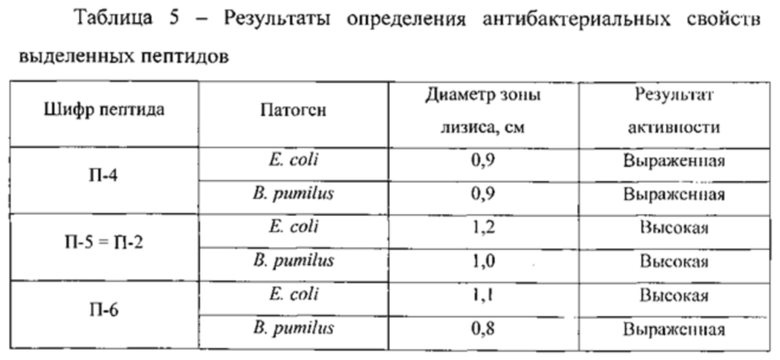
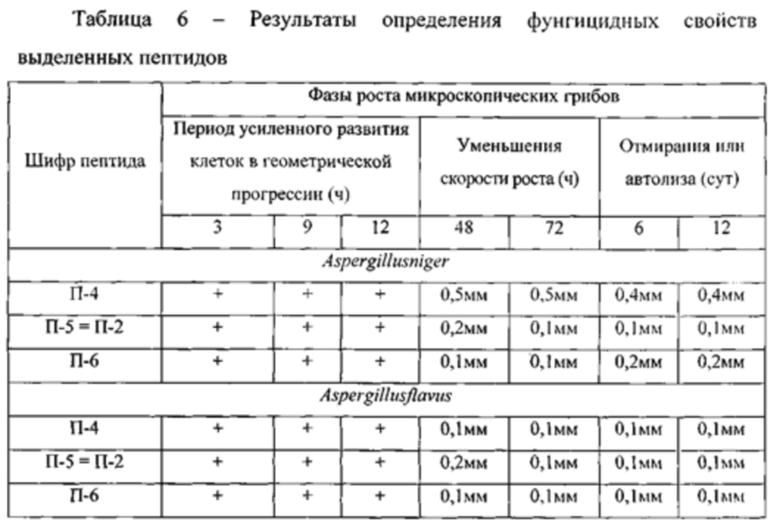
Согласно таблице 5, все три изученные пептидные фракции демонстрируют высокую антагонистическую активность по отношению к Е. coli и В. pumilus. Из таблицы 6 следует, что выделенные пептиды способны ингибировать рост и размножение микроскопических грибов AspergillusnigervL Aspergillusflavus. Наличие у пептидов, выделенных из биомассы бактерий, изолированных из почвы, антибактериальных и фунгицидных свойств позволяет отнести их к бактериоцинам.
Далее готовят бактериоцинсодержащую фармацевтическую композицию путем смешивания бактериоцинов в порционном смесителе при скорости вращения мешалки 50 об/мин при следующем массовом соотношении компонентов, масс. %:
П-4 - 20,0
П-2 - 55,0
П-6 - 25,0.
Результаты определения антибактериальных и фунгицидных свойств фармацевтической композиции представлены в таблицах 7 и 8, соответственно.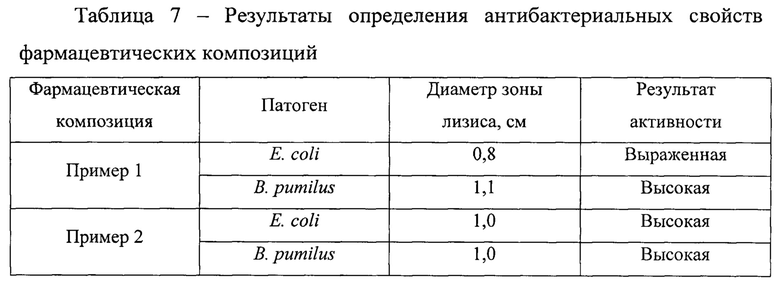
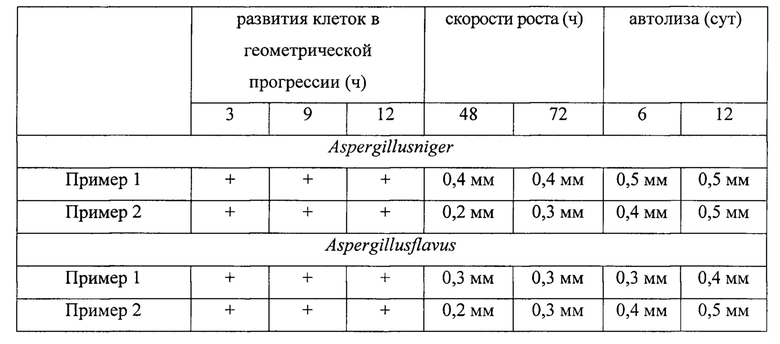
Из таблиц 7-8 следует, что бактериоцинсодержащие фармацевтические композиции, полученные согласно двум примерам, проявляют высокую антимикробную активность по отношению к бактериям и микроскопическим грибам.
Таким образом, техническим результатом заявленного способа является разработка нового способа получения фармацевтической композиции с широким спектром антимикробного действия, содержащей бактериоцины, для лечения инфекционных заболеваний, имеющих микробиологическую природу.
Источники информации:
1. Мухина, Е.Г. Социальная проблема антибиотикорезистентности / Е.Г. Мухина, М.А. Артемьева, Л.А. Сакунц, Б.Т. Тожибоева // Universum: Медицина и фармакология: электрон, научн. журн. 2017. №6(40). URL: http://7universum.com/ru/meaVarchive/item/4898.
2. Ennahar, S. Class Ilabacteriocins: biosynthesis, structure and activity / S. Ennahar, T. Sashihara, K. Sonomoto, A. Ishizaki // FEMS Microbiology Reviews. 2000. Vol.24. Issue 1. P. 85-106.
3. Popaganni, M. Ribosomallysynthezed peptides with antimicrobial properties: biosynthesis, structure, function, and applications / M. Popaganni // Biotechnol. Adv. 2003. Vol.21. №6. P. 465-499.
4. Забокрицкий, Н.А. Биологически активные вещества, синтезируемые пробиотическими микроорганизмами родов Bacillus и Lactobacillus II Журнал научных статей «Здоровье и образование в XXI веке. 2015. Т. 17. №3.
СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОЦИНСОДЕРЖАЩЕЙ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ МИКРОБИОЛОГИЧЕСКОЙ ПРИРОДЫ
Перечень аминокислотных последовательностей
SEQ ID NO 1
Val Met Cys Leu Ala Arg Lys Cys Ser Gln Gly Leu Ile Val Lys Ala
Pro Leu Met
SEQ ID NO 2
Phe Leu Ala Phe Ala Tyr Leu Pro Ile Pro Gly Trp His Pro Asp Tyr
Asn Gly Arg Ala Met Lys Trp Ala Asn Arg Pro Phe Thr Tyr Ile Cys
His Gly Arg Asp Leu Lys Leu Arg Gln Met Leu Tyr Ser Gly Ala Thr
Ile Gly His Ala Glu Met Arg
SEQ ID NO 3
Ala Val Pro Ser Met Lys Leu Cys Ile Gln Trp Ser Pro Val Arg Ala
Ser Pro Cys Val Met Leu Gly Ile
SEQ ID NO 4
Pro His Gln Gly His Ala Phe Asn Phe Ser Cys Asp Met Glu Thr Ala
Gly Phe Lys Gly Thr Gln Phe Trp Thr Phe Lys Ser Val Ser Pro His
Leu Ala Thr Phe Lys Leu Gly His Met Ser Thr Tyr Ala Ile Leu Gly
Phe Ala Gly Cys His
SEQ ID NO 5
Phe Leu Ala Phe Ala Tyr Leu Pro Ile Pro Gly Trp His Pro Asp Tyr
Asn Gly Arg Ala Met Lys Trp Ala Asn Arg Pro Phe Thr Tyr Ile Cys
His Gly Arg Asp Leu Lys Leu Arg Gln Met Leu Tyr Ser Gly Ala Thr
Ile Gly His Ala Glu Met Arg
SEQ ID NO 6
Phe Val Lys Gly Phe His Pro Ser Met Thr Ala Arg Gly Val Val Ser
Asp Glu Ala Asp Gly Arg Cys Asp Arg Phe Val Lys Gly Phe His Pro
Ser Met Thr Ala Arg Gly Val Val Ser Asp Glu Ala Asp Gly Arg Cys
Asp Arg
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И СООТВЕТСТВУЮЩИЕ КОМПОЗИЦИИ ДЛЯ ИЗГОТОВЛЕНИЯ ПРОДУКТОВ ПИТАНИЯ И КОРМОВ | 2018 |
|
RU2780586C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА | 2018 |
|
RU2805081C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА | 2018 |
|
RU2783258C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ КОНТРОЛЯ ЗАБОЛЕВАНИЙ, ПЕРЕДАВАЕМЫХ ПЕРЕНОСЧИКАМИ | 2018 |
|
RU2777518C2 |
| КОМПОЗИЦИИ И СООТВЕТСТВУЮЩИЕ СПОСОБЫ КОНТРОЛЯ ЗАБОЛЕВАНИЙ, ПЕРЕДАВАЕМЫХ ПЕРЕНОСЧИКАМИ | 2018 |
|
RU2804136C2 |
| СПОСОБЫ УЛУЧШЕНИЯ ЗДОРОВЬЯ РАСТЕНИЯ С ПРИМЕНЕНИЕМ СВОБОДНЫХ ФЕРМЕНТОВ И МИКРООРГАНИЗМОВ, ЭКСПРЕССИРУЮЩИХ ФЕРМЕНТЫ НА ПОВЫШЕННОМ УРОВНЕ | 2017 |
|
RU2802848C2 |
| ПОЛИПЕПТИДНЫЕ КОНСТРУКЦИИ ЛИЗИН-ПРОТИВОМИКРОБНЫЙ ПЕПТИД (AMP), ЛИЗИНЫ, ВЫДЕЛЕННЫЕ ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ, А ТАКЖЕ ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2803121C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛА К PCSK-9, И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2782792C2 |
| Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с BCMA, и его применение | 2022 |
|
RU2820350C2 |
| Синергетическое действие SMN1 и miR-23a при лечении спинальной мышечной атрофии | 2021 |
|
RU2839898C2 |
Изобретение относится к биотехнологии, а именно к способу получения бактериоцинсодержащей композиции, обладающей антимикробной активностью. Проводят культивирование бактерий, выделенных из почвы, при температуре 37°С на агаризованной питательной среде состава, г/л: бактопептон - 10, аммоний лимоннокислый - 2, мясной экстракт - 10, натрий уксуснокислый - 5, дрожжевой экстракт - 5, MgSO4⋅7H2O - 0,1, глюкоза - 20, MnSO4⋅5H2O - 0,05, твин 80 - 1, Na2HPO4 - 2, либо на агаризованной питательной среде состава, г/л: триптон - 10, дрожжевой экстракт - 5, NaCl – 10. Отделяют биомассу центрифугированием при 3900 об/мин. Проводят сублимационную сушку надосадочной жидкости при вакууме 0,05 мБар и температуре –20°С. Сухую массу надосадочной жидкости растворяют в 0,25 Μ фосфатном буфере. Осаждают сульфатом аммония общий белок. Разделяют белки на бактериоцины методом гель-проникающей ВЭЖХ. Очищают бактериоцины на смоле Amberlite XAD-2. Сушат сублимационным методом при вакууме 0,05 мБар и температуре –30°С. Смешивают бактериоцины в соответствии с рецептурами получения бактериоцинсодержащей композиции. Изобретение позволяет расширить ассортимент композиций, содержащих бактериоцины, с широким спектром антимикробного действия для лечения заболеваний, имеющих микробиологическую природу. 2 з.п. ф-лы, 8 табл., 2 пр.
1. Способ получения бактериоцинсодержащей композиции, обладающей антимикробной активностью, включающий:
культивирование бактерий, выделенных из почвы, при температуре 37°С на агаризованной питательной среде состава, г/л: бактопептон - 10, аммоний лимоннокислый - 2, мясной экстракт - 10, натрий уксуснокислый - 5, дрожжевой экстракт - 5, MgSO4⋅7H2O - 0,1, глюкоза - 20, MnSO4⋅5H2O - 0,05, твин 80 - 1, Na2HPO4 - 2,
либо на агаризованной питательной среде состава, г/л: триптон - 10, дрожжевой экстракт - 5, NaCl - 10,
отделение биомассы от питательной среды центрифугированием при 3900 об/мин,
сублимационную сушку надосадочной жидкости при вакууме 0,05 мБар и температуре –20°С,
осаждение сульфатом аммония общего белка из сухой массы надосадочной жидкости, предварительно растворенной в 0,25 Μ фосфатном буфере,
разделение белка на бактериоцины методом гель-проникающей ВЭЖХ,
очистку бактериоцинов осуществляют хроматографически на гидрофобных смолах Amberlite XAD-2,
сушку полученных бактериоцинов сублимационным методом при вакууме 0,05 мБар и температуре –30°С и
смешивание бактериоцинов в соответствии с рецептурами получения бактериоцинсодержащей композиции, обладающей антимикробной активностью.
2. Способ по п. 1, отличающийся тем, что культивирование бактерий, выделенных из почвы, осуществляют на питательной среде состава, г/л: бактопептон - 10, аммоний лимоннокислый - 2, мясной экстракт - 10, натрий уксуснокислый - 5, дрожжевой экстракт - 5, MgSO4⋅7H2O - 0,1, глюкоза - 20, MnSO4⋅5H2O - 0,05, твин 80 - 1, Na2HPO4 - 2; получают бактериоцины, имеющие аминокислотные последовательности SEQ ID NO. 1 (П-1), SEQ ID NO. 2 (П-2) и SEQ ID NO. 3 (П-3), которые смешивают для приготовления бактериоцинсодержащей композиции при следующем соотношении компонентов, мас. %:
3. Способ по п. 1, отличающийся тем, что культивирование бактерий, выделенных из почвы, осуществляют на питательной среде состава, г/л: триптон - 10, дрожжевой экстракт - 5, NaCl - 10; получают бактериоцины, имеющие аминокислотные последовательности SEQ ID NO. 4 (П-4), SEQ ID NO. 2 (П-2) и SEQ ID NO. 6 (П-6), которые смешивают для приготовления бактериоцинсодержащей композиции при следующем соотношении компонентов, мас. %:
| ШТАММЫ BACILLUS SAFENSIS ВКПМ В-12180, BACILLUS LICHENIFORMIS ВКПМ В-1224, BACILLUS PUMILUS ВКПМ В-12182, BACILLUS ENDOPHYTICUS ВКПМ В-12181 - ПРОДУЦЕНТЫ БАКТЕРИОЦИНОВ ПРОТИВ БАКТЕРИАЛЬНЫХ ПАТОГЕНОВ, СПОСОБ ПОЛУЧЕНИЯ НИЗИНА | 2017 |
|
RU2694590C2 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ПРЕПАРАТА С ПРОБИОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2605626C2 |
| RU 2014150635 A, 15.12.2014 | |||
| ЗИМИНА М.И | |||
| и др | |||
| Определение оптимальных условий культивирования для синтеза бактериоцинов штаммами Bacillus endopheticus и Bacillus licheniformis и изучение их стабильности | |||
| Техника и технология пищевых производств | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| МИКРОБИЦИДНАЯ ИЛИ МИКРОБИОСТАТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ БАКТЕРИОЦИН И ЭКСТРАКТ РАСТЕНИЯ СЕМЕЙСТВА LABIATAE | 2004 |
|
RU2395204C2 |
Авторы
Даты
2022-05-30—Публикация
2020-03-03—Подача