Изобретение относится к медицине, а именно кардиоонкологии и медицинской генетике, и может быть использовано для прогнозирования риска развития подострой кардиотоксичности до применения антрациклиновых препаратов у пациентов - носителей полиморфизма rs28714259 в гомозиготном и гетерозиготном состоянии.
Современные методы в области диагностики и лечения онкологических заболеваний значительно повысили выживаемость пациентов. Антрациклиновые антиобиотики являются одними из самых мощных химиотерапевтических агентов с момента открытия их лекарственных свойств. Однако помимо противоопухолевого эффекта, антрациклиновые антибиотики обладают также дозазависимым кардиотоксическим свойством. Сердечнососудистые осложнения на фоне антрациклиновой химиотерапии считаются одной из причин смертности больных раком молочной железы (РМЖ) [1].
Различают три типа антрациклин-опосредованной кардиотоксичности (АОК): острая, подострая и хроническая. Острая АОК проявляется в течение первой недели применения антрациклиновых препаратов в виде нарушений сердечного ритма и сопровождается изменениями на электрокардиограмме (ЭКГ) [2]. Несмотря на то, что описанные изменения обратимы, они могут быть связаны в дальнейшем с ранними и поздними проявлениями хронической АОК.
Подострая АОК возникает в течение нескольких дней или недель с момента начала химиотерапии и характеризуется острой сердечной недостаточностью, миокардитом и перикардитом [3]. Первые проявления ранней хронической АОК обнаруживаются, как правило, через год после завершения последнего курса химиотерапии - в частности, бессимптомная дисфункция желудочков, застойная сердечная недостаточность и аритмия [4]. Поздняя форма хронической АОК диагностируется через 3-5 лет после завершения антрациклиновой химиотерапии и большую часть времени развивается бессимптомно. Основным ее проявлением является хроническая сердечная недостаточность [5].
Предотвращение кардиотоксичного эффекта и благоприятный прогноз напрямую зависят от точного определения индивидуальных рисков для каждого больного.
В настоящее время выбор клинициста ограничен инструментальными и биохимическими методами, которые применяются, в основном, в диагностике АОК, тогда как прогностическая часть завершается на изучении общих факторов риска: возраст старше 65 лет, ранее перенесенный инфаркт миокарда, гипертоническая болезнь, лучевая терапия в анамнезе и др. [6].
К широкодоступным методам диагностики АОК относятся ЭКГ и 2D эхокардиография (ЭхоКГ). Тем не менее, несмотря на доступность, ЭКГ отличается низкой специфичностью и нередко приводит к ложноположительным результатам [3]. ЭхоКГ применяется прежде всего для определения фракции выброса левого желудочка - основного параметра, определяющего развитие АОК. Вместе с тем, недостатком данного метода считается низкая чувствительность и вариабельность результатов между различными наблюдениями [7].
Меньшее распространение получили такие инструментальные методы, как 3D ЭхоКГ, радионуклидная ангиография, спекл-трекинг эхокардиография и магнитно-резонансная томография. К их ограничениям относятся: зависимость от качества изображения (3D ЭхоКГ) [8], радиационное воздействие (радионуклидная ангиография), сложность выбора оптимальной частоты кадров и необходимость повторных исследований (спекл-трекинг эхокардиография) [9], высокая стоимость исследования (магнитно-резонансная томография) [7]. Биохимические маркеры такие, как тропонины I и Т, натрийуретический пептид, миелопероксидаза, растворимый ST-2 и галектин-3 в качестве диагностических тестов обладают разными критериями информативности и сильно зависимы от формы и проявлений АОК [10].
Практическая потребность определения механизмов осложнений лекарственного лечения привела к широкому развитию фармакогенетики, определяющей ассоциации между аллельными вариациями генов, ответственных за метаболизм лекарств, и индивидуальными различиями ответов на лекарственную терапию.
Известно, что локус rs28714259 локализован в некодирующей области 5-й хромосомы и участвует в дальних геномных взаимодействия с хромосомной областью, в которой локализован ген глюкокортикоидного рецептора. Предполагается, что глюкокортикоидный сигнальный путь регулирует формирование сердечной мышцы и его нарушения приводят к развитию хронической сердечной недостаточности (ХСН) на фоне антрациклиновой терапии [11]. Полиморфизм rs28714259 ранее не использовался для прогнозирования развития АОК до применения химиотерапии с антрациклиновыми антибиотиками.
Анализ патентных источников (см. www.fips.ru) показал наличие одного близкого по тематике изобретения «Способ прогнозирования развития антрациклин-индуцированной кардиотоксичности после полихимиотерапии антибиотиками антрациклинового ряда у пациенток с раком молочной железы» [12], основанного на генотипировании аллелей гена матриксной металлопротеиназы-3, а именно полиморфизма 5А/6А (rs3025058), методом ПЦР в реальном времени. Отметим, что аллели 5А или 6А связывают с повышенным риском инфаркта миокарда или ишемической болезнью сердца. Относительно недавний метаанализ, объединяющий семь ранее опубликованных исследований, показал, что аллель 6А связан с прогрессией коронарного атеросклероза. Тем не менее, все эти исследования демонстрируют большую гетерогенность результатов, - пол, возраст и этническая принадлежность могут изменить влияние этих аллелей []. Кроме того, описанный способ обладает меньшей чувствительностью, чем предлагаемый нами.
Сущность заявленного способа заключается в генотипировании rs28714259 у больных с РМЖ методом HRM-PCR (High Resolution Melt Polymerase chain reaction). Высокий риск развития подострой АОК прогнозируют у носителей генотипов G/A и А/А.
Техническим результатом заявляемого изобретения является создание недорогого, простого в исполнении, высокоинформативного способа прогнозирования риска АОК у онкологических больных до применения антибиотиков антрациклинового ряда.
Технический результат достигается тем, что проводят генотипирование методом полимеразной цепной реакции полиморфизма rs28714259 на матрице ДНК, выделенной подходящим способом из крови или буккального эпителия и при наличии генотипов G/A или А/А прогнозируют высокий риск развития подострой антрациклин-опосредованной кардиотоксичности.
Предлагаемый способ может быть использован для стратификации группы риска больных и выбора оптимальной схемы лечения на основании полученного прогноза.
Заявленный способ включает следующие приемы: выделение тотальной ДНК из венозной крови или буккального эпителия любым подходящим методом; определение полиморфизма rs28714259 методом HRM-PCR в присутствии красителя EvaGreen® Dye и специфичных праймеров на матрице очищенной ДНК; анализ первичных данных с помощью программного продукта амплификатора с определением генотипа относительно референсных образцов.
Способ осуществляется следующим образом.
Геномную ДНК из 200 мкл цельной венозной крови или соскоба буккального эпителия выделяют подходящим методом, например, с помощью комплекта реагентов для экстракции ДНК из клинического материала «АмплиПрайм ДНК-сорб В» («АмплиСенс», Россия) согласно инструкции производителя.
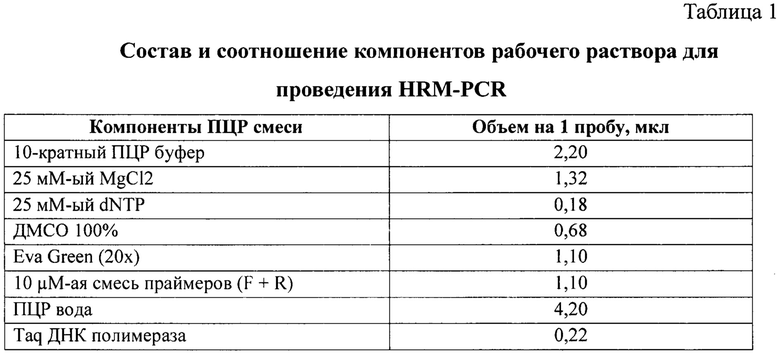
Идентификацию SNP проводят методом HRM-PCR, который представляет собой ПЦР в реальном времени с последующим плавлением наработанных ампликонов. Для приготовления рабочей смеси используют компоненты ПЦР и неспецифический ДНК-связывающий краситель типа EvaGreen® Dye, 20-кратный водный раствор (Biotium, США). Состав и соотношение компонентов рабочего раствора на один исследуемый образец представлены в таблице 1.
Метод HRM предполагает наличие референсных образцов - нормальной гомозиготы, вариантной гетерозиготы и гомозиготы. Характеристики праймеров для HRM и секвенирования указаны в работе [13].
По завершении амплификации проводят анализ кривых плавления, который основывается на детекции уровня флуоресценции как функции температуры.
Предлагаемым способом было генотипирована ДНК 230 женщин с диагнозом РМЖ, европеоидного типа, в возрасте от 32 до 65 лет (медиана возраста - 55 лет), проходивших лечение на базе ФГБУ «НМИЦ онкологии» Минздрава России.
Для всех пациенток было показано проведение 4 курсов химиотерапии с антрациклиновыми антибиотиками: доксорубицин 60 мг/м2 + эндоксан 600 мг/м2 в/в капельно в 1 день каждые 3 недели. Кумулятивная доза доксорубицина составила 240 мг/м2.
На основании анализа клинических показателей пациентки, получавшие химиотерапию с антрациклиновыми антибиотиками, были разделены на две группы: группа 1 (216 человек) без диагностированных сердечно-сосудистых изменений; группа 2 - пациентки с подострой кардиотоксичностью (14 человек). Во вторую группу вошли пациентки, у которых первые проявления подострой кардиотоксичности были диагностированы в течение шести месяцев от начала терапии.
Установлено, что у женщин с подострой АОК частота генотипов G/A и -А/А была достоверно выше по сравнению с группой женщин без диагностированных сердечно-сосудистых изменений (р<0,001).
Результаты ROC-анализа свидетельствовали о том, что значения AUC нашего теста превышали соответствующие значения прототипа: 0,86 против 0,73.
Рассчитанное значение AUC отражает хорошие прогностические качества предложенного нами способа [16].
Работоспособность способа прогнозирования риска развития АОК у пациенток с РМЖ иллюстрируется следующими клиническими примерами:
ПРИМЕР 1.
Пациентка Л, 61 год, 90 кг.
По поводу рака правой молочной железы, cT2N0M0, st IIA, клиническая группа IIa проведена химиотерапия доксорубицином 60 мг/м2 и циклофосфамидом 600 мг/м2. Введение препаратов каждые 3 недели в течение 4 курсов. Суммарная доза доксорубицина 460 мг и циклофосфамида 4600 мг. Исходно жалоб активно не предъявляет. Толерантность к нагрузке умеренная, ходит в быстром темпе, свободно понимается на 4 этаж (см. Табл. 2). Объективно: кожные покровы обычной окраски, бледно-розовые, чистые. Язык влажный, чистый. Тоны сердца ритмичные, ясные. АД 125/80 мм рт ст., ЧСС 71 уд/мин. Дыхание везикулярное, проводится по всем отделам, хрипов нет. Живот не увеличен, при пальпации мягкий, безболезненный, перистальтика кишечника выслушивается. Печень, селезенка не увеличены. Периферических отеков нет. Мочеиспускание свободное.
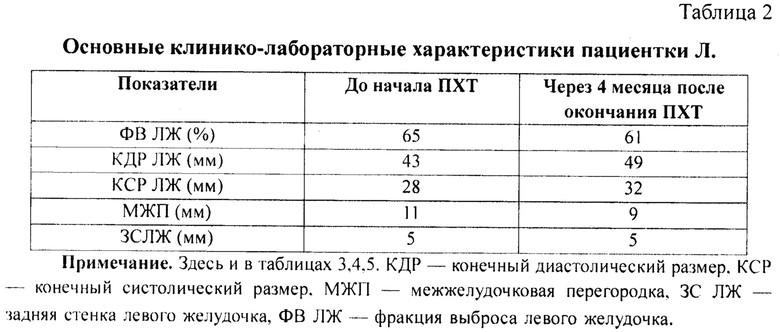
При генотипировании rs28714259 выявлен генотип G/G.
Через 12 мес. после проведенной ПХТ состояние больной стабильное, субъективно без ухудшения самочувствия. Толерантность к физической нагрузке осталась на прежнем уровне. Объективно: кожные покровы чистые, обычной окраски. Язык влажный, чистый. АД - 120/80 мм рт.ст., тоны сердца ясные, ритмичные, ЧСС 74 уд/мин. Дыхание везикулярное, проводится по всем отделам, хрипы не выслушиваются, частота дыхания 15 в минуту. Живот не увеличен, при пальпации мягкий, безболезненный, перистальтика выслушивается. Печень по краю реберной дуги, не увеличена, селезенка не пальпируется. Отеков нет. Мочеиспускание свободное. По данным Эхо-КГ: параметры ФВ ЛЖ, КДР, КСР ЛЖ и МЖП значимо не изменились по сравнению с исходными параметрами, толщина ЗСЛЖ соответствует исходному значению.
ПРИМЕР 2
Пациентка П., 55 лет, 65 кг.
По поводу рака правой молочной железы, cT2N0M0, St IIa, клиническая группа IIa, проведена химиотерапия доксорубицином 60 мг/м2 и циклофосфамидом 600 мг/м2. Введение препаратов каждые три недели в течение 4 курсов. Суммарно введено доксорубицина 420 мг и циклофосфамида 4200 мг. Исходно жалобы пациенткой активно не предъявлялись. Толерантность к физической нагрузке умеренная (см. Табл. 3). Объективно: кожные покровы и видимые слизистые обычной окраски, без элементов сыпи. Язык влажный, чистый. АД - 125/80 мм рт.ст., ЧСС - 70 ударов в минуту, тоны сердца ясные, ритмичные. Дыхание везикулярное, проводится по всем отделам, хрипов нет. Живот не увеличен, при пальпации мягкий, безболезненный, перистальтика кишечника выслушивается. Печень, селезенка не увеличены. Периферических отеков нет. Мочеиспускание свободное.

При генотипировании rs28714259 выявлен генотип G/A.
После 4 курса ПХТ появились жалобы на одышку при привычной физической нагрузке, чувство перебоев в работе сердца. Объективно: кожные покровы бледно-розовые, чистые. Язык влажный, чистый. АД - 125/70, тоны сердца приглушенные, ритмичные, пульс 79 уд/мин. Частота дыхания 16 в минуту, удовлетворительного наполнения и напряжения. Тургор тканей сохранен. Живот обычной формы, мягкий, безболезненный при пальпации во всех точках. Мочеиспускание свободное, безболезненное. ФК ХСН - I по NYHA. По данным Эхо-КГ: уменьшилась ФВ ЛЖ, увеличились КДР ЛЖ, КСР ЛЖ и толщина МЖП.
ПРИМЕР 3
Пациентка Я., 38 лет, 81 кг.
По поводу рака левой молочной железы, cT2N1M0, st IIB, клиническая группа IIa проведена химиотерапия доксорубицином 60 мг/м2 и циклофосфамидом 600 мг/м2. Введение препаратов каждые 3 недели в течение 4 курсов. Суммарная доза 456 мг доксорубицина и циклофосфамида 4560 мг. Исходно жалобы пациенткой активно не предъявлялись. Толерантность к физической нагрузке умеренная (см. Табл. 4). Объективно: кожные покровы бледно-розовые, чистые. Язык влажный, чистый. АД - 125/80 мм рт.ст., ЧСС 72 уд. в минуту, тоны сердца ясные, ритмичные. Дыхание везикулярное, проводится по всем отделам, хрипов пег, частота дыхания 16 в минуту. Живот не увеличен, при пальпации мягкий, безболезненный, перистальтика кишечника выслушивается. Печень, селезенка не увеличены. Периферических отеков нет. Мочеиспускание свободное.

При генотипировании rs28714259 выявлен генотип А/А.
Через 4 месяца после проведенной химиотерапии состояние пациентки значительно ухудшилось. Толерантность к нагрузке снизилась на 21%, появилась отдышка при подъеме на второй этаж, жалобы на быструю утомляемость. Объективно: кожные покровы бледно-розовые, чистые. Язык влажный, чистый. АД 115/70 мм рт.ст., тоны сердца приглушены, ритмичные, пульс 80 уд/мин. Дыхание жесткое, проводится по всем отделам, частота - 18 в минуту. Живот не увеличен, при пальпации мягкий, безболезненный, перистальтика кишечника выслушивается. Печень, селезенка не увеличены. Периферических отеков нет. Мочеиспускание свободное. ФК ХСН - I по NYHA. По данным Эхо-КГ: уменьшилась ФВ ЛЖ, увеличились КДР ЛЖ, КСР ЛЖ, толщина МЖП и ЗСЛЖ.
Таким образом, технико-экономическая эффективность «Способ прогнозирования развития подострой антрациклин-опосредованной кардитоксичности у онкологических пациентов» позволяет своевременно оценить вероятность развития АОК и выделить группу риска больных, для которых будет применен персонифицированный подход с индивидуальным планом: мониторинга кардиотоксичности, частоты осмотров терапевта, кардиолога, выполнения ЭКГ и ЭхоКГ, своевременного назначения оптимальной сопроводительной кардиотропной терапии.
Заявляемый способ позволяет оперативно составить прогноз развития АОК еще до начала терапии и может способствовать предотвращению преждевременной смертности пациенток по причине сердечно-сосудистых осложнений.
СПИСОК ЛИТЕРАТУРЫ
1. Costello В.Т., Roberts T.J., Elowden E.J. et al. Exercise Attenuates Cardiotoxicity of Anthracycline Chemotherapy Measured by Global Longitudinal Strain. J Am Coll Cardiol CardioOnc, 2019; 1(2): 298-301.
2. Johnson R., Shabalala S., Louw J. et al. Aspalathin Reverts Doxorubicin-Induced Cardiotoxicity through Increased Autophagy and Decreased Expression of p53/mTOR/p62 Signaling. Molecules. 2017; 22(10): E1589.
3. Cai F., Luis M.A.F., Lin X. et al. Anthracycline-induced cardiotoxicity in the chemotherapy treatment of breast cancer: Preventive strategies and treatment. Mol Clin Oncol. 2019; 11(1): 15-23.
4. Rocca C., Pasqua Т., Cerra M.C. et al. Cardiac Damage in Anthracyclines Therapy: Focus on Oxidative Stress and Inflammation. Antioxid Redox Signal. 2020; 1-48.
5. Wenningmann N., Knapp M., Ande A. et al. Insights into Doxorubicin-induced Cardiotoxicity: Molecular Mechanisms, Preventive Strategies, and Early Monitoring. Mol Pharmacol. 2019; 96(2): 219-232.
6. Curigliano G., Lenihan D., Fradley M. et al. Management of cardiac disease in cancer patients throughout oncological treatment: ESMO consensus recommendations. Ann Oncol. 2020; 31(2): 171-190.
7. Armstrong G.T., Plana J.C., Zhang N. et al. Screening adult survivors of childhood cancer for cardiomyopathy: comparison of echocardiography and cardiac magnetic resonance imaging. J. Clin. Oncol. 2012; 30: 2876-2884.
8. Dorosz J.L., Lezotte D.C., Weitzenkamp D.A. et al. Performance of 3-dimensional echocardiography in measuring left ventricular volumes and ejection fraction: a systematic review and meta-analysis. J. Am. Coll. Cardiol. 2012; 59(20): 1799-1808.
9. Negishi K., Negishi Т., Hare J.L., Haluska B.A., Plana J.C., Marwick Т.Н. Independent and incremental value of deformation indices for prediction of trastuzumab-induced cardiotoxicity. J. Am Soc Echocardiogr. 2013; 26(5): 493-498.
10. Ky В., Putt M., Sawaya H. et al. Early increases in multiple biomarkers predict subsequent cardiotoxicity in patients with breast cancer treated with doxorubicin, taxanes, and trastuzumab. J. Am. Coll. Cardiol. 2014; 63(8): 809-816.
11. Knowles D.A., Burrows C.K., Blischak J.D. et al. Determining the genetic basis of anthracycline-cardiotoxicity by molecular response QTL mapping in induced cardiomyocytes. Elife. 2018; 7: e33480.
12. Тепляков А.Т., Гракова E.B., Шилов C.H., Березикова Е.Н., Попова А.А., Неупокоева М.Н., Копьева К.В. Способ прогнозирования антрациклин-индуцированной кардиотоксичности у женщин с раком молочной железы // Патент Рос. Федерация №2714683. Опубл 19.02.2020, Бюл. №5. - 9 с.
13. Гвалдин Д.Ю., Омельчук Е.П., Новикова И.А. и др. Исследование генетических полиморфизмов, ассоциированных с развитием антрациклин-опосредованной каридиотоксичности, у пациенток с онкопатологией молочной железы. Современные проблемы науки и образования. 2019; 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования антрациклин-индуцированной кардиотоксичности у женщин с раком молочной железы | 2019 |
|
RU2714683C1 |
| Способ прогнозирования прогрессирования хронической сердечной недостаточности у пациенток с раком молочной железы после химиотерапии антрациклинами | 2022 |
|
RU2790788C1 |
| Способ прогнозирования развития кардиотоксичности у пациенток с раком молочной железы в течение 12 месяцев после химиотерапии препаратами антрациклинового ряда | 2018 |
|
RU2680139C1 |
| Способ персонифицированного отбора больных с антрациклин-индуцированной кардиомиопатией после полихимиотерапии рака молочной железы для эффективного лечения карведилолом | 2021 |
|
RU2778612C1 |
| Способ прогнозирования прогрессирования хронической сердечной недостаточности, индуцированной антрациклинами, у пациенток с раком молочной железы в течение 24 месяцев | 2022 |
|
RU2793672C1 |
| СПОСОБ ПРОФИЛАКТИКИ АНТРАЦИКЛИНОВОЙ КАРДИОТОКСИЧНОСТИ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2546399C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КУМУЛЯТИВНОЙ КАРДИОТОКСИЧНОСТИ ХИМИОТЕРАПЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2012 |
|
RU2510240C2 |
| Способ прогнозирования развития кардиотоксичности у больных HER2 позитивным раком молочной железы исходно низкого/умеренного сердечно-сосудистого риска, получающих таргетную терапию трастузумабом после антрациклин-содержащей химиотерапии | 2020 |
|
RU2741371C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2014 |
|
RU2545899C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ СУБКЛИНИЧЕСКОЙ СИСТОЛИЧЕСКОЙ ДИСФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА У ПАЦИЕНТОВ С ХРОНИЧЕСКИМ ЛИМФОЛЕЙКОЗОМ В ПРОЦЕССЕ ХИМИОТЕРАЦИИ В РЕЖИМЕ FCR | 2019 |
|
RU2727003C1 |
Изобретение относится к области медицины, в частности к кардиоонкологии и медицинской генетике, и предназначено для прогнозирования развития подострой антрациклин-опосредованной кардиотоксичности у онкологических пациентов. Проводят генотипирование полиморфизма rs28714259 на матрице ДНК, выделенной из крови или буккального эпителия. При наличии генотипов G/A или А/А прогнозируют высокий риск развития подострой антрациклин-опосредованной кардиотоксичности. Изобретение обеспечивает создание недорогого, простого в исполнении, высокоинформативного способа прогнозирования риска антрациклин-опосредованной кардиотоксичности у онкологических больных до применения антибиотиков антрациклинового ряда. 4 табл., 3 пр.
Способ прогнозирования развития подострой антрациклин-опосредованной кардиотоксичности у онкологических пациентов, заключающийся в том, что проводят генотипирование методом полимеразной цепной реакции полиморфизма rs28714259 на матрице ДНК, выделенной подходящим способом из крови или буккального эпителия, и при наличии генотипов G/A или А/А прогнозируют высокий риск развития подострой антрациклин-опосредованной кардиотоксичности.
| KNOWLES D.A | |||
| et al | |||
| Determining the genetic basis of anthracycline-cardiotoxicity by molecular response QTL mapping in induced cardiomyocytes | |||
| eLife | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ прогнозирования антрациклин-индуцированной кардиотоксичности у женщин с раком молочной железы | 2019 |
|
RU2714683C1 |
| Способ прогнозирования развития кардиотоксичности у пациенток с раком молочной железы в течение 12 месяцев после химиотерапии препаратами антрациклинового ряда | 2018 |
|
RU2680139C1 |
Авторы
Даты
2021-03-15—Публикация
2020-07-27—Подача