Область техники, к которой относится изобретение
Настоящее изобретение относится к мультиспецифическим антигенсвязывающим молекулам, их применениям и т.п.
Предпосылки создания изобретения
Антитела привлекают внимание в качестве терапевтических средств благодаря их высокой стабильности в плазме и небольшому количеству нежелательных реакций (непатентные документы 1 и 2). Известно, что антитела индуцируют не только антигенсвязывающую активность, агонистическое действие и антагонистическое действие, но также и опосредуемые эффектором виды цитотоксической активности (которые называют также эффекторными функциями), такие как антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), антителозависимый клеточный фагоцитоз (ADCP) и комплементзависимая цитотоксичность (CDC), и обладают противоопухолевыми действиями в отношении раковых клеток (непатентный документ 3). ADCC представляет собой обусловленную эффекторными клетками цитотоксичность в отношении «нагруженных» антителом раковых клеток-мишеней посредством связывания Fc-области антитела с Fc-рецептором, присутствующим на эффекторных клетках, таких как NK-клетки и макрофаги. Комплекс системы комплемента связывается с комплементсвязывающим сайтом, присутствующим в структуре антитела. CDC представляет собой цитотоксичность, которая является результатом клеточной деструкции, при которой приток воды и ионов в клетки усиливается благодаря образованию пор на клеточной мембране «нагруженных» антителом клеток с помощью компонентов комплемента, присутствующих в комплексе. Создан ряд терапевтических антител с установленными очень высокими противоопухолевыми действиями в качестве фармацевтических средств для лечения рака (непатентный документ 4); и хотя установлено, что известные терапевтические антитела обладают очень высокими действиями, достигаемый при применении указанных антител исход лечения все еще остается неудовлетворительным.
Для того чтобы антитело обладало ADCC, ADCP и CDC, необходимо наличие Fc-области в антителе и присутствие рецептора для антитела (FcγR) на эффекторных клетках, таких как NK-клетки и макрофаги, и различных компонентов комплемента, пригодных для связывания. У человека описаны изоформы FcγRIa, FcγRIIa, FcγRIIb, FcγRIIIa и FcγRIIIb в качестве семейства белка FcγR, кроме того, описаны соответствующие аллотипы (непатентный документ 5). Среди указанных изоформ FcγRIa, FcγRIIa и FcγRIIIa несут активирующий мотив на основе тирозина иммунорецептора (ITAM) во внутриклеточном домене, и передают сигналы активации. С другой стороны, только FcγRIIb несет домен, известный как ингибирующий мотив на основе рецептора тирозина (ITIM), во внутриклеточном домене и передает сигналы ингибирования. Известно, что каждый из FcγR передает сигналы посредством перекрестного сшивания иммунными комплексами и т.п. (непатентный документ 6). Когда антитела фактически проявляют эффекторную функцию на раковых клетках, FcγR на мембране эффекторной клетки образуют кластеры на Fc-областях нескольких антител, связанных на мембране раковой клетки, и сигналы активации передаются эффекторными клетками. В результате проявляется цитоцидное действие, но поскольку FcγR перекрестно сшиваются только на эффекторных клетках, которые в это время присутствуют вблизи раковых клеток, установлено, что активация иммунитета происходит локально в раковых клетках (непатентный документ 7).
Встречающиеся в естественных условиях иммуноглобулины связываются с антигенами в их вариабельных областях и связываются с рецепторами, такими как FcγR, FcRn, FcαR и FcεR, и комплементами в их константных областях. FcRn является одной из связывающихся молекул, которые взаимодействуют с Fc-областью IgG, и установлено, что, поскольку каждая из тяжелых цепей антитела связывается с одной молекулой FcRn, две молекулы FcRn связываются с одном молекулой антитела IgG-типа. Однако, в отличие от FcRn и др., FcγR взаимодействует с шарнирной областью антитела и СН2-доменом, и только одна молекула FcγR связывается с одной молекулой антитела IgG-типа (непатентный документ 8). Кроме того, каноническое встречающееся в естественных условиях антитело IgG-типа распознает и связывает единичный эпитоп через его вариабельную область (Fab); поэтому оно может связываться только с одним антигеном. С другой стороны, известно, что с раком и воспалением связано много типов белков и поэтому может иметь место перекрестная помеха между белками. Например, известно, что несколько воспалительных цитокинов (TNF, IL1 и IL6) могут участвовать в иммунологических заболеваниях (непатентный документ 9). Кроме того, известно, что одним из механизмов приобретения устойчивости рака к лекарственным средствам является активация других рецепторов (непатентный документ 10). В таких случаях канонические антитела, которые распознают единичный эпитоп, не могут ингибировать несколько белков.
Антитела (биспецифические антитела), одна молекула которых связывается с двумя или большим количеством типов антигенов, изучены в качестве молекул, которые ингибируют несколько мишеней. Можно получать связывающие активности с двумя различными антигенами (первый антиген и второй антиген) путем модификации встречающихся в естественных условиях антител IgG-типа (непатентный документ 11). Таким образом, можно не только нейтрализовать два или большее количество типов антигенов с помощью одной молекулы, но также усиливать противоопухолевую активность с помощью перекрестных связей между клетками, которые обладают цитотоксической активностью, и раковыми клетками. К настоящему времени в качестве молекулярных форматов биспецифического антитела описаны молекула, содержащая антигенсвязывающий сайт, добавленный к N- или С-концу антитела (DVD-Ig и scFv-IgG), молекула, имеющая различные последовательности двух Fab-областей антитела (содержащее общую L-цепь биспецифическое антитело и гибридная гибридома), молекула, в которой одна область Fab распознает два антигена (IgG два-в-одном), и молекула, имеющая петлю СН3-области в качестве нового антигенсвязывающего сайта (Fcab) (непатентный документы 12 и 13). Поскольку все биспецифические антитела взаимодействуют на их Fc-областях с FcγR, эффекторные функции антитела сохраняются. Таким образом, биспецифическое антитело связывается с любым антигеном, который оно распознает, и одновременно связывается с FcγR, и обусловливает ADCC-активность в отношении клеток, экспрессирующих антиген.
Если все антигены, распознаваемые биспецифическим антителом, специфически экспрессируются при раке, то биспецифическое антитело обладает цитотоксическим действием в отношении раковых клеток, когда оно связывается с любым из антигенов. Таким образом, по сравнению с каноническим фармацевтическим антителом, которое распознает один антиген, можно ожидать, что указанное антитело будет обладать более эффективным противоопухолевым действием. Однако в случае, когда любой один из антигенов, распознаваемых биспецифическим антителом, экспрессируется в здоровых тканях или клетках, экспрессируемых на иммуноцитах, то имеет место повреждение здоровых тканей или высвобождение цитокинов в результате перекрестного связывания с FcγR (непатентный документ 14). В результате индуцируются сильные нежелательные реакции.
Перенаправляющее Т-клетку антитело, которое использует цитотоксичность, активируя Т-клетки в качестве эффекторных клеток, что является механизмом его противоопухолевого действия, известно с 1980-х годов (непатентные документы 15, 16 и 17). В отличие от антител, которые используют ADCC, активируя NK-клетки или макрофаги в качестве эффекторных клеток, что является механизмом их противоопухолевого действия, перенаправляющее Т-клетки антитело представляет собой антитело против любой одной из субъединиц, из которых состоит комплекс Т-клеточного рецептора (TCR) на Т-клетках, и представляет собой специфическое биспецифическое антитело, которое содержит антитело, связывающееся с эпсилон-цепью CD3, и антитело, связывающееся с антигеном на раковой клетке-мишени. Т-клетки приходят в контакт с раковыми клетками посредством одновременного связывания эпсилон-цепи CD3 и ракового антигена с помощью перенаправляющего Т-клетки антитела. Это в результате приводит к противоопухолевому действию в отношении раковых клеток благодаря цитотоксической активности, обусловленной Т-клетками.
Катумаксомаб, известный в качестве перенаправляющего Т-клетки антитела, связывается на посредством двух Fab с раковым антигеном (ЕрСАМ) и с CD3ε- (CD3-эпсилон) цепью, экспрессируемой на Т-клетках. Катумаксомаб индуцирует опосредуемую Т-клетками цитотоксическую активность путем одновременного связывания с раковым антигеном и CD3ε и индуцирует цитотоксическую активность, опосредуемую антигенпрезентирующими клетками, такими как NK-клетки и макрофаги, путем одновременного связывания с раковым антигеном и FcγR. Благодаря указанным двум видам цитотоксической активности катумаксомаб обладает высоким терапевтическим действием в отношении злокачественных асцитов при внутрибрюшинном введении и поэтому его применение разрешено в Европе (непатентный документ 18). Кроме того, известны случаи, когда по имеющимся сведениям введение катумаксомаба приводит к образованию реактивных в отношении раковых клеток антител, что четко демонстрирует индукцию приобретенного иммунитета (непатентный документ 19). С учетом указанного результата привлекли внимание антитела, которые обладают как опосредуемой Т-клетками цитотоксической активностью, так и опосредуемыми FcγR видами активности таких клеток как NK-клетки или макрофаги (указанные антитела обозначают как трехфункциональные антитела), поскольку для них можно ожидать сильное противоопухолевое действие и индукцию приобретенного иммунитета.
Однако трехфункциональные антитела связываются одновременно с CD3ε и FcγR даже в отсутствии ракового антигена и поэтому обеспечивают перекрестное сшивание экспрессирующих CD3ε Т-клеток с экспрессирующими FcγR клетками даже при отсутствии в окружении раковых клеток, что приводит к производству в больших количествах различных цитокинов. Указанная независящая от ракового антигена индукция производства различных цитокинов в настоящее время ограничивает применении трехфункциональных антител внутрибрюшинным путем (непатентный документ 20). Трехфункциональные антитела очень трудно вводить системно из-за серьезных напоминающих «цитокиновый шторм» нежелательных реакций. Фактически, на фазе I клинического испытания было установлено, что максимальной переносимой дозой при системном введении катумаксомаба пациентам с немелкоклеточным раком легкого является очень низкая доза, составляющая 5 мкг/организм, и что введение более высокой дозы вызывает серьезные нежелательные реакции, (непатентный документ 21).
Так, созданные с помощью общепринятых методик биспецифические антитела могут связываться с обоими антигенами, при этом первый антиген представляет собой раковый антиген (ЕрСАМ), а второй антиген представляет собой CD3ε, одновременно с этим они связываются с FcγR; и поэтому с учетом их молекулярной структуры невозможно избежать нежелательных реакций, вызываемых одновременным связыванием с FcγR и вторым антигеном CD3ε.
При этом, в отличие от катумаксомаба, BiTE (биспецифический активатор (проводник) Т-клеток) не содержит сайт связывания Fcγ-рецептора и поэтому у него отсутствует перекрестное сшивание с рецепторами, которые экспрессируются на Т-клетках и таких клетках, как NK-клетки и макрофаги, независимым от ракового антигена образом. Так, было продемонстрировано, что BiTE не вызывает независимую от ракового антигена индукцию цитокинов, которая обнаружена при введении катумаксомаба. Однако, поскольку BiTE представляет собой модифицированную низкомолекулярную молекулу антитела без Fc-области, проблема заключается в том, что время ее полужизни в крови после введения пациенту, существенно короче, чем в случае антител IgG-типа, которые обычно применяют в качестве терапевтических антител. Фактически, согласно опубликованным данным время полужизни в крови BiTE при его применении in vivo составляет примерно несколько часов (непатентные документы 22 и 23). При проведении клинических испытаний блинатумомаба его вводили путем непрерывной внутривенной инфузии с помощью мининасоса. Такой метод введения не только чрезвычайно неудобен для пациентов, но также имеет потенциальный риск медицинских осложнений, связанных с неисправностью устройства или т.п. Таким образом, нельзя считать, что указанный метод введения является желательным.
В последние годы применение Fc-области с пониженной способностью связываться с FcγR позволило сохранять сильную противоопухолевую активность, свойственную BiTE, и очень хорошие характеристики безопасности без индукции «цитокинового шторма» независимым от ракового антигена образом, и обеспечило создание новых полипептидных структур с продолжительным временем полужизни в крови (патентный документ 1).
С другой стороны, когда происходит экспрессия созданного с помощью общепринятых методик биспецифического антитела, то экспрессируются два типа Н-цепей и два типа L-цепей, что может приводить к получению десяти комбинаций. Из них только одна из полученных комбинаций обладает представляющей интерес специфичностью связывания. Таким образом, для получения представляющего интерес биспецифического антитела одно представляющее интерес антитело должны быть выделено из десяти типов антител, такой путь является очень неэффективным и сложным.
В качестве решения указанной проблемы был описан метод, заключающийся в предпочтительном секретировании IgG с гетеродимерной комбинацией Н-цепей, например, с комбинацией Н-цепи против антигена А и Н-цепи против антигена Б, посредством интродукции аминокислотных замен в СН3-область Н-цепи IgG (патентные документы 2, 3, 4, 5, 6, 7 и непатентные документы 24 и 25). В качестве таких методов описаны методы на основе создания физического нарушения, т.е., «выступа» и «впадины», и метод на основе отталкивания электрических зарядов.
Для получения представляющей интерес молекулы с повышенной эффективностью, описаны методы, основанные на применении L-цепей, которые могут связываться с двумя различными антигенами, даже хотя L-цепи имеют одинаковую аминокислотную последовательность (патентные документы 8 и 9). Однако аффинность к антигену может значительно уменьшаться при применении общих L-цепей и трудно найти общие L-цепи, при использовании которых сохраняется аффинность к антигену.
Блинатумомаб в виде BiTE одобрен для применения при остром лимфобластном лейкозе (ALL) и также проходит тестирование в клинических испытаниях для лечения рака крови, такого как неходжскинская лимфома (NHL) и хронический лимфоцитарный лейкоз (CLL). Начаты также клинические испытания соединения AMG330, представляющего собой BiTE, мишенью которого является CD33, для оценки его действия в отношении острого миелоидного лейкоза (AML). Кроме того, в разработке находятся BiTE против солидных опухолей. Проходят клинические испытания такие соединения, как AMG211, представляющее собой BiTE, мишенью которого является СЕА, AMG110, представляющее собой BiTE, мишенью которого является ЕрСАМ, AMG212, представляющее собой BiTE, мишенью которого является PSMA, и т.д. Однако чувствительность солидных опухолей к BiTE остается недоказанной (непатентный документ 26).
В последние годы продемонстрировано, что иммунотерапевтические агенты, представителями которых являются ингибиторы, мишенями которых являются молекулы иммунных контрольных точек, такие как CTLA-4, PD-1 и PD-L1, обладают эффективностью в качестве лекарственных средств в клинических условиях. Однако указанные фармацевтические агенты не обладают эффективностью для любого пациента, и поэтому требуется дальнейшее повышение их эффективности в качестве лекарственных средств Касательно совместного применения нескольких иммунотерапии, то установлено, что совместное применения ниволумаба и ипилимумаба позволяло достигать повышенной эффективности в качестве лекарственного средства против меланомы по сравнения с индивидуальным применением ипилимумаба (непатентный документ 27).
Перечень процитированных документов
[Патентные документы]
[Патентный документ 1] WO 2012/073985;
[Патентный документ 2] WO 96/27011;
[Патентный документ 3] WO 2006/106905;
[Патентный документ 4] WO 2007/147901;
[Патентный документ 5] WO 2009/089004;
[Патентный документ 6] WO 2010/129304;
[Патентный документ 7] WO 2013/065708;
[Патентный документ 8] WO 98/050431;
[Патентный документ 9] WO 2006/109592.
[Непатентные документы]
[Непатентный документ 1] Nat. Biotechnol. 23, 2005, сс. 1073-1078;
[Непатентный документ 2] Eur J Pharm Biopharm. 59 (3), 2005, сс. 389-396;
[Непатентный документ 3] Drug Des Devel Ther 3, 2009, сс. 7-16;
[Непатентный документ 4] Clin Cancer Res. 16 (1), 2010, сс. 11-20;
[Непатентный документ 5] Immunol. Lett. 82, 2002, сс. 57-65;
[Непатентный документ 6] Nat. Rev. Immunol. 8, 2008, сс. 34-47;
[Непатентный документ 7] Ann. Rev. Immunol. 6, 1988, сс. 251-281;
[Непатентный документ 8] J. Bio. Chem., 276, 2001, сс. 16469-16477;
[Непатентный документ 9] Nat. Biotech., 28, 2011, сс. 502-510;
[Непатентный документ 10] Endocr Relat Cancer 13, 2006, сс. 45-51;
[Непатентный документ 11] MAbs. 1 марта 2012 г., 4(2);
[Непатентный документ 12] Nat. Rev. 10, 2010, сс. 301-316;
[Непатентный документ 13] Peds 23(4), 2010, сс. 289-297;
[Непатентный документ 14] J. Immunol. 163(3), 1 августа 1999 г., сс. 1246-1252;
[Непатентный документ 15] Nature 314 (6012), 1985, сс. 628-631;
[Непатентный документ 16] Int J Cancer 41 (4), 1988, сс. 609-615;
[Непатентный документ 17] Proc Natl Acad Sci USA 83 (5), 1986, сс. 1453-1457;
[Непатентный документ 18] Cancer Treat Rev. 36(6), октябрь 2010 г., сс. 458-467;
[Непатентный документ 19] Future Oncol. 8(1), январь 2012 г., сс. 73-85;
[Непатентный документ 20] Cancer Immunol Immunother. 56(9), 2007, сс. 1397-1406;
[Непатентный документ 21] Cancer Immunol Immunother. 56 (10), 2007, сс. 1637-1644;
[Непатентный документ 22] Cancer Immunol Immunother. 55(5), 2006, сс. 503-514;
[Непатентный документ 23] Cancer Immunol Immunother. 58(1), 2009, сс. 95-109;
[Непатентный документ 24] Protein Engineering, т. 9, 1996, сс. 617-621;
[Непатентный документ 25] Nature Biotechnology, т. 16, 1998, сс. 677-681;
[Непатентный документ 26] Immunological Reviews, т. 270, 2016, сс. 193-208;
[Непатентный документ 27] N. J. Med., т. 373, 2015, сс. 23-34.
Краткое изложение сущности изобретения
Задачи, положенные в основу настоящего изобретения
Настоящее изобретение было создано с учетом вышеуказанных обстоятельств. В основу настоящего изобретения была положена задача создать противораковые агенты, содержащие в качестве активного ингредиента мультиспецифические антигенсвязывающие молекулы, которые обладают способностью приводить в контакт Т-клетки с раковыми клетками-мишенями и которые можно применять для лечения рака, используя цитотоксическую активность Т-клеток против раковых тканей-мишеней, содержащих экспрессирующие глипикан 3 клетки, и которые представляют собой молекулярные формы, которые можно получать с высокой эффективностью. Другой задачей настоящего изобретения было разработать комбинированные терапии с использованием мультиспецифических антигенсвязывающих молекул и других фармацевтических агентов.
Средства решения указанных задач
При создании настоящего изобретения описана L-цепь, общая с доменом, который содержит связывающуюся с глипиканом 3 вариабельную область антитела, и доменом, который содержит связывающуюся с комплексом Т-клеточного рецептора вариабельную область антитела, при этом общая L-цепь обладает способностью повышать аффинность к обоим антигенам. Это обеспечивает получение молекулярных форм с высокой эффективностью, и дополнительно описаны новые мультиспефические антигенсвязывающие молекулы, которые сохраняют сильную противоопухолевую активность, характерную для перенаправляющих Т-клетки антител, таких как BiTE, и обладают очень хорошими характеристиками безопасности, не индуцируя «цитокиновый шторм» независимым от ракового антигена образом, а также обладают продолжительным временем полужизни в крови. Кроме того, при создании настоящего изобретения установлено, что мультиспецифические антигенсвязывающие молекулы, которые содержат общие L-цепи, нацелены на экспрессирующие глипикан 3 раковые клетки и вызывают цитотоксичность.
На основе указанного открытия при создании настоящего изобретения установлено, что мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, вызывают повреждение раковых тканей, которые содержат экспрессирующие глипикан 3 раковые клетки. При создании настоящего изобретения были выявлены противораковые агенты, которые содержат в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу; предложены способы лечения или предупреждения рака путем совместного применения мультиспецифической антигенсвязывающей молекулы и другого противоракового агента; мультиспецифические антигенсвязывающие молекулы, противораковые агенты или фармацевтические композиции, содержащие комбинацию мультиспецифической антигенсвязывающей молекулы и противоракового агента, каждый из которых применяют в комбинированных терапиях.
Конкретно, в настоящем изобретении предложены:
[1] Противораковый агент, содержащий в качестве активного ингредиента биспецифическое антитело, описанное ниже в одном из подпунктов (а)-(в), содержащее вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3, и вариабельную область антитела, которая обладает связывающей активностью в отношении CD3:
(а) биспецифическое антитело, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[2] Противораковый агент, содержащий в качестве активного ингредиента биспецифическое антитело, которое содержит Н-цепь антитела, имеющую SEQ ID NO: 385, которая обладает связывающей активностью в отношении глипикана 3, Н-цепь антитела, имеющую SEQ ID NO: 402, которая обладает связывающей активностью в отношении CD3, и общие L-цепи, имеющие SEQ ID NO: 410.
[3] Противораковый агент по п. [1] или п. [2], где рак представляет собой позитивный по глипикану 3 рак.
[4] Противораковый агент по п. [3], где позитивный по глипикану 3 рак представляет собой рак, при котором количество антигенов глипикана 3 на клеточной поверхности на клетку составляет 100 или более.
[5] Противораковый агент по одному из п.п. [1]-[4], где рак представляет собой любой рак, выбранный из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, опухоли пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
[6] Противораковый агент по одному из п.п. [1]-[5], предназначенный для лечения пациента, который имеет рак, устойчивый к лечению ингибитором иммунных контрольных точек.
[7] Фармацевтическая композиция, предназначенная для применения в комбинации с другим противораковым агентом, где фармацевтическая композиция содержит в качестве активного ингредиента биспецифическое антитело, указанное ниже в любом одном из подпунктов (а)-(в), которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3:
(а) биспецифическое антитело, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[8] Фармацевтическая композиция, содержащая в качестве активного ингредиента биспецифическое антитело, которое содержит Н-цепь антитела, имеющую SEQ ID NO: 385, которая обладает связывающей активностью в отношении глипикана 3, Н-цепь антитела, имеющую SEQ ID NO: 402, которая обладает связывающей активностью в отношении CD3, и общие L-цепи, имеющие SEQ ID NO: 410, где фармацевтическая композиция предназначена для применения в комбинации с другим противораковым агентом.
[9] Фармацевтическая композиция по п. [7] или п. [8], где биспецифическое антитело вводят одновременно с указанным другим противораковым агентом.
[10] Фармацевтическая композиция по п. [7] или п. [8], где биспецифическое антитело вводят до или после введения указанного другого противоракового агента.
[11] Фармацевтическая композиция по одному из п.п. [7]-[10], где указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[12] Фармацевтическая композиция по п. [11], где химиотерапевтический агент представляет собой антиметаболит, растительный алкалоид или соединение платины.
[13] Фармацевтическая композиция по п. [11], где активирующий Т-клетки агонистический агент представляет собой агонистическое антитело против TNFRSF.
[14] Фармацевтическая композиция по п. [11], где ингибитор иммунных контрольных точек представляет собой антитело к PD1, антитело к PDL1, антитело к TIM3 или антитело к LAG3.
[15] Фармацевтическая композиция по п. [11], где ингибитор ангиогенеза представляет собой антитело к VEGFR2.
[16] Агент для индукции цитотоксичности, агент для подавления пролиферации клеток, агент для ингибирования пролиферации клеток, агент для активации иммунного ответа, агент для лечения рака или агент для предупреждения рака который содержит фармацевтическую композицию по одному из п.п. [7]-[15].
[17] Противораковый агент по п. [1], в котором CDR1, CDR2 и CDR3 представляют собой CDR1-, CDR2- и CDR3-участки, определенные на основе нумерации по Кэботу.
В настоящем изобретении предложены также:
[2-1] Противораковый агент, содержащий в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу, которая содержит:
(1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3,
(2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и
(3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора,
в которой вариабельные области L-цепи, содержащиеся в вариабельной области, указанной в подпункте (1), и в вариабельной области, указанной в подпункте (2), имеют общую аминокислотную последовательность; где мультиспецифическая антигенсвязывающая молекула обладает цитотоксической активностью, эквивалентной или более высокой по сравнению с активностью биспецифического антитела GPC3_ERY22_rCE115, которое содержит домен, связывающий глипикан 3, содержащий SEQ ID NO: 47 и 48, и домен, связывающий комплекс Т-клеточного рецептора, содержащий SEQ ID NO: 49 и 50.
[2-2] Противораковый агент по п. [2-1], цитотоксическая активность которого представляет собой зависимую от Т-клетки цитотоксическую активность.
[2-3] Противораковый агент по п. [2-1] или п. [2-2], в котором связывающая активность в отношении комплекса Т-клеточного рецептора представляет собой связывающую активность в отношении Т-клеточного рецептора.
[2-4] Противораковый агент по одному из п.п. [2-1]-[2-3], в котором связывающая активность в отношении комплекса Т-клеточного рецептора представляет собой связывающую активность в отношении CD3ε-цепи.
[2-5] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельная область антитела, указанная в подпункте (1) в п. [2-1], представляет собой вариабельную область антитела, которая содержит любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (a1)-(a5), или функционально эквивалентную вариабельную область антитела:
(a1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40;
(а2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197;
(а3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206;
(а4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и
(а5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215.
[2-6] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельная область антитела, указанная в подпункте (2) в п. [2-1] представляет собой вариабельную область антитела, которая содержит любую одну из комбинаций аминокислотных последовательностей CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (б1)-(б15), или функционально эквивалентную вариабельную область антитела:
(б1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 52;
(б2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103;
(б3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122;
(б4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128;
(б5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129;
(б6) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132;
(б7) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(б8) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(б9) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(б10) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(б11) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 421;
(б12) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424;
(б13) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 426;
(б14) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 429; и
(б15) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 430.
[2-7] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [2-1], представляют собой вариабельные области антитела, которые содержат любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (в1)-(в19), или функционально эквивалентные вариабельные области антитела:
(в1) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 52;
(в2) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 421;
(в3) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 426;
(в4) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 429;
(в5) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 430;
(в6) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128;
(в7) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(в8) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(в9) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(в10) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(в11) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(в12) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(в13) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(в14) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(в15) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103;
(в16) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122;
(в17) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129;
(в18) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132; и
(в19) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424.
[2-8] Противораковый агент по одному из п.п. [2-5]-[2-7], в котором CDR1, CDR2 и CDR3 представляют собой CDR1-, CDR2- и CDR3-участки, определенные на основе нумерации по Кэботу.
[2-9] (a1) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 40;
(а2) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 197;
(а3) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206;
(а4) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 211; и
(а5) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 215.
[2-10] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельная область антитела, указанная в подпункте (2) в п. [2-1], представляет собой вариабельную область антитела, которая содержит любую одну из вариабельных областей Н-цепи, выбранную из указанных ниже в подпунктах (б1)-(б15), или функционально эквивалентную вариабельную область антитела:
(б1) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 52;
(б2) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 103;
(б3) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 122;
(б4) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 128;
(б5) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 129;
(б6) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 132;
(б7) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 142;
(б8) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 144;
(б9) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 164;
(б10) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 168;
(б11) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 421;
(б12) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 424;
(б13) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 426;
(б14) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 429; и
(б15) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 430.
[2-11] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [2-1], представляют собой вариабельные области антитела, которые содержат любую одну из комбинацией вариабельных областей Н-цепи, выбранную из указанных ниже в подпунктах (в1)-(в19), или функционально эквивалентные вариабельные области антитела:
(в1) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 52;
(в2) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 421;
(в3) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 426;
(в4) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 429;
(в5) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 430;
(в6) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 197; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 128;
(в7) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 142;
(в8) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 144;
(в9) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 164;
(в10) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 168;
(в11) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 142;
(в12) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 144;
(в13) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 164;
(в14) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 168;
(в15) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 103;
(в16) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 122;
(в17) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 129;
(в18) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 132; и
(в19) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], которая имеет аминокислотную последовательность SEQ ID NO: 424.
[2-12] Противораковый агент по одному из п.п. [2-1]-[2-11], в котором общая L-цепь, указанная в п. [2-1], представляет собой общую L-цепь, которая содержит любую одну из комбинаций CDR1, CDR2 и CDR3, выбранную из указанных ниже в подпунктах (г1)-(г11), или функциональный эквивалент общей L-цепи:
(г1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(г2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(г3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(г4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 301;
(г5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 302;
(г6) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 304;
(г7) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 306;
(г8) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 307;
(г9) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 309;
(г10) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 310; и
(г11) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 319.
[2-13] Противораковый агент по одному из п.п. [2-1]-[2-11], в котором вариабельная область L-цепи, указанная в п. [2-1], представляет собой вариабельную область любой одной из аминокислотных последовательностей L-цепи, выбранных из указанных ниже в подпунктах (г1)-(г11):
(г1) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 53;
(г2) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 223;
(г3) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 299;
(г4) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 301;
(г5) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 302;
(г6) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 304;
(г7) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 306;
(г8) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 307;
(г9) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 309;
(г10) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 310; и
(г11) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 319.
[2-14] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [2-1], и вариабельная область общей L-цепи представляют собой вариабельные области антитела, содержащие любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи и CDR1, CDR2 и CDR3 L-цепи, выбранную из указанных ниже в подпунктах (д1)-(д25), или функционально эквивалентные вариабельные области антитела:
(д1) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д2) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д3) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 310;
(д4) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 319;
(д5) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д6) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д7) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д8) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д9) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д10) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д11) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д12) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям SEQ ID NO: 223;
(д13) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д14) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д15) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д16) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 301;
(д17) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 302;
(д18) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 304;
(д19) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 306;
(д20) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 307;
(д21) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 309;
(д22) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д23) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д24) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53; и
(д25) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53.
[2-15] Противораковый агент по одному из п.п. [2-1]-[2-4], в котором вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [2-1], и вариабельная область общей L-цепи представляют собой вариабельные области антитела, содержащие любую одну из комбинаций вариабельных областей, выбранные из указанных ниже в подпунктах (e1)-(e26), или функционально эквивалентные вариабельные области антитела:
(e1) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е2) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(е3) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 310;
(е4) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 319;
(е5) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е6) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 144; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е7) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 164; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е8) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е9) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е10) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(e11) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 144; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(e12) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 164; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е13) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(e14) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(e15) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(e16) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область It-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 301;
(e17) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 302;
(e18) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 304;
(e19) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 306;
(е20) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 307;
(е21) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 309;
(е22) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 122; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е23) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 129; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е24) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 132; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е25) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [2-1], и идентична аминокислотной последовательности SEQ ID NO: 424; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53; и
(е26) мультиспецифическая антигенсвязывающая молекула, которая связывается с эпитопом, перекрывающимся с каждым из эпитопов глипикана 3, и комплекса Т-клеточного рецептора, который связывается мультиспецифической антигенсвязывающей молекулой, указанной в одном из подпунктов (e1)-(e25), и которая имеет общую L-цепь.
[2-16] Противораковый агент по одному из п.п. [2-1]-[2-15], в котором Fc-область, указанная в подпункте (3) в п. [2-1], представляет собой Fc-область с аминокислотной мутацией любой из образующих Fc-область аминокислотных последовательностей SEQ ID NO: 23-26 (IgG1-IgG4).
[2-17] Противораковый агент по п. [2-16], в котором Fc-область, указанная в подпункте (3) в п. [2-1], представляет собой Fc-область с мутацией по меньшей мере одной аминокислоты, выбранной из аминокислот в следующих аминокислотных положениях, указанных согласно EU-нумерации: положение 220, положение 226, положение 229, положение 231, положение 232, положение 233, положение 234, положение 235, положение 236, положение 237, положение 238, положение 239, положение 240, положение 264, положение 265, положение 266, положение 267, положение 269, положение 270, положение 295, положение 296, положение 297, положение 298, положение 299, положение 300, положение 325, положение 327, положение 328, положение 329, положение 330, положение 331 и положение 332.
[2-18] Противораковый агент по п. [2-16], в котором Fc-область, указанная в подпункте (3) в п. [2-1], представляет собой Fc-область, которая содержит по меньшей мере одну аминокислоту, выбранную из указанных ниже аминокислот, согласно EU-нумерации:
Arg в аминокислотном положении 234, Ala или Arg в аминокислотном положении 235, Lys в аминокислотном положении 239 и Ala в аминокислотном положении 297.
[2-19] Противораковый агент по одному из п.п. [2-16]-[2-18], в котором Fc-область, указанная в подпункте (3) в п. [2-1], дополнительно содержит аминокислотную мутацию, усиливающую образование гетеродимерной Fc-области.
[2-20] Противораковый агент по п. [2-19], в котором гетеродимерная Fc-область представляет собой указанную ниже комбинацию (ж1) или (ж2) аминокислотных последовательностей:
(ж1) комбинация аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 57, и аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 58; и
(ж2) комбинация аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 60 или 62, и аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 61.
[2-21] Противораковый агент по одному из п.п. [2-1]-[2-20], в котором мультиспецифическая антигенсвязывающая молекула представляет собой биспецифическое антитело.
[2-22] Противораковый агент, содержащий в качестве активного ингредиента биспецифическое антитело по одному из указанных ниже подпунктов (з1)-(з25):
(з1) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 424, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з2) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з3) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з4) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 301;
(з5) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 302;
(з6) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 304;
(з7) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 306;
(з8) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 307;
(з9) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 309;
(з10) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 122, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з11) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 129, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з12) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 132, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з13) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з14) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 310;
(з15) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 319;
(з16) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з17) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з18) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з19) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 144, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з20) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 144, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з21) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з22) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з23) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з24) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223; и
(з25) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223.
Кроме того, настоящее изобретение относится к противораковому агенту, содержащему в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу, которая содержит следующие домены:
(3-1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3,
(3-2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора;
в которой вариабельные области L-цепи, входящие в вариабельные области, указанные в подпунктах (3-1) и (3-2), имеют общую аминокислотную последовательность. Настоящее изобретение относится также к противораковому агенту, содержащему в качестве активного ингредиента домен, указанный в подпункте (3-1), который более конкретно представляет собой домен, содержащий вариабельные области тяжелой цепи и/или легкой цепи антитела, которые обладают связывающей активностью в отношении глипикана 3, и которые входит в состав мультиспецифической антигенсвязывающей молекулы. Настоящее изобретение относится также к противораковому агенту, содержащему в качестве активного ингредиента домен, указанный в подпункте (3-2), который более конкретно представляет собой домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и который входит в состав мультиспецифической антигенсвязывающей молекулы. Компоненты доменов, указанных в подпунктах (3-1) и (3-2), могут включать указанные выше в п.п. [2-1]-[2-22]. Мультиспецифическая антигенсвязывающая молекула может представлять собой биспецифическое антитело. Кроме того, мультиспецифическая антигенсвязывающая молекула может содержать домен, включающий Fc-область, и Fc-область может обладать пониженной активностью в отношении связывания Fcγ-рецептора. Компоненты домена, содержащего Fc-область, могут включать компоненты, указанные выше в п.п. [2-1]-[2-22]. Кроме того, настоящее изобретение относится к противораковому агенту, который содержит мультиспецифическую антигенсвязывающую молекулу и фармацевтически приемлемый носитель. Противораковый агент может индуцировать цитотоксичность, цитотоксичность может представлять собой зависимую от Т-клеток клеточную цитотоксичность, и агент можно вводить пациенту, который нуждается в применении мультиспецифической антигенсвязывающей молекулы.
Настоящее изобретение относится также к противораковому агенту, который содержит в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу, которая связывается с эпитопами, перекрывающимися и/или конкурирующими с эпитопами и глипикана 3, и комплекса Т-клеточного рецептора, связывающимися мультиспецифической антигенсвязывающей молекулой, указанной выше в одном из подпунктов (д1)-(д25) в п. [2-14], и мультиспецифическую антигенсвязывающую молекулу, которая связывается с эпитопами, перекрывающимися и/или конкурирующими с эпитопами и глипикана 3, и комплекса Т-клеточного рецептора, связывающимися мультиспецифической антигенсвязывающей молекулой, указанной выше в одном из подпунктов (e1)-(e25) в п. [2-15].
Касательно двух Fc-областей, описанных выше в подпунктах (ж1) и (ж2) в п. [2-20], первая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, а вторая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора; или первая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, а вторая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3.
Настоящее изобретение относится также к противораковому агенту, содержащему в качестве активного ингредиента биспецифическое антитело, которое связывается с эпитопами, перекрывающимися и/или конкурирующими с эпитопами и глипикана 3, и комплекса Т-клеточного рецептора, связывающимися биспецифическим антителом, которое имеет Н-цепь антитела, имеющую SEQ ID NO: 385, которая обладает связывающей активностью в отношении глипикана 3, Н-цепь антитела, имеющую SEQ ID NO: 402, которая обладает связывающей активностью в отношении CD3, и общие L-цепи, имеющие SEQ ID NO: 410.
В настоящем изобретении предложены также:
[4-1] Фармацевтическая композиция, содержащая другой противораковый агент в качестве активного ингредиента, где фармацевтическая композиция предназначена для применения в комбинации с биспецифическим антителом, указанным ниже в любом одном из подпунктов (а)-(в):
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-2] Фармацевтическая композиция по п. [4-1], где другой указанный противораковый агент вводят одновременно с биспецифическим антителом.
[4-3] Фармацевтическая композиция по п. [4-1], где указанный другой противораковый агент вводят до или после введения биспецифического антитела.
[4-4] Фармацевтическая композиция для лечения или предупреждения рака, содержащая комбинацию биспецифического антитела по любому одному из указанных ниже подпунктов (а)-(в) и другого противоракового агента:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-5] Фармацевтическая композиция по п. [4-4], которая представляет собой комбинированный препарат.
[4-6] Фармацевтическая композиция по п. [4-4], где биспецифическое антитело и указанный другой противораковый агент вводят раздельно.
[4-7] Фармацевтическая композиция по п. [4-6], где биспецифическое антитело и указанный другой противораковый агент вводят одновременно или последовательно.
[4-8] Фармацевтическая композиция по одному из п.п. [4-1]-[4-7], где указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[4-9] Фармацевтическая композиция по одному из п.п. [4-1]-[4-8], предназначенная для лечения или предупреждения любого рака, выбранного из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
[4-10] Агент для индукции цитотоксичности, агент для подавления пролиферации клеток, агент для ингибирования пролиферации клеток, агент для активации иммунного ответа, агент для лечения рака или агент для предупреждения рака, который содержит фармацевтическую композицию по одному из п.п. [4-1]-[4-9].
В настоящем изобретении предложены также:
[4-11] Комбинация биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в), и другого противоракового агента:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-12] Комбинация по п. [4-11], где биспецифическое антитело вводят одновременно с указанным другим противораковым агентом.
[4-13] Комбинация по п. [4-11], где биспецифическое антитело вводят до или после введения указанного другого противоракового агента.
[4-14] Комбинация по одному из п.п. [4-11]-[4-13], где указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[4-15] Комбинация по одному из п.п. [4-11]-[4-14], предназначенная для лечения или предупреждения любого рака, выбранного из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
[4-16] Агент для индукции цитотоксичности, агент для подавления пролиферации клеток, агент для ингибирования пролиферации клеток, агент для активации иммунного ответа, агент для лечения рака или агент для предупреждения рака, который содержит комбинацию по одному из п.п. [4-11]-[4-15].
В настоящем изобретении предложены также:
[4-17] Способ индукции цитотоксичности, подавления пролиферации клеток, ингибирования пролиферации клеток, активации иммунного ответа, лечения рака или предупреждения рака у индивидуума, включающий введение в эффективном количестве биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в), и в эффективном количестве другого противоракового агента:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223, соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-18] Способ индукции цитотоксичности, подавления пролиферации клеток, ингибирования пролиферации клеток, активации иммунного ответа, лечения рака или предупреждения рака у индивидуума с помощью совместного применения биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в), включающий введение индивидууму в эффективном количестве другого противоракового агента:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDRS-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-19] Способ индукции цитотоксичности, подавления пролиферации клеток, ингибирования пролиферации клеток, активации иммунного ответа, лечения рака или предупреждения рака у индивидуума с помощью совместного применения другого противоракового агента, включающий введение индивидууму в эффективном количестве биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в):
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-20] Способ повышения воздействий индукции цитотоксичности, подавления пролиферации клеток, ингибирования пролиферации клеток, активации иммунного ответа, лечения рака или предупреждения рака у индивидуума с помощью биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в), включающий введение индивидууму в эффективном количестве другого противоракового агента:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-21] Способ повышения воздействий индукции цитотоксичности, подавления пролиферации клеток, ингибирования пролиферации клеток, активации иммунного ответа, лечения рака или предупреждения рака у индивидуума с помощью совместного применения другого противоракового агента, включающий введение индивидууму в эффективном количестве биспецифического антитела, указанного ниже в любом одном из подпунктов (а)-(в):
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-22] Способ по одному из п.п. [4-17]-[4-21], в котором биспецифическое антитело и указанный другой противораковый агент вводят раздельно.
[4-23] Способ по одному из п.п. [4-17]-[4-22], в котором биспецифическое антитело и указанный другой противораковый агент вводят одновременно или последовательно.
[4-24] Способ по одному из п.п. [4-17]-[4-23], в котором указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[4-25] Способ по одному из п.п. [4-17]-[4-24], в котором рак представляет собой любой рак, выбранный из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
В настоящем изобретении предложен также:
[4-26] Набор, содержащий:
(A) фармацевтическую композицию, которая содержит биспецифическое антитело, указанное ниже в любом одном из подпунктов (а)-(в);
(Б) контейнер; и
(B) инструкцию или этикетку с указанием, что биспецифическое антитело и по меньшей мере один тип другого противоракового агента вводят индивидууму в комбинации для лечения или предупреждения рака у индивидуума;
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-27] Набор, содержащий:
(A) другой противораковый агент; (Б) контейнер; и
(B) инструкцию или этикетку с указанием, что указанный другой противораковый агент и фармацевтическую композицию, содержащую по меньшей мере один тип биспецифического антитела, указанного ниже в подпунктах (а)-(в), вводят индивидууму в комбинации для лечения или предупреждения рака у индивидуума;
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-28] Набор, содержащий:
(А) фармацевтическую композицию, которая содержит биспецифическое антитело, указанное ниже в любом одном из подпунктов (а)-(в):
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410;
(Б) контейнер; и
(В) другой противораковый агент.
[4-29] Набор по любому одному из п.п. [4-26]-[4-28], где биспецифическое антитело вводят одновременно с указанным другим противораковым агентом.
[4-30] Набор по любому одному из п.п. [4-26]-[4-28], где биспецифическое антитело вводят до или после введения указанного другого противоракового агента.
[4-31] Набор по любому одному из п.п. [4-26]-[4-30], где указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[4-32] Набор по любому одному из п.п. [4-26]-[4-31], где рак представляет собой любой рак, выбранный из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
В настоящем изобретении предложены также:
[4-33] Способ индукции повреждения раковой клетки или содержащей раковую клетку опухолевой ткани или способ подавления пролиферации раковой клетки или роста содержащей раковую клетку опухолевой ткани, путем приведения в контакт раковой клетки с биспецифическим антителом, указанным ниже в любом одном из подпунктов (а)-(в), и другим противораковым агентом:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-34] Способ оценки того, индуцирует ли биспецифическое антитело и другой противораковый агент повреждение раковой клетки или содержащей раковую клетку опухолевой ткани или подавляет ли пролиферацию раковой клетки или рост содержащей раковую клетку опухолевой ткани, при приведении в контакт раковой клетки с биспецифическим антителом, указанным ниже в любом одном из подпунктов (а)-(в), и другим противораковым агентом:
(а) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDRS-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, в котором вариабельная область антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
[4-35] Способ по п. [4-33] или п. [4-34], в котором указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
[4-36] Способ по одному из п.п. [4-33]-[4-35], в котором раковая клетка представляет собой любую раковую клетку, выбранную из группы, которая состоит из клетки рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
В настоящем изобретении предложены также:
[5-1] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для повышения и/или поддержания экспрессии CD3ε-цепи у индивидуума по сравнению с введением только биспецифического антитела по любому одному из п. [7] подпунктов (а)-(в) или только указанного другого противоракового агента.
[5-2] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для увеличения популяции Т-клеток у индивидуума по сравнению с введением только биспецифического антитела по любому одному из подпунктов (а)-(в) п. [7] или только указанного другого противоракового агента.
[5-3] Фармацевтическая композиция по п. [5-2], где популяция Т-клеток представляет собой популяцию активированных Т-клеток.
[5-4] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для повышения экспрессии цитокина и/или хемокина у индивидуума по сравнению с введением только биспецифического антитела по любому одному из п. [7] подпунктов (а)-(в) или только указанного другого противоракового агента.
[5-5] Фармацевтическая композиция по п. [5-4], где цитокин и/или хемокин представляет собой один или несколько цитокинов и/или хемокинов, выбранных из группы, которая состоит из IFNγ, IL2, IL6, IL7, IL8, IL10, IL17A, TNF, CXCL9 и CXCL10.
[5-6] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для повышения экспрессии гена, участвующего в гибели клеток, у индивидуума по сравнению с введением только биспецифического антитела по любому одному из п. [7] подпунктов (а)-(в) или только указанного другого противоракового агента.
[5-7] Фармацевтическая композиция по п. [5-6], где ген, участвующий в гибели клеток, представляет собой один или несколько генов, выбранных из группы, которая состоит из TNFSF10, FAS, FASL, каспазы 8 и каспазы 7.
[5-8] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для ингибирования гена, участвующего в ускорении (прогрессирования) клеточного цикла, у индивидуума по сравнению с введением только биспецифического антитела по любому одному из п. [7] подпунктов (а)-(в) или только указанного другого противоракового агента.
[5-9] Фармацевтическая композиция по п. [5-8], где ген, участвующий в ускорении (прогрессирования) клеточного цикла, представляет собой один или несколько генов, выбранных из группы, которая состоит из PCNA, CCNA2 и CDK4.
[5-10] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для повышения экспрессии гена, участвующего в подавлении клеточного цикла, у индивидуума по сравнению с введением только биспецифического антитела по любому одному из п. [7] подпунктов (а)-(в) или только указанного другого противоракового агента.
[5-11] Фармацевтическая композиция по п. [5-10], где ген, участвующий в подавлении клеточного цикла, представляет собой р21.
[5-12] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для увеличения (уровня) маркера лейкоцитов у индивидуума по сравнению с введением только биспецифического антитела по любому одному из подпунктов (а)-(в) п. [7] или только указанного другого противоракового агента.
[5-13] Фармацевтическая композиция по п. [5-12], где маркер лейкоцитов представляет собой CD45.
[5-14] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для увеличения (уровня) маркера Т-клеток и/или маркера активации Т-клеток у индивидуума по сравнению с введением только биспецифического антитела по любому одному из подпунктов (а)-(в) п. [7] или только указанного другого противоракового агента.
[5-15] Фармацевтическая композиция по п. [5-14], где маркер Т-клеток и/или маркер активации Т-клеток представляет собой один или несколько маркеров Т-клеток и/или маркеров активации Т-клеток, выбранных из группы, которая состоит из CD3, CD4, CD8a, GZB, PRF1 и IFNγ.
[5-16] Фармацевтическая композиция по любому одному из п.п. [7]-[12] и [4-1]-[4-9], которая предназначена для повышения экспрессии гена иммунных контрольных точек у индивидуума по сравнению с введением только биспецифического антитела по любому одному из подпунктов (а)-(в) п. [7] или только указанного другого противоракового агента.
[5-17] Фармацевтическая композиция по п. [5-16], где ген иммунных контрольных точек представляет собой один или несколько генов, выбранных из группы, которая состоит из PD-L1, PD-1, TIM3, LAG3 и CTLA4.
В каждом из указанных выше пунктов [4-1]-[4-36] понятие «другой противораковый агент» относится к противораковому агенту, который содержит в качестве активного ингредиента субстанцию, которая отличается от биспецифического антитела, упомянутого в каждом пункте. В частности, понятие «другой противораковый агент» исключительно свидетельствует о том, что каждый пункт изобретения определяется в качестве объектов изобретения, в которых иной/другой противораковый агент представляет собой противораковый агент, содержащий в качестве активного ингредиента субстанцию, которая отличается от биспецифического антитела, и что изобретение не ограничено объектами изобретения, в которых биспецифическое антитело применяют в качестве противоракового агента. Например, даже, если в каждом из пунктов [4-1]-[4-36] изобретения упоминается понятие «другой противораковый агент», изобретение включает также варианты осуществления изобретения, в которых не применяют никакой иной противораковый агент, отличный от «другого противоракового агента», и в этом случае изобретение включает варианты осуществления изобретения, в которых биспецифическое антитело применяют в качестве энхансера, комбинации лекарственных средств, эксципиента или т.п.для другого противоракового агента.
Эффекты изобретения
В настоящем изобретении предложены новые мультиспецифические антигенсвязывающие молекулы, имеющие молекулярные формы, которые можно получать с высокой эффективностью, которые сохраняют сильную противоопухолевую активность, характерную для BiTE, и очень хорошие характеристики безопасности, что приводит к отсутствию индукции независимого от ракового антигена «цитокинового шторма» и т.п., и обладают длительным временем полужизни в крови. Противораковые агенты, которые содержат мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, в качестве активного ингредиента и комбинированные терапии, в которых используют мультиспецифическую антигенсвязывающую молекулу и другой противораковый агент, направленно воздействуют на раковые ткани, которые содержат экспрессирующие глипикан 3 раковые клетки, обусловливая цитотоксичность, и их можно применять для лечения или предупреждения различных видов рака. Изобретение обеспечивает требуемое лечение, которое не только обладает высоким уровнем безопасности, но и снижает физическую нагрузку на пациентов и является очень удобным для них.
Краткое описание чертежей
На чертежах показано:
на фиг. 1-1 - графики, демонстрирующие цитотоксическую активность антитела-38, когда в качестве клеток-мишеней применяют клеточные линии, полученные из различных типов рака;
на фиг. 1-2 - графики, демонстрирующие цитотоксическую активность антитела-38, когда в качестве клеток-мишеней применяют клеточные линии, полученные из различных типов рака (продолжение фиг. 1-1);
на фиг. 1-3 - графики, демонстрирующие цитотоксическую активность антитела-38, когда в качестве клеток-мишеней применяют клеточные линии, полученные из различных типов рака (продолжение фиг. 1-2);
на фиг. 2 - графики, демонстрирующие противоопухолевую активность антитела-38 в отношении ксенотрансплантатов опухолей, полученных из различных типов рака, на модели с трансплантированными человеческими Т-клетками;
на фиг. 3 - график, демонстрирующий противоопухолевую активность антител-39 и -40 в отношении ксенотрансплантата опухоли РС-10 на модели с трансплантированными человеческими Т-клетками;
на фиг. 4 - график, демонстрирующий противоопухолевую активность антител-30, -31, -32 и -33 в отношении ксенотрансплантата опухоли SK-HEP-1/hGPC3 (SK-pca31a) на модели с трансплантированными человеческими Т-клетками;
на фиг. 5 - график, демонстрирующий противоопухолевую активность антитела-38 в отношении ксенотрансплантата опухоли РС-10 на гуманизированной мышиной (линия NOG) модели;
на фиг. 6 - график, демонстрирующий противоопухолевую активность антитела-38 и антитела к человеческому GPC3, антитела к мышиному CTLA-4, антитела к мышиному PD-1 или антитела к мышиному PD-L1 в отношении сингенной опухоли LLC1/hGPC3 на модифицированной человеческим геном CD3εδγ мышиной модели;
на фиг. 7 - графики, демонстрирующие противоопухолевую активность индивидуального антитела или комбинации антитела и капецитабина, цисплатина или паклитаксела в отношении ксенотрансплантата опухоли MKN45 на модели с трансплантированными человеческими Т-клетками;
на фиг. 8 - графики, демонстрирующие противоопухолевую активность индивидуально антитела или комбинации антитела и цисплатина или паклитаксела в отношении ксенотрансплантата опухоли NCI-H446 на модели с трансплантированными человеческими Т-клетками;
на фиг. 9 - графики, демонстрирующие противоопухолевую активность индивидуально антитела-38 или комбинации антитела-38 и антитела к мышиному TIM-3, антитела к мышиному LAG-3, антитела к мышиному CD137 или антитела к мышиному VEGFR2 в отношении сингенной опухоли Hepa1-6/hGPC3 на модифицированной человеческим геном CD3εδγ мышиной модели;
на фиг. 10 - график, демонстрирующий противоопухолевую активность индивидуально антитела-38 или комбинации антитела-38 и антитела к мышиному CD137 в отношении сингенной опухоли LLCl/hGPC3 на модифицированной человеческим геном CD3εδγ мышиной модели;
на фиг. 11 - графики, демонстрирующие противоопухолевую активность индивидуально антитела-38 или комбинации антитела-38 и антитела к PD-1 или антитела к мышиному PD-L1 в отношении сингенной опухоли Hepal-6/hGPC3 на модифицированной человеческим геном CD3εδγ мышиной модели;
на фиг 12 - схематическая диаграмма a: ERY22 и б: ERY27;
на фиг. 13 - график, иллюстрирующий цитотоксическую активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 при применении в качестве клетки-мишени NCI-H446. Закрашенными ромбами  и закрашенными треугольниками
и закрашенными треугольниками  обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
на фиг. 14 - график, иллюстрирующий цитотоксическую активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 при применении в качестве клетки-мишени РС-10. Закрашенными ромбами  и закрашенными треугольниками
и закрашенными треугольниками  обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
на фиг. 15 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 16 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 17 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 18 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 19 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 20 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 21 - данные о противоопухолевой активности in vivo оптимизированных антител при применении в качестве клетки-мишени РС-10;
на фиг. 22 - данные о противоопухолевой активности in vivo оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 23 - зависимость между аминокислотными остатками, образующими Fc-области IgG1, IgG2, IgG3 и IgG4, и системой нумерации EU по Кэботу (также обозначена в контексте настоящего описания как EU-индекс);
на фиг. 24-1 - последовательности вариабельных областей тяжелой цепи и их нумерация согласно Кэботу с соавторами;
на фиг. 24-2 - последовательности вариабельных областей тяжелой цепи и их нумерация согласно Кэботу с соавторами;
на фиг. 25 - последовательности вариабельных областей легкой цепи и их нумерация согласно Кэботу с соавторами;
на фиг. 26А - (1) структура геномной ДНК, содержащая мышиные гены Cd3ε, Cd3δ и Cd3γ, (2) вектор с модификацией гена Cd3, сконструированный путем модификации клона бактериальной искусственной хромосомы (ВАС), содержащий полную генную область, (3) структура геномной ДНК, в которой последовательности loxP и Rox встроены в целевое положение с использованием вышеуказанного вектора, и (4) структура аллеля с дефицитом гена Cd3ε, Cd3δ и Cd3γ, полученная под действием рекомбиназ Cre и Dre;
на фиг. 26Б -структуры клона ВАС, содержащие (а) человеческие гены CD3ε, CD3δ и CD3γ; (б) 5'-модифицирующую кассету и (в) 3'-модифицирующую кассету, которые обе модифицируют клон ВАС; и (г) вектор для интродукции области человеческого гена CD3, сконструированный с использованием описанных выше модификаций;
на фиг. 27 - репрезентативные примеры результатов ПЦР-анализов, которые осуществляли для создания модифицированных мышиным геном Cd3 ES-клеток (эмбриональные стволовые клетки);
на фиг. 28 - репрезентативные примеры результатов ПЦР-анализов генотипов клонов ES-клеток, полученных путем интродукции в модифицированные мышиным геном Cd3 ES-клеток вектора для интродукции области человеческого гена CD3 наряду с экспрессионным вектором Cre и экспрессионным вектором Dre;
на фиг. 28А - репрезентативные примеры результатов ПЦР, которые позволили обнаружить дефицит области мышиного гена Cd3;
на фиг. 28Б - репрезентативные примеры результатов ПЦР, которые позволили обнаружить интродукцию области человеческого гена CD3;
на фиг. 29 - репрезентативные макроскопические фотографии тимусов, полученных из каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3, мышей с дефицитом гена Cd3, дикого типа и мышей с интродуцированным человеческим геном CD3ε. Показаны тимусы, изъятые у самцов соответствующих генотипов возрастом 12-13-недель;
на фиг. 30 - результаты измерения массы ткани селезенок и тимусов, полученных из каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3, мышей с дефицитом гена Cd3, мышей дикого типа и мышей с интродуцированным человеческим геном CD3ε. Рассчитывали отношения массы ткани к массе организма, и полученные для каждой особи величины обозначены на графике черной точкой, а средние величины обозначены столбиками;
на фиг. 31- результаты оценки с помощью ОТ-ПЦР экспрессии каждой из молекул человеческого CD3 и каждого из мышиных генов Cd3 в каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3, мышей с дефицитом гена Cd3, мышей дикого типа и мышей с интродуцированным человеческим геном CD3ε (hCD3ε Tg). Среди созданных линий мышей, несущих в качестве замены человеческий ген CD3, сигналы, специфические для hCD3ε, hCD3δ и hCD3γ, обнаружены в линиях с номерами 1С3 и 8I12. Сигналы не обнаружены в линиях с номерами 3В1 и 2А4;
на фиг. 32 -репрезентативные примеры иммуногистологического окрашивания CD3 в тимусе (А) и селезенке (Б) в каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3 (1С3, 8I12 и 4НН3). В обоих типах тканей такое же окрашивание, что и у мышей дикого типа, выявлено только в зоне Т-клеток. Кроме того, окрашивание не выявлено у мышей с дефицитом гена Cd3, и это свидетельствует о том, что окрашивание мышей, несущих в качестве замены человеческий ген CD3, является результатом экспрессии интродуцированных человеческих генов CD3;
на фиг. 33 - репрезентативные результаты FACS-анализов относительного содержания зрелых Т-клеток в тимусе каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3;
на фиг. 34- результаты измерения концентраций в сыворотке специфических в отношении куриного овальбумина (OVA) IgG1 и IgE в каждой из созданных линий мышей, несущих в качестве замены человеческий ген CD3, иммунизированных OVA. Концентрации OVA-специфических сывороточных IgG1 и IgE для каждой особи представлены в виде гистограмм. Номерами под гистограммой обозначены идентификационные номера каждой особи;
на фиг. 35-1 - результаты полного анализа РНК опухолевых тканей при применении паклитаксела и антитела-38 в комбинации;
на фиг. 35-2 - результаты полного анализа РНК опухолевых тканей при применении паклитаксела и антитела-38 в комбинации (продолжение фиг. 35-1);
на фиг. 35-3 - результаты полного анализа РНК опухолевых тканей при применении паклитаксела и антитела-38 в комбинации (продолжение фиг. 35-2);
на фиг. 35-4 - результаты полного анализа РНК опухолевых тканей при применении капецитабина и антитела-38 в комбинации;
на фиг. 35-5 - результаты полного анализа РНК опухолевых тканей при применении капецитабина и антитела-38 в комбинации (продолжение фиг. 35-4);
на фиг. 35-6 - результаты полного анализа РНК опухолевых тканей при применении капецитабина и антитела-38 в комбинации (продолжение фиг. 35-5);
на фиг. 36-1 - результаты анализа инфильтрующих опухоль лимфоцитов (TIL) в опухолевых тканях при применении паклитаксела и антитела-38 в комбинации;
на фиг. 36-2 результаты анализа инфильтрующих опухоль лимфоцитов (TIL) в опухолевых тканях при применении цисплатина и антитела-38 в комбинации.
Варианты осуществления изобретения
Представленные ниже определения даны с целью облегчения понимания настоящего изобретения.
Антитело
В контексте настоящего описания «антитело» относится к встречающемуся в естественных условиях иммуноглобулину или иммуноглобулину, полученному полностью или частично путем синтеза. Антитела можно выделять из встречающихся в естественных условиях источников, таких как встречающиеся в естественных условиях плазма и сыворотка, или из супернатантов культур продуцирующих антитела гибридом. Альтернативно этому, антитела можно частично или полностью синтезировать с использованием таких методик, как генетическая рекомбинация. Предпочтительными антителами являются, например, антитела, принадлежащие к какому-либо изотипу иммуноглобулинов или его подклассу. Известные человеческие иммуноглобулины включают антитела следующих девяти классов (изотипов): IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE и IgM. Из этих изотипов антитела, предлагаемые в изобретении, могут включать IgG1, IgG2, IgG3 и IgG4.
Методы получения антитела с требуемой связывающей активностью известны специалистам в данной области. Ниже представлен пример, в котором описан метод получения антитела (антитело к GPC3), связывающегося с глипиканом-3 (ниже в настоящем описании обозначен как GPC3), который принадлежит к семейству GPI-заякоренных рецепторов (Int J Cancer. 103(4), 2003, сс. 455-465). Согласно описанному ниже примеру можно получать также антитела, которые связываются с комплексом Т-клеточного рецептора.
Антитела к GPC3 можно получать в виде поликлональных или моноклональных антител с помощью известных методов. Антитела к GPC3 предпочтительно получали в виде моноклональных антител, происходящих из организма млекопитающих. Указанные происходящие из организма млекопитающих антитела включают антитела, полученные с помощью гибридом или клеток-хозяев, трансформированных экспрессионным вектором, который несет ген антитела, с помощью методов генетической инженерии.
Гибридомы, продуцирующие моноклональные антитела, можно получать с использованием известных методов, например, описанных ниже. В частности, млекопитающих иммунизируют с помощью общепринятых методов иммунизации, используя белок GPC3 в качестве сенсибилизирующего антигена. Образовавшиеся иммунные клетки сливают с известными родительскими клетками с помощью общепринятых методов слияния. Затем гибридомы, продуцирующие антитело к GPC3, можно отбирать путем скрининга в отношении продуцирующих моноклональные антитела клеток с помощью общепринятых методов скрининга.
В частности, моноклональные антитела получают согласно описанному ниже методу. Сначала ген GPC3, нуклеотидная последовательность которого представлена в RefSeq под регистрационным номером NM_001164617.1 (SEQ ID NO: 1), можно экспрессировать с получением белка GPC3, последовательность которого представлена в RefSeq под регистрационным номером NP_001158089.1 (SEQ ID NO: 2), который можно применять в качестве сенсибилизирующего антигена для получения антитела. Для этого генную последовательность, кодирующую GPC3, встраивают в известный экспрессионный вектор и соответствующие клетки-хозяева трансформируют этим вектором. Требуемый человеческий белок GPC3 очищают из клеток-хозяев или супернатантов культур с помощью известных методов. Например, для получения растворимого GPC3 из супернатантов культур удаляют путем делеции аминокислоты в положениях 564-580, которые формируют гидрофобную область, соответствующую GPI-заякоривающей последовательности, применяемой для заякоривания GPC3 на клеточной мембране, из полипептидной последовательности GPC3 SEQ ID NO: 2, а затем образовавшийся белок экспрессируют вместо белка GPC3, имеющего SEQ ID NO: 2. В альтернативном варианте в качестве сенсибилизирующего антигена можно применять очищенный встречающийся в естественных условиях белок GPC3.
Очищенный белок GPC3 можно применять в качестве сенсибилизирующего антигена для иммунизации млекопитающих. В качестве сенсибилизирующих антигенов можно применять также неполные пептиды GPC3. В этом случае неполные пептиды можно получать химическим синтезом на основе аминокислотной последовательности человеческого GPC3. Кроме того, их можно получать также путем встраивания части гена GPC3 в экспрессионный вектор и осуществлять экспрессию в нем. Кроме того, их можно получать путем расщепления белка GPC3 протеазой, однако конкретный вариант осуществления изобретения не накладывает ограничения на длину и область пептида GPC3, применяемого в качестве неполного пептида. В качестве предпочтительной области можно выбирать любую последовательность из аминокислотной последовательности, которая соответствует аминокислотам в положениях 524-563, или более предпочтительно любую последовательность из аминокислотной последовательности, которая соответствует аминокислотам в положениях 537-563 в аминокислотной последовательности SEQ ID NO: 2. Предпочтительно можно выбирать любую последовательность из аминокислотной последовательности области, не содержащую аминокислотную последовательность, которая соответствует аминокислотам в положениях 550-663 в аминокислотной последовательности SEQ ID NO: 2. Предпочтительно можно выбирать любую последовательность, соответствующую положениям 544-553, и более предпочтительно можно выбирать любую последовательность из аминокислотной последовательности, соответствующей положениям 546-551, в аминокислотной последовательности SEQ ID NO: 2. Количество аминокислот, образующих пептид, который можно применять в качестве сенсибилизирующего антигена, предпочтительно составляет по меньшей мере пять или более, или предпочтительно, например, шесть или более, или семь или более. Более конкретно, в качестве сенсибилизирующего антигена можно применять пептид, состоящий из 8-50 остатков, более предпочтительно из 10-30 остатков.
В альтернативном варианте в качестве сенсибилизирующего антигена можно применять слитый белок, полученный путем слияния требуемого неполного полипептида или пептида белка GPC3, с другим полипептидом. Например, для получения слитых белков, предназначенных для применения в качестве сенсибилизирующих антигенов, предпочтительно применяют Fc-фрагменты антитела и пептидные метки. Векторы для экспрессии указанных слитых белков можно конструировать путем слияния в рамке считывания генов, кодирующих два или большее количество требуемых полипептидных фрагментов, и встраивания слитого гена в экспрессионный вектор, описанный выше. Методы получения слитых белков описаны в Molecular Cloning, 2-ое изд. (Sambrook J. и др., Molecular Cloning, 2-ое изд. 1989, 9.47-9.58, изд-во Cold Spring Harbor Lab. Press). Методы получения GPC3, предназначенного для применения в качестве сенсибилизирующего антигена, и методы иммунизации с использованием GPC3 конкретно описаны в WO 2003/000883, WO 2004/022754 и WO 2006/006693.
Конкретные ограничения, касающиеся млекопитающих, подлежащих иммунизации с помощью сенсибилизирующего антигена, отсутствуют. Однако предпочтительно следует выбирать млекопитающих с учетом их совместимости с родительскими клетками, применяемыми для клеточного слияния. В целом, предпочтительно применяют грызунов, таких как мыши, крысы, а также хомяки, кролики, и обезьян.
Вышеуказанных животных иммунизируют сенсибилизирующим антигеном с помощью известных методов. Общепринятыми методами иммунизации млекопитающих являются, например, внутрибрюшинная или подкожная инъекция сенсибилизирующего антигена. В частности, сенсибилизирующий антиген можно соответствующим образом разводить в ЗФР (забуференный фосфатом физиологический раствор), физиологическом соляном растворе или т.п.При необходимости с антигеном смешивают общепринятый адъювант, такой как полный адъювант Фрейнда, и смесь эмульгируют. Затем сенсибилизирующий антиген вводят млекопитающему несколько раз с 4-21-дневными интервалами. При иммунизации сенсибилизирующим антигеном можно использовать соответствующие носители. В частности, когда в качестве сенсибилизирующего антигена используют низкомолекулярный неполный пептид, то иногда для иммунизации требуется сочетать пептид, представляющий собой сенсибилизирующий антиген, с белком-носителем, таким как альбумин или гемоцианин лимфы улитки.
Альтернативно этому, можно получать продуцирующие требуемое антитело гибридомы с помощью описанной ниже ДНК-иммунизации. ДНК-иммунизация представляет собой метод иммунизации, который обеспечивает иммуностимуляцию посредством экспрессии сенсибилизирующего антигена в организме иммунизированного животного в результате введения ДНК-вектора, сконструированного таким образом, чтобы он обеспечивал экспрессию гена, кодирующего антигенный белок, в организме животного. По сравнению с общепринятыми методами иммунизации, при которых животным, подлежащим иммунизации, вводят белковый антиген, ДНК-иммунизация, по-видимому, имеет следующие преимущества:
- можно осуществлять иммуностимуляцию, сохраняя при этом структуру мембранного белка, такого как GPC3; и
- отсутствует необходимость в очистке антигена для иммунизации.
Для получения моноклонального антитела, предлагаемого в настоящем изобретении, с использованием ДНК-иммунизации сначала вводят животному, подлежащему иммунизации, ДНК, экспрессирующую белок GPC3. ДНК, кодирующую GPC3, можно синтезировать с помощью известных методов, таких как ПЦР. Полученную ДНК встраивают в соответствующий экспрессионный вектор и затем его вводят животному, подлежащему иммунизации. Предпочтительно применяемые для этой цели экспрессионные векторы включают, например, поступающие в продажу экспрессионные векторы, такие как pcDNA3.1. Векторы можно вводить в организм с помощью общепринятых методов. Например, ДНК-иммунизацию осуществляют с использованием генной пушки для интродукции золотых частиц, покрытых экспрессионным вектором, в клетки тела животного, подлежащего иммунизации. Антитела, распознающие GPC3, можно получать также методами, описанными в WO 2003/104453. После описанной выше иммунизации млекопитающего у него подтверждают в сыворотке повышенный титр GPC3-связывающего антитела. После этого получают из организма млекопитающего иммунные клетки и затем используют их для клеточного слияния. В частности, в качестве иммунных клеток предпочтительно применяют спленоциты.
Клетку миеломы млекопитающих применяют в качестве клетки, подлежащей слиянию с вышеуказанным иммуноцитом. Клетки миеломы предпочтительно содержат приемлемый маркер селекции для скрининга. Маркер селекции придает клеткам характеристики, обеспечивающие их выживание (или гибель) в специфических условиях культивирования. В качестве маркера селекции известны дефицит гипоксантин-гуанин-фосфорибозилтрансферазы (сокращенно обозначенный далее в контексте настоящего описания как дефицит HGPRT) и дефицит тимидинкиназы (сокращенно обозначенный далее в контексте настоящего описания как дефицит ТК). Клетки с дефицитом HGPRT или ТК обладают чувствительностью к гипоксантин-аминоптерин-тимидину (сокращенно обозначена далее в контексте настоящего описания как ГАТ-чувствительность). Клетки с ГАТ-чувствительностью не могут синтезировать ДНК в селекционной ГАТ-среде и в результате погибают. Однако, когда клетки сливают со здоровыми клетками, они могут продолжать синтез ДНК с использованием «реутилизационного» пути здоровых клеток, и в результате они могут расти даже в селекционной ГАТ-среде.
Клетки с HGPRT-дефицитом и ТК-дефицитом можно отбирать в среде, содержащей 6-тиогуанин, 8-азагуанин (сокращенно обозначенный далее в контексте настоящего описания как 8AG) или 5'-бромдезоксиуридин соответственно. Здоровые клетки уничтожаются, поскольку они включают эти пиримидиновые аналоги в их ДНК. При этом клетки с дефицитом этих ферментов могут выживать в селекционной среде, поскольку они не могут включать указанные пиримидиновые аналоги. Кроме того, к маркеру селекции относится устойчивость к G418, которая обеспечивается геном устойчивости к неомицину, придающим устойчивость к 2-дезоксистрептаминовым антибиотикам (аналоги гентамицина). Известны различные типы клеток миелом, которые можно применять для клеточного слияния.
Например, в качестве клеток миеломы предпочтительно можно применять следующие клетки:
P3(P3x63Ag8.653) (J. Immunol. 123 (4), 1979, сс. 1548-1550);
P3x63Ag8U.1 (Current Topics in Microbiology and Immunology 81, 1978, cc. 1-7);
NS-1 (C. Eur. J. Immunol. 6 (7), 1976, cc. 511-519);
MPC-11 (Cell 8 (3), 1976, cc. 405-415);
SP2/0 (Nature 276 (5685), 1978, cc. 269-270);
FO (J. Immunol. Methods 35 (1-2), 1980, cc. 1-21);
S194/5.XX0.BU.1 (J. Exp. Med. 148 (1), 1978, cc. 313-323);
R210 (Nature 277 (5692), 1979, cc. 131-133) и т.д.
Клеточное слияние иммуноцитов и клеток миеломы, как правило, осуществляют с помощью известных методов, например, метода, описанного у Kohler и Milstein и др. (Methods Enzymol. 73, 1981, cc. 3-46).
Более конкретно, клеточное слияние можно осуществлять, например, в общепринятой культуральной среде в присутствии усиливающего клеточное слияние агента. Усиливающие клеточное слияние агенты включают, например, полиэтиленгликоль (ПЭГ) и вирус Сендай (гемагглютинирующий японский вирус мышей) (HVJ). При необходимости для повышения эффективности слияния добавляют также вспомогательную субстанцию, такую как диметилсульфоксид.
Соотношение иммуноцитов и клеток миеломы можно определять по усмотрению исследователя, предпочтительно, например, одна клетка миеломы на каждые 1-10 иммуноцитов. Культуральные среды, применяемые для клеточных слияний, включают, например, среды, пригодные для выращивания клеточных линий миелом, такие как среда RPMI1640 и среда MEM, а также другая общепринятая культуральная среда, применяемая для данного типа клеточной культуры. Кроме того, в культуральную среду предпочтительно можно добавлять добавки в виде сыворотки, такой как фетальная телячья сыворотка (FCS). Для клеточного слияния указанные выше иммунных клетки и клетки миеломы, взятые в предварительно определенных количествах, хорошо перемешивают в указанной выше культуральной среде. Затем к ней добавляют предварительно нагретый до температуры примерно 37°С раствор ПЭГ (например, средняя молекулярная масса которого составляет примерно от 1000 до 6000) в концентрации, составляющей, как правило, от 30 до 60% (мас./об.). Смесь осторожно перемешивают до получения требуемых слитых клеток (гибридомы). Затем указанную выше культуральную среду постепенно добавляют к клеткам и повторно центрифугируют для удаления супернатанта. Таким путем можно удалять агенты для клеточного слияния, которые являются нежелательными для роста гибридом.
Полученные таким образом гибридомы можно отбирать путем культивирования, используя общепринятую селективную среду, например, ГАТ-среду (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). Клетки, отличные от требуемых гибридом (неслитые клетки), можно уничтожать путем последующего культивирования в вышеуказанной ГАТ-среде в течение достаточного периода времени. Как правило, период составляет от нескольких дней до нескольких недель. Затем осуществляют скрининг гибридом, продуцирующих требуемое антитело, и по отдельности клонируют с помощью общепринятых методов серийных разведений.
Полученные таким образом гибридромы можно отбирать, используя селекционную среду на основе маркера селекции, который несут клетки миеломы, применяемые для клеточного слияния. Например, клетки с HGPRT-или TK-дефицитом можно отбирать путем культивирования с использованием ГАТ-среды (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). А частности, когда для клеточного слияния используют чувствительные к ГАТ клетки миеломы, то клетки, для которых характерно успешное слияние со здоровыми клетками, могут избирательно размножаться в ГАТ-среде. Клетки, отличные от требуемых гибридом (неслитые клетки), можно уничтожать путем культивирования в вышеуказанной ГАТ-среде в течение достаточного периода времени. В частности, требуемые гибридомы можно отбирать путем культивирования, как правило, в течение периода времени, составляющего от нескольких дней до нескольких недель. Затем можно осуществлять скрининг гибридом, продуцирующих требуемое антитело, и их можно по отдельности клонировать с помощью общепринятых методов серийных разведений.
Требуемые антитела предпочтительно можно отбирать и по отдельности клонировать с помощью методов скрининга, основанных на известной реакции антиген/антитело. Например, GPC3-связывающее моноклональное антитело может связываться с GPC3, экспрессируемым на клеточной поверхности. Можно осуществлять скрининг указанных моноклональных антител с помощью метода разделения клеток на основе возбуждения флуоресценции (FACS). FACS представляет собой систему, которая позволяет оценивать связывание антитела с клеточной поверхностью посредством анализа клеток, контактирующих с флуоресцентным антителом, с использованием лазерного пучка, и путем оценки флуоресценции, испускаемой индивидуальными клетками.
Для скрининга с использованием FACS в отношении гибридом, которые продуцируют моноклональное антитело, предлагаемое в настоящем изобретении, прежде всего получают экспрессирующие GPC3 клетки. Клетки, которые предпочтительно используют для скрининга, представляют собой клетки млекопитающих, в которых происходит принудительная экспрессия GPC3. В качестве контроля можно избирательно определять с использованием нетрансформированных клеток млекопитающих в качестве клеток-хозяев способность антитела связываться с расположенным на клеточной поверхности GPC3. В частности, гибридомы, продуцирующие моноклональное антитело к GPC3, можно выделять путем отбора гибридом, которые продуцируют антитело, связывающееся с клетками, принудительно экспрессирующими GPC3, но не с клетками-хозяевами.
Альтернативно этому, способность антитела связываться с иммобилизованными экспрессирующими GPC3 клетками можно оценивать на основе принципа ELISA. Например, экспрессирующие GPC3 клетки иммобилизуют на лунках планшета для ELISA. Супернатанты культур гибридом приводят в контакт с иммобилизованными клетками в лунках и выявляют антитела, которые связываются с иммобилизованными клетками. Когда моноклональные антитела имеют мышиное происхождение, то антитела, связанные с клетками, можно выявлять с помощью антитела к мышиному иммуноглобулину. Гибридомы, продуцирующие требуемое антитело, которое обладает антигенсвязывающей активностью, отбирают путем описанного выше скрининга, и их можно клонировать методом серийных разведений или аналогичным методом.
Полученные таким путем гибридомы, продуцирующие моноклональные антитела, можно пересевать в общепринятую культуральную среду и хранить в жидком азоте в течение длительного периода времени.
Указанные выше гибридомы культивируют с помощью общепринятого метода и требуемые моноклональные антитела можно получать из супернатантов культур. Альтернативно этому, гибридомы интродуцируют и выращивают в пригодных для этой цели млекопитающих, и моноклональные антитела получают из асцитов. Первый метод пригоден для получения антител с высокой степенью чистоты.
Предпочтительно можно применять также антитела, кодируемые генами антител, которые клонированы из продуцирующих антитела клеток, таких как указанные выше гибридомы. Клонированный ген антитела встраивают в соответствующий вектор и его интродуцируют в хозяина для экспрессии кодируемого геном антитела. Методы выделения генов антител, встраивания генов в векторы и трансформации клеток-хозяев разработаны ранее (см., например, Vandamme и др., Eur. J. Biochem. 192(3), 1990, сс. 767-775). Методы получения рекомбинантных антител также известны и описаны ниже.
Например, кДНК, кодирующую вариабельную область (V-область) антитела к GPC3, получают из клеток гибридомы, экспрессирующих антитело к GPC3. Для этой цели сначала из гибридом экстрагируют общую РНК. Методы, которые применяют для экстракции мРНК из клеток, включают, например:
- метод ультрацентрифугирования в присутствии гуанидина (Biochemistry 18(24), 1979, сс. 5294-5299) и
- AGPC-метод (Anal. Biochem. 162(1), 1987, сс. 156-159).
Экстрагированные мРНК можно очищать с помощью набора для очистки мРНК (фирма GE Healthcare Bioscience) или аналогичного набора. В качестве альтернативы можно применять также поступающие в продажу наборы для экстракции мРНК непосредственно из клеток, такие как набор для очистки мРНК QuickPrep (фирма GE Healthcare Bioscience). мРНК можно получать из гибридом с использованием таких наборов. Кодирующие V-область антитела кДНК можно синтезировать из полученных мРНК с помощью обратной транскриптазы. кДНК можно синтезировать с помощью набора для синтеза первой цепи кДНК, содержащего обратную транскриптазу AMV (Reverse Transcriptase First-strand cDNA Synthesis Kit) (фирма Seikagaku Co.) или аналогичного набора. Кроме того, для синтеза и амплификации кДНК можно применять набор для амплификации кДНК SMART RACE (фирма Clontech) и основанный на ПЦР 5'-RACE-(быстрая амплификация концов кДНК)-метод (Proc. Natl. Acad. Sci. USA 85(23), 1988, cc. 8998-9002; Nucleic Acids Res. 17(8), 1989, cc. 2919-2932). При таком процессе синтеза кДНК соответствующие описанные ниже сайты, распознаваемые рестриктазами, можно интродуцировать на оба конца кДНК.
Представляющий интерес фрагмент кДНК очищают из полученного ПЦР-продукта и затем его встраивают путем лигирования в ДНК-вектор. Таким путем создают рекомбинантный вектор и интродуцируют в Е. coli или подобного хозяина. После селекции колоний требуемый рекомбинантный вектор можно получать из колониеобразующих Е. coli. Затем с использованием известного метода, такого как дидезокси-метод (метод терминации нуклеотидной цепи), определяют, имеет ли рекомбинантный вектор представляющую интерес нуклеотидную последовательность кДНК.
5'-RACE-метод, в котором используют праймеры для амплификации гена вариабельной области, как правило, применяют для выделения гена, кодирующего вариабельную область. Сначала конструируют библиотеку кДНК, применяемую для 5'-RACE (5'-RACE-библиотека кДНК) с использованием РНК, экстрагированных из клеток гибридомы, в качестве матрицы. Для синтеза 5'-RACE-библиотеки кДНК можно использовать поступающий в продажу набор, такой как набор для амплификации кДНК SMART RACE.
Ген антитела амплифицируют с помощью ПЦР, используя полученную 5'-RACE-библиотеку кДНК в качестве матрицы. Праймеры для амплификации гена мышиного антитела можно создавать на основе известных генных последовательностей антител. Нуклеотидные последовательности праймеров варьируются в зависимости от подкласса иммуноглобулина. Таким образом, предпочтительно предварительно определять подкласс с помощью доступного набора, такого как набор для изотипирования мышиных моноклональных антител Iso Strip (Iso Strip mouse monoclonal antibody isotyping kit) (фирма Roche Diagnostics).
В частности, например, для выделения генов, кодирующих мышиный IgG, можно применять праймеры, которые обеспечивают амплификацию генов, кодирующих тяжелые цепи γ1, γ2а, γ2b и γ3 и легкие цепи κ и λ. В целом, праймер, сайт гибридизации («отжига») которого с константной областью расположен вблизи вариабельной области, применяют в качестве 3'-концевого праймера для амплификации гена вариабельной области IgG. При этом праймер, присоединенный к набору конструкций 5' RACE-библиотеки кДНК, применяют в качестве 5'-концевого праймера.
Амплифицированные таким образом ПЦР-продукты применяют для реконструирования иммуноглобулинов, состоящих из комбинации тяжелых и легких цепей. Требуемое антитело можно отбирать, используя в качестве показателя GPC3-связывающую активность реконструированного иммуноглобулина. Например, когда задачей является выделение антитела к GPC3, то более предпочтительно, чтобы связывание антитела с GPC3 являлось специфическим. Можно осуществлять скрининг GPC3-связывающих антител, например, с использованием следующих стадий, на которых:
(1) приводят в контакт экспрессирующую GPC3 клетку с антителом, содержащим V-область, которая кодируется кДНК, выделенной из гибридомы;
(2) определяют связывание антитела с экспрессирующей GPC3 клеткой; и
(3) отбирают антитело, которое связывается с экспрессирующей GPC3 клеткой.
Методы определения связывания антитела с экспрессирующими GPC3 клетками, являются известными. В частности, связывание антитела с экспрессирующими GPC3 клетками можно определять с помощью описанных выше методик, таких как FACS. Иммобилизованные образцы экспрессирующих GPC3 клеток можно применять для оценки связывающей активности антитела.
Предпочтительные методы скрининга антител, в которых используют связывающую активность в качестве показателя, включают также методы пэннинга, основанные на использовании фаговых векторов. Методы скрининга с использованием фаговых векторов имеют преимущество, когда гены антитела выделяют из библиотек подкласса тяжелой цепи и легкой цепи из популяции клеток, экспрессирующих поликлональные антитела. Гены, кодирующие вариабельные области тяжелой цепи и легкой цепи, можно сшивать с помощью приемлемой линкерной последовательности с образованием одноцепочечного Fv (scFv). Фаги, презентирующие на своей поверхности scFv, можно получать путем встраивания гена, кодирующего scFv, в фаговый вектор. Фаги приводят в контакт с представляющим интерес антигеном. Затем ДНК, кодирующую scFv, который обладает представляющей интерес связывающей активностью, можно выделять путем сбора фагов, связанных с антигеном. Указанный процесс можно повторять при необходимости для обогащения scFv, которые обладают представляющей интерес связывающей активностью.
После выделения кДНК, кодирующей V-область представляющего интерес антитела к GPC3, кДНК расщепляют рестриктазами, которые распознают сайты рестрикции, интродуцированные в оба конца кДНК. Предпочтительные рестриктазы распознают и расщепляют нуклеотидную последовательность, которая встречается с низкой частотой в нуклеотидной последовательности гена антитела. Кроме того, для встраивания однокопийного расщепленного фрагмента в правильной ориентации предпочтительно интродуцируют в представляющий интерес вектор сайт рестрикции для фермента, который образует «липкий» конец. Кодирующую V-область антитела к GPC3 кДНК расщепляют согласно описанному выше методу и встраивают в приемлемый экспрессионный вектор для создания экспрессионного вектора антитела. В том случае, когда ген, кодирующий константную область (С-область) антитела, и ген, кодирующий указанную выше V-область, сливают в рамке считывания, то получают химерное антитело. В контексте настоящего описания «химерное антитело» означает, что константная область и вариабельная область отличаются по своему происхождению. Так, помимо мышиных/человеческих гетерохимерных антител к химерным антителам, предлагаемым в настоящем изобретении, относятся также человеческие/человеческие аллохимерные антитела. Экспрессионный вектор химерного антитела можно создавать путем встраивания указанного выше гена V-области в экспрессионный вектор, который уже содержит константную область. В частности, например,
последовательность, распознаваемую рестриктазой, которая вырезает указанный выше ген V-области, предпочтительно следует помещать в 5'-область экспрессионного вектора, несущего ДНК, которая кодирует константную область (С-область) требуемого антитела. Экспрессионный вектор химерного антитела создают путем слияния в рамке считывания двух генов, расщепленных одной и той же комбинацией рестриктаз.
Для получения моноклонального антитела к GPC3 гены антитела встраивают в экспрессионный вектор таким образом, чтобы экспрессия генов происходила под контролем регулирующей экспрессию области. Регулирующая экспрессию область, предназначенная для экспрессии антител, включает, например, энхансеры и промоторы. Кроме того, соответствующую сигнальную последовательность можно присоединять к аминоконцу таким образом, чтобы антитело секретировалось из клеток наружу. В приведенных для справки примерах в качестве сигнальной последовательности применяют пептид, который имеет аминокислотную последовательность
 . Наряду с ней можно присоединять другие приемлемые сигнальные последовательности. Экспрессированный полипептид расщепляется на карбоксильном конце указанной выше последовательности и образовавшийся полипептид секретируется из клеток наружу в виде зрелого полипептида. Затем приемлемые клетки-хозяева трансформируют экспрессионным вектором и получают рекомбинантные клетки, экспрессирующие ДНК, которая кодирует антитело к GPC3.
. Наряду с ней можно присоединять другие приемлемые сигнальные последовательности. Экспрессированный полипептид расщепляется на карбоксильном конце указанной выше последовательности и образовавшийся полипептид секретируется из клеток наружу в виде зрелого полипептида. Затем приемлемые клетки-хозяева трансформируют экспрессионным вектором и получают рекомбинантные клетки, экспрессирующие ДНК, которая кодирует антитело к GPC3.
ДНК, которые кодируют тяжелую цепь антитела (Н-цепь) и легкую цепь антитела (L-цепь), встраивают по отдельности в различные экспрессионные векторы для экспрессии гена антитела. Молекулу антитела, имеющую Н- и L-цепи, можно экспрессировать, осуществляя для этой цели контрансфекцию одной и той же клетки-хозяина векторами, в которые встроены соответственно гены Н-цепи и L-цепи. В качестве альтернативы, клетки-хозяева можно трансформировать одним экспрессионным вектором, в который встроены ДНК, кодирующие Н- и L-цепи (см. WO 94/1 1523).
Известны различные комбинации клеток-хозяев/экспрессионных векторов для получения антитела путем интродукции выделенных генов антител в соответствующих хозяев. Все эти системы экспрессии можно применять для выделения антигенсвязывающих доменов, включая вариабельные области антитела, предлагаемого в настоящем изобретении. Приемлемыми эукариотическими клетками, которые применяют в качестве клеток-хозяев, являются клетки животных, клетки растений и клетки грибов. В частности, клетки животных представляют собой, например, следующие клетки:
(1) клетки млекопитающих: СНО, COS, миеломы, почки детеныша хомяка (BHK), HeLa, Vero или т.п.;
(2) клетки амфибий: ооциты шпорцевой лягушки (Xenopus) или т.п. и
(3) клетки насекомых: sf9, sf21, Tn5 или т.п.
Кроме того, в качестве растительной клетки известна система экспрессии генов антитела, в которой используют клетки, полученные из представителей рода Nicotiana, например, Nicotiana tabacum. Для трансформации растительных клеток можно применять культивированные клетки каллуса.
Кроме того, следующие клетки можно применять в качестве грибных клеток:
дрожжи: рода Saccharomyces, например, Saccharomyces cerevisiae, и рода Pichia, например, Pichia pastoris, и
нитчатые грибы: рода Aspergillus, например, Aspergillus niger.
Кроме того, известны системы экспрессии генов антитела, в которых используют прокариотические клетки. Например, согласно настоящему изобретению можно применять бактериальные клетки, т.е. клетки Е. coli, клетки Bacillus subtilis и т.п. Экспрессионные векторы, которые несут представляющие интерес гены антитела, интродуцируют в эти клетки путем трансфекции. Трансфектированные клетки культивируют in vitro, и требуемое антитело можно получать из культуры трансформированных клеток.
Помимо указанных выше клеток-хозяев для получения рекомбинантного антитела можно применять также трансгенных животных. Это означает, что антитело можно получать из животного, в организм которого интродуцирован ген, кодирующий представляющее интерес антитело. Например, ген антитела можно создавать в виде слитого гена посредством встраивания в рамке считывания в ген, который кодирует белок, специфически образующийся в молоке. В качестве белка, секретируемого в молоко, можно применять, например, козий β-казеин. ДНК-фрагменты, содержащие слитый ген, в который входит ген антитела, инъецируют в эмбрион козы и затем этот эмбрион интродуцируют в самку козы. Требуемые антитела можно получать в виде белка, слитого с молочным белком из молока трансгенной козы, родившейся от козы, являющейся реципиентом эмбриона (или ее потомства). Кроме того, для увеличения объема молока, содержащего требуемое антитело, которое продуцируется трансгенной козой, трансгенной козе можно при необходимости вводить гормоны (Ebert K. M. и др., Bio/Technology 12 (7), 1994, сс. 699-702).
Когда антигенсвязывающую молекулу, представленную в настоящем описании, вводят человеку, то в качестве домена антигенсвязывающей молекулы можно применять домен, происходящий из антитела, полученного путем генетической рекомбинации, которое искусственно модифицировано для снижения гетерологичной антигенности в отношении человека и других животных. Указанные антитела, полученные путем генетической рекомбинации, включают, например, гуманизированные антитела. Эти модифицированные антитела можно получать с помощью известных методов.
Вариабельная область антитела, применяемая для получения домена антигенсвязывающей молекулы, который включает вариабельную область антитела, представленного в настоящем описании, как правило, состоит из трех гипервариабельных участков (CDR), разделенных четырьмя каркасными участками (FR). CDR представляет собой область, которая в значительной степени определяет специфичность связывания антитела. Для аминокислотных последовательностей CDR характерна высокая степень вариабельности. С другой стороны, образующие FR аминокислотные последовательности часто обладают высокой идентичностью даже среди антител с различными специфичностями связывания. Таким образом, как правило, путем трансплантации CDR специфичность связывания конкретного антитела можно интродуцировать в другое антитело.
Гуманизированное антитело называют также реконструированным человеческим антителом. В частности, известны гуманизированные антитела, полученные путем трансплантации CDR антитела животного кроме человека, такого как мышиное антитело, в человеческое антитело и т.п. Известны также общепринятые методики генной инженерии, предназначенные для получения гуманизированных антител. В частности, например, ПЦР с перекрывающимися праймерами представляет собой известный метод трансплантации CDR мышиного антитела в человеческий FR. При осуществлении ПЦР с перекрывающимися праймерами нуклеотидную последовательность, которая кодирует CDR мышиного антитела, подлежащий трансплантации, добавляют к праймерам, предназначенным для синтеза FR человеческого антитела. Получают праймеры для каждого из четырех FR. Принято считать, что когда осуществляют трансплантацию мышиного CDR в человеческий FR, то для поддержания функции CDR целесообразно выбирать человеческий FR, обладающий высоким уровнем идентичности с мышиным FR. Таким образом, как правило, является предпочтительным применять человеческий FR, который содержит аминокислотную последовательность, обладающую высоким уровнем идентичности с аминокислотной последовательностью FR, который примыкает к подлежащему трансплантации мышиному CDR.
Нуклеотидные последовательности, подлежащие лигированию, создают таким образом, чтобы они были соединены друг с другом в рамке считывания. Человеческие FR синтезируют индивидуально с использованием соответствующих праймеров. В результате получают продукты, в которых ДНК, кодирующая мышиный CDR, присоединена к ДНК, кодирующим индивидуальные FR. Нуклеотидные последовательности, кодирующие мышиный CDR каждого продукта, создают таким образом, чтобы они перекрывались друг с другом. Затем осуществляют реакцию синтеза комплементарной цепи для «отжига» перекрывающихся CDR-участков продуктов, синтезированных с использованием гена человеческого антитела в качестве матрицы. С помощью этой реакции человеческие FR встраивают путем лигирования через мышиные CDR-последовательности.
Полноразмерный ген V-области, в которую, в конце концов, лигированы три CDR и четыре FR, амплифицируют с использованием праймеров, гибридизующихся с 5'- или 3'-концом, которые добавляют с последовательностями, распознаваемыми приемлемыми рестриктазами. Экспрессионный вектор для гуманизированного антитела можно получать путем встраивания полученной согласно описанному выше методу ДНК и ДНК, которая кодирует С-область человеческого антитела, в экспрессионный вектор таким образом, чтобы лигировать их в рамке считывания. После трансфекции хозяина рекомбинантным вектором для создания рекомбинантных клеток рекомбинантные клетки культивируют и ДНК, кодирующую гуманизированное антитело, экспрессируют с получением гуманизированного антитела в культуре клеток (см. публикацию европейского патента ЕР 239400 и публикацию международной заявки на патент WO 1996/002576).
Путем качественной или количественной оценки и измерения антигенсвязывающей активности гуманизированного антитела, полученного согласно описанному выше методу, можно отбирать FR человеческого антитела, которые позволяют CDR образовывать предпочтительный антигенсвязывающий центр при лигировании с использованием CDR. Аминокислотные остатки в FR при необходимости можно заменять так, чтобы CDR реконструированного человеческого антитела образовывали приемлемый антигенсвязывающий центр. Например, мутации аминокислотной последовательности можно интродуцировать в FR, используя ПЦР-метод, применяемый для трансплантации мышиного CDR в человеческий FR. Более конкретно, мутации неполной нуклеотидной последовательности можно интродуцировать в праймеры, гибридизующиеся с FR. Мутации нуклеотидной последовательности интродуцируют в FR, синтезированные с использованием указанных праймеров. Мутантные последовательности FR, имеющие требуемые характеристики, можно отбирать путем измерения и оценки активности мутантного антитела с аминокислотной заменой в отношении связывания с антигеном с помощью упомянутого выше метода (Sato K. и др., Cancer Res. 53, 1993, сс. 851-856).
В качестве альтернативы, требуемые человеческие антитела можно получать путем иммунизации трансгенных животных, имеющих полный спектр генов человеческого антитела (см. публикации международных заявок на патент WO 1993/012227; WO 1992/003918; WO 1994/002602; WO 1994/025585; WO 1996/034096; WO 1996/033735), с использованием ДНК-иммунизации.
Кроме того, известны методики получения человеческих антител путем пэннинга с использованием библиотек человеческих антител. Например, V-область человеческого антитела экспрессируют в виде одноцепочечного антитела (scFv) на поверхности фага с использованием метода фагового дисплея. Можно отбирать фаги, экспрессирующие scFv, который связывается с антигеном. Последовательность ДНК, кодирующую V-область человеческого антитела, которая связывается с антигеном, можно определять путем анализа генов отобранных фагов. Определяют последовательность ДНК scFv, который связывается с антигеном. Экспрессионный вектор можно получать путем слияния последовательности V-области в рамке считывания с последовательностью С-области требуемого человеческого антитела и последующего встраивания в приемлемый экспрессионный вектор. Экспрессионный вектор интродуцируют в клетки, пригодные для указанной выше экспрессии. Человеческое антитело можно получать путем экспрессии гена, кодирующего человеческое антитело, в клетках. Такие методы уже описаны (см. публикации международных заявок на патент WO 1992/001047; WO 1992/020791; WO 1993/006213; WO 1993/011236; WO 1993/019172; WO 1995/001438; WO 1995/015388).
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3 (GPC3)
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3 (GPC3)» относится к области антитела, которая содержит область, которая специфически связывается с описанным выше белком GPC3 или со всем или с участком неполного пептида белка GPC3, и является также комплементарной ему. Домены, содержащие вариабельную область антитела, можно получать из вариабельных доменов одного или множества антител. Предпочтительно домены, содержащие вариабельную область антитела, содержат вариабельные области легкой цепи и тяжелой цепи (VL и VH) антитела. Приемлемыми примерами таких доменов, содержащих вариабельные области антитела, являются «одноцепочечный Fv (scFv)», «одноцепочечное антитело», «Fv», «одноцепочечный Fv2 (scFv2)», «Fab», «F(ab')2» и т.д.
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора» относится к области антитела, которая содержит область, которая специфически связывается со всем или с участком комплекса Т-клеточного рецептора, и является также комплементарной ему. Комплекс Т-клеточного рецептора может представлять собой сам Т-клеточный рецептор или адапторную молекулу, которая входит в комплекс Т-клеточного рецептора наряду с Т-клеточным рецептором. Пригодной в качестве адапторной молекулы является CD3.
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении Т-клеточного рецептора
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении Т-клеточного рецептора» относится к области антитела, связывающейся с Т-клеточным рецептором, полученной путем включения области, которая специфически связывается со всем или с участком Т-клеточного рецептора и является также комплементарной ему.
Участок Т-клеточного рецептора, с которым связывается домен, предлагаемый в настоящем изобретении, может представлять собой вариабельную область или константную область, но предпочтительным является эпитоп, присутствующий в константной области. Примеры последовательности константной области включают α-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq. САА26636.1 (SEQ ID NO: 4), β-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq С25777 (SEQ ID NO: 5), γ1-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq А26659 (SEQ ID NO: 6), γ2-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq ААВ63312.1 (SEQ ID NO: 7), и δ-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq ААА61033.1 (SEQ ID NO: 8).
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении CD3 (CD3-связывающей активностью)
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении_CD3» относится к CD3-связывающему участку антитела, который получают путем включения области, которая специфически связывается со всем или с участком CD3, и который является также комплементарным ему.
Предпочтительно домен содержит вариабельные области легкой цепи и тяжелой цепи (VL и VH) антитела к CD3. Приемлемыми примерами такого домена являются «одноцепочечный Fv (scFv)», «одноцепочечное антитело», «Fv», «одноцепочечный Fv2 (scFv2)», «Fab», «F(ab')2» и т.д.
Предлагаемый в изобретении домен, содержащий вариабельную область антитела, которая обладает CD3-связывающей активностью, может представлять собой любой эпитопсвязывающий домен, если эпитоп присутствует в последовательности γ-цепи, δ-цепи или ε-цепи, образующей человеческий CD3. Предпочтительно в настоящем изобретении можно использовать домен, содержащий вариабельную область легкой цепи (VL) антитела к CD3, и вариабельную область тяжелой цепи (VH) антитела к CD3, которые связываются с эпитопом, присутствующим во внеклеточной области ε-цепи комплекса человеческого CD3. Помимо вариабельной области легкой цепи (VL) антитела к CD3, и вариабельной области тяжелой цепи (VH) антитела к CD3, которые описаны в разделе «Приведенные для справки примеры», известные CD3-связывающие домены, которые содержат вариабельную область легкой цепи (VL) антитела к CD3, и вариабельную область тяжелой цепи (VH) антитела к CD3 и полученные из антитела OKT3 (Proc. Natl. Acad. Sci. USA 77, 1980, сс. 4914-4917), можно применять в качестве указанных доменов. Соответственно можно применять содержащий вариабельную область антитела домен, полученный из антитела к CD3, которое обладает требуемыми свойствами, созданное путем иммунизации требуемого животного с использованием описанного выше метода γ-цепью, δ-цепью или ε-цепью, образующей человеческий CD3. Человеческие антитела и соответствующим образом гуманизированные антитела можно применять соответственно в качестве антитела к CD3 для создания домена, содержащего вариабельную область антитела, который обладает CD3-связывающей активностью. Что касается структуры γ-цепи, δ-цепи или ε-цепи, образующей человеческий CD3, то их полинуклеотидные последовательности представлены в SEQ ID NO: 9 (NM_000073.2), 10 (NM_000732.4) и 11 (NM_000733.3), а их полипептидные последовательности представлены в SEQ ID NO: 12 (NP 000064.1), 13 (NP 000723.1) и 14 (NP_000724.1) (в скобках указаны регистрационные номера в базе данных RefiSeq).
Домены, содержащие вариабельные области антитела, в антигенсвязывающих молекулах, предлагаемых в настоящем изобретении, могут связываться с одним и тем же эпитопом. В контексте настоящего описания один и тот же эпитоп может присутствовать в белке, который содержит аминокислотную последовательность SEQ ID NO: 2 или 14. Альтернативно этому, домены, содержащие вариабельные области антитела, в антигенсвязывающих молекулах, предлагаемых в настоящем изобретении, могут связываться с различными эпитопами соответственно. В контексте настоящего описания различные эпитопы могут присутствовать в белке, который содержит аминокислотную последовательность SEQ ID NO: 2 или 14.
Специфичность
Понятие «специфичность» означает, что одна из молекул, участвующих в специфическом связывании, не обладает какой-либо значимой способностью связываться с молекулами, отличными от одного или нескольких партнеров по связыванию молекул. Кроме того, понятие используют также, когда домен, содержащий вариабельную область антитела, является специфическим в отношении конкретного эпитопа из нескольких эпитопов, входящих в антиген. Когда эпитоп, с которым связывается домен, содержащий вариабельную область антитела, входит в несколько различных антигенов, то антигенсвязывающие молекулы, содержащие домен, включающий вариабельную область, могут связываться с различными антигенами, которые содержат эпитоп.
Эпитоп
«Эпитоп» означает антигенную детерминанту в антигене и относится к антигенному сайту, с которым связывается представленный в настоящем описании домен антигенсвязывающей молекулы, включающий вариабельную область антитела. Так, например, эпитоп можно характеризовать на основе его структуры. Альтернативно этому, эпитоп можно характеризовать на основе антигенсвязывающей активности антигенсвязывающей молекулы, которая распознает эпитоп. Когда антиген представляет собой пептид или полипептид, то эпитоп можно определять по аминокислотным остаткам, образующим эпитоп. Альтернативно этому, когда эпитоп представляет собой сахарную цепь, то эпитоп можно определять по специфической для него структуре сахарной цепи.
Линейный эпитоп представляет собой эпитоп, который содержит эпитоп, у которого распознается первичная аминокислотная последовательность. Указанный линейный эпитоп, как правило, содержит по меньшей мере три и наиболее часто по меньшей мере пять, например, примерно от 8 до 10 или от 6 до 20 аминокислотных остатков в определенной последовательности.
В отличие от линейного эпитопа «конформационный эпитоп» представляет собой эпитоп, в котором первичная аминокислотная последовательность, образующая эпитоп, не является единственной детерминантой распознаваемого эпитопа (например, не является обязательным, чтобы первичная аминокислотная последовательность конформационного эпитопа распознавалась специфическим в отношении эпитопа антителом). Конформационные эпитопы могут содержать большее количество аминокислотных остатков по сравнению с линейными эпитопами. Распознающее конформационный эпитоп антитело распознает трехмерную структуру пептида или белка. Например, когда белковая молекула уложена и образует трехмерную структуру, аминокислоты и/или полипептидные основные цепи, которые образуют конформационный эпитоп, выравниваются, и эпитоп становится распознаваемым для антитела. Методы определения конформаций эпитопов включают (но, не ограничиваясь только ими), например, рентгеновскую кристаллографию, двухмерный ядерный магнитный резонанс, сайтспецифическое спиновое мечение и электронный парамагнитный резонанс (см., например, Epitope Mapping Protocols in Methods in Molecular Biology, под ред. Morris, т. 66, 1996).
Пример метода оценки связывания эпитопа тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, описан ниже, и метод, подтверждающий связывание с эпитопом тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, можно осуществлять также согласно приведенным ниже примерам.
Например, для подтверждения того, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает линейный эпитоп в молекуле GPC3, можно применять описанный ниже метод. Для указанной выше цели синтезируют линейный пептид, содержащий аминокислотную последовательность, образующую внеклеточный домен GPC3. Пептид можно синтезировать химически. Альтернативно этому, его можно получать с помощью методов генной инженерии, используя область в кДНК GPC3, которая кодирует аминокислотную последовательность, соответствующую внеклеточному домену. Затем оценивают связывающую активность между линейным пептидом, который содержит аминокислотную последовательность, образующую внеклеточный домен, и тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью. Например, иммобилизованный линейный пептид можно применять в качестве антигена при осуществлении ELISA для оценки связывающей активности антигенсвязывающей молекулы в отношении пептида. Альтернативно этому, связывающую активность в отношении линейного пептида можно оценивать по уровню ингибирования линейным пептидом связывания антигенсвязывающей молекулы с экспрессирующими GPC3 клетками. Эти анализы могут демонстрировать связывающую активность антигенсвязывающих молекул в отношении линейного пептида.
Кроме того, для подтверждения того, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает трехмерную структуру эпитопа, можно применять следующий метод. Для указанной выше цели получают экспрессирующие GPC3 клетки. Считается, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает конформационный эпитоп, если она при контакте отличается сильным связыванием с экспрессирующими GPC3 клетками, но в незначительной степени связывается с иммобилизованным линейным пептидом, который содержит аминокислотную последовательность, образующую внеклеточный домен GPC3. В контексте настоящего описания «связывается в незначительной степени» означает, что активность связывания составляет 80% или менее, как правило, 50% или менее, предпочтительно 30% или менее и наиболее предпочтительно 15% или менее по сравнению с активностью связывания с клетками, экспрессирующими человеческий GPC3.
Методы анализа связывающей активности тестируемой антигенсвязывающей молекулы, содержащей домен, который связывается с антигеном GPC3, в отношении экспрессирующих GPC3 клеток, включают, например, методы, описанные в: Antibodies: A Laboratory Manual (под ред. Harlow, David Lane, изд-во Cold Spring Harbor Laboratory, 1988, cc. 359-420). В частности, оценку можно осуществлять на основе принципа ELISA или метода разделения клеток на основе возбуждения флуоресценции (FACS) с использованием в качестве антигена экспрессирующих GPC3 клеток.
В формате ELISA связывающую активность тестируемой антигенсвязывающей молекулы, содержащей домен, который связывается с антигеном GPC3, в отношении экспрессирующих GPC3 клеток, можно оценивать количественно путем сравнения уровней сигналов, возникающих в процессе ферментативной реакции. В частности, тестируемую антигенсвязывающую молекулу добавляют в планшет для ELISA, на котором иммобилизованы экспрессирующие GPC3 клетки. Затем тестируемую антигенсвязывающую молекулу, связанную с клетками, выявляют с помощью меченного ферментом антитела, которое распознает тестируемую антигенсвязывающую молекулу. Альтернативно этому, когда применяют FACS, приготавливают серийные разведения тестируемой антигенсвязывающей молекулы и титр антитела, связывающегося с экспрессирующими GPC3 клетками, можно определять путем сравнения активности связывания с экспрессирующими GPC3 клетками.
Связывание тестируемой антигенсвязывающей молекулы с антигеном, который экспрессируется на поверхности клеток, суспендированных в буфере или в сходной среде, можно выявлять с помощью проточного цитометра. Известными проточными цитометрами являются, например, следующие устройства:
FACSCanto™ II,
FACSAria™,
FACSArray™,
FACSVantage™ SE
FACSCalibur™ (все товарные знаки фирмы BD Biosciences),
EPICS ALTRA HyPerSort,
Cytomics FC 500,
EPICS XL-MCL ADC EPICS XL ADC,
Cell Lab Quanta/Cell Lab Quanta SC (все товарные знаки фирмы Beckman Coulter).
Предпочтительные методы анализа связывающей активности тестируемой антигенсвязывающей молекулы, содержащей связывающей антиген GPC3 домен, в отношении антигена включают, например, следующий метод. Сначала экспрессирующие GPC3 клетки подвергают взаимодействию с тестируемой антигенсвязывающей молекулой, а затем ее окрашивают меченным с помощью ФИТЦ вторичным антителом, которое распознает полипептидный комплекс. Тестируемую антигенсвязывающую молекулу соответствующим образом разводят приемлемым буфером с получением комплекса в требуемой концентрации. Например, комплекс можно применять в концентрации, составляющей от 10 мкг/мл до 10 нг/мл. Затем определяют интенсивность флуоресценции и количество клеток с помощью FACSCalibur (фирма BD). Интенсивность флуоресценции, определенная с помощью анализов на основе программы CELL QUEST (фирма BD), а именно, выраженная в виде средних геометрических значений, отражает уровень связывания антитела с клетками. Это означает, что активность связывания тестируемой антигенсвязывающей молекулы, которая характеризуется количеством связанной тестируемой антигенсвязывающей молекулы, можно оценивать, определяя среднее геометрическое значение.
Имеет ли тестируемая антигенсвязывающая молекула, которая содержит домен, связывающий антиген GPC3, общий эпитоп с другой
антигенсвязывающей молекулой, можно оценивать по конкуренции между двумя комплексами в отношении одного и того же эпитопа. Конкуренцию между антигенсвязывающими молекулами можно определять путем анализа перекрестной блокады или с помощью сходного анализа. Например, предпочтительным анализом перекрестной блокады является конкурентный ELISA-анализ.
В частности, при осуществлении анализа перекрестной блокады белок GPC3, иммобилизованный в лунках титрационного микропланшета, предварительно инкубируют в присутствии антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, или без нее, а затем вносят тестируемую антигенсвязывающую молекулу. Количество связанной с белком GPC3 тестируемой антигенсвязывающей молекулы в лунках находится в обратной корреляции с активностью связывания антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, который конкурирует за связывание с одним и тем же эпитопом. Это означает, что чем выше аффинность антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, к одному и тому же эпитопу, тем ниже активность связывания тестируемой антигенсвязывающей молекулы с сенсибилизированными белком GPC3 лунками.
Количество тестируемой антигенсвязывающей молекулы, связанной через белок GPC3 с лунками, легко определять путем предварительного мечения антигенсвязывающей молекулы. Например, меченную биотином антигенсвязывающую молекулу оценивают с использованием конъюгата авидин/пероксидаза и соответствующего субстрата. В частности, анализ перекрестной блокады, в котором применяют в качестве меток ферменты, такие как пероксидаза, называют «ELISA-анализом в конкурентных условиях (конкурентный анализ)». Антигенсвязывающую молекулу можно метить также с помощью других предназначенных для мечения субстанций, которые можно выявлять или оценивать. В частности, известны радиоактивные метки, флуоресцентные метки и т.п.
Когда антигенсвязывающая молекула, рассматриваемая в качестве конкурента-кандидата, может блокировать связывание тестируемой антигенсвязывающей молекулы, которая содержит домен, связывающий антиген GPC3, по меньшей мере на 20%, предпочтительно по меньшей мере на 20-50% и предпочтительно по меньшей мере на 50% по сравнению со связывающей активностью, установленной в контрольном эксперименте, который проводят в отсутствии антигенсвязывающей молекулы, рассматриваемой в качестве конкурента, то считается, что для тестируемой антигенсвязывающей молекулы характерна выраженная способность к связыванию с тем же эпитопом, с которым связывается антигенсвязывающая молекула, рассматриваемая в качестве конкурента, или она конкурирует за связывание с тем же самым эпитопом.
Если структура эпитопа, связанного с тестируемой антигенсвязывающей молекулой, которая содержит домен, связывающий антиген GPC3, уже идентифицирована, то для решении вопроса о том, имеют ли тестируемая и контрольная антигенсвязывающие молекулы один и тот же эпитоп, можно сравнивать связывающие активности двух антигенсвязывающих молекул с пептидом, полученным путем интродукции аминокислотных мутаций в пептид, образующий эпитоп.
Для оценки указанных выше связывающих активностей, например, сравнивают связывающие активности тестируемой и контрольной антигенсвязывающих молекул с линейным пептидом, в который интродуцирована мутация, с помощью указанного выше формата ELISA. Помимо метода ELISA связывающую активность в отношении мутантного пептида, связанного с колонкой, можно определять, пропуская через колонку тестируемую и контрольную антигенсвязывающую молекулу и затем оценивая количество антигенсвязывающей молекулы, элюированной в раствор для элюции. Известны методы адсорбции мутантного пептида на колонке, например, в форме слитого с GST пептида.
Альтернативно этому, когда идентифицированный эпитоп представляет собой конформационный эпитоп, то для решения вопроса о том, имеют ли тестируемая и контрольная антигенсвязывающие молекулы общий эпитоп, можно применять следующий метод. Сначала получают экспрессирующие GPC3 клетки и клетки, экспрессирующие GPC3 с мутацией, интродуцированной в эпитоп. Тестируемую и контрольную молекулы добавляют в клеточную суспензию, полученную путем суспендирования этих клеток в приемлемом буфере, таком как ЗФР. Затем клеточные суспензии соответствующим образом промывают буфером и добавляют меченное с помощью ФИТЦ антитело, которое распознает тестируемую и контрольную антигенсвязывающие молекулы. Определяют интенсивность флуоресценции и количество клеток, окрашенных меченым антителом, используя FACSCalibur (фирма BD). Тестируемый и контрольный полипептидные комплексы соответствующим образом разводят приемлемым буфером и применяют в требуемой концентрации. Например, их можно применять в концентрации от 10 мкг/мл до 10 нг/мл. Интенсивность флуоресценции определяют с помощью анализа, для оценки результатов которого применяют программу CELL QUEST (фирма BD), а именно, определяют среднее геометрическое значение, которое отражает количество меченого антитела, связанного с клетками. Это означает, что связывающие активности тестируемой и контрольной антигенсвязывающих молекул, которые характеризуются количеством связанного меченого антитела, можно определять, оценивая среднее геометрическое значение.
При осуществлении описанного выше метода для решения вопроса о том, характерно ли для антигенсвязывающей молекулы «незначительное связывание с клетками, которые экспрессируют мутантный GPC3», можно применять, например, следующий метод. Сначала тестируемую и контрольную антигенсвязывающие молекулы, связанные с клетками, которые экспрессируют мутантный GPC3, окрашивают меченым антителом. Затем определяют интенсивность флуоресценции в клетках. Когда для оценки флуоресценции используют проточный цитометр, то интенсивность флуоресценции можно анализировать с помощью программы CELL QUEST. На основе средних геометрических значений в присутствии антигенсвязывающей молекулы и без нее можно рассчитывать согласно приведенной ниже формуле используемое для сравнения значение (ΔGeo-Mean), характеризующее степень увеличения интенсивности флуоресценции в результате связывания с антигенсвязывающей молекулой.
ΔGeo-Mean=Geo-Mean (в присутствии антигенсвязывающей молекулы)/Geo-Mean (в отсутствии антигенсвязывающей молекулы)
Используемое для сравнения среднее геометрическое значение (значение ΔGeo-Mean для мутантной молекулы GPC3), определенное с помощью описанного выше анализа, которое отражает количество тестируемой антигенсвязывающей молекулы, связанной с клетками, которые экспрессируют мутантный GPC3, сравнивают с относительным значением ΔGeo-Mean, которое отражает количество тестируемой антигенсвязывающей молекулы, связанной с экспрессирующими GPC3 клетками. В этом случае концентрации тестируемой антигенсвязывающей молекулы, применяемые для определения относительных значений ΔGeo-Mean для экспрессирующих GPC3 клеток и клеток,
экспрессирующих мутантный GPC3, наиболее предпочтительно регулируют таким образом, чтобы они были одинаковыми или практически одинаковыми. Антигенсвязывающую молекулу, для которой подтверждена способность распознавать эпитоп в GPC3, применяют в качестве контрольной антигенсвязывающей молекулы.
Если используемое для сравнения значение ΔGeo-Mean тестируемой антигенсвязывающей молекулы в отношении клеток, экспрессирующих мутантный GPC3, ниже чем используемое для сравнения значение ΔGeo-Mean тестируемой антигенсвязывающей молекулы в отношении клеток, экспрессирующих GPC3, по меньшей мере на 80%, предпочтительно на 50%, более предпочтительно на 30% и наиболее предпочтительно на 15%, то считают, что тестируемая антигенсвязывающая молекула «незначительно связывается с клетками, которые экспрессируют мутантный GPC3». Формула определения значения Geo-Mean (среднее геометрическое значение) описана в руководстве по применению программы CELL QUEST (фирма BD biosciences). Когда путем сравнения установлено, что относительные значения являются практически эквивалентными, то можно считать, что тестируемая и контрольная антигенсвязывающие молекулы имеют одинаковый эпитоп.
Вариабельный фрагмент (Fv)
В контексте настоящего описания понятие «вариабельный фрагмент (Fv)» относится к минимальной единице полученного из антитела антигенсвязывающего домена, который состоит из пары, включающей вариабельную область легкой цепи антитела (VL) и вариабельную область тяжелой цепи антитела (VH). В 1988 г. Skerra и Pluckthun обнаружили, что гомогенные и активные антитела можно получать из периплазматической фракции Е. coli путем встраивания гена антитела по ходу транскрипции относительно бактериальной сигнальной последовательности и индукции экспрессии гена в Е. coli (Science 240(4855), 1988, сс. 1038-1041). В Fv, полученном из периплазматической фракции, VH ассоциируется с VL таким образом, чтобы связываться с антигеном.
Согласно настоящему описанию Fv предпочтительно включает, например, пару Fv, которые представляют собой антигенсвязывающую молекулу или т.п., содержащую:
(1) двухвалентный антигенсвязывающий домен, который представляет собой двухвалентный scFv, в котором один одновалентный scFv двухвалентного scFv сцеплен с одним полипептидом, образующим Fc-домен, посредством тяжелой цепи Fv-фрагмента, образующего CD3-связывающий домен, а другой одновалентный scFv сцеплен с другим полипептидом, образующим Fc-домен, посредством легкой цепи Fv-фрагмента, образующего CD3-связывающий домен;
(2) домен, содержащий Fc-домен, который не обладает связывающей активностью в отношении Fcy-рецептора и который получен из аминокислот, образующих Fc-домен IgG1, IgG2a, IgG3 или IgG4, и
(3) по меньшей мере один одновалентный CD3-связывающий домен,
где легкая цепь и тяжелая цепь Fv-фрагментов в результате ассоциации образуют такой CD3-связывающий домен, который может связываться с антигеном CD3.
scFv, одноцепочечное антитело и sc(Fv)2
В контексте настоящего описания понятия «scFv», «одноцепочечное антитело» и «sc(Fv)2» все относятся к фрагменту антитела в виде одной полипептидной цепи, которая содержит вариабельные области, полученные из тяжелой и легкой цепей, но не содержит константную область. Как правило, одноцепочечное антитело содержит также полипептидный линкер между VH- и VL-доменами, позволяющий образовывать требуемую структуру, которая, вероятно, обеспечивает связывание антигена. Одноцепочечное антитело подробно описано у Pluckthun в: «The Pharmacology of Monoclonal Antibodies», т. 113, под ред. Rosenburg и Moore, изд-во Springer-Verlag, New York, 1994, cc. 269-315» (см. также публикацию международного патента WO 1988/001649; US №№4946778 и 5260203). В конкретном варианте осуществления изобретения одноцепочечное антитело может быть биспецифическим и/или гуманизированным.
scFv представляет собой антигенсвязывающий домен, в котором VH и VL, образующие Fv, сцеплены друг с другом с помощью пептидного линкера (Proc. Natl. Acad. Sci. U.S.A. 85(16), 1988, cc. 5879-5883). VH и VL могут удерживаться в непосредственной близости с помощью пептидного линкера.
sc(Fv)2 представляет собой одноцепочечное антитело, в котором четыре вариабельные области двух VL и двух VH сцеплены линкерами такими как пептидные линкеры, с образованием одной цепи (J Immunol. Methods 231(1-2), 1999, cc. 177-189). Две VH и две VL можно получать из различных моноклональных антител. Указанные sc(Fv)2 предпочтительно включают, например, биспецифический sc(Fv)2, распознающий два эпитопа, которые присутствуют в одном антигене, что описано в Journal of Immunology 152(11), 1994, cc. 5368-5374. sc(Fv)2 можно получать методами, известными специалистам в данной области. Например, sc(Fv)2 можно получать путем связывания scFv с помощью линкера, такого как пептидный линкер.
Согласно настоящему описанию к форме антигенсвязывающего домена, образующего sc(Fv)2, относится антитело, в котором две единицы VH и две единицы VL организованы в следующем порядке: VH, VL, VH и VL ([VH]-линкер-[VL]-линкер-[VH]-линкер-[VL]), начиная с N-конца одноцепочечного полипептида. Порядок расположения двух единиц VH и двух единиц VL не ограничен указанной выше формой, и их можно организовывать в любом порядке. Пример порядка расположения в различных формах приведен ниже.
[VL]-линкер-[VH]-линкер-[VH]-линкер-[VL],
[VH]-линкер-[VL]-линкер-[VL]-линкер-[VH],
[VH]-линкер-[VH]-линкер-[VL]-линкер-[VL],
[VL]-линкер-[VL]-линкер-[VH]-линкер-[VH],
[VL]-линкер-[VH]-линкер-[VL]-линкер-[VH].
Молекулярная форма sc(Fv)2 подробно описана также в WO 2006/132352. Таким образом, согласно указанным описаниям специалисты в данной области могут получать требуемый sc(Fv)2, предназначенный для создания антигенсвязывающих молекул, представленных в настоящем описании.
Кроме того, антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, можно конъюгировать с полимером-носителем, таким как ПЭГ, или органическим соединением, таким как противораковое средство. Альтернативно этому, дополнительную последовательность сахарной цепи предпочтительно встраивают в полипептидные комплексы для того, чтобы сахарная цепь обеспечивала требуемое действие.
Линкеры, предназначенные для связывания вариабельных областей антитела, представляют собой произвольные пептидные линкеры, которые можно интродуцировать с помощью генной инженерии, и синтетические линкеры, описанные, например, в: Protein Engineering, 9(3), 1996, сс. 299-305. Однако для целей настоящего изобретения наиболее предпочтительными являются пептидные линкеры. Длина пептидных линкеров специально не ограничена, и специалисты в данной области могут выбирать ее в зависимости от поставленной задачи. Предпочтительная длина составляет пять или большее количество аминокислот (при этом, верхний предел составляет (но, не ограничиваясь только указанным), как правило, вплоть до 30 аминокислот или менее, предпочтительно 20 аминокислот или менее), и наиболее предпочтительно 15 аминокислот.Когда sc(Fv)2 содержит три пептидных линкера, то их длина может быть одинаковой или различной. Например, указанные пептидные линкеры включают:
Ser,
Gly⋅Ser,
Gly⋅Gly⋅Ser,
Ser⋅Gly⋅Gly,
Gly⋅Gly⋅GlySer (SEQ ID NO: 15)
Ser⋅Gly⋅Gly⋅Gly (SEQ ID NO: 16),
Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 17),
Ser⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 18),
Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 19),
Ser⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 20),
Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 21),
Ser⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 22),
(Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 17))n,
(Ser⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 18))n,
где n обозначает целое число от 1 или более. Специалисты в данной области могут выбирать длину или последовательности пептидных линкеров в зависимости от поставленной задачи.
Как правило, для перекрестного сшивания используют синтетические линкеры (химические перекрестносшивающие агенты), они представляют собой, например:
N-гидроксисукцинимид (NHS),
дисукцинимидилсуберат (DSS),
бис(сульфосукцинимидил)суберат (BS3),
дитиобис(сукцинимидилпропионат) (DSP),
дитиобис(сульфосукцинимидилпропионат) (DTSSP),
этиленгликольбис(сукцинимидилсукцинат) (EGS),
этиленгликольбис(сульфосукцинимидилсукцинат) (сульфо-EGS),
дисукцинимидилтартрат (DST), дисульфосукцинимидилтартрат (сульфо-DST),
бис[2-(сукцинимидоксикарбонилокси)этил]сульфон (BSOCOES) и
и бис[2-(сульфосукцинимидоксикарбонилокси)этил]сульфон (сульфо-BSOCOES). Эти перекрестносшивающие агенты поступают в продажу.
Как правило, требуется три линкера для соединения вместе четырех вариабельных областей антитела. Применяемые линкеры могут быть одного типа или различных типов.
Fab. F(ab')2 и Fab'
«Fab» состоит из одной легкой цепи и СН1-домена и вариабельной области из одной тяжелой цепи. Тяжелая цепь молекулы Fab не может образовывать дисульфидные мостики с тяжелой цепью другой молекулы.
«F(ab')2» или «Fab» получают обработкой иммуноглобулина (моноклональное антитело) протеазой, такой как пепсин и папаин, и они относятся к фрагменту антитела, получаемого расщеплением иммуноглобулина (моноклональное антитело) вблизи дисульфидных мостиков, присутствующих между шарнирными областями в каждой из двух Н-цепей. Например, папаин расщепляет IgG перед дисульфидными мостиками, присутствующими между шарнирными областями в каждой из двух Н-цепей, с образованием двух гомологичных фрагментов антитела, в которых L-цепь, содержащая VL (вариабельная область L-цепи), и CL (константная область L-цепи), сцеплены с фрагментом Н-цепи, содержащим VH (вариабельная область Н-цепи) и CHγ1 (γ1-область в константной области Н-цепи), через дисульфидный мостик в их С-концевых областях. Каждый из указанных двух гомологичных фрагментов антител обозначают как Fab'.
«F(ab')2» состоит из двух легких цепей и двух тяжелых цепей, содержащих в константной области СН1-домен и часть СН2-доменов, в результате между двумя тяжелыми цепями образуются дисульфидные мостики. F(ab')2,
образующий антигенсвязывающую молекулу, представленную в настоящем описании, предпочтительно можно получать следующим образом. Полное моноклональное антитело или сходное антитело, содержащее требуемый антигенсвязывающий домен, частично расщепляют протеазой, такой как пепсин; и Fc-фрагменты удаляют путем адсорбции на колонке с белком А. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять полное антитело с образованием F(ab')2 в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Fc-домен
Fc-домен, который образует антигенсвязывающую молекулу, представленную в настоящем описании, предпочтительно можно получать следующим образом. Антитело, такое как моноклональное антитело, частично расщепляют протеазой, такой как пепсин. Затем образовавшийся фрагмент адсорбируют на колонке с белком А или белком G и элюируют соответственным буфером для элюции. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять антитела, такие как моноклональные антитела, в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Антигенсвязывающие молекулы, представленные в настоящем описании, содержат Fc-домен с пониженной способностью связывать FCγ- рецептор, которые включают аминокислоты, образующие Fc-домен IgG1, IgG2, IgG3 или IgG4.
Изотип антитела определяют на основе структуры константной области. Константные области изотипов IgG1, IgG2, IgG3 и IgG4 обозначают как Сγ1, Сγ2, Сγ3 и Сγ4 соответственно. Аминокислотные последовательности Fc-домена полипептидов, которые образуют человеческие Cγ1, Сγ2, Сγ3 и Сγ4, в качестве примера представлены в SEQ ID NO: 23, 24, 25 и 26 соответственно. Взаимосвязь между аминокислотными остатками, образующими каждую аминокислотную последовательность, и EU-нумерацией Кэбота (обозначена в контексте настоящего описания как EU-индекс), представлена на фиг. 23.
Понятие «Fc-домен» относится к области вне F(ab')2, которая содержит две легкие цепи и две тяжелые цепи, содержащие часть константной области, которая включает СН1-домен и область между СН1- и СН2-доменами, что позволяет образовываться дисульфидным мостикам между двумя тяжелыми цепями. Fc-домен, образующий антигенсвязывающую молекулу, представленную в настоящем описании, предпочтительно можно получать следующим образом. Моноклональное антитело в виде IgG1, IgG2, IgG3 или IgG4 или сходное антитело частично расщепляют протеазой, такой как пепсин, с последующей элюцией фракции, адсорбированной на колонке с белком А. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять полное антитело с образованием F(ab')2 в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Fcγ-рецептор
Понятие «Fcy-рецептор» относится к рецептору, обладающему способностью связываться с Fc-доменом моноклональных антител в виде IgG1, IgG2, IgG3 или IgG4, и оно включает всех представителей, принадлежащих к семейству белков, которые кодируются главным образом геном Fcy-рецептора. У человека семейство включает FcγRI (CD64), включая изоформы FcγRIa, FcγRIb и FcγRIc; FcγRII (CD32), включая изоформы FcγRIIa (в том числе аллотип H131 и R131), FcγRIIb (включая FcγRIIb-1 и FcγRIIb-2) и FcγRIIc; и FcγRIII (CD16), включая изоформу FcγRIIIa (в том числе аллотипы V158 и F158), и FcγRIIIb (в той числе аллотипы FcγRIIIb-NA1 и FcγRIIIb-NA2); а также все неидентифицированные человеческие FcγR, изоформы FcγR и их аллотипы. Однако Fcγ-рецептор не ограничен указанными примерами. FcγR включает (но не ограничиваясь только ими) FcγR, полученные из антител человека, мышей, крыс, кроликов и обезьян. FcγR можно получать из любого организма. Мышиный FcγR включает (но, не ограничиваясь только ими) FcγRI (CD64), FcγRII (CD32), FcγRIII (CD16) и FcγRIII-2 (CD 16-2), а также все неидентифицированные мышиные FcγR, изоформы FcγR и их аллотипы. Указанные предпочтительные Fcγ-рецепторы включают, например, человеческие FcγI (CD64), FcγIIA (CD32), FcγIIB (CD32), FcγIIIA (CD16) и/или FcγIIIB (CD16).
Полинуклеотидная последовательность и аминокислотная последовательность FcγI представлены в SEQ ID NO: 27 (NM_000566.3) и 28 (NP_000557.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIA представлены в SEQ ID NO: 29 (ВС020823.1) и 30 (ААН20823.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIB представлены в SEQ ID NO: 31 (ВС146678.1) и 32 (AAI46679.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIIA представлены в SEQ ID NO: 33 (ВС033678.1) и 34 (ААН33678.1) соответственно и полинуклеотидная последовательность и аминокислотная последовательность FcγIIIB представлены в SEQ ID NO: 35 (ВС128562.1) и 36 (AAI28563.1) соответственно (в скобках указан регистрационный номер каждой последовательности в базе данных RefSeq). Обладает ли Fcγ-рецептор способностью связываться с Fc-доменом моноклонального антитела IgG1, IgG2, IgG3 или IgG4, можно оценивать с помощью ALPHA Screen®-анализа (гомогенный анализ усиленной за счет эффекта близости люминесценции (Amplified Luminescent Proximity Homogeneous Assay)), BIACORE-метода на основе поверхностного плазмонного резонанса (SPR) и др. (Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010), помимо описанных выше форматов FACS и ELISA.
При этом понятие «Fc-лиганд» или «эффекторный лиганд» относится к молекуле и предпочтительно полипептиду, который связывается с Fc-доменом антитела, образуя комплекс Fc/Fc-лиганд. Молекулу можно получать из любого организма. Связывание Fc-лиганда с Fc предпочтительно индуцирует одну или несколько эффекторных функций. Указанные лиганды включают (но, не ограничиваясь только ими) Fc-рецепторы, FcγR, FcαR, FcεR, FcRn, Clq и С3, маннансвязывающий лектин, маннозный рецептор, белок A Staphylococcus, белок G Staphylococcus и вирусные FcγR. Fc-лиганды включают также гомологи Fc-рецептора (FcRH) (Davis и др., Immunological Reviews 190, 2002, cc. 123-136), которые представляют собой семейство Fc-рецепторов, гомологичных FcγR. К Fc-лигандам относятся также неидентифицированные молекулы, которые связываются с Fc.
Активность связывания с Fcγ-рецептором
Нарушение активности связывания Fc-домена с любым из Fcγ-рецепторов FcγI, FcγIIA, FcγIIB, FcγIIIA и/или FcγIIIB можно оценивать, используя описанные выше форматы FACS и ELISA, а также ALPHA Screen-анализ (гомогенный анализ усиленной за счет эффекта близости люминисценции, BIACORE-метод на основе поверхностного плазменного резонанса (SPR) (Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010).
ALPHA Screen-анализ осуществляют на основе технологии ALPHA, которая основана на описанном ниже принципе, с использованием двух типов гранул. Люминисцентный сигнал становится обнаруживаемым только тогда, когда происходит биологическое взаимодействие молекул, связанных с гранулами-донорами, с молекулами, связанными с гранулами-акцепторами, и когда обе гранулы находятся в непосредственной близости друг от друга. Возбужденный лазерным пучком фотосенсибилизатор в гранулах-донорах превращает кислород в возбужденный синглетный кислород. Когда синглетный кислород диффундирует из гранул-доноров и достигает гранул-акцепторов, локализованных в непосредственной близости, то индуцируется хемилюминесцентная реакция в гранулах-акцепторах. В итоге эта реакция приводит к испусканию света. Если молекулы, связанные с гранулами-донорами, не взаимодействуют с гранулами-акцепторами, то синглетный кислород, который продуцируется гранулами-донорами, не достигает гранул-акцепторов и хемилюминесцентная реакция не происходит.
Например, меченную биотином антигенсвязывающую молекулу иммобилизуют на гранулах-донорах, а меченный глутатион-S-трансферазой (GST) Fcγ-рецептор иммобилизуют на гранулах-акцепторах. В отсутствии антигенсвязывающей молекулы, содержащей конкурирующий мутантный Fc-домен, Fcγ-рецептор взаимодействует с антигенсвязывающей молекулой, содержащей Fc-домен дикого типа, индуцируя в результате сигнал с длиной волны от 520 до 620 нм. Антигенсвязывающая молекула, содержащая немеченый мутантный Fc-домен, конкурирует с антигенсвязывающей молекулой, содержащей Fc-домен дикого типа, за взаимодействие с Fcγ-рецептором. Относительную аффинность связывания можно оценивать, определяя количественно снижение флуоресценции в результате конкуренции. Методы биотинилирования антигенсвязывающих молекул, таких как антитела, с помощью сульфо-NHS-биотина или подобных агентов являются известными. Приемлемые методы введения GST-метки в Fcγ-рецептор включают методы, которые предусматривают слияние полипептидов, кодирующих Fcγ и GST, в рамке считывания, экспрессию слитого гена с использованием клеток, в которые интродуцирован вектор, несущий ген, и последующую очистку с помощью содержащей глутатион колонки. Индуцированный сигнал предпочтительно можно анализировать, например, посредством подгонки к односайтовой модели конкуренции на основе нелинейного регрессионного анализа с использованием такой программы, как GRAPHPAD PRISM (фирма GraphPad; Сан-Диего).
Одну из субстанций, предназначенных для исследования их взаимодействия, иммобилизуют в качестве лиганда на тонком слое золота сенсорного чипа. Когда свет проникает на заднюю поверхность сенсорного чипа так, что имеет место полное отражение на границе раздела между тонким слоем золота и стеклом, то интенсивность отраженного света в определенном сайте частично снижается (SPR-сигнал). Другую субстанцию, предназначенную для исследования ее взаимодействия, инъецируют в качестве аналита на поверхность сенсорного чипа. Когда аналит связывается с лигандом, то масса иммобилизованной молекулы-лиганда возрастает. Это изменяет показатель преломления растворителя на поверхности сенсорного чипа. Изменение показателя преломления вызывает положительный сдвиг SPR-сигнала (и наоборот, диссоциация сдвигает сигнал назад в исходное положение). В Biacore-системе уровень описанного выше сдвига (т.е. изменение массы на поверхности сенсорного чипа) откладывают по вертикальной оси, и таким образом в качестве количественных данных получают график изменения массы в зависимости от времени (сенсограмма). Кинетические параметры (константа скорости ассоциации (ka) и константа скорости диссоциации (kd)) определяют из представленных в виде кривых сенсограмм, и определяют аффинность (KD) как соотношение указанных двух констант. BIACORE-методы предпочтительно применяют для анализа ингибирования. Примеры такого анализа ингибирования описаны в Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010.
В контексте настоящего описания «пониженная активность связывания с Fcγ-рецептором» означает, например, что при использовании описанного выше метода анализа конкурентная активность тестируемой антигенсвязывающей молекулы составляет 50% или менее, предпочтительно 45% или менее, 40% или менее, 35% или менее, 30% или менее, 20% или менее или 15% или менее и наиболее предпочтительно 10% или менее, 9% или менее, 8% или менее, 7% или менее, 6% или менее, 5% или менее, 4% или менее, 3% или менее, 2% или менее или 1% менее, по сравнению с конкурентной активностью контрольной антигенсвязывающей молекулы.
Антигенсвязывающие молекулы, содержащие Fc-домен моноклонального антитела в виде IgG1, IgG2, IgG3 или IgG4, можно использовать соответственно в качестве контрольных антигенсвязывающих молекул. Структуры Fc-домена представлены в SEQ ID NO: 37 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААС82527.1), SEQ ID NO: 38 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААВ59393.1), SEQ ID NO: 25 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером САА27268.1) и SEQ ID NO: 39 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААВ59394.1). Кроме того, когда антигенсвязывающую молекулу, содержащую мутантный Fc-домен антитела конкретного изотипа, используют в качестве тестируемой субстанции, то воздействие мутации мутанта на активность связывания с Pcγ-рецептором оценивают с использованием в качестве контроля антигенсвязывающей молекулы, содержащей Fc-домен такого же изотипа. Как описано выше, соответственно получают антигенсвязывающие молекулы, содержащие мутантный Fc-домен с действительно пониженной активностью связывания с Fcγ-рецептором.
Такие известные мутанты включают, например, мутанты с делецией аминокислот 231A-238S (EU-нумерация) (WO 2009/011941), а также мутанты C226S, C229S, P238S, (C220S) (J. Rheumatol 34, 2007, с. 11); C226S и C229S (Hum. Antibod. Hybridomas 1(1), 1990, cc. 47-54); C226S, C229S, Е233Р, L234V, и L235A (Blood 109, 2007, cc. 1185-1192).
В частности, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен с заменой аминокислоты в положении 220, 226, 229, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 264, 265, 266, 267, 269, 270, 295, 296, 297, 298, 299, 300, 325, 327, 328, 329, 330, 331 или 332 (EU-нумерация) в аминокислотах, образующих Fc-домен антитела конкретного изотипа. Изобретение не ограничено изотипом антитела, из которого получают Fc-домен, и можно использовать соответствующий Fc-домен, полученный из моноклонального антитела в виде IgG1, IgG2, IgG3 или IgG4. Предпочтительно следует применять Fc-домен, полученный из антител в виде IgG1.
Предпочтительными антигенсвязывающими молекулами являются, например, молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяется согласно EU-нумерации (каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены), среди аминокислот, образующих Fc-домен антитела в виде IgG1:
(a) L234F, L235E, P331S;
(б) C226S, C229S, P238S;
(в) C226S, C229S;
(г) C226S, C229S, Е233Р, L234V, L235A;
(д) L234A, L235A или L235R, N297A;
(е) L235A или L235R, S239K, N297A,
а также молекулы, которые содержат Fc-домен с делецией аминокислот в положениях 231-238.
Кроме того, предпочтительными антигенсвязывающими молекулами являются также молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG2:
(ж) H268Q, V309L, A330S и P331S;
(з) V234A;
(и) G237A;
(к) V234A и G237A;
(л) А235Е и G237A;
(м) V234A, А235Е и G237A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Кроме того, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG3:
(н) F241A;
(о) D265A;
(п) V264A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Кроме того, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG4:
(р) L235A, G237A и Е318А;
(с) L235E;
(т) F234A и L235A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Другие предпочтительные антигенсвязывающие молекулы представляют собой молекулы, содержащие Fc-домен, в котором любая аминокислота в положении 233, 234, 235, 236, 237, 327, 330 или 331 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена на аминокислоту, которая находится в соответствующем положении согласно EU-нумерации в соответствующем IgG2 или IgG4.
Предпочтительные антигенсвязывающие молекулы представляют собой также молекулы, содержащие Fc-домен, в котором одна или несколько аминокислот в положениях 234, 235 и 297 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена(ы) на другие аминокислоты. Изобретение не ограничено типом аминокислоты после замены; однако наиболее предпочтительными являются антигенсвязывающие молекулы, содержащие Fc-домен, в котором одна или несколько аминокислот в положениях 234, 235 и 297 заменена(ы) на аланин.
Предпочтительные антигенсвязывающие молекулы представляют собой также молекулы, содержащие Fc-домен, в котором аминокислота в положении 265 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена другой аминокислотой. Изобретение не ограничено типом аминокислоты после замены; однако наиболее предпочтительными являются антигенсвязывающие молекулы, содержащие Fc-домен, в котором аминокислота в положении 265 заменена на аланин.
Мультиспецифические антигенсвязывающие молекулы
Примеры предпочтительных вариантов «мультиспецифической антигенсвязывающей молекулы», предлагаемой в настоящем изобретении, включают мультиспецифические антитела. Когда Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора применяют в качестве Fc-области мультиспецифического антитела, то соответственно можно применять Fc-область, полученную из мультиспецифического антитела. Биспецифические антитела являются наиболее предпочтительными в качестве мультиспецифических антител, предлагаемых в настоящем изобретении. В этом случае биспецифическое антитело представляет собой антитело, имеющее две различные специфичности. Биспецифические антитела IgG-типа можно секретировать из гибридной гибридомы (квадромы), полученной путем слияния двух типов гибридом, продуцирующих антитело в виде IgG (Milstein С. и др., Nature 305, 1983, cc. 537-540).
Кроме того, биспецифические антитела IgG-типа секретируют посредством интродукции в клетки в целом четырех генов, т.е. генов L-цепей и Н-цепей, образующих представляющие интерес IgG двух типов, и их коэкспрессии. Однако теоретически существует десять комбинаций Н-цепей и L-цепей IgG, которые можно получать такими методами. При этом трудно очищать IgG, состоящий из требуемой комбинации Н-цепей и L-цепей из десяти типов IgG. Кроме того, теоретическое количество секретируемого IgG с требуемой комбинацией, также в значительной степени снижено, поэтому требуется осуществлять крупномасштабное культивирование. Это дополнительно увеличивает стоимость производства.
Таким образом, для мультиспецифических антигенсвязывающих молекул, предлагаемых к настоящем изобретении, можно применять методики, усиливающие ассоциацию между Н-цепями и между L- и Н-цепями, имеющими требуемые комбинации.
Например, методики подавления нежелательной ассоциации Н-цепей путем интродукции электростатического отталкивания на поверхности раздела второго константного участка или третьего константного участка Н-цепи антитела (СН2 или СН3) можно применять для ассоциации мультиспецифического антитела (WO 2006/106905).
При осуществлении метода подавления нежелательной ассоциации Н-цепей путем интродукции электростатического отталкивания на поверхности раздела СН2 или СН3, примеры аминокислотных остатков, контактирующих на поверхности раздела с другим константным участком Н-цепи, включают области, соответствующие остаткам, находящимся согласно EU-нумерации в положениях 356, 439, 357, 370, 399 и 409 в СН3-участке.
Более конкретно, примеры включают антитело, содержащее два типа СН3-участков Н-цепи, в которых 1-3 пары аминокислотных остатков в СН3-участке первой Н-цепи, выбранные из пар аминокислотных остатков, указанных ниже в подпунктах (1)-(3), несут одинаковый типа заряда: (1) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 356 и 439; (2) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 357 и 370; и (3) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 399 и 409.
Кроме того, антитело может представлять собой антитело, в котором пары аминокислотных остатков в СН3-участке второй Н-цепи, который отличается от указанного выше СН3-участка первой Н-цепи, выбирают из вышеуказанных в подпунктах (1)-(3) пар аминокислотных остатков, в котором 1-3 пары аминокислотных остатков, которые соответствуют вышеуказанным в подпунктах (1)-(3) парам аминокислотных остатков, несущим такой же тип заряда, что и указанный выше для СН3-участка первой Н-цепи, несут противоположные заряды относительно соответствующих аминокислотных остатков в указанном выше СН3-участке первой Н-цепи.
Соответствующие аминокислотные остатки, указанные выше в подпунктах (1)-(3), при ассоциации располагаются близко друг к другу. Специалисты в данной области могут установить для требуемого СН3-участка Н-цепи или константной области Н-цепи сайты, которые соответствуют вышеуказанным остаткам, указанным в подпунктах (1)-(3), посредством моделирования гомологии и т.п., используя поступающую в продажу программу, и аминокислотные остатки этих сайтов можно подвергать при необходимости модификациям.
В указанных выше антителах «имеющие заряд аминокислотные остатки» предпочтительно выбирают, например, из аминокислотных остатков, которые входят в любую одну из указанных ниже групп (а) и (б):
(а) глутаминовая кислота (Е) и аспарагиновая кислота (D) и
(б) лизин (K), аргинин (R) и гистидин (Н).
Касательно указанных выше антител то, что они «имеют одинаковый тип заряда» означает, например, что два или большее количество аминокислотных остатков все представляют собой аминокислотные остатки, включенные в любую одну из вышеуказанных групп (а) и (б). Понятие «имеют противоположный заряд» означает, например, что, когда по меньшей мере один из двух или большего количества аминокислотных остатков представляет собой аминокислотный остаток, включенный в любую одну из вышеуказанных групп (а) и (б), остальные остатки должны представлять собой аминокислотные остатки, включенные в другую группу.
В предпочтительном варианте вышеуказанного антитела СН3-участок первой Н-цепи и СН3-участок второй Н-цепи могут быть перекрестно сшиты дисульфиднымм мостиками.
Согласно настоящему изобретению аминокислотные остатки, подлежащие изменению, не ограничены аминокислотными остатками константной области или вариабельной области описанного выше антитела. Касательно полипептидных мутантов или гетеромультимеров специалисты в данной области могут установить аминокислотные остатки, которые образуют поверхность раздела, посредством моделирования гомологии и т.п., используя поступающую в продажу программу, и аминокислотные остатки этих сайтов можно подвергать при необходимости изменениям для того, чтобы регулировать ассоциацию.
Другие известные методики можно применять также для ассоциации мультиспецифических антител, предлагаемых в настоящем изобретении. Полипептиды с различными аминокислотами в Fc-области можно эффективно ассоциировать друг с другом путем замены боковой цепи аминокислоты, присутствующей в одной из вариабельных областей Н-цепи антитела, на более крупную боковую цепь («выступ») и замены боковой цепи аминокислоты в соответствующей вариабельной области другой Н-цепи на меньшую боковую цепь («впадина») так, что «выступ» помещается во «впадину» (WO 1996/027011; Ridgway J.B. и др., Protein Engineering 9, 1996, cc. 617-621; Merchant A.M. и др., Nature Biotechnology 16, 1998, cc. 677-681 и US 20130336973).
Кроме того, другие известные методики можно применять также для ассоциации мультиспецифических антител, предлагаемых в настоящем изобретении. Ассоциацию полипептидов, имеющих различные последовательности, можно эффективно индуцировать путем комплементарной ассоциации СН3-областей, используя сконструированный СН3-домен с обменом цепей, полученный путем изменения части СН3 в одной из Н-цепей антитела на соответствующую полученную из IgA последовательность и интродукции в комплементарную часть СН3 в другой Н-цепи соответствующей полученной из IgA последовательности (Protein Engineering Design & Selection, 23, 2010, cc. 195-202). Указанную известную методику можно применять также для эффективного получения представляющих интерес мультиспецифических антител.
Кроме того, для получения мультиспецифических антител можно применять следующие методики: методики получения антител на основе ассоциации СН1 и CL антитела и ассоциации VH и VL, которые описаны в WO 2011/028952, WO 2014/018572 и в Nat Biotechnol. 32(2), февраль 2014 г., cc. 191-198; методики получения биспецифических антител с использованием в комбинации полученных по отдельности моноклональных антител (обмен плечей Fab, (Fab arm exchange, FAE), описанные в WO 2008/119353 и WO 2011/131746; методики регуляции ассоциации между СН3-доменом тяжелых цепей антител, описанные в WO 2012/058768 и WO 2013/063702; методики получения биспецифических антител, состоящих из двух типов легких цепей и одного типа тяжелой цепи, описанные в WO 2012/023053; методики получения биспецифических антител с использованием двух штаммов бактериальных клеток, которые индивидуально экспрессируют одну из цепей антитела, содержащего одну Н-цепь и одну L-цепь, описанные Christoph и др., Nature Biotechnology т. 31, 2013, cc. 753-758).
Один из вариантов путей получения мультиспецифического антитела включает методы получения биспецифических антител путем смешения двух типов моноклональных антител в присутствии восстановителя для расщепления дисульфидных связей в коровой шарнирной области с последующей повторной ассоциацией для гетеродимеризации (FAE), как описано выше. При этом, интродукция электростатических взаимодействий на поверхности взаимодействия СН3-участка (WO 2006/106905) может индуцировать еще более эффективную гетеродимеризацию в процессе повторной ассоциации (WO 2015/046467). При осуществлении FAE с использованием встречающегося в естественных условиях IgG повторная ассоциация происходит произвольно; и поэтому теоретически биспецифические антитела можно получать лишь с 50%-ной эффективностью; однако при применении указанного метода можно получать биспецифические антитела с высоким выходом.
Альтернативно этому, даже, если представляющее интерес мультиспецифическое антитело нельзя получать эффективно, мультиспецифическое антитело, предлагаемое в настоящем изобретении, можно получать путем отделения представляющего интерес мультиспецифического антитела от полученных антител и его очистки. Например, описан метод, позволяющий осуществлять очистку двух типов гомомерных форм и представляющего интерес гетеромерного антитела с помощью ионообменной хроматографии, путем установления различия в изоэлектрических точках в результате интродукции аминокислотных замен в вариабельные области двух типов Н-цепей (WO 2007/114325). К настоящему времени в качестве метода для очистки гетеромерных форм описан метод, основанный на применении белка А для очистки гетеродимерного антитела, содержащего Н-цепь мышиного IgG2a, которая связывается с белком А, и Н-цепь крысиного IgG2b, которая не связывается с белком А (WO 98/050431 и WO 95/033844). Кроме того, само гетеродимеризованное антитело можно эффективно очищать путем применения Н-цепей, в которых аминокислотные остатки в сайте связывания IgG-белок А в положениях 435 и 436 (EU-нумерация) заменены на аминокислотные остатки, которые обеспечивают другую аффинность связывания с белком А, такие как Tyr, His или т.п., или с использованием Н-цепей с различной аффинностью к белку А, которые получают согласно методу, указанному в приведенном для справки примере 9, для изменения взаимодействия каждой из Н-цепей с белком А, и последующего применения колонки с белком А.
Альтернативно этому, можно получать общую L-цепь, которая может обеспечивать способность связываться с несколькими различными Н-цепями, и применять ее в качестве общей L-цепи мультиспецифического антитела. Для достижения эффективной экспрессии мультиспецифического IgG можно интродуцировать в клетки гены указанной общей L-цепи и нескольких различных Н-цепей и экспрессировать IgG (Nature Biotechnology, 16, 1998, cc. 677-681). Метод селекции общей L-цепи, для которой характерна выраженная способность к связыванию с любыми различными Н-цепями, можно применять также для селекции общей Н-цепи (WO 2004/065611).
Кроме того, Fc-область, отличающуюся улучшенной C-концевой гетерогенностью, можно применять в качестве Fc-области, предлагаемой в настоящем изобретении. Более конкретно, предложены Fc-области, в которых отсутствуют глицин в положении 446 и лизин в положении 447 (EU-нумерация) в аминокислотных последовательностях двух полипептидов, образующих Ре-область, которая происходит из IgG1, IgG2, IgG3 или IgG4.
Несколько, например, две или большее количество, указанных методик можно применять в сочетании друг с другом. Кроме того, эти методики можно соответствующим образом и раздельно применять к двум Н-цепям, подлежащим ассоциации. Кроме того, указанные методики можно применять в комбинации с описанной выше Fc-областью, у которой снижена активность связывания с Fcγ-рецептором. Кроме того, антигенсвязывающая молекула, предлагаемая в настоящем изобретении, может представлять собой молекулу, полученную отдельно на основе антигенсвязывающей молекулы, подвергнутой таким описанным выше модификациям, что она имеет такую же аминокислотную последовательность.
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, содержащие в качестве активного ингредиента биспецифическое антитело, указанное ниже в любом одном из подпунктов (а)-(в), которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3:
(а) биспецифическое антитело, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и COR3-участков, которые содержатся в SEQ ID NO: 206 соответственно; CDR1, CDR2, и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, имеют последовательности, идентичные по меньшей мере на 80% аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223 соответственно;
(б) биспецифическое антитело, в котором вариабельная область антитела, обладающая связывающей активностью в отношении глипикана 3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 206; вариабельная область антитела, которая обладает связывающей активностью в отношении CD3, представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой последовательность, идентичную по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 223; и
(в) биспецифическое антитело, которое имеет Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 385; Н-цепь антитела, которая обладает связывающей активностью в отношении CD3 и идентична по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 402; и общие L-цепи, идентичные по меньшей мере на 80% аминокислотной последовательности SEQ ID NO: 410.
В биспецифическом антителе, указанное выше в любом одном из подпунктов (а)-(в), аминокислотная последовательность идентична каждому из указанных CDR1, CDR2 и CDR3 тяжелой цепи и легкой цепи, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной тяжелой цепи и полной легкой цепи по меньшей мере на 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89% или более 90% и более предпочтительно по меньшей мере на 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или более.
В контексте настоящего описания идентичность последовательности рассчитывают как процент остатков, идентичных остаткам в исходной аминокислотной последовательности вариабельной области тяжелой цепи или легкой цепи, определенный после выравнивания последовательностей и интродукции при необходимости соответствующих брешей для увеличения до максимума идентичности последовательности.
В биспецифическом антителе, указанном выше в любом одном из подпунктов (а)-(в), если антитело обладает связывающей активностью в отношении глипикана 3 или CD3, то одну или несколько аминокислот можно заменять, изымать путем делеции, добавлять и/или встраивать в аминокислотные последовательности CDR1, CDR2 и CDR3 тяжелой цепи и легкой цепи, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной тяжелой цепи и полной легкой цепи. Хорошо известные специалистам в данной области методы получения такой аминокислотной последовательности, в которой одна или несколько аминокислот заменена(ы), удалена(ы) путем делеции, добавлена(ы) и/или встроена(ы), включает метод интродукции мутаций в белки. Например, специалисты в данной области могут получать мутанты, функционально эквивалентные вариабельной области тяжелой цепи или легкой цепи биспецифического антитела, которое содержит Н-цепь антитела, имеющую SEQ ID NO: 385, которая обладает связывающей активностью в отношении глипикана 3, Н-цепь антитела, имеющую SEQ ID NO: 402, которая обладает связывающей активностью в отношении CD3, и общие L-цепи антитела, имеющие SEQ ID NO: 410, путем интродукции соответственно мутаций в аминокислотную последовательность антитела, обладающего связывающей активностью в отношении глипикана 3 или CD3, с помощью сайтнаправленного мутагенеза (Hashimoto-Gotoh Т., Mizuno Т., Ogasahara Y. и Nakagawa M., An oligodeoxyribonucleotide-directed dual amber method for site-directed mutagenesis. Gene 152, 1995, cc. 271-275; Zoller M.J. и Smith M. Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors. Methods Enzymol. 100, 1983, cc. 468-500; Kramer W, Drutsa V, Jansen H.W., Kramer B, Pflugfelder M. и Fritz H.J. The gapped duplex DNA approach to oligonucleotide-directed mutation construction. Nucleic Acids Res. 12, 1984, cc. 9441-9456; Kramer W. и Fritz H.J. Oligonucleotide-directed construction of mutations via gapped duplex DNA Methods. Enzymol. 154, 1987, cc. 350-367; Kunkel T.A. Rapid and efficient site-specific mutagenesis without phenotypic selection. Proc Natl Acad Sci USA. 82, 1985, cc. 488-492) или т.п. В настоящем изобретении фраза «функциональный эквивалент» означает, что аффинности связывания антигена являются эквивалентными, или альтернативно этому, означает, что цитотоксическая активность в отношении экспрессирующих глипикан 3 клеток или тканей, которые содержат указанные клетки, эквивалентна при использовании в виде мультиспецифической антигенсвязывающей молекулы. Аффинность связывания и цитотоксическую активность можно измерять на основе указанного описания. Детали описаны подробно ниже.
Количество аминокислот, которые можно изменять, не ограничено и, например, составляет 40 или менее, 30 или менее, 20 или менее, предпочтительно 18 или менее, 16 или менее, 15 или менее, 12 или менее, 10 или менее, 9 или менее, 8 или менее, 7 или менее, 6 или менее, 5 или менее, 4 или менее, 3 или менее или 2 или менее.
Когда изменяют аминокислотный остаток, то аминокислоту предпочтительно заменяют в результате мутации на другую(ие) аминокислоту(ы), которая(ые) сохраняет(ют) особенности боковой цепи аминокислоты. Примеры особенностей боковых цепей аминокислот включают: гидрофобные аминокислоты (A, I, L, M, F, P, W, Y и V), гидрофильные аминокислоты (R, D, N, С, Е, Q, G, Н, К, S и Т), аминокислоты с алифатическими боковыми цепями (G, А, V, L, I и P), аминокислоты с содержащими гидроксильную группу боковыми цепями (S, Т и Y), аминокислоты с содержащими серу боковыми цепями (С и M), аминокислоты с содержащими карбоновую кислоту и амид боковыми цепями (D, N, Е и Q), аминокислоты с основными боковыми цепями (R, K и Н) и аминокислоты с ароматическими боковыми цепями (Н, F, Y и W) (аминокислоты в скобках обозначены с помощью однобуквенного кода). Замены аминокислот в каждой из указанных групп обозначают как консервативные замены. К настоящему времени известно, что полипептид, имеющий модифицированную аминокислотную последовательность, в которой один или несколько аминокислотных остатков в данной аминокислотной последовательности удален(ы) путем делеции, добавлен(ы) и/или заменен(ы) другими аминокислотами, может сохранять биологическую активность (Mark D.F. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc. 5662-5666; Zoller M.J. и Smith M., Nucleic Acids Res. 10, 1982, cc. 6487-6500; Wang А. и др., Science 224, 1984, cc. 1431-1433; Dalbadie-McFarland G. и др., Proc. Natl. Acad. Sci. USA 79 1982, cc. 6409-6413).
Альтернативно этому, аминокислотная последовательность, обладающая связывающей активностью в отношении глипикана 3 или CD3, которая несет замену, делецию, добавление и/или инсерцию одной или нескольких аминокислот в аминокислотной последовательности CDR-участка, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной области тяжелой цепи или полной области легкой цепи, можно получать путем гибридизации нуклеиновых кислот, которые гибридизуются в строгих условиях с нуклеиновыми кислотами, которые содержат нуклеотидную последовательность, кодирующую аминокислотную последовательность CDR-участка, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной области тяжелой цепи или полной области легкой цепи. Строгие условия гибридизации для выделения нуклеиновой кислоты, которая гибридизуется в строгих условиях с нуклеиновой кислотой, которая содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность CDR-участка, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной области тяжелой цепи или полной области легкой цепи, включают, например, такие условия, как 6М мочевина, 0,4% ДСН, 0,5 × SSC и 37°С, или условия гибридизации, эквивалентные им по строгости. Выделение нуклеиновых кислот с максимально высокой гомологией можно ожидать при использовании более строгих условий, например, таких условий, как 6М мочевина, 0,4% ДСН, 0,1 × SSC и 42°С. Условия промывки после гибридизации представляют собой, например, промывку с использованием 0,5 × SSC (1 × SSC в 0,15М NaCl и 0,015М цитрате натрия, pH 7,0) и 0,1% ДСН при 60°С, более предпочтительно промывку с использованием 0,2 × SSC и 0,1% ДСН при 60°С, еще более предпочтительно промывку с использованием 0,2 × SSC и 0,1% ДСН при 62°С, еще более предпочтительно промывку с использованием 0,2 × SSC и 0,1% ДСН при 65°С и еще более предпочтительно промывку с использованием 0,1 × SSC и 0,1% ДСН при 65°С. Продолжительность промывки и количество промывок можно соответствующим образом регулировать, например, 20-минутную промывку можно осуществлять три раза. Последовательности выделенных нуклеиновых кислот можно определять с помощью известных методов, описанных ниже. Гомология всей нуклеотидной последовательности выделенной нуклеиновой кислоты составляет по меньшей мере 50% или более, предпочтительно 70% или более, 75% или более, 80% или более, 85% или более и более предпочтительно 90% или более (например, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) при определении на основе идентичности последовательности.
Вместо описанных выше методов, основанных на применении методик гибридизации, методы генной амплификации, например, полимеразную цепную реакцию (ПЦР) с использованием праймеров, синтезированных на основе информации о нуклеотидной последовательности, которая кодирует аминокислотную последовательность CDR-участка, вариабельной области тяжелой цепи, вариабельной области легкой цепи, полной области тяжелой цепи или полной области легкой цепи, можно применять также для выделения нуклеиновой кислоты, которая гибридизуется в строгих условиях с нуклеиновой кислотой, которая содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность области.
Идентичность одной нуклеотидной последовательности или аминокислотной последовательности можно определять с помощью алгоритма BLAST, описанного у Karlin и Altschul (Proc. Natl. Acad. Sci. USA 90, 1993, cc. 5873-5877). На основе этого алгоритма разработаны программы BLASTN и BLASTX (Altschul и др., J. Mol. Biol. 215, 1990, cc. 403-410). Для анализа нуклеотидных последовательностей согласно BLASTN на основе BLAST устанавливают параметры, такие, например, как балл = 100 и длина слова = 12. С другой стороны, параметры, применяемые для анализа аминокислотных последовательностей с помощью BLASTX на основе BLAST, включают, например, балл = 50 и длина слова = 3. Задаваемые по умолчанию параметры применяют для каждой программы, когда используют программы BLAST и Gapped BLAST. В данной области известны конкретные методики указанных анализов (см. веб-сайт National Center for Biotechnology Information (NCBI), Basic Local Alignment Search Tool (BLAST); http://www.ncbi.nlm.nih.gov).
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, которое имеет две Н-цепи и общие L-цепи антитела, обозначенного как антитело из образца №38 (таблица 17), которые описаны в примерах и приведенных для справки примерах. Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, которое имеет вариабельные области двух Н-цепей и общие L-цепи антитела, обозначенного как антитело из образца №38, и которое обладает связывающей активностью в отношении глипикана 3 и CD3. Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, которое имеет соответствующие аминокислотные последовательности CDR1-, CDR2- и CDR3- участков, содержащихся в двух H-цепях и общих L-цепях антитела, обозначенного как антитело из образца №38, и которое обладает связывающей активностью в отношении глипикана 3 и CD3.
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, которое имеет Н-цепь антитела, имеющую SEQ ID NO: 385, которая обладает связывающей активностью в отношении глипикана 3, Н-цепь антитела, имеющую SEQ ID NO: 402, которая обладает связывающей активностью в отношении CD3, и общие L-цепи антитела, имеющие SEQ ID NO: 410.
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, в котором CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, представляют собой аминокислотные последовательности CDR1-, CDR2- и CDR3-участков, содержащихся в SEQ ID NO: 206 соответственно; CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, которая обладает связывающей активностью в отношении CD3, представляют собой аминокислотные последовательности CDR1-, CDR2- и CDR3-участков, содержащихся в SEQ ID NO: 168 соответственно; и CDR1, CDR2 и CDR3, содержащиеся в вариабельной области общей L-цепи антитела, представляют собой аминокислотные последовательности CDR1-, CDR2- и CDR3-участков, содержащихся в SEQ ID NO: 223 соответственно.
Аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельной области антитела, можно идентифицировать методами, известными специалистам в данной области, и такие методы не ограничены конкретными методами. CDR1-, CDR2- и CDR3-участки могут представлять собой участки, пронумерованные на основе систем, известных специалистам в данной области, например, Кэбота, Хотиа или нумерации участвующих в контакте остатков, или их нумерация может быть основана на других критериях. В не ограничивающем объем изобретения варианте осуществления настоящего изобретения CDR1-, CDR2- и CDR3-участки в SEQ ID NO: 206 включают участки аминокислотных последовательностей в положениях 31-35 (SEQ ID NO: 456), положениях 50-66 (SEQ ID NO: 457) и положениях 99-104 (SEQ ID NO: 458) соответственно (нумерация по Кэботу); участки аминокислотных последовательностей в положениях 26-32 (SEQ ID NO: 459), положениях 52-57 (SEQ ID NO: 460) и в положениях 97-104 (SEQ ID NO: 461) соответственно (нумерация по Хотиа);и участки аминокислотных последовательностей в положениях 30-35 (SEQ ID NO: 462), положениях 47-59 (SEQ ID NO: 463) и положениях 97-103 (SEQ ID NO: 464) соответственно (нумерация участвующих в контакте остатков); однако CDR-участки могут представлять собой участки, нумерация которых основана на других критериях.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения CDR1-, CDR2- и CDR3-участки в SEQ ID NO: 168 включают участки аминокислотных последовательностях в положениях 31-35 (SEQ ID NO: 465), положениях 50-68 (SEQ ID NO: 466) и положениях 101-111 (SEQ ID NO: 467) соответственно (нумерация по Кэботу); участки аминокислотных последовательностей в положениях 26-32 (SEQ ID NO: 468), положениях 52-59 (SEQ ID NO: 469) и положениях 99-111 (SEQ ID NO: 470) соответственно (нумерация по Хотиа); и участки аминокислотных последовательностей в положениях 30-35 (SEQ ID NO: 471), положениях 47-61 (SEQ ID NO: 472) и положениях 99-110 (SEQ ID NO: 473) соответственно (нумерация участвующих в контакте остатков); однако CDR-участки могут представлять собой участки, нумерация которых основана на других критериях.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения CDR1-, CDR2- и CDR3-участки в SEQ ID NO: 223 включают участки аминокислотных последовательностях в положениях 24-39 (SEQ ID NO: 474), положениях 55-61 (SEQ ID NO: 475) и положениях 94-102 (SEQ ID NO: 476) соответственно (нумерация по Кэботу и нумерация по Хотиа); и участки аминокислотных последовательностей в положениях 35-41 (SEQ ID NO: 477), положениях 51-56 (SEQ ID NO: 478) и положениях 94-101 (SEQ ID NO: 479) (нумерация участвующих в контакте остатков); однако CDR-участки могут представлять собой участки, нумерация которых основана на других критериях (см. фиг. 24-1, 24-2 и 25).
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются противораковые агенты, которые содержат в качестве активного ингредиента биспецифическое антитело, в котором вариабельная область антитела, обладающая связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; вариабельная область антитела, обладающая связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 168; и вариабельная область общей L-цепи антитела представляет собой аминокислотную последовательность SEQ ID NO: 223.
Приемлемая мультиспецифическая антигенсвязывающая молекула, содержащаяся в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, содержит
(1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3;
(2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора; и
(3) домен, содержащий Fc-область с пониженной способностью связываться с Fcγ-рецептором, при этом ее структура не ограничена указанной структурой.
Согласно настоящему изобретению каждый из вышеуказанных доменов может быть сшит непосредственно с помощью пептидных связей. Например, когда применяют F(ab')2 в качестве домена, содержащего вариабельную область антитела, указанного в подпунктах (1) и (2), и указанные Fc-области в качестве домена, содержащего Fc-область с пониженной способностью связываться с Fcγ-рецептором, указанного в подпункте (3), то полипептиды, образованные путем сшивания содержащих вариабельных области доменов, указанных в подпунктах (1) и (2), и содержащего Fc-область домена, указанного в подпункте (3), с помощью пептидных связей, могут образовывать структуру антитела. Такие антитела можно получать путем очистки из указанной выше культуральной среды гибридомы, а также путем очистки антител из культуральной среды требуемых клеток-хозяев, которые стабильно несут полинуклеотиды, кодирующие полипептиды, которые образуют антитело.
Примеры предпочтительной вариабельной области Н-цепи антитела, содержащейся в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, которая содержится в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, включают вариабельные области Н-цепи антитела, которые представлены в таблице 1, или вариабельные области Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях Н-цепи, которые указаны в таблице 1, или вариабельные области Н-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.

Примеры предпочтительной вариабельной области антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащейся в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, включают вариабельные области антитела, обладающие связывающей активностью в отношении Т-клеточного рецептора. Из Т-клеточных рецепторов предпочтительным является CD3, а наиболее предпочтительным CD3ε. Примеры вариабельной области Н-цепи антитела, содержащейся в указанных вариабельных областях антитела, включают вариабельные области Н-цепи антитела, которые представлены в таблице 2, или вариабельные области Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях Н-цепи, которые указаны в таблице 2, или вариабельные области Н-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.
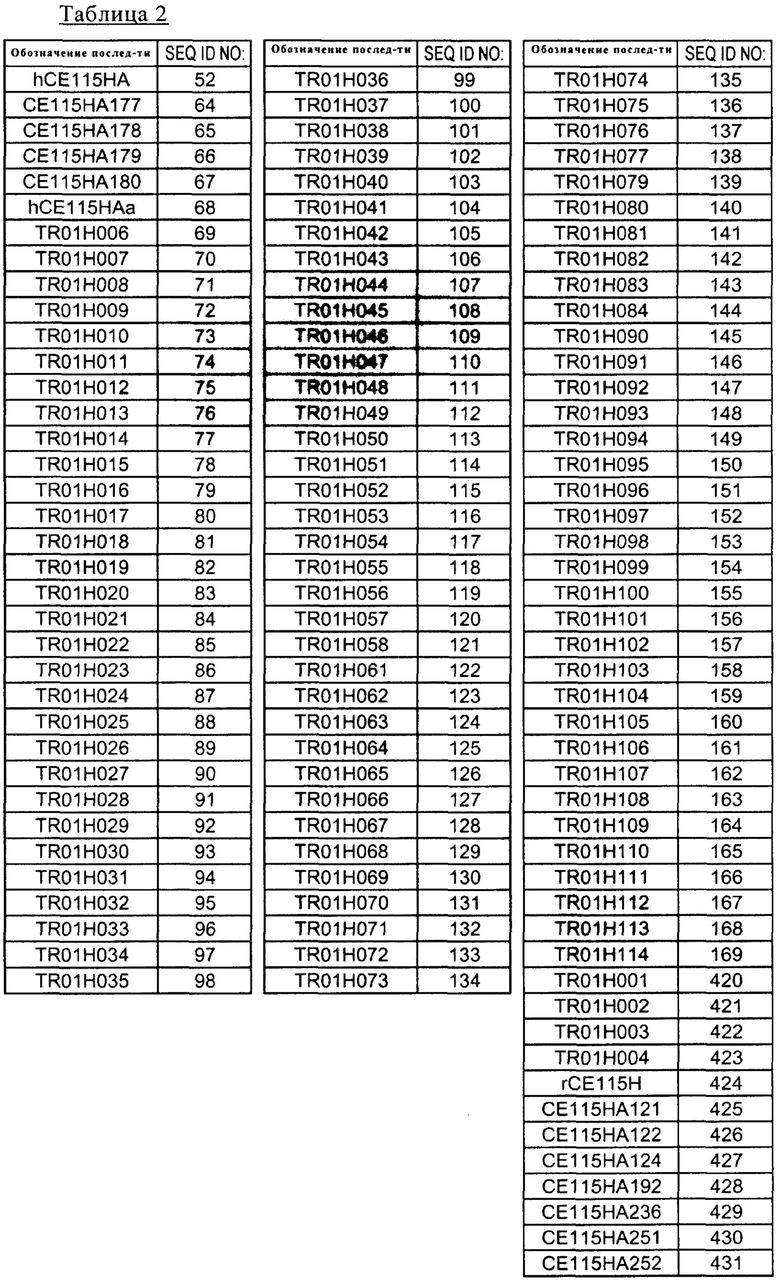
Взаимосвязь между аминокислотными остатками CDR-участков, образующих аминокислотную последовательность Н-цепи антитела, и EU-нумерацией Кэбота, представлена на фиг. 24 (фиг. 24-1 и 24-2).
Касательно вариабельных областей L-цепи антитела, содержащихся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, и вариабельной области антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, которые содержатся в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, то предпочтительно следует получать общую L-цепь, которая может придавать связывающую активность Н-цепи, которая обладает связывающей активностью в отношении глипикана 3, и связывающую активность Н-цепи, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и применять ее в качестве вариабельной области общей L-цепи мультиспецифической антигенсвязывающей молекулы.
Примеры вариабельной области общей L-цепи, которую можно применять согласно настоящему изобретению, включают вариабельные области L-цепи, указанные в таблице 3, вариабельные области L-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях L-цепи антитела, указанных в таблице 3, и вариабельные области L-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.
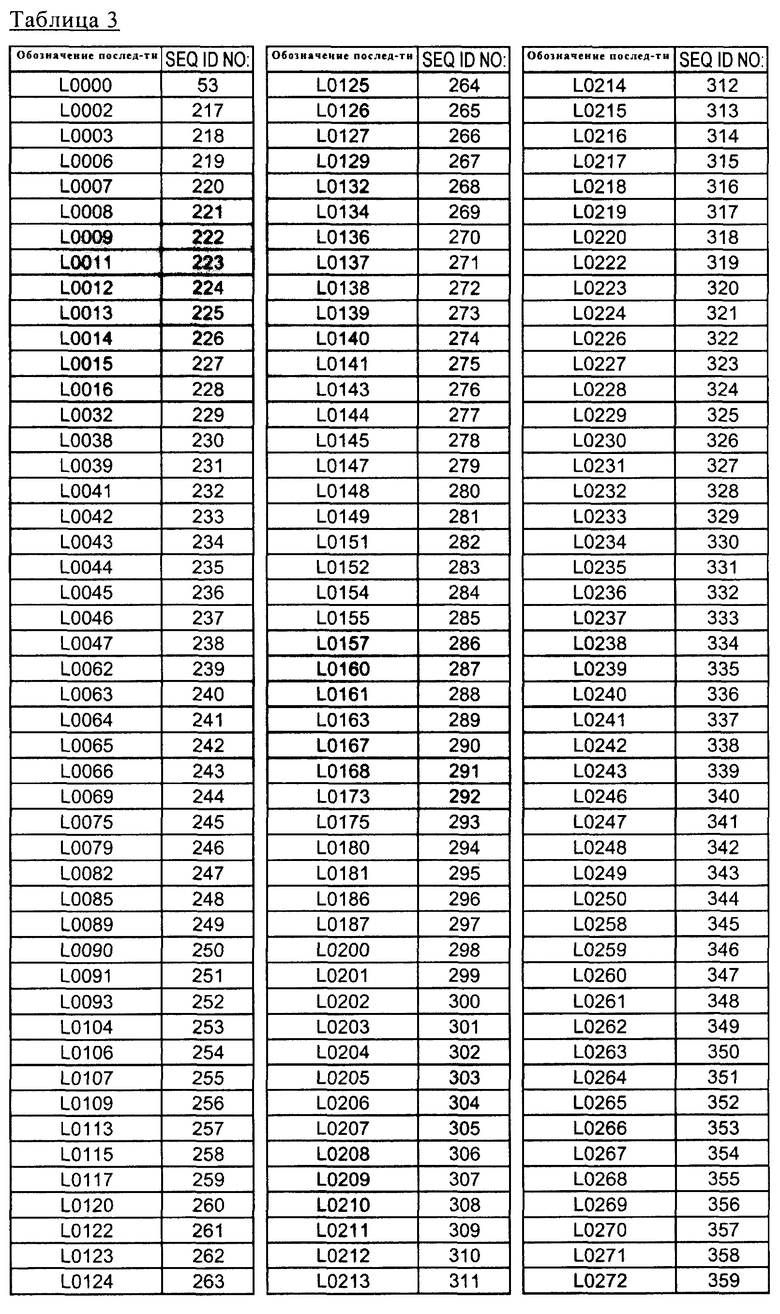
Взаимосвязь между аминокислотными остатками CDR-участков, образующих аминокислотную последовательность L-цепи антитела, и EU-нумерацией Кэбота, представлена на фиг. 25.
В настоящем изобретении фраза «функционально эквивалентный» означает, что аффинности связывания с антигеном эквиваленты или в альтернативном варианте означает, что цитотоксическая активность в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, эквивалентна при применении в качестве мультиспецифической антигенсвязывающей молекулы. Аффиность связывания и цитотоксическую активность можно измерять с помощью метода, указанного в настоящем описании. Клетки, применяемые для измерения цитотоксической активности, могут представлять собой требуемые экспрессирующие GPC3 клетки или требуемую ткань, содержащую указанные клетки, и, например, можно применять человеческие раковые линии клеток и PC-10 или NCI-H446, которые экспрессируют GPC3. Касательно константных областей антитела фраза может означать, что связывающая активность в отношении Fcγ-рецептора является эквивалентной.
Например, фраза «вариабельная область Н-цепи антитела, функционально эквивалентная вариабельной области Н-цепи антитела, указанной в настоящем описании (т.е. исходной вариабельной области Н-цепи)», означает, что эта область имеет такую же аффинность связывания, когда ее объединяют с вариабельной областью L-цепи антитела, указанной в настоящем описании, которая образует пару с исходной Н-цепью, или в альтернативном варианте означает, что область обладает такой же цитотоксической активностью в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, когда ее применяют для получения мультиспецифической антигенсвязывающей молекулы. Кроме того, фраза «вариабельная область L-цепи антитела, функционально эквивалентная вариабельной области L-цепи антитела, указанной в настоящем описании (т.е. исходной вариабельной области L-цепи)», означает, что эта область имеет такую же аффинность связывания, когда ее объединяют с вариабельной областью Н-цепи антитела, указанной в настоящем описании, которая образует пару с исходной L-цепью, или в альтернативном варианте означает, что область обладает такой же цитотоксической активностью в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, когда ее применяют для получения мультиспецифической антигенсвязывающей молекулы.
Понятие «эквивалентный» не обязательно подразумевает наличие такого же уровня активности, и активность может быть повышенной. В частности, антигенсвязывающая аффинность, включает, например, случай, в котором коэффициент (величина KD/величина KD родительского антитела), полученный путем сравнения с аффинностью связывания вариабельной области антитела, которая служит в качестве контроля (величина KD родительского антитела) составляет 1,5 или менее. Коэффициент величина KD/величина KD родительского антитела предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее, или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. Более конкретно, согласно настоящему изобретения коэффициент величина KD/величина KD родительского антитела предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3. Касательно цитотоксической активности, примеры включают случай, в котором коэффициент (скорость ингибирования клеточной пролиферации/скорость ингибирования клеточной пролиферации родительским антителом), полученный путем сравнения со скоростью ингибирования клеточной пролиферации мультиспецифической антигенсвязывающей молекулой, которая служит в качестве контроля (скорость ингибирования клеточной пролиферации родительским антителом), составляет 0,7 или более. Концентрацию добавленной мультиспецифической антигенсвязывающей молекулы можно определять соответствующим образом, но предпочтительно она составляет, например 0,01, 0,05, 0,1, 0,5 или 1 нМ; и предпочтительно измерения осуществляют при концентрации 0,05 или 0,1 нМ. Коэффициент скорость ингибирования клеточной пролиферации/скорость ингибирования клеточной пролиферации родительским антителом предпочтительно составляет 0,8 или более, более предпочтительно 0,9 или более, 1,0 или более, 1,2 или более, 1,5 или более, 2 или более, 3 или более, 5 или более, 10 или более или 20 или более. При этом не существует верхнего предела, коэффициент может составлять 10, 102, 103, 104, 105 или 106.
Кроме того, касательно цитотоксической активности примеры включают случай, в котором коэффициент (концентрация, вызывающая ингибирование клеточной пролиферации на 50% / концентрация родительского антитела, вызывающая ингибирование клеточной пролиферации на 50%), полученный путем сравнения с концентрацией исходной мультиспецифической антигенсвязывающей молекулы, вызывающей ингибирование клеточной пролиферации на 50% (концентрация родительского антитела, вызывающая ингибирование клеточной пролиферации на 50%), составляет 1,5 или менее. Концентрация, вызывающая ингибирование клеточной пролиферации на 50%, означает концентрацию мультиспецифической антигенсвязывающей молекулы, необходимую для снижения скорости клеточной пролиферации наполовину по сравнению с вариантом, в котором не добавляют мультиспецифическую антигенсвязывающую молекулу. Коэффициент «концентрация, вызывающая ингибирование клеточной пролиферации на 50%/концентрация родительского антитела, вызывающая ингибирование клеточной пролиферации на 50%» предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. В частности, коэффициент предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3.
Касательно домена, содержащего вариабельную область антитела, которая обладает GPC3-связывающей активностью, величина KD, характеризующая связывание с GPC3 (например, человеческим GPC3) может составлять, например, 5×10-9 М или менее, предпочтительно 4×10-9 М или менее, например, 3×10-9 М или менее, 2×10-9 М или менее, 1×10-9 М или менее, 8×10-10 M или менее, 5×10-10 М или менее, 4×10-10 М или менее, 3×10-10 М или менее, 2×10-10 M или менее, 1×10-10 М или менее, 8×10-11 М или менее, 5×10-11 М или менее, 4×10-11 М или менее, 3×10-11 М или менее, 2×10-11 М или менее, 1×10-11 М или менее, 8×10-12 М или менее, 5×10-12 М или менее, 4×10-12 М или менее, 3×10-12 М или менее, 2×10-12 М или менее, 1×10-12 М или менее, 8×10-13 М или менее, 5×10-13 M или менее, 4×10-13 М или менее, 3×10-13 М или менее, 2×10-13 М или менее или 1×10-13 М или менее.
Касательно домена, содержащего вариабельную область, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, величина KD, характеризующая связывание с человеческим комплексом Т-клеточного рецептора, такого как человеческий Т-клеточный рецептор или более конкретно, например, человеческий CD3ε, может составлять, например, 2×10-7 М или менее, предпочтительно 1,5×10-7 М или менее, например, 1,4×10-7 М или менее, 1,3×10-7 М или менее, 1,2×10-7 М или менее, 1×10-7 М или менее, 3×10-8 М или менее, 2×10-8 М или менее, 1×10-8 М или менее, 8×10-9 М или менее, 5×10-9 М или менее, 4×10-9 М или менее, 3×10-9 М или менее, 2×10-9 М или менее, 1×10-9 М или менее, 8×10-10 М или менее, 5×10-10 М или менее, 4×10-10 М или менее, 3×10-10 М или менее, 2×10-10 М или менее, 1×10-10 М или менее, 8×10-11 М или менее, 5×10-11 М или менее, 4×10-11 М или менее, 3×10-11 М или менее, 2×10-11 М или менее, 1×10-11 М или менее,, 8×10-12 М или менее, 5×10-12 М или менее, 4×10-12 М или менее, 3×10-12 М или менее, 2×10-12 М или менее или 1×10-12 М или менее.
Мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, предпочтительно имеют величины KD, характеризующая связывание с человеческим GPC3 и человеческим комплексом Т-клеточного рецептора (например, с человеческой CD3ε-цепью), которые составляют 5×10-9 М или менее и 2×10-7 М или менее соответственно и более предпочтительно 1×10-9 М или менее и 5×10-8 М или менее соответственно.
В настоящем изобретении вариабельные области антитела, которые являются «функционально эквивалентными» не ограничены конкретными областями, если они представляют собой вариабельные области Н-цепи и/или L-цепи антитела, которые удовлетворяют вышеуказанным требованиям. Примеры таких вариабельных областей антитела включают области, полученные путем интродукции замены, делеции, добавления и/или инсерции одной или нескольких аминокислот (например, 1, 2, 3, 4, 5 или 10 аминокислот) в аминокислотные последовательности вариабельных областей, которые представлены выше в таблицах 1-3. Хорошо известный специалистам в данной области метод интродукции одной или нескольких аминокислотных замен, делеций, добавлений и/или инсерций в аминокислотную последовательность представляет собой метод интродукции мутаций в белки. Например, специалисты в данной области могут получать вариабельные области, которые являются функциональными эквивалентами вариабельных областей антитела, обладающих указанными выше функциями, путем интродукции соответствующих мутаций в аминокислотные последовательности с использованием таких методов как сайтнаправленный мутагенез (Hashimoto-Gotoh Т., Mizuno Т., Ogasahara Y. и Nakagawa M., An oligodeoxyribonucleotide-directed dual amber method for site-directed mutagenesis. Gene 152, 1995, cc. 271-275; Zoller M.J. и Smith M., Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors. Methods Enzymol. 100, 1983, cc. 468-500; Kramer W. Drutsa V., Jansen H.W., Kramer В., Pflugfelder M. и Fritz H.J., The gapped duplex DNA approach to oligonucleotide-directed mutation construction. Nucleic Acids Res. 12, 9441-9456; Kramer W. и Fritz, H.J., Oligonucleotide-directed construction of mutations via gapped duplex DNA Methods. Enzymol. 154, 1987, cc. 350-367; и Kunkel T.A., Rapid and efficient site-specific mutagenesis without phenotypic selection. Proc Nati Acad. Sci. USA. 82, 1985, cc. 488-492).
Когда аминокислотный остаток изменяют, аминокислоту предпочтительно заменяют в результате мутации на другую(ие) аминокислоту(ы), сохраняющую(ие) характеристики боковых цепей аминокислот, указанные выше. Примерами аминокислот с такими характеристиками боковых цепей являются: гидрофобные аминокислоты (A, I, L, M, F, P, W, Y и V), гидрофильные аминокислоты (R, D, N, С, Е, Q, G, Н, K, S и Т), аминокислоты, содержащие алифатические боковые цепи (G, А, V, L, I и P), аминокислоты с содержащими гидроксильную группу боковыми цепями (S, Т и Y), аминокислоты с содержащими атом серы боковыми цепями (С и M), аминокислоты с содержащими карбоновую кислоту и амид боковыми цепями (D, N, Е и Q), аминокислоты с основными боковыми цепями (R, K и Н) и аминокислоты с ароматическими боковыми цепями (Н, F, Y и W) (в скобках представлены обозначения аминокислот в соответствии с однобуквенным кодом). Аминокислотные замены внутри каждой из указанных групп обозначают как консервативные замены. Хорошо известно, что полипептид, содержащий модифицированную аминокислотную последовательность, в которой один или несколько аминокислотных остатков в указанной аминокислотной последовательности подвергнут делеции, добавлен и/или заменен на другие аминокислоты, может сохранять исходную биологическую активность (Mark D. F. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc. 5662-5666; Zoller M. J. и Smith M., Nucleic Acids Res. 10, 1982, cc. 6487-6500; Wang А. и др., Science 224, 1984, cc. 1431-1433; Dalbadie-McFarland G. и др., Proc. Natl. Acad. Sci. USA) 79, 1982, cc. 6409-6413). Вариабельные области, предлагаемые в настоящем изобретении, содержащие указанные аминокислотные модификации, имеют аминокислотные последовательности, которые идентичны по меньшей мере на 70%, более предпочтительно по меньшей мере на 75%, еще более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 85%, еще более предпочтительно по меньшей мере на 95% аминокислотным последовательностям CDR-последовательностей, FR-последовательностям вариабельной области или полным вариабельным областям до модификации. В контексте настоящего описания идентичность последовательностей определяют в виде процента остатков, идентичных остаткам в исходной аминокислотной последовательности вариабельной области Н-цепи или вариабельной области L-цепи, определенного после выравнивания последовательностей и интродукции соответствующих брешей для увеличения до максимума при необходимости идентичности последовательностей. Идентичность аминокислотных последовательностей можно определять с помощью описанного ниже метода.
Кроме того, «функционально эквивалентную вариабельную область антитела» можно получать, например, из нуклеиновых кислот, которые гибридизуются в строгих условиях с нуклеиновыми кислотами, которые содержат нуклеотидную последовательность, кодирующую аминокислотную последовательность вариабельной области, указанной выше в таблицах 1-3. Строгие условия гибридизации, применяемые для выделения нуклеиновой кислоты, которая гибридизуется в строгих условиях с нуклеиновой кислотой, которая содержат нуклеотидную последовательность, кодирующую аминокислотную последовательность вариабельной области, включают, например, следующие условия: 6 М мочевина, 0,4% ДСН, 0,5×SSC и 37°С или условия гибридизации в значительной степени эквивалентные указанным выше. Выделение нуклеиновых кислот с максимально высокой гомологией можно ожидать при применении более строгих условий, например, следующих условий: 6 М мочевина, 0,4% ДСН, 0,1×SSC и 42°С. Условия промывки после гибридизации представляют собой, например, промывку с использованием 0,5×SSC (1×SSC представляет собой 0,15 М NaCl и 0,015 М цитрат натрия, рН 7,0) и 0,1% ДСН при 60°С, более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 60°С, еще более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 62°С, еще более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 65°С и еще более предпочтительно промывку с использованием 0,1×SSC и 0,1% ДСН при 65°С, как указано выше. Последовательности выделенных нуклеиновых кислот можно определять известными методами, которые описаны ниже. Общая гомология нуклеотидной последовательности выделенной нуклеиновой кислоты составляет по меньшей мере 50% или выше, предпочтительно 70% или выше и наиболее предпочтительно 90% или выше (например, 95%, 96%, 97%, 98%, 99% или выше) при оценке степени идентичности последовательностей.
Нуклеиновые кислоты, которые гибридизуются в строгих условиях с нуклеиновой кислотой, содержащей нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области, можно выделять также, применяя вместо описанных выше методов на основе гибридизации, методы амплификации генов, такие как полимеразная цепная реакция (ПЦР), в которой используют праймеры, синтезированные на основе информации о нуклеотидной последовательности, которая кодирует аминокислотную последовательность вариабельной области.
Идентичность одной нуклеотидной последовательности или аминокислотной последовательности можно определять с помощью алгоритма BLAST, описанного выше у Karlin и Altschul (Proc. Natl. Acad. Sci. USA 90, 1993, cc. 5873-5877). На основе этого алгоритма разработаны программы BLASTN и BLASTX (Altschul и др., J. Mol. Biol. 215, 1990, сс. 403-410). Для анализа нуклеотидных последовательностей согласно BLASTN на основе BLAST устанавливают параметры, такие, например, как балл = 100 и длина слова = 12. С другой стороны, параметры, применяемые для анализа аминокислотных последовательностей с помощью BLASTX на основе BLAST, включают, например, балл - 50 и длина слова = 3. Задаваемые по умолчанию параметры применяют для каждой программы, когда используют программы BLAST и Gapped BLAST. В данной области известны конкретные методики указанных анализов (см. веб-сайт National Center for Biotechnology Information (NCBI), Basic Local Alignment Search Tool (BLAST); http://www.ncbi.nlm.nih.gov).
Комбинация вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, входящая в мультиспецифическую антигенсвязывающую молекулу, содержащуюся в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, не ограничена конкретной комбинацией, если она обладает указанными выше видами активности. Однако согласно настоящему изобретению цитотоксическая активность мультиспецифической антигенсвязывающей молекулы предпочтительно эквивалентна или выше, чем активность биспецифического антитела GPC3_ERY22_rCE115, описанного в приведенном для справки примере 3. В контексте настоящего описания понятие «эквивалентный» необязательно подразумевает такую же степень указанной выше активности, и активность может быть более высокой. Молекула является эквивалентной GPC3_ERY22_rCE115, например, когда коэффициент (скорость ингибирования клеточной пролиферации/скорость ингибирования клеточной пролиферации (GPC3_ERY22_rCE115)) относительно скорости ингибирования клеточной пролиферации GPC3_ERY22_rCE115 (скорость ингибирования клеточной пролиферации (GPC3_ERY22_rCE115)) составляет 0,7 или более, предпочтительно 0,8 или более, 0,9 или более, 1,0 или более, 1,2 или более, 1,5 или более, 2 или более, 3 или более, 5 или более, 10 или более или 20 или более. В то время как не существует верхнего предела, показатель может составлять, например, 10, 102, 103, 104, 105 или 106. Концентрацию добавленной мультиспецифической антигенсвязывающей молекулы можно определять соответствующим образом, но предпочтительно она составляет, например 0,01, 0,05, 0,1, 0,5 или 1 нМ; и предпочтительно измерения осуществляют при концентрации 0,05 или 0,1 нМ.
Кроме того, примеры включают вариант, когда коэффициент «концентрация, вызывающая ингибирование клеточной пролиферации на 50%/концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточной пролиферации на 50%», полученный путем сравнения с концентрацией (GPC3_ERY22_rCE115), которая вызывает ингибирование клеточной пролиферации на 50% (концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточной пролиферации на 50%), составляет 1,5 или менее. Коэффициент «концентрация, вызывающая ингибирование клеточной пролиферации на 50%/концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточной пролиферации на 50%» предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. В частности, коэффициент предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3.
Предпочтительные конкретные величины KD, характеризующие связывание с человеческим GPC3 и комплексом человеческого Т-клеточного рецептора (например, с человеческой CD3ε-цепью) также соответствуют указанным выше. Можно применять соответствующие экспрессирующие GPC3 клетки или соответствующую ткань, содержащую указанные клетки, и, например, можно применять человеческие раковые линии клеток РС-10 или NCl-Н446, которые экспрессируют GPC3.
Примеры указанной комбинации вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, включают комбинации вариабельных областей Н-цепи антитела, которые представлены в таблице 4, комбинации вариабельных областей Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что и аминокислотные последовательности CDR1, CDR2 и CDR3, которые входят в вариабельные области Н-цепи антитела, представленные в таблице 4, и комбинации вариабельных областей Н-цепи антитела, функционально эквивалентные указанным вариабельным областям. В контексте настоящего описания понятие «функционально эквивалентные» имеет значение, указанное выше.
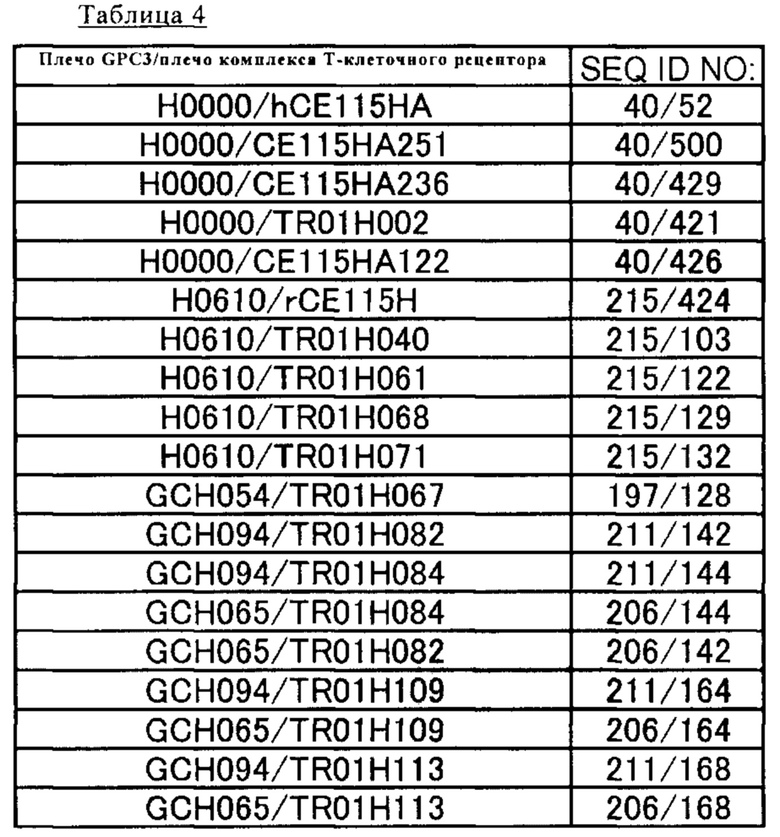
Предпочтительная общая L-цепь для таких комбинаций вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, включает, например, L0000, L0011, L0201, L0203, L0204, L0206, L0208, L0209, L0211, L0212, L0222 и общую L-цепь, которая имеет последовательности CDR (аминокислотные последовательности CDR1, CDR2 и CDR3), идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3, указанным выше для общей L-цепи. Конкретные комбинации включают, например, комбинации вариабельных областей Н-цепи антитела и общей L-цепи, которые представлены в таблице 5, комбинации вариабельных областей антитела, которые имеют последовательности CDR (аминокислотные последовательности CDR1, CDR2 и CDR3), идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3, которые входят в вариабельные области общей L-цепи, представленные в таблице 5, и комбинации вариабельных областей Н-цепи антитела и общей L-цепи, функционально эквивалентные указанным вариабельным областям. В контексте настоящего описания понятие «функционально эквивалентные» имеет значение, указанное выше.
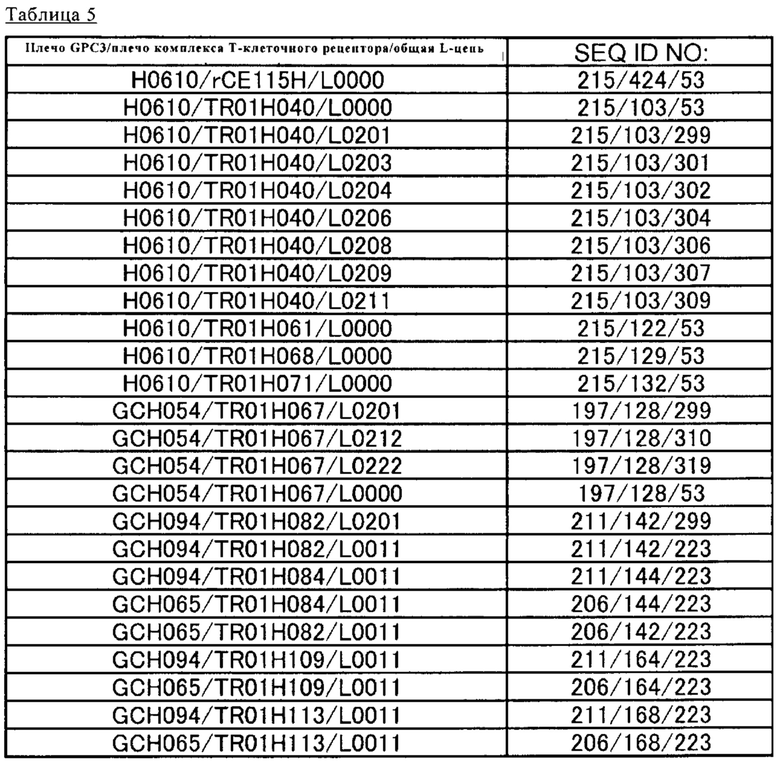
Не накладываются конкретные ограничения на Fc-область, входящую в мультиспецифическую антигенсвязывающую молекулу, которая содержится в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, если она представляет собой Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора, но примеры предпочтительной Fc-области, предлагаемой в настоящем изобретении, включают комбинацию участка Fc-области E22Hh и участка Fc-области E22Hk, комбинацию участка Fc-области E2702GsKsc и участка Fc-области E2704sEpsc и комбинацию участка Fc-области E2702sKsc и участка Fc-области E2704sEpsc.
Примеры предпочтительной мультиспецифической антигенсвязывающей молекулы, которая содержится в противораковом агенте или фармацевтической композиции, предлагаемом/предлагаемой в настоящем изобретении, включают биспецифические антитела, которые содержат вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3ε. Более предпочтительно цитотоксическая активность является такой же или превышает активность биспецифического антитела GPC3_ERY22_rCE115. Примеры указанных биспецифических антител включают биспецифические антитела, содержащие Н- и L-цепи, указанные в таблице 17, и биспецифические антитела, которые связываются с эпитопом, перекрывающимся с эпитопом, связывающимся с указанными выше антителами, и которые содержат Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора.
Распознает ли антитело эпитоп, который перекрывается с эпитопом, распознаваемым другим антителом, можно определять на основе конкуренции между двумя антителами за эпитоп. Конкуренцию между антителами можно оценивать с помощью анализов связывания в условиях конкуренции, таких как твердофазный иммуноферментный анализ (ELISA), метод на основе флуоресцентного резонансного переноса энергии (FRET) и метод на основе технологии флуорометрического микрообъемного анализа (FMAT (зарегистрированный товарный знак)). Количество антитела, связанного с антигеном, косвенно коррелирует со связывающей способностью конкурирующего антитела-кандидата (тестируемое антитело), которое конкурентно связывается с перекрывающимся эпитопом. Другими словами, если количество или аффинность тестируемого антитела к перекрывающемуся эпитопу возрастает, то количество антитела, связанного с антигеном, снижается, а количество антигена, связанного тестируемым антителом, возрастает. В частности, соответствующим образом меченое антитело и антитело, подлежащее изучению, добавляют одновременно к антигену, и антитело, которое в результате связывается, обнаруживают с помощью метки. Количество связанного с антигеном антитела легко можно определять с помощью предварительно меченого антитела. Указанная метка не ограничена конкретной меткой и метод мечения выбирают в зависимости от применяемой методики анализа. В частности метод мечения включает введение флуоресцентной метки, радиоактивной метки, ферментной метки и т.п.
Например, флуоресцентно меченое антитело и немеченое антитело или тестируемое антитело одновременно добавляют к гранулам, на которых иммобилизован GPC3 или CD3ε, и меченое антитело выявляют с помощью технологии флуорометрического микрообъемного анализа.
В контексте настоящего описания «антитело, которое связывается с перекрывающимся эпитопом» означает тестируемое антитело, которое может снижать количество связанного меченого антитела по меньшей мере на 50% в концентрации, которая, как правило, выше в 100 раз, предпочтительно выше в 80 раз, более предпочтительно выше в 50 раз, еще более предпочтительно выше в 30 раз и еще более предпочтительно выше в 10 раз концентрации, в которой немеченое антитело снижает на 50% количество связанного меченого антитела (IC50).
Мультиспецифические антигенсвязывающие молекулы, которые имеют антигенсвязывающие сайты антитела, связывающиеся с эпитопами, которые перекрываются с эпитопами, связывающимися вышеуказанными антителами, могут обладать очень высокой цитотоксической активностью.
Мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, получают с помощью такой же технологии, которая описана выше в качестве метода получения рекомбинантных антител.
Комбинированные терапии и фармацевтические композиции
Одним из не ограничивающих объем изобретения вариантом осуществления настоящего изобретения являются способы комбинированной терапии, предлагаемой в настоящем изобретении, обеспечивающие повреждение клеток, подавление клеточной пролиферации, активацию иммунитета против раковых клеток или содержащих раковые клетки опухолевых тканей, способы лечения рака или предупреждения рака, в каждом из указанных способов подразумевается введения в эффективных количествах описанного выше биспецифического антитела и другого противоракового агента. В некоторых вариантах осуществления изобретения комбинированная терапия, предлагаемая в настоящем изобретении, обладает высокой эффективностью в отношении повреждения клеток, подавления клеточной пролиферации, активации иммунитета против раковых клеток или содержащих раковые клетки опухолевых тканей, лечения рака или предупреждения рака по сравнению с монотерапией, в которой используется описанное выше биспецифическое антитело или другой противораковый агент.В другом варианте осуществления изобретения комбинированная терапия, предлагаемая в настоящем изобретении, обладает синергетическими действиями или аддитивными действиями в отношении повреждения клеток, подавления клеточной пролиферации, активации иммунитета против раковых клеток или содержащих раковые клетки опухолевых тканей, лечения рака или предупреждения рака.
В некоторых вариантах осуществления изобретения понятие «эффективное количество» согласно настоящему изобретению относится к дозе указанного выше биспецифического антитела и/или другого противоракового агента, которая является эффективной в отношении лечения или предупреждения заболевания у индивидуума. Заболевание не ограничено конкретным заболеванием, но предпочтительно оно представляет собой рак.
В некоторых вариантах осуществления изобретения «лечение/лечить/терапевтическое действие» согласно настоящему изобретению означает, что комбинированная терапия, предлагаемая в настоящем изобретении, снижает количество раковых клеток у индивидуумов, подавляет пролиферацию раковых клеток, уменьшает размер опухоли, подавляет инфильтрацию раковых клеток в периферические органы, подавляет метастазы раковых клеток или облегчает различные симптомы, обусловленные раком. Кроме того, в некоторых вариантах осуществления изобретения понятие «предупреждение/предупреждать/профилактическое действие» согласно настоящему изобретению относится к ингибированию увеличения количества раковых клеток из-за репопуляции раковых клеток, количество которых было снижено, к ингибированию репопуляции раковых клеток, пролиферация которых подавлена, и к ингибированию повторного увеличения уменьшенного размера опухолей.
Некоторыми вариантами осуществления изобретения являются способы комбинированной терапии, предлагаемой в настоящем изобретении, обеспечивающие повышение терапевтических или профилактических действий другого противоракового агента путем применения указанного выше биспецифического антитела для лечения или предупреждения рака в сочетании с другим противораковым агентом. Другим вариантом осуществления настоящего изобретения являются способы комбинированной терапии, предлагаемой в настоящем изобретении, обеспечивающие повышение терапевтических или профилактических действий описанного выше биспецифического антитела путем применения другого противоракового агента для лечения или предупреждения рака в сочетании с биспецифическим антителом. В контексте настоящего описания повышение терапевтических или профилактических действий относится, например, к повышению уровня эффективности лечения, снижению количества противоракового агента, применяемого для лечения, и/или укорочению периода лечения противораковым агентом, но не ограничено указанным. Другим вариантом осуществления изобретения являются способы комбинированной терапии, предлагаемой в настоящем изобретении, обеспечивающие удлинение периода выживаемости без прогрессирования у индивидуумов, где способ включает введение в эффективном количестве указанного выше биспецифического антитела и другого противоракового агента.
В некоторых вариантах осуществления изобретения комбинированная терапия, предлагаемая в настоящем изобретении, предусматривает введение указанного выше биспецифического антитела и другого противоракового агента. Биспецифическое антитело и другой противораковый агент можно применять с использованием любых пригодных методов, известных в данной области. Например, биспецифическое антитело и другой противораковый агент можно применять параллельно (т.е. одновременно) или последовательно (т.е. в различные моменты времени). В некоторых вариантах осуществления изобретения, в которых биспецифическое антитело и другой противораковый агент применяют последовательно (т.е. в различные моменты времени), интервал между введением биспецифического антитела и другого противоракового агента не ограничен конкретно, и интервал можно определять с учетом таких факторов, как путь введения и лекарственная форма. Интервал составляет, например, от 0 до 168 ч, предпочтительно от 0 до 72 ч, более предпочтительно от 0 до 24 ч и еще более предпочтительно от 0 до 12 ч, но не ограничен указанными интервалами.
В некоторых вариантах осуществления изобретения указанное выше биспецифическое антитело и другой противораковый агент вводят одновременно. В некоторых вариантах осуществления изобретения биспецифическое антитело вводят с определенными интервалами (т.е. с перерывами). В некоторых вариантах осуществления изобретения биспецифическое антитело вводят до введения другого противоракового агента. В некоторых вариантах осуществления изобретения биспецифическое антитело вводят после введения другого противоракового агента.
В некоторых вариантах осуществления изобретения другой противораковый агент вводят с определенными интервалами (т.е. с перерывами). В некоторых вариантах осуществления изобретения другой противораковый агент вводят до введения биспецифического антитела. В некоторых вариантах осуществления изобретения другой противораковый агент вводят после введения биспецифического антитела.
В некоторых вариантах осуществления изобретения биспецифические антитела, указанные в настоящем описании, и противораковые агенты, которые являются известными или указаны в настоящем описании, можно применять в указанных выше комбинированных терапиях, в которых используют биспецифические антитела и другие противораковые агенты.
В некоторых вариантах осуществления изобретения можно осуществлять дополнительную терапию помимо комбинированных терапий, в которых используют указанное выше биспецифическое антитело и другой противораковый агент. В некоторых вариантах осуществления изобретения терапия, которую добавляют к комбинированной терапии, предлагаемой в настоящем изобретении, может включать дополнительное введение биспецифического антитела и/или другого противоракового агента.
Вариантом осуществления настоящего изобретения, не ограничивающим его объем, являются агенты для индукции цитотоксичности, агенты для подавления пролиферации (агенты для ингибирования клеточной пролиферации), агенты для активации иммунного ответа против раковых клеток или содержащих раковые клетки опухолевых тканей, агенты для лечения рака и агенты для предупреждения рака (ниже в контексте настоящего описания обозначены как фармацевтические композиции и т.п.), каждый из которых содержит указанное выше биспецифическое антитело, другой противораковый агент или комбинацию биспецифического антитела и другого противоракового агента. В некоторых вариантах осуществления изобретения фармацевтические композиции и т.п., указанные в настоящем изобретении, можно применять в комбинированной терапии, предлагаемой в настоящем изобретении. В некоторых вариантах осуществления изобретения фармацевтические композиции и т.п., предлагаемые в настоящем изобретении, обладают высокой эффективностью в отношении повреждения клеток, подавления клеточной пролиферации, активации иммунитета против раковых клеток или содержащих раковые клетки опухолевых тканей, лечения рака или предупреждения рака в результате совместного применения указанного выше биспецифического антитела и другого противоракового агента по сравнению с монотерапией, в которой используется описанное выше биспецифическое антитело или другой противораковый агент. В другом варианте осуществления изобретения фармацевтические композиции, предлагаемые в настоящем изобретении, обладают синергетическими действиями или аддитивными действиями в отношении повреждения клеток, подавления клеточной пролиферации, активации иммунитета против раковых клеток или содержащих раковые клетки опухолевых тканей, лечения рака или предупреждения рака в результате совместного применения указанного выше биспецифического антитела и другого противоракового агента.
В некоторых вариантах осуществления изобретения понятие «фармацевтические композиции и т.п., предлагаемые в настоящем изобретении, содержащие комбинацию биспецифического антитела и другого противоракового агента» относится к фармацевтическим композициям и т.п., в которых указанное выше биспецифическое антитело и другой противораковый агент объединены для применения путем одновременного, раздельного или последовательного введения при лечении или предупреждении заболевания. Например, фармацевтические композиции и т.п., предлагаемые в настоящем изобретении, могут находиться в форме комбинированного препарата, содержащего как биспецифическое антитело, так и противораковый агент. Альтернативно этому, например, касательно фармацевтических композиций и т.п., предлагаемых в настоящем изобретении, фармацевтический агент, содержащий биспецифическое антитело, и фармацевтический агент, содержащий другой противораковый агент, можно приготавливать отдельно и указанные фармацевтические агенты можно применять одновременно или последовательно. Заболевание не ограничено конкретным заболеванием, но предпочтительно представляет собой рак.
Некоторыми вариантами осуществления настоящего изобретения являются фармацевтические композиции и т.п., предназначенные для применения в комбинации с другим противораковым агентом, композиции, содержащие указанное выше биспецифическое антитело в качестве активного ингредиента.
Некоторыми вариантами осуществления настоящего изобретения являются фармацевтические композиции и т.п., предназначенные для применения в комбинации с указанным выше биспецифическим антителом, композиции, содержащие другой противораковый агент в качестве активного ингредиента.
Некоторыми вариантами осуществления настоящего изобретения являются фармацевтические композиции и т.п., предназначенные для усиления терапевтических действий другого противоракового агента при лечении рака с использованием указанного другого противоракового агента, например, путем применения указанного выше биспецифического в виде фармацевтических композиций и т.п., предлагаемых в настоящем изобретении, антитела в комбинации с указанным другим противораковым агентом.
Некоторыми вариантами осуществления настоящего изобретения являются фармацевтические композиции и т.п., предназначенные для усиления терапевтических действий указанного выше биспецифического антитела при лечении рака с использованием биспецифического антитела, путем применения другого противоракового агента в комбинации с биспецифическим антителом.
Некоторыми вариантами осуществления настоящего изобретения является применение описанного выше биспецифического антитела и/или другого противоракового агента для приготовления фармацевтических композиций и т.п., содержащих в качестве активных ингредиентов биспецифическое антитело и/или другой противораковый агент.
В настоящем изобретении выражение «содержащая в качестве активных ингредиентов описанное выше биспецифическое антитело и/или другой противораковый агент» означает присутствие биспецифического антитела и/или другого (иного) противоракового агента в качестве основного(ых) действующего(их) вещества(в)», и оно не ограничено содержанием биспецифического антитела и/или другого противоракового агента.
В некоторых вариантах осуществления изобретения биспецифические антитела, указанные в настоящем описании, и другие противораковые агенты, которые являются известными или указаны в настоящем описании, можно применять в описанных выше фармацевтических композициях и других формах.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения описанные выше другие противораковые агенты включают (но, не ограничиваясь только ими) аналоги горчичного газа (иприта), алкилсульфонаты, этиленимины, нитрозомочевины, эпоксиды, другие алкилирующие агенты, аналоги фолиевой кислоты, аналоги пуринов, аналоги пиримидинов, другие антиметаболиты, алкалоиды барвинка или их аналоги, производные подофиллотоксина, аналоги камптотекана, производные колхицина, таксаны, другие растительные алкалоиды или встречающиеся в естественных условиях субстанции, актиномицины, антрациклины или родственные субстанции, другие цитотоксические антибиотики, соединения платины, метилгидразины, ингибиторы киназ, ингибиторы ангиогенеза, гормональные агенты, ингибиторы ДНК-модифицирующих ферментов, иммуностимуляторы, ингибиторы протеосом, ферменты, ингибиторы деацетилазы гистонов, препараты цитокинов, ретиноиды, ингибиторы иммунных контрольных точек, ингибиторы индоламин-2,3-диоксигеназы (IDO), активаторы костимуляторных молекул, активаторы естественных клеток-киллеров, моноклональные антитела, другие таргетируемые молекулами агенты и другие противораковые агенты. В не ограничивающем объем изобретения варианте осуществления настоящего изобретения другие противораковые агенты, предлагаемые в настоящем изобретении, включают (но, не ограничиваясь только ими), например, антитела, описанные в WO 2015/174439 и WO 2015/156268.
В некоторых вариантах осуществления изобретения понятие «иммунная контрольная точка», предлагаемая в настоящем изобретении, относится к молекуле, которая экспрессируется на иммунокомпетентных клетках (включая Т-клетки) и связывается с лигандом, что приводит к трансдукции сигналов иммунокомпетентных клеток, которые ингибируют иммунный ответ. Примеры иммунных контрольных точек и их лигандов включают (но, не ограничиваясь только ими) такие молекулы как PD-1, CTLA-4, TIM3, LAG3, PD-L1, PD-L2, BTNL2, В7-Н3, В7-Н4, CD48, CD80, 2В4, BTLA, CD160, CD60, CD86 и VISTA. В некоторых вариантах осуществления изобретения понятие «ингибитор иммунной контрольной точки», предлагаемый в настоящем изобретении, относится к фармацевтическому агенту, который ингибирует связывание между иммунной контрольной точкой и ее лигандом и тем самым ингибирует трансдукцию сигнала, обусловленную иммунной контрольной точкой.
Не ограничивающим объем изобретения вариантом осуществления настоящего изобретения являются фармацевтические композиции и т.п., в которых другой противораковый агент представляет собой химиотерапевтический агент, активирующий Т-клетки агонистический агент, ингибитор иммунной контрольной точки или ингибитор антиагиогенеза.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения химиотерапевтические агенты включают (но, не ограничиваясь только ими) антиметаболиты, растительные алкалоиды и соединения платины. Предпочтительные примеры антиметаболитов включают (но, не ограничиваясь только ими) эноцитабин, капецитабин, кармофур, гемцитабин, цитарабин, тегафур, тегафур + урацил, неларабин, фторурацил, флударабин, пеметрексед, пентостатин и метотрексат. Наиболее предпочтительные антиметаболиты включают, например, капецитабин. Предпочтительные примеры растительных алкалоидов включают (но, не ограничиваясь только ими) иринотекан, этопозид, собузоксан, доцетаксел, ногитекан, паклитаксел, винорелбин, винкристин, виндезин и винбластин. Наиболее предпочтительные растительные алкалоиды включают, например, паклитаксел. Предпочтительные примеры соединений платины включают (но, не ограничиваясь только ими) оксалиплатин, карбоплатин, цисплатин и недаплатин. Наиболее предпочтительные соединения платины включают, например, цисплатин.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения активирующие Т-клетки агонистические агенты включают (но, не ограничиваясь только ими) агонистические антитела против (представителей) суперсемейства TNF-рецептора (TNFRSF) и агонистические антитела против костимуляторных молекул. Молекулы-мишени для «агонистических антител против (представителей) суперсемейства TNF-рецептора» не ограничены конкретно, если они представляют собой факторы, которые активируют клетки, экспрессирующие суперсемейство TNF-рецептора (например, Т-клетки и NK-клетки), но предпочтительно представляют собой факторы, принадлежащие к «суперсемейству TNF» или «суперсемейству TNF-рецептора». Известные факторы, принадлежащие к «суперсемейству TNF» или «суперсемейству TNF-рецептора» включают лиганды, имеющие трехмерную структуру, и рецепторы, имеющие трехмерную структуру, с которым связываются лиганды, участвующие в активации различных иммунных клеток (Nat. Rev. Immunol., 12, 2012, сс. 339-351). Примеры факторов, принадлежащих к суперсемейству TNF или суперсемейству TNF-рецептора, включают CD137, CD137L, CD40, CD40L, ОХ40, OX40L, CD27, CD70, HVEM, LIGHT, RANK, RANKL, CD30, CD153, GITR, GITRL, TNFRSF25 и TL1A. Предпочтительные факторы включают, например, CD137. Примеры агонистического антитела к CD137 включают урелумаб (CAS №934823-49-1), PF-05082566 и различные известные агонистические антитела к CD137.
Факторы, принадлежащие к костимуляторным молекулам, включают TMIGD2, HHLA2, ICOS, лиганд ICOS, CD28, CD80, CD86 и т.п. Примеры агонистического антитела к ОХ40 включают MOXR0916, MEDI6469, MEDI0562, MEDI6383, PF-04518600, GSK-3174998 и различные известные агонистические антитела к ОХ40. Примеры агонистического антитела к CD40 включают RG-7876, ADC-1013, SEA-CD40, АРХ005М, дацетузумаб и различные агонистические антитела к CD40. Примеры агонистического антитела к GITR включают AMG228, АМК-1248, МК-4166, BMS-986156, TRX518 и различные агонистические антитела к GITR. Примеры агонистического антитела к CD27 включают варлилумаб (CAS №1393344-72-3) и различные известные агонистические антитела к CD27.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения предпочтительные примеры ингибитора иммунных контрольных точек включают (но, не ограничиваясь только ими) антитела к PD1, антитела к PDL1, антитела к CTLA-4, антитела к TIM3 и антитела к LAG3. Примеры антитела к PD-1 включают пембролизумаб (CAS №. 1374853-91-4), ниволумаб (CAS №. 946414-94-4), MEDI0680, PDR001, BGB-A317, REGN2810, SHR-1210, PF-06801591 и различные известные антитела к PD1. Примеры антитела к PD-L1 включают атезолизумаб (CAS №1380723-44-3), авелумаб (CAS №1537032-82-8), дурвалумаб (CAS №1428935-60-7), MDX-1105 и различные известные антитела к PD-L1. Примеры антитела к CTLA-4 включают ипилимумаб (CAS №477202-00-9), тремелимумаб (CAS №745013-59-6) и различные известные антитела к CTLA-4. Примеры антитела к TIM3 включают MBG452 и различные известные антитела к TIM3. Примеры антитела к LAG3 включают BMS-986016, LAG525 и различные известные антитела к LAG3.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения предпочтительные примеры ингибитора ангиогенеза включают (но, не ограничиваясь только ими) антитела к VEGFR2. Примеры ингибитора ангиогенеза включают бевацизумаб, сорафениб, эверолимус, темсиролимус и различные известные ингибиторы ангиогенеза.
В некоторых вариантах осуществления изобретения другие противораковые агенты, предлагаемые в настоящем изобретении, не ограничены конкретно и можно применять любой противораковый агент, если при использовании в комбинации с биспецифическим антителом, предлагаемым в настоящем изобретении, повышается терапевтическое действие или профилактическое действие другого противоракового агента или повышается терапевтическое действие или профилактическое действие биспецифического антитела.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения комбинированная терапия, предлагаемая в настоящем изобретении, может включать применение описанного выше биспецифического антитела и по меньшей мере одного другого терапевтического агента, иммуномодулятора, терапевтической противораковой вакцины, адаптивной Т-клеточной терапии, истощения Treg или т.п., но терапия не ограничена указанным. Предпочтительные терапевтические противораковые вакцины включают (но, не ограничиваясь только ими) вакцины на основе цельных опухолевых клеток, вакцины на основе опухолевого антигена, вакцины на основе вектора, вакцины на основе онколитических вирусов и вакцины на основе дендритных клеток. Можно применять мультимодальную терапию с использованием хирургической операции, облучения или т.п. в комбинации, в дополнение к вышеописанной терапии.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения комбинированную терапию, предлагаемую в настоящем изобретении, можно осуществлять с использованием описанного выше биспецифического антитела в комбинации с цитокиновой терапией с использованием цитокина, такого как агент, усиливающий противоопухолевый иммунный ответ. В указанной терапии цитокины включают (но, не ограничиваясь только ими) IL-2, IL-7, IL-12, IL-15, IL-17, IL-18, IL-21, IL-23, IL-27, GM-CSF, интерферон-α (IFNα), IFNα-2b, IFNβ и IFNγ.
Не ограничивающим объем изобретения вариантом осуществления настоящего изобретения являются агенты, предназначенные для индукции цитотоксичности, агенты, предназначенные для подавления клеточной пролиферации, агенты, предназначенные для ингибирования клеточной пролиферации, агенты, предназначенные для активации иммунного ответ, агенты, предназначенные для лечения рака, и агенты, предназначенные для предупреждения рака, каждый из которых содержит описанную выше фармацевтическую композицию.
В некоторых вариантах осуществления изобретения понятие «индивидуум», которому вводят указанное выше биспецифическое антитело и/или другой противораковый агент, относится к человеку или животному кроме человека, например, млекопитающему, такому как корова, лошадь, собака, овца или кошка. Индивидуум предпочтительно представляет собой человека. Индивидуум включает пациентов (включая человека и млекопитающих кроме человека). В некоторых вариантах осуществления изобретения индивидуум представляет собой пациента, имеющего раковые клетки или содержащие раковые клетки опухолевые ткани. Раковые клетки или содержащие раковые клетки опухолевые ткани, которые становятся мишенями противоракового агента или комбинированной терапии, предлагаемой в настоящем изобретении, не ограничены конкретно, если они экспрессируют глипикан 3. В настоящем изобретении предпочтительные экспрессирующие глипикан 3 клетки, т.е. глипикан 3-позитивные клетки, представляют собой раковые клетки. Более предпочтительные типы рака включают (но, не ограничиваясь только ими), например, рак желудка, рак головы и шеи (H&N), рак пищевода, рак легкого, рак печени, рак яичника, рак молочной железы, рак ободочной кишки, рак почки, рак кожи, мышечную опухоль, рак поджелудочной железы, рак предстательной железы, рак яичек, рак матки, холангиосаркому, карциному из клеток Меркеля, рак мочевого пузыря, рак щитовидной железы, шванному, адренальный рак (рак надпочечных желез), рак ануса, опухоль центральной нервной системы, опухоль нейроэндокринной ткани, рак пениса, опухоль плевры, опухоль слюнных желез, рак вульвы, тимому и педиатрический рак (опухоль Вильмса, нейробластома, саркома, гепатобластома и опухоль из зародышевых клеток). Еще более предпочтительные типы рака включают (но, не ограничиваясь только ими) рак желудка, рак головы и шеи (H&N), рак пищевода, рак легкого, рак печени, рак яичника, рак молочной железы, рак ободочной кишки, рак почки, рак кожи, мышечную опухоль, рак поджелудочной железы, рак предстательной железы, рак яичек и рак матки (Tumori 98, 2012, сс. 478-484; Tumor Biol. 36, 2015, сс. 4671-4679; Am J Clin Pathol 130, 2008, сс. 224-230; Adv Anat Pathol 21, 2014, cc. 450-460; Med Oncol 29, 2012, cc. 663-669; Clinical Cancer Research 10, 2004, cc. 6612-6621; Appl Immunohistochem Mol Morphol 17, 2009, cc. 40-46; Eur J Pediatr Surg 25, 2015, cc. 138-144; J Clin Pathol 64, 2011, cc. 587-591; Am J Surg Pathol 30, 2006, cc. 1570-1575; Oncology 73, 2007, cc. 389-394; Diagnostic Pathology 64, 2010, cc. 1-6; Diagnostic Pathology 34, 2015, cc. 1-6; Am J Clin Pathol 129, 2008, cc. 899-906; Virchows Arch 466, 2015, cc. 67-76).
В некоторых вариантах осуществления изобретения пациенты представляют собой пациентов, которые получали лечение с использованием указанного выше биспецифического антитела и/или некоторого типа противоракового(ых) агента(ов) до комбинированной терапии, в которой применяют биспецифическое антитело и другой противораковый агент. В некоторых вариантах осуществления изобретения пациенты представляют собой пациентов, которые не могли получать стандартную терапию или для которых стандартная терапия была не эффективной. В некоторых вариантах осуществления изобретения рак, который имеет пациент, представляет собой рак на ранней стадии или на последней стадии.
В контексте настоящего описания понятие «рак» относится не только к эпителиальному злокачественному заболеванию, такому как рак яичника или рак желудка, но также и к неэпителиальному злокачественному заболеванию, включая гематопоэтические опухоли, такие как хронический лимфоцитарный лейкоз или лимфома Ходжкина. В контексте настоящего описания понятия «рак», «карцинома», «опухоль» «неоплазма» и т.п. не отличаются друг от друга и являются взаимозаменяемыми.
Однако в некоторых вариантах осуществления изобретения типы рака, которые становятся мишенями противораковых агентов или фармацевтических композиций (комбинированная терапия), предлагаемых в настоящем изобретении, предпочтительно представляют собой такие типы, при которых количество антигенов глипикана-3 на клеточной поверхности составляет на клетку 100 или более, более предпочтительно представляют собой такие типы, при которых количество антигенов глипикана-3 на клеточной поверхности составляет на клетку 200 или более, 300 или более, 400 или более, 500 или более, 600 или более, 700 или более, 800 или более, 900 или более, 1000 или более, 1200 или более, 1400 или более, 1600 или более, 1800 или более, или 2000 или более, и еще более предпочтительно представляют собой такие типы, при которых количество антигенов глипикана-3 на клеточной поверхности составляет на клетку 3000 или более, 4000 или более, 5000 или более, 6000 или более, 7000 или более, 8000 или более, 9000 или более, 10000 или более, 20000 или более, 30000 или более, 40000 или более или 50000 или более.
Количество антигенов глипикана-3 на клеточной поверхности на клетку можно определять соответственно с использованием методов, указанных в настоящем описании, или известных специалистам в данной области, например, рассчитывая связывающую способность антитела (ABC) с GPC3 на клеточной поверхности с помощью проточной цитометрии с использованием QIFIKIT (фирма DAKO). Количество антигенов глипикана-3 на клеточной поверхности на клетку в образце ткани, выделенной из кандидата-мишени, можно определять для решения вопроса о том, может ли кандидат являться мишенью, в которую следует вводить противораковый агент или фармацевтическую композицию (комбинированная терапия), предлагаемый/предлагаемую в настоящем изобретении. Когда количество антигенов глипикана-3 на клеточной поверхности на клетку удовлетворяет описанным выше критериям, то мишень, из которой получен образец, может являться мишенью, в которую следует вводить противораковый агент или фармацевтическую композицию (комбинированная терапия), предлагаемый/предлагаемую в настоящем изобретении.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения противораковые агенты, предлагаемые в настоящем изобретении, можно применять для лечения пациентов, имеющих рак, устойчивый к лечению с помощью ингибитора иммунных контрольных точек. Например, пациентов с глипикан 3-позитивным раком, введение которым ингибитора иммунных контрольных точек не позволяло достигать требуемого действия лекарственного средства, можно лечить с использованием противоракового агента, предлагаемого в настоящем изобретении. Другими словами, глипикан 3-позитивный рак, который уже лечили с помощью терапии на основе ингибитора иммунных контрольных точек, можно лечить с использованием противоракового агента, предлагаемого в настоящем изобретении.
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения фармацевтические композиции (комбинированная терапия), предлагаемые в настоящем изобретении, можно применять для лечения пациентов, имеющих рак, устойчивый к лечению с помощью ингибитора иммунных контрольных точек. Например, пациентов с GPC-позитивным раком, введение которым ингибитора иммунных контрольных точек не позволяло достигать требуемого действия лекарственного средства, можно лечить с использованием фармацевтической композиции (комбинированная терапия), предлагаемой в настоящем изобретении. Другими словами, глипикан 3-позитивный рак, который уже лечили с помощью терапии на основе ингибитора иммунных контрольных точек, можно лечить с использованием фармацевтической композиции (комбинированная терапия), предлагаемой в настоящем изобретении. Предпочтительные примеры другого противоракового агента, содержащегося в фармацевтической композиции, включают ингибиторы иммунных контрольных точек (но не ограничены только ими).
В не ограничивающем объем изобретения варианте осуществления настоящего изобретения фармацевтические композиции (комбинированная терапия), предлагаемые в настоящем изобретении, можно применять для лечения пациентов, имеющих рак, устойчивый к лечению с помощью противоракового агент, предлагаемого в настоящем изобретении. Например, пациентов с GPC-позитивным раком, у которых рак стал устойчивым к противораковому агенту, предлагаемому в настоящем изобретении, после введения противоракового агента или введение которым противоракового агента, предлагаемого в настоящем изобретении, не позволяло достигать требуемого действия лекарственного средства, можно лечить с использованием фармацевтической композиции (комбинированная терапия), предлагаемой в настоящем изобретении. Другими словами, глипикан 3-позитивный рак, который уже лечили с помощью терапии с использованием противоракового агента, предлагаемого в настоящем изобретении, можно лечить с помощью фармацевтической композиции (комбинированная терапия), предлагаемой в настоящем изобретении. Предпочтительные примеры другого противоракового агента, содержащегося в фармацевтической композиции, включают ингибиторы иммунных контрольных точек (но не ограничены только ими).
Касательно глипикан 3-позитивного рака (рак, у которого подтверждена экспрессия глипикана 3), специалисты в данной области могут соответственно оценивать позитивность в отношении глипикана 3 с использованием методов, известных в данной области, таких как иммуногистохимическое окрашивание или проточная цитометрия.
Другим объектом настоящего изобретения являются противораковые агенты, содержащие в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу, которая содержит: (1) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, (2) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, и (3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора.
В настоящем изобретении фраза «содержит в качестве активного ингредиента мультиспецифическую антигенсвязывающую молекулу, которая содержит: (1) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, (2) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, и (3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора» означает, что композиция содержит антигенсвязывающую молекулу в качестве основного действующего вещества; однако не имеется конкретных ограничений касательно относительного содержания антигенсвязывающей молекулы.
При необходимости мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, можно капсулировать в микрокапсулы (микрокапсулы, изготовленные из гидроксиметилцеллюлозы, желатина, поли(метилметакрилата) и т.п.), и можно включать в компоненты коллоидных систем, предназначенных для введения лекарственных веществ (липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) (например, см. ((Remington's Pharmaceutical Science 16-ое изд.», под ред. Oslo, 1980)). Кроме того, хорошо известны методы приготовления агентов в виде средств с замедленным высвобождением, и их можно применять для мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении (J. Biomed. Mater. Res. 15, 1981, cc. 267-277; Chemtech. 12, 1982, cc. 98-105; US №3773719; опубликованные европейские патенты (ЕР) ЕР 58481 и ЕР 133988; Biopolymers 22, 1983, cc. 547-556).
Фармацевтические композиции или противораковые агенты, предлагаемые в настоящем изобретении, можно вводить пациенту орально или парентерально, и предпочтительным является парентеральное введение. Указанные примеры методов введения включают инъекцию, введение в нос, транспульмонарное введение и чрескожное введение. Примеры введения путем инъекции включают, например, внутривенную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию и подкожную инъекцию. Фармацевтическую композицию или противораковый агент, предлагаемую/предлагаемый в настоящем изобретении, можно применять местно или системно путем инъекции. Метод введения можно выбирать в зависимости от возраста пациента и симптомов. Дозу можно выбирать, например, из следующего диапазона: от 0,0001 до 1000 мг на кг веса тела на каждое введение. Альтернативно этому, дозу можно выбирать, например, из следующего диапазона: от 0,001 до 100000 мг/пациента. Дозу можно определять, например, как количество мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, которая содержится в качестве активного ингредиента в фармацевтической композиции. Однако дозы фармацевтических композиций или противораковых агентов, предлагаемых в настоящем изобретении, не ограничены указанными дозами.
Фармацевтические композиции или противораковые агенты, предлагаемые в настоящем изобретении, можно приготавливать с помощью общепринятых методов (например, см. Remington's Pharmaceutical Science, последнее изд., изд-во Mark Publishing Company, Easton, U.S.A.), и они могут содержать также фармацевтически приемлемые носители и добавки. Их примерами являются (но, не ограничиваясь только ими) поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корригенты и можно применять другие общепринятые носители. Конкретными примерами носителей являются легкая безводная кремниевая кислота, лактоза, кристаллическая целлюлоза, маннит, крахмал, кармеллоза кальция, кармеллоза натрия, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилацетальдиэтиламиноацетат, поливинилпирролидон, желатин, триглицерид со средней длиной цепи, полиоксиэтиленированное гидрогенизированное касторовое масло 60, сахароза, карбоксиметилцеллюлоза, кукурузный крахмал, неорганическая соль и т.п.
Не ограничивающим объем изобретения вариантом осуществления настоящего изобретения являются также способы повреждения экспрессирующих в качестве антигена глипикан 3 клеток или опухолевых тканей, содержащих экспрессирующие антиген клетки, или способы подавления роста указанных клеток или опухолевых тканей путем приведения в контакт клеток, экспрессирующих в качестве антигена глипикан 3, с мультиспецифической антигенсвязывающей молекулой, предлагаемой в настоящем изобретении, которая связывается с антигеном, и другим противораковым агентом. Мультиспецифическая антигенсвязывающая молекула, которая связывается с антигеном, описана выше в качестве антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, которая связывается с антигеном, она содержится в противораковых агентах, предлагаемых в настоящем изобретении. Клетки, с которыми связывается мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, которая связывается с антигеном, не ограничены конкретными клетками, если эти клетки экспрессируют антиген.
Согласно настоящему изобретению «приведение в контакт» можно осуществлять, например, добавляя мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, которая связывается с антигеном, и другой противораковый агент в культуральную среду экспрессирующих антиген GPC3 клеток, которые культивируют in vitro. В этом случае добавляемую антигенсвязывающую молекулу и/или добавляемый другой противораковый агент можно применять в пригодной для этой цели форме, такой как раствор или твердое вещество, полученное путем лиофилизации, или т.п. При добавлении в виде водного раствора он может представлять собой водный раствор, который содержит только мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или может представлять собой также раствор, содержащий, например, указанные выше поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корригенты. На концентрацию добавляемой молекулы не накладывается специальных ограничений; однако конечная концентрация в культуральной среде предпочтительно составляет от 1 пг/мл до 1 г/мл, более предпочтительно от 1 нг/мл до 1 мг/мл и еще более предпочтительно от 1 мкг/мл до 1 мг/мл.
Кроме того, согласно другому варианту осуществления настоящего изобретения «приведение в контакт» осуществляют также путем введения антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, и другого противоракового агента животным кроме человека, в организм которых трансплантированы экспрессирующие антиген GPC3 клетки, и животным, у которых эндогенно происходит экспрессия антигена. Метод введения может быть оральным или парентеральным, и предпочтительным является парентеральное введение. Указанные примеры методов введения включают инъекцию, введение в нос, транспульмонарное введение и чрескожное введение. Примеры введения путем инъекции включают, например, внутривенную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию и подкожную инъекцию. Фармацевтическую композицию или противораковый агент, предлагаемую/предлагаемый в настоящем изобретении, можно применять местно или системно, например, путем инъекции. Метод введения можно выбирать в зависимости от возраста подопытного животного и симптомов. При введении в виде водного раствора можно применять водный раствор, содержащий только мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или можно применять раствор, содержащий также указанные выше поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корригенты и т.п. Дозу можно выбирать из следующего диапазона: от 0,0001 до 1000 мг на кг веса тела на одно введение. Альтернативно этому, дозу можно выбирать, например, из следующего диапазона: от 0,001 до 100000 мг/пациента. Дозу можно определять, например, как количество мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, которая содержится в качестве активного ингредиента в фармацевтической композиции. Однако вводимое количество мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, не ограничено указанными дозами.
Описанный ниже метод предпочтительно используют в качестве метода оценки или измерения повреждения клетки, индуцированного в клетках, экспрессирующих в качестве антигена глипикан 3, который связывается доменом, который несет вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, который входит в антигенсвязывающую молекулу, что является результатом контактирования клеток с мультиспецифической антигенсвязывающей молекулой или другим противораковым агентом, предлагаемой/предлагаемым в настоящем изобретении. Примеры метода оценки или измерения цитотоксической активности in vitro включает методы измерения активности цитотоксических Т-клеток или т.п. Обладает ли мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, Т-клеточной цитотоксичностью, можно определять с помощью известных методов (см., например, Current protocols in Immunology, глава 7. Immunologic studies in humans, под ред. John E, Coligan и др., изд-во, John Wiley & Sons, Inc., 1993). При измерении активности антигенсвязывающую молекулу, которая связывается с антигеном, отличным от глипикана 3, представляющим собой антиген, который не экспрессируется в клетках, применяемых для оценки, можно использовать в качестве контроля, который анализируют таким же образом, что и мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, и активность можно определять, оценивая, обладает ли мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, более выраженной цитотоксической активностью, чем применяемая в качестве контроля антигенсвязывающая молекула.
Для оценки или измерения цитотоксической активности in vivo, например, клетки, экспрессирующие в качестве антигена глипикан 3, внутрикожно или подкожно трансплантируют подопытному животному кроме человека, а затем тестируемую антигенсвязывающую молекулу и/или другой противораковый агент вводят внутривенно или внутрибрюшинно каждый день или с интервалами в несколько дней, начиная со дня трансплантации или на следующий после него день. Цитотоксическую активность можно определять путем ежедневного измерения размера опухолей, определяя различие в изменении размера опухолей. Аналогично методу, применяемому для оценки in vitro, можно считать, что антигенсвязывающая молекула, предлагаемая в настоящем изобретении, обладает цитотоксической активностью, если при введении контрольной антигенсвязывающей молекулы обнаружено, что размер опухолей в группе, которой вводили антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, существенно меньшей, чем размер опухолей в группе, которой вводили контрольную антигенсвязывающую молекулу.
В качестве метода оценки или измерения подавляющего действия на пролиферацию клеток, экспрессирующих в качестве антигена глипикан 3, можно применять метод измерения поглощения меченного изотопом тимидина клетками или МТТ-метод. В качестве метода оценки или измерения подавляющего действия на пролиферацию клеток in vivo, можно применять метод, аналогичный описанному выше для оценки или измерения цитотоксической активности in vivo.
Наборы
В некоторых вариантах осуществления настоящего изобретения предложен набор, содержащий:
(1) указанное выше биспецифическое антитело;
(2) контейнер; и
(3) инструкцию или этикетку с указанием, что биспецифическое антитело и по меньшей мере один тип противоракового агента вводят в комбинации тестируемому субъекту для лечения рака у индивидуума. Другим вариантом осуществления настоящего изобретения является набор, содержащий:
(1) другой противораковый агент;
(2) контейнер; и
(3) инструкцию или этикетку с указанием, что указанный другой противораковый агент и по меньшей мере один тип указанного выше биспецифического антитела вводят в комбинации индивидууму для лечения рака у индивидуума.
Другим вариантом осуществления настоящего изобретения является набор, содержащий:
(1) указанное выше биспецифическое антитело;
(2) другой противораковый агент;
(3) контейнер; и
(4) инструкцию или этикетку с указанием, что биспецифическое антитело и другой противораковый агент вводят в комбинации индивидууму для лечения рака у индивидуума.
В некоторых вариантах осуществления изобретения набор дополнительно содержит фармацевтически приемлемый носитель. Набор может дополнительно содержать стерильный разбавитель, который предпочтительно хранится в отдельном дополнительном контейнере. Набор может содержать также инструкцию по применению комбинированной терапии для лечения или предупреждения рака.
В некоторых вариантах осуществления изобретения понятие «инструкция» относится к письменной инструкции, как правило, содержащейся в поступающей в продажу коробке с фармацевтическим средством, и может содержать информацию, касающуюся показаний, применения, дозы, введения, противопоказаний и/или мер предосторожности при применении фармацевтического средства.
Наборы могут представлять собой наборы, которые используют исключительно с целью совместного применения биспецифического антитела, предлагаемого в настоящем изобретении, и другого противоракового агента. Альтернативно этому, наборы могут представлять собой наборы, которые используют для других целей наряду с совместным применением биспецифического антитела, предлагаемого в настоящем изобретении, и другого противоракового агента. Например, наряду с тем, что в инструкции и этикетке к набору, предлагаемому в настоящем изобретении, указано, что биспецифическое антитело и другой противораковый агент вводят в комбинации индивидууму, в других вариантах осуществления изобретения в инструкции или этикете может быть указано, например, что биспецифическое антитело или другой противораковый агент применяют в качестве индивидуального агента.
Настоящее изобретение относится также к молекулам, обладающим GPC3-связывающей активностью, которые содержат домен, содержащий вариабельную область антитела, которая обладает GPC3-связывающей активностью, мультиспецифической антигенсвязывающей молекулы, содержащейся в противораковом агенте или фармацевтической композиции, предлагаемой в настоящем изобретении. Кроме того, настоящее изобретение относится к молекуле, которая обладает GPC3-связывающей активностью, которая содержит вариабельные области Н- и L-цепей антитела соответственно, содержащие три CDR Н- и L-цепей (всего шесть CDR), которые входят в молекулу. Настоящее изобретение относится также к молекулам, обладающим связывающей активностью в отношении комплекса Т-клеточного рецептора, которые содержат домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, мультиспецифической антигенсвязывающей молекулы, содержащейся в противораковом агенте или фармацевтической композиции, предлагаемой в настоящем изобретении. Кроме того, настоящее изобретение относится к молекуле, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, которая содержит вариабельные области Н- и L-цепей антитела соответственно, содержащие три CDR Н- и L-цепей (всего шесть CDR), которые входят в молекулу. Указанные молекулы могут представлять собой антитела или полипептиды, содержащие антигенсвязывающие фрагменты антитела. Настоящее изобретение относится также к антителам, которые связываются с эпитопами, перекрывающимися или конкурирующими с указанными молекулами или полипептидами, которые содержат их антигенсвязывающие фрагменты. Приемлемыми примерами таких полипептидов, которые содержат антигенсвязывающие фрагменты антитела, являются scFv, одноцепочечное антитело, Fv, одноцепочечный Fv2 (scFv2), Fab и F(ab')2. Кроме того, указанные молекулы необязательно должны быть мультиспецифическими (биспецифическими), а могут связываться только либо с GPC3, либо с комплексом Т-клеточного рецептора (например, CD3ε-цепью).
Указанные молекулы включают молекулу, которая содержит домен, содержащий вариабельную область антитела, которая обладает GPC3-связывающей активностью, мультиспецифической антигенсвязывающей молекулы, подробное описание которой представлено в разделе «Приведенные для справки примеры» в настоящем описании (которая содержит вариабельные области Н-цепи, обладающие ОРС3-связывающей активностью и вариабельную область общей L-цепи), молекулу, которая содержит домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, мультиспецифической антигенсвязывающей молекулы, подробное описание которой представлено в разделе «Приведенные для справки примеры» в настоящем описании (которая содержит вариабельные области Н-цепи, обладающие связывающей активностью в отношении комплекса Т-клеточного рецептора и вариабельную область общей L-цепи), а также молекулу, обладающую способностью связываться с таким же антигенным белком (GPC3 или комплекс Т-клеточного рецептора), которая содержит три CDR каждой из Н- и L-цепей (всего шесть CDR), которые входят в указанную выше молекулу.
Указанные молекулы имеют CDR, которые являются одинаковыми (общими) с CDR мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении; и поэтому ожидается, что они будут связываться с эпитопом, перекрывающимся с эпитопом мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении. Таким образом, указанные молекулы могут конкурировать с мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении, при их совместном присутствии с мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении. Таким образом, эти молекулы можно применять, например, в качестве регуляторных агентов для подавления различных видов активности (таких как антигенсвязывающая активность, цитотоксическая активность и противоопухолевая активность) мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении. Кроме того, указанная молекула может быть предварительно связана с белком-мишенью (GPC3 или комплекс Т-клеточного рецептора), и после добавления мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, можно выявлять молекулы, диссоциирующие в результате конкуренции. При таком применении молекула пригодна в качестве агента, предназначенного для оценки связывания мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, с белком-мишенью. Согласно настоящему изобретению молекулы можно метить соответствующими флуоресцентными субстанциями или т.п. Альтернативному этому, указанные молекулы можно применять для скрининга новых антител, которые связываются с эпитопами, перекрывающимися с эпитопами, которые связываются мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении. Как указано выше, указанную молекулу можно предварительно связывать с белком-мишенью (GPC3 или комплекс Т-клеточного рецептора), а затем добавлять тестируемое антитело, при этом, если имеет место диссоциация связанных молекул, то тестируемое антитело является перспективным (кандидатом) в качестве антитела против эпитопа, перекрывающегося с эпитопом, с которым связывается мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении. Это позволяет осуществлять эффективный скрининг новых мультиспецифических антигенсвязывающих молекул.
Приведенные в настоящем описании в качестве примеров комбинации в виде комбинаций каждого CDR мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении, можно применять непосредственно в качестве конкретных комбинаций CDR вариабельных областей Н-цепи и L-цепи этих молекул. Аффинность к антигену этих молекул (величины KD) предпочтительно характеризуется величинами, приведенными в качестве примера KD мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, но не ограничена этими величинами.
В настоящем изобретении упоминание понятия в единственном числе подразумевает его упоминание его в количестве, равном одному, двум или более (т.е. равном по меньшей мере одному). Например, «компонент» относится к одному компоненту или двум или большему количеству компонентов.
Специалистам в данной области, естественно, должно быть очевидно, что любые комбинации одного или нескольких вариантов осуществления изобретения, указанных в настоящем описании, также включены в настоящее изобретение, если только это не является технически неприемлемым с позиций существующего уровня техники, известного специалистам в данной области.
Все процитированные в настоящем описании документы, характеризующие известный уровень техники, включены в настоящее описание в качестве ссылки.
Примеры
Ниже настоящее изобретение описано со ссылкой на конкретные примеры, которые не ограничивают объем изобретения.
Пример 1 Зависимая от Т-клеток клеточная цитотоксичность (TDCC-активность) каждого из тестируемых антител при использовании в качестве эффекторных клеток мононуклеарных клеток периферической крови человека
TDCC-активность каждого из тестируемых антител измеряли описанным ниже методом. Мононуклеарные клетки периферической крови человека (ниже в контексте настоящего описания обозначены как человеческие РВМС) применяли в качестве эффекторных клеток и TDCC-активность каждого из тестируемых антител измеряли согласно описанному ниже методу.
(1) Получение раствора человеческих РВМС
50 мл периферической крови получали из организма здорового человека на фирме Chugai Pharmaceytical Co. Ltd. с помощью шприца, в который предварительно вносили 500 мкл раствора гепарина с концентрацией 5000 ед./5 мл. Периферическую кровь, разведенную двукратно с помощью ЗФР, разделяли на 4 аликвоты и добавляли в пробирки Leucosep (фирма GE Healthcare) для отделения лимфоцитов, в которые заранее загружали 15 мл фиколла-пак PLUS и центрифугировали. Разделительные пробирки, содержащие аликвоты периферической крови, центрифугировали при скорости 1000 g в течение 10 мин при комнатной температуре, а затем собирали слой фракции мононуклеарных клеток. Затем клетки, присутствующие в каждом слое фракции, однократно промывали средой RPMI-1640 (фирма SIGMA), содержащей 10% FBS (ниже в контексте настоящего описания обозначена как 10% FBS/RPMI-1640), клетки суспендировали при клеточной плотности 2×106 клеток/мл в культуральной среде, соответствующей каждой линии клеток-мишеней. Клеточные суспензии применяли в качестве эффекторных клеток в последующих экспериментах.
(2) Анализ высвобождения ЛДГ (TDCC-активность)
TDCC-активность оценивали с помощью анализа высвобождения ЛДГ (набор для детекции цитотоксичности ЛДГ (LDH Cytotoxicity Detection Kit), фирма TAKARA). Сначала раствор антитела разводили с помощью культуральной среды для каждой линии клеток-мишеней до указанных концентраций (0,000004, 0,00004, 0,0004, 0,004, 0,04, 0,4, 4 и 40 мкг/мл), которые в 4 раза превышали конечные концентрации, и аликвоты объемом 50 мкл растворов антитела с соответствующими концентрациями добавляли в каждую лунку 96-луночного круглодонного планшета. Затем высевали аликвоты клеток-мишеней объемом 50 мкл, приготовленные с плотностью 2×105 клеток/мл в культуральной среде, соответствующей каждой линии клеток-мишеней (1×104 клеток/лунку), и давали выстояться при комнатной температуре в течение 15 мин. В каждую лунку планшета добавляли аликвоты объемом 100 мкл суспензии человеческих РВМС, приготовленной в культуральной среде, соответствующей каждой линии клеток-мишеней (2×105 клеток/лунку), согласно методу, описанному в подпункте (1). Планшету давали выстояться в газовом инкубаторе с 5% диоксида углерода при 37°С в течение примерно 24 ч, после чего центрифугировали. По 100 мкл супернатанта культуры в каждой лунке планшета переносили в 96-луночный плоскодонный планшет. Раствор катализатора растворяли в 1 мл Н2О и смешивали с раствором красителя в соотношении 1:45. Раствор, представляющий собой смесь растворов катализатора и красителя, добавляли в виде аликвот по 100 мкл/лунку в 96-луночный плоскодонный планшет, в который были перенесены супернатанты культур. Планшету давали выстояться при комнатной температуре в течение 15-30 мин. Измеряли абсорбцию при 490-492 нм с помощью планшет-ридера. В качестве длины референс-волны использовали длину от 600 до 620 нм и вычитали абсорбцию из абсорбции, полученной при 490-492 нм. Величины, полученные путем вычитания среднего значения для лунок, содержащих только культуральную среду (пустой контроль), подставляли в приведенное ниже уравнение.
Уравнение:
Цитотоксичность (TDCC) (%) = ((А-Б)-В)) × 100/(Г-В)
Цитотоксическую активность определяли на основе этого уравнения.
В нем А обозначает абсорбцию смеси клеток-мишеней, эффекторных клеток и антитела; Б обозначает абсорбцию эффекторных клеток; В обозначает абсорбцию клеток-мишеней; и Г обозначает абсорбцию клеток-мишеней, к которым добавлен Тритон Х-100.
В результате была выявлена выраженная TDCC биспецифического антитела к человеческой CD3ε-цепи и человеческому GPC3 (антитело из образца №38, описанное в таблице 17 приведенного для справки примера 3) (фиг. 1).
Пример 2. Определение количества GPC3, экспрессируемого на клеточной поверхности каждой линии клеток
Связывающую способность антитела (ABC) в отношении GPC3 на клеточной поверхности рассчитывали для каждой линии клеток с помощью проточной цитометрии с использованием QIFIKIT (фирма DAKO).
После промывки буфером CellWASH (фирма BD Bioscience), дополненным 5% БСА (ниже в контексте настоящего описания обозначен как FACS/ЗФР), приготавливали 5×105 клеток из каждой линии клеток в 50 мкл раствора, содержащего мышиное антитело к человеческому GPC или контрольное антитело в конечной концентрации 20 мкг/мл, и давали выстояться на льду в течение 30 мин. Клетки промывали FACS/ЗФР. Затем к клеткам добавляли 50 мкл раствора, содержащего меченное ФИТЦ козье антитело к мышиному IgG, разведенное в 50 раз FACS/ЗФР. Клеткам давали выстояться в течение 30 мин на льду. После промывки с помощью FACS/ЗФР клетки анализировали с помощью проточной цитометрии. ABC рассчитывали с помощью метода, описанного в инструкции, прилагаемой к набору QIFI.
ABC в отношении GPC3 на клеточной поверхности рассчитывали для каждой линии клеток, и результаты представлены в таблице 6.
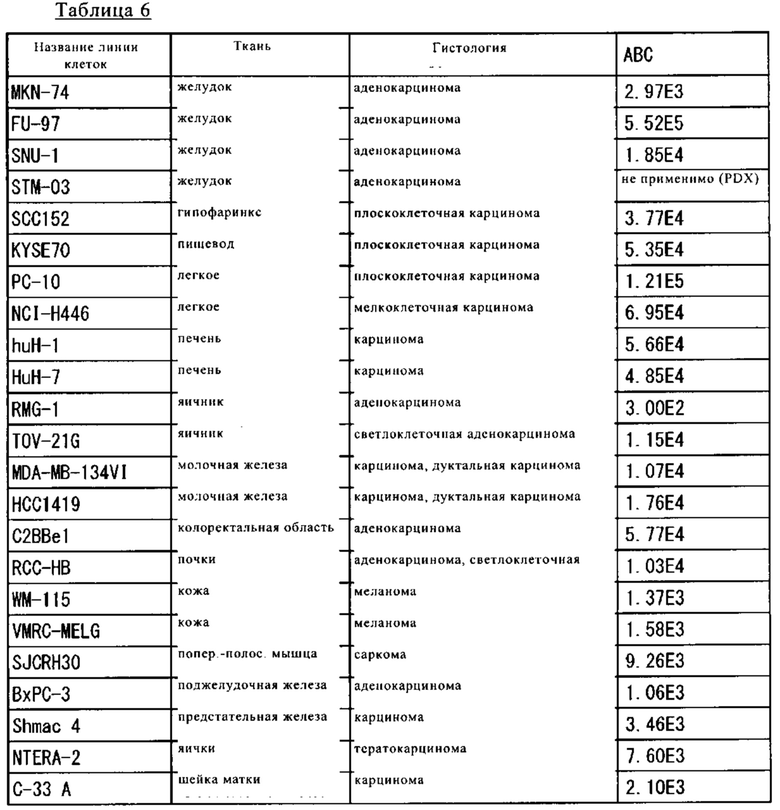
Пример 3 Оценка in vivo эффективности лекарственного средства (биспецифическое антитело к человеческой CD3ε-цепи и человеческому GPC3) (опыты по оценке эффективности лекарственного средства осуществляли с использованием антител из образцов №№30, 31, 32, 33 и 38, или антител из образцов №№39 и 40, описанных в таблице 17 в приведенном для справки примере 3, в качестве индивидуального агента)
Эффективность in vivo лекарственного средства оценивали с использованием в качестве моделей мышей, несущих опухоли из линий клеток, в отношении которых обнаружена цитотоксическая активность в опыте in vitro, описанном в примере 1, а также линий, полученных путем пассажей in vivo.
Для оценки in vivo эффективности лекарственного средства_применяли методы с использованием модели, обозначенной как NOD scid/c инъецированными Т-клетками, гуманизированной мышиной модели NOG; и модифицированной человеческим геном CD3εδγ мышиной модели. Анализ с использованием модели NOD scid/c инъецированными Т-клетками осуществляли следующим образом. NOD scid-мышам трансплантировали некоторые из линий клеток, в отношении которых обнаружена цитотоксическая активность в опыте in vitro, а также линий клеток, полученных путем пассажей in vivo. Т-клетки, размноженные путем культивирования человеческих РВМС in vitro, инъецировали NOD scid-мышам, у которых было подтверждено образование опухолей. Мышей обрабатывали путем введения биспецифического антитела-38 и биспецифического антитела-30, -31, -32 или -33. Анализ с использованием гуманизированной мышиной модели осуществляли следующим образом. CD34-позитивные гематопоэтические стволовые клетки, полученные из крови пупочного канатика, трансплантировали NOG-мышам путем инъекции в хвостовую вену. Мышам на постоянной основе вводили человеческие Т-клетки, их обозначали как гуманизированные NOG-мыши. Линию клеток PC-10 трансплантировали гуманизированным NOG-мышам. Гуманизированных NOG-мышей у которых было подтверждено образование РС-10-опухоли, обрабатывали путем введения антитела-38. Анализ с использованием модифицированной человеческим геном CD3εδγ мышиной модели осуществляли следующим образом. Клетки из мышиной клеточной линии с усиленной экспрессией человеческого GPC3 трансплантировали в модифицированную человеческим геном CD3εδγ мышиную модель, которую получали согласно методу, описанному в приведенном для справки примере 10. Мышей модифицированной человеческим геном CD3εδγ линии, у которых было подтверждено образование опухоли, обрабатывали путем введения антитела-38.
Опыты по оценке эффективности в качестве лекарственного средства биспецифического антитела-38 и биспецифических антител-30, -31, -32 и -33 с использованием модели_NOD scid/c инъецированными Т-клетками осуществляли следующим образом. Размножение Т-клеток в культуре осуществляли с использованием РВМС, выделенных их крови, полученной из организма здорового донора, и набора для активации/экспансии человеческих Т-клеток (Т cell activation/expansion kit/human). Каждую из человеческих линий раковых клеток (MKN74, FU-97, SNU-1, SCC152, KYSE70, РС-10, HuH-7, TOV-21G, RMG-1 и SK-pca31a (SK-HEP-1/hGPC3)) смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно мышам NOD scid (фирма CLEA Japan). Полученную путем пассажей in vivo линию (STM-03) трансплантировали в виде примерно 2-миллиметровых кусочков опухолевой ткани подкожно мышам NOD (фирма CLEA Japan). День трансплантации обозначали как день 0. За 1 день до трансплантации мышам внутрибрюшинно вводили антитело к асиало-ганглиозиду M1 (асиало-GM1) (фирма Wako Pure Chemical Industries) из расчета 0,2 мг/мышь. После точного подтверждения образования опухолей после трансплантация мышей разделяли на группы в зависимости от размера опухолей и веса тела. Затем вновь внутрибрюшинно вводили антитело к асиало-GM1 из расчета 0,2 мг/мышь. На следующий день внутрибрюшинно трансплантировали Т-клетки, полученные вышеописанным методом размножения в культуре из расчета от 1,5×107 до 3×107 клеток/мышь. Примерно через 2-5 ч после трансплантации Т-клеток вводили антитело-38 в дозе 1 мг/кг (MKN74, FU-97, SNU-1, SCC152, KYSE70, РС-10, HuH-7, TOV-21G, RMG-1 и STM-03) через хвостовую вену. Обработку осуществляли только один раз. Биспецифические антитела-30, -31, -32 и -33 вводили в дозе 5 мг/кг (SK-рса31а) через хвостовую вену. Обработку осуществляли только один раз.
Биспецифические антитела-39 и -40 вводили в дозе 1 мг/кг (РС-10) через хвостовую вену. Обработку осуществляли только один раз. Антитела-39 и -40, применяемые в эксперименте, имеют различные последовательности константных областей, но имеют одинаковые аминокислотные последовательности CD3-связывающей вариабельной области, GPC3-связывающей вариабельной области и вариабельной области общей L-цепи (CD3-связывающая вариабельная область: SEQ ID NO: 433, GPC-связывающая вариабельная область: SEQ ID NO: 434, вариабельная область общей L-цепи: SEQ ID NO: 435). Антитела получали с помощью метода, известного специалистам в данной области.
В результате установлено, что биспецифическое антитело-38 обладало выраженным противоопухолевым действием по сравнению с обработанной наполнителем группой (фиг. 2).
В результате установлено, что биспецифические антитела-39 и -40 обладали выраженным противоопухолевым действием по сравнению с обработанной наполнителем группой (фиг. 3).
В результате установлено, что биспецифические антитела-30, -31, -32 и -33- обладали выраженным противоопухолевым действием по сравнению с обработанной наполнителем группой (фиг. 4).
Опыт по оценке эффективности в качестве лекарственного средства антитела-38 на гуманизированной мышиной модели NOG осуществляли следующим образом. NOG-мышей (фирма In-Vivo Science Inc.,  ) облучали рентгеновскими лучами в дозе 2,5 Гр. На следующий день 1×105 CD34-позитивных гематопоэтических стволовых клеток, которые получали из крови пупочного канатика, трансплантировали NOG-мышам путем инъекции в хвостовую вену. Через 16 недель человеческие раковые клетки РС-10 смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно гуманизированным NOG-мышам. День трансплантации обозначали как день 0. После точного подтверждения образования опухолей мышей разделяли на группы в зависимости от размера опухолей и веса тела. Антитело-38 вводили в дозе 0,008, 0,04, 0.2 или 1 мг/кг через хвостовую вену. Антитело-38 вводили только один раз.
) облучали рентгеновскими лучами в дозе 2,5 Гр. На следующий день 1×105 CD34-позитивных гематопоэтических стволовых клеток, которые получали из крови пупочного канатика, трансплантировали NOG-мышам путем инъекции в хвостовую вену. Через 16 недель человеческие раковые клетки РС-10 смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно гуманизированным NOG-мышам. День трансплантации обозначали как день 0. После точного подтверждения образования опухолей мышей разделяли на группы в зависимости от размера опухолей и веса тела. Антитело-38 вводили в дозе 0,008, 0,04, 0.2 или 1 мг/кг через хвостовую вену. Антитело-38 вводили только один раз.
В результате установлено, что биспецифическое антитело-38 обладало выраженным зависящим от дозы противоопухолевым действием по сравнению с обработанной наполнителем группой (фиг. 5).
Опыт по оценке эффективности в качестве лекарственного средства антитела-38 с использованием модифицированной человеческим геном CD3εδγ мышиной модели осуществляли следующим образом. Раковые клетки LLC1/hGPC3, которые представляют собой мышиную линию раковых клеток, сверхэкспрессирующую человеческий GPC3, трансплантировали подкожно модифицированным человеческим геном CD3εδγ мышам (фирма Chugai Pharmaceytical Co. Ltd,  ). День трансплантации обозначали как день 0. В день 11 мышей разделяли на группы в зависимости от размера опухолей и веса тела. Антитело-38 вводили в дозе 5 мг/кг через хвостовую вену. Антитело-38 вводили дважды (день 11 и день 14). Антитело к человеческому GPC3 (WO 006/006693, обозначение клона: GC33), антитело к мышиному CTLA-4 (фирма BioXCell, каталожный № ВЕ0032), антитело к мышиному PD-1 (фирма BioXCell, каталожный № ВЕ0146) антитело к мышиному PD-L1 (фирма BioXCell, каталожный № ВЕ0101), которые представляли собой фармацевтические агенты, применяемые в качестве контролей, вводили в дозе 25 мг/кг через хвостовую вену. Антитело к человеческому GPC3, антитело к мышиному CTLA-4, антитело к мышиному PD-1 и антитело к мышиному PD-L1 вводили дважды (в день 11 и день 14).
). День трансплантации обозначали как день 0. В день 11 мышей разделяли на группы в зависимости от размера опухолей и веса тела. Антитело-38 вводили в дозе 5 мг/кг через хвостовую вену. Антитело-38 вводили дважды (день 11 и день 14). Антитело к человеческому GPC3 (WO 006/006693, обозначение клона: GC33), антитело к мышиному CTLA-4 (фирма BioXCell, каталожный № ВЕ0032), антитело к мышиному PD-1 (фирма BioXCell, каталожный № ВЕ0146) антитело к мышиному PD-L1 (фирма BioXCell, каталожный № ВЕ0101), которые представляли собой фармацевтические агенты, применяемые в качестве контролей, вводили в дозе 25 мг/кг через хвостовую вену. Антитело к человеческому GPC3, антитело к мышиному CTLA-4, антитело к мышиному PD-1 и антитело к мышиному PD-L1 вводили дважды (в день 11 и день 14).
В результате установлено, что биспецифическое антитело-38 обладало выраженным противоопухолевым действием по сравнению с обработанной растворителей группой или группой, обработанной антителом к человеческому GPC3, антителом к мышиному CTLA-4, антителом к мышиному PD-1 и антителом к мышиному PD-L1 (фиг. 6).
Пример 4 Оценка in vivo эффективности лекарственного средства (опыт по оценке эффективности в качестве лекарственного средства комбинации антитела-38 и других агентов)
Эффективность in vivo в качестве лекарственного средства комбинации антитела-38 и других агентов оценивали с использованием в качестве моделей несущих опухоли мышей. Для оценки in vivo эффективности комбинации в качестве лекарственного средства использовали модель NOD scid/c инъецированными Т-клетками, описанную в примере 3, модифицированную человеческим геном CD3εδγ мышиную модель, описанную в примере 3, или модифицированную человеческим геном CD3ε мышиную модель. Изучение комбинации с использованием модели NOD scid/c инъецированными Т-клетками осуществляли следующим образом. Линии клеток MKN45 или NCI-H446 трансплантировали мышам NOD scid. Т-клетки, размноженные культивированием человеческих РВМС in vitro, вводили путем инъекции мышам NOD scid, у которых подтверждено образование заметных опухолей. Мышей обрабатывали путем введения антитела-38 в комбинации с капецитабином, цисплатином или паклитакселом. Опыт по оценке комбинации с использованием модифицированной человеческим геном CD3εδγ мышиной модели осуществляли следующим образом. Раковые клетки LLC1/hGPC3 или клетки Hepa1-6/hGPC3, которые представляли собой полученные из мышей клеточные линии с усиленной экспрессией GPC3, трансплантировали мышам, модифицированным человеческим геном CD3εδγ. Мышей, модифицированных человеческим геном CD3εδγ, у которых подтверждено образование заметных опухолей, обрабатывали путем введения антитела-38 в комбинации с антителом к мышиному TIM-3 (фирма BioXCell, каталожный № ВЕ0115), антителом к мышиному LAG-3 (фирма BioXCell, каталожный № ВЕ0174), антителом к мышиному CD137 (фирма BioXCell, каталожный № ВЕ0169) или антителом к мышиному VEGFR2 (фирма BioXCell, каталожный № ВР0060). Опыт по оценке комбинации с использованием модифицированной человеческим геном CD3ε мышиной модели осуществляли следующим образом. Раковые клетки Hepa1-6/hGPC3, которые представляли собой полученные из мышей клеточные линии с усиленной экспрессией GPC3, трансплантировали мышам, модифицированным человеческим геном CD3ε. Мышей, модифицированных человеческим геном CD3ε, у которых подтверждено образование заметных опухолей, обрабатывали путем введения антитела-38 в комбинации с антителом к мышиному PD-1 (фирма BioXCell, каталожный № ВЕ0146) или антителом к мышиному PD-L1 (фирма BioXCell, каталожный № ВЕ0101).
Опыт по оценке эффективности к качестве лекарственного средства антитела-38 и других агентов с использованием модели NOD scid/c инъецированными Т-клетками осуществляли следующим образом. Размножение Т-клеток в культуре осуществляли с использованием РВМС, выделенных их крови, полученной из организма здорового донора и набора для активации/экспансии человеческих Т-клеток (Т cell activation/expansion kit/human). Каждую из человеческих линий раковых клеток (MKN45 и NCI-Н446) смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно мышам NOD scid (фирма CLEA Japan). День трансплантации обозначали как день 0. За 1 день до трансплантации мышам внутрибрюшинно вводили антитело асиало-GM1 (фирма Wako Pure Chemical Industries) из расчета 0,2 мг/мышь. После подтверждения образования заметных опухолей после трансплантация мышей разделяли на группы в зависимости от размера опухолей и веса тела. Затем вновь внутрибрюшинно вводили антитело к асиало-GM1 из расчета 0,2 мг/мышь. На следующий день внутрибрюшинно трансплантировали Т-клетки, полученные вышеописанным методом размножения в культуре, из расчета 3×107 клеток/мышь. Примерно через 2-5 ч после трансплантации Т-клеток вводили антитело-38. В комбинации с антителом-38 вводили капецитабин, цисплатин или паклитаксел с использованием дозы и режима дозирования, которые указаны в таблице 7.
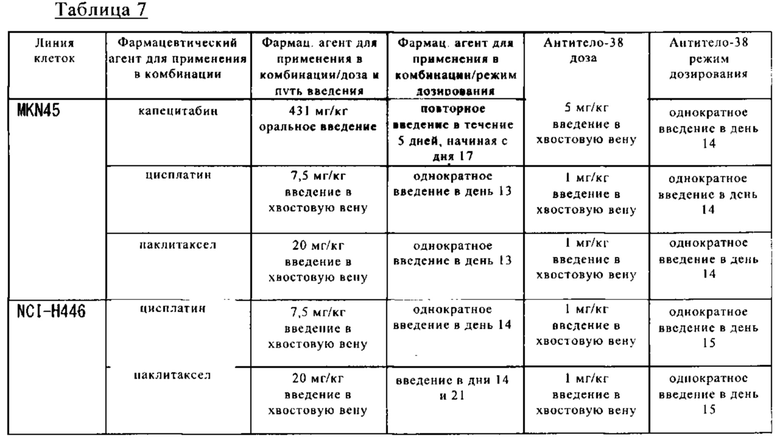
В результате установлено, что противоопухолевое действие повышалось в обработанных комбинацией группах, которым вводили антитело-38 и фармацевтический агент, предназначенный для применения в комбинации, по сравнению с группами, которым антитело-38 или фармацевтический агент, предназначенный для применения в комбинации, вводили в качестве индивидуального средства (фиг. 7 и 8).
РНК экстрагировали из образцов опухолей после введения паклитаксела, цисплатина или капецитабина и антитела-38. Полный анализ РНК с применением nCounter®, анализ инфильтрующих опухоль лимфоцитов (TIL) и анализ патологий осуществляли следующим образом.
Образцы опухолей приготавливали следующим образом. Образцы опухолей при использовании антитела-38 в комбинации с химиотерапевтическим агентом на гуманизированной мышиной (NOG) модели приготавливали согласно описанной ниже процедуре. NOG-мышей (фирма In-Vivo Science Inc.,  ) облучали рентгеновскими лучами в дозе 2,5 Гр. На следующий день 1×105 CD34-позитивных гематопоэтических стволовых клеток, которые получали из крови пупочного канатика, трансплантировали NOG-мышам путем инъекции в хвостовую вену. Через 16-20 недель каждую из человеческих линий раковых клеток (MKN45 и NCI-H446) смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно гуманизированным NOG-мышам. День трансплантации обозначали как день 0.
) облучали рентгеновскими лучами в дозе 2,5 Гр. На следующий день 1×105 CD34-позитивных гематопоэтических стволовых клеток, которые получали из крови пупочного канатика, трансплантировали NOG-мышам путем инъекции в хвостовую вену. Через 16-20 недель каждую из человеческих линий раковых клеток (MKN45 и NCI-H446) смешивали с матриксом базальной мембраны Matrigel™ и трансплантировали подкожно гуманизированным NOG-мышам. День трансплантации обозначали как день 0.
После подтверждения образования опухолей мышей разделяли на группы в зависимости от размера опухолей и веса тела. Антитело-38 и фармацевтические агенты, предназначенные для применения в комбинации, вводили с использованием дозы и режима дозирования, которые указаны в таблице 21. Мышей умерщвляли в указанные в таблице 21 моменты времени и опухоль изымали и сохраняли для применения в анализе инфильтрующих опухоль лимфоцитов (TIL), анализе патологий или анализе РНК.
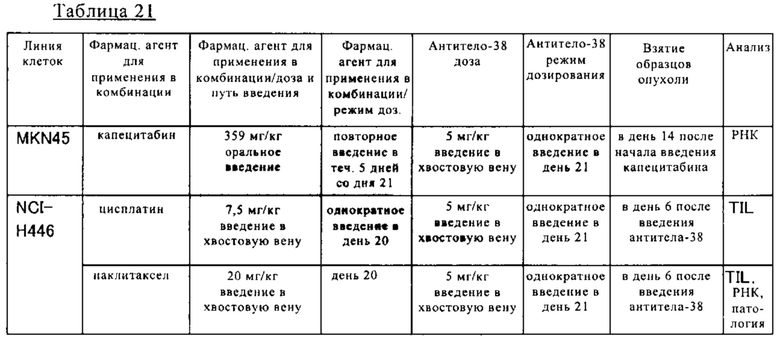
Анализ РНК осуществляли следующим образом. РНК экстрагировали (набор miRNeasy Mini, фирма QIAGEN) из описанных выше образцов опухолей и определяли концентрации РНК (NanoDrop, фирма Thermo Fisher Scientific). 100 нг РНК подвергали всеобъемлющему анализу экспрессии (человеческой) РНК с использованием панели основных генов, участвующих в пути развития рака (nCounter PanCancer Pathway Panel), и панели иммунного профиля экспрессии генов рака (PanCancer Immune Profiling Panel) (фирма NanoStrng). Стандартизацию осуществляли с использованием генов «домашнего хозяйства», включенных в панель. Применяемое программное обеспечения анализа представляло собой nSolver (фирма NanoStrng).
В результате установлено, что экспрессия маркеров иммунных клеток, хемокинов, цитокинов, генов, участвующих в клеточной гибели, генов, участвующих в регуляции клеточного цикла, повышалась, а экспрессия генов, участвующих в развитии клеточного цикла, подавлялась, когда антитело-38 применяли в комбинации с химиотерапевтическим агентом, т.е. паклитакселом или капецитабином, по сравнению с группой, которой антитело-38 или химиотерапевтический агент вводили в качестве индивидуального средства (фиг. 35-1-35-6).
Анализ TIL осуществляли следующим образом. Опухолевые ткани, полученные из мышей, трансплантированных NCI-H446, указанные в таблице 21, на шестой день после введения антитело-38 расщепляли на клетки путем обработки ферментами с использованием устройства для мягкой диссоциации MACS™ Octo. Клетки метили с помощью антител к CD45, CD3, CD4, CD8 и GZMB и оценивали положительные уровни в каждой фракции TIL с использованием устройства BD LSRFortessa Х-20.
В результате установлено, что популяции клеток, экспрессирующих маркеры Т-клеток, маркеры активированных Т-клеток и белки, участвующие в цитотоксической активности, увеличивались, когда антитело-38 применяли в комбинации с химиотерапевтическим агентом, т.е. паклитакселом или капецитабином, по сравнению с группой, которой антитело-38 или химиотерапевтический агент вводили в качестве индивидуального средства (фиг. 36-1 и 36-2).
При осуществлении гистологического анализа опухолевых тканей образцы опухолей из мышей через 6 дней после введения антитела-38 и паклитаксела фиксировали в нейтральном буферном растворе 10%-ного формальдегида. Затем приготавливали окрашенные гематоксилин-эозином (НЕ) образцы согласно общепринятому методу и осуществляли гистопатологическую оценку с использованием светового микроскопа.
В результате установлено, что, когда вводили антитело 38, обнаружена инфильтрация иммунных клеток вокруг периферии опухоли, область инфильтрации расширялась, когда антитело-38 применяли в комбинации с паклитакселом.
Опыт по оценке эффективности в качестве лекарственного средства антитела-38 и других агентов с использованием модифицированной человеческим геном CD3εδγ мышиной модели осуществляли следующим образом. Линии раковых клеток Hepa1-6/hGPC3 и LLC1/hGPC3, которые представляют собой мышиные линии раковых клеток, сверхэкспрессирующие человеческий GPC3, трансплантировали подкожно модифицированным человеческим геном CD3εδγ мышам (фирма Chugai Pharmaceytical Co. Ltd). День трансплантации обозначали как день 0. После подтверждения образования видимых опухолей мышей разделяли на группы в зависимости от размера опухолей и веса тела. Обработку осуществляли путем введения антитела-38 в комбинации с антителом к мышиному TIM-3, антителом к мышиному LAG-3, антителом к мышиному CD137 или антителом к мышиному VEGFR2. Доза каждого фармацевтического агента, который применяли в комбинации с антителом-38, указана в таблице 8.
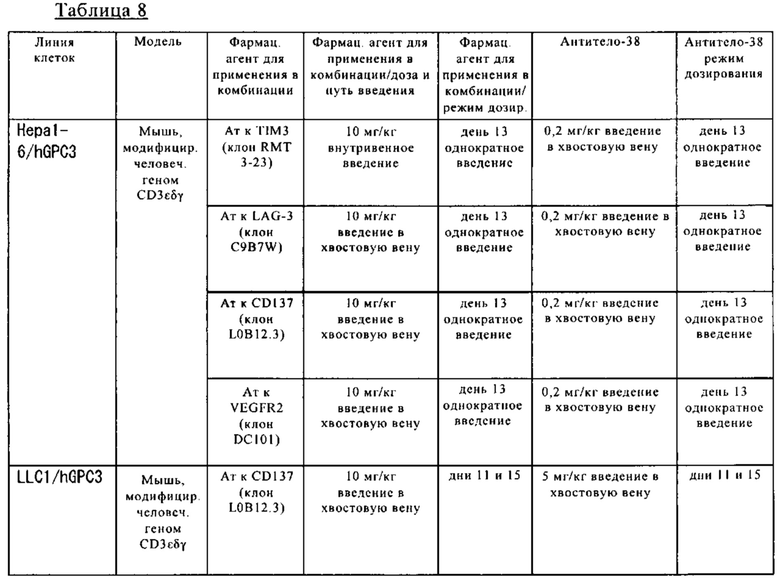
В результате установлено, что противоопухолевое действие повышалось в обработанных комбинацией группах, которым вводили антитело-38 и фармацевтический агент, предназначенный для применения в комбинации, по сравнению с группами, которым антитело-38 или фармацевтический агент, предназначенный для применения в комбинации, вводили в качестве индивидуального средства (фиг. 9 и 10).
Опыт по оценке эффективности в качестве лекарственного средства антитела-38 и других агентов с использованием модифицированной человеческим геном CD3ε мышиной модели осуществляли следующим образом. Линию раковых клеток Hepa1-6/hGPC3, которая представляет собой мышиную линию раковых клеток, сверхэкспрессирующую человеческий GPC3, трансплантировали подкожно модифицированным человеческим геном CD3ε мышам (фирма Chugai Pharmaceutical Co. Ltd). День трансплантации обозначали как день 0. В день 15 мышей разделяли на группы в зависимости от размера опухолей и веса тела. Обработку осуществляли путем введения антитела-38 в комбинации с антителом к мышиному PD-1 или антителом к мышиному PD-L1. Доза каждого фармацевтического агента, который применяли в комбинации с антителом-38, указана в таблице 9.

В результате установлено, что противоопухолевое действие повышалось в обработанных комбинацией группах, которым вводили антитело-38 и фармацевтический агент, предназначенный для применения в комбинации, по сравнению с группами, которым антитело-38 или фармацевтический агент, предназначенный для применения в комбинации, вводили в качестве индивидуального средства (фиг. 11).
Приведенные для справки примеры
Приведенный для справки пример 1 Получение GPC3_ERY22_rCE115 и измерение цитотоксической активности
(1-1) Получение GPC3_ERY22_rCE115
Молекулу, в которой один из Fab заменяли на домен, связывающий CD3 эпсилон, получали, используя IgG против ракового антигена (GPC3) в качестве основной структуры. В этом случае Fc-область IgG, которую применяли в качестве основной структуры, представляла собой молчащую Fc с ослабленной аффинностью к FcgR (Fcγ- (Fc-гамма) рецептор). Антитело к GPC3 Н0000 (SEQ ID NO: 40)/GL4 (SEQ ID NO: 41) применяли в качестве GPC3-связывающего домена. Антитело к CD3 rCE115H/rCE115L (SEQ ID NO: 42/SEQ ID NO: 43) применяли в качестве CD3-связывающего домена.
Конструкцию G1d, полученную удалением Gly и Lys на С-конце IgG1, применяли в качестве константной области Н-цепи антитела и ее применяли в комбинации с H0000/GL4 и rCE115H/rCE115L. Когда константную область Н-цепи антитела обозначали как H1, последовательность, соответствующую Н-цепи антитела, несущую Н0000 в вариабельной области, обозначали как Н0000-Н1. В настоящем описании аминокислотное изменение обозначали, например, как D356K. Первый алфавитный символ (соответствует D в D356K) представляет собой однобуквенный код аминокислотного остатка до модификации, следующий за ним номер (соответствует 356 в D356K) обозначает положение модификации согласно EU-нумерации, а последний алфавитный символ (соответствует K в D356K) представляет собой однобуквенный код аминокислотного остатка после модификации. G1dh (SEQ ID NO: 44), полученную путем удаления Gly и Lys на С-конце IgG1, ERY22_Hk (SEQ ID NO: 45), созданную путем интродукции мутаций L234A/L235A/Y349C/T366W в G1dh, а ERY22_Hh (SEQ ID NO: 46), созданную путем интродукции мутаций L234A/L235A/D356C/T366S/L368A/Y407V в G1dh, получали согласно методу, описанному в приведенном для справки примере 5. Мутации L234A и L235A интродуцировали в соответствующие Н-цепи для ослабления аффинности к FcgR (Fcγ-рецептор), а мутации Y349C/T366W и D356C/T366S/L368A/Y407V интродуцировали для эффективного образования гетеромеров каждой Н-цепи при получении гетеродимерных антител, содержащих два типа Н-цепей.
Гетеродимерное антитело GPC3_ERY22_rCE115, полученное заменой VH- и VL-доменов Fab против GPC3, создавали согласно методу, описанному в приведенном для справки примере 5 (фиг. 12а).
Серии экспрессионных векторов со встроенным полинуклеотидом, кодирующим каждую из конструкций GL4-ERY22_Hk (SEQ ID NO: 47), H0000-ERY22_L (SEQ ID NO: 48), rCE115H-ERY22_Hh (SEQ ID NO: 49) и rCE115L-k0 (SEQ ID NO: 50), получали с помощью методов, хорошо известных специалистам в данной области, таких как методы на основе ПЦР с использованием добавленных праймеров, которые имели соответствующие последовательности, аналогичные применяемым в описанном выше методе.
В клетки FreeStyle 293-F интродуцировали представленную ниже комбинацию экспрессионных векторов для кратковременной экспрессии каждой молекулы-мишени.
Молекула-мишень: GPC3_ERY22_rCE115
Полипептиды, кодируемые полинуклеотидами, встроенными в экспрессионные векторы: GL4-ERY22_Hk, H0000-ERY22_L, rCE115H-ERY22_Hh, rCE115L-k0.
(1-2) Очистка GPC3_ERY22_rCE115
Полученный супернатант культуры добавляли в колонку с антителом к FLAG М2 (фирма Sigma) и затем колонку промывали, после чего элюировали, используя пептид FLAG (фирма Sigma) в концентрации 0,1 мг/мл. Фракции, содержащие представляющую интерес молекулу, добавляли в колонку HisTrap HP (фирма GE Healthcare), а затем колонку промывали, после чего элюировали с использованием концентрационного градиента имидазола. Фракцию, содержащую представляющую интерес молекулу, концентрировали с использованием метода ультрафильтрации и затем концентрат вносили в колонку, заполненную Супердекс 200 (фирма GE Healthcare), и каждую из очищенных представляющих интерес молекул получали, собирая только мономерные фракции.
(1-3) Измерение цитотоксической активности GPC3_ERY22_rCE115 с использованием мононуклеарных клеток периферической крови человека
Оценивали in vitro цитотоксическую активность GPC3_ERY22_rCE115.
(1-3-1) Получение раствора мононуклеарных клеток периферической крови человека (РВМС)
Получали образцы по 50 мл периферической крови здоровых добровольцев (взрослых) с использованием шприцев, предварительно заполненных 100 мкл (1000 ед./мл) раствора гепарина (Novo-Heparin 5000 ед. на инъекцию; фирма Novo Nordisk). Эту периферическую кровь двукратно разводили ЗФР(-), разделяли на четыре аликвоты и добавляли в пробирки для разделения лимфоцитов Leucosep (каталожный №227290; фирма Greiner bio-one), в которые предварительно вносили 15 мл фиколл-пак PLUS и центрифугировали. После центрифугирования пробирок для разделения (2150 об/мин, 10 мин, комнатная температура) собирали фракции мононуклеарных клеток. Клетки во фракции мононуклеарных клеток однократно промывали с использованием модифицированной по методу Дульбекко среды Игла (фирма SIGMA), содержащей 10% FBS (далее в контексте настоящего описания обозначена как 10% FBS/D-MEM), а затем плотность клеток доводили до 4×106 клеток/мл с помощью 10% FBS/D-MEM. Полученную таким образом клеточную суспензию применяли в качестве раствора человеческих РВМС в последующих экспериментах.
(1-3-2) Измерение цитотоксической активности
Цитотоксическую активность оценивали на основе степени ингибирования клеточного пролиферации с помощью анализатора клеток в реальном времени xCELLigence (фирма Roche Diagnostics). Применяемые клетки-мишени представляли собой клеточную линию рака человека NCI-H446 или клеточную линию рака человека РС-10, экспрессирующую GPC3. Клетки NCI-H446 или РС-10 отделяли от чашек и высевали в планшет E-Plate 96 (фирма Roche Diagnostics) в виде аликвот по 100 мкл/лунку, регулируя их количество на уровне 1×104, и начинали анализ жизнеспособных клеток с помощью анализатора клеток в реальном времени xCELLigence. На следующий день планшет удаляли из анализатора клеток в реальном времени xCELLigence и в планшет добавляли по 50 мкл каждого соответствующего полученного антитела в различных концентрациях (0,004, 0,04, 0,4 и 4 нМ). После осуществления реакции в течение 15 мин при комнатной температуре добавляли 50 мкл раствора человеческих РВМС (2×105 клеток/лунку), полученного согласно методу, описанному в разделе (1-2) и клетки вновь помещали в анализатор клеток в реальном времени xCELLigence и начинали анализ жизнеспособных клеток. Реакцию проводили в атмосфере 5% газообразного диоксида азота при 37°С и степень ингибирования пролиферации клеток (%) определяли с помощью приведенной ниже формулы с использованием величины клеточного индекса, определенной через 72 ч после добавления человеческих РВМС. Применяемую для расчета величину клеточного индекса стандартизовали таким образом, что величину клеточного индекса, определенную непосредственно перед добавлением антитела, принимали за 1.
Степень ингибирования пролиферации клеток (%) = (А-Б) × 100/(А-1)
В этой формуле А обозначает среднюю величину клеточного индекса в лунках без добавления антитела (только клетки-мишени и человеческие РВМС), а Б обозначает среднюю величину клеточного индекса в каждой лунке. Измерение осуществляли в трех повторностях.
Когда мононуклеарные клетки периферической крови (РВМС), полученные из человеческой крови, применяли в качестве эффекторных клеток для анализа цитотоксичности GPC3_ERY22_rCE115, обнаружена очень сильная активность (фиг. 13).
Приведенный для справки пример 2 Гуманизация Н-цепи антитела к CD3, rCE115, и «совместное использование» общей L-цепи
(2-1) Создание hCE115HA, гуманизированной вариабельной области Н-цепи антитела rCE115
Гуманизировали вариабельную область Н-цепи антитела rCE115 к CD3 (SEQ ID NO: 42). CDR и FR определяли по Кэботу (нумерация Кэбота).
Сначала выбирали последовательность человеческого FR путем сравнения последовательностей вариабельных областей человеческих антител в базе данных с крысиной последовательностью вариабельной области rCE115. В качестве базы данных применяли базу данных IMGT (http://www.imgt.org/) и NCBI GenBank (http://www.ncbi.nlm.nih.gov/genbank/). Гуманизированную последовательность вариабельной области Н-цепи создавали, сшивая последовательность CDR вариабельной области Н-цепи rCE115 с выбранной последовательностью человеческого FR. Таким путем получали гуманизированную последовательность вариабельной области Н-цепи, hCE115HL (SEQ ID NO: 51).
Аминокислотный остаток в положении 93 согласно нумерации Кэбота представляет собой Ala в выбранной последовательности человеческого FR3 Н-цепи, но представляет собой Arg в последовательности вариабельной области rCE115. При использовании базы данных последовательностей крысиных и человеческих зародышевых линий (база данных IMGT (http://www.imgt.org/)) обнаружено лишь несколько последовательностей, которые содержат в этом сайте Arg. Известно, что аминокислотный остаток в положении 94 согласно нумерации Кэбота принимает участие в стабилизации структуры антитела путем образования верхнего ядра (Ewert и др., Methods 34(2) октябрь 2004 г., сс. 184-199). На основе указанной информации создавали новую последовательность гуманизированной вариабельной области Н-цепи, в которой аминокислотные остатки в положениях по Кэботу 93 и 94 в FR3 Н-цепи заменяли на остатки, присутствующие в последовательности вариабельной области rCE115. Таким путем получали гуманизированную последовательность вариабельной области Н-цепи hCE115HA (SEQ ID NO: 52).
(2-2) Создание общей L-цепи L0000 для антитела к CD3 rCE115 и антитела к GPC3
Осуществляли перестановку FR/CDR вариабельной области L-цепи rCE115L (SEQ ID NO: 43) антитела к CD3 rCE115 и вариабельной области L- цепи GL4 (SEQ ID NO: 41) антитела к GPC3.
Выбирали последовательность FR GL4 в качестве последовательности FR L-цепи. CDR2 L-цепи был одинаковым в rCE115L и GL4. CDR1 L-цепи выбирали из последовательностей CDR GL4, а CDR3 L-цепи выбирали из последовательностей CDR rCE115L соответственно. Кроме того, вновь создавали CDR3 L-цепи путем замены аминокислотного остатка Asp в положении 94 по Кэботу выбранного CDR3 L-цепи на остаток Val, присутствующий в GL4.
Гуманизированную последовательность вариабельной области L-цепи создавали, сшивая отобранные FR и CDR, описанные выше. В результате получали гуманизированную последовательность вариабельной области L-цепи, L0000 (SEQ ID NO: 53).
(2-3) Оценка аффинности к человеческому GPC3
Оценивали связывающую активность в отношении человеческого GPC3 при применении GL4 (SEQ ID NO: 41) и L0000 (SEQ ID NO: 53) в качестве вариабельных областей L-цепей. Для осуществления этого применяли молекулярную форму антитела с одним плечом, несущего один Fab, гетеродимеризованный в Fc-области человеческого IgG1 с помощью технологии «knobs-into-hole». Н0000 (SEQ ID NO: 40) применяли в качестве вариабельной области Н-цепи антитела к GPC3.
Константы аффинности и связывания антитела к GPC3 в отношении антигена измеряли с помощью метода многоциклической кинетики на основе поверхностного плазмонного резонанса с использованием устройства Biacore™-Т200 (фирма GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания белка A/G с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Каждое антитело к GPC3 приготавливали таким образом, чтобы примерно 100 RU «захватывалось» белком A/G. Человеческий GPC3, применяемый в качестве аналита, приготавливали в концентрации 8, 16, 32, 64 и 128 нМ, используя HBS-EP+. При осуществлении измерений сначала давали белку A/G связываться с раствором антитела, а затем инъецировали раствор человеческого GPC3 со скоростью потока 30 мкл/мин в течение 3 мин, давая пройти реакции. Затем раствор заменяли на буфер HBS-EP+ и осуществляли оценку фазы диссоциации в течение 15 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Аналогично осуществляли измерение при концентрации 0, давая белку A/G осуществлять «захват» в растворе антитела, осуществляя инъекцию HBS-EP+ в течение 3 мин, давая пройти реакции, и затем, заменяя раствор на HBS-EP+ для оценки фазы диссоциации в течение 15 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Для анализа данных применяли только программу для Biacore-анализа, программу Biacore Т200 Evaluation, версия 1.0 применяли для осуществления кинетического анализа для расчета константы скорости реакции связывания (ka), константы скорости реакции диссоциации (kd) и соотношения констант скорости на основе полученных сенсограмм. Результаты представлены в таблице 10.

(2-4) Оценка аффинности к человеческому CD3
Оценивали связывающую активность в отношении человеческого CD3 при применении hCE115HA (SEQ ID NO: 52) в качестве вариабельной области Н-цепи и L0000 (SEQ ID NO: 53) в качестве вариабельной области L-цепи. Для осуществления этого применяли молекулярную форму антитела с одним плечом, несущего один Fab, гетеродимеризованный в Fc-области человеческого IgG1 с помощью технологии «knobs-into-hole».
Константы аффинности и связывания антитела к CD3 в отношении антигена измеряли с помощью метода одноциклической кинетики на основе поверхностного плазмонного резонанса с использованием устройства Biacore™-Т200 (фирма GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания человеческого CD3 с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Антитело к CD3, применяемое в качестве аналита, приготавливали в концентрациях 5 и 20 мкг/мл, используя HBS-EP+. Измерения осуществляли путем первой инъекции каждого из растворов антитела к CD3 в концентрациях 5 и 20 мкг/мл в течение 3 мин при скорости потока 20 мкл/мин, давая пройти реакции. Затем раствор заменяли на HBS-EP+ и осуществляли оценку фазы диссоциации в течение 3 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Для анализа данных применяли только программу для Biacore-анализа, программу Biacore Т200 Evaluation, версия 1.0 применяли для осуществления кинетического анализа для расчета константы скорости реакции связывания (ka), константы скорости реакции диссоциации (kd) и соотношения констант скорости на основе полученных сенсограмм. Результаты представлены в таблице 11.

(2-5) Получение GPC3_ERY27_hCE115
IgG4 к раковому антигену (GPC3) применяли в качестве основной структуры для получения молекулы ERY27 (фиг. 12), в которой вариабельную область Н-цепи одного из Fab заменяли на домен, связывающий CD3-эпсилон, а L-цепь была общей для обоих Fab. В этом случае Fc IgG4, которую применяли в качестве основной структуры, представляла собой молчащую Fc с ослабленной аффинностью к FcgR (Fcγ-(Fc-гамма) рецептор). Н0000 (SEQ ID NO: 40) применяли в качестве вариабельной области Н-цепи GPC3-связывающего домена, а hCE115HA (SEQ ID NO: 52) применяли в качестве вариабельной области Н-цепи CD3-связывающего домена. L0000 (SEQ ID NO: 53) применяли в качестве вариабельной области L-цепи. Мутации D356K и K439E интродуцировали в соответствующие Н-цепи для эффективного образования гетеромеров каждой Н-цепи при получении гетеродимерных антител, содержащих два типа Н-цепей (WO 2006/106905). H435R представляет собой модификацию, которая нарушает связывание с белком А, и ее интродуцировали для эффективного разделения гетеромера и гомомера (WO 2011/078332).
Серии экспрессионных векторов со встроенным полинуклеотидом, кодирующим каждую из конструкций f H0000-ERY27_HK (SEQ ID NO: 54), hCE115HA-ERY27_HE (SEQ ID NO: 55) и L0000-k0 (SEQ ID NO: 56), получали хорошо известными методами.
В клетки FreeStyle 293-F интродуцировали следующую комбинацию экспрессионных векторов для кратковременной экспрессии каждой молекулы-мишени.
Молекула-мишень: GPC3_ERY27_hCE115
Полипептиды, кодируемые полинуклеотидами, встроенными в экспрессионные векторы: H0000-ERY27_HK, hCE115HA-ERY27_HE и L0000-k0.
(2-6) Очистка GPC3_ERY27_hCE115
Каждую представляющую интерес молекулу очищали методом, описанным в приведенном для справки примере 1-2.
(2-7) Измерение цитотоксической активности с использованием мононуклеарных клеток периферической крови человека
(2-7-1) Получение раствора мононуклеарных клеток периферической крови человека (РВМС)
Раствор приготавливали согласно методу, описанному в приведенном для справки примере 1-3-1.
(2-7-2) Оценка цитотоксической активности
Цитотоксическую активность оценивали согласно методу, описанному в приведенном для справки примере 1-3-2.
Когда РВМС, полученные из человеческой крови, применяли в качестве эффекторных клеток для оценки цитотоксичности GPC3_ERY27_hCE115, было обнаружено снижение активности в результате гуманизации Н-цепи rCE115 и «совместного использования» общей L-цепи (фиг. 13).
Приведенный для справки пример 3 Получение и оценка гуманизированных вариантов биспецифических антител для улучшения различных свойств
Зависимая от Т-клеток цитотоксическую активность (TDCC-активность) биспецифического гуманизированного антитела к CD3-цепи (CD3-эпсилон) и к GPC3, полученного согласно методу, описанному в приведенном для справки примере 2, GPC3_ERY27_hCE115 (SEQ ID NO: 54, 55 и 56), оказалась ниже, чем зависимая от Т-клеток цитотоксическая активность GPC3_ERY22_rCE115 (SEQ ID NO: 47, 48, 49 и 50). Это может являться результатом ослабления аффинности к GPC3 и CD3ε-цепи в результате гуманизации и «совместного использования» общей L-цепи. Касательно антигенов, таких как GPC3 и CD3ε-цепи, которые имеют независимые друг от друга последовательности, к настоящему времени отсутствуют данные о гуманизированных биспецифических антителах с повышенной зависимой от Т-клеток цитотоксической активностью и улучшенной аффинностью к обоим антигенам при использовании общей L-цепи антитела. Таким образом, представляется сложным получение гуманизированных антител с двойной специфичностью, обладающих эффективностью в качестве лекарственных средств, эквивалентной или более высокой, чем у антитела GPC3_ERY22_rCE115.
С учетом указанных обстоятельств при создании изобретения получали модифицированные гуманизированные биспецифические антитела с модифицированной аффинностью к человеческому GPC3 и человеческой CD3ε-цепи с помощью методов, известных специалистам в данной области, которые включали обширную замену аминокислотных остатков, кодируемых геном антитела, с получением вариантов антител против обоих антигенов, а именно человеческого GPC3 и человеческой CD3ε-цепи, осуществление различных оценок с помощью скрининга. Кроме того, аналогичные методы применяли для получения модифицированных гуманизированных биспецифических антител с модифицированными физико-химическими свойствами. Кроме того, путем объединения замен аминокислотных остатков, обладающих эффективностью в отношении модификации аффинности и физико-химических свойств, получали оптимизированные биспецифические антитела с TDCC-активностью, эквивалентной или более высокой, чем зависимая от Т-клеток клеточная цитотоксичность GPC3_ERY22_rCE115 до гуманизиации.
Интродукцию точечных мутаций, экспрессию и очистку антител, оценку аффинности к антигену и определение зависимой от Т-клеток клеточной цитотоксичности при оптимизации гуманизированных биспецифических антител осуществляли согласно методам, аналогичным описанным в приведенных для справки примерах 1 и 2. CDR и FR определяли согласно Кэботу (нумерация Кэбота).
В зависимости от цели следующие конструкции применяли в качестве константных областей Н-цепи антитела (номера соответствуют EU-нумерации): E22Hh (SEQ ID NO: 57), которую получали путем интродукции мутаций L234A/L235A/N297A/D356C/T366S/L368A/Y407V/G446-делеция/K447-делеция в человеческий IgG1; E22Hk (SEQ ID NO: 58), которую получали путем интродукции мутаций L234A/L235A/N297A/Y349C/T366W/G446-делеция/K447-делеция, и инсерционной мутации Ser-Ser непосредственно перед положением 118 в человеческом IgG1; G1dh получали путем интродукции мутаций D356C/T366S/L368A/Y407V/G446-делеция/K447-делеция в человеческий IgG1; none-Hi-Kn010G3 получали путем интродукции делеции 118-215 и мутаций C220S/Y349C/T366W/H435R в человеческий IgG1; E2702GsKsc (SEQ ID NO: 60) получали путем интродукции мутаций L235R/S239K/N297A/E356K/R409K/H435R/L445P/G446-делеция/K447-делеция в человеческий IgG4; E2704sEpsc (SEQ ID NO: 61) получали путем интродукции мутаций K196Q/L235R/S239K/N297A/R409K/K439E/L445P/G446-делеция/K447-делеция в человеческий IgG4; и E2702sKsc (SEQ ID NO: 62) получали путем интродукции мутаций L235R/S239K/N297A/E356K/R409K/L445P/G446-делеция/K447-делеция в человеческий IgG4. Кроме того, человеческую κ-цепь (каппа-цепь) k0 (SEQ ID NO: 63) и E22L (SEQ ID NO: 432) получали путем интродукции мутаций R108A/T109S в человеческую κ-цепь, применяемую в качестве константных областей L-цепи антитела.
Мутация, приводящая к замене Asp на Cys в положении 356 согласно EU-нумерации, мутация, приводящая к замене The на Ser в положении 366 согласно EU-нумерации, мутация, приводящая к замене Leu на Ala в положении 368 согласно EU-нумерации, мутация, приводящая к заменам Tyr на Val в положении 407 согласно EU-нумерации, мутация, приводящая к замене Tyr на Cys в положении 349 согласно EU-нумерации, мутация, приводящая к замене Thr на Trp в положении 366 согласно EU-нумерации, и мутация, приводящая к вставке Ser-Ser непосредственно перед положением 118 согласно EU-нумерации, представляют собой мутации, предназначенные для эффективного образования гетеродимерных молекул каждой Н-цепи при создании гетеромерных антител. Аналогично этому, мутация, приводящая к замене Glu на Lys в положении 356 согласно EU-нумерации, и мутация, приводящая к замене Lys на Glu в положении 439 согласно EU-нумерации, также представляют собой мутации, предназначенные для эффективного образования гетеродимерных молекул каждой Н-цепи при создании гетеромерных антител. Как ожидается, они должны повышать эффективность производства биспецифических антител.
Мутация, приводящая к замене Leu на Ala в положение 234 согласно EU-нумерации, мутация, приводящая к заменам Leu на Ala или Arg в положение 235 согласно EU-нумерации, мутация, приводящая к замене Ser на Lys в положение 239 согласно EU-нумерации, и мутация, приводящая к замене Asn на Ala в положение 297 согласно EU-нумерации, представляют собой мутации, предназначенные для ослабления аффинности к Fcγ-рецептору и комплементу (C1q). Как ожидается, они должны подавлять связывание Fab с CD3 и опосредуемое Fc перекрестное сшивание Fcγ-рецептора или комплемента и позволять избегать синдрома высвобождения цитокинов, который сопровождает повышение неспецифических эффекторных функций.
Н-цепь, в которую интродуцированы делеционные мутации в положениях 118-215 согласно EU-нумерации, можно объединять с полноразмерной последовательностью Н-цепи с получением антитела, которое имеет только один Fab (одновалентное антитело), и ее можно применять для оценки аффинности.
Мутация, приводящая к замене Arg на Lys в положении 409 согласно EU-нумерации, и мутация, приводящая к замене His на Arg в положении 435 согласно EU-нумерации, представляют собой мутации, приводящие к модификации свойства антитела, приближая их к свойствам человеческого IgG1 и человеческого IgG3 соответственно.
(3-1) Модификация аффинности гуманизированного антитела к CD3 с помощью точечных мутаций
Сначала интродуцировали точечные мутации в последовательность FR1, FR2, FR3, CDR1, CDR2 и CDR3 гуманизированного антитела к человеческой CD3ε-цепи, полученного согласно методу, описанному в приведенном для справки примере 2, hCE115HA-ERY27_HE (SEQ ID NO: 55), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимой человеческой CD3ε-цепи. Объединяя сайты, которые обладают способностью повышать аффинность модифицированных антител, получали модифицированные антитела, аффинности которых представлены в таблице 12.



(3-2) Модификация аффинности гуманизированного антитела к GPC3 с помощью точечных мутаций
Сначала интродуцировали точечные мутации в последовательность CDR1, CDR2 и CDR3 биспецифического антитела, полученного согласно методу, описанному в примере 2, H0000-ERY27_HK (SEQ ID NO: 54), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимому человеческому GPC3. Объединяя сайты, которые обладают способностью повышать аффинность модифицированных антител, получали модифицированные антитела, аффинности которых представлены в таблице 13.



(3-3) Модификация pI с помощью точечных мутаций
При коммерческом производстве биспецифических антител требуется высокой уровень чистоты. При использовании ионообменной хроматографии эффективной является модификация изоэлектрической точки (р1) молекул (PLoS One. 2013;8(2):e57479). По этой причине интродуцировали мутации для модификаций pI в последовательность CDR1, CDR2 и CDR3 гуманизированного антитела к человеческому GPC3, полученного согласно методу, описанному в примере 2, H0000-ERY27_HK (SEQ ID NO: 54), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимому человеческому GPC3.
В результате установлено, что аминокислотным модификациям, которые могут приводить к снижению pI, сохраняя при этом аффинность к человеческому GPC3, следует подвергать аминокислоты в положениях 19, 43, 53 и 61 согласно нумерации Кэбота.
Объединяя сайты, которые обладают способностью поддерживать аффинность к человеческому GPC3 и снижать pI, получали антитела, аффинности и р1 которых представлены в таблице 14.

(3-4) Модификация способности связывать внеклеточный матрикс с помощью точечной мутации
Известно, что неспецифическое связывание с внеклеточным матриксом (ЕСМ) и т.п. может оказывать влияние на фармакокинетику (MAbs. 4(6), ноябрь-декабрь 2012 г., ее. 753-760). Таким образом, ЕСМ-связывающую способность модифицированных антител, полученных согласно описанным в приведенных для справки примерах методам, определяли с помощью метода, представленного в приведенном для справки примере 8. В результате было подтверждено, что гуманизированное биспецифическое антитело к человеческой CD3ε-цепи и к человеческому GPC3, GPC3_ERY27_hCE115 (SEQ ID NO: 54, 55 и 56), обладало высокой ЕСМ-связывающей способностью. Таким путем изучали любую из оцененных в приведенных для справки примерах 3-1, 3-2 и 3-3 точечных мутаций в последовательности гуманизированного антитела к человеческой CD3ε-цепи hCE115HA-ERY27JHE (SEQ ID NO: 55) в качестве комбинации для снижения ЕСМ-связывающей способности. В результате было установлено, что аминокислоты в положениях 11, 16, 52а, 53, 98 и 100 согласно нумерации Кэбота участвуют в поддержании аффинности к CD3ε и могут влиять на снижение ЕСМ-связывающей способности, и получали антитела с пониженной ЕСМ-связывающей способностью по сравнению со способностью варианта гуманизированного биспецифического антитела к человеческой CD3ε-цепи и к человеческому GPC3, GPC3_ERY27_hCE115 (таблица 15).

(3-5) Модификация способности связываться с лигандом SuRe с помощью точечных мутаций
Известен пример того, что связывание антитела с белком А зависит от последовательности вариабельной области (VH3) (J Biomol Tech. 22(2), июль 2011 г., ее. 50-52). При очистке на белке А гуманизированного биспецифического антитела к человеческой CD3ε-цепи и к человеческому GPC3, удаление гомомерного антитела к CD3 являлось важным для подавления неспецифических реакцией посредством CD3. Таким образом, представляется желательным подавлять связывание гомомерного антитела к CD3 с белком А. Вероятно, лиганд SuRe™ можно применять при коммерческом производстве и поэтому точечные мутации, влияющие на связывание с лигандом SuRe™, интродуцировали в CDR2 Н-цепи вариантов гуманизированного антитела к CD3, TR01H082-E2702GsKsc и TR01H084-E2702GsKsc (SEQ ID NO: 398 и 399), для получения модифицированных антител. Связывающую способность этих модифицированных антител с лигандом SuRe определяли с помощью метода, представленного в приведенном для справки примере 9. В результате было установлено, что аминокислоты в положениях 19, 57 и 59 согласно нумерации Кэбота участвуют в поддержании аффинности к CD3ε и могут влиять на способность связываться с лигандом Sure, и получали антитела с пониженной способностью связываться с лигандом Sure по сравнению со способностью антител TR01H082-E2702GsKsc/L0011-k0 (SEQ ID NO: 398 и 410) или TR01H084-E2702GsKsc/L0011-k0 (SEQ ID NO: 399 и 410) (таблица 16).
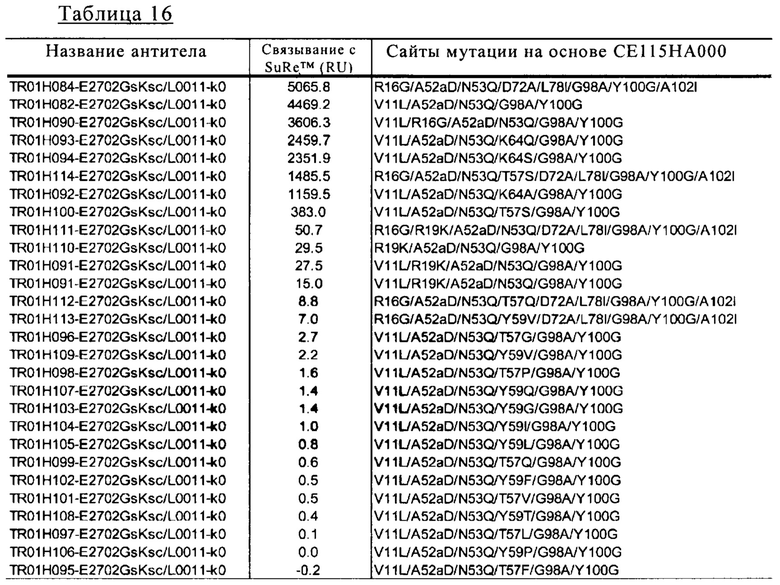
(3-6) Получение оптимизированных биспецифических антител путем объединения точечных мутаций, приводящих к улучшению различных свойств
Оптимизированные модифицированные антитела можно получать, объединяя точечные мутации, которые приводят к улучшению различных свойств, описанных в приведенных для справки примерах 3-1-3-5. В качестве примеров указанных модифицированных антител получали антитела, представленные в таблице 17, и у них оценивали зависимую от Т-клеток клеточную цитотоксичность (TDCC) с помощью методов, аналогичных описанным в приведенном для справки примере 1. Результаты представлены на фиг. 15-20. В результате получали оптимизированные гуманизированные биспецифические антитела к человеческой CD3ε-цепи и к человеческому GPC3, обладающие эквивалентной или более высокой зависимой от Т-клеток клеточной цитотоксичностью, чем GPC3_ERY22_rCE115 до его гуманизации.

В приведенных для справки примерах 3-1-3-6 продемонстрировано, что указанные ниже аминокислотные остатки, например, являются важными для поддержания свойств оптимизированных биспецифических антител к человеческой CD3ε-цепи и к человеческому GPC3, которые обладали эквивалентной или более высокой зависимой от Т-клеток клеточной цитотоксичностью, чем GPC3_ERY22_rCE115 до его гуманизации.
В антителах к человеческой CD3ε-цепи присутствуют, например. Leu в положении 11, Gly в положении 16, Asp в положении 52а, Gln в положении 53, Ala в положении 72, Не в положении 78, Ala в положении 98, Gly в положении 100 и Ile в положении 102. В антителах к человеческому GPC3 присутствуют, например, Thr в положении 19, Glu в положении 43, Gly в положении 52а, Pro или Glu в положении 53, Pro в положении 55 и Glu в положении 61. Кроме того, в общих L-цепях присутствуют, например. Pro в положении 25, Pro в положении 27а, Pro в положении 27b, Не в положении 33, Gln в положении 34, Arg или Trp в положении 56 и Tyr в положении 89 (все положения обозначены согласно нумерации Кэбота).
Приведенный для справки пример 4 Оценка эффективности in vivo
Эффективность некоторых из описанных выше антител оценивали in vivo с использованием несущих опухоли модельных животных.
Оценку эффективности in vivo осуществляли для репрезентативных антител из представленных в таблице 17, для которых продемонстрировано наличие цитотоксической активности при оценке с использованием анализа in vitro, описанного в приведенном для справки примере 3-6. При оценке эффективности in vivo следует принимать во внимание любое влияние, вызываемое различиями в микроокружении из-за образования агрегатов опухолей, на результаты оценки. Для изучения использовали два типа клеточных линий человеческого рака с различной чувствительностью к действию применяемых в качестве лекарственных средств антител, т.е. линии PC-10 и NCI-H446, несмотря на то, что уровни экспрессии GPC3 в этих клетках были практически одинаковыми. Клеточные линии трансплантировали мышам с тяжелым комбинированным иммунодефицитом (NOD scid) и мышам NOD scid, у которых было подтверждено образование опухолей, инъецировали Т-клетки, выращенные культивированием in vitro человеческих РВМС. Мышей (которых обозначали как модель с инъецированными Т-клетками) обрабатывали путем введения оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3.
Более конкретно, в опытах по оценке эффективности в качестве лекарственных средств оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3, в которых применяли клетки линии PC-10 на модели с инъецированными Т-клетками, осуществляли описанные ниже опыты. Т-клетки размножали культивированием с использованием РВМС, выделенных из крови здоровых доноров, и набора для активации/экспансии человеческих Т-клеток (Т cell activation/expansion kit/human) (фирма MACS Miltenyi biotec). Смешивали клеточную линию человеческого рака PC-10 (1×107 клеток) с матриксом базальной мембраны Matrigel (фирма BD) и трансплантировали подкожно в паховую область мышей NOD scid (фирма CLEA Japan, самки возрастом 6 недель). День трансплантации обозначали как день 0. За 1 день до трансплантации мышам внутрибрюшинно вводили антитело к асиало-ганглиозиду M1 (асиало-GM1) (фирма Wako Pure Chemical Industries) из расчета 0,2 мг/мышь. Через 13-15 дней после трансплантации мышей разделяли на группы в зависимости от веса тела и размера опухолей и вновь внутрибрюшинно вводили антитело к асиало-GM1 из расчета 0,2 мг/мышь. На следующий день внутрибрюшинно трансплантировали Т-клетки, полученные вышеописанным методом размножения культивированием, из расчета 3х10 клеток/мышь. Через 4 ч после трансплантации Т-клеток внутривенно через каудальную вену вводили оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 из расчета 1 мг/кг. Оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 вводили только один раз.
В результате установлена более выраженная противоопухолевая активность в группе, обработанной оптимизированными биспецифическими антителами к человеческой CD3ε-цепи и человеческому GPC3, по сравнению с группой, обработанной растворителем (фиг. 21а, б).
Аналогичными методами осуществляли опыты по оценке эффективности в качестве лекарственных средств оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3, в которых применяли клетки линии NCI-H446, на модели с инъецированными Т-клетками. Для оценки воздействия на NCI-H446 оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 вводили один раз через каудальную вену из расчета 5 мг/кг.
В результате установлена более выраженная противоопухолевая активность в группе, обработанной оптимизированными биспецифическими антителами к человеческой CD3ε-цепи и человеческому GPC3, по сравнению с группой, обработанной растворителем (фиг. 22а, б).
Приведенный для справки пример 5 Получение экспрессионных векторов антител и экспрессия, и очистка антител
Аминокислотные замены интродуцировали методами, известными специалистам в данной области, например, с использованием набора для сайтнаправленного мутагенеза QuikChange (фирма Stratagene), ПЦР или набора для ПЦР-клонирования In-fusion Advantage (фирма TAKARA), для создания экспрессионных векторов. Нуклеотидные последовательности полученных экспрессионных векторов определяли с помощью метода, известного специалистам в данной области. Полученные плазмиды кратковременно интродуцировали в клетки клеточной линии, полученной из почки человеческого эмбриона НЕК293Н (фирма Invitrogen) или FreeStyle293 (фирма Invitrogen) для экспрессии антител. Из полученных супернатантов культуры антитела очищали с использованием колонки rProtein A Sepharose Fast Flow (фирма GE Healthcare) с помощью метода, известного специалистам в данной области. Измеряли абсорбцию при 280 нм растворов очищенных антител с помощью спектрофотометра, и концентрацию антител рассчитывали на основе определенных величин, применяя коэффициент абсорбции, рассчитанный с помощью метода РАСЕ (Protein Science 4, 1995, ее. 2411-2423).
Приведенный для справки пример 6 Определение ADCC-активности каждого из тестируемых антител с использованием мононуклеарных клеток периферической крови человека в качестве эффекторных клеток
ADCC-активность каждого из тестируемых антител определяли с помощью описанного ниже метода.
Мононуклеарные клетки периферической крови человека (обозначены далее как человеческие РВМС) применяли в качестве эффекторных клеток для измерения ADCC-активности каждого из тестируемых антител согласно описанному ниже методу.
(1) Получение раствора человеческих РВМС
Получали на фирме Chugai Pharmaceutical Co. Ltd. образцы по 50 мл периферической крови здоровых добровольцев (взрослые мужчины) с использованием шприцев, предварительно заполненных 200 мкл (1000 ед./мл) раствора гепарина (Novo-Heparin 5000 ед. на инъекцию; фирма Novo Nordisk). Эту периферическую кровь двукратно разводили ЗФР(-), разделяли на четыре аликвоты и добавляли в пробирки для разделения лимфоцитов Leucosep (фирма Greiner bio-one), в которые предварительно вносили 15 мл фиколл-пак PLUS и центрифугировали. После центрифугирования пробирок для разделения, содержащих аликвоты периферической крови, при 2150 об/мин в течение 10 мин при комнатной температуре собирали фракции мононуклеарных клеток. Клетки в каждой фракции однократно промывали с использованием модифицированной по методу Дульбекко среды Игла (фирма SIGMA), содержащей 10% FBS (далее в контексте настоящего описания обозначена как 10% FBS/D-MEM), а затем плотность клеток доводили до 5×10 клеток/мл с помощью 10% FBS/D-MEM. Клеточную суспензию в приведенных ниже экспериментах использовали в качестве клетки-мишени.
(2) Анализ высвобождения хрома (АРСС-активность)
ADCC-активность оценивали по удельной скорости высвобождения хрома, определенной методом определения высвобождения хрома. Сначала растворы антитела в каждой из приготовленных концентраций (0, 0,004, 0,04, 0,4, 4 и 40 мкг/мл) добавляли в 96-луночный планшет с U-образным дном из расчета 50 мкл на лунку. Затем высевали клетки-мишени из расчета 50 мкл на лунку (1×104 клеток/лунку) и давали выстояться при комнатной температуре в течение 15 мин. Раствор человеческих РВМС, приготовленный согласно методу, описанному в подпункте (1), добавляли из расчета 100 мкл на лунку (5×105 клеток/лунку) и планшет выдерживали в инкубаторе в атмосфере, содержащей 5% диоксида углерода, при 37°С в течение 4 ч, после чего центрифугировали. Радиоактивность в 100 мкл супернатанта культуры в каждой лунке планшета измеряли с помощью гамма-счетчика. Удельную скорость высвобождения хрома определяли по следующей формуле:
удельная скорость высвобождения хрома (%)=(А-Б)×100/(Б-В), где А представляет собой среднее значение радиоактивности (cpm) 1 00 мкл супернатанта культуры в каждой лунке; Б представляет собой среднее значение радиоактивности (cpm) 100 мкл супернатанта культуры в лунках, в которых к клеткам-мишеням добавляли 100 мкл 2%-ного водного раствора NP-40 (Nonidet Р-40, фирма Nacalai Tesque) и 50 мкл 10%-ной среды FBS/D-MEM; и В представляет собой среднее значение радиоактивности (cpm) 100 мкл супернатанта культуры в лунках, в которых к клеткам-мишеням добавляли 150 мкл 10%-ной среды FBS/D-MEM. Эксперименты осуществляли в трех повторностях и по результатам вышеуказанного эксперимента вычисляли среднее значение и стандартное отклонение удельной скорости высвобождения хрома (%), отражающей ADCC-активность, для каждого из тестируемых антител.
Приведенный для справки пример 7 Определение Tm модифицированных антител с помощью дифференциальной сканирующей флуорометрии
При такой оценке определяли величину Tm (температура тепловой денатурации) модифицированных антител с помощью дифференциальной сканирующей флуорометрии с использованием устройства Rotor-Gene Q (фирма QIAGEN). Известно, что этот метод обеспечивает предпочтительную корреляцию с величиной Tm, установленной с использованием дифференциального сканирующего калориметра, что является широко известным методом оценки термостабильности антител (Journal of Pharmaceutical Science 4, 2010, ее. 1707-1720).
5000-кратный концентрат SYPRO™ оранжевого (фирма Molecular Probes) разводили ЗФР (фирма Sigma) и затем смешивали с растворами антител с получением образцов для измерения. Аликвоты по 20 мкл каждого образца вносили в измерительные пробирки и температуру повышали с 30°С до 99°С со скоростью повышения температуру 240°С/ч. Изменения флуоресценции, сопровождающие повышение температуры, определяли при 470 нм (длина волны возбуждения)/555 нм (длина волны флуоресцентного испускания).
Данные анализировали с использованием программы Rotor-Gene Q Series (фирма QIAGEN) для расчета температуры, при которой наблюдается переход флуоресценции, и эту температуру принимали за Тт.
Приведенный для справки пример 8А Определение ЕСМ-связывающей способности
Определение осуществляли согласно методу, описанному в WO 2012/093704. В целом, метод состоял в следующем: BD-Matrigel (фирма BD Biosciences, №356237) получали в концентрации 2 мг/мл с использованием TBS (фирма Takara, №Т903) и переносили в 96-луночный планшет для измерения (фирма Meso Scale Discovery, № L15XB-3(High Bind, высокая способность связываться)) из расчета 5 мкл на лунку и затем давали выстояться в течение ночи в холодном месте. Затем в каждую лунку планшета вносили по 150 мкл блокирующего ECL-буфера (ЗФР, содержащий 0,05% Твин20, 0,5% БСА и 0,01% азида натрия) и давали выстояться при комнатной температуре в течение 2 ч или более.
Козий античеловеческий IgG(γ) (фирма Invitrogen, №628400) метили рутением с использованием сложного эфира NHS, меченного MSD-SULFO (фирма Meso Scale Discovery, №R91AN-2) согласно прилагаемым инструкциям. Его разводили ECL-буфером для разведения (ЗФР, содержащий 0,01% Твин20, 0,1% БСА и 0,01% азида натрия) до конечной концентрации 2 мкг/мл. Кроме того, стандартное антитело и тестируемые антитела разводили ЗФР-Т (ЗФР, содержащий 0,05% Твин20 и 0,01% азида натрия) до получения конечной концентрации 3 мкг/мл.
В 96-луночный планшет для проведения реакции (фирма Thermo scientific, Nunc №145399), последовательно добавляли 10 мкл ECL-буфера для разведения, 20 мкл стандартного антитела и тестируемого антитела (3 мкг/мл) и 30 мкл меченного рутением антитела (2 мкг/мл), и давали прореагировать в течение 1 ч при комнатной температуре при перемешивании в темноте.
Блокирующий ECL-буфер удаляли из 96-луночного планшета для измерения путем опрокидывания, добавляли 50 мкл раствора образца из 96-луночного реакционного планшета и давали выстояться в темноте при комнатной температуре в течение 1 ч. После этого удаляли раствор образца из 96-луночного планшета для измерения (измерительный планшет) путем опрокидывания и немедленно добавляли 150 мкл 2хТ-буфера (4х MSD Т-буфер для считывания (фирма Meso Scale Discovery), двукратно разведенный с помощью ECL-буфера для разведения), осуществляли измерения ECL. Для измерений использовали устройство SECTOR Imager 2400 (фирма Meso Scale Discovery).
Анализы осуществляли путем деления интенсивности флуоресценции тестируемого антитела на интенсивность флуоресценции стандартного антитела, для расчета и сравнения интенсивностей, принимая величину для стандартного антитела за 1.
Приведенный для справки пример 9. Определение способности связывать лиганд SuRe™
Способность связываться с лигандом SuRe оценивали, используя Biacore™-Т200 (GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания лиганда Mab Select SuRe (фирма GE Healthcare Japan) с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Антитело, применяемое в качестве аналита, приготавливали в концентрации 5 мкг/мл с использованием HBS-EP+. Для осуществления измерений сначала инъецировали раствор с концентрацией антитела 5 мкг/мл со скоростью потока 10 мкл/мин в течение 3 мин, затем аналит заменяли на HBS-EP+ и оценивали ответ (RU) после пропускания потока в течение 0,5 мин. После завершения измерений сенсорный чип регенерировали, промывая ЮмМ Gly-HCl при рН 1,5. В контрольной проточной ячейке осуществляли такой же эксперимент без ковалентного связывания лиганда с чипом, и аффинность к лиганду SuRe™ анализировали на основе различий между ответами (RU).
Последовательности, соответствующие номерам последовательностей (SEQ ID NO:), упомянутым в приведенных для справки примерах, представлены ниже в таблице.

Приведенный для справки пример 10. Получение мышей, несущих в качестве замены человеческий ген CD3
(1) Конструирование вектора с модификацией области мышиного гена Cd3 (фиг. 26А)
Применяли клон искусственной бактериальной хромосомы (ВАС), в которой была клонирована геномная область с расположенными в ней мышиными генами CD3ε, CD3δ и CD3γ. Последовательность loxP встраивали в положение, расположенное примерно на расстоянии 3,5 т.п.н. в обратном направлении относительно 5'-конца генной области, кодирующей мышиный Cd3ε в указанной ВАС, и удаляли расположенную далее в обратном положении область, оставляя участок размером примерно 3,1 т.п.н. Одновременно интродуцировали последовательность loxP в сочетании с кассетой гена, обусловливающего устойчивость к неомицину (пео), и осуществляли инсерцию путем гомологичной рекомбинации с использованием системы Red/ET (фирма GeneBridges). В этом случае отбирали из клонов Escherichia coli, растущих в дополненной канамицином среде, клоны, для которых полимеразная цепная реакция (ПЦР-метод) приводила к правильной амплификации. Затем последовательность loxP и последовательности Rox помещали на 3'-конец в прямом направлении относительно гена Cd3γ в ВАС. Более конкретно, последовательность loxP и последовательности Rox интродуцировали вместе с кассетой гена, обусловливающего устойчивость к гигромицину (Hyg), и инсерцию осуществляли путем гомологичной рекомбинации с использованием системы Red/ET. В этом случае из клонов Escherichia coli, растущих в дополненной гигромицицином среде, отбирали клоны, в которые, как и ожидалось, были встроены последовательность loxP и последовательности Rox, по данным ПЦР-метода. Затем, удаляли геномную область, расположенную на 3'-конце в прямом направлении относительно кассеты гена Hyg, оставляя участок размером примерно 3,4 т.п.н.
(2) Интродукция вектора с модификацией области мышиного гена Cd3 в мышиные эмбриональные стволовые клетки (ES-клетки) (фиг. 26А)
Описанный выше вектор с модификацией области мышиного гена Cd3 интродуцировали в мышиные ES-клетки (клетки, полученные из мыши линии C57B L/6N) путем электропорации и после культивирования в селективной среде с добавлением G418 получали устойчивые к лекарственному средству клоны. Указанные клоны подвергали скринингу в отношении продуктов гомологичной рекомбинации с помощью метода ПЦР. Для электропорации линеаризовали 60 мкг вектора с модификацией области мышиного гена_Cd3 с помощью NotI, или экстрагировали необработанный NotI кольцевой вектор с помощью фенола/хлороформа, осаждали этанолом и затем растворяли в ЗФР.
Применяемые для скрининга ES-клетки культивировали в 96-луночном планшете и промывали дважды, используя 200 мкл раствора ЗФР на лунку. Затем лунки обрабатывали при 55°С в течение 2 ч после добавления буфера для лизиса клеток следующего состава (5 мкл 10× LA-буфера II (LA-буфер фирмы TAKARA для Taq), 5 мкл 25 мМ MgCl2, 5 мкл 5% NP-40, 2 мкл протеиназы K (фирма TAKARA, 20 мг/мл) и 33 мкл дистиллированной воды), а затем обрабатывали при 95°С в течение 15 мин для инактивации протеиназы K, получая в результате образцы для ПЦР.
Приготавливали реакционную смесь для ПЦР, содержащую вплоть до 1 мкл образца, 2,5 мкл 10 × LA-буфера II, 2,5 мкл 25 мМ MgCl2, 4 мкл дНТФ (2,5 мМ), по 0,1 мкл каждого из праймеров (50 мкМ каждый), 0,25 мкл LA Taq (фирма TAKARA) и 14,55 мкл дистиллированной воды (в целом 25 мкл). Условия ПЦР включали предварительное нагревание при 94°С в течение 2 мин, 35 циклов амплификации при 98°С в течение 10 с и 68°С в течение 4 мин 30 с и дополнительное нагревание при 68°С в течение 5 мин.
Применяли указанные ниже праймеры. Праймеры представляли собой HygF1474, который помещали внутрь кассеты гена Hyg в качестве прямого праймера, и g4989R, который помещали в качестве обратного праймера в мышиную геномную область в прямом направлении с 3'-стороны 3'-гомологичного плеча в векторе с модификацией области мышиного гена Cd3 (см. фиг. 27). В образцах ES-клеток, в которых имела место гомологичная рекомбинация, амплифицировали полосу, соответствующую размеру примерно 4 т.п.н. HygF1474 (прямой) 5'-TATCAGAGCTTGGTTGACGG-3' (SEQ ID NO: 436); и g4989R (обратный) 5'-ACTCGTTGTGGCTTAGAAGCAGTAACAATACC-3' (SEQ ID NO: 437). Кроме того, клоны, для которых получали сигналы амплификации при использовании вышеуказанного набора праймеров, подвергали валидации с использованием другого набора праймеров. Более конкретно, e27248F помещали в качестве прямого праймера в мышиную геномную область в обратном направлении с 5'-стороны 5'-гомологичного плеча в векторе с модификацией области мышиного гена_Cd3, a Neo0635R помещали в качестве обратного праймера внутрь кассеты гена Neo. В образцах ES-клеток, в которых имела место гомологичная рекомбинация, амплифицировали полосу, соответствующую размеру примерно 4 т.п.н. e27248F (прямой) 5'-ACTGTAATCCTAGTACTTAGGAGGCTGAGG-3' (SEQ ID NO: 438); и Neo0635R (обратный) 5'-AATCCATCTTGTTCAATGGCCGATCC-3' (SEQ ID NO: 439).
(3) Конструирование вектора с интродукцией области человеческого гена CD3 (фиг. 26Б)
Применяли клон ВАС, в которой была клонирована геномная область с расположенными в ней человеческими генами CD3ε, CD35 и CD3γ. Последовательность loxP встраивали в обратном направлении относительно 5'-конца генной области, кодирующей человеческий CD3ε, в указанной ВАС. Одновременно последовательность loxP интродуцировали наряду с кассетой гена Hyg и инсерцию осуществляли путем гомологичной рекомбинации с использованием системы Red/ET (фирма GeneBridges). В этом случае из клонов Escherichia coli, растущих в дополненной гигромицином среде, отбирали клоны, для которых ПЦР-метод приводил к правильной амплификации. Затем в прямом направлении относительно 3'-конца человеческого гена CD3γ в ВАС интродуцировали ген, обусловливающий устойчивость к пуромицину (Puro), фланкированный на обоих концах последовательностями Frt, в сочетании с кассетой гена Neo для помещения последовательности Rox далее в прямом направлении, и осуществляли инсерцию с помощью гомологичной рекомбинации, используя систему Red/ET. В этом случае из клонов Escherichia coli, растущих на дополненной канамицином среде, с помощью ПЦР-метода отбирали клоны, в которые, как и ожидалось, были встроены последовательности Frt, ген Puro, последовательность Rox и ген Neo.
(4) Встраивание вектора с интродукцией области человеческого гена CD3 и вектора для экспрессии рекомбиназ в мышиные ES-клетки с модифицированной областью гена Cd3
Вектор с интродукцией области человеческого гена CD3, вектор для экспрессии рекомбиназы Cre и вектор для экспрессии рекомбиназы Dre интродуцировали путем электропорации в клоны ES-клеток (1D4, 5Н1, 615 и 3А5), в которые на описанной выше стадии были правильно встроены последовательности loxP и последовательности Rox в требуемые области в область гена Cd3; и после культивирования в селективной среде с пуромицином осуществляли генотипирование выросших клонов ES-клеток.
Сначала осуществляли ПЦР-скрининг для отбора клонов, в которых имела место рекомбинация между последовательностями loxP и последовательностями Rox в области мышиного гена Cd3 под воздействием Cre и Dre, и удаляли геномную область от Cd3ε до Cd3γ. Применяемые для скрининга ES-клетки культивировали в 96-луночном планшете, промывали дважды, используя по 200 мкл раствора ЗФР на лунку, затем лунки обрабатывали при 55°С в течение 2 ч после добавления буфера для лизиса клеток следующего состава (5 мкл 10 × LA-буфера II (LA-буфер фирмы TAKARA для Taq), 5 мкл 25 мМ MgCl2, 5 мкл 5% NP-40, 2 мкл протеиназы K (фирма TAKARA, 20 мг/мл) и 33 мкл дистиллированной воды), а затем обрабатывали при 95°С в течение 15 мин для инактивации протеиназы K, получая в результате образцы для ПЦР.
Готовили реакционную смесь для ПЦР, содержащую вплоть до 1 мкл образца, 2,5 мкл 10 × LA-буфера II, 2,5 мкл 25 мМ MgCl2, 4 мкл дНТФ (2,5 мМ), по 0,1 мкл каждого из праймеров (50 мкМ каждый), 0,25 мкл LA Taq (фирма TAKARA) и 14,55 мкл дистиллированной воды (в целом 25 мкл). Условия ПЦР включали предварительное нагревание при 94°С в течение 2 мин, 35 циклов амплификации при 98°С в течение 10 с и 68°С в течение 4 мин 30 с и дополнительное нагревание при 68°С в течение 5 мин.
Применяли указанные ниже праймеры. Праймеры представляли собой e30230F, который помещали в качестве прямого праймера в геномную область в обратном направлении с 5'-стороны мышиного гена Cd3ε, и g1439R, который помещали в качестве обратного праймера в геномную область в прямом направлении с 3'-стороны мышиного гена Cd3γ (см. фиг. 28А). В образцах ES-клеток, из которых удаляли область гена Cd3, амплифицировали полосу, соответствующую размеру примерно 0,7 т.п.н. e30230F (прямой) 5'-TAGCAGCCTTCAGATGAAGAGGTAGGACTC-3' (SEQ ID NO: 440); и g1439R (обратный) 5'-TTGATGTGCCACCTCACTGCTGCACTGG-3' (SEQ ID NO: 441).
Осуществляли ПЦР-скрининг для отбора клонов, в которые интродуцирована область человеческого гена CD3, из клонов ES-клеток с дефицитом в области мышиного гена Cd3. Скринингу подвергали ПЦР-образцы, которые использовали для детекции делеции области мышиного гена Cd3. Готовили реакционную смесь для ПЦР, содержащую вплоть до 1 мкл образца, 2,5 мкл 10 × LA-буфера II, 2,5 мкл 25 мМ MgCl2, 4 мкл дНТФ (2,5 мМ), по 0,1 мкл каждого из праймеров (50 мкМ каждый), 0,25 мкл LA Taq (фирма TAKARA) и 14,55 мкл дистиллированной воды (в целом 25 мкл). Условия ПЦР включали предварительное нагревание при 94°С в течение 2 мин, 35 циклов амплификации при 94°С в течение 30 с, 58°С в течение 1 мин и 72°С в течение 5 мин и дополнительное нагревание при 72°С в течение 5 мин. Применяли указанные ниже праймеры. Праймеры представляли собой hCD3ε_5arm_F2, который помещали в качестве прямого праймера в геномную область в обратном направлении с 5'-стороны человеческого гена CD3ε, и hCD3ε_ex2_R2, который помещали в качестве обратного праймера внутрь второго экзона человеческого гена CD3ε (см. фиг. 28Б). В образцах ES-клеток, в которые интродуцировали область человеческого гена CD3, амплифицировали полосу, соответствующую размеру примерно 5,5 т.п.н. hCD3ε_5arm_F2 (прямой) 5'-AACTGACAATGGGACATCAGCTGA-3' (SEQ ID NO: 442); и hCD3ε_ex2_R2 (обратный) 5'-ATGGGACTGTTACTTTACTAAGAT-3' (SEQ ID NO: 443).
(5) Получение мышей с дефицитом мышиного гена Cd3 и с интродуцированным человеческим геном CD3
Полученные в результате гомологичной рекомбинации клоны ES суспендировали обработкой трипсином и промывали средой для ES-клеток. Скрещивали самок мышей линии BALB/c, которых подвергали обработке для суперовуляции путем введения 5 ME лошадиного хорионического гонадотропина (eCG) и человеческого хорионического гонадотропина (hCG) внутрибрюшинно с 48-часовыми интервалами, с самцами мышей этой же линии. День, когда у самок мышей было подтверждено наличие овуляционной пробки, принимали за день 0,5. В день беременности 3,5 в эмбрионы на стадии бластоцитов, собранные путем перфузии матки, которые применяли в качестве эмбрионов-хозяев, инъецировали 10-15 ES-клеток. После инъекции эмбрионы переносили в матку самок-реципиентов линии ICR в день 2,5 ложной беременности и через 17 дней получали их потомство. Скрининг на основе цвета шерстяного покрова потомства, полученного путем инъекции ES-клеток в бластоциты, позволял выявлять химерных мышей, имеющих смесь рекомбинантных ES-клеток (черные) и клеток из бластоцитов хозяина (белоснежные). После полового созревания самцов химерных мышей скрещивали с самками линии C57BL/6N и перенос аллеля knock-in в следующее поколение подтверждали ПЦР-методом с использованием в качестве матрицы геномной ДНК, экстрагированной из тканей мышей второго поколения. ПЦР осуществляли с помощью метода, описанного выше для скрининга ES-клеток. В результате установлено, что были получены особи, у которых обнаружен сигнал, специфический для области человеческого гена CD3 размером 5,5 т.п.н., и специфический для области с дефицитом мышиного гена Cd3 размером 0,7 т.п.н., и был подтвержден перенос аллеля области человеческого гена CD3 и аллеля с дефицитом области мышиного гена Cd3 в указанных особей. Кроме того, размножение мышей, имеющих вышеуказанный генотип, позволял получить особей мышей, у которых обнаружена гомозиготная делеция мышиного гена Cd3 и которые имеют область человеческого гена CD3, это означает, что были получены мыши, несущие в качестве замены область человеческого гена CD3. Трансгенных мышей с интродуцированным только человеческим CD3ε (обозначены далее в контексте настоящего описания как hCD3εTg-мыши) получали согласно методу, описанному у Wang с соавторами (Wang и др., PNAS. 91, 1994, ее. 9402-9406) и их изучали для сравнения в представленных ниже экспериментах.
(6) Масса тимусов и масса селезенок у мышей, несущих в качестве замены человеческий ген CD3
Из мышей получали селезенки и тимусы (12-14-недельные самцы) и определяли массу тканей. Как продемонстрировано на фиг. 29, не обнаружены существенные аномалии в тимусах мышей, несущих в качестве ген человеческого CD3. Для анализа рассчитывали соотношение массы ткани и массы организма. Массы тела и массы тканей (селезенка и тимус) определяли у четырех самцов мышей в каждой группе и представляли в виде графиков. Рассчитывали соотношения массы ткани и массы организма для каждой особи и обозначали на графиках черной точкой, а среднее значение обозначали столбиком (фиг. 30). Касательно массы селезенок обнаружена тенденция к ее повышению у мышей с дефицитом гена Cd3 по сравнению с мышами других генотипов, но не обнаружено значимых различий. С другой стороны, касательно массы тимусов, у мышей с дефицитом Cd3 обнаружено ее снижение до одной третьей или т.п.по сравнению с мышами дикого типа. У мышей, несущих в качестве замены человеческий ген CD3, полученных путем интродукции человеческого гена CD3 в мышей с дефицитом гена Cd3, обнаружено восстановление массы тимусов и прежде всего у особей линии №1С3, масса тимусов восстановилась даже до уровня, эквивалентного массе тимуса у мышей дикого типа. Как описано у Wang с соавторами, у мышей линии hCD3εTg обнаружена атрофия тимусов (Wang и др., PNAS. 91, 1994, ее. 9402-9406).
(7) Подтверждение экспрессии человеческого CD3 и мышиного Cd3 в соответствующих линиях мышей, несущих в качестве замены ген человеческого CD3
- Подтверждение методом ОТ-ПЦР с использованием РНК гемоцитов
Экспрессию человеческого CD3ε, человеческого CD35, человеческого CD3γ, мышиного Cd3ε, мышиного Cd3δ и мышиного Cd3γ анализировали с помощью ОТ-ПЦР с использованием РНК гемоцитов. Применяли набор для выделения РНК Catrimox-14 (фирма TaKaRa Bio), общую РНК получали из крови, собранной из дорзальной плюсневой вены или полой вены брюшной полости. Порцию по 1 мкг каждой общей РНК применяли в качестве матрицы для синтеза кДНК путем осуществления реакций с обратной транскрипцией с использованием набора для синтеза первой цепи кДНК (Superscript III First Strand cDNA Synthesis Kit) (фирма Invitrogen) с использованием праймеров олиго-dT (20). Человеческий CD3ε, человеческий CD35, человеческий CD3γ, мышиный Cd3ε, мышиный Cd3δ и мышиный Cd3γ определяли, осуществляя ПЦР с использованием синтезированных кДНК в качестве матриц. Для определения экспрессии всех генов создавали праймеры для кодирующих белки областей. Человеческий CD3ε определяли с использованием комбинации прямого праймера E0333F (5'-AAGAAATGGGTGGTATTACACAGACACC-3' (SEQ ID NO: 444)) и обратного праймера E0912R (5'-TGGGCCAGCGGGAGGCAGTGTTCTCCAGAGG-3' (SEQ ID NO: 445)). Человеческий CD35 определяли с использованием комбинации прямого праймера D0092F (5'-TAGTTCGGTGACCTGGCTTTATCTACTGG-3' (SEQ ID NO: 446)) и обратного праймера D0685R (5'-ATGGCTGCTTCTAGAAGCCACCAGTCTCAGG-3' (SEQ ID NO: 447)). Человеческий CD3γ определяли с использованием комбинации прямого праймера G0048F (5'-TGCTCCACGCTTTTGCCGGAGGACAG-3' (SEQ ID NO: 448)) и обратного праймера G0666R (5'-TAGGAGGAGAACACCTGGACTACTC-3' (SEQ ID NO: 449)). С другой стороны, мышиный Cd3ε определяли с использованием комбинации прямого праймера e0065F (5'-AGCATTCTGAGAGGATGCGGTGGAACAC-3' (SEQ ID NO: 450)) и обратного праймера e0699R (5'-TGCTCGGAGGGCTGGATCTGGGTCCACAG-3' (SEQ ID NO: 451)). Мышиный Cd38 определяли с использованием комбинации прямого праймера d055F (5'-TCATCCTGTGGCTTGCCTCTATTTGTTGC-3' (SEQ ID NO: 452)) и обратного праймера d651R (5'-TTGCTATGGCACTTTGAGAAACCTCCATC-3' (SEQ ID NO: 453)). Мышиный Cd3γ определяли с использованием комбинации прямого праймера g080F (5'-AATACTTCTACTGGAGAAGCAAAGAG-3' (SEQ ID NO: 454)) и обратного праймера g316R (5'-TAGTTGCATTTAGAGGACTTATTATGC-3' (SEQ ID NO: 455)).
Приготавливали раствор (в целом 25 мкл) реакционной смеси для ПЦР, содержащий вплоть до 1 мкл образца, 2,5 мкл 10 × Ex-буфера, 2 мкл дНТФ (2,5 мМ), по 0,1 мкл каждого из праймеров (50 мкМ каждый), 0,25 мкл Ex Taq (фирма TAKARA) и 19,05 мкл дистиллированной воды. Условия ПЦР для человеческого CD35, человеческого CD3γ, мышиного Cd3δ и мышиного Cd3γ включали предварительное нагревание при 94°С в течение 2 мин, 35 циклов цикла амплификации при 94°С в течение 30 с, 60°С в течение 30 с и 72°С в течение 2 мин и дополнительное нагревание при 72°С в течение 5 мин. Для человеческого CD3ε и мышиного Cd3ε условия ПЦР включали предварительное нагревание при 94°С в течение 2 мин, 40 циклов цикла амплификации при 94°С в течение 30 с, при 60°С в течение 30 с и при 72°С в течение 2 мин и дополнительное нагревание при 72°С в течение 5 мин. ПЦР-праймеры создавали так, чтобы определяемые амплифицированные продукты человеческого CD3ε, человеческого CD38 и человеческого CD3γ имели длину 580 bp (пар оснований), 594 bp и 620 Ьр соответственно, а мышиного Cd3ε, мышиного Cd3δ и мышиного Cd3γ составляли 635 bp, 597 bp и 237 bp соответственно.
При анализе мышей с дефицитом гена Cd3 ПЦР-сигналы, соответствующие указанной мышиной молекуле Cd3, не обнаружены. В образцах, полученных из линий 1С3 и 8I12 среди вышеописанных мышиных линий, несущих в качестве замены человеческий ген CD3 (линии №№1С3, 3В1, 8I12 и 2А4), которые получали путем интродукции области человеческого гена CD3 в мышей с дефицитом гена Cd3, обнаружены только человеческий CD3ε, человеческий CD38 и человеческий CD3γ, но не мышиный Cd3ε, мышиный Cd3δ мышиный Cd3γ (фиг. 31). В образцах, полученных из мышей дикого типа, не обнаружены человеческий CD3ε, человеческий CD35 и человеческий CD3γ, а обнаружены мышиный Cd3ε, мышиный Cd3δ и мышиный Cd3γ (фиг. 31). Эти результаты подтвердили, что были созданы требуемые мыши, экспрессирующие человеческие CD3ε, CD35 и CD3γ вместо мышиных Cd3ε, Cd3δ и Cd3γ. Проанализированная указанная на фиг. 31 линия 4ННЗ соответствовала особи, у которой мышиный аллель Cd3 представлял собой аллель дикого типа и которой интродуцирован человеческий ген CD3, и поэтому у нее обнаружены как соответствующие человеческие молекулы CD3, так и соответствующие мышиные молекулы Cd3. Далее эту особь скрещивали с мышами с дефицитом Cd3, создавая линию с дефицитом мышиного аллеля Cd3 и экспрессирующую человеческий ген CD3.
- Анализ путем иммуногистохимического окрашивания Распределение в тканях изучали, используя антитело к CD3 в качестве первичного антитела. Окрашивание CD3 не обнаружено ни в одной из тканей из мышей с дефицитом Cd3, в то время как CD3-специфическое окрашивание, эквивалентное окрашиванию у мышей дикого типа, обнаружено у мышей, несущих в качестве замены человеческий CD3, которые получали путем интродукции человеческих генов CD3 мышам с дефицитом Cd3. Более конкретно, специфическое окрашивание обнаружено в Т-клеточной зоне в тимусе (фиг. 32А) и селезенке (фиг. 32Б). Во всех тканях окрашивание обнаружено только в Т-клеточной зоне, аналогично окрашиванию, характерному для мышей дикого типа. Кроме того, окрашивание не выявлено у мышей с дефицитом гена Cd3, что свидетельствует о том, что окрашивание тканей мышей, несущих в качестве замены человеческий ген CD3, являлось следствием экспрессии интродуцированных человеческих генов CD3. Кроме того, специфическое для CD3 окрашивание в основных органах оказалось таким же, как у дикого типа, и эктопическое окрашивание не выявлено (таблица 19).
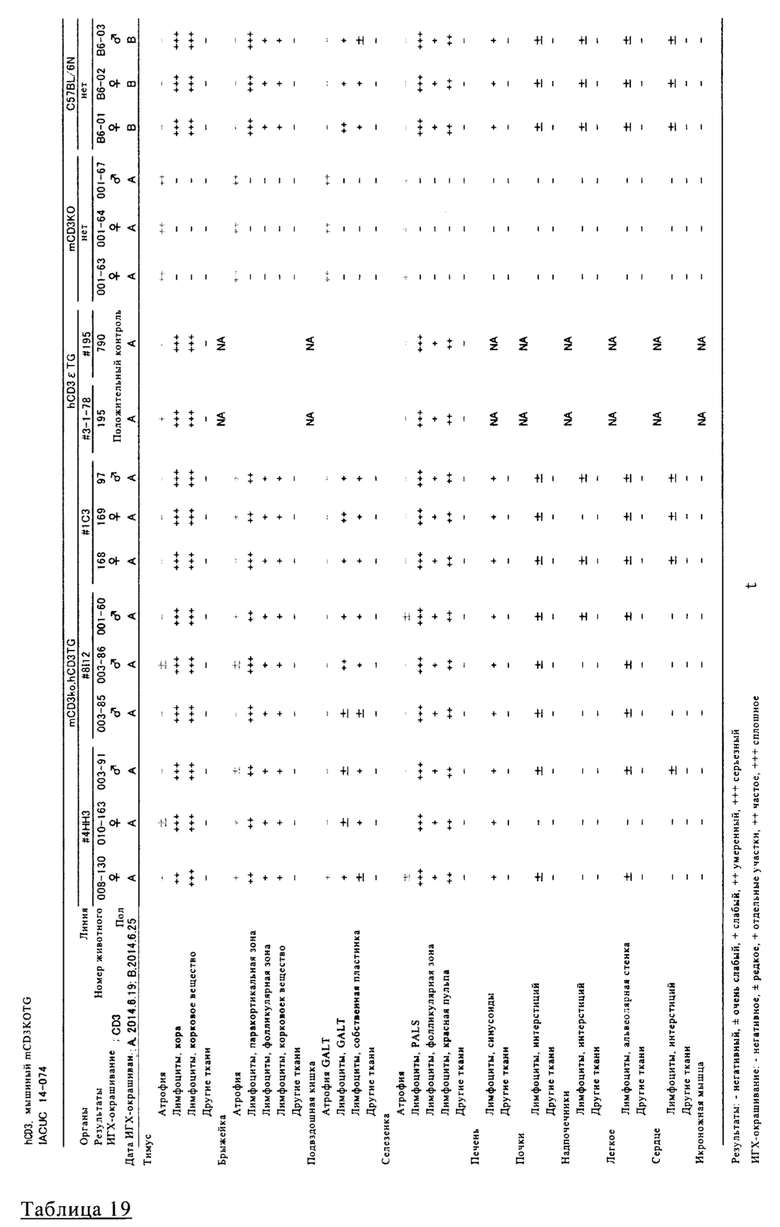
(8) Оценка относительного содержания зрелых Т-клеток в мышах, несущих в качестве замены человеческий ген CD3
Осуществляли FACS-анализы с использованием клеток селезенки. Селезенки изымали у мышей (самцы возрастом 12-14 недель) и клетки выделяли, используя сита с размером отверстий 70 мкм. Эритроциты лизировали, добавляя гемолитический агент (производства фирмы SIGMA). После блокады с помощью блокирующего Fc раствора вносили меченное с помощью ФИТЦ антитело к мышиному Cd3, меченное с помощью ФИТЦ антитело к человеческому CD3, меченное с помощью АРС антитело к мышиному Cd4 и меченное с помощью РЕ антитело к мышиному Cd8 к 2×106 клеток и анализировали количество соответствующих позитивных клеток с помощью проточного цитометра. Было установлено, что у мышей с дефицитом гена Cd3 практически полностью отсутствовали зрелые Т-клетки, т.е. Cd4-и Cd8-позитивные клетки, в то время как эти клетки присутствовали у мышей, несущих в качестве замены человеческий ген CD3 в относительном количестве, эквивалентном дикому типу.
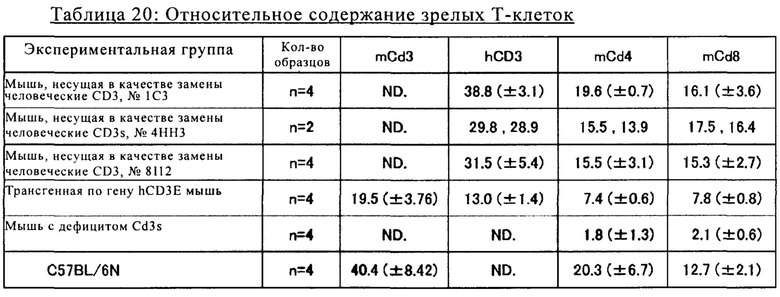
В таблице представлены уровни экспрессии соответствующих позитивных по маркеру клеток относительно количества спленоцитов (ед. %). Для каждой экспериментальной группы представлены средние значения для четырех особей за исключением мышей линии №4 НН3, несущих в качестве замены человеческие CD3, для линии №4 НН3 представлены данные об уровнях экспрессии для двух особей (в скобках дано стандартное отклонение) ND: не определяли.
Приведенный для справки пример 11. Оценка иммунной функции у мышей, несущих в качестве замены человеческий ген CD3
(1) Оценка способности продуцировать специфические антитела в ответ на иммунизацию чужеродным антигеном
Для производства специфических антител против чужеродных антигенов должны существовать функциональные хелперные Т-клетки, которые могут связываться с антигенными пептидами, присутствующими вместе с антигенами главного комплекса гистосовместимости (ГКГС) на поверхности антигенпрезентирующих клеток, таких как дендритные клетки, и Т-клетки должны обладать функциями «давать инструкции» по производству соответствующих антител антителопродуцирующим клеткам. Изучали вопрос о том, несут ли описанные выше мыши, имеющие в качестве замены человеческий ген CD3, хелперные Т-клетки, обладающие нормальными функциями и способностью продуцировать специфические антитела в ответ на иммунизацию чужеродными антигенами. Иммунизацию осуществляли, используя куриный овальбумин (OVA) в качестве сенсибилизирующего антигена в сочетании с адъювантом Фрейнда. Иммунизацию OVA осуществляли дважды с четырехнедельным интервалом. Более конкретно, первую иммунизацию осуществляли путем подкожного внесения в спинную область, используя 100 мкг OVA на животное в сочетании с полным адъювантом Фрейнда, и через 4 недели осуществляли аналогичную иммунизацию путем подкожного внесения в спинную область антигена в сочетании с неполным адъювантом Фрейнда. В качестве мышей, несущих в качестве замены человеческий ген CD3, отбирали две линии (линии №№1С3 и 8112), каждую из которых получали с использованием различных модифицированных клонов ES-клеток, и сравнивали со сверхэкспрессирующими человеческий CD3ε мышами. Кроме того, в качестве контролей использовали мышей дикого типа и мышей с дефицитом гена Cd3 и подвергали их аналогичным иммунизациям антигеном.
Через 1 неделю после второй иммунизации животных подвергали лапаротомии под анестезией изофлураном и затем умерщвляли путем сбора цельной крови и, давая крови вытекать из полой вены брюшной полости. Из собранной крови выделяли сыворотку и определяли концентрации OVA-специфических IgG1 и OVA-специфических IgE (фиг. 34).
В результате установлено, что OVA-специфические антитела ни IgG1-типа, ни IgE-типа не обнаружены в сыворотке мышей с дефицитом Cd3, однако OVA-специфические IgG1 и IgE обнаружены в обеих линиях мышей, несущих в качестве замены человеческий ген CD3, и их уровни оказались эквивалентными уровням у мышей дикого типа. Эти результаты демонстрируют, что мыши, несущие в качестве замены человеческий ген CD3, обладали нормальной способностью продуцировать антитела в ответ на иммунизацию чужеродным антигеном.
Промышленная применимость
В настоящем изобретении предложены противораковые агенты и фармацевтические композиции, предназначенные для применения в комбинации с другим противораковым агентом, агенты или композиции, содержащие новые мультиспецифические антигенсвязывающие молекулы, которые сохраняют сильную противораковую активность, свойственную BiTE, и обладают очень высокой безопасностью, что проявляется в отсутствии индукции независимого от ракового антигена цитокинового шторма и т.п., а также обладают продолжительным временем полужизни в крови. Противораковые агенты и фармацевтические композиции, которые содержат в качестве активного ингредиента антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, могут направленно воздействовать на экспрессирующие глипикан 3 клетки и опухолевые ткани, которые содержат такие клетки, и индуцировать цитотоксичность. Введение мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, пациентам позволяет осуществлять требуемое лечение, которое не только отличается высоким уровнем безопасности, но также снижает физическую нагрузку на пациентов и является очень удобным.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2015 |
|
RU2812875C1 |
| ИНДУЦИРУЮЩИЙ ЦИТОТОКСИЧНОСТЬ ТЕРАПЕВТИЧЕСКИЙ АГЕНТ | 2015 |
|
RU2743464C2 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА 3 | 2011 |
|
RU2611751C2 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА 3 | 2005 |
|
RU2427588C2 |
| ЛЕЧЕНИЕ РАКА С ПОМОЩЬЮ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА К CD33 | 2015 |
|
RU2747384C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАКА ПЕЧЕНИ | 2009 |
|
RU2523897C2 |
| АНТИТЕЛО К CLDN18.2 И ЕГО ПРИМЕНЕНИЯ | 2018 |
|
RU2797709C2 |
| Терапевтические антитела и их применения | 2016 |
|
RU2722381C2 |
| МОДИФИЦИРОВАННЫЙ ЭКЗОТОКСИН А ПСЕВДОМОНАД | 2014 |
|
RU2687143C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ ИНТЕРЛЕЙКИНУ-2 И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2745451C1 |

























































































































































































































































































































































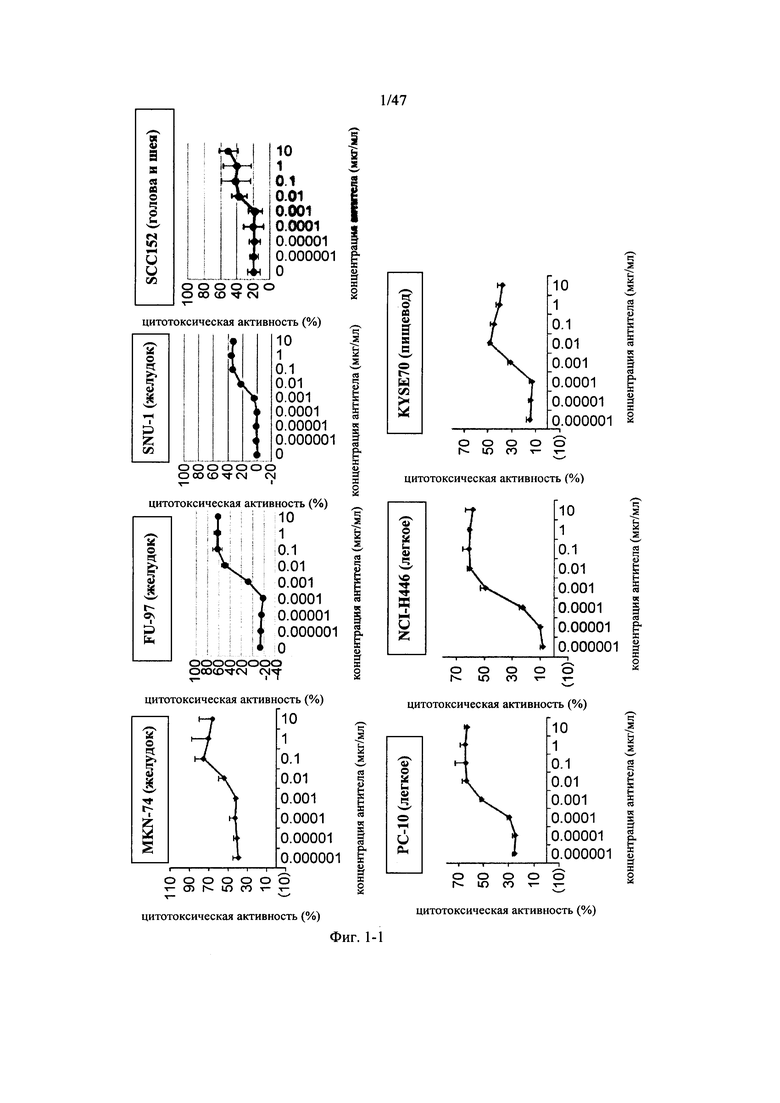
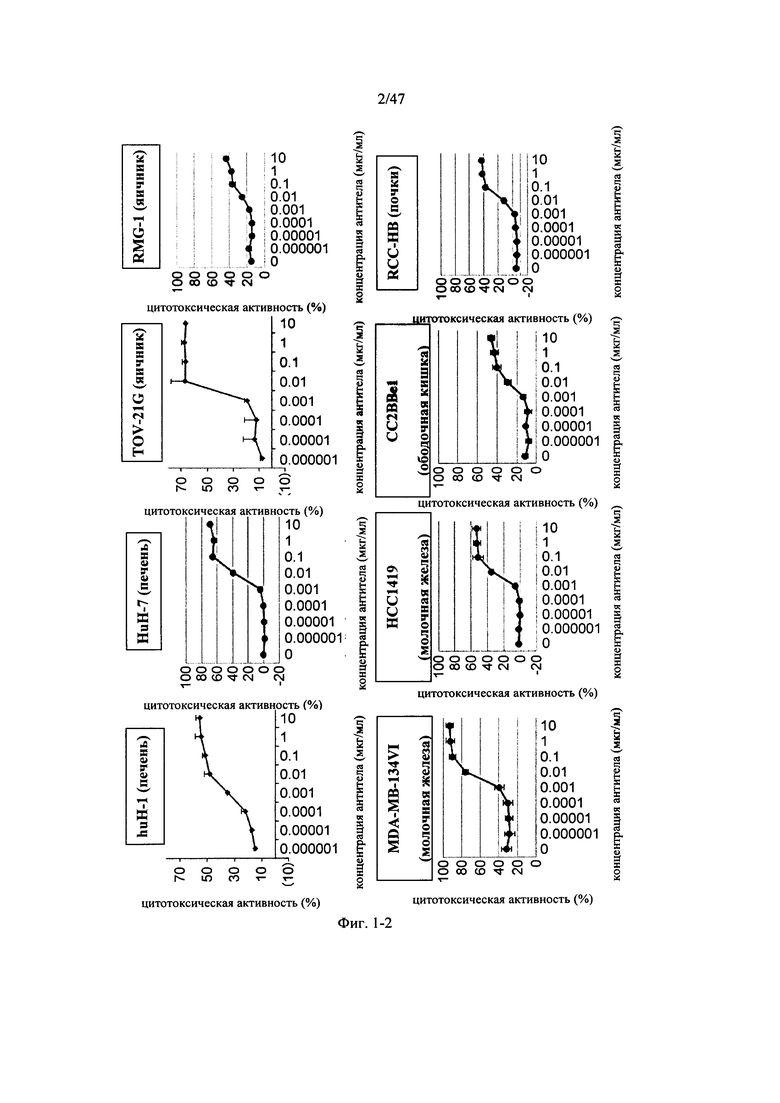

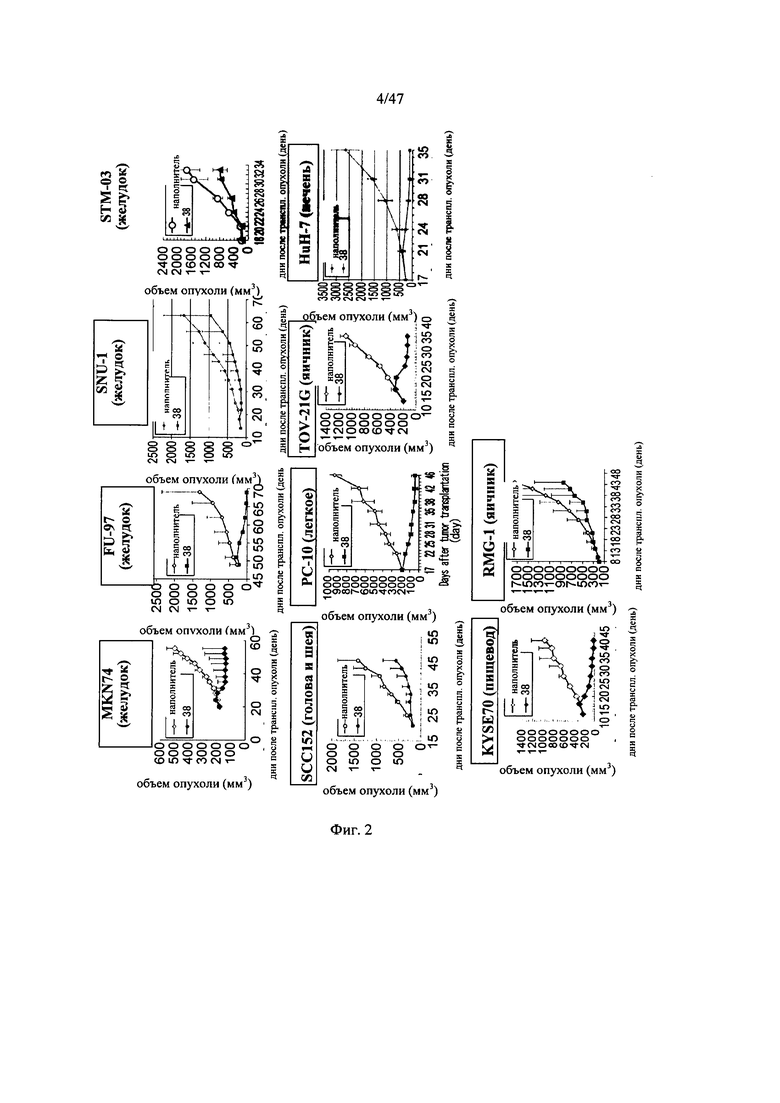



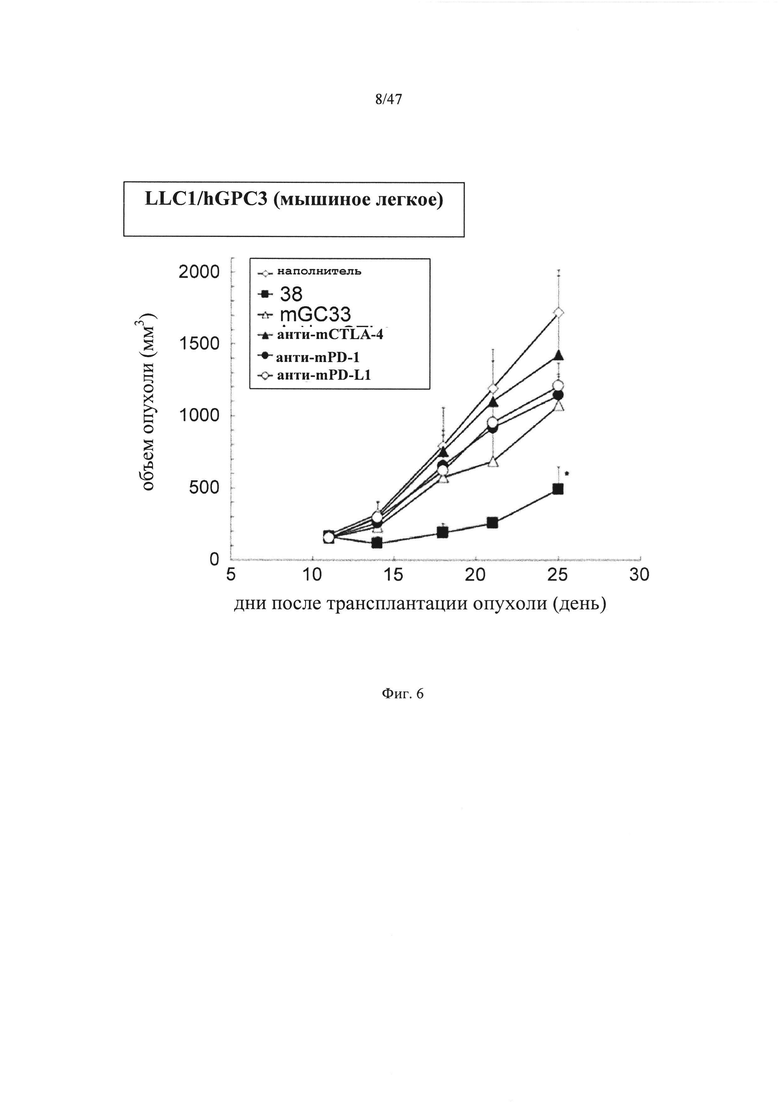
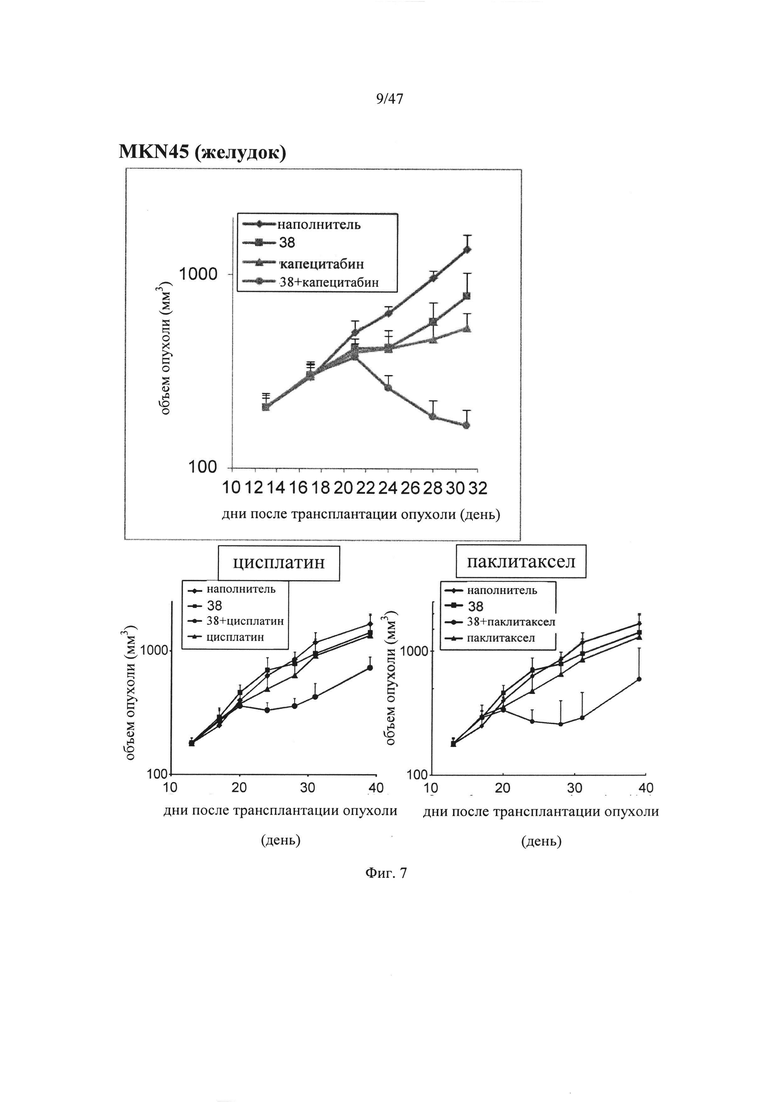
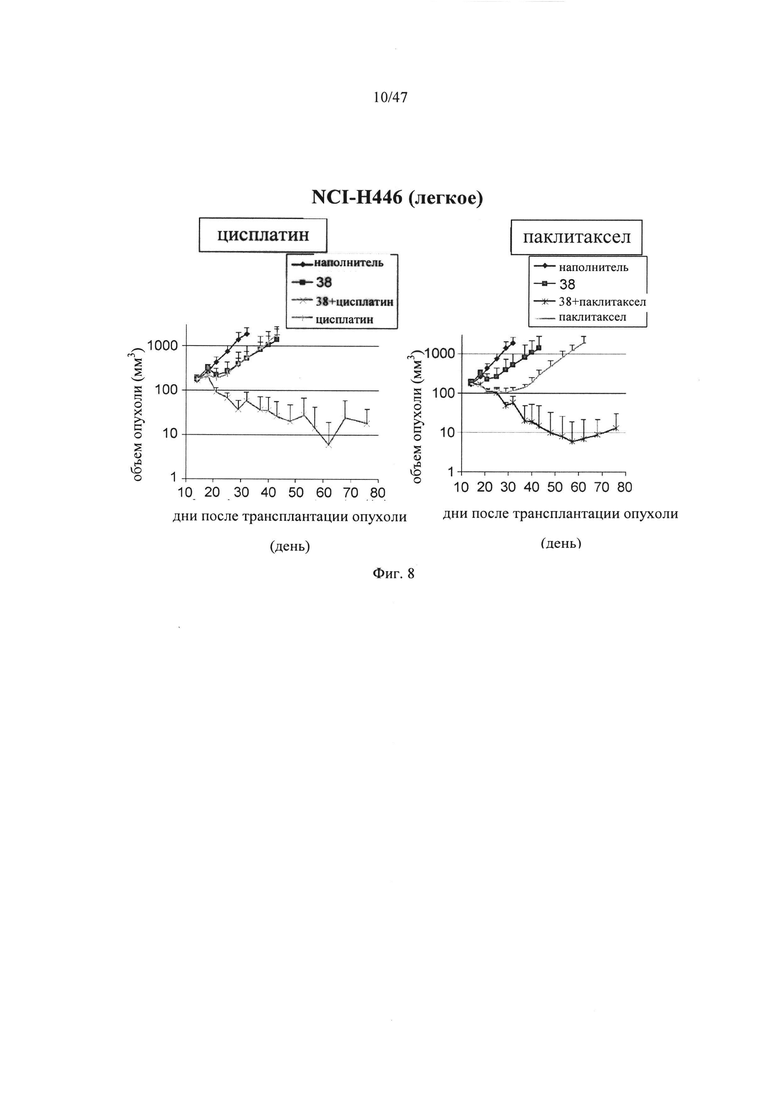
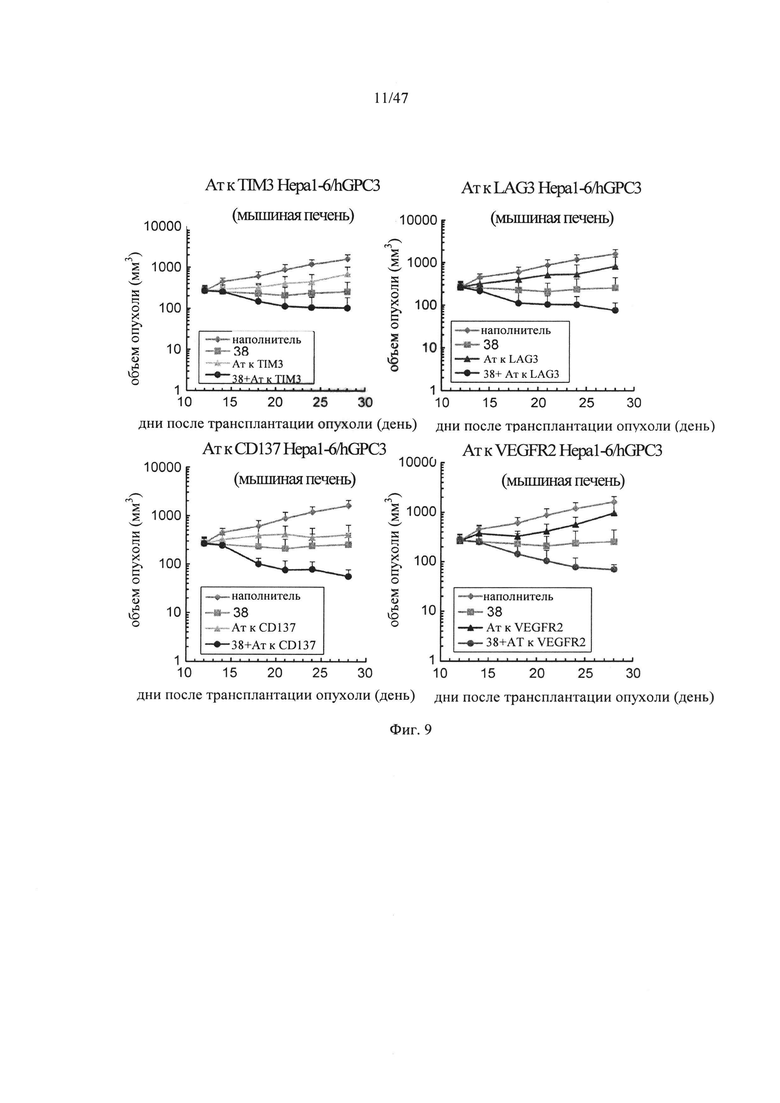
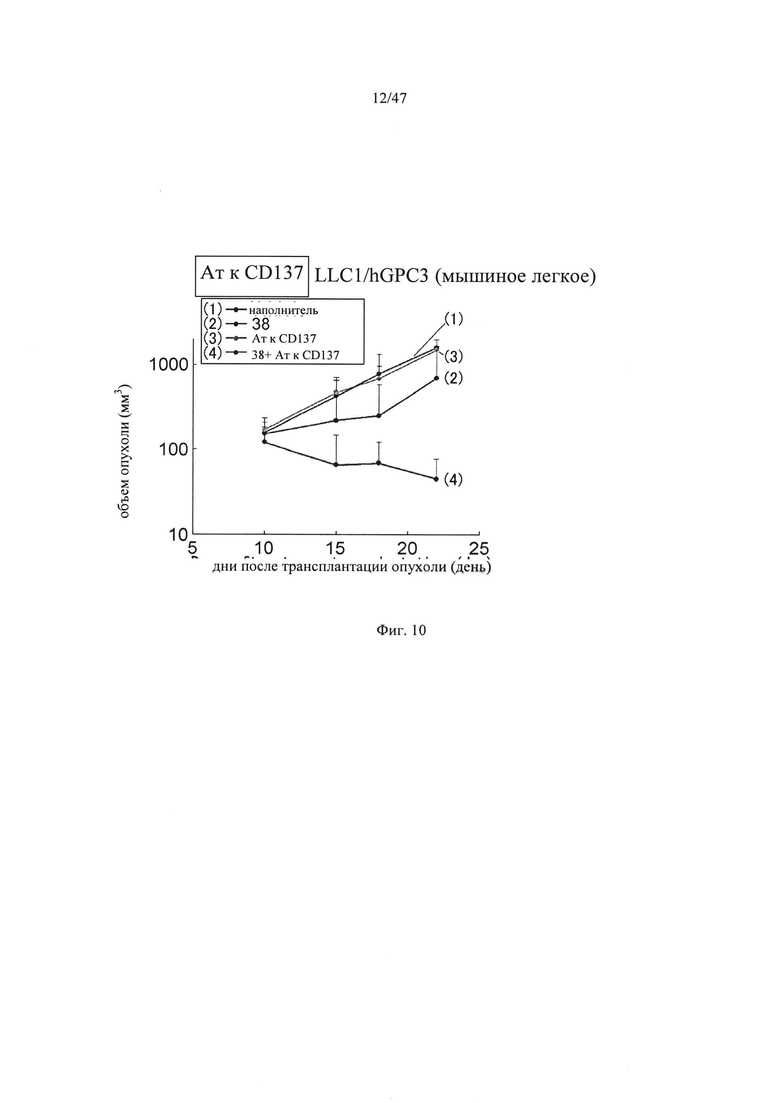



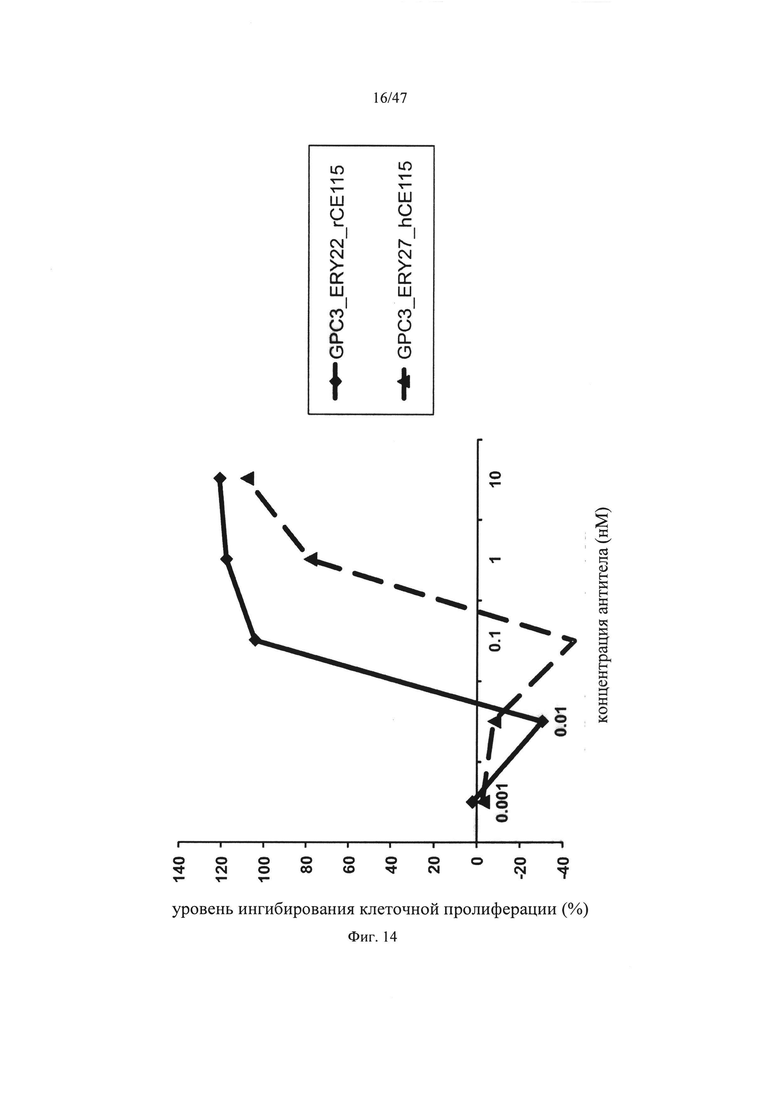

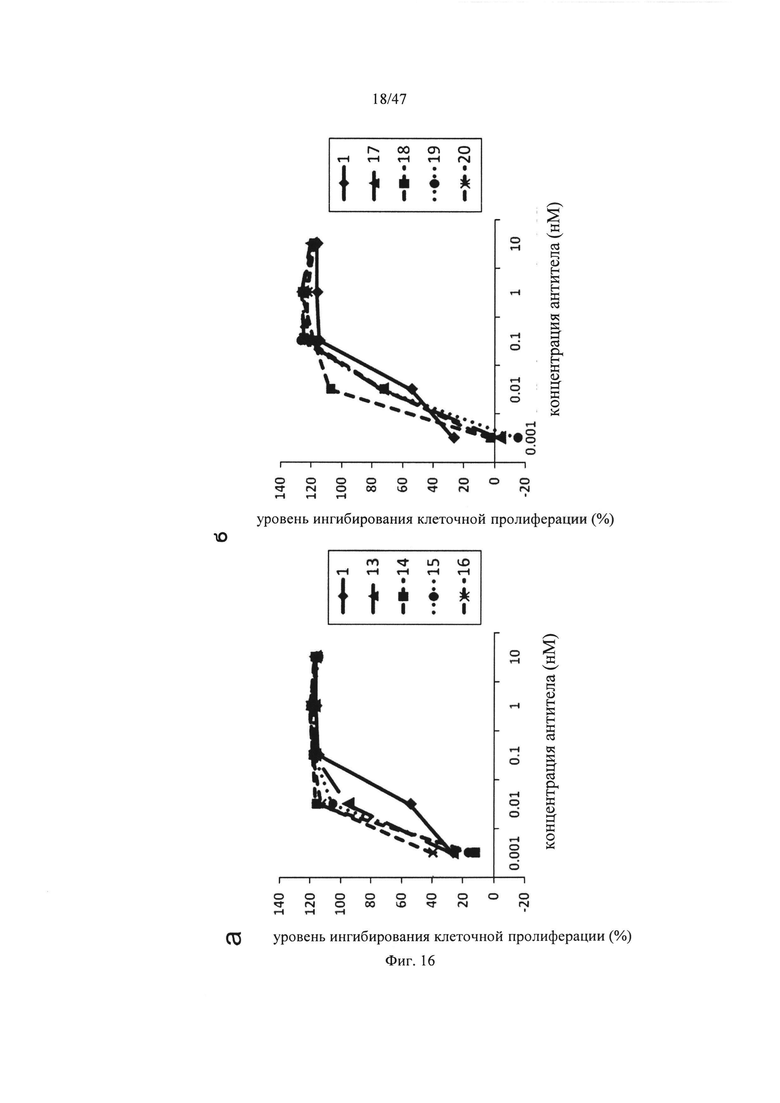

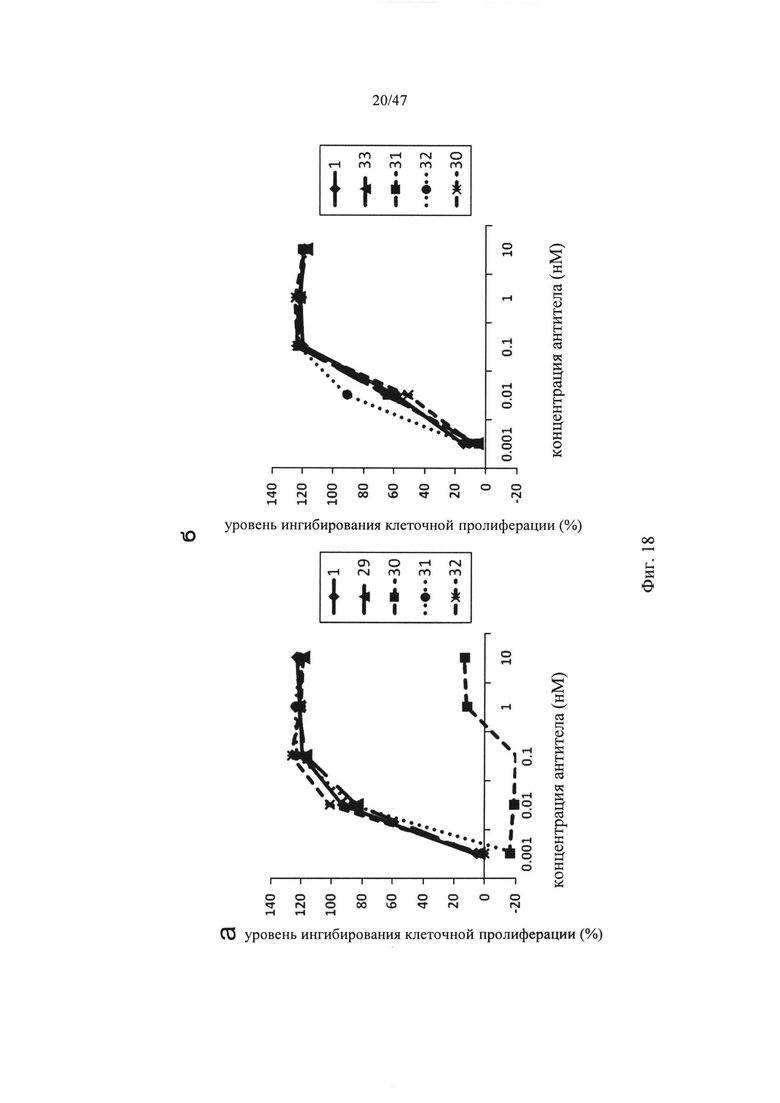
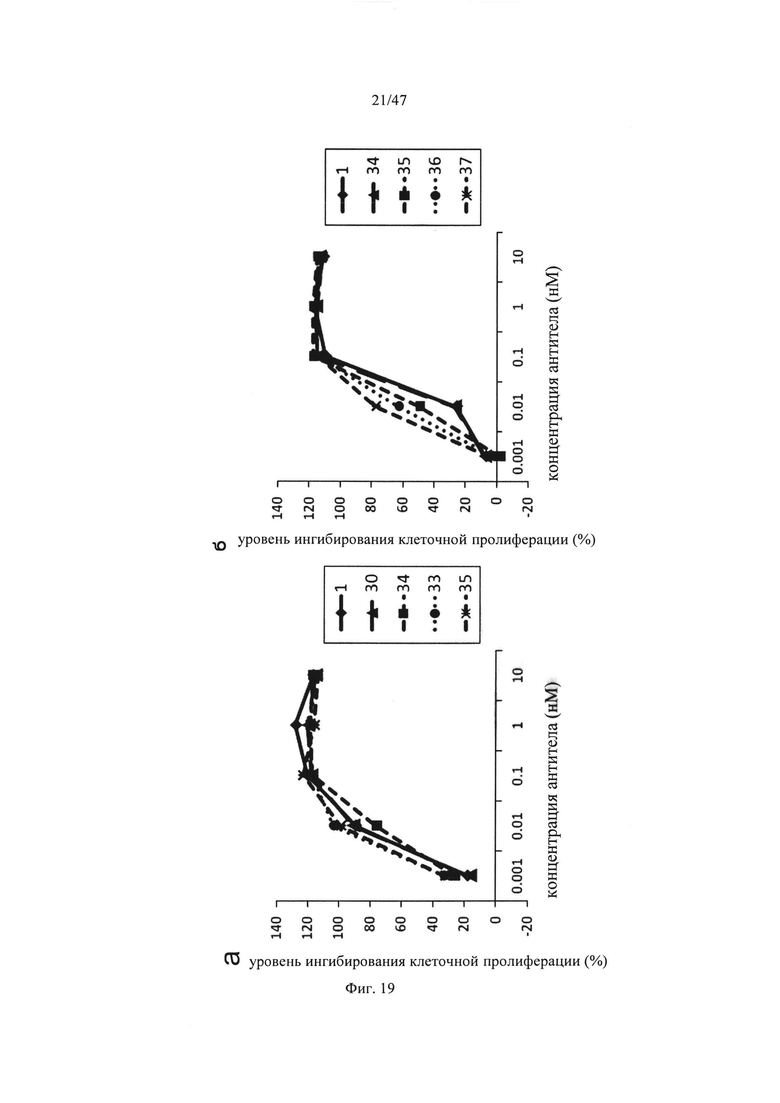
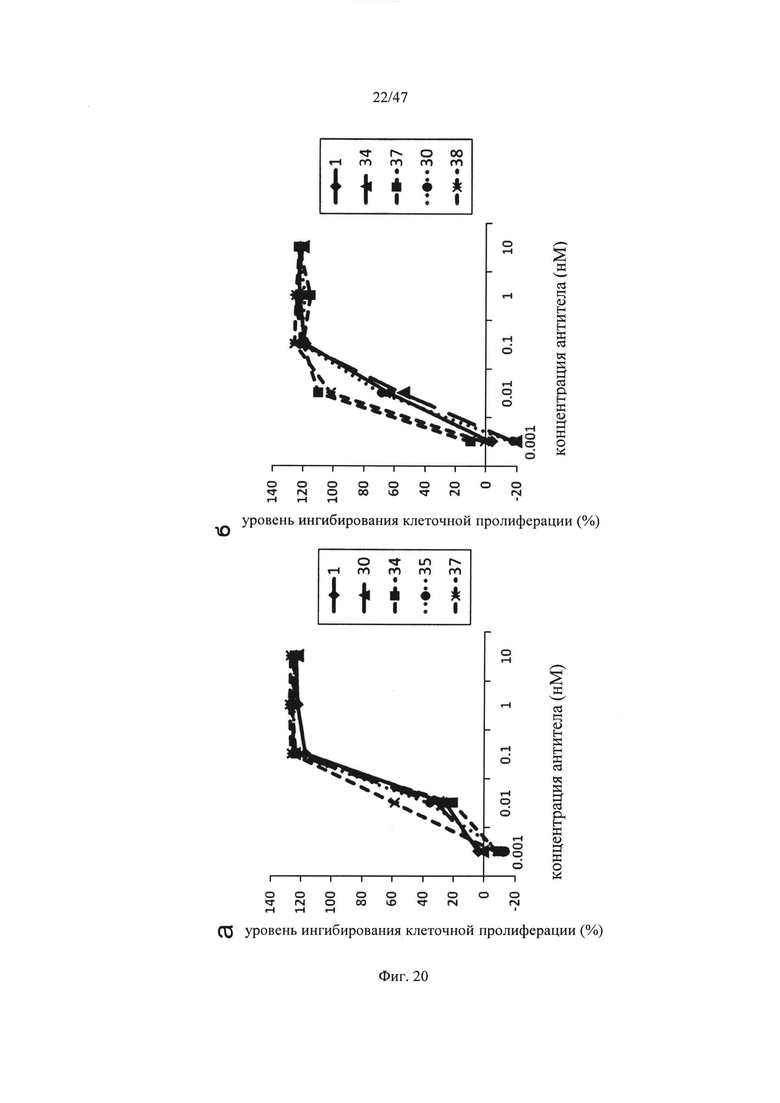
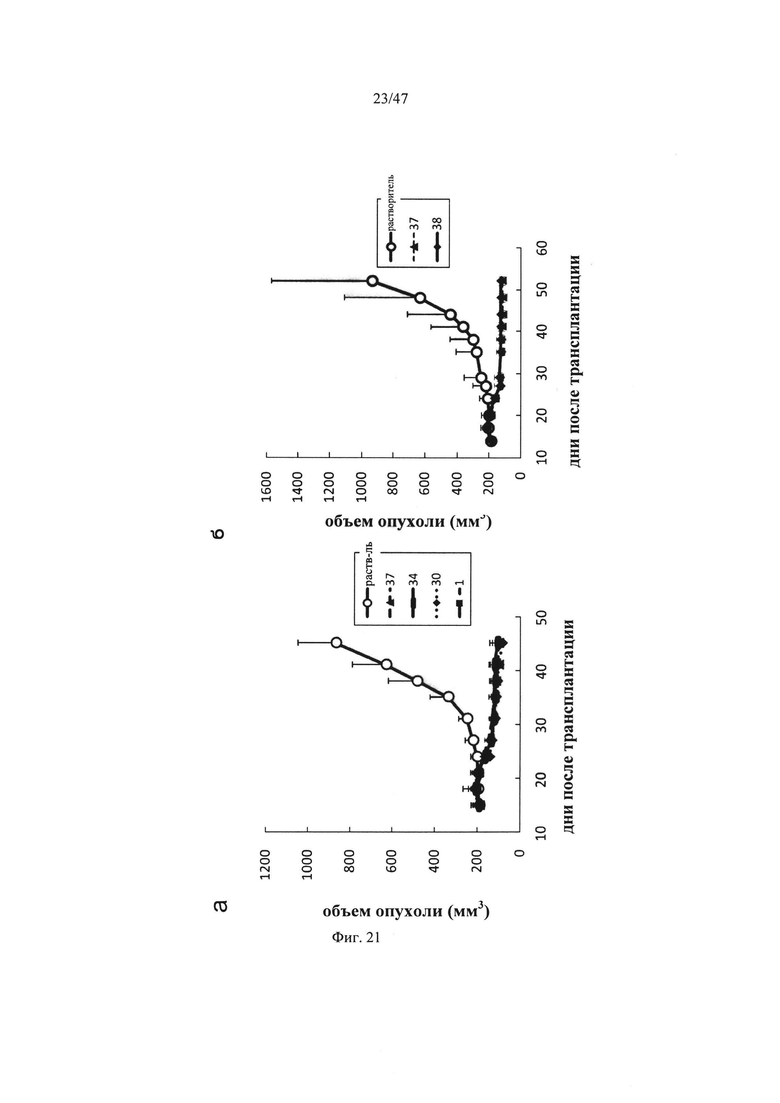
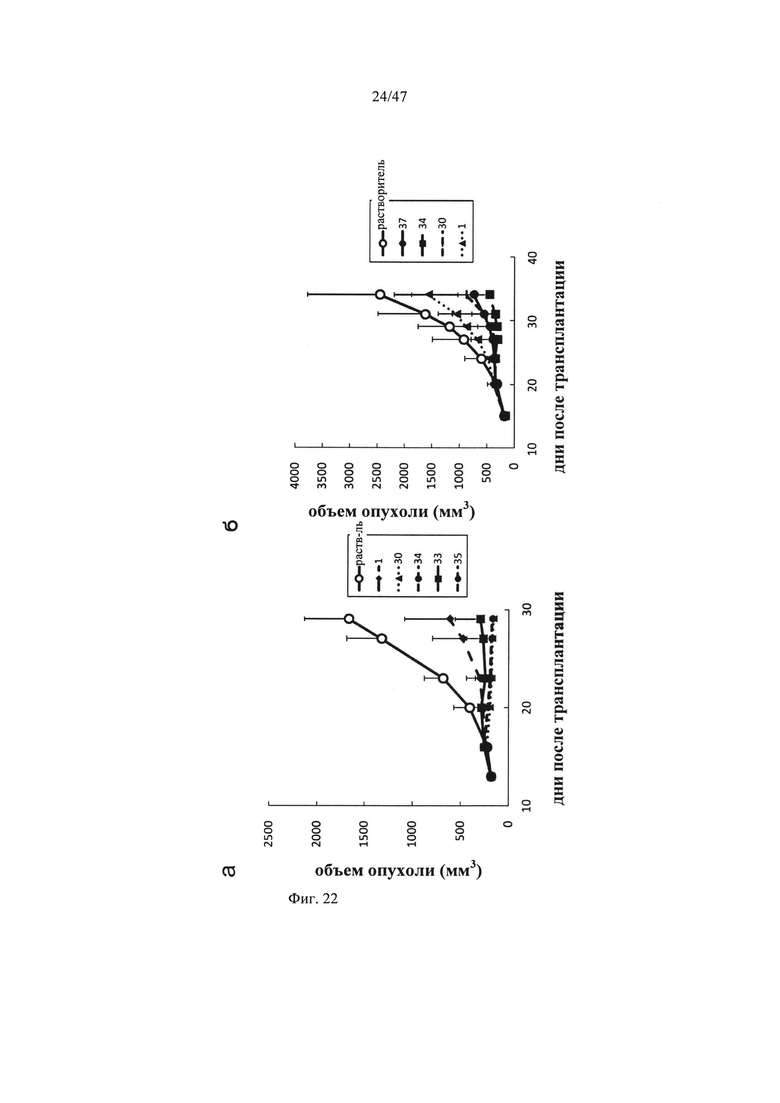
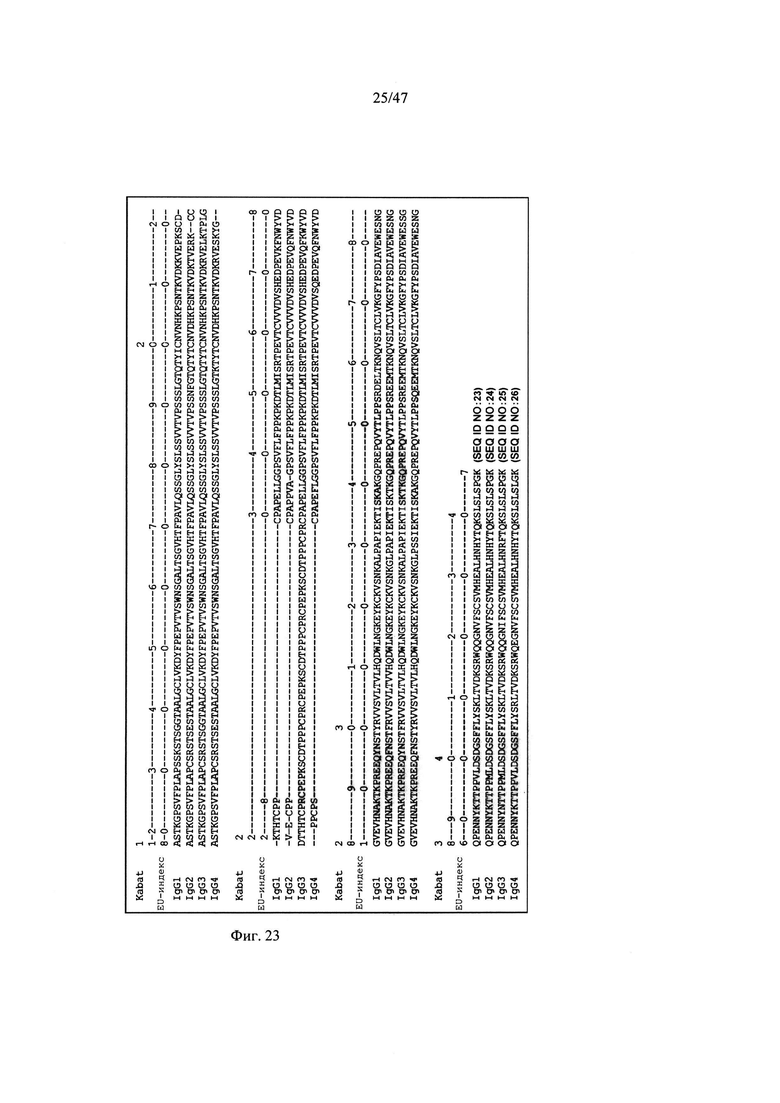

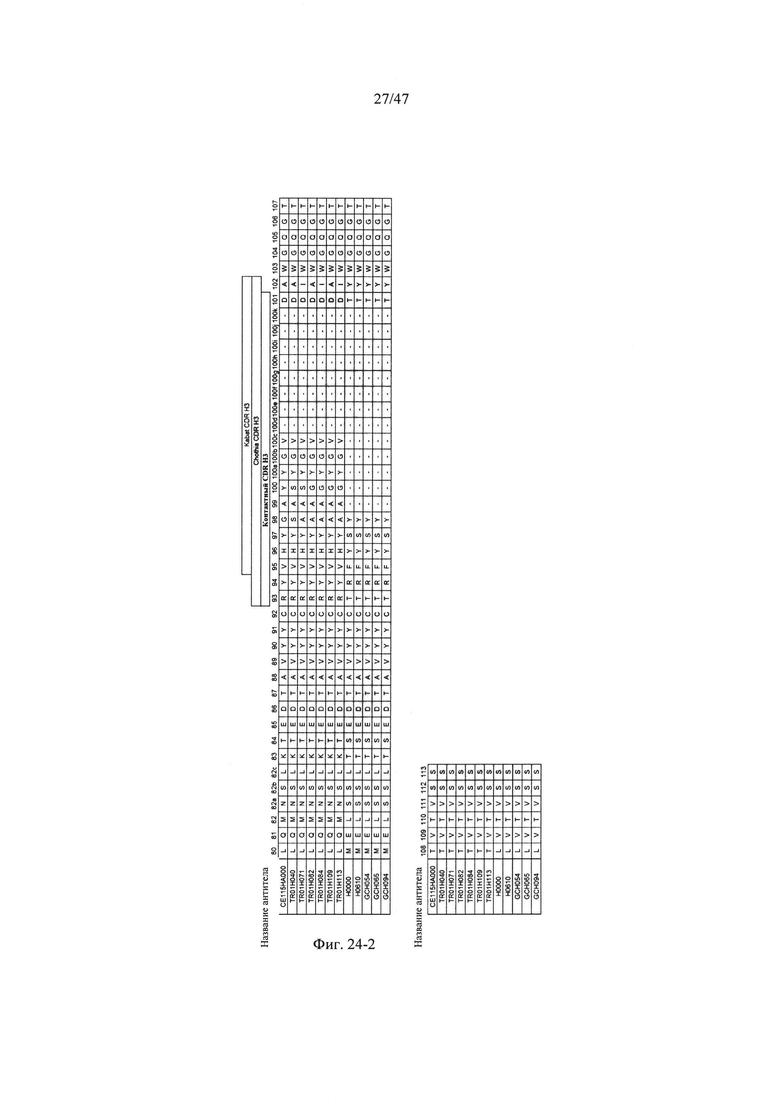
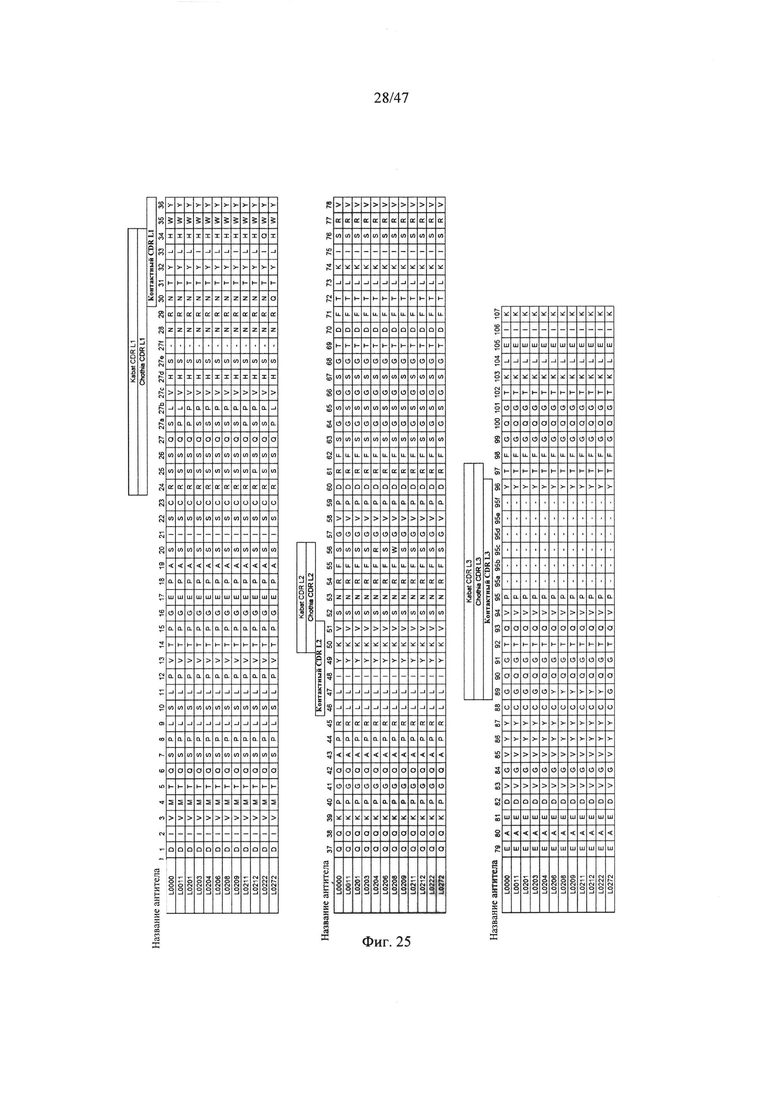
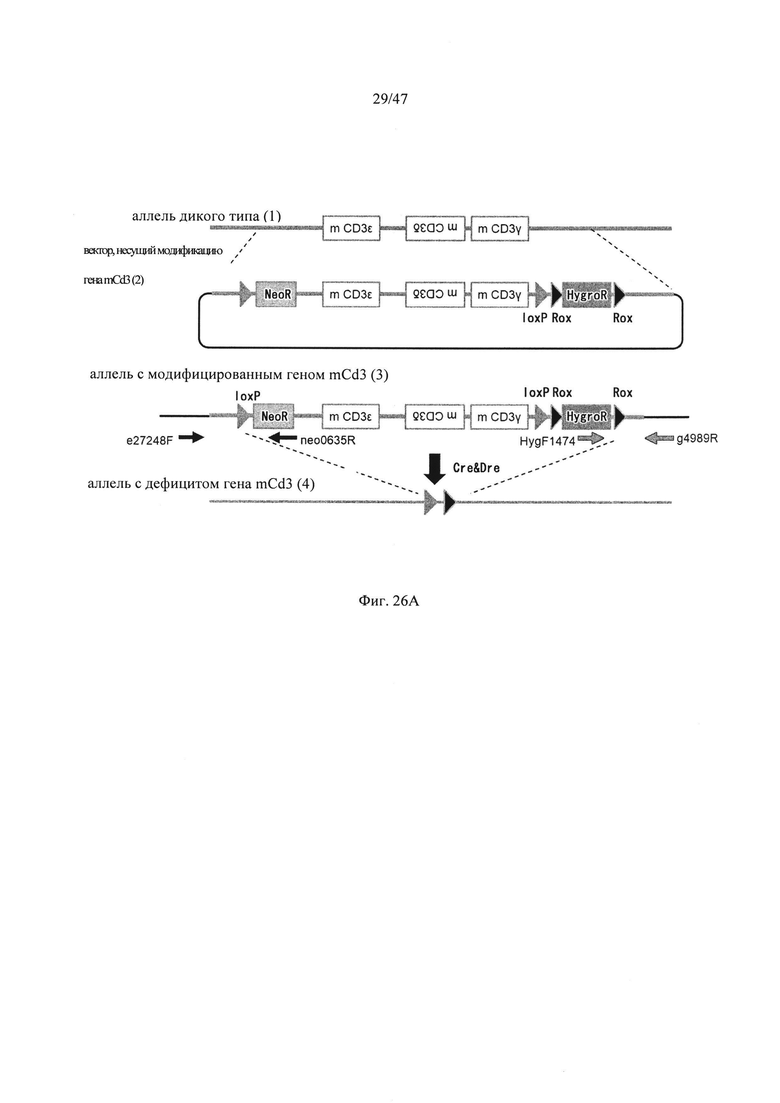

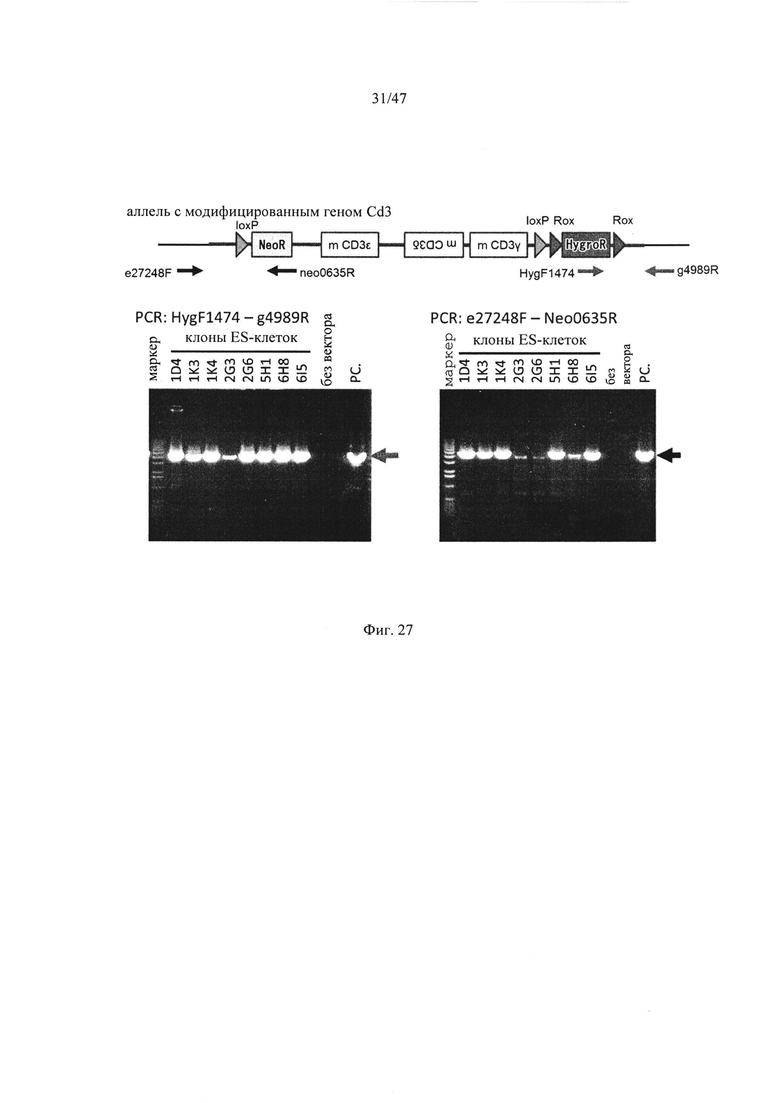

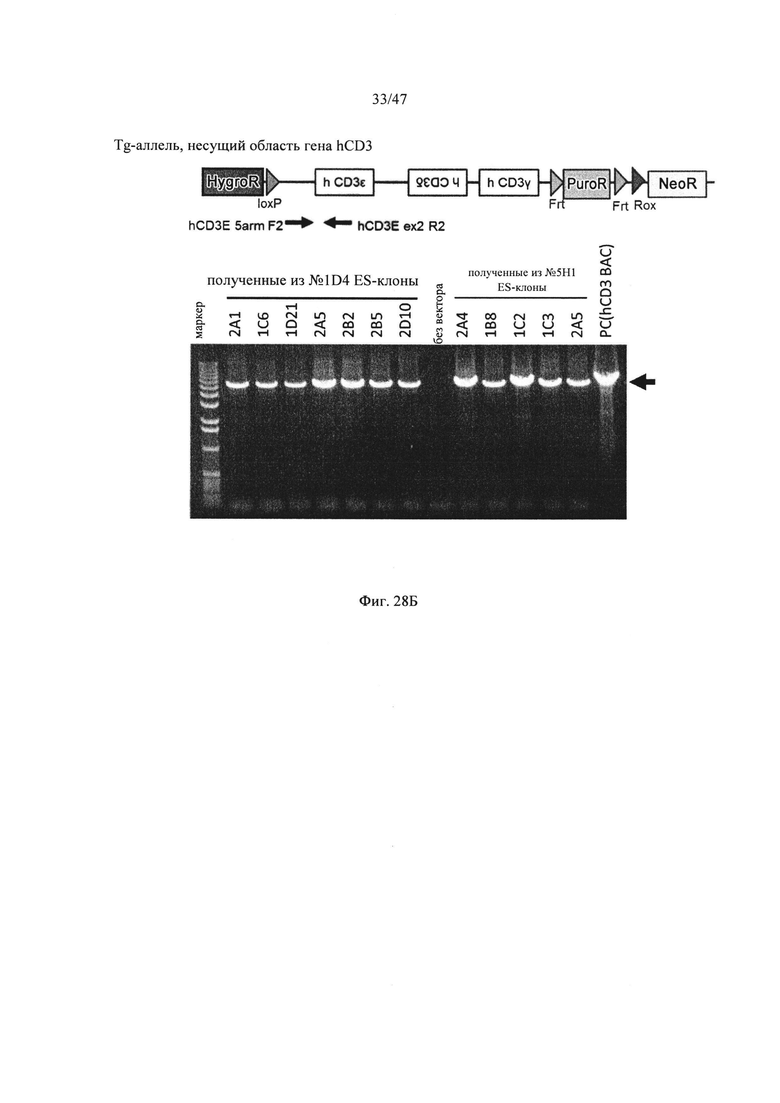

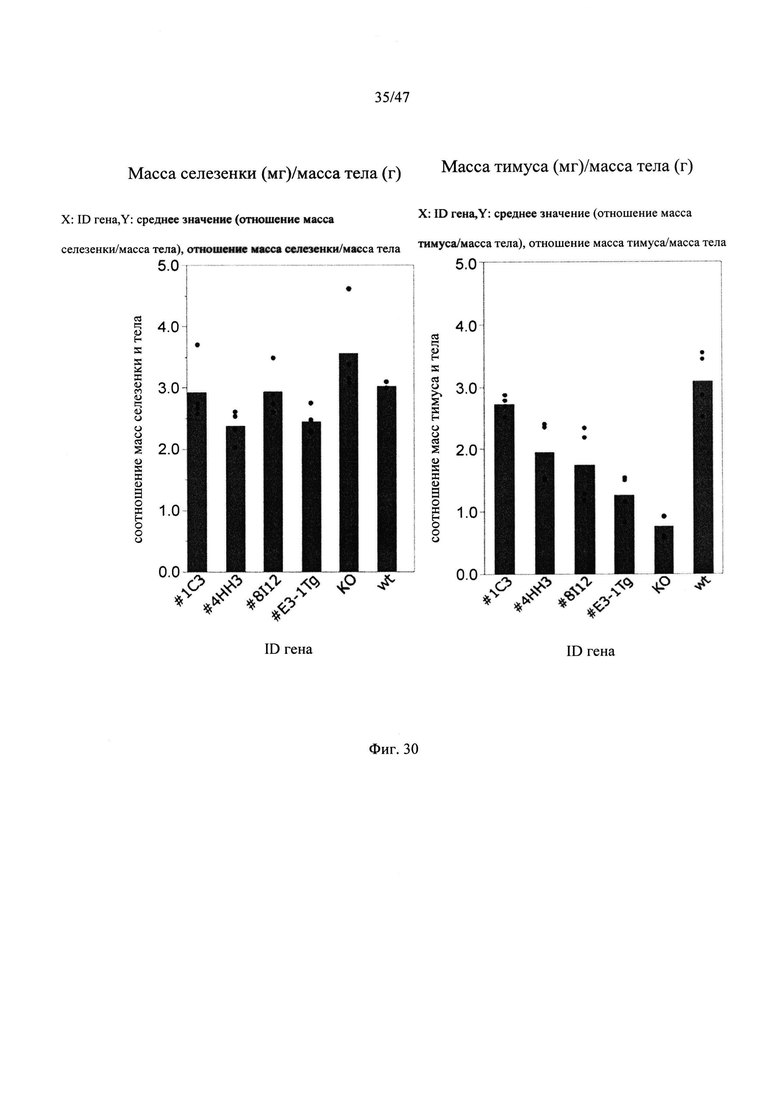
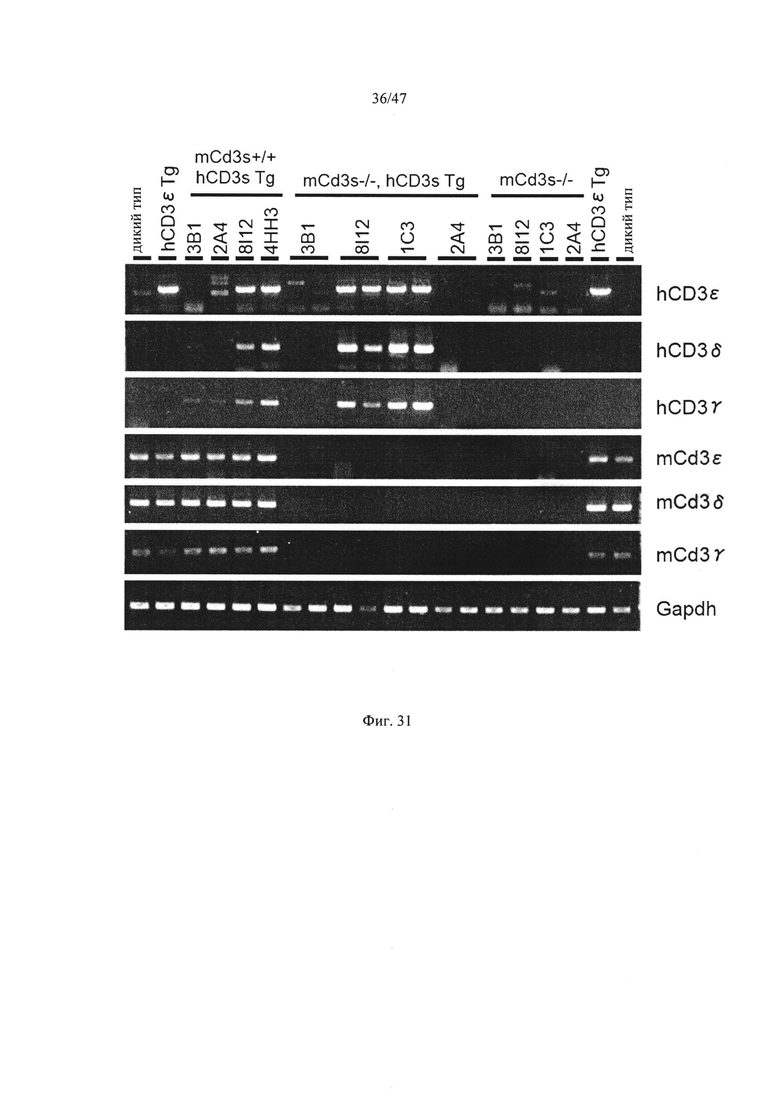
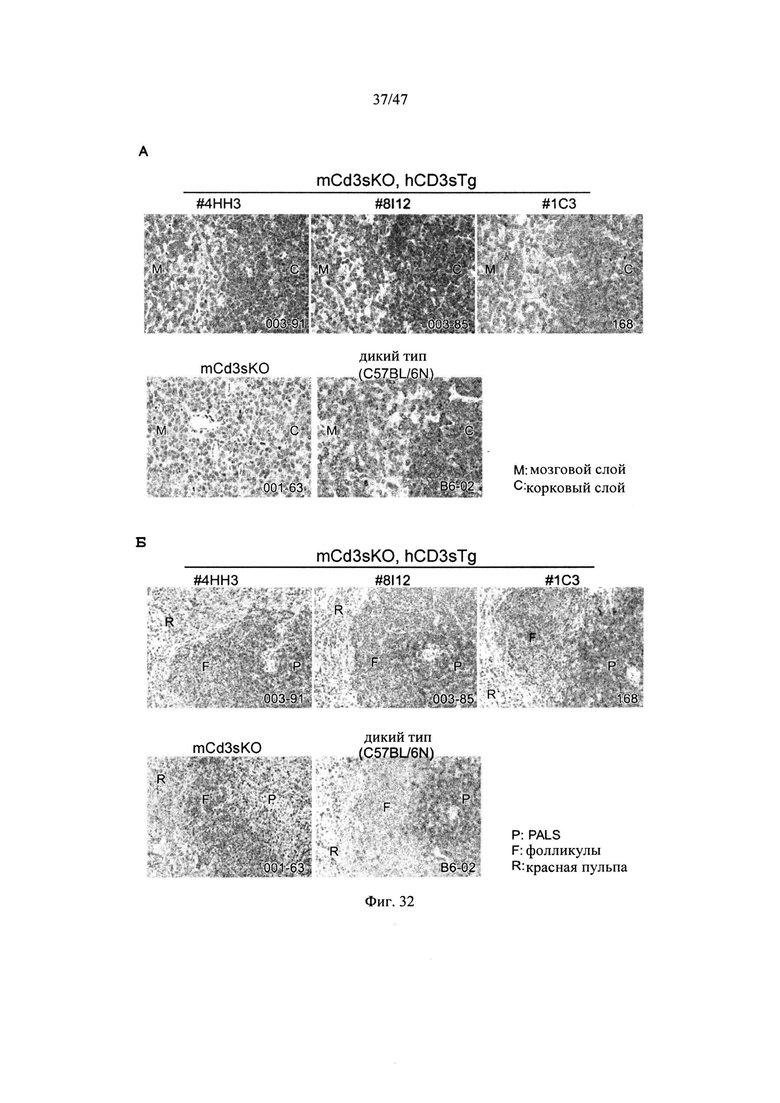




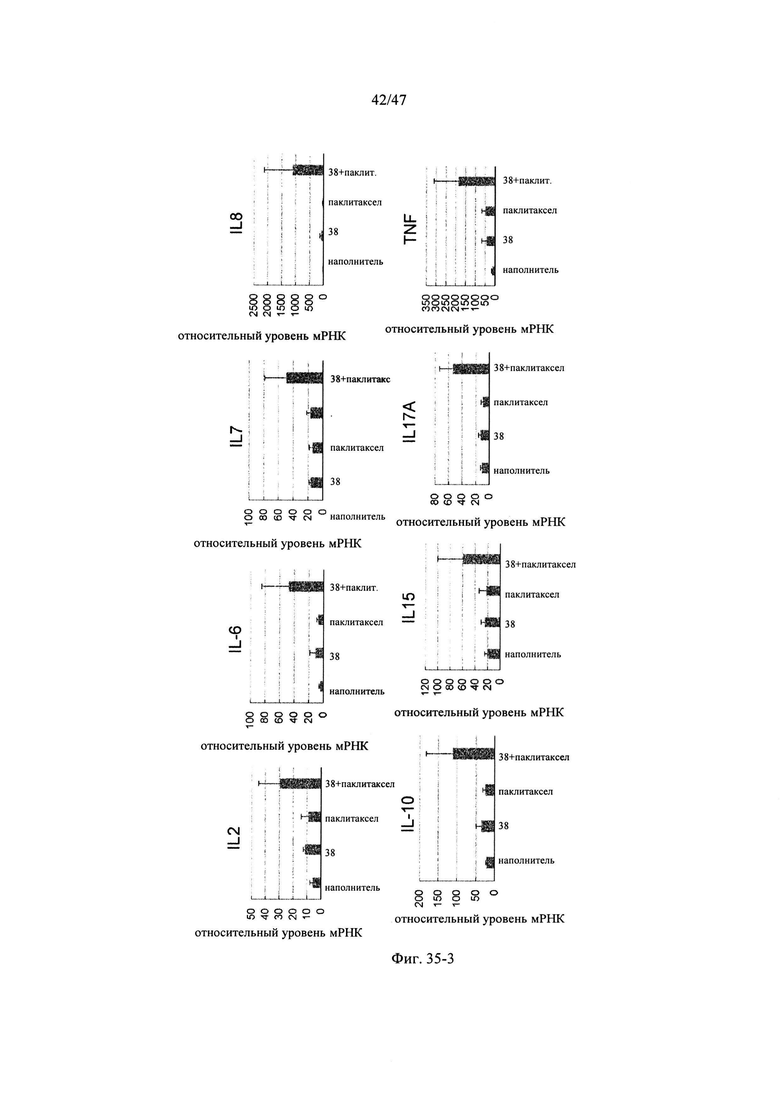
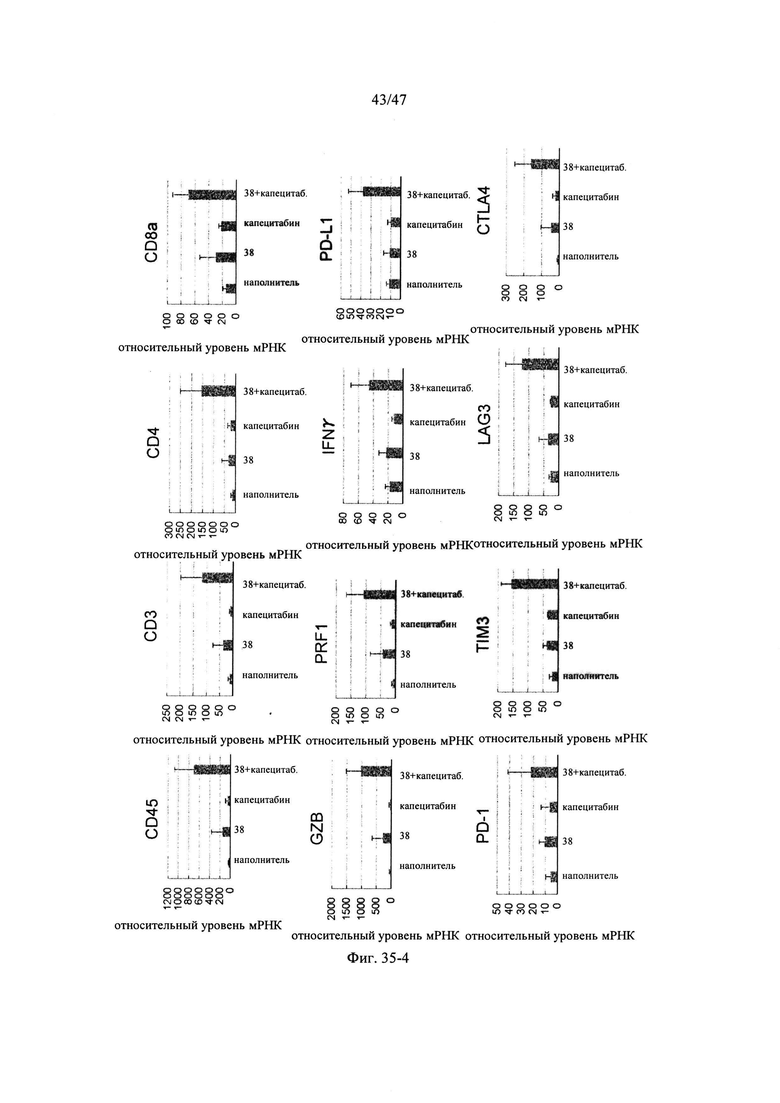


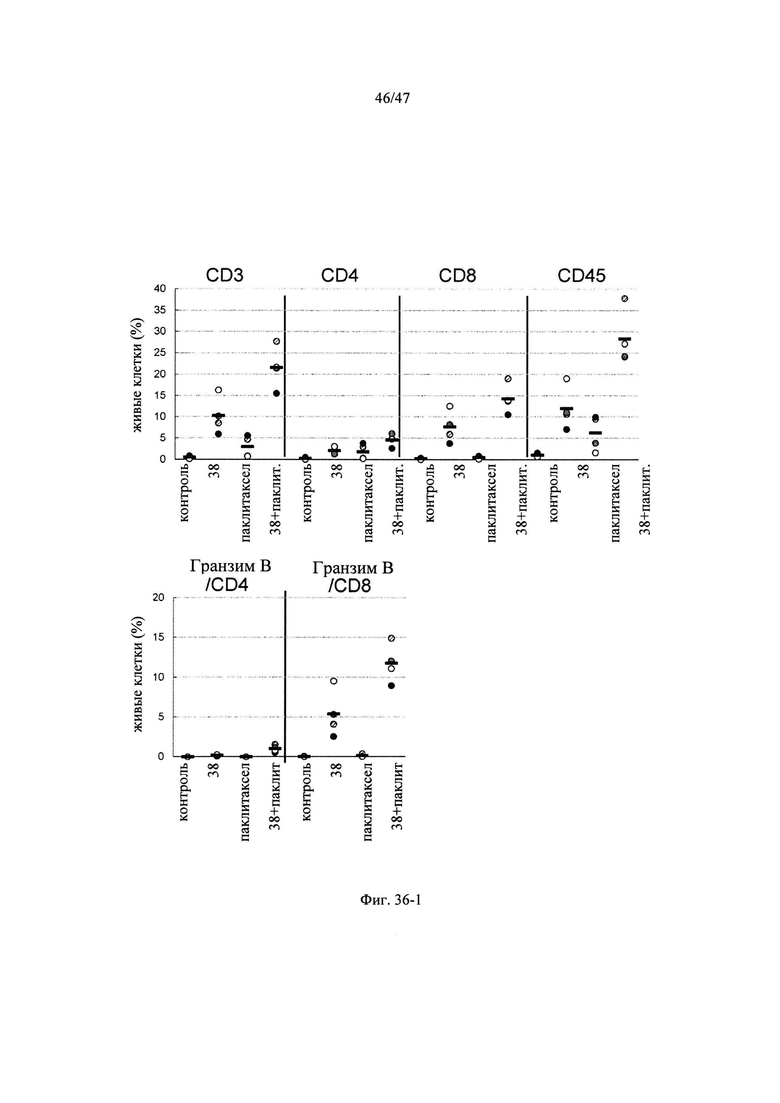

Изобретение относится к области биотехнологии. Предложен противораковый агент, содержащий в качестве активного ингредиента биспецифическое антитело. Указанное биспецифическое антитело содержит вариабельные области антитела, связывающиеся с глипиканом 3 и CD3, а также содержит одинаковые легкие цепи. Также предложена фармацевтическая композиция, которая включает указанное биспецифическое антитело в качестве активного ингредиента. Композиция предназначена для совместного применения с другим противораковым лекарственным средством. Кроме того, изобретение относится к содержащим указанную композицию агентам для индукции цитотоксичности, ингибирования клеточной пролиферации и активации иммунного ответа. Биспецифические антитела представляют собой новые и обладающие высокой безопасностью молекулы, которые характеризуются высокой технологичностью, а также обладают сильной противоопухолевой активностью и очень высокими фармакокинетическими свойствами. Изобретение может быть использовано при лечении различных типов рака. 6 н. и 11 з.п. ф-лы, 47 ил., 21 табл., 15 пр.
1. Противораковый агент, содержащий в качестве активного ингредиента эффективное количество биспецифического антитела, где биспецифическое антитело является биcпецифическим антителом, описанным ниже в одном из подпунктов (а1)-(с5), которое содержит вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3, и вариабельную область антитела, которая обладает связывающей активностью в отношении CD3:
(a1) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 211, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 142, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a2) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 211, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 144, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a3) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 144, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a4) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 142, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(а5) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 168, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, которые содержатся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a6) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 434, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, которые содержатся в SEQ ID NO: 433, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 435, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 435, соответственно;
(b1) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 211; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 142; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b2) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 211; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 144; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b3) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 144; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b4) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 142; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b5) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 168; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b6) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 434; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 433; последовательность вариабельной области легкой цепи антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 435; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 435;
(c1) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 386; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 398; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c2) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 386; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 399; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c3) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 399; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c4) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 398; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410; и
(с5) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 402; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410.
2. Противораковый агент по п. 1, где рак представляет собой позитивный по глипикану 3 рак.
3. Противораковый агент по п. 2, где позитивный по глипикану 3 рак представляет собой рак, при котором количество антигенов глипикана 3 на клеточной поверхности составляет на клетку 100 или более.
4. Противораковый агент по одному из пп. 1-3, где рак представляет собой любой рак, выбранный из группы, которая состоит из рака желудка, рака головы и шеи, рака пищевода, рака легкого, рака печени, рака яичника, рака молочной железы, рака ободочной кишки, рака почки, рака кожи, мышечной опухоли, рака поджелудочной железы, рака предстательной железы, рака яичек, рака матки, холангиосаркомы, карциномы из клеток Меркеля, рака мочевого пузыря, рака щитовидной железы, шванномы, рака надпочечных желез, рака ануса, опухоли центральной нервной системы, опухоли нейроэндокринной ткани, рака пениса, опухоли плевры, опухоли слюнных желез, рака вульвы, тимомы и педиатрического рака.
5. Противораковый агент по одному из пп. 1-4, предназначенный для лечения пациента, который имеет рак, устойчивый к лечению ингибитором иммунных контрольных точек.
6. Фармацевтическая композиция, предназначенная для применения для лечения или профилактики рака в комбинации с другим противораковым агентом, где фармацевтическая композиция содержит эффективное количество биспецифического антитела в качестве активного ингредиента, где биспецифическое антитело является биспецифическим антителом по одному из указанных ниже подпунктов (а1)-(с5), которое содержит вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, которая обладает связывающей активностью в отношении CD3:
(a1) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 211, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 142, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a2) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 211, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 144, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a3) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 144, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a4) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 142, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(а5) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 206, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 168, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, которые содержатся в SEQ ID NO: 223, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223, соответственно;
(a6) биспецифическое антитело, в котором CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 434, соответственно; CDR1, CDR2 и CDR3 тяжелой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, которые содержатся в SEQ ID NO: 433, соответственно; CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области, обладающей связывающей активностью в отношении глипикана 3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 435, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащиеся в вариабельной области антитела, обладающей связывающей активностью в отношении CD3, имеют последовательности, идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 435, соответственно;
(b1) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 211; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 142; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b2) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 211; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 144; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b3) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 144; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b4) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 142; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b5) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 206; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 168; последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 223; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 223;
(b6) биспецифическое антитело, в котором последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 434; последовательность вариабельной области тяжелой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 433; последовательность вариабельной области легкой цепи антитела, которая обладает связывающей активностью в отношении глипикана 3, представляет собой аминокислотную последовательность SEQ ID NO: 435; и последовательность вариабельной области легкой цепи, которая обладает связывающей активностью в отношении CD3, представляет собой аминокислотную последовательность SEQ ID NO: 435;
(c1) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 386; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 398; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c2) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 386; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 399; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c3) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 399; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410;
(c4) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 398; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410; и
(с5) биспецифическое антитело, которое имеет тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 385; тяжелую цепь антитела, последовательность которой представляет собой аминокислотную последовательность SEQ ID NO: 402; две идентичные легкие цепи, последовательность которых представляет собой аминокислотную последовательность SEQ ID NO: 410.
7. Фармацевтическая композиция по п. 6, где биспецифическое антитело вводят одновременно с указанным другим противораковым агентом.
8. Фармацевтическая композиция по п. 6, где биспецифическое антитело вводят до или после введения указанного другого противоракового агента.
9. Фармацевтическая композиция по одному из пп. 6-8, где указанный другой противораковый агент представляет собой химиотерапевтический агент, активирующий T-клетки агонистический агент, ингибитор иммунных контрольных точек или ингибитор ангиогенеза.
10. Фармацевтическая композиция по п. 9, где химиотерапевтический агент представляет собой антиметаболит, растительный алкалоид или соединение платины.
11. Фармацевтическая композиция по п. 9, где активирующий T-клетки агонистический агент представляет собой агонистическое антитело против TNFRSF.
12. Фармацевтическая композиция по п. 9, где ингибитор иммунных контрольных точек представляет собой анти-PD1 антитело, анти-PDL1 антитело и анти-CTLA4 антитело, анти-TIM3 антитело или анти-LAG3 антитело.
13. Фармацевтическая композиция по п. 9, где ингибитор ангиогенеза представляет собой антитело к VEGFR2 или бевацизумаб.
14. Агент для индукции цитотоксичности, который содержит фармацевтическую композицию по одному из пп. 6-13.
15. Агент для подавления пролиферации клеток, который содержит фармацевтическую композицию по одному из пп. 6-13.
16. Агент для ингибирования пролиферации клеток, который содержит фармацевтическую композицию по одному из пп. 6-13.
17. Агент для активации иммунного ответа, который содержит фармацевтическую композицию по одному из пп. 6-13.
| WO 2015046467 A1, 02.04.2015 | |||
| WO 2015046554 A1, 02.04.2015 | |||
| WO 2015156268 A1, 15.10.2015 | |||
| AITZIBER BUQUE et al | |||
| Trial Watch: Immunomodulatory monoclonal antibodies for oncological indications, Oncoimmunology, 2015, vol.4, no.4, e1008814 | |||
| ТЕРАПЕВТИЧЕСКИЕ DLL4-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2010 |
|
RU2570639C2 |
| ЛЕЧЕНИЕ АНТИТЕЛАМИ ПРОТИВ VEGF | 2004 |
|
RU2519669C2 |
Авторы
Даты
2021-04-20—Публикация
2017-02-24—Подача