Область техники, к которой относится изобретение
Настоящее изобретение относится к мультиспецифическим антигенсвязывающим молекулам, их применениям и т.п.
Предпосылки создания изобретения
Антитела привлекают внимание в качестве терапевтических средств благодаря их высокой стабильности в плазме и небольшому количеству нежелательных реакций (непатентные документы 1 и 2). Известно, что антитела индуцируют не только антигенсвязывающую активность, агонистическое действие и антагонистическое действие, но также и опосредуемые эффектором виды цитотоксической активности (которые называют также эффекторными функциями), такие как антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), антителозависимый клеточный фагоцитоз (ADCP) и комплементзависимая цитотоксичность (CDC), и обладают противоопухолевыми действиями в отношении раковых клеток (непатентный документ 3). ADCC представляет собой обусловленную эффекторными клетками цитотоксичность в отношении «нагруженных» антителом раковых клеток-мишеней посредством связывания Fc-области антитела с Fc-рецептором, присутствующим на эффекторых клетках, таких как NK-клетки и макрофаги. Комплекс системы комплемента связывается с комплементсвязывающим сайтом, присутствующим в структуре антитела. CDC является вредной для клеток в результате клеточной деструкции, при которой приток воды и ионов в клетки усиливается благодаря образованию пор на клеточной мембране «нагруженных» антителом клеток с помощью компонентов комплемента, присутствующих в комплексе. Создан ряд терапевтических антител с установленными очень высокими противоопухолевыми действиями в качестве фармацевтических средств для лечения рака (непатентный документ 4); и хотя установлено, что известные терапевтические антитела обладают очень высокими действиями, достигаемый при применении указанных антител исход лечения все еще остается неудовлетворительным.
Для того, чтобы антитело обусловливало ADCC, ADCP и CDC, необходимо наличие Fc-области в антителе и присутствие рецептора для антитела (FcγR) на эффекторных клетках, таких как NK-клетки и макрофаги, и различных компонентов комплемента, пригодных для связывания. У человека описаны изоформы FcγRIa, FcγRIIa, FcγRIIb, FcγRIIIa и FcγRIIIb в качестве семейства белка FcγR, кроме того, описаны соответствующие аллотипы (непатентный документ 5). Среди указанных изоформ FcγRIa, FcγRIIa и FcγRIIIa несут активирующий мотив на основе тирозина иммунорецептора (ITAM) во внутриклеточном домене, и передают сигналы активации. С другой стороны, только FcγRIIb несет домен, известный как ингибирующий мотив на основе рецептора тирозина (ITIM), во внутриклеточном домене и передает сигналы ингибирования. Известно, что каждый из FcγR передает сигналы посредством перекрестного сшивания иммунными комплексами и т.п. (непатентный документ 6). Когда антитела фактически проявляют эффекторную функцию на раковых клетках, FcγR на мембране эффекторной клетки образуют кластеры на Fc-областях нескольких антител, связанных на мембране раковой клетки, и сигналы активации передаются эффекторными клетками. В результате проявляется цитоцидное действие, но поскольку FcγR перекрестно сшиваются только на эффекторных клетках, которые в это время присутствуют вблизи раковых клеток, установлено, что активация иммунитета происходит локально в раковых клетках (непатентный документ 7).
Встречающиеся в естественных условиях иммуноглобулины связываются с антигенами в их вариабельных областях и связываются с рецепторами, такими как FcγR, FcRn, FcαR и FcεR, и комплементами в их константных областях. FcRn является одной из связывающихся молекул, которые взаимодействуют с Fc-областью IgG, и установлено, что, поскольку каждая из тяжелых цепей антитела связывается с одной молекулой FcRn, две молекулы FcRn связываются с одном молекулой антитела IgG-типа. Однако, в отличие от FcRn и др., FcγR взаимодействует с шарнирной областью антитела и СН2-доменом, и только одна молекула FcγR связывается с одной молекулой антитела IgG-типа (непатентный документ 8). Кроме того, каноническое встречающееся в естественных условиях антитело IgG-типа распознает и связывает единичный эпитоп через его вариабельную область (Fab); поэтому оно может связываться только с одним антигеном. С другой стороны, известно, что с раком и воспалением связано много типов белков и поэтому может иметь место перекрестная помеха между белками. Например, известно, что несколько воспалительных цитокинов (TNF, IL1 и IL6) могут участвовать в иммунологических заболеваниях (непатентный документ 9). Кроме того, известно, что одним из механизмов приобретения устойчивости рака к лекарственным средствам является активация других рецепторов (непатентный документ 10). В таких случаях канонические антитела, которые распознают единичный эпитоп, не могут ингибировать несколько белков.
Антитела (биспецифические антитела), одна молекула которых связывается с двумя или большим количеством типов антигенов, изучены в качестве молекул, которые ингибируют несколько мишеней. Можно получать связывающие активности с двумя различными антигенами (первый антиген и второй антиген) путем модификации встречающихся в естественных условиях антител IgG-типа (непатентный документ 11). Таким образом, можно не только нейтрализовать два или большее количество типов антигенов с помощью одной молекулы, но также усиливать противоопухолевую активность с помощью перекрестных связей между клетками, которые обладают цитотоксической активностью, и раковыми клетками. К настоящему времени в качестве молекулярных форматов биспецифического антитела описаны молекула, содержащая антигенсвязывающий сайт, добавленный к N- или С-концу антитела (DVD-Ig и scFv-IgG), молекула, имеющая различные последовательности двух Fab-областей антитела (содержащее общую L-цепь биспецифическое антитело и гибридная гибридома), молекула, в которой одна область Fab распознает два антигена (IgG два-в-одном), и молекула, имеющая петлю СН3-области в качестве нового антигенсвязывающего сайта (Fcab) (непатентный документы 12 и 13). Поскольку все биспецифические антитела взаимодействуют на их Fc-областях с FcγR, эффекторные функции антитела сохраняются. Таким образом, биспецифическое антитело связывается с любым антигеном, который оно распознает, и одновременно связывается с FcγR, и обусловливает ADCC-активность в отношении клеток, экспрессирующих антиген.
Если все антигены, распознаваемые биспецифическим антителом, специфически экспрессируются при раке, то биспецифическое антитело обладает цитотоксическим действием в отношении раковых клеток, когда оно связывается с любым из антигенов. Таким образом, по сравнению с каноническим фармацевтическим антителом, которое распознает один антиген, можно ожидать, что указанное антитело будет обладать более эффективным противоопухолевым действием. Однако в случае, когда любой один из антигенов, распознаваемых биспецифическим антителом, экспрессируется в здоровых тканях или клетках, экспрессируемых на иммуноцитах, то имеет место повреждение здоровых тканей или высвобождение цитокинов в результате перекрестного связывания с FcγR (непатентный документ 14). В результате индуцируются сильные нежелательные реакции.
Перенаправляющее Т-клетку антитело, которое использует цитотоксичность, активируя Т-клетки в качестве эффекторных клеток, что является механизмом его противоопухолевого действия, известно с 1980-х годов (непатентные документы 15, 16 и 17). В отличие от антител, которые используют ADCC, активируя NK-клетки или макрофаги в качестве эффекторных клеток, что является механизмом их противоопухолевого действия, перенаправляющее Т-клетки антитело представляет собой антитело против любой одной из субъединиц, из которых состоит комплекс Т-клеточного рецептора (TCR) на Т-клетках, и представляет собой специфическое биспецифическое антитело, которое содержит антитело, связывающееся с эпсилон-цепью CD3, и антитело, связывающееся с антигеном на раковой клетке-мишени. Т-клетки приходят в контакт с раковыми клетками посредством одновременного связывания эпсилон-цепи CD3 и ракового антигена с помощью перенаправляющего Т-клетки антитела. Это в результате приводит к противоопухолевому действию в отношении раковых клеток благодаря цитотоксической активности, обусловленной Т-клетками.
Катумаксомаб, известный в качестве перенаправляющего Т-клетки антитела, связывается на посредством двух Fab с раковым антигеном (ЕрСАМ) и с CD3ε- (CD3-эпсилон) цепью, экспрессируемой на Т-клетках. Катумаксомаб индуцирует опосредуемую Т-клетками цитотоксическую активность путем одновременного связывания с раковым антигеном и CD3ε и индуцирует цитотоксическую активность, опосредуемую антигенпрезентирующими клетками, такими как NK-клетки и макрофаги, путем одновременного связывания с раковым антигеном и FcγR. Благодаря указанным двум видам цитотоксической активности катумаксомаб обладает высоким терапевтическим действием в отношении злокачественных асцитов при внутрибрюшинном введении и поэтому его применение разрешено в Европе (непатентный документ 18). Кроме того, известны случаи, когда по имеющимся сведениям введение катумаксомаба приводит к образованию реактивных в отношении раковых клеток антител, что четко демонстрирует индукцию приобретенного иммунитета (непатентный документ 19). С учетом указанного результата привлекли внимание антитела, которые обладают как опосредуемой Т-клетками цитотоксической активностью, так и опосредуемыми FcγR действиями таких клеток как NK-клетки или макрофаги (указанные антитела обозначают как трехфункциональные антитела), поскольку для них можно ожидать сильное противоопухолевое действие и индукцию приобретенного иммунитета.
Однако трехфункциональные антитела связываются одновременно с CD3ε и FcγR даже в отутствии ракового антигена и поэтому обеспечивают перекрестное сшивание экспрессирующих CD3ε Т-клеток с экспрессирующими FcγR клетками даже при отсутствии в окружении раковых клеток, что приводит к производству в больших количествах различных цитокинов. Указанная независящая от ракового антигена индукция производства различных цитокинов в настоящее время ограничивает применении трехфункциональных антител внутрибрюшинным путем (непатентный документ 20). Трехфункциональные антитела очень трудно вводить системно из-за серьезных напоминающих «цитокиновый шторм» нежелательных реакций. Фактически, на фазе I клинического испытания было установлено, что максимальной переносимой дозой при системном введении катумаксомаба пациентам с немелкоклеточным раком легкого является очень низкая доза, составляющая 5 мкг/организм, и что введение более высокой дозы вызывает серьезные нежелательные реакции. (непатентный документ 21).
Так, созданные с помощью общепринятых методик биспецифические антитела могут связываться с обоими антигенами, при этом первый антиген представляет собой раковый антиген (ЕрСАМ), а второй антиген представляет собой CD3ε, одновременно с этим они связываются с FcγR; и поэтому с учетом их молекулярной структуры невозможно избежать нежелательных реакций, вызываемых одновременным связыванием с FcγR и вторым антигеном CD3ε.
При этом, в отличие от катумаксомаба, BiTE (биспецифический активатор (проводник) Т-клеток) не содержит сайт связывания Fcγ-рецептора и поэтому у него отсутствует перекрестное сшивание с рецепторами, которые экспрессируются на Т-клетках и таких клетках, как NK-клетки и макрофаги, зависимым от ракового антигена образом. Так, было продемонстрировано, что BiTE не вызывает независимую от ракового антигена индукцию цитокинов, которая обнаружена при введении катумаксомаба. Однако, поскольку BiTE представляет собой модифицированную низкомолекулярную молекулу антитела без Fc-области, проблема заключается в том, что время его полужизни в крови после введения пациенту, существенно короче, чем в случае антител IgG-типа, которые обычно применяют в качестве терапевтических антител. Фактически, согласно опубликованным данным время полужизни в крови BiTE при его применении in vivo составляет примерно несколько часов (непатентные документы 22 и 23). При проведении клинических испытаний блинатумомаба его вводили путем непрерывной внутривенной инфузии с помощью мининасоса. Такой метод введения не только чрезвычайно неудобен для пациентов, но также имеет потенциальный риск медицинских осложнений, связанных с неисправностью устройства или т.п. Таким образом, нельзя считать, что указанный метод введения является желательным.
В последние годы применение Fc-области с пониженной способностью связываться с FcγR позволило сохранять сильную противоопухолевую активность, свойственную BiTE, и очень хорошие характеристики безопасности без индукции «цитокинового шторма» зависимым от ракового антигена образом, и обеспечило создание новых полипептидных структур с продолжительным временем полужизни в крови (патентный документ 1).
С другой стороны, когда происходит экспрессия созданного с помощью общепринятых методик биспецифического антитела, то экспрессируются два типа Н-цепей и два типа L-цепей, что может приводить к получению десяти комбинаций. Из них только одна из полученных комбинаций обладает представляющей интерес специфичностью связывания. Таким образом, для получения представляющего интерес биспецифического антитела одно представляющее интерес антитело должны быть выделено из десяти типов антител, такой путь является очень неэффективным и сложным.
В качестве решения указанной проблемы был описан метод, заключающийся в предпочтительном секретировании IgG с гетеродимерной комбинацией Н-цепей, например, с комбинацией Н-цепи против антигена А и Н-цепи против антигена Б, посредством интродукции аминокислотных замен в СН3-область Н-цепи IgG (патентные документы 2, 3, 4, 5, 6, 7 и непатентные документы 24 и 25). В качестве таких методов описаны методы на основе физического нарушения, т.е., «выступа» и «впадины», и метод на основе отталкивания электрических зарядов.
Для получения представляющей интерес молекулы с повышенной эффективностью, описаны методы, основанные на применении L-цепей, которые могут связываться с двумя различными антигенами, даже хотя L-цепи имеют одинаковую аминокислотную последовательность (патентные документы 8 и 9). Однако аффинность к антигену может значительно уменьшаться при применении общих L-цепей и трудно найти общие L-цепи, при использовании которых сохраняется аффинность к антигену.
Перечень перечисленных документов
[Патентные документы]
[Патентный документ 1] WO 2012/073985.
[Патентный документ 2] WO 96/27011.
[Патентный документ 3] WO 2006/106905.
[Патентный документ 4] WO 2007/147901
[Патентный документ 5] WO 2009/089004.
[Патентный документ 6] WO 2010/129304.
[Патентный документ 7] WO 2013/065708.
[Патентный документ 8] WO 98/050431.
[Патентный документ 9] WO 2006/109592.
[Непатентные документы]
[Непатентный документ 1] Nat. Biotechnol. 23, 2005, сс. 1073-1078.
[Непатентный документ 2] Eur J Pharm Biopharm. 59 (3), 2005, сс. 389-396.
[Непатентный документ 3] Drug Des Devel Ther 3, 2009, сс. 7-16.
[Непатентный документ 4] Clin Cancer Res. 16 (1), 2010, сс. 11-20.
[Непатентный документ 5] Immunol. Lett. 82, 2002, cc. 57-65.
[Непатентный документ 6] Nat. Rev. Immunol. 8, 2008, cc. 34-47.
[Непатентный документ 7] Ann. Rev. Immunol. 6, 1988, cc. 251-281.
[Непатентный документ 8] J. Bio. Chem., 276, 2001, cc. 16469-16477.
[Непатентный документ 9] Nat. Biotech., 28, 2011, cc. 502-510.
[Непатентный документ 10] Endocr Relat Cancer 13, 2006, cc. 45-51.
[Непатентный документ 11] MAbs. 1 марта 2012 г., 4(2).
[Непатентный документ 12] Nat. Rev. 10, 2010, cc. 301-316.
[Непатентный документ 13] Peds 23(4), 2010, cc. 289-297.
[Непатентный документ 14] J. Immunol. 163(3), 1 августа 1999 г., cc. 1246-1252.
[Непатентный документ 15] Nature 314 (6012), 1985, cc. 628-631.
[Непатентный документ 16] Int J Cancer 41 (4), 1988, cc. 609-615.
[Непатентный документ 17] Proc Nati Acad Sci USA 83 (5), 1986, cc. 1453-1457.
[Непатентный документ 18] Cancer Treat Rev. 36(6), октябрь 2010 г., cc. 458-467.
[Непатентный документ 19] Future Oncol. 8(1), январь 2012 г., cc. 73-85.
[Непатентный документ 20] Cancer Immunol Immunother. 56(9), 2007, cc. 1397-1406.
[Непатентный документ 21] Cancer Immunol Immunother. 56 (10), 2007, cc. 1637-1644.
[Непатентный документ 22] Cancer Immunol Immunother. 55(5), 2006, cc. 503-514.
[Непатентный документ 23] Cancer Immunol Immunother. 58(1), 2009, cc. 95-109.
[Непатентный документ 24] Protein Engineering, т. 9, 1996, cc. 617-621.
[Непатентный документ 25] Nature Biotechnology, т. 16, 1998, cc. 677-681.
Краткое изложение сущности изобретения
Задачи, положенные в основу настоящего изобретения
Настоящее изобретение было создано с учетом вышеуказанных обстоятельств. В основу настоящего изобретения была положена задача создать мультиспецифические антигенсвязывающие молекулы, которые обладают способностью приводить в контакт Т-клетки с раковыми клетками-мишенями и которые можно применять для лечения рака, используя цитотоксическую активность Т-клеток против раковых тканей-мишеней, которые содержат экспрессирующие глипикан 3 клетки, и представляют собой молекулярные форматы, которые можно получать с высокой эффективностью; разработать способы получения антигенсвязывающих молекул; и фармацевтические композиции, которые содержат антигенсвязывающие молекулы в качестве действующего вещества.
Средства решения указанных задач
При создании настоящего изобретения описана L-цепь, общая с доменом, который содержит вариабельную область связывающегося с глипиканом 3 антитела, и доменом, который содержит вариабельная область антитела, связывающегося с комплексом Т-клеточного рецептора, при этом общая L-цепь обладает способностью повышать аффинность к обоим антигенам. Это обеспечивает получение молекулярных форм с высокой эффективностью, и дополнительно описаны новые мультиспефические антигенсвязывающие молекулы, которые сохраняют сильную противоопухолевую активность, характерную для перенаправляющих Т-клетки антител, таких как BiTE, и обладают очень хорошими характеристиками безопасности, не индуцируя «цитокиновый шторм» в зависимости от ракового антигена, а также обладают продолжительным временем полужизни в крови. Кроме того, при создании настоящего изобретения установлено, что мультиспецифические антигенсвязывающие молекулы, которые содержат общие L-цепи, нацелены на экспрессирующие глипикан 3 раковые клетки и вызывают повреждение клеток. На основе указанного открытия при создании настоящего изобретения установлено, что мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, вызывают повреждение раковых тканей, которые содержат экспрессирующие глипикан 3 раковые клетки.
Более конкретно, в настоящем изобретении предложены:
[1] Мультиспецифическая антигенсвязывающая молекула, которая содержит:
(1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3,
(2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и
(3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора,
в которой вариабельные области L-цепи, содержащиеся в вариабельной области, указанной в подпункте (1), и в вариабельной области, указанной в подпункте (2), имеют общую аминокислотную последовательность; где мультиспецифическая антигенсвязывающая молекула обладает цитотоксической активностью, эквивалентной или более высокой по сравнению с активностью биспецифического антитела GPC3_ERY22_rCE115, которое содержит домен, связывающий глипикан 3, содержащий SEQ ID NO: 47 и 48, и домен, связывающий комплекс Т-клеточного рецептора, содержащий SEQ ID NO: 49 и 50.
[2] Мультиспецифическая антигенсвязывающая молекула по п. [1], цитотоксическая активность которой представляет собой зависимую от Т-клетки цитотоксическую активность.
[3] Мультиспецифическая антигенсвязывающая молекула по п. [1] или п. [2], в которой связывающая активность в отношении комплекса Т-клеточного рецептора представляет собой связывающую активность в отношении Т-клеточного рецептора.
[4] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[3], в которой связывающая активность в отношении комплекса Т-клеточного рецептора представляет собой связывающую активность в отношении CD3ε-цепи.
[5] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельная область антитела, указанная в подпункте (1) в п. [1], представляет собой вариабельную область антитела, которая содержит любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (а1)-(а5), или функционально эквивалентную вариабельную область антитела:
(а1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40;
(a2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197;
(а3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206;
(а4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и
(а5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215.
[6] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельная область антитела, указанная в подпункте (2) в п. [1], представляет собой вариабельную область антитела, которая содержит любую одну из комбинаций аминокислотных последовательностей CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (б1)-(б15), или функционально эквивалентную вариабельную область антитела:
(б1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 52;
(б2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103;
(б3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122;
(б4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128;
(б5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129;
(б6) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132;
(б7) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(б8) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(б9) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(б10) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(б11) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 421;
(б12) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424;
(б13) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 426;
(б14) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 429; и
(б15) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 430.
[7] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [1], представляют собой вариабельные области антитела, которые содержат любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи, выбранную из указанных ниже в подпунктах (в1)-(в19), или функционально эквивалентные вариабельные области антитела:
(в1) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 52;
(в2) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 421;
(в3) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 426;
(в4) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 429;
(в5) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 40; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 430;
(в6) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128;
(в7) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(в8) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(в9) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(в10) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(в11) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142;
(в12) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144;
(в13) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164;
(в14) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168;
(в15) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103;
(в16) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122;
(в17) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129;
(в18) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132; и
(в19) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424.
[8] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [5]-[7], в которой CDR1, CDR2 и CDR3 представляют собой CDR1-, CDR2- и CDR3-участки, определенные на основе нумерации по Кэботу.
[9] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельная область антитела, указанная в подпункте (1) в п. [1], представляет собой вариабельную область антитела, которая содержит любую одну из вариабельных областей Н-цепи, выбранную из указанных ниже в подпунктах (а1)-(а5), или функционально эквивалентную вариабельную область антитела:
(а1) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 40;
(а2) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 197;
(а3) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206;
(а4) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 211; и
(а5) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 215.
[10] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельная область антитела, указанная в подпункте (2) в п. [1], представляет собой вариабельную область антитела, которая содержит любую одну из вариабельных областей Н-цепи, выбранную из указанных ниже в подпунктах (б1)-(б15), или функционально эквивалентную вариабельную область антитела:
(б1) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 52;
(б2) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 103;
(б3) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 122;
(б4) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 128;
(б5) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 129;
(б6) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 132;
(б7) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 142;
(б8) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 144;
(б9) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 164;
(б10) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 168;
(б11) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 421;
(б12) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 424;
(б13) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 426;
(б14) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 429; и
(б15) вариабельная область Н-цепи, которая имеет аминокислотную последовательность SEQ ID NO: 430.
[11] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [1], представляют собой вариабельные области антитела, которые содержат любую одну из комбинацией вариабельных областей Н-цепи, выбранную из указанных ниже в подпунктах (в1)-(в19), или функционально эквивалентные вариабельные области антитела:
(в1) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область H-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 52;
(в2) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 421;
(в3) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 426;
(в4) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 429;
(в5) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 40; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 430;
(в6) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 197; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 128;
(в7) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 142;
(в8) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 144;
(в9) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 164;
(в10) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 206; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 168;
(в11) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 142;
(в12) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 144;
(в13) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 164;
(в14) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 211; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 168;
(в15) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 103;
(в16) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 122;
(в17) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 129;
(в18) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 132; и
(в19) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 215; и вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], которая имеет аминокислотную последовательность SEQ ID NO: 424.
[12] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[11], в которой общая L-цепь, указанная в п. [1], представляет собой общую L-цепь, которая содержит любую одну из комбинаций CDR1, CDR2 и CDR3, выбранную из указанных ниже в подпунктах (г1)-(г11), или функциональный эквивалент общей L-цепи:
(г1) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(г2) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(г3) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(г4) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 301;
(г5) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 302;
(г6) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 304;
(г7) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 306;
(г8) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 307;
(г9) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 309;
(г10) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 310; и
(г11) CDR1, CDR2 и CDR3, идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 319.
[13] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[11], в котором вариабельная область L-цепи, указанная в п. [1], представляет собой вариабельную область любой одной из аминокислотных последовательностей L-цепи, выбранных из указанных ниже в подпунктах (г1)-(г11):
(г1) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 53;
(г2) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 223;
(г3) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 299;
(г4) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 301;
(г5) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 302;
(г6) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 304;
(г7) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 306;
(г8) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 307;
(г9) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 309;
(г10) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 310; и
(г11) L-цепь, содержащая аминокислотную последовательность SEQ ID NO: 319.
[14] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [1], и вариабельная область общей L-цепи представляют собой вариабельные области антитела, содержащие любую одну из комбинаций CDR1, CDR2 и CDR3 Н-цепи и CDR1, CDR2 и CDR3 L-цепи, выбранную из указанных ниже в подпунктах (д1)-(д25), или функционально эквивалентные вариабельные области антитела:
(д1) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д2) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д3) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 310;
(д4) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 197; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 128; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 319;
(д5) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д6) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д7) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д8) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 206; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д9) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д10) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 142; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д11) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 144; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д12) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 164; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям SEQ ID NO: 223;
(д13) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 211; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 168; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 223;
(д14) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д15) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 299;
(д16) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 301;
(д17) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 302;
(д18) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 304;
(д19) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 306;
(д20) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 307;
(д21) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 103; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 309;
(д22) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 122; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д23) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 129; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53;
(д24) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 132; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53; и
(д25) CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 215; CDR1, CDR2 и CDR3, которые содержатся в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 424; и CDR1, CDR2 и CDR3, которые содержатся в вариабельной области общей L-цепи антитела, и идентичные аминокислотным последовательностям CDR1-, CDR2- и CDR3-участков, которые содержатся в SEQ ID NO: 53.
[15] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[4], в которой вариабельные области антитела, указанные в подпунктах (1) и (2) в п. [1], и вариабельная область общей L-цепи представляют собой вариабельные области антитела, содержащие любую одну из комбинаций вариабельных областей, выбранные из указанных ниже в подпунктах (е1)-(е26), или функционально эквивалентные вариабельные области антитела:
(е1) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е2) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(е3) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 310;
(е4) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 197; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 128; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 319;
(е5) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е6) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 144; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е7) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 164; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е8) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 206; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е9) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е10) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 142; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(e11) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 144; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(e12) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 164; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(е13) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентична аминокислотной последовательности SEQ ID NO: 211; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 168; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 223;
(e14) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(e15) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 299;
(e16) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 301;
(e17) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 302;
(e18) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 304;
(e19) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 306;
(е20) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 307;
(е21) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1],и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 103; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 309;
(е22) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 122; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е23) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 129; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е24) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 132; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53;
(е25) вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (1) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 215; вариабельная область Н-цепи, которая содержится в вариабельной области антитела, указанной в подпункте (2) в п. [1], и идентична аминокислотной последовательности SEQ ID NO: 424; и вариабельная область общей L-цепи антитела, идентичная аминокислотной последовательности вариабельной области, которая содержится в SEQ ID NO: 53; и
(е26) мультиспецическая антигенсвязывающая молекула, которая связывается с эпитопом, перекрывающимся с каждым из эпитопов глипикана 3, и комплекса Т-клеточного рецептора, который связывается мультиспецифической антигенсвязывающей молекулой, указанной в одном из подпунктов (е1)-(е25), и которая имеет общую L-цепь.
[16] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[15], в которой Fc-область, указанная в подпункте (3) в п. [1], представляет собой Fc-область с аминокислотной мутацией любой из образующих Fc-область аминокислотных последовательностей SEQ ID NO: 23-26 (IgG1-IgG4).
[17] Мультиспецифическая антигенсвязывающая молекула по п. [16], в которой Fc-область, указанная в подпункте (3) в п. [1], представляет собой Fc-область с мутацией по меньшей мере одной аминокислоты, выбранной из аминокислот в следующих аминокислотных положениях, указанных согласно EU-нумерации:
положение 220, положение 226, положение 229, положение 231, положение 232, положение 233, положение 234, положение 235, положение 236, положение 237, положение 238, положение 239, положение 240, положение 264, положение 265, положение 266, положение 267, положение 269, положение 270, положение 295, положение 296, положение 297, положение 298, положение 299, положение 300, положение 325, положение 327, положение 328, положение 329, положение 330, положение 331 и положение 332.
[18] Мультиспецифическая антигенсвязывающая молекула по п. [16], в которой Fc-область, указанная в подпункте (3) в п. [1], представляет собой Fc-область, которая содержит по меньшей мере одну аминокислоту, выбранную из указанных ниже аминокислот, согласно EU-нумерации:
Arg в аминокислотном положении 234, Ala или Arg в аминокислотном положении 235, Lys в аминокислотном положении 239 и Ala в аминокислотном положении 297.
[19] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [16]-[18], в которой Fc-область, указанная в подпункте (3) в п. [1], дополнительно содержит аминокислотную мутацию, усиливающую образование гетеродимерной Fc-области.
[20] Мультиспецифическая антигенсвязывающая молекула по п. [19], в котором гетеродимерная Fc-область представляет собой указанную ниже комбинацию (ж1) или (ж2) аминокислотных последовательностей:
(ж1) комбинация аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 57, и аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 58; и
(ж2) комбинация аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 60 или 62, и аминокислотной последовательности, идентичной константной области Fc-области, которая содержит аминокислотную последовательность SEQ ID NO: 61.
[21] Мультиспецифическая антигенсвязывающая молекула по одному из п.п. [1]-[20], где мультиспецифическая антигенсвязывающая молекула представляет собой биспецифическое антитело.
[22] Биспецифическое антитело по одному из указанных ниже подпунктов (з1)-(з25):
(з1) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 424, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з2) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з3) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з4) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 301;
(з5) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 302;
(з6) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 304;
(з7) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 306;
(з8) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 307;
(з9) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 103, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 309;
(з10) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 122, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з11) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 129, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з12) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 215, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 132, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з13) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з14) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 310;
(з15) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 319;
(з16) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 197, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 128, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 53;
(з17) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 299;
(з18) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з19) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 144, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з20) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 144, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з21) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з22) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з23) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223;
(з24) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223; и
(з25) биспецифическое антитело, имеющее Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, содержащую вариабельную область Н-цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60 или 62; и общую L-цепь антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223.
[23] Нуклеиновая кислота, которая кодирует мультиспецифическую антигенсвязывающую молекулу по одному из п.п. [1]-[20] или биспецифическое антитело по п. [21] или п. [22].
[24] Вектор, в который интродуцирована нуклеиновая кислота по п. [23].
[25] Клетка, содержащая нуклеиновую кислоту по п. [23] или вектор по п. [24].
[26] Способ получения мультиспецифической антигенсвязывающей молекулы по одному из п.п. [1]-[20] или биспецифического антитела по п. [21] или п. [22], заключающийся в том, что культивируют клетку по п. [25].
[27] Мультиспецифическая антигенсвязывающая молекула или биспецифическое антитело, полученная/полученное способом по п. [26].
[28] Фармацевтическая композиция, содержащая мультиспецифическую антигенсвязывающую молекулу по одному из п.п. [1]-[20] или биспецифическое антитело по п. [21] или п. [22] и фармацевтически приемлемый носитель.
[29] Фармацевтическая композиция по п. [28], которая индуцирует цитотоксичность.
[30] Фармацевтическая композиция по п. [29], где цитотоксичность представляет собой зависимую от Т-клеток цитотоксичность.
[31] Фармацевтическая композиция по п. [28], которая предназначена для введения пациенту, нуждающемуся в этом, мультиспецифической антигенсвязывающей молекулы по одному из п.п. [1]-[20] или биспецифического антитела по п. [21] или п. [22].
Настоящее изобретение относится также к набору, предназначенному для применения в способе, предлагаемом в настоящем изобретении, который содержат мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или мультиспецифическую антигенсвязывающую молекулу, полученную с помощью способа, предлагаемого в настоящем изобретении. Настоящее изобретение относится также к применению мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, или мультиспецифической антигенсвязывающей молекулы, полученной с помощью способа, предлагаемого в настоящем изобретении, для приготовления фармацевтической композиции для активации цитотоксической активности. Настоящее изобретение относится также к мультиспецифической антигенсвязывающей молекуле, предлагаемой в настоящем изобретении, или мультиспецифической антигенсвязывающей молекуле, полученной с помощью способа, предлагаемого в настоящем изобретении, для применения в способе, предлагаемом в настоящем изобретении. В контексте настоящего описания мультиспецифические антигенсвязывающие молекулы включают биспецифические антитела, предлагаемые в настоящем изобретении.
Кроме того, настоящее изобретение относится к мультиспецифической антигенсвязывающе молекуле, которая содержит следующие домены:
(1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3,
(2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора;
в которой вариабельные области L-цепи, входящие в вариабельные области, указанные в подпунктах (1) и (2), имеют общую аминокислотную последовательность. Настоящее изобретение относится также к домену, указанному в подпункте (1), который более конкретно представляет собой домен, содержащий вариабельные области тяжелой цепи и/или легкой цепи антитела, которые обладают связывающей активностью в отношении глипикана 3, и которые входит в состав мультиспецифической антигенсвязывающей молекулы. Настоящее изобретение относится также к домену, указанному в подпункте (2), который более конкретно представляет собой домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и который входит в состав мультиспецифической антигенсвязывающей молекулы. Компоненты доменов, указанных в подпунктах (1) и (2), могут включать указанные выше в п.п. [1]-[22]. Мультиспецифическая антигенсвязывающая молекула может представлять собой биспецифическое антитело. Кроме того, Мультиспецифическая антигенсвязывающая молекула может содержать домен, включающий Fc-область и Fc-область может обладать пониженной активностью в отношении связывания Fcγ-рецептора. Компоненты домена, содержащего Fc-область, могут включать указанные выше в п.п. [1]-[22]. Настоящее изобретение относится к нуклеиновой кислоте, кодирующей мультиспецифическую антигенсвязывающую молекулу или домены, вектору, в который интродуцирована нуклеиновая кислота, клетке, которая содержит нуклеиновую кислоту или вектор, способу получения мультиспецифической антигенсвязывающей молекулы, заключающемуся в том, что культивируют клетки, и мультиспецифической антигенсвязывающей молекуле или доменам, которые содержат вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3 или связывающей активностью в отношении комплекса Т-клеточного рецептора, полученным с помощью способа. Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей мультиспецифическую антигенсвязывающую молекулу и фармацевтически приемлемый носитель. Фармацевтическая композиция может индуцировать повреждение клеток, повреждение клеток может быть обусловлено зависимой от Т-клеток клеточной цитотоксичностью, и композицию можно вводить пациенту, который нуждается в применении мультиспецифической антигенсвязывающей молекулы.
Настоящее изобретение относится также к мультиспецифической антигенсвязывающей молекуле, которая связывается с эпитопами, перекрывающимися и/или конкурирующими с эпитопами и глипикана 3, и комплекса Т-клеточного рецептора, связывающимися мультиспецифической антигенсвязывающей молекулой, указанной выше в одном из подпунктов (д1)-(д25) в п. [14], мультиспецифической антигенсвязывающей молекуле, которая связывается с эпитопами, перекрывающимися и/или конкурирующими с эпитопами и глипикана 3, и комплекса Т-клеточного рецептора, связывающимися мультиспецифической антигенсвязывающей молекулой, указанной выше в одном из подпунктов (е1)-(е25) в п. [15].
Касательно двух Fc-областей, описанных выше в подпунктах (ж1) и (ж2) в п. [20], первая Fc-область может быть включена в Н-цепь антитела, которая обладает сязывающей активностью в отношении глипикана 3, а вторая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора; или первая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, а вторая Fc-область может быть включена в Н-цепь антитела, которая обладает связывающей активностью в отношении глипикана 3.
Эффекты изобретения
В настоящем изобретении предложены новые мультиспецифические антигенсвязывающие молекулы, имеющие молекулярные формы, которые можно получать с высокой эффективностью, которые сохраняют сильную противоопухолевую активность, характерную для BiTE, и очень хорошие характеристики безопасности, что приводит к отсутствию индукции независимого от ракового антигена «цитокинового шторма» и т.п., и обладают длительным временем полужизни в крови. Фармацевтические композиции, которые активируют цитотоксическую активность, содержащие в качестве действующего вещества мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, направленно воздействуют на раковые ткани, которые содержат экспрессирующие глипикан 3 раковые клетки, вызывая повреждение клеток, и их можно применять для лечения или предупреждения различных видов рака. Изобретение обеспечивает требуемое лечения, которое не только обладает высоким уровнем безопасности, но и снижает физическую нагрузку на пациентов и является очень удобным для пациентов.
Краткое описание чертежей
На чертежах показано:
на фиг 1 - схематическая диаграмма a: ERY22 и б: ERY27;
на фиг. 2 - график, иллюстрирующий цитотоксическую активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 при применении в качестве клетки-мишени NCI-H446. Закрашенными ромбами ( ) и закрашенными треугольниками (
) и закрашенными треугольниками ( ) обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
) обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
на фиг. 3 - график, иллюстрирующий цитотоксическую активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 при применении в качестве клетки-мишени PC-10. Закрашенными ромбами ( ) и закрашенными треугольниками (
) и закрашенными треугольниками ( ) обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
) обозначена цитотоксическая активность GPC3_ERY22_rCE115 и GPC3_ERY27_hCE115 соответственно;
на фиг. 4 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-H446;
на фиг. 5 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-H446;
на фиг. 6 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-H446;
на фиг. 7 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-H446;
на фиг. 8 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 9 - график, иллюстрирующий цитотоксическую активность оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 10 - данные о противоопухолевой активности in vivo оптимизированных антител при применении в качестве клетки-мишени PC-10;
на фиг. 11 - данные о противоопухолевой активности in vivo оптимизированных антител при применении в качестве клетки-мишени NCI-Н446;
на фиг. 12 - зависимость между аминокислотными остатками, образующими Fc-области IgG1, IgG2, IgG3 и IgG4, и системой нумерации EU по Кэботу (обозначена в контексте настоящего описания как EU-индекс);
на фиг. 13-1 - последовательности вариабельных областей тяжелой цепи и их нумерация согласно Кэботу с соавторами;
на фиг. 13-2 - последовательности вариабельных областей тяжелой цепи и их нумерация согласно Кэботу с соавторами;
на фиг. 14 - последовательности вариабельных областей легкой цепи и их нумерация согласно Кэботу с соавторами.
Варианты осуществления изобретения
Представленные ниже определения даны с целью облегчения понимания настоящего изобретения.
Антитело
В контексте настоящего описания «антитело» относится к встречающемуся в естественных условиях иммуноглобулину или иммуноглобулину, полученному полностью или частично путем синтеза. Антитела можно выделять из встречающихся в естественных условиях источников, таких как встречающиеся в естественных условиях плазма и сыворотка, или из супернатантов культур продуцирующих антитела гибридом. Альтернативно этому, антитела можно частично или полностью синтезировать с использованием таких методик, как генетическая рекомбинация. Предпочтительными антителами являются, например, антитела, принадлежащие к какому-либо изотипу иммуноглобулинов или его подклассу. Известные человеческие иммуноглобулины включают антитела следующих девяти классов (изотипов): IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE и IgM. Из этих изотипов к антителам, предлагаемым в изобретении, относятся IgG1, IgG2, IgG3 и IgG4.
Методы получения антитела с требуемой связывающей активностью известны специалистам в данной области. Ниже представлен пример, в котором описан метод получения антитела (антитело к GPC3), связывающегося с глипиканом-3 (ниже в настоящем описании обозначен как GPC3), который принадлежит к семейству GPI-заякоренных рецепторов (Int J Cancer. 103(4), 2003, cc. 455-465). Согласно описанному ниже примеру можно получать также антитела, которые связываются с комплексом Т-клеточного рецептора.
Антитела к GPC3 можно получать в виде поликлональных или моноклональных антител с помощью известных методов. Антитела к GPC3 предпочтительно получали в виде моноклональных антител, происходящих из организма млекопитающих. Указанные происходящие из организма млекопитающих антитела включают антитела, полученные с помощью гибридом или клеток-хозяев, трансформированных экспрессионным вектором, который несет ген антитела, с помощью методов генетической инженерии.
Гибридомы, продуцирующие моноклональные антитела, можно получать с использованием известных методов, например, описанных ниже. В частности, млекопитающих иммунизируют с помощью общепринятых методов иммунизации, используя белок GPC3 в качестве сенсибилизирующего антигена. Образовавшиеся иммунные клетки сливают с известными родительскими клетками с помощью общепринятых методов слияния. Затем гибридомы, продуцирующие антитело к GPC3, можно отбирать путем скрининга в отношении продуцирующих моноклональные антитела клеток с помощью общепринятых методов скрининга.
В частности, моноклональные антитела получают согласно описанному ниже методу. Сначала ген GPC3, нуклеотидная последовательность которого представлена в RefSeq под регистрационным номером NM_001164617.1 (SEQ ID NO: 1), можно экспрессировать с получением белка GPC3, последовательность которого представлена в RefSeq под регистрационным номером NP_001158089.1 (SEQ ID NO: 2), который можно применять в качестве сенсибилизирующего антигена для получения антитела. Для этого генную последовательность, кодирующую GPC3, встраивают в известный экспрессионный вектор и соответствующие клетки-хозяева трансформируют этим вектором. Требуемый человеческий белок GPC3 очищают из клеток-хозяев или супернатантов культур с помощью известных методов. Например, для получения растворимого GPC3 из супернатантов культур удаляют путем делеции аминокислоты в положениях 564-580, которые формируют гидрофобную область, соответствующую GPI-заякоривающей последовательности, применяемой для заякоривания GPC3 на клеточной мембране, из полипептидной последовательности GPC3 SEQ ID NO: 2, а затем образовавшийся белок экспрессируют вместо белка GPC3, имеющего SEQ ID NO: 2. В альтернативном варианте в качестве сенсибилизирующего антигена можно применять очищенный встречающийся в естественных условиях белок GPC3.
Очищенный белок GPC3 можно применять в качестве сенсибилизирующего антигена для иммунизации млекопитающих. В качестве сенсибилизирующих антигенов можно применять также неполные пептиды GPC3. В этом случае неполные пептиды можно получать химическим синтезом на основе аминокислотной последовательности человеческого GPC3. Кроме того, их можно получать также путем встраивания части гена GPC3 в экспрессионный вектор и осуществлять экспрессию в нем. Кроме того, их можно получать путем расщепления белка GPC3 протеазой, однако конкретный вариант осуществления изобретения не накладывает ограничения на длину и область пептида GPC3, применяемого в качестве неполного пептида. В качестве предпочтительной области можно выбирать любую последовательность из аминокислотной последовательности, которая соответствует аминокислотам в положениях 524-563, или более предпочтительно любую последовательность из аминокислотной последовательности, которая соответствует аминокислотам в положениях 537-563 в аминокислотной последовательности SEQ ID NO: 2. Предпочтительно можно выбирать любую последовательность из аминокислотной последовательности области, не содержащую аминокислотную последовательность, которая соответствует аминокислотам в положениях 550-663 в аминокислотной последовательности SEQ ID NO: 2. Предпочтительно можно выбирать любую последовательность, соответствующую положениям 544-553, и более предпочтительно можно выбирать любую последовательность из аминокислотной последовательности, соответствующей положениям 546-551, в аминокислотной последовательности SEQ ID NO: 2. Количество аминокислот, образующих пептид, который можно применять в качестве сенсибилизирующего антигена, предпочтительно составляет по меньшей мере пять или более, или предпочтительно, например, шесть или более, или семь или более. Более конкретно, в качестве сенсибилизирующего антигена можно применять пептид, состоящий из 8-50 остатков, более предпочтительно из 10-30 остатков.
В альтернативном варианте в качестве сенсибилизирующего антигена можно применять слитый белок, полученный путем слияния требуемого неполного полипептида или пептида белка GPC3, с другим полипептидом. Например, для получения слитых белков, предназначенных для применения в качестве сенсибилизирующих антигенов, предпочтительно применяют Fc-фрагменты антитела и пептидные метки. Векторы для экспрессии указанных слитых белков можно конструировать путем слияния в рамке считывания генов, кодирующих два или большее количество требуемых полипептидных фрагментов, и встраивания слитого гена в экспрессионный вектор, описанный выше. Методы получения слитых белков описаны в Molecular Cloning, 2-ое изд. (Sambrook J. и др., Molecular Cloning, 2-ое изд. 1989, 9.47-9.58, изд-во Cold Spring Harbor Lab. Press). Методы получения GPC3, предназначенного для применения в качестве сенсибилизирующего антигена, и методы иммунизации с использованием GPC3 конкретно описаны в WO 2003/000883, WO 2004/022754 и WO 2006/006693.
Конкретное ограничение, касающееся млекопитающих, подлежащих иммунизации с помощью сенсибилизирующего антигена, отсутствует. Однако предпочтительно выбирать млекопитающих с учетом их совместимости с родительскими клетками, применяемыми для клеточного слияния. В целом, предпочтительно применяют грызунов, таких как мыши, крысы, а также хомяки, кролики, и обезьян.
Вышеуказанных животных иммунизируют сенсибилизирующим антигеном с помощью известных методов. Общепринятыми методами иммунизации млекопитающих являются, например, внутрибрюшинная или подкожная инъекция сенсибилизирующего антигена. В частности, сенсибилизирующий антиген можно соответствующим образом разводить в ЗФР (забуференный фосфатом физиологический раствор), физиологическом соляном растворе или т.п. При необходимости с антигеном смешивают общепринятый адъювант, такой как полный адъювант Фрейнда, и смесь эмульгируют. Затем сенсибилизирующий антиген вводят млекопитающему несколько раз с 4-21-дневными интервалами. При иммунизации сенсибилизирующим антигеном можно использовать соответствующие носители. В частности, когда в качестве сенсибилизирующего антигена используют низкомолекулярный неполный пептид, то иногда для иммунизации требуется сочетать пептид, представляющий собой сенсибилизирующий антиген, с белком-носителем, таким как альбумин или гемоцианин лимфы улитки.
Альтернативно этому, можно получать продуцирующие требуемое антитело гибридомы с помощью описанной ниже ДНК-иммунизации. ДНК-иммунизация представляет собой метод иммунизации, который обеспечивает иммуностимуляцию посредством экспрессии сенсибилизирующего антигена в организме иммунизированного животного в результате введения ДНК-вектора, сконструированного таким образом, чтобы он обеспечивал экспрессию гена, кодирующего антигенный белок, в организме животного. По сравнению с общепринятыми методами иммунизации, при которых животным, подлежащим иммунизации, вводят белковый антиген, ДНК-иммунизация, по-видимому, имеет следующие преимущества:
- можно осуществлять иммуностимуляцию, сохраняя при этом структуру мембранного белка, такого как GPC3; и
- отсутствует необходимость в очистке антигена для иммунизации.
Для получения моноклонального антитела, предлагаемого в настоящем изобретении, с использованием ДНК-иммунизации сначала вводят животному, подлежащему иммунизации, ДНК, экспрессирующую белок GPC3. ДНК, кодирующую GPC3, можно синтезировать с помощью известных методов, таких как ПЦР. Полученную ДНК встраивают в соответствующий экспрессионный вектор и затем его вводят животному, подлежащему иммунизации. Предпочтительно применяемые для этой цели экспрессионные векторы включают, например, поступающие в продажу экспрессионные векторы, такие как pcDNA3.1. Векторы можно вводить в организм с помощью общепринятых методов. Например, ДНК-иммунизацию осуществляют с использованием генной пушки для интродукции золотых частиц, покрытых экспрессионным вектором, в клетки тела животного, подлежащего иммунизации. Антитела, распознающие GPC3, можно получать также методами, описанными в WO 2003/104453. После описанной выше иммунизации млекопитающего у него подтверждают в сыворотке повышенный титр GPC3-связывающего антитела. После этого получают из организма млекопитающего иммунные клетки и затем используют их для клеточного слияния. В частности, в качестве иммунных клеток предпочтительно применяют спленоциты.
Клетку миеломы млекопитающих применяют в качестве клетки, подлежащей слиянию с вышеуказанным иммуноцитом. Клетки миеломы предпочтительно содержат приемлемый маркер селекции для скрининга. Маркер селекции придает клеткам характеристики, обеспечивающие их выживание (или гибель) в специфических условиях культивирования. В качестве маркера селекции известны дефицит гипоксантин-гуанин-фосфорибозилтрансферазы (сокращенно обозначенный далее в контексте настоящего описания как дефицит HGPRT) и дефицит тимидинкиназы (сокращенно обозначенный далее в контексте настоящего описания как дефицит TK). Клетки с дефицитом HGPRT или TK обладают чувствительностью к гипоксантин-аминоптерин-тимидину (сокращенно обозначена далее в контексте настоящего описания как ГАТ-чувствительность). Клетки с ГАТ-чувствительностью не могут синтезировать ДНК в селекционной ГАТ-среде и в результате погибают. Однако, когда клетки сливают со здоровыми клетками, они могут продолжать синтез ДНК с использованием «реутилизационного» пути здоровых клеток, и в результате они могут расти даже в селекционной ГАТ-среде.
Клетки с HGPRT-дефицитом и TK-дефицитом можно отбирать в среде, содержащей 6-тиогуанин, 8-азагуанин (сокращенно обозначенный далее в контексте настоящего описания как 8AG) или 5'-бромдезоксиуридин соответственно. Здоровые клетки уничтожаются, поскольку они включают эти пиримидиновые аналоги в их ДНК. При этом клетки с дефицитом этих ферментов могут выживать в селекционной среде, поскольку они не могут включать указанные пиримидиновые аналоги. Кроме того, к маркеру селекции относится устойчивость к G418, которая обеспечивается геном устойчивости к неомицину, придающим устойчивость к 2-дезоксистрептаминовым антибиотикам (аналоги гентамицина). Известны различные типы клеток миелом, которые можно применять для клеточного слияния.
Например, в качестве клеток миеломы предпочтительно можно применять следующие клетки:
P3(P3x63Ag8.653) (J. Immunol. 123 (4), 1979, cc. 1548-1550);
P3x63Ag8U.1 (Current Topics in Microbiology and Immunology 81, 1978, сс. 1-7);
NS-1 (С.Eur. J. Immunol. 6 (7), 1976, cc. 511-519);
MPC-11 (Cell 8 (3), 1976, cc. 405-415);
SP2/0 (Nature 276 (5685), 1978, cc. 269-270);
FO (J. Immunol. Methods 35 (1-2), 1980, cc. 1-21);
S194/5.XX0.BU.1 (J. Exp. Med. 148 (1), 1978, cc. 313-323);
R210 (Nature 277 (5692), 1979, cc. 131-133) и т.д.
Клеточное слияние иммуноцитов и клеток миеломы, как правило, осуществляют с помощью известных методов, например, метода, описанного у Kohler и Milstein и др. (Methods Enzymol. 73, 1981, cc. 3-46).
Более конкретно, клеточное слияние можно осуществлять, например, в общепринятой культуральной среде в присутствии усиливающего клеточное слияние агента. Усиливающие клеточное слияние агенты включают, например, полиэтиленгликоль (ПЭГ) и вирус Сендай (гемагглютинирующий японский вирус мышей) (HVJ). При необходимости для повышения эффективности слияния добавляют также вспомогательную субстанцию, такую как диметилсульфоксид.
Соотношение иммуноцитов и клеток миеломы можно определять по усмотрению исследователя, предпочтительно, например, одна клетка миеломы на каждые 1-10 иммуноцитов. Культуральные среды, применяемые для клеточных слияний, включают, например, среды, пригодные для выращивания клеточных линий миелом, такие как среда RPMI1640 и среда MEM, а также другая общепринятая культуральная среда, применяемая для данного типа клеточной культуры. Кроме того, в культуральную среду предпочтительно можно добавлять добавки в виде сыворотки, такой как фетальная телячья сыворотка (FCS).
Для клеточного слияния указанные выше иммунных клетки и клетки миеломы, взятые в предварительно определенных количествах, хорошо перемешивают в указанной выше культуральной среде. Затем к ней добавляют предварительно нагретый до температуры примерно 37°С раствор ПЭГ (например, средняя молекулярная масса которого составляет примерно от 1000 до 6000) в концентрации, составляющей, как правило, от 30 до 60% (мас./об.). Смесь осторожно перемешивают до получения требуемых слитых клеток (гибридомы). Затем указанную выше культуральную среду постепенно добавляют к клеткам и повторно центрифугируют для удаления супернатанта. Таким путем можно удалять агенты для клеточного слияния, которые являются нежелательными для роста гибридом.
Полученные таким образом гибридомы можно отбирать путем культивирования, используя общепринятую селективную среду, например, ГАТ-среду (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). Клетки, отличные от требуемых гибридом (неслитые клетки), можно уничтожать путем последующего культивирования в вышеуказанной ГАТ-среде в течение достаточного периода времени. Как правило, период составляет от нескольких дней до нескольких недель. Затем осуществляют скрининг гибридом, продуцирующих требуемое антитело, и по отдельности клонируют с помощью общепринятых методов серийных разведении.
Полученные таким образом гибридромы можно отбирать, используя селекционную среду на основе маркера селекции, который несут клетки миеломы, применяемые для клеточного слияния. Например, клетки с HGPRT-или TK-дефицитом можно отбирать путем культивирования с использованием ГАТ-среды (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). А частности, когда для клеточного слияния используют чувствительные к ГАТ клетки миеломы, то клетки, для которых характерно успешное слияние со здоровыми клетками, могут избирательно размножаться в ГАТ-среде. Клетки, отличные от требуемых гибридом (неслитые клетки), можно уничтожать путем культивирования в вышеуказанной ГАТ-среде в течение достаточного периода времени. В частности, требуемые гибридомы можно отбирать путем культивирования, как правило, в течение периода времени, составляющего от нескольких дней до нескольких недель. Затем осуществляют скрининг гибридом, продуцирующих требуемое антитело, и по отдельности клонируют с помощью общепринятых методов серийных разведении.
Требуемые антитела предпочтительно можно отбирать и по отдельности клонировать с помощью методов скрининга, основанных на известной реакции антиген/антитело. Например, GPC3-связывающее моноклональное антитело может связываться с GPC3, экспрессируемым на клеточной поверхности. Можно осуществлять скрининг указанных моноклональных антител с помощью метода разделения клеток на основе возбуждения флуоресценции (FACS). FACS представляет собой систему, которая позволяет оценивать связывание антитела с клеточной поверхностью посредством анализа клеток, контактирующих с флуоресцентным антителом, с использованием лазерного пучка, и путем оценки флуоресценции, испускаемой индивидуальными клетками.
Для скрининга с использованием FACS в отношении гибридом, которые продуцируют моноклональное антитело, предлагаемое в настоящем изобретении, прежде всего получают экспрессирующие GPC3 клетки. Клетки, которые предпочтительно используют для скрининга, представляют собой клетки млекопитающих, в которых происходит принудительная экспрессия GPC3. В качестве контроля можно избирательно определять с использованием нетрансформированных клеток млекопитающих в качестве клеток-хозяев способность антитела связываться с расположенным на клеточной поверхности GPC3. В частности, гибридомы, продуцирующие моноклональное антитело к GPC3, можно выделять путем отбора гибридом, которые продуцируют антитело, связывающееся с клетками, принудительно экспрессирующими GPC3, но не с клетками-хозяевами.
Альтернативно этому, способность антитела связываться с иммобилизованными экспрессирующими GPC3 клетками можно оценивать на основе принципа ELISA. Например, экспрессирующие GPC3 клетки иммобилизуют на лунках планшета для ELISA. Супернатанты культур гибридом приводят в контакт с иммобилизованными клетками в лунках и выявляют антитела, которые связываются с иммобилизованными клетками. Когда моноклональные антитела имеют мышиное происхождение, то антитела, связанные с клетками, можно выявлять с помощью антитела к мышиному иммуноглобулину. Гибридомы, продуцирующие требуемое антитело, которое обладает антигенсвязывающей активностью, отбирают путем описанного выше скрининга, и их можно клонировать методом серийных разведении или аналогичным методом.
Полученные таким путем гибридомы, продуцирующие моноклональные антитела, можно пересевать в общепринятую культуральную среду и хранить в жидком азоте в течение длительного периода времени.
Указанные выше гибридомы культивируют с помощью общепринятого метода и требуемые моноклональные антитела можно получать из супернатантов культур. Альтернативно этому, гибридомы интродуцируют и выращивают в пригодных для этой цели млекопитающих, и моноклональные антитела получают из асцитов. Первый метод пригоден для получения антител с высокой степенью чистоты.
Предпочтительно можно применять также антитела, кодируемые генами антител, которые клонированы из продуцирующих антитела клеток, таких как указанные выше гибридомы. Клонированный ген антитела встраивают в соответствующий вектор и его интродуцируют в хозяина для экспрессии кодируемого геном антитела. Методы выделения генов антител, встраивания генов в векторы и трансформации клеток-хозяев разработаны ранее (см., например, Vandamme и др., Eur. J. Biochem. 192(3), 1990, cc. 767-775). Методы получения рекомбинантных антител также известны и описаны ниже.
Например, кДНК, кодирующую вариабельную область (V-область) антитела к GPC3, получают из клеток гибридомы, экспрессирующих антитело к GPC3. Для этой цели сначала из гибридом экстрагируют общую РНК. Методы, которые применяют для экстракции мРНК из клеток, включают, например:
- метод ультрацентрифугирования в присутствии гуанидина (Biochemistry 18(24), 1979, cc. 5294-5299) и
- AGPC-метод (Anal. Biochem. 162(1), 1987, cc. 156-159).
Экстрагированные мРНК можно очищать с помощью набора для очистки мРНК (фирма GE Healthcare Bioscience) или аналогичного набора. В качестве альтернативы можно применять также поступающие в продажу наборы для экстракции мРНК непосредственно из клеток, такие как набор для очистки мРНК QuickPrep (фирма GE Healthcare Bioscience). мРНК можно получать из гибридом с использованием таких наборов. Кодирующие V-область антитела кДНК можно синтезировать из полученных мРНК с помощью обратной транскриптазы. кДНК можно синтезировать с помощью набора для синтеза первой цепи кДНК, содержащего обратную транскриптазу AMV (Reverse Transcriptase First-strand cDNA Synthesis Kit) (фирма Seikagaku Co.) или аналогичного набора. Кроме того, для синтеза и амплификации кДНК можно применять набор для амплификации кДНК SMART RACE (фирма Clontech) и основанный на ПЦР 5'-RACE-(быстрая амплификация концов кДНК)-метод (Proc. Natl. Acad. Sci. USA 85(23), 1988, cc. 8998-9002; Nucleic Acids Res. 17(8), 1989, cc. 2919-2932). При таком процессе синтеза кДНК соответствующие описанные ниже сайты, распознаваемые рестриктазами, можно интродуцировать на оба конца кДНК.
Представляющий интерес фрагмент кДНК очищают из полученного ПЦР-продукта и затем его встраивают путем лигирования в ДНК-вектор. Таким путем создают рекомбинантный вектор и интродуцируют в Е. coli или подобного хозяина. После селекции колоний требуемый рекомбинантный вектор можно получать из колониеобразующих Е. coli. Затем с использованием известного метода, такого как дидезокси-метод (метод терминации нуклеотидной цепи), определяют, имеет ли рекомбинантный вектор представляющую интерес нуклеотидную последовательность кДНК.
5'-RACE-метод, в котором используют праймеры для амплификации гена вариабельной области, как правило, применяют для выделения гена, кодирующего вариабельную область. Сначала конструируют библиотеку кДНК, применяемую для 5'-RACE (5'-RACE-библиотека кДНК) с использованием РНК, экстрагированных из клеток гибридомы, в качестве матрицы. Для синтеза 5'-RACE-библиотеки кДНК можно использовать поступающий в продажу набор, такой как набор для амплификации кДНК SMART RACE.
Ген антитела амплифицируют с помощью ПЦР, используя полученную 5'-RACE-библиотеку кДНК в качестве матрицы. Праймеры для амплификации гена мышиного антитела можно создавать на основе известных генных последовательностей антител. Нуклеотидные последовательности праймеров варьируются в зависимости от подкласса иммуноглобулина. Таким образом, предпочтительно предварительно определять подкласс с помощью доступного набора, такого как набор для изотипирования мышиных моноклональных антител Iso Strip (Iso Strip mouse monoclonal antibody isotyping kit) (фирма Roche Diagnostics).
В частности, например, для выделения генов, кодирующих мышиный IgG, применяют праймеры, которые обеспечивают амплификацию генов, кодирующих тяжелые цепи γ1, γ2а, γ2b и γ3 и легкие цепи κ и λ. В целом, праймер, сайт гибридизации («отжига») которого с константной областью расположен вблизи вариабельной области, применяют в качестве 3'-концевого праймера для амплификации гена вариабельной области IgG. При этом праймер, присоединенный к набору конструкций 5' RACE-библиотеки кДНК, применяют в качестве 5'-концевого праймера.
Амплифицированные таким образом ПЦР-продукты применяют для реконструирования иммуноглобулинов, состоящих из комбинации тяжелых и легких цепей. Требуемое антитело можно отбирать, используя в качестве показателя GPC3-связывающую активность реконструированного иммуноглобулина. Например, когда задачей является выделение антитела к GPC3, то более предпочтительно, чтобы связывание антитела с GPC3 являлось специфическим. Можно осуществлять скрининг GPC3-связывающих антител, например, с использованием следующих стадий, на которых:
(1) приводят в контакт экспрессирующую GPC3 клетку с антителом, содержащим V-область, которая кодируется кДНК, выделенной из гибридомы;
(2) определяют связывание антитела с экспрессирующей GPC3 клеткой; и
(3) отбирают антитело, которое связывается с экспрессирующей GPC3 клеткой.
Методы определения связывания антитела с экспрессирующими GPC3 клетками, являются известными. В частности, связывание антитела с экспрессирующими GPC3 клетками можно определять с помощью описанных выше методик, таких как FACS. Иммобилизованные образцы экспрессирующих GPC3 клеток можно применять для оценки связывающей активности антитела.
Предпочтительные методы скрининга антител, в которых используют связывающую активность в качестве показателя, включают также методы пэннинга, основанные на использовании фаговых векторов. Методы скрининга с использованием фаговых векторов имеют преимущество, когда гены антитела выделяют из библиотек подкласса тяжелой цепи и легкой цепи из популяции клеток, экспрессирующих поликлональные антитела. Гены, кодирующие вариабельные области тяжелой цепи и легкой цепи, можно сшивать с помощью приемлемой линкерной последовательности с образованием одноцепочечного Fv (scFv). Фаги, презентирующие на своей поверхности scFv, можно получать путем встраивания гена, кодирующего scFv, в фаговый вектор. Фаги приводят в контакт с представляющим интерес антигеном. Затем ДНК, кодирующую scFv, который обладает представляющей интерес связывающей активностью, можно выделять путем сбора фагов, связанных с антигеном. Указанный процесс можно повторять при необходимости для обогащения scFv, которые обладают представляющей интерес связывающей активностью.
После выделения кДНК, кодирующей V-область представляющего интерес антитела к GPC3, кДНК расщепляют рестриктазами, которые распознают сайты рестрикции, интродуцированные в оба конца кДНК. Предпочтительные рестриктазы распознают и расщепляют нуклеотидную последовательность, которая встречается с низкой частотой в нуклеотидной последовательности гена антитела. Кроме того, для встраивания однокопийного расщепленного фрагмента в правильной ориентации предпочтительно интродуцируют в представляющий интерес вектор сайт рестрикции для фермента, который образует «липкий» конец. Кодирующую V-область антитела к GPC3 кДНК расщепляют согласно описанному выше методу и встраивают в приемлемый экспрессионный вектор для создания экспрессионного вектора антитела. В том случае, когда ген, кодирующий константную область (С-область) антитела, и ген, кодирующий указанную выше V-область, сливают в рамке считывания, то получают химерное антитело. В контексте настоящего описания «химерное антитело» означает, что константная область и вариабельная область отличаются по своему происхождению. Так, помимо мышиных/человеческих гетерохимерных антител к химерным антителам, предлагаемым в настоящем изобретении, относятся также человеческие/человеческие аллохимерные антитела. Экспрессионный вектор химерного антитела можно создавать путем встраивания указанного выше гена V-области в экспрессионный вектор, который уже содержит константную область. В частности, например, последовательность, распознаваемую рестриктазой, которая вырезает указанный выше ген V-области, предпочтительно следует помещать в 5'-область экспрессионного вектора, несущего ДНК, которая кодирует константную область (С-область) требуемого антитела. Экспрессионный вектор химерного антитела создают путем слияния в рамке считывания двух генов, расщепленных одной и той же комбинацией рестриктаз.
Для получения моноклонального антитела к GPC3 гены антитела встраивают в экспрессионный вектор таким образом, чтобы экспрессия генов происходила под контролем регулирующей экспрессию области. Регулирующая экспрессию область, предназначенная для экспрессии антител, включает, например, энхансеры и промоторы. Кроме того, соответствующую сигнальную последовательность можно присоединять к аминоконцу таким образом, чтобы антитело секретировалось из клеток наружу. В описанных ниже примерах в качестве сигнальной последовательности применяют пептид, который имеет аминокислотную последовательность MGWSCIILFLVATATGVHS (SEQ ID NO: 3). Наряду с ней можно присоединять другие приемлемые сигнальные последовательности. Экспрессированный полипептид расщепляется на карбоксильном конце указанной выше последовательности и образовавшийся полипептид секретируется из клеток наружу в виде зрелого полипептида. Затем приемлемые клетки-хозяева трансформируют экспрессионным вектором и получают рекомбинантные клетки, экспрессирующие ДНК, которая кодирует антитело к GPC3.
ДНК, которые кодируют тяжелую цепь антитела (Н-цепь) и легкую цепь антитела (L-цепь), встраивают по отдельности в различные экспрессионные векторы для экспрессии гена антитела. Молекулу антитела, имеющую Н- и L-цепи, можно экспрессировать, осуществляя для этой цели контрансфекцию одной и той же клетки-хозяина векторами, в которые встроены соответственно гены Н-цепи и L-цепи. В качестве альтернативы, клетки-хозяева можно трансформировать одним экспрессионным вектором, в который встроены ДНК, кодирующие Н- и L-цепи (см. WO 94/11523).
Известны различные комбинации клеток-хозяев/экспрессионных векторов для получения антитела путем интродукции выделенных генов антител в соответствующих хозяев. Все эти системы экспрессии можно применять для выделения антигенсвязывающих доменов, включая вариабельные области антитела, предлагаемого в настоящем изобретении. Приемлемыми эукариотическими клетками, которые применяют в качестве клеток-хозяев, являются клетки животных, клетки растений и клетки грибов. В частности, клетки животных представляют собой, например, следующие клетки:
(1) клетки млекопитающих: СНО, COS, миеломы, почки детеныша хомяка (BHK), HeLa, Vero или т.п.;
(2) клетки амфибий: ооциты шпорцевой лягушки (Xenopus) или т.п. и
(3) клетки насекомых: sf9, sf21, Tn5 или т.п.
Кроме того, в качестве растительной клетки известна система экспрессии генов антитела, в которой используют клетки, полученные из представителей рода Nicotiana, например, Nicotiana tabacum. Для трансформации растительных клеток можно применять культивированные клетки каллуса.
Кроме того, следующие клетки можно применять в качестве грибных клеток:
дрожжи: рода Saccharomyces, например, Saccharomyces cerevisiae, и рода Pichia, например, Pichia pastoris, и
нитчатые грибы: рода Aspergillus, например, Aspergillus niger.
Кроме того, известны системы экспрессии генов антитела, в которых используют прокариотические клетки. Например, согласно настоящему изобретению можно применять бактериальные клетки, т.е. клетки Е. coli, клетки Bacillus subtilis и т.п. Экспрессионные векторы, которые несут представляющие интерес гены антитела, интродуцируют в эти клетки путем трансфекции. Трансфектированные клетки культивируют in vitro, и требуемое антитело можно получать из культуры трансформированных клеток.
Помимо указанных выше клеток-хозяев для получения рекомбинантного антитела можно применять также трансгенных животных. Это означает, что антитело можно получать из животного, в организм которого интродуцирован ген, кодирующий представляющее интерес антитело. Например, ген антитела можно создавать в виде слитого гена посредством встраивания в рамке считывания в ген, который кодирует белок, специфически образующийся в молоке. В качестве белка, секретируемого в молоко, можно применять, например, козий β-казеин. ДНК-фрагменты, содержащие слитый ген, в который входит ген антитела, инъецируют в эмбрион козы и затем этот эмбрион интродуцируют в самку козы. Требуемые антитела можно получать в виде белка, слитого с молочным белком из молока трансгенной козы, родившейся от козы, являющейся реципиентом эмбриона (или ее потомства). Кроме того, для увеличения объема молока, содержащего требуемое антитело, которое продуцируется трансгенной козой, трансгенной козе можно при необходимости вводить гормоны (Ebert K.М. и др., Bio/Technology 12 (7), 1994, cc. 699-702).
Когда антигенсвязывающую молекулу, представленную в настоящем описании, вводят человеку, то в качестве домена антигенсвязывающей молекулы можно применять домен, происходящий из антитела, полученного путем генетической рекомбинации, которое искусственно модифицировано для снижения гетерологичной антигенности в отношении человека и других животных. Указанные антитела, полученные путем генетической рекомбинации, включают, например, гуманизированные антитела. Эти модифицированные антитела можно получать с помощью известных методов.
Вариабельная область антитела, применяемая для получения домена антигенсвязывающей молекулы, который включает вариабельную область антитела, представленного в настоящем описании, как правило, состоит из трех гипервариабельных участков (CDR), разделенных четырьмя каркасными участками (FR). CDR представляет собой область, которая в значительной степени определяет специфичность связывания антитела. Для аминокислотных последовательностей CDR характерна высокая степень вариабельности. С другой стороны, образующие FR аминокислотные последовательности часто обладают высокой идентичностью даже среди антител с различными специфичностями связывания. Таким образом, как правило, путем трансплантации CDR специфичность связывания конкретного антитела можно интродуцировать в другое антитело.
Гуманизированное антитело называют также реконструированным человеческим антителом. В частности, известны гуманизированные антитела, полученные путем трансплантации CDR антитела животного кроме человека, такого как мышиное антитело, в человеческое антитело и т.п. Известны также общепринятые методики генной инженерии, предназначенные для получения гуманизированных антител. В частности, например, ПЦР с перекрывающимися праймерами представляет собой известный метод трансплантации CDR мышиного антитела в человеческий FR. При осуществлении ПЦР с перекрывающимися праймерами нуклеотидную последовательность, которая кодирует CDR мышиного антитела, подлежащий трансплантации, добавляют к праймерам, предназначенным для синтеза FR человеческого антитела. Получают праймеры для каждого из четырех FR. Принято считать, что когда осуществляют трансплантацию мышиного CDR в человеческий FR, то для поддержания функции CDR целесообразно выбирать человеческий FR, обладающий высоким уровнем идентичности с мышиным FR. Таким образом, как правило, является предпочтительным применять человеческий FR, который содержит аминокислотную последовательность, обладающую высоким уровнем идентичности с аминокислотной последовательностью FR, который примыкает к подлежащему трансплантации мышиному CDR.
Нуклеотидные последовательности, подлежащие лигированию, создают таким образом, чтобы они были соединены друг с другом в рамке считывания. Человеческие FR синтезируют индивидуально с использованием соответствующих праймеров. В результате получают продукты, в которых ДНК, кодирующая мышиный CDR, присоединена к ДНК, кодирующим индивидуальные FR. Нуклеотидные последовательности, кодирующие мышиный CDR каждого продукта, создают таким образом, чтобы они перекрывались друг с другом. Затем осуществляют реакцию синтеза комплементарной цепи для «отжига» перекрывающихся CDR-участков продуктов, синтезированных с использованием гена человеческого антитела в качестве матрицы. С помощью этой реакции человеческие FR встраивают путем лигирования через мышиные CDR-последовательности.
Полноразмерный ген V-области, в которую, в конце концов, лигированы три CDR и четыре FR, амплифицируют с использованием праймеров, гибридизующихся с 5'- или 3'-концом, которые добавляют с последовательностями, распознаваемыми приемлемыми рестриктазами. Экспрессионный вектор для гуманизированного антитела можно получать путем встраивания полученной согласно описанному выше методу ДНК и ДНК, которая кодирует С-область человеческого антитела, в экспрессионный вектор таким образом, чтобы лигировать их в рамке считывания. После трансфекции хозяина рекомбинантным вектором для создания рекомбинантных клеток рекомбинантные клетки культивируют и ДНК, кодирующую гуманизированное антитело, экспрессируют с получением гуманизированного антитела в культуре клеток (см. публикацию европейского патента ЕР 239400 и публикацию международной заявки на патент WO 1996/002576). Путем качественной или количественной оценки и измерения антигенсвязывающей активности гуманизированного антитела, полученного согласно описанному выше методу, можно отбирать FR человеческого антитела, которые позволяют CDR образовывать предпочтительный антигенсвязывающий центр при лигировании с использованием CDR. Аминокислотные остатки в FR при необходимости можно заменять так, чтобы CDR реконструированного человеческого антитела образовывали приемлемый антигенсвязывающий центр. Например, мутации аминокислотной последовательности можно интродуцировать в FR, используя ПЦР-метод, применяемый для трансплантации мышиного CDR в человеческий FR. Более конкретно, мутации неполной нуклеотидной последовательности можно интродуцировать в праймеры, гибридизующиеся с FR. Мутации нуклеотидной последовательности интродуцируют в FR, синтезированные с использованием указанных праймеров. Мутантные последовательности FR, имеющие требуемые характеристики, можно отбирать путем измерения и оценки активности мутантного антитела с аминокислотной заменой в отношении связывания с антигеном с помощью упомянутого выше метода (Sato K. и др.. Cancer Res. 53, 1993, cc. 851-856).
В качестве альтернативы, требуемые человеческие антитела можно получать путем иммунизации трансгенных животных, имеющих полный спектр генов человеческого антитела (см. WO 1993/012227; WO 1992/003918; WO 1994/002602; WO 1994/025585; WO 1996/034096; WO 1996/033735), с использованием ДНК-иммунизации.
Кроме того, известны методики получения человеческих антител путем пэннинга с использованием библиотек человеческих антител. Например, V-область человеческого антитела экспрессируют в виде одноцепочечного антитела (scFv) на поверхности фага с использованием метода фагового дисплея. Можно отбирать фаги, экспрессирующие scFv, который связывается с антигеном. Последовательность ДНК, кодирующую V-область человеческого антитела, которая связывается с антигеном, можно определять путем анализа генов отобранных фагов. Определяют последовательность ДНК scFv, который связывается с антигеном. Экспрессионный вектор получают путем слияния последовательности V-области в рамке считывания с последовательностью С-области требуемого человеческого антитела и последующего встраивания в приемлемый экспрессионный вектор. Экспрессионный вектор интродуцируют в клетки, пригодные для указанной выше экспрессии. Человеческое антитело можно получать путем экспрессии гена, кодирующего человеческое антитело, в клетках. Такие методы уже описаны (см. WO 1992/001047; WO 1992/020791; WO 1993/006213; WO 1993/011236; WO 1993/019172; WO 1995/001438; WO 1995/015388).
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3 (GPC3)
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3 (GPC3)» относится к области антитела, которая содержит область, которая специфически связывается с описанным выше белком GPC3 или со всем или с участком неполного пептида белка GPC3, и является также комплементарной ему. Домены, содержащие вариабельную область антитела, можно получать из вариабельных доменов одного или множества антител. Предпочтительно домены, содержащие вариабельную область антитела, содержат вариабельные области легкой цепи и тяжелой цепи (VL и VH) антитела. Приемлемыми примерами таких доменов, содержащих вариабельные области антитела, являются «одноцепочечный Fv (scFv)», «одноцепочечное антитело», «Fv», «одноцепочечный Fv2 (scFv2)», «Fab», «F(ab')2» и т.д.
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора» относится к области антитела, которая содержит область, которая специфически связывается со всем или с участком комплекса Т-клеточного рецептора, и является также комплементарной ему. Комплекс Т-клеточного рецептора может представлять собой сам Т-клеточный рецептор или адапторную молекулу, которая входит в комплекс Т-клеточного рецептора наряду с Т-клеточным рецептором. Пригодной в качестве адапторной молекулы является CD3.
Домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении Т-клеточного рецептора
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении Т-клеточного рецептора» относится к области антитела, связывающейся с Т-клеточным рецептором, полученной путем включения области, которая специфически связывается со всем или с участком Т-клеточного рецептора и является также комплементарной ему.
Участок Т-клеточного рецептора, с которым связывается домен, предлагаемый в настоящем изобретении, может представлять собой вариабельную область или константную область, но предпочтительным является эпитоп, присутствующий в константной области. Примеры последовательности константной области включают α-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq. CAA26636.1 (SEQ ID NO: 4), β-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq C25777 (SEQ ID NO: 5), γ1-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq А26659 (SEQ ID NO: 6), γ2-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq AAB63312.1 (SEQ ID NO: 7), и δ-цепь Т-клеточного рецептора, которая имеет регистрационный № RefSeq AAA61033.1 (SEQ ID NO: 8).
Домен, содержащий вариабельную область антитела, которая обладает CD3-связывающей активностью
В контексте настоящего описания фраза «домен, содержащий вариабельную область антитела, которая обладает CD3-связывающей активностью» относится к CD3-связывающему участку антитела, который получают путем включения области, которая специфически связывается со всем или с участком CD3, и который является также комплементарным ему.
Предпочтительно домен содержит вариабельные области легкой цепи и тяжелой цепи (VL и VH) антитела к CD3. Приемлемыми примерами такого домена являются «одноцепочечный Fv (scFv)», «одноцепочечное антитело», «Fv», «одноцепочечный Fv2 (scFv2)», «Fab», «F(ab')2» и т.д.
Предлагаемый в изобретении домен, содержащий вариабельную область антитела, которая обладает CD3-связывающей активностью, может представлять собой любой эпитопсвязывающий домен, если эпитоп присутствует в последовательности γ-цепи, δ-цепи или ε-цепи, образующей человеческий CD3. Предпочтительно в настоящем изобретении можно использовать домен, содержащий вариабельную область легкой цепи (VL) антитела к CD3, и вариабельную область тяжелой цепи (VH) антитела к CD3, которые связываются с эпитопом, присутствующим во внеклеточной области ε-цепи комплекса человеческого CD3. Помимо вариабельной области легкой цепи (VL) антитела к CD3, и вариабельной области тяжелой цепи (VH) антитела к CD3, которые описаны в разделе «Примеры», известные CD3-связывающие домены, которые содержат вариабельную область легкой цепи (VL) антитела к CD3, и вариабельную область тяжелой цепи (VH) антитела к CD3 и полученные из антитела OKT3 (Proc. Natl. Acad. Sci. USA 77, 1980, cc. 4914-4917), можно применять в качестве указанных доменов. Соответственно можно применять содержащий вариабельную область антитела домен, полученный из антитела к CD3, которое обладает требуемыми свойствами, созданное путем иммунизации требуемого животного с использованием описанного выше метода γ-цепью, δ-цепью или ε-цепью, образующей человеческий CD3. Человеческие антитела и соответствующим образом гуманизированные антитела можно применять соответственно в качестве антитела к CD3 для создания домена, содержащего вариабельную область антитела, который обладает CD3-связывающей активностью. Что касается структуры γ-цепи, δ-цепи или ε-цепи, образующей человеческий CD3, то их полинуклеотидные последовательности представлены в SEQ ID NO: 9 (NM_000073.2), 10 (NM_000732.4) и 11 (NM_000733.3), а их полипептидные последовательности представлены в SEQ ID NO: 12 (NP_000064.1), 13 (NP_000723.1) и 14 (NP_000724.1) (в скобках указаны регистрационные номера в базе данных RefSeq).
Домены, содержащие вариабельные области антитела, в антигенсвязывающих молекулах, предлагаемых в настоящем изобретении, могут связываться с одним и тем же эпитопом. В контексте настоящего описания один и тот же эпитоп может присутствовать в белке, который содержит аминокислотную последовательность SEQ ID NO: 2 или 14. Альтернативно этому, домены, содержащие вариабельные области антитела, в антигенсвязывающих молекулах, предлагаемых в настоящем изобретении, могут связываться с различными эпитопами соответственно. В контексте настоящего описания различные эпитопы могут присутствовать в белке, который содержит аминокислотную последовательность SEQ ID NO: 2 или 14.
Специфичность
Понятие «специфичность» означает, что одна из молекул, участвующих в специфическом связывании, не обладает какой-либо значимой способностью связываться с молекулами, отличными от одного или нескольких партнеров по связыванию молекул. Кроме того, понятие используют также, когда домен, содержащий вариабельную область антитела, является специфическим в отношении конкретного эпитопа из нескольких эпитопов, входящих в антиген. Когда эпитоп, с которым связывается домен, содержащий вариабельную область антитела, входит в несколько различных антигенов, то антигенсвязывающие молекулы, содержащие домен, включающий вариабельную область, могут связываться с различными антигенами, которые содержат эпитоп.
Эпитоп
«Эпитоп» означает антигенную детерминанту в антигене и относится к антигенному сайту, с которым связывается представленный в настоящем описании домен антигенсвязывающей молекулы, включающий вариабельную область антитела. Так, например, эпитоп можно характеризовать на основе его структуры. Альтернативно этому, эпитоп можно характеризовать на основе антигенсвязывающей активности антигенсвязывающей молекулы, которая распознает эпитоп. Когда антиген представляет собой пептид или полипептид, то эпитоп можно определять по аминокислотным остаткам, образующим эпитоп. Альтернативно этому, когда эпитоп представляет собой сахарную цепь, то эпитоп можно определять по специфической для него структуре сахарной цепи.
Линейный эпитоп представляет собой эпитоп, который содержит эпитоп, у которого распознается первичная аминокислотная последовательность. Указанный линейный эпитоп, как правило, содержит по меньшей мере три и наиболее часто по меньшей мере пять, например, примерно от 8 до 10 или от 6 до 20 аминокислотных остатков в определенной последовательности.
В отличие от линейного эпитопа «конформационный эпитоп» представляет собой эпитоп, в котором первичная аминокислотная последовательность, образующая эпитоп, не является единственной детерминантой распознаваемого эпитопа (например, не является обязательным, чтобы первичная аминокислотная последовательность конформационного эпитопа распознавалась специфическим в отношении эпитопа антителом). Конформационные эпитопы могут содержать большее количество аминокислотных остатков по сравнению с линейными эпитопами. Распознающее конформационный эпитоп антитело распознает трехмерную структуру пептида или белка. Например, когда белковая молекула уложена и образует трехмерную структуру, аминокислоты и/или полипептидные основные цепи, которые образуют конформационный эпитоп, выравниваются, и эпитоп становится распознаваемым для антитела. Методы определения конформаций эпитопов включают (но не ограничиваясь только ими), например, рентгеновскую кристаллографию, двухмерный ядерный магнитный резонанс, сайтспецифическое спиновое мечение и электронный парамагнитный резонанс (см., например, Epitope Mapping Protocols in Methods in Molecular Biology, под ред. Morris, т. 66, 1996).
Пример метода оценки связывания эпитопа тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, описан ниже, и метод, подтверждающий связывание с эпитопом тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, можно осуществлять также согласно приведенным ниже примерам.
Например, для подтверждения того, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает линейный эпитоп в молекуле GPC3, можно применять описанный ниже метод. Для указанной выше цели синтезируют линейный пептид, содержащий аминокислотную последовательность, образующую внеклеточный домен GPC3. Пептид можно синтезировать химически. Альтернативно этому, его можно получать с помощью методов генной инженерии, используя область в кДНК GPC3, которая кодирует аминокислотную последовательность, соответствующую внеклеточному домену. Затем оценивают связывающую активность между линейным пептидом, который содержит аминокислотную последовательность, образующую внеклеточный домен, и тестируемой антигенсвязывающей молекулой, содержащей домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью. Например, иммобилизованный линейный пептид можно применять в качестве антигена при осуществлении ELISA для оценки связывающей активности антигенсвязывающей молекулы в отношении пептида. Альтернативно этому, связывающую активность в отношении линейного пептида можно оценивать по уровню ингибирования линейным пептидом связывания антигенсвязывающей молекулы с экспрессирующими GPC3 клетками. Эти анализы могут демонстрировать связывающую активность антигенсвязывающих молекул в отношении линейного пептида.
Кроме того, для подтверждения того, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает трехмерную структуру эпитопа, можно применять следующий метод. Для указанной выше цели получают экспрессирующие GPC3 клетки. Считается, что тестируемая антигенсвязывающая молекула, содержащая домен, который содержит вариабельную область антитела, обладающую GPC3-связывающей активностью, распознает конформационный эпитоп, если она при контакте отличается сильным связыванием с экспрессирующими GPC3 клетками, но в незначительной степени связывается с иммобилизованным линейным пептидом, который содержит аминокислотную последовательность, образующую внеклеточный домен GPC3. В контексте настоящего описания «связывается в незначительной степени» означает, что активность связывания составляет 80% или менее, как правило, 50% или менее, предпочтительно 30% или менее и наиболее предпочтительно 15% или менее по сравнению с активностью связывания с клетками, экспрессирующими человеческий GPC3.
Методы анализа связывающей активности тестируемой антигенсвязывающей молекулы, содержащей домен, который связывается с антигеном GPC3, в отношении экспрессирующих GPC3 клеток, включают, например, методы, описанные в: Antibodies: A Laboratory Manual (под ред. Harlow, David Lane, изд-во Cold Spring Harbor Laboratory, 1988, cc. 359-420). В частности, оценку можно осуществлять на основе принципа ELISA или метода разделения клеток на основе возбуждения флуоресценции (FACS) с использованием в качестве антигена экспрессирующих GPC3 клеток.
В формате ELISA связывающую активность тестируемой антигенсвязывающей молекулы, содержащей домен, который связывается с антигеном GPC3, в отношении экспрессирующих GPC3 клеток, можно оценивать количественно путем сравнения уровней сигналов, возникающих в процессе ферментативной реакции. В частности, тестируемую антигенсвязывающую молекулу добавляют в планшет для ELISA, на котором иммобилизованы экспрессирующие GPC3 клетки. Затем тестируемую антигенсвязывающую молекулу, связанную с клетками, выявляют с помощью меченного ферментом антитела, которое распознает тестируемую антигенсвязывающую молекулу. Альтернативно этому, когда применяют FACS, приготавливают серийные разведения тестируемой антигенсвязывающей молекулы и титр антитела, связывающегося с экспрессирующими GPC3 клетками, можно определять путем сравнения активности связывания с экспрессирующими GPC3 клетками.
Связывание тестируемой антигенсвязывающей молекулы с антигеном, который экспрессируется на поверхности клеток, суспендированных в буфере или в сходной среде, можно выявлять с помощью проточного цитометра. Известными проточными цитометрами являются, например, следующие устройства:
FACSCanto™ II,
FACSAria™,
FACSArray™,
FACSVantage™ SE
FACSCalibur™ (все товарные знаки фирмы BD Biosciences),
EPICS ALTRA HyPerSort,
Cytomics FC 500,
EPICS XL-MCL ADC EPICS XL ADC,
Cell Lab Quanta/Cell Lab Quanta SC (все товарные знаки фирмы Beckman Coulter).
Предпочтительные методы анализа связывающей активности тестируемой антигенсвязывающей молекулы, содержащей связывающей антиген GPC3 домен, в отношении антигена включают, например, следующий метод. Сначала экспрессирующие GPC3 клетки подвергают взаимодействию с тестируемой антигенсвязывающей молекулой, а затем ее окрашивают меченным с помощью ФИТЦ вторичным антителом, которое распознает полипептидный комплекс. Тестируемую антигенсвязывающую молекулу соответствующим образом разводят приемлемым буфером с получением комплекса в требуемой концентрации. Например, комплекс можно применять в концентрации, составляющей от 10 мкг/мл до 10 нг/мл. Затем определяют интенсивность флуоресценции и количество клеток с помощью FACSCalibur (фирма BD). Интенсивность флуоресценции, определенная с помощью анализов на основе программы CELL QUEST (фирма BD), а именно, выраженная в виде средних геометрических значений, отражает уровень связывания антитела с клетками. Это означает, что активность связывания тестируемой антигенсвязывающей молекулы, которая характеризуется количеством связанной тестируемой антигенсвязывающей молекулы, можно оценивать, определяя среднее геометрическое значение.
Имеет ли тестируемая антигенсвязывающая молекула, которая содержит домен, связывающий антиген GPC3, общий эпитоп с другой антигенсвязывающей молекулой, можно оценивать по конкуренции между двумя комплексами в отношении одного и того же эпитопа. Конкуренцию между антигенсвязывающими молекулами можно определять путем анализа перекрестной блокады или с помощью сходного анализа. Например, предпочтительным анализом перекрестной блокады является конкурентный ELISA-анализ.
В частности, при осуществлении анализа перекрестной блокады белок GPC3, иммобилизованный в лунках титрационного микропланшета, предварительно инкубируют в присутствии антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, или без нее, а затем вносят тестируемую антигенсвязывающую молекулу. Количество связанной с белком GPC3 тестируемой антигенсвязывающей молекулы в лунках находится в обратной корреляции с активностью связывания антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, который конкурирует за связывание с одним и тем же эпитопом. Это означает, что чем выше аффинность антигенсвязывающей молекулы, рассматриваемой в качестве конкурента-кандидата, к одному и тому же эпитопу, тем ниже активность связывания тестируемой антигенсвязывающей молекулы с сенсибилизированными белком GPC3 лунками.
Количество тестируемой антигенсвязывающей молекулы, связанной через белок GPC3 с лунками, легко определять путем предварительного мечения антигенсвязывающей молекулы. Например, меченную биотином антигенсвязывающую молекулу оценивают с использованием конъюгата авидин/пероксидаза и соответствующего субстрата. В частности, анализ перекрестной блокады, в котором применяют в качестве меток ферменты, такие как пероксидаза, называют «ELISA-анализом в конкурентных условиях (конкурентный анализ)». Антигенсвязывающую молекулу можно метить также с помощью других предназначенных для мечения субстанций, которые можно выявлять или оценивать. В частности, известны радиоактивные метки, флуоресцентные метки и т.п.
Когда антигенсвязывающая молекула, рассматриваемая в качестве конкурента-кандидата, может блокировать связывание тестируемой антигенсвязывающей молекулы, которая содержит домен, связывающий антиген GPC3, по меньшей мере на 20%, предпочтительно по меньшей мере на 20-50% и предпочтительно по меньшей мере на 50% по сравнению со связывающей активностью, установленной в контрольном эксперименте, который проводят в отсутствии антигенсвязывающей молекулы, рассматриваемой в качестве конкурента, то считается, что для тестируемой антигенсвязывающей молекулы характерна выраженная способность к связыванию с тем же эпитопом, с которым связывается антигенсвязывающая молекула, рассматриваемая в качестве конкурента, или она конкурирует за связывание с тем же самым эпитопом.
Если структура эпитопа, связанного с тестируемой антигенсвязывающей молекулой, которая содержит домен, связывающий антиген GPC3, уже идентифицирована, то для решения вопроса о том, имеют ли тестируемая и контрольная антигенсвязывающие молекулы один и тот же эпитоп, можно сравнивать связывающие активности двух антигенсвязывающих молекул с пептидом, полученным путем интродукции аминокислотных мутаций в пептид, образующий эпитоп.
Для оценки указанных выше связывающих активностей, например, сравнивают связывающие активности тестируемой и контрольной антигенсвязывающих молекул с линейным пептидом, в который интродуцирована мутация, с помощью указанного выше формата ELISA. Помимо метода ELISA связывающую активность в отношении мутантного пептида, связанного с колонкой, можно определять, пропуская через колонку тестируемую и контрольную антигенсвязывающую молекулу и затем оценивая количество антигенсвязывающей молекулы, элюированной в раствор для элюции. Известны методы адсорбции мутантного пептида на колонке, например, в форме слитого с GST пептида.
Альтернативно этому, когда идентифицированный эпитоп представляет собой конформационный эпитоп, то для решения вопроса о том, имеют ли тестируемая и контрольная антигенсвязывающие молекулы общий эпитоп, можно применять следующий метод. Сначала получают экспрессирующие GPC3 клетки и клетки, экспрессирующие GPC3 с мутацией, интродуцированной в эпитоп. Тестируемую и контрольную молекулы добавляют в клеточную суспензию, полученную путем суспендирования этих клеток в приемлемом буфере, таком как ЗФР. Затем клеточные суспензии соответствующим образом промывают буфером и добавляют меченное с помощью ФИТЦ антитело, которое распознает тестируемую и контрольную антигенсвязывающие молекулы. Определяют интенсивность флуоресценции и количество клеток, окрашенных меченым антителом, используя FACSCalibur (фирма BD). Тестируемый и контрольный полипептидные комплексы соответствующим образом разводят приемлемым буфером и применяют в требуемой концентрации. Например, их можно применять в концентрации от 10 мкг/мл до 10 нг/мл. Интенсивность флуоресценции определяют с помощью анализа, для оценки результатов которого применяют программу CELL QUEST (фирма BD), а именно, определяют среднее геометрическое значение, которое отражает количество меченого антитела, связанного с клетками. Это означает, что связывающие активности тестируемой и контрольной антигенсвязывающих молекул, которые характеризуются количеством связанного меченого антитела, можно определять, оценивая среднее геометрическое значение.
При осуществлении описанного выше метода для решения вопроса о том, характерно ли для антигенсвязывающей молекулы «незначительное связывание с клетками, которые экспрессируют мутантный GPC3», можно применять, например, следующий метод. Сначала тестируемую и контрольную антигенсвязывающие молекулы, связанные с клетками, которые экспрессируют мутантный GPC3, окрашивают меченым антителом. Затем определяют интенсивность флуоресценции в клетках. Когда для оценки флуоресценции используют проточный цитометр, то интенсивность флуоресценции можно анализировать с помощью программы CELL QUEST. На основе средних геометрических значений в присутствии антигенсвязывающей молекулы и без нее можно рассчитывать согласно приведенной ниже формуле используемое для сравнения значение (ΔGeo-Mean), характеризующее степень увеличения интенсивности флуоресценции в результате связывания с антигенсвязывающей молекулой.
ΔGeo-Mean = Geo-Mean (в присутствии антигенсвязывающей молекулы)/Сео-Mean (в отсутствии антигенсвязывающей молекулы)
Используемое для сравнения среднее геометрическое значение (значение ΔGeo-Mean для мутантной молекулы GPC3), определенное с помощью описанного выше анализа, которое отражает количество тестируемой антигенсвязывающей молекулы, связанной с клетками, которые экспрессируют мутантный GPC3, сравнивают с относительным значением ΔGeo-Mean, которое отражает количество тестируемой антигенсвязывающей молекулы, связанной с экспрессирующими GPC3 клетками. В этом случае концентрации тестируемой антигенсвязывающей молекулы, применяемые для определения относительных значений ΔGeo-Mean для экспрессирующих GPC3 клеток и клеток, экспрессирующих мутантный GPC3, наиболее предпочтительно регулируют таким образом, чтобы они были одинаковыми или практически одинаковыми. Антигенсвязывающую молекулу, для которой подтверждена способность распознавать эпитоп в GPC3, применяют в качестве контрольной антигенсвязывающей молекулы.
Если используемое для сравнения значение ΔGeo-Mean тестируемой антигенсвязывающей молекулы в отношении клеток, экспрессирующих мутантный GPC3, ниже чем используемое для сравнения значение ΔGeo-Mean тестируемой антигенсвязывающей молекулы в отношении клеток, экспрессирующих GPC3, по меньшей мере на 80%, предпочтительно на 50%, более предпочтительно на 30% и наиболее предпочтительно на 15%, то считают, что тестируемая антигенсвязывающая молекула «незначительно связывается с клетками, которые экспрессируют мутантный GPC3». Формула определения значения Geo-Mean (среднее геометрическое значение) описана в руководстве по применению программы CELL QUEST (фирма BD biosciences). Когда путем сравнения установлено, что относительные значения являются практически эквивалентными, то можно считать, что тестируемая и контрольная антигенсвязывающие молекулы имеют одинаковый эпитоп.
Вариабельный фрагмент (Fv)
В контексте настоящего описания понятие «вариабельный фрагмент (Fv)» относится к минимальной единице полученного из антитела антигенсвязывающего домена, который состоит из пары, включающей вариабельную область легкой цепи антитела (VL) и вариабельную область тяжелой цепи антитела (VH). В 1988 г. Skerra и Pluckthun обнаружили, что гомогенные и активные антитела можно получать из периплазматической фракции Е. coli путем встраивания гена антитела по ходу транскрипции относительно бактериальной сигнальной последовательности и индукции экспрессии гена в Е. coli (Science 240(4855), 1988, cc. 1038-1041). В Fv, полученном из периплазматической фракции, VH ассоциируется с VL таким образом, чтобы связываться с антигеном.
Согласно настоящему описанию Fv предпочтительно включает, например, пару Fv, которые представляют собой антигенсвязывающую молекулу или т.п., содержащую:
(1) двухвалентный антигенсвязывающий домен, который представляет собой двухвалентный scFv, в котором один одновалентный scFv двухвалентного scFv сцеплен с одним полипептидом, образующим Fc-домен, посредством тяжелой цепи Fv-фрагмента, образующего CD3-связывающий домен, а другой одновалентный scFv сцеплен с другим полипептидом, образующим Fc-домен, посредством легкой цепи Fv-фрагмента, образующего CD3-связывающий домен;
(2) домен, содержащий Fc-домен, который не обладает связывающей активностью в отношении Fcγ-рецептора и который получен из аминокислот, образующих Fc-домен IgG1, IgG2a, IgG3 или IgG4, и
(3) по меньшей мере один одновалентный CD3-связывающий домен,
где легкая цепь и тяжелая цепь Fv-фрагментов в результате ассоциации образуют такой CD3-связывающий домен, который может связываться с антигеном CD3.
scFv, одноцепочечное антитело и sc(Fv)2
В контексте настоящего описания понятия «scFv», «одноцепочечное антитело» и «sc(Fv)2» все относятся к фрагменту антитела в виде одной полипептидной цепи, которая содержит вариабельные области, полученные из тяжелой и легкой цепей, но не содержит константную область. Как правило, одноцепочечное антитело содержит также полипептидный линкер между VH- и VL-доменами, позволяющий образовывать требуемую структуру, которая, вероятно, обеспечивает связывание антигена. Одноцепочечное антитело подробно описано у Pluckthun в: «The Pharmacology of Monoclonal Antibodies», т. 113, под ред. Rosenburg и Moore, изд-во Springer- Verlag, New York, 1994, cc. 269-315» (см. также публикацию международного патента WO 1988/001649; US №№4946778 и 5260203). В конкретном варианте осуществления изобретения одноцепочечное антитело может быть биспецифическим и/или гуманизированным.
scFv представляет собой антигенсвязывающий домен, в котором VH и VL, образующие Fv, сцеплены друг с другом с помощью пептидного линкера (Proc. Natl. Acad. Sci. U.S.A. 85(16), 1988, cc. 5879-5883). VH и VL могут удерживаться в непосредственной близости с помощью пептидного линкера.
sc(Fv)2 представляет собой одноцепочечное антитело, в котором четыре вариабельные области двух VL и двух VH сцеплены линкерами такими как пептидные линкеры, с образованием одной цепи (J Immunol. Methods 231(1-2), 1999, cc. 177-189). Две VH и две VL можно получать из различных моноклональных антител. Указанные sc(Fv)2 предпочтительно включают, например, биспецифический sc(Fv)2, распознающий два эпитопа, которые присутствуют в одном антигене, что описано в Journal of Immunology 152(11), 1994, cc. 5368-5374. sc(Fv)2 можно получать методами, известными специалистам в данной области. Например, sc(Fv)2 можно получать путем связывания scFv с помощью линкера, такого как пептидный линкер.
Согласно настоящему описанию к форме антигенсвязывающего домена, образующего sc(Fv)2, относится антитело, в котором две единицы VH и две единицы VL организованы в следующем порядке: VH, VL, VH и VL ([VH]-линкер-[VL]-линкер-[VH]-линкер-[VL]), начиная с N-конца одноцепочечного полипептида. Порядок расположения двух единиц VH и двух единиц VL не ограничен указанной выше формой, и их можно организовывать в любом порядке. Пример порядка расположения в различных формах приведен ниже.
[VL]-линкер-[VH]-линкер-[VH]-линкер-[VL],
[VH]-линкер-[VL]-линкер-[VL]-линкер-[VH],
[VH]-линкер-[VH]-линкер-[VL]-линкер-[VL],
[VL]-линкер-[VL]-линкер-[VH]-линкер-[VH],
[VL]-линкер-[VH]-линкер-[VL]-линкер-[VH].
Молекулярная форма sc(Fv)2 подробно описана также в WO 2006/132352. Таким образом, согласно указанным описаниям специалисты в данной области могут получать требуемый sc(Fv)2, предназначенный для создания антигенсвязывающих молекул, представленных в настоящем описании.
Кроме того, антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, можно конъюгировать с полимером-носителем, таким как ПЭГ, или органическим соединением, таким как противораковое средство. Альтернативно этому, дополнительную последовательность сахарной цепи предпочтительно встраивают в полипептидные комплексы для того, чтобы сахарная цепь обеспечивала требуемое действие.
Линкеры, предназначенные для связывания вариабельных областей антитела, представляют собой произвольные пептидные линкеры, которые можно интродуцировать с помощью генной инженерии, синтетические линкеры и линкеры, описанные, например, в: Protein Engineering, 9(3), 1996, cc. 299-305. Однако для целей настоящего изобретения наиболее предпочтительными являются пептидные линкеры. Длина пептидных линкеров специально не ограничена, и специалисты в данной области могут выбирать ее в зависимости от поставленной задачи. Предпочтительная длина составляет пять или большее количество аминокислот (при этом, верхний предел составляет (но не ограничиваясь только указанным), как правило, вплоть до 30 аминокислот или менее, предпочтительно 20 аминокислот или менее), и наиболее предпочтительно 15 аминокислот. Когда sc(Fv)2 содержит три пептидных линкера, то их длина может быть одинаковой или различной.
Например, указанные пептидные линкеры включают:
Ser,
Gly⋅Ser,
Gly⋅Gly⋅Ser,
Ser⋅Gly⋅Gly,
Gly⋅Gly⋅Gly⋅Ser(SEQ ID NO: 15),
Ser⋅Gly⋅Gly⋅Gly (SEQ ID NO: 16),
Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 17),
Ser⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 18),
Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 19),
Ser⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 20),
Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 21),
Ser⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 22),
(Gly⋅Gly⋅Gly⋅Gly⋅Ser (SEQ ID NO: 17))n,
(Ser⋅Gly⋅Gly⋅Gly⋅Gly (SEQ ID NO: 18))n,
где n обозначает целое число от 1 или более. Специалисты в данной области могут выбирать длину или последовательности пептидных линкеров в зависимости от поставленной задачи.
Как правило, для перекрестного сшивания используют синтетические линкеры (химические перекрестносшивающие агенты), они представляют собой, например:
N-гидроксисукцинимид (NHS),
дисукцинимидилсуберат (DSS),
бис(сульфосукцинимидил)суберат (BS3),
дитиобис(сукцинимидилпропионат) (DSP),
дитиобис(сульфосукцинимидилпропионат) (DTSSP),
этиленгликольбис(сукцинимидилсукцинат) (EGS),
этиленгликольбис(сульфосукцинимидилсукцинат) (сульфо-EGS),
дисукцинимидилтартрат (DST), дисульфосукцинимидилтартрат (сульфо-DST),
бис[2-(сукцинимидоксикарбонилокси)этил]сульфон (BSOCOES) и
и бис[2-(сульфосукцинимидоксикарбонилокси)этил]сульфон (сульфо-BSOCOES). Эти перекрестносшивающие агенты поступают в продажу.
Как правило, требуется три линкера для соединения вместе четырех вариабельных областей антитела. Применяемые линкеры могут быть одного типа или различных типов.
Fab, F(ab')2 и Fab'
«Fab» состоит из одной легкой цепи и СН1-домена и вариабельной области из одной тяжелой цепи. Тяжелая цепь молекулы Fab не может образовывать дисульфидные мостики с тяжелой цепью другой молекулы.
«F(ab')2» или «Fab» получают обработкой иммуноглобулина (моноклональное антитело) протеазой, такой как пепсин и папаин, и они относятся к фрагменту антитела, получаемого расщеплением иммуноглобулина (моноклональное антитело) вблизи дисульфидных мостиков, присутствующих между шарнирными областями в каждой из двух Н-цепей. Например, папаин расщепляет IgG перед дисульфидными мостиками, присутствующими между шарнирными областями в каждой из двух Н-цепей, с образованием двух гомологичных фрагментов антитела, в которых L-цепь, содержащая VL (вариабельная область L-цепи), и CL (константная область L-цепи), сцеплены с фрагментом Н-цепи, содержащим VH (вариабельная область Н-цепи) и CHγ1 (γ1-область в константной области Н-цепи), через дисульфидный мостик в их С-концевых областях. Каждый из указанных двух гомологичных фрагментов антител обозначают как Fab'.
«F(ab')2» состоит из двух легких цепей и двух тяжелых цепей, содержащих в константной области СН1-домен и часть СН2-доменов, в результате между двумя тяжелыми цепями образуются дисульфидные мостики. F(ab')2, образующий антигенсвязывающую молекулу, представленную в настоящем описании, предпочтительно можно получать следующим образом. Полное моноклональное антитело или сходное антитело, содержащее требуемый антигенсвязывающий домен, частично расщепляют протеазой, такой как пепсин; и Fc-фрагменты удаляют путем адсорбции на колонке с белком А. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять полное антитело с образованием F(ab')2 в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Fc-домен
Fc-домен, который образует антигенсвязывающую молекулу, представленнцю в настоящем описании, предпочтительно можно получать следующим образом. Антитело, такое как моноклональное антитело, частично расщепляют протеазой, такой как пепсин. Затем образовавшийся фрагмент адсорбируют на колонке с белком А или белком G и элюируют соответственным буфером для элюции. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять антитела, такие как моноклональные антитела, в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Антигенсвязывающие молекулы, представленные в настоящем описании, содержат Fc-домен с пониженной способностью связывать Fcγ-рецептор, которые включают аминокислоты, образующие Fc-домен IgG1, IgG2, IgG3 или IgG4.
Изотип антитела определяют на основе структуры константной области. Константные области изотипов IgG1, IgG2, IgG3 и IgG4 обозначают как Сγ1, Сγ2, Сγ3 и Сγ4 соответственно. Аминокислотные последовательности Fc-домена полипептидов, которые образуют человеческие Сγ1, Сγ2, Сγ3 и Сγ4, в качестве примера представлены в SEQ ID NO: 23, 24, 25 и 26 соответственно. Взаимосвязь между аминокислотными остатками, образующими каждую аминокислотную последовательность, и EU-нумерацией Кэбота (обозначена в контексте настоящего описания как EU-индекс), представлена на фиг. 12.
Понятие «Fc-домен» относится к области вне F(ab')2, которая содержит две легкие цепи и две тяжелые цепи, содержащие часть константной области, которая включает СН1-домен и область между СН1- и СН2-доменами, что позволяет образовываться дисульфидным мостикам между двумя тяжелыми цепями. Fc-домен, образующий антигенсвязывающую молекулу, представленную в настоящем описании, предпочтительно можно получать следующим образом. Моноклональное антитело в виде IgG1, IgG2, IgG3 или IgG4 или сходное антитело частично расщепляют протеазой, такой как пепсин, с последующей элюцией фракции, адсорбированной на колонке с белком А. Не существует ограничения касательно конкретной протеазы, если она обладает способностью избирательно расщеплять полное антитело с образованием F(ab')2 в соответствующих для данного фермента реакционных условиях, таких как значение рН. Указанные протеазы представляют собой, например, пепсин и фицин.
Fcγ-рецептор
Понятие «Fcγ-рецептор» относится к рецептору, обладающему способностью связываться с Fc-доменом моноклональных антител в виде IgG1, IgG2, IgG3 или IgG4, и оно включает всех представителей, принадлежащих к семейству белков, которые кодируются главным образом геном Fcγ-рецептора. У человека семейство включает FcγRI (CD64), включая изоформы FcγRIa, FcγRIb и FcγRIc; FcγRII (CD32), включая изоформы FcγRIIa (в том числе аллотип Н131 и R131), FcγRIIb (включая FcγRIIb-1 и FcγRIIb-2) и FcγRIIc; и FcγRIII (CD16), включая изоформу FcγRIIIa (в том числе аллотипы V158 и F158),и FcγRIIIb (в той числе аллотипы FcγRIIIb-NA1 и FcγRIIIb-NA2); а также все неидентифицированные человеческие FcγR, изоформы FcγR и их аллотипы. Однако Fcγ-рецептор не ограничен указанными примерами. FcγR включает (но не ограничиваясь только ими) FcγR, полученные из антител человека, мышей, крыс, кроликов и обезьян. FcγR можно получать из любого организма. Мышиный FcγR включает (но не ограничиваясь только ими) FcγRI (CD64), FcγRII (CD32), FcγRIII (CD16) и FcγRIII-2 (CD16-2), а также все неидентифицированные мышиные FcγR, изоформы FcγR и их аллотипы. Указанные предпочтительные Fcγ-рецепторы включают, например, человеческие FcγI (CD64), FcγIIA (CD32), FcγIIB (CD32), FcγIIIA (CD16) и/или FcγIIIB (CD16). Полинуклеотидная последовательность и аминокислотная последовательность FcγI представлены в SEQ ID NO: 27 (NM_000566.3) и 28 (NP_000557.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIA представлены в SEQ ID NO: 29 (BC020823.1) и 30 (ААН20823.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIB представлены в SEQ ID NO: 31 (ВС 146678.1) и 32 (AAI46679.1) соответственно; полинуклеотидная последовательность и аминокислотная последовательность FcγIIIA представлены в SEQ ID NO: 33 (ВС033678.1) и 34 (ААН33678.1) соответственно и полинуклеотидная последовательность и аминокислотная последовательность FcγIIIB представлены в SEQ ID NO: 35 (ВС128562.1) и 36 (AAI28563.1) соответственно (в скобках указан регистрационный номер каждой последовательности в базе данных RefSeq). Обладает ли Fcγ-рецептор способностью связываться с Fc-доменом моноклонального антитела IgG1, IgG2, IgG3 или IgG4, можно оценивать с помощью ALPHA Screen®-анализа (гомогенный анализ усиленной за счет эффекта близости люминесценции (Amplified Luminescent Proximity Homogeneous Assay)), BIACORE-метода на основе поверхностного плазменного резонанса (SPR) и др. (Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010), помимо описанных выше форматов FACS и ELISA.
При этом понятие «Fc-лиганд» или «эффекторный лиганд» относится к молекуле и предпочтительно полипептиду, который связывается с Fc-доменом антитела, образуя комплекс Fc/Fc-лиганд. Молекулу можно получать из любого организма. Связывание Fc-лиганда с Fc предпочтительно индуцирует одну или несколько эффекторных функций. Указанные лиганды включают (но не ограничиваясь только ими) Fc-рецепторы, FcγR, FcαR, FcεR, FcRn, C1q и С3, маннансвязывающий лектин, маннозный рецептор, белок A Staphylococcus, белок G Staphylococcus и вирусные FcγR. Fc-лиганды включают также гомологи Fc-рецептора (FcRH) (Davis и др., Immunological Reviews 190, 2002, cc. 123-136), которые представляют собой семейство Fc-рецепторов, гомологичных FcγR. К Fc-лигандам относятся также неидентифицированные молекулы, которые связываются с Fc.
Активность связывания с Fcγ-рецептором
Нарушение активности связывания Fc-домена с любым из Fcγ-рецепторов FcγI, FcγIIA, FcγIIB, FcγIIIA и/или FcγIIIB можно оценивать, используя описанные выше форматы FACS и ELISA, а также ALPHA Screen-анализ (гомогенный анализ усиленной за счет эффекта близости люминисценции, BIACORE-метод на основе поверхностного плазменного резонанса (SPR) (Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010).
ALPHA Screen-анализ осуществляют на основе технологии ALPHA, которая основана на описанном ниже принципе, с использованием двух типов гранул. Люминисцентный сигнал становится обнаруживаемым только тогда, когда происходит биологическое взаимодействие молекул, связанных с гранулами-донорами, с молекулами, связанными с гранулами-акцепторами, и когда обе гранулы находятся в непосредственной близости друг от друга. Возбужденный лазерным пучком фотосенсибилизатор в гранулах-донорах превращает кислород в возбужденный синглетный кислород. Когда синглетный кислород диффундирует из гранул-доноров и достигает гранул-акцепторов, локализованных в непосредственной близости, то индуцируется хемилюминисцентная реакция в гранулах-акцепторах. В итоге эта реакция приводит к испусканию света. Если молекулы, связанные с гранулами-донорами, не взаимодействуют с гранулами-акцепторами, то синглетный кислород, который продуцируется гранулами-донорами, не достигает гранул-акцепторов и хемилюминисцентная реакция не происходит.
Например, меченную биотином антигенсвязывающую молекулу иммобилизуют на гранулах-донорах, а меченный глутатион-S-трансферазой (GST) Fcγ-рецептор иммобилизуют на гранулах-акцепторах. В отсутствии антигенсвязывающей молекулы, содержащей конкурирующий мутантный Fc-домен, Fcγ-рецептор взаимодействует с антигенсвязывающей молекулой, содержащей Fc-домен дикого типа, индуцируя в результате сигнал с длиной волны от 520 до 620 нм. Антигенсвязывающая молекула, содержащая немеченый мутантный Fc-домен, конкурирует с антигенсвязывающей молекулой, содержащей Fc-домен дикого типа, за взаимодействие с Fcγ-рецептором. Относительную аффинность связывания можно оценивать, определяя количественно снижение флуоресценции в результате конкуренции. Методы биотинилирования антигенсвязывающих молекул, таких как антитела, с помощью сульфо-NHS-биотина или подобных агентов являются известными. Приемлемые методы введения GST-метки в Fcγ-рецептор включают методы, которые предусматривают слияние полипептидов, кодирующих Fcγ и GST, в рамке считывания, экспрессию слитого гена с использованием клеток, в которые интродуцирован вектор, несущий ген, и последующую очистку с помощью содержащей глутатион колонки. Индуцированный сигнал предпочтительно можно анализировать, например, посредством подгонки к односайтовой модели конкуренции на основе нелинейного регрессионного анализа с использованием такой программы, как GRAPHPAD PRISM (фирма GraphPad; Сан-Диего).
Одну из субстанций, предназначенных для исследования их взаимодействия, иммобилизуют в качестве лиганда на тонком слое золота сенсорного чипа. Когда свет проникает на заднюю поверхность сенсорного чипа так, что имеет место полное отражение на границе раздела между тонким слоем золота и стеклом, то интенсивность отраженного света в определенном сайте частично снижается (SPR-сигнал). Другую субстанцию, предназначенную для исследования ее взаимодействия, инъецируют в качестве аналита на поверхность сенсорного чипа. Когда аналит связывается с лигандом, то масса иммобилизованной молекулы-лиганда возрастает. Это изменяет показатель преломления растворителя на поверхности сенсорного чипа. Изменение показателя преломления вызывает положительный сдвиг SPR-сигнала (и наоборот, диссоциация сдвигает сигнал назад в исходное положение). В Biacore-системе уровень описанного выше сдвига (т.е. изменение массы на поверхности сенсорного чипа) откладывают по вертикальной оси, и таким образом в качестве количественных данных получают график изменения массы в зависимости от времени (сенсограмма). Кинетические параметры (константа скорости ассоциации (ka) и константа скорости диссоциации (kd)) определяют из представленных в виде кривых сенсограмм, и определяют аффинность (KD) как соотношение указанных двух констант. BIACORE-методы предпочтительно применяют для анализа ингибирования. Примеры такого анализа ингибирования описаны в Proc. Natl. Acad. Sci. USA 103(11), 2006, cc. 4005-4010.
В контексте настоящего описания «пониженная активность связывания с Fcγ-рецептором» означает, например, что при использовании описанного выше метода анализа конкурентная активность тестируемой антигенсвязывающей молекулы составляет 50% или менее, предпочтительно 45% или менее, 40% или менее, 35% или менее, 30% или менее, 20% или менее или 15% или менее и наиболее предпочтительно 10% или менее, 9% или менее, 8% или менее, 7% или менее, 6% или менее, 5% или менее, 4% или менее, 3% или менее, 2% или менее или 1% менее, по сравнению с конкурентной активностью контрольной антигенсвязывающей молекулы.
Антигенсвязывающие молекулы, содержащие Fc-домен моноклонального антитела в виде IgG1, IgG2, IgG3 или IgG4, можно использовать соответственно в качестве контрольных антигенсвязывающих молекул. Структуры Fc-домена представлены в SEQ ID NO: 37 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААС82527.1), SEQ ID NO: 38 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААВ59393.1), SEQ ID NO: 25 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером САА27268.1) и SEQ ID NO: 39 (А добавлен к N-концу последовательности, представленной в RefSeq под регистрационным номером ААВ59394.1). Кроме того, когда антигенсвязывающую молекулу, содержащую мутантный Fc-домен антитела конкретного изотипа, используют в качестве тестируемой субстанции, то воздействие мутации мутанта на активность связывания с Fcγ-рецептором оценивают с использованием в качестве контроля антигенсвязывающей молекулы, содержащей Fc-домен такого же изотипа. Как описано выше, соответственно получают антигенсвязывающие молекулы, содержащие мутантный Fc-домен с действительно пониженной активностью связывания с Fcγ-рецептором.
Такие известные мутанты включают, например, мутанты с делецией аминокислот 231A-238S (EU-нумерация) (WO 2009/011941), а также мутанты C226S, C229S, P238S, (C220S) (J. Rheumatol 34, 2007, с. 11); C226S и C229S (Hum. Antibod. Hybridomas 1(1), 1990, cc. 47-54); C226S, C229S, Е233Р, L234V, и L235A (Blood 109, 2007, cc. 1185-1192).
В частности, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен с заменой аминокислоты в положении 220, 226, 229, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 264, 265, 266, 267, 269, 270, 295, 296, 297, 298, 299, 300, 325, 327, 328, 329, 330, 331 или 332 (EU-нумерация) в аминокислотах, образующих Fc-домен антитела конкретного изотипа. Изобретение не ограничено изотипом антитела, из которого получают Fc-домен, и можно использовать соответствующий Fc-домен, полученный из моноклонального антитела в виде IgG1, IgG2, IgG3 или IgG4. Предпочтительно следует применять Fc-домен, полученный из антител в виде IgG1.
Предпочтительными антигенсвязывающими молекулами являются, например, молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяется согласно EU-нумерации (каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены), среди аминокислот, образующих Fc-домен антитела в виде IgG1:
(а) L234F,L235E,P331S;
(б) C226S, C229S, P238S;
(в) C226S, C229S;
(г) C226S, C229S, Е233Р, L234V, L235A;
(д) L234A, L235A или L235R, N297A;
(е) L235A или L235R, S239K, N297A,
а также молекулы, которые содержат Fc-домен с делецией аминокислот в положениях 231-238.
Кроме того, предпочтительными антигенсвязывающими молекулами являются также молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG2:
(ж) H268Q, V309L, A330S и P331S;
(з) V234A;
(и) G237A;
(к) V234A и G237A;
(л) А235Е и G237A;
(м) V234A, А235Е и G237A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Кроме того, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG3:
(н) F241A;
(о) D265A;
(п) V264A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Кроме того, предпочтительными антигенсвязывающими молекулами являются молекулы, которые содержат Fc-домен, содержащий одну из указанных ниже замен, положение которой определяют согласно EU-нумерации, среди аминокислот, образующих Fc-домен антитела в виде IgG4:
(р) L235A, G237A и Е318А;
(с) L235E;
(т) F234A и L235A.
Каждый номер обозначает положение аминокислотного остатка согласно EU-нумерации; и однобуквенный символ аминокислоты, который находится перед номером, обозначает аминокислотный остаток до его замены, а однобуквенный символ аминокислоты, расположенный за номером, обозначает аминокислотный остаток после замены.
Другие предпочтительные антигенсвязывающие молекулы представляют собой молекулы, содержащие Fc-домен, в котором любая аминокислота в положении 233, 234, 235, 236, 237, 327, 330 или 331 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена на аминокислоту, которая находится в соответствующем положении согласно EU-нумерации в соответствующем IgG2 или IgG4.
Предпочтительные антигенсвязывающие молекулы представляют собой также молекулы, содержащие Fc-домен, в котором одна или несколько аминокислот в положениях 234, 235 и 297 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена(ы) на другие аминокислоты. Изобретение не ограничено типом аминокислоты после замены; однако наиболее предпочтительными являются антигенсвязывающие молекулы, содержащие Fc-домен, в котором одна или несколько аминокислот в положениях 234, 235 и 297 заменена(ы) на аланин.
Предпочтительные антигенсвязывающие молекулы представляют собой также молекулы, содержащие Fc-домен, в котором аминокислота в положении 265 (EU-нумерация) среди аминокислот, образующих Fc-домен антитела в виде IgG1, заменена другой аминокислотой. Изобретение не ограничено типом аминокислоты после замены; однако наиболее предпочтительными являются антигенасвязывающие молекулы, содержащие Fc-домен, в котором аминокислота в положении 265 заменена на аланин.
Мультиспецифическая антигенсвязывающая молекула
Примеры предпочтительных вариантов «мультиспецифической антигенсвязывающей молекулы», предлагаемой в настоящем изобретении, включают мультиспецифические антитела. Когда Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора применяют в качестве Fc-области мультиспецифического антитела, то соответственно можно применять Fc-область, полученную из мультиспецифического антитела. Биспецифические антитела являются наиболее предпочтительными в качестве мультиспецифических антител, предлагаемых в настоящем изобретении. В этом случае биспецифическое антитело представляет собой антитело, имеющее две различные специфичности. Биспецифические антитела IgG-типа можно секретировать из гибридной гибридомы (квадромы), полученной путем слияния двух типов гибридом, продуцирующих антитело в виде IgG (Milstein С.и др., Nature 305, 1983, cc. 537-540).
Кроме того, биспецифические антитела IgG-типа секретируют посредством интродукции в клетки в целом четырех генов, т.е. генов L-цепей и Н-цепей, образующих представляющие интерес IgG двух типов, и их коэкспрессии. Однако теоретически существует десять комбинаций Н-цепей и L-цепей IgG, которые можно получать такими методами. При этом трудно очищать IgG, состоящий из требуемой комбинации Н-цепей и L-цепей из десяти типов IgG. Кроме того, теоретическое количество секретируемого IgG с требуемой комбинацией, также в значительной степени снижено, поэтому требуется осуществлять крупномасштабное культивирование. Это дополнительно увеличивает стоимость производства.
Таким образом, для мультиспецифических антигенсвязывающих молекул, предлагаемых к настоящем изобретении, можно применять методики, усиливающие ассоциацию между Н-цепями и между L- и Н-цепями, имеющими требуемые комбинации.
Например, методики подавления нежелательной ассоциации Н-цепей путем интродукции электростатического отталкивания на поверхности раздела второго константного участка или третьего константного участка Н-цепи антитела (СН2 или СН3) можно применять для ассоциации мультиспецифического антитела (WO 2006/106905).
При осуществлении метода подавления нежелательной ассоциации Н-цепей путем интродукции электростатического отталкивания на поверхности раздела СН2 или СН3, примеры аминокислотных остатков, контактирующих на поверхности раздела с другим константным участком Н-цепи, включают области, соответствующие остаткам, находящимся согласно EU-нумерации в положениях 356, 439, 357, 370, 399 и 409 в СН3-участке.
Более конкретно, примеры включают антитело, содержащее два типа СН3-участков Н-цепи, в которых 1-3 пары аминокислотных остатков в СН3-участке первой Н-цепи, выбранные из пар аминокислотных остатков, указанных ниже в подпунктах (1)-(3), несут одинаковый типа заряда: (1) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 356 и 439; (2) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 357 и 370; и (3) аминокислотные остатки в СН3-участке Н-цепи, которые находятся согласно EU-нумерации в положениях 399 и 409.
Кроме того, антитело может представлять собой антитело, в котором пары аминокислотных остатков в СН3-участке второй Н-цепи, который отличается от указанного выше СН3-участка первой Н-цепи, выбирают из вышеуказанных в подпунктах (1)-(3) пар аминокислотных остатков, в котором 1-3 пары аминокислотных остатков, которые соответствуют вышеуказанным в подпунктах (1)-(3) парам аминокислотных остатков, несущим такой же тип заряда, что и указанный выше для СН3-участка первой Н-цепи, несут противоположные заряды относительно соответствующих аминокислотных остатков в указанном выше СН3-участке первой Н-цепи.
Соответствующие аминокислотные остатки, указанные выше в подпунктах (1)-(3), при ассоциации располагаются близко друг к другу. Специалисты в данной области могут установить для требуемого СН3-участка Н-цепи или константной области Н-цепи сайты, которые соответствуют вышеуказанным остаткам, указанным в подпунктах (1)-(3), посредством моделирования гомологии и т.п., используя поступающую в продажу программу, и аминокислотные остатки этих сайтов можно подвергать при необходимости модификациям.
В указанных выше антителах «имеющие заряд аминокислотные остатки» предпочтительно выбирают, например, из аминокислотных остатков, которые входят в любую одну из указанных ниже групп (а) и (б):
(а) глутаминовая кислота (Е) и аспарагиновая кислота (D) и
(б) лизин (K), аргинин (R) и гистидин (Н).
Касательно указанных выше антител то, что они «имеют одинаковый тип заряда» означает, например, что два или большее количество аминокислотных остатков все представляют собой аминокислотные остатки, включенные в любую одну из вышеуказанных групп (а) и (б). Понятие «имеют противоположный заряд» означает, например, что, когда по меньшей мере один из двух или большего количества аминокислотных остатков представляет собой аминокислотный остаток, включенный в любую одну из вышеуказанных групп (а) и (б), остальные остатки должны представлять собой аминокислотные остатки, включенные в другую группу.
В предпочтительном варианте вышеуказанного антитела СН3-участок первой Н-цепи и СН3-участок второй Н-цепи могут быть перекрестно сшиты дисульфиднымм мостиками.
Согласно настоящему изобретению аминокислотные остатки, подлежащие изменению, не ограничены аминокислотными остатками константной области или вариабельной области описанного выше антитела. Касательно полипептидных мутантов или гетеромультимеров специалисты в данной области могут установить аминокислотные остатки, которые образуют поверхность раздела, посредством моделирования гомологии и т.п., используя поступающую в продажу программу, и аминокислотные остатки этих сайтов можно подвергать при необходимости изменениям для того, чтобы регулировать ассоциацию.
Другие известные методики можно применять также для ассоциации мультиспецифических антител, предлагаемых в настоящем изобретении. Полипептиды с различными аминокислотами в Fc-области можно эффективно ассоциировать друг с другом путем замены боковой цепи аминокислоты, присутствующей в одной из вариабельных областей Н-цепи антитела, на более крупную боковую цепь («выступ») и замены боковой цепи аминокислоты в соответствующей вариабельной области другой Н-цепи на меньшую боковую цепь («впадина») так, что «выступ» помещается во «впадину» (WO 1996/027011; Ridgway J.B. и др., Protein Engineering 9, 1996, cc. 617-621; Merchant A.M. и др., Nature Biotechnology 16, 1998, cc. 677-681 и US 20130336973).
Кроме того, другие известные методики можно применять также для ассоциации мультиспецифических антител, предлагаемых в настоящем изобретении. Ассоциацию полипептидов, имеющих различные последовательности, можно эффективно индуцировать путем комплементарной ассоциации СН3-областей, используя сконструированный СН3-домен с обменом цепей, полученный путем изменения части СН3 в одной из Н-цепей антитела на соответствующую полученную из IgA последовательность и интродукции в комплементарную часть СН3 в другой Н-цепи соответствующей полученной из IgA последовательности (Protein Engineering Design & Selection, 23, 2010, cc. 195-202). Указанную известную методику можно применять также для эффективного получения представляющих интерес мультиспецифических антител.
Кроме того, для получения мультиспецифических антител можно применять следующие методики: методики получения антител на основе ассоциации СН1 и CL антитела и ассоциации VH и VL, которые описаны в WO 2011/028952, WO 2014/018572 и в Nat Biotechnol. 32(2), февраль 2014 г., сс. 191-198; методики получения биспецифических антител с использованием в комбинации полученных по отдельности моноклональных антител (обмен плечей Fab, (Fab arm exchange, FAE), описанные в WO 2008/119353 и WO 2011/131746; методики регуляции ассоциации между СН3-доменом тяжелых цепей антител, описанные в WO 2012/058768 и WO 2013/063702; методики получения биспецифических антител, состоящих из двух типов легких цепей и одного типа тяжелой цепи, описанные в WO 2012/023053; методики получения биспецифических антител с использованием двух штаммов бактериальных клеток, которые индивидуально экспрессируют одну из цепей антитела, содержащего одну Н-цепь и одну L-цепь, описанные Christoph и др.. Nature Biotechnology т. 31, 2013, cc. 753-758).
Альтернативно этому, даже, если представляющее интерес мультиспецифическое антитело нельзя получать эффективно, мультиспецифическое антитело, предлагаемое в настоящем изобретении, можно получать путем отделения представляющего интерес мультиспецифического антитела от полученных антител и его очистки. Например, описан метод, позволяющий осуществлять очистку двух типов гомомерных форм и представляющего интерес гетеромерного антитела с помощью ионообменной хроматографии, путем установления различия в изоэлектрических точках в результате интродукции аминокислотных замен в вариабельные области двух типов Н-цепей (WO 2007/114325). К настоящему времени в качестве метода для очистки гетеромерных форм описан метод, основанный на применении белка А для очистки гетеродимерного антитела, содержащего Н-цепь мышиного IgG2a, которая связывается с белком А, и Н-цепь крысиного IgG2b, которая не связывается с белком А (WO 98/050431 и WO 95/033844). Кроме того, гетеродимеризованное антитело само можно эффективно очищать с использованием колонки с белком А путем изменения взаимодействия между каждой из Н-цепей и белком А, путем применения Н-цепей, в которых аминокислотные остатки в сайте связывания IgG-белок А в положениях 435 и 436 (EU-нумерация) заменены на аминокислотные остатки, которые обеспечивают другую аффинность связывания с белком А, такие как Tyr, His или т.п., или с использованием Н-цепей с различной аффинностью к белку А, которые получают согласно методу, указанному в приведенном для сравнения примере 5, для изменения взаимодействия каждой из Н-цепей с белком А, и последующего применения колонки с белком А.
Альтернативно этому, можно получать общую L-цепь, которая может обеспечивать способность связываться с множеством различных Н-цепей, и применять в качестве общей L-цепи мультиспецифического антитела. Для достижения эффективной экспрессии мультиспецифического IgG можно интродуцировать в клетки гены указанной общей L-цепи и множества различных Н-цепей и экспрессировать IgG (Nature Biotechnology, 16, 1998, cc. 677-681). Метод селекции общей L-цепи, для которой характерна выраженная способность к связыванию с любыми различными Н-цепями, можно применять также для селекции общей Н-цепи (WO 2004/065611).
Кроме того, Fc-область, отличающуюся улучшенной С-концевой гетерогенностью, можно применять в качестве Fc-области, предлагаемой в настоящем изобретении. Более конкретно, предложены Fc-области, в которых отсутствуют глицин в положении 446 и лизин в положении 447 (EU-нумерация) в аминокислотных последовательностях двух полипептидов, образующих Fc-область, которая происходит из IgG1, IgG2, IgG3 или IgG4.
Несколько, например, две или большее количество, указанных методик можно применять в сочетании друг с другом. Кроме того, эти методики можно соответствующим образом и раздельно применять к двум Н-цепям, подлежащим ассоциации. Кроме того, указанные методики можно применять в комбинации с описанной выше Fc-областью, у которой снижена активность связывания с Fcγ-рецептором. Кроме того, антигенсвязывающая молекула, предлагаемая в настоящем изобретении, может представлять собой молекулу, полученную отдельно на основе антигенсвязывающей молекулы, подвергнутой таким описанным выше модификациям, что она имеет такую же аминокислотную последовательность.
Приемлемая мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, содержит
(1) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении глипикана 3;
(2) домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора; и
(3) домен, содержащий указанную Fc-область с пониженной способностью связываться с Fcγ-рецептором, ее структура не ограничена указанной.
Согласно настоящему изобретению каждый из вышеуказанных доменов может быть сшит непосредственно с помощью пептидных связей. Например, когда применяют F(ab')2 в качестве домена, содержащего вариабельную область антитела, указанного в подпунктах (1) и (2), и указанные Fc-области в качестве домена, содержащего Fc-область с пониженной способностью связываться с Fcγ-рецептором, указанного в подпункте (3), то полипептиды, образованные путем сшивания содержащих вариабельных области доменов, указанных в подпунктах (1) и (2), и содержащего Fc-область домена, указанного в подпункте (3), с помощью пептидных связей, могут образовывать структуру антитела. Такие антитела можно получать путем очистки из указанной выше культуральной среды гибридомы, а также путем очистки антител из культуральной среды требуемых клеток-хозяев, которые стабильно несут полинуклеотиды, кодирующие полипептиды, которые образуют антитело.
Примеры предпочтительной вариабельной области Н-цепи антитела, предлагаемой в настоящем изобретении, содержащееся в вариабельной области антитела со связывающей активностью в отношении глипикана 3, включают вариабельные области Н-цепи антитела, которые представлены в таблице 1, или вариабельные области Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях Н-цепи, которые указаны в таблице 1, или вариабельные области Н-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.

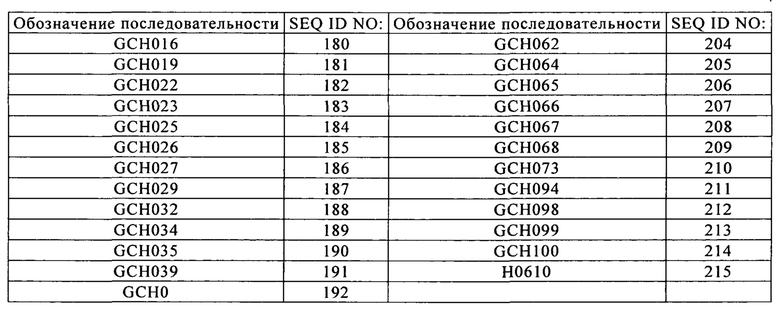
Примеры предпочтительной вариабельной области антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, предлагаемой в настоящем изобретении, включают вариабельные области антитела, обладающие связывающей активностью в отношении Т-клеточного рецептора. Из Т-клеточных рецепторов предпочтительным является CD3, а наиболее предпочтительным CD3ε. Примеры вариабельной области Н-цепи антитела, содержащейся в указанных вариабельных областях антитела, включают вариабельные области Н-цепи антитела, которые представлены в таблице 2, или вариабельные области Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях Н-цепи, которые указаны в таблице 2, или вариабельные области Н-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.
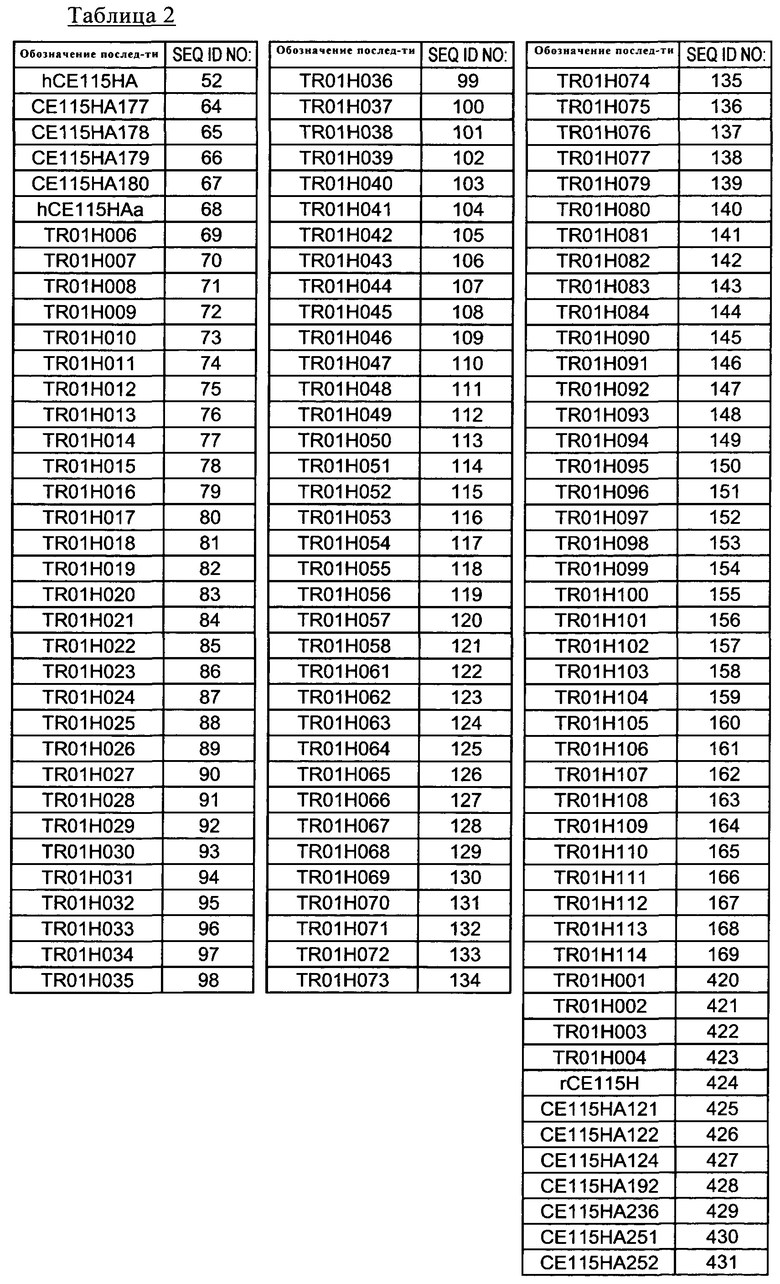
Взаимосвязь между аминокислотными остатками CDR-участков, образующих аминокислотную последовательность Н-цепи антитела, и EU-нумерацией Кэбота, представлена на фиг. 13.
Касательно вариабельных областей L-цепи антитела, содержащихся в вариабельной области антитела, которая обладает связывающей активностью в отношении глипикана 3, и вариабельной области антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, предлагаемых в настоящем изобретении, предпочтительно следует получать общую L-цепь, которая может придавать связывающую активность Н-цепи, которая обладает связывающей активностью в отношении глипикана 3, и связывающую активность Н-цепи, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, и применять ее в качестве вариабельной области общей L-цепи мультиспецифической антигенсвязывающей молекулы.
Примеры вариабельной области общей L-цепи, которую можно применять согласно настоящему изобретению, включают вариабельные области L-цепи, указанные в таблице 3, вариабельные области L-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что аминокислотные последовательности CDR1, CDR2 и CDR3, содержащиеся в вариабельных областях L-цепи антитела, указанных в таблице 3, и вариабельные области L-цепи антитела, которые функционально эквивалентны вышеуказанным вариабельным областям.
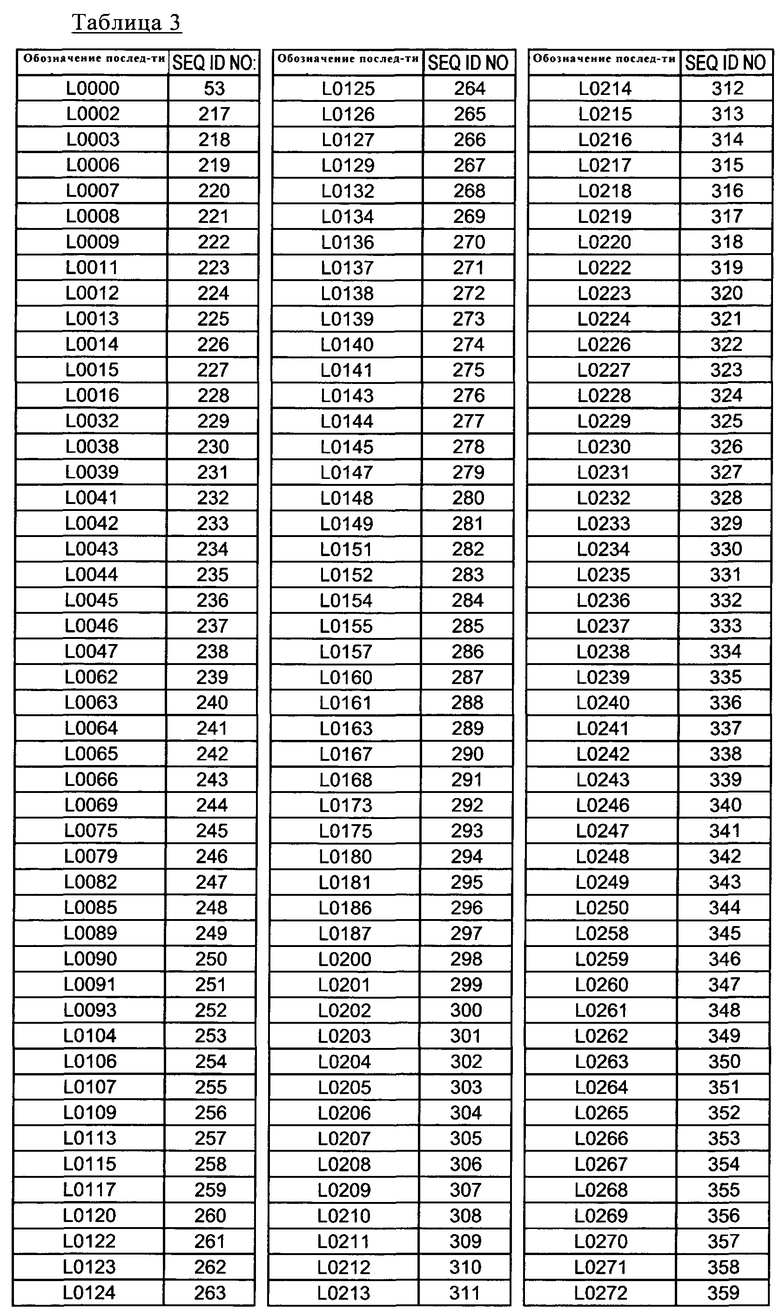
Взаимосвязь между аминокислотными остатками CDR-участков, образующих аминокислотную последовательность L-цепи антитела, и EU-нумерацией Кэбота, представлена на фиг. 14.
В настоящем изобретении фраза «функционально эквивалентный» означает, что аффинности связывания с антигеном эквиваленты или в альтернативном варианте означает, что цитотоксическая активность в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, эквивалентна при примении в качестве мультиспецифической антигенсвязывающей молекулы. Аффиность связывания и цитотоксическую активность можно измерять с помощью метода, указанного в настоящем описании. Клетки, применяемые для измерения цитотоксической активности, могут представлять собой требуемые экспрессирующие GPC3 клетки или требуемую ткань, содержащую указанные клетки, и, например, можно применять человеческие раковые линии клеток и PC-10 или NCI-H446, которые экспрессируют GPC3. Касательно константных областей антитела фраза может означать, что связывающая активность в отношении Fcγ-рецептора является эквивалентной.
Например, фраза «вариабельная область Н-цепи антитела, функционально эквивалентная вариабельной области Н-цепи антитела, указанной в настоящем описании (т.е. исходной вариабельной области Н-цепи)», означает, что эта область имеет такую же аффинность связывания, когда ее объединяют с вариабельной областью L-цепи антитела, указанной в настоящем описании, которая образует пару с исходной Н-цепью, или в альтернативном варианте означает, что область обладает такой же цитотоксической активностью в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, когда ее применяют для получения мультиспецифической антигенсвязывающей молекулы. Кроме того, фраза «вариабельная область L-цепи антитела, функционально эквивалентная вариабельной области L-цепи антитела, указанной в настоящем описании (т.е. исходной вариабельной области L-цепи)», означает, что эта область имеет такую же аффинность связывания, когда ее объединяют с вариабельной областью Н-цепи антитела, указанной в настоящем описании, которая образует пару с исходной L-цепью, или в альтернативном варианте означает, что область обладает такой же цитотоксической активностью в отношении экспрессирующих глипикан 3 клеток или тканей, содержащих указанные клетки, когда ее применяют для получения мультиспецифической антигенсвязывающей молекулы.
Понятие «эквивалентный» не обязательно подразумевает наличие такого же уровня активности, и активность может быть повышенной. В частности, антигенсвязывающая аффинность, включает, например, случай, в котором коэффициент (величина KD/величина KD родительского антитела), полученный путем сравнения с аффинностью связывания вариабельной области антитела, которая служит в качестве контроля (величина KD родительского антитела) составляет 1,5 или менее. Коэффициент величина KD/величина KD родительского антитела предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее, или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. Более конкретно, согласно настоящему изобретения коэффициент величина KD/величина KD родительского антитела предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3. Касательно цитотоксической активности, примеры включают случай, в котором коэффциент (скорость ингибирования клеточного роста/скорость ингибирования клеточного роста родительским антителом), полученный путем сравнения со скоростью ингибирования роста клетки мультиспецифической антигенсвязывающей молекулой, которая служит в качестве контроля (скорость ингибирования клеточного роста родительским антителом), составляет 0,7 или более. Концентрацию добавленной мультиспецифической антигенсвязывающей молекулы можно определять соответствующим образом, но предпочтительно она составляет, например 0,01, 0,05, 0,1, 0,5 или 1 нМ; и предпочтительно измерения осуществляют при концентрации 0,05 или 0,1 нМ. Коэффициент скорость ингибирования клеточного роста/скорость ингибирования клеточного роста родительским антителом предпочтительно составляет 0,8 или более, более предпочтительно 0,9 или более, 1,0 или более, 1,2 или более, 1,5 или более, 2 или более, 3 или более, 5 или более, 10 или более или 20 или более. При этом не существует верхнего предела, коэффициент может составлять 10, 102, 103, 104, 105 или 106.
Кроме того, касательно цитотоксической активности примеры включают случай, в котором коэффициент (концентрация, вызывающая ингибирование клеточного роста на 50% / концентрация родительского антитела, вызывающая ингибирование клеточного роста на 50%), полученный путем сравнения с концентрацией исходной мультиспецифической антигенсвязывающей молекулы, вызывающей ингибирование клеточного роста на 50% (концентрация родительского антитела, вызывающая ингибирование клеточного роста на 50%), составляет 1,5 или менее. Концентрация, вызывающая ингибирование клеточного роста на 50%, означает концентрацию мультиспецифической антигенсвязывающей молекулы, необходимую для снижения скорости клеточной пролиферации наполовину по сравнению с вариантом, в котором не добавляют мультиспецифическую антигенсвязывающую молекулу. Коэффициент «концентрация, вызывающая ингибирование клеточного роста на 50%/концентрация родительского антитела, вызывающая ингибирование клеточного роста на 50%» предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. В частности, коэффициент предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3.
Касательно домена, содержащего вариабельную область антитела, которая обладает GPC3-связывающей активностью, величина KD, характеризующая связывание с GPC3 (например, человеческим GPC3) может составлять, например, 5×10-9 М или менее, предпочтительно 4×10-9 М или менее, например, 3×10-9 М или менее, 2×10-9 М или менее, 1×10-9 М или менее, 8×10-10 М или менее, 5×10-10 М или менее, 4×10-10 М или менее, 3×10-10 М или менее, 2×10-10 М или менее, 1×10-10 М или менее, 8×10-11 М или менее, 5×10-11 М или менее, 4×10-11 М или менее, 3×10-11 М или менее, 2×10-11 М или менее, 1×10-11 М или менее, 8×10-12 М или менее, 5×10-12 М или менее, 4×10-12 М или менее, 3×10-12 М или менее, 2×10-12 М или менее, 1×10-12 М или менее, 8×10-13 М или менее, 5×10-13 М или менее, 4×10-13 М или менее, 3×10-13 М или менее, 2×10-13 М или менее или 1×10-13 М или менее.
Касательно домена, содержащего вариабельную область, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, величина KD, характеризующая связывание с человеческим комплексом Т-клеточного рецептора, такого как человеческий Т-клеточный рецептор или более конкретно, например, человеческий CD3ε, может составлять, например, 2×10-7 М или менее, предпочтительно 1,5×10-7 М или менее, например, 1,4×10-7 М или менее, 1,3×10-7 М или менее, 1,2×10-7 М или менее, 1×10-7 М или менее, 3×10-8 М или менее, 2×10-8 М или менее, 1×10-8 М или менее, 8×10-9 М или менее, 5×10-9 М или менее, 4×10-9 М или менее, 3×10-9 М или менее, 2×10-9 М или менее, 1×10-9 М или менее, 8×10-10 М или менее, 5×10-10 М или менее, 4×10-10 М или менее, 3×10-10 М или менее, 2×10-10 М или менее, 1×10-10 М или менее, 8×10-11 М или менее, 5×10-11 М или менее, 4×10-11 М или менее, 3×10-11 М или менее, 2×10-11 М или менее, 1×10-11 М или менее, , 8×10-12 М или менее, 5×10-12 М или менее, 4×10-12 М или менее, 3×10-12 М или менее, 2×10-12 М или менее или 1×10-12 М или менее.
Мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, предпочтительно имеют величины KD, характеризующая связывание с человеческим GPC3 и человеческим комплексом Т-клеточного рецептора (например, с человеческой CD3ε-цепью), которые составляют 5×10-9 М или менее и 2×10-7 М или менее соответственно и более предпочтительно 1×10-9 М или менее и 5×10-8 М или менее соответственно.
В настоящем изобретении вариабельные области антитела, которые являются «функционально эквивалентными» не ограничены конкретными областями, если они представляют собой вариабельные области Н-цепи и/или L-цепи антитела, которые удовлетворяют вышеуказанным требованиям. Примеры таких вариабельных областей антитела включают области, полученные путем интродукции замены, делеции, добавления и/или инсерции одной или нескольких аминокислот (например, 1, 2, 3, 4, 5 или 10 аминокислот) в аминокислотные последовательности вариабельных областей, которые представлены выше в таблицах 1-3. Хорошо известный специалистам в данной области метод интродукции одной или нескольких аминокислотных замен, делеций, добавлений и/или инсерций в аминокислотную последовательность представляет собой метод интродукции мутаций в белки. Например, специалисты в данной области могут получать вариабельные области, которые являюся функциональными эквивалентами вариабельных областей антитела, обладающих указанными выше функциями, путем интродукции соответствующих мутаций в аминокислотные последовательности с использованием таких методов как сайтнаправленный мутагенез (Hashimoto-Gotoh Т., Mizuno Т., Ogasahara Y. и Nakagawa M., An oligodeoxyribonucleotide-directed dual amber method for site-directed mutagenesis. Gene 152, 1995, cc. 271-275; Zoller M.J. и Smith M., Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors. Methods Enzymol. 100, 1983, cc. 468-500; Kramer W. Drutsa V., Jansen H.W., Kramer В., Pflugfelder M. и Fritz H.J., The gapped duplex DNA approach to oligonucleotide-directed mutation construction. Nucleic Acids Res. 12, 9441-9456; Kramer W. и Fritz, H.J., Oligonucleotide-directed construction of mutations via gapped duplex DNA Methods. Enzymol. 154, 1987, cc. 350-367; и Kunkel T.A., Rapid and efficient site-specific mutagenesis without phenotypic selection. Proc Nati Acad. Sci. USA. 82, 1985, cc. 488-492).
Когда аминокислотный остаток изменяют, аминокислоту предпочтительно заменяют в результате мутации на другую(ие) аминокислоту(ы), сохраняющую(ие) характеристики боковых цепей аминокислот. Примерами аминокислот с такими характеристиками боковых цепей являются: гидрофобные аминокислоты (A, I, L, M, F, P, W, Y и V), гидрофильные аминокислоты (R, D, N, С, Е, Q, G, Н, K, S и Т), аминокислоты, содержащие алифатические боковые цепи (G, А, V, L, I и P), аминокислоты с содержащими гидроксильную группу боковыми цепями (S, Т и Y), аминокислоты с содержащими атом серы боковыми цепями (С и M), аминокислоты с содержащими карбоновую кислоту и амид боковыми цепями (D, N, Е и Q), аминокислоты с основными боковыми цепями (R, K и Н) и аминокислоты с ароматическими боковыми цепями (Н, F, Y и W) (в скобках представлены обозначения аминокислот в соответствии с однобуквенным кодом). Аминокислотные замены внутри каждой из указанных групп обозначают как консервативные замены. Хорошо известно, что полипептид, содержащий модифицированную аминокислотную последовательность, в которой один или несколько аминокислотных остатков в указанной аминокислотной последовательности подвергнут делеции, добавлен и/или заменен на другие аминокислоты, может сохранять исходную биологическую активность (Mark D.F. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc. 5662-5666; Zoller M.J. и Smith M., Nucleic Acids Res. 10, 1982, cc. 6487-6500; Wang А. и др., Science 224, 1984, cc. 1431-1433; Dalbadie-McFarland G. и др., Proc. Natl. Acad. Sci. USA) 79, 1982, cc. 6409-6413). Вариабельные области, предлагаемые в настоящем изобретении, содержащие указанные аминокислотные модификации, имеют аминокислотные последовательности, которые идентичны по меньшей мере на 70%, более предпочтительно по меньшей мере на 75%, еще более предпочтительно по меньшей мере на 80%, еще более предпочтительно по меньшей мере на 85%, еще более предпочтительно по меньшей мере на 95% аминокислотным последовательностям CDR-последовательностей, FR-последовательностям вариабельной области или полным вариабельным областям до модификации. В контексте настоящего описания идентичность последовательностей определяют в виде процента остатков, идентичных остаткам в исходной аминокислотной последовательности вариабельной области Н-цепи или вариабельной области L-цепи, определенного после выравнивания последовательностей и интродукции соответствующих брешей для увеличения до максимума при необходимости идентичности последовательностей. Идентичность аминокислотных последовательностей можно определять с помощью описанного ниже метода.
Кроме того, «функционально эквивалентную вариабельную область антитела» можно получать, например, из нуклеиновых кислот, которые гибридизуются в строгих условиях с нуклеиновыми кислотами, которые содержат нуклеотидную последовательность, кодирующую аминокислотную последовательность вариабельной области, указанной выше в таблицах 1-3. Строгие условия гибридизации, применяемые для выделения нуклеиновой кислоты, которая гибридизуется в строгих условиях с нуклеиновой кислотой, которая содержат нуклеотидную последовательность, кодирующую аминокислотную последовательность вариабельной области, включают, например, следующие условия: 6М мочевина, 0,4% ДСН, 0,5×SSC и 37°С или условия гибридизации в значительной степени эквивалентные указанным. Выделение нуклеиновых кислот с максимально высокой гомологией можно ожидать при применении более строгих условий, например, следующих условий: 6М мочевина, 0,4% ДСН, 0,1×SSC и 42°С. Условия промывки после гибридизации представляют собой, например, промывку с использованием 0,5×SSC (1×SSC представляет собой 0.15М NaCl и 0,015М цитрат натрия, рН 7,0) и 0,1% ДСН при 60°С, более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 60°С, еще более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 62°С, еще более предпочтительно промывку с использованием 0,2×SSC и 0,1% ДСН при 65°С и еще более предпочтительно промывку с использованием 0,1×SSC и 0,1% ДСН при 65°С. Последовательности выделенных нуклеиновых кислот можно определять известными методами, которые описаны ниже. Общая гомология нуклеотидной последовательности выделенной нуклеиновой кислоты составляет по меньшей мере 50% или выше, предпочтительно 70% или выше и наиболее предпочтительно 90% или выше (например, 95%, 96%, 97%, 98%, 99% или выше) при оценке степени идентичности последовательностей.
Нуклеиновые кислоты, которые гибридизуются в строгих условиях с нуклеиновой кислотой, содержащей нуклеотидную последовательность, которая кодирует аминокислотную последовательность вариабельной области, можно выделять также, применяя вместо описанных выше методов на основе гибридизации, методы амплификации генов, такие как полимеразная цепная реакция (ПЦР), в которой используют праймеры, синтезированные на основе информации о нуклеотидной последовательности, которая кодирует аминокислотную последовательность вариабельной области.
Идентичность одной нуклеотидной последовательности или аминокислотной последовательности можно определять с помощью алгоритма BLAST, описанного у Karlin и Altschul (Proc. Natl. Acad. Sci. USA 90, 1993, cc. 5873-5877). На основе этого алгоритма разработаны программы BLASTN и BLASTX (Altschul и др., J. Mol. Biol. 215, 1990, cc. 403-410). Для анализа нуклеотидных последовательностей согласно BLASTN на основе BLAST устанавливают параметры, такие, например, как балл = 100 и длина слова = 12. С другой стороны, параметры, применяемые для анализа аминокислотных последовательностей с помощью BLASTX на основе BLAST, включают, например, балл = 50 и длина слова = 3. Задаваемые по умолчанию параметры применяют для каждой программы, когда используют программы BLAST и Gapped BLAST. В данной области известны конкретные методики указанных анализов (см. веб-сайт National Center for Biotechnology Information (NCBI), Basic Local Alignment Search Tool (BLAST); http://www.ncbi.nlm.nih.gov).
Комбинация вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, входящая в мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, не ограничена конкретной комбинацией, если она обладает указанными выше видами активности. Однако согласно настоящему изобретению цитотоксическая активность мультиспецифической антигенсвязывающей молекулы предпочтительно эквивалентна или выше, чем активность биспецфического антитела GPC3_ERY22_rCE115, описанного в примере 3. В контексте настоящего описания понятие «эквивалентный» необязательно подразумевает такую же степень указанной выше активности, и активность может быть более высокой. Молекула является эквивалентной GPC3_ERY22_rCE115, например, когда коэффициент (скорость ингибирования клеточного роста/скорость ингибирования клеточного роста (GPC3_ERY22_rCE115)) относительно скорости ингибирования клеточного роста GPC3_ERY22_rCE115 (скорость ингибирования клеточного роста (GPC3_ERY22_rCE115)) составляет 0,7 или более, предпочтительно 0,8 или более, 0,9 или более, 1,0 или более, 1,2 или более, 1,5 или более, 2 или более, 3 или более, 5 или более, 10 или более или 20 или более. В то время как не существует верхнего предела, показатель может составлять, например, 10, 102, 103, 104, 105 или 106. Концентрацию добавленной мультиспецифической антигенсвязывающей молекулы можно определять соответствующим образом, но предпочтительно она составляет, например 0,01, 0,05, 0,1, 0,5 или 1 нМ; и предпочтительно измерения осуществляют при концентрации 0,05 или 0,1 нМ.
Кроме того, примеры включают вариант, когда коэффициент «концентрация, вызывающая ингибирование клеточного роста на 50%/концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточного роста на 50%», полученный путем сравнения с концентрацией (GPC3_ERY22_rCE115), которая вызывает ингибирование клеточного роста на 50% (концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточного роста на 50%), составляет 1,5 или менее. Коэффициент «концентрация, вызывающая ингибирование клеточного роста на 50%/концентрация (GPC3_ERY22_rCE115), вызывающая ингибирование клеточного роста на 50%» предпочтительно составляет 1,3 или менее, более предпочтительно 1,2 или менее, 1,1 или менее, 1,0 или менее, 0,9 или менее, 0,8 или менее, 0,7 или менее, 0,6 или менее или 0,5 или менее. При этом не существует нижнего предела, примеры включают коэффициенты, составляющие 10-1, 10-2, 10-3, 10-4, 10-5 или 10-6. В частности, коэффициент предпочтительно составляет от 10-6 до 1,5×10-0, более предпочтительно от 10-6 до 10-1, еще более предпочтительно от 10-6 до 10-2 и еще более предпочтительно от 10-6 до 10-3.
Предпочтительные конкретные величины KD, характеризующие связывание с человеческим GPC3 и комплексом человеческого Т-клеточного рецептора (например, с человеческой CD3ε-цепью) также соответствуют указанным выше. Можно применять соответствующие экспрессирующие GPC3 клетки или соответствующую ткань, содержащую указанные клетки, и, например, можно применять человеческие раковые линии клеток PC-10 или NCI-Н446, которые экспрессируют GPC3.
Примеры указанной комбинации вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, включают комбинации вариабельных областей Н-цепи антитела, которые представлены в таблице 4, комбинации вариабельных областей Н-цепи антитела, которые имеют последовательности CDR, аминокислотные последовательности CDR1, CDR2 и CDR3 которых являются такими же, что и аминокислотные последовательности CDR1, CDR2 и CDR3, которые входят в вариабельные области Н-цепи антитела, представленные в таблице 4, и комбинации вариабельных областей Н-цепи антитела, функционально эквивалентные указанным вариабельным областям. В контексте настоящего описания понятие «функционально эквивалентные» имеет значение, указанное выше.
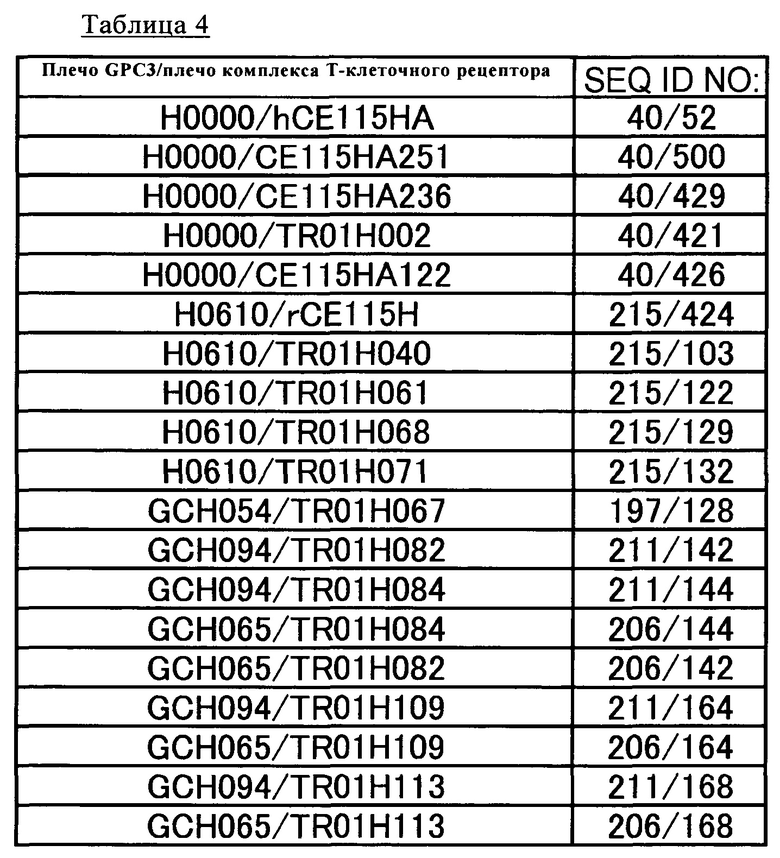
Предпочтительная общая L-цепь для таких комбинаций вариабельной области антитела, обладающей связывающей активностью в отношении глипикана 3, и вариабельной области антитела, обладающей связывающей активностью в отношении комплекса Т-клеточного рецептора, вкючает, например, L0000, L0011, L0201, L0203, L0204, L0206, L0208, L0209, L0211, L0212, L0222 и общую L-цепь, которая имеет последовательности CDR (аминокислотные последовательности CDR1, CDR2 и CDR3), идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3, указанным выше для общей L-цепи. Конкретные комбинации включают, например, комбинации вариабельных областей Н-цепи антитела и общей L-цепи, которые представлены в таблице 5, комбинации вариабельных областей антитела, которые имеют последовательности CDR (аминокислотные последовательности CDR1, CDR2 и CDR3), идентичные аминокислотным последовательностям CDR1, CDR2 и CDR3, которые входят в вариабельные области общей L-цепи, представленные в таблице 5, и комбинации вариабельных областей Н-цепи антитела и общей L-цепи, функционально эквивалентные указанным вариабельным областям. В контексте настоящего описания понятие «функционально эквивалентные» имеет значение, указанное выше.
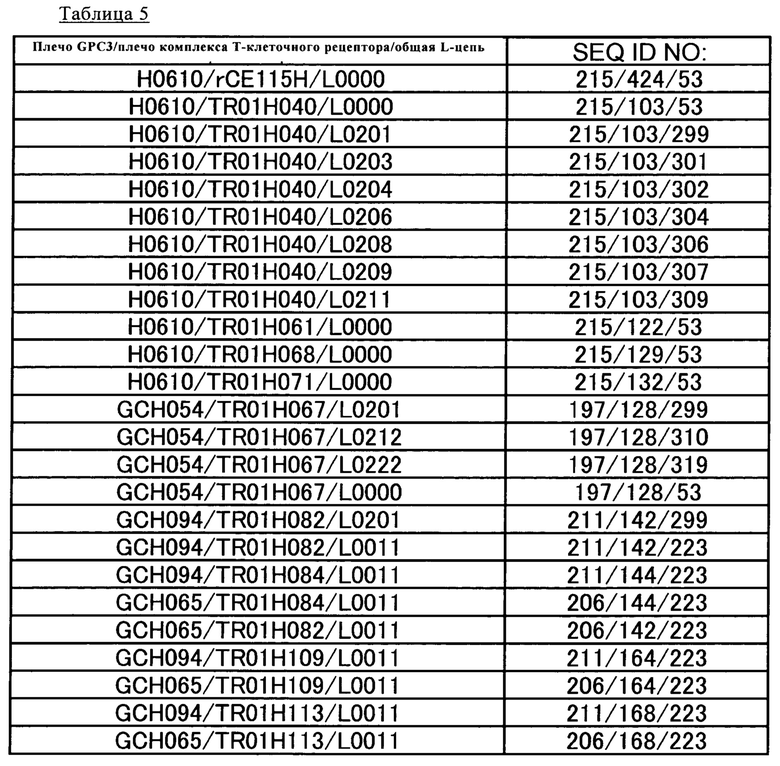
Не накладываются конкретные ограничения на Fc-область, входящую в мультиспецифическую антигенсвязывающую молекулу, предлагаемую в изобретении, если она представляет собой Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора, но примеры предпочтительной Fc-области, предлагаемой в настоящем изобретении, включают комбинацию участка Fc-области E22Hh и участка Fc-области E22Hk, комбинацию участка Fc-области E2702GsKsc и участка Fc-области E2704sEpsc и комбинацию участка Fc-области E2702sKsc и участка Fc-области E2704sEpsc.
Примеры предпочтительной мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, включают биспецифические антитела, которые содержат вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, и вариабельную область антитела, обладающую связывающей активностью в отношении CD3ε. Более предпочтительно цитотоксическая активность является такой же или превышает активность биспецифического антитела GPC3_ERY22_rCE115. Примеры указанных биспецифических антител включают биспецифические антитела, содержащие Н- и L-цепи, указанные в таблице 13, и биспецифические антитела, которые связываются с эпитопом, перекрывающимся с эпитопом, связывающимся с указанными выше антителами, и которые содержат Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора.
Распознает ли антитело эпитоп, который перекрывается с эпитопом, распознаваемым другим антителом, можно определять на основе конкуренции между двумя антителами за эпитоп. Конкуренцию между антителами можно оценивать с помощью анализов связывания в условиях конкуренции, таких как твердофазный иммуноферментный анализ (ELISA), метод на основе флуоресцентного резонансного переноса энергии (FRET) и метод на основе технологии флуорометрического микрообъемного анализа (FMAT (зарегистрированный товарный знак)). Количество антитела, связанного с антигеном, косвенно коррелирует со связывающей способностью конкурирующего антитела-кандидата (тестируемое антитело), которое конкурентно связывается с перекрывающимся эпитопом. Другими словами, если количество или аффинность тестируемого антитела к перекрывающемуся эпитопу возрастает, то количество антитела, связанного с антигеном, снижается, а количество антигена, связанного тестируемым антителом, возрастает. В частности, соответствующим образом меченное антитело и антитело, подлежащее изучению, добавляют одновременно к антигену, и антитело, которое в результате связывается, обнаруживают с помощью метки. Количество связанного с антигеном антитела легко можно определять с помощью предварительно меченого антитела. Указанная метка не ограничена конкретной меткой и метод мечения выбирают в зависимости от применяемой методики анализа. В частности метод мечения включает введение флуоресцентной метки, радиоактивной метки, ферментной метки и т.п.
Например, флуоресцентно меченное антитело и немеченое антитело или тестируемое антитело одновременно добавляют к гранулам, на которых иммобилизован GPC3 или CD3ε, и меченое антитело выявляют с помощью технологии флуорометрического микрообъемного анализа.
В контексте настоящего описания «антитело, которое связывается с перекрывающимся эпитопом» означает тестируемое антитело, которое может снижать количество связанного меченого антитела по меньшей мере на 50% в концентрации, которая, как правило, выше в 100 раз, предпочтительно выше в 80 раз, более предпочтительно выше в 50 раз, еще более предпочтительно выше в 30 раз и еще более предпочтительно выше в 10 раз концентрации, в которой немеченое антитело снижает на 50% количество связанного меченого антитела (IC50).
Мультиспецифические антигенсвязывающие молекулы, которые имеют антигенсвязывающие сайты антитела, связывающиеся с эпитопами, которые перекрываются с эпитопами, связывающимися вышеуказанными антителами, могут обладать очень высокой цитотоксической активностью.
Мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, получают с помощью такой же технологии, которая описана выше в качестве метода получения рекомбинантных антител.
Настоящее изобретение относится также к полинуклеотидам, кодирующим антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, и их можно встраивать в требуемые экспрессионные векторы. Приемлемые клетки-хозяева можно трансформировать экспрессионными векторами с получением клеток, которые экспрессируют антигенсвязывающие молекулы. Антигенсвязывающие молекулы, кодируемые полинуклеотидами, можно получать путем культивирования клеток, которые экспрессируют антигенсвязывающие молекулы, и сбора продуктов экспрессии из супернатантов культуры. Таким образом, настоящее изобретение относится к векторам, которые содержат полинуклеотид, кодирующий антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, клеткам, которые несут указанный вектор, и к способам получения антигенсвязывающих молекул, которые заключаются в том, что культивируют клетки и собирают антигенсвязывающие молекулы из супернатантов культуры. Их можно получать с помощью таких же технологий, которые описаны выше для получения рекомбинантных антител.
Фармацевтические композиции
Другим объектом настоящего изобретения являются фармацевтические композиции, содержащие в качестве действующего вещества мультиспецифическую антигенсвязывающую молекулу, которая содержит: (1) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, (2) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, и (3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора. Кроме того, настоящее изобретение относится к фармацевтическим композициям, которые индуцируют повреждение клеток, содержащим в качестве действующего вещества антигенсвязывающую молекулу. Фармацевтические композиции, предлагаемые в настоящем изобретении, которые индуцируют требуемое повреждение клеток, прежде всего зависимую от Т-клеток клеточную цитотоксичность, предпочтительно вводят индивидууму, который страдает заболеванием, при котором необходимы указанные виды активности для предупреждения или лечения, или индивидууму, у которого возможен рецидив заболевания.
Кроме того, согласно настоящему изобретению индуцирующие цитотоксичность агенты и ингибирующие рост клеток агенты, и противораковые агенты, которые содержат в качестве действующего вещества мультиспецифическую антигенсвязывающую молекулу, которая содержит:
(1) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3,
(2) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, и
(3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора,
можно применять в способе индукции повреждения клеток, который заключается в том, что содержит стадию, на которой вводят индивидууму антигенсвязывающую молекулу, или можно применять антигенсвязывающую молекулу для приготовления индуцирующего цитотоксичесность агента и ингибирующего роста клеток агента.
В настоящем изобретении фраза «содержит в качестве действующего вещества мультиспецифическую антигенсвязывающую молекулу, которая содержит: (1) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, (2) домен, содержащий вариабельную область антитела, обладающую связывающей активностью в отношении комплекса Т-клеточного рецептора, и (3) домен, содержащий Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора» означает, что композиция содержит антигенсвязывающую молекулу в качестве основного действующего вещества; однако не имеется конкретных ограничений на относительное содержание антигенсвязывающей молекулы.
При необходимости мультиспецифические антигенсвязывающие молекулы, предлагаемые в настоящем изобретении, можно капсулировать в микрокапсулы (микрокапсулы, изготовленные из гидроксиметилцеллюлозы, желатина, поли(метилметакрилата) и т.п.), и можно включать в компоненты коллоидных систем, предназначенных для введения лекарственных веществ (липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) (например, см. «Remington's Pharmaceutical Science 16-oe изд.», под ред. Oslo, 1980)). Кроме того, хорошо известны методы приготовления агентов в виде средств с замедленным высвобождением, и их можно применять для мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении (J. Biomed. Mater. Res. 15, 1981, cc. 267-277; Chemtech. 12, 1982, cc. 98-105; US №3773719; опубликованные европейские патенты (ЕР) ЕР 58481 и ЕР 133988; Biopolymers 22, 1983, cc. 547-556).
Фармацевтические композиции, предлагаемые в настоящем изобретении, или индуцирующие цитотоксичность агенты и ингибирующие рост клеток агенты можно вводить пациенту орально или парентерально, и предпочтительным является парентеральное введение. Указанные примеры методов введения включают инъекцию, введение в нос, транспульмонарное введение и чрескожное введение. Примеры введения путем инъекции включают, например, внутривенную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию и подкожную инъекцию. Фармацевтическую композицию, предлагаемую в настоящем изобретении, или индуцирующий цитотоксичность агент и ингибирующий рост клеток агент можно применять местно или системно путем инъекции. Метод введения можно выбирать в зависимости от возраста пациента и симптомов. Дозу можно выбирать, например, из следующего диапазона: от 0,0001 до 1000 мг на кг веса тела на каждое введение. Альтернативно этому, дозу можно выбирать, например, из следующего диапазона: от 0,001 до 100000 мг/пациента. Однако дозы фармацевтической композиции, предлагаемой в настоящем изобретении, или индуцирующего цитотоксичность агента и ингибирующего рост клеток агента не ограничены указанными дозами.
Фармацевтические композиции, предлагаемые в настоящем изобретении, или индуцирующие цитотоксичность агенты и ингибирующие рост клеток агенты можно приготавливать с помощью общепринятых методов (например, см. Remington's Pharmaceutical Science, последнее изд., изд-во Mark Publishing Company, Easton, U.S.A.), и они могут содержать также фармацевтически приемлемые носители и добавки. Их примерами являются (но не ограничиваясь только ими) поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корригенты и можно применять другие общепринятые носители. Конкретными примерами носителей являются легкая безводная кремниевая кислота, лактоза, кристаллическая целлюлоза, маннит, крахмал, кармеллоза кальция, кармеллоза натрия, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилацетальдиэтиламиноацетат, поливинилпирролидон, желатин, триглицерид со средней длиной цепи, полиоксиэтиленированное гидрогенизированное касторовое масло 60, сахароза, карбоксиметилцеллюлоза, кукурузный крахмал, неорганическая соль и т.п.
В настоящем изобретении предложены также способы повреждения экспрессирующих в качестве антигена глипикан 3 клеток или опухолевых тканей, содержащих экспрессирующие антиген клетки, или способы подавления роста указанных клеток или опухолевых тканей путем приведения в контакт клеток, экспрессирующих в качестве антигена глипикан 3, с мультиспецифической антигенсвязывающей молекулой, предлагаемой в настоящем изобретении, которая связывается с антигеном. Мультиспецифическая антигенсвязывающая молекула, которая связывается с антигеном, описана выше в качестве антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, которая связывается с антигеном, которая содержится в индуцирующих цитотоксичность агентах и ингибирующих рост клеток агентах, предлагаемых в настоящем изобретении. Клетки, с которыми связывается Мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, которая связывается с антигеном, не ограничены конкретными клетками, если эти клетки экспрессируют антиген.
Согласно настоящему изобретению «приведение в контакт» можно осуществлять, например, добавляя мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, которая связывается с антигеном, в культуральную среду экспрессирующих антиген GPC3 клеток, которые культивируют in vitro. В этом случае добавляемую антигенсвязывающую молекулу можно применять в пригодной для этой цели форме, такой как раствор или твердое вещество, полученное путем лиофилизации, или т.п. При добавлении в виде водного раствора он может представлять собой водный раствор, который содержит только мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или может представлять собой также раствор, содержащий, например, указанные выше поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корригенты. На концентрацию добавляемой молекулы не накладывается специальных ограничений; однако конечная концентрация в культуральной среде предпочтительно составляет от 1 пг/мл до 1 г/мл, более предпочтительно от 1 нг/мл до 1 мг/мл и еще более предпочтительно от 1 мкг/мл до 1 мг/мл.
Кроме того, согласно другому варианту осуществления настоящего изобретения «приведение в контакт» осуществляют также путем обработки животных кроме человека, в организм которых трансплантированы экспрессирующие антиген GPC3 клетки, и животных, у которых эндогенно происходит экспрессия антигена. Метод введения может быть оральным или парентеральным, и предпочтительным является парентеральное введение. Указанные примеры методов введения включают инъекцию, введение в нос, транспульмонарное введение и чрескожное введение. Примеры введения путем инъекции включают, например, внутривенную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию и подкожную инъекцию. Фармацевтическую композицию, предлагаемую в настоящем изобретении, или индуцирующий цитотоксичность агент и ингибирующий рост клеток агент можно применять местно или системно, например, путем инъекции. Метод введения можно выбирать в зависимости от возраста подопытного животного и симптомов. При введении в виде водного раствора можно применять водный раствор, содержащий только мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или можно применять раствор, содержащий также указанные выше поверхностно-активные вещества, эксципиенты, красители, ароматизаторы, консерванты, стабилизаторы, буферы, суспендирующие агенты, придающие изотоничность агенты, связующие вещества, разрыхлители, замасливатели, повышающие текучесть агенты и корргиенты и т.п. Дозу можно выбирать из следующего диапазона: от 0,0001 до 1000 мг на кг веса тела на одно введение.
Альтернативно этому, дозу можно выбирать, например, из следующего диапазона: от 0,001 до 100000 мг/пациента. Однако вводимое количество мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, не ограничено указанными дозами.
Описанный ниже метод предпочтительно используют в качестве метода оценки или измерения повреждения клетки, индуцированного в клетках, экспрессирующих в качестве антигена глипикан 3, который связывается доменом, который несет вариабельную область антитела, обладающую связывающей активностью в отношении глипикана 3, который входит в антигенсвязывающую молекулу, что является результатом контактирования клеток с мультиспецифической антигенсвязывающей молекулой, предлагаемой в настоящем изобретении. Примеры метода оценки или измерения цитотоксической активности in vitro включает методы измерения активности цитотоксических Т-клеток или т.п. Обладает ли мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, Т-клеточной цитотоксичностью, можно определять с помощью известных методов (см., например. Current protocols in Immunology, глава 7. Immunologic studies in humans, под ред. John E, Coligan и др., изд-во, John Wiley & Sons, Inc., 1993). При измерении активности антигенсвязывающую молекулу, которая связывается с антигеном, отличным от глипикана 3, представляющим собой антиген, который не экспрессируется в клетках, применяемых для оценки, можно использовать в качестве контроля, который анализируют таким же образом, что и мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, и активность можно определять, оценивая, обладает ли мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении, более выраженной цитотоксической активностью, чем применяемая в качестве контроля антигенсвязывающая молекула.
Для оценки или измерения цитотоксической активности in vivo, например, клетки, экспрессирующие в качестве антигена глипикан 3, внутрикожно или подкожно трансплантируют подопытному животному кроме человека, а затем тестируемую антигенсвязывающую молекулу вводят внутривенно или внутрибрюшинно каждый день или с интервалами в несколько дней, начиная со дня трансплантации или на следующий после него день. Цитотоксическую активность можно определять путем ежедневного измерения размера опухолей, определяя различие в изменении размера опухолей. Аналогично методу, применяемому для оценки in vitro, можно считать, что антигенсвязывающая молекула, предлагаемая в настоящем изобретении, обладает цитотоксической активностью, если при введении контрольной антигенсвязывающей молекулы обнаружено, что размер опухолей в группе, которой вводили антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, существенно меньшей, чем размер опухолей в группе, которой вводили контрольную антигенсвязывающую молекулу
В качестве метода оценки или измерения подавляющего действия на пролиферацию клеток, экспрессирующих в качестве ангигена глипикан 3, можно применять метод измерения поглощения меченного изотопом тимидина клетками или МТТ-метод. В качестве метода оценки или измерения подавляющего действия на пролиферацию клеток in vivo, можно применять метод, аналогичный описанному выше для оценки или измерения цитотоксической активности in vivo.
В настоящем изобретении предложены также наборы, которые можно применять в способах, предлагаемых в настоящем изобретении, которые содержат мультиспецифическую антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, или мультиспецифическую антигенсвязывающую молекулу, созданную способом получения, предлагаемым в настоящем изобретении. Альтернативно этому, наборы могут быть упакованы вместе с дополнительным фармацевтически приемлемым носителем, растворителем и инструкциями с описанием метода применения.
Настоящее изобретение относится также к мультиспецифической антигенсвязывающей молекуле, предлагаемой в настоящем изобретении, или мультиспецифической антигенсвязывающей молекуле, полученной способом, предлагаемым в настоящем изобретении, для применения в способе, предлагаемом в настоящем изобретении.
Настоящее изобретение относится также к молекулам, обладающим GPC3-связывающей активностью, которые содержат домен, содержащий вариабельную область антитела, которая обладает GPC3-связывающей активностью, мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении. Кроме того, настоящее изобретение относится к молекуле, которая обладает GPC3-связывающей активностью, которая содержит вариабельные области Н- и L-цепей антитела соответственно, содержащие три CDR Н- и L-цепей (всего шесть CDR), которые входят в молекулу. Настоящее изобретение относится также к молекулам, обладающим связывающей активностью в отношении комплекса Т-клеточного рецептора, которые содержат домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении. Кроме того, настоящее изобретение относится к молекуле, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, которая содержит вариабельные области Н- и L-цепей антитела соответственно, содержащие три CDR Н- и L-цепей (всего шесть CDR), которые входят в молекулу. Указанные молекулы могут представлять собой антитела или полипептиды, содержащие антигенсвязывающие фрагменты антитела. Настоящее изобретение относится также к антителам, которые связываются с эпитопами, перекрывающимися или конкурирующими с указанными молекулами или полипептидами, которые содержат их антигенсвязывающие фрагменты. Приемлемыми примерами таких полипептидов, которые содержат антигенсвязывающие фрагменты антитела, являются scFv, одноцепочечное антитело, Fv, одноцепочечный Fv2 (scFv2), Fab и F(ab')2. Кроме того, указанные молекулы необязательно должны быть мультиспецифическими (биспецифическими), а могут связываться только либо с GPC3, либо с комплексом Т-клеточного рецептора (например, CD3ε-цепью).
Указанные молекулы включают молекулу, которая содержит домен, содержащий вариабельную область антитела, которая обладает GPC3-связывающей активностью, мультиспецифической антигенсвязывающей молекулы, подробное описание которой представлено в разделе «Примеры» в настоящем описании (которая содержит вариабельные области Н-цепи, обладающие GPC3-связывающей активностью и вариабельную область общей L-цепи), молекулу, которая содержит домен, содержащий вариабельную область антитела, которая обладает связывающей активностью в отношении комплекса Т-клеточного рецептора, мультиспецифической антигенсвязывающей молекулы, подробное описание которой представлено в разделе «Примеры» в настоящем описании (которая содержит вариабельные области Н-цепи, обладающие связывающей активностью в отношении комплекса Т-клеточного рецептора и вариабельную область общей L-цепи), а также молекулу, обладающую способностью связываться с таким же антигенным белком (GPC3 или комплекс Т-клеточного рецептора), которая содержит три CDR каждой из Н- и L-цепей (всего шесть CDR), которые входят в указанную выше молекулу.
Указанные молекулы имеют CDR, которые являются одинаковыми (общими) с CDR мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении; и поэтому ожидается, что они будут связываться с эпитопом, перекрывающимся с эпитопом мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении. Таким образом, указанные молекулы могут конкурировать с мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении, при их совместном присутствии с мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении. Таким образом, эти молекулы можно применять, например, в качестве регуляторных агентов для подавления различных видов активности (таких как антигенсвязывающая активность, цитотоксическая активность и противоопухолевания активность) мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении. Кроме того, указанная молекула может быть предварительно связана с белком-мишенью (GPC3 или комплекс Т-клеточного рецептора), и после добавления мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, можно выявлять молекулы, диссоциирующие в результате конкуренции. При таком применении молекула пригодна в качестве агента, предназначенного для оценки связывания мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, с белком-мишенью. Согласно настоящему изобретению молекулы можно метить соответствующими флуоресцентными субстанциями или т.п. Альтернативному этому, указанные молекулы можно применять для скрининга новых антител, которые связываются с эпитопами, перекрывающимися с эпитопами, которые связываются мультиспецифическими антигенсвязывающими молекулами, предлагаемыми в настоящем изобретении. Как указано выше, указанную молекулу можно предварительно связывать с белком-мишенью (GPC3 или комплекс Т-клеточного рецептора), а затем добавлять тестируемое антитело, при этом, если имеет место диссоциация связанных молекул, то тестируемое антитело является перспективным (кандидатом) в качестве антитела, которое связывается с эпитопом, перекрывающимся с эпитопом, с которым связывается мультиспецифическая антигенсвязывающая молекула, предлагаемая в настоящем изобретении. Это позволяет осуществлять эффективный скрининг новых мультиспецифических антигенсвязывающих молекул.
Приведенные в настоящем описании в качестве примеров комбинации в виде комбинаций каждого CDR мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении, можно применять непосредственно в качестве конкретных комбинаций CDR вариабельных областей Н-цепи и L-цепи этих молекул. Аффинность к антигену этих молекул (величины KD) предпочтительно характеризуется величинами, приведенными в качестве примера KD мультиспецифической антигенсвязывающей молекулы, предлагаемой в настоящем изобретении, но не ограничена этими величинами.
Настоящее изобретение относится также к нуклеиновым кислотам, кодирующим эти молекулы, векторам, содержащим нуклеиновые кислоты, клеткам, содержащим нуклеиновые кислоты или векторы, способам получения молекул путем культивирования клеток и молекулам, полученным с помощью этих способов.
Все процитированные в настоящем описании документы, характеризующие известный уровень техники, включены в настоящее описание в качестве ссылки.
Примеры
Ниже настоящее изобретение описано со ссылкой на конкретные примеры, которые не ограничивают объем изобретения.
Пример 1. Получение GPC3_ERY22_rCE115 и измерение цитотоксической активности
(1-1) Получение GPC3_ERY22_rCE115
Молекулу, в которой один из Fab заменяли на домен, связывающий CD3 эпсилон, получали, используя IgG против ракового антигена (GPC3) в качестве основной структуры. В этом случае Fc-область IgG, которую применяли в качестве основной структуры, представляла собой молчащую Fc с ослабленной аффинностью к FcgR (Fcγ- (Fc-гамма) рецептор). Антитело к GPC3 Н0000 (SEQ ID NO: 40)/GL4 (SEQ ID NO: 41) применяли в качестве GPC3-связывающего домена. Антитело к CD3 rCE115H/rCE115L (SEQ ID NO: 42/SEQ ID NO: 43) применяли в качестве CD3-связывающего домена.
Конструкцию G1d, полученную удалением Gly и Lys на С-конце IgG1, применяли в качестве константной области Н-цепи антитела и ее применяли в комбинации с H0000/GL4 и rCE115H/rCE115L. Когда константную область Н-цепи антитела обозначали как H1, последовательность, соответствующую Н-цепи антитела, несущую Н0000 в вариабельной области, обозначали как Н0000-Н1. В настоящем описании аминокислотное изменение обозначали, например, как D356K. Первый алфавитный символ (соответствует D в D356K) представляет собой однобуквенный код аминокислотного остатка до модификации, следующий за ним номер (соответствует 356 в D356K) обозначает положение модификации согласно EU-нумерации, а последний алфавитный символ (соответствует K в D356K) представляет собой однобуквенный код аминокислотного остатка после модификации. G1dh (SEQ ID NO: 44), полученную путем удаления Gly и Lys на С-конце IgG1, ERY22_Hk (SEQ ID NO: 45), созданную путем интродукции мутаций L234A/L235A/Y349C/T366W в G1dh, a ERY22_Hh (SEQ ID NO: 46), созданную путем интродукции мутаций L234A/L235A/D356C/T366S/L368A/Y407V в G1dh, получали согласно методу, описанному в приведенном для справки примере 1. Мутации L234A и L235A интродуцировали в соответствующие Н-цепи для ослабления аффинности к FcgR (Fcγ-рецептор), а мутации Y349C/T366W и D356C/T366S/L368A/Y407V интродуцирлвали для эффективного образования гетеромеров каждой Н-цепи при получении гетеродимерных антител, содержащих два типа Н-цепей.
Гетеродимерное антитело GPC3_ERY22_rCE115, полученной заменой VH- и VL-доменов Fab против GPC3, создавали согласно методу, описанному в приведенном для справки примере 1 (фиг. 1а).
Серии экспрессионных векторов со встроенным полинуклеотидом, кодирующим каждую из конструкций GL4-ERY22_Hk (SEQ ID NO: 47), H0000-ERY22JL (SEQ ID NO: 48), rCE115H-ERY22_Hh (SEQ ID NO: 49) и rCE115L-k0 (SEQ ID NO: 50), получали с помощью методов, хорошо известных специалистам в данной области, таких как методы на основе ПЦР с использованием добавленных праймеров, которые имели соответствующие последовательности, аналогичные применяемым в описанном выше методе.
Следующую комбинацию экспрессионных векторов интродуцировали в клетки FreeStyle 293-F для кратковременной экспрессии каждой молекулы-мишени.
Молекула-мишень: GPC3_ERY22_rCE115
Полипептиды, кодируемые полинуклеотидами, встроенными в экспрессионные векторы: GL4-ERY22_Hk, H0000-ERY22_L, rCE115H-ERY22_Hh, rCE115L-k0.
(1-2) Очистка GPC3_ERY22_rCE115
Полученный супернатант культуры добавляли в колонку с антителом к FLAG M2 (фирма Sigma) и затем колонку промывали, после чего элюировали, используя пептид FLAG (фирма Sigma) в концентрации 0,1 мг/мл. Фракции, содержащие представляющую интерес молекулу, добавляли в колонку HisTrap HP (фирма GE Healthcare), а затем колонку промывали, после чего элюировали с использованием концентрационного градиента имидазола. Фракцию, содержащую представляющую интерес молекулу, концентрировали с испотзованием метода ультрафильтрации и затем концентрат вносили в колонку, заполненную Супердекс 200 (фирма GE Healthcare), и каждую из очищенных представляющих интерес молекул собирали только в виде мономерных фракций из элюированного раствора.
(1-3) Измерение цитотоксической активности GPC3_ERY22_rCE115 с использованием мононуклеарных клеток периферической крови человека
Оценивали in vitro цитотоксическую активность GPC3_ERY22_rCE115.
(1-3-1) Получение раствора мононуклеарных клеток периферической крови человека (РВМС)
Получали образцы по 50 мл периферической крови здоровых добровольцев (взрослых) с использованием шприцев, предварительно заполненных 100 мкл (1000 ед./мл) раствора гепарина (Novo-Heparin 5000 ед. на инъекцию; фирма Novo Nordisk). Эту периферическую кровь двукратно разводили ЗФР(-), разделяли на четыре аликвоты и добавляли в пробирки для разделения лимфоцитов Leucosep (каталожный №227290; фирма Greiner bio-one), в которые предварительно вносили 15 мл фиколл-пак PLUS и центрифугировали. После центрифугирования пробирок для разделения (2150 об/мин, 10 мин, комнатная температура) собирали фракции мононуклеарных клеток. Клетки во фракции мононуклеарных клеток однократно промывали с использованием модифицированной по методу Дульбекко среды Игла (фирма SIGMA), содержащей 10% FBS (далее в контексте настоящего описания обозначена как 10%FBS/D-MEM), а затем плотность клеток доводили до 4×106 клеток/мл с помощью 10%FBS/D-MEM. Полученную таким образом клеточную суспензию применяли в качестве раствора человеческих РВМС в последующих экспериментах.
(1-3-2) Анализ цитотоксической активности
Цитотоксическую активность оценивали на основе степени ингибирования клеточного роста с помощью анализатора клеток в реальном времени xCELLigence (фирма Roche Diagnostics). Применяемые клетки-мишени представляли собой клеточную линию рака человека NCI-H446 или клеточную линию рака человека PC-10, экспрессирующую GPC3. Клетки NCI-H446 или PC-10 отделяли от чашек и высевали в планшет E-Plate 96 (фирма Roche Diagnostics) в виде аликвот 100 мкл/лунку, регулируя их количество на уровне 1×104, и начинали анализ жизнеспособных клеток с помощью анализатора клеток в реальном времени xCELLigence. На следующий день планшет удаляли из анализатора клеток в реальном времени xCELLigence и в планшет добавляли по 50 мкл каждого соответствующего полученного антитела в различных концентрациях (0,004, 0,04, 0,4 и 4 нМ). После осуществления реакции в течение 15 мин при комнатной температуре добавляли 50 мкл раствора человеческих РВМС (2×105 клеток/лунку), полученного согласно методу, описанному в разделе (1-2) и клетки вновь помещали в анализатор клеток в реальном времени xCELLigence и начинали анализ жизнеспособных клеток. Реакцию проводили в атмосфере 5% газообразного диоксида азота при 37°С и степень ингибирования роста клеток (%) определяли с помощью приведенной ниже формулы с использованием величины клеточного индекса, определенной через 72 ч после добавления человеческих РВМС. Применяемую для расчета величину клеточного индекса стандартизовали таким образом, что величину клеточного индекса, определенную непосредственно перед добавлением антитела, принимали за 1.
Степень ингибирования роста клеток (%) = (А-Б) × 100/(А-1)
А обозначает среднюю величину клеточного индекса в лунках без добавления антитела (только клетки-мишени и человеческие РВМС), а Б обозначает среднюю величину клеточного индекса в каждой лунке. Измерение осуществляли в трех повторностях.
Когда мононуклеарные клетки периферической крови (РВМС), полученные из человеческой крови, применяли в качестве эффекторных клеток для анализа цитотоксичности GPC3_ERY22_rCE115, обнаружена очень сильная активность (фиг. 2).
Пример 2. Гуманизация Н-цепи антитела к CD3, rCE115, и «совместное использование» общей L-цепи
(2-1) Создание hCE115HA, гуманизированной вариабельной области Н-цепи антитела rCE115
Гуманизировали вариабельную область Н-цепи антитела rCE115 к CD3 (SEQ ID NO: 42). CDR и FR определяли по Кэботу (нумерация Кэбота).
Сначала выбирали последовательность человеческого FR путем сравнения последовательностей вариабельных областей человеческих антител в базе данных с крысиной последовательностью вариабельной области rCE115. В качестве базы данных применяли базу данных IMGT (http://www.imgt.org/) и NCBI GenBank (http://www.ncbi.nlm.nih.gov/genbank/). Гуманизированную последовательность вариабельной области Н-цепи создавали, сшивая последовательность CDR вариабельной области Н-цепи rCE115 с выбранной последовательностью человеческого FR. Таким путем получали гуманизированную последовательность вариабельной области Н-цепи, hCE115HL(SEQ ID NO: 51).
Аминокислотный остаток в положении 93 согласно нумерации Кэбота представляет собой Ala в выбранной последовательности человеческого FR3 Н-цепи, но представляет собой Arg в последовательности вариабельной области rCE115. При использовании базы данных последовательностей крысиных и человеческих зародышевых линий (база данных IMGT (http://www.imgt.org/)) обнаружено лишь несколько последовательностей, которые содержат в этом сайте Arg. Известно, что аминокислотный остаток в положении 94 согласно нумерации Кэбота принимает участие в стабилизации структуры антитела путем образования верхнего ядра (Ewert и др.. Methods 34(2)октябрь 2004 г., cc. 184-199). На основе указанной информации создавали новую последовательность гуманизированной вариабельной области Н-цепи, в которой аминокислотные остатки в положениях по Кэботу 93 и 94 в FR3 Н-цепи заменяли на остатки, присутствующие в последовательности вариабельной области rCE115. Таким путем получали гуманизированную последовательность вариабельной области Н-цепи hCE115HA (SEQ ID NO: 52).
(2-2) Создание общей L-цепи L0000 для антитела к CD3 rCE115 и антитела к GPC3
Осуществляли перестановку FR/CDR вариабельной области L-цепи rCE115L (SEQ ID NO: 43) антитела к CD3 rCE115 и вариабельной области L-цепи GL4 (SEQ ID NO: 41) антитела к GPC3.
Выбирали последовательность FR GL4 в качестве последовательности FR L-цепи. CDR2 L-цепи был одинаковым в rCE115L и GL4. CDR1 L-цепи выбирали из последовательностей CDR GL4, a CDR3 L-цепи выбирали из последовательностей CDR rCE115L соответственно. Кроме того, вновь создавали CDR3 L-цепи путем замены аминокислотного остатка Asp в положении 94 по Кэботу выбранного CDR3 L-цепи на остаток Val, присутствующий в GL4.
Гуманизированную последовательность вариабельной области L-цепи создавали, сшивая отобранные FR и CDR, описанные выше. В результате получали гуманизированную последовательность вариабельной области L-цепи, L0000 (SEQ ID NO: 53).
(2-3) Оценка аффинности к человеческому GPC3
Оценивали связывающую активность в отношении человеческого GPC3 при применении GL4 (SEQ ID NO: 41) и L0000 (SEQ ID NO: 53) в качестве вариабельных областей L-цепей. Для осуществления этого применяли молекулярную форму антитела с одним плечом, несущего один Fab, гетеродимеризованный в Fc-области человеческого IgG1 с помощью технологии «knobs-into-hole». H0000 (SEQ ID NO: 40) применяли в качестве вариабельной области Н-цепи антитела к GPC3.
Константны аффинности и связывания антитела к GPC3 в отношении антигена измеряли с помощью метода многоциклической кинетики на основе поверхностного плазменного резонанса с использованием устройства Biacore™-Т200 (фирма GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания белка A/G с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Каждое антитело к GPC3 приготавливали таким образом, чтобы примерно 100 RU «захватывалось» белком A/G. Человеческий GPC3, применяемый в качестве аналита, приготавливали в концентрации 8, 16, 32, 64 и 128 нМ, используя HBS-EP+. При осуществлении измерений сначала давали белку A/G связываться с раствором антитела, а затем инъецировали раствор человеческого GPC3 со скоростью потока 30 мкл/мин в течение 3 мин, давая пройти реакции. Затем раствор заменяли на буфер HBS-EP+ и осуществляли оценку фазы диссоциации в течение 15 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Аналогично осуществляли измерение при концентрации 0, давая белку A/G осуществлять «захват» в растворе антитела, осуществляя инъекцию HBS-EP+ в течение 3 мин, давая пройти реакции, и затем заменяя раствор на HBS-EP+ для оценки фазы диссоциации в течение 15 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Для анализа данных применяли только программу для Biacore-анализа, программу Biacore T200 Evaluation, версия 1.0 применяли для осуществления кинетического анализа для расчета константы скорости реакции связывания (ka), константы скорости реакции диссоциации (kd) и соотношения констант скорости на основе полученных сенсограмм. Результаты представлены в таблице 6.
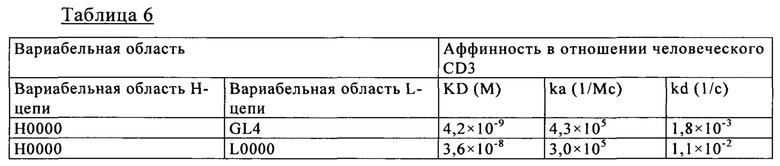
(2-4) Оценка аффинности к человеческому CD3
Оценивали связывающую активность в отношении человеческого CD3 при применении hCE115HA (SEQ ID NO: 52) в качестве вариабельной области Н-цепи и L0000 (SEQ ID NO: 53) в качестве вариабельной области L-цепи. Для осуществления этого применяли молекулярную форму антитела с одним плечом, несущего один Fab, гетеродимеризованный в Fc-области человеческого IgG1 с помощью технологии «knobs-into-hole».
Константы аффинности и связывания антитела к CD3 в отношении антигена измеряли с помощью метода одноциклической кинетики на основе поверхностного плазменного резонанса с использованием устройства Biacore™-Т200 (фирма GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания человеческого CD3 с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Антитело к CD3, применяемое в качестве аналита, приготавливали в концентрациях 5 и 20 мкг/мл, используя HBS-EP+. Измерения осуществляли путем первой инъекции каждого из растворов антитела к CD3 в концентрациях 5 и 20 мкг/мл в течение 3 мин при скорости потока 20 мкл/мин, давая пройти реакции. Затем раствор заменяли на HBS-EP+ и осуществляли оценку фазы диссоциации в течение 3 мин. После завершения оценки фазы диссоциации сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. Для анализа данных применяли только программу для Biacore-анализа, программу Biacore T200 Evaluation, версия 1.0 применяли для осуществления кинетического анализа для расчета константы скорости реакции связывания (ka), константы скорости реакции диссоциации (kd) и соотношения констант скорости на основе полученных сенсограмм. Результаты представлены в таблице 7.

(2-5) Получение GPC3_ERY27_hCE115
IgG4 к раковому антигену (GPC3) применяли в качестве основной структуры для получения молекулы ERY27 (фиг. 16), в которой вариабельную область Н-цепи одного из Fab заменяли на домен, связывающий CD3 эпсилон, а L-цепь была общей для обоих Fab. В этом случае Fc IgG4, которую применяли в качестве основной структуры, представляла собой молчащую Fc с ослабленной аффинностью к FcgR (Fcγ- (Fc-гамма) рецептор). Н0000 (SEQ ID NO: 40) применяли в качестве вариабельной области Н-цепи GPC3-связывающего домена, a hCE115HA (SEQ ID NO: 52) применяли в качестве вариабельной области Н-цепи CD3-связывающего домена. L0000 (SEQ ID NO: 53) применяли в качестве вариабельной области L-цепи. Мутации D356K и K439E интродуцировали в соответствующие Н-цепи для эффективного образования гетеромеров каждой Н-цепи при получении гетеродимерных антител, содержащих два типа Н-цепей (WO 2006/106905). H435R представляет собой модификацию, которая нарушает связывание с белком А, и ее интродуцировали для эффективного разделения гетеромера и гомомера (WO 2011/078332).
Серии экспрессионных векторов со встроенным полинуклеотидом, кодирующим каждую из конструкций f H0000-ERY27_HK (SEQ ID NO: 54), hCE115HA-ERY27_HE (SEQ ID NO: 55) и L0000-k0 (SEQ ID NO: 56), получали хорошо известными методами.
Следующую комбинацию экспрессионных векторов интродуцировали в клетки FreeStyle 293-F для кратковременной экспрессии каждой молекулы-мишени.
Молекула-мишень: GPC3_ERY27_hCE115
Полипептиды, кодируемые полинуклеотидами, встроенными в экспрессионные векторы: H0000-ERY27_HK, hCE115HA-ERY27_HE и L0000-k0
(2-6) Очистка GPC3_ERY27_hCE115
Каждую представляющую интерес молекулу очищали методом, описанным в примере 1-2.
(2-7) Измерение цитотоксической активности с использованием мононуклеарных клеток периферической крови человека
(2-7-1) Получение раствора мононуклеарных клеток периферической крови человека (РВМС)
Раствор приготавливали согласно методу, описанному в примере 1-3-1.
(2-7-2) Оценка цитотоксической активности
Цитотоксическую активность оценивали согласно методу, описанному в примере 1-3-2.
Когда РВМС, полученные из человеческой крови, применяли в качестве эффекторных клеток для оценки цитотоксичности GPC3_ERY27_hCE115, было обнаружено снижение активности в результате гуманизации Н-цепи rCE115 и «совместного использования» общей L-цепи (фиг. 2).
Пример 3. Получение и оценка гуманизированных вариантов биспецифических антител для улучшения различных свойств
Зависимая от Т-клеток цитотоксическую активность (TDCC-активность) биспецифического гуманизированного антитела к CD3-цепи (CD3 эпсилон) и к GPC3, полученного согласно методу, описанному в примере 2, GPC3_ERY27_hCE115 (SEQ ID NO: 54, 55 и 56), оказалась ниже, чем зависимая от Т-клеток цитотоксическая активность GPC3_ERY22_rCE115 (SEQ ID NO: 47, 48, 49 и 50). Это может являться результатом ослабления аффинности к GPC3 и CD3ε-цепи в результате гуманизации и «совместного использования» общей L-цепи. Касательно антигенов, таких как GPC3 и CD3ε-цепи, которые имеют независимые друг от друга последовательности, к настоящему времени отсутствуют данные о гуманизированных биспецифических антителах с повышенной зависимой от Т-клеток цитотоксической активностью и улучшенной аффинностью к обоим антигенам при использовании общей L-цепи антитела. Таким образом, представляется сложным получение гуманизированных антител с двойной специфичностью, обладающих эффективностью в качестве лекарственных средств, эквивалентной или более высокой, чем у антитела GPC3_ERY22_rCE115.
С учетом указанных обстоятельств при создании изобретения получали модифицированные гуманизированные биспецифические антитела с модифицированной аффинностью к человеческому GPC3 и человеческой CD3ε-цепи с помощью методов, известных специалистам в данной области, которые включали обширную замену аминокислотных остатков, кодируемых геном антитела, с получением вариантов антител против обоих антигенов, а именно человеческого GPC3 и человеческой CD3ε-цепи, осуществление различных оценок с помощью скрининга. Кроме того, аналогичные методы применяли для получения модифицированных гуманизированных биспецифических антител с модифицированными физико-химическими свойствами. Кроме того, путем объединения замен аминокислотных остатков, обладающих эффективностью в отношении модификации аффинности и физико-химических свойств, получали оптимизированные биспецифические антитела с TDCC-активностью, эквивалентной или более высокой, чем зависимая от Т-клеток клеточная цитотоксичность GPC3_ERY22_rCE115 до гуманизиации.
Интродукцию точечных мутаций, экспрессию и очистку антител, оценку аффинности к антигену и определение зависимой от Т-клеток клеточной цитотоксичности при оптимизации гуманизированных биспецифических антител осуществляли согласно методам, аналогичным описанным в примерах 1 и 2. CDR и FR определяли согласно Кэботу (нумерация Кэбота).
В зависимости от цели следующие конструкции применяли в качестве константных областей Н-цепи антитела (номера соответствуют EU-нумерации): E22Hh (SEQ ID NO: 57), которую получали путем интродукции мутаций L234A/L235A/N297A/D356C/T366S/L368A/Y407V/G446-делеция/K447-делецияв человеческий IgG1; E22Hk (SEQ ID NO: 58), которую получали путем интродукции мутаций L234A/L235A/N297A/Y349C/T366W/G446-делеция/K447-делеция, и инсерционной мутации Ser-Ser непосредственно перед положением 118 в человеческом IgG1; G1dh получали путем интродукции мутаций D356C/T366S/L368A/Y407V/G446-делеция/K447-делеция в человеческий IgG1; none-Hi-Kn010G3 получали путем интродукции делеции 118-215 и мутаций C220S/Y349C/T366W/H435R в человеческий IgG1; E2702GsKsc (SEQ ID NO: 60) получали путем интродукции мутаций L235R/S239K/N297A/E356K/R409K/H435R/L445P/G446-делеция/K447-делецияв человеческий IgG4; E2704sEpsc (SEQ ID NO: 61) получали путем интродукции мутаций K196Q/L235R/S239K/N297A/R409K/K439E/L445P/G446-делеция/K447-делеция в человеческий IgG4; и E2702sKsc (SEQ ID NO: 62) получали путем интродукции мутаций L235R/S239K/N297A/E356K/R409K/L445P/G446-делеция/K-447-делеция в человеческий IgG4. Кроме того, человеческую κ-цепь (каппа-цепь) k0 (SEQ ID NO: 63) и E22L (SEQ ID NO: 432) получали путем интродукции мутаций R108A/T109S в человеческую κ-цепь, применяемую в качестве константных областей L-цепи антитела.
Мутация, приводящая к замене Asp на Cys в положении 356 согласно EU-нумерации, мутация, приводящая к замене The на Ser в положении 366 согласно EU-нумерации, мутация, приводящая к замене Leu на Ala в положении 368 согласно EU-нумерации, мутация, приводящая к заменам Tyr на Val в положении 407 согласно EU-нумерации, мутация, приводящая к замене Tyr на Cys в положении 349 согласно EU-нумерации, мутация, приводящая к замене Thr на Trp в положении 366 согласно EU-нумерации, и мутация, приводящая к вставке Ser-Ser непосредственно перед положением 118 согласно EU-нумерации, представляют собой мутации, предназначенные для эффективного образования гетеродимерных молекул каждой Н-цепи при создании гетеромерных антител. Аналогично этому, мутация, приводящая к замене Glu на Lys в положении 356 согласно EU-нумерации, и мутация, приводящая к замене Lys на Glu в положении 439 согласно EU-нумерации, также представляют собой мутации, предназначенные для эффективного образования гетеродимерных молекул каждой Н-цепи при создании гетеромерных антител. Как ожидается, они должны повышать эффективность производства биспецифических антител.
Мутация, приводящая к замене Leu на Ala в положение 234 согласно EU-нумерации, мутация, приводящая к заменам Leu на Ala или Arg в положение 235 согласно EU-нумерации, мутация, приводящая к замене Ser на Lys в положение 239 согласно EU-нумерации, и мутация, приводящая к замене Asn на Ala в положение 297 согласно EU-нумерации, представляют собой мутации, предназначенные для ослабления аффинности к Fcγ-рецептору и комплементу (C1q). Как ожидается, они должны подавлять связывание Fab с CD3 и опосредуемое Fc перекрестное сшивание Fcγ-рецептора или комплемента и позволять избегать синдрома высвобождения цитокинов, который сопровождает повышение неспецифических эффекторных функций.
Н-цепь, в которую интродуцированы делеционные мутации в положениях 118-215 согласно EU-нумерации, можно объединять с полноразмерной последовательностью Н-цепи с получением антитела, которое имеет только один Fab (одновалентное антитело), и ее можно применять для оценки аффинности.
Мутация, приводящая к замене Arg на Lys в положении 409 согласно EU-нумерации, и мутация, приводящая к замене His на Arg в положении 435 согласно EU-нумерации, представляют собой мутации, приводящие к модификации свойства антитела, приближая их к свойствам человеческого IgG1 и человеческого IgG3 соответственно.
(3-1) Модификация аффинности гуманизированного антитела к CD3 с помощью точечных мутаций
Сначала интродуцировали точечные мутации в последовательность FR1, FR2, FR3, CDR1, CDR2 и CDR3 гуманизированного антитела к человеческой CD3ε-цепи, полученного согласно методу, описанному в примере 2, hCE115HA-ERY27_HE (SEQ ID NO: 55), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимой человеческой CD3ε-цепи. Объединяя сайты, которые обладают способностью повышать аффинность модифицированных антител, получали модифицированные антитела, аффинности которых представлены в таблице 8.



(3-2) Модификация аффинности гуманизированного антитела к GPC3 с помощью точечных мутаций
Сначала интродуцировали точечные мутации в последовательность CDR1, CDR2 и CDR3 биспецифического антитела, полученного согласно методу, описанному в примере 2, H0000-ERY27_HK (SEQ ID NO: 54), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимому человеческому GPC3. Объединяя сайты, которые обладают способностью повышать аффинность модифицированных антител, получали модифицированные антитела, аффинности которых представлены в таблице 9.



(3-3) Модификация pI с помощью точечных мутаций
При коммерческом производстве биспецифических антител требуется высокой уровень чистоты. При использовании ионообменной хроматографии эффективной является модификация изоэлектрической точки (pI) молекул (PLoS One. 2013; 8(2):e57479). По этой причине интродуцировали мутации для модификаций pI в последовательность CDR1, CDR2 и CDR3 гуманизированного антитела к человеческому GPC3, полученного согласно методу, описанному в примере 2, H0000-ERY27_HK (SEQ ID NO: 54), для получения модифицированных антител. Затем определяли аффинность указанных модифицированных антител к растворимому человеческому GPC3.
В результате установлено, что аминокислотным модификациям, которые могут приводить к снижению pI, сохраняя при этом аффинность к человеческому GPC3, следует подвергать аминокислоты в положениях 19, 43, 53 и 61 согласно нумерации Кэбота.
Объединяя сайты, которые обладают способностью поддерживать аффинность к человеческому GPC3 и снижать pI, получали антитела, аффинности и pI которых представлены в таблице 10.
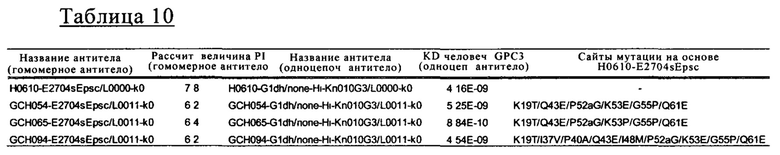
(3-4) Модификация способности связывать внеклеточный матрикс с помощью точечной мутации
Известно, что неспецифическое связывание с внеклеточным матриксом (ЕСМ) и т.п. может оказывать влияние на фармакокинетику (MAbs. 4(6), ноябрь-декабрь 2012 г., cc. 753-760). Таким образом, ЕСМ-связывающую способность модифицированных антител, полученных согласно описанным в примерах методам, определяли с помощью метода, представленного в приведенном для справки примере 4. В результате было подтверждено, что гуманизированное биспецифическое антитело к человеческой CD3ε-цепи и к человеческому GPC3, GPC3_ERY27_hCE115 (SEQ ID NO: 54, 55 и 56), обладало высокой ЕСМ-связывающей способностью. Таким путем изучали любую из оцененных в примерах 3-1, 3-2 и 3-3 точечных мутаций в последовательности гуманизированного антитела к человеческой CD3ε-цепи hCE115HA-ERY27_HE (SEQ ID NO: 55) в качестве комбинации для снижения ЕСМ-связывающей способности. В результате было установлено, что аминокислоты в положениях 11, 16, 52а, 53, 98 и 100 согласно нумерации Кэбота участвуют в поддержании аффинности к CD3ε и могут влиять на снижение ЕСМ-связывающей способности, и получали антитела с пониженной ЕСМ-связывающей способностью по сравнению со способностью варианта гуманизированного биспецифического антитела к человеческой CD3ε-цепи и к человеческому GPC3, GPC3_ERY27_hCE115 (таблица 11).
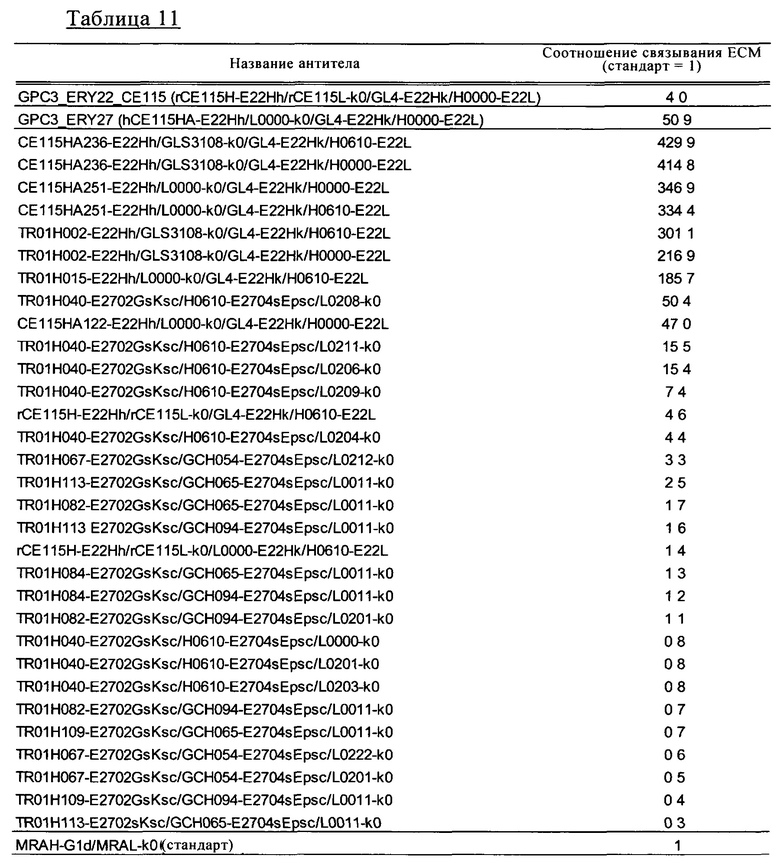
(3-5) Модификации способности связываться с лигандом SuRe™ с помощью точечных мутаций
Известен пример того, что связывание антитела с белком А зависит от последовательности вариабельной области (VH3) (J Biomol Tech. 22(2), июль 2011 г., cc. 50-52). При очистке на белке А гуманизированного биспецифического антитела к человеческой CD3ε-цепи и к человеческому GPC3, удаление гомомерного антитела к CD3 являлось важным для подавления неспецифических реакцией посредством CD3. Таким образом, представляется желательным подавлять связывание гомомерного антитела к CD3 с белком А. Вероятно, лиганд SuRe™ можно применять при коммерческом производстве и поэтому точечные мутации, влияющие на связывание с лигандом SuRe™, интродуцировали в CDR2 Н-цепи вариантов гуманизированного антитела к CD3, TR01H082-E2702GsKsc и TR01H084-E2702GsKsc (SEQ ID NO: 398 и 399), для получения модифицированных антител. Связывающую способность этих модифицированных антител с лигандом SuRe™ определяли с помощью метода, представленного в приведенном для справки примере 5. В результате было установлено, что аминокислоты в положениях 19, 57 и 59 согласно нумерации Кэбота участвуют в поддержании аффинности к CD3ε и могут влиять на способность связываться с лигандом Sure™, и получали антитела с пониженной способностью связываться с лигандом Sure™ по сравнению со способностью антител TR01H082-E2702GsKsc/L0011-k0 (SEQ ID NO: 398 и 410) или TR01H084-E2702GsKsc/L0011-k0 (SEQ ID NO: 399 и 410) (таблица 12).
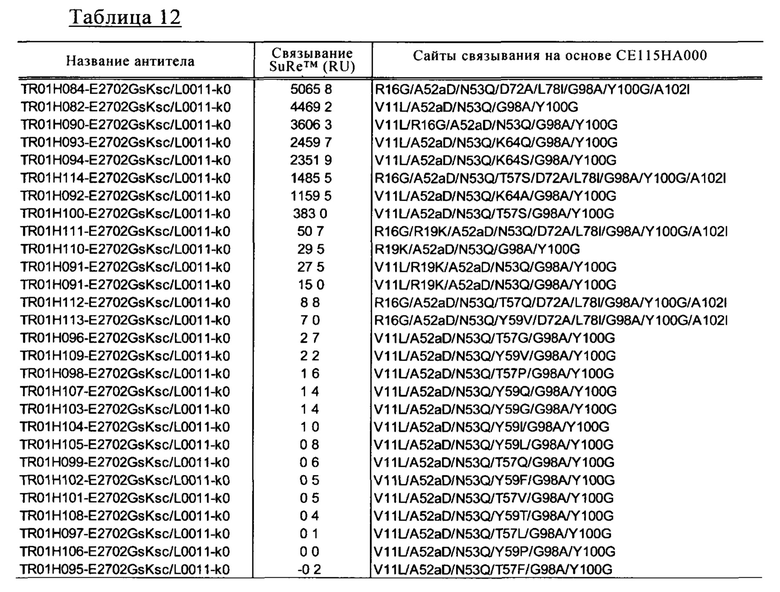
(3-6) Получение оптимизированных биспецифических антител путем объединения точечных мутаций, приводящих к улучшению различных свойств
Оптимизированные модифицированные антитела можно получать, объединяя точечные мутации, которые приводят к улучшению различных свойств, описанных в примерах 3-1-3-5. В качестве примеров указанных модифицированных антител получали антитела, представленные в таблице 13, и у них оценивали зависимую от Т-клеток клеточную цитотоксичность (TDCC) с помощью методов, аналогичных описанным в примере 1. Результаты представлены на фиг. 4-9. В результате получали оптимизированные гуманизированные биспецифические антитела к человеческой CD3ε-цепи и к человеческому GPC3, обладающие эквивалентной или более высокой зависимой от Т-клеток клеточной цитотоксичностью, чем GPC3_ERY22_rCE115 до его гуманизации.

В примерах 3-1-3-6 продемонстрировано, что указанные ниже аминокислотные остатки, например, являются важными для поддержания свойств оптимизированных биспецифических антител к человеческой CD3ε-цепи и к человеческому GPC3, которые обладали эквивалентной или более высокой зависимой от Т-клеток клеточной цитотоксичностью, чем GPC3_ERY22_rCE115 до его гуманизации.
В антителах к человеческой CD3ε-цепи присутствуют, например, Leu в положении 11, Gly в положении 16, Asp в положении 52а, Gln в положении 53, Ala в положении 72, Ile в положении 78, Ala в положении 98, Gly в положении 100 и Ile в положении 102. В антителах к человеческому GPC3 присутствуют, например, Thr в положении 19, Glu в положении 43, Gly в положении 52а, Pro или Glu в положении 53, Pro в положении 55 и Glu в положении 61. Кроме того, в общих L-цепях присутствуют, например. Pro в положении 25, Pro в положении 27а, Pro в положении 27b, Ile в положении 33, Gln в положении 34, Arg или Trp в положении 56 и Tyr в положении 89 (все положения обозначены согласно нумерации Кэбота).
Пример 4. Оценка эффективности in vivo
Эффективность некоторых из описанных выше антител оценивали in vivo с использованием несущих опухоли модельных животных.
Оценку эффективности in vivo осуществляли для репрезентативных антител из представленных в таблице 13, для которых продемонстрировано наличие цитотоксической активности при оценке с использованием анализа in vitro, описанного в примере 3-6. При оценке эффективности in vivo следует принимать во внимание любое влияние, вызываемое различиями в микроокружении из-за образования агрегатов опухолей, на результаты оценки. Для изучения использовали два типа клеточных линий человеческого рака с различной чувствительностью к действию применяемых в качестве лекарственных средств антител, т.е. линии PC-10 и NCI-H446, несмотря на то, что уровни экспрессии GPC3 в этих клетках были практически одинаковыми. Клеточные линии трансплантировали мышам с тяжелым комбинированным иммунодефицитом (NOD scid) и мышам NOD scid, у которых было подтверждено образование опухолей, трансплантировали Т-клетки, выращенные культивированием in vitro человеческих РВМС. Мышей (которых обозначали как модель с инъецированными Т-клетками) обрабатывали путем введения оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3.
Более конкретно, в опытах по оценке эффективности в качестве лекарственных средств оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3, в которых применяли клетки линии PC-10 на модели с инъецированными Т-клетками, осуществляли описанные ниже опыты. Т-клетки размножали культивированием с использованием РВМС, выделенных из крови здоровых доноров, и набора для активации/экспансии человеческих Т-клеток (Т cell activation/expansion kit/human) (фирма MACS Miltenyi biotec). Смешивали клеточную линию человеческого рака PC-10 (1×107 клеток) с матриксом базальной мембраны Matrigel™ (фирма BD) и трансплантировали подкожно в паховую область мышей NOD scid (фирма CLEA Japan, самки возрастом 6 недель). День трансплантации обозначали как день 0. За 1 день до трансплантации мышам внутрибрюшинно вводили антитело к асиало-ганглиозиду M1 (асиало-GM1) (фирма Wako Pure Chemical Industries) из расчета 0,2 мг/мышь. Через 13-15 дней после трансплантации мышей разделяли на группы в зависимости от веса тела и размера опухолей и вновь внутрибрюшинно вводили антитело к асиало-GM1 из расчета 0,2 мг/мышь. На следующий день внутрибрюшинно трансплантировали Т-клетки, полученные вышеописанным методом размножения культивированием, из расчета 3×107 клеток/мышь. Через 4 ч после трансплантации Т-клеток внутривенно через каудальную вену вводили оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 из расчета 1 мг/кг. Оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 вводили только один раз.
В результате установлена более выраженная противоопухолевая активность в группе, обработанной оптимизированными биспецифическими антителами к человеческой CD3ε-цепи и человеческому GPC3, по сравнению с группой, обработанной растворителем (фиг. 10а, б).
Аналогичными методами осуществляли опыты по оценке эффективности в качестве лекарственных средств оптимизированных биспецифических антител к человеческой CD3ε-цепи и человеческому GPC3, в которых применяли клетки линии NCI-H446, на модели с инъецированными Т-клетками. Для оценки воздействия на NCI-H446 оптимизированные биспецифические антитела к человеческой CD3ε-цепи и человеческому GPC3 вводили один раз через каудальную вену из расчета 5 мг/кг.
В результате установлена более выраженная противоопухолевая активность в группе, обработанной оптимизированными биспецифическими антителами к человеческой CD3ε-цепи и человеческому GPC3, по сравнению с группой, обработанной растворителем (фиг. 11a, б).
Приведенные для справки примеры
Приведенный для справки пример 1. Получение экспрессионных векторов антител и экспрессия и очистка антител
Аминокислотные замены интродуцировали методами, известными специалистам в данной области, например, с использованием набора для сайтнаправленного мутагенеза QuikChange (фирма Stratagene), ПЦР или набора для ПЦР-клонирования In-fusion Advantage (фирма TAKARA), для создания экспрессионных векторов. Нуклеотидные последовательности полученных экспрессионных векторов определяли с помощью метода, известного специалистам в данной области. Полученные плазмиды кратковременно интродуцировали в клетки клеточной линии, полученной из почки человеческого эмбриона HEK293H (фирма Invitrogen) или FreeStyle293 (фирма Invitrogen) для экспрессии антител. Из полученных супернатантов культуры антитела очищали с использованием колонки rProtein A Sepharose Fast Flow (фирма GE Healthcare) с помощью метода, известного специалистам в данной области. Измеряли абсорбцию при 280 нм растворов очищенных антител с помощью спектрофотометра, и концентрацию антител рассчитывали на основе определенных величин, применяя коэффициент абсорбции, рассчитанный с помощью метода PACE (Protein Science 4, 1995, cc. 2411-2423).
Приведенный для справки пример 2. Определение ADCC-активности каждого из тестируемых антител с использованием мононуклеарных клеток периферической крови человека в качестве эффекторных клеток
ADCC-активность каждого из тестируемых антител определяли с помощью описанного ниже метода.
Мононуклеарные клетки периферической крови человека (обозначены далее как человеческие РВМС) применяли в качестве эффекторных клеток для измерения ADCC-активности каждого из тестируемых антител согласно описанному ниже методу.
(1) Получение раствора человеческих РВМС
Получали образцы по 50 мл периферической крови здоровых добровольцев (взрослые мужчины) с использованием шприцев, предварительно заполненных 200 мкл (1000 ед./мл) раствора гепарина (Novo-Heparin 5000 ед. на инъекцию; фирма Novo Nordisk). Эту периферическую кровь двукратно разводили ЗФР(-), разделяли на четыре аликвоты и добавляли в пробирки для разделения лимфоцитов Leucosep (фирма Greiner bio-one), в которые предварительно вносили 15 мл фиколл-пак PLUS и центрифугировали. После центрифугирования пробирок для разделения, содержащих аликвоты периферической крови, при 2150 об/мин в течение 10 мин при комнатной температуре собирали фракции мононуклеарных клеток. Клетки в каждой фракции однократно промывали с использованием модифицированной по методу Дульбекко среды Игла (фирма SIGMA), содержащей 10% FBS (далее в контексте настоящего описания обозначена как 10%FBS/D-MEM), а затем плотность клеток доводили до 5×106 клеток/мл с помощью 10% FBS/D-MEM. Клеточную суспензию в приведенных ниже экспериментах использовали в качестве клетки-мишени.
(2) Анализ высвобождения хрома (ADCC-активность)
ADCC-активность оценивали по удельной скорости высвобождения хрома, определенной методом определения высвобождения хрома. Сначала растворы антитела в каждой из приготовленных концентраций (0, 0,004, 0,04, 0,4, 4 и 40 мкг/мл) добавляли в 96-луночный планшет с U-образным дном из расчета 50 мкл на лунку. Затем высевали клетки-мишени из расчета 50 мкл на лунку (1×104 клеток/лунку) и давали выстояться при комнатной температуре в течение 15 мин. Раствор человеческих РВМС, приготовленный согласно методу, описанному в подпункте (1), добавляли из расчета 100 мкл на лунку (5×105 клеток/лунку) и планшет выдерживали в инкубаторе в атмосфере, содержащей 5% диоксида углерода, при 37°С в течение 4 ч, после чего центрифугировали. Радиоактивность в 100 мкл супернатанта культуры в каждой лунке планшета измеряли с помощью гамма-счетчика. Удельную скорость высвобождения хрома определяли по следующей формуле:
удельная скорость высвобождения хрома (%) = (А-Б)×100/(Б-В),
где А представляет собой среднее значение радиоактивности (cpm) 100 мкл супернатанта культуры в каждой лунке; Б представляет собой среднее значение радиоактивности (cpm) 100 мкл супернатанта культуры в лунках, в которых к клеткам-мишеням добавляли 100 мкл 2%-ного водного раствора NP-40 (Nonidet Р-40, фирма Nacalai Tesque) и 50 мкл 10%-ной среды FBS/D-MEM; и В представляет собой среднее значение радиоактивности (cpm) 100 мкл супернатанта культуры в лунках, в которых к клеткам-мишеням добавляли 150 мкл 10%-ной среды FBS/D-MEM. Эксперименты осуществляли в трех повторностях и по результатам вышеуказанного эксперимента вычисляли среднее значение и стандартное отклонение удельной скорости высвобождения хрома (%), отражающей ADCC-активность, для каждого из тестируемых антител.
Приведенный для справки пример 3. Определение Tm модифицированных антител с помощью дифференциальной сканирующей флуорометрии
При такой оценке определяли величину Tm (температура тепловой денатурации) модифицированных антител с помощью дифференциальной сканирующей флуорометрии с использованием устройства Rotor-Gene Q (фирма QIAGEN). Известно, что этот метод обеспечивает предпочтительную корреляцию с величиной Tm, установленной с использованием дифференциального сканирующего калориметра, что является широко известным методом оценки термостабильности антител (Journal of Pharmaceutical Science 4, 2010, cc. 1707-1720).
5000-кратный концентрат SYPRO оранжевого (фирма Molecular Probes) разводили ЗФР (фирма Sigma) и затем смешивали с растворами антител с получением образцов для измерения. Аликвоты по 20 мкл каждого образца вносили в измерительные пробирки и температуру повышали с 30°С до 99°С со скоростью повышения температуру 240°С/ч. Изменения флуоресценции, сопровождающие повышение температуры, определяли при 470 нм (длина волны возбуждения)/555 нм (длина волны флуоресцентного испускания).
Данные анализировали с использованием программы Rotor-Gene Q Series (фирма QIAGEN) для расчета температуры, при которой наблюдается переход флуоресценции, и эту температуру принимали за Тm.
Приведенный для справки пример 4. Определение ЕСМ-связывающей способности
Определение осуществляли согласно методу, описанному в WO 2012/093704. В целом, метод состоял в следующем: BD-Matrigel (фирма BD Biosciences, №356237) получали в концентрации 2 мг/мл с использованием TBS (фирма Takara, № Т903) и переносили в 96-луночный планшет для измерения (фирма Meso Scale Discovery, № L15XB-3(High Bind, высокая способность связываться)) из расчета 5 мкл на лунку и затем давали выстояться в течение ночи в холодном месте. Затем в каждую лунку планшета вносили по 150 мкл блокирующего ECL-буфера (ЗФР, содержащий 0,05% Твин20, 0,5% БСА и 0,01% азида натрия) и давали выстояться при комнатной температуре в течение 2 ч или более.
Козий античеловеческий IgG(γ) (фирма Invitrogen, №628400) метили рутением с использованием сложного эфира NHS, меченного MSD-SULFO (фирма Meso Scale Discovery, № R91AN-2) согласно прилагаемым инструкциям. Его разводили ECL-буфером для разведения (ЗФР, содержащий 0,01% Твин20, 0,1% БСА и 0,01% азида натрия) до конечной концентрации 2 мкг/мл. Кроме того, стандартное антитело и тестируемые антитела разводили ЗФР-Т (ЗФР, содержащий 0,05% Твин20 и 0,01% азида натрия) до получения конечной концентрации 3 мкг/мл.
В 96-луночный планшет для проведения реакции (фирма Thermo scientific, Nunc №145399), последовательно добавляли 10 мкл ECL-буфера для разведения, 20 мкл стандартного антитела и тестируемого антитела (3 мкг/мл) и 30 мкл меченного рутением антитела (2 мкг/мл), и давали прореагировать в течение 1 ч при комнатной температуре при перемешивании в темноте.
Блокирующий ECL-буфер удаляли из 96-луночного планшета для измерения путем опрокидывания, добавляли 50 мкл раствора образца из 96-луночного реакционного планшета и давали выстояться в темноте при комнатной температуре в течение 1 ч. После этого удаляли раствор образца из 96-луночного планшета для измерения (измерительный планшет) путем опрокидывания и немедленно добавляли 150 мкл 2×Т-буфера (4× MSD Т-буфер для считывания (фирма Meso Scale Discovery), двукратно разведенный с помощью ECL-буфера для разведения), осуществляли измерения ECL. Для измерений использовали устройство SECTOR Imager 2400 (фирма Meso Scale Discovery).
Анализы осуществляли путем деления интенсивности флуоресценции тестируемого антитела на интенсивность флуоресценции стандартного антитела, для расчета и сравнения интенсивностей, принимая величину для стандартного антитела за 1.
Приведенный для справки пример 5. Определение способности связывать лиганд SuRe™
Способность связываться с лигандом SuRe™ оценивали, используя Biacore™-Т200 (GE Healthcare Japan). В качестве подвижного буфера применяли HBS-EP+ (фирма GE Healthcare Japan) и набор для аминного сочетания (фирма GE Healthcare Japan) применяли для ковалентного связывания лиганда Mab Select SuRe™ (фирма GE Healthcare Japan) с СМ5-чипом (чип, покрытый карбоксиметилдекстраном). Антитело, применяемое в качестве аналита, приготавливали в концентрации 5 мкг/мл с использованием HBS-EP+. Для осуществления измерений сначала инъецировали раствор с концентрацией антитела 5 мкг/мл со скоростью потока 10 мкл/мин в течение 3 мин, затем аналит заменяли на HBS-EP+ и оценивали ответ (RU) после пропускания потока в течение 0,5 мин. После завершения измерений сенсорный чип регенерировали, промывая 10 мМ Gly-HCl при рН 1,5. В контрольной проточной ячейке осуществляли такой же эксперимент без ковалентного связывания лиганда с чипом, и аффинность к лиганду SuRe™ анализировали на основе различии между ответами (RU).
Последовательности, соответствующие упомянутым выше номерам последовательностей (SEQ ID NO:) представлены ниже в таблице.
Промышленная применимость
В настоящем изобретении предложены новые мультиспецифические антигенсвязывающие молекулы, которые сохраняют сильную противораковую активность, свойственную BiTE, и обладают очень высокой безопасностью, что проявляется в отсутствии индукции независимого от ракового антигена цитокинового шторма, а также обладают продолжительным времененм полужизни в крови. Индуцирующие цитотоксичность агенты, которые содержат в качестве действующего вещества антигенсвязывающую молекулу, предлагаемую в настоящем изобретении, могут направленно воздействлвать на экспрессирующие глипикан 3 клетки и опухолевые ткани, которые содержат такие клетки, и индуцировать повреждение клеток. Введение мультиспецифических антигенсвязывающих молекул, предлагаемых в настоящем изобретении, пациентам позволяет осуществлять требуемое лечение, которое не только отличается высоким уровнем безопасности, но также снижает физическую нагрузку на пациентов и является очень удобным.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Чугаи Сейяку Кабусики Кайся
<120> Индуцирующий цитотоксичность терапевтический агент
<130> C1-A1408P
<140> PCT/JP2015/077024
<141> 2015-09-25
<150> JP 2014-197315
<151> 2014-09-26
<160> 432
<170> PatentIn версия 3.5
<210> 1
<211> 2398
<212> ДНК
<213> Homo sapiens
<400> 1
agccccgccc tgccccgcgc cgccaagcgg ttcccgccct cgcccagcgc ccaggtagct 60
gcgaggaaac ttttgcagcg gctgggtagc agcacgtctc ttgctcctca gggccactgc 120
caggcttgcc gagtcctggg actgctctcg ctccggctgc cactctcccg cgctctccta 180
gctccctgcg aagcaggatg gccgggaccg tgcgcaccgc gtgcttggtg gtggcgatgc 240
tgctcagctt ggacttcccg ggacaggcgc agcccccgcc gccgccgccg gacgccacct 300
gtcaccaagt ccgctccttc ttccagagac tgcagcccgg actcaagtgg gtgccagaaa 360
ctcccgtgcc aggatcagat ttgcaagtat gtctccctaa gggcccaaca tgctgctcaa 420
gaaagatgga agaaaaatac caactaacag cacgattgaa catggaacag ctgcttcagt 480
ctgcaagtat ggagctcaag ttcttaatta ttcagaatgc tgcggttttc caagaggcct 540
ttgaaattgt tgttcgccat gccaagaact acaccaatgc catgttcaag aacaactacc 600
caagcctgac tccacaagct tttgagtttg tgggtgaatt tttcacagat gtgtctctct 660
acatcttggg ttctgacatc aatgtagatg acatggtcaa tgaattgttt gacagcctgt 720
ttccagtcat ctatacccag ctaatgaacc caggcctgcc tgattcagcc ttggacatca 780
atgagtgcct ccgaggagca agacgtgacc tgaaagtatt tgggaatttc cccaagctta 840
ttatgaccca ggtttccaag tcactgcaag tcactaggat cttccttcag gctctgaatc 900
ttggaattga agtgatcaac acaactgatc acctgaagtt cagtaaggac tgtggccgaa 960
tgctcaccag aatgtggtac tgctcttact gccagggact gatgatggtt aaaccctgtg 1020
gcggttactg caatgtggtc atgcaaggct gtatggcagg tgtggtggag attgacaagt 1080
actggagaga atacattctg tcccttgaag aacttgtgaa tggcatgtac agaatctatg 1140
acatggagaa cgtactgctt ggtctctttt caacaatcca tgattctatc cagtatgtcc 1200
agaagaatgc aggaaagctg accaccactg aaactgagaa gaaaatatgg cacttcaaat 1260
atcctatctt cttcctgtgt atagggctag acttacagat tggcaagtta tgtgcccatt 1320
ctcaacaacg ccaatataga tctgcttatt atcctgaaga tctctttatt gacaagaaag 1380
tattaaaagt tgctcatgta gaacatgaag aaaccttatc cagccgaaga agggaactaa 1440
ttcagaagtt gaagtctttc atcagcttct atagtgcttt gcctggctac atctgcagcc 1500
atagccctgt ggcggaaaac gacacccttt gctggaatgg acaagaactc gtggagagat 1560
acagccaaaa ggcagcaagg aatggaatga aaaaccagtt caatctccat gagctgaaaa 1620
tgaagggccc tgagccagtg gtcagtcaaa ttattgacaa actgaagcac attaaccagc 1680
tcctgagaac catgtctatg cccaaaggta gagttctgga taaaaacctg gatgaggaag 1740
ggtttgaaag tggagactgc ggtgatgatg aagatgagtg cattggaggc tctggtgatg 1800
gaatgataaa agtgaagaat cagctccgct tccttgcaga actggcctat gatctggatg 1860
tggatgatgc gcctggaaac agtcagcagg caactccgaa ggacaacgag ataagcacct 1920
ttcacaacct cgggaacgtt cattccccgc tgaagcttct caccagcatg gccatctcgg 1980
tggtgtgctt cttcttcctg gtgcactgac tgcctggtgc ccagcacatg tgctgcccta 2040
cagcaccctg tggtcttcct cgataaaggg aaccactttc ttattttttt ctattttttt 2100
ttttttgtta tcctgtatac ctcctccagc catgaagtag aggactaacc atgtgttatg 2160
ttttcgaaaa tcaaatggta tcttttggag gaagatacat tttagtggta gcatatagat 2220
tgtccttttg caaagaaaga aaaaaaacca tcaagttgtg ccaaattatt ctcctatgtt 2280
tggctgctag aacatggtta ccatgtcttt ctctctcact ccctcccttt ctatcgttct 2340
ctctttgcat ggatttcttt gaaaaaaaat aaattgctca aataaaaaaa aaaaaaaa 2398
<210> 2
<211> 603
<212> PRT
<213> Homo sapiens
<400> 2
Met Ala Gly Thr Val Arg Thr Ala Cys Leu Val Val Ala Met Leu Leu
1 5 10 15
Ser Leu Asp Phe Pro Gly Gln Ala Gln Pro Pro Pro Pro Pro Pro Asp
20 25 30
Ala Thr Cys His Gln Val Arg Ser Phe Phe Gln Arg Leu Gln Pro Gly
35 40 45
Leu Lys Trp Val Pro Glu Thr Pro Val Pro Gly Ser Asp Leu Gln Val
50 55 60
Cys Leu Pro Lys Gly Pro Thr Cys Cys Ser Arg Lys Met Glu Glu Lys
65 70 75 80
Tyr Gln Leu Thr Ala Arg Leu Asn Met Glu Gln Leu Leu Gln Ser Ala
85 90 95
Ser Met Glu Leu Lys Phe Leu Ile Ile Gln Asn Ala Ala Val Phe Gln
100 105 110
Glu Ala Phe Glu Ile Val Val Arg His Ala Lys Asn Tyr Thr Asn Ala
115 120 125
Met Phe Lys Asn Asn Tyr Pro Ser Leu Thr Pro Gln Ala Phe Glu Phe
130 135 140
Val Gly Glu Phe Phe Thr Asp Val Ser Leu Tyr Ile Leu Gly Ser Asp
145 150 155 160
Ile Asn Val Asp Asp Met Val Asn Glu Leu Phe Asp Ser Leu Phe Pro
165 170 175
Val Ile Tyr Thr Gln Leu Met Asn Pro Gly Leu Pro Asp Ser Ala Leu
180 185 190
Asp Ile Asn Glu Cys Leu Arg Gly Ala Arg Arg Asp Leu Lys Val Phe
195 200 205
Gly Asn Phe Pro Lys Leu Ile Met Thr Gln Val Ser Lys Ser Leu Gln
210 215 220
Val Thr Arg Ile Phe Leu Gln Ala Leu Asn Leu Gly Ile Glu Val Ile
225 230 235 240
Asn Thr Thr Asp His Leu Lys Phe Ser Lys Asp Cys Gly Arg Met Leu
245 250 255
Thr Arg Met Trp Tyr Cys Ser Tyr Cys Gln Gly Leu Met Met Val Lys
260 265 270
Pro Cys Gly Gly Tyr Cys Asn Val Val Met Gln Gly Cys Met Ala Gly
275 280 285
Val Val Glu Ile Asp Lys Tyr Trp Arg Glu Tyr Ile Leu Ser Leu Glu
290 295 300
Glu Leu Val Asn Gly Met Tyr Arg Ile Tyr Asp Met Glu Asn Val Leu
305 310 315 320
Leu Gly Leu Phe Ser Thr Ile His Asp Ser Ile Gln Tyr Val Gln Lys
325 330 335
Asn Ala Gly Lys Leu Thr Thr Thr Glu Thr Glu Lys Lys Ile Trp His
340 345 350
Phe Lys Tyr Pro Ile Phe Phe Leu Cys Ile Gly Leu Asp Leu Gln Ile
355 360 365
Gly Lys Leu Cys Ala His Ser Gln Gln Arg Gln Tyr Arg Ser Ala Tyr
370 375 380
Tyr Pro Glu Asp Leu Phe Ile Asp Lys Lys Val Leu Lys Val Ala His
385 390 395 400
Val Glu His Glu Glu Thr Leu Ser Ser Arg Arg Arg Glu Leu Ile Gln
405 410 415
Lys Leu Lys Ser Phe Ile Ser Phe Tyr Ser Ala Leu Pro Gly Tyr Ile
420 425 430
Cys Ser His Ser Pro Val Ala Glu Asn Asp Thr Leu Cys Trp Asn Gly
435 440 445
Gln Glu Leu Val Glu Arg Tyr Ser Gln Lys Ala Ala Arg Asn Gly Met
450 455 460
Lys Asn Gln Phe Asn Leu His Glu Leu Lys Met Lys Gly Pro Glu Pro
465 470 475 480
Val Val Ser Gln Ile Ile Asp Lys Leu Lys His Ile Asn Gln Leu Leu
485 490 495
Arg Thr Met Ser Met Pro Lys Gly Arg Val Leu Asp Lys Asn Leu Asp
500 505 510
Glu Glu Gly Phe Glu Ser Gly Asp Cys Gly Asp Asp Glu Asp Glu Cys
515 520 525
Ile Gly Gly Ser Gly Asp Gly Met Ile Lys Val Lys Asn Gln Leu Arg
530 535 540
Phe Leu Ala Glu Leu Ala Tyr Asp Leu Asp Val Asp Asp Ala Pro Gly
545 550 555 560
Asn Ser Gln Gln Ala Thr Pro Lys Asp Asn Glu Ile Ser Thr Phe His
565 570 575
Asn Leu Gly Asn Val His Ser Pro Leu Lys Leu Leu Thr Ser Met Ala
580 585 590
Ile Ser Val Val Cys Phe Phe Phe Leu Val His
595 600
<210> 3
<211> 19
<212> PRT
<213> Artificial
<220>
<223> An artificially generated sequence
<400> 3
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser
<210> 4
<211> 141
<212> PRT
<213> Homo sapiens
<400> 4
Asp Ile Gln Asn Pro Asp Pro Ala Val Tyr Gln Leu Arg Asp Ser Lys
1 5 10 15
Ser Ser Asp Lys Ser Val Cys Leu Phe Thr Asp Phe Asp Ser Gln Thr
20 25 30
Asn Val Ser Gln Ser Lys Asp Ser Asp Val Tyr Ile Thr Asp Lys Thr
35 40 45
Val Leu Asp Met Arg Ser Met Asp Phe Lys Ser Asn Ser Ala Val Ala
50 55 60
Trp Ser Asn Lys Ser Asp Phe Ala Cys Ala Asn Ala Phe Asn Asn Ser
65 70 75 80
Ile Ile Pro Glu Asp Thr Phe Phe Pro Ser Pro Glu Ser Ser Cys Asp
85 90 95
Val Lys Leu Val Glu Lys Ser Phe Glu Thr Asp Thr Asn Leu Asn Phe
100 105 110
Gln Asn Leu Ser Val Ile Gly Phe Arg Ile Leu Leu Leu Lys Val Ala
115 120 125
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
130 135 140
<210> 5
<211> 179
<212> PRT
<213> Homo sapiens
<400> 5
Glu Asp Leu Lys Asn Val Phe Pro Pro Glu Val Ala Val Phe Glu Pro
1 5 10 15
Ser Glu Ala Glu Ile Ser His Thr Gln Lys Ala Thr Leu Val Cys Leu
20 25 30
Ala Thr Gly Phe Tyr Pro Asp His Val Glu Leu Ser Trp Trp Val Asn
35 40 45
Gly Lys Glu Val His Ser Gly Val Ser Thr Asp Pro Gln Pro Leu Lys
50 55 60
Glu Gln Pro Ala Leu Asn Asp Ser Arg Tyr Cys Leu Ser Ser Arg Leu
65 70 75 80
Arg Val Ser Ala Thr Phe Trp Gln Asn Pro Arg Asn His Phe Arg Cys
85 90 95
Gln Val Gln Phe Tyr Gly Leu Ser Glu Asn Asp Glu Trp Thr Gln Asp
100 105 110
Arg Ala Lys Pro Val Thr Gln Ile Val Ser Ala Glu Ala Trp Gly Arg
115 120 125
Ala Asp Cys Gly Phe Thr Ser Glu Ser Tyr Gln Gln Gly Val Leu Ser
130 135 140
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
145 150 155 160
Val Leu Val Ser Ala Leu Val Leu Met Ala Met Val Lys Arg Lys Asp
165 170 175
Ser Arg Gly
<210> 6
<211> 173
<212> PRT
<213> Homo sapiens
<400> 6
Asp Lys Gln Leu Asp Ala Asp Val Ser Pro Lys Pro Thr Ile Phe Leu
1 5 10 15
Pro Ser Ile Ala Glu Thr Lys Leu Gln Lys Ala Gly Thr Tyr Leu Cys
20 25 30
Leu Leu Glu Lys Phe Phe Pro Asp Val Ile Lys Ile His Trp Gln Glu
35 40 45
Lys Lys Ser Asn Thr Ile Leu Gly Ser Gln Glu Gly Asn Thr Met Lys
50 55 60
Thr Asn Asp Thr Tyr Met Lys Phe Ser Trp Leu Thr Val Pro Glu Lys
65 70 75 80
Ser Leu Asp Lys Glu His Arg Cys Ile Val Arg His Glu Asn Asn Lys
85 90 95
Asn Gly Val Asp Gln Glu Ile Ile Phe Pro Pro Ile Lys Thr Asp Val
100 105 110
Ile Thr Met Asp Pro Lys Asp Asn Cys Ser Lys Asp Ala Asn Asp Thr
115 120 125
Leu Leu Leu Gln Leu Thr Asn Thr Ser Ala Tyr Tyr Met Tyr Leu Leu
130 135 140
Leu Leu Leu Lys Ser Val Val Tyr Phe Ala Ile Ile Thr Cys Cys Leu
145 150 155 160
Leu Arg Arg Thr Ala Phe Cys Cys Asn Gly Glu Lys Ser
165 170
<210> 7
<211> 204
<212> PRT
<213> Homo sapiens
<400> 7
Lys Gln Leu Asp Ala Asp Val Ser Pro Lys Pro Thr Ile Phe Leu Pro
1 5 10 15
Ser Ile Ala Glu Thr Lys Leu Gln Lys Ala Gly Thr Tyr Leu Cys Leu
20 25 30
Leu Glu Lys Phe Phe Pro Asp Ile Ile Lys Ile His Trp Gln Glu Lys
35 40 45
Lys Ser Asn Thr Ile Leu Gly Ser Gln Glu Gly Asn Thr Met Lys Thr
50 55 60
Asn Asp Thr Tyr Met Lys Phe Ser Trp Leu Thr Val Pro Glu Glu Ser
65 70 75 80
Leu Asp Lys Glu His Arg Cys Ile Val Arg His Glu Asn Asn Lys Asn
85 90 95
Gly Ile Asp Gln Glu Ile Ile Phe Pro Pro Ile Lys Thr Asp Val Thr
100 105 110
Thr Val Asp Pro Lys Asp Ser Tyr Ser Lys Asp Ala Asn Asp Val Thr
115 120 125
Thr Val Asp Pro Lys Tyr Asn Tyr Ser Lys Asp Ala Asn Asp Val Ile
130 135 140
Thr Met Asp Pro Lys Asp Asn Trp Ser Lys Asp Ala Asn Asp Thr Leu
145 150 155 160
Leu Leu Gln Leu Thr Asn Thr Ser Ala Tyr Tyr Met Tyr Leu Leu Leu
165 170 175
Leu Leu Lys Ser Val Val Tyr Phe Ala Ile Ile Thr Cys Cys Leu Leu
180 185 190
Gly Arg Thr Ala Phe Cys Cys Asn Gly Glu Lys Ser
195 200
<210> 8
<211> 177
<212> PRT
<213> Homo sapiens
<400> 8
Pro Ser Tyr Thr Gly Gly Tyr Ala Asp Lys Leu Ile Phe Gly Lys Gly
1 5 10 15
Thr Arg Val Thr Val Glu Pro Arg Ser Gln Pro His Thr Lys Pro Ser
20 25 30
Val Phe Val Met Lys Asn Gly Thr Asn Val Ala Cys Leu Val Lys Glu
35 40 45
Phe Tyr Pro Lys Asp Ile Arg Ile Asn Leu Val Ser Ser Lys Lys Ile
50 55 60
Thr Glu Phe Asp Pro Ala Ile Val Ile Ser Pro Ser Gly Lys Tyr Asn
65 70 75 80
Ala Val Lys Leu Gly Lys Tyr Glu Asp Ser Asn Ser Val Thr Cys Ser
85 90 95
Val Gln His Asp Asn Lys Thr Val His Ser Thr Asp Phe Glu Val Lys
100 105 110
Thr Asp Ser Thr Asp His Val Lys Pro Lys Glu Thr Glu Asn Thr Lys
115 120 125
Gln Pro Ser Lys Ser Cys His Lys Pro Lys Ala Ile Val His Thr Glu
130 135 140
Lys Val Asn Met Met Ser Leu Thr Val Leu Gly Leu Arg Met Leu Phe
145 150 155 160
Ala Lys Thr Val Ala Val Asn Phe Leu Leu Thr Ala Lys Leu Phe Phe
165 170 175
Leu
<210> 9
<211> 1311
<212> ДНК
<213> Homo sapiens
<400> 9
agtctagctg ctgcacaggc tggctggctg gctggctgct aagggctgct ccacgctttt 60
gccggaggac agagactgac atggaacagg ggaagggcct ggctgtcctc atcctggcta 120
tcattcttct tcaaggtact ttggcccagt caatcaaagg aaaccacttg gttaaggtgt 180
atgactatca agaagatggt tcggtacttc tgacttgtga tgcagaagcc aaaaatatca 240
catggtttaa agatgggaag atgatcggct tcctaactga agataaaaaa aaatggaatc 300
tgggaagtaa tgccaaggac cctcgaggga tgtatcagtg taaaggatca cagaacaagt 360
caaaaccact ccaagtgtat tacagaatgt gtcagaactg cattgaacta aatgcagcca 420
ccatatctgg ctttctcttt gctgaaatcg tcagcatttt cgtccttgct gttggggtct 480
acttcattgc tggacaggat ggagttcgcc agtcgagagc ttcagacaag cagactctgt 540
tgcccaatga ccagctctac cagcccctca aggatcgaga agatgaccag tacagccacc 600
ttcaaggaaa ccagttgagg aggaattgaa ctcaggactc agagtagtcc aggtgttctc 660
ctcctattca gttcccagaa tcaaagcaat gcattttgga aagctcctag cagagagact 720
ttcagcccta aatctagact caaggttccc agagatgaca aatggagaag aaaggccatc 780
agagcaaatt tgggggtttc tcaaataaaa taaaaataaa aacaaatact gtgtttcaga 840
agcgccacct attggggaaa attgtaaaag aaaaatgaaa agatcaaata accccctgga 900
tttgaatata attttttgtg ttgtaatttt tatttcgttt ttgtataggt tataattcac 960
atggctcaaa tattcagtga aagctctccc tccaccgcca tcccctgcta cccagtgacc 1020
ctgttgccct cttcagagac aaattagttt ctcttttttt tttttttttt tttttttttg 1080
agacagtctg gctctgtcac ccaggctgaa atgcagtggc accatctcgg ctcactgcaa 1140
cctctgcctc ctgggttcaa gcgattctcc tgcctcagcc tcccgggcag ctgggattac 1200
aggcacacac taccacacct ggctaatttt tgtattttta gtagagacag ggttttgctc 1260
tgttggccaa gctggtctcg aactcctgac ctcaagtgat ccgcccgcct c 1311
<210> 10
<211> 771
<212> ДНК
<213> Homo sapiens
<400> 10
agagaagcag acatcttcta gttcctcccc cactctcctc tttccggtac ctgtgagtca 60
gctaggggag ggcagctctc acccaggctg atagttcggt gacctggctt tatctactgg 120
atgagttccg ctgggagatg gaacatagca cgtttctctc tggcctggta ctggctaccc 180
ttctctcgca agtgagcccc ttcaagatac ctatagagga acttgaggac agagtgtttg 240
tgaattgcaa taccagcatc acatgggtag agggaacggt gggaacactg ctctcagaca 300
ttacaagact ggacctggga aaacgcatcc tggacccacg aggaatatat aggtgtaatg 360
ggacagatat atacaaggac aaagaatcta ccgtgcaagt tcattatcga atgtgccaga 420
gctgtgtgga gctggatcca gccaccgtgg ctggcatcat tgtcactgat gtcattgcca 480
ctctgctcct tgctttggga gtcttctgct ttgctggaca tgagactgga aggctgtctg 540
gggctgccga cacacaagct ctgttgagga atgaccaggt ctatcagccc ctccgagatc 600
gagatgatgc tcagtacagc caccttggag gaaactgggc tcggaacaag tgaacctgag 660
actggtggct tctagaagca gccattacca actgtacctt cccttcttgc tcagccaata 720
aatatatcct ctttcactca gaaaaaaaaa aaaaaaaaaa aaaaaaaaaa a 771
<210> 11
<211> 1534
<212> ДНК
<213> Homo sapiens
<400> 11
tattgtcaga gtcctcttgt ttggccttct aggaaggctg tgggacccag ctttcttcaa 60
ccagtccagg tggaggcctc tgccttgaac gtttccaagt gaggtaaaac ccgcaggccc 120
agaggcctct ctacttcctg tgtggggttc agaaaccctc ctcccctccc agcctcaggt 180
gcctgcttca gaaaatgaag tagtaagtct gctggcctcc gccatcttag taaagtaaca 240
gtcccatgaa acaaagatgc agtcgggcac tcactggaga gttctgggcc tctgcctctt 300
atcagttggc gtttgggggc aagatggtaa tgaagaaatg ggtggtatta cacagacacc 360
atataaagtc tccatctctg gaaccacagt aatattgaca tgccctcagt atcctggatc 420
tgaaatacta tggcaacaca atgataaaaa cataggcggt gatgaggatg ataaaaacat 480
aggcagtgat gaggatcacc tgtcactgaa ggaattttca gaattggagc aaagtggtta 540
ttatgtctgc taccccagag gaagcaaacc agaagatgcg aacttttatc tctacctgag 600
ggcaagagtg tgtgagaact gcatggagat ggatgtgatg tcggtggcca caattgtcat 660
agtggacatc tgcatcactg ggggcttgct gctgctggtt tactactgga gcaagaatag 720
aaaggccaag gccaagcctg tgacacgagg agcgggtgct ggcggcaggc aaaggggaca 780
aaacaaggag aggccaccac ctgttcccaa cccagactat gagcccatcc ggaaaggcca 840
gcgggacctg tattctggcc tgaatcagag acgcatctga ccctctggag aacactgcct 900
cccgctggcc caggtctcct ctccagtccc cctgcgactc cctgtttcct gggctagtct 960
tggaccccac gagagagaat cgttcctcag cctcatggtg aactcgcgcc ctccagcctg 1020
atcccccgct ccctcctccc tgccttctct gctggtaccc agtcctaaaa tattgctgct 1080
tcctcttcct ttgaagcatc atcagtagtc acaccctcac agctggcctg ccctcttgcc 1140
aggatattta tttgtgctat tcactccctt ccctttggat gtaacttctc cgttcagttc 1200
cctccttttc ttgcatgtaa gttgtccccc atcccaaagt attccatcta cttttctatc 1260
gccgtcccct tttgcagccc tctctgggga tggactgggt aaatgttgac agaggccctg 1320
ccccgttcac agatcctggc cctgagccag ccctgtgctc ctccctcccc caacactccc 1380
taccaacccc ctaatcccct actccctcca ccccccctcc actgtaggcc actggatggt 1440
catttgcatc tccgtaaatg tgctctgctc ctcagctgag agagaaaaaa ataaactgta 1500
tttggctgca agaaaaaaaa aaaaaaaaaa aaaa 1534
<210> 12
<211> 182
<212> PRT
<213> Homo sapiens
<400> 12
Met Glu Gln Gly Lys Gly Leu Ala Val Leu Ile Leu Ala Ile Ile Leu
1 5 10 15
Leu Gln Gly Thr Leu Ala Gln Ser Ile Lys Gly Asn His Leu Val Lys
20 25 30
Val Tyr Asp Tyr Gln Glu Asp Gly Ser Val Leu Leu Thr Cys Asp Ala
35 40 45
Glu Ala Lys Asn Ile Thr Trp Phe Lys Asp Gly Lys Met Ile Gly Phe
50 55 60
Leu Thr Glu Asp Lys Lys Lys Trp Asn Leu Gly Ser Asn Ala Lys Asp
65 70 75 80
Pro Arg Gly Met Tyr Gln Cys Lys Gly Ser Gln Asn Lys Ser Lys Pro
85 90 95
Leu Gln Val Tyr Tyr Arg Met Cys Gln Asn Cys Ile Glu Leu Asn Ala
100 105 110
Ala Thr Ile Ser Gly Phe Leu Phe Ala Glu Ile Val Ser Ile Phe Val
115 120 125
Leu Ala Val Gly Val Tyr Phe Ile Ala Gly Gln Asp Gly Val Arg Gln
130 135 140
Ser Arg Ala Ser Asp Lys Gln Thr Leu Leu Pro Asn Asp Gln Leu Tyr
145 150 155 160
Gln Pro Leu Lys Asp Arg Glu Asp Asp Gln Tyr Ser His Leu Gln Gly
165 170 175
Asn Gln Leu Arg Arg Asn
180
<210> 13
<211> 171
<212> PRT
<213> Homo sapiens
<400> 13
Met Glu His Ser Thr Phe Leu Ser Gly Leu Val Leu Ala Thr Leu Leu
1 5 10 15
Ser Gln Val Ser Pro Phe Lys Ile Pro Ile Glu Glu Leu Glu Asp Arg
20 25 30
Val Phe Val Asn Cys Asn Thr Ser Ile Thr Trp Val Glu Gly Thr Val
35 40 45
Gly Thr Leu Leu Ser Asp Ile Thr Arg Leu Asp Leu Gly Lys Arg Ile
50 55 60
Leu Asp Pro Arg Gly Ile Tyr Arg Cys Asn Gly Thr Asp Ile Tyr Lys
65 70 75 80
Asp Lys Glu Ser Thr Val Gln Val His Tyr Arg Met Cys Gln Ser Cys
85 90 95
Val Glu Leu Asp Pro Ala Thr Val Ala Gly Ile Ile Val Thr Asp Val
100 105 110
Ile Ala Thr Leu Leu Leu Ala Leu Gly Val Phe Cys Phe Ala Gly His
115 120 125
Glu Thr Gly Arg Leu Ser Gly Ala Ala Asp Thr Gln Ala Leu Leu Arg
130 135 140
Asn Asp Gln Val Tyr Gln Pro Leu Arg Asp Arg Asp Asp Ala Gln Tyr
145 150 155 160
Ser His Leu Gly Gly Asn Trp Ala Arg Asn Lys
165 170
<210> 14
<211> 207
<212> PRT
<213> Homo sapiens
<400> 14
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr
20 25 30
Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr
35 40 45
Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys
50 55 60
Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp
65 70 75 80
His Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr
85 90 95
Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu
100 105 110
Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met
115 120 125
Ser Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu
130 135 140
Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys
145 150 155 160
Pro Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn
165 170 175
Lys Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg
180 185 190
Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile
195 200 205
<210> 15
<211> 4
<212> PRT
<213> Artificial
<220>
<223> An artificially generated sequence
<400> 15
Gly Gly Gly Ser
1
<210> 16
<211> 4
<212> PRT
<213> Artificial
<220>
<223> An artificially generated sequence
<400> 16
Ser Gly Gly Gly
1
<210> 17
<211> 5
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 17
Gly Gly Gly Gly Ser
1 5
<210> 18
<211> 5
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 18
Ser Gly Gly Gly Gly
1 5
<210> 19
<211> 6
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 19
Gly Gly Gly Gly Gly Ser
1 5
<210> 20
<211> 6
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 20
Ser Gly Gly Gly Gly Gly
1 5
<210> 21
<211> 7
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 21
Gly Gly Gly Gly Gly Gly Ser
1 5
<210> 22
<211> 7
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 22
Ser Gly Gly Gly Gly Gly Gly
1 5
<210> 23
<211> 330
<212> PRT
<213> Homo sapiens
<400> 23
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 24
<211> 326
<212> PRT
<213> Homo sapiens
<400> 24
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 25
<211> 377
<212> PRT
<213> Homo sapiens
<400> 25
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro
100 105 110
Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg
115 120 125
Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys
130 135 140
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
145 150 155 160
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
165 170 175
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
180 185 190
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp Tyr
195 200 205
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
210 215 220
Gln Tyr Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu His
225 230 235 240
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
245 250 255
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
260 265 270
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
275 280 285
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
290 295 300
Ser Asp Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu Asn Asn
305 310 315 320
Tyr Asn Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
325 330 335
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Ile
340 345 350
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln
355 360 365
Lys Ser Leu Ser Leu Ser Pro Gly Lys
370 375
<210> 26
<211> 327
<212> PRT
<213> Homo sapiens
<400> 26
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 27
<211> 2268
<212> ДНК
<213> Homo sapiens
<400> 27
aatatcttgc atgttacaga tttcactgct cccaccagct tggagacaac atgtggttct 60
tgacaactct gctcctttgg gttccagttg atgggcaagt ggacaccaca aaggcagtga 120
tcactttgca gcctccatgg gtcagcgtgt tccaagagga aaccgtaacc ttgcactgtg 180
aggtgctcca tctgcctggg agcagctcta cacagtggtt tctcaatggc acagccactc 240
agacctcgac ccccagctac agaatcacct ctgccagtgt caatgacagt ggtgaataca 300
ggtgccagag aggtctctca gggcgaagtg accccataca gctggaaatc cacagaggct 360
ggctactact gcaggtctcc agcagagtct tcacggaagg agaacctctg gccttgaggt 420
gtcatgcgtg gaaggataag ctggtgtaca atgtgcttta ctatcgaaat ggcaaagcct 480
ttaagttttt ccactggaat tctaacctca ccattctgaa aaccaacata agtcacaatg 540
gcacctacca ttgctcaggc atgggaaagc atcgctacac atcagcagga atatctgtca 600
ctgtgaaaga gctatttcca gctccagtgc tgaatgcatc tgtgacatcc ccactcctgg 660
aggggaatct ggtcaccctg agctgtgaaa caaagttgct cttgcagagg cctggtttgc 720
agctttactt ctccttctac atgggcagca agaccctgcg aggcaggaac acatcctctg 780
aataccaaat actaactgct agaagagaag actctgggtt atactggtgc gaggctgcca 840
cagaggatgg aaatgtcctt aagcgcagcc ctgagttgga gcttcaagtg cttggcctcc 900
agttaccaac tcctgtctgg tttcatgtcc ttttctatct ggcagtggga ataatgtttt 960
tagtgaacac tgttctctgg gtgacaatac gtaaagaact gaaaagaaag aaaaagtggg 1020
atttagaaat ctctttggat tctggtcatg agaagaaggt aatttccagc cttcaagaag 1080
acagacattt agaagaagag ctgaaatgtc aggaacaaaa agaagaacag ctgcaggaag 1140
gggtgcaccg gaaggagccc cagggggcca cgtagcagcg gctcagtggg tggccatcga 1200
tctggaccgt cccctgccca cttgctcccc gtgagcactg cgtacaaaca tccaaaagtt 1260
caacaacacc agaactgtgt gtctcatggt atgtaactct taaagcaaat aaatgaactg 1320
acttcaactg ggatacattt ggaaatgtgg tcatcaaaga tgacttgaaa tgaggcctac 1380
tctaaagaat tcttgaaaaa cttacaagtc aagcctagcc tgataatcct attacatagt 1440
ttgaaaaata gtattttatt tctcagaaca aggtaaaaag gtgagtgggt gcatatgtac 1500
agaagattaa gacagagaaa cagacagaaa gagacacaca cacagccagg agtgggtaga 1560
tttcagggag acaagaggga atagtataga caataaggaa ggaaatagta cttacaaatg 1620
actcctaagg gactgtgaga ctgagagggc tcacgcctct gtgttcagga tacttagttc 1680
atggcttttc tctttgactt tactaaaaga gaatgtctcc atacgcgttc taggcataca 1740
agggggtaac tcatgatgag aaatggatgt gttattcttg ccctctcttt tgaggctctc 1800
tcataacccc tctatttcta gagacaacaa aaatgctgcc agtcctaggc ccctgccctg 1860
taggaaggca gaatgtaact gttctgtttg tttaacgatt aagtccaaat ctccaagtgc 1920
ggcactgcaa agagacgctt caagtgggga gaagcggcga taccatagag tccagatctt 1980
gcctccagag atttgcttta ccttcctgat tttctggtta ctaattagct tcaggatacg 2040
ctgctctcat acttgggctg tagtttggag acaaaatatt ttcctgccac tgtgtaacat 2100
agctgaggta aaaactgaac tatgtaaatg actctactaa aagtttaggg aaaaaaaaca 2160
ggaggagtat gacacaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa 2220
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaa 2268
<210> 28
<211> 374
<212> PRT
<213> Homo sapiens
<400> 28
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu Gly Leu Gln Leu Pro Thr Pro
275 280 285
Val Trp Phe His Val Leu Phe Tyr Leu Ala Val Gly Ile Met Phe Leu
290 295 300
Val Asn Thr Val Leu Trp Val Thr Ile Arg Lys Glu Leu Lys Arg Lys
305 310 315 320
Lys Lys Trp Asp Leu Glu Ile Ser Leu Asp Ser Gly His Glu Lys Lys
325 330 335
Val Ile Ser Ser Leu Gln Glu Asp Arg His Leu Glu Glu Glu Leu Lys
340 345 350
Cys Gln Glu Gln Lys Glu Glu Gln Leu Gln Glu Gly Val His Arg Lys
355 360 365
Glu Pro Gln Gly Ala Thr
370
<210> 29
<211> 1396
<212> ДНК
<213> Homo sapiens
<400> 29
gggatgacta tggagaccca aatgtctcag aatgtatgtc ccagaaacct gtggctgctt 60
caaccattga cagttttgct gctgctggct tctgcagaca gtcaagctgc tcccccaaag 120
gctgtgctga aacttgagcc cccgtggatc aacgtgctcc aggaggactc tgtgactctg 180
acatgccagg gggctcgcag ccctgagagc gactccattc agtggttcca caatgggaat 240
ctcattccca cccacacgca gcccagctac aggttcaagg ccaacaacaa tgacagcggg 300
gagtacacgt gccagactgg ccagaccagc ctcagcgacc ctgtgcatct gactgtgctt 360
tccgaatggc tggtgctcca gacccctcac ctggagttcc aggagggaga aaccatcatg 420
ctgaggtgcc acagctggaa ggacaagcct ctggtcaagg tcacattctt ccagaatgga 480
aaatcccaga aattctccca tttggatccc accttctcca tcccacaagc aaaccacagt 540
cacagtggtg attaccactg cacaggaaac ataggctaca cgctgttctc atccaagcct 600
gtgaccatca ctgtccaagt gcccagcatg ggcagctctt caccaatggg ggtcattgtg 660
gctgtggtca ttgcgactgc tgtagcagcc attgttgctg ctgtagtggc cttgatctac 720
tgcaggaaaa agcggatttc agccaattcc actgatcctg tgaaggctgc ccaatttgag 780
ccacctggac gtcaaatgat tgccatcaga aagagacaac ttgaagaaac caacaatgac 840
tatgaaacag ctgacggcgg ctacatgact ctgaacccca gggcacctac tgacgatgat 900
aaaaacatct acctgactct tcctcccaac gaccatgtca acagtaataa ctaaagagta 960
acgttatgcc atgtggtcat actctcagct tgctgagtgg atgacaaaaa gaggggaatt 1020
gttaaaggaa aatttaaatg gagactggaa aaatcctgag caaacaaaac cacctggccc 1080
ttagaaatag ctttaacttt gcttaaacta caaacacaag caaaacttca cggggtcata 1140
ctacatacaa gcataagcaa aacttaactt ggatcatttc tggtaaatgc ttatgttaga 1200
aataagacaa ccccagccaa tcacaagcag cctactaaca tataattagg tgactaggga 1260
ctttctaaga agatacctac ccccaaaaaa caattatgta attgaaaacc aaccgattgc 1320
ctttattttg cttccacatt ttcccaataa atacttgcct gtgactaaaa aaaaaaaaaa 1380
aaaaaaaaaa aaaaaa 1396
<210> 30
<211> 316
<212> PRT
<213> Homo sapiens
<400> 30
Met Thr Met Glu Thr Gln Met Ser Gln Asn Val Cys Pro Arg Asn Leu
1 5 10 15
Trp Leu Leu Gln Pro Leu Thr Val Leu Leu Leu Leu Ala Ser Ala Asp
20 25 30
Ser Gln Ala Ala Pro Pro Lys Ala Val Leu Lys Leu Glu Pro Pro Trp
35 40 45
Ile Asn Val Leu Gln Glu Asp Ser Val Thr Leu Thr Cys Gln Gly Ala
50 55 60
Arg Ser Pro Glu Ser Asp Ser Ile Gln Trp Phe His Asn Gly Asn Leu
65 70 75 80
Ile Pro Thr His Thr Gln Pro Ser Tyr Arg Phe Lys Ala Asn Asn Asn
85 90 95
Asp Ser Gly Glu Tyr Thr Cys Gln Thr Gly Gln Thr Ser Leu Ser Asp
100 105 110
Pro Val His Leu Thr Val Leu Ser Glu Trp Leu Val Leu Gln Thr Pro
115 120 125
His Leu Glu Phe Gln Glu Gly Glu Thr Ile Met Leu Arg Cys His Ser
130 135 140
Trp Lys Asp Lys Pro Leu Val Lys Val Thr Phe Phe Gln Asn Gly Lys
145 150 155 160
Ser Gln Lys Phe Ser His Leu Asp Pro Thr Phe Ser Ile Pro Gln Ala
165 170 175
Asn His Ser His Ser Gly Asp Tyr His Cys Thr Gly Asn Ile Gly Tyr
180 185 190
Thr Leu Phe Ser Ser Lys Pro Val Thr Ile Thr Val Gln Val Pro Ser
195 200 205
Met Gly Ser Ser Ser Pro Met Gly Val Ile Val Ala Val Val Ile Ala
210 215 220
Thr Ala Val Ala Ala Ile Val Ala Ala Val Val Ala Leu Ile Tyr Cys
225 230 235 240
Arg Lys Lys Arg Ile Ser Ala Asn Ser Thr Asp Pro Val Lys Ala Ala
245 250 255
Gln Phe Glu Pro Pro Gly Arg Gln Met Ile Ala Ile Arg Lys Arg Gln
260 265 270
Leu Glu Glu Thr Asn Asn Asp Tyr Glu Thr Ala Asp Gly Gly Tyr Met
275 280 285
Thr Leu Asn Pro Arg Ala Pro Thr Asp Asp Asp Lys Asn Ile Tyr Leu
290 295 300
Thr Leu Pro Pro Asn Asp His Val Asn Ser Asn Asn
305 310 315
<210> 31
<211> 1497
<212> ДНК
<213> Homo sapiens
<400> 31
tgtgactgct gtgctctggg cgccagctcg ctccagggag tgatgggaat cctgtcattc 60
ttacctgtcc ttgccactga gagtgactgg gctgactgca agtcccccca gccttggggt 120
catatgcttc tgtggacagc tgtgctattc ctggctcctg ttgctgggac acctgcagct 180
cccccaaagg ctgtgctgaa actcgagccc cagtggatca acgtgctcca ggaggactct 240
gtgactctga catgccgggg gactcacagc cctgagagcg actccattca gtggttccac 300
aatgggaatc tcattcccac ccacacgcag cccagctaca ggttcaaggc caacaacaat 360
gacagcgggg agtacacgtg ccagactggc cagaccagcc tcagcgaccc tgtgcatctg 420
actgtgcttt ctgagtggct ggtgctccag acccctcacc tggagttcca ggagggagaa 480
accatcgtgc tgaggtgcca cagctggaag gacaagcctc tggtcaaggt cacattcttc 540
cagaatggaa aatccaagaa attttcccgt tcggatccca acttctccat cccacaagca 600
aaccacagtc acagtggtga ttaccactgc acaggaaaca taggctacac gctgtactca 660
tccaagcctg tgaccatcac tgtccaagct cccagctctt caccgatggg gatcattgtg 720
gctgtggtca ctgggattgc tgtagcggcc attgttgctg ctgtagtggc cttgatctac 780
tgcaggaaaa agcggatttc agccaatccc actaatcctg atgaggctga caaagttggg 840
gctgagaaca caatcaccta ttcacttctc atgcacccgg atgctctgga agagcctgat 900
gaccagaacc gtatttagtc tccattgtct tgcattggga tttgagaaga aaatcagaga 960
gggaagatct ggtatttcct ggcctaaatt ccccttgggg aggacaggga gatgctgcag 1020
ttccaaaaga gaaggtttct tccagagtca tctacctgag tcctgaagct ccctgtcctg 1080
aaagccacag acaatatggt cccaaataac cgactgcacc ttctgtgctt cagctcttct 1140
tgacatcaag gctcttccgt tccacatcca cacagccaat ccaattaatc aaaccactgt 1200
tattaacaga taatagcaac ttgggaaatg cttatgttac aggttacgtg agaacaatca 1260
tgtaaatcta tatgatttca gaaatgttaa aatagactaa cctctaccag cacattaaaa 1320
gtgattgttt ctgggtgata aaattattga tgatttttat tttctttatt tttctataaa 1380
gatcatatat tacttttata ataaaacatt ataaaaacaa aaaaaaaaaa aaaaaaaaaa 1440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaa 1497
<210> 32
<211> 291
<212> PRT
<213> Homo sapiens
<400> 32
Met Gly Ile Leu Ser Phe Leu Pro Val Leu Ala Thr Glu Ser Asp Trp
1 5 10 15
Ala Asp Cys Lys Ser Pro Gln Pro Trp Gly His Met Leu Leu Trp Thr
20 25 30
Ala Val Leu Phe Leu Ala Pro Val Ala Gly Thr Pro Ala Ala Pro Pro
35 40 45
Lys Ala Val Leu Lys Leu Glu Pro Gln Trp Ile Asn Val Leu Gln Glu
50 55 60
Asp Ser Val Thr Leu Thr Cys Arg Gly Thr His Ser Pro Glu Ser Asp
65 70 75 80
Ser Ile Gln Trp Phe His Asn Gly Asn Leu Ile Pro Thr His Thr Gln
85 90 95
Pro Ser Tyr Arg Phe Lys Ala Asn Asn Asn Asp Ser Gly Glu Tyr Thr
100 105 110
Cys Gln Thr Gly Gln Thr Ser Leu Ser Asp Pro Val His Leu Thr Val
115 120 125
Leu Ser Glu Trp Leu Val Leu Gln Thr Pro His Leu Glu Phe Gln Glu
130 135 140
Gly Glu Thr Ile Val Leu Arg Cys His Ser Trp Lys Asp Lys Pro Leu
145 150 155 160
Val Lys Val Thr Phe Phe Gln Asn Gly Lys Ser Lys Lys Phe Ser Arg
165 170 175
Ser Asp Pro Asn Phe Ser Ile Pro Gln Ala Asn His Ser His Ser Gly
180 185 190
Asp Tyr His Cys Thr Gly Asn Ile Gly Tyr Thr Leu Tyr Ser Ser Lys
195 200 205
Pro Val Thr Ile Thr Val Gln Ala Pro Ser Ser Ser Pro Met Gly Ile
210 215 220
Ile Val Ala Val Val Thr Gly Ile Ala Val Ala Ala Ile Val Ala Ala
225 230 235 240
Val Val Ala Leu Ile Tyr Cys Arg Lys Lys Arg Ile Ser Ala Asn Pro
245 250 255
Thr Asn Pro Asp Glu Ala Asp Lys Val Gly Ala Glu Asn Thr Ile Thr
260 265 270
Tyr Ser Leu Leu Met His Pro Asp Ala Leu Glu Glu Pro Asp Asp Gln
275 280 285
Asn Arg Ile
290
<210> 33
<211> 2137
<212> ДНК
<213> Homo sapiens
<400> 33
cttgtccact ccagtgtggc atcatgtggc agctgctcct cccaactgct ctgctacttc 60
tagtttcagc tggcatgcgg actgaagatc tcccaaaggc tgtggtgttc ctggagcctc 120
aatggtacag ggtgctcgag aaggacagtg tgactctgaa gtgccaggga gcctactccc 180
ctgaggacaa ttccacacag tggtttcaca atgagagcct catctcaagc caggcctcga 240
gctacttcat tgacgctgcc acagttgacg acagtggaga gtacaggtgc cagacaaacc 300
tctccaccct cagtgacccg gtgcagctag aagtccatat cggctggctg ttgctccagg 360
cccctcggtg ggtgttcaag gaggaagacc ctattcacct gaggtgtcac agctggaaga 420
acactgctct gcataaggtc acatatttac agaatggcaa aggcaggaag tattttcatc 480
ataattctga cttctacatt ccaaaagcca cactcaaaga cagcggctcc tacttctgca 540
gggggcttgt tgggagtaaa aatgtgtctt cagagactgt gaacatcacc atcactcaag 600
gtttgtcagt gtcaaccatc tcatcattct ttccacctgg gtaccaagtc tctttctgct 660
tggtgatggt actccttttt gcagtggaca caggactata tttctctgtg aagacaaaca 720
ttcgaagctc aacaagagac tggaaggacc ataaatttaa atggagaaag gaccctcaag 780
acaaatgacc cccatcccat gggggtaata agagcagtag cagcagcatc tctgaacatt 840
tctctggatt tgcaacccca tcatcctcag gcctctctac aagcagcagg aaacatagaa 900
ctcagagcca gatcccttat ccaactctcg acttttcctt ggtctccagt ggaagggaaa 960
agcccatgat cttcaagcag ggaagcccca gtgagtagct gcattcctag aaattgaagt 1020
ttcagagcta cacaaacact ttttctgtcc caaccgttcc ctcacagcaa agcaacaata 1080
caggctaggg atggtaatcc tttaaacata caaaaattgc tcgtgttata aattacccag 1140
tttagagggg aaaaaaaaac aattattcct aaataaatgg ataagtagaa ttaatggttg 1200
aggcaggacc atacagagtg tgggaactgc tggggatcta gggaattcag tgggaccaat 1260
gaaagcatgg ctgagaaata gcaggtagtc caggatagtc taagggaggt gttcccatct 1320
gagcccagag ataagggtgt cttcctagaa cattagccgt agtggaatta acaggaaatc 1380
atgagggtga cgtagaattg agtcttccag gggactctat cagaactgga ccatctccaa 1440
gtatataacg atgagtcctc ttaatgctag gagtagaaaa tggtcctagg aaggggactg 1500
aggattgcgg tggggggtgg ggtggaaaag aaagtacaga acaaaccctg tgtcactgtc 1560
ccaagttgct aagtgaacag aactatctca gcatcagaat gagaaagcct gagaagaaag 1620
aaccaaccac aagcacacag gaaggaaagc gcaggaggtg aaaatgcttt cttggccagg 1680
gtagtaagaa ttagaggtta atgcagggac tgtaaaacca ccttttctgc ttcaatatct 1740
aattcctgtg tagctttgtt cattgcattt attaaacaaa tgttgtataa ccaatactaa 1800
atgtactact gagcttcgct gagttaagtt atgaaacttt caaatccttc atcatgtcag 1860
ttccaatgag gtggggatgg agaagacaat tgttgcttat gaaagaaagc tttagctgtc 1920
tctgttttgt aagctttaag cgcaacattt cttggttcca ataaagcatt ttacaagatc 1980
ttgcatgcta ctcttagata gaagatggga aaaccatggt aataaaatat gaatgataaa 2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa 2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaa 2137
<210> 34
<211> 254
<212> PRT
<213> Homo sapiens
<400> 34
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
145 150 155 160
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
165 170 175
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
Gly Leu Ser Val Ser Thr Ile Ser Ser Phe Phe Pro Pro Gly Tyr Gln
195 200 205
Val Ser Phe Cys Leu Val Met Val Leu Leu Phe Ala Val Asp Thr Gly
210 215 220
Leu Tyr Phe Ser Val Lys Thr Asn Ile Arg Ser Ser Thr Arg Asp Trp
225 230 235 240
Lys Asp His Lys Phe Lys Trp Arg Lys Asp Pro Gln Asp Lys
245 250
<210> 35
<211> 820
<212> ДНК
<213> Homo sapiens
<400> 35
cactccagtg tggcatcatg tggcagctgc tcctcccaac tgctctgcta cttctagttt 60
cagctggcat gcggactgaa gatctcccaa aggctgtggt gttcctggag cctcaatggt 120
acagcgtgct tgagaaggac agtgtgactc tgaagtgcca gggagcctac tcccctgagg 180
acaattccac acagtggttt cacaatgaga gcctcatctc aagccaggcc tcgagctact 240
tcattgacgc tgccacagtc aacgacagtg gagagtacag gtgccagaca aacctctcca 300
ccctcagtga cccggtgcag ctagaagtcc atatcggctg gctgttgctc caggcccctc 360
ggtgggtgtt caaggaggaa gaccctattc acctgaggtg tcacagctgg aagaacactg 420
ctctgcataa ggtcacatat ttacagaatg gcaaagacag gaagtatttt catcataatt 480
ctgacttcca cattccaaaa gccacactca aagatagcgg ctcctacttc tgcagggggc 540
ttgttgggag taaaaatgtg tcttcagaga ctgtgaacat caccatcact caaggtttgg 600
cagtgtcaac catctcatca ttctctccac ctgggtacca agtctctttc tgcttggtga 660
tggtactcct ttttgcagtg gacacaggac tatatttctc tgtgaagaca aacatttgaa 720
gctcaacaag agactggaag gaccataaac ttaaatggag aaaggaccct caagacaaat 780
gacccccatc ccatgggagt aataagagca gtggcagcag 820
<210> 36
<211> 233
<212> PRT
<213> Homo sapiens
<400> 36
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
Gln Trp Tyr Ser Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
Val Asn Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
Gly Lys Asp Arg Lys Tyr Phe His His Asn Ser Asp Phe His Ile Pro
145 150 155 160
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
165 170 175
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
Gly Leu Ala Val Ser Thr Ile Ser Ser Phe Ser Pro Pro Gly Tyr Gln
195 200 205
Val Ser Phe Cys Leu Val Met Val Leu Leu Phe Ala Val Asp Thr Gly
210 215 220
Leu Tyr Phe Ser Val Lys Thr Asn Ile
225 230
<210> 37
<211> 330
<212> PRT
<213> Homo sapiens
<400> 37
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 38
<211> 326
<212> PRT
<213> Homo sapiens
<400> 38
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 39
<211> 327
<212> PRT
<213> Homo sapiens
<400> 39
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 40
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 40
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 41
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 41
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 42
<211> 122
<212> PRT
<213> Rattus norvegicus
<400> 42
Glu Val Gln Leu Val Glu Thr Gly Gly Ser Leu Val Gln Pro Gly Lys
1 5 10 15
Ser Leu Lys Leu Thr Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ser Pro Glu Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Asn
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Glu Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 43
<211> 112
<212> PRT
<213> Rattus norvegicus
<400> 43
Asp Val Val Met Thr Gln Thr Pro Val Ser Met Ser Val Ser Leu Gly
1 5 10 15
Gly Gln Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Gly Asn Thr Tyr Val Ser Trp Tyr Ile Gln Lys Pro Ser Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Ile Ser
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Asp Asp Leu Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Asp Pro Tyr Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 44
<211> 328
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 44
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro
325
<210> 45
<211> 338
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 45
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
1 5 10 15
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
20 25 30
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
35 40 45
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
50 55 60
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
65 70 75 80
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
85 90 95
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
100 105 110
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
115 120 125
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
130 135 140
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
145 150 155 160
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
165 170 175
Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr
180 185 190
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
195 200 205
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
210 215 220
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg
225 230 235 240
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
245 250 255
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
260 265 270
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
275 280 285
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
290 295 300
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
305 310 315 320
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro His His His His His His
325 330 335
His His
<210> 46
<211> 336
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 46
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
325 330 335
<210> 47
<211> 450
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 47
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
115 120 125
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
130 135 140
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
145 150 155 160
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
165 170 175
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
180 185 190
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
195 200 205
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg
340 345 350
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro His His His His His His
435 440 445
His His
450
<210> 48
<211> 222
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 48
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro
115 120 125
Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu
130 135 140
Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn
145 150 155 160
Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser
165 170 175
Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
180 185 190
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly
195 200 205
Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 49
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 49
Glu Val Gln Leu Val Glu Thr Gly Gly Ser Leu Val Gln Pro Gly Lys
1 5 10 15
Ser Leu Lys Leu Thr Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ser Pro Glu Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Asn
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Glu Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 50
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 50
Asp Val Val Met Thr Gln Thr Pro Val Ser Met Ser Val Ser Leu Gly
1 5 10 15
Gly Gln Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Gly Asn Thr Tyr Val Ser Trp Tyr Ile Gln Lys Pro Ser Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Ile Ser
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Asp Asp Leu Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Asp Pro Tyr Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 51
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 51
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Ala Arg Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 52
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 52
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 53
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 53
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 54
<211> 448
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 54
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
210 215 220
Pro Ala Pro Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Phe Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Lys Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Tyr Thr
420 425 430
Gln Lys Ser Leu Ser Leu Ser Leu His His His His His His His His
435 440 445
<210> 55
<211> 455
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 55
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Glu Ser Leu Ser Leu Ser Leu Asp
435 440 445
Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 56
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 56
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 57
<211> 336
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 57
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Val Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
325 330 335
<210> 58
<211> 338
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 58
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
1 5 10 15
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
20 25 30
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
35 40 45
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
50 55 60
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
65 70 75 80
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
85 90 95
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
100 105 110
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
115 120 125
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
130 135 140
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
145 150 155 160
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
165 170 175
Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr
180 185 190
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
195 200 205
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
210 215 220
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg
225 230 235 240
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
245 250 255
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
260 265 270
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
275 280 285
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
290 295 300
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
305 310 315 320
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro His His His His His His
325 330 335
His His
<210> 59
<211> 230
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 59
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
20 25 30
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
35 40 45
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
50 55 60
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
65 70 75 80
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
85 90 95
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
100 105 110
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
115 120 125
Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
130 135 140
Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser
145 150 155 160
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
165 170 175
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
180 185 190
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
195 200 205
Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Tyr Thr Gln Lys
210 215 220
Ser Leu Ser Leu Ser Pro
225 230
<210> 60
<211> 325
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 60
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Lys Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn Arg Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Pro
325
<210> 61
<211> 325
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 61
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Glu Ser
305 310 315 320
Leu Ser Leu Ser Pro
325
<210> 62
<211> 325
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 62
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Lys Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Pro
325
<210> 63
<211> 107
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 63
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 64
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 64
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 65
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 65
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 66
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 66
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 67
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 67
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 68
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 68
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 69
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 69
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 70
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 70
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 71
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 71
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 72
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 72
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Pro
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 73
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 73
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 74
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 74
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 75
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 75
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 76
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 76
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 77
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 77
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Pro
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 78
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 78
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 79
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 79
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Tyr Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 80
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 80
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 81
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 81
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 82
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 82
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 83
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 83
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Pro
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 84
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 84
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 85
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 85
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Pro
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 86
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 86
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 87
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 87
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 88
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 88
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 89
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 89
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 90
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 90
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 91
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 91
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 92
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 92
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 93
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 93
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 94
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 94
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 95
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 95
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 96
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 96
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ser Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 97
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 97
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 98
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 98
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 99
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 99
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 100
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 100
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Pro Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 101
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 101
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 102
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 102
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 103
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 103
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 104
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 104
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 105
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 105
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 106
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 106
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 107
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 107
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 108
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 108
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 109
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 109
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 110
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 110
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 111
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 111
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 112
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 112
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 113
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 113
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 114
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 114
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 115
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 115
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 116
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 116
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 117
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 117
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 118
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 118
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 119
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 119
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 120
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 120
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 121
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 121
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 122
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 122
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 123
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 123
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 124
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 124
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 125
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 125
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ser Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 126
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 126
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 127
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 127
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 128
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 128
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 129
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 129
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 130
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 130
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 131
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 131
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 132
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 132
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 133
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 133
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 134
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 134
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 135
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 135
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 136
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 136
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 137
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 137
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 138
<211> 124
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 138
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ala Glu Met Val Arg Asp Asp
100 105 110
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 139
<211> 128
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 139
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ala Glu Met Val Arg Asp Ser
100 105 110
Tyr Gly Val Asp Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 140
<211> 128
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 140
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Val Arg Arg Arg Leu Ser Ser
100 105 110
Tyr Gly Val Asp Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 141
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 141
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 142
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 142
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 143
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 143
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 144
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 144
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 145
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 145
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 146
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 146
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 147
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 147
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Ala Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 148
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 148
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Gln Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 149
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 149
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Ser Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 150
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 150
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Phe Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 151
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 151
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Gly Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 152
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 152
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Leu Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 153
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 153
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Pro Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 154
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 154
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Gln Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 155
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 155
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Ser Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 156
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 156
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Val Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 157
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 157
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Phe Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 158
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 158
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Gly Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 159
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 159
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Ile Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 160
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 160
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Leu Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 161
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 161
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Pro Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 162
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 162
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Gln Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 163
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 163
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Thr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 164
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 164
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Val Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 165
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 165
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 166
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 166
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 167
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 167
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Gln Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 168
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 168
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Val Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 169
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 169
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Ser Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 170
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Asp Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 171
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 171
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Glu Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 172
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 173
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 173
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Asp Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 174
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 175
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 175
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Asp Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 176
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 176
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Glu Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 177
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 177
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 178
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 178
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 179
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 179
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Glu Ser Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 180
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 180
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Gln Asp Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 181
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 181
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 182
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 182
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 183
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 183
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 184
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 184
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 185
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 185
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Ser Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 186
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 186
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Glu Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 187
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 187
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 188
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 188
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 189
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 189
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 190
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 190
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Glu Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 191
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 191
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Glu Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 192
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 192
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Glu Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 193
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 193
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Glu Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 194
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 194
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Glu Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 195
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 195
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Glu Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 196
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 196
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Glu Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 197
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 197
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 198
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 198
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Asp Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 199
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 199
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 200
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 200
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 201
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 201
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Glu Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 202
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 202
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Glu Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 203
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 203
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 204
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 204
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 205
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 205
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 206
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Pro Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 207
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 207
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Trp Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 208
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 208
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Tyr Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 209
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 210
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 210
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Pro Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Glu Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 211
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 211
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 212
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 212
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Pro Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 213
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 213
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Trp Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 214
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 214
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Tyr Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 215
<211> 115
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 215
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 216
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 216
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile
65 70 75 80
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 217
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 217
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ala Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 218
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 218
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ile Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 219
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 219
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 220
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 220
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Thr Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 221
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 221
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Val Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 222
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 222
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Pro Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 223
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 223
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 224
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 224
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Phe Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 225
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 225
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 226
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 226
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Met Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 227
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 227
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 228
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 228
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Val Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 229
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 229
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val Arg Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 230
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 230
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Phe
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 231
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 231
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His His
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 232
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 232
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Leu
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 233
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 233
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Met
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 234
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 234
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 235
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 235
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Pro
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 236
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 236
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Gln
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 237
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 237
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Val
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 238
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 238
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Trp
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 239
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 239
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asp Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 240
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 240
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Glu Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 241
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 241
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Phe Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 242
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 242
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Gly Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 243
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 243
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg His Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 244
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 244
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Met Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 245
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 245
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Trp Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 246
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 246
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 247
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 247
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 248
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 248
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Glu Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 249
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 249
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Leu Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 250
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 250
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Met Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 251
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 251
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 252
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 252
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 253
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 253
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Phe Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 254
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 254
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser His Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 255
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 255
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Ile Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 256
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 256
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Met Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 257
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 257
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Thr Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 258
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 258
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Trp Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 259
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 259
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 260
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 260
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Gly Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 261
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 261
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Ile Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 262
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 262
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Lys Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 263
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 263
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Leu Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 264
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 264
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Met Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 265
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 265
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Asn Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 266
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 266
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Pro Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 267
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 267
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Arg Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 268
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 268
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Val Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 269
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 269
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Tyr Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 270
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 270
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Phe Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 271
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 271
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Gly Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 272
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 272
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe His Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 273
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 273
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ile Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 274
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 274
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Leu Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 275
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 275
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Met Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 276
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 276
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Pro Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 277
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 277
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Gln Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 278
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 278
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 279
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 279
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Val Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 280
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 280
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 281
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 281
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ala Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 282
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 282
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Glu Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 283
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 283
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 284
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 284
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ile Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 285
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 285
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 286
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 286
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Asn Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 287
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 287
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 288
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 288
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 289
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 289
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 290
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 290
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Ser
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 291
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 291
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Thr
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 292
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 292
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 293
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 293
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln His Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 294
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 294
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Asn Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 295
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 295
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Pro Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 296
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 296
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Trp Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 297
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 297
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Tyr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 298
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 298
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 299
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 299
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 300
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 300
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Trp Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 301
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 301
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 302
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 302
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 303
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 303
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 304
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 304
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 305
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 305
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 306
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 306
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 307
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 307
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 308
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 308
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Trp Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 309
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 309
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 310
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 310
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 311
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 311
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 312
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 312
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 313
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 313
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 314
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 314
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 315
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 315
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 316
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 316
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 317
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 317
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 318
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 318
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 319
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 319
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 320
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 320
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Leu Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 321
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 321
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Pro Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 322
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 322
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ile Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 323
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 323
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 324
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 324
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 325
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 325
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Ser
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 326
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 326
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Thr
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 327
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 327
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Trp Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 328
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 328
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 329
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 329
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Glu Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 330
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 330
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Glu Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 331
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 331
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Glu Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 332
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 332
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Glu Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 333
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 333
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Glu Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 334
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 334
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 335
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 335
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 336
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 336
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 337
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 337
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 338
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 338
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 339
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 339
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Glu Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 340
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 340
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 341
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 341
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ile Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 342
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 342
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 343
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 343
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 344
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 344
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ile Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 345
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 345
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 346
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 346
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 347
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 347
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 348
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 348
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 349
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 349
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ala Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 350
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 350
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ala Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 351
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 351
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ala Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 352
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 352
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ala Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 353
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 353
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 354
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 354
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 355
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 355
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Val Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 356
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 356
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 357
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 357
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Gln Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 358
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 358
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Gln Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 359
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 359
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Leu Val His Ser
20 25 30
Asn Arg Gln Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 360
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 360
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 361
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 361
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 362
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 362
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 363
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 363
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 364
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 364
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 365
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 365
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 366
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 366
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 367
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 367
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 368
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 368
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 369
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 369
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 370
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 370
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 371
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 371
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 372
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 372
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu
100 105 110
<210> 373
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 373
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 374
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 374
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 375
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 375
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 376
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 376
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 377
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 377
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 378
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 378
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 379
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 379
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 380
<211> 112
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 380
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Gln Ala Ser Glu Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Thr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 381
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 381
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 382
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 382
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Ala Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 383
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 383
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 384
<211> 440
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 384
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
210 215 220
Pro Ala Pro Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Phe Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Glu Ser Leu Ser Leu Ser Pro
435 440
<210> 385
<211> 440
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 385
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Pro Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
210 215 220
Pro Ala Pro Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Phe Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Glu Ser Leu Ser Leu Ser Pro
435 440
<210> 386
<211> 440
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 386
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Thr Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Glu Gly Leu Glu Trp Met
35 40 45
Gly Ala Ile Asp Gly Glu Thr Pro Asp Thr Ala Tyr Ser Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
210 215 220
Pro Ala Pro Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Phe Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Glu Ser Leu Ser Leu Ser Pro
435 440
<210> 387
<211> 440
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 387
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
210 215 220
Pro Ala Pro Glu Phe Arg Gly Gly Pro Lys Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Phe Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Glu Ser Leu Ser Leu Ser Pro
435 440
<210> 388
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 388
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 389
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 389
Glu Val Gln Leu Val Glu Thr Gly Gly Ser Leu Val Gln Pro Gly Lys
1 5 10 15
Ser Leu Lys Leu Thr Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ser Pro Glu Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Asn
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Glu Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 390
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 390
Glu Val Gln Leu Val Glu Thr Gly Gly Ser Leu Val Gln Pro Gly Lys
1 5 10 15
Ser Leu Lys Leu Thr Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ser Pro Glu Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Asn
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Glu Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 391
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 391
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Lys Lys Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 392
<211> 458
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 392
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Gly Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Cys Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 393
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 393
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ser Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 394
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 394
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 395
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 395
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 396
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 396
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 397
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 397
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Ser Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 398
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 398
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 399
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 399
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 400
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 400
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Val Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 401
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 401
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Val Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 402
<211> 447
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 402
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Asp Lys Ser Gln Asn Tyr Ala Thr Tyr Val Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Ala Asp Ser Lys Asn Ser
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Ala Ala Gly Tyr Gly Val Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr
210 215 220
Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Arg Gly Gly Pro
225 230 235 240
Lys Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp
260 265 270
Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Ala Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Gln Lys Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 403
<211> 450
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 403
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
115 120 125
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
130 135 140
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
145 150 155 160
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
165 170 175
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
180 185 190
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
195 200 205
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg
340 345 350
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro His His His His His His
435 440 445
His His
450
<210> 404
<211> 450
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 404
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
115 120 125
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
130 135 140
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
145 150 155 160
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
165 170 175
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
180 185 190
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
195 200 205
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
210 215 220
Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Cys Thr Leu Pro Pro Ser Arg
340 345 350
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro His His His His His His
435 440 445
His His
450
<210> 405
<211> 222
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 405
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro
115 120 125
Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu
130 135 140
Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn
145 150 155 160
Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser
165 170 175
Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
180 185 190
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly
195 200 205
Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 406
<211> 222
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 406
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Gly Lys Thr Pro Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro
115 120 125
Ser Asp Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu
130 135 140
Asn Asn Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn
145 150 155 160
Ala Leu Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser
165 170 175
Lys Asp Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala
180 185 190
Asp Tyr Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly
195 200 205
Leu Ser Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 407
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 407
Asp Val Val Met Thr Gln Thr Pro Val Ser Met Ser Val Ser Leu Gly
1 5 10 15
Gly Gln Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Asn
20 25 30
Asn Gly Asn Thr Tyr Val Ser Trp Tyr Ile Gln Lys Pro Ser Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Ile Ser
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Pro Asp Asp Leu Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Asp Pro Tyr Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 408
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 408
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 409
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 409
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 410
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 410
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 411
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 411
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 412
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 412
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 413
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 413
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Arg Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gly Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 414
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 414
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 415
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 415
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Trp Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 416
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 416
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 417
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 417
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Pro Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 418
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 418
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Pro Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 419
<211> 219
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 419
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Ile Gln Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Tyr Gln Gly
85 90 95
Thr Gln Val Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 420
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 420
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 421
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 421
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Lys Lys Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 422
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 422
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Arg Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 423
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 423
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Arg Val His Tyr Tyr Tyr Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 424
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 424
Glu Val Gln Leu Val Glu Thr Gly Gly Ser Leu Val Gln Pro Gly Lys
1 5 10 15
Ser Leu Lys Leu Thr Cys Ala Thr Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ser Pro Glu Lys Gln Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Asn
65 70 75 80
Ile Tyr Leu Gln Met Asn Ser Leu Lys Glu Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 425
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 425
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 426
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 426
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 427
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 427
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Leu Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Gly Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 428
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 428
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Ala Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 429
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 429
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Ala Tyr Tyr Gly Val Gln Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 430
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 430
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Ala Thr Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 431
<211> 122
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 431
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Gln Ile Lys Ala Lys Ser Asn Asn Tyr Lys Lys Tyr Tyr Ala Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Ser
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Tyr Val His Tyr Tyr Tyr Tyr Tyr Gly Val Asp Ala Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 432
<211> 107
<212> PRT
<213> Искусственная
<220>
<223> Искусственно синтезированная последовательность
<400> 432
Ala Ser Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |
| АНТИТЕЛО К TIGIT И ЕГО ИСПОЛЬЗОВАНИЕ | 2019 |
|
RU2786434C2 |
| МОЛЕКУЛЫ АНТИТЕЛ ПРОТИВ ВИРУСА BK | 2021 |
|
RU2835801C1 |
| АНТИТЕЛА К ТАУ И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2787779C2 |
| ИММУНОАКТИВИРУЮЩАЯ АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА | 2015 |
|
RU2722788C2 |
| МОНОСПЕЦИФИЧЕСКИЕ И БИСПЕЦИФИЧЕСКИЕ БЕЛКИ С РЕГУЛИРОВАНИЕМ ИММУННОЙ КОНТРОЛЬНОЙ ТОЧКИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2793167C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ИЛИ ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ, КОТОРОЕ СПЕЦИФИЧЕСКИ СВЯЗЫВАЕТСЯ С IL-4Rα, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2808563C2 |
| ВАРИАНТЫ FC-ОБЛАСТИ С МОДИФИЦИРОВАННОЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬСЯ С FCRN И С СОХРАНЕННОЙ СПОСОБНОСТЬЮ СВЯЗЫВАТЬСЯ С БЕЛКОМ А | 2015 |
|
RU2727639C2 |
| ВАРИАНТЫ FC-ОБЛАСТИ С МОДИФИЦИРОВАННЫМИ СПОСОБНОСТЯМИ СВЯЗЫВАТЬСЯ С FCRN | 2015 |
|
RU2730592C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ НА ОСНОВЕ АКТИВИРУЮЩИХ Т-КЛЕТКИ БИСПЕЦИФИЧЕСКИХ АНТИГЕНСВЯЗЫВАЮЩИХ МОЛЕКУЛ ПРОТИВ CD3 И ФОЛАТНОГО РЕЦЕПТОРА 1 (FOLR1) И АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХСЯ С ОСЬЮ PD-1 | 2015 |
|
RU2753902C2 |
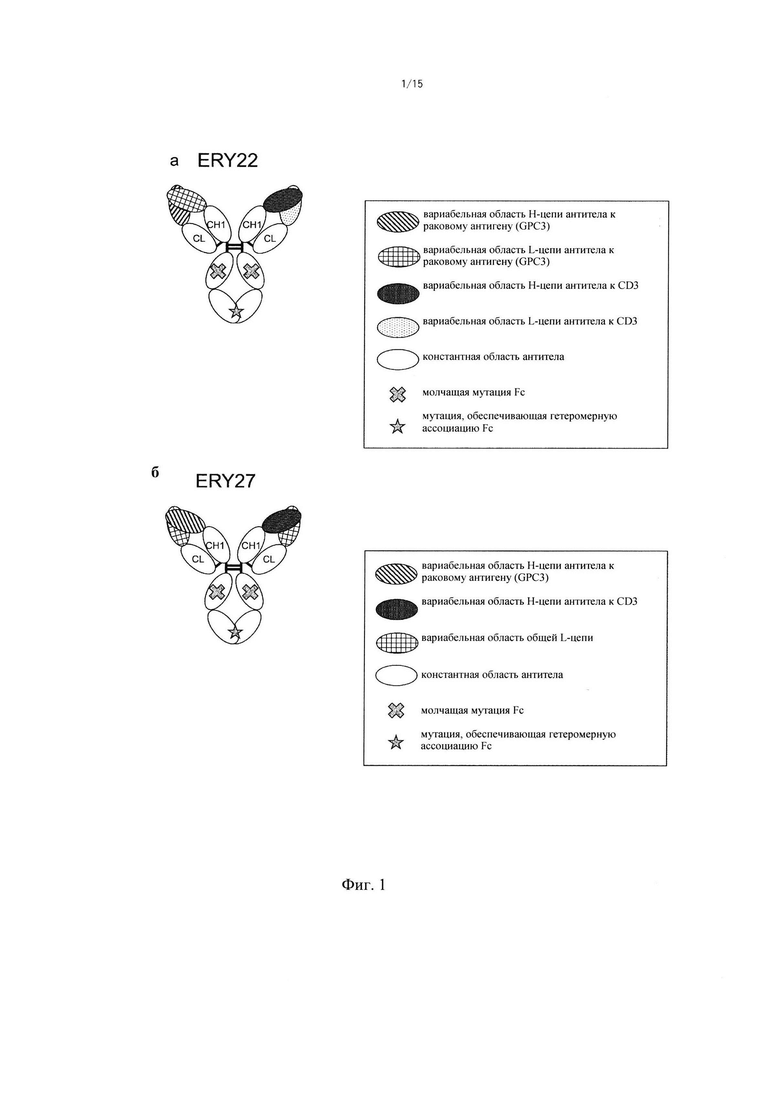
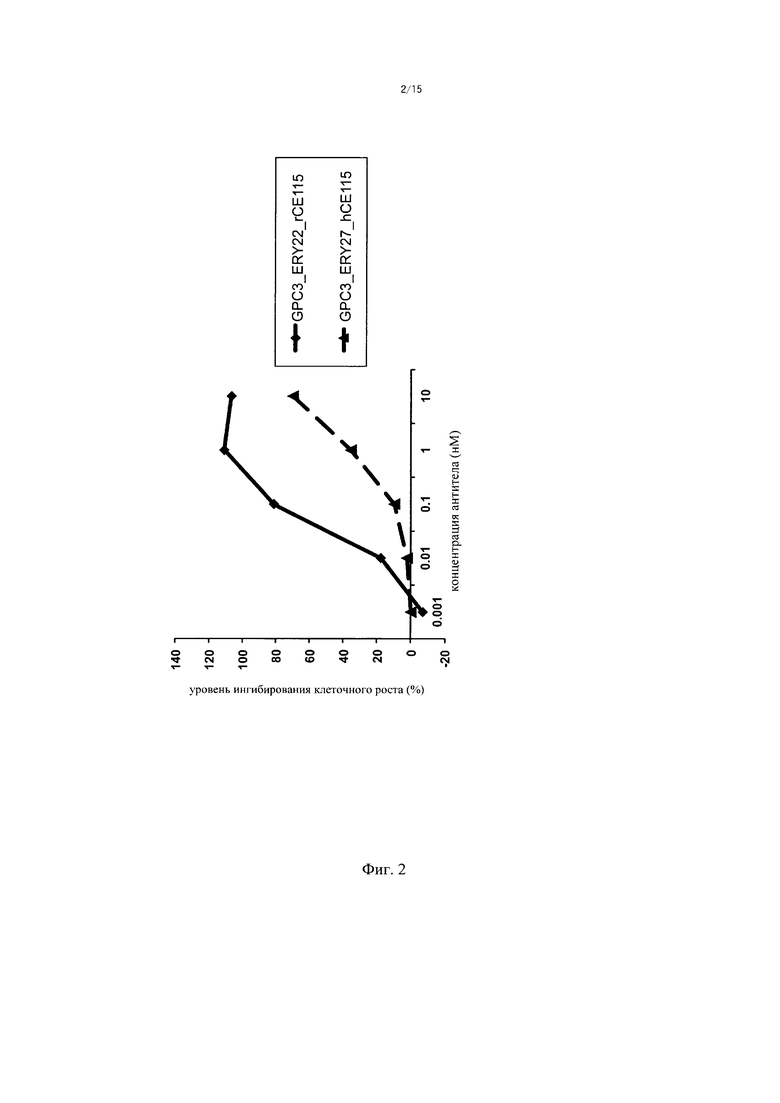
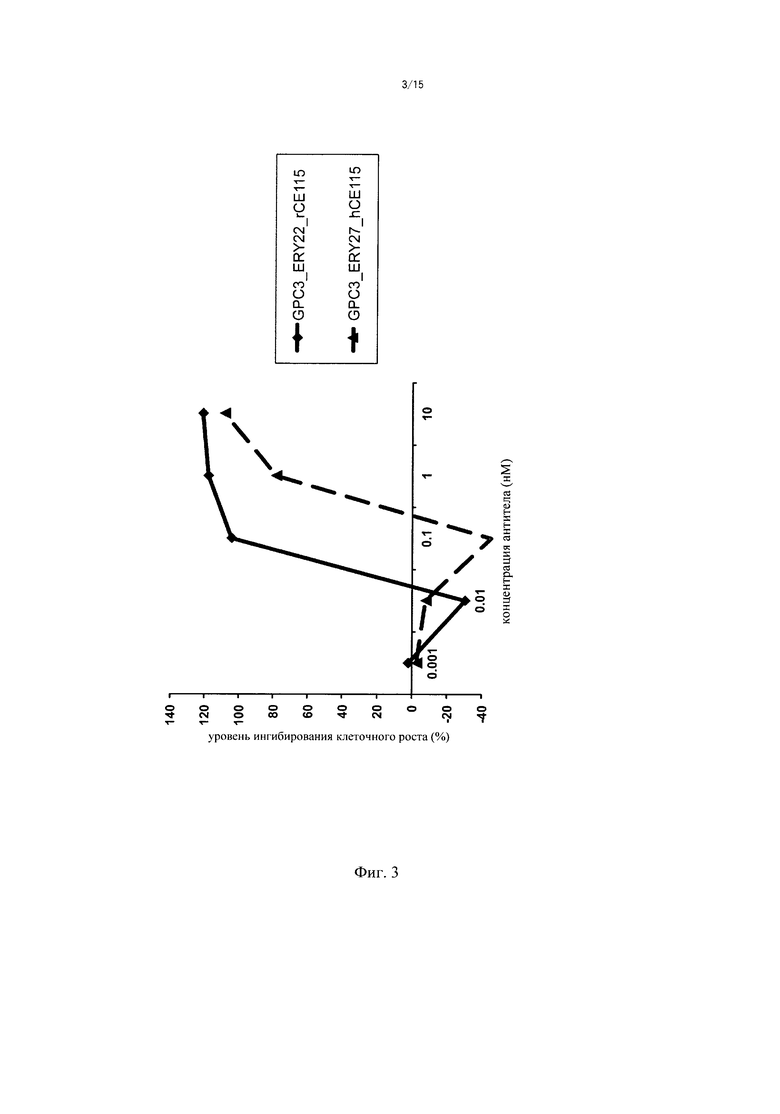
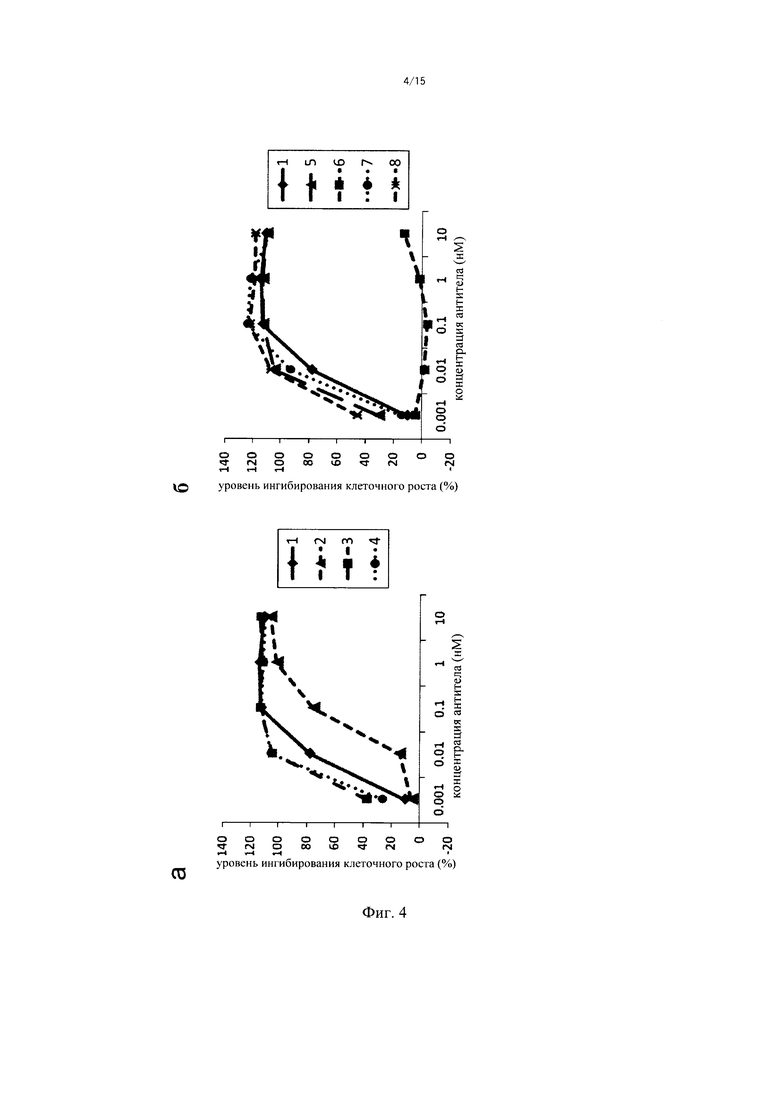
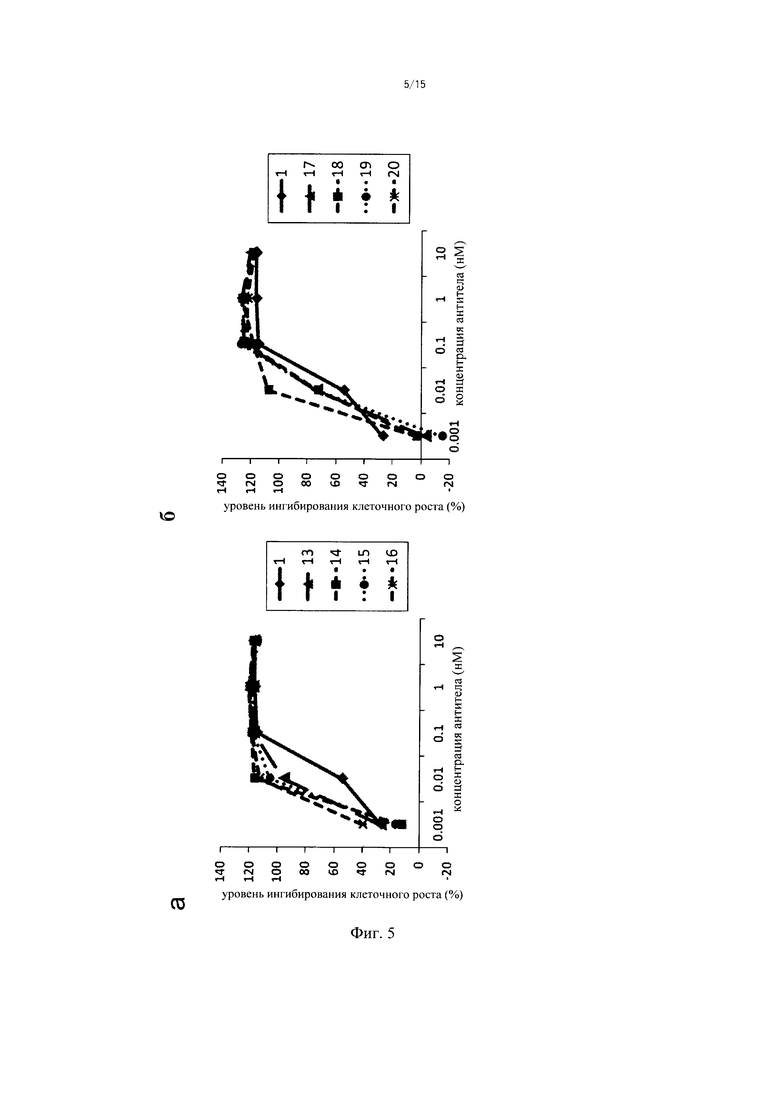
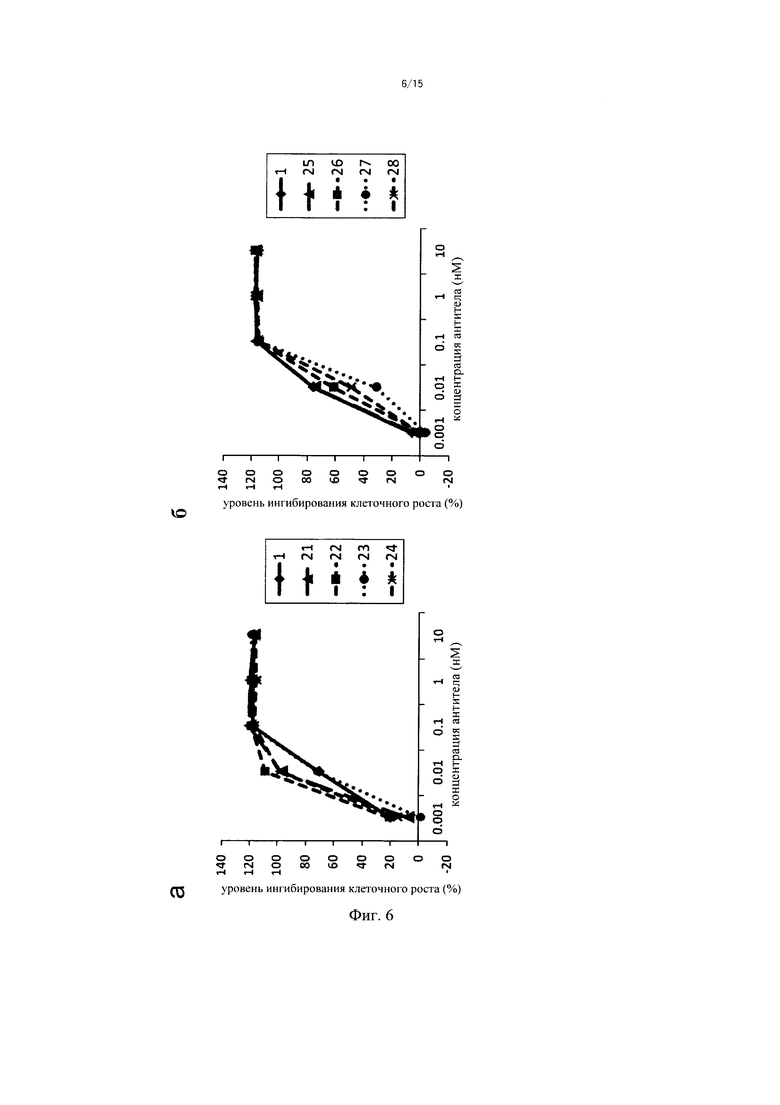
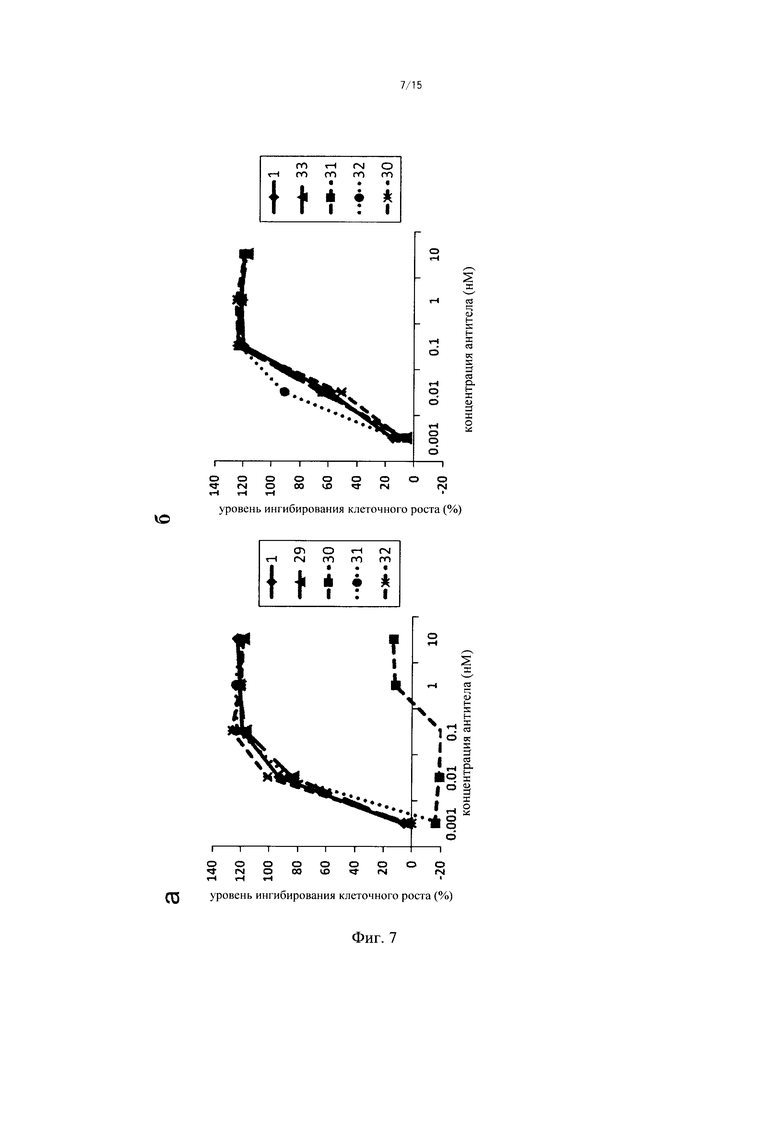
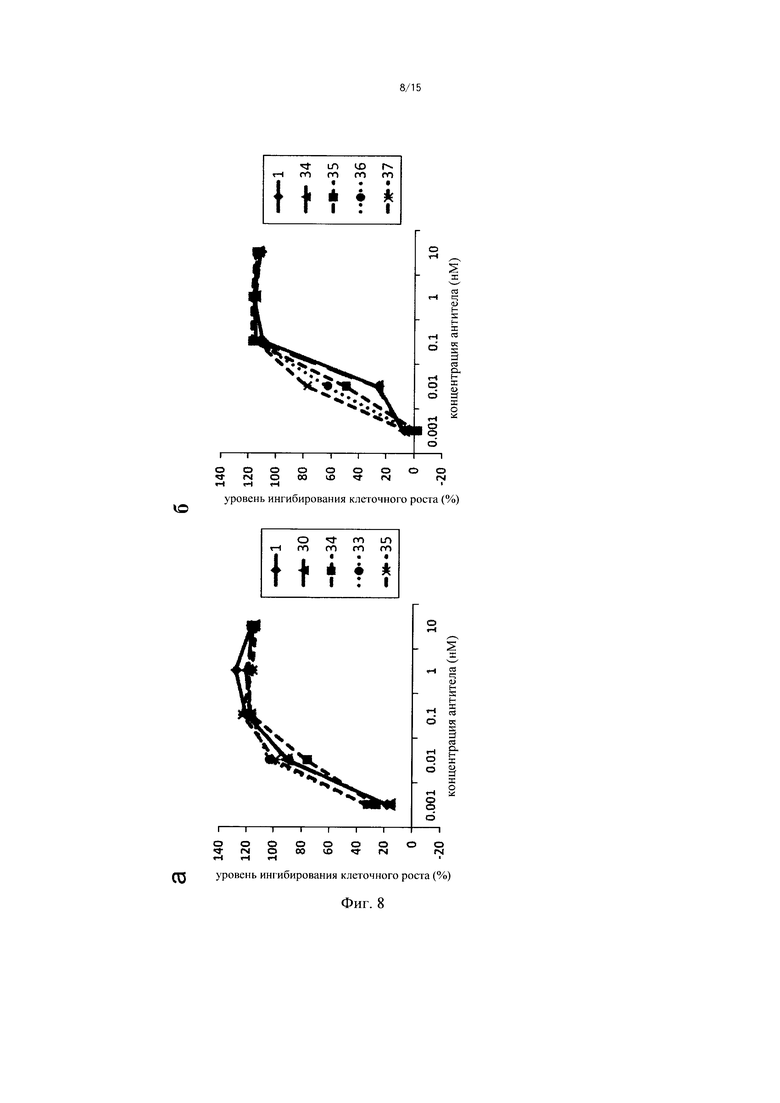
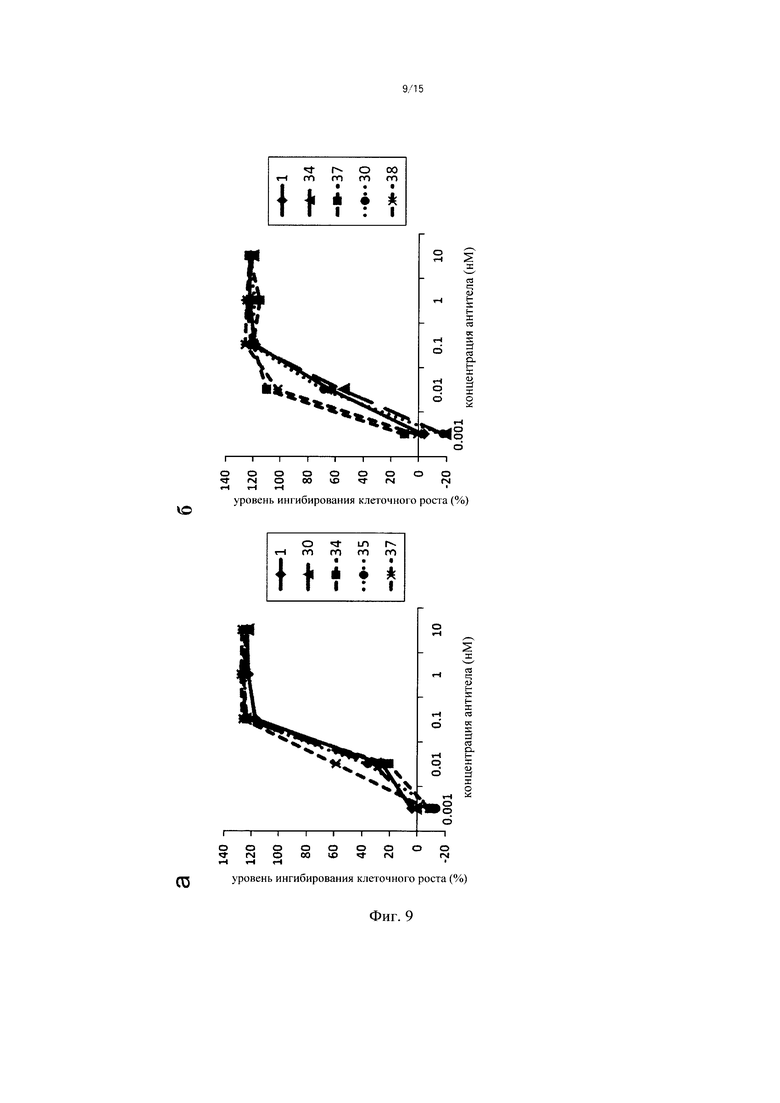
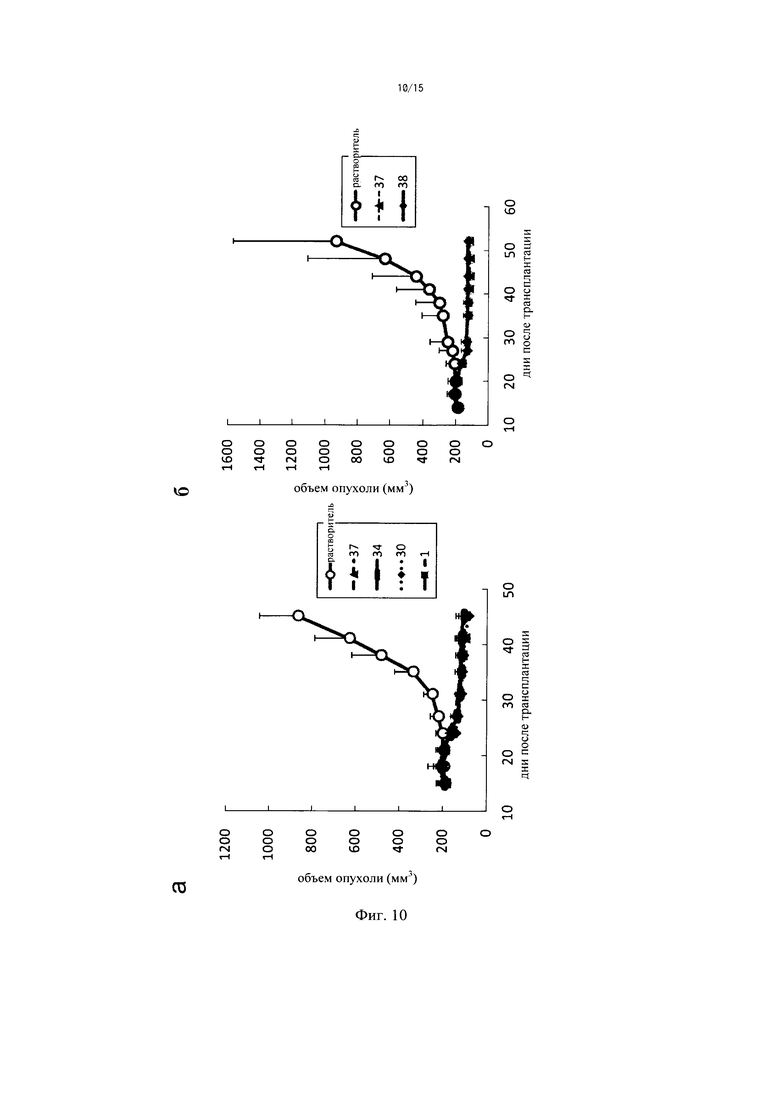
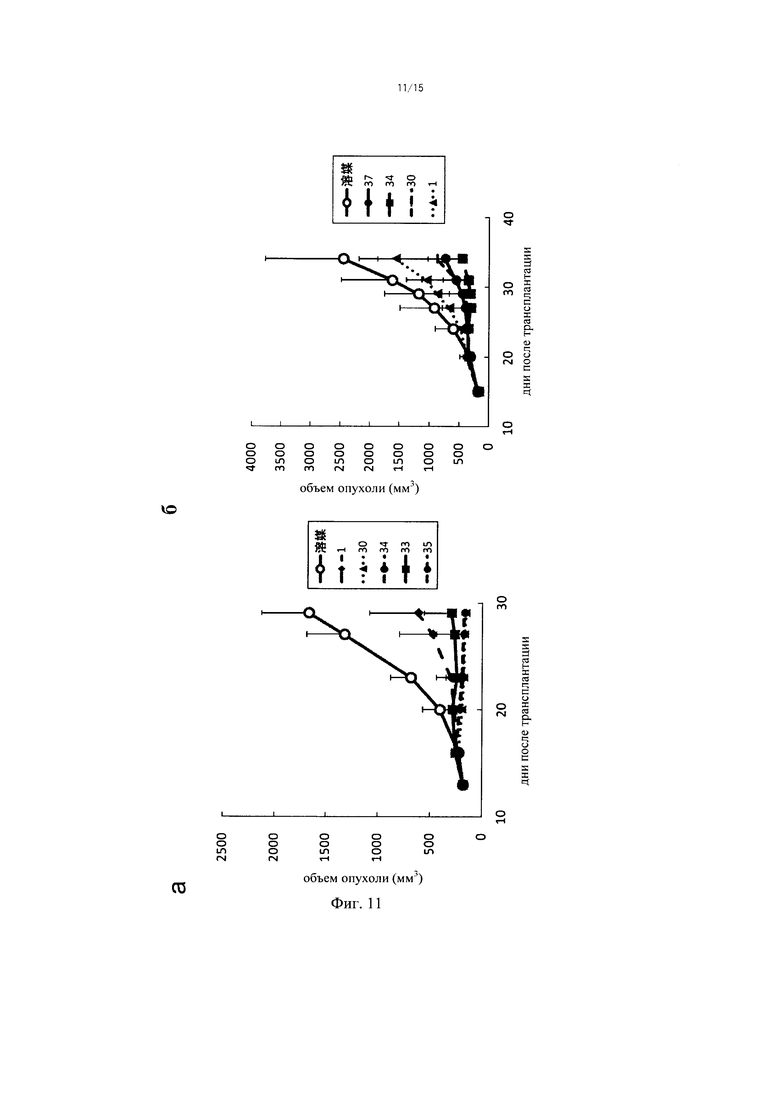


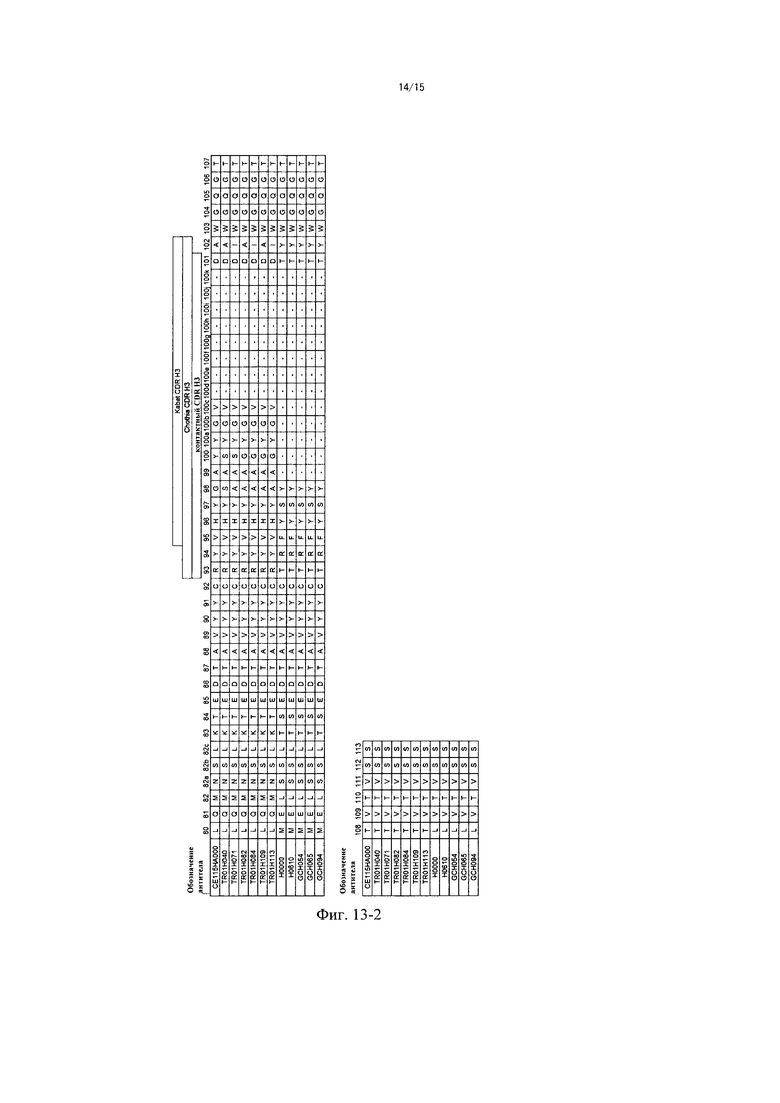
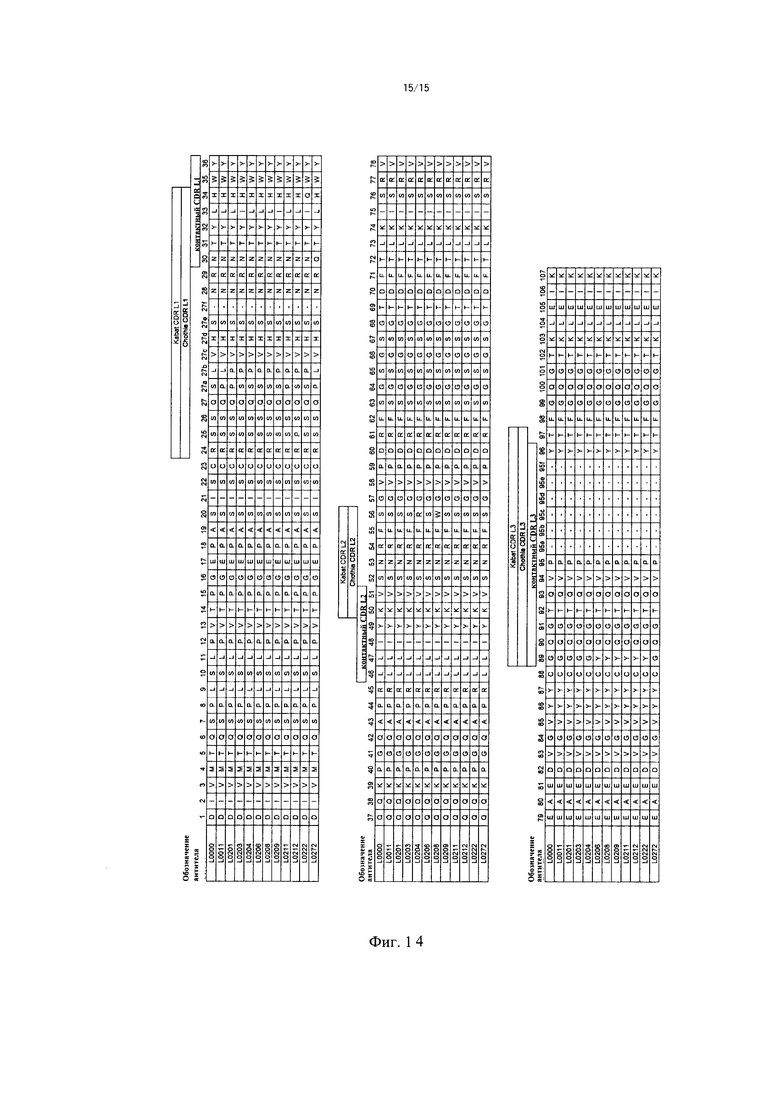
Изобретение относится к области биотехнологии. Предложены биспецифические антитела, которые специфически связываются с глипиканом 3 и CD3 эпсилон. Также изобретение относится к нуклеиновым кислотам, кодирующим биспецифические антитела, к векторам и клеткам для их экспрессии, к способу получения указанных антител. Кроме того, представлена фармацевтическая композиция, предназначенная для лечения или предупреждения различных типов рака. Изобретение обеспечивает высокую цитотоксическую активность биспецифических антител в отношении клеток и тканей, экспрессирующих глипикан 3, в сочетании с высокой безопасностью. 9 н. и 1 з.п. ф-лы, 15 ил., 14 табл., 9 пр.
1. Биспецифическое антитело, которое специфически связывается с глипиканом 3 и CD3 эпсилон и содержит:
(1) вариабельные области тяжелой и легкой цепи антитела, которое обладает связывающей активностью в отношении глипикана 3,
(2) вариабельные области тяжелой и легкой цепи антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, и
(3) Fc-область с пониженной связывающей активностью в отношении Fcγ-рецептора,
в котором вариабельные области легкой цепи, указанные в подпункте (1) и в подпункте (2), имеют общую аминокислотную последовательность SEQ ID NO: 223; при этом вариабельная область тяжелой цепи, указанная в подпункте (1), имеет аминокислотную последовательность SEQ ID NO: 211 или 206, вариабельная область тяжелой цепи, указанная в подпункте (2), имеет аминокислотные последовательности, выбранные из группы, состоящей из SEQ ID NO: 142, 164 или 168, a Fc-область, указанная в подпункте (3), является Fc-областью, включенной в константную область тяжелой цепи, которая имеет аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 60, 61 и 62.
2. Биспецифическое антитело по п. 1, дополнительно включающее константные области легкой цепи, имеющие общую аминокислотную последовательность SEQ ID NO: 63.
3. Биспецифическое антитело, которое специфически связывается с глипиканом 3 и CD3 эпсилон и содержит:
(1) вариабельную область тяжелой цепи антитела, которое обладает связывающей активностью в отношении глипикана 3,
(2) вариабельную область тяжелой цепи антитела, которое обладает связывающей активностью в отношении CD3 эпсилон,
(3) идентичные вариабельные области легкой цепи, которые включают CDR1, CDR2 и CDR3, аминокислотная последовательность которых идентична аминокислотной последовательности CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 223; и
(4) гетеродимерную Fc область, которая является комбинацией двух аминокислотных последовательностей, где первая аминокислотная последовательность идентична Fc области, содержащейся в константной области тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 60 или 62, и вторая аминокислотная последовательность идентична Fc области, содержащейся в константной области тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 61,
при этом вариабельная область тяжелой цепи, указанная в подпункте (1), включает CDR1, CDR2 и CDR3, аминокислотная последовательность которых идентична аминокислотной последовательности CDR1, CDR2 и CDR3 областей, содержащихся в SEQ ID NO: 211 или 206,
вариабельная область тяжелой цепи, указанная в подпункте (2), включает CDR1, CDR2 и CDR3, аминокислотная последовательность которых идентична аминокислотной последовательности CDR1, CDR2 и CDR3 областей, содержащихся в аминокислотных последовательностях, выбранных из группы, состоящей из SEQ ID NO: 142, 164 или 168.
4. Биспецифическое антитело, которое специфически связывается с глипиканом 3 и CD3 эпсилон и содержит:
(1) вариабельную область тяжелой цепи антитела, которое обладает связывающей активностью в отношении глипикана 3,
(2) вариабельную область тяжелой цепи антитела, которое обладает связывающей активностью в отношении CD3 эпсилон,
(3) идентичные вариабельные области легкой цепи, имеющие аминокислотную последовательность SEQ ID NO: 223; и
(4) гетеродимерную Fc область, которая является комбинацией двух аминокислотных последовательностей, где первая аминокислотная последовательность идентична Fc области, содержащейся в константной области тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 60 или 62, и вторая аминокислотная последовательность идентична Fc области, содержащейся в константной области тяжелой цепи, имеющей аминокислотную последовательность SEQ ID NO: 61, при этом вариабельная область тяжелой цепи, указанная в подпункте (1), имеет аминокислотную последовательность SEQ ID NO: 211 или 206, вариабельная область тяжелой цепи, указанная в подпункте (2), имеет аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 142, 164 или 168.
5. Биспецифическое антитело, которое специфически связывается с глипиканом 3 и CD3 эпсилон, по одному из указанных ниже подпунктов (a1)-(a6):
(a1) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелую цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60; и две идентичные легкие цепи, содержащие вариабельную область легкой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63;
(а2) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелую цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 142, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60; и две идентичные легкие цепи антитела, содержащие вариабельную область легкой цепи антитела, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63;
(а3) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелую цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60; и две идентичные легкие цепи антитела, содержащие вариабельную область легкой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63;
(а4) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелая цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60; и две идентичные легкие цепи антитела, содержащие вариабельную область легкой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63;
(а5) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 206, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелую цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 168, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 62; и две идентичные легкие цепи антитела, содержащие вариабельную область легкой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63; и
(а6) биспецифическое антитело, имеющее тяжелую цепь, которое обладает связывающей активностью в отношении глипикана 3, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 211, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 61; тяжелую цепь антитела, которое обладает связывающей активностью в отношении CD3 эпсилон, содержащую вариабельную область тяжелой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 164, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 60; и две идентичные легкие цепи антитела, содержащие вариабельную область легкой цепи, которая имеет аминокислотную последовательность SEQ ID NO: 223, и константную область, которая имеет аминокислотную последовательность SEQ ID NO: 63.
6. Нуклеиновая кислота, кодирующая биспецифическое антитело по любому из пп. 1-5.
7. Вектор, обеспечивающий экспрессию биспецифического антитела по любому пп. 1-5 с интродуцированной нуклеиновой кислотой по п. 6.
8. Клетка, предназначенная для получения биспецифического антитела по любому из пп. 1-5, включающая вектор по п. 7.
9. Способ получения биспецифического антитела по любому из пп. 1-5, предусматривающий трансформацию клетки-хозяина вектором по п. 7 и культивирование клетки по п. 8.
10. Фармацевтическая композиция для лечения рака, включающая эффективное количество биспецифического антитела по любому из пп. 1-5 и фармацевтически приемлемый носитель.
| ТЕПЛОВЫДЕЛЯЮЩАЯ СБОРКА ЯДЕРНОГО РЕАКТОРА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2016 |
|
RU2647707C1 |
| WO 2004065611 A1, 05.08.2004 | |||
| DAE YOUNG KIM et al., Antibody light chain variable domains and their biophysically improved versions for human immunotherapy, MABS, January/February 2014, vol | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА 3 | 2005 |
|
RU2427588C2 |
Авторы
Даты
2021-02-18—Публикация
2015-09-25—Подача