Изобретение относится к медицине, а именно к диагностике онкологических заболеваний, и может быть использовано для определения степени регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом компьютерной томографии (КТ).
Учитывая клинические рекомендации ведущих онкологических ассоциаций (European Society for Medical Oncology, ESMO; National Comprehensive Cancer Network, NCCN; Российское Общество Клинической Онкологии, RUSSCO), пациентам с местно-распространенным раком желудка (cT2-4bN0-3) перед хирургической резекцией с лимфодиссекцией проводится неоадъювантная химиотерапия, что подтверждается исследованиями, демонстрирующими улучшение показателей общей и безрецидивной выживаемости (R.T. Grundmann,  A. Bembenek, Ε. Bollschweiler and others. Diagnostik und Therapie des Magenkarzinoms -Workflow, Diagnosis of and Therapy for Gastric Cancer -Work-Flow; DOI 10.1055/s-0029-1224534 Zentralbl Chir 2009; 134: 362-374.).
A. Bembenek, Ε. Bollschweiler and others. Diagnostik und Therapie des Magenkarzinoms -Workflow, Diagnosis of and Therapy for Gastric Cancer -Work-Flow; DOI 10.1055/s-0029-1224534 Zentralbl Chir 2009; 134: 362-374.).
Хирургическое лечение больных раком желудка с наличием единичных отдаленных метастазов может быть рассмотрено у тщательно отобранных пациентов с обсуждением на мультидисциплинарном консилиуме, с учетом хорошего ответа на проведенную неоадъювантную терапию и с возможностью радикального удаления метастазов - достижения R0 резекции (Клинические рекомендации Рак желудка МКБ 10: С16; 2019; Общероссийский национальный союз "Ассоциация онкологов России", Общероссийская общественная организация " Российское общество клинической онкологии".). Таким образом, и развитие противоопухолевой терапии, и современные рекомендации по хирургическому лечению диктуют необходимость разработки систем оценки ответа на методы лечения (Tumor Regression Grade, TRG).
Существующие на сегодняшний день системы TRG разработаны для патоморфологов, и способны дать ответ уже после оперативного вмешательства. Хотя целью систем TRG является не только определение правильного прогноза, выбор послеоперационной адъювантной терапии и определение интенсивности наблюдения, но и непосредственное влияние на принятие клинических решений, в том числе, влияющих на хирургическую тактику.
Для оценки эффекта химиотерапии методами инструментальной диагностики используются рекомендации экспертов ВОЗ (Критерии Всемирной Организации Здравоохранения, WHO-критерии), критерии оценки регрессии РЖ после неоадъювантной терапии, предложенные японским исследовательским обществом по изучению рака желудка (JRSGC) в 1985 году, и система RECIST.
Рекомендации экспертов ВОЗ включают 4 степени реакции опухоли на проводимое лечение (полный ответ - complete response, CR; частичный ответ - particular response, PR; стабилизация заболевания - stable disease, SD; прогрессирование заболевания - progression disease, PD), основанные на расчете суммы наибольших размеров по данным КТ (sum of the products of diameters; SPD). Предполагается оценка размеров опухоли и метастазов как производное двух наибольших перпендикулярных диаметров, что и является искомой SPD (Zhenhui Li, Dafu Zhang, Youguo Dai, Jian Dong, Lin Wu, Yajun Li, Zixuan Cheng, Yingying Ding, Zaiyi Liu; Computed tomography-based radiomics for prediction of neoadjuvant chemotherapy outcomes in locally advanced gastric cancer: A pilot study. Chinese Journal of Cancer Research. All rights reserved. Res 2018;30(4):406-414; doi: 10.21147/j.issn.l000-9604.2018.04.03.).
Недостатком данного способа является то, что даже минимальные погрешности измерения таргетного очага могут привести к значимому изменению SPD. Также данная система TRG основана только на изменении размеров без учета изменений структуры опухоли и метастазов, что, в свою очередь, не отражает характер ангиогенеза опухоли и, соответственно, степень ответа на лечение. Новые терапевтические схемы лечения в определенных случаях могут вызвать парадокс увеличения в размере после лечения, несмотря на благоприятный ответ, и наоборот, небольшое изменение морфологических признаков после определенных цитостатических препаратов могут быть неправильно классифицированы как стабилизация процесса, несмотря на клиническое прогрессирование (Xiang Ji, Qiaoyun Yang, Hui Qin, Jie Zhou and Wenming Liu; Tumor blood supply may predict neoadjuvant chemotherapy response and survival in patients with gastric cancer; Journal of International Medical Research; 2019, Vol. 47(6) 2524-2532.).
Известен способ оценки регрессии РЖ после неоадъювантной терапии, разработанный на основе критериев ВОЗ японским исследовательским обществом по изучению рака желудка (JRSGC) в 1985 году, включающий новые критерии оценки регрессии РЖ после неоадъювантной терапии, в том числе количественные критерии для первичной оценки опухоли. Основные акценты были сделаны на использование рентгеновского и эндоскопического методов первичной диагностики и специфичность метода для диффузных типов рака. Метод основан на оценке линейных размеров опухоли на рентгеновских снимках и изменении площади просвета желудка (Japanese Gastric Cancer Association. Japanese Classification of Gastric Carcinoma - 2nd English Edition - Response assessment of chemotherapy and radiotherapy for gastric carcinoma: clinical criteria; Gastric Cancer (2001) 4: 1-8.).
В этой системе TRG также не интегрирована оценка структуры опухоли и оценка лимфатических узлов в целом, а ответ, оцененный только в первичной опухоли, не может самостоятельно отражать химиотерапевтический эффект или прогноз, что является значительным недостатком способа.
Таким образом, основной системой оценки опухолевого процесса на дооперационном этапе в настоящее время остается RECIST, основанная на оценке измеряемого очага только по одному наибольшему размеру. При этом любые очаги менее 10 мм считаются неизмеримыми. В 2009 г.система RECIST была пересмотрена с преобразованием версии RECIST 1.0 в RECIST 1.1. (Е.А. Eisenhauera, P. Therasseb, J. Bogaertsc, L.H. Schwartzd, D. Sargente, R. Fordf, J. Danceyg, S. Arbuckh, S. Gwytheri, M. Mooneyg, L. Rubinsteing, L. Shankarg, L. Doddg, R. Kaplanj, D. Lacombec, J. Verweijk; New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1); EUROPEAN JOURNAL OF CANCER 45(2009) 228-247).
Система RECIST основана на оценке динамики линейных размеров, а учитывая большую распространенность опухолей с инфильтративным типом роста, диффузного РЖ, становится затруднительным применение ее в практике.
Помимо оценки первичной опухоли не менее важную роль имеют региональные лимфатические узлы, оценка которых также претерпевает значительные трудности, ведь средний размер метастатически пораженных лимфатических узлов при РЖ составляет около 6 мм (Felix Berlth, Seung-Hun Chon, Mickael Chevallay, Minoa Karin Jung,  Preoperative staging of nodal status in gastric cancer; Translational Gastroenterology and Hepatology. All rights reserved. 2017;2:8. doi:10.21037/tgh.2017.01.08.), a по системе RECIST 1.1. ЛУ могут считаться таргетными очагами узлы от 15 мм по короткой оси и более, от 10 мм до 15 мм включительно -расцениваются как нетаргетные очаги, а менее 10 мм - как не патологические. По данным литературы наличие остаточной опухоли в лимфатическом узле, а не регрессионное изменение в лимфатическом узле, является важным предиктором прогноза после неоадъювантной химиотерапии.
Preoperative staging of nodal status in gastric cancer; Translational Gastroenterology and Hepatology. All rights reserved. 2017;2:8. doi:10.21037/tgh.2017.01.08.), a по системе RECIST 1.1. ЛУ могут считаться таргетными очагами узлы от 15 мм по короткой оси и более, от 10 мм до 15 мм включительно -расцениваются как нетаргетные очаги, а менее 10 мм - как не патологические. По данным литературы наличие остаточной опухоли в лимфатическом узле, а не регрессионное изменение в лимфатическом узле, является важным предиктором прогноза после неоадъювантной химиотерапии.
В настоящее время структурированного алгоритма в отношении протокола КТ исследования для оценки регрессии местно-распространенного РЖ после проведения неоадъювантной терапии нет.
Техническим результатом изобретения является возможность определения степени регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом КТ на этапе клинического стадирования с высокой точностью.
Указанный технический результат достигается в способе определения степени регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом КТ, в котором до и после проведения неоадъювантной химиотерапии проводят КТ с внутривенным болюсным введением контрастного препарата в артериальную, портальную и отсроченную фазы сканирования с приемом газовой смеси, при этом измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, который расценивают как метастатический, при этом если по КТ все парагастральные лимфатические узлы расценивают как не метастатические, то измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, исключая при этом узлы групп №8 и №12 (JGCA, 2nd English Edition, 1998), причем, если размер лимфатического узла по короткой оси составляет более 6 мм, то степень патоморфологического регресса по КТ устанавливают как TRG 0/1, если размер лимфатического узла по короткой оси составляет менее 6 мм или равен 6 мм, то определяют максимальные показатели денситометрической плотности опухоли желудка в артериальную фазу сканирования и при показателях плотности более 59 HU степень патоморфологического регресса по КТ определяют как TRG 1/2, если менее либо равно 59 HU - TRG 2/3.
Способ иллюстрируется фиг. 1-9, где:
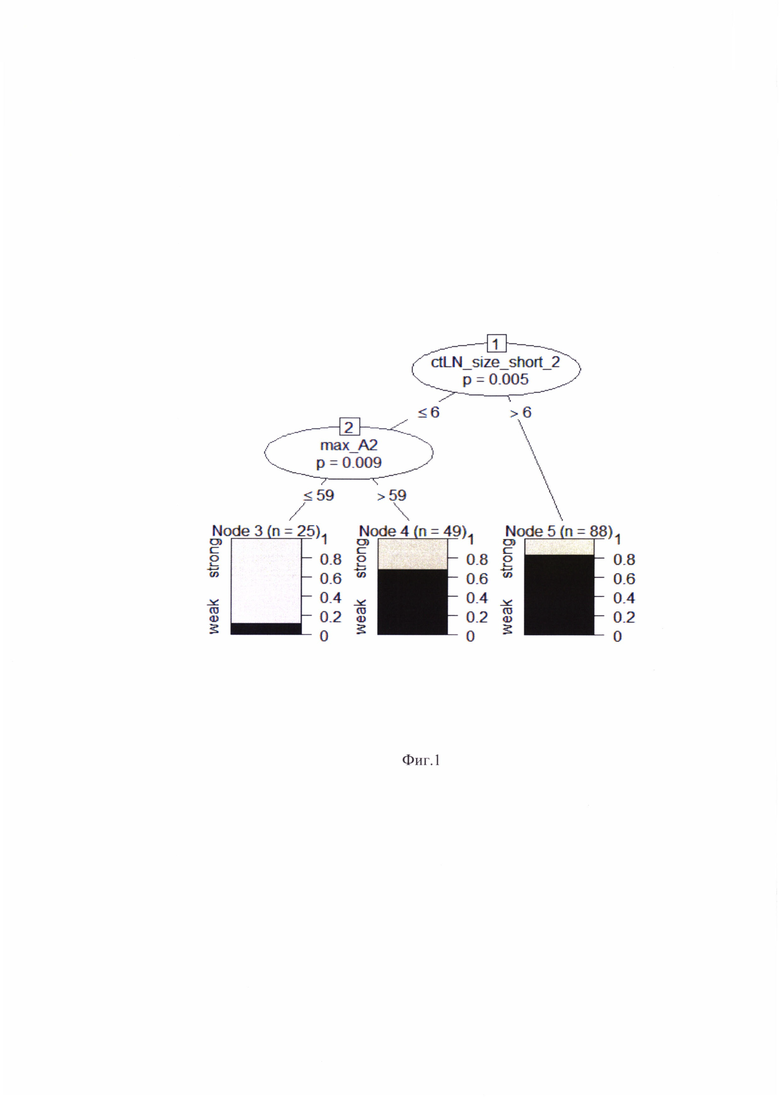
на фиг. 1 - прогностическая модель, построенная методом дерева условного вывода (англ. Conditional Inference Trees) с трехкратной 10-блочной перекрестной валидацией с помощью языка програмирования R и библиотеки caret [Max Kuhn. Contributions from Jed Wing, Steve Weston, Andre Williams, Chris Keefer, Allan Engelhardt, Tony Cooper, Zachary Mayer, Brenton Kenkel, the R Core Team, Michael Benesty, Reynald Lescarbeau, Andrew Ziem, Luca Scrucca, Yuan Tang and Can Candan. (2016). caret: Classification and Regression Training. R package version 6.0-71. https://CRAN.R-project.org/package=caret];
на фиг. 2, 3 - КТ-пневмогастрография до (фиг. 2) и после (фиг. 3) неоадъювантной химиотерапии у пациента, пример 1
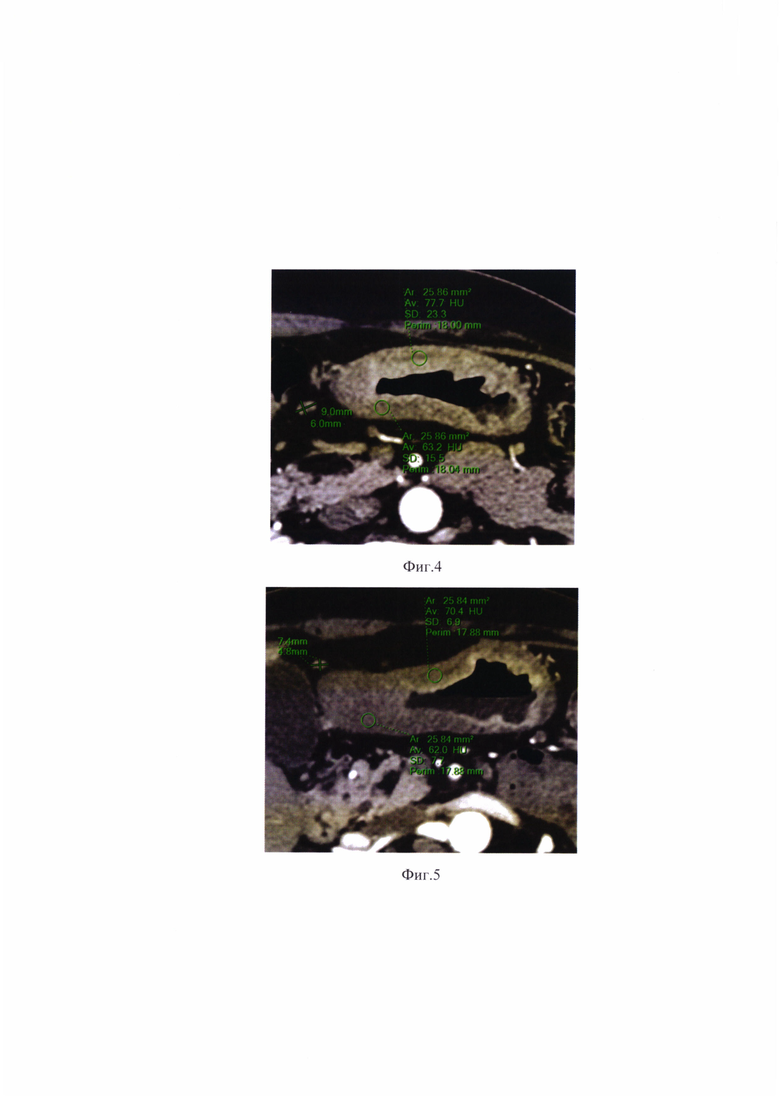
на фиг. 4, 5 - КТ-пневмогастрография до (фиг. 4) и после (фиг. 5) неоадъювантной химиотерапии у пациента, пример 2;
на фиг. 6-9 - КТ-пневмогастрография до (фиг. 6, 7) и после (фиг. 8, 9) неоадъювантной химиотерапии у пациента, пример 3.
В исследование было включено 162 пациента, получавших неоадъювантную химиотерапию. Всем пациента проведена КТ-пневмогастрография по известной методике (Патент РФ 2621952, опубл. 08.06.2017) до начала химиотерапии и после, непосредственно перед оперативным вмешательством. Методика включает внутривенное болюсное введение контрастного препарата в артериальную, портальную и отсроченную фазы сканирования с приемом газовой смеси. Отсроченная фаза сканирования необходима для визуализации опухоли желудка, так как в ряде случаев без раздувания просвета желудка опухоль достаточно сложно дифференцировать на КТ изображениях. Отсроченная фаза сканирования с раздуванием желудка газом позволяет оценить опухоль желудка и спроецировать ее локализацию в артериальную фазу сканирования.
Всем пациентам патоморфологически была определена степень регресса опухоли на проведенную неоадъювантную химиотерапию с учетом классификации JGCA, 3rd English edition. Согласно системе TRG Японской ассоциации по изучению РЖ (JCGC) оценка регрессии опухоли основана на соотношении остаточной жизнеспособной опухолевой ткани, способной к пролиферации, к ложу опухоли: степень регресса 0 - нет эффекта; степень регресса 1 - слабый эффект (степень 1а - очень слабый эффект -жизнеспособные опухолевые клетки занимают более 2/3 области опухоли, степень регресса 1b - слабый эффект - жизнеспособные опухолевые клетки остаются в более 1/3, но менее 2/3 области опухоли); степень регресса 2 -значительный эффект - жизнеспособные опухолевые клетки остаются менее чем в 1/3 от области опухоли; степень регресса 3 - полный ответ - нет жизнеспособных опухолевых клеток (Yuelu Zhu, Yongkun Sun, Shangying Hu, Yong Jiang, Jiangying Yue, Xuemin Xue, Lin Yang and Liyan Xue; Comparison of five tumor regression grading systems for gastric adenocarcinoma after neoadjuvant chemotherapy: a retrospective study of 192 cases from National Cancer Center in China; BMC Gastroenterology (2017) 17:41; DOI: 10.1186/s12876-017-0598-5).
Мы оценили 96 КТ - характеристик опухоли и метастатически измененных парагастральных лимфатических узлов для всех пациентов данного исследования при различных pTRG (JGCA): размер опухоли желудка, размеры лимфатических узлов по короткой и длинной оси до и после неоадъювантной химиотерапии, абсолютную и относительную разницу размера лимфатического узла по короткой и длинной оси до и после неоадъювантной химиотерапии, относительную разницу объема опухоли желудка, абсолютную и относительную разницу средней плотности опухоли желудка и лимфатических узлов в артериальную, портальную и отсроченную фазы сканирования.
В качестве прогнозируемого параметра мы выбрали степень патоморфоза TRG JGCA, упрощенную до двух степеней: хороший ответ, куда входили TRG 2,3 и плохой ответ, куда входили TRG 0,1.
Прогностическая модель (см. фиг. 1) была построена методом дерева условного вывода (англ. Conditional Inference Trees) с трехкратной 10-блочной перекрестной валидацией с помощью языка програмирования R и библиотеки caret [Max Kuhn. Contributions from Jed Wing, Steve Weston, Andre Williams, Chris Keefer, Allan Engelhardt, Tony Cooper, Zachary Mayer, Brenton Kenkel, the R Core Team, Michael Benesty, Reynald Lescarbeau, Andrew Ziem, Luca Scrucca, Yuan Tang and Can Candan. (2016). caret: Classification and Regression Training. R package version 6.0-71. https://CRAN.R-project.org/package=caret].
Согласно полученной прогностической модели, если размер наибольшего парагастрального лимфатического узла по короткой оси после проведения неоадъювантной химиотерапии превышал 6 мм, то имелся слабый ответ на лечение TRG 0-1, если размер парагастрального лимфатического узла по короткой оси после проведения неоадъювантной химиотерапии был меньше или равен 6 мм и максимальная КТ - плотность опухоли в артериальную фазу сканирования при КТ-исследовании после неоадъювантной химиотерапии была меньше или равна 59 HU, то определялся TRG 2-3, если плотность опухоли была больше 59 HU, то - TRG 1-2.
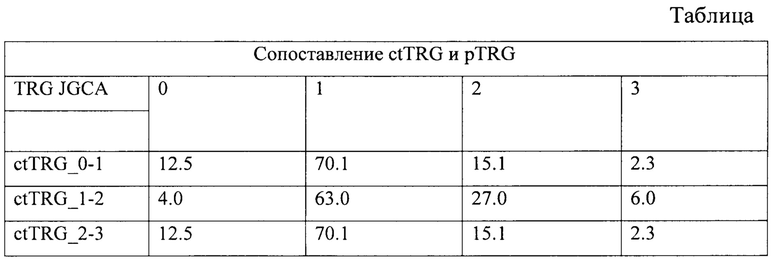
Точность определения ctTRG 0-1 составляет 82,6%, ctTRG 1-2 - 90,0%, ctTRG 2-3 - 88%. Ошибки в определении ctTRG определяются в 18% случаев (каждый 5 случай). Большая часть ошибок приходится на pTRG 2.
Таким образом, разработан алгоритм оценки степени регресса местно-распространенного рака желудка после проведения неоадъювантной химиотерапии на этапе клинического стадирования.
Способ осуществляют, например, следующим образом.
Пациенту с местно-распространенным РЖ до и после проведения неоадъювантной химиотерапии проводят КТ с внутривенным болюсным введением контрастного препарата в артериальную и портальную фазы сканирования, затем пациент принимает per os газообразующую смесь в составе Acidum Citricum - 1±0,5 г, растворенной в 5±1 мл воды, и Natrii Bicarbonati - 2±0,5 г, запивая небольшим количеством воды в объеме не более 30 мл, и на 5 минуте после артериальной фазы проводят раннюю отсроченную фазу сканирования, при этом пациент удерживает образовавшийся газ до окончания исследования. При оценке показателя объема желудка после применения газообразующей смеси отмечено, что указанного количества химических веществ достаточно для адекватного растяжения просвета желудка, позволяющего провести последующий анализ патологических изменений в стенках желудка.
Для определения степени регрессии по КТ измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, который расценивают как метастатический, Если по КТ все парагастральные лимфатические узлы расценивают как не метастатические, то по короткой оси оценивают наиболее крупный не метастатический парагастральный лимфатический узел, исключая при этом узлы групп №8 и №12, причем, если размер лимфатического узла по короткой оси составляет более 6 мм, то степень патоморфологического регресса по КТ устанавливают как TRG 0/1, если размер лимфатического узла по короткой оси составляет менее 6 мм или равен 6 мм, то определяют максимальные показатели денситометрической плотности опухоли желудка в артериальную фазу сканирования и при показателях плотности более 59 HU степень патоморфологического регресса по КТ определяют как TRG 1/2, если менее либо равно 59 HU - TRG 2/3.
Способ иллюстрируется следующими клиническими примерами.
Пример 1. Пациенту с местно-распространенным раком желудка проведена КТ-пневмогастрография до (фиг. 2) и после (фиг. 3) неоадъювантной химиотерапии. При КТ после неоадъювантной химиотерапии размер наиболее крупного парагастрального лимфатического узла, расцениваемого как метастатический, уменьшился с 15x10 мм до 13x8 мм, т.е. размер по короткой оси составляет более 6 мм. Таким образом степень патоморфологического регресса по КТ устанавливают, как TRG 0/1. По результатам патоморфологического заключения у данного пациента степень патологического ответа расценена как «слабый ответ» - pTRG 1.
Пример 2. Пациенту с местно-распространенным раком желудка проведена КТ-пневмогастрография до (фиг. 4) и после (фиг. 5) неоадъювантной химиотерапии. При КТ после неоадъювантной химиотерапии размер наиболее крупного парагастрального лимфатического узла, расцениваемого как метастатический, уменьшился с 9x6 мм до 7x4 мм, т.е. размер по короткой оси составляет менее 6 мм. Поэтому следующим этапом была определена денситометрическая плотность опухоли желудка в артериальную фазу сканирования, которая составила 62-70 HU, т.е. более 59 HU. Таким образом, степень патоморфологического регресса по КТ установлена - TRG 1/2. По результатам патоморфологического заключения у данного пациента степень патологического ответа расценена как «значительный ответ» - pTRG 2.
Пример 3. Пациенту с местно-распространенным раком желудка проведена КТ-пневмогастрография до (фиг. 6, 7) и после (фиг. 8, 9) неоадъювантной химиотерапии. При КТ после неоадъювантной химиотерапии размер наиболее крупного парагастрального лимфатического узла, расцениваемого как метастатический, уменьшился с 16x12 мм до 12x5 мм, т.е. размер по короткой оси составляет менее 6 мм. Поэтому следующим этапом была определена денситометрическая плотность опухоли желудка в артериальную фазу сканирования, которая составила 47-55 HU, т.е. менее 59 HU. Таким образом, степень патоморфологического регресса по КТ установлена - TRG 2/3. По результатам патоморфологического заключения у данного пациента степень патологического ответа расценена как «значительный ответ» - pTRG 2.
Способ позволяет определить степень регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом КТ с высокой точностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ТИПА РАКА ЖЕЛУДКА ПО КЛАССИФИКАЦИИ LAUREN МЕТОДОМ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ | 2020 |
|
RU2743221C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННОГО РАКА ЖЕЛУДКА С ВЫСОКОЙ МЕТАБОЛИЧЕСКОЙ И ПРОЛИФЕРАТИВНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2552289C1 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ ПРЯМОЙ КИШКИ С ИСПОЛЬЗОВАНИЕМ НЕОАДЪЮВАНТНОЙ ЛУЧЕВОЙ ТЕРАПИИ И КОНСОЛИДИРУЮЩЕЙ ХИМИОТЕРАПИИ | 2021 |
|
RU2770989C2 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА ЖЕЛУДКА | 2020 |
|
RU2725079C2 |
| Способ комбинированного лечения местнораспространённого кардиоэзофагельного рака | 2021 |
|
RU2765845C1 |
| Способ оценки непосредственных результатов лечения больных диссеминированными формами злокачественных опухолей | 2023 |
|
RU2806483C1 |
| Способ комбинированного лечения операбельного рака желудка с позитивным PDL-статусом | 2020 |
|
RU2756870C1 |
| Способ диагностики регресса рака молочной железы после неоадъювантной лекарственной терапии | 2022 |
|
RU2806299C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С BRCA-АССОЦИИРОВАННЫМ ТРИЖДЫ НЕГАТИВНЫМ МЕСТНОРАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2814578C1 |
| Способ оценки непосредственных результатов лечения диссеминированного почечно-клеточного рака | 2020 |
|
RU2751086C1 |



Изобретение относится к медицине, а именно к диагностике онкологических заболеваний, и может быть использовано для определения степени регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом компьютерной томографии (КТ). До и после проведения неоадъювантной химиотерапии проводят КТ с внутривенным болюсным введением контрастного препарата в артериальную, портальную и отсроченную фазы сканирования с приемом газовой смеси. При этом измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, который расценивают как метастатический. Если по КТ все парагастральные лимфатические узлы расценивают как неметастатические, то измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, исключая при этом узлы групп №8 и №12. Если размер лимфатического узла по короткой оси составляет более 6 мм, то степень патоморфологического регресса по КТ устанавливают как TRG 0/1. Если размер лимфатического узла по короткой оси составляет менее 6 мм или равен 6 мм, то определяют максимальные показатели денситометрической плотности опухоли желудка в артериальную фазу сканирования и при показателях плотности более 59 HU степень патоморфологического регресса по КТ определяют как TRG 1/2, если менее либо равно 59 HU - TRG 2/3. Способ позволяет определить степень регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом КТ за счет заявленных КТ-характеристик опухоли. 1 табл., 3 пр., 9 ил.
Способ определения степени регрессии местно-распространенного рака желудка после проведения неоадъювантной химиотерапии методом компьютерной томографии (КТ), отличающийся тем, что до и после проведения неоадъювантной химиотерапии проводят КТ с внутривенным болюсным введением контрастного препарата в артериальную, портальную и отсроченную фазы сканирования с приемом газовой смеси, при этом измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, который расценивают как метастатический, при этом если по КТ все парагастральные лимфатические узлы расценивают как неметастатические, то измеряют по короткой оси наиболее крупный парагастральный лимфатический узел, исключая при этом узлы групп №8 и №12, причем если размер лимфатического узла по короткой оси составляет более 6 мм, то степень патоморфологического регресса по КТ устанавливают как TRG 0/1, если размер лимфатического узла по короткой оси составляет менее 6 мм или равен 6 мм, то определяют максимальные показатели денситометрической плотности опухоли желудка в артериальную фазу сканирования и при показателях плотности более 59 HU степень патоморфологического регресса по КТ определяют как TRG 1/2, если менее либо равно 59 HU - TRG 2/3.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ РИСКА РАЗВИТИЯ НЕДОСТАТОЧНОСТИ АНАСТОМОЗОВ В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ У БОЛЬНЫХ РАКОМ ПИЩЕВОДА | 2015 |
|
RU2599209C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННОГО РАКА ЖЕЛУДКА С ВЫСОКОЙ МЕТАБОЛИЧЕСКОЙ И ПРОЛИФЕРАТИВНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2552289C1 |
| СПОСОБ КОМПЬЮТЕРНО-ТОМОГРАФИЧЕСКОГО ИССЛЕДОВАНИЯ ЖЕЛУДКА | 2016 |
|
RU2621952C1 |
| БОЙКОВ И | |||
| В | |||
| и др | |||
| Совмещенная позитронно-эмиссионная и компьютерная томография в диагностике и стадировании опухолей грудной и брюшной полости | |||
| Вестник Российской военно-медицинской академии | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| JOON SEOK LIM et al | |||
| CT and PET in Stomach Cancer: | |||
Авторы
Даты
2021-06-09—Публикация
2020-11-23—Подача