Изобретение относится к медицине, а именно к патологической анатомии и онкологии, и может быть применено в качестве способа диагностики регресса рака молочной железы (РМЖ) после неоадъювантной лекарственной терапии.
Известна оценка морфологического регресса рака молочной железы (РМЖ) после неодъювантной терапии (HAT). Наиболее широко используемая и проверенная в клинической практике - концепция определения индекса остаточной опухолевой нагрузки (PCR - pathologic complete response). В 2014 г. FDA (Food and Drug Administration) одобрило применение оценки PCR в качестве суррогатного маркера эффективности HAT как имеющего существенное прогностическое значение для пациентов РМЖ [1 - Bossuyt V., Provenzano Е., Symmans W.F., Boughey J.C., Coles С, Curiglianoet G. et al. Recommendation forstandardized pathological characterization of residual disease for neoadjuvant clinical trials of breast cancer by the BIG-NAB CG collaboration. Ann.Oncol. 2015; 26(7): 1280-1291]. Данный способ принят за аналог.
Известен способ оценки морфологического регресса молочной железы. Полная морфологическая регрессия - это отсутствие жизнеспособных опухолевых клеток инвазивного РМЖ как в ткани молочной железы, так и в регионарных лимфатических узлах, причем, статус лимфатических узлов является важным прогностическим фактором. Данный способ принят за прототип [2 - Fayanju О.М., Ren Y., Thomas S.M., Greenup R.A., Plichta J.K., Rosenberger L.H. at el. The Clinical Significance of Breast-only and Node-only Pathologic Complete Response (PCR) After Neoadjuvant Chemotherapy (NA CT): A Review of 20,000 Breast Cancer Patients in the National Cancer Data Base (NCDB). Ann Surg. 2018; 268(4): 591-601]. Однако, данная система не полностью обеспечивает объективный ответ на HAT за счет отсутствия многофакторного анализа.
Цель - повышение точности оценки регресса рака молочной железы на неодъювантную терапию.
Технический результат достигается тем, что в способе диагностики регресса рака молочной железы после неоадъювантной лекарственной терапии, включающим рентгенографию, дополнительно оценивают размеры наибольшей площади плоскости поперечного сечения рентген-позитивного ложа, выполняют серийные срезы для изготовления гистологических препаратов с одновременным цифровым картированием ложа и маркировкой гистологическими красителями, получением процента карциномы in situ, числа лимфатических узлов с метастазами и размера наибольшего метастаза, с последующим расчетом индекса регресса опухоли по формуле:
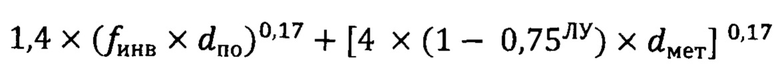
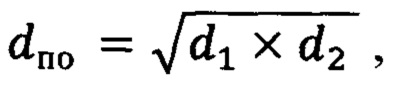
где d1, d2 - микроскопические размеры ложа опухоли, dпо - наибольшая площадь плоскости поперечного сечения ложа первичной опухоли.
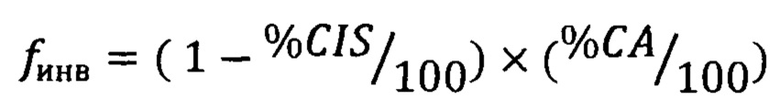 - выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
- выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
ЛУ - число лимфатических узлов с метастазами,
dмет - наибольший диаметр метастаза в лимфатическом узле при этом результатом вычислений является класс регресса опухоли, ранжированный от I до III:
I минимальная остаточная опухоль, индекс менее 1,36;
II умеренная остаточная опухоль, индекс 1,37-3,28;
III выраженная остаточная опухоль, индекс более 3,29
На Фиг. 1 представлена рентгенография образца до разреза ткани. Идентификация рентген-позитивного ложа первичной опухоли и точное определение локализации металлической клипсы, имплантированной в опухоль до начала лечения.
На Фиг. 2 представлена рентгенография образца после разреза ткани на серийных слайсах толщиной 3-5 мм. Исследование ложа опухоли, измерение размеров наибольшей площади плоскости поперечного сечения ложа (в мм2), оценка расстояния до краев резекции (в мм), идентификация микрокальцинатов и других подозрительных участков с повышенной контрастностью.
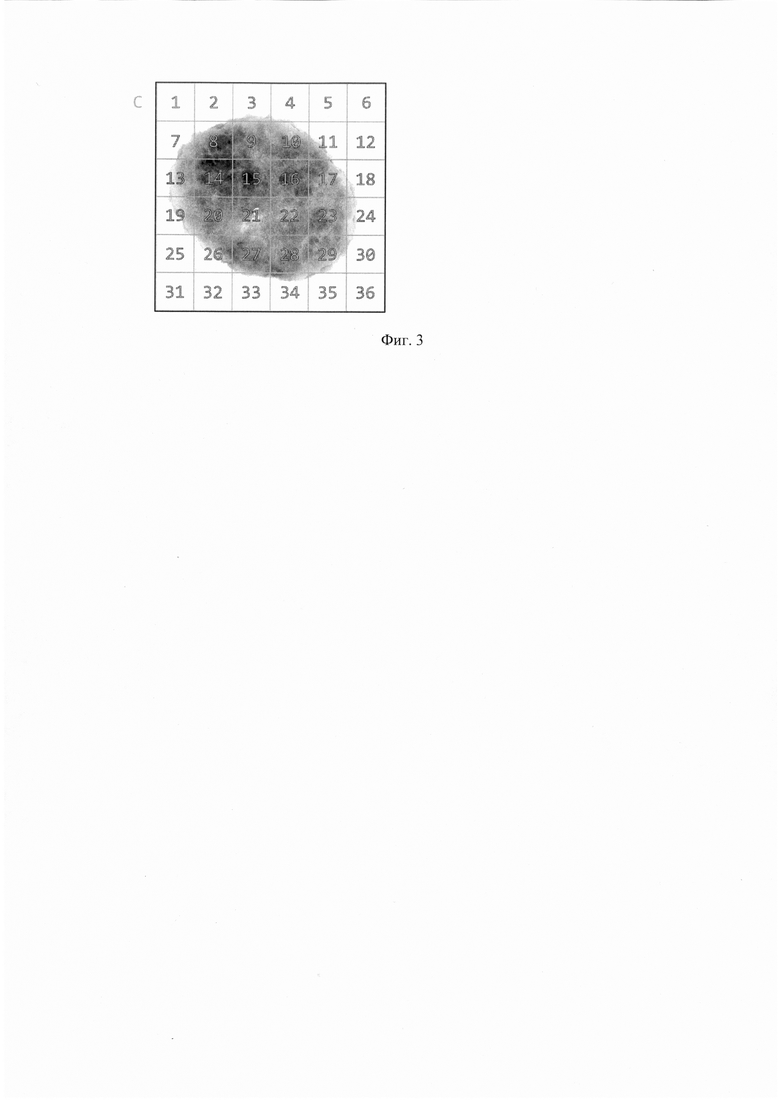
На Фиг. 3 представлена радиографическая оценка и цифровое картирование ложа опухоли.
На Фиг. 4 представлено картирование и маркировка в соответствии с цифровым изображением для гистопатологического исследования: а) ложе опухоли, б) код среза, в) маркированные стекла со срезами.
Способ осуществляется следующим образом.
Термин «неоадъювантная терапия» (HAT) подразумевает проведение системной химио- или гормонотерапии перед началом локального лечения [3 - Tyulyadin S.A. The value of preoperative chemotherapy in patients with breast cancer. IV Russian oncology conference. M.; 2000.]. В настоящее время морфологическая оценка регресса опухоли несет в себе и прогностическую, и предиктивную значимость. HAT представляет модель валидации in vivo эффективности проводимого лекарственного лечения. Суррогатная конечная точка, ответ на химиотерапию, является значимым прогностическим фактором риска рецидива, особенно при HER2+и тройном негативном раке молочной железы [4 - Rapoport B.L., Demetriou G.S., Moodley S.D., Benn C.A. When and How Do I Use Neoadjuvant Chemotherapy for Breast Cancer? // Current Treatment Options in Oncology. 2014; 15: 86-98. Doi: 10.1007/s11864-013-0266-0.]. HAT при РМЖ - это быстро развивающееся направление, вызывающее огромный интерес к текущим клиническим испытаниям. В результате активного внедрения HAT существует значительная вариабельность в методах патоморфологической оценки регресса опухоли, интерпретации самой оценки, и, исходя из этого, появляются различные последующие клинические решения [5 - Bossuyt V., Provenzano Е., Symmans W.F., Boughey J.C., Coles С, Curiglianoet G. et al. Recommendation for standardized pathological characterization of residual disease for neoadjuvant clinical trials of breast cancer by the BIG-NABCG collaboration. Ann.Oncol. 2015; 26(7): 1280-1291.]. Предпринимаются многочисленные попытки выявить молекулярно-биологические маркеры, позволяющие предсказать ответ опухоли на лечение, тем не менее единственным доказательным способом определения эффекта от лекарственного препарата остается морфологическая оценка регресса. На сегодняшний день известно множество различных систем оценки морфологического регресса РМЖ после HAT.
В России традиционно более широко распространена система оценки лечебного регресса по Г.А. Лавниковой. Эта система базируется на оценке повреждения опухоли и включает четыре степени. Однако данная система не учитывает статус лимфатических узлов и не полностью обеспечивает объективную оценку ответа опухоли на HAT за счет отсутствия многофакторного анализа. Данный способ принят за аналог. В клинических рекомендациях Европейского общества онкологов (ESMO) с 2015 г, клинических рекомендациях по патологоанатомической диагностике РМЖ 2018 г. Российского общества патологоанатомов (РОП) и в современной гистологической классификации опухолей молочной железы всемирной организации здравоохранения (2019), для определения выраженности лечебного эффекта HAT при РМЖ рекомендуется использовать систему оценки ложа остаточной опухоли, RCB (residual cancer burden). Система RCB - математическая модель, предложенная Symmans W. с соавт. в 2007 году, на основании оценки характеристик остаточной опухоли и кривых безрецидивной выживаемости больных, стратифицирует пациентов при неполной морфологической регрессии [6 - Campbell J.I., Yau С, Krass P., Moore D., Carey L.A., Au A., et al. Comparison of residual cancer burden, American Joint Committee on Cancer staging and pathologic complete response in breast cancer after neoadjuvant chemotherapy: results from the I-SPY 1 TRIAL (CALGB 150007/150012; ACRIN 6657). Breast Cancer Res. Treat. 2017; 165: 181-191. Doi: 10.1007/s10549-017-4303-8.]. RCB базируется на следующих параметрах остаточной опухоли: микроскопические размеры ложа опухоли; процент клеточности; процент рака in situ; количество пораженных регионарных лимфатических узлов и наибольший размер метастаза. Однако данная система также не полностью обеспечивает объективную оценку ответа опухоли на HAT за счет трудностей определения числовых характеристик опухолевого ложа. Наиболее сложной задачей метода RCB является точное определение размера ложа опухоли, так как критерии его недостаточно четкие [7 - Andreeva Yu.Yu., Moskvina L.V., Berezina T.A., Podberezina Yu.L., Loktev S.S., Frank G.A. Procedure for intraoperative material examination in breast cancer after neoadjuvant therapy to estimate residual cancer burden using the RCB system. Arkh Patol. 2016; 78(2): 41-46.].
Образец доставляют в лабораторию патоморфологии в течение часа после операции, так как идентификация ложа опухоли должна производиться строго на нативном материале. Сопроводительное направление на морфологическое исследование должно включать: дозы и сроки неоадъювантной терапии, сведения о признаках клинического ответа на проведенное лечение, размерах и локализации первичной опухоли по данным пальпации и лучевых методов до начала лечения и после, данные о размещении металлического маркера и вовлечении лимфатических узлов до лечения. Морфологическое исследование начинается с констатации факта соответствия доставленного материала и его маркировки сведениям, указанным в направлении.
Начальный этап исследования и описания материала включает в себя следующий алгоритм:
• правильная ориентация препарата;
• окрашивание краев маркировочной гистологической краской (рекомендуется использовать разные цвета, чтобы идентифицировать каждый из должным образом ориентированных краев образца);
• определение размеров образца в трех плоскостях (ткань железы, лоскут кожи и регионарная клетчатка измеряются отдельно)
• оценка состояния поверхности кожи, соска и ареолы (цвет, плотность, мацерация, втяжение, изъязвление и т.д.);
• оценка состояния фасциального края
• идентификация хирургических меток при их наличии
Макроскопически ложе опухоли после HAT чаще выглядит как фиброзное уплотнение, а не как отграниченное опухолевое образование. Кроме того, РМЖ высокой степени злокачественности может регрессировать и вовсе без видимого фиброза. При выраженном регрессе (частичном или полном клиническом ответе) макроскопически сложно достоверно определить ложе опухоли и его размеры, особенно в крупных образцах или образцах с массивным фиброзом окружающей нормальной ткани молочной железы. Постановка металлической метки в опухоль при биопсии до начала HAT также может быть неэффективной, в результате ее механического смещения, миграции или поломки [8 - Maker W., Holtschmidt J., Thangarajah F., Mallmann P., Krug В., Warm M. et al. First Reported Use of the Faxitron LOCalizer™ Radiofrequency Identification (RFID) System in Europe - A Feasibility Trial, Surgical Guide and Review for Non-palpable Breast Lesions. In Vivo. 2019; 33(5): 1559-1564.]. При определении ложа первичной остаточной опухоли при макроскопическом исследовании измеряют и указывают результаты в трех проекциях (в мм), также определяют два наибольшие размера поперечной плоскости с учетом асимметрии опухоли. Необходимо также оценить расстояние от опухоли до краев хирургической резекции. Пространственная оценка остаточного ложа опухоли - это наиболее сложная посредством визуального осмотра и пальпации задача, так как размеры и границы ложа опухоли трудно точно оценить при выраженном регрессе.
Рентгенография образца проводится дважды. Первый раз до разреза ткани, для точной идентификации металлической клипсы, имплантированной в ложе первичной опухоли до начала лечения во избежание ее механического смещения (Фиг. 1). Второй раз после разреза образца на серийных слайсах толщиной 3-5 мм (Фиг. 2). Для исследования ложа опухоли, оцениваются размеры наибольшей площади плоскости поперечного сечения рентген-позитивного ложа (в мм2), расстояние до краев резекции (в мм), микрокальцинаты и другие подозрительные участки с повышенной контрастностью. Проводится радиографическая оценка и цифровое картирование ложа опухоли для дальнейшего сопоставления с гистологическими препаратами. Файл цифровой карты для патоморфолога сохраняется в формате DICOM, являющимся стандартом получения и обработки цифровых изображений в медицинских целях. Изображения макропрепаратов служат картой для описания макроскопического исследования и локализации каждого среза ткани для гистопатологического исследования (Фиг. 3). Однако при значительной площади поражения точно реконструировать пластину микропрепаратов крайне сложно. Поэтому дополнительно производится маркировка гистологическими красителями соответствующих по цвету краев стыковки фрагментов ложа до их помещения в гистологическую кассету. Важно отметить, что идентификация микрокальцинатов в макропрепарате молочной железы при морфологическом исследовании выступает в качестве значимого параметра, так как микрокальцинаты являются индикатором карциномы in situ (CIS) и ложа опухоли. В плановое микроскопическое исследование тотально берется плоскость максимального размера опухолевого ложа, производится картирование в соответствии с цифровым изображением выбранных слайсов, маркировка производится слева-направо, сверху-вниз (Фиг. 4).
При работе с цифровым рентгеном важно соблюдать последовательность запуска системы, давать системе выполнять полную калибровку до начала использования.
Основные процедуры визуализации включают в себя:
1. размещение образца внутри установки
2. выбор и введение данных пациента в программное обеспечение
3. запуск системы
4. появление изображения (время, затраченное на генерацию изображения составляет в среднем 10 секунд)
5. выполнение необходимых измерений, нанесение дополнительных разметок
6. сохранение файла цифровой карты в формате DICOM
Основная информация, которая должна быть получена после макроскопического и микроскопического исследования, это точная пространственная оценка остаточного инвазивного рака и доля карциномы in situ. Основная информация, которая должна быть получена при оценке регионарных лимфатических узлов, это общее количество лимфатических узлов, число лимфатических узлов с метастазами и размер наибольшего метастаза.
Затем производится расчет индекса регресса опухоли по формуле:
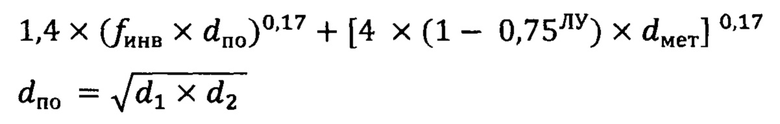
Где d1, d2 - микроскопические размеры ложа опухоли, dпо - наибольшая площадь плоскости поперечного сечения ложа первичной опухоли.
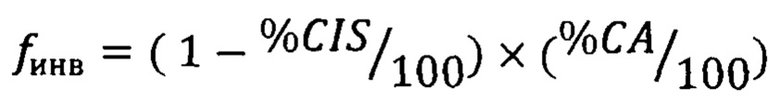 - выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
- выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
ЛУ - число лимфатических узлов с метастазами,
dмет - наибольший диаметр метастаза в лимфатическом узле.
Результатом вычислений является класс регресса опухоли (остаточная опухолевая нагрузка), ранжированный от I до III:
• I минимальная остаточная опухоль, индекс менее 1,36;
• II умеренная остаточная опухоль, индекс 1,37-3,28;
• III выраженная остаточная опухоль, индекс более 3,29
Морфологическая оценка регресса опухоли является золотым стандартом определения эффективности проведенной лекарственной терапии. Показатель индекса регресса опухоли несет в себе прогностическую и предиктивную (в отношении назначения адъювантного лечения) значимость, что подтверждает актуальность разработки новых методов (способов) и протоколов морфологического исследования.
Предлагаемый способ обеспечивает повышение точности определения количественных и качественных показателей ложа опухоли, необходимых для оценки степени патоморфологического регресса РМЖ в ответ на лечение. Способ имеет прикладное значение, так как позволяет облегчить, улучшить и оптимизировать морфологическую диагностику ложа остаточной опухоли после проведенной HAT у пациенток больных раком молочной железы, до сих пор вызывающей значительные трудности в работе практикующих врачей патологоанатомов.
Для цифровой рентгенографии образцов применялась рентгеновская система визуализации PathVision Faxitron® (digital X-Ray). В когорту исследования вошли женщины, средний возраст которых составил 45,5±14 лет. Главным критерием включения послужила выраженная положительная клиническая динамика в ответ на лечение, уменьшение размеров или исчезновение опухолевого узла по данным пальпации и лучевых методов визуализации. Используемые клинические данные содержали сведения о проведенной неоадъювантной терапии, размерах и локализации первичной опухоли до начала лечения. Описаны и проанализированы макроскопические параметры остаточной опухоли на операционном материале. Определена диагностическая эффективность макроскопического исследования образцов молочной железы с применением цифровой рентгенографии. Разработан алгоритм морфологического исследования операционного материала при раке молочной железы после неоадьювантной химиотерапии с применением цифровой рентгенографии. Способ подтверждается следующими примерами:
Пример №1.
Пациент: М. (Ж), 51 (1968 г.)
Диагноз при поступлении: С50.8 Рак левой молочной железы ycT2N1fM0, IIB ст. Люминальный иммунофенотип В, Her2neu позитивный. Состояние после неоадьювантной химиотерапии по протоколу В040747. Последнее введение от 25.12.2019 г
Положительная динамика., CT2N1M0, стадия IIB, II кл. группа.
Состояние при поступлении в стационар
Жалобы при поступлении: на образование в левой молочной железе.
Анамнез болезни: считает себя больной с июля 2019 г, когда при плановом обследовании обнаружили образование в левой молочной железе. Пациентка обследована в МКНЦ ДЦ «Клиника женского здоровья»: маммография, УЗИ молочных желез, трепан биопсия левой молочной железы, ИГХ исследования. Установлен диагноз: рак левой молочной железы ycT2N1fM0, IIB ст. Люминальный иммунофенотип В, Her2neu позитивный. Консультирована онкологом, на первом этапе лечения рекомендовано проведение неоадьювантной химиотерапии. Состояние после неоадьювантной химиотерапии по протоколу В040747. Последнее введение от 25.12.2019 г Положительная динамика. На онкологическом консилиуме от 01.02.2020 г МКНЦ, на втором этапе рекомендовано проведение хирургического лечения в объеме радикальной резекции левой молочной железы. Направлена в МКНЦ на хирургическое лечение.
Местный статус: молочные железы симметричные, кожные покровы бледно розовые, сосок и ареола без особенностей. При пальпации в верхненаружном квадранте пальпируется образование 2,0×2,0 см с нечеткими контурами, плотной консистенции. Регионарные лимфоузлы не увеличены.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у слева от 09.07.19: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования от 08.07.19: цитограмма рака.
• Протокол КТ от 05.08.19: в нижнем наружном квадранте левой молочной железы определяется неоднородной структуры образование с достаточно четкими неровными контурами, до 19×14×21 мм, максимально, подмышечные л/у до 10 мм с липидным компонентом.
• Остеосцинтиграфия от 06.08.19: сцинтиграфических признаков вторичного поражения костей скелета не выявлено.
• Маммография от 03.07.19: в верхне-наружном квадранте левой молочной железы обнаружено узловое образование высокой плотности с нечеткими неровными лучистыми контурами размером 2.3×2,0 см - Suspicio Bl mammae sinistra.
• Маммография от 09.01.20: в зоне ранее определяемого образования определяется участок уплотнения ткани без четких контуров, примерными размерами ~ 2,0 × 2,5 см. В проекции данного участка определяется тень металлической метки. Определяются единичные рассеянные кальцинаты и единичные группы кальцинатов. Аксиллярные лимфатические узлы не визуализируются, в видимой части аксиллярная область без особенностей. При сопоставлении с исследованием от 03.07.2019 г. отмечается положительная динамика в виде уменьшения образования в размере. BIRADS 6 слева. С50.8 Rg картина BL.mam.sin. Положительная динамика от 03.07.2019 г. Состояние после неоадьювантной химиотерапии.
• Протокол УЗИ от 03.07.19: BIRADS 5 слева.
• Протокол УЗИ от 09.01.20: узловые образования - в зоне интереса достоверно не лоцируется. УЗ признаки Bl. mam. sin. Мтс измененный аксиллярный лимфатический узел слева. Состояние после НАПХТ, положительная динамика от 03.07.19 г. в виде УЗ регресса образования левой молочной железы.
Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 09.07.19: Инвазивная карцинома молочной железы неспецифического типа, ядерный grade 2 (по Nottingham Histologic Score). ICD О code 8500/3.
• Заключение по иммуногистохимическому исследованию от 17.07.19: иммунофенотип люминальной типа В карциномы молочной железы HER2/neu позитивной.
Лечение: радикальная резекция левой молочной железы от 03.02.20. Результаты патогистологического исследования послеоперационного материала: При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 1,5×2
Наибольший размер инвазивного компонента опухоли (мм) - 2
Клеточность остаточной опухоли (%) - 1
Доля рака in situ в остаточной опухоли (%) - 100
Количество лимфатических узлов с метастазами (шт) - 0
Длина наибольшего метастаза в лимфатическом узле (мм) - 0
Для определения степени регресса опухоли использован калькулятор в Excel
Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии - I 0,702, минимальная остаточная опухоль. ypT1aNO (TNM AJCC 8th).
Пример №2.
Пациент: С.(Ж), 52 (1966 г.)
Диагноз при поступлении: С50.4 Рак правой молочной железы ycT4bN3M0, III С ст. Классический, her2 позитивный. Состояние после неоадьювантной химиотерапии по схеме: 4 АС+12 еженедельных введений Паклитаксела. В процессе таргетной терапии (Трастузумаб+Пертузумаб)., cT4bN3aM0, стадия IIIC, II кл. группа.
Состояние при поступлении в стационар
Жалобы при поступлении: на наличие образования в правой молочной железе. Анамнез болезни: считает себя больной с сентября 2018 г, когда при контрольном обследовании обнаружили конгломерат лимфоузлов в правой аксиллярной области, образование в правой молочной железе. Пациентка обследована в МКНЦ ДЦ «Клиника женского здоровья»: маммография, УЗИ молочных желез, трепан биопсия образования правой молочной железы, открытая биопсия подмышечного лимфоузла, ИГХ исследования. Установлен диагноз: рак правой молочной железы cT4bN3M0, III С ст.На первом этапе проведена неоадъювантная химиотерапия по схеме 4 АС+12 еженедельных введений Паклитаксела+таргетная терапия (Трастузумаб+Пертузумаб). Положительная динамика в виде уменьшения размеров опухоли и лимфатических узлов по данным УЗИ молочных желез и маммографии. На онкологическом консилиуме от 23.08.2019 с МКНЦ, на втором этапе рекомендовано проведение хирургического лечения в объеме радикальная мастэктомия по Маддену справа. Направлена в МКНЦ на хирургическое лечение.
Местный статус: молочные железы симметричные, кожные покровы бледно розовые, сосок и ареола без особенностей. При пальпации молочных желез узловые образования не определяются. Регионарные лимфатические узлы не пальпируются.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования: цитограмма рака.
• Протокол КТ от 18.03.19: Выраженная подмышечная лимфаденопатия (mts). Гиперденсные включения в молочных железах.
• Остеосцинтиграфия от 21.03.19: сцинтиграфических признаков вторичного поражения костей скелета не выявлено.
• Маммография от 15.08.19: Правая молочная железа: Структура ткани молочной железы неоднородная, с преобладанием железисто фиброзной и жировой ткани (ACR с тип строения молочной железы). В верхних квадрантах определяется участок асимметрии за счет более плотной ткани без четких контуров, примерным размером ~2,1 × 3,5 см (железистая доля). В верхненаружном квадранте в средней трети молочной железы определяется тень металлического маркера, узловое образование в этой зоне отчетливо не визуализируется. Визуализируются единичные кальцинаты и мелкие тени кистозного характера. Аксиллярные лимфатические узлы определяются размером до 0,8 × 1,0 см., в зоне ранее определяемого конгломерата лимфоузлов с кальцинатами в структуре определяется скопление кальцинатов и лимфоузел с кальцинатами в структуре частично в край снимка. Маммография от 09.01.20: в зоне ранее определяемого образования определяется участок уплотнения ткани без четких контуров, примерными размерами ~ 2,0 × 2,5 см. В проекции данного участка определяется тень металлической метки. Определяются единичные рассеянные кальцинаты и единичные группы кальцинатов. Аксиллярные лимфатические узлы не визуализируются, в видимой части аксиллярная область без особенностей. При сопоставлении с исследованием от 18.03.2019 г. отмечается положительная динамика в виде уменьшения аксиллярных лимфоузлов справа. BIRADS 6 МКБ: С50.4 Rg картина Bl.mam.dex. Mts аксиллярных лимфоузлов справа. Железистая доля? справа. УФКМ слева. Состояние после НАПХТ. Положительная динамика от 18.03.2019 г.
• Протокол УЗИ: BIRADS 5 справа.
Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 10.02.19: в пределах биоптата фрагменты ткани молочной железы с массивным солидным инфильтративным ростом рака неспецифического типа, G2 (3+3+1NGS), с выраженной интра и перитуморальной лимфоцитарной инфильтрацией, без достоверных признаков периневральной (PnO) и лимфоваскулярной (LV0) инвазии. Ткань лимфатического узла в пределах исследованного материала не определяется. Морфологическое заключение: Инфильтративный рак молочной железы неспецифического типа, G2.
• Заключение по иммуногистохимическому исследованию от 20.02.19: с целью определения молекулярного подтипа рака молочной железы проведено ИГХ исследование с антителами к ER, PR, Ki 67, Her2/Neu (Roche Ventana): ER -отрицательная реакция в клетках опухоли (0 баллов Allred Score), PgR -отрицательная реакция в клетках опухоли (0 баллов Allred Score), Ki67 - в 65% клеток опухоли, Her2/Neu - позитивная экспрессия (3+). Положительный контроль позитивный. Отрицательный контроль негативный. Иммуногистохимическое заключение: Молекулярный подтип рака Нелюминальный, HER2 позитивный. Лечение: Радикальная мастэктомия по Маддену справа от 27.08.19. Результаты патогистологического исследования послеоперационного материала: При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 16×15
Наибольший размер инвазивного компонента опухоли (мм) - 4
Клеточность остаточной опухоли (%) - 5
Доля рака in situ в остаточной опухоли (%) - 0
Количество лимфатических узлов с метастазами (шт) - 0
Длина наибольшего метастаза в лимфатическом узле (мм) - 0
Для определения степени регресса опухоли использован калькулятор в Excel Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии -1 1,34, минимальная остаточная опухоль. ypT1aNO (TNM AJCC 8th).
Пример №3.
Пациент: Н. (Ж), 54 (1968 г.)
Диагноз при поступлении: С50.4 Рак левой молочной железы ycT4bN1fM0, III В ст. Классический, Her2 позитивный. Состояние в процессе комбинированного лечения: неоадьювантной химиотерапии по схеме: 4 АС+12 еженедельных введений Паклитаксела, последнее введение от 04.09.2019 г. В процессе таргетной терапии (Перктзумаб+Трастузумаб)., cT4bN1M0, стадия IIIB, II кл. группа.
Состояние при поступлении в стационар
Жалобы при поступлении: на наличие образования в левой молочной железе.
Анамнез болезни: считает себя больной с апреля 2019 г, когда при контрольном обследовании обнаружили образование в левой молочной железе. Пациентка обследована в МКНЦ ДЦ «Клиника женского здоровья»: маммография, УЗИ молочных желез, трепан биопсия образования левой молочной железы, ТАБ лимфоузла, ИГХ исследования, установлен диагноз: Рак левой молочной железы cT4bN1fM0, III В ст.На первом этапе проведена неоадъювантная химиотерапия по схеме 4 АС+12 еженедельных введение Паклитаксела, последнее введение от 04.09.2019 г. В процессе таргетной терапии (Пертузумаб+Трастузумабом). Положительная динамика в виде уменьшения размеров по данным УЗИ молочных желез и маммографии. На онкологическом консилиуме от 17.09.2019 МКНЦ, на втором этапе рекомендовано проведение хирургического лечения в объеме радикальная мастэктомия по Маддену слева. Местный статус: молочные железы симметричные, D=S. При визуальном осмотре правая и левая молочные железы без особенностей. Направлена в МКНЦ на хирургическое лечение.
Местный статус: при пальпации в левой молочной железе в проекции нижненаружного квадранта пальпируется уплотнение ткани размерами 2,0 × 1,5 см. При пальпации в правой молочной железе узловых образований не обнаружено. Выделений из сосков нет. Регионарные лимфатические узлы справа и слева не пальпируются. На амбулаторном приеме от 29.03.2019 выявлен отек сосково-ареолярного комплекса слева.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования: цитограмма рака.
• Протокол КТ от 12.04.19: КТ картина новообразования левой молочной железы с левосторонней подмышечной лимфаденопатией. КТ признаков вторичного поражения легких, печени и костей не получено.
• Остеосцинтиграфия от 15.04.19: сцинтиграфических признаков вторичного поражения костей скелета не выявлено.
• Маммография от 09.09.19: Левая молочная железа: Кожа молочной железы слева утолщена до 0,3 см. Сосок слева отчетливо не визуализируется. Левая молочная железа: Структура ткани молочной железы неоднородная, с преобладанием железисто фиброзной и жировой ткани (ACR с тип строения молочной железы). Преимущественно на границе нижних квадрантов в среднем отделе молочной железы определяется тень металлического маркера. На этом фоне определяются множественные рассеянные разнокалиберные кальцинаты. В нижне внутреннем квадранте в средней трети железы сохраняется прежним размером участок очаговой асимметрии ткани без четких контуров. Визуализируются единичные мелкие тени кистозного характера. Аксиллярные лимфатические узлы не визуализируются, в видимой части аксиллярная область без особенностей. При сопоставлении с исследованием от 12.04.2019 г. отмечается незначительная положительная динамика в видеуменынения толщины кожи слева. BIRADS 6 слева МКБ: С50.9 Rg картина Bl.mam.sin.
• Протокол УЗИ: BIRADS 5 слева.
Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 16.03.19: В биоптатах ткани молочной железы - инфильтративный рост рака неспецифического типа, G3, со структурами внутрипротоковой карциномы, без достоверных признаков сосудистой (LV0) и периневральной (Pn0) инвазии. Морфологическое заключение: Инфильтративный рак молочной железы неспецифического типа, G3.
• Заключение по иммуногистохимическому исследованию от 25.03.19: Реакция опухолевых клеток с рецепторами прогестерона негативная: отсутствие экспрессии в 100% клеток опухоли, 0 баллов по Allred. Реакция опухолевых клеток с рецепторами белка HER2/neu: выраженное полное мембранное окрашивание в 10% клеток опухоли, 3 балла, сверхэкспрессия позитивная. Индекс Ki67 90%. Иммуногистохимическое заключение: Молекулярный подтип рака Нелюминальный, HER2 позитивный.
Лечение: Радикальная мастэктомия по Маддену слева от 19.09.19.
Результаты патогистологического исследования послеоперационного материала:
При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 15×10
Наибольший размер инвазивного компонента опухоли (мм) - 6
Клеточность остаточной опухоли (%) - 1
Доля рака in situ в остаточной опухоли (%) - 10
Количество лимфатических узлов с метастазами (шт) - 1
Длина наибольшего метастаза в лимфатическом узле (мм) - 2
Для определения степени регресса опухоли использован калькулятор в Excel Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии - II (1.754, умеренная остаточная опухоль). ypT1bN1mi (TNM AJCC 8th).
Пример №4.
Пациент: К. (Ж), 58 (1960 г.)
Диагноз при поступлении: С50.8 Рак левой молочной железы ycT2(m)N3fM0, III С ст. Люминальный В, her2 позитивный. Состояние после неоадьювантной химиотерапии по схеме 4 АС+12 еженедельных введений Паклитаксела+Пертузумаб+Трастузумаб, последнее введение от 10.09.2019 г.
Состояние при поступлении в стационар
Жалобы при поступлении: на наличие образования в левой молочной железе. Анамнез болезни: считает себя больной с марта 2019 г., когда при контрольном обследовании обнаружили образования в левой молочной железе. Пациентка обследована в МКНЦ ДЦ «Клиника женского здоровья»: маммография, УЗИ молочных желез, трепан-биопсия образований левой молочной железы, ТАБ лимфоузла, ИГХ исследования, установлен диагноз: Рак левой молочной железы cT2(m)N3fM0, III С ст.На первом этапе проведена неоадъювантная химиотерапия по схеме 4 АС+12 еженедельных введений Паклитаксела (последнее введение 10.09.2019 г.), в процессе таргетной терапии (Трастузумаб+Пертузумаб). Положительная динамика в виде уменьшения размеров по данным УЗИ молочных желез и маммографии. На онкологическом консилиуме от 20.09.2019 МКНЦ, на втором этапе рекомендовано проведение хирургического лечения в объеме радикальная мастэктомия по Маддену слева Направлена в МКНЦ на хирургическое лечение.
Местный статус: Молочные железы симметричные, D=S. Выделений из сосков нет. При пальпации молочных желез узловые образования четко не определяются. Регионарные лимфатические узлы не пальпируются.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования: цитограмма рака.
• Маммография от 17.09.19: В нижне-внутреннем квадранте в среднем отделе молочной железы в зоне ранее определяемого образования отчетливее в медиолатеральной проекции определяется участок перестройки структуры ткани размером ~1,1 × 1,2 × 1,4 см, так же в этой зоне определяется тень металлического маркера. При сопоставлении с исследованием от 22.03.2019 г. - положительная динамика в виде уменьшения образований слева в размере. BIRADS-6. Rg-картина BL.mam.sin. Состояние после ПХТ. Положительная динамика от 22.03.2019 г.
• Протокол УЗИ: BIRADS 6 слева. Мтс измененный аксиллярный л/узел слева Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 26.03.19: Столбчатые фрагменты ткани молочной железы с инвазивным ростом неспецифицированного рака молочной железы II степени по Ноттингемской системе (3+2+1) без достоверных признаков ангиолимфатической и периневральной инвазии. Морфологическое заключение: 8500/3 Инвазивный неспецифицированный рак левой молочной железы.
• Заключение по иммуногистохимическому исследованию от 11.04.19: Реакция клеток опухолевых клеток с рецепторами эстрогенов - положительная (7 баллов). Реакция опухолевых клеток с рецепторами прогестерона - отрицательная (0 баллов). Реакция опухолевых клеток с рецепторами белка Her-2-neu - положительная (3+). Индекс мечения Ki 67-35%. Иммуногистохимическое заключение: Иммунофенотип люминального типа В рака молочной железы, her-2 позитивного.
Лечение: Радикальная мастэктомия по Маддену слева от 30.09.2019.
Результаты патогистологического исследования послеоперационного материала:
При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 20×18
Наибольший размер инвазивного компонента опухоли (мм) - 4
Клеточность остаточной опухоли (%) - 10
Доля рака in situ в остаточной опухоли (%) - 0
Количество лимфатических узлов с метастазами (шт) - 15
Длина наибольшего метастаза в лимфатическом узле (мм) - 6
Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии - II (3,273, умеренная остаточная опухоль). ypT1aN3a. (TNM AJCC 8th).
Пример №5.
Пациент: М. (Ж), 33 (1985 г.)
Диагноз при поступлении: С50.4 Рак левой молочной железы IIB ст., ycT2N1fM0G2 Люминальный тип В Her-2-пеи-позитивный. Состояние после неоадьювантной химиотерапии врежиме 4 курсов Доксорубицин+циклофосфомид. Положительная динамика. Атезолизумаб+пертозумаб+герцептин+Трастузумаб. Положительная динамика. +12 введений паклитаксел, CT2N1M0, стадия IIB, II кл. группа.
Состояние при поступлении в стационар
Жалобы при поступлении: На наличие образования в левой молочной железе. Анамнез болезни: Считает себя больной с февраля 2019 года, когда по результатам инструментальных методов исследования обнаружили образование в левой молочной железе. Обратилась в поликлинику по месту пребывания, где выполнили обследование молочных желез в объеме: УЗИ и маммографии. Пациентке проведена неоадъювантная химиотерапия в режиме 4АС. В начале августа обратилась в МКНЦ ДЦ «Клиника женского здоровья», где выполнено комплексное обследование в объеме:
- Кт органов грудной клетки от 04.04.2019: КТ-картина образования левой молочной железы с регионарной лимфаденопатией. В феврале выполнена трепан-биопсия узлового образования левой молочной железы и ТАБ аксиллярного лимфатического узла слева. По результатам гистологического исследования от 20.02.2019: В биоптатах молочной железы
- инфильтративный рост рака, преимущественно микропапиллярного строения, G2. Имеются фокусы крайне подозрительные по принадлежности к лимфоваскулярной (LVX) инвазии. К гистологическому материалу выполнено иммуногистохимическое исследование от 25.02.2018: Молекулярный подтип рака Люминальный, HER2 статус неопределенный. Необходимо дополнительное исследование амплификации гена HER2 с использованием метода Гибридизации in situ (ISH). Выявлены множественные опухолевые эмболы в лимфатических капиллярах (LV1). По заключению SISH №28/19 от 18.03.2019: HER2-статус положительный. Цитологическое исследование пунктата узла аксиллярной области слева от 21.02.2019: Элементы крови, лимфоидные элементы разной степени зрелости, метастаз рака в лимфоузел. На основании комплексного обследования установлен диагноз: рак левой молочной железы ПВст.cT1cN1fM0G2. Люминальный тип В her-2-neu-позитивный. Пациентка обсуждена на онкологическом консилиуме МКНЦ, вторым этапом в рамках омс рекомендовано проведение хирургического лечения в объеме радикальной мастэктомии по Маддену слева. Направлена в МКНЦ на хирургическое лечение. Направлена в МКНЦ на хирургическое лечение.
Местный статус: Молочные железы симметричны D=S. При визуализации молочные железы без особенностей. Сосково-ареолярный комплекс визуально не изменен. Кожа над всей поверхности нормальной температуры. При глубокой пальпации левой молочной железы узловых образований не определяется. При пальпации аксиллярных областей без особенностей.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования: цитограмма рака.
• КТ от 04.04.19: На границе верхних квадрантов левой молочной железы ближе к ретроареолярной зоне определяется образование неправильной формы, размером 21×11×10 мм, неоднородно накапливающее контрастный препарат с 35-40 Н в НФ до 65-70 Н в ВФ и ОФ. В левой аксиллярной области определяются немногочисленные лимфатические узлы, размером до 10 мм, однородной структуры, неравномерно накапливающие КП с 40 Н до 80 Н.
• Остеосцинтиграфия от 03.04.19: сцинтиграфических признаков вторичного поражения костей скелета не выявлено.
• Маммография от 04.04.19: BIRADS-6 С50.8 Rg-картина Bl.mam.sin., (mts) аксиллярного лимфоузла слева. Протокол УЗИ: BIRADS 6 слева. Мтс измененный аксиллярный л/узел слева. На границе верхних квадрантов в среднем отделе молочной железы определяется тень образования неправильной формы с тяжистым контуром с плеоморфными кальцинатами в структуре, размером ~ 2,4 × 2,8 см. Определяются единичные разнокалиберные кальцинаты. Аксиллярные лимфатические узлы визуализируются уплотненный размером 1,4 × 1,8 см, в видимой части аксиллярная область без особенностей.
• УЗИ от 04.06.19: BIRADS-5. susp mts в аксиллярные л/у слева? Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 25.02.19: В биоптатах молочной железы - инфильтративный рост рака, преимущественно микропапиллярного строения, G2. Имеются фокусы крайне подозрительные по принадлежности к лимфоваскулярной (LVX) инвазии.
Заключение по иммуногистохимическому исследованию от 05.03.19: Молекулярный подтип рака Люминальный, HER2 статус неопределенный. Необходимо дополнительное исследование амплификации гена HER2 с использованием метода Гибридизации in situ (ISH). Выявлены множественные опухолевые эмболы в лимфатических капиллярах (LV1). Лечение: Радикальная мастэктомия по Маддену слева от 09.09.2019. Результаты патогистологического исследования послеоперационного материала: При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 35×27
Наибольший размер инвазивного компонента опухоли (мм) - 8
Клеточность остаточной опухоли (%) - 10
Доля рака in situ в остаточной опухоли (%) - 0
Количество лимфатических узлов с метастазами (шт) - 10
Длина наибольшего метастаза в лимфатическом узле (мм) - 5
Для определения степени регресса опухоли использован калькулятор в Excel
Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии - III (3,342, выраженная остаточная опухоль). ypT1bN3a. (TNM AJCC 8th).
Пример №6.
Пациент: X (Ж), 44 (1975 г.)
Диагноз при поступлении: С50.8 Рак левой молочной железы ycT4bN1M0 IIIB ст. Нелюминальный тип. Her2 позитивный иммунофенотип. Состояние после неоадьювантной полихимиотерапии 4 курса по схеме АС в режиме dose-dense+12 еженедельных введений паклитаксела +/- исследуемый препарат, последнее введение 15.08.2019 г., cT4bN1M0, стадия IIIB, II кл. группа.
Состояние при поступлении в стационар
Жалобы при поступлении: на наличие образования в левой молочной железе. Анамнез болезни: считает себя больной с января 2019 г., когда при обследовании обнаружили образование в левой молочной железе. Пациентка обследована в МКНЦ ДЦ "Клиника женского здоровья": маммография, УЗИ молочных желез, цитологическое исследование узлового образования левой молочной железы, трепан-биопсия узлового образования левой молочной желез, ИГХ исследования, установлен диагноз: Рак левой молочной железы, IIIB ст., cT4bN1M0 G2. Нелюминальный тип. Her-2 позитивный иммунофенотип. На первом этапе пациентка прошла 4 курса химиотерапии АС в режиме dose-dense, затем 12 введений паклитаксела, в еженедельном режиме +/- исследуемый препарат. Клинически отмечена положительная динамика в виде уменьшения размеров опухоли и лимфатического узла слева. На онкологическом консилиуме МКНЦ от 04.09.2019 г., на втором этапе рекомендовано проведение хирургического лечения в объеме: радикальная мастэктомия по Маддену слева. Направлена в МКНЦ на хирургическое лечение.
Местный статус: молочные железы не симметричные, D<S. Выделений из сосков нет. При пальпации молочных желез в левой молочной железе на границе внутренних квадрантов пальпируется узловое образование ~0,5×1,0 см с нечеткими контурами, плотной консистенции, подвижное. Сосок свободен. Кожа не изменена. В правой молочной железе узловые образования не определяются. Регионарные лимфатические узлы не пальпируются.
Результаты диагностических и инструментальных исследований:
• Цитологическое исследование л/у: метастаз рака в лимфоузел.
• Цитологическое исследование узлового образования: цитограмма рака.
• КТ от 27.03.19: В левой молочной железе в верхнем наружном квадранте, нечетко дифференцируется образование, ориентировочными размерами ~27×16 мм, с нечеткими контурами. Остеосцинтиграфия от 03.04.19: сцинтиграфических признаков вторичного поражения костей скелета не выявлено. КТ-картина образования левой молочной железы (по данным гистологического исследования -cr). Аксиллярная лимфаденопатия слева.
• Маммография от 26.03.19: Левая молочная железа: Структура ткани молочной железы неоднородная, с преобладанием фиброзно-жировой и отдельными включениями железистой ткани (ACR-b тип строения молочной железы). В ВНК в задней трети железы определяется участок очаговой асимметрии ткани без четких контуров по типу перестройки структуры с микроСа++, размером ~2,6 см в d. Аксиллярные лимфатические узлы не визуализируются, в видимой части аксиллярная область без особенностей. В зоне Зоргиуса справа тень накожного образования. BIRADS-6 (sin) BIRADS-3 (dex). Rg-картина BL. mam sin. Очаговая асимметрия ткани справа.
• Остеосцинтиграфия от 28.03.19: Сцинтиграфических признаков вторичного (mts) поражения костей скелета не выявлено.
Результаты патогистологических исследований биопсийного материала:
• Заключение по морфологическому исследованию от 19.02.19: фрагменты ткани молочной железы с разрастанием инвазивного рака неспецифического типа G2 с внутрипротоковым компонентом G2.
• Заключение по иммуногистохимическому исследованию от 26.02.19: Рецепторы эстрогенов 0%. рецепторы прогестерона 0%, HER2/neu 3+, Ki67 - 40%.
Лечение: Радикальная мастэктомия по Маддену слева от 06.09.2019. Результаты патогистологического исследования послеоперационного материала: При морфологическом исследовании послеоперационного образца с целью идентификации и исследования опухолевого ложа применялась рентгеновская система визуализации PathVision FAXITRON®. Плоскость максимального размера опухолевого ложа картирована в соответствие с цифровым изображением выбранного слайса слева-направо, сверху-вниз, исследована тотально. Применение цифровой рентгенографии при морфологическом исследовании послеоперационных образцов от больных раком молочной железы после проведенного неоадъювантного лечения позволило улучшить оценку степени патоморфологического регресса опухоли. За счет повышения видимости опухолевого ложа, облегчения идентификации размещенных в ложе опухоли металлических маркеров, микрокальцинатов и измененных очагов.
Оценка степени остаточной опухолевой нагрузки после неоадьювантной лекарственной терапии:
Размер наибольшей площади плоскости поперечного сечения опухолевого ложа (мм2) - 35×27.
Наибольший размер инвазивного компонента опухоли (мм) - 15
Клеточность остаточной опухоли (%) - 80
Доля рака in situ в остаточной опухоли (%) - 10
Количество лимфатических узлов с метастазами (шт) - 5
Длина наибольшего метастаза в лимфатическом узле (мм) - 10
Для определения степени регресса опухоли использован калькулятор в Excel
Патоморфологическое заключение: Степень регресса опухоли после неоадьювантной химиотерапии - III (4,248, выраженная остаточная опухоль). ypT1cN2a. (TNM AJCC 8th).
Способ основан на результатах проведенного ретро- и проспективного когортного исследования по теме «Морфологическая оценка ответа опухоли на неоадъювантное лечение с применением цифровой рентгенографии при раке молочной железы», выполненного на материале от 32 пациентов, проходивших лечение в Московском клиническом научном центре им. А.С. Логинова по поводу РМЖ за период с 2019 по 2020 год. Цель изобретения - повышение точности оценки регресса рака молочной железы на неодъювантную терапию достигнут за счет количественной оценки степени регресса опухоли.
Источники информации
1. Bossuyt V., Provenzano E., Symmans W.F., Boughey J.C., Coles C, Curiglianoet G. et al. Recommendation forstandardized pathological characterization of residual disease for neoadjuvant clinical trials of breast cancer by the BIG-NAB CG collaboration. Ann. Oncol. 2015; 26(7): 1280-1291
2. Fayanju O.M., Ren Y., Thomas S.M., Greenup R.A., Plichta J.K., Rosenberger L.H. at el. The Clinical Significance of Breast-only and Node-only Pathologic Complete Response (PCR) After Neoadjuvant Chemotherapy (NA CT): A Review of 20,000 Breast Cancer Patients in the National Cancer Data Base (NCDB). Ann Surg. 2018; 268(4): 591-601
3. Tyulyadin S.A. The value of preoperative chemotherapy in patients with breast cancer. IV Russian oncology conference. M.; 2000
4. Rapoport B.L., Demetriou G.S., Moodley S.D., Benn C.A. When and How Do I Use Neoadjuvant Chemotherapy for Breast Cancer? // Current Treatment Options in Oncology. 2014; 15: 86-98. Doi: 10.1007/s11864-013-0266-0
5. Bossuyt V., Provenzano E., Symmans W.F., Boughey J.C., Coles C, Curiglianoet G. et al. Recommendation for standardized pathological characterization of residual disease for neoadjuvant clinical trials of breast cancer by the BIG-NABCG collaboration. Ann.Oncol. 2015; 26(7): 1280-1291
6. Campbell J.I., Yau C, Krass P., Moore D., Carey L.A., Au A., et al. Comparison of residual cancer burden, American Joint Committee on Cancer staging and pathologic complete response in breast cancer after neoadjuvant chemotherapy: results from the I-SPY 1 TRIAL (CALGB 150007/150012; ACRIN 6657). Breast Cancer Res. Treat. 2017; 165: 181-191. Doi: 10.1007/sl0549-017-4303-8
7. Andreeva Yu.Yu., Moskvina L.V., Berezina T.A., Podberezina Yu.L., Loktev S.S., Frank G.A. Procedure for intraoperative material examination in breast cancer after neoadjuvant therapy to estimate residual cancer burden using the RCB system. Arkh Patol. 2016; 78(2): 41-46. Doi: 10.17116/patol201678241-46
8. Maker W., Holtschmidt J., Thangarajah F., Mallmann P., Krug В., Warm M. et al. First Reported Use of the Faxitron LOCalizer™ Radiofrequency Identification (RFID) System in Europe - A Feasibility Trial, Surgical Guide and Review for Non-palpable Breast Lesions. In Vivo. 2019; 33(5): 1559-1564. Doi: 10.21873/invivo.11637.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения болевого синдрома при постмастэктомическом синдроме | 2022 |
|
RU2806297C1 |
| СПОСОБ ОЦЕНКИ ГИСТОЛОГИЧЕСКОГО МАТЕРИАЛА, ПОЛУЧЕННОГО ПРИ ИСПОЛЬЗОВАНИИ ВАКУУМ-АССИСТИРОВАННОЙ БИОПСИИ ДЛЯ УДАЛЕНИЯ ЛОЖА ОПУХОЛИ У ПАЦИЕНТОВ С ДИАГНОЗОМ РАК МОЛОЧНОЙ ЖЕЛЕЗЫ HER2-ПОЗИТИВНОГО ИЛИ ТРИЖДЫ НЕГАТИВНОГО ПОДТИПА ПОСЛЕ НЕОАДЪЮВАНТНОЙ СИСТЕМНОЙ ТЕРАПИИ | 2023 |
|
RU2824957C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОРГАНОСОХРАНЯЮЩЕЙ ОПЕРАЦИИ ПУТЕМ ВАКУУМ-АССИСТИРОВАННОЙ БИОПСИИ ЛОЖА ОПУХОЛИ МОЛОЧНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПРОВЕДЕННОЙ НЕОАДЪЮВАНТНОЙ ХИМИОТЕРАПИИ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ HER2-ЗАВИСИМОГО ИЛИ ТРИЖДЫ НЕГАТИВНОГО ПОДТИПА | 2023 |
|
RU2810795C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С BRCA-АССОЦИИРОВАННЫМ ТРИЖДЫ НЕГАТИВНЫМ МЕСТНОРАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2814578C1 |
| Способ прогнозирования гематогенного метастазирования при инвазивной карциноме неспецифического типа молочной железы у пациенток с хорошим ответом на неоадъювантную химиотерапию | 2016 |
|
RU2627649C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ОЦЕНКИ ДОСТАТОЧНОСТИ ОБЪЕМА РЕЗЕКЦИИ ПРИ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЯХ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2023 |
|
RU2819490C1 |
| Способ прогнозирования риска лимфогенного метастазирования при раке молочной железы на основе экспрессии гена белка YKL-39 | 2016 |
|
RU2632115C1 |
| Способ прогнозирования безметастатической выживаемости у больных раком молочной железы на основе экспрессии генов сомато-стволового перехода в резидуальной опухоли после предоперационной терапии | 2018 |
|
RU2682879C1 |
| Способ прогнозирования гематогенного метастазирования при инвазивной карциноме неспецифического типа молочной железы у пациенток с плохим ответом на неоадъювантную химиотерапию | 2016 |
|
RU2623150C1 |
| Способ отсроченной препекторальной реконструкции после мастэктомии при раке молочной железы с помощью перманентного имплантата | 2024 |
|
RU2831000C1 |



Изобретение относится к медицине, а именно к патологической анатомии и онкологии, и может быть использовано для диагностики регресса рака молочной железы (РМЖ) после неоадъювантной лекарственной терапии. Для этого проводят рентгенографическое исследование ткани опухоли. Оценивают размеры наибольшей площади плоскости поперечного сечения рентген-позитивного ложа. Выполняют серийные срезы для изготовления гистологических препаратов с одновременным цифровым картированием ложа и маркировкой гистологическими красителями. Определяют процент карциномы in situ, число лимфатических узлов с метастазами, размер наибольшего метастаза. Рассчитывают индекс регресса опухоли по формуле: 1,4×(fивн×dпо)0,17+[4×(1-0,75ЛУ)×dмет]0,17, 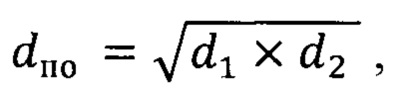 где d1, d2 - микроскопические размеры ложа опухоли, dпо - наибольшая площадь плоскости поперечного сечения рентген-позитивного ложа первичной опухоли.
где d1, d2 - микроскопические размеры ложа опухоли, dпо - наибольшая площадь плоскости поперечного сечения рентген-позитивного ложа первичной опухоли. 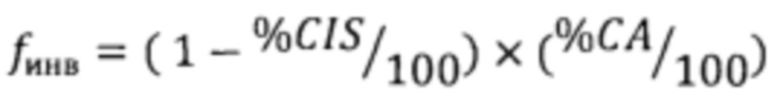 - выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли, ЛУ - число лимфатических узлов с метастазами, dмет - наибольший диаметр метастаза в лимфатическом узле. Результатом вычислений является класс регресса опухоли, ранжированный от I до III: I минимальная остаточная опухоль, индекс менее 1,36; II умеренная остаточная опухоль, индекс 1,37-3,28; III выраженная остаточная опухоль, индекс 3,29 и более. Изобретение обеспечивает повышение точности определения количественных и качественных показателей ложа опухоли, необходимых для оценки степени патоморфологического регресса рака молочной железы в ответ на лечение. 6 пр., 4 ил.
- выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли, ЛУ - число лимфатических узлов с метастазами, dмет - наибольший диаметр метастаза в лимфатическом узле. Результатом вычислений является класс регресса опухоли, ранжированный от I до III: I минимальная остаточная опухоль, индекс менее 1,36; II умеренная остаточная опухоль, индекс 1,37-3,28; III выраженная остаточная опухоль, индекс 3,29 и более. Изобретение обеспечивает повышение точности определения количественных и качественных показателей ложа опухоли, необходимых для оценки степени патоморфологического регресса рака молочной железы в ответ на лечение. 6 пр., 4 ил.
Способ диагностики регресса рака молочной железы после неоадъювантной лекарственной терапии, включающий рентгенографию, отличающийся тем, что дополнительно оценивают размеры наибольшей площади плоскости поперечного сечения рентген-позитивного ложа, выполняют серийные срезы для изготовления гистологических препаратов с одновременным цифровым картированием ложа и маркировкой гистологическими красителями, получением процента карциногмы in situ, числа лимфатических узлов с метастазами и размера наибольшего метастаза с последующим расчетом индекса регресса опухоли по формуле:
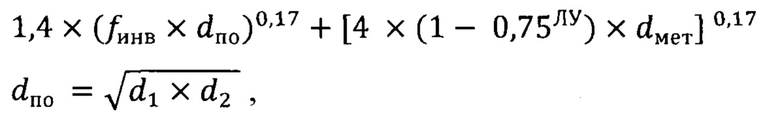
где d1, d2 - микроскопические размеры ложа опухоли, dпо - наибольшая площадь плоскости поперечного сечения рентген-позитивного ложа первичной опухоли;
 - выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
- выраженность инвазивного компонента, рассчитанная на основании процента карциномы in situ (CIS) инвазивного рака (СА) в опухоли,
ЛУ - число лимфатических узлов с метастазами,
dмет - наибольший диаметр метастаза в лимфатическом узле, при этом результатом вычислений является класс регресса опухоли, ранжированный от I до III:
I минимальная остаточная опухоль, индекс менее 1,36;
II умеренная остаточная опухоль, индекс 1,37-3,28;
III выраженная остаточная опухоль, индекс более 3,29.
| Способ определения прогноза эффективности терапии рака молочной железы | 2021 |
|
RU2757590C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ МЕСТНЫХ РЕЦИДИВОВ В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ У БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2020 |
|
RU2734719C1 |
| Прибор для определения в сыпучих материалах объемного содержания зерен разной крупности | 1930 |
|
SU21486A1 |
| WO 2014074785 A1, 15.05.2014 | |||
| АНДРЕЕВА Ю.Ю | |||
| и др | |||
| Методика исследования операционного материала при раке молочной железы после неоадъювантной терапии для оценки остаточной опухолевой нагрузки (по системе RCB) | |||
| Архив патологии | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| HAN D | |||
| et al | |||
Авторы
Даты
2023-10-30—Публикация
2022-06-23—Подача