Область техники, к которой относится изобретение
Изобретение относится к области медицины, а именно - эндоскопии, пульмонологии и фтизиатрии, и может быть использовано для быстрого и эффективного заживления полостных образований в легком с поражением их внутренней стенки хроническим легочным микозом (аспергиллезом).
Уровень техники
Хронический микоз легких, чаще всего в виде хронического легочного аспергиллеза (ХЛА) (Chronic pulmonary aspergillosis (CPA)) распространен во всем мире и нередко является осложнением других острых и хронических заболеваний легких [Maghrabi F, Denning DW. The Management of Chronic Pulmonary Aspergillosis: The UK National Aspergillosis Centre Approach. Curr Fungal Infect Rep. 2017;11(4):242-251. Epub 2017 Nov 13. PubMed PMID: 29213345; PubMed Central PMCID: PMC5705730].
Так аспергиллезом могут поражаться полостные образования в легких, появившиеся в результате другого инфекционного заболевания, часто туберкулеза. Конидии гриба прорастают и образуют сеть гифов на внутренней поверхности полости, повреждая окружающую паренхиму [Latgé J-P. Aspergillus fumigatus, a saprotrophic pathogenic fungus. Mycologist. 2003;17(2):56-61. doi: 10.1017/S0269915X0300209X]. У некоторых пациентов рост грибов в полости прогрессирует до образования «грибкового тела» - аспергиллемы (мицетомы), которая препятствует заживлению полостного образования, даже если предыдущий процесс благоприятно закончился. При этом у пациентов могут наблюдаться различные респираторные и конституциональные симптомы: одышка, хронический кашель, выделение мокроты, дискомфорт в груди, потеря массы тела, усталость и быстрая утомляемость [Godet C, Laurent F, Beraud G., et al. Phenotyping chronic pulmonary aspergillosis by cluster analysis. Eur Respir J. 2015;46(5):1509-1512. doi: 10.1183/13993003.00869-2015; Denning DW, Riniotis K, Dobrashian R, Sambatakou H. Chronic cavitary and fibrosing pulmonary and pleural aspergillosis: case series, proposed nomenclature change, and review. Clin Infect Dis. 2003;37(Suppl 3(s3)):S265-S280. doi: 10.1086/376526; Al-Shair K, Muldoon EG, Morris J, Atherton GT, Kosmidis C, Denning DW. Characterisation of fatigue and its substantial impact on health status in a large cohort of patients with chronic pulmonary aspergillosis (CPA) Respir Med. 2016;114:117-122. doi: 10.1016/j.rmed.2016.03.020]. У пациентов с ХЛА также нередко наблюдаются повторяющиеся кровохарканья и даже угрожающие жизни кровотечения (>150 мл/сут), что является основной причиной летальности при ХЛА [Betancourt BY, Garofoli AC, Sandhu JS, Boma N, Sy AM. Pulmonary aspergillosis presenting with recurrent haemoptysis. BMJ Case Rep. 2015:bcr2015211249. doi:10.1136/bcr-2015-211249; Farid S, Mohamed S, Devbhandari M, et al. Results of surgery for chronic pulmonary Aspergillosis, optimal antifungal therapy and proposed high risk factors for recurrence. National Centre’s experience. J Cardiothorac Surg. 2013;8:180. Published 2013 Aug 5. doi:10.1186/1749-8090-8-180]. Все вышеперечисленное обуславливает необходимость лечения данной патологии.
Основным методом лечения ХЛА является системное применение различных противогрибковых препаратов с длительностью курса 4-12 месяцев, часто сопровождающимся проявлениями токсичности препаратов, непереносимостью их пациентом, особенно при взаимодействии с лекарственными средствами, назначаемыми при сопутствующей патологии [David W. Denning, Jacques Cadranel, Catherine Beigelman-Aubry, Florence Ader, Arunaloke Chakrabarti, Stijn Blot, Andrew J. Ullmann, George Dimopoulos, Christoph. Chronic pulmonary aspergillosis: rationale and clinical guidelines for diagnosis and management. Lange on behalf of the European Society for Clinical Microbiology and Infectious Diseases and European Respiratory Society European Respiratory Journal 2016 47: 45-68; DOI: 10.1183/13993003.00583-2015].
Группа исследователей установила, что препараты итраконазол и вориконазол умеренно эффективны при ХЛА, если они назначаются в течение 12 месяцев (доза вориконазола в среднем 400 мг/сут (от 200-500 мг), при этом менее чем у 50% пациентов удается осуществить терапию такой длительности. Нежелательные явления более чем у трети пациентов являются причиной прекращения терапии [Bongomin F, Harris C, Hayes G, Kosmidis C, Denning DW. Twelve-month clinical outcomes of 206 patients with chronic pulmonary aspergillosis. PLoS One. 2018 Apr 10;13(4):e0193732. doi: 10.1371/journal.pone.0193732. eCollection 2018]. Нежелательные реакции при лечении азолами являются общими, включая периферическую невропатию, сердечную недостаточность, повышенные печеночные ферменты, удлинение интервала QTc, фиксируемое при электрокардиографии.
В случае неэффективности консервативного лечения методом выбора в настоящий момент является хирургическое лечение - резекция легкого различного объема. [David W. Denning, Jacques Cadranel, Catherine Beigelman-Aubry, Florence Ader, Arunaloke Chakrabarti, Stijn Blot, Andrew J. Ullmann, George Dimopoulos, Christoph. Chronic pulmonary aspergillosis: rationale and clinical guidelines for diagnosis and management. Lange on behalf of the European Society for Clinical Microbiology and Infectious Diseases and European Respiratory Society European Respiratory Journal 2016 47: 45-68; DOI: 10.1183/13993003.00583-2015]. При этом хирургическое лечение связано с риском таких осложнений, как неэффективность аэростаза, раневая инфекция, возникновение остаточной плевральной полости, развитие эмпиемы плевры и бронхоплевральных свищей [Kim YT, Kang MC, Sung SW, et al. Good long-term outcomes after surgical treatment of simple and complex pulmonary aspergilloma. Ann Thorac Surg 2005; 79: 294-298.; Akbari JG, Varma PK, Neema PK, et al. Clinical profile and surgical outcome for pulmonary aspergilloma: a single center experience. Ann Thorac Surg 2005; 80: 1067-1072.]. И только при невозможности применения хирургического лечения по разным причинам рекомендуются иные методы.
В литературе описаны методы лечения ХЛА (в виде аспергиллемы внутри полостного образования легких) при его осложнении кровотечением с применением местного введения противогрибковых препаратов и/или кровоостанавливающих средств [Rumbak M, Kohler G, Eastrige C, et al. Topical treatment of life threatening haemoptysis from aspergillomas. Thorax 1996; 51:253-255].
Использовались такие противогрибковые препараты, как амфотерицин В, нистатин, препараты группы триазолов. Доставка в бронхиальное дерево раствора препарата проводилась во время бронхоскопии по катетеру, введенному в бронх, редко в пораженную полость [Yamada H, Kohno S, Koga H, et al. Topical treatment of pulmonary aspergilloma by antifungals: relationship between duration of the disease and efficacy of therapy. Chest 1993; 103: 1421-1425; David W. Denning, Jacques Cadranel, Catherine Beigelman-Aubry, Florence Ader, Arunaloke Chakrabarti, Stijn Blot, Andrew J. Ullmann, George Dimopoulos, Christoph. Chronic pulmonary aspergillosis: rationale and clinical guidelines for diagnosis and management. Lange on behalf of the European Society for Clinical Microbiology and Infectious Diseases and European Respiratory Society European Respiratory Journal 2016 47: 45-68; DOI: 10.1183/13993003.00583-2015]. Недостатком данного метода является неизбежный частичный рефлюкс лекарственного средства из места введения в более крупные бронхи, что не может предотвратить даже специальное позиционирование пациента. Постоянные дыхательные движения, мукоцилиарный клиренс, изменение положения тела пациента приводят к резкому уменьшению концентрации препарата и его экспозиции в очаге грибковой инфекции. Концентрация кислорода во вдыхаемом воздухе также способствует инактивации введенного препарата. Такое введение лекарственного средства в приведенных источниках проводили курсами 1-5 раз до прекращения легочного кровотечения, при этом не анализировалось разрушение аспергиллемы и заживление полости ее содержавшей.
Известен способ чрескожного внутриполостного введения противогрибковых препаратов по катетеру для лечения аспергиллемы, расположенной в полостном образовании легкого. Под местной анестезией при рентгенологическом контроле игла через грудную стенку и легочную ткань вводится в полость, через эту иглу проводится катетер, затем игла удаляется. Через такой катетер многократно вводился противогрибковый препарат [Jackson M, Flower CD, Shneerson JM. Treatment of symptomatic pulmonary aspergillomas with intracavitary instillation of amphotericin B through an indwelling catheter. Thorax 1993; 48: 928-930.; Munk PL, Vellet AD, Rankin RN, et al. Intracavitary aspergilloma: transthoracic percutaneous injection of amphotericin gelatin solution. Radiology 1993; 188: 821-823.]. Введение препарат продолжали до прекращения кровотечения (кровохарканья). Сообщено, что рецидив серьезного кровохарканья произошел в 6 случаях из 18. К недостаткам метода следует отнести: невозможность длительного (несколько недель) использования чрескожного катетера из-за высокой вероятности инфицирования его, вероятно по этой причине нет данных по заживлению полостей; при введении лекарства через катетер в полость значительная часть его попадает в дыхательные пути через дренирующий бронх, что манифестируется возникновением кашля при введении; чрескожная установка катетера в полость невозможна при малых размерах полости или глубоком ее расположении по отношению к грудной стенке; при установке чрескожного катетера возможны осложнения - особенно часто, пневмоторакс (до 26% случаев [Shapiro MJ, Albelda SM, Mayock RL, et al. Severe hemoptysis associated with pulmonary aspergilloma: percutaneous intracavitary treatment. Chest 1988; 94: 1225-1231]).
Имеются сообщения, что для повышения концентрации препарата в полость по чрескожному катетеру вводили пасту с амфотерицином, при этом у 26 из 40 пациентов рентгенологически исчезла аспергиллема, а у 3 (7,5%) зажила и полость [Giron J, Poey C, Fajadet P, et al. CT-guided percutaneous treatment of inoperable pulmonary aspergillomas: a study of 40 cases. Eur J Radiol 1998; 28: 235-242]. Авторам удалось путем изменения консистенции препарата преодолеть потерю его концентрации, но частота заживления полости, пораженной аспергиллемой, составила всего 7,5%. Сохранение же полости это возможность рецидива аспергиллемы.
Известен способ эндоскопического удаления внутриполостной аспергиллемы легкого при помощи ригидной и гибкой бронхоскопии [Stather DR, Tremblay A, MacEachern P., et al., Bronchoscopic removal of a large intracavitary pulmonary aspergilloma. Chest 2013; 143: 238-241; Stather D, Tremblay A, MacEachern P., et al., Intracavitary pulmonary aspergilloma removal using combined virtual, ultrathin, and rigid bronchoscopy-a case series. Chest 2013; 144: 817A.]. Однако данный способ применим только для больших полостей с аспергиллемами, имеющих крупный дренирующий бронх, метод требует использования дорогостоящего оборудования (несколько видов бронхоскопов, включая ультратонкий), применение наркоза и искусственной вентиляции легких, и связан с риском развития осложнений - прежде всего кровотечения.
Установка в бронх специально разработанного эндобронхиального клапана, создающего локальный коллапс пораженного участка легких успешно применяется для остановки легочных кровотечений и заживления полостей при деструктивных формах туберкулеза легких [Левин А.В., Цеймах Е.А., Зимонин П.Е. и др. Применение клапанной бронхоблокации в комплексном лечении больных распространённым деструктивным туберкулёзом лёгких, осложнённым лёгочным кровотечением//Пробл. туб. -2007. -№ 9. -С. 13-16; Levin, A., Sklyuev, S., Felker, I.; Tceymach, E., Krasnov, D. Endobronchial valve treatment of destructive multidrug-resistant tuberculosis The International Journal of Tuberculosis and Lung Disease, 2016, 20:1539-1545]. Однако, случаев успешного применения эндобронхиального клапана при внутриполостной мицетоме, развившейся в полости, образовавшейся в результате иного заболевания, в том числе туберкулеза в литературе не описано.
Раскрытие изобретения
Способ лечения полостей распада в легком, осложненных хроническим аспергиллезом, заключается в том, что после проведения диагностической бронхоскопии для оценки состояния бронхов в пораженной области с одновременным взятием бронхиальных смывов для определения лекарственной чувствительности и при отсутствии противопоказаний при повторной фибробронхоскопии устанавливается эндобронхиальный клапан в долевой или сегментарный бронх, вентилирующий участок легкого, в котором находится полость с мицетомой, затем между стенкой эндобронхиального клапана и стенкой бронха, в который установлен клапан, проводится тонкий пластиковый катетер до выхода дистального конца катетера за пределы клапана и по нему вводится водный раствор противогрибкового лекарственного препарата для внутривенного введения, содержащий разовую дозу препарата, после чего катетер освобождается от раствора введением воды для инъекций, а затем катетер извлекают в канал фибробронхоскопа и вместе с ним из дыхательных путей. При этом введение противогрибкового лекарственного препарата предпочтительно проводить сразу после установки эндобронхиального клапана, а повторную фибробронхоскопию проводят через 3-5 дней после проведения диагностической фибробронхоскопии. В качестве противогрибкового лекарственного препарата используют препарат, к которому установлена чувствительность гриба при выполнении диагностической бронхоскопии. Предпочтительно в качестве противогрибкового лекарственного препарата использовать вориконазол в дозе 200 мг, а для освобождения просвета катетера от препарата вводят 1-2 мл воды для инъекций.
Заявляемый способ имеет следующие преимущества:
1. Установка эндобронхиального клапана, уменьшает объем и воздушность пораженного сегмента или доли легкого, уменьшая в нем активность дыхательных движений, и не позволяет препарату вытекать из пораженного участка легкого, все это способствует высокой концентрации лекарственного препарата в зоне поражения. К тому же в коллабированном участке легкого препарат до всасывания соприкасается с воздухом с пониженным содержанием кислорода, что замедляет его окисление и потерю активности.
2. Способ является малоинвазивным и может проводиться под местной анестезией. Нет риска пневмоторакса и других осложнений, возможных при хирургическом лечении и при установке чрескожного катетера. Нет нарушения целостности и структуры легкого, как при резекционных операциях.
3. Не обязательно точное попадание инструментом (катетером) в полостное образование с мицетомой, это делает наш метод пригодным для лечения полостей любых размеров, в том числе маленьких и расположенных в любых отделах легкого. Как правило, хватает однократного введения препарата в разовой дозе, но при отсутствии рентгенологического эффекта через 2 месяца введение препарата можно повторить, используя уже установленный ЭК.
4. Не требуется ежедневных вливаний антимикотических препаратов, что позволяет избежать нежелательных реакций и лекарственных взаимодействий, возникающих при его системном (внутривенном) ежедневном многомесячном применении. Не требует от пациента длительного времени для многократного приема капельных вливаний. Практически не ограничивается активность пациента, лечение может осуществляться амбулаторно.
5. Резко снижаются материальные затраты на лечение мицетомы - минимизируется общая доза необходимого на курс лечения препарата до 1 разовой дозы, введенной однократно.
6. Способ является комплексным, так как разрушает мицетому (действие препарата в улучшенных условиях для соблюдения дозировки и воздействия на мицетому) и способствует заживлению полости (коллапсотерапия под длительным воздействием эндобронхиального клапана), исключая возможность рецидива гриба в сохранившейся полости.
Очистившаяся от мицетомы полость может заживать до 4-6 месяцев, однако все это время пациенту не требуется стационарное лечение и не требуется введение противогрибковых препаратов. Также не наблюдается нежелательных явлений на введение противогрибковых препаратов из-за разовости их введения. Пробу на аллергические реакции на препарат пациентам делают до его введения, нанося препарат на слизистую губы.
Краткое описание чертежей
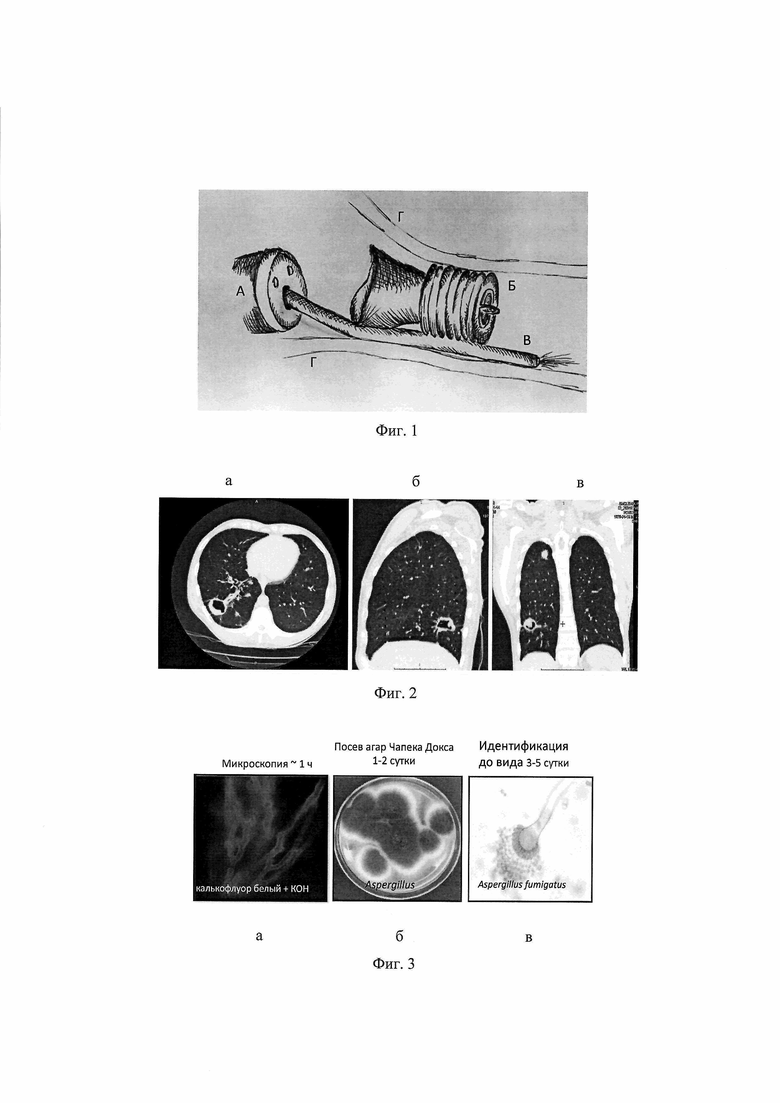
На фиг. 1 показана схема введения противогрибкового препарата в бронх дистальнее установленного эндобронхиального клапана, где А - дистальный конец фибробронхоскопа; Б - эндобронхиальный клапан (ЭК); В - катетер введенный в канал фибробронхоскопа, а затем проведенный между ЭК и стенкой бронха, через него вводится лекарственный раствор; Г - стенка бронха.
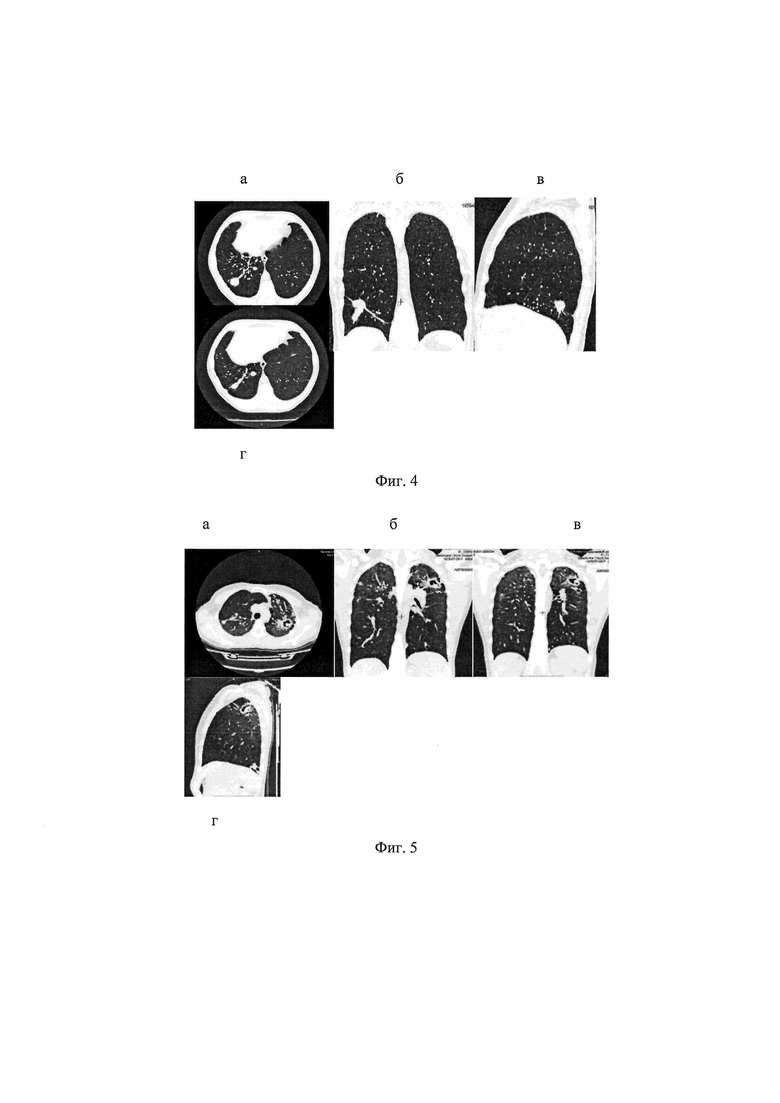
На фиг. 2 представлены данные пациента Н. - МСКТ ОГК (а) реконструкции б - сагиттальная и в - фронтальная на момент поступления в ФГБУ «НМИЦ ФПИ» Минздрава России. В С10 правого легкого определялся фокус с неровными тяжистыми контурами размером 37×37×27 мм с полостью распада 28×35×17 мм, в просвете которой определялась округлая тень, характерная для аспергиллемы.
На фиг. 3 представлены фотографии методов исследования бронхиального смыва пациента Н. на грибы и длительность от начала исследования до готовности результата: а - результат микроскопии (длительность 1 час), б - фото роста гриба Aspergillus на агаре Чапека Докса (длительность 1-2 суток), в - идентификация Aspergillus fumigatus до вида (длительность 3-5 суток).
На фиг. 4 представлены данные пациента Н. - МСКТ ОГК (а) и реконструкции б - фронтальная и в - сагиттальная перед удалением эндобронхиального клапана - заживление мицетомы очагом.
На фиг. 5 представлены данные пациентки В. МСКТ ОГК и реконструкции б, в - фронтальные и г - сагиттальная при поступлении в ФГБУ «НМИЦ ФПИ» МИНЗДРАВА РОССИИ. Мицетома С-2 левого легкого, постуберкулезные очаги в правом и левом легких.
На фиг. 6 представлены данные пациентки В после применения метода лечения мицетомы. МСКТ ОГК (а) и фронтальная реконструкция (б) - сегменты С-1-2 и 3 левого легкого находятся в ателектазе. Мицетома не определяется. На сагиттальной реконструкции (в) в просвете левого главного бронха (указано стрелкой) видна хвостовая часть эндобронхиального клапана, которая указана стрелкой на увеличенном фрагменте (г).
На фиг. 7 представлены данные пациентки В. отдаленный результат после успешного завершения лечения мицетомы и удаления ЭК. МСКТ ОГК (а), сагиттальная реконструкция (б) и фронтальная реконструкция (в) - после лечения мицетомы: верхняя доля левого легкого расправлена, полостное образование с мицетомой не определяется, на его месте крупный плотный очаг, в легких множественные плотные посттуберкулезные очаги.
На фиг. 8 представлены результаты проведения КТ исследования пациента Н. до (А) - полость с неровной внутренней поверхностью и (Б) через 4 мес после установки ЭК 11.09.19 - сегменты в ателектазе, полость с мицетомой уменьшилась, но не закрылась.
На фиг. 9 представлены результаты проведения фронтального КТ исследования пациента Н. до (А) - полость с неровной внутренней поверхностью и (Б) после установки ЭК 11.09.19 - сегменты в ателектазе, полость с мицетомой уменьшилась, но не закрылась.
Осуществление изобретения
Диагностика внутриполостной аспергиллемы (мицетомы) происходит при рентгенологическом исследовании (как правило, МСКТ ОГК (мультисрезовая компьютерная томография органов грудной клетки) - иногда патология имеет характерный вид, в виде округлого образования, заполняющего полость - синдром «погремушки», но чаще - это участки утолщенной внутренней оболочки полости, выступающие в ее просвет. При этом определяется точная топика полостного образования - до сегмента. У таких пациентов определение наличия патогенного гриба осуществляется при микологическом исследовании: в основном (особенно при небольших размерах полости) из бронхиального смыва пораженного сегмента легкого, полученного при бронхоскопии, редко мокроты (редко). При микологическом исследовании определяется не только наличие грибковой инвазии, но и лекарственная чувствительность гриба. Любой из препаратов, к которому сохранена чувствительность и имеется лекарственная форма для внутривенного введения, может быть использован. Как правило, это препарат - вориконазол лиофилизат для внутривенного введения. При бронхоскопии также оценивается состояние бронха, на предмет возможности установка клапанного бронхоблокатора.
При отсутствии изменений бронха, препятствующих установке эндобронхиального клапана (выраженная деформация, наличие воспалительного процесса на его слизистой) и получении данных о наличии инвазии гриба и его лекарственной чувствительности применяется предлагаемый способ лечения.
При фибробронхоскопии (как правило, - это фибробронхоскопия под местной анестезией, но, по показаниям, может использоваться наркоз, а также жесткая бронхоскопия под наркозом) устанавливается эндобронхиальный клапан (ЭК) (методика разрешена МЗ РФ к использованию [Ловачева О.В., Елькин А.В., Зимонин П.Е., Краснов Д.В., Краснов В.А., Левин А.В., Склюев С.В., Скорняков С.Н., Степанов Д.В., Цеймах Е.А., Шумская И.Ю. Федеральные клинические рекомендации по использованию метода клапанной бронхоблокации в лечении туберкулеза легких и его осложнений. Издательство «Нью-Терра». - Москва. - 2015. - с. 24 http://roftb.ru/netcat_files/doks2015/rec7.pdf]). Эндобронхиальный клапан устанавливали в долевой или сегментарный бронх, вентилирующий участок легкого, в котором находится полость с мицетомой. ЭК - это устройство, позволяющее воздуху, бронхиальному содержимому при кашле выходить из блокированного участка, но препятствующее поступлению воздуха на вдохе в блокированный участок. В РФ зарегистрирован и разрешен для использования ЭК фирмы «Медланг» РФ.
После установки эндобронхиального клапана (ЭК) можно сразу после его установки вводить водный раствор антигрибкового препарата, а лучше через 3-5 дней, когда заблокированный участок легкого снизит свою воздушность, соответственно, объем, участие в дыхательной функции, а ЭК плотно за счет отека слизистой зафиксируется в бронхе и пациент привыкнет к своему состоянию и не будет кашлять, проводить повторную бронхоскопию. Для введения антигрибкового препарата между эндобронхиальным клапаном и стенкой бронха, его охватывающей, проводится тонкий пластиковый катетер до выхода дистального конца катетера за пределы клапана в дистальные бронхи (фиг. 1), что легко контролируется по длине части катетера, заведенной параллельно головной части ЭК, длина которой известна. По катетеру медленно вводится 10 мл раствора лекарственного препарата для внутривенного введения (к которому установлена чувствительность гриба), содержащего одну разовую дозу препарата (для вориконазола лиофилизата это 200 мг растворенных в воде для инъекций). После завершения введения препарата в катетер вводят еще 1-2 мл воды для инъекций, чтобы освободить просвет катетера от препарата (это зависит от объема жидкости необходимой для заполнения катетера, то есть от его диаметра и длины), а затем извлекают катетер в канал фибробронхоскопа и вместе с ним из дыхательных путей. После извлечения катетера из пространства между клапаном и стенкой бронха, канал его проникновения моментально закрывается за счет эластичности материала эндобронхиального клапана и обратного истечения препарата не происходит. Для эндобронхиального введения лекарственное средство готовится согласно инструкции к препарату, где указывается разовая и суточная дозы, а также растворитель, мы вводили одну разовую дозу препарата вориконазол лиофилизат, растворенного в воде для инъекций. Мы не наблюдали нежелательных явлений на введение противогрибковых препаратов. Пробу на аллергические реакции на препарат пациентам делаем до его введения, нанося препарат на слизистую губы.
Локализация и размер полости с мицетомой в заблокированном участке легкого не имеет значения, так как не обязательно попадание препарата прямо в полость, что невозможно при ее маленьких размерах, достаточно насытить препаратом в высокой дозе окружающую ткань, что происходит всегда. При необходимости установку ЭК и введение лекарственного препарата возможно проводить во время одной бронхоскопии, но это удлиняет время манипуляции, что хуже переносится пациентом и препарат попадает в участок легкого, заполненный воздухом с содержанием кислорода, как во вдыхаемом воздухе, к тому же пациент может сильно кашлять после установки ЭК, что приведет к потери части препарата.
Как правило, хватает одного введения препарата в разовой дозе, но при отсутствии рентгенологического эффекта через 2-3 недели введение препарата можно повторить, используя уже установленный ЭК.
ЭК остается в бронхах до получения полного желаемого эффекта «уничтожения мицетомы и закрытия полости распада», что может занять от 2 до 12 месяцев. Разрушение мицетомы обычно фиксировалось нами при первом контрольном МСКТ, проводимом через 2 месяца после процедуры введения препарата (контрольные рентгеновские исследования обычно рекомендуется проводить не чаще, чем через 2 месяца). Если при этом полость сохраняется, то не следует удалять ЭК до прекращения положительной рентгенологической динамики, чтобы уменьшить частоту случаев «излечения мицетомы при сохранении полости».
Клапан препятствует поступлению в блокированный участок легкого новых порций воздуха, а имевшийся в легком содержит значительно меньше кислорода и при каждом выдохе воздуха становиться все меньше - участок легкого начинает спадаться, производя сдавливание полости, что способствует ее заживлению. Но заживления не произойдет, пока в полости есть мицетома. Введение местно лекарственного препарата в высокой концентрации губительно действует на грибы, что разрушает мицетому, ее сцепление со стенками полости исчезает, она фрагментируется и поступает из полости в бронхи, а затем через клапан с мокротой выводится из дыхательных путей. Пациенты иногда отмечают присутствие в мокроте темных плотных комочков. Освободившаяся от мицетомы полость сдавливается в результате коллапса из-за ЭК, стенки ее соединяются и срастаются, образуя рубец, или уменьшенная полость заполняется, превращаясь в плотный очаг.
Вориконазол - противогрибковое средство системного применения из группы триазолов. Вориконазол активен (как in vitro, так и по результатам клинических исследований при лечении ряда инфекций) в отношении большинства штаммов следующих микроорганизмов: Aspergillus spp. (включая A. flavus, A. fumigatus, A. terreus, A. niger), Candida spp. (включая штаммы С. krusei, устойчивые к флуконазолу, резистентные штаммы С. glabrata и С. albicans, а также С. parapsilosis и С. tropicalis) и в отношении патогенных грибов, ставших актуальными в последнее время, в т.ч. Scedosporium apiospermum (бесполая форма Pseudallescheria boydii) и Fusarium spp., включая Fusarium solani, которые ограниченно чувствительны к существующим противогрибковым средствам. На курс лечения требуется не менее 42-84 суточных доз препарата (при рекомендуемой продолжительности лечения не менее 6-12 недель [Patterson TF, Thompson GR 3rd, Denning DW, et al. Practice Guidelines for the Diagnosis and Management of Aspergillosis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2016 Aug 15;63(4):e1-e60. doi: 10.1093/cid/ciw326. Epub 2016 Jun 29].
Клапанная бронхоблокация - это малоинвазивный немедикаментозный метод лечения некоторых видов полостных образований в легком, в том числе туберкулезных каверн, основанный на создании лечебной гиповентиляции в пораженном участке легкого с сохранением дренажной функции блокированного бронха. При интенсивном выдохе и кашле через ЭК из очага поражения выходят воздух и бронхиальное содержимое. При этом на вдохе ЭК не допускает поступления атмосферного воздуха через блокированный бронх, чем достигается постепенное состояние лечебной гиповентиляции, в ряде случаев вплоть до ателектаза легочной ткани. Метод сертифицирован и разрешен для лечения туберкулеза и его осложнений.
Особенностью предлагаемого способа, вызывающего гибель мицетомы и заживление полости, является сочетание местного эндобронхиального и внутриполостного введения раствора противогрибкового препарата (например, вориконазола) и устройства, препятствующего удалению лекарственного препарата из зоны поражения (эндобронхиального клапана) и вызывающего снижение вентиляции и уменьшение объема пораженного участка легкого.
После установки эндобронхиального клапана (ЭК) при бронхоскопии можно сразу после выполнения, а лучше через несколько дней при повторной бронхоскопии по каналу гибкого бронхоскопа проводится тонкий пластиковый катетер, который заводят в заблокированное пространство между стенкой бронха и ЭК. По катетеру производится введение водного раствора антигрибкового препарата (например, вориконазола лиофилизата в 10 мл раствора воды для инъекций в дозировке, рекомендуемой производителем для разового введения - 200 мг), после чего катетер освобождается от раствора введением 2 мл воды для инъекций.
Примеры реализации изобретения
Пример 1
Больной Н., 43 г., поступил в ФГБУ «НМИЦ ФПИ» Минздрава России с жалобами на кашель с отделением большого количества слизисто-гнойной мокроты, повышение температуры тела до 38,2°С, одышку при незначительной физической нагрузке, плохой аппетит. Из анамнеза известно, что лечение по поводу данного эпизода туберкулеза проходит с 2016 г. в стационаре по месту жительства. Больной находился в стационаре в течение 2,5 лет, получал схему лечения из 5 противотуберкулезных препаратов. Последний эпизод бактериовыделения (М.tuberculosis) был зафиксирован за 6 месяцев до поступления в ФГБУ «НМИЦ ФПИ» Минздрава России, куда он был направлен, так как не заживала полость, расцениваемая как туберкулезная каверна. При поступлении клинический диагноз: Кавернозный туберкулёз нижней доли правого лёгкого в фазе распада и обсеменения. МБТ (+). ШЛУ МБТ. Сопутствующий: Сахарный диабет 1 типа. Диабетическая ангиопатия обоих глаз. Хронический гепатит С. Хронический панкреатит. Осложнения: - Дыхательная недостаточность (ДН) 1-2.
При поступлении МСКТ ОГК в S10 правого легкого определялся фокус с неровными тяжистыми контурами размером 37×37×27 мм с полостью распада 28×35×17 мм, в просвете которой определялась округлая тень, характерная для аспергиллемы (фиг. 2). В S2,9,10 определяются три фокуса уплотнения легочной ткани до 14 мм и мелкие отграниченные очаги. Проведена диагностическая бронхоскопия, при которой патологии в бронхах не обнаружено. Из В-10 правого легкого взят бронхиальный смыв, в котором в микологической лаборатории обнаружен рост гриба Aspergillus fumigatus (фиг. 3) и установлена его лекарственная чувствительность к вориканазолу. В мокроте, сданной после бронхоскопии, также обнаружен рост гриба Aspergillus fumigatus с аналогичной лекарственной чувствительностью. Анализ материала на МБТ (М.tuberculosis) всеми методами оказался отрицательным. Клинический диагноз изменен: посттуберкулезные изменения, ХЛА (полость с мицетомой (аспергиллемой) С10 правого лёгкого), Сопутствующий: Сахарный диабет 1 типа. Диабетическая ангиопатия обоих глаз. Хронический гепатит С. Хронический панкреатит. Осложнения: - Дыхательная недостаточность (ДН) 1-2.
Учитывая наличие нескольких сопутствующих заболеваний, решено не применять хирургических резекционных методов лечения аспергиллемы и использовать комбинированное местное лечение (заявляемый способ). Под местной анестезией (2% раствор лидокаина - 6,0 мл + лидокаин-спрей 10% - 6 доз) при фибробронхоскопии произведена установка ЭК в В-10 правого легкого. Через 4 дня при бронхоскопии в заблокированное пространство по катетеру введено 10 мл раствора вориконазола лиофилизата (200 мг действующего вещества). Манипуляции пациент перенес хорошо, осложнений нет. Далее пациент не получал противогрибковых препаратов. Через 2 месяца выполнена контрольная МСКТ ОГК: нижняя доля правого легкого несколько уменьшена в объеме, в ней сохраняются множественные мелкие очаги, однако полость распада, в которой была мицетома, не определяется, на ее месте сформировался плотный очаг неправильной формы (фиг. 4). Для закрепления эффекта и учитывая хорошую переносимость лечения пациентом, принято решение об удалении ЭК через месяц, что и было выполнено при бронхоскопии под местной анестезией. При наблюдении в течение года, рецидива полости и мицетомы нет.
Комментарий. У пациента в результате туберкулеза легких образовалась каверна в правом легком. При длительном лечении - более 2 лет, туберкулезный процесс завершился, а в сохранившейся посттуберкулезной полости на фоне длительного приема антибиотиков, входящих в схему лечения туберкулеза, произошла инвазия гриба Aspergillus fumigatus, образовавшего мицетому - аспергиллему. Учитывая наличие нескольких сопутствующих заболеваний и частое осложнение мицетом кровотечениями, было решено применить предлагаемое для патентования комбинированное лечение. Лечение дало хороший эффект - гибель аспергиллемы и заживление полости. Это было зафиксировано при первом же контрольном рентгенологическом исследовании. Далее ЭК был удален.
Клинический пример 2
Пациентка В., 40 л. Из анамнеза известно, что с декабря 2017 года пациентка состоит на учете у фтизиатра с диагнозом: Фиброзно-кавернозный туберкулез верхней доли левого легкого в фазе инфильтрации и обсеменения МБТ (+) пре ШЛУ МБТ. В течение 5 месяцев пациентка лечилась в стационаре, затем амбулаторно. Она получала лечение 7-ю противотуберкулезными препарата в течение года, в том числе антибиотики линезолид и левофлоксацин. На фоне лечения отмечалась положительная рентгенологическая динамика туберкулеза легких в виде рассасывания очагово-инфильтративных изменений и заживления нескольких полостей распада, но в верхней доле левого легкого некоторые полости сохранялись. Бактериовыделение (М.tuberculosis) прекратилось через 4 месяца (с марта 2018 г.) после начала лечения. Консультирована торакальным хирургом. В связи с наличием полостей распада рекомендовано оперативное лечение.
В апреле 2019 года пациентка была госпитализирована в ФГБУ «НМИЦ ФПИ» Минздрава России, проведено дообследование. Состояние при поступлении удовлетворительное, жалоб нет. При МСКТ ОГК выявлены полости распада в верхней доле левого легкого. Внутри самой крупной из них, расположенной во 2 сегменте левого легкого, имелось округлое образование, что характерно для мицетомы (фиг. 5). При бронхоскопии патологии в бронхах не выявили, в бронхиальном смыве из в-зонального бронха при посеве на грибы обнаружены Aspergillus flavus с сохраненной чувствительностью к вориканазолу. Учитывая двусторонний туберкулезный процесс, выраженные посттуберкулезные изменения, в том числе в участке легкого окружающем полость с мицетомой и планируемый из-за этого большой объем операции пациентка изъявила желание попробовать нехирургический метод лечения (предлагаемый к патентованию).
При фибробронхоскопии произведена установка ЭК в верхнезональный бронх левого легкого, а через 5 дней проведено введение раствора вориканазола в дозировке 200 мг. Манипуляцию пациентка перенесла хорошо, осложнений нет, выписана по месту жительства, Противогрибковые препараты не принимала, контрольную МСКТ ОГК выполнила через 3 месяца - три сегмента верхней доли левого легкого находятся в ателектазе, полости, в том числе с мицетомой не определяется, в просвете левого главного бронха видна хвостовая часть ЭК (фиг. 6). Лечение полости с мицетомой признано завершенным и ЭК удален. При контрольной МСКТ через 6 месяцев: верхняя доля левого легкого расправлена, на всем ее протяжении отмечаются склеротические изменения, плотные разновеликие очаги. Полостное образование с мицетомой не определяется, на его месте крупный плотный очаг (фиг. 7), в нижней доле левого легкого отмечаются единичные посттуберкулезные частично кальцинированные очаги 10 и 13 мм, в верхней доле и сегментах 6, 8 правого легкого - склеротические изменения и немногочисленные посттуберкулезные плотные очаги.
Комментарий: у пациентки с фиброзно-кавернозным туберкулезом удалось в результате длительного лечения добиться успеха - излечения туберкулеза (прекращение бактериовыделения рассасывания инфильтрации, закрытия нескольких каверн), при этом в стенке одной из постуберкулезных полостей произошла инвазия гриба Aspergillus flavus с образованием мицетомы. Применение предлагаемого к патентованию метода привело к гибели мицетомы и закрытию полости распада крупным очагом. Последнее контрольное исследование показало стабильность достигнутого результата. У пациентки удалось сохранить весь объем функционирующей легочной ткани, тогда как при хирургическом лечении планировалось удаление всей верхней доли левого легкого.
Клинический пример 3 (сравнительный пример лечения полости с мицетомой, когда применялась только установка ЭК, но противогрибковый препарат не вводился).
Пациент Н., 17 лет. Болен с начала января 2019 г., когда появились кашель и лихорадка. 15.01.19 г. при рентгенологическом исследовании в нижней доле левого легкого выявлена инфильтрация, далее при компьютерной томографии от 25.02.19 г.: в нижней доле левого легкого были выявлены множественные очаговые изменения, местами сливающиеся в обширные участки консолидации легочной ткани с полостями распада. При исследовании мокроты от 20.02.19 г. методом ПЦР установило наличие ДНК МБТ, выставлен диагноз «инфильтративный туберкулез легких в фазе распада», пациент переведен в туберкулезную больницу.
Получал лечение: 6 противотуберкулезными препаратами. КТ легких и средостения от 27.05.19 г.: рассасывание и уплотнение очагов, но одна из полостей распада сохранялась. Лечение с 31.05.19 г. до 30.09.2019 г. проводилось уже 3 противотуберкулезными препаратами. После 20.02.19 года все анализы мокроты на МБТ и ДНК МБТ были отрицательными. КТ от 29.07.19 г. (фиг. 8 (А) и фиг. 9 (А)) - дальнейшее рассасывание изменений в нижней доле левого легкого, полость распада 24,3×20,l мм сохранялась, контур ее внутренней стенки был неровный с участком, которой выбухал в просвет в виде округлого утолщения. В сентябре 2019 г. заочно консультирован в ФГБУ «НМИЦ ФПИ» Минздрава России, а затем 10.09.19 госпитализирован. Принято решение для закрытия полости распада в легком провести установку ЭК. Общее состояние пациента удовлетворительное. По другим органам и системам патологии нет. Во время бронхоскопии 11.09.19 г. был взят бронхиальный смыв из участка легкого с вышеописанной полостью на МБТ и грибы, а затем в нижнезональный бронх левого легкого проведена установка ЭК, что перекрыло поступление воздуха в участок легкого с полостью распада. Пациент манипуляцию перенес удовлетворительно, самочувствие хорошее, наличие клапана в бронхе не чувствует. Аускультативно - в нижних отделах левого легкого дыхание ослаблено, хрипов нет. Через несколько дней из лаборатории были получены результаты об обнаружении в бронхиальном смыве роста гриба Aspergillus fumigatus, МБТ и ДНК МБТ обнаружены не были.
Выписан 19.09.2019 г. по месту жительства с рекомендацией выполнения контрольного КТ через 4 месяца. Компьютерную томографию выполнил 16.01.2020 г. (фиг. 8 (Б), фиг. 9 (Б) - сегменты 7, 8, 9, 10 левого легкого в ателектазе, пониженной прозрачности, что является результатом установки ЭК, но полость распада в зоне ателектаза сохраняется, она изменила конфигурацию, внутри нее четко определяется мицетома. Принято решение об удаления клапана из-за его неэффективности по закрытию полости распада с мицетомой. Применение данному пациенту предлагаемого к патентованию метода не рассматривалось, так как родители были настроены на хирургическое лечение. ЭК удален во время бронхоскопии. Пациенту рекомендована операция - резекция сегментов н-доли левого легкого с окончательным уточнением объема во время операции. Диагноз посттуберкулезных изменений н-доли левого легкого, ХЛА с наличием полостного образования, с инвазией стенки грибом Aspergillus fumigatus.
Установка ЭК вызвала ателектаз сегментов нижней доли левого легкого, но полость с наличием мицетомы не зажила за последующие 4 месяца.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ ДЕСТРУКТИВНЫМИ ФОРМАМИ ТУБЕРКУЛЕЗА ЛЕГКИХ | 2009 |
|
RU2413471C1 |
| Способ экстракции эндобронхиальных клапанов | 2023 |
|
RU2837575C2 |
| Способ лечения туберкулеза легких и бронхов при различных рентгенологических синдромах | 2023 |
|
RU2826098C1 |
| Способ лечения эмпиемы плевры | 2017 |
|
RU2661090C1 |
| Способ профилактики бронхоплеврального свища после правосторонней пневмонэктомии при деструктивном туберкулезе легких с лекарственной устойчивостью микобактерий туберкулеза | 2021 |
|
RU2786336C1 |
| Способ лечения больных с туберкулезом легких | 2024 |
|
RU2830337C1 |
| Способ лечения рубцовых и компрессионных стенозов трахеи | 2021 |
|
RU2771934C1 |
| Способ лечения туберкулеза легких с множественной лекарственной устойчивостью микобактерий туберкулеза | 2018 |
|
RU2687743C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕСТРУКТИВНОГО ТУБЕРКУЛЕЗА ЛЕГКИХ | 2010 |
|
RU2450820C2 |
| Способ выбора укороченных режимов химиотерапии при лечении туберкулеза легких | 2022 |
|
RU2805496C1 |


Изобретение относится к области медицины, а именно к эндоскопии, пульмонологии и фтизиатрии. Проводят диагностическую бронхоскопию для оценки состояния бронхов в пораженной области с одновременным взятием бронхиальных смывов для подтверждения грибковой инвазии и определения лекарственной чувствительности. При отсутствии противопоказаний к установке эндобронхиального клапана при следующей фибробронхоскопии устанавливают эндобронхиальный клапан в долевой, зональный или сегментарный бронх, вентилирующий участок легкого, в котором находится полость с мицетомой. Через 3-5 дней во время бронхоскопии между стенкой эндобронхиального клапана и стенкой бронха, в который установлен клапан, проводят пластиковый катетер до выхода дистального конца катетера за пределы клапана. По катетеру вводят водный раствор противогрибкового лекарственного препарата для внутривенного введения, содержащий разовую дозу препарата. После этого катетер освобождают от раствора введением воды для инъекций. Затем катетер извлекают в канал фибробронхоскопа и вместе с ним из дыхательных путей. Способ позволяет обеспечить высокую концентрацию лекарственного препарата в зоне поражения, разрушить мицетому после разового введения противогрибкового препарата, способствует быстрому и эффективному заживлению полости, снижая риск развития рецидива и осложнений. 4 з.п. ф-лы, 3 пр., 9 ил.
1. Способ лечения полостей распада в легком, осложненных хроническим аспергиллезом, характеризующийся тем, что после проведения диагностической бронхоскопии для оценки состояния бронхов в пораженной области с одновременным взятием бронхиальных смывов для подтверждения грибковой инвазии и определения лекарственной чувствительности, и при отсутствии противопоказаний к установке эндобронхиального клапана, при следующей фибробронхоскопии устанавливают эндобронхиальный клапан в долевой, зональный или сегментарный бронх, вентилирующий участок легкого, в котором находится полость с мицетомой, через 3-5 дней во время бронхоскопии между стенкой эндобронхиального клапана и стенкой бронха, в который установлен клапан, проводят пластиковый катетер до выхода дистального конца катетера за пределы клапана и по нему вводят водный раствор противогрибкового лекарственного препарата для внутривенного введения, содержащий разовую дозу препарата; после чего катетер освобождают от раствора введением воды для инъекций, а затем катетер извлекают в канал фибробронхоскопа и вместе с ним из дыхательных путей.
2. Способ по п. 1, характеризующийся тем, что в качестве противогрибкового лекарственного препарата используют препарат, к которому установлена чувствительность грибковой инвазии при выполнении диагностической бронхоскопии.
3. Способ по п. 2, характеризующийся тем, что в качестве противогрибкового лекарственного препарата используют вориконазол.
4. Способ по п. 3, характеризующийся тем, что разовая доза вориконазола для введения составляет 200 мг.
5. Способ по п. 1, характеризующийся тем, что для освобождения катетера от лекарственного раствора вводят 1-2 мл воды для инъекций.
| Левин А.В | |||
| и др | |||
| Применение клапанной бронхоблокации при осложненном туберкулезе легких | |||
| Пособие для врачей, издание 2-е, переработанное и дополненное | |||
| ООО "Медланг" | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА ЛЕГКИХ | 2002 |
|
RU2244517C2 |
| US 10226299 B2 12.03.2019 | |||
| John M | |||
| Hance et al | |||
| Endobronchial Valves in the Treatment of Persistent Air Leaks | |||
| Ann Thorac Surg | |||
Авторы
Даты
2021-06-11—Публикация
2020-05-20—Подача