Изобретение относится к медицине, а именно к способам проведения хирургических операций с применением глубокого замораживания с помощью жидкого азота.
Из уровня техники известно, что в реальной клинической практике в арсенале эндоскопических отделений лечебно-профилактических организаций для экстракции эндобронхиальных клапанов (ЭК), например, типа «МЕДЛАНГ», используют щипцы для гибкой бронхоскопии, реже -«петлю» из эндо(электро)хирургической установки (без режима «endocut»), либо при наличии набора инструментов для ригидной бронхоскопии -жесткие щипцы по типу «аллигатор» либо жесткие оптические щипцы.
Зачастую экстракция ЭК гибкими щипцами для эндобронхиальной биопсии бывает неэффективна, и представляет технические сложности вследствие массивных разрастаний грануляционной ткани вокруг радиальной части («головки») ЭК, при длительном его нахождении в устье бронха. Неадекватная техника захвата гибкими щипцами только лепестковой части («хвоста») ЭК приводит к фрагментированию объекта, и не выполняет задачу удаления ЭК.
Попытка скусывания (эксцизии) грануляционных разрастаний щипцами для гибкой эндоскопии требует многократных попыток (раскрытие браншей щипцов позволяет захватывать ткань объемом не более 2-3 мм3), что приводит к повышенной кровоточивости в зоне скусывания щипцами, и ухудшает визуализацию ЭК, планируемого к экстракции, усиление кашля у пациента и затрудняет действия эндоскописта в случае проведения лечебной бронхоскопии в условиях местной анестезии. В случае не функционирования ЭК («залипания» лепестковой части, деформации резины, и наличия на лепестковой и радиальной части гнойно-некротических наложений бактериального или грибкового генеза) эндоскопические щипцы могут соскальзывать при захвате и попытке экстракции, что не обеспечивает визуально контролируемую эксцизию ЭК и удлиняет время манипуляции усиливая кашлевой рефлекс пациента.
При использовании для экстракции ЭК щипцов для ригидной бронхоскопии их применение ограничено крупным размером инструментов и невозможностью доступа к устьям бронхов с большим углом отхождения (более 70°) (правый верхнедолевой бронх, левый верхнезональный бронх).
Вышеуказанные аспекты заставляют искать пути оптимизации экстракции ЭК при лечебной бронхоскопии, в том числе, основанных на принципах использования криотехнологий - эндоскопической эндобронхиальной криобиопсии и криодевитализации (криотерапии) [2, 3].
Предлагаемая технология криоэкстракции ЭК позволяет решить проблемы безопасного и малотравматичного удаления ЭК и обеспечивает комфортную работу врача-эндоскописта, позволяя совмещать 2 режима для решения проблемы борьбы с разрастанием грануляционной ткани вокруг ЭК (криодеструкция), и его удаления даже в труднодоступных зонах трахеобронхиального дерева.
Применение эндобронхиальной криобиопсии и трансбронхиальной криобиопсии нашло широкое применение в эндоскопической диагностике эндобронхиальной патологии при диффузных и интерстициальных заболеваниях легких, неопластических процессах, что отражено в Национальных Клинических Рекомендациях по диагностике Идиопатического легочного фиброза [1]. Помимо широкого использования криотехнологий в респираторной эндоскопической диагностике в литературе имеется ряд сообщений об криоэкстракции инородных тел, чем «по сути» является эндобронхиальный клапан в просвете трахеобронхиального дерева [2-6].
Криотехнологии. Техника эндобронхиальной криобиопсии (ЭБКБ) основана на использовании эффекта Джоуля-Томсона: поток сжиженного газа (СО2) содержится в баллоне под высоким давлением. При высвобождении газ быстро охлаждается в результате расширения при атмосферном давлении и доставляется по проводнику к зоне биопсии, что приводит к замораживанию объекта до (-50…-60)°С дистальнее зонда на расстоянии до 1 см.
Для криобиопсии применяют криохирургическую станцию Erbecryo II (Tubingen, Германия) с многоразовыми гибкими зондами 2,4 и 1,9 мм. В результате обработки криозондом в течение 4-10 секунд участок замораживаемого объекта (ткани, инородного тела) фиксируется к наконечнику криозонда, и при тракции криозонда происходит либо фрагментация объекта (например, опухолевого экзофита бронха) с получением кусочков 0,5-1 см3, либо полная экстракция объекта (инородное тело органического, либо неорганического происхождения).
В отличие от зондов предыдущего поколения для криодеструкции в новой модели имеется более прочный узкий канал для поступления газа с возможностью расширения поверхности зонда с целью усиления мощности замораживания, что позволяет выполнять фиксированную тракцию, например, больших фрагментов ткани опухоли с исключением возможности его отрыва и дислокации. Гидрофильное пластиковое покрытие зонда позволяет легко проводить его в рабочий канал гибкого бронхоскопа.
Время воздействия криозондом прямо пропорционально зависит от объема удаляемого объекта. Криозонд заводится в трахеобронхиальное дерево через инструментальный канал гибкого бронхоскопа. Ввиду того что, как правило, размеры биоптатов или инородных тел существенно превышают диаметр инструментального канала эндоскопа (2,0-2,8 мм), их извлекают в блоке с гибким бронхоскопом. При этом эндоскописту необходимо одной рукой фиксировать зонд у входа в инструментальный канал и не допускать его смещения в момент осуществления рывка и отделения объекта от массива внутрипросветного образования или стенки бронха.
В литературе описано извлечение различного рода субстанций из просвета дыхательных путей (инородных тела, крупные сгустки крови или очень вязкие слепки мокроты), которое выполняется аналогично эндобронхиальной криобиопсии: после криофиксации в течение 5-7 секунд осуществляли криоэкстракцию, при этом криовоздействие прекращали только после полного удаления бронхоскопа в блоке с криозондом и ЭК из дыхательных путей пациента.
Наиболее близким по технической сущности к предложенному является способ локальной деструкции первичных и метастатических новообразований органов брюшной полости и забрюшинного пространства с лапароскопическим доступом [RU 2770279, C1, А61В 17/94, 15.04.2022], включающий комбинированное крио- и РЧА-воздействие, для чего в новообразование через троакар вводят криозонд, осуществляют замораживание новообразования до достижения температуры около -184°С, после пассивного оттаивания криозонд извлекают, через тот же троакар в новообразование по ходу ранее стоявшего криозонда вводят активный РЧА-электрод, осуществляют абляцию сначала новообразования, а затем пункционного канала.
Недостатком наиболее близкого технического решения является относительно высокая сложность, вызванная необходимостью осуществления помимо крио- еще и РЧА-воздействия, относительно длительная процедура удаления, что приводит к нежелательным осложнениям, и относительно низкая температура замораживания, что также приводит к нежелательным осложнениям.
Поставленная задача заключается в создании способа экстракции эндобронхиальных клапанов, отличающегося от известных способов меньшей сложностью, меньшей по длительности процедурой и более высокой температурой замораживания.
Требуемый технический результат заключается в упрощении и ускорении процесса удаления эндобронхиальных клапанов (ЭК) и снижения уровня низкотемпературного воздействия.
Поставленная задача решается, а требуемый технический результат достигается тем, что в способе, включающем процедуру криовоздействия, согласно изобретению, во время процедуры воздействуют на грануляционную ткань вокруг радиальной части эндобронхиальных клапанов в режиме криодевитализации и осуществляют последовательно нескольких циклов, в каждом из которых грануляционную ткан замораживают на 20 с до температуры -80°С, с последующим оттаиванием.
Кроме того, требуемый технический результат достигается тем, что, в процедуру криовоздействия используют 3 циклов криодевитализации.
Кроме того, требуемый технический результат достигается тем, что, процедуру криовоздействия повторяют через 1-2 недели.
На изображениях представлены:
на фиг. 1 - этапы подготовки и выполнения криоэкстрации эндобронхиального клапана при лечебной бронхоскопии у пациента М;
на фиг. 2 - этапы выполнения криоэкстрации эндобронхиального клапана из устья левого верхнедолевого бронха при лечебной бронхоскопии у пациентки В;
на фиг. 3 - этапы подготовки и выполнения криоэкстрации эндобронхиального клапана при лечебной бронхоскопии у пациента И.
Предложенный способ реализуется следующим образом.
В случае массивного разрастания грануляционной ткани вокруг радиальной части ЭК можно применять режим криодевитализации (криотерапии) грануляционной ткани при использовании нескольких циклов замораживания по 20 с до -80°С, с последующим оттаиванием, что по данным публикаций эффективно при эндоскопической терапии доброкачественных (карциноидов) или малоинвазивных опухолей бронхов (местнораспространенного центрального рак легкого / карциномой in situ).
При контакте зонда с опухолевой или грануляционной тканью многократно чередовали циклы замораживания и последующего оттаивания. Криовоздействие осуществляли в течение 20 с. у 5 пациентов с, у 4 - с бронха, у 2 - с регионарными метастазами и у одного больного с гемангиомой. Повторный курс лечения был проведен через 1-2 нед. Общая эффективность составила 80%.
Заявляемое решение при лечебной бронхоскопии в условиях ригидной интубации тубусом жесткого бронхоскопа и внутривенного наркоза с миорелаксацией и высокочастотной вентиляцией позволяет оценить трудности экстракции ЭК, выбрать размер криозонда (варьирует размер 1,9 мм, 2,4 мм) и экспозицию криоэкстракции и быстро удалить эндобронхиальный клапан с последующим осмотром устья бронха после криоэкстракции.
Предложенная технология является решением проблемы, особенно в тех случаях, когда попытки неоднократной эксцизии ЭК гибкими эндоскопическими щипцами при предыдущих лечебных бронхоскопиях были неуспешны из-за выраженных грануляционных разрастаний вокруг радиальной его части («головка» клапана), не функционирования «лепестковой» части клапана (наличие гнойно-некротических налетов, осклизняющих его поверхность).
Также предложенное решение по использованию криоэкстракции ЭК эффективно в ситуациях, когда применение высокоэнергетического лазера для вапоризации разрастаний грануляционной ткани вокруг «радиальной» части ЭК связано с техническими трудностями из-за необходимости постоянного извлечения катетера для подачи кислорода под высоким давлением (ВЧ вентиляция) и выжидания времени для эвакуации О2 из просвета трахеобронхиального дерева.
Технической проблемой, решение которой обеспечивает предлагаемая методика, является возможность быстрой криоэксцизии длительно находящегося в просвете бронха ЭК при гибридной лечебной бронхоскопии, особенно в случаях выраженного разрастания грануляционной ткани, нефункционирования (несостоятельности («залипания») лепестковой его части) клапана, изменение свойств резины (что может привести к фрагментированию при попытке эксцизии гибкими щипцами), и возможности оценить в дальнейшем состояние просвета бронха после удаления ЭК (в условиях бронхоскопии под местной анестезией требуется переинтубация, что может утяжелить состояние пациента).
Технический результат заключается в упрощении и ускорении процесса удаления ЭК и сокращения сроков лечебной бронхоскопии с возможностью оценить просвет бронха после удаления ЭК, что ведет к уменьшению срока пребывания в стационаре или позволяет проводить процедуру пациентов в амбулаторных условиях.
Заявляемый технически результат достигается посредством использования представленной на рынке криохирургической станции Erbecryo II (Tubingen, Германия) с многоразовыми гибкими зондами 2,4 и 1,9 мм. Длительность (экспозиция) криовоздействия на ЭК составляет на 20 с в зависимости от размера эндобронхиального клапана Левина (от №6 до №13), обширности грануляционных разрастаний вокруг ЭК, и размера просвета и угла отхождения бронха, подвергнутого ЭКББ.
Таким образом, указанный технический результат обеспечивается комплексной мультидисциплинарной оценкой состояния ЭК во время бронхоскопии (угол доступности блокированного бронха, степень разрастания грануляционной ткани вокруг радиальной части ЭК, оценка состояния лепестковой части ЭК (состояние резины, наличие секрета гнойно-некротического характера на ней)), оценка срока длительности ЭКББ), персонифицированного выбора размера криозонда от 1,9 до 2,4 мм в зависимости от размера удаляемого ЭК и ранее перечисленных аспектов, выбора длительности (эскпозиции в секундах) криовоздействия криозондом (криоэкстракции) в зависимости от степени разрастания грануляционной ткани с помощью криохирургической станции Erbecryo II.
Клиническое наблюдение №1.
Пациент М., 41 года. Поступил в июле 2022 в хирургическое отделение лечебно-профилактической организации с диагнозом А15.2 Фиброзно-кавернозный туберкулез правого легкого в фазе обсеменения. Туберкулемы верхней доли левого легкого. МЛУ МВТ. Поздний рецидив. Ранее диагноз туберкулеза установлен в 2010 г. Была развернута противотуберкулезная терапия в объеме: Моксифлоксацин 0.4 в\в, Пиразинамид 1.5, Циклосерин 0.75, Капреомицин 1.0, Линезолид 0.6 в\в, Бедаквилин 0.2 по схеме. Терапию переносил удовлетворительно. На фоне проводимой терапии отмечена положительная рентгенологическая и клиническая динамика в виде рассасывания перикавитарной инфильтрации и уменьшения степени проявления одышки. 10.08.2022 пациенту выполнена Эндоскопическая клапанная бронхоблокация (ЭКББ) с установкой ЭК в устье правого верхнедолевого бронха (ПВДБ). Процедуру перенес удовлетворительно. 24.08.2022 выполнена ЭКББ с установкой ЭК в устье В6 справа. На КТ ОГК от 15.09.2022 выраженная положительная динамика. При контрольном КТ ОГК в устье В6 справа ЭК не визуализировался. Учитывая КТ картину, а также опрос пациента «отмечает, что проглотил какой-то «объект» после утреннего кашля» - нельзя исключить отсутствие эндобронхиального клапана в В6 справа и его миграцию из трахеобронхиального дерева. При контрольной бронхоскопии от 07.10.2022: выявлено, что в устье ПВДБ сохраняется ЭК, не функционирует. При осмотре устьев В-6 с обеих сторон блокаторов не выявлено.
Учитывая положительную динамику и ограничение процесса в левом легком с формированием туберкулем пациенту (при сохранении ЭКББ ПВДБ) 10.10.2022 выполнена ВАТС атипичная резекция S1-S2 левого легкого. Ранний послеоперационный период протекал без осложнений, дренажи удалены на 8-е сутки. 07.11.2022 у пациента выявлен позитивный тест ПЦР на SARS CoV-2, что отложило дальнейшее этапное хирургическое лечение. Через полтора месяца после операции 24.11.2022 пациент отметил жалобы на тяжелое дыхание и боли в левой половине грудной клетки. При осмотре: грудная клетка без особенностей, дыхание не проводится. На рентгенографии ОГК: Левое легкое коллабировано более чем на 1/3 объема за счет базального пневмоторакса. Верхние и средние отделы легкого удерживаются от спадения плевральными сращениями. 25.11.2022 в условия чистой перевязочной, выполнено дренирование плевральной полости в VI межреберье слева, по задней аксиллярной линии, получен воздух, дренаж подключен к системе по Бюлау, далее к аппарату активной аспирации.
12.12.2022 по данным КТ ОГК: левое легкое коллабировано на 1/2 объема, от полного спадения удерживается плевральными спайками. Заключение: Субтотальный многокамерный пневмоторакс слева без достоверно определяемых бронхоплевральных свищей (решетчатое легкое?) в области верхушки легкого и паракардиально каудальнее корня легкого) Учитывая многокамерную полость и отсутствие достоверных данных за наличие бронхоплевральных свищей и источника воздухотечения 15.12.2022 выполнена ВАТС слева ревизия плевральной полости, ушивание дефектов, частичная плеврэктомия с декортикацией легкого по поводу спонтанного пневмоторакса. Послеоперационный период протекал без осложнений.
В течение 3-х месяцев после ВАТС ревизии состояние пациента было стабильным, рецидива пневмоторакса не отмечено. Динамики по данным КТ ОГК также выявлено не было, что привело к решению вопроса об удалении эндобронхиального клапана из просвета ПВДБ.
На КТ ОГК от 03.03.2023 в просвете ПГБ визуализируется лепестковая («хвостовая») часть ЭК, блокирующего устье ПВДБ (радиальная часть - «головка» в устье ПВДБ) (рисунок 1а).
Учитывая сложность ведения пациента (снижение вентиляционной способности легких (ОФВ1- 61,3% от должного, ЖЕЛ - 63,4% от должного, Индекс Тиффно - 76%) при исследовании газов крови от 27.02.2023 - умеренная гипоксемия (рО2 75%, повышение альвеолярно-капиллярного градиента), осложнение раннего послеоперационного периода в виде левостороннего спонтанного пневмоторакса и перенесенной инфекции SARS CoV-2, длительности ЭКББ - 7 месяцев, снижения массы тела (ИМТ-17,76), выявление нефункционирования ЭК по данным бронхоскопии от октября 2022) принято решение о проведении удаления ЭК из устья ПВДБ с применением метода криоэкстрации в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа с ВЧ вентиляцией и тотальной внутривенной анестезией.
21.03.2023. в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа (Карл Шторц №12) с ВЧ вентиляцией и тотальной внутривенной анестезией, оценено состояние ЭК в устье ПВДБ. Справа в просвете главного бронха визуализируется лепестковая часть ЭК (рисунок 1б), радиальная часть установлена в устье ПВДБ, клапан не функционирует (рисунок 1в). Отмечено «обрастание» радиальной части грануляционной тканью и «залипание» хвостовой части ЭК).
Была выполнена криоэкстрация ЭК из устья ПВДБ этапы которой представлены на фиг. 1.
Криоэкстракция проводилась с помощью криозонда 1,9 мм криохирургической станции Erbecryo II с экспозицией 7 секунд (рисунки 1 г, 1д). ЭК удален полностью, осмотрен после извлечения, разрывов и фрагментирования не найдено (рисунок 1е).
После удаления ЭК: слизистая ПВДБ гиперемировна, отечна, определяются единичные грануляции, из устья В2 дренируется вязкое отделяемое слизисто-гнойного характера. Устья бронхов 1-5 порядка с обеих сторон открыты, не деформированы, шпоры их острые. Слизистая видимых бронхов очагово гиперемирована, сосудистый рисунок усилен.
Длительность лечебной бронхоскопии от момента интубации трахеи тубусом жесткого бронхоскопа до экстубации составила 5 минут
Клиническое наблюдение демонстрирует, что выбранная технология криоэкстракции ЭК у оперированного пациента торакального профиля со снижением вентиляционной способности легкого заняла малое время и позволила быстро выполнить удаление ЭК без развития каких-либо осложнений со стороны слизистой ТБД, так и вентиляционной способности.
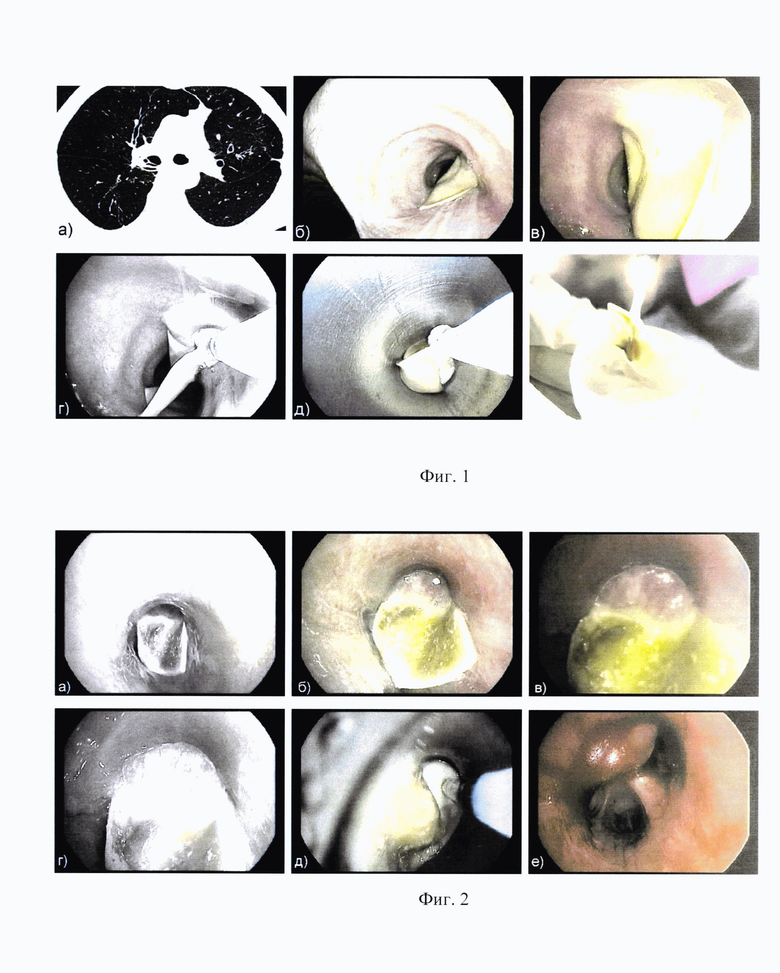
На фиг. 1 представлены этапы подготовки и выполнения криоэкстрации эндобронхиального клапана при лечебной бронхоскопии у пациента М:
а) КТ ОГК пациента М, аксиальное легочное окно, перед лечебной бронхоскопией: в устье правого верхнедолевого бронха (ПВДБ) определяется эндобронхиальный клапан (визуализируются его радиальная часть -«головка», обтурирующая устье ПВДБ и лепестковая часть («хвост») в просвете правого главного бронха (выделены желтым цветом);
б) лепестковая часть ЭК в просвете правого главного бронха при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
в) радиальная часть ЭК в устье правого верхнедолевого бронха при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
г) момент «замораживания» - криовоздействия на эндобронхиальный клапан криозондом 1,9 мм (криостанция Erbe Cryo II, Erbe Elektromedizin, Germany), экспозиция 7 секунд, на наконечнике и дистальной части криозонда определяется формирование кристаллов льда;
д) криоэкстракция: извлечение ЭК с продолжающимся криовоздейсвием в тубусе ригидного бронхоскопа (ригидный тубус Karl Storz №12);
е) вид эндобронхиального клапана, адгезированного к криозонду после извлечения из тубуса ригидного бронхоскопа, определяются неповрежденные лепестковая и радиальная части эндобронхиального клапана.
Клиническое наблюдение №2.
Пациентка В., 23 года
В октябре 2021 года перенесла новую коронавирусную инфекцию. Находилась на лечении в инфекционном отделении лечебно-профилактической организации с 10.10.21 г. по 14.10.21 г. с диагнозом «Коронавирусная инфекция, вызванная вирусом COVID-19, вирус не идентифицирован. Среднетяжелое течение. Двусторонняя внебольничная полисегментарная вирусная пневмония. ДН 0-1. NEWS2-1 б. КТ - 2 от 10.10.21 г. Анемия средней степени тяжести.» Получала лечение в объеме: бромгексин 16 мг, фавипиравир 1600 мг, надропарин кальция 5700 анти-Ха ME, железа III гидроксид полимальтозат 100 мг, левилимаб 324 мг, дексаметазон 20 мг, 16 мг, 12 мг, 8 мг, 4 мг. Выписана с положительной динамикой на амбулаторное лечение. Со слов пациентки, ранее проводилось микробиологическое исследование мокроты от 08.10.21 г., при микроскопии выявлены кислотоустойчивые микроорганизмы (КУМ). При обращении поступила для обследования и решения вопроса о дальнейшей тактике лечения. Лечение проводилось по 1 индивидуализированному режиму химиотерапии (РХТ), учитывая тяжесть состояния, распространенный специфический процесс: Рифампицин 0,45 в/в капельно, Изониазид 5,0 в/м и лимфотропно, Амикацин 0,75 в/м, Пиразинамид 1,5, Этамбутол 1,2, Левофлоксацин 0,75 в/в капельно, Переносимость удовлетворительная, терапия коррегировалась. Проводилась дезинтоксикационная, железосодержащая терапия. Диагноз при поступлении: Инфильтративный туберкулез легких в фазе распада. Лекарственная чувствительность МБТ в тест системе ПЦР «СИНТОЛ», Россия к изониазиду, рифампицину и фторхинолонам. Переносимость удовлетворительная.
18.02.2022 г. выполнена эндоскопическая клапанная бронхоблокация - установлен ЭК в устье левого верхнедолевого бронха ЛВДБ, которая поддерживалась искусственным пневмоперитонеумом (ИПП) (объем 600-700 мл) 1 раз в неделю. Процедуру переносила удовлетворительно. На фоне лечения: улучшение общего самочувствия, отсутствие симптомов интоксикации, отсутствие кашля, восстановление гемоглобина по данным клинического анализа крови, прибавка в весе, отсутствие бактериовыделения методом люминесцентной микроскопии, по данным посевов более 3-х раз, рентгенологически положительная динамика в виде рассасывания очагово-инфильтративных изменений легких, закрытие полостей распада в правом легком. После выполнения ЭКББ устья ЛВДБ- закрытие полостей распада в левом легком. 04.04.2022 пациентка была выписана из 3 т.о. для дальнейшего лечения в ПТД по месту жительства. ИПП проводились регулярно.
Пациентка поступила повторно после окончания интенсивной и поддерживающей фазы химиотерапии с диагнозом: Цирротический туберкулез легких. МБТ (-). ЛЧ МБТ по СИНТОЛ. Состояние после ЭКББ устья ЛВДБ слева от 18.02.2022 года в 3 т.о. для удаления эндобронхиального клапана при бронхоскопии.
ФВД от 05.08.2022 г. нарушение вентиляционной функции легких по рестриктивному типу. Снижение вентиляционной способности легких средней степени тяжести.
Учитывая сложность ведения пациента (снижение вентиляционной способности легких, длительность ЭКББ - 6 месяцев, перенесение коронавирусной инфекции в анамнезе) принято решение о проведении удаления ЭК из устья ЛВДБ с применением метода криоэкстрации в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа с ВЧ вентиляцией и тотальной внутривенной анестезией. Этапы криоэкстрации ЭК из устья ЛВДБ представлены на фиг. 2.
19.08.2022 г в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа (Карл Шторц №12) с ВЧ вентиляцией и тотальной внутривенной анестезией, оценено состояние ЭК в устье ЛВДБ. В просвете левого главного бронха (ЛГБ) определяется лепестковая часть ЭК (фиг. 2а), радиальная часть блокирует устье ЛВДБ, не функционирует (фиг. 2б), отмечаются выраженные разрастания грануляционной ткани вокруг ЭК (фиг. 2в, 2г), лепестковая часть покрыта налетом коричневого цвета (фиг. 26, 2в, 2г). Устья остальных бронхов 1-5 порядка с обеих сторон открыты не деформированы, слизистая без признаков воспаления.
Произведена криоэкстракция ЭК из устья ЛВДБ (криозонд 1,9 мм экспозиция 9 сек) (фиг. 2д).
После удаления ЭК устье ЛВДБ отечно, с выраженными разрастаниями грануляций (фиг. 2е), из устья поступает вязкий слизистый секрет.
ФВД от 30.08.2022 после удаления эндобронхиального клапана показано умеренную обструкцию мелких бронхов.
Длительность лечебной бронхоскопии от момента интубации трахеи тубусом жесткого бронхоскопа до экстубации составила 9 минут
На фиг 2 илллюстрируется последовательность выполнения криоэкстрации эндобронхиального клапана из устья левого верхнедолевого бронха при лечебной бронхоскопии у пациентки В:
а) лепестковая часть ЭК в просвете левого главного бронха при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
б) радиальная часть ЭК в устье левого верхнедолевого бронха при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
в) налет коричневого цвета на деформированной резине лепестковой части ЭК при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
г) разрастание грануляционной ткани вокруг радиальной части ЭК в устье ЛВДБ. Радиальная часть ЭК практически не визуализируется из-за грануляций вокруг при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ15 J10, видеосистема Pentax DEFINA);
д) момент «замораживания» - криовоздействия на эндобронхиальный клапан криозондом 1,9 мм (криостанция Erbe Cryo II, Erbe Elektromedizin, Germany), экспозиция 9 секунд;
е) вид устья левого верхнедолевого бронха после криоэкстракции. В дистальной части просвета левого главного бронха визуализируется крупная грануляция над левой междолевой шпорой.
Клиническое наблюдение №3.
Пациент И., 33 лет, 21.01.1989 года рождения с рецидивом туберкулеза легких.
Пациент в 2011 г. болел туберкулезом легких, обратился в лечебно-профилактическое учреждение, где получал терапию по I РХТ с положительной динамикой, далее выписан для продолжения лечения в ПТД по м/ж, где пациент самостоятельно прервал лечение и далее не лечился.
С конца 2017 г по апрель 2019 г с разной периодичностью проживал в странах Азии: Китай, Тайланд, Индонезия. По возвращении в Россию возобновился кашель, со слизисто-гнойной мокротой, отмечались повышение температуры тела до 39,4°С, инспираторная одышка при незначительной физической нагрузке, потливость по ночам, потеря массы тела. Самостоятельно обратился в ФГБНУ ЦНИИТ для дообследования и лечения, госпитализирован в 1 т.о. 11.06.19, где установлен диагноз: Фиброзно-кавернозный туберкулез легких в фазе инфильтрации и обсеменения. МБТ (+). Лекарственно устойчивый (устойчивость к изониазиду, этионамиду, этамбутолу) Сахарный диабет 2 типа. ЛУ МБТ тест-системой СИНТОЛ от 18.06.19 №19-4100 - к R Fq чувствительные, к Н устойчивые. Результат исследования лекарственной чувствительности культуры МБТ в системе ВАСТЕС MGIT 960 от 17.06.19: ЛУ к Н, Е, Et; ЛЧ к R, Z, Am, Cm, lfx. Получал терапию по индивидуальному РХТ с учетом данных ЛУ МБТ и индивидуальной непереносимости ПТП (циклосерин -эпизоды агрессии, линезолид - полинейропатия) с 26.06.19 г в объеме рифампицин 0,45, амикацин 0,5, моксифлоксацин 0,4, бедаквилин на фоне патогенетической и симптоматической терапии.
18.12.19 г пациенту выполнена ЭКББ устья правого верхнедолевого бронха для формирования локального коллапса верхней доли правого легкого. Далее пациент был выписан под наблюдение фтизиатра по месту жительства
07.07.20 г. повторно обратился в консультативное отделение ФГБНУ ЦНИИТ с жалобами на навязчивый сухой кашель. На КТ ОГК от 07.07.20 отмечено состояние после установки ЭК в устье ПВДБ, определяются гигантские раздутые фиброзные полости в верхних отделах легких, больше слева. В начале июля 2020 повторно консультирован эндоскопистом. С целью коллапсотерапии гигантской полости распада в верхней доле левого легкого в июле 2020 г. была проведена ЭКББ устья ЛВДБ с установкой ЭК №11.
В марте 2021 г. появились жалобы на сухой, навязчивый кашель. Пациент повторно обратился в центр диагностики и реабилитации заболеваний органов дыхания с целью рассмотрения возможности стационарного лечения в условиях института. Находился в 1 т/о с 22.03.21 г. по 2.04.21 г, где 31.02.21 г. выполнена ФБС оценкой устья ПВДБ справа и состояния ЭК (корректная установка эндобронхиального клапана) и была продолжена противотуберкулезная химиотерапия. После выписка противотуберкулезная химиотерапия была завершена. Далее наблюдался в ПТД по м/ж.
20.07.22 г. обратился с жалобами на кашель с мокротой с резиновым привкусом, в связи с чем госпитализирован в 1 т.о. для удаления эндобронхиального клапана из устья ПВДБ.
Учитывая сложность ведения пациента (снижение вентиляционной способности легких, длительность ЭКББ устья ПВДБ в течение 33 месяцев, наличие сахарного диабета (СД) 2 типа и выраженных реакций непереносимости лекарственных препаратов с возникновением серьезных нежелательных явлений) принято решение о проведении удаления ЭК из устья ПВДБ с применением метода криоэкстрации в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа с ВЧ вентиляцией и тотальной внутривенной анестезией. Была выполнена криоэкстрации ЭК из устья ПВДБ этапы которой представлены на фиг. 3.
30.09.2022 в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа (Фридель №11) с ВЧ вентиляцией и тотальной внутривенной анестезией, оценено состояние ЭК, находящихся в устьях ЛВДБ и ПВДБ. Устья главных бронхов - открыты. В устье правого главного бронха - видна лепестковая часть ЭК, в устье ПВДБ умеренное разрастание грануляционной ткани вокруг радиальных лепестков, клапан не функционирует (фиг. 3г). Слева ЛГБ - проходим. В устье в/долевого бронха определяется лепестковая часть ЭК, имеет изъеденный рельеф, не функционирует, покрыта коричнево-черным налетом. Остальные бронхи правого и левого легких открыты, без особенностей, слизистая - умеренно гиперемирована, сосудистый рисунок сглажен.
Выполнена криоэкстракция ЭК из устья ПВДБ криозондом 1,9 мм экспозиция 7 сек (рисунок 3д).
После удаления ЭК - устье осмотрено, поступление секрета в небольшом количестве, явления стенозирования и грануляций - не выражены.
ЭК удален полностью, осмотрен после извлечения, разрывов и фрагментирования не найдено (фиг. 3е).
После удаления ЭК: устье ПВДБ осмотрено, поступление секрета в небольшом количестве, явления стенозирования и грануляций - не выражены.
Длительность лечебной бронхоскопии от момента интубации трахеи тубусом жесткого бронхоскопа до экстубации составила 6 минут.
Клиническое наблюдение демонстрирует, что выбранная технология криоэкстракции ЭК у пациента с наличием коморбидности (СД2), со снижением вентиляционной способности легкого и двусторонней билатеральной клапанной бронхоблокацией верхнедолевых бронхов справа и слева заняла малое время и позволила быстро выполнить удаление ЭК без развития каких-либо осложнений со стороны слизистой ТБД, так и вентиляционной способности пациента.
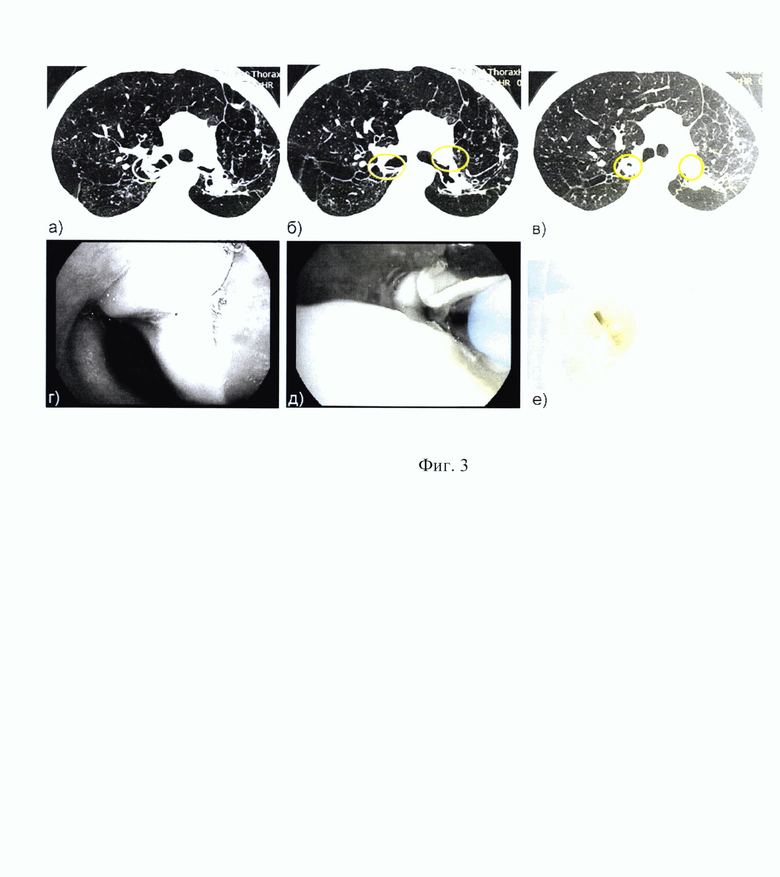
На фиг. 3 представлены этапы подготовки и выполнения криоэкстрации эндобронхиального клапана при лечебной бронхоскопии у пациента И:
а) КТ ОГК пациента И., аксиальное легочное окно, перед лечебной бронхоскопией: в устье правого верхнедолевого бронха (ПВДБ) определяется эндобронхиальный клапан (визуализируются его радиальная часть - «головка», обтурирующая устье ПВДБ и лепестковая часть («хвост») в просвете правого главного бронха (выделены желтым цветом);
б) КТ ОГК пациента И., аксиальное легочное окно, перед лечебной бронхоскопией: в просветах правого главного бронха (ПГБ) и левого главного бронха определяются эндобронхиальные клапаны (визуализируются их и лепестковые части («хвост») (выделены желтым цветом);
в) КТ ОГК пациента И., аксиальное легочное окно, перед лечебной бронхоскопией: в просветах правого верхнедолевого бронха (ПВДБ) и левого верхнедолевого бронха (ЛВДБ) определяются эндобронхиальные клапаны (визуализируются их радиальные части («головки») (выделены желтым цветом);
г) лепестковая часть ЭК с разрастанием грануляционной ткани в просвете правого главного бронха при бронхоскопии высокого разрешения в условиях интубации тубусом ригидного бронхоскопа (гибкий видеобронхоскоп Pentax ЕВ 15 J10, видеосистема Pentax DEFINA);
д) момент «замораживания» - криовоздействия на эндобронхиальный клапан криозондом 1,9 мм (криостанция Erbe Cryo II, Erbe Elektromedizin, Germany), экспозиция 7 секунд;
е) вид эндобронхиального клапана, после криоэкстракции, определяются неповрежденные лепестковая и радиальная части эндобронхиального клапана.
Таким образом, в предложении достигается требуемый технический результат, который заключается в упрощении и ускорении процесса удаления эндобронхиальных клапанов (ЭК) и снижения уровня низкотемпературного воздействия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭНДОСКОПИЧЕСКОЙ ДИАГНОСТИКИ САРКОИДОЗА ОРГАНОВ ДЫХАНИЯ ПУТЕМ СЕРИЙНОЙ ЭНДОБРОНХИАЛЬНОЙ КРИОБИОПСИИ | 2024 |
|
RU2836009C1 |
| Способ лечения туберкулеза легких и бронхов при различных рентгенологических синдромах | 2023 |
|
RU2826098C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЭНДОСКОПИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ОПУХОЛЕВЫМИ СТЕНОЗАМИ БИФУРКАЦИИ ТРАХЕИ И БРОНХОВ 1-3 ПОРЯДКА | 2024 |
|
RU2835734C1 |
| Способ лечения рубцовых и компрессионных стенозов трахеи | 2021 |
|
RU2771934C1 |
| СПОСОБ АБЛЯЦИИ ОБРАЗОВАНИЙ, СТЕНОЗИРУЮЩИХ ПРОСВЕТ ПОЛЫХ ОРГАНОВ | 2013 |
|
RU2531974C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ ДЕСТРУКТИВНЫМИ ФОРМАМИ ТУБЕРКУЛЕЗА ЛЕГКИХ | 2009 |
|
RU2413471C1 |
| СПОСОБ ЛЕЧЕНИЯ СТЕНОЗОВ ТРАХЕИ | 2009 |
|
RU2391929C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ ПАТОЛОГИЕЙ ОРГАНОВ ДЫХАНИЯ, ОСЛОЖНЕННОЙ ЛЕГОЧНЫМИ КРОВОТЕЧЕНИЯМИ | 1998 |
|
RU2140211C1 |
| СПОСОБ ЛЕЧЕНИЯ ПОЛОСТЕЙ РАСПАДА В ЛЕГКОМ, ОСЛОЖНЕННЫХ ХРОНИЧЕСКИМ АСПЕРГИЛЛЕЗОМ (МИКОЗОМ) | 2020 |
|
RU2749489C1 |
| СПОСОБ ЛЕЧЕНИЯ РУБЦОВЫХ СТЕНОЗОВ ТРАХЕИ | 2012 |
|
RU2484780C1 |
Изобретение относится к медицине, а именно к хирургии. Проводят криовоздействие на грануляционную ткань вокруг радиальной части эндобронхиальных клапанов в режиме криодевитализации. Осуществляют последовательно нескольких циклов, в каждом из которых грануляционную ткань замораживают на 20 с до температуры -80°С с последующим оттаиванием. Затем осуществляют рывок и отделение эндобронхиального клапана. Способ позволяет упростить и ускорить процесс удаления эндобронхиальных клапанов, снизить уровень низкотемпературного воздействия. 2 з.п. ф-лы, 3 ил., 3 пр.
1. Способ экстракции эндобронхиальных клапанов, включающий процедуру криовоздействия, отличающийся тем, что во время процедуры воздействуют на грануляционную ткань вокруг радиальной части эндобронхиальных клапанов в режиме криодевитализации и осуществляют последовательно нескольких циклов, в каждом из которых грануляционную ткань замораживают на 20 с до температуры -80°С, с последующим оттаиванием, и затем осуществляют рывок и отделение эндобронхиального клапана.
2. Способ по п. 1, отличающийся тем, что в процедуре криовоздействия используют 3 цикла криодевитализации.
3. Способ по п. 1, отличающийся тем, что процедуру криовоздействия повторяют через 1-2 недели.
| Способ определения влажности дерева и тому подобных материалов | 1939 |
|
SU58898A1 |
| Данилевская О.В и др./ Криотехнологии в эндоскопической диагностике и лечении заболеваний дыхательных путей | |||
| Что нужно, чтобы начать? / Эндоскопическая хирургия | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| DiBardino DM et.al | |||
| /Bronchoscopic Cryotherapy | |||
| Clinical applications of the cryoprobe, cryospray, and cryoadhesion/ Ann Am Thorac Soc | |||
| Токарный резец | 1924 |
|
SU2016A1 |
Авторы
Даты
2025-04-01—Публикация
2023-07-10—Подача