ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к биомаркерам для прогнозирования, диагностики и стратификации риска лиц с ишемией миокарда или головного мозга или связанным с ней ишемическим повреждением тканей, а также для проявления рецидивирующих ишемических событий у лиц со стабильной ишемической болезнью сердца (ИБС).
УРОВЕНЬ ТЕХНИКИ
Острые коронарные синдромы (ОКС) и цереброваскулярные нарушения являются наиболее частыми клиническими проявлениями атеротромбоза и составляют основную причину смерти и инвалидности по всему миру. Ранняя диагностика имеет большое значение в связи с важностью ранней реваскуляризации и высоким риском смерти и/или потери качества жизни. В данном контексте биомаркеры представляются важными инструментами для дополнения клинических анализов для диагностики, сортировки, стратификации риска и лечения пациентов с предполагаемыми ОКС, а также для установления различий между ишемическим и геморрагическим инсультом. Эти биомаркеры должны быть информативными в отношении патологического процесса и должны составлять альтернативу более сложным и дорогостоящим методикам диагностики (таким как магнитно-резонансная, помимо прочего).
В действительности высокий процент случаев поступления в отделение неотложной помощи связан с экстракардиальными нарушениями, симптомы проявления которых аналогичны симптомам кардиальных ишемических событий (боль в связи с дыхательными или мышечными патологиями). В случае цереброваскулярного заболевания существует насущная необходимость в наличии дискриминаторов геморрагического и ишемического инсульта, обеспечивающих возможность правильного и быстрого начала лечения пациентов.
Таким образом, существует неудовлетворенная потребность в определении новых биомаркеров для раннего, специфического и чувствительного выявления ишемии. К настоящему моменту исследованы маркеры воспаления, сердечной функции и некроза. Однако неясно, можно ли использовать их измерение для диагностики и прогнозирования ишемических синдромов. Ишемическое повреждение органов, как правило, предшествует некрозу тканей и при своевременном выявлении оно является обратимым. Такое отсутствие применяемых маркеров для точного и раннего выявления ишемии влечет за собой повышенные необязательные экономические издержки по всему миру.
В настоящее время диагностика и лечение острых коронарных синдромов (ОКС) основываются на клинических анализах, результатах электрокардиограммы и уровнях тропонина (единственная группа принятых биомаркеров). Применение данного протокола сопряжено с несколькими ограничениями, которые вызывают необходимость в поиске новых биомаркеров для лечения пациентов с ишемией миокарда. Первый недостаток заключается в том, что сердечные тропонины (cTn) - это маркеры необратимого некроза (гибели клеток), поздней стадии поражения миокарда. Кроме того, высокочувствительные анализы на cTn (hs-cTn) показали определенную неспецифичность. Кроме того, в текущих руководствах подчеркивается необходимость выполнения последовательных измерений hs-cTn для надлежащей сортировки пациентов с острой болью в груди.
Способ определения ишемического повреждения тканей на основе изменения профиля распределения изоформ аполипопротеина J (Аро J) был описан в публикации WO 2011098645, а также у Cubedo, J., et al., (J. Proteome Res., 2011, 10: 211-220). В этих исследованиях две различные группы изоформ Аро J - Аро J-15 и Аро J-29, определялись с использованием двумерного электрофореза с последующей масс-спектрометрией. Эти формы Аро J были связаны с повреждением тканей и, в частности, с повреждением сердца, вызванным ОИМ. При ишемическом повреждении своевременное и точное выявление ишемического события имеет ключевое значение для предотвращения его прогрессирования, которое может привести к необратимому повреждению тканей. В данном сценарии способ, основанный на двумерном электрофорезе с масс-спектрометрией для определения изменений в профиле распределения Аро J, нельзя использовать в клинической практике, поскольку он является слишком сложным, длительным и дорогостоящим для диагностики ишемии.
Таким образом, в области техники существует необходимость в усовершенствованных способах выявления повреждений сосудов и ОИМ, в частности.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Согласно первом объекту, изобретение относится к способу диагностики ишемии или ишемического повреждения тканей у пациента, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, или к способу диагностики ишемии или ишемического повреждения тканей у пациента, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, который способен специфически связываться с лектином Datura stramonium, или уровней гликозилированного Аро J, который способен специфически связываться с лектином Triticum vulgaris.
Согласно первому объекту ишемия может представлять собой ишемию миокарда или головного мозга.
Согласно первому объекту ишемия миокарда может представлять собой острую ишемию миокарда или микрососудистую стенокардию.
Согласно первому объекту ишемия головного мозга может представлять собой инсульт.
Согласно первому объекту пациент может предположительно переносить ишемическое событие.
Согласно первому объекту определение могут осуществлять в течение первых 6 часов после начала предполагаемого ишемического события, до повышения уровней, по меньшей мере, одного маркера некроза или до получения пациентом любого лечения для предполагаемого ишемического события.
Согласно второму объекту, изобретение относится к способу прогнозирования прогрессирования ишемии у пациента, перенесшего ишемическое событие, или определения прогноза у пациента, перенесшего ишемическое событие, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, в котором пониженные уровни гликозилированного Аро J по отношению к опорному значению указывают на прогрессирование ишемии или неблагоприятный прогноз для пациента.
Согласно второму объекту гликозилированный Аро J может представлять собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc), или гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты.
Согласно второму объекту ишемическое событие может представлять собой миокардиальное ишемическое событие.
Согласно второму объекту миокардиальное ишемическое событие может представлять собой инфаркт миокарда с подъемом сегмента ST.
Согласно второму объекту прогноз для пациента могут определять как риск рецидива в течение 6 месяцев, риск больничной смертности или риск смертности в течение 6 месяцев.
Согласно еще одному объекту, изобретение относится к способу определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, в котором пониженные уровни гликозилированного Аро J по отношению к опорному значению указывают на повышенный риск возникновения у пациента рецидивирующего ишемического события.
Согласно еще одному объекту гликозилированный Аро J может представлять собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc), или гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты.
Согласно еще одному объекту пациент, страдающий стабильной ишемической болезнью, мог переносить острый коронарный синдром перед стабильной ишемической болезнью сердца.
Согласно еще одному объекту рецидивирующее ишемическое событие может представлять собой острый коронарный синдром, инсульт или преходящее ишемическое событие.
Согласно еще одному объекту уровень гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), может соответствовать уровню Аро J, способного специфически связываться с лектином Datura stramonium, или в котором уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) или сиаловой кислоты, могут соответствовать уровням Аро J, способного специфически связываться с лектином Triticum vulgaris.
Согласно еще одному объекту образец может представлять собой биологическую жидкость.
Согласно еще одному объекту биологическая жидкость может представлять собой плазму или сыворотку крови.
Согласно еще одному объекту, изобретение относится к набору, содержащему:
a. Первый реактив, представляющий собой лектин, который специфически связывается с гликановым остатком, выбранным из N-ацетилглюкозамина и сиаловой кислоты, и
b. Второй реактив, который способен специфически связываться с полипептидом Аро J.
Согласно еще одному объекту лектин может представлять собой лектин из Triticum vulgaris, лектин из Datura stramonium или их сочетание.
Согласно еще одному объекту второй реактив может представлять собой антитела или их фрагменты, содержащие антигенсвязывающую область.
Согласно еще одному объекту первый реактив может быть иммобилизирован.
Согласно еще одному объекту второй реактив может содержать метку.
Согласно еще одному объекту метка может быть определена посредством изменения по меньшей мере одного из ее химических, электрических или магнитных свойств.
Согласно еще одному объекту третий реактив может быть выполнен с возможностью специфически связываться со вторым реактивом.
Согласно еще одному объекту третий реактив может представлять собой антитела или их фрагменты, содержащие антигенсвязывающую область.
Согласно еще одному объекту, изобретение относится к набору в соответствии с изобретением для диагностики ишемии или ишемического повреждения тканей у пациента, для определения прогрессирования ишемии у пациента, перенесшего ишемическое событие, для определения прогноза у пациента, перенесшего ишемическое событие, или для определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью.
Согласно еще одному объекту, изобретение относится к способу определения гликозилированного Аро J в образце, содержащем этапы:
(i) Введения образца в контакт с лектином, который специфически связывается с гликановым остатком, присутствующим в гликозилированном Аро J, при условиях, подходящих для образования комплекса между гликозилированным Аро J из образца и лектином, и
(ii) Определения количества комплекса, содержащего лектин и гликозилированный Аро J.
Согласно еще одному объекту лектин, используемый на этапе (i), может представлять собой лектин, который специфически связывается с N-ацетилглюкозамином, или лектин, который специфически связывается с N-ацетилглюкозамином и сиаловой кислотой.
Согласно еще одному объекту лектин, который специфически связывается с N-ацетилглюкозамином, может представлять собой лектин Datura stramonium, или, когда лектин специфически связывается с N-ацетилглюкозамином и сиаловой кислотой, он представляет собой лектин Triticum vulgaris.
Согласно еще одному объекту лектин, который специфически связывается с гликановым остатком, иммобилизирован.
Согласно еще одному объекту комплекс на этапе (ii) могут обнаруживать с использованием реактива, который специфически связывается с полипептидом Аро J.
Согласно еще одному объекту реактив, который специфически связывается с полипептидом Аро J, может представлять собой антитела или их фрагменты, содержащие антигенсвязывающую область.
Согласно еще одному объекту антитела могут быть связаны с обнаруживаемой меткой.
Согласно еще одному объекту метка может быть определена посредством изменения, по меньшей мере, одного из ее химических, электрических или магнитных свойств.
Согласно еще одному объекту обнаружение могут осуществлять с использованием реактива, способного специфически связываться с реактивом, который специфически связывается с полипептидом Аро J.
Согласно еще одному объекту третий реактив, способным специфически связываться с реактивом, который специфически связывается с полипептидом Аро J, может представлять собой антитела или их фрагменты, содержащие антигенсвязывающую область.
Согласно еще одному объекту определение уровня гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, могут выполнять с использованием вышеуказанных набора или способа.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1. Профиль Аро J 2-DE. Репрезентативная структура кластера Аро J в 2-DE из контрольного образца сыворотки и образца сыворотки пациента с ишемией до ОИМ. Аро J в сыворотке был определен как кластер из 13 пятен с pI в диапазоне от 4,5 до 5,0 и молекулярной массой от 37,1 до 47,3 кДа. Пятна, определенные как Аро J, были пронумерованы от кислого к основному рН. Пятно 2 наблюдалось только у пациентов с ишемией до ОИМ. Обратите внимание, что пятна с обозначениями 1, 3, 7, 8, 10, 11 и 13 показывали повышенные уровни обнаружения при ишемии до ОИМ, тогда как пятна 6 и 9 показывали сниженную интенсивность в гелях образцов пациента с ишемией до ОИМ по сравнению с контрольной группой. Пятна 3, 7, 8 и 11 представляют собой Аро J-29, а пятна 6 и 9-Аро J-15.
Фигура 2. Гликозилированные формы Аро J. Репрезентативные изображения 2-DE кластера Аро J в гликозилированной фракции сыворотки (выделенной путем ее связывания со смесью конкавалина А и лектинов Triticum vulgaris), полученной у здоровых доноров и пациентов с ишемией до ОИМ. Было определено шесть пятен (1, 2, 4, 5, 8 и 11), соответствующих по pI и ММ пятнам, определенным для цельной сыворотки. Как и для фигуры 1, пятна были пронумерованы от кислого к основному рН. Интенсивность пятен Аро J была ниже у пациентов с ишемией до ОИМ по сравнению с контролями. Снижение было наиболее выраженным для пятен 4 и 8.
Фигура 3. О-гликозилированные формы Аро J. Представительное изображение 2-DE кластера Аро J в О-гликозилированной фракции сыворотки (выделенный путем ее связывания с лектином Artocarpus integrifolia). Было определено девять пятен (1, 3, 4, 6, 7, 8, 9, 11 и 12), соответствующих по pI и ММ пятнам, определенным для цельной сыворотки. Как и для фигур 1 и 2, пятна были пронумерованы от кислого к основному рН.
Фигура 4. Относительное содержание гликозилированных форм Аро J. Столбчатая диаграмма, показывающая относительное содержание различных гликозилированных форм Аро J в образцах плазмы крови человека на основании специфических измерений с использованием нового оригинального иммуноаффинного анализа ферментативного гликозилирования, или EGA.
Фигура 5. Диагностическое значение. (А) Коробчатая диаграмма, показывающая уровни Аро J-GlcNAc+Neu5Ac+Аро J-GlcNAc на ранней стадии ишемии (N=38) и у здоровых участников (N=144). (В) Рабочая характеристическая кривая (ROC), отображающая диагностическое значение для определения наличия ишемии миокарда уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc с площадью под кривой (AUC) 0,934 (Р<0,0001) и пороговым значением 332цмкг/мл при чувствительности 97% и специфичности 71%.
Фигура 6. Диагностическое значение у пациентов с инфарктом миокарда с подъемом сегмента ST (MMnST). (А) Коробчатая диаграмма, показывающая уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у пациентов с MMnST на момент госпитализации (N=212) и у здоровых участников (N=144). (В) Рабочая характеристическая кривая (ROC), отображающая дискриминирующее значение для определения наличия ишемии уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc с площадью под кривой (AUC) 0,713 (Р<0,0001) и пороговым значением 409 μмкг/мл при чувствительности 80% и специфичности 53%. (С) Коробчатая диаграмма, показывающая уровни Аро J-GlcNAc у пациентов с MMnST на момент госпитализации (N=340) и у здоровых участников (N=139). (D) Рабочая характеристическая кривая (ROC), отображающая дискриминирующее значение для определения наличия ишемии уровней Аро J-GlcNAc с площадью под кривой (AUC) 0,830 (Р<0,0001) и пороговым значением 393 μмкг/мл при чувствительности 81% и специфичности 72%.
Фигура 7. Прогрессирование ишемии. (А) График регрессии, отображающий значимую обратную корреляцию между уровнями Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc на момент госпитализации и временем ишемии. (В) Коробчатая диаграмма, показывающая последовательное снижение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у 82 пациентов с HMnST через 3 суток после госпитализации (t=72 ч). (С) График регрессии, отображающий значимую обратную корреляцию между уровнями Аро J-GlcNAc на момент госпитализации и временем ишемии.
Фигура 8. Прогностическое значение. Коробчатые диаграммы, показывающие значимое различие уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc на момент госпитализации по отношению к (А) конечной степени кровотока по классификации TIMI, которая, по известным данным, непосредственно связана с больничной смертностью и смертностью в течение 6 месяцев, и (В) наличию кардиогенного шока (65 пациентов имели кардиогенный шок, 147 - нет), который связан с более неблагоприятным прогнозом после перенесенного MMnST.
Фигура 9. Стратификация риска. (А) График регрессии, отображающий значимую обратную корреляцию между уровнями Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc на момент госпитализации и оценкой риска по шкале GRACE. (В)
Коробчатая диаграмма, показывающая связь между самыми высокими значениями оценки риска по шкале GRACE и снижением уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc через 3 дня после госпитализации у пациентов с HMnST. (С) График регрессии, отображающий значимую обратную корреляцию между уровнями Аро J-GlcNAc на момент госпитализации и оценкой риска по шкале GRACE.
Фигура 10. Рецидивирующие события и смертность в 6-месячный период последующего наблюдения пациентов с HMnST. Кривые Каплана-Мейера, показывающие зависимость: уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc (А) и тропонина Т (В) при госпитализации и возникновения рецидивирующего ишемического события или смерти через 6 месяцев последующего наблюдения; уровней Аро J-GlcNAc при госпитализации и смертности (С) или сочетания рецидивирующего ишемического события и смерти (D) через 6 месяцев последующего наблюдения.
Фигура 11. Прогностическое значение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в плазме крови. (А) Схема, отображающая время взятия образцов и последующего наблюдения пациентов со стабильной ИБС: пациенты страдали острым коронарным синдромом (ОКС) в среднем за 0,6±0,04 года до взятия образцов и наблюдались на протяжении 2,3±0,3 года после него. (В) Коробчатая диаграмма, отображающая сравнение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у пациентов с хронической ИБС, перенесших рецидивирующее ишемическое событие в период последующего наблюдения (N=16), и у пациентов без рецидивирующего события (N=18). (С) Рабочая характеристическая кривая (ROC), отображающая прогностическое значение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc для проявления рецидивирующих ишемических событий у пациентов со стабильной ИБС.
Фигура 12. Диагностическое значение Аро J-GlcNAc+Neu5Ac+Аро J-GlcNAc при ишемии головного мозга. Коробчатая диаграмма, показывающая уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в плазме крови у пациентов, перенесших инсульт (N=174), и у здоровых участников (N=164).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Способы диагностики ишемического повреждения тканей
Авторы настоящего изобретения наблюдали, что уровни Аро J, содержащего остатки GlcNAc, или уровни Аро J, содержащего остатки GlcNAc и сиаловой кислоты (Neu5Ac), на ранней стадии ишемии снижались по отношению к уровням, наблюдаемым у контрольных участников. Несмотря на то, что корреляция между уровнями гликозилированного Аро J и сердечной ишемией у пациентов уже была описана, данное исследование было проведено путем определения уровней гликозилированного Аро J с использованием смеси лектинов, способных связываться с гликанами, содержащими остатки α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac. Этот способ не обеспечивал возможность определения форм гликозилированного Аро J, которые преимущественно позволяли отличать пациентов от контрольных участников. Авторам настоящего изобретения удалось определить гликозилированные формы Аро J, которые преимущественно позволяют отличать образцы пациентов, страдающих ишемией, от контрольных образцов. Известно, что авторами предыдущего исследования опубликованы данные, согласно которым уровень Аро J-29 возрастал при ишемии до ОИМ в противоположность тому, что наблюдается для Аро J, содержащего остатки GlcNAc, или Аро J, содержащего GlcNAc и сиаловую кислоту (Neu5Ac). Кроме того, у пациентов с ишемией до ОИМ наблюдалось 25% снижение определенных Аро J с остатками α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac, тогда как специфическое определение Аро J, содержащего остатки GlcNAc, или Аро J, содержащего GlcNAc и сиаловую кислоту (Neu5Ac), показало снижение их содержания у пациентов с ишемией до ОИМ на 45-50%. Таким образом, определение этих гликозилированных форм Аро J обеспечивает возможность диагностики ишемии с повышенной чувствительностью и специфичностью по сравнению с диагностикой, основанной на использовании гликозилированных форм Аро J, определяемых с использованием способа, описанного в предыдущем уровне техники.
Соответственно, согласно первому объекту, изобретение относится к способу (далее - способ диагностики изобретения) диагностики ишемии или ишемического повреждения тканей у пациента, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в котором пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина, по отношению к опорному значению или пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, по отношению к опорному значению указывают на то, что пациент страдает ишемией или ишемическим повреждением тканей. Изобретение также относится к способу диагностики ишемии или ишемического повреждения тканей у пациента, содержащему определение в образце упомянутого пациента гликозилированного Аро J, который способен специфически связываться с лектином Datura stramonium, или уровней гликозилированного Аро J, который способен специфически связываться с лектином Triticum vulgaris, в котором пониженные уровни гликозилированного Аро J, который способен специфически связываться с лектином Datura stramonium, или пониженные уровни гликозилированного Аро J, который способен специфически связываться с лектином Triticum vulgaris, по отношению к опорному значению указывают на то, что пациент страдает ишемией или ишемическим повреждением тканей.
Способ диагностики изобретения является особенно полезным, поскольку он обеспечивает возможность определения острого ишемического события до наступления необратимых некротических повреждений соответствующего органа или ткани (независимо от уровней тропонина в случае ОКС). Это обеспечивает диагностическое значение для определения наличия ишемии в течение уже первых шести часов после начала события.
В контексте настоящего изобретения термин «диагностика» относится к способности установления различий между образцами пациентов с ишемией миокарда или головного мозга либо связанными с ними ишемическими повреждениями тканей и образцами лиц, не страдающих данными патологиями и/или повреждениями, применительно способу, описанному в настоящей заявке. Данное определение, как должно быть понятно специалисту в данной области техники, не предусматривает получение на 100% правильных результатов для всех образцов. Однако для него требуется правильная классификация статистически значимого количества проанализированных образцов. Количество, которое является статистически значимым, может быть установлено специалистом в данной области с использованием различных средств статистического анализа, например, но не ограничиваясь, путем определения доверительных интервалов, определения р-значения, критерия Стьюдента и дискриминантной функции Фишера. Предпочтительно, доверительные интервалы составляют, по меньшей мере, 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 98% или меньше 99%. Предпочтительно, р-значение составляет меньше 0,05, 0,01, 0,005 или 0,0001. Предпочтительно, настоящее изобретение способно правильно выявлять ишемию или ишемические повреждения у по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или, по меньшей мере, 90% участников определенной испытуемой группы или популяции.
Термин «ишемия» используется здесь взаимозаменяемо с термином «ишемическое событие» и относится к любой ситуации, связанной со снижением или прекращением кровотока к органу или ткани. Ишемия бывает преходящей или постоянной.
Выражения «ишемическое повреждение тканей», «ишемическое поражение тканей», «повреждение тканей вследствие ишемии», «повреждение тканей, связанной с ишемией», «повреждение тканей в результате ишемии», «повреждение тканей, вызванное ишемией» и «ишемически поврежденные ткани» относятся к морфологическим, физиологическим и/или молекулярным повреждениям органа, ткани или клеток в результате периода ишемии.
В одном варианте осуществления повреждения, вызванные ишемией, представляют собой повреждения сердечной ткани. В еще более предпочтительном варианте осуществления повреждения сердечной ткани вызваны инфарктом миокарда.
Термин «ишемия миокарда» относится к нарушениям кровообращения, обусловленным атеросклерозом коронарных сосудов и/или недостаточным снабжением миокарда кислородом. Например, острый инфаркт миокарда представляет собой необратимый ишемический инсульт ткани миокарда. Этот инсульт происходит в результате окклюзивного (например, тромботического или эмболического) явления в коронарном кровообращении и создает среду, в которой метаболические требования миокарда превышают подачу кислорода к ткани миокарда.
В еще одном варианте осуществления повреждения вызваны микрососудистой стенокардией. Используемый здесь термин «микрососудистая стенокардия» относится к состоянию, вызванному недостаточным кровотоком через малые сердечные кровеносные сосуды.
В одном варианте осуществления повреждения, вызванные ишемией, представляют собой повреждения ткани головного мозга. В еще одном варианте осуществления, повреждения ткани головного мозга вызваны ишемическим инсультом. Термин «ишемический инсульт» относится к внезапной потере функции головного мозга, вызванной закупоркой кровеносного сосуда к головному мозгу (которая приводит к недостатку поступления кислорода в мозг), которая характеризуется потерей контроля над мышцами, снижением или потерей восприятия или сознания, головокружением, невнятной речью или другими симптомами, которые зависят от объема и степени тяжести повреждений головного мозга, также именуется инсультом или острым нарушением мозгового кровообращения. Термин «ишемия головного мозга» (или «инсульт») также относится к недостаточному притоку крови к головному мозгу, что часто приводит к недостаточному поступлению кислорода в головной мозг.
Термин «участник» или «лицо», или «животное», или «пациент» включает любого пациента, в частности, пациента-млекопитающего, для которого предназначается терапия. Пациенты-млекопитающие включают людей, домашних животных, сельскохозяйственных животных, животных из зоопарков и домашних питомцев, таких как собаки, кошки, морские свинки, кролики, крысы, мыши, лошади, крупный рогатый скот, коровы и т.д. В предпочтительном варианте осуществления изобретения пациент представляет собой млекопитающее. В более предпочтительном варианте осуществления изобретения пациент представляет собой человека.
Используемый здесь термин «образец» или «биологический образец» относится к биологическому материалу, выделенному у пациента. Биологический образец содержит любой биологический материал, пригодный для определения уровней гликозилированных форм заданного белка, например, Аро J. Образец может быть выделен из любой подходящей ткани или биологической жидкости, такой как, например, кровь, слюна, плазма, сыворотка, моча, спинномозговая жидкость (СМЖ) или кал. В конкретном варианте осуществления образец представляет собой образец ткани или биологической жидкости. В более конкретном варианте осуществления изобретения биологическая жидкость выбрана из группы, состоящей из крови, сыворотки или плазмы.
Предпочтительно образец, который используется для определения уровней гликозилированных форм Аро J, представляет собой образец того же типа, который используется для определения опорного значения, в том случае, если определение носит относительный характер. В качестве примера, если определение Аро J, содержащего остатки GlcNAc, или Аро J, содержащего остатки GlcNAc и сиаловой кислоты, выполняется в образце плазмы крови, в таком случае для определения опорного значения также используется образец плазмы. Если образец представляет собой биологическую жидкость, опорный образец также представляет собой биологическую жидкость того же типа, например, кровь, сыворотку, плазму, спинномозговую жидкость.
Используемый здесь термин Аро J относится к полипептиду, также известному как «кластерин», «тестостерон-репрессированный предстательный транскрипт», «аполипопротеин J», «комплемент-связанный белок SP-40,40», «ингибитор цитолиза комплемента», «ингибитор лизиса комплемента», «сульфатированный гликопротеин», «Ku70-связывающй белок», «NA1/NA2», «TRPM-2», «KUB1», «ИЛК». Аро J человека - это полипептид, зарегистрированный под номером доступа Р10909 в базе данных UniProtKB/Swiss-Prot (версия записи 187 от 16 марта 2016 года).
Используемый здесь термин «Аро J, содержащий остатки GlcNAc» относится к любой молекуле Аро J, содержащей по меньшей мере один повтор GlcNAc в по меньшей мере одной гликановой цепи, хотя, как правило, Аро J содержит по меньшей мере один N-ацетилглюкозамин в каждой гликановой цепи. «Аро J, содержащий остатки GlcNAc» включает молекулы Аро J, содержащие по меньшей мере один остаток GlcNAc в высокоманнозных N-гликанах, N-гликанах комплексного типа, олигосахаридах N-гликанах гибридного типа или О-гликанах. В зависимости от типа N-гликанов GlcNAc может быть прикреплен непосредственно к полипептидной цепи или в дистальном положении N-гликана.
Термин «GlcNAc» или «N-ацетилглюкозамин» относится к производной глюкозы, полученной амидированием глюкозамина уксусной кислотой и имеющей общую структуру:
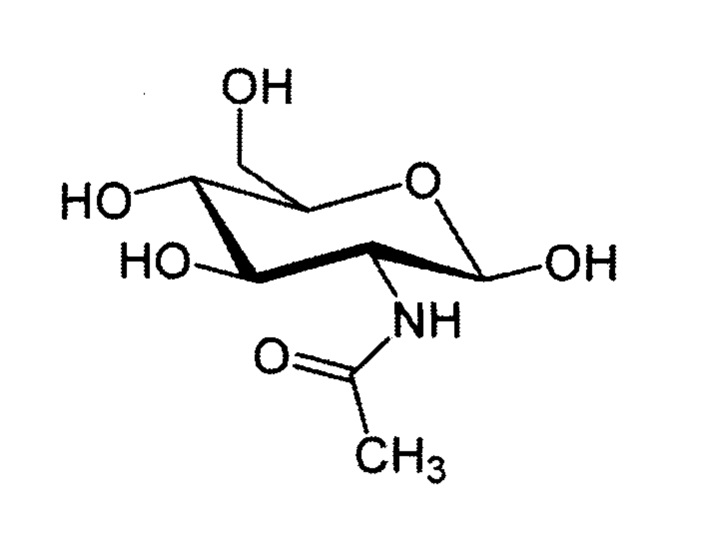
В одном варианте осуществления Аро J, содержащий остатки GlcNAc, содержит два остатка GlcNAc и именуется по тексту настоящей заявки как (GlcNAc)2. Молекулы Аро J, содержащие остатки (GlcNAc)2, включают молекулы, в которых (GlcNAc)2 содержится в высокоманнозных N-гликанах, N-гликанах комплексного типа, олигосахаридах N-гликанах гибридного типа или О-гликанах. В зависимости от типа N-гликанов (GlcNAc)2 может быть прикреплен непосредственно к полипептидной цепи или в дистальном положении N-гликана.
В предпочтительном варианте осуществления уровень гликозилированного Аро J, содержащего остатки GlcNAc или (GlcNac)2, определяется как уровень Аро J, способного специфически связываться с лектином Datura stramonium.
Под термином «специфическое связывание» при использовании в настоящем изобретении для обозначения связывания с лектином гликозилированной формы Аро J понимается способность лектина связываться специфически с гликозилированной формой Аро J в связи с наличием комплементарности между трехмерными структурами двух молекул с существенно более высокой аффинностью к неспецифическому связыванию, так что связывание между упомянутым лектином и гликозилированной формой Аро J предпочтительно происходит до связывания любой из упомянутых молекул по отношению к другим молекулам, присутствующим в реакционной смеси. Это приводит к тому, что лектин не дает перекрестных реакций с другими гликанами, которые могут как присутствовать, так и отсутствовать в молекуле Аро J. Перекрестная реактивность исследуемого лектина может быть испытана, например, путем оценки связывания упомянутого лектина в обычных условиях с соответствующим гликаном, а также с рядом более или менее (структурно и/или функционально) близкородственных гликанов. Только если лектин связывается с соответствующим гликаном, но не связывается или по существу не связывается с любыми иными гликанам, он считается специфическим к соответствующему гликану. Например, связывание может считаться специфическим если аффинность связывания между лектином и гликозилированным Аро J имеет константу диссоциации (Kd) менее 10-6 М, менее 10-7 М, менее 10-8 М, менее 10-9 М, менее 10-10 М, менее 10-11 М, менее 10-12 М, менее 10-13 М, менее 10-14 М или менее 10-15 М.
В предпочтительном варианте осуществления «Аро J, содержащий остатки GlcNAc», по существу, не содержит N-связанные или О-связанные углеводы других типов. В одном варианте осуществления «Аро J, содержащий остатки GlcNAc», не содержит N-связанные или О-связанные α-маннозные остатки. В другом варианте осуществления «Аро J, содержащий остатки GlcNAc», не содержит N-связанные или О-связанные α-глюкозные остатки. В еще одном варианте осуществления «Аро J, содержащий остатки GlcNAc», не содержит N-связанные или О-связанные α-маннозные остатки или N-связанные или О-связанные α-глюкозные остатки.
Используемый здесь термин «Аро J, содержащий остатки GlcNAc и сиаловой кислоты», относится к любой молекуле Аро J, содержащей по меньшей мере один повтор N-ацетилглюкозы и гликановой цепи и по меньшей мере один повтор остатка сиаловой кислоты.
Используемый здесь термин «сиаловая кислота» относится к моносахариду, известному как N-ацетилнейраминовая кислота (Neu5Ac) и имеющему общую структуру
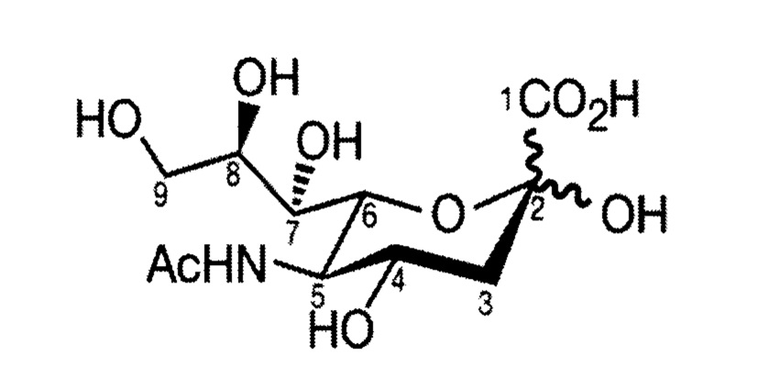
В одном варианте осуществления Аро J содержит два остатка GlcNAc и один остаток сиаловой кислоты (далее - (GlcNAc)2-Neu5Ac). В другом варианте осуществления остатки GlcNAc и сиаловой кислоты связаны посредством одного или более моносахаридов.
В одном варианте осуществления уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, соответствуют уровням Аро J, способного специфически связываться с лектином Triticum vulgaris.
В предпочтительном варианте осуществления «Аро J, содержащий остатки GlcNAc и сиаловой кислоты», по существу не содержит N-связанные или О-связанные углеводы других типов. В одном варианте осуществления «Аро J, содержащий остатки GlcNAc и сиаловой кислоты», не содержит N-связанные или О-связанные α-маннозные остатки. В другом варианте осуществления «Аро J, содержащий остатки GlcNAc и сиаловой кислоты», не содержит N-связанные или О-связанные α-глюкозные остатки. В еще одном варианте осуществления «Аро J, содержащий остатки GlcNAc и сиаловой кислоты» не содержит N-связанные или О-связанные α-маннозные остатки или N-связанные или О-связанные α-глюкозные остатки.
В предпочтительном варианте осуществления «гликозилированный Аро J, способный специфически связываться с лектином T.vulgaris», соответствует любой гликозилированной форме Аро J, содержащей по меньшей мере один остаток сиаловой кислоты или по меньшей мере один остаток GlcNAc, включая Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc), но не содержащий остатки сиаловой кислоты, Аро J, содержащий остатки (GlcNAc)2, но не содержащий остатки сиаловой кислоты, Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc) и остатки сиаловой кислоты, Аро J, содержащий остатки (GlcNAc)2 и сиаловой кислоты, а также Аро J, содержащий остатки сиаловой кислоты, но не содержащий остатки GlcNAc или (GlcNAc)2. Должно быть понятно, что остатки (GlcNAc) и остатки (GlcNAc)2 могут содержаться в той же гликановой цепи, что и остатки сиаловой кислоты. В качестве альтернативы остатки сиаловой кислоты могут содержаться в гликановых цепях, не содержащих остатки (GlcNAc) или остатки (GlcNAc)2.
В предпочтительном варианте осуществления «гликозилированный Аро J, способный специфически связываться с лектином D.stramonium», соответствует любой гликозилированной форме Аро J, содержащей, по меньшей мере, один остаток GlcNAc, включая Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc), и Аро J, содержащий остатки (GlcNAc)2.
Термин «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), относится к любому уровню экспрессии Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), в образце ниже опорного значения. Так уровни экспрессии Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), считаются пониженными или ниже опорного значения, когда они по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более ниже опорного значения.
Термин «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, относится к любому уровню экспрессии Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в образце ниже опорного значения. Так уровни экспрессии Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, считаются пониженными или ниже опорного значения, когда они по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более ниже опорного значения.
Термин «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J, способного специфически связываться с лектином Т.vulgaris, относится к любому уровню экспрессии Аро J, способного специфически связываться с лектином T.vulgaris, в образце ниже опорного значения. Так уровни экспрессии Аро J, способного специфически связываться с лектином T.vulgaris, считаются пониженными или ниже опорного значения, когда они по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере, на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере, на 90%, по меньшей мере на 95%, по меньшей мере, на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более ниже опорного значения.
Термин «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, относится к любому уровню экспрессии Аро J, способного специфически связываться с лектином D.stramonium, в образце, который ниже опорного значения. Так уровни экспрессии Аро J, способного специфически связываться с лектином D.stramonium, считаются пониженными или ниже опорного значения, когда они, по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более ниже опорного значения.
Способ диагностики изобретения содержит сравнение уровней, полученных для обследуемого пациента, с опорным значением, при этом пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина, по отношению к опорному значению или пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, по отношению к опорному значению указывают на то, что пациент страдает ишемией или ишемическим повреждением тканей. Способ диагностики изобретения в качестве альтернативы содержит сравнение уровней, полученных для обследуемого пациента, с опорным значением, при этом пониженные уровни Аро J, способного специфически связываться с лектином D.stramonium, по отношению к опорному значению или пониженные уровни Аро J, способного специфически связываться с лектином T.vulgaris, по отношению к опорному значению указывают на то, что пациент страдает ишемией или ишемическим повреждением тканей.
Используемый здесь термин «опорное значение» относится к предварительно заданным критериям, используемым в качестве ориентира для оценки значений или данных, полученных для образцов, взятых у пациента. Опорное значение или опорный уровень может представлять собой абсолютное значение; относительное значение; значение, имеющее верхний или нижний предел; диапазон значений; усредненное значение; медианное значение; среднее значение или значение в сравнении с определенным контрольным или исходным значением. Опорное значение может быть основано на значении отдельного образца, например, представлять собой значение, полученное для образца испытуемого, но в более ранний момент времени. Опорное значение может быть основано на большом количестве образцов, например, популяции пациентов из группы, подобранной по календарному возрасту, либо основываться на пуле образцов, включая или не включая испытуемый образец. В одном варианте осуществления опорное значение соответствует уровням Аро J, содержащего остатки GlcNAc, уровням Аро J, содержащего GlcNAc и сиаловую кислоту (Neu5Ac), уровням Аро J, способного специфически связываться с лектином T.vulgaris, или уровням Аро J, способного специфически связываться с лектином D.stramonium, определенным у здорового участника, в котором под здоровым участником понимается участник, демонстрирующий отсутствие ишемических повреждений тканей на момент определения уровней Аро J, содержащего остатки GlcNAc, уровней Аро J, содержащего GlcNAc и сиаловую кислоту (Neu5Ac), уровней Аро J, способного специфически связываться с лектином T.vulgaris, или уровням Аро J, способного специфически связываться с лектином D.stramonium, и предпочтительно демонстрирующий отсутствие ишемических повреждений в анамнезе.
В другом варианте осуществления опорное значение соответствует усредненному или среднему уровню соответствующего биомаркера, определенному для пула образцов, полученных у группы пациентов, хорошо задокументированных с клинической точки зрения и не страдающих заболеваниями, в частности, не страдающих ишемическим повреждением тканей, в частности, не страдающих ишемическим повреждением миокарда или ишемическим повреждением головного мозга. В упомянутых образцах уровни экспрессии могут быть определены, например, путем определения среднего уровня экспрессии в контрольной популяции. При определении опорного значения необходим учитывать некоторые характеристики типа образца, такие как возраст, пол, физическое состояние или другие характеристики пациента. Например, контрольный образец может быть получен из одинаковых количеств группы, включающей от по меньшей мере 2, по меньшей мере 10, по меньшей мере 100 до более 1000 участников, чтобы популяция была статистически значимой.
Следует понимать, что контрольное значение, используемое для диагностики пациентов в соответствии со способом диагностики изобретения, представляет собой значение, полученное для образца того же типа и того же биомаркера, что и маркер, учитываемый при диагностике. Соответственно, если способ диагностики осуществляется путем определения уровней гликозилированного Аро J, содержащего GlcNAc или (GlcNAc)2, то контрольное значение, используемое для диагностики, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки GlcNAc или (GlcNAc)2 в соответствующих случаях, полученного у здорового участника или из пула образцов, как определено выше. В еще одном варианте осуществления, если способ диагностики осуществляется путем определения уровней гликозилированного Аро J, содержащего остатки GlcNAc и сиаловой кислоты, контрольное значение, используемое при диагностике, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, как пояснено выше. В еще одном варианте осуществления, если способ диагностики осуществляется путем определения уровней гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, контрольное значение, используемое при диагностике, также представляет собой уровень экспрессии гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, как пояснено выше. В еще одном варианте осуществления, если способ диагностики осуществляется путем определения уровней гликозилированного Аро J, способного специфически связываться с лектином T.vulgaris, контрольное значение, используемое при диагностике, также представляет собой уровень экспрессии гликозилированного Аро J, способного специфически связываться с лектином T.vulgaris, как пояснено выше.
В еще одном варианте осуществления, если для диагностики повреждения тканей миокарда определяется биомаркер, контрольное значение будет представлять собой уровни того же биомаркера у здорового участника, который демонстрирует отсутствие повреждений тканей миокарда и предпочтительно не имеет повреждений тканей миокарда в анамнезе. Если контрольное значение представляет собой средний уровень того же биомаркера, полученный для пула образцов участников, то участники, из образцов которых составлен пул, представляют собой участников, которые демонстрируют отсутствие повреждений тканей миокарда и предпочтительно не имеют повреждений тканей миокарда в анамнезе.
В еще одном варианте осуществления, если для диагностики повреждения тканей головного мозга определяется биомаркер, контрольное значение будет представлять собой уровни того же биомаркера у здорового участника, который демонстрирует отсутствие повреждений тканей головного мозга и предпочтительно не имеет повреждений тканей головного мозга в анамнезе.
Если контрольное значение представляет собой средний уровень того же биомаркера, полученный для пула образцов участников, то участники, из образцов которых составлен пул, представляют собой участников, которые демонстрируют отсутствие повреждений тканей головного мозга и предпочтительно не имеют повреждений тканей головного мозга в анамнезе.
Опорное значение, используемое в способе диагностики изобретения, может быть оптимизировано для достижения необходимой специфичности и чувствительности.
В одном варианте осуществления опорное значение, используемое при диагностике ишемии миокарда, составляет 332 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc или 393 мкг/мл Аро J-GlcNac при необходимых чувствительности 97% и специфичности 71% или 393 мкг/мл Аро J-GlcNAc при необходимых чувствительности 81% и специфичности 72% (т.е. способ диагностики в соответствии с настоящим изобретением обеспечивает возможность диагностики ишемии миокарда с чувствительностью 97% и специфичностью 71%, если пациент демонстрирует меньше 332 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc, или с чувствительностью 81% и специфичностью 72%, когда пациент демонстрирует меньше 393 мкг/мл Аро J-GlcNAc).
В еще одном варианте осуществления, опорное значение, используемое при диагностике ишемии головного мозга, составляет 424 мкг/мл Аро J-GlcNAc+Neu5Ac + ApoJ-GlcNAc при необходимых чувствительности 66% и специфичности 51% (т.е. способ диагностики в соответствии с настоящим изобретением обеспечивает возможность диагностики ишемии головного мозга с чувствительностью 66% и специфичностью 51%, если пациент демонстрирует меньше 424 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc).
В одном варианте осуществления опорное значение, используемое при диагностике ишемии миокарда, составляет 332 мкг/мл Аро J, способного связываться с лектином T.vulgaris, при необходимых чувствительности 97% и специфичности 71% или 393 мкг/мл Аро J, способного связываться с лектином D.stramonium, при необходимых чувствительности 81% и специфичности 72% (т.е. способ диагностики в соответствии с настоящим изобретением обеспечивает возможность диагностики ишемии миокарда с чувствительностью 97% и специфичностью 71%, если пациент демонстрирует меньше 332 мкг/мл Apo J, способного связываться с лектином T.vulgaris, или с чувствительностью 81% и специфичностью 72%, когда пациент демонстрирует меньше 393 мкг/мл Аро J, способного связываться с лектином D.stramonium).
В еще одном варианте осуществления, опорное значение, используемое при диагностике ишемии головного мозга, составляет 424 мкг/мл Apo J, способного связываться с лектином T.vulgaris, при необходимых чувствительности 66% и специфичности 51% (т.е. способ диагностики в соответствии с настоящим изобретением обеспечивает возможность диагностики ишемии головного мозга с чувствительностью 66% и специфичностью 51%, если пациент демонстрирует меньше 424 мкг/мл Аро J, способного связываться с лектином T.vulgaris).
В предпочтительном варианте осуществления, определение уровней гликозилированного Аро J, содержащего N-ацетилглюкозамин (GlcNAc), уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, уровней Аро J, способного связываться с лектином D.stramonium, или уровне гликозилированного Аро J, способного связываться с лектином T.vulgaris, выполняется до определения в образце заметного повышения уровня маркера некроза. В предпочтительном варианте осуществления, маркер некроза представляет собой тропонин Т или КК. В еще одном предпочтительном варианте осуществления, определение уровней гликозилированного Аро J, содержащего N-ацетилглюкозамин (GlcNAc), уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, уровней Аро J, способного связываться с лектином D.stramonium, или уровне гликозилированного Аро J, способного связываться с лектином T.vulgaris, выполняется в образце, полученном в течение 1 часа, 2 часов, 3 часов, 4 часов, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 12 часов, 14 часов, 16 часов, 18 часов, 20 часов, 30 часов, 40 часов, 50 часов или более с начала симптомов ишемического повреждения. В предпочтительном варианте осуществления, в случае ишемических повреждений миокарда симптомы, как правило, представляют собой боль в груди, одышку, повышенное потоотделение, слабость, головокружение, тошноту, рвоту и ощущение сердцебиения. В одном варианте осуществления, пациент представляет собой пациента до ОИМ.
В еще одном варианте осуществления, в случае ишемического повреждения головного мозга симптомы ишемических повреждений включают без ограничений измененное обоняние, вкус, слух или зрение, опущение века или слабость глазных мышц, снижение рефлексов: рвотного, глотательного, реакции зрачка на свет, снижение чувствительности и слабость мышц лица, нарушения равновесия и нистагм, афазию, апраксию (измененные произвольные движения), выпадения поля зрения, дизартрию, нарушения памяти, геминеглект, дезорганизованное мышление, спутанность сознания, гиперсексуальные жесты (с вовлечением лобной доли), отсутствие адекватной самооценки, обычно связанное с инсультом, инвалидность, измененную походку, измененную координацию движений, головокружение или потерю равновесия.
В еще одном варианте осуществления, определение уровней гликозилированных форм Аро J в соответствии со способом диагностики изобретения осуществляется в образце пациента, у которого он был получен, перед приемом пациентом любых лекарственных средств, предназначенных для снижения ишемии или снижения ишемического повреждения тканей. В одном варианте осуществления, в случае ишемических повреждений миокарда определение уровней гликозилированных форм Аро J осуществляется в образце пациента, который был получен до начала лечения пациента статинами, антитромбоцитарными препаратами и/или антикоагулянтными препаратами.
В одном варианте осуществления в случае ишемических повреждений головного мозга определение уровней гликозилированных форм Аро J осуществляется в образце пациента, который был получен до начала лечения пациента тканевым активатором плазминогена, антитромбоцитарными препаратами и/или антикоагулянтными препаратами.
Способ прогнозирования у пациентов, перенесших ишемические повреждения Авторами настоящего изобретения также было неожиданно установлено, что уровни гликозилированного Аро J полезны не только для выявления текущего ишемического события, но и для прогнозирования у пациентов, которые перенесли ишемическое событие.
Так, согласно еще одному объекту, изобретение относится к способу прогнозирования прогрессирования ишемии у пациента (далее - способ прогнозирования изобретения), перенесшего ишемическое событие, или определения прогноза у пациента, перенесшего ишемическое событие, содержащему определение в образце упомянутого пациента уровней гликозилированного Аро J, в котором пониженные уровни гликозилированного Аро J по отношению к опорному значению указывают на прогрессирование ишемии или неблагоприятный прогноз для пациента.
В контексте настоящего изобретения термин «прогнозирование прогрессирования» относится к способности прогнозирования динамики заболевания после перенесенной ишемии или связанного с ней ишемического повреждения тканей с применением способа, описанного в настоящей заявке. Данное определение, как должно быть понятно специалисту в данной области техники, не предусматривает получение на 100% правильных результатов для всех образцов. Однако для него требуется правильная классификация статистически значимого количества проанализированных образцов. Количество, которое является статистически значимым, может быть установлено специалистом в данной области с использованием различных средств статистического анализа, например, но не ограничиваясь, путем определения доверительных интервалов, определения р-значения, критерия Стьюдента и дискриминантной функции Фишера. Предпочтительно, доверительные интервалы составляют, по меньшей мере, 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 98% или меньше 99%. Предпочтительно, р-значение составляет меньше 0,05, 0,01, 0,005 или 0,0001. Предпочтительно, настоящее изобретение способно правильно выявлять ишемию или ишемические повреждения у по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или, по меньшей мере, 90% участников определенной испытуемой группы или популяции.
В контексте настоящего изобретения, термин «определение прогноза», используемый взаимозаменяемо с термином «прогнозирование», относится к способности прогнозирования исхода пациентов после перенесенной ишемии миокарда или головного мозга или связанного с ней ишемического повреждения тканей с применением способа, описанного в настоящей заявке. Данное определение, как должно быть понятно специалисту в данной области техники, не предусматривает получение на 100% правильных результатов для всех образцов. Однако для него требуется правильная классификация статистически значимого количества проанализированных образцов. Количество, которое является статистически значимым, может быть установлено специалистом в данной области с использованием различных средств статистического анализа, например, но не ограничиваясь, путем определения доверительных интервалов, определения р-значения, критерия Стьюдента и дискриминантной функции Фишера. Предпочтительно, доверительные интервалы составляют, по меньшей мере, 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 98% или меньше 99%. Предпочтительно, р-значение составляет меньше 0,05, 0,01, 0,005 или 0,0001. Предпочтительно, настоящее изобретение способно правильно выявлять ишемию или ишемические повреждения у по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или, по меньшей мере, 90% участников определенной испытуемой группы или популяции.
В предпочтительном варианте осуществления прогноз для пациента определяется как риск рецидива в течение 6 месяцев. В случае определения рецидива в течение 6 месяцев должно быть понятно, что рецидив относится ко второму ишемическому событию, возникающему в течение первых 6 месяцев после первого ишемического события. В одном варианте осуществления, второе ишемическое событие принадлежит к тому же типу, что и первое ишемическое событие, т.е. если первое ишемическое событие представляет собой ишемию миокарда, то прогноз определяется как риск возникновения у пациента второго миокардиального ишемического события. В еще одном варианте осуществления, второе ишемическое событие относится к другому типу по сравнению с первым ишемическим событием, т.е. если первое ишемическое событие представляет собой ишемию миокарда, то прогноз определяется как риск возникновения у пациента церебрального ишемического события, или наоборот, если первое ишемическое событие представляет собой ишемию головного мозга, то прогноз определяется как риск возникновения у пациента миокардиального ишемического события.
В еще одном варианте осуществления, прогноз для пациента определяется как риск больничной смертности.
В предпочтительном варианте осуществления, прогноз для пациентов определяется как риск смертности в течение 6 месяцев.
Термины «Аро J», «пациент», «ишемическое событие» и «образец» были подробно описаны в контексте способа диагностики изобретения и в равной степени применимы к настоящему способу.
В одном варианте осуществления, образец представляет собой биологическую жидкость. В еще одном варианте осуществления, биологическая жидкость представляет собой плазму или сыворотку крови.
В одном варианте осуществления, ишемическое событие представляет собой миокардиальное ишемическое событие. В еще одном варианте осуществления, миокардиальное ишемическое событие представляет собой инфаркт миокарда с подъемом сегмента ST (ИMпST). В еще одном варианте осуществления, ишемическое событие представляет собой церебральное ишемическое событие.
Используемый здесь термин «гликозилированный Аро J» относится к любой форме Аро J, которая содержит по меньшей мере одну цепь N-связанного или О-связанного олигосахарида, прикрепленную к полипептидной цепи. Термин «гликозилированный Аро J» включает оба варианта, содержащих N-связанные и О-связанные олигосахариды. Этот термин также включает Аро J, содержащий N-связанные олигосахариды комплексного типа, высокоманнозные олигосахариды или олигосахариды гибридного типа.
В одном варианте осуществления, гликозилированный Аро J, который определяется в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc). В еще одном предпочтительном варианте осуществления, уровень гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), соответствует уровню Аро J, способного специфически связываться с лектином Datura stramonium. В одном варианте осуществления, гликозилированный Аро J, который определяется в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, способный специфически связываться с лектином Datura stramonium.
В еще одном варианте осуществления, гликозилированный Аро J, определяемый в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты. В еще более предпочтительном варианте осуществления, уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, соответствуют уровням Аро J, способного специфически связываться с лектином Triticum vulgaris. В одном варианте осуществления, гликозилированный Аро J, который определяется в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, способный специфически связываться с лектином Triticum vulgaris.
Термины «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J относится к любому уровню экспрессии гликозилированного Аро J в образце, который ниже опорного значения. Так уровни гликозилированного Аро J считаются пониженными или ниже опорного значения, когда они по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более, ниже опорного значения. В предпочтительном варианте осуществления уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc)2, ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, способного специфически связываться с лектином T.vulgaris, ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, ниже определенных в контрольном образце.
Термин «опорное значение» в контексте способа прогнозирования изобретения относится к предварительно заданным критериям, используемым в качестве ориентира для оценки значений или данных, полученных для образцов, взятых у пациента. Опорное значение или опорный уровень может представлять собой абсолютное значение; относительное значение; значение, имеющее верхний или нижний предел; диапазон значений; усредненное значение; медианное значение; среднее значение или значение в сравнении с определенным контрольным или исходным значением. Опорное значение может быть основано на значении отдельного образца, например, представлять собой значение, полученное для образца испытуемого, но в более ранний момент времени. Опорное значение может быть основано на большом количестве образцов, например, популяции пациентов из группы, подобранной по календарному возрасту, либо основываться на пуле образцов, включая или не включая испытуемый образец. В одном варианте осуществления, опорное значение соответствует уровням гликозилированного Аро J, определенным у пациента, перенесшего ишемическое событие, у которого ишемия не прогрессирует или показывает благоприятное прогрессирование. В случае определения прогрессирования как риска рецидива в течение 6 месяцев в качестве опорного значения можно принять урони гликозилированного Аро J в образце, взятом у пациента на момент ишемического события, но если при этом у пациента не возникали другие ишемические события по меньшей мере через 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 18 месяцев, 24 месяца, 36 месяцев, 48 месяцев или более с момента первого ишемического события. В еще одном варианте осуществления, когда прогрессирование определяется как риск больничной смертности, в качестве опорного значения можно принять уровни гликозилированного Аро J у пациента на момент ишемического события, но если при этом пациент был выписан из больницы. В случае определения прогрессирования как риска смертности в течение 6 месяцев в качестве опорного значения можно принять урони гликозилированного Аро J в образце, взятом у пациента на момент ишемического события, но если при этом пациент остается в живых по меньшей мере через 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 18 месяцев, 24 месяца, 36 месяцев, 48 месяцев или более с момента ишемического события.
В еще одном варианте осуществления, опорное значение соответствует усредненному или среднему уровню соответствующего биомаркера, определенному для пула образцов, полученных у группы пациентов, хорошо задокументированных с клинической точки зрения и для которых после перенесенного ишемического события определен благоприятный прогноз, как определено в предыдущем пункте. В упомянутых образцах уровни экспрессии могут быть определены, например, путем определения среднего уровня экспрессии в контрольной популяции. При определении опорного значения необходимо учитывать некоторые характеристики типа образца, такие как возраст, пол, физическое состояние и другие характеристики пациента. Например, контрольный образец может быть получен из одинаковых количеств группы, включающей от по меньшей мере 2, по меньшей мере 10, по меньшей мере 100 до более 1000 участников, чтобы популяция была статистически значимой.
Следует понимать, что контрольное значение, используемое для прогнозирования у пациентов в соответствии со способом прогнозирования изобретения, представляет собой значение, полученное для образца того же типа и того же биомаркера, что и маркер, учитываемый при диагностике. Соответственно, если способ прогнозирования осуществляется путем определения уровней гликозилированного Аро J, содержащего GlcNAc или (GlcNAc)2, то контрольное значение, используемое для прогнозирования, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки GlcNAc или (GlcNAc)2 в соответствующих случаях, полученного у здорового участника или из пула образцов, как определено выше. В еще одном варианте осуществления, если способ прогнозирования осуществляется путем определения уровней гликозилированного Аро J, содержащего остатки GlcNAc и сиаловой кислоты, контрольное значение, используемое при прогнозировании, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, как пояснено выше.
Если способ прогнозирования осуществляется путем определения уровней гликозилированного Аро J, способного связываться с лектином D.stramonium, контрольное значение, используемое при прогнозировании, также представляет собой уровень экспрессии гликозилированного Аро J, способного связываться с лектином D.stramonium, полученный для здорового участника или из пула образцов, как определено выше. В еще одном варианте осуществления, если способ прогнозирования осуществляется путем определения уровней гликозилированного Аро J, способного связываться с лектином T.vulgaris, контрольное значение, используемое при прогнозировании, также представляет собой уровень экспрессии гликозилированного Аро J, способного связываться с лектином T.vulgaris, как пояснено выше.
В еще одном варианте осуществления, если для прогнозирования у пациента, перенесшего повреждение тканей миокарда, определяется биомаркер, контрольное значение будет представлять собой уровни того же биомаркера у участника, для которого после перенесенного миокардиального ишемического события определен благоприятный прогноз в соответствии с любыми определенными выше критериями (отсутствие рецидива ишемического события через 6 месяцев, больничной смерти или смерти в течение 6 месяцев). Если контрольное значение представляет собой средний уровень того же биомаркера, полученный для пула образцов участников, то участники, из образцов которых составлен пул, представляют собой участников, для которых после перенесенного миокардиального ишемического события определен благоприятный прогноз в соответствии с любыми определенными выше критериями (отсутствие рецидива ишемического события через 6 месяцев, больничной смерти или смерти в течение 6 месяцев).
В еще одном варианте осуществления, если для прогнозирования повреждение тканей головного мозга, определяется биомаркер, контрольное значение будет представлять собой уровни того же биомаркера у участника, для которого после перенесенного церебрального ишемического события определен благоприятный прогноз в соответствии с любыми определенными выше критериями (отсутствие рецидива ишемического события через 6 месяцев, больничной смерти или смерти в течение 6 месяцев). Если контрольное значение представляет собой средний уровень того же биомаркера, полученный для пула образцов участников, то участники, из образцов которых составлен пул, представляют собой участников, для которых после перенесенного церебрального ишемического события определен благоприятный прогноз в соответствии с любыми определенными выше критериями (отсутствие рецидива ишемического события через 6 месяцев, больничной смерти или смерти в течение 6 месяцев).
Опорное значение, используемое в способе прогнозирования изобретения, может быть оптимизировано для достижения необходимой специфичности и чувствительности.
В конкретном варианте осуществления, опорное значение, используемое при прогнозировании смертности и рецидивирующих событий, составляет 287 мкг/мл Аро J-GlcNAc при необходимых чувствительности 58% и специфичности 51% (т.е. способ прогнозирования в соответствии с настоящим изобретением обеспечивает возможность прогнозирования смертности и рецидивирующих событий с чувствительностью 58% и специфичностью 61%, если пациент демонстрирует меньше 287 мкг/мл Аро J-GlcNAc).
В конкретном варианте осуществления, опорное значение, используемое при прогнозировании смертности и рецидивирующих событий, составляет 398 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc при необходимых чувствительности 55% и специфичности 65% (т.е. способ прогнозирования в соответствии с настоящим изобретением обеспечивает возможность прогнозирования смертности и рецидивирующих событий с чувствительностью 55% и специфичностью 65%, если пациент демонстрирует меньше 398 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc).
В конкретном варианте осуществления, опорное значение, используемое при прогнозировании смертности и рецидивирующих событий, составляет 398 мкг/мл Аро J, способного специфически связываться с T.vulgaris, при необходимых чувствительности 55% и специфичности 65% (т.е. способ прогнозирования в соответствии с настоящим изобретением обеспечивает возможность прогнозирования смертности и рецидивирующих событий с чувствительностью 55% и специфичностью 65%, если пациент демонстрирует меньше 398 мкг/мл Аро J, способного специфически связываться с T.vulgaris).
В конкретном варианте осуществления, опорное значение, используемое при прогнозировании смертности и рецидивирующих событий, составляет 287 мкг/мл Аро J, способного связываться с лектином D. stramonium, при необходимых чувствительности 58% и специфичности 51% и 273 мкг/мл Apo J, способного связываться с лектином D.stramonium, при необходимых чувствительности 64% и специфичности 50% (т.е. способ прогнозирования в соответствии с настоящим изобретением обеспечивает возможность прогнозирования смертности и рецидивирующих событий с чувствительностью 58% и специфичностью 51%, если пациент демонстрирует меньше 287 мкг/мл Аро J, способного связываться с лектином D.stramonium, или прогнозирования смертности с чувствительностью 64% и специфичностью 50%, когда пациент демонстрирует меньше 273 мкг/мл Аро J, способного связываться с лектином D.stramonium).
Способ стратификации риска изобретения
Авторы настоящего изобретения также показали, что уровни гликозилированного Аро J и, в частности, уровень гликозилированного Аро J, содержащего GlcNAc и Neu5Ac, также являются полезным биомаркером для определения риска возникновения у пациента, страдающего стабильной ишемической болезнью сердца (ИБС), рецидивирующего ишемического события. Этот способ обеспечивает возможность стратификации пациентов в соответствии с риском возникновения ишемических событий и соответственно полезен для назначения специфической профилактической терапии пациентам в зависимости от риска.
Так, согласно еще одном объекту, изобретение относится к способу определения риска (далее - способ стратификации риска изобретения) возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью, упомянутый способ содержит определение в образце упомянутого пациента уровней гликозилированного Аро J, в котором пониженные уровни гликозилированного Аро J по отношению к опорному значению указывают на повышенный риск возникновения у пациента рецидивирующего ишемического события.
В контексте настоящего изобретения термин «определение риска» или «стратификация риска» относится к способности определения риска или вероятности: а) возникновения дополнительных клинических осложнений у пациентов, перенесших ишемию миокарда или головного мозга или связанных с ними ишемических повреждений тканей, и/или b) пользы от специфического лечения ишемии миокарда или головного мозга или связанных с ними ишемических повреждений тканей - при использовании способа, описанного в настоящей заявке. Данное определение, как должно быть понятно специалисту в данной области техники, не предусматривает получение на 100% правильных результатов для всех образцов. Однако для него требуется правильная классификация статистически значимого количества проанализированных образцов. Количество, которое является статистически значимым, может быть установлено специалистом в данной области с использованием различных средств статистического анализа, например, но не ограничиваясь, путем определения доверительных интервалов, определения р-значения, критерия Стьюдента и дискриминантной функции Фишера. Предпочтительно, доверительные интервалы составляют, по меньшей мере, 90%, по меньшей мере 95%, по меньшей мере 97%, по меньшей мере 98% или меньше 99%. Предпочтительно р-значение составляет меньше 0,1, 0,05, 0,01, 0,005 или 0,0001. Предпочтительно, настоящее изобретение способно правильно выявлять ишемию или ишемические повреждения у по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или, по меньшей мере, 90% участников определенной испытуемой группы или популяции.
Термины «пациент», «ишемическое событие», «образец», «Аро J» и «гликозилированный Аро J» были подробно описаны в контексте способов диагностики и прогнозирования изобретения и в равной степени применимы к способу стратификации риска изобретения.
В одном варианте осуществления, рецидивирующее ишемическое событие представляет собой острый коронарный синдром, инсульт или преходящее ишемическое событие.
В одном варианте осуществления, образец представляет собой биологическую жидкость. В еще одном варианте осуществления, биологическая жидкость представляет собой плазму или сыворотку крови.
В одном варианте осуществления, ишемическое событие представляет собой миокардиальное ишемическое событие. В еще одном варианте осуществления, миокардиальное ишемическое событие представляет собой инфаркт миокарда с подъемом сегмента ST (ИМпSТ). В еще одном варианте осуществления, ишемическое событие представляет собой церебральное ишемическое событие.
В одном варианте осуществления, гликозилированный Аро J, который определяется в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc). В еще одном варианте осуществления уровень гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), соответствует уровню Аро J, способного специфически связываться с лектином Datura stramonium.
В еще одном варианте осуществления, гликозилированный Аро J, определяемый в способе прогнозирования изобретения, представляет собой гликозилированный Аро J, содержащий остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты. В еще одном варианте осуществления, уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, соответствуют уровням Аро J, способного специфически связываться с лектином Triticum vulgaris.
Термины «стабильная ишемическая болезнь» и «стабильная ишемическая болезнь сердца» имеют одинаковое значение и используются взаимозаменяемым образом. Оба термина относятся к заболеванию стабильной ишемической болезни сердца (СИБС). «Стабильный» в контексте терминов «стабильное сердечно-сосудистое заболевание», «стабильная болезнь сердца» или «стабильная ишемическая болезнь сердца» определяется как любые условия выявленного сердечно-сосудистого заболевания при отсутствии острых сердечно-сосудистых событий. Таким образом, например, стабильная ишемическая болезнь сердца относится к различным стадиям развития ишемической болезни, за исключением ситуаций, в которых в клинической картине преобладает тромбоз коронарных артерий (острый коронарный синдром). Пациенты, страдающие СИБС, определяются по одному или нескольким из следующих состояний: стабильная стенокардия с положительной пробой ЭКГ с нагрузкой или положительная сцинтиграфия миокарда, или стеноз >50 процентов коронарной артерии, острый коронарный синдром в анамнезе, коронарная реваскуляризация, лечение антитромбоцитарными препаратами, антикоагулянтными препаратами и/или статинами со стабильной дозировкой на протяжении по меньшей мере 3 месяцев.
В предпочтительном варианте осуществления, пациенты, страдающие стабильной ишемической болезнью, перенесли острый коронарный синдром перед стабильной ишемической болезнью сердца. В предпочтительных вариантах осуществления пациенты, страдающие стабильной ишемические болезнью сердца, перенесли острый коронарный синдром по меньшей мере за 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 18 месяцев, 24 месяцев, 36 месяцев, 48 месяцев, 60 месяцев или более до стабильной ишемической болезни.
Термины «пониженные уровни» или «низкие уровни» по отношению к уровням гликозилированного Аро J в способе прогнозирования изобретения относится к любому уровню экспрессии гликозилированного Аро J в образце, который ниже опорного значения. Так уровни гликозилированного Аро J считаются пониженными или ниже опорного значения, когда они по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 100%, по меньшей мере на 110%, по меньшей мере на 120%, по меньшей мере на 130%, по меньшей мере на 140%, по меньшей мере на 150% или более, ниже опорного значения. В предпочтительном варианте осуществления уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc)2, ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, способного связываться с лектином T.vulgaris, ниже определенных в контрольном образце. В еще одном варианте осуществления, уровни гликозилированного Аро J, способного связываться с лектином D.stramonium, ниже определенных в контрольном образце.
Термин «опорное значение» в контексте способа стратификации изобретения относится к предварительно заданным критериям, используемым в качестве ориентира для оценки значений или данных, полученных для образцов, взятых у пациента. Опорное значение или опорный уровень может представлять собой абсолютное значение; относительное значение; значение, имеющее верхний или нижний предел; диапазон значений; усредненное значение; медианное значение; среднее значение или значение в сравнении с определенным контрольным или исходным значением. Опорное значение может быть основано на значении отдельного образца, например, представлять собой значение, полученное для образца испытуемого, но в более ранний момент времени. Опорное значение может быть основано на большом количестве образцов, например, популяции пациентов из группы, подобранной по календарному возрасту, либо основываться на пуле образцов, включая или не включая испытуемый образец. В одном варианте осуществления, опорное значение соответствует уровням гликозилированного Аро J, определенным у пациента, страдающего стабильной ишемической болезнью, но который не переносил рецидивирующих ишемических событий. В этом случае подходящими пациентами для определения опорного значения являются пациенты, которые страдают стабильной ишемической болезнью сердца, но не переносили рецидивирующих ишемических событий в течение по меньшей мере 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 18 месяцев, 24 месяцев, 36 месяцев, 48 месяцев или более после начала стабильной ишемической болезни.
В еще одном варианте осуществления, опорное значение соответствует усредненному или среднему уровню соответствующего биомаркера, определенному для пула образцов, полученных у группы пациентов, хорошо задокументированных с клинической точки зрения и страдающих стабильной ишемической болезнью, но не переносивших рецидивирующих ишемических событий в течение по меньшей мере 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 18 месяцев, 24 месяцев, 36 месяцев, 48 месяцев или более после начала стабильной ишемической болезни. В упомянутых образцах уровни экспрессии могут быть определены, например, путем определения среднего уровня экспрессии в контрольной популяции. При определении опорного значения необходим учитывать некоторые характеристики типа образца, такие как возраст, пол, физическое состояние и другие характеристики пациента. Например, контрольный образец может быть получен из одинаковых количеств группы, включающей от по меньшей мере 2, по меньшей мере 10, по меньшей мере 100 до более 1000 участников, чтобы популяция была статистически значимой.
Следует понимать, что контрольное значение, используемое для стратификации риска пациентов в соответствии со способом стратификации риска изобретения, представляет собой значение, полученное для образца того же типа и того же биомаркера, что и маркер, учитываемый при диагностике. Соответственно, если способ стратификации риска осуществляется путем определения уровней гликозилированного Аро J, содержащего GlcNAc или (GlcNAc)2, то контрольное значение, используемое для стратификации риска, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки GlcNAc или (GlcNAc)2 в соответствующих случаях, полученного у участника или из пула образцов, как определено выше. В еще одном варианте осуществления, если способ стратификации риска осуществляется путем определения уровней гликозилированного Аро J, содержащего остатки GlcNAc и сиаловой кислоты, контрольное значение, используемое при стратификации риска, также представляет собой уровень экспрессии гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, как пояснено выше.
В еще одном варианте осуществления, если способ стратификации риска осуществляется путем определения уровней гликозилированного Аро J, способного специфически связываться с лектином T.vulgaris, контрольное значение, используемое при стратификации риска, также представляет собой уровень экспрессии гликозилированного Аро J, способного специфически связываться с лектином T.vulgaris, как пояснено выше. В еще одном варианте осуществления, если способ стратификации риска осуществляется путем определения уровней гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, контрольное значение, используемое при стратификации риска, также представляет собой уровень экспрессии гликозилированного Аро J, способного специфически связываться с лектином D.stramonium, как пояснено выше.
Опорное значение, используемое в способе стратификации риска изобретения, может быть оптимизировано для достижения необходимой специфичности и чувствительности. В конкретном варианте осуществления, опорное значение, используемое в способе стратификации риска, составляет 485 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc при необходимых чувствительности 94% и специфичности 64% (т.е. способ стратификации риска в соответствии с настоящим изобретением обеспечивает возможность прогнозирования рецидивирующих событий у пациентов, страдающих ИБС, с чувствительностью 94% и специфичностью 64%, если пациент демонстрирует меньше 485 мкг/мл Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc).
В еще одном варианте осуществления опорное значение, используемое в способе стратификации риска, составляет 485 мкг/мл Аро J, способного специфически связываться с лектином T.vulgaris, при необходимых чувствительности 94% и специфичности 64% (т.е. способ стратификации риска в соответствии с настоящим изобретением обеспечивает возможность прогнозирования рецидивирующих событий у пациентов, страдающих ИБС, с чувствительностью 94% и специфичностью 64%, если пациент демонстрирует меньше 485 мкг/мл Аро J, способного специфически связываться с лектином T.vulgaris).
Наборы для определения биомаркеров в соответствии с изобретением.
Авторами настоящего изобретения также был получен набор, обеспечивающий возможность определения гликозилированного Аро J, который подходит для диагностики заболеваний, указанных в настоящей заявке, а также других заболеваний, которые связаны с изменением уровня гликозилированного Аро J.
Так, согласно еще одному объекту, изобретение относится к набору, содержащему:
Первый реактив, представляющий собой лектин, который специфически связывается с гликановым остатком, выбранным из N-ацетилглюкозамина и сиаловой кислоты, и
Второй реактив, который способен специфически связываться с полипептидом Аро J.
Используемый в настоящем изобретении термин «лектин, который специфически связывается с гликановым остатком, выбранным из N-ацетилглюкозамина и сиаловой кислоты», относится к любому белку, отличающемуся от антитела, с возможностью связывания Сахаров, образующихся в любом организме, а также их вариантов, полученных рекомбинантным образом, который обладает возможностью связывания с остатками Сахаров в гликопротеинах. Примеры лектинов, пригодные для использования в настоящем изобретении, включают без ограничений лектины Conavalia ensiformis, Anguilla anguilla, Tritium vulgaris, Datura stramonium, Galanthus nivalis, Maackia amurensis, Arachis hypogaea, Sambucus nigra, Erythtina cristagalli, Lens culinaris, Glycine max, Phaseolus vulgaris, Allomyrina dichotoma, Dolichos biflorus, Lotus tetragonolobus, Ulex europaeus, и Ricinus communis.
Примеры лектинов, пригодных для использования в настоящем изобретении, включают без ограничений лектины, приведенные в таблице 1, в которой указано общепринятое название лектина, организм его происхождения, и сахар, который специфически связывается с упомянутым лектином.
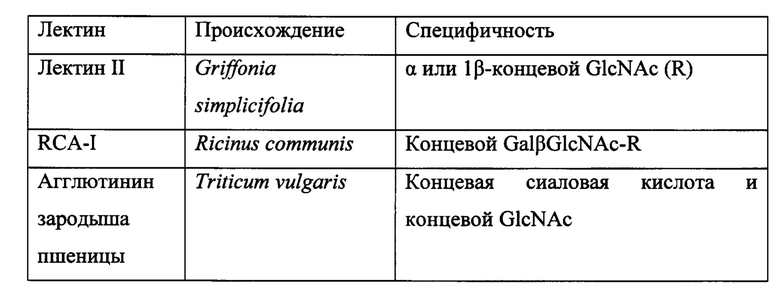
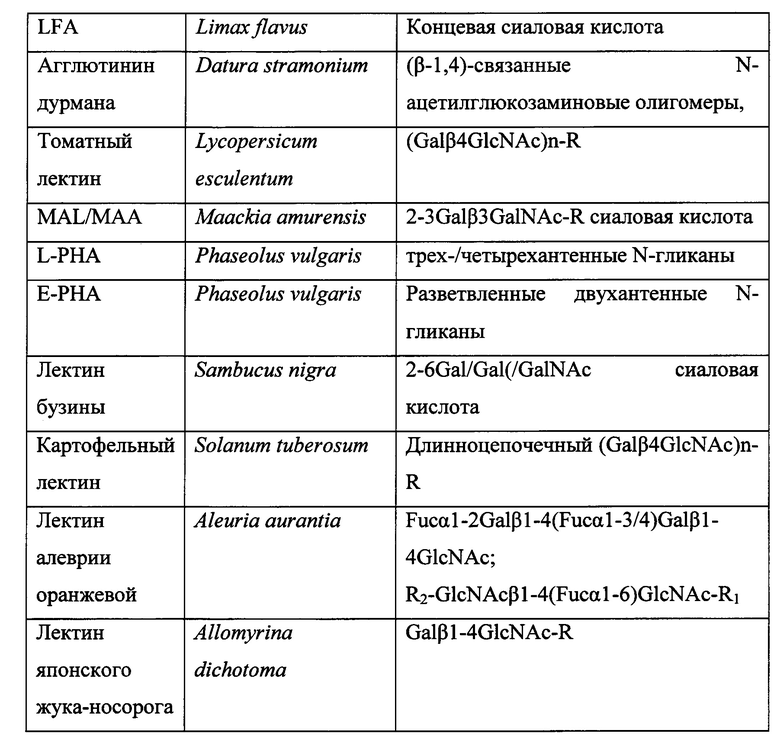
В предпочтительном варианте осуществления, лектин представляет собой лектин из Triticum vulgaris, лектин из Datura stramonium или их сочетание.
В предпочтительном варианте осуществления, второй реактив представляет собой антитела к Аро J или их фрагменты, содержащие антигенсвязывающую область.
В контексте настоящего изобретения, термин «антитела к Аро J» относится к молекулам иммуноглобулинов и их иммунологически активным частям, т.е. молекулам, которые содержат антигенсвязывающий участок, который специфически связывает гликозилированный Аро J, как определено в настоящей заявке. Антитела, пригодные для и использования в соответствии с настоящим изобретением, которые распознают один или более эпитопов, расположенных в полипептидной части гликозилированного Аро J, при условии, что на связывание не оказывает влияния присутствие N-связанных или О-связанных углеводов. Эти антитела способны связываться как с гликозилированными, так и с негликозилированными формами Аро J.
Примеры частей иммунологически активных молекул иммуноглобулинов включают F(ab) и F(ab')2, которые могут быть получены путем обработки антител ферментом, таким как пепсин. Антитела могут быть поликлональными (как правило, включают различные антитела, направленные против различных детерминант или эпитопов) или моноклональными антителами (направленными против одной детерминанты на антигене). Антитело также может быть рекомбинантным, гибридным, гуманизированным, синтетическим или любым сочетанием указанных вариантов.
В одном варианте осуществления лектин иммобилизирован. Иммобилизация, как правило, достигается путем прикрепления к подложке. Используемый в настоящем изобретении термин «подложка» относится к любому твердому материалу, к которому физически прикрепляются компоненты изобретения с обеспечением их иммобилизации. Твердые подложки, пригодные для использования в настоящем изобретении, включают в себя, но не ограничиваются, силикон, стекло, кварц, полиимид, акрилат, полиметилметакрилат, керамику, нитроцеллюлозу, металлы, аморфный карбид кремния, полистирол, а также любой другой материал, пригодный для микропроизводства или микролитографии.
Лектин может быть иммобилизирован на подложке посредством ковалентных связей или посредством нековалентных связей, таких как водородные мостики, гидрофобные взаимодействия или ионные связи. Общий обзор подходящих микропанелей и подложек был описан в публикации Shalon et al. (Genome Research 6: 639-645 (1996)), LeGendre (BioTechniques 9: 788-805 (1990)), US 6197599 и US 6140045. В качестве альтернативы можно использовать подложки, активируемые посредством эпоксидных групп, винилсульфоновых групп, активных сложноэфирных групп, аминогрупп, тиольных групп, изоцианатных групп и т.п. В том случае, когда подложка активируется посредством эпоксидных групп, эти группы включают 3-глицидоксипропилтриметоксисилан (ГТМС), 2-(3,4-эпоксициклогексил)-этилтриметоксисилан, 3-глицидоксипропилметилдиэтоксисилан, 3-глицидоксипропилтриэтоксисилан и т.п.
В одном варианте осуществления, компоненты набора в соответствии с изобретением содержат метку. По существу, изобретение предполагает использование любой метки при условии, что возможна ковалентная конъюгация с компонентом b набора и что она обеспечивает возможность последующего определения упомянутого компонента. В предпочтительном варианте осуществления метка может быть определена путем изменения по меньшей мере одного из ее химических, электрических или магнитных свойств Так изобретение предполагает возможность изменения белков с использованием радиоизотопа типа 3Н, 11С, 14С, 18F, 32Р, 35S, 64Cu, 68Ga, 86Y, 99Тс, 111In, 123I, 124I, 125I, 131I, 133Хе, 177Lu, 211At или 213В. Мечение радиоизотопами, как правило, осуществляется с использованием хелатных лигандов, которые способны образовывать комплексы с ионами металлов, таких как DOTA, DOTP, DOTMA, DTPA и ТЕТА (Macrocyclics, Даллас, штат Техас).
Тем не менее, в предпочтительном варианте осуществления для мечения компонента используется флуоресцентная группа. Подходящие флуоресцентные соединения для использования в настоящем изобретении включают без ограничений бромид этидия, SYBR Green, флуоресцеинизотиоцианат (ФИТЦ), тетраметилродаминизотиол (ТРИТ), 5-карбоксифлуоресцеин, 6-карбоксифлуоресцеин, флуоресцеин, HEX (6-карбокси-2',4,4',5',7,7'-гексахлорфлуоресцеин), Oregon Green 488, Oregon Green 500, Oregon Green 514, Joe (6-карбокси-4',5'-дихлор-2',7'-диметоксифлуоресцеин), 5-карбокси-2',4',5',7'-тетрахлорфлуоресцеин, 5-карбоксиродамин, родамин, тетраметилродамин (Tamra), Rox (карбокси-Х-родамин), R6G (родамин 6G), фталоцианины, азиметины, цианины (Су2, Су3 и Су5), Texas Red, Princeston Red, BODIPY FL-Br2, BODIPY 530/550, BODIPY TMR, BODIPY 558/568, BODIPY 564/570, BODIPY 576/589, BODIPY 581/591, BODIPY TR, BODIPY 630/650, BODIPY 650/665, DABCYL, эозин, эритрозин, бромид этидия, зеленый флуоресцентный белок (ЗФБ) и их аналоги, неорганические флуоресцентные метки на основе полупроводниковых нанокристаллов (квантовая точка), флуоресцентные метки на основе лантаноидов, таких как Еи3+ и Sm3+ и т.п.
В еще одном варианте осуществления, набор содержит третий компонент (компонент с), который способен специфически связываться с компонентом b. В этом случае определение Аро J, закрепленного на подложке лектином, осуществляется не путем прямого определения компонента b, а путем определения компонента с после его связывания с компонентом а.
В качестве третьего компонента набора может использоваться любая молекула при условии, что она способна специфически связываться с компонентом b. В одном варианте осуществления, компонент b модифицируется первым членом связывающей пары, а компонент с модифицируется вторым членом связывающей пары.
Термин «связывающая пара» относится к паре молекул (именуемых первым и вторым членом связывающей пары), обладающих способностью к специфическому связыванию посредством любого типа межмолекулярных взаимодействий, включая, но не ограничиваясь, биохимические, физиологические и/или химические взаимодействия. Связывающая пара включает любое взаимодействие иммунного типа, такое как антиген/антитело, антиген/фрагмент антитела, гаптен/антигаптен, а также взаимодействия неиммунного типа, такие как авидин/биотин, авидин/биотинилированные молекулы, фолиевая кислота/фолат-связывающий белок, гормон/рецептор гормона, лектин/углевод, лектин/молекула, модифицированная углеводами, фермент/субстрат фермента, фермент/ингибитор фермента, белок А/антитело; белок G/антитело; комплементарные нуклеиновые кислоты (включая последовательности ДНК, РНК и пептидные нуклеиновые кислоты (ПНК)), полинуклеотид/полинуклеотид-связывающий белок и т.п.
Должно быть понятно, что термины «первый» и «второй» член связывающей пары являются относительными и что каждый из вышеуказанных членов может рассматриваться как первый или второй член связывающей пары.
В еще более предпочтительном варианте осуществления, в котором компонент b набора в соответствии с изобретением представляет собой антитело, третий компонент представляет собой антитело, способное специфически связываться с упомянутым компонентом b. В этом случае второе антитело содержит метку. Для третьего компонента набора пригодны те же метки, что указаны выше для компонента b набора. Метка третьего компонента набора может представлять собой флуоресцентную группу, люминесцентную группу или фермент. Если обнаруживаемое соединение представляет собой фермент, то этот фермент должен быть способен производить обнаруживаемый сигнал, например, после добавления активатора, субстрата, усиливающего средства и т.п. Ферменты, пригодные в качестве обнаруживаемых меток для настоящего изобретения, и соответствующие субстраты включают:
 Щелочную фосфатазу:
Щелочную фосфатазу:
 Хромогенные субстраты: субстраты на основе п-нитрофенилфосфата (п-НФФ), 5-бром-4-хлор-3-индолилфосфата/нитросинего тетразолия (БХИФ/НСТ), быстрого красного/нафтол-AS-TS фосфата
Хромогенные субстраты: субстраты на основе п-нитрофенилфосфата (п-НФФ), 5-бром-4-хлор-3-индолилфосфата/нитросинего тетразолия (БХИФ/НСТ), быстрого красного/нафтол-AS-TS фосфата
 Флуорогенные субстраты: 4-метилумбеллиферилфосфат (4-МУФ), 2-(5'-хлор-2'-фосфорилоксифенил)-6-хлор-4-(3Н)-хиназолинон (ХФФХХ), 3,6-флуоресцеиндифосфат (3,6-ФДФ), соли диазония или быстрый голубой ВВ, быстрый красный TR или быстрый красный фиолетовый LB.
Флуорогенные субстраты: 4-метилумбеллиферилфосфат (4-МУФ), 2-(5'-хлор-2'-фосфорилоксифенил)-6-хлор-4-(3Н)-хиназолинон (ХФФХХ), 3,6-флуоресцеиндифосфат (3,6-ФДФ), соли диазония или быстрый голубой ВВ, быстрый красный TR или быстрый красный фиолетовый LB.
 Пероксидазы:
Пероксидазы:
 Хромогенные субстраты, имеющие в основе 2,2-азинобис (3-этилбензотиазолин-6-сульфоновая кислота) (ABTS), о-фенилендиамин (ОРТ), 3,3',5,5-тетраметилбензидин (ТМБ), о-дианизидин, 5-аминосалициловая кислота, 3-диметиламинобензойная кислота (ДМАБ) и 3-метил-2-бензотиазолингидразон (МБТГ), 3-амино-9-этилкарбазол (АЭК) и 3,3'-диаминобензидинтетрагидрохлорид (DAB).
Хромогенные субстраты, имеющие в основе 2,2-азинобис (3-этилбензотиазолин-6-сульфоновая кислота) (ABTS), о-фенилендиамин (ОРТ), 3,3',5,5-тетраметилбензидин (ТМБ), о-дианизидин, 5-аминосалициловая кислота, 3-диметиламинобензойная кислота (ДМАБ) и 3-метил-2-бензотиазолингидразон (МБТГ), 3-амино-9-этилкарбазол (АЭК) и 3,3'-диаминобензидинтетрагидрохлорид (DAB).
 Флуорогенные субстраты: 4-гидрокси-3-метоксифенилуксусная кислота, восстановленные феноксазины и восстановленные бензотиазины, включая реактив Amplex® красный, Amplex инфракрасный и восстановленные дигидроксантены.
Флуорогенные субстраты: 4-гидрокси-3-метоксифенилуксусная кислота, восстановленные феноксазины и восстановленные бензотиазины, включая реактив Amplex® красный, Amplex инфракрасный и восстановленные дигидроксантены.
 Гликозидазы:
Гликозидазы:
 Хромогенные субстраты: о-нитрофенил-β-D-галактозид (О-НФГ), п-нитрофенил-β-D-галактозид и 4-метилумбеллифенил-β-D-галактозид (МУГ) для B-D-галактозидазы.
Хромогенные субстраты: о-нитрофенил-β-D-галактозид (О-НФГ), п-нитрофенил-β-D-галактозид и 4-метилумбеллифенил-β-D-галактозид (МУГ) для B-D-галактозидазы.
 Флуорогенные субстраты: резоруфин-β-D-галактопиранозид, флуоресцеиндигалактозид (ФДГ). флуоресцеиндиглюкуронид,
Флуорогенные субстраты: резоруфин-β-D-галактопиранозид, флуоресцеиндигалактозид (ФДГ). флуоресцеиндиглюкуронид,
4-метилумбеллиферил-β-D-галактопиранозид,
карбоксиумбеллиферил-β-D-галактопиранозид и
фторированные кумарин-β-D-галактопиранозиды.
 Оксидоредуктазы (люцифераза):
Оксидоредуктазы (люцифераза):
 Люминесцентные субстраты: люциферин.
Люминесцентные субстраты: люциферин.
В случае ферментной метки набор может содержать в качестве дополнительного компонента один или более субстратов фермента
В еще более предпочтительном варианте осуществления, обнаруживаемое соединение, которое связывается со вторым членом связывающей пары, представляет собой флуоресцентное соединение. Используемый в настоящем изобретении термин «флуоресцентное соединение» относится ко всем соединениям, которые поглощают световое излучение определенной длины волны или диапазона длин волн и испускают свет определенной длины волны или диапазона длин волн. Флуоресцентные соединения, подходящие для использования в настоящем изобретении включают без ограничений бромид этидия, SYBR Green, флуоресцеинизотиоцианат (ФИТЦ), тетраметилродаминизотиол (ТРИТ), 5-карбоксифлуоресцеин, 6-карбоксифлуоресцеин, флуоресцеин, HEX (6-карбокси-2',4,4',5',7,7'-гексахлорфлуоресцеин), Oregon Green 488, Oregon Green 500, Oregon Green 514, Joe (6-карбокси-4',5'-дихлор-2',7'-диметоксифлуоресцеин), 5-карбокси-2',4',5',7'-тетрахлорфлуоресцеин, 5-карбоксиродамин, родамин, тетраметилродамин (Tamra), Rox (карбокси-Х-родамин), R6G (родамин 6G), фталоцианины, азиметины, цианины (Су2, Су3 и Су5), Texas Red, Princeston Red, BODIPY FL-Br2, BODIPY 530/550, BODIPY TMR, BODIPY 558/568, BODIPY 564/570, BODIPY 576/589, BODIPY 581/591, BODIPY TR, BODIPY 630/650, BODIPY 650/665, DABCYL, эозин, эритрозин, бромид этидия, зеленый флуоресцентный белок (ЗФБ) и их аналоги, неорганические флуоресцентные метки на основе полупроводниковых нанокристаллов (квантовая точка), флуоресцентные метки на основе лантаноидов, таких как Еи3+ и Sm3+ и т.п.
В некоторых случаях в дополнительном варианте осуществления набор содержит холостую пробу в качестве фонового контроля и/или стандартной кривой, содержащей различные концентрации гликозилированного Аро J.
В дополнительных объектах изобретение относится к использованию набора в соответствии с изобретением и как определено выше в способе для диагностики ишемии или ишемического повреждения тканей у пациента, для прогнозирования прогрессирования ишемии у пациента, перенесшего ишемическое событие, для определения прогноза у пациента, перенесшего ишемическое событие, или для определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью.
Способ определения гликозилированного Аро J в образце
Согласно еще одному объекту, изобретение относится к способу определения гликозилированного Аро J в образце, содержащем этапы:
(i) Введения образца в контакт с лектином, который специфически связывается с гликановым остатком, присутствующим в гликозилированном Аро J, при условиях, подходящих для образования комплекса между гликозилированным Аро J из образца и лектином, и
(ii) Определение количества комплекса, содержащего лектин и
гликозилированный Аро J, с N-ацетилглюкозамином (GlcNAc).
Термины «гликозилированный Аро J», «образец» и «лектин, который специфически связывается с гликановым остатком, присутствующим в гликозилированном Аро J» были подробно описаны в контексте способов диагностики и прогнозирования изобретения, а также в контексте набора в соответствии с изобретением, и в равной степени применимы к способу определения гликозилированного Аро J в соответствии с изобретением.
На этапе (i) способ определения гликозилированного Аро J содержит введение образца в контакт с лектином, который специфически связывается с гликановым остатком, присутствующим в гликозилированном Аро J, при условиях, подходящих для образования комплекса между гликозилированным Аро J из образца и лектином.
Подходящие условия для образования упомянутого комплекса могут быть определены специалистом в данной области и включают соответствующую температуру, время инкубации и рН. В конкретном варианте осуществления, температура составляет от 4 до 40°С, в частности, от 10 до 35°С, более конкретно от 15 до 30°С, предпочтительно от 20 до 25°С (комнатная температура). В конкретном варианте осуществления, рН составляет от 2 до 10, предпочтительно от 4 до 10. В конкретном варианте осуществления, этап (i) проводится в течение по меньшей мере 1 минуты, предпочтительно, по меньшей мере 5 минут, более предпочтительно по меньшей мере 30 минут, еще более предпочтительно по меньшей мере 60 минут.
В некоторых вариантах осуществления образец разводят перед введением в контакт с лектином. Подходящие разведения образца составляют от 1:10 до 1:100000, предпочтительно от 1:100 до 1:1000, более предпочтительно разведение образца плазмы крови составляет 1:200 или 1:1500
В одном варианте осуществления, лектин, используемый на этапе (i), представляет собой лектин, который специфически связывается с N-ацетилглюкозамином, или лектин, который специфически связывается с N-ацетилглюкозамином и сиаловой кислотой. В более предпочтительном варианте осуществления, лектин, который специфически связывается с N-ацетилглюкозамином, представляет собой лектин Datura stramonium, или, когда лектин специфически связывается с N-ацетилглюкозамином и сиаловой кислотой, он представляет собой лектин Triticum vulgaris.
В еще одном варианте осуществления, лектин, который специфически связывается с гликановым остатком, иммобилизирован. Подходящие подложки описаны в наборе изобретения.
После осуществления этапа (i) на протяжении времени, достаточного для образования комплекса между лектином и гликозилированным Аро J, присутствующим в образце, выполняется этап (ii). На этапе (ii) способ определения гликозилированного Аро J содержит определение количества комплекса, содержащего лектин и гликозилированный Аро J.
В одном варианте осуществления, комплексы, полученные на этапе (i), промывают до начала этапа (ii) для удаления любого Аро J, который может быть прикреплен к подложке посредством неспецифического связывания. Промывка после этапа (i) выполняется с использованием промывочного раствора. В конкретном варианте осуществления, промывочный раствор содержит одну или более солей. Предпочтительно соль, содержащаяся в промывочном растворе, представляет собой NaCl, содержащуюся в трис-буфере (ТСБ) или фосфатном буфере (ФСБ). Дополнительно или в качестве альтернативы промывочный раствор содержит по меньшей мере одно моющее средство. Предпочтительно, моющее средство выбрано из группы, состоящей из полисорбата 20 (Твин 20) и Тритона Х-100
Определение количества комплекса, содержащего лектин и гликозилированный Аро J, как правило, осуществляется с использованием реактива, который специфически связывается с полипептидом Аро J. В предпочтительном варианте осуществления, реактив, который специфически связывается с полипептидом Аро J, представляет собой антитела или их фрагменты, содержащие антигенсвязывающую область.
Антитела, пригодные для использования на этапе (ii) способа определения гликозилированного Аро J, были определены в контексте набора в соответствии с изобретением и в равной степени применимы к настоящему способу. В одном варианте осуществления, антитела связаны с обнаруживаемой меткой. Пригодные метки для антител к Аро J определены выше в контексте набора в соответствии с изобретением. В предпочтительном варианте осуществления, метка может быть определена посредством изменения по меньшей мере одного из ее химических, электрических или магнитных свойств.
В еще одном варианте осуществления, определение количества комплекса, содержащего лектин и гликозилированный Аро J осуществляется с использованием реактива, способного специфически связываться с реактивом, который специфически связывается с полипептидом Аро J. В еще одном варианте осуществления, третий реактив, способный специфически связываться с реактивом, который специфически связывается с полипептидом Аро J, представляет собой антитела или их фрагменты, содержащие антигенсвязывающую область, при этом комплекс обнаруживается посредством обнаружения антител, связанных с реактивом, который специфически связывается с Аро J. Это осуществляется путем использования антител, которые содержат обнаруживаемую метку. Пригодные метки для использования в антителах определены выше в контексте набора в соответствии с изобретением.
Метка может представлять собой флуоресцентную метку или ферментную метку.
***
Настоящее изобретение будет проиллюстрировано на следующих примерах, которые не предназначены для ограничения объема настоящего изобретения.
ПРИМЕРЫ
ПРИМЕР 1
Диагностическое значение Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и Аро J-GlcNAc при сердечной ишемии.
Протеомный профиль Аро J у пациентов с сердечной ишемией был ранее охарактеризован с использованием двумерного электрофореза (2-DE) с последующим определением посредством масс-спектрометрии (Cubedo, J., et al., 2011, Journal of proteome research 10: 211-220). В данном исследовании было продемонстрировано, что уровни специфических форм Аро J повышались (Аро J-29) или понижались (Аро J-15) в течение первых шести часов после начала события (фиг. 1). С применением этих критериев было выдвинуто предположение, что специфические формы Аро J (Аро J-15 и Аро J-29) являются маркерами повреждения тканей, вызываемого острым инфарктом миокарда (ОИМ). В том же исследовании также было проанализировано, могут ли изменения, определенные для Аро J-15 и Аро J-29, быть связаны с изменением профиля гликозилирования Аро J. В частности, были выделены сывороточные гликопротеины с использованием смеси конкавалина А и лектинов Triticum vulgaris (которая связывает белки с остатками α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac). Выделенные белки были проанализированы с использованием анализа 2-DE с последующим определением с использованием масс-спектрометрии. В данном анализе (фиг. 2) было установлено, что только пятна 1, 2, 4, 5, 8 и 11 содержали остатки α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac, тогда как пятна 3, 6, 7, 9, 10, 12 и 13 не имели этих остатков. Интенсивность пятен гликозилированного Аро J с остатками α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac была ниже у пациентов с ишемией до ОИМ по сравнению с контролями. Снижение было наиболее выраженным для форм 4 и 8. На ранней стадии ишемии наблюдалось 25% снижение общей интенсивности гликозилированного Аро J с остатками α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac. И наоборот, содержание форм Аро J без этих остатков (3, 6, 7, 10, 12 и 13) на ранней стадии ишемии повышалось.
Однако в связи с множественной специфичностью лектинов, использованных в приведенных выше анализах, эти анализы были не в состоянии определить, какие из различных гликозилированных форм Аро J (форм, содержащих остатки α-маннозы, форм, содержащих остатки α-глюкозы, форм, содержащих остатки (GlcNAc)2, и/или форм, содержащих остатки Neu5Ac) представляли собой биомаркеры, связанные с ишемическими повреждениями. Кроме того, с использованием лектина Artocarpus integrifolia, который связывается с белками с остатками α-галактозы и GalNAc, присутствующими только в О-гликанах, было установлено (фиг. 3), что только пятна 1, 3, 4, 6, 7, 8, 9, 11 и 12 содержали остатки α-галактозы и GalNAc, тогда как пятна 2, 5, 10 и 13 не содержали таких остатков. Таким образом, ранее опубликованное понижение в пятнах 1, 2, 4, 5, 8 и 11 указывало не только на понижение уровней форм, содержащих остатки α-маннозы, α-глюкозы, (GlcNAc)2 и Neu5Ac, поскольку некоторые из этих пятен также содержат О-гликозилированные остатки и более конкретно остатки α-галактозы и GalNAc.
Для определения присутствия различных типов остатков Аро J был использован специальный способ. Этот способ (далее - иммуноаффинный анализ ферментативного гликозилирования, или EGA) обеспечивает специфическое обнаружение и количественное определение различных гликозилированных форм Аро J. Этот EGA основан на: 1) первом этапе, на котором белки иммобилизируются путем их связывания со специфическим остатком гликозилирования (таблица 1), 2) втором этапе, на котором Аро J обнаруживается с использованием моноклональных или поликлональных антител к белковой последовательности Аро J, 3) конечном этапе, на котором количество специфической гликозилированной формы Аро J далее обнаруживается и количественно определяется репортерной системой или молекулой. Эта репортерная система может включать: а) колориметрическую систему, такую как вторичное антитело в сочетании с репортерной системой, такой как биотин-стрептавидин-HRP; b) физико-химическое изменение в системе (например, химическое, электрическое или магнитное изменение).
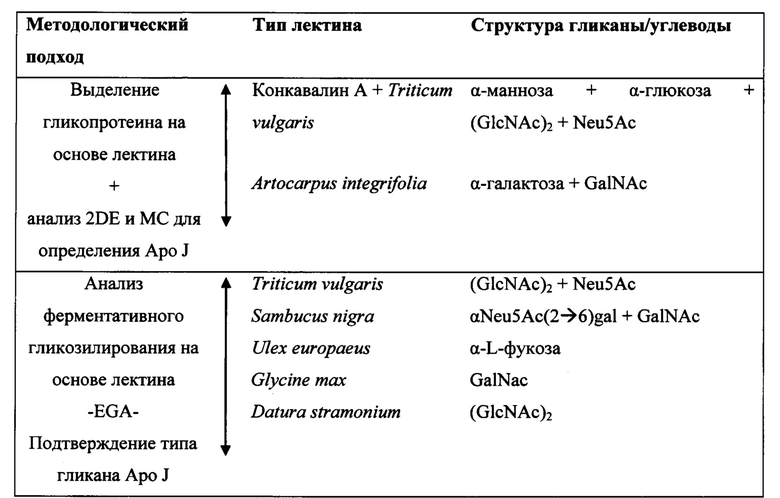
Таблица 1. Структуры гликанов и углеводов, присутствующие в Аро J, и специфический методологический подход на основе лектина для их обнаружения.
С использованием этого способа с различными лектинами было установлено, что гликозилированный Аро J может содержать следующие гликановые остатки: a) (GlcNAc)2 + Neu5Ac; b) aNeu5Ac(2→6)gal + GalNAc; с) α-L-фукоза; d) только GalNAc; e) только (GlcNAc)2 (фиг. 4).
EGA был далее использован для специфического измерения уровней Аро J с остатками (GlcNAc)2 + Neu5Ac (Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc) в образцах плазмы крови 38 пациентов с ишемией до ОИМ и 144 здоровых контрольных участников. Было установлено, что пациенты с ишемией до ОИМ показали понижение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc на 45% на ранней стадии ишемии по сравнению с контролями (ишемия до ОИМ - 264±18; контроль 473±6 цмкг/мл; Р<0,0001; фиг. 5А). Образцы у пациентов с ишемией до ОИМ были взяты на момент госпитализации (t=0) в течение первых 6 часов после начала боли в груди и до появления маркеров некроза (тропонин Т и КК). На этот момент пациенты не получали лечения с начала события. Статистический анализ правильности полученных измерений показал, что измерение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc с использованием EGA демонстрирует высокое дискриминирующее значение для определения наличия ишемии миокарда с площадью под кривой (AUC) 0,934 (Р<0,0001) и пороговым значением 332 μмкг/мл при чувствительности 97% и специфичности 71% (фиг. 5В и таблица 2). Таким образом, измерение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc можно использовать в качестве биомаркера для диагностики ишемии.
Далее мы проанализировали уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у 212 пациента с ИMпST с использованием способа EGA. Образцы отбирали у пациентов с ИMпST (включая новые и вторичные события) на момент госпитализации с различным временем развития ишемической боли (1-60 ч), включая пациентов с положительным выявлением тропонина Т на момент госпитализации (группа пациентов с некрозом). Пациенты с ИMпST показали снижение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в плазме крови на 15% на момент госпитализации по сравнению с контрольной группой (ИMпST - 402±8 vs. контроль 473±6 μг/мл; Р<0,0001; фиг. 6А). - Статистический анализ правильности полученных измерений показал, что измерение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc с использованием EGA демонстрирует дискриминирующую способность для определения наличия ишемии миокарда с площадью под кривой (AUC) 0,713 (Р<0,0001) и пороговым значением 409 цмкг/мл при чувствительности 80% и специфичности 53% (фиг. 6В).
После дальнейшего применения EGA для специфического измерения Аро J с остатками (GlcNAc)2 (Аро J-GlcNAc) с использованием лектина Datura stramonium у 340 пациентов с ИMпST и 139 здоровых контролей у пациентов с ИMпST было установлено снижение уровней Аро J-GlcNAc в плазме крови на 35% на момент госпитализации (ИMпST - 328±7 vs. контроль 506±12 μмкг/мл; Р<0,0001; фиг. 6С). Статистический анализ правильности полученных измерений показал, что измерение уровней Аро J-GlcNAc с использованием EGA демонстрирует высокую дискриминирующую способность для определения наличия ишемии миокарда с площадью под кривой (AUC) 0,830 (Р<0,0001) и пороговым значением 393ц г/мл при чувствительности 81% и специфичности 72% (фиг.6D).
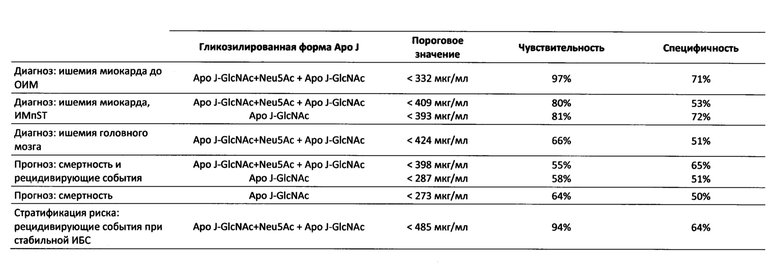
Таблица 2. Пороговые значения и связанная чувствительность и специфичность, применимые для способа диагностики повреждений миокарда, способа диагностики ишемии головного мозга, способа прогнозирования смертности и рецидивирующих событий и для способа стратификации риска у пациентов, страдающих стабильной ИБС, с соответствующими значениями чувствительности и специфичности.
ПРИМЕР 2
Прогностическое значение Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и Аро J-GlcNAc
На втором этапе мы оценили, может ли специфическое количественное определение гликозилированных форм Аро J иметь прогностическое значение. Уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc значимо обратно коррелировали со временем ишемии (определенным как прошедшее время с начала симптомов до госпитализации; R=-0,259, Р=0,0003; фиг. 7А). Кроме того, измерение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у 82 пациентов с ИMпST через 3 дня после госпитализации показало прогрессирование заболевания по сравнению с моментом госпитализации (t=72 ч: 331±10 vs. t=0: 402±8 μг/мл; Р<0,0001; фиг. 7В). При анализе уровней Аро J-GlcNAc наблюдалась значимая обратная корреляция со временем ишемии (R=-0,113, Р=0,048; фиг. 7С). Эти результаты подчеркивают, что Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и Аро J-GlcNAc являются новыми биомаркерами прогрессирования ишемии.
Кроме того, у пациентов с ИMпST с конечной степенью кровотока по классификации TIMI 0 или 1, которая связана с неблагоприятным прогнозом в связи с повышенным риском больничной смертности и смертности в течение 6 месяцев, были продемонстрированы сниженные уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в плазме по сравнению с уровнями у пациентов с ИMпST с конечной степенью кровотока по классификации TIMI ≥2 (фиг. 8А). Кроме того, у пациентов, перенесших кардиогенный шок, связанный с неблагоприятным прогнозом после ИMпST, были продемонстрированы уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в плазме крови на 12% ниже при госпитализации по сравнению с пациентами, которые не переносили кардиогенного шока (фиг. 8В).
Кроме того, наблюдалась значимая обратная корреляция между уровнями Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и оценкой риска по шкале GRACE, которая связана со смертностью (R=-0,257, Р=0,0002; фиг. 9А). Кроме того, исследуя изменения уровней Аро J-GlcNAc+Neu5Ac при последующем наблюдении 82 пациентов с ИMпST, мы установили, что у этих пациентов, уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc которых через 3 дня после события были даже ниже, чем на момент госпитализации, значения оценки риска по шкале GRACE были выше (Р=0,002; фиг. 9В). Аналогичным образом уровни Аро J-GlcNAc также значимо обратно коррелировали с оценкой риска GRACE (R=-0,184, Р=0,0006; фиг. 9С). Все эти результаты указывают на неожиданную роль Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и Аро J-GlcNAc в качестве маркеров стратификации риска в контексте ишемических событий.
Кроме того, анализ выживаемости Каплана-Мейера показал для пациентов с уровнями Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc ниже медианного значения группы ИMпST на момент госпитализации значимые различия встречаемости рецидивирующих ишемических событий и смертности через 6 месяцев последующего наблюдения (Р=0,008; фиг. 10А). Этот эффект не наблюдался при выполнении того же анализа с использованием тропонина Т (Р=0,363; фиг. 10В). Уровни Аро J-GlcNAc также имеют прогностическое значение, поскольку анализ выживаемости Каплана-Мейера показал для пациентов с ИMпST с уровнями Аро J-GlcNAc в пределах самого низкого квартиля на момент поступления (<236,8 μмкг/мл) значимое снижение выживаемости через 6 месяцев последующего наблюдения (Р=0,015; фиг. 10С). Значимые различия также наблюдались при использовании встречаемости рецидивирующих ишемических событий и смертности через 6 месяцев в качестве конечных точек в анализе Каплана-Мейера между пациентами с ИMпST с уровнями Аро J-GlcNAc в пределах самого низкого квартиля на момент поступления (<236,8 μг/мл) и пациентами с более высокими значениями Аро J-GlcNAc на момент поступления (Р=0,031; фиг. 10D). Таким образом, наши результаты указывают на роль уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc и Аро J-GlcNAc в плазме крови в качестве прогностических маркеров после проявления ишемии.
ПРИМЕР 3
Прогностическое значение Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc для проявления рецидивирующих ишемических событий (сердечных или церебральных) в контексте стабильной ишемической болезни сердца (СИБС). Настоящее исследование показало неожиданное свойство измерения Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc - прогностическое значение для проявления рецидивирующих ишемических событий (сердечных или церебральных) в контексте стабильной ишемической болезни сердца (СИБС). Мы анализировали уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в группе пациентов с хронической ИБС (N=34), которые перенесли острый коронарный синдром (ОКС) в среднем за 0,6±0,04 года до взятия образцов и наблюдались на протяжении 2,3±0,3 года после этого (фиг. 11А). Образцы плазмы крови были получены у пациентов из двух групп: тех, которые перенесли острое ишемическое событие (любой острый коронарный синдром (ОКС), инсульт или преходящее ишемическое событие (ПИС)) с последующим наблюдением (N=16), и тех, которые не имели острых ишемических событий (N=18) в течение периода последующего наблюдения. Значимые различия в возрасте, встречаемости диабета и гипертензии, а также уровнях холестерина между обеими группами отсутствовали. Никто из включенных пациентов не был курильщиком, и все принимали антитромботические препараты на момент взятия образцов. У пациентов, которые перенесли рецидивирующее событие, наблюдались уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc на 28% ниже перед событием по сравнению с пациентами без событий в период последующего наблюдения (фиг. 11В). Рабочая характеристическая кривая (ROC) показала прогностическое значение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc для проявления рецидивирующих ишемических событий у пациентов со стабильной ИБС (фиг. 11С). В частности, в настоящем исследовании уровни Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc ниже 485 μмкг/мл обеспечивали возможность прогнозирования проявления рецидивирующего ишемического события у пациентов со стабильной ИБС с чувствительностью 94% и специфичностью 64% (таблица 2). Таким образом, Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc демонстрирует дополнительную ценность в качестве маркера скрытого ишемического процесса, предшествующего проявлению рецидивирующего ишемического события у пациентов со стабильной ИБС.
ПРИМЕР 4
Роль Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc в качестве биомаркера при ишемии головного мозга Кроме того, измерение уровней Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc у 174 пациентов с инсультом показало 8% снижение по сравнению со 164 здоровыми контролями (инсульт - 418±7 vs. контроль 453±7 μмкг/мл; Р=0,0008; фиг. 12), показывая, что Аро J-GlcNAc+Neu5Ac + Аро J-GlcNAc также является биомаркером ишемии головного мозга.
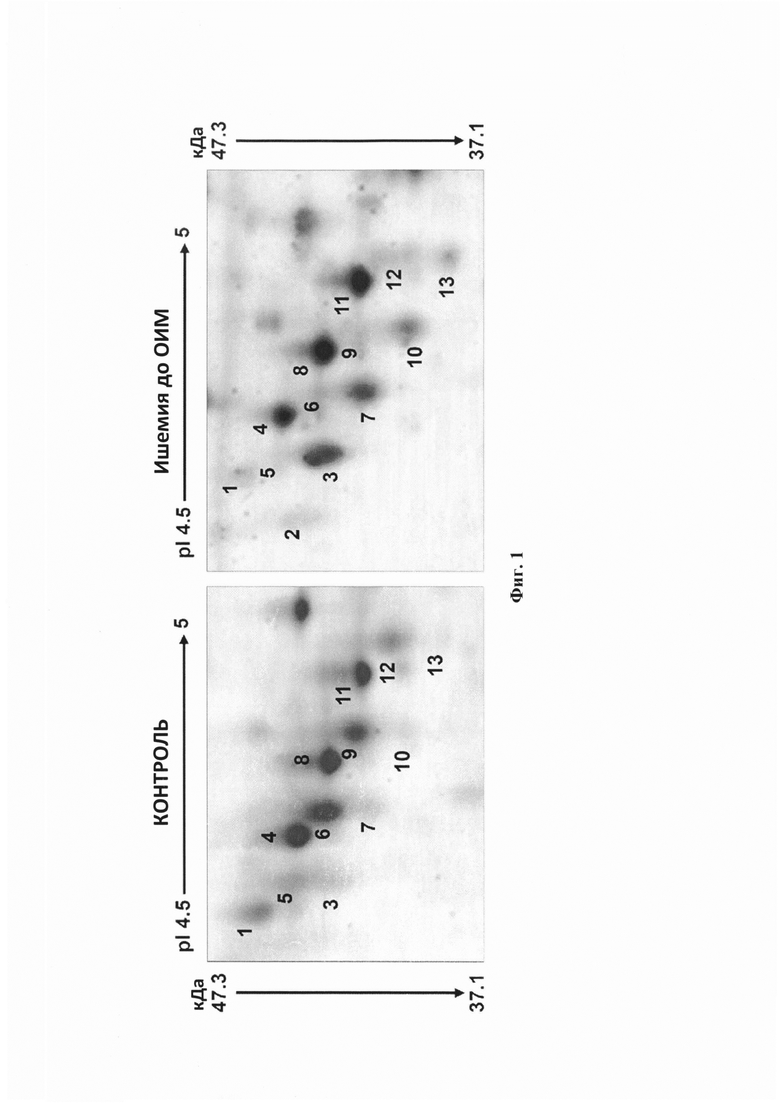
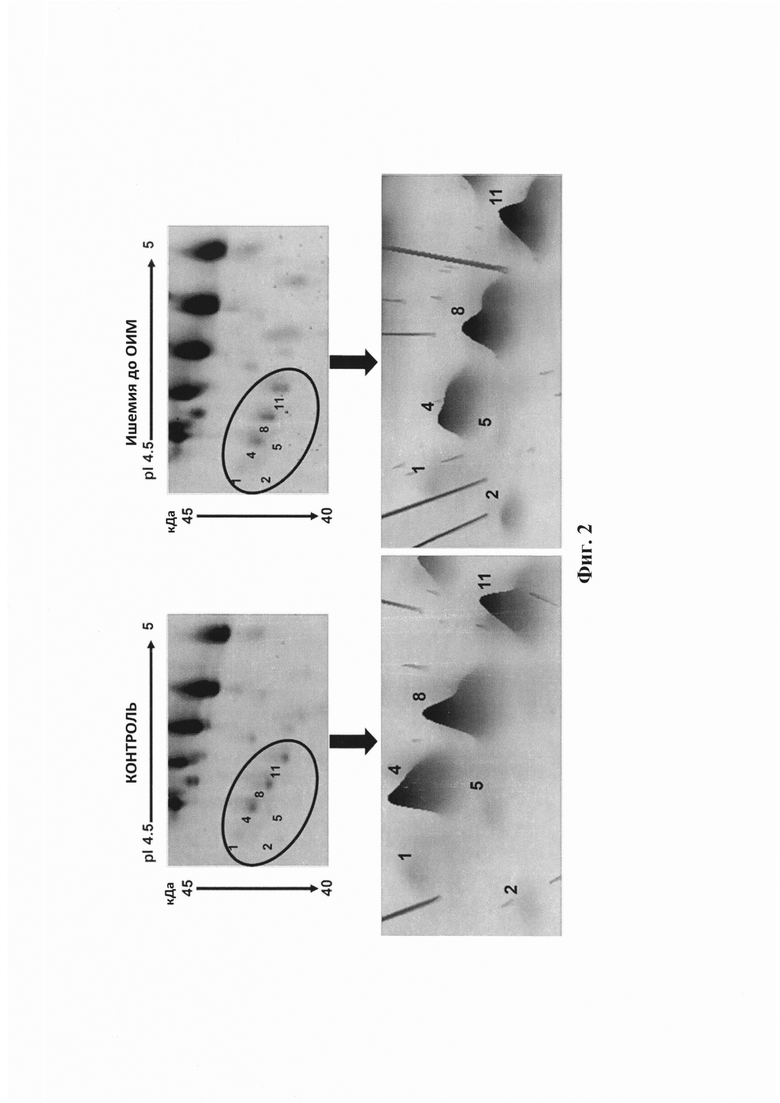
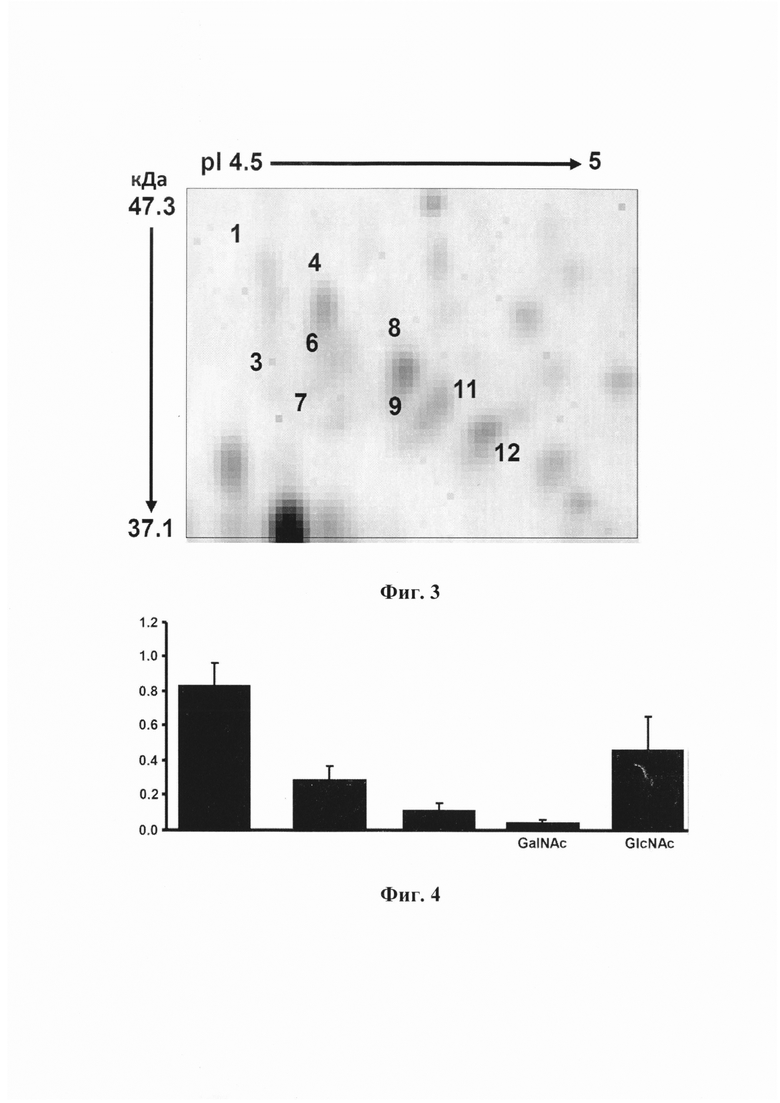
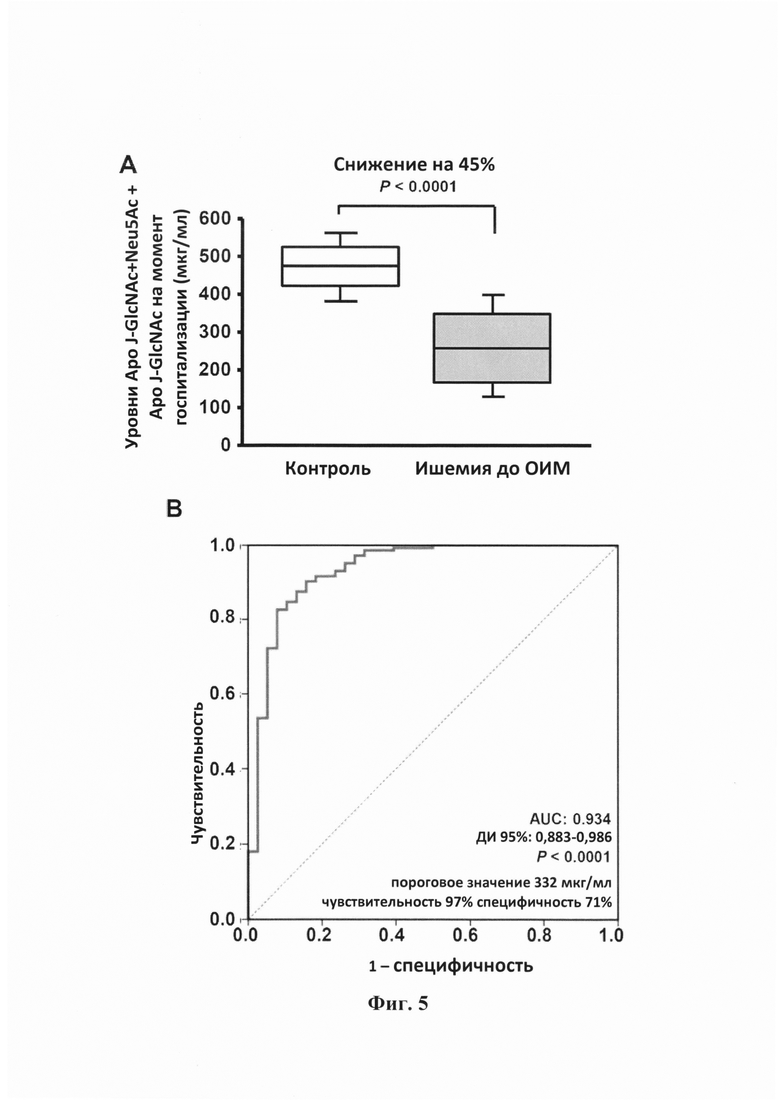
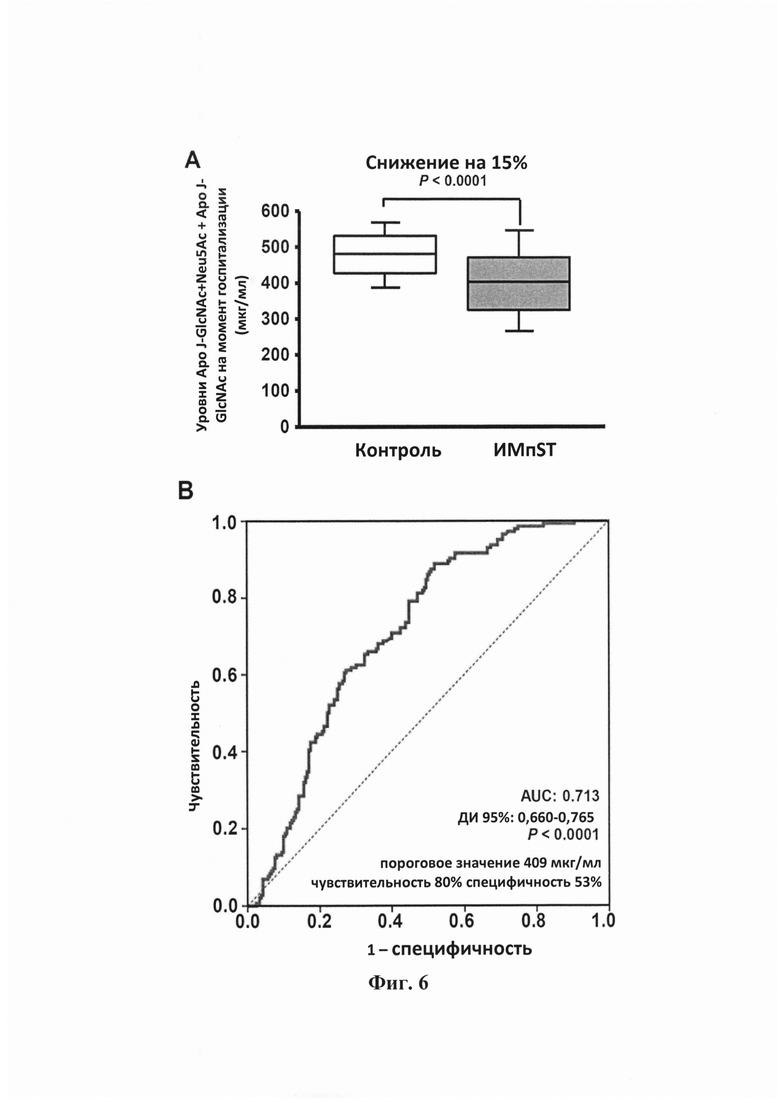
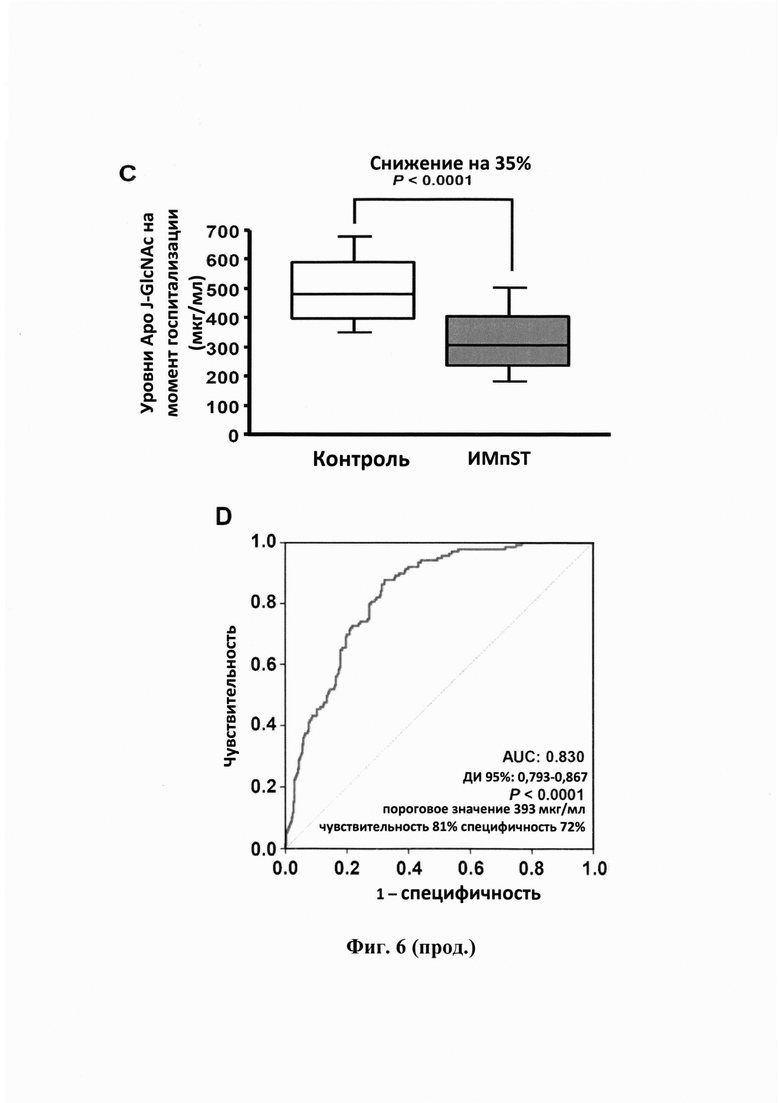
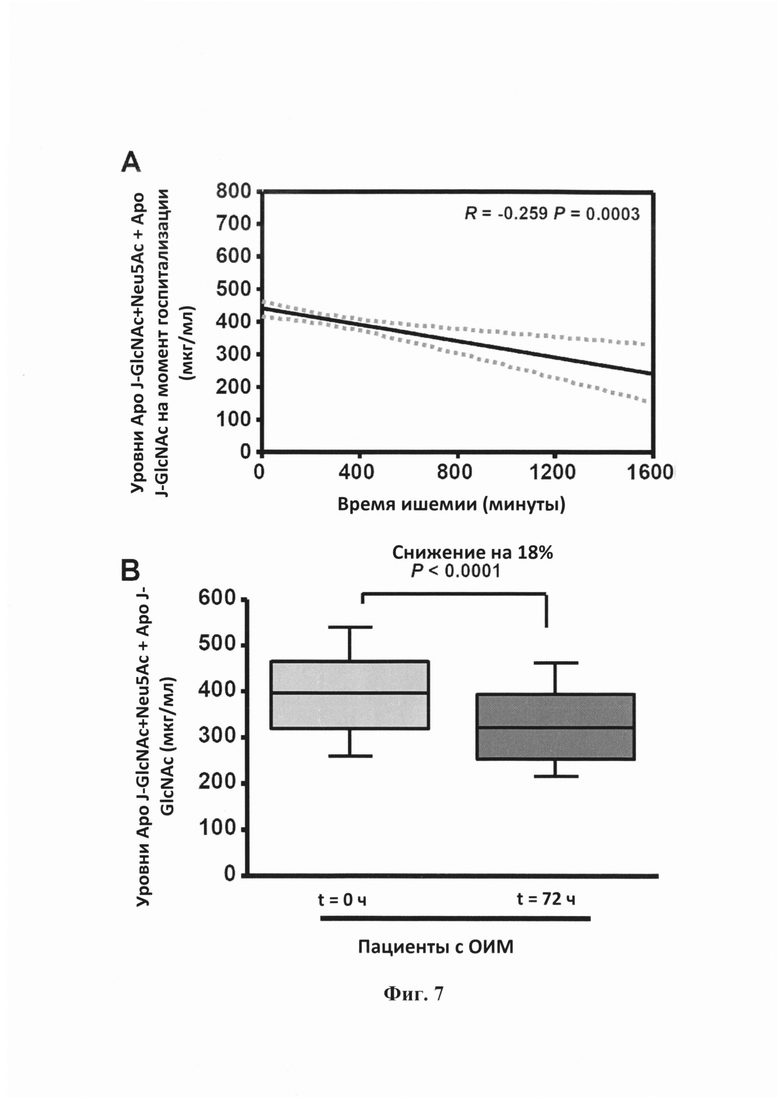
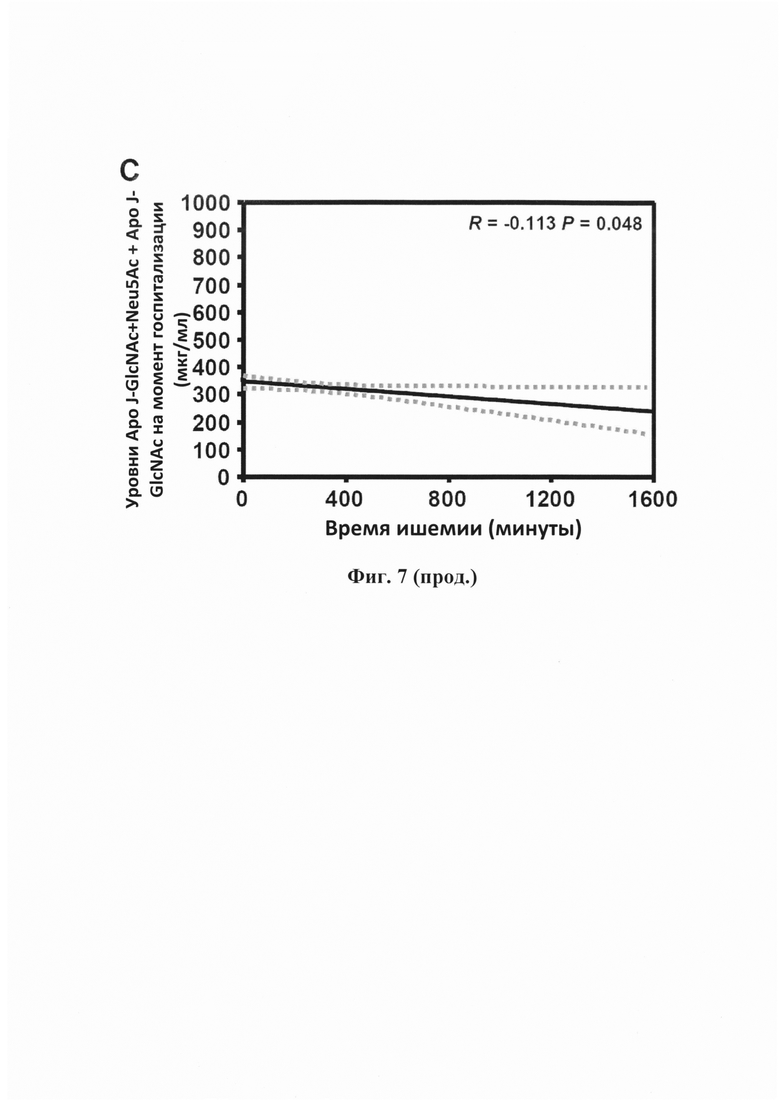
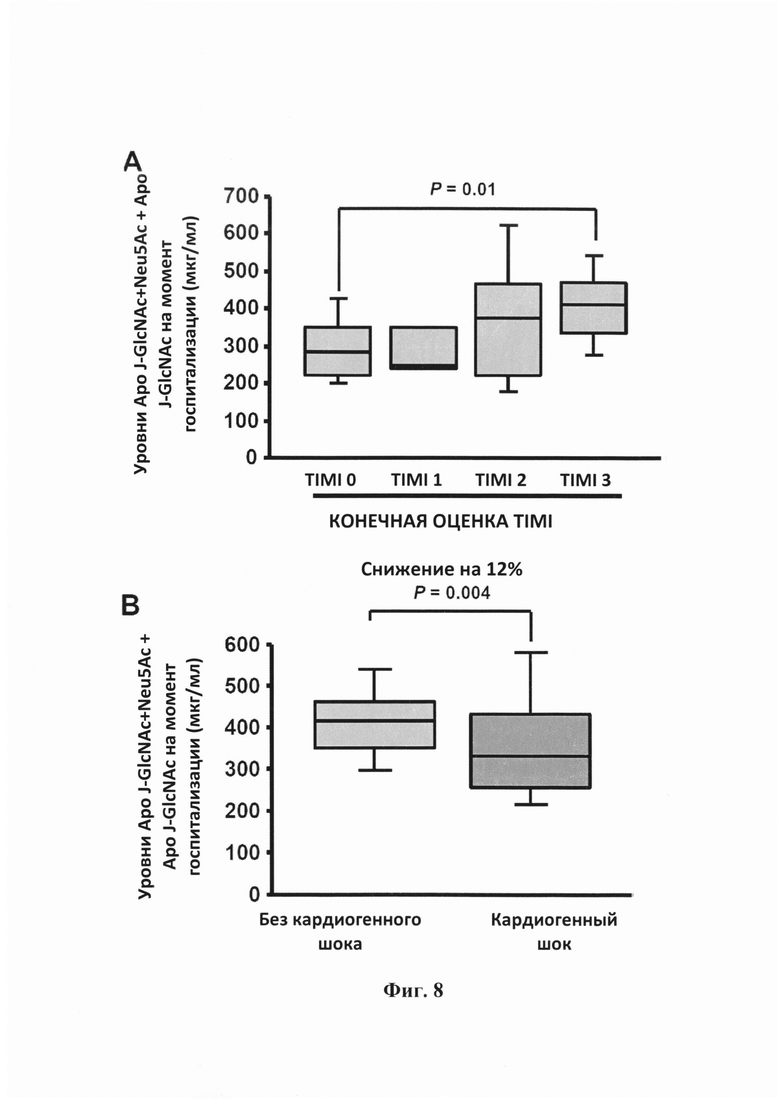
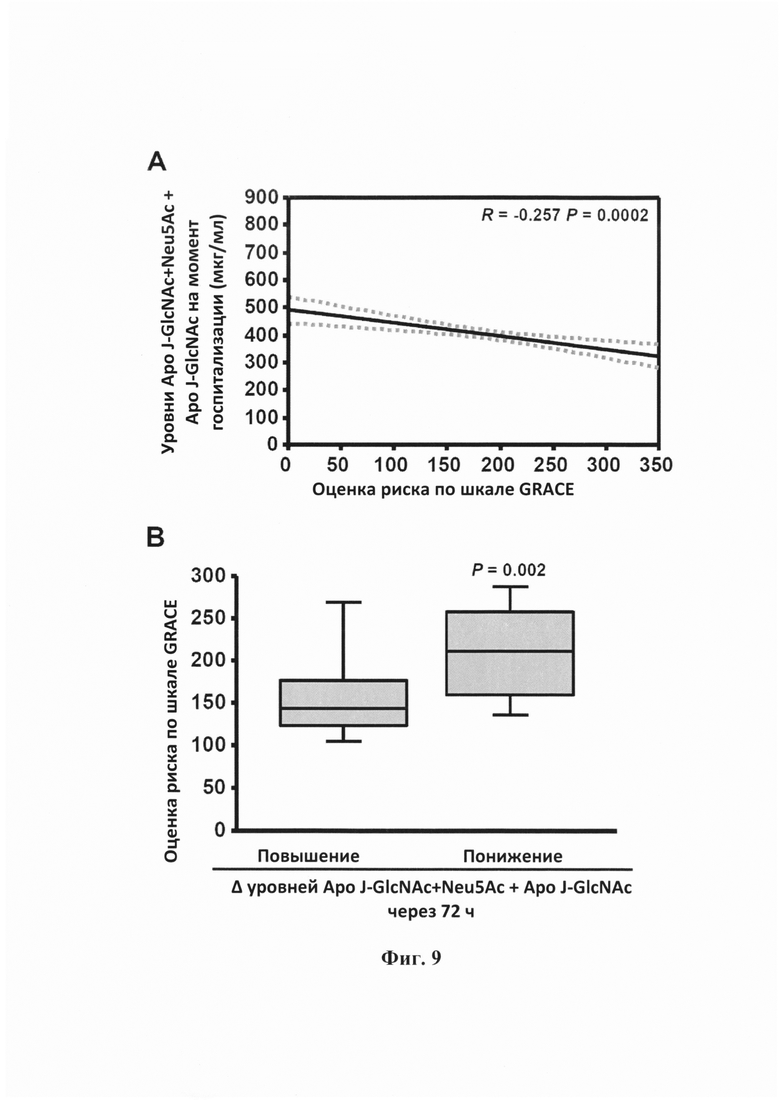
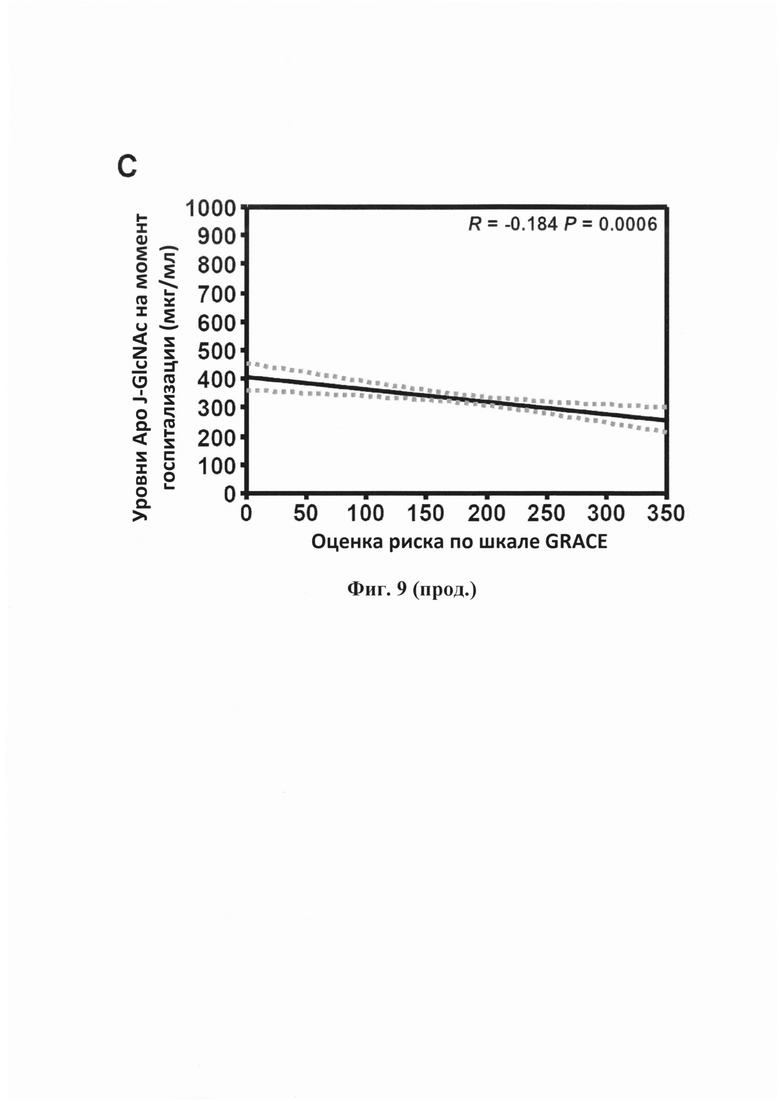
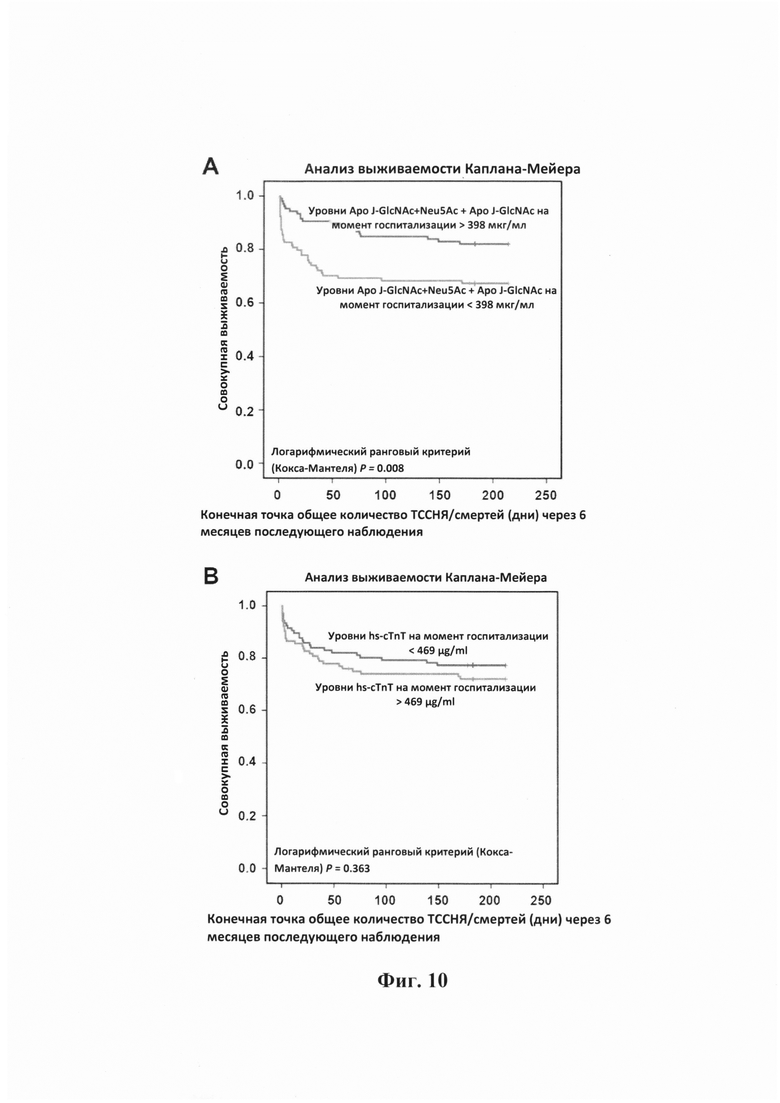
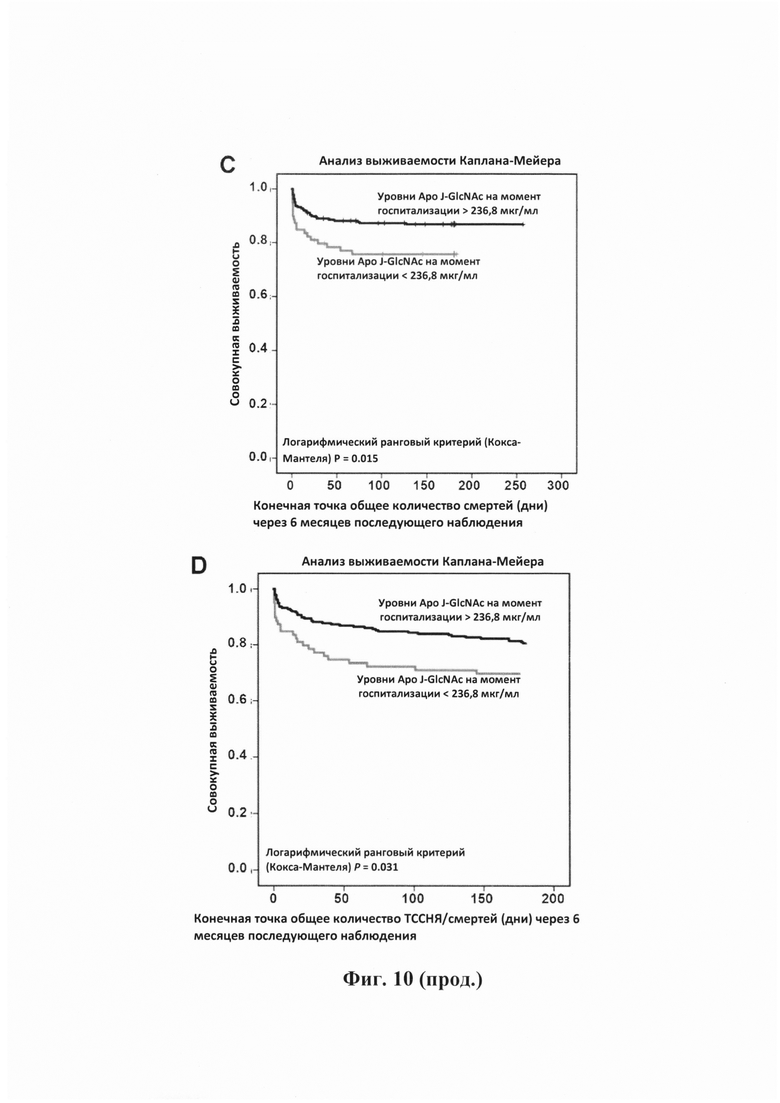
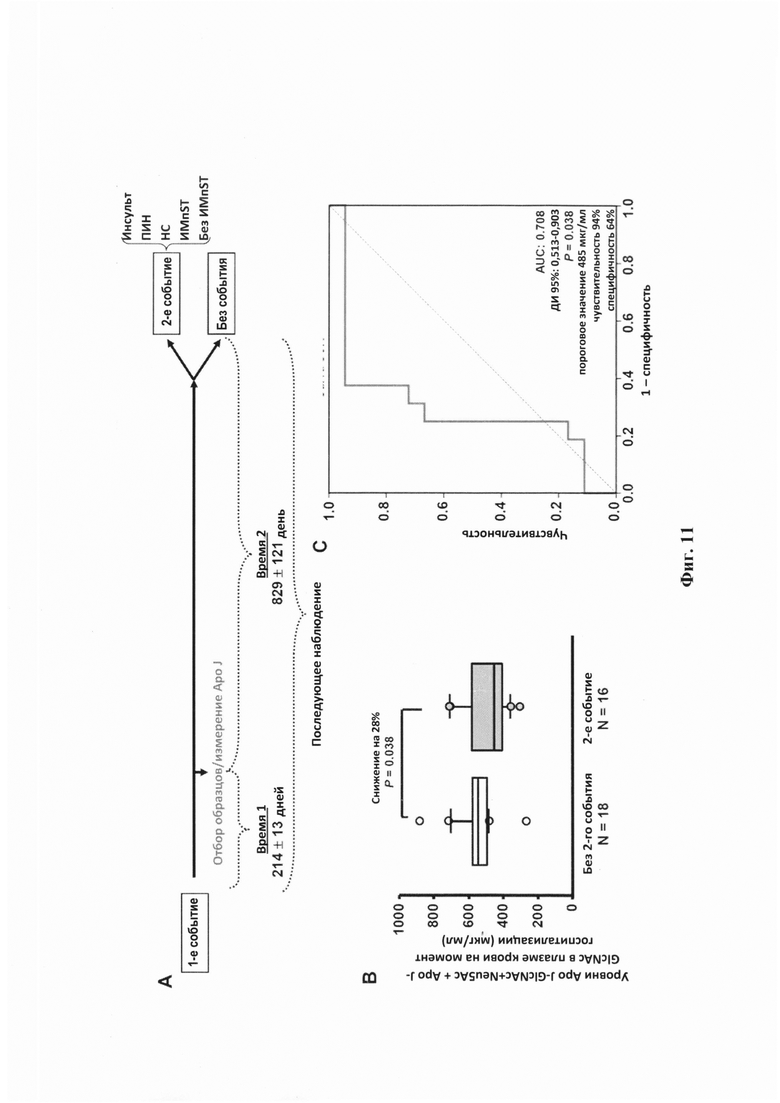
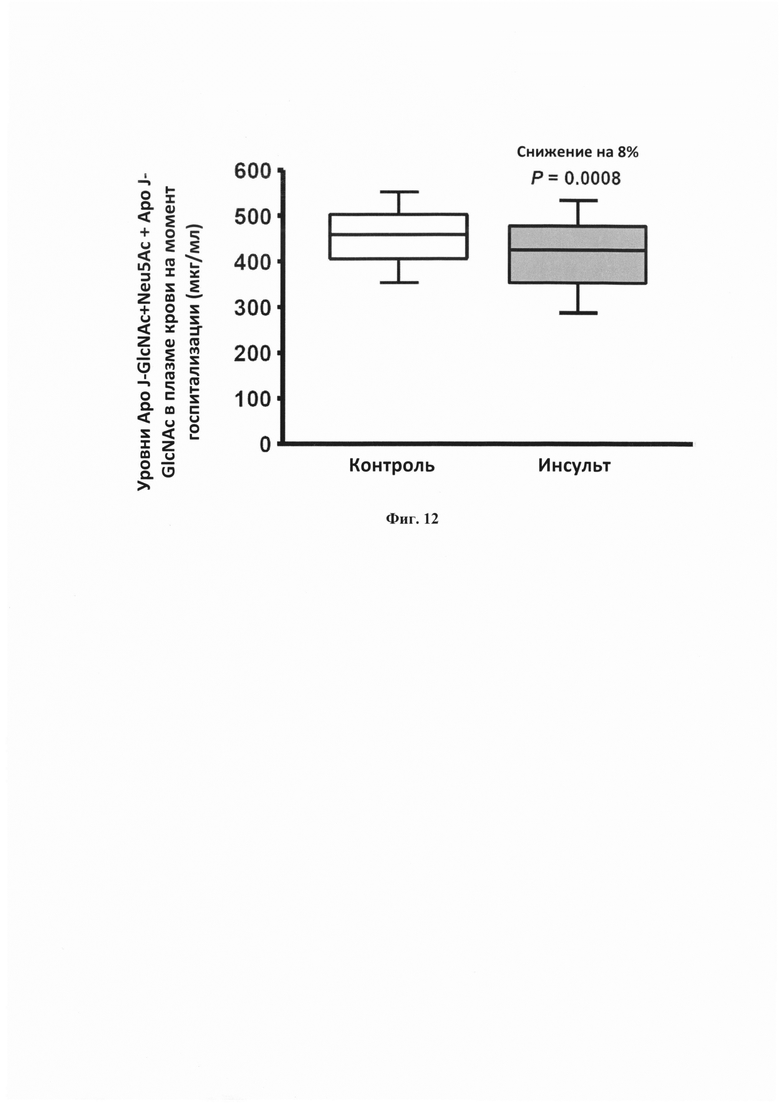
Группа изобретений относится к области химии и медицины. 1-3 объекты представляют собой способы диагностики ишемии или ишемического повреждения тканей у пациента, прогнозирования прогрессирования ишемии или определения прогноза у пациента, перенесшего ишемическое событие, определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью, включающие определение в образце пациента уровней гликозилированного аполипопротеина J (Аро J), содержащего остатки N-ацетилглюкозамина или содержащего остатки N-ацетилглюкозамина и сиаловой кислоты. 4 и 5 объекты – набор для определения указанных форм гликозилированного Аро J в образце, содержащий иммобилизированный на подложке лектин, и соответствующее вышеуказанным способам применение набора. 6 объект – способ определения гликозилированного Аро J в образце. Технический результат заключается в высокой чувствительности к изменениям концентрации указанных форм гликозилированного Аро J при их определении в образце и специфичности диагностики ишемии, основанной на определении указанных гликозилированных форм Аро J, а также в применении определения уровней указанных форм гликозилированного Аро J для выявления текущего ишемического события, для прогнозирования у пациентов, которые перенесли ишемическое событие, и для определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью сердца. 6 н. и 26 з.п. ф-лы, 12 ил., 2 табл., 4 пр.
1. Способ диагностики ишемии или ишемического повреждения тканей у пациента, включающий определение в образце указанного пациента уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в котором пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина, по отношению к опорному значению или пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, по отношению к опорному значению указывают на то, что пациент страдает ишемией или ишемическим повреждением тканей, при этом образцом является биологическая жидкость, выбранная из группы, включающей кровь, слюну, плазму, сыворотку, мочу, спинномозговую жидкость или кал.
2. Способ по п. 1, в котором под ишемией понимают ишемию миокарда или головного мозга.
3. Способ по п. 2, в котором под ишемией миокарда понимают острую ишемию миокарда или микрососудистую стенокардию.
4. Способ по п. 2, в котором под ишемией головного мозга понимают инсульт.
5. Способ по п. 1, в котором пациент предположительно переносит ишемическое событие.
6. Способ по п. 5, в котором определение осуществляют в течение первых 6часов после начала предполагаемого ишемического события, до повышения уровней, по меньшей мере, одного маркера некроза или до получения пациентом любого лечения для предполагаемого ишемического события.
7. Способ прогнозирования прогрессирования ишемии у пациента, перенесшего ишемическое событие, или определения прогноза у пациента, перенесшего ишемическое событие, включающий определение в образце указанного пациента уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в котором пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина, по отношению к опорному значению или пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, по отношению к опорному значению указывают на прогрессирование ишемии или неблагоприятный прогноз для пациента, при этом образцом является биологическая жидкость, выбранная из группы, включающей кровь, слюну, плазму, сыворотку, мочу, спинномозговую жидкость или кал.
8. Способ по п. 7, в котором под ишемическим событием понимают миокардиальное ишемическое событие.
9. Способ по п. 8, в котором под миокардиальным ишемическим событием понимают инфаркт миокарда с подъемом сегмента ST.
10. Способ по п. 7, в котором прогноз для пациента определяют как рискрецидива в течение 6 месяцев, риск больничной смертности или риск смертности в течение 6 месяцев.
11. Способ определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью, включающий определение в образце указанного пациента уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в котором пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина, по отношению к опорному значению или пониженные уровни Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, по отношению к опорному значению указывают на повышенный риск возникновения у пациента рецидивирующего ишемического события, при этом образцом является биологическая жидкость, выбранная из группы, включающей кровь, слюну, плазму, сыворотку, мочу, спинномозговую жидкость или кал.
12. Способ по п. 11, в котором пациент, страдающий стабильной ишемической болезнью, переносил острый коронарный синдром перед стабильной ишемической болезнью сердца.
13. Способ по п. 11, в котором под рецидивирующим ишемическим событием понимают острый коронарный синдром, инсульт или преходящее ишемическое событие.
14. Способ по любому из пп. 1-13, в котором уровень гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), соответствует уровню Аро J, способного специфически связываться с лектином Datura stramonium, или в котором уровни гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) или сиаловой кислоты, соответствуют уровням Аро J, способного специфически связываться с лектином Triticum vulgaris.
15. Набор для определения гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, в образце, содержащий
a. Первый реактив, представляющий собой лектин, выполненный с возможностью специфически связываться с гликановым остатком, выбранным из группы, включающей N-ацетилглюкозамин и сиаловую кислоту, при этом лектин иммобилизирован на подложке, и
b. Второй реактив, выполненный с возможностью специфически связываться с полипептидом Аро J.
16. Набор по п. 15, в котором лектин представляет собой лектин из Triticum vulgaris, лектин из Datura stramonium или их сочетание.
17. Набор по п. 15, в котором второй реактив представляет собой антитела или их фрагменты, содержащие антигенсвязывающую область.
18. Набор по п. 15, в котором второй реактив содержит метку.
19. Набор по п. 18, в котором метка может быть определена посредством изменения по меньшей мере одного из ее химических, электрических или магнитных свойств.
20. Набор по п. 15, содержащий третий реактив, выполненный с возможностью специфически связываться со вторым реактивом.
21. Набор по п. 20, в котором третий реактив представляет собой антитела или их фрагменты, содержащие антигенсвязывающую область.
22. Применение набора по любому из пп. 15-21 для диагностики ишемии или ишемического повреждения тканей у пациента, для определения прогрессирования ишемии у пациента, перенесшего ишемическое событие, для определения прогноза у пациента, перенесшего ишемическое событие, или для определения риска возникновения рецидивирующего ишемического события у пациента, страдающего стабильной ишемической болезнью.
23. Способ определения гликозилированного Аро J в образце, включающий этапы:
(i) Введения образца в контакт с лектином, который специфически связывается с гликановым остатком, присутствующим в гликозилированном Аро J, при условиях, подходящих для образования комплекса между гликозилированным Аро J из образца и лектином, при этом лектин, который специфически связывается с гликановым остатком, иммобилизирован на подложке, и
(ii) Определения количества комплекса, содержащего лектин и гликозилированный Аро J.
24. Способ по п. 23, в котором под лектином, используемым на этапе (i), понимают лектин, который специфически связывается с N-ацетилглюкозамином, или лектин, который специфически связывается с N-ацетилглюкозамином и сиаловой кислотой.
25. Способ по п. 23, в котором лектин, который специфически связывается с N-ацетилглюкозамином, представляет собой лектин Datura stramonium, или, когда лектин специфически связывается с N-ацетилглюкозамином и сиаловой кислотой, он представляет собой лектин Triticum vulgaris.
26. Способ по п. 23, в котором комплекс на этапе (ii) обнаруживают с использованием реактива, который специфически связывается с полипептидом Аро J.
27. Способ по п. 26, в котором под реактивом, который специфически связывается с полипептидом Аро J, понимают антитела или их фрагменты, содержащие антигенсвязывающую область.
28. Способ по п. 27, в котором антитела связаны с обнаруживаемой меткой.
29. Способ по п. 28, в котором метка может быть определена посредством изменения, по меньшей мере, одного из ее химических, электрических или магнитных свойств.
30. Способ по любому из пп. 23-29, в котором обнаружение осуществляют с использованием реактива, способного специфически связываться среактивом, который специфически связывается с полипептидом Аро J.
31. Способ по п. 30, в котором под реактивом, способным специфически связываться с реактивом, который специфически связывается с полипептидом Аро J, понимают антитела или их фрагменты, содержащие антигенсвязывающую область.
32. Способ по любому из пп. 1-14, в котором определение уровня гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc), или уровней гликозилированного Аро J, содержащего остатки N-ацетилглюкозамина (GlcNAc) и сиаловой кислоты, выполняют с использованием набора по любому из пп. 15-21, или способа по любому из пп. 23-31.
| WO 2011098645 A1, 18.08.2011 | |||
| CUBEDO J | |||
| et al | |||
| Proteomic signature of Apolipoprotein J in the early phase of new-onset myocardial infarction // Journal of proteome research | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| - Vol | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| - No | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - P | |||
| Способ добывания бензина и иных продуктов из нефти, нефтяных остатков и пр. | 0 |
|
SU211A1 |
| COMUNALE M | |||
| A | |||
| et al | |||
| Novel changes in glycosylation of serum Apo-J in patients with hepatocellular carcinoma // Cancer Epidemiology | |||
Авторы
Даты
2021-06-21—Публикация
2017-04-12—Подача