Область техники, к которой относится изобретение
Настоящее изобретение относится к композициям, включающим конъюгаты фактора VII, которые обладают заданным характером гликозилирования.
Предпосылки создания изобретения
Фактор VII представляет собой витамин К-зависимый белок плазмы, синтезируемый в печени и секретируемый в кровоток в виде одноцепочечного гликопротеина с молекулярной массой примерно 50 кДа. Зимоген фактора VII превращается в активированную форму (фактор VIIа (FVIIа)) путем протеолитического расщепления. FVIIа в комплексе с тканевым фактором (ТФ) способен превращать и фактор IX, и фактор Х в их активированные формы, которые впоследствии участвуют в реакциях, ведущих к быстрому генерированию тромбина и образованию фибрина.
Белки, участвующие в каскаде процесса свертывания крови, включающие, например, фактор VII, фактор VIII, фактор IX, фактор Х и белок С, являются, как уже доказано, полезными терапевтическими средствами, применяемыми для лечения множества патологических состояний. Соответственно, имеется повышенная потребность в композициях, включающих указанные белки, которые были бы фармацевтически приемлемыми и обладали однородной и заданной клинической эффективностью.
В связи с тем, что использование человеческой плазмы в качестве источника фармацевтических продуктов имеет множество недостатков, предпочтительно получать такие белки с использованием рекомбинантных систем. Белки свертывания, однако, являются объектом множества модификаций, осуществляемых в процессе трансляции и после трансляции, которые включают, например, аспарагинсвязанное (N-связанное) гликозилирование, О-связанное гликозилирование и γ-карбоксилирование остатков глутаминовой кислоты. Указанные модификации могут количественно и качественно отличаться в случае использования гетерологичных клеток в качестве хозяйских клеток для крупномасштабного получения белков. В частности, процесс получения в системе гетерологичных клеток зачастую приводит к получению разной совокупности гликоформ, которые характеризуются наличием идентичных полипептидов, обладающих разными ковалентно присоединенными олигосахаридными структурами.
В разных системах вариации в структуре олигосахаридной части терапевтических белков связаны, в том числе, с изменениями в иммуногенности и клиренсе in vivo.
Кроме клиренса in vivo существенным для определения периода полувыведения in vivo является длительность периода времени, в течение которого указанные соединения являются "терапевтически доступными" в организме.
Период полувыведения циркулирующего в крови rFVIIа составляет примерно 2,3 часа ("Summary Basis for Approval for NovoSeven©", FDA reference number 96-0597).
Коммерческие препараты человеческого рекомбинантного фактора VIIа предлагаются в виде препарата NovoSeven®. Препарат NovoSeven® представляет собой единственный рекомбинантный фактор VIIа, применяемый для эффективного и надежного лечения кровотечений, который доступен на фармацевтическом рынке. Относительно высокие дозы и частое введение препарата необходимы для достижения и поддержания желательного терапевтического или профилактического эффекта. Как следствие такого режима возникает сложность в регуляции адекватной дозы и потребность в частых внутривенных введениях, что накладывает определенные ограничения на качество жизни пациентов.
Молекула с более длительным периодов полувыведения из кровотока могла бы способствовать снижению количества необходимых введений. В связи со связью имеющегося в настоящее время продукта фактора VIIа с частыми введениями имеется явная потребность в создании улучшенных молекул фактора VII.
Одним из способов улучшения циркуляции является создание условий, при которых уровень клиренса из организма будет снижен. Как отмечалось, вариации в структуре олигосахарида в терапевтических белках связаны, в числе других факторов, с клиренсом in vivo. Более того, присоединение химического фрагмента к полипептидам может сказываться на снижении почечного клиренса полипептида.
Имеются сообщения о неактивных формах фактора VII. Инактивированная форма способна вступать в конкуренцию с фактором VII или фактором VIIа дикого типа по связыванию с тканевым фактором и ингибировать свертывающую активность. Предполагается, что инактивированная форма фактора VIIа будет использоваться для лечения пациентов в состояниях, характеризующихся гиперкоагуляцией, таких как пациенты с сепсисом, пациенты, имеющие риск развития инфаркта миокарда или тромботического кровоизлияния.
В патенте WO 98/32466 высказывается предположение о том, что фактор VII в числе многих других белков может подвергаться модификации с присоединением ПЭГ-группировки, то есть ПЭГилированию, но никакой другой информации по данному аспекту в указанном патенте не содержалось.
В патенте WO 01/58935 заявляются конъюгаты неполипептидных фрагментов (например, ПЭГ) с полипептидом, аминокислотная последовательность которого отличается от последовательности фактора VII дикого типа за счет того, что в нее вводится или из нее удаляется по меньшей мере один аминокислотный остаток, включающий присоединяемую группу для неполипептидного фрагмента.
В патенте США 4847325 высказывается предположение о том, что колониестимулирующий фактор-1 (КСФ-1) может быть присоединен к ПЭГ посредством реакции производных ПЭГ с окисленным КСФ-1.
Таким образом, имеется потребность в создании композиций и разработке способов, которые обеспечили бы получение белковых препаратов для свертывания крови, в частности препаратов, содержащих улучшенный рекомбинантный человеческий фактор VII, модифицированный фактор VII или фактор VII-родственный полипептид.
Краткое описание сущности изобретения
Авторы настоящего изобретения показали, что препараты полипептида фактора VII, обладающие характеристиками гликоформы и содержащие по меньшей мере одну олигосахаридную группу, ковалентно присоединенную по меньшей мере к одной полимерной группе, проявляют улучшенные функциональные свойства. Соответственно, настоящее изобретение относится к способам и композициям, которые обеспечивают получение таких конъюгатных белковых препаратов.
Соответственно, настоящее изобретение относится, в первом аспекте, к препарату, включающему множество полипептидов фактора VII или фактор VII-родственных полипептидов, где указанные полипептиды включают аспарагин-связанные и/или серин-связанные олигосахаридные цепи и где по меньшей мере одна олигосахаридная группа ковалентно присоединена по меньшей мере к одной полимерной группе.
В одном варианте осуществления настоящего изобретения полимерная группа ковалентно присоединяется к фрагменту сиаловой кислоты. В другом варианте осуществления настоящего изобретения полимерная группа ковалентно присоединяется к фрагменту галактозы.
В одном варианте осуществления изобретения примерно 94-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты.
В одном варианте осуществления изобретения примерно 94-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты, где менее чем примерно 25% олигосахаридных цепей включают по меньшей мере одну не кэппированную антенну.
В одном варианте осуществления настоящего изобретения меньше, чем примерно 10%, олигосахаридных цепей включают по меньшей мере одну не кэппированную антенну.
В одном варианте осуществления настоящего изобретения меньше, чем примерно 5%, предпочтительно меньше, чем примерно 2%, олигосахаридных цепей содержат по меньшей мере одну не кэппированную антенну.
В одном варианте осуществления изобретения примерно 96-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты.
В одном варианте осуществления настоящего изобретения примерно 98-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты.
В одном варианте осуществления настоящего изобретения аспарагинсвязанные олигосахаридные цепи расположены в положениях, соответствующих аминокислотным остаткам Asn-145 и Asn-322 человеческого фактора VIIа дикого типа (см. в конце описания).
В одном варианте осуществления настоящего изобретения серинсвязанные олигосахаридные цепи расположены в положениях, соответствующих аминокислотным остаткам Ser-52 и Ser-60 человеческого фактора VIIа дикого типа (фиг. 1).
В одном варианте осуществления настоящего изобретения указанные полимеры выбирают из группы, состоящей из полиалкиленоксидов (ПАО), включающих полиалкиленгликоль (ПАГ), такой как полиэтиленгликоль (ПЭГ) и полипропиленгликоль (ППГ), разветвленные ПЭГи, поливиниловый спирт (ПВС), поликарбоксилат, поливинилпирролидон, ангидрид сополимера полиэтилена и малеиновой кислоты, ангидрид сополимера полистирола и малеиновой кислоты и декстран, включающий карбоксиметилдекстран, полиуретан, полиэфир и полиамид.
В одном варианте осуществления настоящего изобретения указанный полимер представляет собой полиэтиленгликоль (ПЭГ), в одном варианте осуществления настоящего изобретения полиэтиленгликоль представляет собой ПЭГ с молекулярной массой 300-100000 Да, такой как примерно 500-20000 Да или примерно 500-15000 Да, или 2-15 кДа, или 3-15 кДа, или 3-12 кДа, или примерно 10 кДа.
В одном варианте осуществления настоящего изобретения полипептид имеет аминокислотную последовательность фактора VII дикого типа (фиг.1). В одном варианте осуществления настоящего изобретения полипептиды представляют собой фактор VIIа дикого типа.
В одном варианте осуществления настоящего изобретения полипептиды фактора VII выбирают из группы, состоящей из S52-фактора VII, S60-фактора VII, фактора VII, который был протеолитически расщеплен на участке между остатками 290 и 291; фактора VII, который был протеолитически расщеплен на участке между остатками 315 и 316; фактора VII, который был окислен, L305V-FVII, L305V/M306D/D309S-FVII, L305I-FVII, L305T-FVII, F347P-FVII, V158T/M298Q-FVII, V158D/E296V/M298Q-FVII, K337A-FVII, M298Q-FVII, V158D/M298Q-FVII, L305V/K337A-FVII, V158D/E296V/M298Q/L305V-FVII, V158D/E296V/M298Q/K337A-FVII, V158D/E296V/M298Q/L305V/K337A-FVII, K157A-FVII, E296V-FVII, E296V/M298Q-FVII, V158D/E296V-FVII, V158D/M298K-FVII, S336G-FVII; вариантных последовательностей фактора VII, где аминокислотный остаток в положениях 290 и/или 291, предпочтительно 290, замещен, и вариантных последовательностей фактора VII, где аминокислотный остаток в положениях 315 и/или 316, предпочтительно 315, замещен. В другом варианте осуществления настоящего изобретения полипептиды фактора VII выбирают из группы, состоящей из вариантов фактора VII, обладающих повышенной биологической активностью в сравнении с фактором VIIа дикого типа, описанных в документах WO 01/83725, WO 02/22776, WO 02/77218, WO 03/27147 и WO 03/37932: 


полипептидов фактора FVII, включающих замещения, добавления или делеции в аминокислотной последовательности фактора VII на участке от 233Thr до 240Asn, фактора VII, включающего замещения, добавления или делеции в аминокислотной последовательности на участке от 304Arg до 329Cys, и фактора VII, включающего замещения, делеции или добавления в аминокислотной последовательности на участке от Ile153 до Arg223.
В одном варианте осуществления изобретения фактор VII-родственные полипептиды выбирают из группы, состоящей из: R152E-фактора VII, S344A-фактора VII, FFR-фактора VII и фактора VII, не содержащего Gla-домена.
В одном варианте осуществления настоящего изобретения фактор VII-родственные полипептиды демонстрируют активность по меньшей мере примерно на уровне 25%, предпочтительно по меньшей мере примерно на уровне 50%, более предпочтительно по меньшей мере примерно на уровне 75% и, наиболее предпочтительно по меньшей мере примерно на уровне 90% от удельной активности фактора VIIа дикого типа, который получают в том же типе клеток, при анализе в рамках одного или более тестов: тесте на свертывание, тесте на протеолиз или тесте на связывание с TФ, как описано в настоящем описании.
В одном варианте осуществления настоящего изобретения фактор VII-родственные полипептиды демонстрируют активность менее чем примерно на уровне 25%, предпочтительно менее чем примерно на уровне 10%, более предпочтительно менее чем примерно на уровне 5%, и наиболее предпочтительно менее чем примерно на уровне 1%, от удельной активности фактора VIIа дикого типа, который получают в том же типе клеток, при анализе в рамках одного или более тестов: тесте на свертывание, тесте на протеолиз или тесте на связывание с TФ, как описано в настоящем описании.
В различных вариантах осуществления настоящего изобретения конъюгированный полипептид демонстрирует биологическую доступность, которая составляет по меньшей мере примерно 110% от биологической доступности эталонного препарата, например, по меньшей мере примерно 120% или по меньшей мере примерно 130%, или по меньшей мере примерно 140% от биологической доступности эталонного препарата.
В одном варианте осуществления настоящего изобретения конъюгированный полипептид демонстрирует период полувыведения сыворотки, который составляет по меньшей мере примерно 125% от периода полувыведения эталонного препарата, в частности по меньшей мере примерно 150% или по меньшей мере 200%, или по меньшей мере примерно 250% от периода полувыведения эталонного препарата.
В одном варианте осуществления настоящего изобретения конъюгированный полипептид получают путем ферментативной модификации фрагментов сиаловой кислоты или галактозы в полипептиде.
В еще одном аспекте настоящее изобретение относится к способу получения препарата по пункту 1, где указанный способ включает стадию приведения в контакт олигосахаридсодержащего полипептида с полимерной молекулой в условиях, при которых по меньшей мере одна полимерная молекула ковалентно присоединяется по меньшей мере к одной из ологисахаридных цепей полипептидов.
В еще одном аспекте настоящее изобретение относится к фармацевтической композиции, включающей препарат, определенный в любом из пунктов 1-22, и фармацевтически приемлемый носитель или адъювант.
В еще одном аспекте настоящее изобретение относится к применению препарата, включающего множество полипептидов фактора VII или фактор VII-родственных полипептидов, где указанные полипептиды включают аспарагинсвязанные и/или серинсвязанные олигосахаридные цепи и где по меньшей мере одна олигосахаридная группа ковалентно присоединяется по меньшей мере к одной полимерной группе, при получении лекарственного средства, предназначенного для лечения фактор VII-реактивного синдрома.
В еще одном аспекте настоящее изобретение относится к способу лечения фактор VII-реактивного синдрома, где указанный способ включает введение фармацевтической композиции, содержащей препарат, описанный в пунктах 1-22, пациенту, при потребности в таком лечении, в условиях, которые приводят к снижению кровотечению и/или к повышению уровня свертывания крови.
В одном варианте осуществления настоящего изобретения указанный синдром выбирают из группы, состоящей из гемофилии А, гемофилии В, недостаточности фактора XI, недостаточности фактора VII, тромбоцитопении, болезни Виллебранда, состояния, связанного с наличием ингибитора фактора свертывания, после хирургического вмешательства, после травмы, после антикоагуляционной терапии, включающей дилюционную коагулопатию, а также внутричерепного кровотечения, трансплантации стволовых клеток, кровотечения в верхней части желудочно-кишечного тракта и болезни печени.
В еще одном аспекте настоящее изобретение относится к способу предотвращения нежелательного кровотечения, где указанный способ включает введение фармацевтической композиции, содержащей препарат, описанный в пунктах 1-22, пациенту, при потребности в таком лечении, в условиях, которые приводят к снижению уровня кровотечения и/или к повышению уровня свертывания крови.
В еще одном аспекте настоящее изобретение относится к способу предотвращения нежелательного свертывания крови, где указанный способ включает введение фармацевтической композиции, содержащей препарат, описанный в пунктах 1-22, пациенту, при потребности в таком лечении, в условиях, эффективных для подавления свертывания.
В одном варианте осуществления настоящего изобретения нежелательное свертывание крови связано с состоянием, выбранным из группы, состоящей из ангиопластики, тромбоза глубоких вен, легочной эмболии, кровоизлияния, синдрома диссеминированного внутрисосудистого свертывания крови (ДВС-синдрома), отложения фибрина в легких и почках, связанного с эндотоксемией, вызванной грамотрицательными бактериями, и инфаркта миокарда.
В одном аспекте настоящее изобретение относится к способу предотвращения реакций, опосредованных тканевым фактором, где указанный способ включает введение фармацевтической композиции, содержащей препарат, описанный в пунктах 1-22, пациенту, при потребности в таком лечении, в условиях, эффективных для подавления свертывания крови.
В одном варианте осуществления настоящего изобретения указанная реакция, опосредованная тканевым фактором, относится к состоянию, выбранному из группы, состоящей из воспаления, рака, роста опухоли, метастаз, ангиогенеза, ССВР(SIRS), ОПЛ (ALI), РДСВ, МНО (MOF), ГУС (HUS) и ТЦП.
Описание изобретения
Авторы настоящего изобретения обнаружили, что препараты, включающие белки коагуляции, обладают характеристиками гликоформ, в которых по меньшей мере одна олигосахаридная группа ковалентно присоединяется по меньшей мере к одной полимерной группе, такой как например ПЭГ, демонстрируя при этом улучшенные функциональные свойства. Соответственно, настоящее изобретение относится к способам и композициям, которые позволяют создать указанные препараты конъюгированного белка. В частности, настоящее изобретение относится к препаратам, включающим полипептиды фактора VII и фактор VII-родственные полипептиды, обладающие характеристиками аспарагинсвязанных (N-связанных) и серинсвязанных (О-связанных) олигосахаридов, ковалентно присоединенных по меньшей мере к одной полимерной группе. Препараты по настоящему изобретению демонстрируют измененные свойства, которые включают, без ограничения, улучшенные фармакокинетические свойства и повышенную клиническую эффективность. Настоящее изобретение также относится к фармацевтическим композициям, которые включают указанные препараты, а также к способам лечения с помощью данных композиций.
В контексте настоящего описания термин "ковалентное присоединение" указывает на то, что олигосахаридный фрагмент и полимерная молекула либо непосредственно ковалентно соединены друг с другом, либо опосредованно ковалентно соединены друг с другом через разделяющий фрагмент или фрагменты, такие как мостик, спейсер или один или более связующих фрагментов.
Термин "конъюгат" или используемый взаимозаменяемо термин "конъюгированный полипептид" обозначают гетерогенную (в смысле композитную или химерную) молекулу, образованную при ковалентном присоединении одного или более полипептидов к одной или более полимерным молекулам.
Термин "полимерная молекула" или используемый взаимозаменяемо термин "полимерная группа" или "полимерный фрагмент" или "молекула полимера" относится к молекуле, которая способна конъюгировать с присоединяющей группой в полипептиде. При использовании данного термина для описания конъюгата по настоящему изобретению следует понимать, что полимерная молекула (или фрагмент) соединяются с полипептидной частью конъюгата через присоединяющую группу олигосахаридной цепи гликопротеина, предпочтительно полимерная молекула присоединяется к фрагменту сиаловой кислоты, кэппирующему олигосахарид («кэппинг-группа сиаловой кислоты»), или к галактозному фрагменту.
Полимерная молекула представляет собой молекулу, образованную путем ковалентного связывания двух или более мономеров, где ни один из мономеров не представляет собой аминокислотный остаток. Предпочтительные полимеры представляют собой полимерные молекулы, выбранные из группы, состоящей из полиалкиленоксида (ПАО), включающего полиалкиленгликоль (ПАГ), такой как полиэтиленгликоль (ПЭГ) и полипропиленгликоль (ППГ), разветвленные ПЭГи, поливиниловый спирт (ПВС), поликарбоксилат, поливинилпирролидон, ангидрид сополимера полиэтилена и малеиновой кислоты, ангидрид сополимера полистирола и малеиновой кислоты и декстран, включающий карбоксиметилдекстран, при этом особенно предпочтительным является ПЭГ.
Термин "присоединяющая группа" в контексте настоящего описания обозначает функциональную группу олигосахаридного фрагмента, способную присоединять полимерную молекулу. Используемые полимерные группы включают, например, амин, гидроксил, карбоксил, альдегид, кетон, сульфгидрил, сукцинимидил, малеимид, винилсульфон и галогенацетат.
Присоединяющая группа на олигосахаридном фрагменте может быть активирована перед реакцией с полимером. Альтернативно, группа, присутствующая на полимере, может быть активирована перед реакцией с олигосахаридным фрагментом. Активированная группа, которая может присутствовать на олигосахаридном или полимерном фрагменте, может иметь вид активированной удаляемой группы.
Термин "активированная удаляемая группа" включает фрагменты, которые легко замещаются в реакции замещения, осуществляемой с помощью органических соединений или ферментов. Активированные удаляемые группы известны в данной области техники и описаны в литературе (см., например, Vocadlo et al., In Carbohydrate Chemistry and Biology, Vol 2, Wiley-VCH Verlag, Germany (2000); Kodama et al., Tetrahedron Letters 34: 6419 (1993); Lougheed et al., J. Biol. Chem. 274:37717 (1999)).
Методы и химическая природа активации полимеров описаны в литературе. Обычно используемые методы активации полимеров включают активацию функциональных групп цианогенбромидом, периодатом, глутаральдегидом, биэпоксидами, эпихлоргидрином, дивинилсульфоном, карбодиимидом, сульфонилгалогенидами, трихлортриазином и т.п. (см., например, Taylor (1991), Protein Immobilization, Fundamentals and Application, Marsel Dekker, N.Y.: Wong (1992), Chemistry of Protein Conjugation and Crosslinking, CRC Press, Boca Raton; Hermanson et al., (1993) Immobilized Affinity Ligand Techniques, Academic Press, N.Y.; Dunn et al., Eds. Polymeric Drugs and Drug Delivery Systems, ACS Symposium Series Vol. 469, American Chemical Society, 1991).
Реактивные группы и классы реакций, используемые в практике осуществления настоящего изобретения, в основном включают те из них, которые осуществляются в относительно мягких условиях. Указанные группы и классы включают, без ограничения, реакции нуклеофильного замещения (например, реакции аминов и спиртов с ацилгалогенидами, активными сложными эфирами), реакции электрофильного замещения (например, реакции енамина) и реакции присоединения к углерод-углеродным связям и связям углерод-гетероатом (например, реакция Михаэля, реакции присоединения Дильса-Альдера). Указанные и другие используемые в технике методы описаны в соответствующих руководствах (см., например, March, Advanced Organic Chemistry, 3rd edition, John Wiley & Sons, N.Y. 1985; Hermanson, Bioconjugate Techniques, Academic Press, San Diego, 1996; Feeney et al., Modification of Proteins, Advances in Chemistry Series, Vol 198, American Chemical Society, 1982).
Реактивные функциональные группы могут быть выбраны таким образом, что они не будут участвовать или препятствовать реакциям, необходимым для сборки олигосахаридного и полимерного фрагмента. Альтернативно, реактивная функциональная группа может быть защищена от участия в реакции за счет присутствия защитной группы. Примеры используемых защитных групп приведены, в частности, в работе Грина с соавт. (Green et al., Protective groups in Organic Synthesis, John Wiley&Sons, N.Y., 1991).
Основные подходы, осуществляемые для объединения углеводов с другими молекулами, описаны в литературе (см, например, Lee et al., Biochemistry 28: 1856 (1989); Bhatia et al., Anal. Biochem. 178: 408 (1989); Janda et al., J. Am. Chem. Soc. 112: 8886 (1990); и Bednarski et al., WO 92/18135).
Термин "природный сайт гликозилирования" в контексте настоящего описания обозначает сайты гликозилирования в положениях Asn-145 (N145), Asn-322 (N322), Ser-52 (S52), и Ser-60 (S60). Аналогично, термин "природный сайт О-гликозилирования in vivo" включает положения S52 и S60, тогда как термин "природный сайт N-гликозилирования in vivo" включает положения N145 и N322.
Термин "функциональный полупериод существования in vivo" используется в обычном значении для данного термина, то есть указывает время, в течение которого 50% биологической активности полипептида или конъюгата все еще присутствуют в организме и/или в органе-мишени, или время, в течение которого активность полипептида или конъюгата составляет 50% от его исходного значения. В качестве альтернативного варианта определения функционального полупериода существования in vivo может быть использован термин "период полувыведения из сыворотки", определяемый как время, в течение которого 50% полипептидных или конъюгатных молекул циркулируют в плазме или кровотоке перед выведением из организма. Определение периода полувыведения из сыворотки часто проще, чем определение функционального полупериода существования, и значение периода полувыведения из сыворотки обычно является хорошим показателем величины функционального полупериода существования in vivo. Альтернативные термины для характеристики периода полувыведения из сыворотки включают период полувыведения из плазмы, период полувыведения из кровотока, полупериод циркуляции в крови, клиренс из сыворотки, клиренс из плазмы и полупериод клиренса. Полипептид или конъюгат выводится из организма посредством функционирования одной или более ретикулоэндотелиальных систем (РЭС), почки, селезенки или печени, под действием тканевого фактора, рецептора SEC или путем выведения, опосредованного другими рецепторами, или путем специфического или неспецифического протеолиза. В норме величина клиренса зависит от размеров (относительно размера отсекаемых при клубочковой фильтрации соединений), заряда, природы присоединяемых углеводных цепей и от наличия клеточных рецепторов для белка. Сохраняемую функциональность обычно выбирают из прокоагулирующей, протеолитической активности, активности по связыванию с кофактором или рецептором. Функциональный полупериод существования и период полувыведения из сыворотки может быть определен способом, известным в данной области техники, который описан ниже (см. раздел "Функциональные свойства препаратов фактора VII").
Термин "повышенный" в контексте определения функционального полупериода существования in vivo или периода полувыведения из плазмы в контексте настоящего описания указывает на то, что релевантный период полувыведения полипептида или конъюгата статистически значимо повышается в сравнении с соответствующим показателем для эталонной молекулы, такой как неконъюгированный фактор VIIа (например фактор VIIа дикого типа) при определении в сравнимых условиях. Например, релевантный период полувыведения может быть повышен по меньшей мере примерно на 25%, в частности по меньшей мере примерно на 50%, в частности по меньшей мере примерно на 100%, 150%, 200%, 250% или 500%.
Термин "иммуногенность" препарата относится к способности препарата при его введении в организм человека выявлять неблагоприятный иммунный ответ, независимо от того, является ли он гуморальным, клеточным или имеет объединенную природу. В отношении полипептида фактора VIIa и фактора VIIa-родственных полипептидов неизвестно, чтобы они проявляли заметные иммунные реакции у людей. Тем не менее, в любой подгруппе людей могут встречаться индивидуумы, которые проявляют чувствительность к конкретным вводимым белкам. Иммуногенность может быть определена путем количественного измерения уровня имеющихся антител к фактору VII и/или Т-клеток, реактивных в отношении фактора VII, у чувствительных индивидуумов с использованием традиционных методик, известных в данной области техники. В некоторых вариантах осуществления настоящего изобретения описываемые в нем препараты приводят к снижению уровня иммуногенности у чувствительного индивидуума по меньшей мере примерно на 10%, предпочтительно по меньшей мере примерно на 25%, более предпочтительно по меньшей мере примерно на 40% и наиболее предпочтительно по меньшей мере примерно на 50% относительно иммуногенности, свойственной индивидууму на эталонный препарат.
Термин "аминокислотный остаток, соответствующий аминокислотным остаткам S52, S60, N145, N322 на фиг.1 (FVII масс.)" обозначает аминокислотные остатки Asn и Ser, соответствующие последовательности фактора VII дикого типа (фиг.1), при сопоставлении последовательностей. Гомогенность/идентичность аминокислотных последовательностей определяется при сопоставлении последовательности с использованием соответствующей компьютерной программы, применяемой для сопоставления последовательностей, такой как, например, программа ClustalW, версия 1.8, 1999 (Thompson et al., 1994, Nucleic Acid Research, 22: 4673-4680).
Полипептиды фактора VII и фактор VII-родственные полипептиды
Настоящее изобретение относится к полипептидам человеческого фактора VII, таким как, например, полипептиды, имеющие аминокислотную последовательность, описанную в патенте США No. 4784905 (фактор VII дикого типа). В контексте настоящего описания термины "фактор VII" и "полипептид фактора VII" обозначают фактор VII дикого типа, а также варианты фактора VII, обладающие по существу той же или улучшенной биологической активностью, что и фактор VII дикого типа. Термин "фактор VII" в контексте настоящего описания обозначает полипептиды фактора VII в их нерасщепленной форме (в форме зимогена), а также такие формы, которые после протеолитической обработки образуют соответствующие биологически активные формы и которые могут быть обозначены как фактор VIIа. В типичном случае фактор VII расщепляется на участке между остатками 152 и 153 с образованием фактора VIIа.
В контексте настоящего описания термин "фактор VII-родственные полипептиды" относится к полипептидам, включая их варианты, для которых биологическая активность указанного фактора VIIа по существу модифицирована или снижена относительно активности фактора VII дикого типа. Указанные полипептиды включают, без ограничения, фактор VII или фактор VIIа, которые были химически модифицированы, и варианты фактора VII, в которые введены специфические изменения аминокислотной последовательности, модифицирующие или нарушающие биологическую активность полипептида.
Биологическая активность фактора VIIа в процессе свертывания крови вытекает из его способности (i) связываться с тканевым фактором (ТФ) и (ii) катализировать протеолитическое расщепление фактора IX или фактора Х с образованием активированных форм фактора IX или фактора Х (фактора IХа или фактора Ха, соответственно). Для целей настоящего изобретения биологическая активность фактора VIIа может быть количественно определена путем измерения способности данного препарата ускорять свертывание крови с использованием плазмы, дефицитной по фактору VII и тромбопластину, как описано, например, в патенте США No. 5997864. В данном тесте биологическая активность выражается в виде снижения времени свертывания крови относительно контрольного образца и указанную величину преобразуют в "единицы фактора VII" при сравнении с объединенной стандартной сывороткой человека, содержащей активность фактора VII, равную 1 Ед/мл. Альтернативно, биологическая активность фактора VII может быть количественно определена (i) путем измерения способности фактора VIIа образовывать фактор Ха в системе, включающей ТФ, погруженный в липидную мембрану, и фактор Х (Persson et al., J. Biol. Chem. 272:19919-19924, 1997); (ii) путем измерения уровня гидролиза фактора Х в водной системе (см. приведенный ниже пример 5); (iii) путем измерения уровня физического связывания ТФ с использованием инструмента, основанного на поверхностном резонансе плазмона (Persson, FEBS Letts. 413:359-363, 1997) (iv) путем измерения уровня гидролиза синтетических субстратов (см. приведенный ниже пример 4); и (v) путем измерения уровня образования тромбина в ТФ-независимой системе in vitro.
Варианты фактора VII, обладающие по существу той же или улучшенной биологической активностью в сравнении с фактором VII дикого типа, включают те из них, которые демонстрируют активность по меньшей мере примерно на уровне 25%, предпочтительно, по меньшей мере примерно на уровне 50%, более предпочтительно, по меньшей мере примерно на уровне 75% и, наиболее предпочтительно, по меньшей мере примерно на уровне 90% от удельной активности фактора VIIа дикого типа, который продуцируется в клетках того же типа, при тестировании в одном или более тестах: тесте на свертывание крови, тесте на протеолиз или тесте на связывание с ТФ, как описано выше. Варианты фактора VII, обладающие по существу сниженной биологической активностью относительно фактора VIIа дикого типа, включают те из них, которые демонстрируют активность, составляющую менее чем примерно 25%, предпочтительно менее чем примерно 10%, более предпочтительно менее чем примерно 5% и наиболее предпочтительно менее чем примерно 1% от удельной активности фактора VIIа дикого типа, который продуцируется в клетках того же типа при тестировании в одном или более тестах: тесте на свертывание крови, тесте на протеолиз или тесте на связывание с ТФ, как описано выше. Варианты фактора VII, обладающие по существу модифицированной биологической активностью относительно фактора VII дикого типа, включают, без ограничения, варианты фактора VII, которые демонстрируют ТФ-независимую протеолитическую активность фактора Х и которые связываются с ТФ, но не расщепляют фактор Х.
Варианты фактора VII, независимо от того, демонстрируют ли они по существу ту же или улучшенную биологическую активность фактора VII дикого типа или, альтернативно, демонстрируют по существу модифицированную или сниженную биологическая активность фактора VII дикого типа, включают, без ограничения, полипептиды, имеющие аминокислотную последовательность, которая отличается от последовательности фактора VII дикого типа за счет наличия вставок, делеций или замещений одной или более аминокислот.
Неограничивающие примеры фактор VII-родственных полипептидов, обладающих по существу той же или улучшенной биологической активностью, что и фактор VII дикого типа, включают S52A-FVII, S60A-FVII (Lino et al., Arch. Biochem. Biophys. 352: 182-192, 1998); L305V-FVII, L305V/M306D/D309S-FVII, L305I-FVII, L305T-FVII, F374P-FVII, V158T/M298Q-FVII, V158D/E296V/M298Q-FVII, K337A-FVII, M298Q-FVII, V158D/M298Q-FVII, L305V/K337A-FVII, V158D/E296V/M298Q/L305V-FVII, V158D/E296V/M298Q/K337A-FVII, V158D/E296V/M298Q/L305V/K337A-FVII, K157A-FVII, E296V-FVII, E296V/M298Q-FVII, V158D/E296V-FVII, V158D/M298K-FVII и S336G-FVII; варианты FVIIa, которые демонстрируют повышенную протеолитическую активность, как описано в патенте США No. 5580560; фактор VIIа, который был протеолитически расщеплен на участке между остатками 290 и 291 или между остатками 315 и 316 (Mollerup et al., Biotechnol. Bioeng. 48:501-505, 1995); окисленные формы фактора VIIа (Kornfelt et al., Arch. Biochem. Biophys. 363:43-54, 1999), варианты последовательности фактора VII, в которых аминокислотные остатки в положении 290 и/или 291 (фиг. 1), предпочтительно 290, замещены, и варианты последовательности фактора VII, в которых были замещены аминокислотные остатки в положениях 315 и/или 316 (фиг. 1), предпочтительно в положении 315.
Неограничивающие примеры фактор VII-родственных полипептидов, обладающих по существу той же или улучшенной биологической активностью, что и фактор VII дикого типа, включают: варианты фактора VII, обладающие повышенной биологической активностью в сравнении с фактором VII дикого типа, раскрытым в WO 01/83725, WO 02/22776, WO 02/77218, WO 03/27147 и WO 03/37932, включающие, без ограничения,



фактор VII, включающий замещения, добавки или делеции в аминокислотной последовательности на участке от 233Thr до 240Asn, фактор VII, включающий замещения, добавки или делеции в аминокислотной последовательности на участке от 304Arg до 329Cys, и фактор VII, включающий замещения, добавки или делеции в аминокислотной последовательности на участке от Ile153 до Arg223.
Неограничивающие примеры фактор VII-родственных полипептидов, обладающих по существу сниженной или модифицированной биологической активностью относительно фактора VII дикого типа, включают R152E-FVIIa (Wildgoose et al., Biochem. 29:3413-3420, 1990), S344A-FVIIa (Kazama et al., J.Biol. Chem. 270:66-72, 1995), FFR-FVIIa (Holst et al., Eur. J. Vasc Endovasc. Surg. 15:515-520, 1998), фактор VIIа, в котором отсутствует домен Gla (Nicolaisen et al., FEBS Letts. 317:245-249, 1993), и фактор VII, в котором Lys341 заменен на Ala. Неограничивающие примеры химически модифицированных полипептидов фактор VII и вариантов последовательностей приведены, например, в патенте США No. 5997864.
Гликозилирование
В контексте настоящего описания термины "характер гликозилирования" или "характер гликоформ", "распределение" или "спектр" относятся к представлению конкретных олигосахаридных структур в данной популяции полипептидов фактора VII или фактор VII-родственных полипептидов. Неограничивающие примеры таких характеристик включают относительную долю олигосахаридных цепей, которые (i) включают по меньшей мере один остаток сиаловой кислоты; (ii) не содержат остатков сиаловой кислоты (например, имеют нейтральный заряд); (iii) содержат по меньшей мере один терминальный остаток галактозы; (iv) содержат по меньшей мере один остаток N-ацетилгалактозамина; (v) содержат по меньшей мере одну не кэппированную антенну, то есть имеют по меньшей мере один терминальный остаток галактозы или остаток N-ацетилгалактозамина; или (vi) содержат по меньшей мере одну фукозу, соединенную связью α1->3 с антенным остатком N-ацетилглюкозамина.
В контексте настоящего описания термин "олигосахаридная цепь" относится к полной структуре олигосахарида, который ковалентно соединен с одним аминокислотным остатком. Фактор VII в норме гликозилируется по остаткам Asn 145 и Asn 322 (N-связанное гликозилирование) и Ser-52 и Ser-60 (O-связанное гликозилирование). N-связанная олигосахаридная цепь, представленная на факторе VII, которая образуется в организме человека in situ, может представлять собой би-, три- и тетра-антенную структуру, где каждая такая антенна имеет структуру Neu5Ac(α2->3 или α2->6)Gal(β1->4)GlcNAc, соединенную связью (β1->2,4 или 6) с остатком Man, который соединен связью (α1->3 или 6) с остатком Man(β1->4)GlсNAc(β1->4)GlcNAc-Asn. (Neu5Ac означает N-ацетилнейраминовую кислоту (сиаловую кислоту), Gal означает галактозу, GlcNAc означает N-ацетилглюкозамин и Man означает маннозу). Олигосахаридные цепи могут включать остатки фукозы, которые могут быть соединены связью 1->6 с GlcNAc.
O-связанная олигосахаридная цепь, имеющаяся в факторе VII, продуцируется в организме человека in situ в виде моноантенной структуры, где антенна Ser-52 может обладать структурой Xyl-Xyl-Glc-Ser или Glc-Ser, и антенна Ser-60 имеет структуру Neu5Ac(α2->3 или α2->6)Gal(β1->4)GlcNAc-Fuc-Ser или Fuc-Ser (Fuc обозначает фукозу, Glc обозначает глюкозу и Xyl обозначает ксилозу).
В том случае, когда фактор VII образуется в организме человека in situ, некоторые из N-связанных олигосахаридный цепей теряют ядерные остатки фукозы, все цепи теряют антенные остатки фукозы и обе N-связанных цепи почти полностью сиалилированы, то есть терминальный сахарный остаток в каждой антенне представляет собой N-ацетилнейраминовую кислоту, соединенную с галактозой через α2->3 или α2->6 связь.
В случае образования при других обстоятельствах фактор VII может содержать олигосахаридные цепи, обладающие различными терминальными структурами на одной или более антеннах, такими как наличие остатков без сиаловой кислоты, остатков, содержащих N-гликолилнейраминовую кислоту (Neu5Gc), остатков, содержащих терминальный остаток N-ацетилгалактозамина (GalNAc) вместо галактозы и т.п. В случае образования, например, в клетках BHK в присутствии сыворотки теленка препараты фактора VII демонстрируют следующие характеристики в структуре олигосахаридов: 87-93% олигосахаридных цепей содержат по меньшей один остаток сиаловой кислоты, 7-13% являются нейтральными (то есть не содержат сиаловой кислоты), 9-16% содержат по меньшей мере один терминальный остаток галактозы, 19-29% содержат по меньшей мере один терминальный остаток N-ацетилгалактозамина и 30-39% содержат по меньшей мере одну не кэппированную антенну, то есть содержат по меньшей мере один терминальный остаток галактозы или N-ацетилгалактозамина.
В случае образования в других типах клеток или в других условиях культивирования (в бессывороточной, полностью химической среде) препарат фактора VII может характеризоваться следующими свойствами структуры олигосахаридов (описаны в WO 02/29025):
(i) примерно 94-100% олигосахаридных цепей содержат по меньшей мере один остаток сиаловой кислоты, в частности примерно 94-99%, примерно 95-98% или примерно 96-97%. В других вариантах по меньшей мере 94%, 95%, 96%, или 97% олигосахаридных цепей содержат по меньшей мере один остаток сиаловой кислоты.
(ii) 6% или менее олигосахаридных цепей являются нейтральными, составляя, в частности, такое количество, как примерно от 1,5 до 6% или от 2 до 4%.
(iii) менее чем примерно 16%, предпочтительно менее чем примерно 10% олигосахаридных цепей содержат по меньшей мере один терминальный остаток галактозы, то есть примерно от 6 до 10% или примерно от 8 до 9%.
(iv) менее чем примерно 25%, предпочтительно менее чем примерно 10% олигосахаридных цепей содержат по меньшей мере один терминальный остаток GalNAc, то есть примерно от 6 до 9% или примерно от 7 до 8%.
(v) менее чем примерно 30%, предпочтительно менее чем примерно 25% олигосахаридных цепей содержат по меньшей мере одну не кэппированную антенну, то есть примерно от 11 до 23% или примерно от 12 до 18%; и
(vi) менее чем примерно 2%, предпочтительно менее чем примерно 5%, более предпочтительно по меньшей мере примерно 10% или 20% и наиболее предпочтительно по меньшей мере примерно 40% олигосахаридных цепей содержат по меньшей мере одну фукозу, соединенную связью α1->3 c остатком N-ацетилглюкозамина в антенне (то есть содержит остаток N-ацетилглюкозамина, который соединен связью β1->2,4 или 6 c остатком маннозы).
Кроме того, степень сиалилирования (то есть количество остатков сиаловой кислоты, присоединяемых к олигосахаридной цепи) может быть повышена за счет проведения энзиматической обработки препарата экспрессированного фактора VII или фактор VII-родственного полипептида in vitro сиалилилтрансферазой в присутствии молекулы - донора сиаловой кислоты, например, как описано в патенте США No. 6399336. В рамках этого способа по существу все антенны на полисахаридных цепях сиалилируются (то есть происходит кэппирование остатками сиаловой кислоты). В некоторых случаях N-глюканы в факторе VII или фактор VII-родственном полипептиде также не полностью галактозилированы, и стадия галактозилирования, включающая галактозилтрансферазу и субстрат - донор УДФ-галактозы, осуществляемая перед стадией сиалилирования, будет способствовать повышению уровня сиаловой кислоты в продукте.
Авторы настоящего изобретения получили препараты фактора VII, содержащие олигосахаридные структуры, включающие по меньшей мере одну полимерную группу, ковалентно присоединенную по меньшей мере к одной олигосахаридной группе. В одном варианте осуществления настоящего изобретения указанные препараты включают полипептиды фактора VII или фактор VII-родственные полипептиды, демонстрирующие по меньшей мере одну из указанных ниже характеристик гликоформ:
(i) примерно от 94 до 100% олигосахаридных цепей содержат по меньшей мере один остаток сиаловой кислоты, в частности примерно 94-99%, примерно 95-98% или примерно 96-97%. В разных вариантах осуществления изобретения по меньшей мере примерно 94%, 95%, 96%, 97%, 98% или 99% олигосахаридных цепей содержат по меньшей мере один остаток сиаловой кислоты;
(ii) 6% или менее олигосахаридных цепей являются нейтральными, в частности примерно от 0,5 до 6% или от 1,5 до 6% или примерно от 2 до 4% или от 0,5 до 4% или примерно от 0,5 до 2%;
(iii) менее чем примерно 16%, предпочтительно менее чем примерно 10% олигосахаридных цепей содержат по меньшей мере один терминальный остаток галактозы, в частности примерно от 6 до 10% или примерно от 8 до 9%;
(iv) менее чем примерно 25%, предпочтительно менее чем примерно 10% олигосахаридных цепей содержат по меньшей мере один терминальный остаток GalNAc, в частности примерно от 6 до 9% или примерно от 7 до 8%.
(v) менее чем примерно 30%, предпочтительно менее чем примерно 25% олигосахаридных цепей содержат по меньшей мере одну не кэппированную антенну, в частности примерно от 11 до 23% или примерно от 12 до 18%; и
(vi) менее чем примерно 2%, предпочтительно менее чем примерно 5%, более предпочтительно по меньшей мере примерно 10% или 20% и наиболее предпочтительно по меньшей мере примерно 40% олигосахаридных цепей содержат по меньшей мере одну фукозу, соединенную связью α1->3 с остатком N-ацетилглюкозамина в антенне (то есть содержит остаток N-ацетилглюкозамина, который соединен связью β1->2,4 или 6 с остатком маннозы).
Следует понимать, что каждый из вариантов (i)-(vi) представляет собой структуру гликоформы определенного характера, которая охватывается настоящим изобретением, то есть структуру гликоформы препарата по настоящему изобретению, в которой по меньшей мере одна полимерная группа ковалентно присоединена по меньшей мере к одному олигосахариду, представляя при этом одну из структур, описанную в приведенных выше пунктах (i)-(vi). Альтернативно, структура гликоформы препарата по настоящему изобретению может быть описана более чем одной структурой из числа приведенных в пунктах (i)-(vi).
Кроме того, препарат по настоящему изобретению может быть описан одной или несколькими структурами (i)-(vi) в сочетании с одной или более другими структурными особенностями. Так, например, настоящее изобретение относится к препаратам, включающим полипептиды фактора VII и фактор VII-родственные полипептиды, в которых остатки сиаловой кислоты (Neu5Ac или Neu5Gc) соединены с галактозой исключительно в конфигурации α2->3. Настоящее изобретение также относится к препаратам, включающим полипептиды фактора VII или фактор VII-родственные полипептиды, которые содержат остаток фукозы, соединенный связью α1->6 с N-ацетилгалактозаминовым и/или фукозным ядром, который присоединен посредством связи α1->3 к N-ацетилглюкозамину антенны. В одной серии вариантов осуществления настоящего изобретения описываемые в нем препараты включают фактор VII или фактор VII-родственные полипептиды, в которых более чем 99% олигосахаридных цепей содержат по меньшей мере один остаток сиаловой кислоты и (а) остатки сиаловой кислоты соединены исключительно в конфигурации α2->3 и/или (b) имеются остатки фукозы, соединенные с N-ацетилглюкозаминами ядра и/или (с) выявляемое количество антенн несет на концах N-ацетилгалактозамин. В одном варианте осуществления настоящего изобретения описываются препараты, включающие фактор VIIа дикого типа, в котором более 99% олигосахаридных цепей содержит по меньшей мере один остаток сиаловой кислоты, и указанные остатки сиаловой кислоты соединены с галактозой исключительно в конфигурации α2->3. В другом варианте осуществления настоящего изобретения описываются препараты, включающие фактор VIIа дикого типа, в котором более 99% олигосахаридных цепей содержит по меньшей мере один остаток сиаловой кислоты, и по меньшей мере некоторые из олигосахаридных цепей содержат N-ацетилгалактозамин.
Структура N-связанных и/или О-связанных олигосахаридов может быть определена с использованием любого известного в технике метода, включающего, без ограничения, высокоэффективную жидкостную хроматографию (ВЭЖХ), капиллярный электрофорез (КЭ), ядерный магнитный резонанс (ЯМР), масс-спектрометрию (МС) с использованием методик ионизации, таких как бомбардировка быстрыми атомами, электронапыление или лазерная десорбция с использованием матрицы (МАLDI), газовую хроматографию (ГХ) и обработку экзогликозидазами в сочетании с анионообменной (АИО)-ВЭЖХ, вытеснительную хроматографию (ВХ), масс-спектроскопию (МС), гель-электрофорез (ДСН-ПААГ, КЭ-ПААГ), изоэлектрофокусирование с использованием гелей и изоэлектрофокусирование с использованием капиллярного электрофореза (КЭ-ИФ). См., например, Weber et. al., Anal. Biochem. 225:135 (1995): Klausen et. al., J. Chromatog. 718: 195 (1995); Morris et. al., в Mass Spectrometry of Biological Materials, McEwen et. al., eds., Marcel Dekker, (1990), pp 137-167; Conboy et. al., Biol. Mass Spectrom. 21: 397, 1992; Hellerqvist, Meth. Enzymol. 193: 554 (1990); Sutton et. al., Anal. Biochem. 318: 34 (1994); Harvey et. al., Organic Mass Spectrometry 29: 752 (1994).
После разрешения олигосахаридных цепей из фактора VII с использованием любого из указанных способов (или любого другого способа, который позволяет разрешить олигосахаридные цепи с разными структурами) полученные при указанном разрешении виды относят к одной из групп (i)-(vi). Относительное содержание каждой из структур (i)-(vi) вычисляется в виде суммы олигосахаридов, относящихся к данной группе, относительно общего содержания олигосахаридных цепей в образце.
Так, например, с использованием АИО ВЭЖХ 13 или более N-связанных олигосахаридных пиков могут быть разрешены из рекомбинантного препарата фактора VII, полученного в клетках ВHK (см, например, Klausen et. al., Mol. Biotechnol. 9:195, 1998). Пять пиков (обозначенных как 1-5 в работе Клаусена) не содержат сиаловую кислоту, тогда как восемь пиков (обозначенных 6, 7 и 10-15) содержат сиаловую кислоту.
Следует понимать, что в этом анализе число и распределение цепей, содержащих сиаловую кислоту и не содержащих сиаловую кислоту, может зависеть от (а) природы экспрессируемого полипептида; (b) типа клеток и условий культивирования; (с) имеющихся в структуре гликоформы модификаций, создаваемых путем химической и/или ферментативной обработки после экспрессии, и (d) используемого способа анализа, и что получаемая структура подлежит соответствующему варьированию.
В любом случае, после разрешения олигосахаридов, содержащих сиаловую кислоту, из олигосахаридов, которые не содержали сиаловой кислоты, может использоваться традиционная программа анализа данных, включающая вычисление площади под каждым пиком, общей площади пика и процентного содержания каждого конкретного пика от общей площади пика. В рамках этого способа для случая каждого конкретного препарата сумма площадей содержащих сиаловую кислоту пиков/общая площадь пиков х 100% дает процентное значение уровня сиалилирования в препарате по настоящему изобретению (то есть пропорцию олигосахаридных цепей, содержащих по меньшей мере один остаток сиаловой кислоты). Аналогичным образом может быть вычислен процент цепей, не содержащих остатки сиаловой кислоты или содержащих по меньшей мере один остаток галактозы и один остаток N-ацетилглюкозамина.
Полимеры
Полимерная молекула, которая подлежит связыванию с полипептидом, может представлять собой любую подходящую молекулу, такую как природный или синтетический гомополимер или гетерополимер, который в типичном случае имеет молекулярную массу в диапазоне примерно 300-100000 Да, такую как примерно 500-20000 Да или примерно 500-15000 Да, или 2-15 кДа, или 3-15 кДа, или примерно 10 кДа. В случае использования термина "примерно" в контексте определенного молекулярного веса по настоящему описанию он указывает приблизительное распределение средней молекулярной массы в данном препарате полимера.
Примеры гомополимеров включают полиспирты (то есть поли-ОН), полиамины (то есть поли-NH2) и поликарбоновые кислоты (то есть поли-COOH). Гетерополимер представляет собой полимер, включающий различные связывающие группы, такие как гидроксильная группа и аминогруппа.
Примеры подходящих полимерных молекул включают полимерные молекулы, выбранные из группы, состоящей из полиалкиленоксида (ПАО), включающего полиалкиленгликоль (ПАГ), такой как полиэтиленгликоль (ПЭГ) и полипропиленгликоль (ППГ), разветвленные ПЭГи, поливиниловый спирт (ПВС), поликарбоксилат, поливинилпирролидон, ангидрид сополимера полиэтилена и малеиновой кислоты, ангидрид сополимера полистирола и малеиновой кислоты, декстран, включающий карбоксиметилдекстран, полиуретан, полиэфир и полиамид, или любой другой полимер, пригодный для снижения иммуногенности и/или повышения полупериода функциональной активности in vivo и/или периода полувыведения из сыворотки. В основном, полимеры на основе полиалкиленгликоля являются биосовместимыми, нетоксичными, неантигенными и неиммуногенными молекулами, обладающими разными свойствами водорастворимости, которые легко выводятся из живых организмов.
ПЭГ является предпочтительной полимерной молекулой, поскольку она содержит лишь небольшое число реакционных групп, способных к поперечному сшиванию, в сравнении, например, с полисахаридами, такими как декстран. В частности, представляет особый интерес монофункциональный ПЭГ, например метоксиполиэтиленгликоль (мПЭГ), поскольку его химическое связывание является относительно простым (только одна реакционная группа способна конъюгировать с присоединяющими группами на олигосахариде). Соответственно, устраняется риск поперечного сшивания и полученные полипептидные конъюгаты становятся более гомогенными, а реакцию полимерных молекул с полипептидом легче контролировать.
Для облегчения ковалентного присоединения одной или более полимерных молекул к пептиду концевые гидроксильные группы и полимерные молекулы должны находиться в активированной форме, то есть должны содержать реактивные функциональные группы, примеры которых включают первичные аминогруппы, гидразид (ГЗ), тиол, сукцинат (СУК), сукцинимидилсукцинат (СС), сукцинимидилсукцинамид (ССА), сукцинимидилпропионат (СПА), сукцинимидилкарбоксиметилат (СКМ), бензотриазолкарбонат (БТК), N-гидроксисукцинимид (N-ГС), альдегид, нитрофенилкарбонат (НФК) и трезилат (ТРЕС). Подходящие активированные полимерные молекулы коммерчески доступны, например, от компании Schearwater Polymers (Inc., Huntsville, AL, СШA) или от компании PolyMASC Pharmaceuticals plc (Великобритания). Альтернативно, полимерные молекулы могут быть активированы обычными способами, известными в данной области техники, например описанными в патенте WO 90/13540. Конкретные примеры активированных линейных или разветвленных полимерных молекул, используемых в настоящем изобретении, описаны в каталогах компании Schearwater Polymers, Inc., 1997 года и 2000 года (Functionalized Biocompatible Polymers for Research and Pharmaceuticals, Polyethylene Glycol and Derivatives), включенных в настоящее описание в качестве ссылки.
Конкретные примеры активированных ПЭГ полимеров включают следующие линейные ПЭГи: N-ГС-ПЭГ (например СПА-ПЭГ, ССПА-ПЭГ, СБА-ПЭГ, СС-ПЭГ, ССА-ПЭГ, СК-ПЭГ, СГ-ПЭГ и СКМ-ПЭГ) и NOR-ПЭГ, БТК-ПЭГ, ЭПОКС-ПЭГ, NСО-ПЭГ, NФК-ПЭГ, КДИ-ПЭГ, АЛД-ПЭГ, ТРЕС-ПЭГ, ВС-ПЭГ, ИОД-ПЭГ и МАЛ-ПЭГ, а также разветвленные ПЭГи, такие как ПЭГ2-N-ГС, и виды ПЭГов, описанные в документах US 5932462 и US 5643575, которые оба включены в настоящее описание в качестве ссылки. Кроме того, в приведенных в качестве ссылки публикациях описаны полезные полимерные молекулы и/или химические механизмы ПЭГилирования: US 5824778, US 5476653, WO 97/32607, EP 229108, EP 402378, US 4902502, US 281698, US 5122614, US 5219564, WO 92/16555, WO 94/04193, WO 94/14758, WO 94/17039, WO 94/18247, WO 94/28024, WO 95/00162; WO 95/11924, WO 95/13090, WO 95/33490, WO 96/00080, WO 97/18832, WO 98/41562, WO 98/48837, WO 99/32134, WO 99/32139, WO 99/32140, WO 96/40791, WO 98/32466, WO 95/06058, EP 439 508, WO 97/03106, WO 96/21469, WO 95/13312, EP 921131, US 5736625, WO 98/05363, EP 809996, US 5629384, WO 96/41813, WO 96/07670, US 5473034, US 5516673, EP 605963, US 305382657, EP 510356, EP 400472, EP 183503 и EP 154316.
Конъюгирование олигосахаридных цепей полипептидов и активированных полимерных молекул осуществляется при использовании любого традиционного способа. Обычные способы известны специалистам в данной области.
Специалист в данной области понимает, что способ активирования и/или химический механизм конъюгирования, используемые в данном случае, зависят от природы присоединяющих групп в олигосахариде(ах), а также от природы функциональных групп в полимерной молекуле (которая может представлять собой амин, гидроксил, карбоксил, альдегид, кетон, сульфгидрил, сукцинимидил, малеимид, винилсульфон или галогенацетат).
Следует понимать, что конъюгирование полимеров направлено на получение оптимальной структуры молекулы с точки зрения числа присоединенных полимерных молекул, размера и формы таких молекул (то есть для достижения линейной или разветвленной структуры) и сайта(ов) прикрепления в одной или более олигосахаридных цепей. Молекулярная масса используемого полимера может быть выбрана, исходя из желательного эффекта. В частности, если основной целью конъюгации является получение конъюгата с высокой молекулярной массой (например, для снижения почечного клиренса), обычно бывает желательно проводить конъюгирование настолько малого числа молекул высокомолекулярного полимера, насколько это возможно для достижения желательной молекулярной массы.
В соответствии с настоящим изобретением, также предусматривается вариант сопряжения молекул полимера с полипептидом через линкер. Подходящие линкеры известны специалистам в данной области. Предпочтительным примером линкера является хлорид циануровой кислоты (Abuchowski et al., (1997), J. Biol. Chem., 252, 3578-3581; US 4179337; Shafer et al., (1996), J. Polym. Sci. Polym. Chem. Ed., 24, 375-378). После конъюгации оставшиеся активированные молекулы полимера блокируют с использованием способов, известных в данной области, например, путем добавления первичного амина к реакционной смеси, после чего полученные инактивированные полимерные молекулы удаляют соответствующим способом. Такие способы известны специалистам в данной области (см., например, March, Advanced Organic Chemistry, 3rd edition, John Wiley & Sons, N.Y. 1985; Greene et al., Protective Groups in Organic Synthesis, John Wiley & Sons, N.Y. 1991; Taylor (1991), Protein Immobilization, Fundamentals and Application, Marcel Dekker, N.Y.; Wong (1992), Chemistry of Protein Conjugation and Crosslinking, CRC Press, Boca Raton; Hermanson et. al., (1993), Immobilized Affinity Ligand Techniques, Academic Press, N.Y.; Dunn et al., Eds. Polymeric Drugs and Drug Delivery Systems, ACS Symposium Series Vol. 469, American Chemical Society, 1991).
Следует понимать, что в зависимости от условий, например, от аминокислотной последовательности полипептида, природы используемого активированного соединения ПЭГ и от конкретных условий ПЭГилирования, включая молярное соотношение ПЭГ к полипептиду, могут быть достигнуты разные степени ПЭГилирования, при этом больший уровень ПЭГилирования в основном получают при использовании более высокого отношения количества ПЭГ к количеству полипептида. ПЭГилированные полипептиды, получаемые в результате любого данного процесса ПЭГилирования, будут в норме включать стохастическое распределение полипептидных конъюгатов, обладающих несколько различающимися уровнями ПЭГилирования.
В соответствии с одним интересным вариантом осуществления настоящего изобретения предлагаемый в нем полипептидный конъюгат включает полимерную молекулу, ковалентно присоединенную к одной из групп сиаловой кислоты, расположенных на терминальном конце олигосахаридной группы полипептида фактора VII, где указанная полимерная молекула представляет собой лишь ту полимерную молекулу, которая присоединена к полипептиду. В другом варианте осуществления настоящего изобретения две полимерных молекулы ковалентно соединяются с одной или более олигосахаридными группами полипептида фактора VII, в еще одном варианте три, четыре, пять, шесть или семь полимерных молекул ковалентно присоединяются к полипептиду фактора VII.
В одном варианте осуществления настоящего изобретения полипептид фактора VII представляет собой полипептид фактора VII или фактора VIIа дикого типа, показанный на фиг. 1, в другом варианте полипептид фактора VII представляет собой фактор VII-родственный полипептид, в еще одном варианте фактор VII-родственный полипептид представляет собой вариант аминокислотной последовательности фактора VII.
Предпочтительно, указанные полипептидные конъюгаты представляют собой такие конъюгаты, которые включают одну молекулу ПЭГ. В частности, включают линейную или разветвленную молекулу ПЭГ с молекулярной массой, составляющей примерно 5 кДА, в частности, предпочтительно молекулу с молекулярной массой примерно 10-25 кДА, такой как 15-25 кДа, в частности, примерно 20 кДа или примерно 10 кДа.
Предпочтительно, в конъюгате по настоящему изобретению количество и молекулярная масса полимерных молекул выбираются таким образом, чтобы общая молекулярная масса, добавляемая к полимерной молекуле, находилась в диапазоне 5-25 кДа, например, в диапазоне 10-25 кДа, и составляла, в частности, примерно 5 кДа, примерно 10 кДа, примерно 15 кДа или примерно 20 кДа.
Способы получения препарата фактора VII с присоединенным полимером, характеризующегося заданной структурой олигосахаридов
Способы получения препарата фактора VII. Фактор VII, варианты фактора VII или фактор VII-родственные полипептиды могут быть получены с использованием соответствующих хозяйских клеток, которые экспрессируют гликозилированные полипептиды фактора VII или фактор VII-родственные полипептиды (например хозяйские клетки, способные присоединять олигосахаридные группы в сайтах гликозилирования полипептидов). Фактор VII может быть также выделен из плазмы людей или представителей других видов животных.
В некоторых вариантах осуществления настоящего изобретения хозяйские клетки представляют собой клетки человека, экспрессирующие эндогенный ген фактора VII. В указанных клетках эндогенный ген может быть интактным или может быть модифицирован in situ или последовательность за пределами гена фактора VII может быть модифицирована in situ с целью изменения картины экспрессии эндогенного гена фактора VII. Может быть использована любая клетка человека, способная экспрессировать эндогенный ген фактора VII.
В другом варианте осуществления настоящего изобретения клетки гетерологичного хозяйского организма программируют для экспрессии человеческого фактора VII на основе рекомбинантного гена. Хозяйские клетки могут представлять собой клетки позвоночных животных, насекомых или грибов. Предпочтительно, указанные клетки представляют собой клетки млекопитающих, способные осуществлять полный спектр N-связанного гликозилирования, свойственного млекопитающим; О-связанного гликозилирования и γ-карбоксилирования. См., например, патент США No. 4784950. Предпочтительные клеточные линии млекопитающих включают клеточные линии CHO (ATCC CCL 61), COS-1 (ATCC CRL 1650), клетки почки детеныша хомячка (BHK) и HEK293 (ATCC CRL 1573; Graham et al., J. Gen. Virol. 36: 59-72, 1977). Предпочтительной клеточной линией BHK является клеточная линия tk- ts13 BHK (Waechter and Baserga, Proc. Natl. Acad. Sci. USA 79: 1106-1110, 1982), которая далее обозначается как клетки BHK 570. Клеточная линия BHK 570 доступна от Американской Коллекции типовых культур (American Type Culture Collection, 12301 Parklawn Dr., Rockville, MD 20852) под номером ATCC CRL 10314. Клеточная линия tk- ts13 BHK доступна также от Американской коллекции типовых культур АТСС под номером CRL 1632. Кроме того, может использоваться множество других клеточных линий, включая линии Rat Hep I (линия клеток гепатомы крысы; ATCC CRL 1600), Rat Hep II (линия клеток гепатомы крысы; ATCC CRL 1548), TCMK (ATCC CCL 139), клеточную линию легкого человека (ATCC HB 8065), NCTC 1469 (ATCC CCL 9.1) и клетки DUKX (клеточная линия CHO) (Urlaub and Chasin, Proc. Natl. Acad. Sci. USA 77: 4216-4220, 1980), (клетки DUKX обозначают также как клетки CX11) и DG44 (клеточная линия CHO) (Cell, 33:405, 1983, и Somatic Cell and Molecular Genetics 12: 555, 1986). Могут использоваться также клетки 3Т3, клетки Namalwa, клетки миеломы и клетки, полученные при слиянии клеток миеломы с другими клетками. В особенно предпочтительном варианте осуществления настоящего изобретения хозяйские клетки представляют собой клетки BHK 21, которые адаптированы для роста в отсутствие сыворотки и запрограммированы на экспрессию фактора VII. В некоторых вариантах осуществления настоящего изобретения хозяйские клетки могут представлять собой мутантные или рекомбинантные клетки, которые экспрессируют количественно или качественно иной спектр ферментов гликозилирования (таких как, например, гликозилтрансферазы и/или гликозидазы) в сравнении с типом клеток, из которых они были получены. Клетки могут быть также запрограммированы на экспрессию других гетерологичных пептидов или белков, включая, например, усеченные формы фактора VII. В одном варианте осуществления настоящего изобретения хозяйские клетки представляют собой клетки CHO, которые запрограммированы на совместную экспрессию как интересующего полипептида фактора VII (например, полипептида фактора VII или фактор VII-родственного полипептида), так и другого гетерологичного пептида или полипептида, такого как, например, модифицированный фермент или фрагмент фактора VII.
Способы получения препарата фактора VII, включающие любые гликоформные структуры, описанные выше как структуры (i)-(vi), и способы оптимизации распределения гликоформ фактора VII и фактор VII-родственных полипептидов могут быть осуществлены с использованием следующих стадий:
(а) культивирование клетки, экспрессирующей фактор VII или фактор VII-родственные полипептиды в первом наборе заданных условий культивирования;
(b) восстановление фактора VII или фактор VII-родственных полипептидов из культуры с получением препаратов, включающих полипептиды; и
c) анализ структуры олигосахаридов, связанных с полипептидами, для установления характера полученных гликоформ.
Указанные способы могут также включать:
(d1) внесение изменений в условия культивирования на стадии (а) с целью достижения второго набора заданных условий культивирования;
(e1) повторение стадий (b)-(d1) до достижения желательного характера гликоформных структур;
(f1) осуществление контакта фактора VII или фактор VII-родственных полипептидов с полимерной молекулой в условиях, при которых полимерная молекула ковалентно присоединяется к олигосахаридной группе полипептида.
Альтернативно, указанные способы могут также включать:
(d2) химическую и/или энзиматическую обработку препарата с целью изменения структуры олигосахарида и
(e2) повторение стадий (b)-(d2) до достижения желательной структуры гликоформ.
Указанные способы могут также включать стадию тестирования препаратов, обладающих заданной структурой гликоформы, в рамках по меньшей мере одного теста на биологическую активность (включая, например, тест на свертывание крови, тест на протеолиз фактора Х или тест на связывание с ТФ) или для определения другого функционального параметра (такого как, например, фармакокинетический профиль или стабильность) и выявления наличия корреляции между конкретными характеристиками гликоформы и конкретной биологической активностью или функциональным параметром для идентификации желательного характера гликоформы.
Параметры условий культивирования, которые могут быть изменены на стадии (d1), включают, без ограничения, клетку, которая может быть получена из разных источников, такую как, например, клетка, полученная из вида, отличного от ранее использованного, или мутантная или рекомбинантная клетка, несущая изменения в одной или более гликозилтрансферазах или гликозидазах, или других компонентах механизма гликозилирования (см. Grabenhorst et al., Glycoconjugate J. 16:81, 1999; Bragonzi et al., Biochem Biophys. Acta 1474:273, 2000; Weikert, Nature Biotechnol. 17: 1116, 1999), уровень экспрессии полипептида, метаболические условия, такие как, например, концентрация глюкозы или глутамина, отсутствие или наличие сыворотки, концентрация витамина К; наличие гидролизатов белка, гормонов, следов металлов, солей, а также такие параметры процесса, как температура, уровень растворенного кислорода и величина pH.
Ферментативная обработка, которая может использоваться на стадии (d2) для модификации структуры олигосахаридов в препарате, включает, без ограничения, обработку последовательности одним или более ферментами из числа приведенных ниже: сиалидазой (нейраминидазой), галактозидазой, фукозидазой; галактозилтрансферазой, фукозилтрансферазой и/или сиалилтрансферазой, в условиях, которые позволяют достичь желательной модификации в распределении олигосахаридных цепей, имеющих определенные терминальные структуры. Гликозилтрансферазы коммерчески доступны от компании Calbiochem (La Jolla, CA), и гликозидазы коммерчески доступны от компании Glyco, Inc. (Novato, CA).
В серии вариантов осуществления настоящего изобретения хозяйские клетки, экспрессирующие фактор VII или родственные ему полипептиды, подвергают специфическим условиях культивирования, в которых они секретируют гликозилированные полипептиды фактора VII, обладающие олигосахаридными структурами с желательными характеристиками, описанными в приведенных выше пунктах (i)-(vi). Такие условия культивирования включают, без ограничения, снижение содержания или полное отсутствие сыворотки. Предпочтительно, хозяйские клетки адаптируют для роста в отсутствие сыворотки и культивируют в отсутствие сыворотки как в фазе роста, так и в ходе продуктивной фазы. Такие процедуры адаптации описаны в литературе (см, например, Scharfenberg et al., Animal Cell Technology Developments towards the 21 st Century, E.C. Beuvery et al., (Eds.), Kluwer Academic Publishers, pp.619-623, 1995 (клетки BHK и CHO); Cruz, Biotechnol. Tech. 11:117-120, 1997 (клетки насекомых); Keen, Cytotechnol. 17: 203-211, 1995 (клетки миеломы); Berg et al., Biotechniques 14:972-978, 1993 (клетки 293 почки человека)). В предпочтительном варианте осуществления настоящего изобретения ростовая среда, которую добавляют к клеткам, не содержит белка или другого компонента, который был выделен из ткани животного или из культуры клеток животного. См., например, приведенный ниже пример 1. В типичном случае, дополнительно к традиционным компонентам, среда, подходящая для получения фактора VII, содержит витамин К в концентрации от 0,1 до 50 мг/литр, который требуется для γ-карбоксилирования остатков глутамина в факторе VII.
В другой серии вариантов осуществления настоящего изобретения гликоформы получают путем энзиматической и/или химической модификации N-связанных и/или О-связанных олигосахаридов в препарате фактора VII или фактор VII-родственных полипептидов, такой как, например, модификация, достигаемая в препарате под действием сиалилтрансферазы или галактозилтрансферазы, как описано, например, в патенте США No. 6399336. Предпочтительно, модификации подвергают N-связанные олигосахариды. Сиалилтрансфераза способна к сиалилированию высокого процента акцепторных групп (например концевой галактозы) в гликопротеине. Желательного результата обычно достигают при использовании примерно 50 мЕ сиалилтрансферазы в расчете на мг гликопротеина или менее. В типичном случае олигосахаридные цепи в гликопротеине, обладающие соответствующими гликоформными характеристиками, изменяют в соответствии с данным способом, что приводит в результате к получению большего процента сиалилированных концевых остатков галактозы, чем в неизмененном полипептиде. По существу, при использовании указанных способов может быть сиалилировано до 100% концевых остатков галактозы. Описанные способы в типичном случае позволяют достичь желательного уровня сиалилирования примерно за 48 часов или менее. Предпочтительно, для гликозилирования N-связанных углеводов в гликопротеинах используемая сиалилтрансфераза позволяет переносить сиаловую кислоту к последовательности Gal(β1-<4)GlcNAc-, которая представляет собой чаще всего встречающуюся предпоследнюю последовательность относительно терминальной сиаловой кислоты в полностью сиалилированных углеводных структурах. Примеры сиалилтрансфераз, которые используют Gal(β1->4)GlcNAc- в качестве акцепторной группы, включают ST3Gal III, ST3Gal IV или ST3Gal V (присоединяют NeuAC посредством связи α2->3) и ST6Gal I и ST6Gal II (присоединяют NeuAC посредством связи α2->6) (см. патент США 6399336). (Номенклатура сиалилтрансфераз описана в работе Тсуджи с соавт. (Tsuji et al., Glycobiology 6:v-vix (1996)).
Таким образом, смесь двух ферментов может представлять собой полезный вариант, если в готовом продукте желательны обе связи. В общих чертах, сиалилирование гликопротеина достигается с использованием, например, циклической обработки сиалилтрансферазой, которая включает синтетазу ЦМФ-сиаловой кислоты. ЦМФ-регенерирующая система в данном цикле включает цитидинмонофосфат (ЦМФ), нуклеозидтрифосфат, донор фосфата, киназу, способную переносить фосфат от донора фосфата к нуклеозиддифосфатам и нуклеозидмонофосфаткиназу, способную переносить терминальный фосфат от нуклеозидтрифосфата к ЦМФ. В регенерирующей системе также используется синтетаза ЦМФ-сиаловой кислоты, которая переносит сиаловую кислоту к ЦМФ. В цикле сиалилирования ЦМФ превращается в ЦДФ с помощью нуклеозидмонофосфаткиназы в присутствии добавленного АТФ. АТФ каталитически регенерируется из своего промежуточного продукта АДФ под действием пируваткиназы (ПК) в присутствии добавленного фосфоенолпирувата (ФЕП), ЦДФ далее превращается в ЦТФ, где указанное превращение катализируется ПК в присутствии ФЕП. ЦТФ взаимодействует с сиаловой кислотой с образованием неорганического пирофосфата (ПФн) и ЦМФ-сиаловой кислоты, где последняя реакция катализируется синтетазой ЦМФ-сиаловой кислоты. После сиалилирования галактозилглюкозида высвобожденный ЦМФ вновь поступает в систему регенерации с образованием ЦДФ, ЦТФ и ЦМФ-сиаловой кислоты. Образованный ПФн подвергается раскислению с образованием неорганического фосфата в качестве побочного продукта. Пируват также представляет собой побочный продукт. За счет наличия соли и циклического характера данной методики, в случае присутствия всех реагентов и ферментов, реакция продолжается до потребления первого из субстратов (например, свободного NeuAC и ФЕП или акцептора). Использование циклов сиалилтрансферазы описано, например, в патентах США Nо. 5374541 и 6399336.
Акцепторы для сиалилтрансферазы должны присутствовать в гликопротеине, подлежащем модификации. Подходящие акцепторы включают, например, Gal(β1->4)GlcNAc-, Gal(β1->4)GalNAc-, Gal(β1->3)GalNAc-, Gal(β1->3)GlcNAc-, Gal(β1->6)GlcNAc-, Gal(β1->4)Glc-, а также другие акцепторы, известные специалистам в данной области (см, например, Paulson et al., (1978) J. Biol. Chem. 253: 5617-5624). В типичном случае в олигосахаридные цепи включаются рецепторы, которые присоединяются к остаткам аспарагина, серина или треонина, присутствующим в полипептиде.
Гликопротеин может быть «триммирован», полностью или частично, для того, чтобы либо стать свободным для доступа акцептора сиалилтрансферазы, либо стать фрагментом, к которому могут быть добавлены один или более соответствующих остатков с получением подходящего акцептора. Фрагменты, такие как гликозилтрансферазы и эндогликозидазы, используются для реакции присоединения и триммирования. Например, гликопротеин может быть триммирован путем обработки его сиалидазой с образованием терминальных групп галактозы перед введением белка в цикл обработки сиалилтрансферазой или для дальнейшего снижения уровня N-ацетилглюкозамина путем обработки галактозидазами. См, например, патент США 5272066, в котором описаны способы получения полипептидов, включающих подходящие акцепторы для сиалилирования.
Способы ковалентного присоединения полимерных молекул к полипептидам фактора VII:
Различные химические фрагменты, такие как полимерные молекулы, использованные при разработке настоящего изобретения, могут быть ковалентно присоединены к олигосахаридам в молекуле полипептида фактора VII путем либо химического синтеза, либо энзиматической обработки полипептида, например, модифицированной сиаловой кислотой. Полимерная молекула может быть также сопряжена с олигосахаридом через линкер. Подходящие линкеры известны специалистам в данной области. Примеры линкеров включают, без ограничения, N-(4-ацетилфенил)малеимид, сложный сукцинимидиловый эфир активированных производных малеимида, такой как коммерчески доступный сукцинимидил-4-малеимидобутаноат, 1,6-бисмалеимидогексаны.
Различные химические фрагменты, такие как полимерные молекулы, используемые при разработке настоящего изобретения, могут быть ковалентно присоединены к сиаловой кислоте, и такая "модифицированная" (или конъюгированная) сиаловая кислота впоследствии включается в цикл сиалилтрансферазы с образованием полимерной молекулы, которая ковалентно присоединяется к гликопротеину. Конъюгированная сиаловая кислота может быть получена традиционными способами, известными специалистам в данной области. Полимерная молекула может быть также соединена с сиаловой кислотой через линкер.
Хемоэнзиматическая дериватизация фактора VII и аналогов фактора VII
Используемые в практике осуществления настоящего изобретения фосфонуклеотиды с модифицированной сахарной частью могут быть заменены в соответствии с приведенными ниже общими формулами I и II:
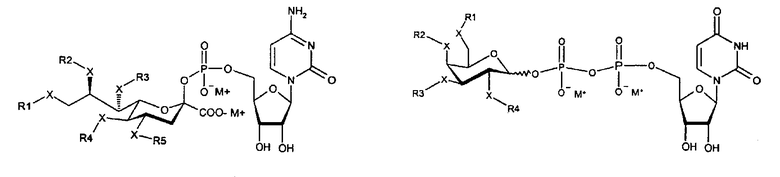
где
- Х независимо выбирают из S, O, NH или валентной связи;
- R1, R2, R3, R4 и R5 независимо выбирают из H, полимера и линкерной молекулы, ковалентно присоединенной к полимеру, ацила (включая ацетил и гидроксиацетил) и алкила;
- М+ представляет собой катион, выбранный из Na+, K+, Li+, тетрабутиламмония или аналогичного катиона.
В предпочтительном варианте осуществления изобретения R1 и R2 обозначают, каждый, независимо полимер на основе ПЭГ с молекулярной массой 1-40000 кДа.
В еще более предпочтительном варианте осуществления изобретения R1 обозначает независимо полимер на основе ПЭГ с молекулярной массой 1-40000 кДа.
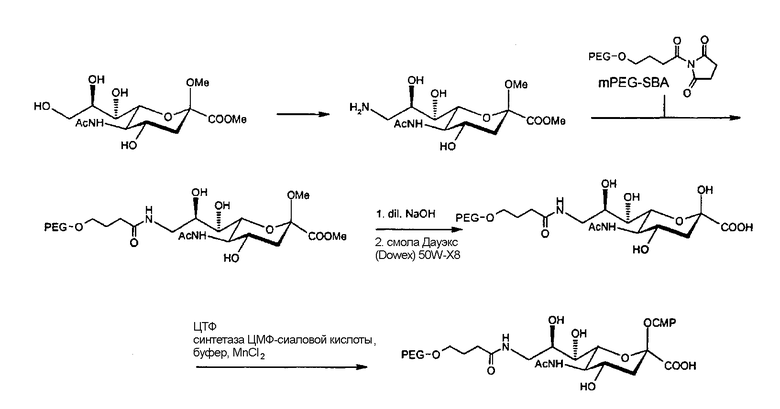
В иллюстративном варианте осуществления настоящего изобретения, приведенном на схеме 1, нейраминовую кислоту, защищенную по амино-, 2-гидрокси- и карбоксильной группам, вначале превращают в 9-аминопроизводное по методике Изекке и Броссмера (Isecke, R.; Brossmer, R., Tetrahedron 1994, 50(25), 7445-7460), которое затем подвергают дериватизации с использованием ПЭГ-COOH в стандартных условиях связывания. Далее у ПЭГ-производного продукта удаляют защитную группу в мягких кислотных условиях, и полученный продукт превращают в соответствующий сахар нуклеотида.
Схема 1:
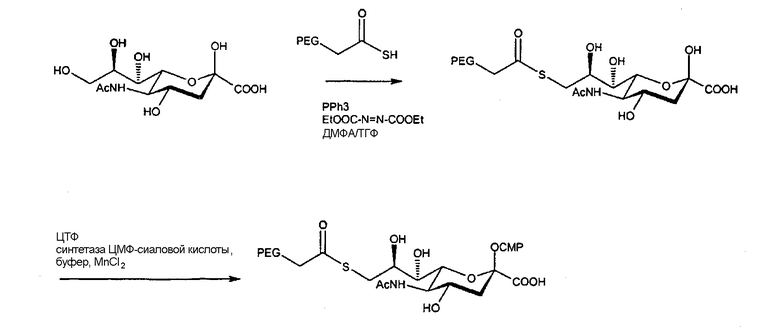
В другом иллюстративном варианте осуществления настоящего изобретения, приведенном на схеме 2, N-ацетилнейраминовую кислоту обрабатывают ПЭГ-производными тиокислот в условиях реакции Мицунобу с получением ПЭГ-производного N-ацетилнейраминовой кислоты, которое затем превращают в соответствующий сахар-содержащий нуклеотид.
Схема 2:
В другом иллюстративном варианте осуществления настоящего изобретения, приведенном на схеме 3, тиол модифицированной галактозы взаимодействует с ПЭГ-содержащим фрагментом малеимида. Соединение на основе ПЭГ-галактозы может быть затем превращено в соответствующий сахар-содержащий нуклеотид с использованием способов энзиматической или химической реакции.
Схема 3:
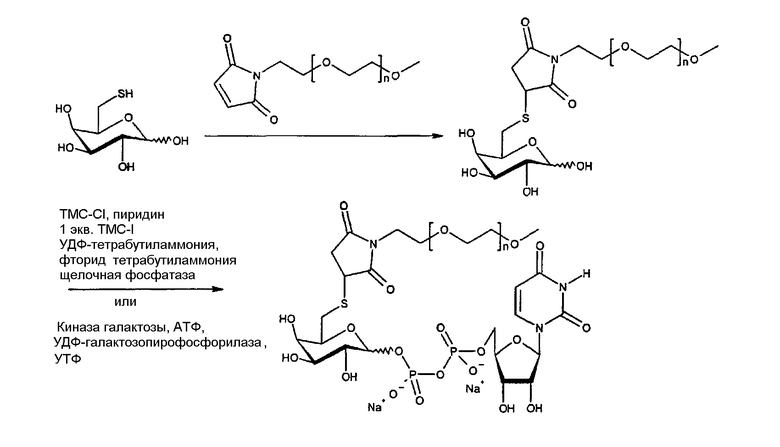
В другом иллюстративном варианте осуществления настоящего изобретения, приведенном на схеме 4, 6-аминогалактоза (Fernandez, J. et al., J. Org. Chem. 1993, 58(19), 5192-5199) взаимодействует с ПЭГ, содержащим защищенный по амину фрагмент кислоты. Сложный метиловый эфир подвергают сапонификации. ПЭГ-галактоза далее может быть превращена в соответствующий нуклеотидный сахар с использованием энзиматических или химических методов.
Схема 4:
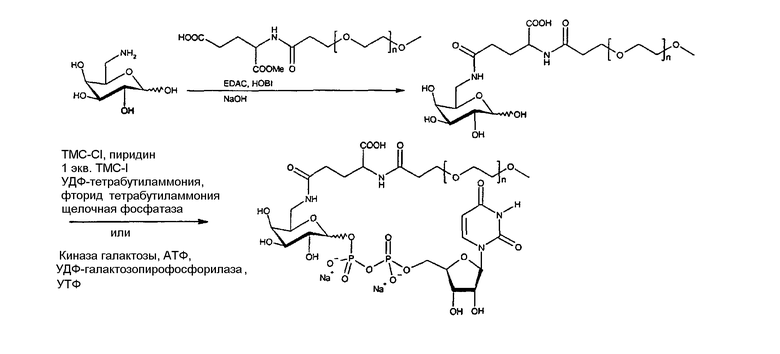
В другом иллюстративном варианте осуществления настоящего изобретения, приведенном на схеме 5, защищенная 6-бромгалактоза (Hodosi, G., Podanyi, B., and Kuszmann, J., Carbohydr. Res., 1992, 230(2), 327-342) взаимодействует с ПЭГ-содержащим защищенным фрагментом аминокислоты. Сложный метиловый эфир подвергается сапонификации. ПЭГ-галактоза далее может быть превращена в соответствующий нуклеотидный сахар с использованием энзиматических или химических методов.
Схема 5:
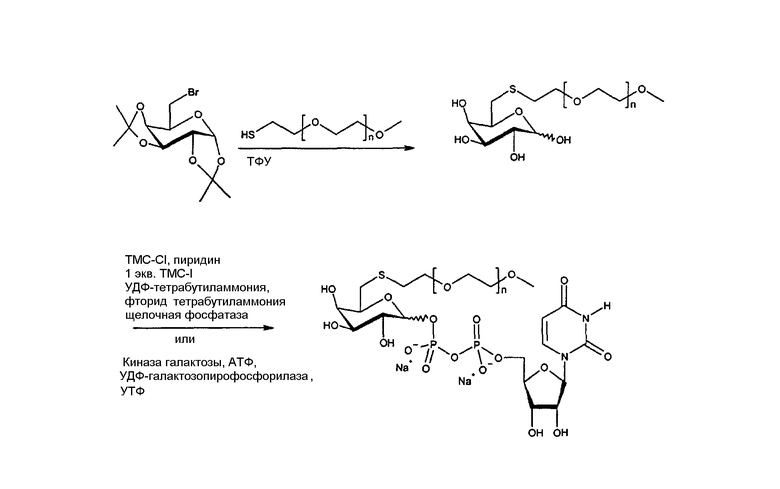
В другом иллюстративном варианте осуществления изобретения, приведенном на схеме 6, защищенная галактуроновая кислота (Godage, Y.S. and Fairbanks, A.J., Tetrahedron Lett., 2000, 41(39), 7589-7594) взаимодействует с фрагментом ПЭГ, содержащим аминогруппу. Изопропилиденовые группы удаляют в кислых условиях. Соединение на основе ПЭГ-галактозы далее может быть превращено в соответствующий нуклеотидный сахар с использованием энзиматических или химических методов.
Схема 6:
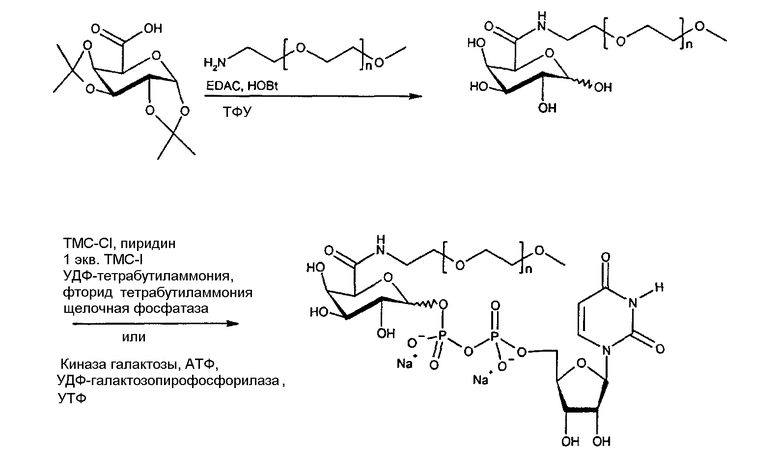
В основном сахарсодержащие нуклеотиды, такие как приведенные выше, могут быть подвергнуты ферментативному переносу на соответствующие гликопротеины, такие как фактор VII или фактор VII-родственный полипептид, с использованием природных или мутированных гликозилтрансфераз, которые включают в качестве иллюстрации, но не ограничиваются приведенными ниже ферментами: α2,3-сиалилтрансферазы, α2,6-сиалилтрансферазы или β1,4-галактозилтрансферазы. В зависимости от выбора ПЭГ-производного нуклеотида сахара (ЦМФ-СА-ПЭГ или УДФ-Gal-ПЭГ), можно предпочтительно проводить обработку фактор VII-родственного полипептида сиалидазой, галактозидазой или обоими фрагментами, перед проведением реакции с использованием гликозилтрансфераз и ПЭГ-производного сахарного нуклеотида.
Таким образом, в одном предпочтительном варианте осуществления настоящего изобретения аналог фактора VII обрабатывают сиалидазой с получением асиало аналога фактора VII, который впоследствии обрабатывают сиалилтрансферазой и аналогом ЦМФ-СА-ПЭГ общей формулы I с получением ПЭГ-производного аналога фактора VII.
В другом варианте осуществления настоящего изобретения фактор VII-родственный полипептид последовательно обрабатывают, вначале сиалидазой и далее галактозидазой с получением асиало агалакто-FVII-родственного полипептида. Указанный аналог затем обрабатывают галактозилтрансферазой и аналогом УДФ-Gal-ПЭГ общей формулы II с получением ПЭГ-производного аналога фактора VII.
В серии вариантов осуществления настоящего изобретения могут использоваться модифицированные галактозные соединения, которые ковалентно соединены с полимером либо непосредственно, либо через линкерный фрагмент. Можно использовать либо фактор VII, либо фактор VII-родственные полипептиды непосредственно для достижения более низких уровней включения полимера в полипептид, либо проводить вначале обработку фактора VII или фактор VII-родственных полипептидов сиалидазой для удаления терминальной сиаловой кислоты для того, чтобы достичь более высоких уровней содержания полимера в пептиде. При обработке полипептида галактозидазой точки присоединения модифицированных галактозных соединений становятся доступными. Связь между модифицированными галактозными соединениями и обработанным полипептидом может быть сформирована за счет использования активированной формы УДФ, модифицированных галактозных соединений и галактозилтрансферазы. Иллюстративный вариант осуществления указанного способа приведен на схеме 7, в которой черные кружки указывают фактор VII или фактор VII-родственные полипептиды, а также показана терминальная часть нескольких углеводов.
Схема 7:
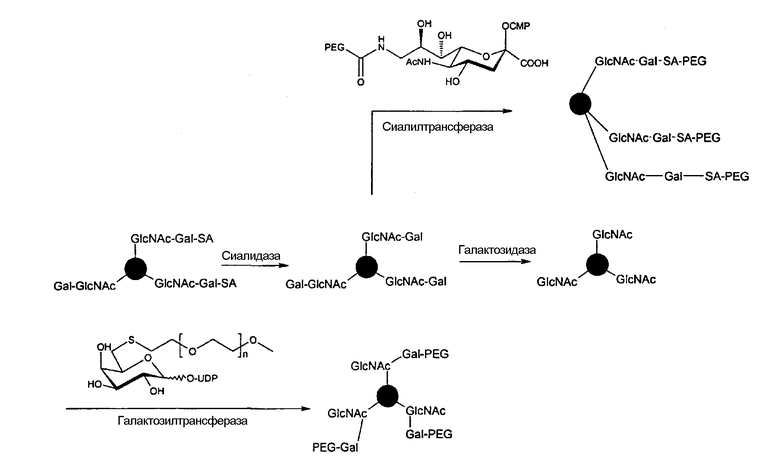
Химическая дериватизация фактора VII и аналогов фактора VII
Химическое окисление углеводных остатков с использованием периодата натрия представляет собой альтернативный способ получения конъюгатов фактора VII-ПЭГ. Химическое окисление углеводов в основном приводит к получению множества реактивных альдегидных групп, каждая из которых способна реагировать с ПЭГ-нуклеофилами, такими как ПЭГ-гидразид, ПЭГ-О-гидроксиламин и ПЭГ-амин.
С использованием ПЭГ-гидразида и ПЭГ-О-гидроксиламина могут быть получены стабильные конъюгаты FVII-ПЭГ-ацилгидразона и FVII-ПЭГ-оксима, соответственно. С использованием ПЭГ-аминов получают менее стабильные конъюгатные формы Шиффова основания. Однако указанные конъюгаты могут быть далее стабилизированы путем восстановления цианборгидридом натрия, в ходе которого образуется вторичная аминная связь. Конъюгаты фактора VII-ПЭГ-ацилгидразона также могут быть восстановлены с использованием цианборгидрида натрия, в результате чего образуются N,N'-связанные гидразиновые конъюгаты.
Очистка препаратов конъюгированных гликоформ фактора VII
В контексте настоящего описания фраза "препарат фактора VII" относится к множеству полипептидов фактора VII, полипептидов фактора VIIа или фактор VII-родственных полипептидов, включающих их варианты и химические модифицированные формы, которые были получены отделением от клеток или реакционной среды, где они были синтезированы.
Очистка препаратов фактора VII и конъюгатов:
Отделение рекомбинантных полипептидов от клеток, в которых они были получены, может быть достигнуто любыми известными в данной области способами, включающими, без ограничения, удаление культуральной среды от приклеившихся клеток, содержащей желательный продукт, центрифугирование или фильтрование для удаления не приклеившихся клеток и т.п.
Необязательно, полипептиды фактора VII могут быть подвергнуты очистке. Очистка может быть проведена с использованием любого способа, известного в данной области, включающего, без ограничения, афинную хроматографию, такую как хроматография на колонке с антителом против фактора VII (см, например, Wakabayashi et al., J. Biol. Chem. 261: 11097, 1986; и Thim et al., Biochem. 27: 7785, 1988), хроматографию на основе гидрофобного взаимодействия, ионообменную хроматографию, вытеснительную хроматографию, процедуры электрофоретического разделения (например, препаративное изоэлектрофокусирование (ИЭФ)), разделение на основе разной растворимости (например осаждение сульфатом аммония) или экстракцию и т.п. В основном указанные методы описаны, например, в работе Скоупса (Scopes, Protein Purification, Springer-Verlag, New York, 1983; и Protein Purification, J.-C. Janson and Lars Ryden, editors, VCH Publishers, New York, 1989). После очистки препарат содержит, предпочтительно, менее чем примерно 10 мас.%, более предпочтительно менее чем примерно 5 мас.% и, наиболее предпочтительно менее чем примерно 1 мас.% полученных из хозяйской клетки белков, не относящихся к фактору VII.
Фактор VII и фактор VII-родственные полипептиды могут быть активированы путем протеолитического расщепления с использованием фактора XIIа или других протеаз, обладающих трипсин-подобной специфичностью, таких как, например, фактор IХа, калликреин, фактор Ха и тромбин (см, например, Osterud et al., Biochem., 11: 2853 (1972); Thomas, патент США No. 4 456 591 и Hedner et al., J. Clin. Invest., 71:1836 (1983)). Альтернативно, фактор VII может быть активирован путем пропускания его через колонку для ионообменной хроматографии, такую как Mono Q® (Pharmacia) или аналогичную колонку. Полученный активированный фактор VII может быть далее включен в состав композиции и использован для введения, как описано ниже.
Функциональные характеристики препаратов фактора VII
Препараты полипептидов фактора VII и фактор VII-родственных полипептидов по настоящему изобретению, обладающие заданными параметрами олигосахаридных структур с ковалентно присоединенными полимерными молекулами, демонстрируют улучшенные функциональные характеристики в сравнении с эталонными препаратами. Улучшенные функциональные характеристики могут включать, без ограничения, (а) физические свойства, такие как, например, стабильность при хранении; (b) фармакокинетические свойства, такие как, например, биологическая доступность и период полувыведения и (с) иммуногенность для человека.
Эталонный препарат относится к препарату, содержащему полипептид, который имеет аминокислотную последовательность, идентичную последовательности, характерной для препарата по настоящему изобретению, который используют для целей сравнения данного исследуемого препарата (такой как, например, неконъюгированные формы фактора VII дикого типа или его определенный вариант или химически модифицированная форма), но который не был конъюгирован с какой-либо одной или более полимерными молекулами, имеющимися в препарате по настоящему изобретению. Так, например, в типичном случае эталонные препараты включают неконъюгированный фактор VII дикого типа или неконъюгированные фактор VII-родственные полипептиды.
Стабильность при хранении препарата фактора VII может быть оценена при определении (а) времени, необходимого для того, чтобы 20% биологической активности препарата при хранения в виде сухого порошка при 25°С было разрушено и/или (b) времени, необходимого для удвоения доли агрегатных форм фактора VIIа в препарате.
В некоторых вариантах осуществления настоящего изобретения рассматриваемые в нем препараты демонстрируют повышение по меньшей мере примерно на 30%, предпочтительно по меньшей мере на 60% и более предпочтительно по меньшей мере примерно на 100% времени, необходимого для разрушения на 20% биологической активности, относительно времени, необходимого для того же процесса в эталонном препарате в случае хранения обоих препаратов в виде сухих порошков при 25°С. Измерение биологической активности может быть осуществлено с использованием любого из известных тестов: теста на свертывание крови, теста на протеолиз, теста на связывание с ТФ или теста на ТФ-независимое образование тромбина.
В некоторых вариантах осуществления настоящего изобретения рассматриваемые в нем препараты демонстрируют повышение по меньшей мере примерно на 30%, предпочтительно, по меньшей мере примерно на 60% и, более предпочтительно, по меньшей мере примерно на 100% времени, необходимого для удвоения числа агрегатных форм, в сравнении с эталонным препаратом, при хранении обоих препаратов в виде сухих порошков в условиях 25°С. Содержание агрегатных форм определяют с помощью гель-проникающей ВЭЖХ на колонке Protein Pak 300 SW (7,5 мм х 300 мм) (Waters, 80013) по описанной ниже методике. Колонку уравновешивают элюентом А (0,2 М сульфата аммония, 5% изопропанола, pH доводят до значения 2,5 фосфорной кислотой и затем pH доводят до значения 7,0 при помощи триэтиламина), после чего в колонку вносят 25 мкг образца. Затем проводят элюирование элюентом А со скоростью течения 0,5 мл/мин в течение 30 минут и проводят выявление путем измерения уровня поглощения при длине волны 215 нм. Содержание агрегатных форм вычисляют как площадь пика агрегатных форм фактора VII/общая площадь пиков фактора VII (мономер и агрегаты).
Термин "биологическая доступность" относится к доле введенной дозы препарата фактора VII или фактор VII-родственных полипептидов, которая может быть обнаружена в плазме в заданные временные точки после введения. В типичном случае биологическую доступность определяют у экспериментальных животных путем введения дозы препарата в количестве от 25 до 250 мкг/кг, с последующим отбором образцов плазмы в заданные временные точки после введения и измерением количества фактора VII или фактор VII-родственных полипептидов в образцах в рамках одного или более тестов: теста на свертывание крови (или любого биотеста), или в рамках иммуноанализа или эквивалентных методик. Получаемые данные обычно изображаются на экране графически в виде значения [фактор VII] относительно времени, а величину биологической доступности выражают в виде площади под кривой (AUC). Относительная биодоступность исследуемого препарата представляет собой соотношение между показателями AUC исследуемого препарата и эталонного препарата.
В некоторых вариантах осуществления настоящего изобретения рассматриваемые в нем препараты демонстрируют относительную биологическую доступность, которая составляет по меньшей мере примерно 110%, предпочтительно по меньшей мере примерно 120%, более предпочтительно по меньшей мере примерно 130% и наиболее предпочтительно по меньшей мере примерно 140% от биологической доступности эталонного препарата. Биологическая доступность может быть измерена у млекопитающего любого вида, предпочтительно у собак, и заданные временные точки, используемые для вычисления AUC, могут включать различные интервалы повышения значения параметра от 10 минут до 8 часов.
Термин "период полувыведения" обозначает время, необходимое для того, чтобы концентрация полипептидов фактора VII или фактор VII-родственных полипептидов в плазме снизилась от данного значения до половины данного значения. Период полувыведения может быть определен с использованием той же процедуры, что и для определения биологической доступности. В некоторых вариантах осуществления настоящего изобретения рассматриваемые в нем препараты демонстрируют повышение периода полувыведения, равное примерно 0,25 часа, предпочтительно по меньшей мере примерно 0,5 часа, более предпочтительно по меньшей мере примерно 1 час и наиболее предпочтительно по меньшей мере примерно 2 часа, в сравнении с периодом полувыведения эталонного препарата.
Термин "иммуногенность" препарата относится к способности препарата при введении в организм человека вызывать вредную иммунную реакцию гуморального, клеточного типа или сочетанного типа. В отношении полипептидов фактора VII или фактор VII-родственных полипептидов неизвестно, чтобы они приводили к развитию выявляемых иммунных реакций у людей. Тем не менее, в каждой подгруппе людей могут существовать индивидуумы, обладающие чувствительностью к конкретным вводимым белкам. Иммуногенность может быть определена путем количественного измерения уровня антител против фактора VII и/или Т-клеток, реактивных в отношении фактора VII, у чувствительного индивидуума с использованием традиционных методик, известных в данной области техники. В некоторых вариантах осуществления настоящего изобретения рассматриваемые в нем препараты демонстрируют снижение иммуногенности у чувствительных индивидуумов по меньшей мере примерно на 10%, предпочтительно по меньшей мере примерно на 25%, более предпочтительно по меньшей мере примерно на 40% и наиболее предпочтительно по меньшей мере примерно на 50% относительно уровня иммуногенности у индивидуума, выявляемой на эталонный препарат.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
Препараты по настоящему изобретению могут использоваться для лечения любого синдрома, реактивного в отношении фактора VII, такого как, например, расстройства, связанные к кровотечением, которые включают, без ограничения, расстройства, связанные с недостаточностью факторов свертывания крови (например, гемофилия А и В или недостаточность факторов свертывания крови XI или VII); расстройства, вызванные тромбоцитопенией, или болезнь Виллебранда, или расстройства, определяемые наличием ингибиторов факторов свертывания, или избыточным кровотечением, возникшим по любой другой причине. Указанные препараты могут также вводиться пациентам в сочетании с хирургическими процедурами или пациентам, имеющим другие травмы, или пациентам, проходящим лечение антикоагуляционными препаратами.
Препараты, включающие фактор VII-родственные полипептиды по настоящему изобретению, которые обладают существенно сниженной биологической активностью относительно фактора VII дикого типа, могут использоваться в качестве антикоагулянтов, например, в случае пациентов, подвергающихся ангиопластике или другим хирургическим процедурам, которые могут повышать риск тромбоза или закупорки кровеносных сосудов, что происходит, например, при рестенозе. Другие медицинские показания для применения антикоагулянтов включают, без ограничения, тромбоз глубоких вен, легочную эмболию, кровоизлияние, синдром диссеминированного внутрисосудистого свертывания крови (ДВС-синдром), отложение фибрина в легких и почках, связанное с эндотоксемией, вызванной грамотрицательными бактериями, инфаркт миокарда, острый респираторный дистресс-синдром взрослых (ARDS), синдром системной воспалительной реакции (SIRS), гемолитический уремический синдром (HUS), MOF и TTP.
Фармацевтические композиции, включающие препараты фактора VII и фактор VI-родственных полипептидов по настоящему изобретению, прежде всего предназначены для парентерального введения с профилактической и/или терапевтической целью. Предпочтительно, фармацевтические композиции вводятся парентерально, например, внутривенным, подкожным или внутримышечным способом. Указанные препараты могут вводиться путем непрерывной или пульсирующей инфузией.
Фармацевтические композиции или рецептуры включают препарат по настоящему изобретению в сочетании с фармацевтически приемлемым носителем, предпочтительно при растворении в фармацевтически приемлемом носителе, предпочтительно в водном растворителе или разбавителе. Может использоваться множество водных носителей, таких как вода, забуференная вода, 0,4% солевой раствор, 0,3% раствор глицина и т.п. Препараты по настоящему изобретению могут также изготавливаться в виде липосомных препаратов для доставки или для целевого введения в места поражения. Липосомные препараты описаны в основном, например, в патентах США No. 4837028, 4501728 и 4975282. Композиции могут быть подвергнуты стерилизации с использованием обычных хорошо известных методик стерилизации. Полученные водные растворы могут быть упакованы для дальнейшего использования или отфильтрованы в асептических условиях и далее лиофилизированы, после чего лиофилизированный препарат объединяют со стерильным водным раствором перед введением.
Композиции могут содержать фармацевтически приемлемые дополнительные вещества или адъюванты, включающие, без ограничения, средства для корректировки pH и забуферивающие средства и/или средства для корректировки тоничности, такие как, например, ацетат натрия, лактат натрия, хлорид натрия, хлорид калия, хлорид кальция и т.п.
Концентрация фактора VII или фактор VII-родственных полипептидов в указанных композициях может широко варьировать, например, от значений менее чем примерно 0,5 мас.%, обычно по меньшей мере примерно 1 мас.%, до 15-20 мас.%, где указанная концентрация выбирается прежде всего в зависимости от объемов жидкости, вязкости и т.п., в соответствии с конкретным выбранным режимом введения.
Таким образом, типичная фармацевтическая композиция, предназначенная для внутривенной инфузии, может быть получена с содержанием 250 мл стерильного раствора Рингера и 10 мг препарата. Практические способы приготовления парентеральной композиции известны специалистам в данной области и описаны более детально, например, в руководстве Ремингтона (Remington's Pharmaceutical Sciences, 18th ed., Mack Publishing Company, Easton, PA (1990)).
Композиции, содержащие препараты по настоящему изобретению, могут вводиться с целью профилактического или терапевтического использования. В терапевтических вариантах применения указанные композиции вводят пациенту, который уже имеет заболевание из числа описанных выше, в количестве, достаточном для излечивания, облегчения или частичной остановки заболевания или его осложнения. Количество, адекватное для достижения указанной цели, определяется как "терапевтически эффективное количество". Эффективное количество для достижения каждой заданной цели зависит от тяжести заболевания или поражения, а также от веса и общего состояния здоровья пациента. В целом, однако, эффективное количество укладывается в диапазон от примерно 0,05 мг до примерно 500 мг препарата в день для пациента весом 70 кг, где чаще всего используемыми являются дозировки от примерно 1,0 мг до примерно 200 мг препарата в день. Следует понимать, что определение соответствующей дозировки может быть осуществлено с помощью рутинного эксперимента путем построения матрицы переменных и тестирования различных точек в данной матрице.
Местная доставка препаратов по настоящему изобретению, такая как, например, в случае местного нанесения, может быть осуществлена, в частности, с помощью распыления, перфузии, двойных балонных катетеров, стентов, включения в сосудистые трансплантируемые участки ткани или стенты, гидрогелей, используемых для покрытия балонных катетеров, а также с помощью других хорошо установленных методик. В каждом случае фармацевтические композиции должны обеспечивать доставку количества препарата, достаточного для эффективного лечения пациента.
Фармацевтические композиции по настоящему изобретению могут также включать другие биологически активные средства, такие как факторы свертывания или антикоагулянты, не связанные с фактором VII.
Препараты с длительным высвобождением
Примеры препаратов с длительным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие полипептид или конъюгат, где указанные матрицы обладают подходящей формой, такой как пленка или микрокапсулы. Примеры матриц с длительным высвобождением включают полиэфиры, гидрогели (например, поли(2-гидроксиэтилметакрилат) или поли(виниловый спирт)), полилактиды, сополимеры L-глутаминовой кислоты и этил-L-глутамата, не деградируемый этиленвинилацетат, разлагаемые сополимеры молочной кислоты и гликолевой кислоты, такие как сополимеры от компаний ProLease® technology или Lupron Depot® (инъецируемые микросферы, состоящие из сополимера молочной кислоты и гликолевой кислоты и ацетата леупролида), и поли-D-(-)-3-гидроксимасляная кислота. Тогда как полимеры, такие как этиленвинилацетат и сополимер молочной и гликолевой кислот, позволяют достичь высвобождения молекул в течение длительного периода времени, такого как, например, в течение периода более 100 дней, некоторые гидрогели высвобождают белки в течение более коротких периодов времени. В том случае, когда инкапсулированные полипептиды остаются в организме в течение дополнительного периода времени, они могут повергаться денатурации или агрегированию в результате воздействия влаги при 37°С, что приводит к потере биологический активности и возможным изменениям иммуногенности. Рациональная стратегия предполагает стабилизацию, достижение которой зависит от имеющегося механизма. Например, если было обнаружено, что указанный механизм агрегации осуществляется через внутримолекулярную S-S связь, которая образуется путем обмена тиосульфидных связей, стабилизация может быть достигнута за счет модификаций сульфгидрильных остатков, лиофилизации из кислотных растворов, контроля содержания влаги, с использованием соответствующих добавок и посредством разработки специфических композиций полимерных матриц.
Приведенные ниже неограничивающие примеры иллюстрируют некоторые аспекты настоящего изобретения.
ПРИМЕРЫ
Пример 1
Гликопэгилирование продукта с высоким содержанием сиаловой кислоты
Полиэтиленгликоль-ЦМФ-сиаловую кислоту (ПЭГ-ЦМФСК) получают путем ковалентного присоединения ПЭГ с М.в. 10000 Да к сиаловой кислоте.
Фактор VIIа с содержанием сиаловой кислоты 87-99% обрабатывают сиалидазой, например, как описано в патенте США No. 5272066, и подвергают повторному сиалилированию сиалилтрансферазой с использованием ПЭГ-ЦМФСК в качестве донорной молекулы (например, как описано в патенте США No. 6399336). После того, как реакция пэгилирования приводит к достижению максимального включения, добавляют ЦМФСК к реакционной смеси для кэппинга выступающих терминальных остатков галактозы.
Включение пэгилированной сиаловой кислоты анализируют методом ДСН ПААГ, КЭ-ПААГ, методом изоэлектрофокусирования с использованием гелей и КЭ-ИЭФ.
Включается 94-100% сиаловой кислоты и в среднем включается 1-4 группы ПЭГ.
Пример 2
Гликопэгилирование продукта со средним уровнем содержания сиаловой кислоты
Полиэтиленгликоль-ЦМФ-сиаловую кислоту (ПЭГ-ЦМФСК) получают путем ковалентного присоединения ПЭГ с М.в. 10000 Да к сиаловой кислоте.
Фактор VIIа с содержанием сиаловой кислоты на уровне 87-93% обрабатывают сиалилтрансферазой с использованием ПЭГ-ЦМФСК в качестве донорной молекулы (например, как описано в патенте США No. 6399336). После того, как реакция пэгилирования приводит к достижению максимального включения, добавляют ЦМФСК к реакционной смеси для кэппинга любых открытых терминальных остатков галактозы.
Включение пэгилированной сиаловой кислоты анализируют методом ДСН ПААГ, КЭ-ПААГ, методом изоэлектрофокусирования с использованием гелей и КЭ-ИЭФ.
Включается 87-100% сиаловой кислоты и в среднем включается 0,1-0,5 групп ПЭГ.
Пример 3
Пэгилированное производное цитидин-5'-монофосфатсиаловой кислоты (ЦМФ-СК-ПЭГ): сложный метиловый эфир N-ацетил-О2-метил-9-амино-9-дезоксинейраминовой кислоты (10 мг, 0,031 ммоль, полученный по известной методике (Isecke, R.; Brossmer, R., Tetrahedron 1994, 50(25), 7445-7460)) растворяют в воде (2 мл) и добавляют мПЭГ-СБК (170 мг, 0,03 ммоль, 5 кДа, (Shearwater 2M450H01)). Смесь перемешивают при температуре окружающей среды до завершения реакции, определяемого по результатам анализа методом ТСХ. Растворитель удаляют лиофилизацией и остаток перерастворяют в смеси (1:1) метанола и 0,1 М раствора NaOH (5 мл). Смесь перемешивают при комнатной температуре в течение 1 часа, затем пропускают через колонку со смолой Дауэкс (Dowex) 50W-X8 (H+) при температуре 4°С и лиофилизируют. Остаток перерастворяют в воде (5 мл), добавляют смолу Дауэкс (Dowex) 50W-X8 (H+) и смесь перемешивают до завершения реакции, определяемого по результатам анализа ТСХ.
Цитидин-5'-монофосфатные аналоги производных сиаловой кислоты общей формулы I получают в основном по методике Симона с соавт. (E.S. Simon, M.D. Bednarski and G.M. Whitesides, J. Am. Chem. Soc., 1998, 110, 7159-7163) следующим образом: синтетазу цитидин 5'-монофосфатнейраминовой кислоты растворяют в растворе 9-пэгилированной N-ацетил-9-амино-9-дезокси-нейраминовой кислоты, полученной по описанной выше методике, и добавляют к раствору ЦТФ. Смесь доводят до pH 8,5 и добавляют MgCl2•6H2O. Реакционную смесь перемешивают при комнатной температуре и добавляют 1N NaOH с помощью перистальтического насоса для подержания значения pH около 8,5. По результатам анализа аликвоты методом 1H-ЯМР, указывающим на завершение реакции, продукт выделяют методами стандартной ионообменной хроматографии.
Пример 4
Фактор VIIа (1 мг), растворенный в 1 мл 0,1М ацетата натрия при pH 5,5, окисляют до уровня гликанов при комнатной температуре в течение 30 минут с использованием 10 мМ периодата натрия. Затем раствор диализуют против 100 мМ ацетата натрия, pH 5,5. После диализа ПЭГ-С(О)-NHNH2 (полученный путем гидразинолиза мПЭГ-СБК (2 мг, 5 кДа (Shearwater 2M450H01)) смешивают с окисленным фактором VIIа и оставляют для взаимодействия в течение ночи при комнатной температуре и при осторожном покачивании. Полученный таким образом раствор конъюгата FVIIа-ПЭГ подвергают диализу (диализные мембраны с отсечением молекул размером 10 кДа) против 100 мМ буфера Трис-HCl, pH 7,5 и хранят при температуре 4°С.
ФАРМАКОЛОГИЧЕСКИЕ МЕТОДЫ
Приведенные ниже тесты используют для определения биологический активности, периода полувыведения и биологической доступности фактора VII и фактор VII-родственных полипептидов.
Тест (I)
Тест на гидролиз in vitro
Приведенный ниже метод может служить для анализа биологической активности фактора VIIа. Тест проводят в микротитрационном планшете (MaxiSorp, Nunc, Дания). Хромогенный субстрат D-Ile-Pro-Arg-п-нитроанилид (S-2288, Chromogenix, Швеция) в конечной концентрации 1 мМ добавляют к фактору VIIа (конечная концентрация 100 нМ) в 50 мМ буфера Hepes, pH 7,4, содержащего 0,1 M NaCl, 5 мМ CaCl2 и 1 мг/мл бычьего сывороточного альбумина. Величину поглощения при длине волны 405 нм измеряют непрерывно на счетчике для микротитрационных планшетов SpectraMaxTM 340 (Molecular Devices, USA). Развившееся в ходе 20-минутной инкубации поглощение после вычитания уровня поглощения контрольной пробы в ячейке, не содержащей фермента, используют для вычисления соотношения между активностью исследуемого и эталонного фактора VIIа.
Тест (II)
Тест на протеолиз in vitro
Приведенный ниже метод используют для анализа биологической активности фактора VIIа. Тест проводят в микротитрационном планшете (MaiSxorp, Nunc, Denmark). Фактор VIIа (10 нМ) и фактор Х (0,8 микроМ) в 100 мкл 50 мМ буфера Hepes, pH 7,4, содержащего 0,1 M NaCl, 5 мМ CaCl2 и 1 мг/мл бычьего сывороточного альбумина, инкубируют в течение 15 минут. Затем останавливают расщепление фактором Х добавлением 50 мМ буфера Hepes, pH 7,4, содержащего 0,1 M NaCl, 20 мМ ЭДТА и 1 мг/мл бычьего сывороточного альбумина. Количество образованного фактора Ха определяют при добавлении хромогенного субстрата Z-D-Arg-Gly-Arg-п-нитроанилида (S-2765, Chromogenix, Швеция) до конечной концентрации 0,5 мМ. Величину поглощения при длине волны 405 нм измеряют непрерывно на счетчике для микротитрационных планшетов SpectraMaxTM 340 (Molecular Devices, USA). Развившееся в ходе 10-минутной инкубации поглощение после вычитания уровня поглощения контрольной пробы в ячейке, не содержащей фермента, используют для вычисления соотношения между активностью исследуемого и эталонного фактора VIIа.
Тест (III)
Измерение функционального полупериода существования in vivo
Измерение функционального полупериода существования in vivo может быть проведено с использованием множества способов, описанных в литературе. Пример теста для измерения полупериода in vivo rFVIIа и его вариантов описан в руководстве Администрации по контролю за лекарственными препаратами, пищевыми продуктами и косметическими средствами США (FDA) под номером 96-0597. Вкратце, процедура состоит в том, что свертывающую активность фактора VIIa измеряют в отобранном образце плазмы в течение 24 часов после введения конъюгата, полипептида или композиции. Измеряют средний кажущийся объем распределения в устойчивом состоянии и определяют среднее значение клиренса.
Тест (IV)
Биологическая доступность полипептидов фактора VII
Биологическая доступность может быть измерена, например, на модели собак следующим образом: Эксперимент проводят в перекрестном исследовании четырех ног собак у 12 собак бигль, разделенных на четыре группы. Всем животным дают исследуемый препарат А и эталонный препарат В в дозе, составляющей примерно 90 мкг/кг в глицилглициновом буфере (pH 5,5), содержащем хлорид натрия (2,92 мг/мл), дигидрат хлорида кальция (1,47 мг/мл), маннит (30 мг/мл) и полисорбат 80. Образцы крови отбирают в точках 10, 30 и 60 минут, а также 2, 3, 4, 6 и 8 часов после исходного введения. Из отобранных образцов получают плазму и определяют количественное содержание фактора VII методом ELISA.
Биологическую доступность каждого образца выражают в виде дозы, соответствующей площади под концентрационной кривой для фактора VII в плазме (AUC/доза). Относительную биодоступность выражают в виде соотношения между средним значением AUC/доза для исследуемого и стандартного препарата х 100 и вычисляют 90% доверительный интервал относительной биодоступности.
Изобретение относится к области биотехнологии, конкретно к получению полипептидов фактора VII, и может быть использовано в медицине. Получают конъюгат полипептида фактора VII, включающий полипептид фактора VII с аспарагинсвязанными и/или серинсвязанными олигосахаридными цепями, которые включают фрагменты сиаловой кислоты или фрагменты галактозы. При этом по меньшей мере одна из олигосахаридных цепей ковалентно связана с по меньшей мере одной полимерной группой, представляющей собой полиэтиленгликоль, имеющий молекулярную массу в диапазоне приблизительно 300-100000 Да. Полученный конъюгат фактора VII используют в составе фармацевтической композиции для лечения фактор VII-реактивного синдрома. Изобретение позволяет получить конъюгат фактора VII с ПЭГ с заданным характером гликозилирования для получения гомогенно модифицированного препарата. 4 н. и 18 з.п. ф-лы, 1 ил.
1. Конъюгат полипептида фактора VII, включающий полипептид фактора VII, включающий аспарагин-связанные и/или серин-связанные олигосахаридные цепи, включающие фрагменты сиаловой кислоты или фрагменты галактозы, где по меньшей мере одна из олигосахаридных цепей ковалентно связана с по меньшей мере одной полимерной группой, представляющей собой полиэтиленгликоль, имеющий молекулярную массу в диапазоне приблизительно 300-100000 Да.
2. Конъюгат полипептида фактора VII по п.1, в котором указанная полимерная группа присоединяется к фрагменту сиаловой кислоты.
3. Конъюгат полипептида фактора VII по п.1 или 2, в котором 94-100% олигосахаридных цепей содержат по меньшей мере один фрагмент сиаловой кислоты.
4. Конъюгат полипептида фактора VII по п.3, в котором 94-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты, и где менее чем 25% олигосахаридных цепей содержат одну не кэппированную антенну.
5. Конъюгат полипептида фактора VII по п.4, в котором меньше, чем 10% олигосахаридных цепей, содержат по меньшей мере одну не кэппированную антенну.
6. Конъюгат полипептида фактора VII по п.5, в котором меньше, чем 5%, предпочтительно 2% олигосахаридных цепей содержат по меньшей мере одну не кэппированную антенну.
7. Конъюгат полипептида фактора VII по любому из пп.4-6, в котором 96-100% олигосахаридных цепей содержат по меньшей мере один фрагмент сиаловой кислоты.
8. Конъюгат полипептида фактора VII по п.7, в котором 98-100% олигосахаридных цепей включают по меньшей мере один фрагмент сиаловой кислоты.
9. Конъюгат полипептида фактора VII по любому из пп.1-8, в котором аспарагин-связанные олигосахаридные цепи расположены в положениях, соответствующих аминокислотным остаткам Asn-145 и Asn-322 человеческого фактора VIIa дикого типа (фиг.1).
10. Конъюгат полипептида фактора VII по любому из пп.1-9, в котором серин-связанные олигосахаридные цепи расположены в положениях, соответствующих аминокислотным остаткам Ser-52 и Ser-60 человеческого фактора VIIa дикого типа (фиг.1).
11. Конъюгат полипептида фактора VII по любому из пп.1-10, в котором указанный полипептид имеет аминокислотную последовательность человеческого фактора VIIa дикого типа (фиг.1).
12. Конъюгат полипептида фактора VII по любому из пп.1-11, в котором указанные полипептиды представляют собой полученный из плазмы человеческий фактор VIIa.
13. Конъюгат полипептида фактора VII по любому из пп.1-12, в котором полипептиды фактора VII выбраны из группы, состоящей из: S52А-Фактора VII, S60A-Фактора VII, Фактора VII, протеолитически расщепленного между остатками 290 и 291; Фактора VII, протеолитически расщепленного между остатками 315 и 316;
окисленного Фактора VII, L305V-FVII, L305WM306D/D309S-FVII, L3051-FVII, L305T-FVII, F374P-FVII, V158T/M298Q-FVII, V158D/E296V/M298Q-FVII, K337A-FVII, M298Q-FVII, V158D/M298Q-FVII, L305V/K337A-FVII, V158D/E296V/M298Q/L305V-FVII, V158D/E296V/M298Q/K337A-FVII, V158D/E296V/M298Q/L305V/K337A-FVII, K157A-FVII, E296V-FVII, E296V/M298Q-FVII, V158D/E296V-FVII, V158D/M298K-FVII, S336G-FVII; вариантов последовательности Фактора VII, в которых заменен аминокислотный остаток в положениях 290 и/или 291, предпочтительно, 290, и вариантов последовательности Фактора VII, в которых заменен аминокислотный остаток в положениях 315 и/или 316, предпочтительно 315.
14. Конъюгат полипептида фактора VII по любому из пп.1-12, в котором полипептиды фактора VII выбраны из группы, состоящей из: L305V/K337A-FVII, L305VN158D-FVII, L305WE296V-FVII, L305WM298Q-FVII, L305VN158T-FVII, L305WK337AN158T-FVII, L305WK337A/M298Q-FVII, L305V/K337A/E296V-FVII, L305V/K337AN158D-FVII, L305VN1 58D/M298Q-FVII, L305VN1 58D/E296V-FVII, L305VN1 58T/M298Q-FVII, L305VN1 58T/E296V-FVII, L305V/E296V/M298Q-FVII, L305V/V158D/E296V/M298Q-FVII, L305V/V158T/E296V/M298Q-FVII, L305VN15 8T/K337A/M298Q-FVII, L305V/V158T/E296V/K337A-FVII, L305V/V158D/K337A/M298Q-FVII, L305VN1 58D/E296V/K337A-FVII, L305VN158D/E296V/M298Q/K337A-FVII, L305VN158T/E296WM298Q/K337A-FVII, S314Е/К316H-FVII, S314Е/К316Q-FVII, S314E/L305V-FVII, S314E/K337A-FVII, S314EN158D-FVII, S314E/E296V-FVII, S314E/M298Q-FVII, S314EN158T-FVII, K316H/L305V-FVII, K316H/K337A-FVII, K316HN158D-FVII, K316H/E296V-FVII, K316H/M298Q-FVII, K316HN158T-FVII, K316Q/L305V-FVII, K316Q/K337A-FVII, K316QN158D-FVII, K316Q/E296V-FVII, K316Q/M298Q-FVII, K316QN158T-FVII, S314E/L305V/K337A-FVII, S314E/L305VN158D-FVII, S314E/L305V/E296V-FVII, S314E/L305WM298Q-FVII, S314E/L305VN158T-FVII, S314E/L305V/K337A/V158T-FVII, S314E/L305V/K337A/M298Q-FVII, S314E/L305V/K337A/E296V-FVII, S314E/L305V/K337A/V158D-FVII, S314E/L305V/V158D/M298Q-FVII, S314E/L305V/V158D/E296V-FVII, S314E/L305V/V158T/M298Q-FVII, S314E/L305V/V158T/E296V-FVII, S314E/L305V/E296V/M298Q-FVII, S314E/L305VN158D/E296V/M298Q-FVII, S314E/L305VN158T/E296WM298Q-FVII, S314E/L305VN158T/K337A/M298Q-FVII, S314E/L305VN158T/E296V/K337A-FVII, S314E/L305VN158D/K337A/M298Q-FVII, S314E/L305VN158D/E296V/K337A-FVII, S314E/L305V/V158D/E296V/M298Q/K337A-FVII, S314E/L305V/V158T/E296V/M298Q/K337A-FVII, K316H/L305V/K337A-FVII, K316H/L305V/V158D-FVII, K316H/L305V/E296V-FVII, K316H/L305V/M298Q-FVII, K316H/L305VN158T-FVII, K316H/L305V/K337AN158T-FVII, K316H/L305WK337A/M298Q-FVII, K316H/L305WK337A/E296V-FVII, K316H/L305WK337A/V158D-FVII, K316H/L305VN158D/M298Q-FVII, K316H/L305VN158D/E296V-FVII, K316H/L305VN158T/M298Q-FVII, K316H/L305V/V158T/E296V-FVII, K316H/L305V/E296V/M298Q-FVII, K316H/L305V/V158D/E296V/M298Q-FVII, K316H/L305V/V158T/E296V/M298Q-FVII, K316H/L305VN158T/K337A/M298Q-FVII, K316H/L305VN158T/E296V/K337A-FVII, K316H/L305VN158D/K337A/M298Q-FVII, K316H/L305VN158D/E296V/K337A-FVII, K316H/L305V/V158D/E296V/M298Q/K337A-FVII, K316H/L305V/V158T/E296V/M298Q/K337A-FVII, K316Q/L305V/K337A-FVII, K316Q/L305V/V158D-FVII, K316Q/L305V/E296V-FVII, K316Q/L305WM298Q-FVII, K316Q/L305VN158T-FVII, K316Q/L305WK337AN 158T-FVII, K316Q/L305V/K337A/M298Q-FVII, K316Q/L305V/K337A/E296V-FVII, K316Q/L305V/K337AN158D-FVII, K316Q/L305VN158D/M298Q-FVII, K316Q/L305VN158D/E296V-FVII, K316Q/L305V/V158T/M298Q-FVII, K316Q/L305V/V158T/E296V-FVII, K316Q/L305V/E296V/M298Q-FVII, K316Q/L305VN 158D/E296WM298Q-FVII, K316Q/L305VN 158T/E296V/M298Q-FVII, K316Q/L305V/V158T/K337A/M298Q-FVII, K316Q/L305V/V158T/E296V/K337A-FVII, K316Q/L305V/V158D/K337A/M298Q-FVII, K316Q/L305V/V158D/E296V/K337A-FVII, K316Q/L305VN158D/E296V/M298Q/K337A-FVII, K316Q/L305V/V158T/E296V/M298Q/K337A-FVII, F374Y/K337A-FVII, F374YN158D-FVII, F374Y/E296V-FVII, F374Y/M298Q-FVII, F374YN158T-FVII, F374Y/S314E-FVII, F374Y/L305V-FVII, F374Y/L305V/K337A-FVII, F374Y/L305VN158D-FVII, F374Y/L305V/E296V-FVII, F374Y/L305V/M298Q-FVII, F374Y/L305VN158T-FVII, F374Y/L305V/S314E-FVII, F374Y/K337A/S314E-FVII, F374Y/K337A/V158T-FVII, F374Y/K337A/M298Q-FVII, F374Y/K337A/E296V-FVII, F374Y/K337AN158D-FVII, F374YN158D/S314E-FVII, F374YN158D/M298Q-FVII, F374YN158D/E296V-FVII, F374YN158T/S314E-FVII, F374Y/V158T/M298Q-FVII, F374Y/V158T/E296V-FVII, F374Y/E296V/S314E-FVII, F374Y/S314E/M298Q-FVII, F374Y/E296V/M298Q-FVII, F374Y/L305V/K337A/V158D-FVII, F374Y/L305V/K337A/E296V-FVII, F374Y/L305WK337A/M298Q-FVII, F374Y/L305WK337AN158T-FVII, F374Y/L305V/K337A/S314E-FVII, F374Y/L305V/V158D/E296V-FVII, F374Y/L305VN158D/M298Q-FVII, F374Y/L305VN158D/S314E-FVII, F374Y/L305V/E296V/M298Q-FVII, F374Y/L305V/E296VN158T-FVII, F374Y/L305V/E296V/S314E-FVII, F374Y/L305V/M298QN158T-FVII, F374Y/L305V/M298Q/S314E-FVII, F374Y/L305VN158T/S314E-FVII, F374Y/K337A/S314EN158T-FVII, F374Y/K337A/S314E/M298Q-FVII, F374Y/K337A/S314E/E296V-FVII, F374Y/K337A/S314EN158D-FVII, F374Y/K337AN158T/M298Q-FVII, F374Y/K337AN158T/E296V-FVII, F374Y/K337A/M298Q/E296V-FVII, F374Y/K337A/M298QN158D-FVII, F374Y/K337A/E296VN158D-FVII, F374YN158D/S314E/M298Q-FVII, F374YN158D/S314E/E296V-FVII, F374YN158D/M298Q/E296V-FVII, F374YN158T/S314E/E296V-FVII, F374Y/V158T/S314E/M298Q-FVII, F374Y/V158T/M298Q/E296V-FVII, F374Y/E296V/S314E/M298Q-FVII, F374Y/L305V/M298Q/K337A/S314E-FVII, F374Y/L305V/E296V/K337A/S314E-FVII, F374Y/E296V/M298Q/K337A/S314E-FVII, F374Y/L305V/E296V/M298Q/K337A-FVII, F374Y/L305V/E296V/M298Q/S314E-FVII, F374Y/V158D/E296V/M298Q/K337A-FVII, F374YN1 58D/E296V/M298Q/S314E-FVII, F374Y/L305VN158D/K337A/S314E-FVII, F374YN1 58D/M298Q/K337A/S314E-FVII, F374YN1 58D/E296V/K337A/S314E-FVII, F374Y/L305VN1158D/E296V/M298Q-FVII, F374Y/L305VN1158D/M298Q/K337A-FVII, F374Y/L305V/V158D/E296V/K337A-FVII, F374Y/L305V/V158D/M298Q/S314E-FVII, F374Y/L305VN1 58D/E296V/S314E-FVII, F374YN1 58T/E296V/M298Q/K337A-FVII, F374YN158T/E296V/M298Q/S314E-FVII, F374Y/L305VN158T/K337A/S314E-FVII, F374Y/V158T/M298Q/K337A/S314E-FVII, F374Y/V158T/E296V/K337A/S314E-FVII, F374Y/L305V/V158T/E296V/M298Q-FVII, F374Y/L305V/V158T/M298Q/K337A-FVII, F374Y/L305V/V158T/E296V/K337A-FVII, F374Y/L305V/V158T/M298Q/S314E-FVII, F374Y/L305VN1 58T/E296WS314E-FVII, F374Y/E296WM298Q/K337AN1 58T/S314E-FVII, F374Y/V158D/E296V/M298Q/K337A/S314E-FVII, F374Y/L305V/V158D/E296V/M298Q/S314E-FVII, F374Y/L305WE296WM298QN158T/S314E-FVII, F374Y/L305WE296WM298Q/K337AN158T-FVII, F374Y/L305V/E296V/K337AN158T/S314E-FVII, F374Y/L305V/M298Q/K337AN158T/S314E-FVII, F374Y/L305VN1158D/E296V/M298Q/K337A-FVII, F374Y/L305VN158D/E296V/K337A/S314E-FVII, F374Y/L305V/V158D/M298Q/K337A/S314E-FVII, F374Y/L305V/E296V/M298Q/K337A/V158T/S314E-FVII, F374Y/L305V/V158D/E296V/M298Q/K337A/S314E-FVII, S52A-Factor VII, S60A-Factor VII; и P11Q/K33E-FVII, T106N-FVII, K143N/N145T-FVII, V253N-FVII, R290N/A292T-FVII, G291N-FVII, R315NN317T-FVII, K143N/N145T/R315N/V137T-FVII; FVII, имеющего замены, добавления или делеции в аминокислотной последовательности от 233Thr до 240Asn, FVII, имеющего замены, добавления или делеции в аминокислотной последовательности от 304Arg до 329Cys, и FVII, имеющего замены, добавления или делеции в аминокислотной последовательности Ilе153-Arg223.
15. Конъюгат полипептида фактора VII по любому из пп.1-12, в котором полипептид фактора VII выбирают из группы, состоящей из M298Q-FVII, L305V/M298Q-FVII и фактора VIIa, в котором отсутствует область Gla.
16. Конъюгат полипептида фактора VII по любому из пп.1-15, в котором фактор VII-родственный полипептид имеет по меньшей мере 25%, предпочтительно по меньшей мере 50%, более предпочтительно по меньшей мере 75% и наиболее предпочтительно по меньшей мере 90% от удельной активности фактора VIIa дикого типа, который образуется в клетках того же типа, при тестировании в одном или более тестах: на свертывание, на протеолиз или связывание с ТФ, как показано в настоящем описании.
17. Конъюгат полипептида фактора VII по любому из пп.1-15, в котором фактор VII-родственные полипептиды имеют меньше, чем 25%, предпочтительно меньше, чем 10%, более предпочтительно меньше, чем 5% и наиболее предпочтительно меньше, чем 1% от удельной активности фактора VIIa дикого типа, который образуется в клетках того же типа, при тестировании в одном или более тестах: на свертывание, на протеолиз или связывание с ТФ, как показано в настоящем описании.
18. Конъюгат полипептида фактора VII по любому из пп.1-15, в котором указанный препарат имеет биодоступность, которая составляет по меньшей мере 110% от биологической доступности эталонного препарата, в частности, по меньшей мере 120%, по меньшей мере 130% или по меньшей мере 140% от биологической доступности эталонного препарата.
19. Конъюгат полипептида фактора VII по любому из пп.1-15, в котором указанный препарат имеет период полувыведения из сыворотки, который составляет по меньшей мере 125% от периода полувыведения эталонного препарата, в частности, по меньшей мере 150%, по меньшей мере 200% или по меньшей мере 250% от периода полувыведения эталонного препарата.
20. Способ получения конъюгата полипептида фактора VII по пп.1-19, включающий приведение в контакт полипептида фактора VII, содержащего аспарагин-связанные и/или серин-связанные олигосахаридные цепи, содержащие группу сиаловой кислоты или группу галактозы, причем по меньшей мере одна из этих олигосахаридных цепей ковалентно связана с по меньшей мере одной полимерной группой, представляющей собой полиэтиленгликоль, имеющий молекулярную массу в диапазоне приблизительно 300-100000 Да.
21. Фармацевтическая композиция для лечения фактор VII-реактивного синдрома, включающая конъюгат полипептида фактора VII по любому из пп.1-19 и фармацевтически приемлемый носитель или адъювант.
22. Применение конъюгата полипептида фактора VII по любому из пп.1-19, для получения лекарственного средства, предназначенного для лечения фактор VII-реактивного синдрома.
| 0 |
|
SU158935A1 | |
| 0 |
|
SU202764A1 | |
| ВОДОРАСТВОРИМЫЙ ГИДРОЛИТИЧЕСКИ СТАБИЛЬНЫЙ АКТИВИРОВАННЫЙ ПОЛИМЕР, СПОСОБ ПОЛУЧЕНИЯ АКТИВИРОВАННОГО ПОЛИЭТИЛЕНГЛИКОЛЯ (ВАРИАНТЫ), БИОЛОГИЧЕСКИ АКТИВНЫЙ КОНЪЮГАТ | 1994 |
|
RU2176253C2 |
Авторы
Даты
2009-07-27—Публикация
2003-06-20—Подача