Перекрестная ссылка на родственные заявки
В этой заявке испрашивается приоритет по дате подачи предварительной заявки на патент США 62/363284, поданной 17 июля 2016 года, полное содержание которой включено в настоящий документ в качестве ссылки.
Предшествующий уровень техники
Плектрантус ароматный (Plectranthus amboinicus) (также известный ранее или альтернативно как Coleus amboinicus Lour., Coleus aromaticus Benth., Coleus aromaticus auct., Plectranthus aromaticus Roxb., Plectranthus aromaticus Benth. и Plectranthus amboinicus (Lour.) Spreng.) представляет собой многолетнее лекарственное растение семейства Lamiaceae (также известного как Labiatae), произрастающее в Южной и Восточной Африке. Растение Plectranthus amboinicus также известно как пачули, кубинский орегано, индийский огуречник, индийская мята, мексиканская мята, мексиканский орегано, огуречник (country borage) и испанский тимьян.
Центелла азиатская (Centella asiatica) (также известная ранее или альтернативно как Centella asiatica Urban, Centella asiatica (L.) Urban, Hydrocotyle asiatica L. и Trisanthus cochinchinensis Lour.) представляет собой многолетнее лекарственное растение семейства Mackinlayaceae или подсемейства Mackinlayoideae семьи Apiaceae (также известной как Umbelliferae), произрастающее в Азии, Африке и Южной Америке. Растение Centella asiatica также известно как европейская водяная мята, готу кола, кoлa, щитолистник, индийский щитолистник, болотный щитолистник, pennyweed, индийский женьшень, «конское копыто», пегага, мандукапарни, тигриная трава, «широкий лист», или тоно. Экстракты Centella asiatica обычно содержат два основных соединения: азиатикозид и мадекассовую кислоту.
Краткое описание изобретения
Настоящее изобретение основано, по меньшей мере отчасти, на превосходных терапевтических эффектах состава для местного применения, содержащего комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica, как описано в настоящем документе, которые содержат салвигенин и/или азиатикозид, в отношении стимулирования заживления ран, например, у больных сахарным диабетом с диабетической язвой стопы. Например, состав для местного применения успешно улучшал заживление язвы стопы у пациентов с диабетом, и эффективность была намного выше, чем Aquacel®, положительного контроля. Местное нанесение состава для местного применения также показало ограниченное системное распределение по меньшей мере активных ингредиентов, содержащихся в нем (салвигенин и/или азиатикозид) у больных DFU и, как было установлено, является безопасным для пациентов.
Таким образом, в настоящем изобретении предлагается состав для местного применения, содержащий: (i) активный агент, содержащий салвигенин в количестве около 0,0001-0,5% (масса/масса) (например, около 0,0001-0,1 мас.%) и азиатикозид в количестве около 0,05-5% (масса/масса) (например, около 0,05-1 мас.%); (ii) увеличивающий вязкость агент в количестве около 1,0-10% (мас.%); (iii) мазевую основу в количестве около 5-30% (масса/масса); (iv) антимикробный консервант в количестве около 0,005-0,2% (масса/масса); и (v) эмульгирующий агент в количестве около 0,5-10% (масса/масса).
В некоторых вариантах осуществления активный агент представляет собой экстракт Plectranthus amboinicus (PA), экстракт Centella asiatica (CA) или комбинацию экстрактов PA и СА, которые (по отдельности или в комбинации) содержат салвигенин и азиатикозид.
В одном варианте осуществления активный агент представляет собой комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica. Активный агент может составлять около 0,1-30% (масса/масса) и содержит по меньшей мере салвигенин и азиатикозид. В некоторых случаях состав для местного применения может содержать салвигенин в диапазоне от около 0,0001% до 0,5% (масса/масса), например, от около 0,0001% до 0,1% (масса/масса). В некоторых случаях состав для местного применения может содержать салвигенин в диапазоне от около 0,0001% до 0,1% (масса/масса) и азиатикозид в диапазоне от около 0,05% до 1% (масса/масса). В любом из составов для местного применения, описанных в настоящем документе, активный агент, содержащийся в нем, может дополнительно содержать цирсимаритин, мадекассосид или их комбинацию.
Содержание экстракта Plectranthus amboinicus в составе для местного применения может составлять около 0,1-5% (масса/масса) или около 0,1-1% (масса/масса). В некоторых вариантах осуществления экстракт Plectranthus amboinicus содержит флавоноиды, эфирные масла, фенольные соединения, терпеноиды или их комбинацию.
Экстракт Plectranthus amboinicus может быть получен путем приведения в контакт целого растения Plectranthus amboinicus или его части с растворителем, имеющим индекс полярности ниже 7 (например, менее 5), с получением раствора и сушки раствора с получением экстракта Plectranthus amboinicus. В конкретном варианте осуществления экстракт Plectranthus amboinicus получали с помощью способа, включающего: (i) приведение в контакт целого растения Plectranthus amboinicus или его части со спиртом (например, этанолом) с получением неочищенного экстракта Plectranthus amboinicus; (ii) приведение в контакт неочищенного экстракта с неионной адсорбирующей смолой; (iii) элюирование неионной адсорбирующей смолы растворителем, имеющим индекс полярности ниже 7 (например, ниже 5) с получением раствора; и (iv) сушку раствора с получением экстракта Plectranthus amboinicus.
В качестве альтернативы или дополнительно, экстракт Centella asiatica может содержать азиатикозид, мадекассосид или и то и другое. В некоторых вариантах осуществления содержание экстракта Centella asiatica в составе для местного применения составляет около 0,1-20% (масса/масса) или около 0,5-5% (масса/масса).
В некоторых вариантах осуществления соотношение между экстрактом Plectranthus amboinicus и экстрактом Centella asiatica составляет от около 1:10 до около 10:1, например, от около 1:5 до около 5:1.
Состав для местного применения может содержать увеличивающий вязкость агент в количестве около 1,0-10% (масса/масса). Примеры увеличивающих вязкость агентов включают, но без ограничения, цетостеариловый спирт, холестерин, стеариловый спирт, хлоркрезол, белый воск, стеариновую кислоту, цетиловый спирт или их комбинацию.
Состав для местного применения может содержать мазевую основу в количестве около 5-30% (масса/масса) (например, 10-30 мас.%). В некоторых случаях мазевая основа может представлять собой кремовую основу. Примеры мазевой основы включают, но без ограничения, одно или несколько соединений петролатума (например, жидкий петролатум, белый петролатум).
Содержание антимикробного консерванта в составе для местного применения, описанном в настоящем документе, может составлять около 0,005-0,2% (масса/масса) (например, 0,01-0,2 мас.%). Он может представлять собой одно или несколько парабеновых соединений (например, метилпарабен и/или пропилпарабен).
Содержание эмульгирующего агента (например, Span® 60 и/или Tween® 60) в составе для местного применения может составлять около 0,5-10% (масса/масса) (например, 0,5-6 мас.%).
В некоторых примерах состав для местного применения, описанный в настоящем документе, может содержать мазевую основу в количестве около 10-30% (масса/масса), антимикробный консервант в количестве около 0,01-0,2% (масса/масса) и эмульгирующий агент в количестве около 0,5-6% (масса/масса).
Любой из составов для местного применения, описанных в настоящем документе, может, кроме того, содержать один или несколько растворителей, например, пропиленгликоль.
В одном примере состав для местного применения, описанный в настоящем документе, содержит комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica в количестве около 0,1-30% (масса/масса), цетостеариловый спирт в количестве около 1,0-10% (масса/масса) (например, около 2-8% или около 3-7%), комбинацию белого петролатума и жидкого петролатума в общем количестве около 5-30% (масса/масса) (например, около 5-25% или около 5-20%), комбинацию метилпарабена и пропилпарабена в общем количестве около 0,005-0,2% (масса/масса), и комбинацию моностеарата сорбитана и полисорбата 60 в общем количестве около 0,5-10% (масса/масса) (например, 0,5-8% или 0,5-6%). Такой состав для местного применения может, кроме того, содержать пропиленгликоль в количестве около 2-20% (масса/масса) (например, 2-10% или 4-15%).
В другом аспекте настоящее изобретение обеспечивает способ для заживления ран, включающий нанесение состава для местного применения, раскрытого в настоящем документе, на участок раны субъекта, нуждающегося в этом. В одном варианте осуществления состав для местного применения можно наносить по меньшей мере один раз в день, например, два раза в день.
В одном примере субъектом, подлежащим лечению, может являться пациент-человек с диабетом, страдающий диабетической язвой стопы. Например, пациент-человек с диабетом может иметь диабет типа I или типа II. В другом примере субъектом является пациент-человек, имеющий открытую рану, например, ссадину, резаную рану, глубокий порез, прокол или разрыв. В другом примере субъектом является пациент-человек, имеющий хроническую рану, которая может представлять собой хирургическую рану, травматическую рану, пролежневую язву, венозную язву, диабетическую язву или рану, вызванную карциномой, ожогом, атопическим дерматитом, пролежнем. В некоторых примерах субъектом является пациент-человек, имеющий акне.
Объем настоящего изобретения также охватывает (i) состав для местного применения, описанный в настоящем документе, предназначенный для стимулирования заживления ран, и (ii) использование экстракта Plectranthus amboinicus, экстракта Centella asiatica или их комбинации в изготовлении лекарственного средства, предназначенного для стимулирования заживления ран, при этом экстракт Plectranthus amboinicus, экстракт Centella asiatica или их комбинацию включают в состав для местного применения, как описано в настоящем документе.
Детали одного или нескольких вариантов осуществления изобретения приведены ниже в описании. Другие особенности и преимущества настоящего изобретения будут очевидны из нижеследующих чертежей и подробного описания нескольких вариантов осуществления, а также из прилагаемой формулы изобретения.
Краткое описание чертежей
На фигуре 1 представлена блок-схема, показывающая иллюстративный способ получения экстрактов Plectranthus amboinicus.
На фигуре 2 представлена блок-схема, показывающая иллюстративный способ получения экстрактов Centella asiatica.
На фигурах 3А и 3В представлены диаграммы, показывающие эффекты экстракта Plectranthus amboinicus (PA) и экстракта Centella asiatica (CA) на пролиферацию эндотелиальных клеток по данным анализа MTT (фигура 3A) и на миграцию эндотелиальных клеток по данным анализа методом зарастания царапины (фигура 3B).
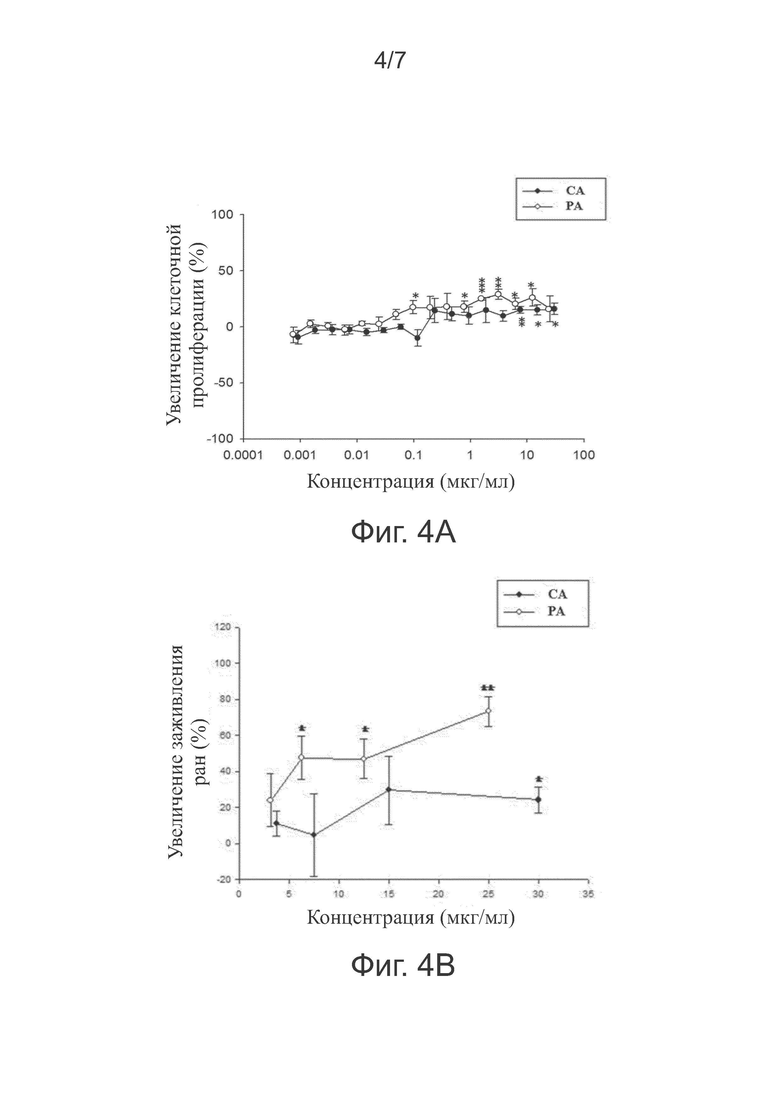
На фигурах 4А и 4В представлены диаграммы, показывающие эффект экстракта Plectranthus amboinicus (PA) и Centella asiatica (CA) на клеточную пролиферацию кератиноцитов по данным анализа с использованием SRB (фигура 4A), и на клеточную миграцию кератиноцитов по данным анализа методом зарастания царапины (фигура 4B).
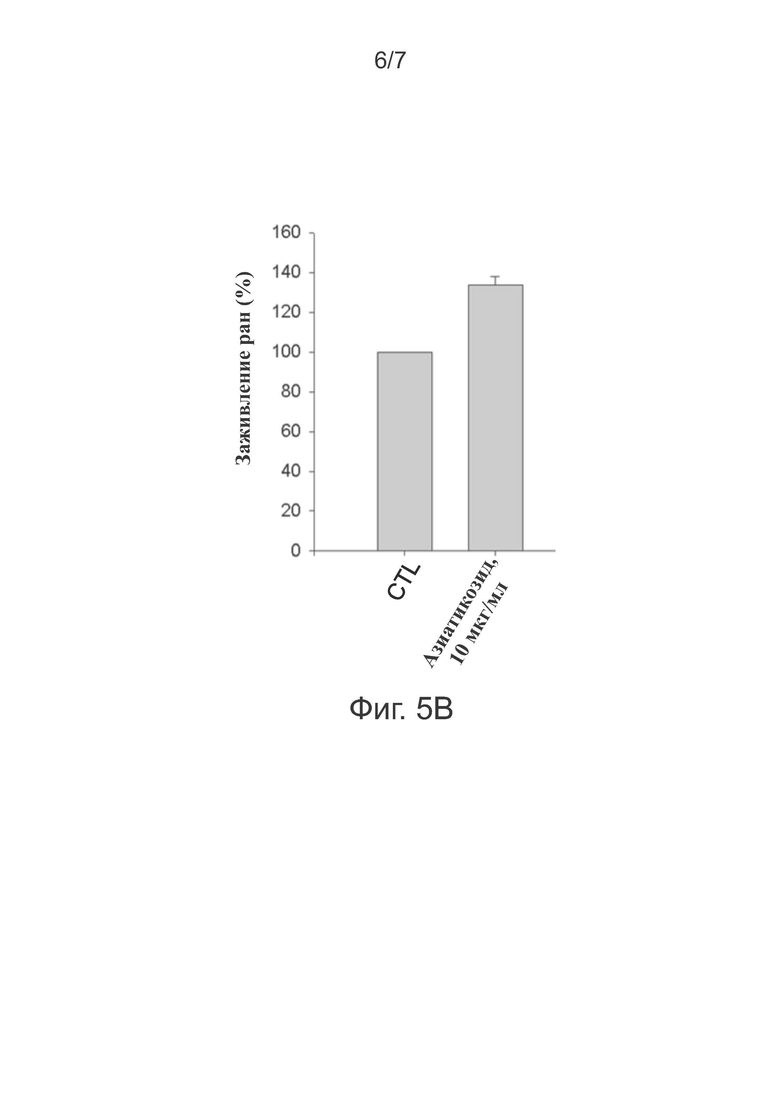
На фигурах 5А и 5В представлена диаграмма, показывающая эффект салвигенина в отношении стимуляции заживления ран в in vitro анализе формирования капиллярной трубочки и диаграмма, показывающая эффект азиатикозида в содействии миграции кератиноцитов.
На фигуре 6 представлена диаграмма, показывающая эффект экстракта Plectranthus amboinicus (PA) и экстракта Centella asiatica (CA) на нормальное заживление ран в животной модели.
Подробное описание изобретения
Язвы на ногах являются распространенным осложнением, связанным с диабетом, в результате разрушения кожной ткани и обнажения нижних слоев. Все диабетики подвержены риску развития язв на ногах. Приблизительно у 15-20% диабетиков будут развиваться язвы на ногах. Среди них приблизительно 33% пациентов нуждаются в ампутации.
Доступные в настоящее время способы лечения диабетических язв на стопах (DFU) включают ношение защитных средств, таких как обувь для диабетиков, гипсовая повязка, фиксаторы для стоп, компрессионные бинты и вкладные стельки для предотвращения образования мозолей и костных мозолей. Такие медицинские средства могут быть дорогостоящими и часто доставлять неудобства в повседневной жизни пациентов. Альтернативно, хирургические процедуры могут быть выполнены для удаления язв на стопе с проведением дебридмента. На сегодняшний день Regranex® является единственным лекарственным средством, одобренным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения DFU. В июне 2008 года FDA объявило о новом изменении маркировки Regranex® для указания того, что в группе, подвергнутой воздействию Regranex®, риск смертности от рака увеличился в пять раз.
Настоящее раскрытие основано, по меньшей мере частично, на разработке состава для местного применения, содержащего комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica, который показал значительно более высокую эффективность в отношении стимулирования заживления ран и низкие побочные эффекты у пациентов с DFU. Этот состав для местного применения имеет кремовую основу и содержит по меньшей мере около 0,0001-0,5% (масса/масса) салвигенина в качестве активного ингредиента. В некоторых вариантах осуществления состав для местного применения может, кроме того, содержать около 0,05-5% (масса/масса) азиатикозида в качестве дополнительного активного ингредиента. Состав для местного применения, кроме того, содержит около 1,0-10% (масса/масса) увеличивающего вязкость агента (агентов), около 5-30% (масса/масса) мазевой основы (основ) (например, кремовую основу), около 0,005-0,2% (масса/масса) антимикробного консерванта (консервантов); и около 0,5-10% (масса/масса) эмульгирующего агента (агентов). Все компоненты могут быть растворены в одном или нескольких подходящих растворителях, таких как пропиленгликоль и вода.
Фармакокинетические исследования кремового состава для местного применения, указанного выше, показали его безопасность у пациентов с DFU. Что еще более важно, местное нанесение состава в виде крема привело к очень низкому системному распределению по меньшей мере двух активных ингредиентов, салвигенина и азиатикозида, после местного нанесения на участки раны пациентов и, как было обнаружено, является безопасным у пациентов, получающих локальное лечение составом для местного применения.
Кроме того, клиническое исследование III фазы проводили для оценки эффективности состава для местного применения на кремовой основе для лечения хронической диабетической язвы стопы. Неожиданно, мазь для местного применения показала значительно более высокую эффективность в отношении стимулирования закрытия язв у пациентов с диабетом, особенно у тех, у кого имелись большие язвы или подошвенные язвы; в сравнении с контрольным продуктом Aquacel®.
Таким образом, в настоящем документе предлагаются составы для местного применения, которые содержат один или оба экстракта Plectranthus amboinicus и Centella asiatica, и способы их применения для стимулирования заживления раны у субъекта, нуждающегося в лечении.
Составы для местного применения
В настоящем изобретении предлагается состав для местного применения для стимулирования заживления ран (например, заживления ран для пациентов с диабетом), содержащий активный агент, который может представлять собой экстракт Plectranthus amboinicus, содержащий салвигенин, экстракт Centella asiatica, содержащий азиатикозид, или комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica. Состав для местного применения, описанный в настоящем документе, может содержать салвигенин в количестве от около 0,0001% до около 0,5% (масса/масса) и необязательно азиатикозид, который может присутствовать в количестве от около 0,05% до около 5% (масса/масса). В некоторых вариантах осуществления состав для местного применения содержит экстракт Plectranthus amboinicus, экстракт Centella asiatica или оба в количестве около 0,1-30% (масса/масса).
Состав для местного применения, кроме того, содержит один или несколько носителей или вспомогательных веществ, включая один или несколько увеличивающих вязкость агентов (например, около 1,0-10%), одну или несколько мазевых основ (например, одну или несколько кремовых основ) в количестве около 5-30%, один или несколько антимикробных консервантов (например, около 0,005-0,2 мас.%), один или несколько эмульгирующих агентов (около 0,5-10 мас.%), или их комбинацию. Эти компоненты могут быть растворены или распределены в подходящем растворителе.
(i) Активные агенты
Активный агент в составе для местного применения, описанном в настоящем документе, содержит салвигенин и необязательно азиатикозид. В некоторых вариантах осуществления активный агент может представлять собой либо экстракт Plectranthus amboinicus, который содержит салвигенин, либо экстракт Centella asiatica, который содержит только азиатикозид, или их комбинацию. Концентрация активного агента в составе для местного применения может составлять около 0,1-30% (масса/масса). Например, содержание активного агента может составлять около 0,1-5%, 0,5-3%, 1-2%, 1-3%, 2-10%, 5-10%, 5-15%, 10-15%, 15-20%, 10-20%, 20-25%, 15-30%, 20-30%, 10-30% или 25-30% (масса/масса) состава для местного применения. Концентрация активного агента в составе для местного применения, описанном в настоящем документе, относится к проценту общей массы активного агента в сухой форме от общей массы состава для местного применения в целом.
Состав для местного применения, описанный в настоящем документе, может содержать около 0,0001-0,5% (масса/масса) салвигенина, например, около 0,001-0,5% (масса/масса), около 0,001-0,3% (масса/масса), 0,001-0,2% (масса/масса), около 0,01-0,1% (масса/масса), около 0,002-0,5% (масса/масса), около 0,002-0,4% (масса/масса), около 0,002-0,3% (масса/масса), около 0,001-0,1% (масса/масса), около 0,005-0,01% (масса/масса), около 0,01-0,5% (масса/масса), около 0,02-0,5% (масса/масса) и около 0,1-0,5% (масса/масса). Альтернативно или дополнительно, состав для местного применения, описанный в настоящем документе, может содержать азиатикозид в количестве от около 0,05% до около 5% (масса/масса), например, около 0,1-2,5% (масса/масса), около 0,1-2% (масса/масса), около 0,1-1% (масса/масса), около 0,25-2,5% (масса/масса), около 0,5-5% (масса/масса), около 0,5-2,5% (масса/масса) или около 0,5-1% (масса/масса).
Используемый в настоящем документе термин «около» относится к строгой числовой границе для указанных параметров (включая как верхний, так и нижний пределы). Специалист в данной области поймет значение «около» исходя из конкретного контекста. В некоторых случаях термин «около» относится к конкретному значению +/- 5% (например, +/- 3% или +/- 2%).
В одном варианте осуществления активный агент в составе для местного применения представляет собой комбинацию экстракта Plectranthus amboinicus, который содержит салвигенин, и экстракта Centella asiatica, который содержит азиатикозид. Соотношение между Plectranthus amboinicus и экстрактом Centella asiatica может составлять от около 1:10 до 10:1. Например, соотношение между экстрактом Plectranthus amboinicus и экстрактом Centella asiatica в составе для местного применения может составлять около 1:10 - 1:1, около 1:1 - 10:1, около 1:10 - 1:5, около 1:5 - 1:1, около 10:1 - 5:1, около 5:1 - 1:1, около 1:10 - 1:4, около 1:4 - 1:1, около 10:1 - 4:1 или около 4:1 - 1:1.
Экстракт Plectranthus amboinicus относится к экстракту, полученному из растения Plectranthus amboinicus с использованием одного или нескольких подходящих растворителей. В некоторых случаях по меньшей мере один из растворителей, используемых для получения экстракта, имеет индекс полярности ниже 7 (например, ниже 5). См. таблицу 1 ниже. Используемый в настоящем документе растворитель относится к веществу или смеси веществ, которые растворяют другое вещество с образованием раствора. Описанный в настоящем документе экстракт Plectranthus amboinicus может быть получен с использованием одного растворителя. Растворитель, используемый на каждой стадии экстракции для получения экстрактов, описанных в настоящем документе (включая оба экстракта Plectranthus amboinicus и Centella asiatica), может представлять собой один растворитель. Альтернативно, это может быть смесь двух или более растворителей.
Экстракт Plectranthus amboinicus, описанный в настоящем документе, может содержать терпеноиды (например, монотерпеноиды, дитерпеноиды, тритерпеноиды и/или сесквитерпеноиды), флавоноиды, фенольные соединения, эфирные масла или их комбинации. Экстракт Plectranthus amboinicus может присутствовать в составе для местного применения при концентрации около 0,1-5% (масса/масса). Например, состав для местного применения может содержать около 0,1-0,5%, 0,5-1%, 1-1,5%, 1,5-2%, 2-2,5%, 2,5-3%, 3-3,5%, 3,5-4%, 4-4,5% или 4,5-5% (масса/масса) экстракта Plectranthus amboinicus. Альтернативно, состав для местного применения может содержать около 0,1-1%, 0,1-2%, 0,1-3%, 0,1-4% или 0,1-5% (масса/масса) экстракта Plectranthus amboinicus. В конкретном варианте осуществления состав для местного применения содержит около 0,1-1% или 0,1-0,5% экстракта Plectranthus amboinicus.
Экстракт Plectranthus Amboinicus, описанный в настоящем документе, может быть получен путем экстракции целого растения Plectranthus amboinicus или его части с помощью одного или нескольких подходящих растворителей с получением раствора и последующей сушки раствора с получением экстракта Plectranthus amboinicus. Поскольку экстракт Plectranthus Amboinicus содержит флавоноиды, терпеноиды (например, монотерпеноиды, дитерпеноиды, тритерпеноиды и/или сесквитерпеноиды), фенольные соединения или эфирные масла, которые являются неполярными молекулами, по меньшей мере один из экстрагирующих растворителей может иметь относительно низкую полярность (например, иметь индекс полярности ниже 7) для облегчения растворения неполярных молекул. Экстракцию можно осуществлять либо путем приведения в контакт материала Plectranthus Amboinicus непосредственно с подходящим растворителем, либо путем элюирования активных компонентов Plectranthus amboinicus из смол, на которые прикрепляются активные компоненты.
В приведенной ниже таблице 1 перечислены обычно используемые растворители и их индекс полярности (индекс полярности Снайдера):
Таблица 1. Иллюстративные растворители и их индексы полярности
В некоторых примерах растворитель, имеющий индекс полярности ниже 7, может быть использован для экстракции активных компонентов из Plectranthus Amboinicus с получением экстракта Plectranthus amboinicus. Таким растворителем может являться этилацетат, метилацетат, пропанол, бутанол или хлороформ. Альтернативно, растворитель может представлять собой смесь одного или нескольких растворителей, имеющих различный индекс полярности. Примеры включают, но без ограничения, смесь этанола и этилацетата, этилацетата и бутанола, этанола и пропанола, метилацетата и бутанола.
В некоторых вариантах осуществления экстракт Plectranthus Amboinicus может быть получен с помощью способа, включающего использование одного растворителя, такого как растворитель, имеющий индекс полярности ниже 7 (например, < около 6,5, < около 6,0; < около 5.5, < около 5,0, < 4,9, < 4,8, < 4,7, < 4,6 или < 4,5). Примеры включают, но без ограничения, метанол, этанол, ацетон, этилацетат, бутанол, дихлорметан или их комбинацию.
Иллюстративный способ получения экстракта Plectranthus Amboinicus представлен ниже. См. также фигуру 1.
Материалы Plectranthus amboinicus, которые могут представлять собой целое растение Plectranthus amboinicus или его часть (например, листья), могут быть получены с помощью стандартной методики. Материал Plectranthus Amboinicus может представлять собой свежее растение или его часть. Альтернативно, материал Plectranthus Amboinicus может находиться в сухом виде. Растение Plectranthus Amboinicus может быть необязательно высушено с образованием порошков, которые можно использовать в качестве материала Plectranthus Amboinicus для получения экстракта Plectranthus amboinicus.
Любой из описанных в настоящем документе материалов Plectranthus Amboinicus может быть экстрагирован один или несколько раз подходящим растворителем с получением неочищенного экстракта. Растворителем, используемым для получения неочищенного экстракта, может являться высокополярный растворитель, например, имеющий индекс полярности выше 5 и предпочтительно ниже 7 (например, > 5,2; > 5,5, > 5,8, > 6 или выше и предпочтительно ниже 7). Примеры включают, но без ограничения, этанол, ацетон, метанол, воду или их комбинацию. Если необходимо, неочищенный экстракт может быть концентрирован обычным способом с получением концентрированного неочищенного экстракта.
Затем неочищенный экстракт может быть приведен в контакт с подходящей смолой (например, неионной абсорбирующей смолой) в подходящих условиях, которые обеспечивают связывание активных компонентов в неочищенном экстракте на смоле. Примеры смол для использования при получении экстракта Plectranthus Amboinicus включают, но без ограничения, DIAION® HP20, DIAION® HP20SS, Sepabeads® SP207, Amberlite™ XAD-2 или Amberlite™ XAD-4.
После этого смолу промывают один или несколько раз и элюируют подходящим растворителем, например, растворителем, имеющим индекс полярности ниже 7, с получением экстракта Plectranthus Amboinicus, который затем подвергают сушке обычным способом (например, сушка вымораживанием, распылительная сушка или сушка концентрированием) с получением сухого экстракта Plectranthus Amboinicus, находящегося в полутвердой или пастообразной форме.
В некоторых вариантах осуществления стадия абсорбции на смоле может быть выполнена путем смешивания неочищенного экстракта со смолой в контейнере. В других вариантах осуществления стадия отделения от смолы может быть выполнена на хроматографической колонке.
Экстракт Centella Asiatica, описанный в настоящем документе, относится к экстракту, полученному из целых растений Centella asiatica или их частей. Экстракт Centella Asiatica может содержать азиатиказид, мадекассоновую кислоту или их комбинацию.
Экстракт Centella Asiatica может присутствовать в составе для местного применения при концентрации около 0,1-20% (масса/масса). Например, состав для местного применения может содержать около 0,1-0,5%, 0,5-1%, 1-1,5%, 1,5-2%, 2-2,5%, 2,5-3%, 3-3,5%, 3,5-4%, 4-4,5%, 4,5-5%, 5-5,5%, 5,5-6%, 6-6,5%, 6,5-7%, 7-7,5%, 7,5-8%, 8-8,5%, 8,5-9%, 9-9,5%, 9,5-10%, 10-10,5%, 10,5-11%, 11-11,5%, 11,5-12%, 12-12,5%, 12,5-13%, 13-13,5%, 13,5-14%, 14-14,5%, 14,5-15%, 15-15,5%, 15,5-16%, 16-16,5%, 16,5-17%, 17-17,5%, 17,5-18%, 18-18,5%, 18,5-19%, 19-19,5% или 19,5-20% (масса/масса) экстракта Centella asiatica. Альтернативно, состав для местного применения может содержать около 0,1-5%, 0,1-10%, 0,1-15%, 0,1-20%, 0,5-5%, 0,5-10%, 0,5-15% или 0,5-20% (масса/масса) экстракта Centella asiatica. В конкретных примерах состав для местного применения может содержать около 0,1, 0,2, 0,3, 0,4, 0.5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 процентов (масса/масса) экстракта Centella asiatica.
Экстракт Centella Asiatica может быть получен общепринятым способом, например, описанным в патентах США №№5834437, 6417349, 6475536 и 6267996, CN 1313124, CN 1089497 и CN 1194154.
Материалы Centella asiatica могут быть получены с использованием стандартной практики. Такими материалами могут быть свежие растения Centella Asiatica или их части, или высушенное растение Centella asiatica. Материалы Centella Asiatica экстрагируют подходящим растворителем, таким как вода, этанол или их смесь с получением неочищенного экстракта. Неочищенный экстракт, который может быть необязательно концентрирован, либо смешивают с подходящей смолой, либо наносят на колонку, упакованную смолой. После промывания один или несколько раз смолу элюируют подходящим растворителем. Полученный в результате элюент концентрируют с образованием пасты, которую подвергают сушке обычным способом, например, в вакууме с получением порошков экстракта Centella Asiatica. При необходимости порошок Centella Asiatica может быть измельчен через сито (например, №100 меш). См. также фигуру 2.
В одном примере экстракт Plectranthus Amboinicus получают следующим образом. Надземную часть Plectranthus Amboinicus (около 1,5 г), включая листья и/или стебли, собирают и экстрагируют растворителем, имеющим полярность менее 7 (например, метанол, этанол, ацетон, этилацетат, бутанол, дихлорметан или их комбинация) при комнатной температуре в течение от 30 минут до 6 часов. Альтернативно, этот процесс экстракции можно проводить при температуре около 50-80°С. Полученный неочищенный экстракт непосредственно наносят на колонку с неионной адсорбирующей смолой и элюируют растворителем, имеющим полярность менее 6 (например, этанол, этилацетат, бутанол, дихлорметан, гексан, толуол или их комбинация). Элюированные компоненты собирают и очищают путем экстракции растворителем, имеющим полярность менее 6 (например, описанные в настоящем документе). Полученный фильтрат собирают с получением экстракта РА.
Экстракт Centella Asiatica может быть получен таким же или подобным способом, как описано выше. Экстракт РА и/или экстракт СА можно концентрировать с использованием роторного испарителя с пониженным давлением.
(ii) Носители и вспомогательные вещества
Состав для местного применения, кроме того, содержит один или несколько носителей и вспомогательных веществ, включая увеличивающие вязкость агенты, мазевые основы (например, кремовые основы), антимикробные консерванты, эмульгирующие агенты и/или растворители.
«Увеличивающий вязкость агент» представляет собой агент, который используют для загущения состава. Примеры увеличивающих вязкость агентов включают, например, цетостеариловый спирт, холестерин, стеариловый спирт, хлоркрезол, белый воск, стеариновую кислоту, цетиловый спирт или их комбинацию. Увеличивающий вязкость агент может присутствовать в составе для местного применения при концентрации около 1,0-10% (масса/масса). Например, состав для местного применения может содержать около 1-1,5%, 1,5-2%, 2-2,5%, 2,5-3%, 3-3,5%, 3,5-4%, 4-4,5%, 4,5-5%, 5-5,5%, 5,5-6%, 6-6,5%, 6,5-7%, 7-7,5%, 7,5-8%, 8-8,5%, 8,5-9%, 9-9,5% или 9.5-10% (масса/масса) увеличивающего вязкость агента. Альтернативно, состав для местного применения может содержать около 1-5%, 2,5-7,5% или 5-10% увеличивающего вязкость агента.
«Мазевая основа» может представлять собой любой полутвердый препарат или носитель, в который может быть включен активный агент. Иллюстративные мазевые основы включают, но без ограничения, жировые мазевые основы (например, белый петролатум или белая мазь), абсорбционные мазевые основы (например, гидрофильный петролатум, безводный ланолин, Aquabase™, Aquaphor® и Polysorb®), мазевые основы на основе эмульсии вода/масло (например, холодный крем, водный ланолин, мазь с розовой водой, Hydrocream™, Eucerin® и Nivea®), мазевые основы на основе эмульсии масло/вода (например, гидрофильные мази, Dermabase™, Velvachol® и Unibase®), и смешиваемые с водой мазевые основы (например, мазь на основе полиэтиленгликоля (PEG) и Polybase™). Мазевые основы могут быть фармакологически инертными, но могут захватывать воду с образованием смягчающей защитной пленки. В конкретном варианте осуществления мазевой основой может быть любое соединение петролатума (например, петролатум, белый петролатум, белый мягкий парафин, жидкий петролатум, жидкий парафин). В другом конкретном варианте осуществления мазевой основой является белый петролатум (CAS номер 8009-03-8). Мазевая основа может присутствовать в составе для местного применения при концентрации около 5-30% (масса/масса), например, 10-30% (масса/масса). Например, состав для местного применения может содержать около 5-25%, 5-20%, 5-15%, 5-15%, 10-15%, 15-20%, 20-25% или 25-30% (масса/масса) мазевой основы. В частности, состав для местного применения может содержать около 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 (масса/масса) мазевой основы.
В некоторых вариантах осуществления «мазевая основа», описанная в настоящем документе, содержит менее чем 20% воды и летучих веществ, и более чем 50% углеводородов, восков или полиолов в качестве носителя.
В некоторых вариантах осуществления «мазевая основа», описанная в настоящем документе, представляет собой «кремовую основу», которая содержит более чем 20% воды и летучих веществ и/или обычно содержит менее чем 50% углеводородов, восков или полиолов в качестве носителя для лекарственной субстанции. Кремовая основа может представлять собой многофазный препарат, содержащий липофильную фазу и водную фазу. В некоторых случаях кремовая основа представляет собой липофильную кремовую основу, которая содержит липофильную фазу в качестве непрерывной фазы. Такая кремовая основа обычно содержит эмульгирующие агенты типа вода-в-масле, такие как спирты шерстяного жира, сложные эфиры сорбитана и моноглицериды. В других случаях кремовая основа представляет собой гидрофильную кремовую основу, которая имеет водную фазу в качестве непрерывной фазы. Такая кремовая основа обычно содержит эмульгирующие агенты типа масло-в-воде, такие как натриевые или троламиновые мыла, сульфатированные жирные спирты, полисорбаты и полиоксильные жирные кислоты и сложные эфиры жирных спиртов, которые могут присутствовать в комбинации с эмульгирующими агентами типа вода-в-масле, при необходимости.
«Антимикробный консервант» может представлять собой любое соединение, способное разрушать микробы, предотвращать размножение или рост микробов или предотвращать патогенное действие микробов. Примеры антимикробных консервантов включают, но без ограничения, соединение парабенов (сложный эфир парагидроксибензойной кислоты; например, парабен, метилпарабен, этилпарабен, пропилпарабен, бутилпарабен, гептилпарабен, бензилпарабен, изобутилпарабен, изопропилпарабен, бензилпарабен или их натриевые соли), бензалкония хлорид, бензетония хлорид, бензиловый спирт, борную кислоту, бронопол, цетримид, цетилпиридиния хлорид, хлоргексидин, хлорбутанол, хлоркрезол, хлорксиленол, крезол, этиловый спирт, глицерин, гексетидин, имидмочевину, фенол, феноксиэтанол, фенилэтиловый спирт, нитрат фенилртути, пропиленгликоль и тимеросал. Антимикробный консервант может присутствовать в составе для местного применения при концентрации около 0,005-0,2%, например, около 0,01-0,2% (масса/масса). Например, состав для местного применения может содержать около 0,005-0,01%, 0,01-0,05%, 0,05-0,1%, 0,1-0,15% или 0,15-0,2% (масса/масса) антимикробного консерванта. В частности, состав для местного применения может содержать около 0,005, 0,006, 0,007, 0,008, 0,009, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,1, 0,11, 0,12, 0,13, 0,14, 0,15, 0,16, 0,17, 0,18, 0,19 или 0,2 (масса/масса) антимикробного консерванта.
«Эмульгирующий агент» представляет собой соединение или вещество, которое действует в качестве стабилизатора для смеси двух или более жидкостей, которые обычно являются несмешиваемыми (несмешивающиеся или не поддающиеся смешению). Примеры эмульгирующих агентов включают, но без ограничения, природные эмульгирующие агенты (например, гуммиарабик, агар, альгиновую кислоту, альгинат натрия, трагакант, хондрус, холестерин, ксантан, пектин, желатин, яичный желток, казеин, ланолин, холестерин, воск и лецитин), коллоидные глины (например, бентонит [силикат алюминия] и вигум [алюмосиликат магния]), производные длинноцепочечных аминокислот, высокомолекулярные спирты (например, стеариловый спирт, цетиловый спирт, олеиловый спирт, триацетина моностеарат, этиленгликоля дистеарат, глицерил моностеарат, пропиленгликоля моностеарат и поливиниловый спирт), карбомеры (например, карбоксиполиметилен, полиакриловую кислоту, полимер акриловой кислоты и карбоксивиниловый полимер), каррагенан, производные целлюлозы (например, натрий- карбоксиметилцеллюлозу, порошкообразную целлюлозу, гидроксиметилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и метилцеллюлозу), сложные эфиры сорбитана и жирной кислоты (например, полиоксиэтилен сорбитан монолаурат [Tween® 20], полиоксиэтилен сорбитан [Tween® 60], полиоксиэтилен сорбитан моноолеат [Tween® 80], сорбитан монопальмитат [Span® 40], сорбитан моностеарат [Span® 60], сорбитан тристеарат [Span® 65], глицерил моноолеат и сорбитан моноолеат [Span® 80]), сложные эфиры полиоксиэтилена (например, полиоксиэтилена моностеарат [Myrj® 45], полиоксиэтилен-гидрогенизированное касторовое масло, полиэтоксилированное касторовое масло, полиоксиметилен стеарат и солютол), сложные эфиры сахарозы и жирной кислоты, сложные эфиры полиэтиленгликоля и жирной кислоты (например, Cremophor®), сложные эфиры полиоксиэтилена (например, полиоксиэтилена лауриловый эфир [Brij® 30]), и поли(винилпирролидон), диэтиленгликоля монолаурат, триэтаноламина олеат, натрия олеат, калия олеат, этилолеат, олеиновую кислоту, этиллаурат, натрия лаурилсульфат, плуроник F68, полоксамер 188, цетримония бромид, цетилпиридиния хлорид, бензалкония хлорид и докузат натрия, и/или их комбинации. Эмульгирующий агент может присутствовать в составе для местного применения при концентрации около 0,5-10% (масса/масса), например, 0,5-6% (масса/масса). Например, состав для местного применения может содержать около 0,5-1%, 1-1,5%, 1,5-2%, 2-2,5%, 2,5-3%, 3-3,5%, 3,5-4%, 4-4,5%, 4,5-5%, 5-5,5%, 5,5-6%, 5-10%, 6-10% или 8-10% (масса/масса) эмульгирующего агента. В частности, состав для местного применения может содержать около 0,5, 0,6, 0,7, 0,8, 0,9, 1, 1,5, 2, 2,5, 3, 3,5, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5, 8, 8,5, 9, 9,5 или 10 (масса/масса) эмульгирующего агента.
Состав для местного применения по изобретению может дополнительно содержать один или несколько растворителей (например, неводных растворителей или воду). Примеры неводных растворителей могут включать, но без ограничения, любой известный растворитель, включая пропиленгликоль, гликоль и их смеси. Неводный растворитель может присутствовать в составе для местного применения при концентрации около 2-65% (масса/масса). Например, состав для местного применения может содержать около 2-15%, 15-30%, 30-45% или 45-65% (масса/масса) растворителя. В некоторых вариантах осуществления состав для местного применения по изобретению может также содержать воду.
В некоторых вариантах осуществления состав для местного применения по изобретению может дополнительно содержать одно или несколько смягчающих веществ, отдушек или пигментов. Состав для местного применения можно также применять в сочетании с повязкой на рану (например, пластырь с адгезивным слоем, гипсовый пластырь и т.п.). (например, циклогексан, n-гексан, n-декан, изооктан, октан, бутиловый эфир, четыреххлористый углерод, триэтиламин, изопропиловый эфир, толуол, p-ксилол, трет-бутилметиловый эфир, бензол, бензиловый эфир, дихлорметан, метиленхлорид, хлороформ, дихлорэтан, этилендихлорид, 1-бутанол, изобутиловый спирт, тетрагидрофуран, этилацетат, 1-пропанол, 2-пропанол, метилацетат, циклогексанон, метилэтилкетон (МЕК), нитробензол, бензонитрил, 1,4-диоксан или p-диоксан).
Способы стимулирования заживления ран
Любой из составов для местного применения, описанных в настоящем документе, можно применять для стимулирования заживления ран у субъекта, нуждающегося в лечении. Состав для местного применения можно наносить на участок раны, следуя надлежащему режиму дозирования и лечения. Режим дозирования и лечения для описанного способа будут зависеть от природы и состояния раны, подвергаемой лечению, возраста и состояния пациента, и любой предшествующей или сопутствующей терапии. В некоторых случаях состав для местного применения можно наносить один раз в неделю, один раз через день, один раз в день, дважды в день, три раза в день или четыре раза в день в течение подходящего периода времени. Лечение может быть прекращено после излечения раны. Если это необходимо, то лечение может быть возобновлено, например, при повторном открытии раны.
Термин «рана» относится к повреждению живой ткани, вызванному порезом, ударом или другим воздействием (например, вызвана медицинским состоянием, таким как кожное заболевание), как правило, повреждению, при котором кожа порезана или нарушена. Рана может быть связана с медицинским состоянием, например, кожным заболеванием. Термин «заживление раны» означает динамический и сложный процесс замены девитализированных или отсутствующих клеточных структур и/или слоев ткани. Термин «стимулирование заживления раны» или «стимулирующие заживление раны» означает индукцию повышенного уровня или скорости замены девитализированных или отсутствующих клеточных структур и/или слоев ткани. В качестве примера, на стимулирование заживления раны может указывать частичное или полное закрытие язвы или увеличение скорости заживления язвы (включая, но без ограничения, более быстрые изменения в размере язвы, площади или тяжести, более быстрое закрытие язвы и/или увеличение процентного изменения от исходного размера язвы, площади или тяжести по сравнению с контрольной язвой, обработанной плацебо).
Субъектом, подлежащим лечению составом для местного применения, может являться человек или млекопитающее, не являющееся человеком. В некоторых вариантах осуществления субъектом является пациент-человек, имеющий открытую рану, которая относится к повреждению или травме живых тканей (например, кожи), вызывающей нарушение нормальной непрерывности биологических структур. Открытая рана может включать, но без ограничения, ссадину, резаную рану, глубокий порез, прокол, разрыв, порез или другие аналогичные повреждения.
В других вариантах осуществления субъектом является пациент-человек, имеющий хроническую рану, которая может представлять собой повреждения или травму живых тканей (например, кожи), которая вызывает нарушение нормальной непрерывности биологических структур и не заживает при прохождении определенных стадий и/или за прогнозируемое количество времени. Хроническая рана может включать, но без ограничения: хирургическую рану, травматическую рану, пролежневую язву, венозную язву или диабетическую язву. В других примерах хроническая рана может быть связана с заболеванием или нарушением, например, карциномой, ожогом, пролежнем, кожным заболевание, таком как атопический дерматит.
В одном примере субъектом является пациент-человек, имеющий язву стопы, связанную с диабетом (например, типа I или типа II). Сахарный диабет (также известный как диабет) является группой метаболических заболеваний, которые приводят к высоким уровням сахара в крови в течение длительного периода. Диабет может возникать в результате того, что поджелудочная железа не продуцирует достаточно инсулина или клетки тела не отвечают надлежащим образом на продуцируемый инсулин. Тремя основными типами сахарного диабета являются диабет типа I (также известный как инсулинозависимый сахарный диабет (IDDM), или ювенильный диабет; возникает в результате неспособности поджелудочной железы продуцировать достаточное количество инсулина), типа 2 (также известный как инсулиннезависимый сахарный диабет (NIDDM) или диабет взрослых; возникающий из-за неспособности клеток отвечать надлежащим образом на инсулин) и гестационный диабет (наблюдаемый в период беременности, когда в крови наблюдаются высокие уровни сахара при отсутствии предшествующей истории диабета). Многие серьезные осложнения наблюдаются у больных диабетом, включая, но без ограничения, хронические раны, такие как диабетические язвы стопы (также известные как диабетические язвы).
В некоторых вариантах осуществления субъект, подлежащий лечению с помощью способов, описанных в настоящем документе, имеет тяжелую рану, например, язву площадью более 2 см2 (например, 3 см2, 4 см2 или 5 см2). В некоторых примерах субъект имеет одну или несколько подошвенных язв.
Наборы для применения для стимулирования заживления ран
Настоящее изобретение также относится к наборам, предназначенным для стимулирования заживления ран. Такие наборы могут включать один или более контейнеров, содержащих состав для местного применения, как описано в настоящем документе, который содержит экстракт Plectranthus Amboinicus, экстракт Centella asiatica или комбинацию экстракта Plectranthus Amboinicus и экстракта Centella asiatica.
В некоторых вариантах осуществления набор может содержать инструкции по применению в соответствии с любым из способов, описанных в настоящем документе. Включенные инструкции могут содержать описание нанесения состава для местного применения для стимулирования заживления ран согласно любому из способов, описанных в настоящем документе. Набор может, кроме того, содержать описание отбора индивидуума, подходящего для лечения, на основе идентификации того, имеет ли индивидуум раны, требующие лечения.
Инструкции, относящиеся к применению состава для местного применения, обычно включают информацию, касающуюся дозы, схемы дозирования и пути введения для намеченного лечения. Контейнеры могут представлять собой стандартные дозы, насыпные упаковки (например, многодозовые упаковки) или субстандартные дозы. Инструкции, поставляемые в наборах по изобретению, обычно представляют собой письменные инструкции на этикетке или вкладыше упаковки (например, лист бумаги, включенный в набор), но также приемлемы инструкции, считываемые машиной (например, инструкции на магнитном или оптическом диске для хранения информации).
На этикетке или вкладыше в упаковку указывается, что композицию применяют для стимулирования заживления ран. Инструкции могут быть предоставлены для осуществления любого из способов, описанных в настоящем документе.
Наборы по настоящему изобретению находятся в подходящей упаковке. Подходящая упаковка включает, но без ограничения, флакончики, бутылки, банки, гибкую упаковку (например, запаянные мешочки Mylar или пластиковые мешочки) и т.п. По меньшей мере один активный агент в композиции представляет собой активный агент, выбранный из группы, состоящей из экстракта Plectranthus Amboinicus, экстракта Centella Asiatica и комбинации экстракта Plectranthus amboinicus и экстракта Centella asiatica
Наборы могут необязательно предоставлять дополнительные компоненты, такие как интерпретационная информация. Обычно набор включает контейнер и этикетку или вкладыш (вкладыши) в упаковку на контейнере или связанные с ним. В некоторых вариантах осуществления изобретение обеспечивает готовые изделия, включающие содержимое описанных выше наборов.
Без дальнейшей конкретизации полагают, что специалист в данной области, исходя из приведенного выше описания, сможет использовать настоящее изобретение в полном его объеме. Следующие конкретные варианты осуществления, следовательно, должны истолковываться как лишь иллюстративные, и не ограничивающие остальную часть раскрытия каким-либо образом. Все цитируемые в настоящем документе публикации включены в настоящее описание в качестве ссылок.
ПРИМЕР 1. Эффекты экстракта Plectranthus Amboinicus и экстракта Centella Asiatica на пролиферацию и миграцию эндотелиальных клеток
(i) МТТ Анализ пролиферации
Экстракт Plectranthus Amboinicus (PA) и экстракт Centella Asiatica (CA) получали, следуя описаниям, представленным в настоящем документе. Для этого исследования использовали линию эндотелиальных клеток EA.hy926. Клетки высевали при плотности 4×104 клеток/лунку в 96-луночном планшете в течение одного дня и затем обрабатывали экстрактом РА или СА в бессывороточной среде в течение 70 часов. После обработки клетки окрашивали красителем МТТ в течение 2 часов.
Как показано на фигуре 3А, экстракт РА усиливал пролиферацию клеток, в то время как эффект СА на клеточную пролиферацию был ниже по сравнению с экстрактом РА.
(ii) Анализ методом зарастания царапины (Scratch Assay) - миграция
Эндотелиальные клетки EA.hy926 высевали при плотности 8×104 клеток/лунка в 48-луночном планшете в течение 24 часов. На полученный таким образом конфлюэнтный монослой клеток наносили царапину и обрабатывали экстрактом РА или СА в бессывороточной среде в течение 72 часов.
Результаты, полученные в этом исследовании, показали, что экстракт PA значительно усиливал миграцию эндотелиальных клеток, что является важным для заживления раны. Клетки, обработанные экстрактом СА, также показали признаки миграции, но результат не был столь значителен, как и для экстракта РА. Фигура 3B.
ПРИМЕР 2. Эффекты экстракта Plectranthus Amboinicus и экстракта Centella Asiatica на пролиферацию и миграцию кератиноцитов
(i) Анализ пролиферации с использованием сульфородамина В (SRB)
В данном исследовании использовали клеточную линию кератиноцитов, клетки HaCaT. Клетки высевали при плотности 4×104 клеток/мл в 96-луночном планшете в течение одного дня и затем обрабатывали экстрактом PA или CA, описанным в примере 1 выше, в течение 24 часов. После обработки клетки фиксировали и окрашивали красителем SRB.
Как показано на фигуре 4A, оба PA и CA увеличивают клеточную пролиферацию клеток кератиноцитов.
(ii) Анализ методом зарастания царапины (Scratch Assay) - миграция
Клетки кератиноцитов HaCaT высевали при плотности 8×104 клеток/лунку в 48-луночном планшете в течение одного дня. На полученный таким образом конфлюэнтный монослой клеток наносили царапину и обрабатывали экстрактом РА или СА в течение 24 часов. Количественно оценивали площадь заживления раны.
Результаты, полученные в этом исследовании, показали, что экстракт РА индуцировал миграцию клеток (эффект заживления ран) в кератиноцитах дозозависимым образом. Экстракт СА также усиливал миграцию клеток кератиноцитов при относительно высокой концентрации (например, 30 мкг/мл).
ПРИМЕР 3. Эффект салвигенина и азиатикозида на заживление ран
Анализ in vitro образования капиллярных трубочек с использованием клеток пупочной вены человека (HUVEC) выполняли для исследования эффекта описанного в настоящем документе салвигенина, активного агента экстракта РА, в отношении заживления ран.
Вкратце, 96-луночные планшеты с поверхностью Nunclon покрывали матригелем (50 мкл/лунку) и инкубировали при 37°С в течение 30 минут для стимулирования гелеобразования. Клетки HUVEC культивировали в среде M200, и клетки между пассажами 2 и 4 высевали (при плотности 3×105 клеток в 100 мкл среды) в каждую из покрытых матригелем лунок. Серии разведений тестируемых соединений, как показано на фигуре 5А (включая основной фактор роста фибробластов (bFGF) в качестве положительного контроля и салвигенин), добавляли в культуральную среду для изучения их биологических эффектов на образование трубочек. После 6 часов инкубации при 37°С в увлажненной атмосфере, содержащей 5% CO2, среду аспирировали, клетки HUVEC фиксировали и полные сети капиллярных трубочек в пределах обозначенной области поля малого увеличения (×10) фотографировали и подсчитывали с помощью компьютерного программного обеспечения для обработки изображений ImagePro Plus V.4.5. Данные тестирования выражали в виде процента полного образования капиллярной трубочки относительно необработанных контрольных культур HUVEC, инкубированных в тех же самых условиях.
Как показано на фигуре 5A, салвигенин значительно увеличивал образование трубочек клетками HUVEC
Для изучения эффекта азиатикозида на заживление ран проводили анализ миграции методом зарастания царапины следующим образом. Клетки кератиноцитов HaCaT высевали при плотности 8×104 клеток/лунку в 48-луночном планшете в течение одного дня. На полученный таким образом конфлюэнтный монослой клеток наносили царапину и обрабатывали азиатиказидом в течение 24 часов. Площадь заживления ран оценивали количественно. Результаты, полученные в результате этого исследования, показали, что азиатикозид индуцировал миграцию клеток (эффект заживления ран) в кератиноцитах.
Как показано на фигуре 5В, азиатикозид значительно стимулировал миграцию клеток HaCaT, что могло бы способствовать заживлению ран.
ПРИМЕР 4. Экстракты Plectranthus Amboinicus стимулировали нормальное заживление ран
Это исследование выполняли для изучения эффекта различных составов для местного применения на кремовой основе, включающих экстракт РА, на нормальное закрытие ран в животной модели. Крыс Sprague-Dawley случайным образом распределяли на 4 группы. Затем крыс анестезировали пентобарбиталом и удаляли шерсть на хирургическом поле. Кожу в областях середины спины каждой крысы вырезали (на полную толщину), используя хирургический нож (2 см × 2 см).
Крыс в четырех группах обрабатывали следующими кремовыми составами, которые изготавливали в соответствии со способами, описанными в настоящем документе:
- G1 - крем в качестве отрицательного контроля,
- G2 - мазь Winsolution-b (от фирмы Yungshin Pharma, Co. LTD, Taiwan) в качестве референсного контроля,
- G3 - состав I (1,25% экстракт РА), и
- G4 - состав II (0,25% экстракт РА).
Составы наносили на каждый участок раны два раза в день, и раны покрывали марлей. Колпаки надевали на шеи крыс Sprague-Dawley (n = 6, возраст 12 недель), чтобы предотвратить получение царапин у животных. Для измерения закрытия ран делали снимки ран на дни 4, 6, 8, 10, 12, 14 и 16. Когда делали снимки, перед ранами помещали стандартную линейку. Длину ран стандартизировали в соответствии со шкалой стандартной линейки на фотографиях перед анализом ран с помощью пакета программ обработки изображений Image pro (Media cybernetics), чтобы избежать ошибок, обусловленных различными расстояниями при фотографировании.
Результаты, полученные в этом исследовании, показали, что все Составы I и II проявили многообещающие эффекты в отношении стимулирования закрытия ран у крыс. Таблица 2 и фигура 6.
Таблица 2. Эффекты закрытия ран
* CT50 - время (дни) для закрытия раны на 50%
ПРИМЕР 5. Фармакокинетическое исследование in vivo на креме для местного применения, содержащем экстракт Plectranthus Amboinicus и экстракт Centella Asiatica
Фармакокинетические свойства состава для местного применения, содержащего экстракты Plectranthus Amboinicus и Centella asiatica (в общем количестве 1,25%, содержащем 0,0001-0,1 мас.% салвигенина и 0,05-1 мас.% азиатикозида), оценивали у пациентов-людей, имеющих хронические диабетические язвы стоп (DFU). Экстракты РА и СА в составе для местного применения получали в соответствии со способами, описанными в настоящем документе. Состав для местного применения имеет кремовую основу и, кроме того, содержит цетостеариловый спирт (около 1,0-10 мас.%, например, около 3,5-6,5 мас.%), белый петролатум и жидкий петролатум 350 сП (в общем количестве около 5-30 мас.%, например, в общем количестве около 5-15 мас.%), метилпарабен и пропилпарабен (в общем количестве около 0,005-0,2 мас.%, например, в общем количестве 0,005-0,2 мас.%), эмульгаторы, такие как Span® 60 и Tween® 60 (в общем количестве около 0,5-10 мас.%, например, в общем количестве около 0,5-5 мас.%) и один или несколько растворителей, таких как пропиленгликоль (около 2-20 мас.%, например, около 4-10 мас.%). Экстракты включали в состав для местного применения на кремовой основе, который, кроме того, содержал жидкий петролатум, пропиленгликоль, цетилстеариловый спирт, белый петролатум, Span® 60, Tween® 60, пропилпарабен, метилпарабен и воду.
Всего 12 пациентов завершили исследование. Каждый субъект получал одну дозу кремового состава на День 1 с последующим сбором образцов крови, затем дважды в день со Дня 2 до Дня 13, и последующий сбор образцов крови был запланирован на День 14 после конечной дозы. Образцы крови анализировали для измерения концентраций салвигенина и азиатикозида, двух активных ингредиентов крема, в плазме с помощью утвержденной методики LC/MS/MS. Результаты, полученные после 1-го дня, показали, что из 12 пациентов 2 пациента имели обнаруживаемые концентрации в плазме салвигенина ≤ 12,403 пг/мл; и 5 пациентов имели обнаруживаемые концентрации в плазме азиатикозида ≤ 9,276 нг/мл.
Результаты, полученные после 14-го дня, показали, что 4 из 12 пациентов имели обнаруживаемые в плазме концентрации салвигенина ≤ 16,972 пг/мл, и 5 из 12 пациентов имели обнаруживаемые концентрации в плазме азиатикозида ≤ 6,154 нг/мл.
В целом, результаты, полученные в этом исследовании, показали, что местное нанесение состава для местного применения, используемого в этом клиническом исследовании, привело к ограниченному системному распределению как салвигенина, так и азиатикозида.
Всего 6 нежелательных явлений (AE) сообщалось 3 пациентами. Все AE были слабой интенсивности, и эти AE считались исследователем «не связанными» или «маловероятно связанными» с исследуемым лекарственным средством. После завершения 4 AE были улучшены, и 2 AE остались без изменения. Не было сообщений о значительных АЕ, смерти или серьезных АЕ.
Заключение: Это 14-дневное исследование показало, что местное нанесение состава для местного применения, используемого в данном исследовании, привело к ограниченному системному распределению по меньшей мере активных ингредиентов салвигенина и азиатикозида, и является безопасным для пациентов с DFU.
ПРИМЕР 6. Клиническое испытание фазы III с использованием крема для местного применения, содержащего экстракт Plectranthus Amboinicus и экстракт Centella Asiatica
В промежуточном анализе всего 124 пациента, имеющих DFU, было рандомизировано в многоцентровом испытании для оценки эффекта кремового состава для местного применения, описанного в примере 5 выше, в отношении заживления ран. Критерии включения и исключения для участия в испытании приведены ниже. В качестве контрольного лечения использовали повязку Aquacel® Hydrofiber® (ConvaTec, Princeton, NJ, USA).
Критерии отбора
Критерии включения для пациентов
Пациенты считались пригодными для участия, если были удовлетворены все следующие критерии:
1) подписанное письменное информированное согласие перед проведением первой оценки в исследовании;
2) возраст не менее 20 лет и не старше 80 лет;
3) сахарный диабет (тип 1 или 2) с HbA1c < 12,0%, по данным измерения во время скрининга или в течение трех месяцев до рандомизации;
4) лодыжечно-плечевой индекс на целевой конечности по меньшей мере 0,8, по данным измерения во время скрининга или в течение трех месяцев до рандомизации;
5) целевая язва со следующими характеристиками:
а. степень 1 или 2 согласно системе классификации язвы по Вагнеру (Wagner Ulcer Classification System);
b. не выше, чем у лодыжки;
с. отсутствие активной инфекции;
d. площадь поперечного сечения от 1 до 25 см2 после дебридмента; и
e. присутствие в течение по меньшей мере 4 недель перед рандомизацией;
6) лица детородного возраста имели негативный тест на беременность и не кормили грудью на момент проведения скринингового визита, и
7) способны и имеют желание осуществлять запланированные визиты и следовать процедурам исследования.
Критерии исключения
Пациентов исключали из участия, если были удовлетворены любые из следующих критериев:
1) наличие некроза, метеоризма или синусового тракта, не удаляемых дебридментом;
2) острая нейроартропатия Шарко, определенна путем клинического и/или рентгенографического исследования;
3) подвергание процедуре реваскуляризации, направленной на увеличение кровотока в целевой подвергаемой лечению конечности за < 4 недели до рандомизации;
4) низкий питательный статус, определенный как альбумин < 2,5 г/дл;
5) AST и/или ALT > 3 раз выше нормального верхнего предельного значения;
6) сывороточный креатинин > 2 раз выше нормального верхнего предельного значения;
7) лечение иммунодепрессантами или химиотерапевтическими агентами, лучевой терапией или системными кортикостероидами в течение 4 недель до рандомизации;
8) применение любого исследовательского лекарственного средства или терапии в течение 4 недель до рандомизации;
9) психиатрическое состояние (например, суицидальное мышление), текущая или хроническая проблема злоупотребления алкоголем или наркотиками, рассматриваемая как угроза следованию режима лечения; или
10) по мнению исследователя не подходят для участия в исследовании по какой-либо другой причине.
Критерии прекращения участия в исследовании для индивидуальных пациентов
Пациенты могут прекратить исследование по любой причине и в любое время без указания причины и без штрафа или осуждения.
Кроме того, пациентов исключали из исследования, если были удовлетворены любые из следующих критериев:
1) нарушение и/или значительное отклонение от протокола исследования;
2) недостаточная эффективность (определяемая как ухудшение степени по Вагнеру до уровня 3);
3) соображения безопасности;
4) утрата контактов для последующего наблюдения;
5) согласие на отказ от участия;
6) если это считается в интересах пациента, или
7) прекращение исследования спонсором.
Цели исследования и конечные точки исследования
Первичной целью данного исследования была оценка применения местного состава на кремовой основе для заживления ран у пациентов-людей, страдающих DFU.
Первичная переменная представляла собой число язв-мишеней, заживших в каждой группе в течение 16 недель. Первичной конечной точкой эффективности являлось сравнение частоты полного заживления язвы-мишени между двумя лечебными группами в конце лечения.
Для целей данного исследования полное заживление определялось как полная эпителизация, которая сохранялась без дренирования в течение по меньшей мере 2 недель и была подтверждена экспертом, не владеющим информацией о ходе исследования.
Вторичными конечными точками эффективности являлись: время до полного заживления язв (время первоначального заживления рассматривалось как время до заживления); процентное изменение площади язвенной поверхности от исходного состояния; процент пациентов с 50%-ным уменьшением площади язвенной поверхности; и частота инфицирования целевой язвы.
Конечные точки безопасности включали оценку частоты возникновения нежелательных явлений, вызванных лечением, клинические лабораторные показатели и основные показатели состояния организма.
Поисковой конечной точкой являлось повторное возникновение целевой язвы в течение последующего периода наблюдения, оцениваемое у тех пациентов, которые продемонстрировали полное заживление раны в конце периода сравнения.
Результаты
Эффективность заживления ран у больных диабетом, получавших лечение составом для местного применения на кремовой основе, описанным в примере 5, или Aquacel®, анализировали в популяции для полного анализа (FAS) и модифицированной популяции «всех включенных в исследование пациентов, принявших хотя бы одну дозу того или иного препарата» (mITT). Во всей популяции FAS и mITT результаты, представленные в таблице 3, показывают, что более высокий процент пациентов, получавших лечение составом для местного применения, достигал полного заживления язв по сравнению с пациентами, получавшими лечение Aquacel®. Этот результат показал, что состав для местного применения, используемый в этом исследовании, превосходил Aquacel®, существующий продукт для заживления ран, по меньшей мере в отношении полного заживления язв, которое является первичной конечной точкой исследования.
Кроме того, анализ подгрупп выполняли в популяции пациентов с исходной площадью язв > 5 см2 и подошвенными язвами. Этот тип язвы известен из уровня техники как трудный для лечения. Результаты в таблице 3 показывают, что частота полного заживления у пациентов, получавших лечение составом для местного применения, была выше, чем частота полного заживления у пациентов, получавших лечение Aquacel®.
Таблица 3. Первичная конечная точка: полная частота заживления
Частота полного заживления
Частота полного заживления
* Тест хи-квадрат
Таким образом, промежуточные результаты клинического испытания этой фазы III указывают на то, что состав для местного применения на кремовой основе, подвергнутый испытанию в настоящем документе, содержащий оба экстракта PA и CA, показал превосходные терапевтические эффекты в отношении стимулирования заживления ран у пациентов с DFU по сравнению с контролем Aquacel® Hydrofiber®.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Все признаки, раскрытые в этом описании, могут быть объединены вместе любым способом. Каждый признак, раскрытый в этом описании, может быть заменен альтернативным признаком, имеющим такое же, эквивалентное или аналогичное назначение. Таким образом, если явным образом не указано иное, каждый раскрытый признак является только одним примером из группы эквивалентных или аналогичных признаков.
Из приведенного выше описания специалист в данной области техники может легко определить существенные характеристики настоящего изобретения и, не отступая от сути и объема изобретения, может сделать различные изменения и модификации изобретения для адаптации его к различным применениям и условиям. Таким образом, другие варианты осуществления также находятся в рамках формулы изобретения.
ЭКВИВАЛЕНТЫ И ОБЪЕМ
В формуле изобретения артикли, такие как «а», «an» и «the», могут означать один или более чем один, если не указано иное или если из контекста явно не следует иное. Пункты формулы изобретения или описания, которые включают «или» между одним или более элементами группы, считаются выполненными, если один, более чем один, или все члены группы присутствуют в, использованы в, или иным образом относятся к данному продукту или процессу, если не указано иное или иное не следует из контекста. Изобретение включает варианты осуществления, в которых точно один элемент группы присутствует в, использован в, или иным образом относится к данному продукту или процессу. Изобретение включает варианты осуществления, в которых более чем один или все элементы группы присутствуют в, использованы в, или иным образом относятся к данному продукту или процессу.
Кроме того, изобретение охватывает все варианты, комбинации и перестановки, в которых одно или более ограничений, элементов, пунктов и описательных терминов из одного или более указанных пунктов представлено в другом пункте. Например, любой пункт, который зависит от другого пункта, может быть модифицирован для включения одного или более ограничений, находящихся в любом другом пункте, который зависит от того же самого исходного пункта. Если элементы присутствуют согласно перечислению, например, в формате групп Маркуша, каждая подгруппа элементов также раскрыта, и любой элемент (элементы) можно удалить из группы. Следует понимать, что, в целом, если указывается, что изобретение или аспекты изобретения включают конкретные элементы и/или признаки, то определенные варианты осуществления изобретения или аспекты изобретения состоят или в основном состоят из таких элементов и/или признаков. С целью упрощения эти варианты осуществления не были специально представлены в тех же выражениях в настоящем документе. Кроме того, следует отметить, что термины «включающий» и «содержащий» подразумеваются как открытые и разрешают включение дополнительных элементов или стадий. При указании диапазонов предельные значения включаются. Кроме того, следует понимать, что если не указано иное или если иное не следует из контекста и понятно специалистам в данной области, то значения, выраженные в виде диапазонов, могут подразумевать любое конкретное значение или поддиапазон в рамках указанных диапазонов в других вариантах осуществления изобретения до десятой части единицы нижнего предела диапазона, если из контекста явно не следует иное.
Данная заявка относится к различным выданным патентам и опубликованным патентным заявкам, все из которых включены в настоящий документ путем ссылки. Если имеется конфликт между любыми из включенных ссылок и настоящим описанием, то описание будет превалировать. Кроме того, любой конкретный вариант осуществления настоящего изобретения, который относится к предшествующему уровню техники, может в явной форме быть исключен из любого пункта формулы изобретения. Поскольку такие варианты осуществления считаются известными специалистам в данной области, их можно исключить, даже если исключение явно не выражено в настоящем описании. Любой конкретный вариант осуществления может быть исключен из любого пункта формулы изобретения по любой причине, независимо от того, относится ли он к предыдущему уровню техники.
Специалисты в данной области техники признают или смогут установить, используя не более чем рутинные эксперименты, много эквивалентов описанных здесь конкретных вариантов осуществления. Объем настоящих вариантов осуществления, описанных в настоящем документе, не должен ограничиваться приведенным выше описанием, а скорее определяется прилагаемой формулой изобретения. Специалистам в данной области должно быть понятно, что возможны различные изменения и модификации данного описания без отступления от сущности и объема настоящего изобретения, как определено в следующей формуле изобретения.





Настоящее изобретение обеспечивает состав для местного применения, содержащий активный агент, который содержит салвигенин и азиатикозид. Также, настоящее изобретение относится к применению состава для местного применения для стимулирования заживления ран. 2 н. и 19 з.п. ф-лы, 6 пр., 3 табл., 6 ил.
1. Состав местного применения для стимуляции заживления ран, содержащий:
(i) активный агент для стимуляции заживления ран в количестве 0,1-30% (масса/масса), где активный агент включает салвигенин в количестве 0,0001-0,5% (масса/масса) и азиатикозид в количестве 0,05-5% (масса/масса);
(ii) увеличивающий вязкость агент в количестве 1,0-10% (масса/масса);
(iii) мазевую основу в количестве 5-30% (масса/масса);
(iv) антимикробный консервант в количестве 0,005-0,2% (масса/масса); и
(v) эмульгирующий агент в количестве 0,5-10% (масса/масса).
2. Состав для местного применения по п.1, в котором активный агент представляет собой комбинацию экстракта Plectranthus Amboinicus и экстракта Centella asiatica.
3. Состав для местного применения по любому из пп.1, 2, в котором активный агент содержит салвигенин в количестве от 0,0001% до 0,1% (масса/масса) и азиатикозид в количестве от 0,05% до 1% (масса/масса).
4. Состав для местного применения по любому из пп.1-3, в котором активный агент, кроме того, содержит цирсимаритин, мадекассосид или их комбинацию.
5. Состав для местного применения по любому из пп.1-4, который содержит мазевую основу в количестве 10-30% (масса/масса), антимикробной консервант в количестве 0,01-0,2% (масса/масса) и эмульгирующий агент в количестве 0,5-6% (масса/масса).
6. Состав для местного применения по любому из пп.1-5, в котором экстракт Plectranthus Amboinicus получают путем приведения в контакт целого растения Plectranthus amboinicus или его части с растворителем, имеющим индекс полярности ниже 7, с получением раствора, и сушки раствора с получением экстракта Plectranthus Amboinicus.
7. Состав для местного применения по любому из пп.1-6, который содержит экстракт Plectranthus Amboinicus и экстракт Centella asiatica в массовом соотношении от 1:10 до 10:1, предпочтительно от 1:5 до 5:1.
8. Состав для местного применения по любому из пп.1-7, в котором увеличивающий вязкость агент представляет собой цетостеариловый спирт, холестерин, стеариловый спирт, хлоркрезол, белый воск, стеариновую кислоту, цетиловый спирт или их комбинацию, при этом мазевая основа содержит одно или несколько соединений петролатума, и/или антимикробный консервант содержит одно или несколько соединений парабенов.
9. Состав для местного применения по любому из пп.1-8, в котором эмульгирующий агент включает природные эмульгаторы, коллоидные глины, производные длинноцепочечных аминокислот, высокомолекулярные спирты, карбомеры, каррагинан, производные целлюлозы, сложные эфиры сорбитана и жирных кислот, полиоксиэтиленовые сложные эфиры, сложные эфиры сахарозы и жирных кислот, сложные эфиры полиэтиленгликоля и жирных кислот, простые эфиры полиоксиэтилена, и поли(винилпирролидон), диэтиленгликольмонолаурат, олеат триэтаноламина, олеат натрия, олеат калия, этилолеат, олеиновую кислоту, этиллаурат, лаурилсульфат натрия, Pluronic F68, Poloxamer 188, цетримония бромид, цетилпиридиния хлорид, бензалкония хлорид или докузат натрия и/или любые их комбинации.
10. Состав для местного применения по любому из пп.1-9, в котором мазевая основа представляет собой кремовую основу.
11. Состав для местного применения по любому из пп.1-10, который дополнительно содержит один или несколько растворителей.
12. Состав для местного применения по п.11, в котором один или несколько растворителей содержат пропиленгликоль.
13. Состав для местного применения по п.1, который содержит комбинацию экстракта Plectranthus Amboinicus и экстракта Centella asiatica в количестве около 0,1-30% (масса/масса), цетостеариловый спирт в количестве 1,0-10% (масса/масса), комбинацию белого петролатума и жидкого петролатума в общем количестве 5-30% (масса/масса), комбинацию метилпарабена и пропилпарабена в общем количестве 0,005-0,2 (масса/масса), и комбинацию сорбитана моностеарата и полисорбата 60 в общем количестве 0,5-10% (масса/масса).
14. Состав для местного применения по п.13, который дополнительно содержит пропиленгликоль в количестве 2-20% (масса/масса).
15. Состав для местного применения по любому из пп.1-14, где состав для местного применения включает комбинацию экстракта Plectranthus amboinicus и экстракта Centella asiatica в количестве 0,1-30% (масса/масса), цетостеариловый спирт в количестве 3-7% (масса/масса), комбинацию белого вазелина и жидкого вазелина в общем количестве 5-25% (масса/масса), комбинацию метилпарабена и пропилпарабена в общем количестве 0,005-0,2% (масса/масса) и комбинацию моностеарата сорбитана и полисорбата 60 в общем количестве 0,5-6% (масса/масса).
16. Применение состава для местного применения по любому из пп.1-15 для ускорения заживления ран у субъекта.
17. Применение состава для местного применения по п.16, который предназначен для местного применения по меньшей мере один раз в день, предпочтительно два раза в день.
18. Применение состава для местного применения по п.16 или 17, в котором субъектом является пациент-человек с диабетом, страдающий диабетической язвой стопы.
19. Применение состава для местного применения по любому из пп.16-18, в котором субъектом является пациент-человек, имеющий открытую рану, которая необязательно представляет собой ссадину, резаную рану, глубокий порез, прокол или разрыв.
20. Применение состава для местного применения по п.16 или 17, в котором субъект представляет собой пациента-человека, который имеет хроническую рану, которая необязательно представляет собой хирургическую рану, травматическую рану, пролежневую язву, венозную язву, диабетическую язву или рану, вызванную карциномой, ожогом, пролежнем или атопическим дерматитом.
21. Применение состава для местного применения по п.16 или 17, в котором субъектом является человек, имеющий акне.
| US 2007237841 A1, 2007.10.11 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЭКСТРАКТОВ PLECTRANTHUS AMBOINICUS, ЭКСТРАКТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, НЕОЧИЩЕННЫЙ ЭКСТРАКТ PLECTRANTHUS AMBOINICUS И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, ПЕРЕВЯЗОЧНЫЙ МАТЕРИАЛ НА ОСНОВЕ УПОМЯНУТЫХ КОМПОЗИЦИЙ И УПОМЯНУТЫЕ КОМПОЗИЦИИ В КАЧЕСТВЕ СРЕДСТВА ПРИ ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННОГО СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ КОЖНОГО НАРУШЕНИЯ | 2008 |
|
RU2440819C2 |
| WO 2011103449 A2, 2011.08.25 | |||
| CN 103127215 A, 2013.06.05 | |||
| US 2008194499 A1, 2008.08.14 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООЧИЩЕННОЙ АЗИАТИКОЗИДНОЙ КОМПОЗИЦИИ ИЗ Centella asiatica И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2565410C2 |
Авторы
Даты
2021-06-25—Публикация
2017-07-17—Подача