РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет согласно §119(e) главы 35 Свода законов США на основании предварительной заявки на патент США №61/610480, поданной 14 марта 2012 года, содержание которой включено в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Варианты реализации настоящего изобретения относятся к новым композициям травяных экстрактов, способам их получения и способам применения указанных экстрактов для лечения заболевания.
УРОВЕНЬ ТЕХНИКИ
[0003] Терапевтические композиции, содержащие травяные экстракты растений видов Sambucus nigra, Echinacea purpurea и Centella asiatica, описаны в патенте США номер 7,563,466.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Один из аспектов вариантов реализации настоящего изобретения относится к обеспечению новых терапевтических композиций, содержащих травяные экстракты растений видов Sambucus nigra (бузина черная), Echinacea purpurea (эхинацея пурпурная) и Centella asiatica (центелла азиатская). Указанные композиции демонстрируют повышенную терапевтическую активность при лечении различных воспалительных заболеваний, в частности, воспалительных заболеваний слизистой оболочки или кожи, по сравнению с известными композициями. Кроме того, указанные композиции демонстрируют повышенную растворимость по сравнению с известными композициями.
[0005] В одном из вариантов реализации настоящего изобретения предложена композиция, содержащая экстракты растений видов Sambucus nigra, Echinacea purpurea и Centella asiatica, причем композиции содержат нарингенин в концентрации выше или равной 0,055%. В одном из вариантов реализации настоящего изобретения терапевтическая композиция растворима в пропиленгликоле в концентрации 20%. В одном из вариантов реализации настоящего изобретения отношение Sambucus nigra : Echinacea purpurea : Centella asiatica составляет 7:1:2.
[0006] В одном из вариантов реализации настоящего изобретения предложены способы получения водной терапевтической композиции, содержащей экстракты растений вышеупомянутых видов, с применением по меньшей мере двух экстракций.
[0007] В одном из вариантов реализации настоящего изобретения предложены способы лечения заболеваний, в частности заболеваний слизистой оболочки или кожи, воспалительных заболеваний или заболеваний, патологических состояний или травм, которые могут быть облегчены посредством восстановления тканей, включающие введение композиций, содержащих экстракты растений указанных видов.
[0008] Подразумевается, что в настоящем описании, если не указано иное, определения, такие как «по существу» и «примерно», модифицирующие условие или характеристику связи признака или признаков варианта реализации настоящего изобретения, означают, что указанное условие или характеристика определяется в пределах допусков, которые являются приемлемыми для функционирования варианта реализации настоящего изобретения в области, для которой он предназначен. Если не указано иное, считается, что слово «или» в описании и формуле настоящего изобретения представляет собой включающее «или», а не исключающее или, и указывает на по меньшей мере один из или любую комбинацию элементов, которые оно соединяет.
[0009] Указанное краткое описание приведено для ознакомления с выбором концепций в упрощенном виде, которые дополнительно описаны ниже в подробном описании. Указанное краткое описание не предназначено для определения ключевых признаков или основных признаков заявленного изобретения, а также не предназначено для применения для ограничения объема заявленного изобретения.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[0010] На Фиг. 1а и 1b представлены блок-схемы, изображающие схемы синтеза для производства композиций, содержащих экстракты растений видов Echinacea purpurea, Sambucus nigra и Centella asiatica, согласно вариантам реализации настоящего изобретения;
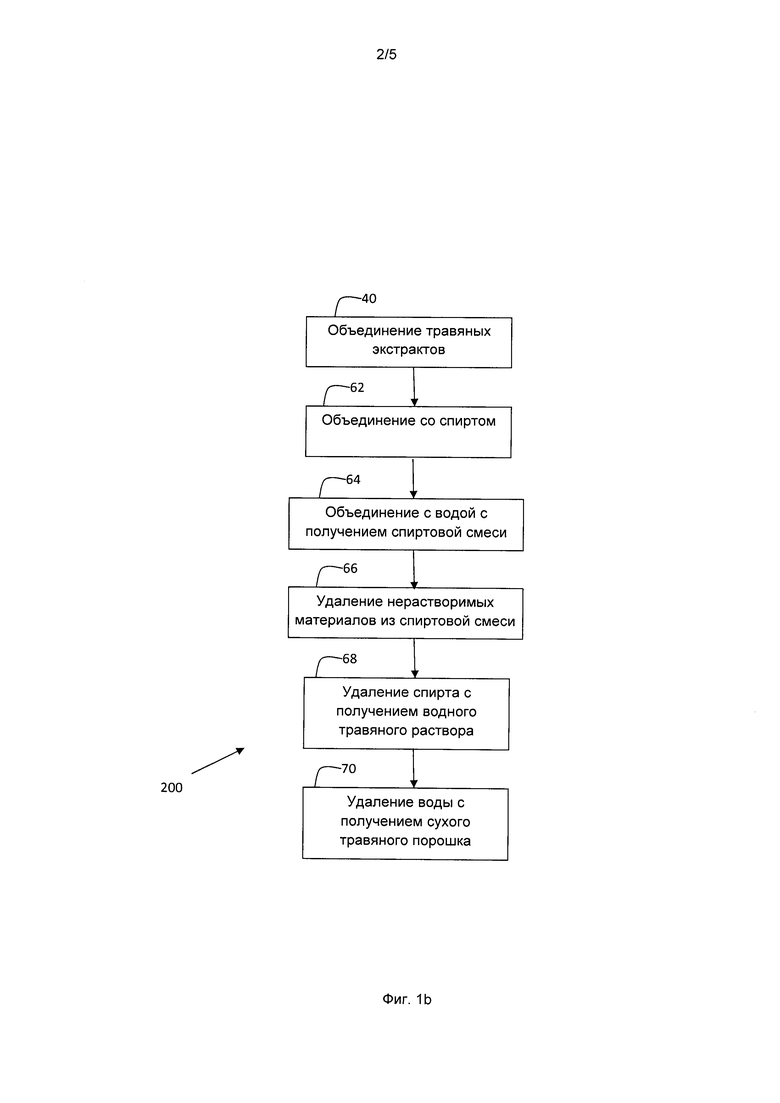
[0011] На Фиг. 2а представлена диаграмма, на которой показано действие травяного экстракта согласно вариантам реализации настоящего изобретения на ингибирование активности интерлейкин-1β-конвертирующего фермента (ICE), которое является показателем воспаления, в сравнении с действием традиционного экстракта в различных концентрациях;
[0012] На Фиг. 2b представлена диаграмма, на которой показано действие травяного экстракта согласно вариантам реализации настоящего изобретения на выделение коллагена из клеток, которое является показателем заживления ран, в сравнении с действием традиционного экстракта в различных концентрациях;
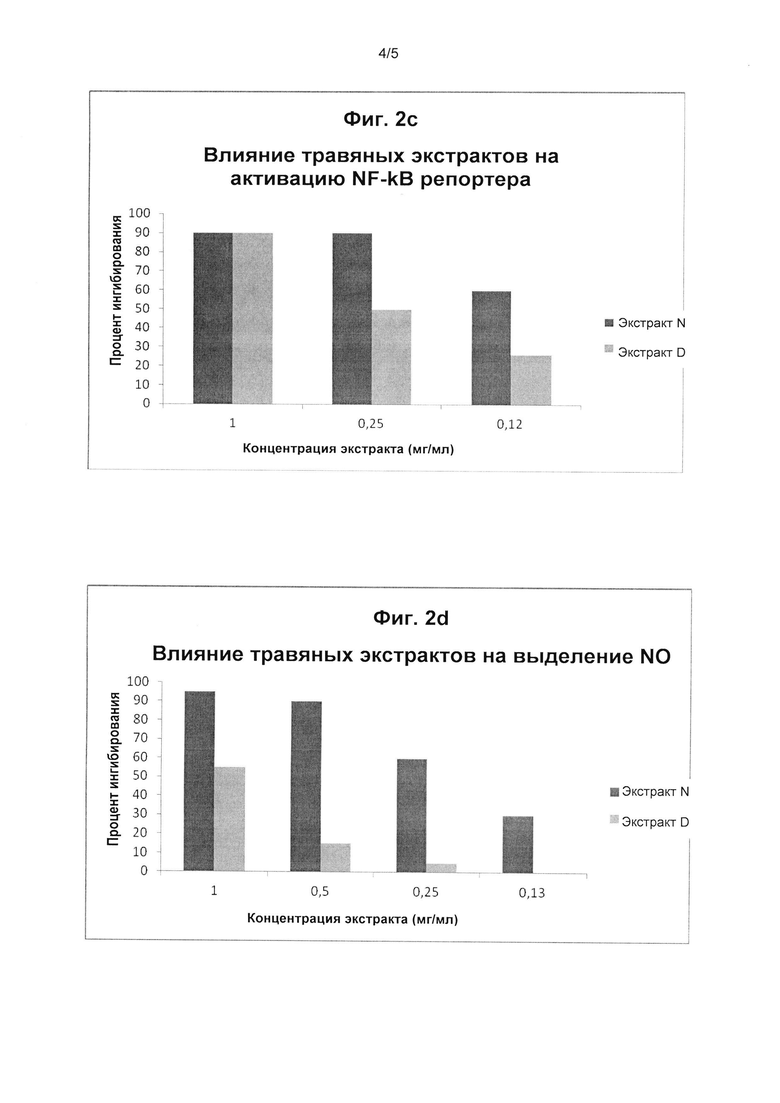
[0013] На Фиг. 2с представлена диаграмма, на которой показано действие травяного экстракта согласно вариантам реализации настоящего изобретения на ингибирование ядерного фактора «каппа-В» (NFκB), являющегося показателем воспаления, в сравнении с действием традиционного экстракта в различных концентрациях;
[0014] На Фиг. 2d представлена диаграмма, на которой показано действие травяного экстракта согласно вариантам реализации настоящего изобретения на ингибирование активности оксида азота (II) (NO) в клетках, которое является показателем воспаления, в сравнении с действием традиционного экстракта в различных концентрациях;
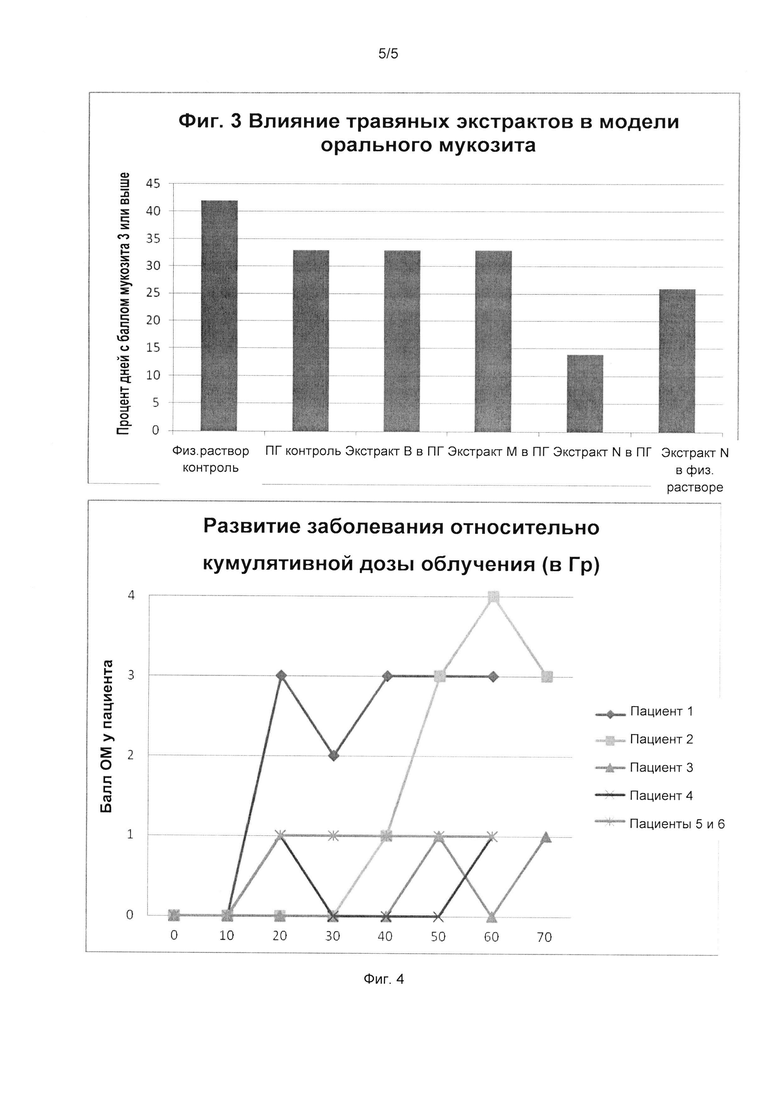
[0015] На Фиг. 3 представлена диаграмма, на которой показано положительное действие составов экстрактов согласно вариантам реализации настоящего изобретения на снижение балльной оценки мукозита у хомячков в модели мукозита полости рта, вызванного радиоактивным облучением; и
[0016] На Фиг. 4 представлен график, на котором показано действие композиций согласно вариантам реализации настоящего изобретения на балльную оценку мукозита полости рта у шести пациентов-людей.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0017] В следующем подробном описании будут описаны новые способы получения композиций, содержащих травяные экстракты. Кроме того, описаны химические и биологические характеристики, свидетельствующие об улучшенных свойствах новых травяных композиций. Приведено описание животных моделей, демонстрирующих повышенный противовоспалительный эффект композиций согласно вариантам реализации настоящего изобретения. Приведено описание клинического испытания, демонстрирующего эффект композиций согласно вариантам реализации настоящего изобретения при лечении людей. Предложены способы лечения с применением новых травяных композиций.
[0018] Пример 1а: Синтез композиций согласно вариантам реализации настоящего изобретения.
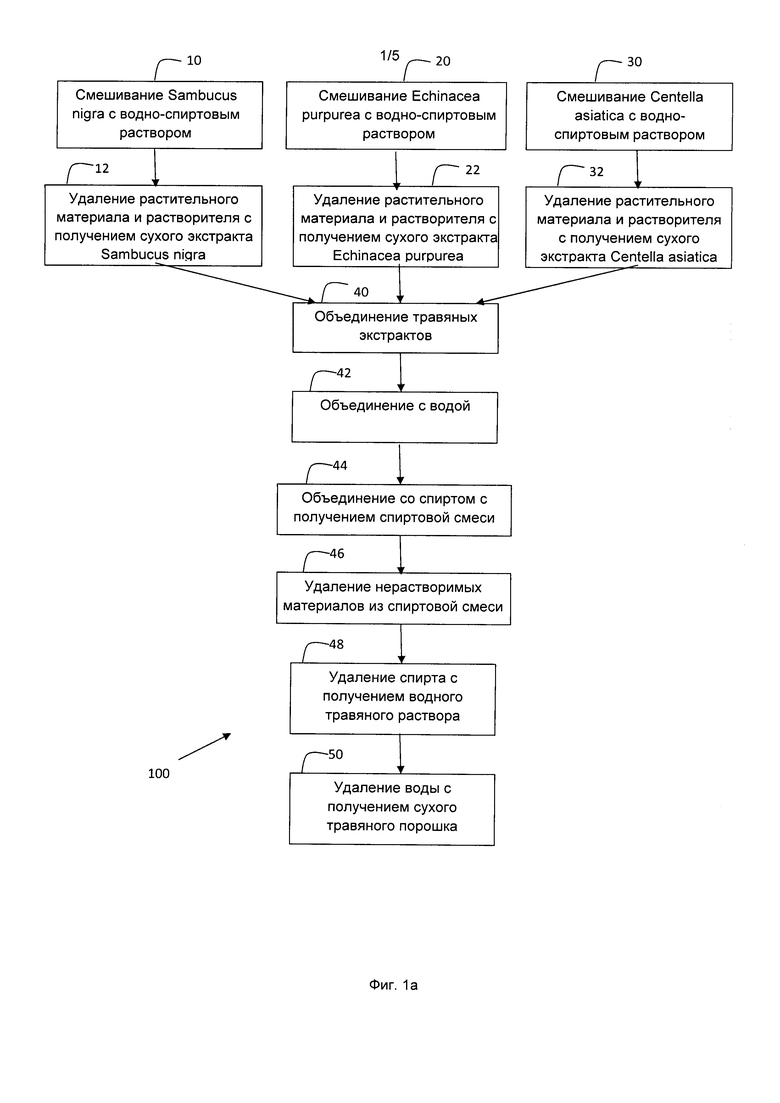
[0019] На Фиг. 1а представлена блок-схема, изображающая схему синтеза 100 для синтезирования различных композиций, содержащих экстракты растений видов Sambucus nigra, Echinacea purpurea и Centella asiatica. Схема синтеза 100 включает блоки 10, 20 и 30, включающие смешивание Sambucus nigra, Echinacea purpurea и Centella asiatica, соответственно, с водно-спиртовым раствором (раствором, содержащим воду и спирт). Блоки 12, 22 и 32 включают удаление нерастворимого растительного материала и растворителя с получением высушенных экстрактов Sambucus nigra, Echinacea purpurea и Centella asiatica, соответственно. Блок 40 включает объединение высушенных травяных экстрактов блоков 12, 22 и 32.
[0020] В одном из вариантов реализации настоящего изобретения водно-спиртовой раствор блоков 10, 20 и/или 30 содержит от 25 до 75% спирта. В одном из вариантов реализации настоящего изобретения водно-спиртовой раствор блока 10, 20 и/или 30 содержит 70% спирта. В одном из вариантов реализации настоящего изобретения спирт в водно-спиртовом растворе содержит этанол. В одном из вариантов реализации настоящего изобретения отношение растворителя к растению в блоке 10, 20 и/или 30 составляет от примерно 6 до примерно 10 частей по массе растворителя к одной части по массе растительного материала. В одном из вариантов реализации настоящего изобретения отношение растворителя к растению в блоке 10, 20 и/или 30 составляет примерно 8:1 по массе. В одном из вариантов реализации настоящего изобретения водно-спиртовой раствор смешивают в течение примерно 8 часов. В одном из вариантов реализации настоящего изобретения способ экстракции является многостадийным. В одном из вариантов реализации настоящего изобретения водно-спиртовой раствор смешивают при температуре примерно 30-40°С (градусов Цельсия). В одном из вариантов реализации настоящего изобретения перед удалением растворителя и растительного материала к водно-спиртовому раствору добавляют вспомогательное вещество. В одном из вариантов реализации настоящего изобретения вспомогательное вещество представляет собой носитель, например мальтодекстрин. В одном из вариантов реализации настоящего изобретения вспомогательное вещество представляет собой безводный коллоидный диоксид кремния. В одном из вариантов реализации настоящего изобретения отношение травяного экстракта к вспомогательному веществу составляет примерно 7:3.
[0021] В одном из вариантов реализации настоящего изобретения растворитель удаляют в блоке 12, 22 и/или 32 посредством распылительной сушки.
[0022] В одном из вариантов реализации настоящего изобретения в блоке 40 травяные экстракты Sambucus nigra : Echinacea purpurea : Centella asiatica объединяют в массовом отношении 2-15:0,5-3:0,5-3, соответственно. В другом варианте реализации настоящего изобретения травяные экстракты Sambucus nigra : Echinacea purpurea : Centella asiatica объединяют в массовом отношении 70:10:20, соответственно.
[0023] Схема синтеза 100 также включает блок 42, включающий объединение воды с объединенным травяным экстрактом блока 40. В одном из вариантов реализации настоящего изобретения воду объединяют в отношении от 3 до 14 литров (л) воды на каждый килограмм (кг) травяного экстракта. В одном из вариантов реализации настоящего изобретения воду объединяют в отношении 9 л воды на каждый кг травяного экстракта. В одном из вариантов реализации настоящего изобретения воду и смесь травяных экстрактов смешивают в течение периода от примерно 6 до примерно 24 часов. В одном из вариантов реализации настоящего изобретения воду и смесь травяных экстрактов смешивают в течение примерно 12 часов.
[0024] Схема синтеза 100 также включает блок 44, включающий объединение спирта со смесью, полученной в блоке 42. В одном из вариантов реализации настоящего изобретения спирт содержит этанол. В одном из вариантов реализации настоящего изобретения применяют 96% или 100% этанол с получением спиртовой смеси, имеющей концентрацию этанола от примерно 50% до примерно 90%. В одном из вариантов реализации настоящего изобретения этанол добавляют до достижения концентрации этанола 70%.
[0025] В одном из вариантов реализации настоящего изобретения спиртовую смесь блока 44 перемешивают в течение периода от примерно 6 до примерно 24 часов, предпочтительно в течение примерно 12 часов.
[0026] Схема синтеза 100 также включает блок 46, включающий удаление нерастворимых материалов из спиртовой смеси, полученной в блоке 44. В одном из вариантов реализации настоящего изобретения нерастворимые материалы удаляют из спиртовой смеси с применением центрифугирования, фильтрования, осаждения или комбинации любого из указанных способов.
[0027] Схема синтеза 100 также включает блок 48, включающий удаление спирта с получением водного травяного раствора. В одном из вариантов реализации настоящего изобретения спирт можно удалять посредством дистилляции или посредством выпаривания с применением роторного испарителя. В одном из вариантов реализации настоящего изобретения спирт представляет собой этанол, и указанный спирт удаляют с применением роторного испарителя при температуре менее 30°С (градусов Цельсия).
[0028] Схема синтеза 100 также включает блок 50, включающий удаление воды из водного раствора блока 48 с получением сухого травяного порошка. Удаление воды можно осуществлять согласно вариантам реализации настоящего изобретения с применением лиофилизации (сублимационной сушки) или распылительной сушки.
[0029] На Фиг. 1b представлена блок-схема, изображающая схему синтеза 200 для синтезирования различных композиций, содержащих экстракты растений видов Sambucus nigra, Echinacea purpurea и Centella asiatica. Схема синтеза 200 включает блок 40, включающий объединение высушенных травяных экстрактов блоков 12, 22 и 32 в схеме синтеза 100, описанной выше.
[0030] В одном из вариантов реализации настоящего изобретения в блоке 40 травяные экстракты Sambucus nigra : Echinacea purpurea : Centella asiatica объединяют в массовом отношении 2-15:0,5-3:0,5-3, соответственно. В другом варианте реализации настоящего изобретения травяные экстракты Sambucus nigra : Echinacea purpurea : Centella asiatica объединяют в массовом отношении 70:10:20, соответственно.
[0031] Схема синтеза 200 также включает блок 62, включающий объединение спирта с объединенным травяным экстрактом блока 40. В одном из вариантов реализации настоящего изобретения спирт применяют в отношении от примерно 3 до примерно 14 л спирта, предпочтительно примерно 9 л спирта, на каждый кг травяного экстракта. В одном из вариантов реализации настоящего изобретения спирт и смесь травяных экстрактов смешивают в течение примерно 12 часов. В одном из вариантов реализации настоящего изобретения спирт содержит этанол. В одном из вариантов реализации настоящего изобретения этанол представляет собой 96%-100% этанол.
[0032] Схема синтеза 200 также включает блок 64, включающий объединение воды со смесью, полученной в блоке 62. В одном из вариантов реализации настоящего изобретения воду применяют с получением спиртовой смеси, имеющей концентрацию этанола от примерно 50% до примерно 90%. В одном из вариантов реализации настоящего изобретения воду применяют до достижения концентрации этанола 70%.
[0033] В одном из вариантов реализации настоящего изобретения спиртовую смесь блока 64 перемешивают. В одном из вариантов реализации настоящего изобретения смесь перемешивают в течение периода от примерно 6 часов до примерно 24 часов, предпочтительно в течение примерно 12 часов.
[0034] Схема синтеза 200 также включает блок 66, включающий удаление нерастворимых материалов из спиртовой смеси, полученной в блоке 64. В одном из вариантов реализации настоящего изобретения нерастворимые материалы удаляют из спиртовой смеси с применением центрифугирования, фильтрования, осаждения или любой комбинации указанных способов.
[0035] Схема синтеза 200 также включает блок 68, включающий удаление спирта с получением водного травяного раствора. В одном из вариантов реализации настоящего изобретения спирт можно удалять с применением дистилляции или выпаривания, например с применением роторного испарителя. В одном из вариантов реализации настоящего изобретения спирт представляет собой этанол, и указанный спирт удаляют с применением роторного испарителя при температуре менее 30°С (градусов Цельсия).
[0036] Схема синтеза 200 также включает блок 70, включающий удаление воды из водного раствора блока 68 с получением сухого травяного порошка. Удаление воды можно осуществлять согласно вариантам реализации настоящего изобретения с применением лиофилизации (сублимационной сушки) или распылительной сушки.
[0037] Пример 1b: Синтез Экстракта N
[0038] Следовали схеме синтеза 100, описанной в примере 1а, со следующими подробностями согласно варианту реализации настоящего изобретения.
[0039] Sambucus nigra (цветочные головки) смешивали с 70% этанолом (отношение растворителя к растению 8:1) согласно блоку 10. После удаления нерастворимого растительного материала и сушки растворителя согласно блоку 12 получили 3,29 кг высушенного экстракта Sambucus nigra.
[0040] Echinacea purpurea (корневище и корни) смешивали с 70% этанолом (отношение растворителя к растению 8:1) согласно блоку 20. После удаления нерастворимого растительного материала и сушки растворителя согласно блоку 22 получили 470 г (граммов) высушенного экстракта Echinacea purpurea.
[0041] Centella asiatica (надземные части) приводили в контакт с 70% этанолом (отношение растворителя к растению 8:1) согласно блоку 30. После удаления нерастворимого растительного материала и сушки растворителя согласно блоку 32 получили 940 г высушенного экстракта Centella asiatica.
[0042] Три высушенных экстракта трех трав (в отношении 70: 10: 20 по массе) объединяли согласно блоку 40. Согласно блоку 42 добавляли 47 л воды, и смесь перемешивали в течение 12 часов. К смеси добавляли 113,9 л 96% этанола с получением 160,9 л спиртовой смеси с концентрацией этанола 70% согласно блоку 44. Смесь фильтровали согласно блоку 46 и нерастворимый материал удаляли. Этанол выпаривали согласно блоку 48 и раствор подвергали распылительной сушке согласно блоку 50 с получением 3,2 кг сухого травяного порошка, называемого Экстрактом N. Выход указанного способа (процент по массе относительно высушенных экстрактов, добавленных согласно блоку 40) составлял 68,7%.
[0043] Пример 1с: Синтез Экстракта Р
[0044] Три высушенных экстракта трех трав (в отношении 70: 10: 20 по массе) объединяли согласно блоку 40 в схеме 100. Затем для получения Экстракта Р следовали схеме 200. Согласно блоку 62 добавляли этанол (100%) в отношении 9 г этанола на каждый 1 г высушенного экстракта. Смесь перемешивали в течение 12 часов. Затем медленно добавляли воду до достижения конечной концентрации этанола 70% согласно блоку 64. Смесь центрифугировали согласно блоку 66 и нерастворимый материал удаляли. Этанол выпаривали с применением роторного испарителя в вакууме согласно блоку 68 и раствор лиофилизировали согласно блоку 70 с получением сухого травяного порошка, называемого Экстрактом Р. Выход Экстракта Р (процент по массе относительно высушенных экстрактов, добавленных согласно блоку 40) составлял 75%.
[0045] Пример 1d: Синтез Экстракта D
[0046] Три высушенных экстракта трех трав (в отношении 70:10:20 по массе) объединяли согласно блоку 40 в схеме 100. Водную смесь получали согласно блоку 42, как описано в примере 1b, и смесь смешивали в течение примерно 17-20 часов. Нерастворимые материалы удаляли из раствора посредством центрифугирования водного раствора и фильтрования с применением фильтра 0,2 микрона. Воду удаляли из фильтрата посредством лиофилизации в течение ночи. Высушенной травяной смеси дали название Экстракт D.
[0047] Пример 1е: Синтез Экстракта В
[0048] Травяной экстракт получали согласно примеру 1а до блока 40. Объединенному травяному экстракту дали название Экстракт В.
[0049] Пример 1f: Синтез Экстракта М:
[0050] Травяной экстракт получали согласно примеру 1а (до блока 40). К объединенному травяному экстракту добавляли 100% этанол и перемешивали в течение 12 часов. К этанольной смеси добавляли воду до достижения концентрации этанола 30%. Затем этанол удаляли с применением роторного испарителя, а затем воду удаляли посредством лиофилизации. Полученному экстракту дали название Экстракт М.
[0051] Пример 2: Химический анализ композиций согласно вариантам реализации настоящего изобретения
[0052] Экстракты согласно вариантам реализации настоящего изобретения включают соединения, обладающие множественной биологической активностью, включая противовоспалительную активность. Для определения химических различий между Экстрактом D и Экстрактом N осуществляли количественный анализ методом ВЭЖХ (высокоэффективной жидкостной хроматографии).
[0053] ВЭЖХ анализ осуществляли с применением колонки Phenomenex Synergi 4 микрометра Hydro-RP 80А с применением 0,01 молярного раствора фосфорной кислоты в воде и ацетонитрила в качестве растворителей для подвижной фазы. Обнаружение осуществляли с применением диодно-матричного детектора.
[0054] Одно из противовоспалительных соединений, определенных в экстрактах согласно вариантам реализации настоящего изобретения, которое происходит из растения Sambucus nigra, представляет собой нарингенин. Для определения количества нарингенина в образцах травяных экстрактов получали маркер с применением нарингенина (полученного от Sigma).
[0055] ВЭЖХ анализ осуществляли в отношении Экстрактов D и N из различных партий. Перед проведением анализа Экстракты D и N разводили до 1% растворов в растворителе, содержавшем 50% ацетонитрила/50% воды. Результаты приведены в таблице 1 ниже, при этом содержание нарингенина выражено в процентах от экстракта.

[0057] Экстракт Р анализировали и определяли содержание нарингенина аналогично Экстракту N.
[0058] Как следует из таблицы 1, концентрация нарингенина постоянно была выше в Экстракте N, чем в Экстракте D, что свидетельствует о том, что Экстракт N имеет улучшенные противовоспалительные свойства по сравнению с Экстрактом D.
[0059] Пример 3: In vitro испытание композиций согласно вариантам реализации настоящего изобретения
[0060] Биологические свойства Экстракта D и Экстракта N сравнивали на различных in vitro моделях.
[0061] Пример 3а: ICE анализ
[0062] ICE (интерлейкин-1β-конвертирующий фермент или ICE-каспаза-1) является членом семейства цистеиновых протеаз, специфичных к аспарагиновой кислоте, который играет ключевую роль в воспалении. Ингибирование ICE посредством Экстрактов D и N определяли для концентраций экстрактов 2,5, 1,25 и 0,625 мг/мл (миллиграммов на миллилитр) с применением следующего способа.
[0063] Пептидный субстрат со структурой Ac-YVAD-AMC представляет собой флуорогенный субстрат для ICE, который содержит флуорохром 7-амино-4-метилкумарин (АМК). АМК выделяют из указанного субстрата в результате расщепления посредством ICE. Интенсивность флуоресцентного сигнала, полученного в результате расщепления, пропорциональна активности ICE, присутствующего в образце. В качестве контрольного образца для возможного ингибирования применяли известный селективный ингибитор ICE, Ac-YVAD-CHO. Для обнаружения флуоресценции образцов применяли черный 96-луночный планшет с флуоресцентным планшетным ридером.
[0064] Результаты ICE анализа представлены на фигуре 2а. Во всех испытанных концентрациях ингибирование ICE с применением Экстракта N превосходило ингибирование с применением Экстракта D. Результаты показывают, что Экстракт N обладает повышенной противовоспалительной активностью по сравнению с Экстрактом D.
[0065] Пример 3d: Анализ выделения коллагена
[0066] Коллагены представляют собой белки, которые в большом количестве присутствуют в соединительной ткани и играют важную роль в заживлении ран. Агенты, которые вызывают выделение коллагена в дермальных фибробластах (клетках, которые способствуют образованию соединительной ткани) могут подходить для применения в качестве агентов, заживляющих раны. Влияние Экстрактов D и N на выделение коллагена в дермальных фибробластах исследовали с применением следующей процедуры.
[0067] Фибробласты крайней плоти человека применяли в «сэндвич»-методе твердофазного ИФА (твердофазного иммуноферментного анализа) на основе пары антител, которые распознают человеческий коллаген 1 типа. Использованные антитела представляли собой козьи антитела к коллагену 1 типа (Goat anti type 1 Collagen), а именно немеченое захватывающее антитело (приобретенное у Southern Biotech, США, каталожный номер 1310-01) и конъюгат детекторного антитела с биотином (приобретенный у Southern Biotech, США, каталожный номер 1310-08).
[0068] Влияние Экстрактов D и N на выделение коллагена исследовали с применением концентраций 1,5, 0,75, 0,38 и 0,19 мг/мл. Результаты анализа выделения коллагена представлены на Фигуре 2b. Во всех испытанных концентрациях Экстракт N обладал большей эффективностью в индуцировании выработки коллагена, чем Экстракт D, что свидетельствует о том, что Экстракт N обладает лучшей способностью к заживлению ран, чем Экстракт D.
[0069] Пример 3с: Репортерный анализ NFκB
[0070] Белок NFκB играет ключевую роль в воспалении, иммунном ответе, пролиферации клеток и защите от апоптоза.
[0071] Линию мышиных клеток-макрофагов RAW264.7 (полученную из Американской коллекции типовых культур (American Type Culture Collection)) трансдуцировали с применением репортерной конструкции NF-κВ и люциферазы и применяли в анализе для определения ингибирующего действия Экстрактов D и N на индукцию белка NF-κВ в клетках, содержавших конструкцию NF-κВ и репортерного гена люциферазы. Липополисахарид (ЛПС) применяли для индуцирования NF-κВ-люциферазного репортера и экстракты испытывали на ингибирующую активность. Кальцеин AM (ацетометоксипроизводное кальцеина) применяли в качестве флуоресцентного красителя для определения количества клеток RAW264.7 для нормализации. Поскольку люминесценцию в модели сопоставляют с экспрессией белка NF-κВ, ингибирование экспрессии может быть определено посредством сопоставления с ингибированием люминесценции.
[0072] Высокий процент ингибирования в указанной модели для композиций свидетельствует о возможности применения указанных композиций для уменьшения воспаления посредством ингибирования белка NF-κВ у млекопитающих. Исследовали влияние Экстрактов D и N в концентрациях 1, 0,25 и 0,12 мг/мл на NF-κВ-люциферазный репортер, и результаты представлены на фигуре 2 с. В двух более низких концентрациях Экстракт N обладал большей эффективностью в ингибировании индукции NF-κВ-люциферазного репортера, чем Экстракт D, что свидетельствует о том, что Экстракт N имеет улучшенные противовоспалительные свойства по сравнению с Экстрактом D и является эффективным в низких дозах.
[0073] Пример 3d: Анализ выделения оксида азота (II)
[0074] Оксид азота (II) (NO) представляет собой важный физиологический мессенджер и эффекторную молекулу, которая вовлечена в процесс воспаления. Ингибирование выработки N0 в клетках может быть показателем противовоспалительных свойств композиций. Экстракты D и N испытывали на NO ингибирующие свойства согласно следующему анализу.
[0075] Для анализа применяли клетки RAW264.7. Наличие NO определяли с применением набора реактивов Грисса, с помощью которого определяют нитрит, один из двух основных стабильных и нелетучих продуктов разложения NO. Нитрит вступает в реакцию с сульфаниламидом и N-1-нафтилэтилендиамин дигидрохлоридом (НЭДА) в кислых (фосфорная кислота) условиях с получением флуоресцентного азосоединения, которое обнаруживают с помощью планшетного ридера. Для индуцирования воспаления в клетках RAW264.7 применяли ЛПС, и ингибирование воспаления исследовали с применением 1,0, 0,5, 0,25 и 0,13 мг/мл Экстрактов D и N.
[0076] Высокий процент ингибирования в указанной модели для композиций свидетельствует о возможности применения указанных композиций для уменьшения воспаления посредством ингибирования выработки NO у млекопитающих. Влияние Экстрактов D и N на выработку NO представлено на фигуре 2d. Во всех концентрациях Экстракт N обладал большей эффективностью в ингибировании выработки NO, чем Экстракт D, что свидетельствует о том, что Экстракт N имеет улучшенные противовоспалительные свойства по сравнению с Экстрактом D.
[0077] Пример 3е: Твердофазный ИФА IL-11 (интерлейкина-11)
[0078] Анализ осуществляли для исследования влияния травяных экстрактов на цитокин-индуцируемое выделение IL-11 в фибробластах, свидетельствующее о мукозальном защитном эффекте. Анализ осуществляли в отношении десневых фибробластов человека.
[0079] Линии клеток, представлявших собой десневые фибробласты, высевали в 150 мкл (микролитрах) питательной среды в 96-луночных планшетах для тканевых культур с начальной плотностью посева 104 клеток/лунка и культивировали в течение 24 часов. Питательную среду удаляли, а затем клетки, представлявшие собой десневые фибробласты, активировали с применением ТРФ-β (трансформирующего ростового фактора бета) в конечной концентрации 2,0 нг/мл (нанограммов на миллилитр), добавленного в 150 мкл БСА-среды (бычьего сывороточного альбумина). Также добавляли травяные экстракты в концентрации 0,5 мг/мл и культуры инкубировали в течение дополнительных 24 часов. Также испытывали только ТРФ-β для того, чтобы определить степень синергии между травяным экстрактом и фактором роста.
[0080] Для определения концентрации IL-11 отбирали образец кондиционированной среды (100 мкл) и клетки, представлявшие собой десневые фибробласты, совместно с оставшимися 50 мкл среды исследовали в ходе люминесцентного анализа жизнеспособности клеток для нормализации результатов. Обеспечивали отрицательный контроль без добавления цитокина. Влияние материалов образца на выработку IL-11 измеряли посредством твердофазного ИФА согласно инструкциям производителя с применением коммерчески доступного набора (R&D Systems, каталожный номер DY 218, MN, США).
[0081] Для каждого экстракта определяли результаты выработки IL-11 в единицах пг/мл (пикограмм/миллилитр) как в присутствии, так и в отсутствии ТРФ-β. Затем с указанными результатами производили вычисления для определения единиц синергии (synergy units), которые представляют собой (концентрацию IL-11 в присутствии ТРФ-β и экстракта)/(концентрацию IL-11 в присутствии только ТРФ-β) + (концентрацию IL-11 в присутствии только экстракта). Значение 1 согласно вышеуказанной формуле свидетельствует о том, что значение, полученное для ТРФ-β + экстракта, совместно добавленных к клеткам, совпадает с суммой значений, полученных для каждого из них, добавленных к десневым фибробластным клеткам по отдельности. Указанное равенство представляет собой аддитивный эффект. Значения больше 1 свидетельствуют о синергическом эффекте травяного экстракта.


[0083] Как можно видеть в таблице 2, Экстракты N и Р демонстрировали синергическую активность, а Экстракт М не демонстрировал синергической активности.
[0084] Пример 4: In vivo испытание композиций согласно вариантам реализации настоящего изобретения с применением модели мукозита полости рта (орального мукозита, ОМ) у хомячков
[0085] Самцов сирийских золотистых хомячков (Syrian Golden Hamsters) («хомячков») массой примерно 95 г случайным образом распределяли по двум контрольным группам, получавшим плацебо, по восемь хомячков в каждой и четырем группам испытываемых образцов по шесть хомячков в каждой. На 0 день исследования каждого хомячка подвергали острому облучению в дозе 40 Гр (грей), направленному на левый защечный мешок. Испытываемые образцы вводили местно три раза в сутки в период от -1 (дня перед получением дозы облучения) до 20 дня. Состояние хомячков оценивали ежедневно и массу тела измеряли один раз в сутки в период от -1 дня до 25 дня. Мукозит оценивали на 7, 10, 13, 16, 19, 22 и 25 день. Производили сравнение продолжительности и тяжести мукозита между группами, подвергавшимися лечению, и не подвергнутой лечению контрольной группой для определения влияния испытываемого образца на течение мукозита.
[0086] Мукозит у хомячков оценивали в баллах согласно таблице 3:


[0087] Двум контрольным группам, получавшим плацебо, вводили или физиологический раствор, или пропиленгликоль (ПГ). Четырем группам, подвергавшимся лечению, вводили лекарственные средства следующим образом:
[0088] Группа 1: 1% Экстракта В в 100% PG;
[0089] Группа 2: 1% Экстракта М в 100% PG;
[0090] Группа 3: 1% Экстракта N в 100% PG;
[0091] Группа 4: 1% Экстракта N, растворенного в физиологическом растворе с последующим перемешиванием вихревым способом в течение одной минуты.
[0092] Каждому хомячку вводили 0,2 мл испытываемых композиций три раза в сутки. Общее число дней, в которые хомячок получал повышенный балл, то есть балл выше трех, суммировали для каждой группы и выражали в виде процента от общего числа дней, в которые производили выставление баллов, для каждой группы. Результаты представлены на фигуре 3.
[0093] Экстракт N в физиологическом растворе оказывал значительное (р=0,024) влияние на снижение балльной оценки мукозита по сравнению с контрольной группой, получавшей физиологический раствор. Аналогично Экстракт N в ПГ оказывал значительное (р=0,003) влияние на снижение балльной оценки мукозита по сравнению с контрольной группой, получавшей ПГ. Экстракты В и М не демонстрировали снижение баллов хомячков ниже 3 по сравнению с контрольной группой, получавшей ПГ.
[0094] Результаты указанного испытания свидетельствуют о том, что Экстракт N может быть эффективным в лечении ОМ у людей. Указанный эффект проявлялся в случае составов Экстракта N на основе воды (физиологического раствора) или ПГ.
[0095] Пример 5: Повышенная растворимость композиций согласно вариантам реализации настоящего изобретения
[0096] Испытание на растворимость осуществляли, чтобы различить Экстракт В и Экстракт N.
[0097] Растворы экстрактов получали с применением Экстрактов В и N в концентрациях 1% (граммов на литр) в воде. При перемешивании оба раствора были мутными. Экстракт В содержал частицы, которые можно было различить на глаз, и которые при перемешивании плавали по окружности в довольно прозрачном растворе. Экстракт N содержал незаметные частицы, хотя раствор был мутным, обеспечивая более однородную дисперсию. Мутность измеряли с применением турбидиметра Micro 100 Turbidimeter, произведенного HF Scientific, и выражали в нефелометрических единицах мутности (НЕМ). Как можно видеть в таблице ниже, существует значительная разница в мутности двух составов с большими частицами в В, выпадающими в осадок намного быстрее, чем частицы в N.
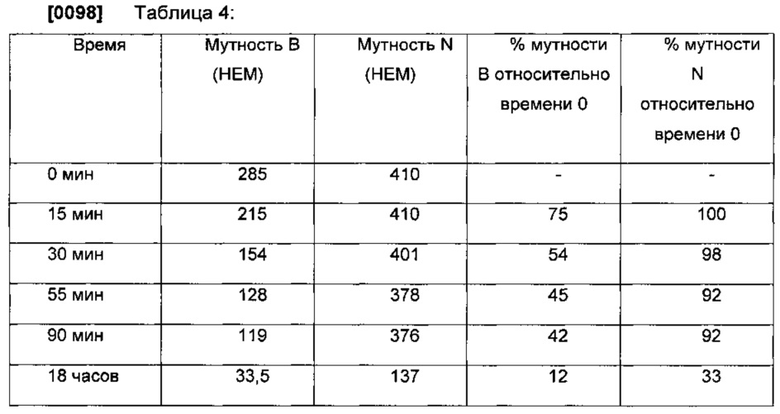
[0099] Растворы в 100% ПГ получали в концентрации 5% (граммов на литр). Экстракт N, по-видимому, полностью растворялся, однако Экстракт В был мутным. Мутность измеряли после перемешивания и получили 385 НЕМ для Экстракта В и 14,7 НЕМ для Экстракта N. После выдерживания в течение ночи большое количество взвешенных частиц выпадало в осадок из суспензии Экстракта В, и не было видимых взвешенных частиц в прозрачной смеси Экстракта N.
[00100] Указанные испытания свидетельствуют о том, что Экстракт N обладает более высокой растворимостью и образует более стабильные суспензии в воде, чем Экстракт В. Кроме того, растворы в ПГ могут быть приготовлены с применением экстракта N в концентрации 5-20% (по массе), в то время как Экстракт В не обеспечивает стабильных растворов в указанных концентрациях. Экстракт N может быть подходящим образом приготовлен в ПГ без необходимости в дополнительных солюбилизирующих агентах.
[00101] Пример 6а: Фармацевтические композиции, содержащие экстракты согласно вариантам реализации настоящего изобретения
[00102] 2,601 кг Экстракта N перемешивали в течение 12 часов с 10,379 кг ПГ и 26,01 г сукралозы с получением концентрированного раствора. 2,5 г концентрированного раствора смешивали с 47,5 мл физиологического раствора с получением ополаскивателя для полости рта.
[00103] Пример 6b: Фармацевтические композиции, содержащие экстракты согласно дополнительным вариантам реализации настоящего изобретения
[00104] В дополнительных вариантах реализации настоящего изобретения композиция согласно настоящему изобретению дополнительно содержит экстракт растения вида Hypericum perforatum (зверобой продырявленный) и Commiphora molmol (коммифора мирровая), Uncaria tomentosa (ункария опушенная), Thymus vulgaris (тимьян обыкновенный), Matricaria recutita (ромашка аптечная), Salix alba (ива белая), Calendula officinalis (календула лекарственная), Usnea barbata (уснея бородатая), Ligusticum porterii-osha (бороздоплодник портери или оша), Gaultheria procumbens (гаультерия лежачая), Camellia sinensis (чайный куст), Vaccinium myrtilltus (черника миртолистная), Melissa officinalis (мелисса лекарственная), Allium sativum (чеснок), Camellia sinensis (чайный куст), Hamamelis virginiana (гамамелис вирджинский) или Krameria triandra (крамерия трехтычинковая).
[00105] В дополнительных вариантах реализации настоящего изобретения фармацевтические композиции могут быть получены в форме пластырей, мазей, паст, лосьонов, кремов, пастилок, конфет, жевательных резинок, растворов, гелей, пен и спреев. Согласно вариантам реализации настоящего изобретения фармацевтические композиции могут быть получены в виде композиций с быстрым высвобождением или замедленным высвобождением.
[00106] Пример 7а: Способы лечение с применением композиций согласно вариантам реализации настоящего изобретения
[00107] ОМ является одним из наиболее часто отмечаемых и, вероятно, наиболее ослабляющих патологических состояний, обусловленных химиотерапией и лучевой терапией рака, при этом заболеваемость находится в диапазоне 10%-75% среди пациентов, получающих химиотерапию или лучевую терапию, 70-90% среди реципиентов трансплантата костного мозга и составляет >95% среди пациентов, получающих комбинацию лучевой терапии и химиотерапии при лечении рака головы и шеи (РГШ). ОМ был связан с повышенным применением болеутоляющих средств и антибиотиков, днями лихорадочного состояния, необходимостью применения желудочного зонда или парентерального питания, продолжительностью госпитализации, незапланированными и срочными посещениями врача и общими медицинскими расходами, причем все вышеперечисленное оказывает негативное влияние на здоровье и экономические показатели. Ежегодно в США ОМ развивается у примерно 500000 пациентов, и считается, что указанное развитие в большинстве случаев невозможно предотвратить.
[00108] Двойное слепое, рандомизированное, плацебо-контролируемое, сравнительное исследование с фиксированной дозой, в котором испытывали воздействие ополаскивателя для полости рта согласно примеру 6а в случае ОМ, осуществляли в отношении пациентов, подвергнутых ХЛТ (химиолучевой терапии) при РГШ. Пациентов случайным образом распределяли по группам для получения или активного ополаскивателя для полости рта, или плацебо согласно схеме рандомизации 1:1. Доза ополаскивателя составляла 15 мл 1% ополаскивателя для полости рта, описанного в примере 6, при частоте полоскания три раза в сутки. Плацебо получали с применением ПГ, сукралозы и пищевого красителя, разведенные в физиологическом растворе.
[00109] Примерно 104 субъекта получали лечение в течение примерно 7-9 недель, проводившееся одновременно с ХЛТ и продолжавшееся до регрессии тяжелого мукозита. Согласно плану субъекты получали непрерывный курс внешнего облучения, производимого с применением модулированной по интенсивности лучевой терапии или объемного (3D) планирования. Кумулятивная назначенная доза составляла 50-70 Гр. Участок полости рта, составлявший минимум 25%, получал дозу 50 Гр или более. Лучевую терапию проводили одновременно с химиотерапией с применением цисплатина в дозе 60-100 мг/м2 (милиграммов на квадратный метр), вводимой раз в 21 сутки, или 30-40 мг/м2, вводимой раз в неделю.
[00110] Безопасность оценивали с помощью общей токсичности на основе основных показателей состояния организма и медицинских осмотров. Эффективность оценивали посредством отношения количества пациентов в группе, подвергавшейся активному лечению, к количеству пациентов в группе плацебо, получивших 3-4 балла по шкале пероральной токсичности ВОЗ (Всемирной организации здравоохранения) для ОМ при кумулятивной дозе облучения 50 Гр.
[00111] Шкала пероральной токсичности ВОЗ для ОМ выглядит следующим образом: балл 0 соответствует отсутствию мукозита или поражений слизистой оболочки; балл 1 соответствует эритеме, чувствительности слизистой оболочки и боли в слизистой оболочке; балл 2 соответствует изъязвлению, способности принимать твердую пищу; балл 3 соответствует изъязвлению, пероральному приему пищи, ограниченному приемом жидкостей; балл 4 соответствует изъязвлению, невозможности перорального приема пищи.
[00112] В открытой части испытания семерых пациентов подвергали воздействию фармацевтической композиции, описанной в примере 6а. График, демонстрирующий балл ОМ относительно кумулятивной дозы облучения, представлен на фигуре 4. Пациенты 5 и 6 при прохождении курса лечения получали совпадающие баллы и обозначены одной линией.
[00113] В испытываемой популяции пациентов у примерно 75% пациентов, которые получали равные кумулятивные дозы облучения полости рта, на основании статистических данных ожидали развития ОМ 3-4 баллов. Один из пациентов выбыл из испытания после очень короткого периода лечения из-за выраженной аллергической реакции на один из компонентов композиции. Из оставшихся 6 пациентов 4 считались имевшими благоприятный ответ на лечение, так как балльная оценка в случае указанных пациентов не превышала 1 на всем протяжении лечения. Еще один пациент считался частично ответившим на лечение, так как развитие ОМ у пациента началось только после получения пациентом кумулятивной дозы облучения >40 Гр.
[00114] Результаты открытой части испытания демонстрируют, что композиции, полученные согласно вариантам реализации настоящего изобретения, эффективны в лечении пациентов, подверженных риску развития ОМ, включая пациентов, которые получили облучение полости рта. Аналогичные результаты ожидают от полного испытания.
[00115] Пример 7b: Применение композиций согласно вариантам реализации настоящего изобретения в отношении пациента, страдающего от ОМ
[00116] Пациента в возрасте примерно 80 лет, страдавшего от рака поджелудочной железы, в течение 3 лет периодически подвергали лечению с применением химиотерапии и облучения. Было установлено, что пациент страдал от ОМ, и указанного пациента подвергали лечению с применением композиции Q (получение описано ниже) в течение примерно 2-3 недель. Значительного улучшения состояния больного ОМ выявлено не было.
[00117] Композицию Q получали с применением следующего способа. Получали этанольные экстракты трав Sambucus nigra, Echinacea purpurea и Centella asiatica, а затем указанные экстракты объединяли в отношении 85:5:10. Затем смесь подвергали экстракции водой в отношении 9 л воды на каждый 1 кг объединенного травяного экстракта. Нерастворимый материал удаляли и растворимую фазу фильтровали. Затем из растворимой фазы готовили композицию Q посредством объединения с водой, динатрия ЭДТА, бензоатом натрия, цетилпиридиний хлоридом моногидратом, ПЭГ-40 гидрированным касторовым маслом 90%, S-молочной кислотой, сорбитом, ПГ, ароматизатором и эриоглауцином. Концентрация твердого вещества в растворимой фазе в случае композиции Q составляла 1%.
[00118] Через 2-3 недели введение композиции Q прекращали, после чего пациенту вводили композицию согласно примеру 6. В течение 25 часов пациент ощутил заметное уменьшение боли, а также произошло уменьшение размера изъявленных участков.
[00119] Помимо лечения ОМ другие заболевания, связанные с воспалением слизистой оболочки, могут быть подвергнуты лечению с применением экстрактов согласно вариантам реализации настоящего изобретения. Слизистая оболочка, подвергнутая лечению с применением экстрактов согласно вариантам реализации настоящего изобретения, может включать слизистую оболочку щеки, пищевода, желудка, кишечника, носа, обонятельной области, полости рта, бронхов, матки, внутриматочную слизистую оболочку, слизистую оболочку влагалища или пениса. Воспалительные заболевания согласно варианту реализации настоящего изобретения включают воспаление кишечника, радиационный проктит и атрофический вагинит.
[00120] Композиции, содержащие экстракты согласно вариантам реализации настоящего изобретения, могут быть применены для лечения или предотвращения различных заболеваний и симптомов. В одном из вариантов реализации настоящего изобретения композиция предназначена для применения в лечении заболеваний слизистой оболочки полости рта. В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении заболевания слизистой оболочки полости рта, выбранного из группы, состоящей из пародонтоза, гингивита, афтозного изъязвления, механической травмы, термической травмы, красного плоского лишая, буллезного пемфигоида, обыкновенной пузырчатки, герпетиформного дерматита, ангулярного хейлита и рецидивирующего герпеса.
[00121] В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении повреждений кожи. В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении травмы кожи. В другом предпочтительном варианте реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении укусов насекомых и других местных поверхностных раздражений.
[00122] В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении анальных повреждений. В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении анального повреждения, связанного с патологическим состоянием, выбранным из группы, состоящей из трещин заднего прохода, геморроя и неспецифического раздражения.
[00123] В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении вагинальных повреждений. В одном из вариантов реализации настоящего изобретения терапевтическая композиция предназначена для применения в лечении вагинального повреждения, связанного с атрофическим вагинитом.
[00124] В вариантах реализации настоящего изобретения предложены способы лечения, включающие введение от 1 мг до 1,5 г травяного экстракта в сутки. В вариантах реализации настоящего изобретения суточная доза составляет 625 мг/сутки. В вариантах реализации настоящего изобретения суточная доза составляет 450 мг/сутки. В другом варианте реализации настоящего изобретения суточная доза составляет 900 мг/сутки.
[00125] Согласно варианту реализации настоящего изобретения дополнительно предложен способ получения водной терапевтической композиции, включающий объединение водно-спиртовых травяных экстрактов Sambucus nigra, Echinacea purpurea и Centella asiatica с водой с получением водной смеси; объединение водной смеси со спиртом с получением спиртовой смеси, имеющей концентрацию спирта более 50%; отделение нерастворимых материалов и спирта от спиртовой смеси с получением водной терапевтической композиции. Спиртовая смесь необязательно содержит примерно 70% спирта. Водную терапевтическую композицию необязательно дополнительно сушат с получением высушенной терапевтической композиции. Спирт необязательно представляет собой этанол. Нерастворимые материалы необязательно отделяют от спиртовой смеси с применением центрифугирования, фильтрования или осаждения. Спирт необязательно отделяют от спиртовой смеси с применением вакуума. Водную терапевтическую композицию необязательно сушат посредством распылительной сушки или сублимационной сушки. Способ необязательно дополнительно включает объединение высушенной терапевтической композиции с по меньшей мере одним фармацевтически приемлемым вспомогательным веществом. Вспомогательное вещество необязательно выбрано из группы, состоящей из пропиленгликоля, полиэтиленгликоля, глицерина и эфирного масла. Водно-спиртовые травяные экстракты Sambucus nigra, Echinacea purpurea и Centella asiatica необязательно получают посредством смешивания растительного материала в растворителе, содержащем примерно 70% спирта. Растительный материал необязательно смешивают в течение примерно 8 часов. Отношение растительного материала к растворителю необязательно составляет примерно 1:8. Способ необязательно дополнительно включает удаление растворителя из смеси растительного материала и растворителя с получением водно-спиртового травяного экстракта.
[00126] Согласно варианту реализации настоящего изобретения дополнительно предложен травяной экстракт, содержащий водно-спиртовые травяные экстракты каждого из растений Sambucus nigra, Echinacea purpurea и Centella asiatica, причем указанный экстракт содержит нарингенин в концентрации выше или равной 0,055%. Травяной экстракт необязательно растворим в пропиленгликоле в виде 20% раствора. Отношение Sambucus nigra : Echinacea purpurea : Centella asiatica необязательно составляет примерно 7:1:2.
[00127] Согласно варианту реализации настоящего изобретения дополнительно предложена фармацевтическая композиция, содержащая травяной экстракт, содержащий водно-спиртовые травяные экстракты каждого из растений Sambucus nigra, Echinacea purpurea и Centella asiatica, причем указанный экстракт содержит нарингенин в концентрации выше или равной 0,055%. Фармацевтическая композиция необязательно дополнительно содержит фармацевтически приемлемый носитель. Носитель необязательно содержит пропиленгликоль. Фармацевтическая композиция согласно варианту реализации настоящего изобретения необязательно находится в форме ополаскивателя для полости рта, пластыря, мази, пасты, лосьона, крема, пастилки, конфеты, жевательной резинки, раствора, геля, пены или спрея.
[00128] Согласно варианту реализации настоящего изобретения дополнительно предложен способ лечения заболевания, включающий введение фармацевтически приемлемого количества фармацевтической композиции, содержащей травяной экстракт, содержащий водно-спиртовой травяные экстракты каждого из растений Sambucus nigra, Echinacea purpurea и Centella asiatica, причем указанный экстракт содержит нарингенин в концентрации выше или равной 0,055%. Указанное заболевание необязательно представляет собой заболевание слизистой оболочки или кожи. Указанное заболевание необязательно представляет собой воспалительное заболевание. Указанное заболевание необязательно облегчают посредством восстановления тканей. Заболевание необязательно выбрано из группы, состоящей из мукозита полости рта, воспаления кишечника, радиационного проктита, атрофического вагинита, пародонтоза, гингивита, афтозного изъязвления, механической травмы, термической травмы, красного плоского лишая, буллезного пемфигоида, обыкновенной пузырчатки, герпетиформного дерматита, ангулярного хейлита и рецидивирующего герпеса. Количество вводимого травяного экстракта необязательно составляет от 1 мг до 1,5 г в сутки.
[00129] В описании и формуле настоящей заявки каждый из глаголов «содержать», «включать» и «иметь», а также слова, представляющие собой результат спряжения указанных глаголов, используют для указания на то, что объект или объекты глагола не обязательно представляют собой полный перечень компонентов, элементов или частей субъекта или субъектов указанного глагола.
[00130] Описания вариантов реализации настоящего изобретения в настоящей заявке предоставлены в качестве примера и не предназначены для ограничения объема настоящего изобретения. Описанные варианты реализации настоящего изобретения включают различные признаки, не все из которых необходимы во всех вариантах реализации настоящего изобретения. В некоторых вариантах реализации настоящего изобретения использованы только некоторые из признаков или возможных комбинаций признаков. Изменения вариантов реализации настоящего изобретения, которые описаны, и варианты реализации настоящего изобретения, включающие различные комбинации признаков, упомянутых в описанных вариантах реализации настоящего изобретения, будут очевидны специалистам в данной области. Объем настоящего изобретения ограничен только формулой.
Изобретение относится к фармацевтической промышленности, в частности к способу получения экстракта для лечения ран, воспалительных заболеваний или орального мукозита. Способ получения комбинированного травяного экстракта для лечения ран, воспалительных заболеваний или орального мукозита, включает: объединение водно-спиртовых травяных экстрактов Sambucus nigra, Echinacea purpurea и Centella asiatica с водой и спиртом с получением спиртовой смеси, имеющей концентрацию спирта более 50%, причем массовое соотношение экстрактов Sambucus nigra: Echinacea purpurea: Centella asiatica в высушенном состоянии составляет 2-15: 0,5-3: 0,5-3; и отделение нерастворимых веществ и спирта от указанной спиртовой смеси с получением водного экстракта; и высушивание указанного водного экстракта с получением высушенного экстракта, причем не менее 0,055% указанного комбинированного травяного экстракта в высушенном состоянии составляет нарингенин и при этом указанный экстракт полностью растворим в пропиленгликоле в массовой концентрации от 5 до 20%. Предложен комбинированный травяной экстракт для лечения ран, воспалительных заболеваний или орального мукозита. Предложена фармацевтическая композиция для лечения ран, воспалительных заболеваний или орального мукозита, а также способ лечения ран, включающий введение фармацевтически приемлемого количества фармацевтической композиции; cпособ лечения воспалительного заболевания слизистой оболочки или кожи, включающий введение фармацевтически приемлемого количества фармацевтической композиции и способ лечения орального мукозита, включающий введение фармацевтически приемлемого количества фармацевтической композиции. Вышеописанный экстракт и композиции на его основе эффективны для лечения ран, воспалительных заболеваний или орального мукозита, обладают выраженной ранозаживляющей и противовоспалительной активностью. 6 н. и 20 з.п. ф-лы, 4 ил., 4 табл., 7 пр.
1. Способ получения комбинированного травяного экстракта для лечения ран, воспалительных заболеваний или орального мукозита, включающий:
объединение водно-спиртовых травяных экстрактов Sambucus nigra, Echinacea purpurea и Centella asiatica с водой и спиртом с получением спиртовой смеси, имеющей концентрацию спирта более 50%, причем массовое соотношение экстрактов Sambucus nigra:Echinacea purpurea: Centella asiatica в высушенном состоянии составляет 2-15:0,5-3: 0,5-3; и
отделение нерастворимых веществ и спирта от указанной спиртовой смеси с получением водного экстракта; и
высушивание указанного водного экстракта с получением высушенного экстракта, причем не менее 0,055% указанного комбинированного травяного экстракта в высушенном состоянии составляет нарингенин и при этом указанный экстракт полностью растворим в пропиленгликоле в массовой концентрации от 5 до 20%.
2. Способ по п. 1, отличающийся тем, что спиртовая смесь содержит 70% спирта.
3. Способ по п. 1, отличающийся тем, что массовое отношение экстрактов Sambucus nigra:Echinacea purpurea:Centella asiatica в высушенном состоянии составляет 7:1:2.
4. Способ по п. 1, отличающийся тем, что спирт представляет собой этанол.
5. Способ по п. 1, отличающийся тем, что нерастворимые вещества отделяют от спиртовой смеси с применением центрифугирования, фильтрования и/или осаждения.
6. Способ по п. 1, отличающийся тем, что спирт отделяют от спиртовой смеси с применением вакуума или дистилляции.
7. Способ по п. 1, отличающийся тем, что комбинированный травяной экстракт сушат посредством распылительной сушки или сублимационной сушки.
8. Способ по п. 1, дополнительно включающий объединение высушенного комбинированного травяного экстракта с по меньшей мере одним фармацевтически приемлемым вспомогательным веществом.
9. Способ по п. 8, отличающийся тем, что вспомогательное вещество выбрано из группы, состоящей из пропиленгликоля, полиэтиленгликоля, глицерина и эфирного масла.
10. Способ по п. 1, отличающийся тем, что водно-спиртовые травяные экстракты каждого из растений Sambucus nigra, Echinacea purpurea и Centella asiatica получают посредством смешивания растительного материала в растворителе, содержащем 70% спирта.
11. Способ по п. 10, отличающийся тем, что растительный материал смешивают в течение 8 ч.
12. Способ по п. 11, отличающийся тем, что отношение растительного материала к растворителю составляет 1:8.
13. Способ по п. 10, дополнительно включающий удаление растворителя из смеси растительного материала и растворителя с получением водно-спиртового травяного экстракта.
14. Комбинированный травяной экстракт для лечения ран, воспалительных заболеваний или орального мукозита, полученный из водно-спиртовых травяных экстрактов каждого из растений Sambucus nigra, Echinacea purpurea и Centella asiatica согласно способу по любому из пп. 1-13, причем не менее 0,055% указанного комбинированного травяного экстракта в высушенном состоянии составляет нарингенин, и указанный комбинированный травяной экстракт в высушенном состоянии растворим в пропиленгликоле в массовой концентрации от 5 до 20%.
15. Фармацевтическая композиция для лечения ран, воспалительных заболеваний или орального мукозита, содержащая травяной экстракт по п. 14.
16. Фармацевтическая композиция по п. 15, дополнительно содержащая фармацевтически приемлемый носитель.
17. Фармацевтическая композиция по п. 16, отличающаяся тем, что указанный носитель содержит пропиленгликоль.
18. Фармацевтическая композиция по п. 15 в форме ополаскивателя для полости рта, пластыря, мази, пасты, лосьона, крема, пастилки, конфеты, жевательной резинки, раствора, геля, пены или спрея.
19. Способ лечения ран, включающий введение фармацевтически приемлемого количества фармацевтической композиции по п. 15.
20. Способ по п. 19, отличающийся тем, что рана выбрана из механической травмы или термической травмы.
21. Способ по п. 19, отличающийся тем, что вводимая композиция содержит от 1 мг до 1,5 г комбинированного травяного экстракта в высушенном состоянии в сутки.
22. Способ лечения восспалительного заболевания слизистой оболочки или кожи, включающий введение фармацевтически приемлемого количества фармацевтической композиции по п. 15.
23. Способ по п. 22 отличающийся тем, что воспалительное заболевание слизистой оболочки или кожи выбрано из воспалительного заболевания кишечника, радиационного проктита, атрофического вагинита, пародонтоза, гингивита, афтозного изъязвления, красного плоского лишая, буллезного пемфигоида, обыкновенной пузырчатки, герпетиформного дерматита, ангулярного хейлита и рецидивирующего герпеса.
24. Способ по п. 22, отличающийся тем, что вводимоая композиция содержит от 1 мг до 1,5 г комбинированного травяного экстракта в высушенном состоянии в сутки.
25. Способ лечения орального мукозита, включающий введение фармацевтически приемлемого количества фармацевтической композиции по п.15.
26. Способ по п. 25, отличающийся тем, что вводимая композиция содержит от 1 мг до 1,5 г комбинированного травяного экстракта в высушенном состоянии в сутки.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| ЭКСТРАКТЫ ECHINACEA ANGUSTIFOLIA | 2003 |
|
RU2317095C2 |
| Способ получения фенольных соединений,обладающих противовоспалительным действием | 1980 |
|
SU931188A1 |
| МИНИНА С | |||
| А | |||
| "Химия и технология фитопрепаратов", 2004, стр.228-229, 239-243. | |||
Авторы
Даты
2019-04-02—Публикация
2013-03-13—Подача