Настоящая группа изобретений относится к новому лиотропному жидкому кристаллу хлоргексидина основания, образующемуся в водной жидкокристаллической системе неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатора и регулятора кислотности, при последовательном смешении компонентов в порядке - деионизированная вода, неионогенное поверхностно-активное вещество или смеси неионогенного и катионного поверхностно-активных веществ, стабилизатор, регулятор кислотности и хлоргексидин основание, характеризующиеся пластинчатой структурой и характеристической вязкостью (η) от 5,099 до 10,197 Па⋅с, способу его получения и применению лиотропного жидкого кристалла хлоргексидина основания по в качестве действующего вещества для получения дезинфицирующих или антисептических средств.
Уровень техники.
Хлоргексидин основание (N,N''-бис(4-хлорфенил)-3,12-диимино-2,4,11,13-тетраазатетрадекандиимидамид), относящийся к классу бигуанидов, является сильным основанием. Обладает крайне плохой растворимостью в воде. При этом, обладает высокими биоцидными свойствами, намного превышающими, такие свойства у водорастворимых солей хлогексидина основания, например, такие как диглюконата, диацетата хлоргексидина. Наиболее широкое применение медицинской практике имеет хлоргексидин диглюконат, являющийся солью хлоргексидина и глюконовой кислоты, который нельзя выделить в чистом твердом виде, в связи с чем на рынке он представлен в виде 20% водного раствора.
Использование хлоргексидина в виде солей приводит к снижению биоцидной активности исходного основания. Данное обстоятельство требует осуществлять поиск новых физиологически приемлемых форм, в том числе нано-форм для доставки и/или биодоступности активных веществ через клеточные липофильные мембраны, которые, при этом, сохраняли бы высокую биоцидную активность, присущую хлоргексидин основанию.
С целью сохранения исходных биоцидных свойств хлоргексидина основания были предприняты попытки получить его активные водорастворимые формы, которые описаны в патентах:
В патенте US 5008038 (GAF Chemicals Corporation, Wayne, N.J., приоритет 10.10.1989, США) была показана попытка получить водорастворимый комплекс хлоргексидина основания путем растворения свободного основания хлоргексидина в лактаме и последующего смешивания полученного раствора с водой;
В патенте IL133395 (DEGUSSA AG, приоритет от 09.12.1999, Израиль) описаны составы хлоргексидина в виде порошкообразной водорастворимой смеси, состоящей из хлоргексидина основания, одной или нескольких сахарных кислот или лактонов из набора глюконовая кислота или глюконолактон, лактобионовая кислота;
В патенте WO 2002051464 (The Trustees of Columbia University, New York, приоритет от 22.12.2000, США), указан состав, где для усиления биоцидного действия описана комбинация свободного хлоргексидина основания и водорастворимой соли хлоргексидина, в одном из воплощений диацетат хлоргексидина, в весовом соотношении примерно от 1:1 до 1:5 в присутствии различных растворителей.
В отрытой печати описаны пути получения водорастворимых солюбилизатов хлоргексидина основания.
В докладе «Ассоциаты на основе хлоргексидина и синергетический эффект», Кардаш Г.Г и др. // Материалы VIII Всероссийского съезда эпидемиологов, микробиологов и паразитологов: Сб. статей, т. 4. М.: Росинэкс, 2002. - С. 21-22, был обозначен подход к переводу в растворимую форму хлоргексидина основания и синергетическому увеличению биоцидной активности путем образования ассоциатов хлоргексидина основания и аминокислоты (глицина). В докладе приведены сравнительные данные биоцидной активности ассоциатов хлоргекисидина основания и глицина, показан синергический эффект на тестовых культурах Gr+ (Staphylococcus aureus), Gr- (Klebsiella pneumonia) и Pseudomonas aeruginosa. Однако, ассоциат хлоргексидина основания и глицина достаточно быстро теряет стабильность.
Подход к получению солюбилизата хлоргексидина основания описан в докладе «Солюбилизация хлоргексидина в водных мицеллярных растворах неионогенных ПАВ», // Сборник тезисов докладов XXIII Всероссийской конференции «Структура и динамика молекулярных систем», Москва, 2016.. с. 74-74.
Данное обстоятельство требует осуществлять поиск новых физиологически приемлемых форм, которые сохраняли бы биоцидную активность, присущую хлоргексидин основанию и/или проявляли синергизм в готовых антисепических, лекарственных и дезинфицирующих препаратах.
Механизм действия хлоргексидина диглюконата хорошо изучен. Катионные молекулы хлоргексидина диглюконата связывают в основном анионные соединения, такие как свободные сульфаты, липополисахариды, фосфатные группы и карбоксильные группы протеинов (Rolla G., Melsen В. On the mechanism of the plaque inhibition by chlorhexidine. J Dental Research 1975; 54:57-62).
В низких концентрациях хлоргексидин снижает проницаемость цитоплазматических мембран, при этом происходит утечка ионов калия, фосфат-ионов и протонов, торможение дыхательных процессов и транспорта веществ, изменяется содержание, метаболизм, осмотическая активность ферментов (A1-Tannir М.А., Goodman H.S. A review of clorhexidine and its use in special populations. Special Care in Dentistry 1994; 14:116-22.; Hugo W.B., Longworth A.R. The effect of chlorhexidine on the electrophoretic mobility, cytoplasmic constituents, dehydrogenase activity and cell walls of Escherichia coli and Staphylococcus aureus. J Pharm Pharmacol 1966; 18:569-78)].
Изменение целостности мембран отражает бактериостатический эффект хлоргексидина и является обратимым (Franch М., Pascual A., Santos А. Colutorios en periodoncia.Parte II. Arch Odontoestomatologia 2005; 21:471-87). При более высоких концентрациях хлоргексидина происходит кристаллизация мембраны, что приводит к потере ее структурной целостности и катастрофической потере внутриклеточного вещества. Это является основой бактерицидного действия хлоргексидина основания, что приводит к преципитации или коагуляции бактериальной цитоплазмы с парадоксальным снижением оттока компонентов через мембрану. Этот процесс в конечном итоге ведет к гибели клеток (Chawner J. A., Gilbert P. А comparative study of the bactericidal and growth inhibitory activities of the bisbiguanides alexidine and chlorhexidine. J Applied Bacteriology 1989; 66:243-52).
Интересный подход для получения водорастворимой композиции хлоргексидина основания с сохранением биоцидных свойств хлоргексидина основания описан в патенте РФ №2696259 (ООО «Сан Системе», приоритет от 23.10.2017), где предложен способ солюбилизации хлоргексидина основания, путем мицеллярного и ламеллярного микрокапсулирования в присутствии аминокислоты и алкиламиноксида. Однако, при хранении полученной солюбилизированной композиции хлоргексидина основания выявился частичный солевой эффект, приводящий к рекристаллизации.
Различные подходы к получению водорастворимых форм хлоргексидина - солюбилизатов, композиций, составов не позволяют приблизиться к устойчивым высоким биоцидным свойствам, которыми обладает само основание, его способности изменять свойства клеточной мембраны микроорганизмов (бактерий, вирусов, грибов) и при этом не вызывать резистентности (Hugo W.B. Disinfection mechanisms. In: Russell A.D., Hugo W.B., Ayliffe G.A.J., eds. Principles and Practice of Disinfection, Preservation and Sterilization - Oxford: Blackwell; 1992:187-210).
Было замечено, что соли хлоргекидина, например, диглюконат, ацетат в определенных условиях могут образовывать жидкокристаллические системы, но практического применения данный факт не нашел.
В монографиях «Влияние жидкокристаллической структуры на высвобождение хлоргексидин диацетата», Е Farkas 1, R Zelko, Z Nemeth, J Palmkas, S Marion, I Racz, Int J Pharm, 05.01.2000 Jan 5, 193(2):239-45, «Влияние разновидностей хлоргексидина на жидкокристаллическую структуру носителя», Farkas Е, Zelko R, Torok G, Racz I, Marion S., Int J Pharm. 01.02.2001 и «Исследование высвобождения основания и солей хлоргексидина из различных жидкокристаллических структур», Edit Farkas, Dorottya Kiss, Romana Zelko, Int J Pharm, 01.08.2007 было исследовано образование жидкокристаллических систем и влияние двух типов солей хлоргексидина -диацетата и -диглюконата на физико-химические свойства жидкокристаллических систем. В исследованиях для приготовления жидкокристаллических систем было выбрано неионогенное поверхностно-активное вещество Синпероник А7 (Synperonic А7, Uniqema) (PEG7-C13-15) и вода. Синпероник А7 представляет собой этоксилированный первично разветвленный С13 спирт с полным насыщением. Было показано, что добавление хлоргексидина диглюконата к образованной жидкокристаллической системе меняет структуру жидкокристаллической системы, что в свою очередь приводит к изменению высвобождения лекарственных средств при использовании различных солей хлоргексидина. Так высвобождение хлоргексидина диацетата из гексагональных жидкокристаллических препаратов характеризовалось кинетикой высвобождения нулевого порядка, в то время как высвобождение лекарственного средства из пластинчатых жидкокристаллических систем описывалось аномальным (нефиковским) переносом. Результаты показали, что кинетика высвобождения лекарственного средства сильно зависит от жидкокристаллической структуры.
Однако, физико-химическое изучение полученных жидкокристаллических систем соединений хлоргексидина диацетата и диглюконата не привело к созданию эффективных антисептических, дезинфицирующих и лекарственных средств. Не было показано, какие именно жидкокристаллические системы образуются с хлоргексидином основанием и каким механизмом действий они могут обладать.
Лиотропные жидкие кристаллы (ЛЖК) представляют уникальный класс самоорганизующихся систем, имеющих существенный потенциал для фундаментальных и прикладных работ. Концептуальным подходом является использование лиотропных жидкокристаллических фаз для контроля самоорганизации наноразмерных ассоциатов, что открывает возможность дизайна новых архитектур и легко перестраиваемых пространственно организованных материалов. ЛЖК системы позволяют регулировать концентрацию, размеры и архитектуру молекулярных структур в макромасштабах путем варьирования состава и температуры системы. Структурное подобие лиомезофаз (олигомеров, мицелл, колонок) мембранным системам позволяет рассматривать ЛЖК в качестве моделей биообъектов, а концепцию ориентационно-упорядоченных структур и коллективного молекулярного движения применять при изучении живой материи клеточных мембран в качестве моделей процессов массо- и теплообмена в клетках.
Техническим результатом предлагаемого изобретения является лиотропный жидкий кристалл хлоргексидина основания, обладающий термодинамической стабильностью, проявляющий высокую биоцидную активность, присущую хлоргексидин основанию, способ его получения, применение лиотропного жидкого кристалла хлоргексидина основания качестве действующего вещества для получения дезинфицирующих или антисептических средств, антисептическая и дезинфицирующая композиции на его основе, обладающие бактерицидной активностью против госпитальных штаммов, в том числа патогенных, биопленок, туберкулоцидной активностью (тестировано на Mycobacterium terrae), грибов рода Candida albicans, Trichophyton rubrum, плесневых грибов (тестировано на тест-штамме Aspergillus niger), возбудителей анаэробных инфекций, вирусов, в том числе Коксаки, ECHO, полиомиелита, энтеральных и парентеральных гепатитов, ротавирусов, норовирусов, ВИЧ, гриппа в том числе H5NI, HINI, и др. возбудителей ОРВИ, аденовирусов, коронавирусов, герпеса, цитомегалии и других), при особо опасных инфекциях (чума, холера, туляремия, легионеллез, сибирская язва).
Возможность использования антисептических и дезинфицирующих средств в госпитальной практике, в том числе для обработки рук хирургов, операционных медицинских сестер, акушерок и других лиц, участвующих в проведения операций, приеме родов в родильных домах, для обработки кожи операционного и инъекционного поля, для обработки локтевых сгибов доноров, для обработки кожи перед введением катетеров и пункцией суставов, для обеззараживания перчаток из различных материалов.
Антисептическая и дезинфицирующая композиции обладают моющим и дезинфицирующим действием, не фиксирует органические загрязнения, не вызывают раздражения кожных покровов при многократном использовании, не вызывают коррозии металлов, сохраняют свои свойства после замерзания и последующего оттаивания, не вызывают резистентности, обладают высокой безопасностью и экономической доступностью.
Краткое описание чертежей
Рисунок №1 - поляризационное микроскопическое изображение кристаллов хлоргексидина основания;
Рисунки №2 и №3 - поляризационное микроскопическое изображение лиотропных жидких кристаллов хлоргекисидина основания виде характерных пластин, стержней;
Таблица №1 - Поляризационные микроскопические данные жидких кристаллов в зависимости от концентрации НПАВ;
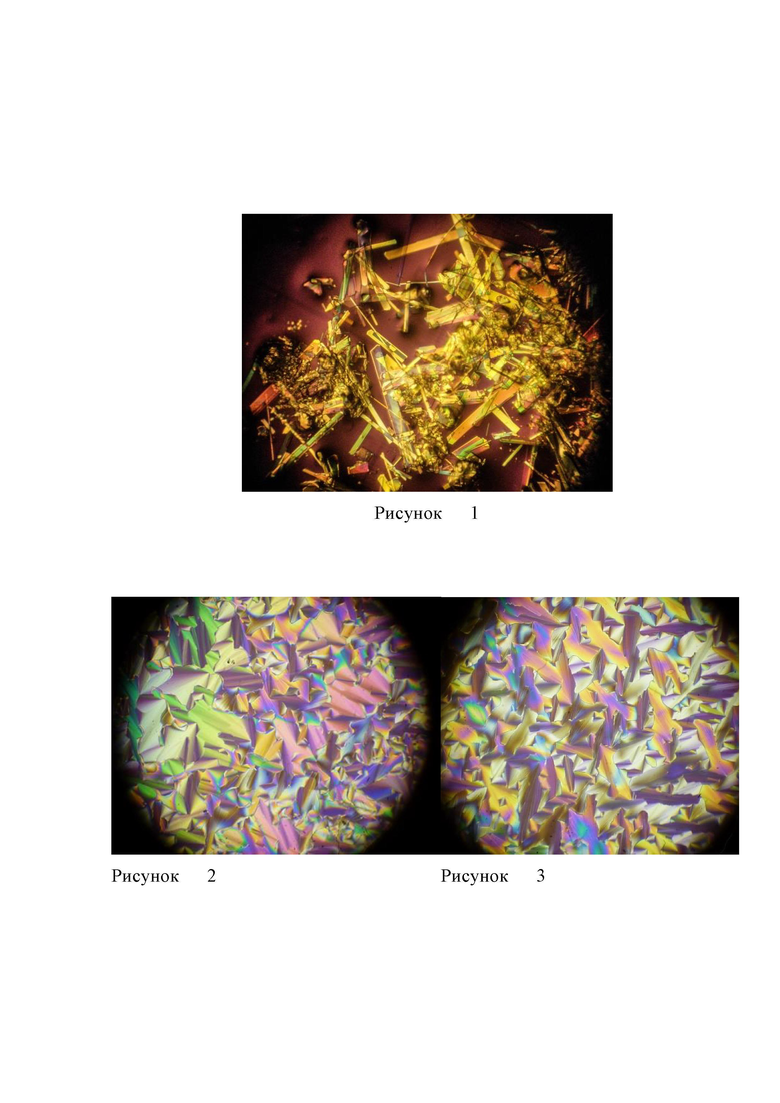
График №1 - Сравнительные данные по концентрации высвобождения хлоргексидина основания и хлоргексидина диглюконата из жидкокристаллических систем;
График №2 - Динамическая вязкость (η*) жидкокристаллических образцов хлоргексидина основания и хлоргексидина диглюконата;
Таблица №2 - Исследования стабильности лиотропных жидких кристаллов хлоргексидина основания, композиций на его основе (поляризационно-микроскопические данные) методом ускоренного старения
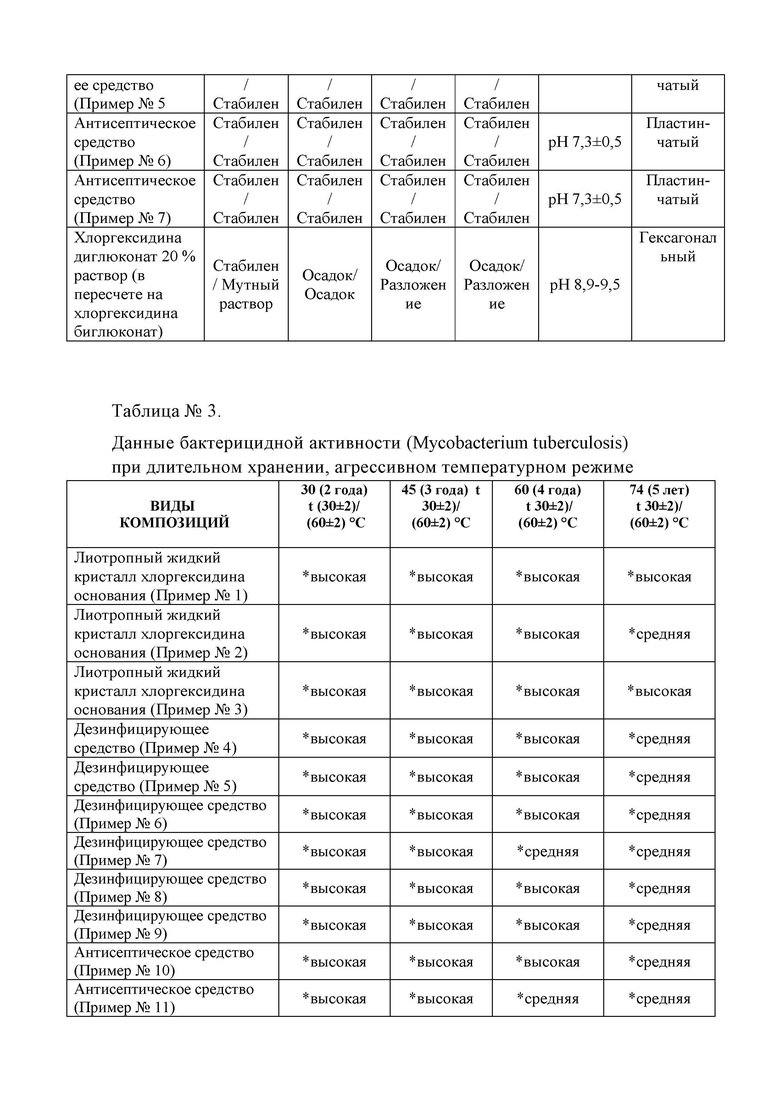
Таблица №3 - Данные бактерицидной активности (Mycobacterium tuberculosis) при длительном хранении, агрессивном температурном режиме;
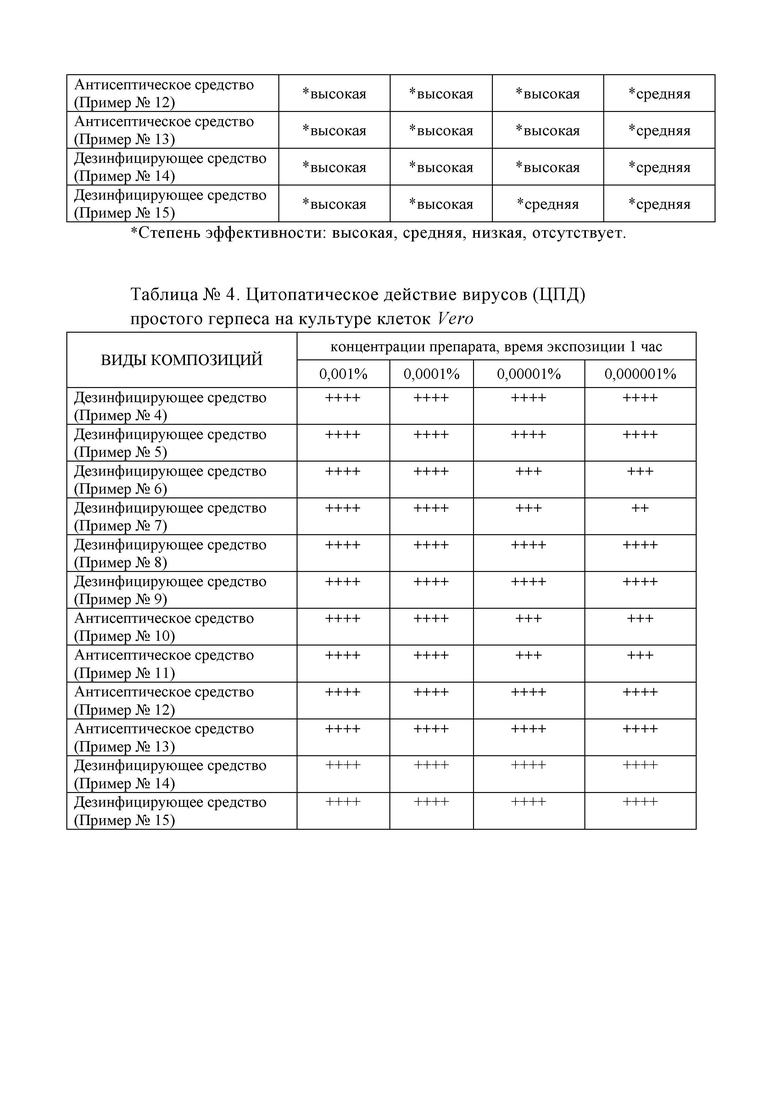
Таблица №4 - Цитопатическое действие вирусов (ЦПД) простого герпеса на культуре клеток Vero;
Рисунок №4 - Контроль клеток Vero - перевиваемые клетки почки зеленой мартышки через 24 часа наблюдения. Клетки веретенообразной формы многоотростчатые, сформирован полный клеточный монослой.
Рисунок №5 - Цитотоксическое действие препарата. Клетки мелкие, округлые без отростков, при специальном окрашивании - отмечаются мертвые клетки, клеточный монослой нарушен;
Рисунок №6 - Цитопатическое действие ВПГ2 (++++) в разведение 1:100 -видны крупные клеточные синцитии, полное нарушение целостности монослоя;
Рисунок №7 - Цитопатическое действие ВПГ-1. Отмечается частичное (50%) нарушение целостности клеточного монослоя (ЦПД++);
Рисунок №8 - Цитопатическое действие ВПГ2 - клетки округлой формы без отростков, видны крупные конгломераты и синцитии клеток, нарушение клеточного монослоя ЦПД (++/+++) (50% - 75%);
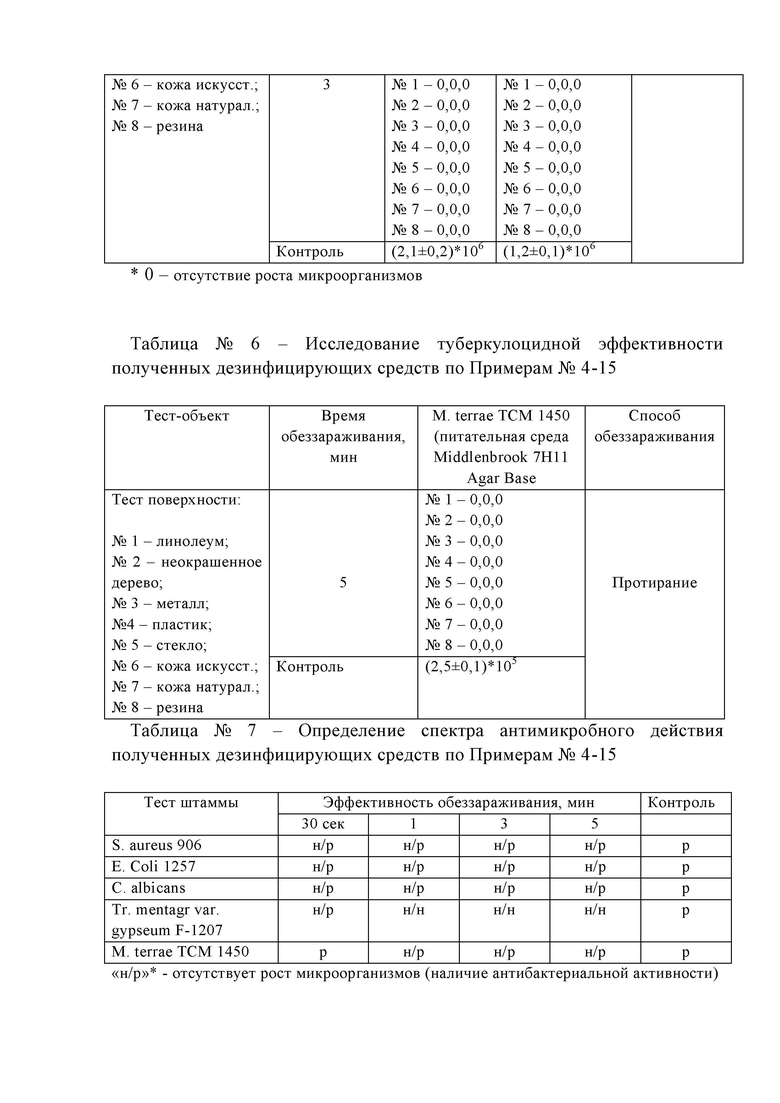
Таблица №5 - Исследование бактерицидной эффективности полученных дезинфицирующих средств по Примерам №4-15;
Таблица №6 - Исследование туберкулоцидной эффективности полученных дезинфицирующих средств по Примерам №4-15;
Таблица №7 - Определение спектра антимикробного действия полученных дезинфицирующих средств по Примерам №4-15;
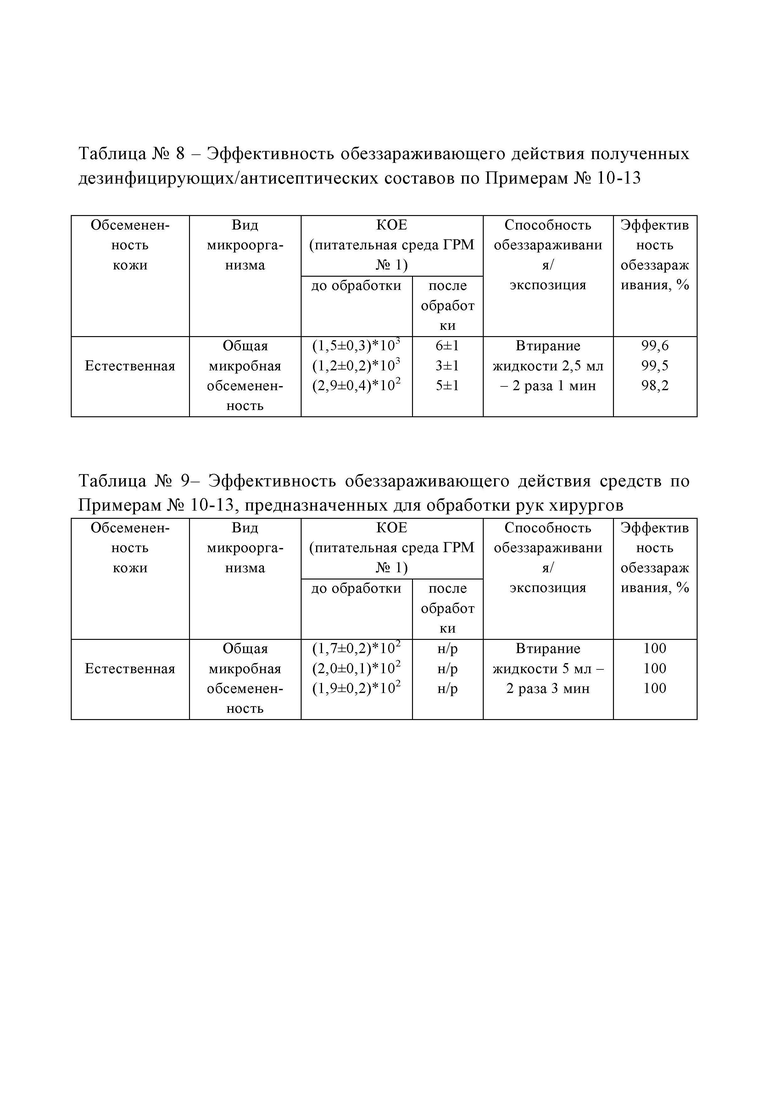
Таблица №8 - Эффективность обеззараживающего действия полученных дезинфицирующих/антисептических составов по Примерам №10-13;
Таблица №9- Эффективность обеззараживающего действия средств по Примерам №10-13, предназначенных для обработки рук хирургов;
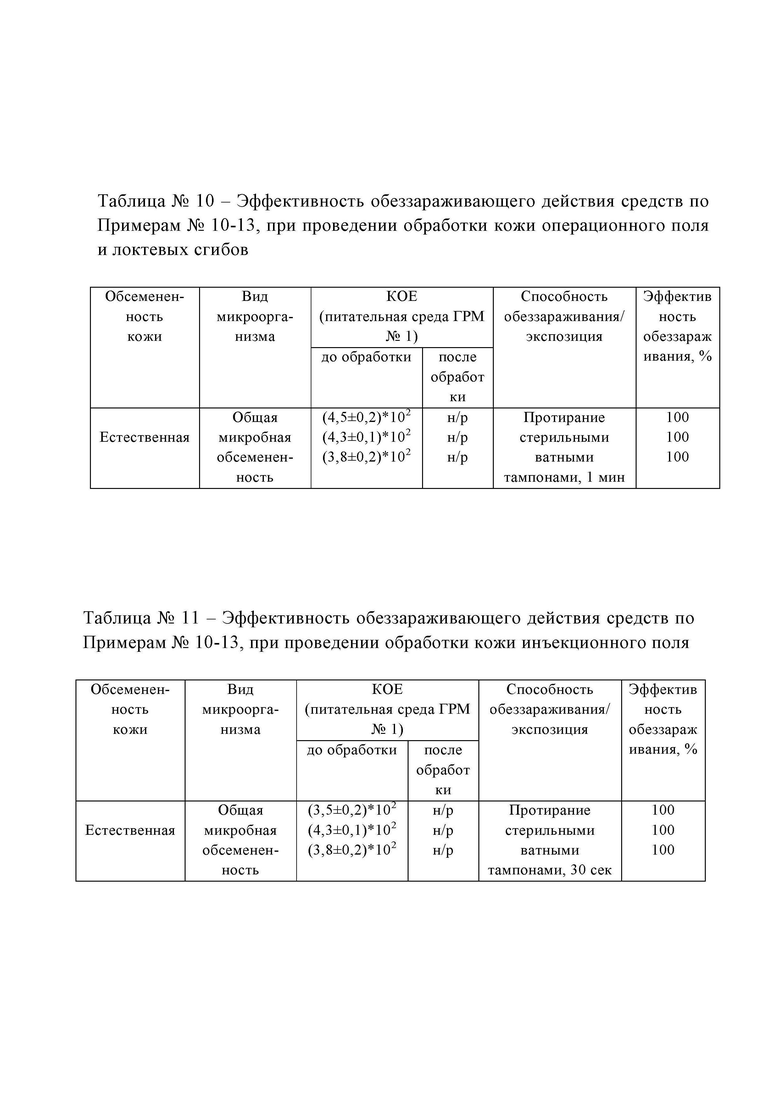
Таблица №10 - Эффективность обеззараживающего действия средств по Примерам №10-13, при проведении обработки кожи операционного поля и локтевых сгибов;
Таблица №11 - Эффективность обеззараживающего действия средств по Примерам №10-13, при проведении обработки кожи инъекционного поля;
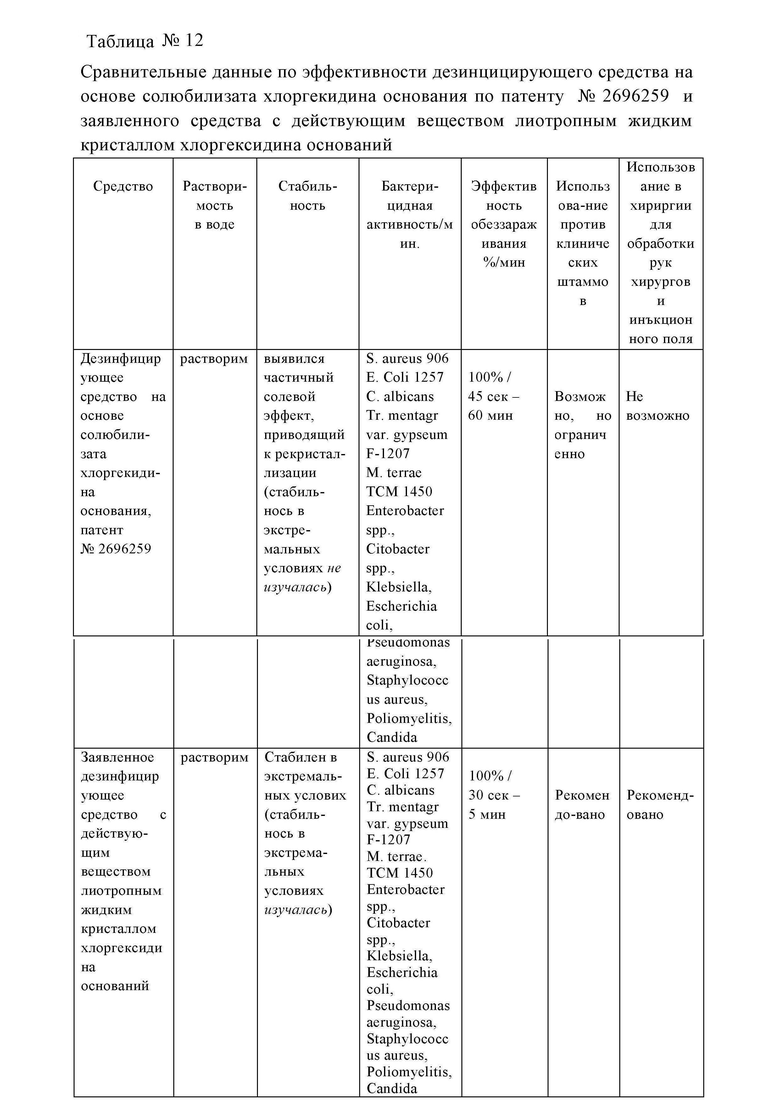
Таблица №12 - Сравнительные данные по эффективности дезинцицирующего средства на основе солюбилизата хлоргекидина основания по патенту № 2696259 и заявленного средства с действующим веществом лиотропным жидким кристаллом хлоргексидина оснований
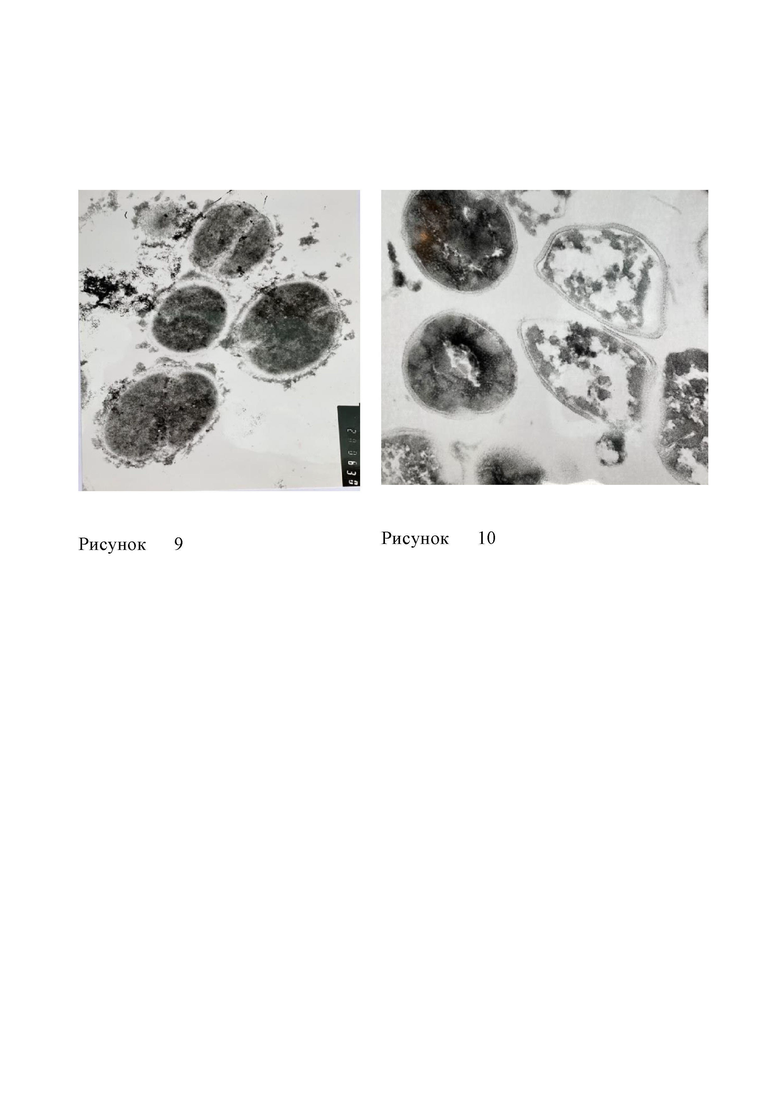
Рисунок №9 и Рисунок №10 - проникновение жидкокристаллической структуры хоргексидина основания через порины клеточной стенки бактерий в цитоплазму с последующим разрушения мембран систем цитоплазмы ДНК и РНК бактерии, и лизиса цитоплазмы.
Сущность изобретения
Технический результат достигается тем, что лиотропный жидкий кристалл хлоргексидина основания образуется в водной жидкокристаллической системе неионогенного_поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатора и регулятора кислотности, при последовательном смешении компонентов -деионизированная вода, поверхностно-активное вещество или их смесь, стабилизатор, регулятор кислотности и хлоргексидин основание, характеризующиеся пластинчатой структурой и характеристической вязкостью (η) от 5,099 до 10,197 Па»с, при следующем соотношении компонентов, масс. %:
Лиотропный жидкий кристалл хлоргексидина основания образуются строго при определенной последовательности смешения компонентов -деионизированная вода, неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, стабилизатор, регулятор кислотности и хлоргексидин основание в стехиометрическиех соотношениях.
В качестве неионогенного поверхностно-активного вещества используют кокоалкилдиметиламинооксид, неонол, оксиэтилированные сорбитаны, в качестве катионного поверхностно-активного вещества используют третичный алкиламин, полигексаметиленгуанидина гидрохлорид или четвертичное аммониевое соединение, выбранное из ряда алкилдиметилбензиламмоний хлорид, дидецилдиметиламмоний хлорид, ундециленамидопропил-тримониум метосульфат, N,N-дидецил-N-метил-поли(оксиэтил) аммониум пропионат, в качестве стабилизатора используют полиэтиленгликоль с молекулярной массой от 200 до 400, этиленгликоль или многоатомные спирты, выбранные из группы глицирин, 1,4-бутандиол, 1,2-пропандиол раздельно или совместно, в качестве регулятора кислотности используют, при условии, что регулятор кислотности не представляет собой аминокислоту, замещенные органические оксикислоты, выбранные из группы: яблочная кислота, молочная кислота, гликолевая кислота, триэтаноламин, комплексоны, выбранные из группы динатриевая соль этилендиаминтетрауксусной кислоты, этилендиаминтетрауксусная кислота.
Амфифильные вещества, которым относится НПАВ склонны спонтанно к образованию самоассоциаций, и с увеличением концентрации могут образовывать высокоупорядоченные агрегаты, такие как пластинчатые, гексагональные и кубические фазы, то есть возникает «лиотропный мезоморфизм» - лиотропные жидкие кристаллы. Устойчивое высвобождение лекарственных гидрофильных веществ из кубических и обратных гексагональных структур было описано (Osborne, D.W., Ward, A.J.I., 1995. Lyotropic liquid crystals as topical drag delivery vehicles. Int. J. Pharm. Adv. 1, 38-45).
Было сделано предположение, что использование пластинчатых или стержневых лиотропных жидкокристаллических фаз для получения высоко растворимых форм труднорастворимых веществ, каким является хлоргексидин основание, является благоприятным из-за термодинамической стабильности или широкого диапазона реологических свойств.
Лиотропный жидкий кристалл хлоргексидина основания был охарактеризован с помощью поляризационной микроскопии и реологического измерения динамической вязкости.
Самый первый, традиционный и доступный способ изучения жидких кристаллов - это поляризационно-оптическая микроскопия. Коротко суть метода: когда поляризованный свет попадает в жидкокристаллическую среду, наблюдается поворот плоскости поляризации, и степень поворота зависит от длины волны. Мезофазы дают характерные картинки, текстуры, при наблюдении в поляризационный микроскоп.Анализ изображения позволяет сделать вывод о том, какая именно жидкокристаллическая фаза образуется.
Текстуру полученных жидкокристаллических образцов изучали с помощью поляризационного микроскопа: M500-PZ, увеличение 40х-1000х. (Polarizing and bright field microscope SKU:M500-PZ), камера Panasonic Lumix DC-FZ 1000 Bridge Camera 20. IMP). Измерения проводились при комнатной температуре. Поляризационные микроскопические изображения жидких кристаллов хлоргексидина основания представлены на Рисунках №1-3.
Образование лиотропного жидкого кристалла хлоргексидин основания показано на примере, где в качестве неионогенного ПАВ использовали N-окисью алкилдиметиламина, полиэтиленгликолем в присутсвии яблочной кислоты образует в воде стабильные сферолитные мицеллы, затем последовательно образуют стрежневые, пластинчатую морфологические структуры, жидко-кристаллические ламеллы или сферолиты, что показано на фотографиях жидкокристаллических структур Рисунки №2-3.
Правильные кристаллы с ограненными формами (Рисунок №1) - это хлоргексидин основание, лиотропные жидкие-кристаллы хлоргекисидина основания виде характерных пластин, стержней представлены на Рисунках №2-3.
Эксперименты показали, что аналогичные характерные пластинчатые структуры лиотропных жидких кристаллов образуются в водной жидкокристаллической системе смеси неионогенного и катионного поверхностно-активных вещества, в присутствие различных стабилизаторов и регуляторов кислотности.
Экспериментальные исследования показали неожиданную зависимость образования пластинчатых форм жидких кристаллов хлоргексидина основания в жидкокристаллической системе поверхностно активных веществ от порядка ввода компонентов и от диапазона концентраций поверхностно активных веществ. Были проведены сравнительные исследования в жидкокристаллической системе поверхностно активных веществ, в которой использовалась хлоргексидин основание и соли хлоргексидина дилюконата. Выявилось, что хлоргексидин основание в жидкокристаллической системе неионогенного, равно в смеси неионогенного и катионного повернностно-активного веществ может образовываться только в пластинчатые, стержневые структуры, в отличие от жидких кристаллов, содержащих соль хлоргексидина диглюконата, которые образуют гексагональные или смешанные структуры. Данное обстоятельство является удобным методом контроля образования лиотропного жидкого кристалла хлоргексидин основания в различных препарата и/или готовых лекарственнх форм. Поляризационные микроскопические данные жидких кристаллов в зависимости от концентрации поверхностно-активных веществ, на примере N-окись алкилдиметиламина приведены в Таблице №1.
Но самым неожиданным явилось то, что при сравнительном исследовании, в зависимости от концентрации поверхностно-активных веществ пластинчатая или стержневая лиотропная жидкокристаллическая система хлоргексидин основания оказалась более эффективной и активной, с большей степенью высвобождения по сравнению с жидкокристаллической системой соли хлоргексидина диглюконата, содержащей упорядоченные гексагональные структурные элементы, что затрудняло высвобождение хлоргексидина диглюконата, а следовательно значительно уменьшало его эффективность. Учитывая, что водорастворимость соли хлоргексидин диглюконата в 10 тысяч раз выше чем у хлоргексидина основания, полученные результаты позволяет утверждать, что высвобождение и/или эффективность полученного лиотропного жидкого кристалла хлоргексидина основания регулируется и определяется главным образом структурой жидкого кристалла.
Механизм образования лиотропной жидкокристаллической системы N-окись алкилдиметиламина-хлоргексидин основание с полиэтиленгликолем представляется следующим: растворимость неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ обеспечивается за счет незаряженных гидратированных ионных групп таких как N-оксидная (N+>O-) и полноксиэтиленовая. Механизм такой ассоциации заключается в том, что полиоксиэтиленовая цепочка, которая по своей химической природе гидрофильная, в водной среде внедряется в структуру гидрофобных алкильных цепей и полярных концевых групп, что является подобно удлинению молекулярных цепей. Это объясняется тем, что полярная группа несет электрический заряд являющийся в отношении мицело образования сильным противодействующим фактором. Промежуточная оксиэтиленовая цепочка экранирует заряд от мицелярной поверхности и является промотором мицелообразования. В силу структурных ограничении такая ассоциация разных молекул делает предпочтительным образование в полярной среде не мицеллы, а ламеллярных ассоциаций. В результате, в растворе образуются ассоциации морфологических структур с анизотропной оптической осью, то есть возникновением двулучепреломленеим. Эти структуры являются жидкими кристаллами, обладающими свойствами, как кристалла, так и жидкости. В созданную нами технология ламелярную морфологическую структуру внедряется хлоргексидин основание. Таким образом, происходит промоторное действие биоцидной активности хлоргексидин основания, поскольку функциональные группы хлоргексидина основания защищены от инактивации в любой среде.
Жидкие кристаллы являются уникальным материалом, который может находиться в состояниях, промежуточных между жидкостью и твердым телом. Эти состояния возникают благодаря анизотропной форме молекул, например, молекулы вытянуты, как палочки (Де Жен П. Физика жидких кристаллов. М.: Мир, 1977; Чандрасекар С. Жидкие кристаллы. М.: Мир, 1980).
Наиболее известными являются нематическое и смектическое жидкокристаллические состояния (фазы). В нематической фазе, молекулы имеют симметричную комформацию. Хлоргексидин основание является характерным нематиком.
При этом, в жидкокристаллической системе неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатра, системы, и регулятора кислотности приобретает свойства смектика.
В смектических фазах молекулы группируются в слои, существует трансляционный порядок в определенном 2-х мерном направлении.
Наблюдается самомоделирующаяся жидкокристаллическая система хлоргекидина основания без образования химических связей.
Наличие таких структур в растворе, объясняет механизм биоцидной активности системы при взаимодействии с клеточной стенкой бактерий и наличие у нее сильного синергического эффекта.
Полученные лиотропные жидкие кристаллы хлоргексидина основания проявили высокую стабильность при хранении, в том числе в экстремальных условиях. Жидкокристаллическая структура сохраняется при получении значительном разбавлении водой при получении различных средств дезинфицирующих или антисептических средств.
При изучении стабильности полученных лиотропных жидких кристаллов и средств на его основе не было выявлено признаков рекристаллизации и/или распада.
Данные по исследованию стабильности полученных средств представлены в Таблице №2.
Количественное определение лиотропного жидкого кристалла хлоргексидина основания и его соли хлоргексидина диглюконата были исследованы спектрофотометр ическим методом при 255 Нм, на спектрофотометометре Shimadzu с УФ-160А. Метод давал линейный отклик в диапазоне концентраций 1-30 м/мл.
Данные по концентрации высвобождения хлоргексидина основания и его соли хлоргексидина диглюконата из жидкокристаллических систем в зависимости от концентрации N-окись алкилдиметиламина (НПАВ) и времени представлены на Графике №1. Образцы содержат (а) лиотропный жидкий кристалл хлоргексидина основания и (Б) соль хлоргексидина диглюконат.
Реологического измерения динамической вязкости проводились с помощью прибора Haake RS 80.
Использовался конусно-пластинчатый датчик диаметром 20 мм и углом конуса 4°. Толщина образца в середине датчика составляла 0,134 мм. Образцы готовили при температуре 25±0,2°С.
Динамическое колебательное исследование проводилось с полученными образцами лиотропным жидким кристаллом хлоргекидина основания и жидким кристаллом хлоргексидина диглюконата. Линейная вязкоупругая область была определена путем измерения комплексного модуля в зависимости от напряжения на данной частоте (0,1 Гц), в качестве амплитуды напряжения выбран показатель 2,5 Па, который как было установлено, находится в линейной вязкоупругой области во всех случаях.
На Графике №2 представлена динамика образования жидкокристаллических структур и их характер. В зависимости от концентрации поверхностно-активного вещества в системе образовались две различные жидкокристаллические структуры.
Была выявлена закономерность в случае соли хлоргексидина диглюконата образуется более вязкая гексагональная структура, в то же время, в случае лиотропного жидкого кристалла хлоргексидина основания образующийся при 1-30% (мас. %) концентрации неионогенного поверхностно активного вещества или смеси неионогенного и катионного поверхностно активного вещества, образуется менее вязкая и более упорядоченная структура с характеристической вязкостью (η) от 5,099 до 10,197 Па⋅с (Паскаль⋅сек.) (График №2).
Возможная причина заключаться в том, что в случае соли хлоргексидина диглюконата вторичные связи могут быть сильнее между молекулами поверхностно активных веществ, так как хлоргексидин гидрофилизуется ацетатом и глюконатом и, таким образом, не может взаимодействовать с липофильной частью молекул поверхностно активного вещества.
Таким образом, было доказано, что хлоргексидин основание в жидкокристаллической системе неионогенного или смеси неионогенного и катионного поверхностно-активных веществ образует пластинчатые или стержневые лиотропные жидкие кристаллы с большим высвобождением активного действующего вещества и, соответственно, препараты являются более активными, чем жидкие кристаллы водорастворимой соли хлоргексидина диглюконата.
Описанные свойства лиотропные жидкие кристаллы хлоргексидина основания открывают путь к созданию высокоэффективных дезинфицирующих, антисептических и лекарственных препаратов при малых концентрациях действующего вещества.
Получены средства, проявляющее дезинфицирующие или антисептические свойства, содержащее в своем составе лиотропный жидкий кристалл хлоргексидина основания, обладающие бактерицидной активностью против госпитальных штаммов, в том числа патогенных, биопленок, туберкулоцидной активностью (тестировано на Mycobacterium terrae), грибов рода Candida albicans, Trichophyton rubrum, плесневых грибов (тестировано на тест-штамме Aspergillus niger), возбудителей анаэробных инфекций, вирусов, в том числе Коксаки, ECHO, полиомиелита, энтеральных и парентеральных гепатитов, ротавирусов, норовирусов, ВИЧ, гриппа в том числе H5NI, HINI, и др. возбудителей ОРВИ, аденовирусов, коронавирусов, герпеса, цитомегалии и других), при особо опасных инфекциях (чума, холера, туляремия, легионеллез, сибирская язва).
Добавление к жидкокристаллической системе хлоргексидина основания дополнительного биоцидного агента позволяет увеличить и расширить биоцидную активность такого комплекса за счет синергетического эффекта.
Получено средство в виде дезинфицирующей композиции, содержащее лиотропный жидкий кристалл хлоргексидина основания, дополнительно содержит биоцидный агент, краситель при следующем соотношении компонентов, масс. %:
В качестве биоцидного агента в дезинфицирующей композиции используют изопропиловый спирт, н-пропиловый спирт, перекись водорода, в качестве красителя используют антрахиноновый краситель, кармуазин (Е122) или триарилметановый краситель (Е133).
Получено средство в виде антисептической композиции, содержащей лиотропный жидкий кристалл хлоргексидина основания, дополнительно содержит биоцидный агент, загуститель для придания вязкости, краситель и ароматизатор, при следующем соотношении компонентов, масс. %:
Антисептическая композиция в качестве биоцидного агента содержит изопропиловый или этиловый спирт, в качестве загустителя используют гидроксиэтилцеллюлозу (натросол 250 HR), карбомер, в качестве красителя используют антрахиноновый краситель, кармуазин (Е122) или триарилметановый краситель (Е133).
Способ получения лиотропного жидкого кристалла хлоргексидина основания, дезинфицирующих и антисептических средств на его основе иллюстрируется следующими примерами.
Пример 1.
Для получения 100 г. лиотропного жидкого кристалла хлоргексидина основания в 57,5 г деионизованной воды добавляют 30 г кокоалкилдиметиламинооксид (Барлокс-12) (неоногенное оверхностно активное вещество), затем при интенсивном перемешивании вводят 5 г. полиэтиленгликоля (Pluriol Е-200), затем 4 г. яблочной кислоты, затем 3,5 г. хлоргексидина основания до полного его растворения и образования лиотропных жидких кристаллов. Характеристическая вязкость полученного лиотропного кристалла 6,10 Па⋅с.
Пример 2.
Для получения 100 г. лиотропного жидкого кристалла хлоргексидина основания в 98,12 г деионизованной воды добавляют 0,5 г кокоалкилдиметиламинооксид (Барлокс-12) и 1,0 г алкилдиметилбензил хлорид (катионное поверхностно-активное вещество), затем при интенсивном перемешивании вводят 0,25 г. полиэтиленгликоля (Pluriol Е-200), затем 0,03 г. яблочной кислоты, затем 0,1 г. хлоргексидина основания до полного его растворения и образования лиотропных жидких кристаллов. Характеристическая вязкость полученного лиотропного кристалла 8,457 Па⋅с.
Пример 3.
Для получения 100 г. лиотропного жидкого кристалла хлоргексидина основания в 79,25 г. деионизованной воды добавляют 5,0 г кокоалкилдиметиламинооксид (Барлокс-12) и 10 г смеси алкилдиметилбензиламмоний хлорид + дидецилдиметиламмоний хлорид (катионные пав) при их соотношении 5 г + 5 г (катионные пав), затем при интенсивном перемешивании вводят 1,0 г. полиэтиленгликоля (Pluriol Е-400) и 1,5 г 1,2-пропандиол, затем 0,75 г. гликолевой кислоты, затем 2,5 г. хлоргексидина основания до полного его растворения и образования лиотропных жидких кристаллов. Характеристическая вязкость полученного лиотропного кристалла 9,896 Па⋅с.
Пример 4.
Для получения 100 г дезинфицирующей водной композиции в 94,545 г деионизированной воды, добавляют 2,5 г кокоалкилдиметиламинооксида, 0,5 г полиэтиленгликоля Е-200, 0,2 г динатриеврй соли этилендиаминтетрауксусной кислоты (Трилон ВД), 0,25 г хлоргексидина основания, 2,0 г перекиси водорода (3%). Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя синего атрахинонового кислотного. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,550 Па⋅с. Полученная композиция имеет рН - 8,5-8,6.
Пример 5.
Для получения 100 г дезинфицирующей водной композиции в 93,095 г деионизированной воды, добавляют 2,0 г кокоалкилдиметиламинооксида, 0,5 г полиэтиленгликоля Е-200, 0,2 г динатриевой соли этилендиаминтетрауксусной кислоты (Трилон ВД), 1,0 г глицерина, 0,2 г хлоргексидина основания, 3,0 г перекиси водорода (3%). Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя синего атрахинонового кислотного. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,640 Па⋅с. Полученная композиция имеет рН - 8,8-8,9.
Пример 6.
Для получения 100 г водной дезинфицирующей композиции в 93,095 г деионизированной воды, добавляют 4,0 г кокоалкилдиметиламинооксида, 0,5 г полиэтиленгликоля Е-200, 0,05 г этилендиаминтетерауксусной кислоты (ЭДТА), 0,35 г хлоргексидина основания, 2,0 г перекиси водорода (3%). Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя синего атрахинонового кислотного. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,302 Па⋅с. Полученная композиция имеет рН -6,5-7,0.
Пример 7.
Для получения 100 г водной дезинфицирующей водной композиции в виде концентрата в 75,595 г деионизированной воды, добавляют 10,0 г кокоалкилдиметиламинооксида, 7,0 г алкилдиметилбензиламмоний хлорида, 1,5 г 1,4-бутандиола, 1,0 г полиэтиленгликоля ПЭГ-400, 0,75 г яблочной кислоты, 0,3 г триэтаноламина, 0,35 г хлоргексидина основания, 3,5 г н-пропиловый спирт. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя синего атрахинонового кислотного. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 8,103 Па⋅с. Полученная композиция имеет рН - 9,4-9,55.
Пример 8.
Для получения 100 г дезинфицирующей водной композиции в виде концентрата в 68,695 г деионизированной воды, добавляют 8,0 г кокоалкилдиметиламинооксида, 12,0 г смеси алкилдиметилбензиламмоний хлорида + дидецилдиметиламмоний хлорида при их соотношении 4 г + 8 г, 2,5 г полиэтиленгликоля ПЭГ-400, 2,8 г молочной кислоты, 2,0 г третичного алкиламина, 2,0 г хлоргексидина основания, 2,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя кармуазин (Е122). Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,921 Па⋅с. Полученная композиция имеет рН - 7,1-7,7.
Пример 9.
Для получения 100 г дезинфицирующей водной композиции в виде концентрата в 72,945 г деионизированной воды, добавляют 10,0 г дидецилдиметиламмоний хлорида, 2,5 г Неонола АФ9/10, 5,0 г кокоалкилдиметиламинооксида, 1,0 г полиэтиленгликоля ПЭГ-400, 4,0 г 1,2-пропандиола, 1,0 г гликолевой кислота, 1,25 г хлоргексидина основания, 2,3 г н-пропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя кармуазин (Е122). Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 6,857 Па⋅с. Полученная композиция имеет рН - 7,0-7,5.
Пример 10.
Для получения 100 г антисептического средства в 36,555 г деионизированной воды добавляют 1,0 г кокоалкилдиметиламинооксида, 0,25 г, 1,2-пропандиола, 0,045 г яблочной кислоты, 0,125 г хлоргексидина основания, 62,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г красителя триарилметановый краситель (Е133), 0,02 г ароматизатор. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 5,989 Па⋅с. Полученная композиция имеет рН - 7,35-7,6.
Пример 11.
Для получения 100 г дезинфицирующего средства в 92,755 г деионизированной воды, добавляют 1,8 г кокоалкилдиметиламинооксида, 0,6 г ундециленамидопропилтримониум метосульфата (Тетранил У), 0,375 г полиэтиленгликоль Е-200, 0,04 г яблочной кислоты, 0,01 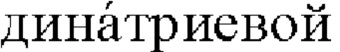 соли
соли 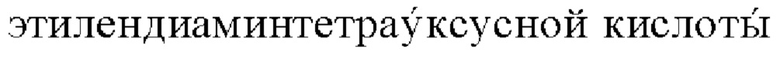 (Трилон ВД), 0,375 г хлоргексидина основания, 4,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г триарилметановый краситель (Е133), 0,02 г загустителя (Натросол 250 HR), 0,02 г ароматизатор. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,850 Па⋅с. Полученная композиция имеет рН - 5,94-6,0.
(Трилон ВД), 0,375 г хлоргексидина основания, 4,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,005 г триарилметановый краситель (Е133), 0,02 г загустителя (Натросол 250 HR), 0,02 г ароматизатор. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,850 Па⋅с. Полученная композиция имеет рН - 5,94-6,0.
Пример 12.
Для получения 100 г антисептического средства в 66,545 г деионизированной воды, добавляют 2,5 г кокоалкилдиметил аминооксида, 0,6 г N,N-дидецил-N-метил-поли(оксиэтил) аммониум пропионат (Бардап -26), 1,0 г полиэтиленгликоль Е-200, 0,03 г яблочной кислоты, 0,3 г хлоргексидина основания, 2,0 г перекись водорода (3%), 27,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,02 г ароматизатор и 0,005 г красителя кармуазин (Е122). Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 8,753 Па⋅с. Полученная композиция имеет рН - 7,0-7,5.
Пример 13.
Для получения 100 г антисептического средства в 34,235 г деионизированной воды, добавляют 1,0 г кокоалкилдиметиламинооксида, 0,6 г N,N-дидецил-N-метил-поли(оксиэтил) аммониум пропионат (Бардап-26), 1,0 г полигексаметиленгуанидина гидрохлорид, 1,0 г 1,2-пропандиола, 0,04 г гликолевой кислоты, 0,1 г хлоргексидина основания, 62,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,02 г ароматизатор и 0,005 г красителя кармуазин (Е122). Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,983 Па⋅с. Полученная композиция имеет рН - 6,0-7,0.
Пример 14.
Для получения 100 г антисептического средства в 34,4 г деионизированной воды, добавляют 0,5 г кокоалкилдиметиламинооксида, 0,6 г N,N-дидецил-N-метил-поли(оксиэтил) аммониум пропионат (Бардап-26), 0,1 г третичного алкиламина, 0,125 полиэтиленгликоль (ПЭГ-400), 0,15 молочной кислоты, 0,1 г хлоргексидина основания, 64,0 г этиловый спирт. Перемешивание продолжают еще 15 мин до полного его растворения, добавляют 0,02 г ароматизатор и 0,005 г триарилметановый краситель (Е133). Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 7,357 Па⋅с. Полученная композиция имеет рН -6,8-7,5.
Пример 15.
Для получения 100 г дезинфицирующего средства в 63,5 г деионизированной воды, добавляют 24,0 г полисорбат-80 (Е 433), 6,0 N,N-дидецил-N-метил-поли(оксиэтил) аммониум пропионат (Бардап-26), 2,3 г этиленгликоля, 0,7 г молочной кислоты, 1,5 г хлоргексидина основания, 2,0 г изопропилового спирта. Перемешивание продолжают еще 15 мин до полного его растворения. Приготовление композиции проводят при комнатной температуре. Расчетная характеристическая вязкость лиотропного жидкого кристалла как действующего вещества 9,103 Па⋅с. Полученная композиция имеет рН - 7,0-8,0.
Полученные высокоорганизованные комплексы гарантируют высокую эффективность и стабильность при долгом хранении, даже при резких температурных колебаниях, что доказано в эксперименте по ускоренному старению, проведенном по требованиям Общей фармакопейной статьи (ОФС.)1.1.0009.15 «Сроки годности лекарственных средств».
Исследования стабильности лиотропный жидких кристаллов хлоргексидина основания, вариантов дезинфицирующихи антисептических композиций методом «ускоренного старения» в условиях при температуре от (30±2)°С до (60±2)°С и рН 5-8 в течение 74 суток, что соответствует пяти годам срока годности приведены в Таблице №2.
Полученные данные стабильности лиотропного жидкого кристалла хлоргексидина основание в сравнении с хлоргексидином биклюконатом методом «ускоренного старения» показали как высокую стабильность лиотропного жидкого кристалла хлоргексидина основания, так и сохранение высокой бактерицидной активности при длительном хранении, даже в агрессивном температурном режиме (Таблица №3).
По окончании испытаний было показано, что лиотропный жидкий кристалл хлоргексидина основания сохранил свою пластинчатую структуру и биоцидную активность в достаточно разбавленной водной композиции антисептического средства по Примеру №11.
По результатам испытания срок хранения дезинфицирующего средства на основе лиотропного жидкого кристалла хлоргексидина основания принят равным 5 годам.
Полученная по Примерам №10, 12-14 антисептические композиции используется для гигиенической обработки рук без их предварительного мытья, дезинфекции кожи при инъекциях, постановке катетеров, пункциях суставов, обработки кожи доноров.
Лиотропные жидкие кристаллы хлоргексидина основания позволяют создавать широкий спектр дезинфицирующих, антисептических и лекарственных препаратов.
Серия экспериментов в изучении цитотоксичности и противовирусной активности, проведенная в лаборатории герпесвирусов ФГБУ "Национальный исследовательский центр эпидемиологии и микробиологии им. Н.Ф. Гамалеи" Минздрава России (ФГБУ "НИЦЭМ" МЗ РФ) подтвердила высокую противовирусную активность препаратов, полученных на основе жидкокристаллической системы хлоргексидина основания.
В исследовании использовали тест-вирусы: вирус простого герпеса 1 типа - ВПГ1-штамм «L2» и вирус простого герпеса 2 типа - ВПГ2 - штамм «ВН», полученные из Государственной Коллекции Вирусов ФГБУ НИЦЭМ им. Н.Ф. Гамалеи. Вирус пассировали и титровали на монослойной культуре клеток Vero.
В исследовании использованы монослойные перевиваемые клетки почек зеленой мартышки (Vero), полученные из лаборатории культур тканей ФГБУ НИЦЭМ им. Н.Ф. Гамалеи. Клетки культивировали на питательной среде ИГЛА-МЭМ (Производства ООО НПП "ПанЭко" с 10% содержанием эмбриональной телячьей сыворотки (ЭТС), мМ L-глутамина и 100 мкг/мл гентамицина при t=+37,5°С и 5% СО2 и 98% влажности, посевная доза клеток - 2×105 клеток/мл. Клетки рассевали в 24-, 48-, 96-луночные пластиковые планшеты («Corning») до формирования полного монослоя, через 24 часа.
В исследовании использовались стерильные растворы, полученные путем фильтрации через мембранные фильтры типа «МйНроге» с диаметром пор 0,22 мкм. Серийные разведения препаратов (10 кратные) используя питательную среду ИГЛА-МЭМ и 0,9% физиологический раствор.
Оценку активности исследуемых препаратов осуществляли по стандартной методике в соответствии с требованиями
Руководства о по экспериментальному (доклиническому) изучению новых фармакологических веществ (под редакцией Хабриева Р.У., Издательство "Медицина" (Москва), 2005 г. ) и Руководства по проведению доклинических исследований лекарственных средств (Часть первая- М, Гриф и К. 2012- 944 с, Миронов А.Н., Бунатян И.Д., Васильев А.Н. и др.).
Статистический анализ выполнен трижды с использованием пакета программного обеспечения Statistica StatSoft 10.0. Достоверность различий между показателями определялась с использованием критерия Стьюдента, различия считали достоверными при р<0,05, высоко достоверными при р<0,001, недостоверными при р>0,05.
Система оценки противовирусного действия препарата в культуре клеток включала в себя изучение подавления цитопатического действия вирусов в культуре клеток (cytopathic effect (CPE) reduction assay), а также влияния на репродукцию вирусов в культуре клеток. Для этого культуру клеток культивировали в 24- и 48- и 96-луночных плато, как было описано ранее, затем питательную среду удаляли, клетки трижды отмывали теплым раствором Хэнкса и заражали тест-вирусом в дозе 100 ТЦД 50/мл и или различными концентрациями вируса в раститровке 10-1 до 10-5.
Цитопатическое действие вирусов (ЦПД) простого герпеса на культуре клеток Vero проявляется гибелью клеток, округлением клеток и потерей их отростчатости, образованием крупных многоядерных синцитиев и конгломератов, то есть видимым при микроскопии нарушением клеточного монослоя, которое рассчитывается по 4-крестной системе оценки: -отсутствие ЦПД, «1+» - поражение клеточного монослоя на 25%, «++» -на 50%, «+++» - на 75%, «++++» - 100% ЦПД, полная гибель клеток представлены в Таблице №4.
Полученные результаты показывают выраженную противовирусную активностью по отношению к ВПГ-1 и ВПГ-2 при внесении через 1 час после заражения (лечебная схема) в концентрациях 10-4 и 10-5 полученных жидкокристаллических композиций. Результаты соответствуют химиотерапевтическому индексу 10, что говорит об уникальных противовирусных свойствах.
Механизм биоцидной активности и синергизма лиотропных жидких кристаллов хлоргексидина основания в жидкокристаллической системе N неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ и стабилизатора представляется следующим образом: атака жидкокристаллического комплекса хлоргексидин основание/поверхностно активное вещество на клеточную структуру бактерии происходит образованной жидкокристаллической системой, которая легко проникает (Рисунок №9) через порины клеточной стенки бактерий в цитоплазму с последующим освобожденим хлоргексидина основания из морфологической структуры комплекса, который производит катастрофические разрушения мембран систем цитоплазмы (Рисунок №10) ДНК и РНК и в конечном итоге лизис цитоплазмы.
В клеточной стенки происходит полное разрушение муреинового каркаса и отслоение мембран от цитоплазмы. Такая картина разрушения клетки приводит к полной гибели бактерий.
Добавление к данной системе дополнительной биоцидной субстанции, позволяет за счет эффекта синергизма и за счет параллельной активности биоцидных субстанций повысить антибактериальную активность композиции до появления спороцидного эффекта, то есть воздействия не только на вегетативную форму B.cereus, но и на его споровую форму.
По параметрам острой токсичности по классификации ГОСТ 12.1.007-76 относится к 4 классу мало опасных веществ, как при введении в желудок, так и при нанесении на кожу, что является особенностью полученных дезинфицирующих и антисептических средств, действующим веществом которых является лиотропный жидкий кристалл хлоргексидина основания.
В Аккредитованном испытательном лабораторном центре Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» (ФБУН «ГНЦ ПМБ») Роспотребнадзора РФ проведена серия экспериментов, подтвердившая высокую активность полученных жидкокристаллических систем в отношении культуры Aspergillus niger АТСС 16404, Bacillus anthracis СТИ -1 (Сибирская язва), E.coli 1257, С.albicans АТСС 10231, M.terrae ТСМ 1450.
Получены уникальные данные исследований, проведенные в Таблицах №5-11, которые показали 100% эффективность полученных средств при дезинфекции госпитальных штаммов, по использованию полученных антисептических и дезинфицирующих составов в различных формах, в том числе в виде спрея, в клинических условиях, в хирургии для обработки поверхностей.
Данные, приведенные в Таблицы №5 объективно показывают, что дезинфицирующие средства по Примерам №4-15 обеззараживают тест-объекты, контаминированные Е. Coli 1257, S. aureus 906 при времени обеззараживании 1 и 3 мин.
Из результатов данныех Таблицы №6 сдедует, что полученные дезинфицирующих средств по Примерам №4-15 эффективно обеззараживают тест-объекты, кантаминированные М. terrae ТСМ 1450 при времени обеззараживания 5 мин.
Данные Таблицы №7 доказывают широкий спектр антимикробного действия полученных дезинфицирующих средств по Примерам №4-15.
Данные, приведенные в Таблице №8 доказываю высокую эффективность применения полученных антисептических средств в качестве кожных антисептиков. Двукратная обработка кожи рук средствами по Примерам №10-13 в течение 1 мин. методом втирания привела к снижению естественной микрофлоры от 99,6% до 98,2%.
В Таблице №9 приведены данный об уникальной эффективности применения полученных антисептических средств при обработки рук хирургов. Обработка рук хирургов средствами по Примерам №10-13 поле двукратного втирания кожи при обеззараживании в течение 3 мин. обеспечивает 100% снижение микробной обсемененности.
Из Таблицы №10 следует, что после последовательного протирания кожи двумя раздельными стерильными тампонами, пропитанными средствами по Примерам №10-13 с выдержкой после обработки в течение 1 мин, достигается 100% снижение количества естественной микрофлоры.
Из Таблицы №11 следует, что при орашении или протирании ватными тампонами обильно смоченными средствами по Примерам №10-13 места инъекции при времени выдержки 30 сек достигается 100% снижении количества естественной микрофлоры.
Были проведены сравнительные исследования дезинфицирующих средства, полученного по патенту №2696259 и заявленного дезинфицирующего средства с действующим веществом лиотропным кристаллом хлоргексидина основания, так в обеих случаях использовалось хлоргексидин основание.
Было выявлено, что дезинцирующее средство по патенту №2696259 при изучении стабильности, в том числе в экстремальных условиях подвергается частичному солевому эффекту, приводящесу к рекристаллизации. Стабильность дезинфицирующего средства по патенту не была изучена. Была выявлена схожая бактериальная активность, однако 100% эффективность дезинфицирующего средства по патенту достигалась в большее количество времени, что ограничивает его использования в хириргии для предоперационной обработки рук хирургов, операционного и инъкционного полей. Сравнительные данные по эффективности дезинцицирующего средства на основе солюбилизата хлоргекидина основания по патенту №2696259 и заявленного средства с действующим веществом лиотропным жидким кристаллом хлоргексидина оснований представлены в Таблице №12.
Таким образом, сравнительные данные проведенных экспериментов позволяют утверждать, что заявленный лиотропный жидкий кристалл хлоргексидина основания, образующийся в водной жидкокристаллической системе неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатора и регулятора кислотности обладает стабильностью и уникальной бактерицидной активностью по отношению Aspergillus mger АТСС 16404, E.coli 1257, С.albicans АТСС 10231, M.terrae ТСМ 1450, в том числе к возбудителю сибирской язвы - бацилле Bacillus anthracis.
Полученные в ходе исследования данные позволяют сделать вывод о высокой эффективности полученных дезинфицирующие и антисептические средства, в которых действующим веществом является лиотропный кристалл хлоргексидина основания и возможности широкого использования средств в госпитальной практике, в том числе для обработки рук хирургов, операционных медицинских сестер, акушерок и других лиц, участвующих в проведения операций, приеме родов в родильных домах, для обработки кожи операционного и инъекционного поля, для обработки локтевых сгибов доноров, для обработки кожи перед введением катетеров и пункцией суставов, для обеззараживания перчаток из различных материалов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЛЮБИЛИЗАЦИЯ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2017 |
|
RU2696259C2 |
| ИНГАЛЯЦИОННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2777197C1 |
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2017 |
|
RU2743997C2 |
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2017 |
|
RU2729188C1 |
| ЭКОЛОГИЧЕСКИ ЧИСТОЕ БИОРАЗЛАГАЕМОЕ ЖИДКОЕ МЫЛО С АНТИБАКТЕРИАЛЬНЫМ ЭФФЕКТОМ | 2020 |
|
RU2747456C1 |
| БАКТЕРИЦИДНО-МОЮЩЕЕ СРЕДСТВО | 1999 |
|
RU2147032C1 |
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2017 |
|
RU2727969C1 |
| ЖИДКАЯ ДЕЗИНФИЦИРУЮЩАЯ И АНТИСЕПТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ И ВЕТЕРИНАРИИ | 2020 |
|
RU2725991C1 |
| КОМПОЗИЦИЯ (СОСТАВ) ДЛЯ ПРОТИВОГРИБКОВОЙ ОБРАБОТКИ НАБУХАЮЩИХ ПОКРЫТИЙ | 2022 |
|
RU2800456C2 |
| ОПТИЧЕСКИЙ ПОЛЯРИЗАТОР | 1998 |
|
RU2140662C1 |



Изобретение относится к лиотропному жидкому кристаллу хлоргексидина основания, образующемуся в водной жидкокристаллической системе неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатора и регулятора кислотности, при условии, что регулятор кислотности не представляет собой аминокислоту, при последовательном смешении компонентов в порядке деионизированная вода, неионогенное поверхностно-активное вещество или смесь неионогенного и катионного поверхностно-активных веществ, стабилизатор, регулятор кислотности и хлоргексидин основание, характеризующемуся пластинчатой структурой и характеристической вязкостью (η) от 5,099 до 10,197 Па⋅с, при следующем соотношении компонентов, масс. %: неионогенное поверхностно-активное вещество или смесь катионного и неионогенного поверхностно-активных веществ 1,0-30,0; стабилизатор 0,1-5,0; регулятор кислотности 0,03-4,0; хлоргексидин основание 0,1-3,5; деионизированная вода до 100. Лиотропный жидкий кристалл хлоргексидина предназначен в качестве действующего вещества для производства дезинфицирующих или антисептических средств. Технический результат – лиотропный жидкий кристалл хлоргексидина основания, обладающий термодинамической стабильностью, проявляющий высокую биоцидную активность. 3 н. и 5 з.п. ф-лы, 10 ил., 12 табл., 15 пр.
1. Лиотропный жидкий кристалл хлоргексидина основания, образующийся в водной жидкокристаллической системе неионогенного поверхностно-активного вещества или смеси неионогенного и катионного поверхностно-активных веществ, в присутствии стабилизатора и регулятора кислотности, при условии, что регулятор кислотности не представляет собой аминокислоту, при последовательном смешении компонентов в порядке деионизированная вода, неионогенное поверхностно-активное вещество или смесь неионогенного и катионного поверхностно-активных веществ, стабилизатор, регулятор кислотности и хлоргексидин основание, характеризующийся пластинчатой структурой и характеристической вязкостью (η) от 5,099 до 10,197 Па⋅с, при следующем соотношении компонентов, масс. %:
2. Лиотропный жидкий кристалл хлоргексидина основания по п. 1, где в качестве неионогенного поверхностно-активного вещества используют кокоалкилдиметиламинооксид, неонол, оксиэтилированные сорбитаны, в качестве катионного поверхностно-активного вещества используют третичный алкиламин, полигексаметиленгуанидина гидрохлорид или четвертичное аммониевое соединение, выбранное из ряда: алкилдиметилбензиламмоний хлорид, дидецилдиметиламмоний хлорид, ундециленамидопропил-тримониум метосульфат, N,N-дидецил-N-метил-поли(оксиэтил)аммониум пропионат, в качестве стабилизатора используют полиэтиленгликоль с молекулярной массой от 200 до 400, этиленгликоль или многоатомные спирты, выбранные из группы глицирин, 1,4-бутандиол, 1,2-пропандиол раздельно или совместно, в качестве регулятора кислотности используют замещенные органические оксикислоты, выбранные из группы яблочная кислота, молочная кислота, гликолевая кислота, триэтаноламин, комплексоны, выбранные из группы динатриевая соль этилендиаминтетрауксусной кислоты, этилендиаминтетрауксусная кислота.
3. Применение лиотропного жидкого кристалла хлоргексидина основания по п. 1 в качестве действующего вещества для производства дезинфицирующих или антисептических средств.
4. Средство, проявляющее дезинфицирующие или антисептические свойства, содержащее в своем составе лиотропный жидкий кристалл хлоргексидина основания по п. 1.
5. Средство по п. 4 в виде дезинфицирующей композиции, содержащее лиотропный жидкий кристалл хлоргексидина основания по п. 1, дополнительно содержащее биоцидный агент, краситель при следующем соотношении компонентов, масс. %:
6. Средство по п. 5 в виде дезинфицирующей композиции, где в качестве биоцидного агента используют изопропиловый спирт, н-пропиловый спирт, перекись водорода, в качестве красителя используют антрахиноновый краситель, кармуазин (Е122) или триарилметановый краситель (Е133).
7. Средство по п. 4 в виде антисептической композиции, содержащее лиотропный жидкий кристалл хлоргексидина по п. 1 основания, дополнительно содержащее биоцидный агент, загуститель для придания вязкости, краситель и ароматизатор, при следующем соотношении компонентов, масс. %:
8. Средство по п. 7 в виде антисептической композиции, где в качестве биоцидного агента используют изопропиловый или этиловый спирт, в качестве загустителя используют гидроксиэтилцеллюлозу (натросол 250 HR), карбомер, в качестве красителя используют антрахиноновый краситель, кармуазин (Е122) или триарилметановый краситель (Е133).
| СОЛЮБИЛИЗАЦИЯ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2017 |
|
RU2696259C2 |
| Farkas, E., et al.: "Influence of chlorhexidine species on the liquid crystalline structure of vehicle", International Journal of Pharmaceutics, 2001, v.213(1-2), p.1-5 | |||
| FARKAS, E., KISS, D., et al.: "Study on the release of chlorhexidine base and salts from different liquid crystalline structures", International | |||
Авторы
Даты
2021-06-29—Публикация
2021-03-05—Подача