Группа изобретений относится к медицине и фармацевтической промышленности, касается ингаляционной фармацевтической композиции, нового лечебно-профилактического средства и может быть использовано в лечебно-профилактических учреждениях и амбулаторных условия.
Распространение антибиотикорезистентности, неэффективность антибиотиков в отношении бактериальных инфекций требует разработки новых терапевтических подходов к терапии и профилактике.
Стратегической задачей здравоохранения является обеспечение качества медицинской помощи и создание безопасной больничной среды.
Четверть всех случаев инфекций, связанны с оказанием медицинской помощи (ИСПМ), происходит в отделениях реанимации и интенсивной терапии (ОРИТ). Пациенты с ИСПМ находятся в больнице в 2,5 раза дольше, чем аналогичные пациенты без признаков инфекции. Риск летального исхода у этих пациентов в 7 раз выше по сравнению с подобными по возрасту, полу, основной и сопутствующей патологии и тяжести больными.
Лаурилдиметиламиноксид является представляет собой поверхностно-активное вещество на основе оксида амина с алкильным хвостом С 12 (додецил), известный под торговым наименованием Барлокс 12 (Barlox 12, Lonza AG), обладающий высоким пенящим эффектом. Это один из наиболее часто используемых поверхностно-активных веществ этого типа.
Как другие поверхностно-активные вещества на основе оксида амина, он является антимикробным, эффективным против распространенных бактерий, таких как S. aureus и Е. coli.
Высокую степенью содержания поверхности-активных веществ Барлокса 12 обеспечивают с-оксид ко камина природного происхождения. Кокамид - это смесь амидов кокосовых жирных кислот, получают путем конденсации алканоламинов и кокосовой жирной кислоты. В ряде публикаций «Антибактериальная и иммуномодулирующая активность кокосового масла первого отжима (VCO) против золотистого стафилококка», 2019 г. Опубликовано Elsevier Ltd. Статья в открытом доступе по лицензии СС BY-NC-ND (http://creativecommons.org/licenses/bync-nd/4.0/), «Антимикробная активность эмульсии кокосового масла в воде на Staphylococcus epidermidis и Escherichia coli ЕРЕС, связанный с Candida kejyr», 2018 г., Published by Elsevier Ltd. This is an open access article under the CC BY-NC-ND license (http://creativecommons.org/licenses/by-nc-nd/4.0/) детально изложены результаты исследований по поиску нового антибактериального средства из кокосового масла первого отжима, а также было продемонстрировано влияние лауриновой кислоты и монолаурина, находящейся в эмульсии кокосового масла в воде на S. aureus и Е. Coli. По результатам проведенных исследований сделан вывод, что насыщенная жирная кислота - лауриновая кислота (LA) (С 12), содержащаяся в кокосовом масле первого отжима, обладает выраженной антибактериальной и иммуномодулирующей активностью.
Однако, использование поверхностно-активных веществ, таких как лаурилдиметиламиноксид (Барлокс 12) в эффективных дозах в качестве компонентов лекарственного средства для внутреннего потребления ограничено в связи с его токсичностью.
Развитие госпитальной пневмонии, в том числе вентилятор-ассоциированной пневмонии при искусственной вентиляции легких (ИВЛ), обычно связанно с микро- и макроаспирацией содержимого ротоглотки. В связи с чем профилактика и лечение инфекций, связанных с оказанием медицинской помощи (ИСПМ), таких как вентилятор-ассоциированной пневмония, требует не только обще дезинфекционных мероприятий известными антисептическими и дезинфицирующими средствами, такими как хлоргексидин биглюконат или соли хлоргексидина, но и обработка или ингаляцию слизистых полости рта, бронхов, легких, поскольку с меньшей вероятностью вызовет устойчивость к антибиотикам [Torres A., Niederman M.S., Chastre J., Ewig S., FernandezVandellos P., Hanberger H., et al. International ERS/ESICM/ESCMIDf ALAT guidelines for the management of hospitalacquired pneumonia and ventilatorassociatedpneumonia. Eur Respir J. 2017;50(3): 1700582. DOT 10.1183/13993003.005822017; Klompas M., Branson R., Eichenwald E.C., Greene L.R., Howell M.D., Lee G, et al. Strategies to prevent ventilatorassociated pneumonia in acute care hospitals: 2014 update. Infect Control Hosp Epidemiol. 2014;35(8):915936. DOI: 10.1086/677144 rinse in reducing prevalence of nosocomial pneumonia in patients undergoing heart surgery. Am J Crit Care. 2002; 11(6):567-570. DOI: 10.4037/ajcc2002.11.6.567].
Опубликованы данные рандомизированных контролируемых клинических исследований, в которых продемонстрирована эффективность обработки полости рта водными растворами солей хлоргексидина в различных концентрациях - от 0,12% до 2%., например хлоргексидином биглюконатом, ацетатом для профилактики ВАП и других госпитальных инфекций дыхательных путей, особенно у пациентов высокого риска [DeRiso A.J., Ladowski J.S., Dillon ТА., Justice J.W., Peterson A.C. Chlorhexidine gluconate 0.12% oral rinse reduces the incidence of total nosocomial respiratory infection and nonprophylactic systemic antibiotic use in patients undergoing heart surgery. Chest. 1996;109(6):1556-1561. DOI: 10.1378/chest.109.6.1556; Houston S., Hougland P., Anderson J.J., LaRocco M., Kennedy V., Gentry L.O. Effectiveness of 0.12% chlorhexidine gluconate oral].
По результатам проведенных клинических исследований, ряд авторитетных европейских и североамериканских экспертных групп (American Thoracic Society, British Society for Antimicrobial Chemotherapy, The European VAP Care Bundle Contributors) рассматривают обработку слизистой оболочки полости рта водным раствором хлоргексидина биглюконата как важнейший компонент профилактики вентилятор-ассоциированной пневмонии [Применение хлоргексидина для профилактики госпитальных инфекций в отделениях реанимации и интенсивной терапии: современное состояние проблемы, Багин В.А. Рудное В.А., Астафьева М.Н., Городская клиническая больница №40, Екатеринбург, Россия, ФГБОУ ВО «Уральский государственный медицинский университет»Минздрава России, Екатеринбург, Россия].
В исследовании, проведенном в медицинском университете Гонконга, опубликованном в научном журнале «The Lancet Microbe» [Alex W H Chin, Julie T S Chu, Mahen R A Perera, Kenrie P Y Hui, Hui-Ling Yen, Michael С W Chan, Malik Peiris, Leo L M Poon. Stability of SARS-CoV-2 in different environmental conditions // The Lancet Microbe online April 2020. doi: 10.1016/S2666-5247(20)30003-3] была доказана эффективность хлоргексидина биглюконата в концентрации 0,05% водного раствора против SARS-CoV-2.
В заявке на патент США №20210401705 «Композиции для ухода за полостью рта» описаны новые водные композиции для ухода за полостью рта в качестве антибактериальных средств при стоматологических манипуляциях, содержащая эффективное количество перорально приемлемого гуанидного антибактериального средства хлоргексидина биглюконата в сочетании с калиевой или натриевой солью линейного пирофосфата или триполифосфат и катионного или неионогенного поверхностно-активного вещества.
В монографии «Пероральный хлоргексидин в профилактике вентиляторассоциированной пневмонии у взрослых в критическом состоянии в отделении интенсивной терапии: систематический обзор» [Оливия Снайдерс, MCur, PGDN (Управление сестринским делом), Dip Nursing Отделение нейрореанимации, Госпиталь национальной гвардии им. короля Фахда, Эр-Рияд, Саудовская Аравия Освелл Хондове, MSc (РТ), MSc АРА, BSc (РТ), Dip РТ, Джанет Белл, MCur, BCur, PGDN, Отделение сестринского дела, Стелленбосский университет, Тигерберг, Западный Кейп, SAJCC, ноябрь 2011 г., Vol. 27, №2] описаны использование хлоргексидина биглюконата в качестве орального дезинфицирующего средства у пациентов с искусственной вентиляцией легких из-за его способности связываться с тканями полости рта с последующим медленным высвобождением антисептических свойств и, следовательно, длительным периодом антибактериального действия.
В патенте WO 2002051464 (PCT/US2001/049205) описано применение хлоргексидина основания, как наиболее сильного антисептика в сравнении с хлоргекидином биглюконатом и/или солью хлоргексидина, в комбинации с солью хлоргекидина для обработки медицинских изделий, применяемых при ИВЛ.
Зарегистрированы в качестве лекарственных средств и используются соли хлоргексидина, такие как хлоргексидина биглюконат в комбинации с метронидазолом (Метроксидин дента®, Метродент®), хлоргексидина дигидрохлорид в комбинации с лидокаином в виде таблеток для рассасывания (Септалор®).
В патенте РФ №2696259 показаны высокоэффективные составы дезинфицирующих и антисептических средств, где в качестве действующего вещества использован солюбилизат хлоргексидина основания.
В патенте №2750598 показано, что наибольшую дезинфицирующую и антисептическую активность проявили композиции с лиотропным жидким кристаллом хлоргексидина основания.
Однако, все известные композиции и составы с хлоргексидином биглюконатом, при их достаточно высокой дезинфицирующей и антисептической активности не могут применяться в качестве фармацевтических ингаляционных композиций для профилактики и лечения заболеваний бронхов и легких, в виду его местно-раздражающего и потенциального кумулятивного токсического эффекта.
Известно гипоосмотическое средство с противомикробной активностью, применяемое для обработки полости рта, представляющее собой водный раствор 0,12-0,2% хлоргексидина биглюконата [Особенности профилактики нозокомиальной пневмонии у больных с острым нарушением мозгового кровообращения, А.В. Зверьков, А.П. Зузова, ГБОУ ВПО «Смоленская государственная медицинская академия» Минздрава России, Смоленск, Клиническая Микробиология и Антимикробная Химиотерапия 2013; Том 15, №2: 95-105). Недостатком данного средства является недоказанная эффективность в профилактике нозокомиальной пневмонии у хирургических и соматических больных в отделениях реанимации.
Наиболее близким к заявляемому изобретению являются средство по патенту RU 2682642, в котором в качестве действующего вещества используют соли хлоргексидина, в основном глюконат хлоргексидина, предпочтительно в концентрации примерно от 1,0%, до 0,02% для предотвращения или уменьшения образования биопленки на участке инфекции путем введения в биопленку водного раствора глюконата хлоргексидина. Как было декларировано в патенте RU 2682642 раствор глюконата хлоргексидина по может быть приготовлен в виде лекарственной формы, пригодной для ингаляции, например, людьми, страдающими пневмонией или другими инфекциями дыхательных путей. В конкретном варианте раствор хлоргексидина готовят в виде лекарственной формы, пригодной для пациентов с муковисцидозом (MB), у которых имеется инфекция легких или которые подвержены риску развития такой инфекции.
Однако, в прототипе вообще не раскрыты, возможные составы лекарственного средства, пригодного для ингаляции, например, людьми, страдающими пневмонией или другими инфекциями дыхательных путей. Не раскрыто влияние глюконата хлоргексидина на другие виды возбудителей, например, Pseudomonas aeruginosa, вызывающих заболевания дыхательной системы.
Общим недостатком известных антисептиков является их не селективность и токсическая опасность для человека в дозировках, зарегистрированных в качестве наружных антисептических или дезинфицирующих средств.
Одним из наиболее частых возбудителей инфекций, связанных с оказанием медицинской помощи, является Pseudomonas aeruginosa. По данным ВОЗ этим микроорганизмом обусловлено более 16% случаев пневмоний, 12% инфекций мочевыводящих путей, 8% инфекций хирургических ран, 10% случаев инфекций кровотока.
Задачей настоящего изобретение является применение хлоргексидина основания в качестве лечебно-профилактического средства для профилактики и лечения широко спектра инфекций у субъектов, включая вентилятор-ассоциированную пневмонию, возникающих по вине инфекций, связанных с оказанием медицинской помощи, в комплексном лечении кистозного фиброза легких, хронической обструктивной болезни легких и лечения ожоговых ран, заболеваний урогенитального тракта, герпетических инфекций как самостоятельно, так и с добавлением в состав дополнительных активных и фармацевтически приемлемых вспомогательных ингредиентов.
Краткое описание чертежей
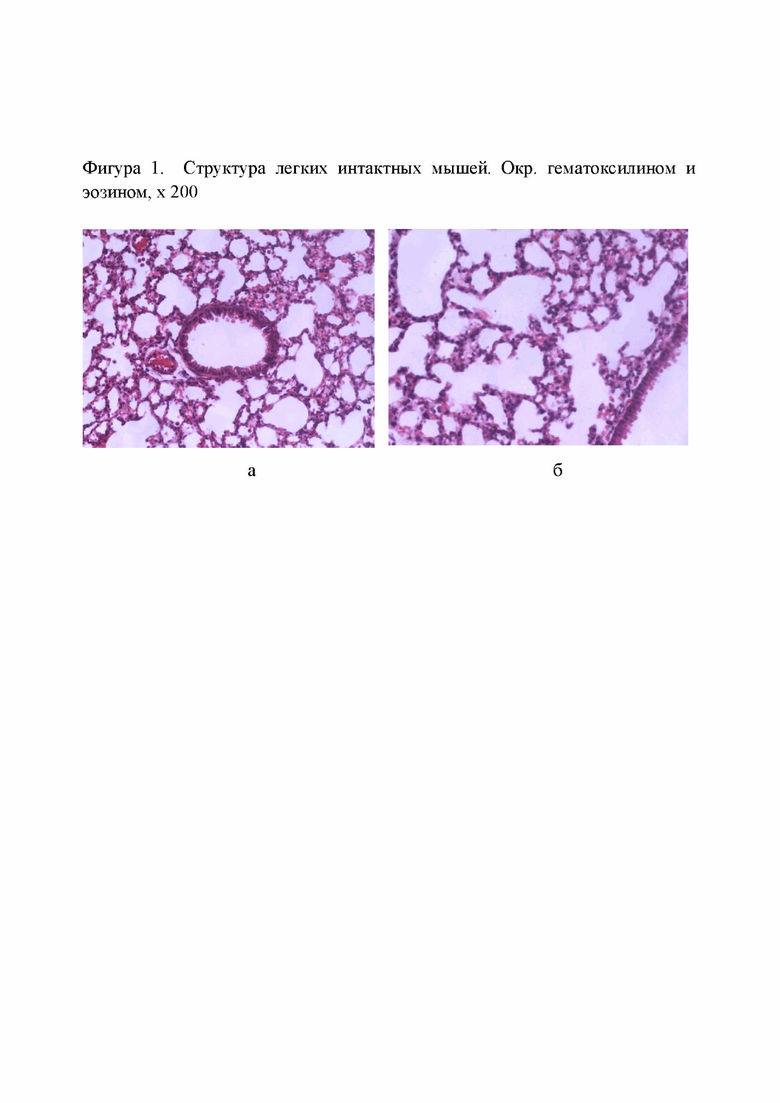
Фигура 1. - Структура легких интактных мышей. Окр. гематоксилином и эозином, х 200;
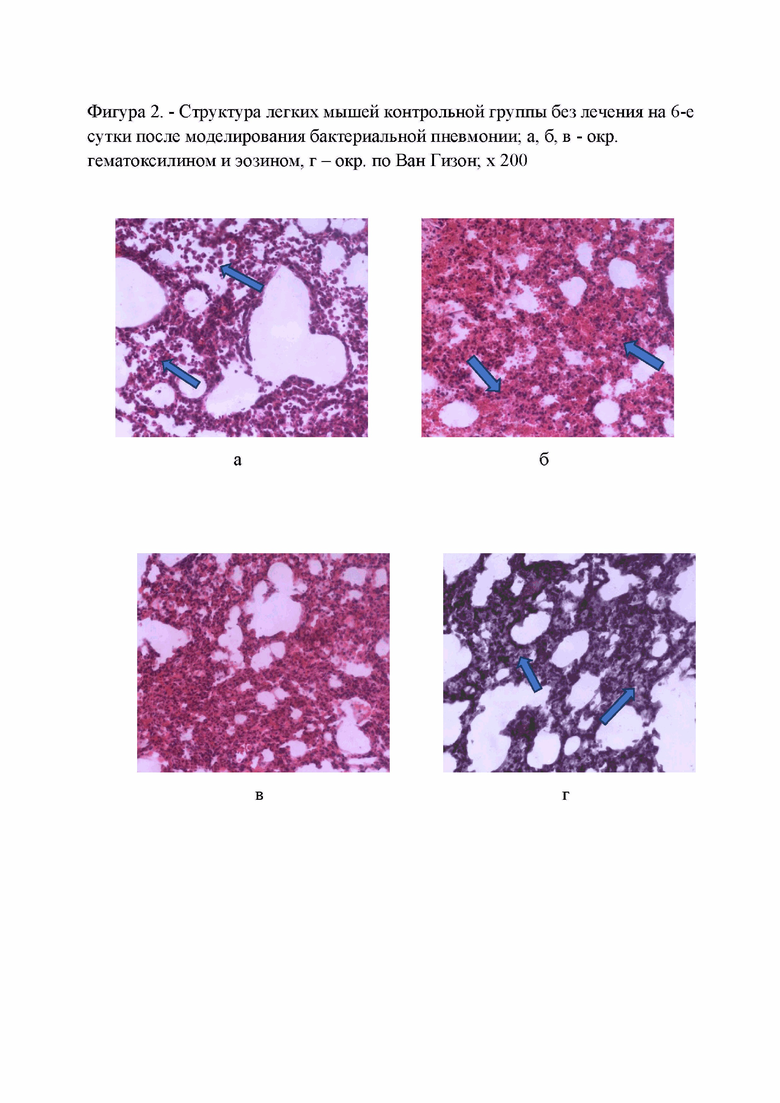
Фигура 2. - Структура легких мышей контрольной группы без лечения на 6-е сутки после моделирования бактериальной пневмонии; а, б, в - окр. гематоксилином и эозином, г - окр. по Ван Гизон; х 200;
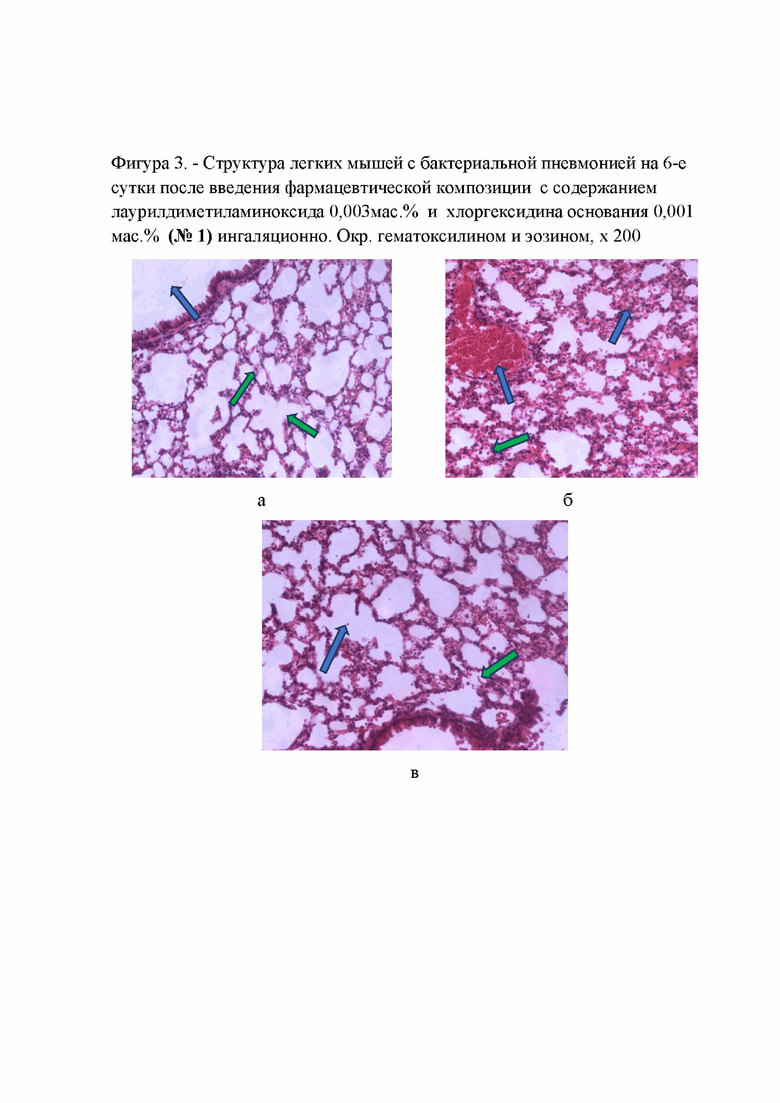
Фигура 3. - Структура легких мышей с бактериальной пневмонией на 6-е сутки после введения фармацевтической композиции с содержанием лаурилдиметиламиноксида 0,003 мас. % и хлоргексидина основания 0,001 мас. % (№1) ингаляционно. Окр. гематоксилином и эозином, х 200;
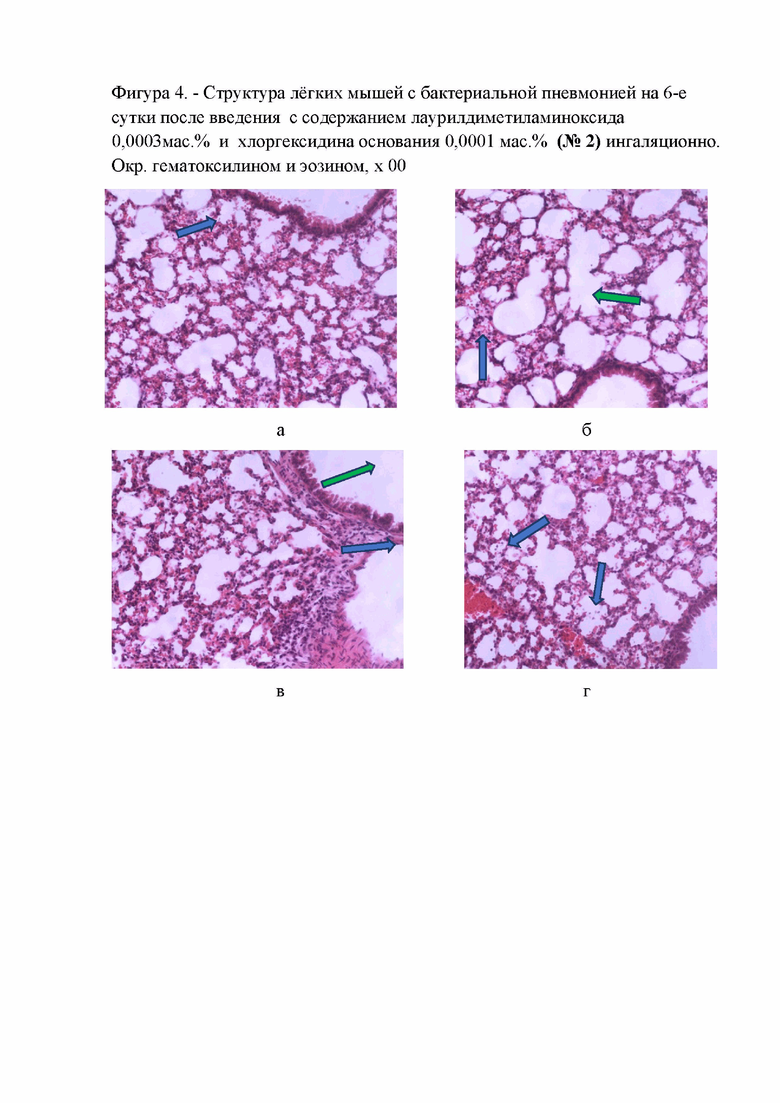
Фигура 4. - Структура легких мышей с бактериальной пневмонией на 6-е сутки после введения с содержанием лаурилдиметиламиноксида 0,0003 мас. % и хлоргексидина основания 0,0001 мас. % (№2) ингаляционно. Окр. гематоксилином и эозином, х 00;
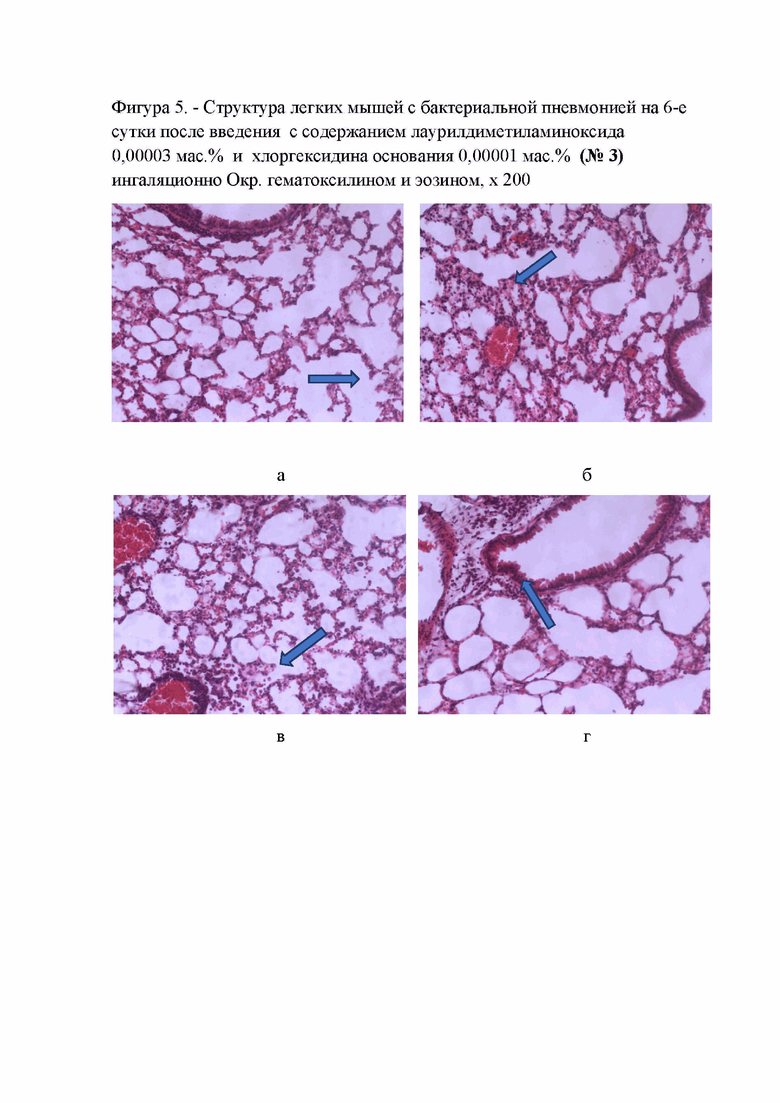
Фигура 5. - Структура легких мышей с бактериальной пневмонией на 6-е сутки после введения с содержанием лаурилдиметиламиноксида 0,00003 мас. % и хлоргексидина основания 0,00001 мас. % (№3) ингаляционно Окр. гематоксилином и эозином, х 200;
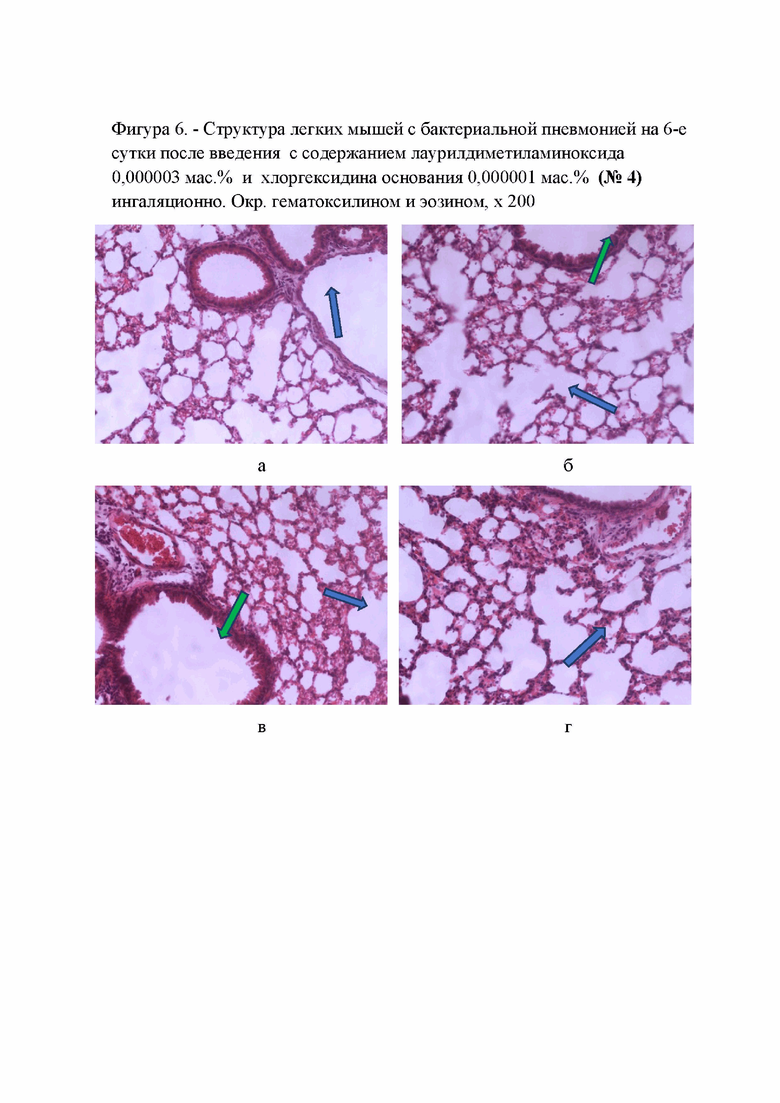
Фигура 6. - Структура легких мышей с бактериальной пневмонией на 6-е сутки после введения с содержанием лаурилдиметиламиноксида 0,000003 мас. % и хлоргексидина основания 0,000001 мас. % (№4) ингаляционно Окр. гематоксилином и эозином, х 200;
Сущность изобретения
Поставленная задача решается созданием ингаляционной фармацевтической композиции для лечения или профилактики бактериальных инфекционных заболеваний, включающей лаурилдиметиламиноксид, полиэтиленгликоль, хлогексидин основание, аминокислоту, деионизированную воду, при следующем соотношении компонентов, мас. %:
В которой за счет сочетания двух компонентов лаурилдиметиламиноксида и хлоргексидина основания при их низких концентрациях достигается антибактериальный синергетический эффект.
Сочетание компонентов, один из которых - лаурилдиметиламиноксид несет двойную функцию, как поверхностно-активное вещество и как антибактериальный агент, второй хлоргексидин основание в присутствии лаурилдиметиламиноксида, полиэтиленгликоля и аминокислоты приобретает водорастворимые свойства и раскрывается как сильный антибактериальный агент.
Полученные данные исследований показывают взаимное синергетическое влияние активных компонентов, что позволяет достаточно сильно разбавленным композициям проявлять высокую антибактериальную активность.
Под лаурилдиметиламиноксидом понимается Барлокс 12 (Lonza AG), под полиэтиленгликолем - Плюриол® Е 200 (Pluriol® Е 200, BASF), под аминокислотой - предпочтительно глицин.
Полученная ингаляционная фармацевтическая композиция представляет собой устойчивую систему, которая предназначена для применения в качестве готового фармацевтического лечебно-профилактического средства для профилактики или лечения вентилятор-ассоциированной пневмонии, кистозного фиброза легких, хронической обструктивной болезни легких.
Готовую фармацевтическую композицию вводят в дыхательные органы прибором для ингаляции или распылители, например, паров, частиц и/или аэрозолей.
Получение готовой ингаляционной фармацевтической композиции характеризуется последовательным смешением компонентов в порядке деионизированная вода, лаурилдиметиламиноксид, полиэтиленгликоль, хлоргексидин основание, аминокислота.
Получение фармацевтической композиции иллюстрируется следующими примерами.
Пример 1. Для получения 100 мл готовой ингаляционной фармацевтической композиции, 3,0 мг лаурилдиметиламиноксид (Барлокс-12, каталог фирмы "Lonza" (Лонза), при комнатной температуре растворяют в 99,002 мл деионизированной воды, добавляют 2,0 мг полиэтиленгликоля, 1,0 мг хлоргексидина основания, 2,0 мг глицина.
Полученная готовая фармацевтическая композиции по примеру 1 представляет собой прозрачный раствор, имеющий рН 7,2.
Пример 2. Осуществляют аналогично примеру 1. Для получения 100 мл готовой ингаляционной фармацевтической композиции, 0,3 мг лаурилдиметиламиноксид (Барлокс-12, каталог фирмы "Lonza" (Лонза), при комнатной температуре растворяют в 99,0002 мл деионизированной воды, добавляют 0,2 мг полиэтиленгликоля, 0,1 мг хлоргексидина основания, 0,2 мг глицина.
Полученная фармацевтическая композиции по примеру 2 представляет собой прозрачный раствор, имеющий рН 7,1.
Пример 3. Осуществляют аналогично примеру 1. Для получения 100 мл готовой ингаляционной фармацевтической композиции, 0,03 мг лаурилдиметиламиноксид (Барлокс-12, каталог фирмы "Lonza" (Лонза), при комнатной температуре растворяют в 99,00002 мл деионизированной воды, добавляют 0,02 мг полиэтиленгликоля, 0,01 мг хлоргексидина основания, 0,02 мг глицина.
Полученная фармацевтическая композиции по примеру 3 представляет собой прозрачный раствор, имеющий рН 7,0.
Пример 4. Осуществляют аналогично примеру 1. Для получения 100 мл готовой ингаляционной фармацевтической композиции, 0,003 мг лаурилдиметиламиноксид (Барлокс-12, каталог фирмы "Lonza" (Лонза), при комнатной температуре растворяют в 99,000002 мл деионизированной воды, добавляют 0,002 мг полиэтиленгликоля, 0,001 мг хлоргексидина основания, 0,002 мг глицина.
Полученная фармацевтическая композиции по примеру 4 представляет собой прозрачный раствор, имеющий рН 6,9.
Для исследования были использованы рабочие растворы фармацевтической композиции, представленные в Таблице №1
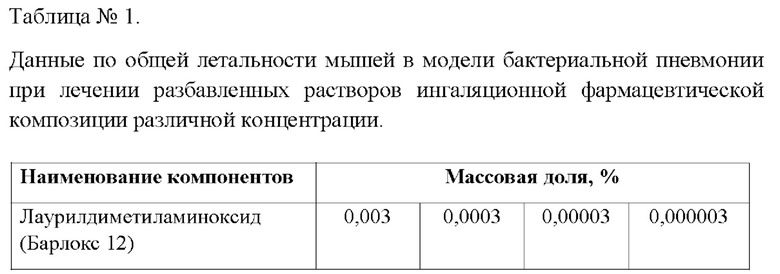
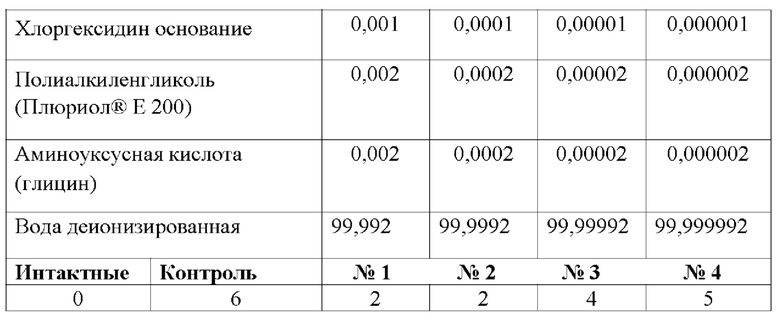
Известно, что один из компонентов ингаляционной фармацевтической композиции лаурилдиметиламиноксид (Барлокс 12) является умеренно токсичным веществом, и в настоящее время не имеет фармацевтического применения. В то время как глицин, как биологически активная аминокислота и полиэтиленгликоль, как вспомогательное вещество имеют широкое фармацевтическое применение.
С целью определения диапазона токсичности полученных разведенных лекарственных форм - растворов фармацевтической композиции были проведены доклинические исследования острой, субхронической токсичности и местнораздражающего действия при внутрижелудочном и ингаляционном способе введения на тест-системах половозрелых аутбредных белых мышах стоков SHK и крысах Wistar.
Исследования фармацевтической композиции с высоким содержанием лаурилдиметиламиноксида и хлоргексидина основания (0,1-0,01 мас. %) показало достаточно высокую токсичность для организма, вызывающую отсроченную гибель животных, особенно при ингаляционном способе введения, проявляющую выраженное местно-раздражающее действие.
Токсикологические исследования показали, что при ингаляционном применении готовой фармацевтической композиции в низких концентрациях, с содержанием лаурилдиметиламиноксид от 0,003 до 0,000003 мас. % и хлоргексидина основания от 0,001 до 0,000001 мас. % (от 10-3 до 10-6), является безопасным для органов и систем организма, не оказывает выраженного местно-раздражающего действия.
После ингаляционного введения готовых лекарственных форм фармацевтической композиции не отмечено каких-либо нарушений структуры носовой полости животных, слизистая оболочка носовой полости была без признаков отека и гиперемии.
Не выявлено каких-либо нарушений структуры легких после ингаляционного введения готовой фармацевтической композиции, с содержанием лаурилдиметиламиноксида от 0,003 до 0,000003 мас. % и хлоргексидина основания от 0,001 до 0,000001 мас. % (от 10-3 до 10-6) у животных. В легких наблюдались хорошо расправленные альвеолы с тонкими стенками и свободным просветом. Ядра альвеолярного эпителия четкие, цитоплазма оксифильная. Бронхиолы и бронхи выстланы кубическим и цилиндрическим эпителием, просвет их свободен. Вокруг крупных бронхов наблюдаются единичные узелки лимфоидной ткани. Наблюдается умеренное полнокровие сосудистого русла.
Данные токсикологических исследований позволили выявить диапазон эффективных и безопасных концентраций лаурилдиметиламиноксида и хлоргексидина основания.
Сравнительные исследования эффективности полученных фармацевтических композиций проводилось согласно критерию потенциальной пользы фармакотерапии и ассоциированных с ней рисков.
Полученные готовые фармацевтические композиции были изучены на предмет фармакологического специфического действия на модели бактериальной пневмонии на примере, вызванной Pseudomonas aeruginosa.
Доклиническое исследование выполнено в соответствии с принципами GLP «Правил надлежащей лабораторной практики в сфере обращения лекарственных средств».
В исследовании препарат вводился ингаляционно. Доставка лекарственных композиций непосредственно в легкие с помощью ингаляции имеет несколько преимуществ по сравнению с пероральным или парентеральным путями. Этот не инвазивный способ введения позволяет добиться высокой концентрации лекарственного препарата непосредственно в легких. Это увеличивает концентрацию лекарства в месте действия лекарства и уменьшает системное воздействие и, следовательно, системные побочные эффекты или взаимодействия лекарства.
Ингаляционное введение хорошо переносится и может применяться как в стационаре, так и амбулаторно.
Введение композиции в легкие снижает влияние печеночных ферментов на вводимые компоненты и обеспечивает их более длительное действие.
Ингаляционный способ введения позволяет добиться достаточной эффективности при введении значительно более низких доз препаратов, в сравнении с пероральным и парэнтеральным введением.
Ингаляционное введение в зависимости от выбранного лечебного агента может использоваться как терапевтически, так и профилактически.
Моделирование бактериальной пневмонии проводилось путем интраназального заражения Pseudomonas aeruginosa, с последующей количественной оценкой колонизации легких.
В экспериментах были использованы следующие тест-системы: половозрелые мыши линии C57BL/6, самцы. Примеры осуществления исследования.
Эксперименты проводились на мышах самцах (n=60), которые были разделены на 6 групп по 10 животных в каждой: 1 группа - Интактные (n=10);
2 группа - Контроль (бактериальная пневмония + растворитель) (n=10);
3 группа - 0,003 мас. % по лаурилдиметиламиноксид и 0,001 мас. % по хлоргексидину основанию, фармацевтическая композиция вводилась ингаляционно (бактериальная пневмония + лечение) (n=10);
4 группа - 0,0003 мас. % по лаурилдиметиламиноксид и 0,0001 мас. % по хлоргексидину основанию, фармацевтическая композиция вводилась ингаляционно (бактериальная пневмония + лечение) (n=10);
5 группа - 0,00003 мас. % по лаурилдиметиламиноксид и 0,00001 мас. % по хлоргексидину основанию, фармацевтическая композиция вводилась ингаляционно (бактериальная пневмония + лечение) (n=10);
6 группа - 0,000003 мас. % по лаурилдиметиламиноксид и 0,000001 мас. % по хлоргексидину основанию, фармацевтическая композиция вводилась ингаляционно (бактериальная пневмония + лечение) (n=10).
Через 24 часа после интраназального заражения суспензией микроорганизмов Pseudomonas aeruginosa (штамм 1456 клинический изолят), исследуемые фармацевтические композиции вводились ингаляционно ежедневно, в течение 5 дней во всех опытных группах.
Через 5 дней, после ингаляционного применения препаратов, произвели забор бронхоальвеолярного лаважа для определения колонизации легких Pseudomonas aeruginosa в контрольной и в экспериментальных группах животных.
Летальность. Исследование показало, что применение фармацевтических композиций снижает летальность в 3 раза.
Летальность мышей при моделировании бактериальной пневмонии в течение 6 суток составила 60% в группе без лечения. Применение исследуемых фармацевтических композиций снизило летальность до 20% в зависимости от концентрации хлоргексидина. Наибольшую терапевтическую эффективность показали фармацевтические композиции с концентрацией по лаурилдиметиламиноксид от 0,003 до 0,0003 мас. % и по хлоргексидину основанию от 0,001 до 0,0001 мас. %, Таблица №1.
Антимикробное действие. Фармацевтическая композиция обладают выраженным антибактериальным действием в отношении возбудителя бактериальной пневмонии Pseudomonas aeruginosa.
Наибольшую эффективность показали фармацевтические композиции в концентрациях по лаурилдиметиламиноксид от 0,003 до 0,0003 мас. % и по хлоргексидину основанию от 0,001 до 0,0001 мас. %.
Применения ингаляционной фармацевтической композиции в концентрациях по лаурилдиметиламиноксид от 0,003 до 0,0003 мас. % и по хлоргексидину основанию от 0,001 до 0,0001 мас. % на протяжении 5 дней привело к полному отсутствию Pseudomonas aeruginosa в исследуемом материале, данные приведены в Таблице 2.
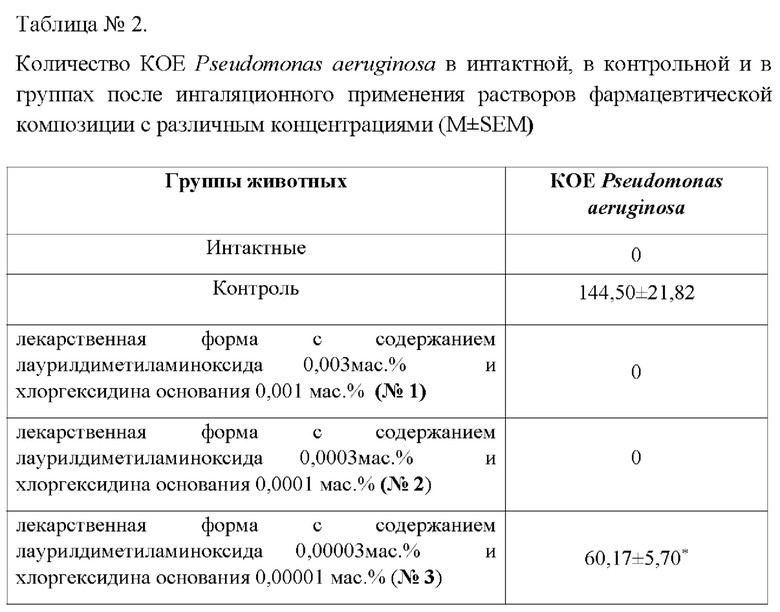

После применения ингаляционных фармацевтических композиций в концентрациях по лаурилдиметиламиноксид от 0,00003 до 0,000003 мас. % и по хлоргексидину основанию от 0,00001 до 0,000001 мас. % на протяжении 5 дней выявлено достоверное уменьшение колонизации легочной ткани по сравнению с контрольной группой.
При моделировании бактериальной пневмонии не зависимо от концентрации лаурилдиметиламиноксида и хлоргексидина основанию, выявился выраженный противовоспалительный эффект фармацевтических композиций в легких, проявляющийся в снижении повышенного содержания лейкоцитов в бронхоальвеолярном лаваже мышей, данные отражены в Таблице 3.
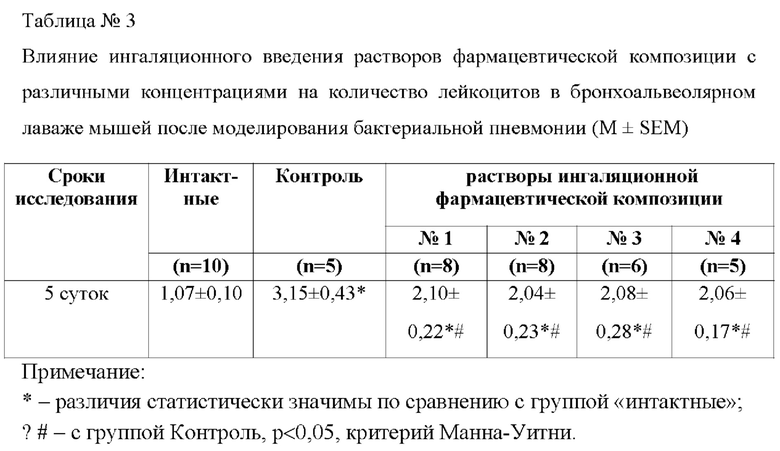
Гистологическое исследование легких показало, что по совокупности всех изученных интегральных показателей наиболее эффективным в лечении бактериальной пневмонии, вызванной Pseudomonas aeruginosa, является разбавленный раствор фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,0003 мас. % и хлоргексидина основания 0,0001 мас. %.
В рамках сравнительных исследований сравнивались биообразцы легких интактных животных, где хорошо видны округлые, хорошо расправленные альвеолы с тонкими стенками и свободным просветом. Ядра альвеолярного эпителия четкие, цитоплазма оксифильная. Бронхиолы и бронхи выстланы кубическим и цилиндрическим эпителием, просвет их свободен (Фигура 1а и б) с образцами легких мышей, не получавших и получавших лечение.
Контроль без лечения.
Развитие бактериальной пневмонии в легких на 6-й день сопровождалось участками умеренно выраженного отека рыхлой соединительной ткани, окружающей бронхи и сопутствующие им сосуды с диффузной инфильтрацией воспалительными элементами. В просвете альвеол определялись скопления макрофагов, лимфоцитов, полиморфноядерных лейкоцитов и клеток альвеолярного эпителия (Фигура 2а, синие стрелки). В части паренхимы легких наблюдались участки с выраженным утолщением стенок альвеол за счет их отека, полнокровия сосудов, инфильтрации клетками воспалительного ряда, кровоизлияния (Фигура 2б, синие стрелки). Отмечены участки с нарушением гистоархитектоники респираторного отдела легких с закрытием просветов альвеол, выраженным утолщением их стенок (Фигура 2, в), с признаками фиброза в виде тонких волокон коллагена (Фигура 2, в, г, синие стрелки).
Применение лекарственной фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,003 мас. % и хлоргексидина основания 0,001 мас. % на 6-е сутки после его введения показало отсутствие перибронхиального отека, бронхи и мелкие бронхиолы имели открытый чистый просвет (Фигура 3, а, синяя стрелка). Подавляющее большинство альвеол были расправлены, имели открытый чистый просвет (Фигура 3, а, зеленые стрелки). Отмечены значительные участки полнокровия сосудистого русла (Фигура 3, б, синие стрелки) и небольшие участки с неравномерным растяжением альвеолярных стенок (Фигура 3, в синяя стрелка). В некоторых участках паренхимы легких в стенке альвеол наблюдались единичные воспалительные клетки (Фигура 3, б, в, зеленая стрелка).
При применении лекарственной фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,0003 мас. % и хлоргексидина основания 0,0001 мас. % у животных на 6-е сутки после его введения в ткани легких наблюдались наряду с нормальными альвеолами участки альвеол с утолщением их стенок за счет отека и полнокровия капилляров (Фигура 4, а, б, синие стрелки). Альвеолы в подавляющем большинстве расправлены, с чистым просветом. Отмечались участки с неравномерным растяжением альвеол (Фигура 4б, зеленая стрелка). Единичными явлениями было наличие слабо выраженного воспалительного инфильтрата вокруг бронхов и крупных сосудов (Фигура 4, в, синяя стрелка). Бронхи и мелкие бронхиолы имели открытый чистый просвет (Фигура 4, в, зеленая стрелка). В паренхиме легкого редко встречались участки с воспалительными клетками в стенке альвеол и единичные мелкие участки с несколькими клетками воспалительного ряда и альвеолярного эпителия в просвете альвеол (Фигура 4, г, синие стрелки).
Применение лекарственной фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,00003 мас. % и хлоргексидина основания 0,00001 мас. % приводило к купированию проявлений бактериальной пневмонии у животных на 6-е сутки после его введения. Подавляющее большинство альвеол были расправлены, имели открытый чистый просвет и тонкие стенки, в то же время, часть альвеол была перерастянута (Фигура 5а, синяя стрелка). Наблюдались единичные участки с утолщением стенок альвеол как за счет полнокровия капилляров, так и за счет незначительного содержания в стенках альвеол клеток воспалительного ряда (Фигура 5б, синяя стрелка). Отмечены участки ткани легкого, где в просвете альвеол определялись единичные воспалительные клетки и клетки слущенного альвеолярного эпителия (Фигура 5в, синяя стрелка). Также выявлен незначительный перибронхиальный и периваскулярный отек, сопровождающийся слабовыраженным воспалительным инфильтратом (Фигура 5г, синяя стрелка).
При применении лекарственной формы фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,000003 мас. % и хлоргексидина основания 0,000001 мас. % у животных на 6-е сутки после его введения наблюдался незначительный перибронхиальный и периваскулярный отек, сопровождающийся слабовыраженным воспалительным инфильтратом (Фигура 6а, синяя стрелка). Бронхи и мелкие бронхиолы имели открытый чистый просвет (Фигура 6б, в зеленая стрелка). Подавляющее большинство альвеол были расправлены, имели открытый чистый просвет и тонкие стенки, наблюдались единичные участки с утолщением стенок альвеол за счет полнокровия капилляров или слабой инфильтрации их стенки воспалительными элементами (Фигура 6в, синяя стрелка). Часть альвеол была с перерастянутыми стенками и увеличенным объемом (Фигура 6б, г, синяя стрелка).
Таким образом, на 6-е сутки развития бактериальной пневмонии в легких контрольной группы животных без лечения обнаружено выраженное нарушение структуры: интерстициальный отек, локализованный в перибронхиальной области и вокруг сопутствующих сосудов, диффузный воспалительный инфильтрат в этой области. Отмечено утолщение альвеолярных перегородок с участками нарушения гистоархитектоники респираторного отдела с признаками фиброза, заполнением альвеол клетками воспалительного ряда, кровоизлияниями.
Применение ингаляционной фармацевтической композиции хлоргексидина основания на 6-е сутки лечения независимо от концентрации приводило к значительному снижению выраженности как перибронхиального и периваскулярного отека, так и резкому уменьшению воспалительного инфильтрата. При этом лучший результат по этим признакам показан в группах животных с лечением раствором фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,0003 мас. % и хлоргексидина основания 0,0001 мас. %, где практически не выявлен отек вокруг бронхов и сосудов и выявлены лишь редкие небольшие участки с единичными воспалительными клетками в стенке и просвете альвеол. При лечении раствором фармацевтической композиции с концентрацией лаурилдиметиламиноксида 0,00003-0,000003 мас. % и хлоргексидина основания 0,00001-0,000001 мас. % перибронхиальный и периваскулярный отек, сопровождающийся воспалительным инфильтратом, также были слабо выражены.
Во всех группах животных с лечением подавляющее большинство альвеол были расправлены, имели открытый чистый просвет, отмечались участки с неравномерным растяжением альвеол.
Однако, обращает на себя внимание, что лечение ингаляционной фармацевтической композицией с концентрацией лаурилдиметиламиноксида 0,003 мас. % и хлоргексидина основания 0,001 мас. % приводило к появлению в паренхиме легких больших участков с полнокровием капилляров стенок альвеол, что, по-видимому, явилось результатом раздражающего действия препарата в более высоких концентрациях.
В группах животных, получавших лечение фармацевтической композицией во всех заявленных концентрациях практически все количественные показатели, характеризующие эффективность лечения, статистически достоверно снижались относительно повышенных у контрольных животных, данные приведены в Таблице 4.
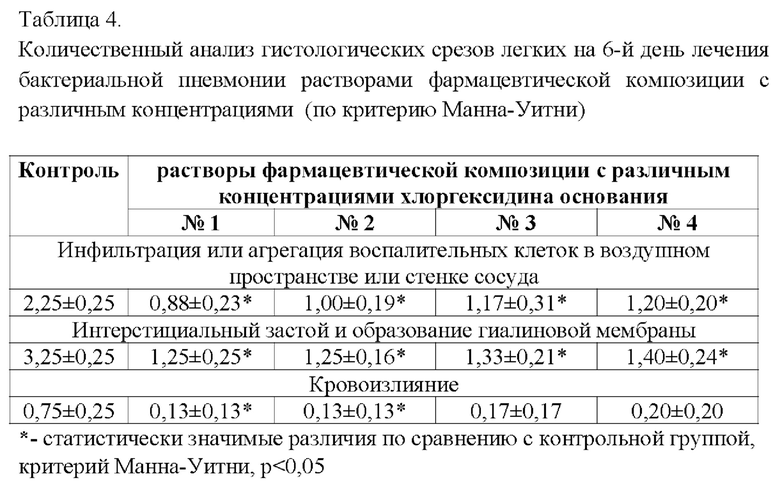
Проведенные экспериментальные доклинические исследования показали высокую эффективность, путем достижения синергетического эффекта и безопасность фармацевтической композиции с концентрацией лаурилдиметиламиноксида от 0,003 до 0,000003 мас. % и хлоргексидина основания от 0,001 до 0,000001 мас. % для профилактики и комплексного лечения заболеваний у человека, вызванных широким спектром возбудителей, включая вентилятор-ассоциированную пневмонию, возникающих по вине инфекций, связанных с оказанием медицинской помощи, в комплексном лечении кистозного фиброза легких, хронической обструктивной болезни легких, при муковисцидозе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЛЮБИЛИЗАЦИЯ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2017 |
|
RU2696259C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ В ПОЛОСТИ РТА И ВЕРХНИХ ДЫХАТЕЛЬНЫХ ПУТЯХ | 2023 |
|
RU2813879C1 |
| ЛИОТРОПНЫЙ ЖИДКИЙ КРИСТАЛЛ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2021 |
|
RU2750598C1 |
| Способ лечения и профилактики рецидивов нозокомиальной пневмонии | 2021 |
|
RU2794585C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРА АЛЬФА1-ПРОТЕИНАЗЫ (АЛЬФА1-АНТИТРИПСИНА) ДЛЯ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО ДИСТРЕСС СИНДРОМА И СПОСОБ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО ДИСТРЕСС СИНДРОМА С ИСПОЛЬЗОВАНИЕМ АЛЬФА1-АНТИТРИПСИНА | 2020 |
|
RU2757875C1 |
| Стоматологическая пленка для лечения и профилактики альвеолита с фитопелоидной композицией | 2019 |
|
RU2734250C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНЫМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ, И ЕЕ ПРИМЕНЕНИЯ | 2009 |
|
RU2590980C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2021 |
|
RU2761303C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНЫМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2016 |
|
RU2650998C2 |
| ПЛЕНКООБРАЗУЮЩЕЕ АНТИСЕПТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2009 |
|
RU2410092C1 |
Группа изобретений относится к медицине и фармацевтической промышленности и может быть использована для лечения или профилактики бактериальных инфекционных заболеваний. Ингаляционная фармацевтическая композиция для лечения или профилактики бактериальных инфекционных заболеваний включает лаурилдиметиламиноксид, полиэтиленгликоль, хлогексидин основание, аминокислоту и деионизированную воду при следующем соотношении компонентов, мас.%: лаурилдиметиламиноксид 0,003 - 0,000003; полиэтиленгликоль 0,002 - 0,000002; хлоргексидин основание 0,001 - 0,000001; аминокислота 0,002 - 0,000002; вода деионизированная до 100. Предложены также применение указанной композиции для лечения и профилактики бактериальных инфекционных заболеваний, включая вентилятор-ассоциированную пневмонию, кистозный фиброз легких и хроническую обструктивную болезнь легких, и способ получения указанной композиции, включающий стадии последовательного смешения компонентов в порядке деионизированная вода, лаурилдиметиламиноксид, полиэтиленгликоль, хлоргексидин основание, аминокислота. Обеспечивается синергетический антибактериальный эффект, что позволяет достаточно сильно разбавленным композициям проявлять высокую антибактериальную активность. 3 н. и 2 з.п. ф-лы, 6 ил., 4 табл., 4 пр.
1. Ингаляционная фармацевтическая композиция для лечения или профилактики бактериальных инфекционных заболеваний, включающая лаурилдиметиламиноксид, полиэтиленгликоль, хлогексидин основание, аминокислота, деионизированная вода, при следующем соотношении компонентов, мас.%:
2. Ингаляционная фармацевтическая композиция по п.1, где лаурилдиметиламиноксид предпочтительно представляет собой Барлокс 12, полиалкиленгликоль предпочтительно представляет собой Плюриол® Е 200, аминокислота предпочтительно представляет собой глицин.
3. Применение ингаляционной фармацевтической композиции по пп.1, 2 для лечения и профилактики бактериальных инфекционных заболеваний.
4. Применение ингаляционной фармацевтической композиции по п.3, где указанные инфекционные заболевания выбраны из вентилятор-ассоциированной пневмонии, кистозного фиброза легких, хронической обструктивной болезни легких.
5. Способ получения фармацевтической композиции по пп.1, 2, включающий стадии последовательного смешения компонентов в порядке деионизированная вода, лаурилдиметиламиноксид, полиэтиленгликоль, хлоргексидин основание, аминокислота.
| СОЛЮБИЛИЗАЦИЯ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2017 |
|
RU2696259C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ РАЗЛИЧНОЙ ЭТИОЛОГИИ ПУТЕМ ОРОМУКОЗНОГО ВВЕДЕНИЯ | 2013 |
|
RU2538433C1 |
| ПРОТИВОМИКРОБНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2500394C2 |
| МАТЕРИАЛЫ И СПОСОБЫ БОРЬБЫ C ИНФЕКЦИЯМИ | 2014 |
|
RU2682642C1 |
| ЛИОТРОПНЫЙ ЖИДКИЙ КРИСТАЛЛ ХЛОРГЕКСИДИНА ОСНОВАНИЯ, АНТИСЕПТИЧЕСКАЯ И ДЕЗИНФИЦИРУЮЩАЯ КОМПОЗИЦИИ | 2021 |
|
RU2750598C1 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе диоксидина | 2016 |
|
RU2667974C2 |
| WO 2020236718 A1, 26.11.2020. | |||
Авторы
Даты
2022-08-01—Публикация
2022-05-24—Подача