Изобретение относится к медицине, а именно к экспериментальной онкологии, и касается способа трансплантации фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки иммунодефицитных мышей для получения ортотопической пациентоподобной модели, наиболее точно отражающей молекулярно-биохимические, цитологические и гистологические особенности канцерогенеза, происходящего в организме человека.
В настоящее время рак толстой кишки представляет собой одну из наиболее распространенных форм злокачественных новообразований во всех странах. Каждый год в мире выявляется около 1 миллиона новых случаев рака толстой кишки (Имянитов Е.Н. Клинико-молекулярные аспекты колоректального рака: этиопатогенез, профилактика, индивидуализация лечения // Практическая онкология. - 2005. - Т. 6, №2. - С. 65-70). Причем в последние десятилетия наблюдается тенденция увеличения числа больных с данным диагнозом (Helm J.F., Sandler R.S. Colorectal cancer screening // Med. Clin. North. Am. - 1999. - Vol. 83. - P. 1403-1422; Jean Faivre Screening for colorectal cancer: who, when, haw // 3 International conference, June 7-9, 2001, Dublin, Ireland. - P. 13.). По данным ВОЗ, рак толстой кишки занимает 3-4 место в структуре онкологической заболеваемости. Данная патология составляет 15% от всех первично диагностированных опухолей всех локализаций. При этом около 6% случаев связывают с наследственной природой заболевания. (Базин И.С. Рак толстой кишки - состояние проблемы // Русский мед. журн. - 2003. - Т. 11. - №11. - Режим доступа: http://www.rmj.ru/main.htm/rmj/t11/n11/674.htm.).
Каждый год от колоректального рака умирает около 100 тыс. человек (Аксель Е.М. Барулина Н.М. Колоректальный рак (заболеваемость, смертность, социально-экономический ущерб) // Рос. онколог. журн. - 1999. - №6. - С. 40-46; Ханевич М.Д. Колоректальный рак. Выбор хирургического лечения при толстокишечной непроходимости. - СПб.: Аграф+, 2008. - 136 с.). Максимальная смертность отмечается в Чехии, Венгрии и Новой Зеландии (Ханевич М.Д. Колоректальный рак. Выбор хирургического лечения при толстокишечной непроходимости. - СПб.: Аграф+, 2008. - 136 с.). Пятилетняя выживаемость в Европе составляет от 50% (в Швейцарии, Финляндии, Нидерландах, Испании) до 30-39% (в Италии, Дании, Великобритании, Германии и Франции) (Myrhoy Т. Hereditary nonpolyposis colorectal cancer: clinical features and survival // Progr. Colorect. Cane. - 1998. - Vol. 2. - P. 1-12; Longo W.E. Risk factors for morbidity and mortality after colectomy for colon cancer // Dis. Colon. Rectum. - 2000. - Vol.43. - P. 83-91). Принято считать опухоли толстой кишки более характерным заболеванием для индустриализованных стран, что связывают с высоким потреблением продуктов животного происхождения, а также чрезмерным питанием в сочетании с низкой физической активностью (Boyle P., Leon М.Е. Epidemiology of colorectal cancer // Brit. Med. Bull. - 2002. - Vol. 64. - P. 1-25; Имянитов E.H. Клинико-молекулярные аспекты колоректального рака: этиопатогенез, профилактика, индивидуализация лечения // Практическая онкология. - 2005. - Т. 6, №2. - С. 65-70).
Большой проблемой является высокий уровень смертности: на 100 вновь выявленных больных приходится более 70 умерших, из них на 1-м году с момента установления диагноза - около 40%. Это связано с высоким процентом диагностирования (71,4%) данного заболевания на поздних стадиях (III-IV стадии) (Давыдов М.И., Аксель Е.М. Злокачественные новообразования в России и странах СНГ в 2000 году. - М., 2002. - 281 с.).
В последнее время отмечается значительный прогресс в лечении рака толстой кишки, благодаря чему средняя продолжительность жизни была увеличена с 4-6 мес при проведении симптоматической терапии до 20-24 мес в случае присоединения к химиотерапии (XT) таргетных препаратов (Chau I., Cunningham D. Treatment in advanced colorectal cancer: what, when and how? // Br J Cancer. - 2009. - 100. - P. 1704-1719). При этом наблюдается переход от монотерапии 5-фторурацилом до комбинированных схем лечения с включением хирургического компонента, что значительно увеличивает продолжительность жизни (Nordlinger В., van Cutsem Е., Rougier P. et al. Does chemotherapy prior to liver resection increase the potential for cure in patients with metastatic colorectal cancer? A report from the European Colorectal Metastases Treatment Group // Eur J Cancer. - 2007. - 43(14). - P. 2037-2045). Отсюда следует, что существует обоснованная необходимость разработки новых терапевтических средств для лечения данного заболевания, непременным этапом которой являются доклинические исследования. Важным инструментом в исследованиях эффективности новых лекарственных средств являются животные модели, в том числе ксенографты опухолей на иммунодефицитных мышах.
Многочисленными исследованиями было установлена разница между проксимальным (правым) отделом толстой кишки, к которому относятся слепая кишка, восходящий и поперечный отделы ободочной кишки и дистальным (левым) отделом толстой кишки, к которому относятся нисходящая часть ободочной кишки, сигмовидная кишка и прямая кишка. Проксимальные и дистальные отделы толстой кишки проявляют значительные различия в отношении эмбрионального происхождения, морфологических и биохимических характеристик, а также паттерна экспрессии генов. (Bufill J.A. Colorectal cancer: evidence for distinct genetic categories based on proximal or distal tumor location // Ann. Int. Med. - 1990. - Vol. 113. - P. 779-788). Важен тот факт, что проксимальные отделы толстой кишки, в отличие от дистальных, относительно чувствительны к терапии фторпиримидинами и его аналогами (Iacopetta В. Are there two sides to colorectal cancer // Int. J. Cancer. - 2002. - Vol. 101. - P. 403-408; Lindblom A. Different mechanisms in the tumorigenesis of proximal and distal colon cancers // Curr. Opin. Oncol. - 2001. - Vol. 13. - P. 63-69). Поэтому в исследованиях новых методов и средств лечения нисходящего отдела толстой кишки необходимым является создание адекватной модели онкозаболевания данной локализации.
Известен способ подкожной трансплантации фрагментов опухоли толстой кишки в бок иммунодефицитных мышей (см. Mitsunobu Takeda, Jun Koseki, Hidekazu Takahashi et al. Disruption of Endolysosomal RAB5/7 Efficiently Eliminates Colorectal Cancer Stem Cells // Cancer Res. - 2019. - 79(7). - P. 1426-1437; Magdalena Cybulska, Tomasz Olesinski, Krzysztof Goryca et al. Challenges in Stratifying the Molecular Variability of Patient-Derived Colon Tumor Xenografts // BioMed Research International. - 2018. - P. 1-9; Ruidi Teng, Jingjing Zhao, Yiding Zhao et al. Chimeric Antigen Receptor-modified T Cells Repressed Solid Tumors and Their Relapse in an Established Patient-derived Colon Carcinoma Xenograft Model // J Immunother. - 2019. №2. - P. 33-42). Преимуществом данной модели является удобство при мониторинге ее развития. Недостатком этой модели является имплантация опухолевого материала в сайт с чужеродным микроокружением, влияние которого способствует появлению характеристик, не свойственных реальной опухоли человека.
Известен способ создания ортотопической модели рака кишечника, при котором в первом пассаже из фрагмента опухоли пациента делают суспензию в матригеле, которую вводят подкожно в бок мыши. По достижении опухолью необходимого для перевивки размера ее делят на фрагменты, которые подшивают к кишке (Mukohyama J., Shimono Y., Yamashita K., Sumi Y., Mukohara Т., Minami H., Kakeji Y. Effect of Xenotransplantation Site on MicroRNA Expression of Human Colon Cancer Stem Cells // Anticancer Research. - 2016. - 36. - P. 3679-3686). Недостатком данного способа является имплантация в первом пассаже опухолевого материала под кожу мыши, где на процессы канцерогенезы будет влиять чужеродное микроокружение, что может привести к значительному изменению молекулярно-биохимических и гистологических характеристик опухоли. В конечном счете, полученная во втором и последующих пассажах ортотопическая модель не может считаться адекватной.
Техническим результатом предлагаемого изобретения является разработка способа трансплантации фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки иммунодефицитных мышей, преимуществом которого является оптимальный доступ к искомому органу мыши с дорсальной поверхности туловища по сравнению с более травматичным доступом с брюшной стороны тела, при котором для поиска нисходящего отдела толстой кишки мыши приходится выводить в операционную рану практически весь кишечник ввиду того, что данный отдел толстой кишки прилежит к дорсальной поверхности брюшной полости. Данный способ позволяет получить адекватную модель, наиболее точно отражающую молекулярно-биохимические характеристики опухолей толстой кишки человека.
Технический результат изобретения достигается тем, что осуществляют трансплантацию фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки иммунодефицитных мышей, включающую наркоз мышей, послойное рассечение кожи, мышц и тканей брюшной стенки, отличающуюся тем, что производят рассечение кожи, мышц и тканей брюшной стенки пояснично-крестцовой области спины вдоль оси туловища на расстоянии 3 мм от позвоночника, разрез протяженностью 10 мм начинается на расстоянии 7 мм от основания хвоста, расширяя при помощи анатомических пинцетов операционную рану, визуализируют прямую кишку, на расстоянии 5 мм от места перехода нисходящего отдела толстой кишки в прямую кишку производят продольное рассечение серозно-мышечного слоя толстой кишки на протяжении 3 мм, при помощи лигатуры фиксируют фрагмент опухоли толстой кишки человека объемом 27 мм3 над сделанным ранее разрезом, послойно ушивают стенку брюшной полости и кожу мыши.
Способ осуществляют следующим образом.
Фрагмент опухоли толстой кишки пациента сразу же после иссечения помещается в 5% раствор гентамицина в среде Хенкса. Непосредственно перед трансплантацией вырезают кусочки объемом 27 мм3. Для успешного приживления опухолевого материала необходимо, чтобы время от момента резекции опухолевого материала у человека до имплантации в слепую кишку иммунодефицитной мыши не превышало 20 минут.
Реципиентом опухолевого материала служат иммунодефицитные мыши Balb/c Nude.
Наркоз животных осуществляют с использованием ксилазина концентрацией 20 мг/мл и золетила концентрацией 22,57 мг/мл.
Пояснично-крестцовую область спины мыши обрабатывают 10% раствором повидон-йода.
При помощи ножниц рассекают кожу, мышцы, а также ткани брюшной стенки в пояснично-крестцовой области спины вдоль оси туловища на расстоянии 3 мм от позвоночника. Разрез протяженностью 10 мм начинается на расстоянии 7 мм от основания хвоста. С помощью анатомических пинцетов расширяют операционную рану и визуализируют прямую кишку. На расстоянии 5 мм от зоны перехода нисходящего отдела толстой кишки в прямую кишку производят продольное рассечение серозно-мышечного слоя толстой кишки на протяжении 3 мм. Фрагмент опухоли толстой кишки человека объемом 27 мм3 подшивают с помощью лигатуры к толстой кишке мыши над сделанным раннее разрезом. Послойно ушивают стенку брюшной полости и кожу мыши.
Изобретение иллюстрируется фигурами (1-3).
На Фиг 1. изображена имплантация фрагмента опухоли человека в нисходящий отдел толстой кишки иммунодефицитной мыши Balb/c Nude.
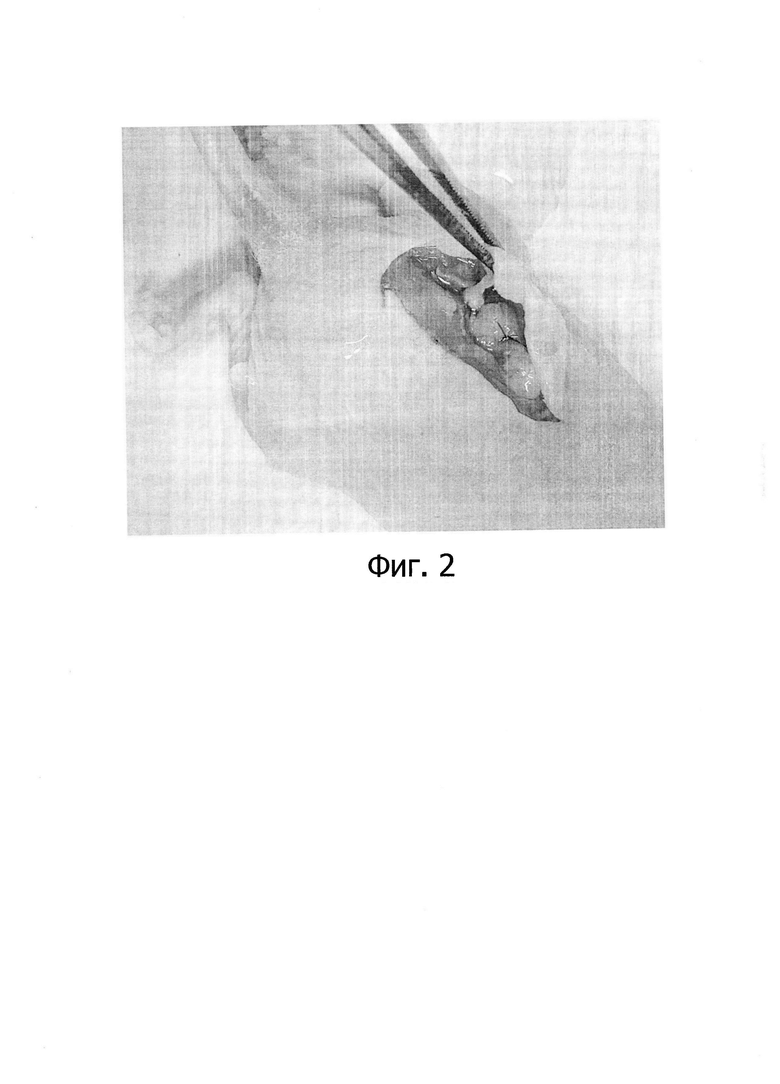
На Фиг 2. изображен зафиксированный фрагмент опухоли человека на нисходящем отделе толстой кишки иммунодефицитной мыши Balb/c Nude.
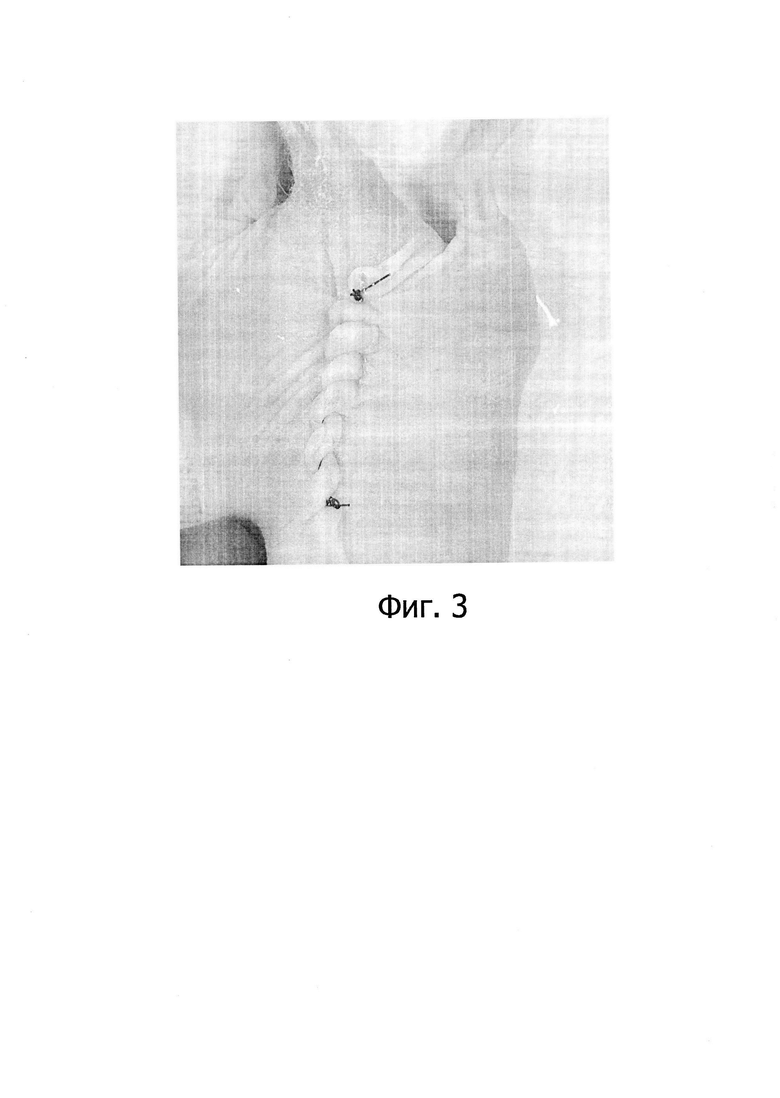
На Фиг. 3. изображен конечный вид после трансплантации фрагмента опухоли человека в нисходящий отдел толстой кишки иммунодефицитной мыши Balb/c Nude.
Данным способом произведена трансплантация фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки 20 иммунодефицитных мышей Balb/c Nude.
Технико-экономическая эффективность данного способа заключается в создании ортотопической пациентоподобной модели рака нисходящего отдела толстой кишки, наиболее точно повторяющей характеристики опухолей нисходящего отдела толстой кишки человека и необходимой для проведения доклинических исследований механизмов онкогенеза и новых терапевтических средств и методов.
Пример
Данным способом была прооперирована самка иммунодефицитной мыши Balb/c Nude возрастом 7 недель массой 24 г. В качестве трансплантируемого материала служил фрагмент опухоли нисходящего отдела толстой кишки человека, который сразу же после выделения из организма человека был помещен в среду Хенкса. Интервал между выделением опухолевого материала из донорского организма до его имплантации в тело животного составил 12 минут.
Премедикацию осуществляли при помощи ксилазина концентрацией 20 мг/мл. В качестве основного наркотизирующего вещества использовали золетила концентрацией 22,57 мг/мл.
Крестцово-поясничную область спины мыши обработали 10% раствором повидон-йода. Далее послойно рассекли кожу, мышцы и ткани брюшной стенки в пояснично-крестцовой области спины вдоль оси туловища на расстоянии 3 мм от позвоночника. Начало разреза было расположено на расстоянии 7 мм от основания хвоста. Длина разреза составила 10 мм. Далее, раздвигая края операционной раны, визуализировали прямую кишку. После этого рассекли серозно-мышечный слой нисходящего отдела толстой кишки мыши длиной 3 мм на расстоянии 5 мм от места перехода нисходящего отдела толстой кишки в прямую кишку. После этого выделили фрагмент опухоли толстой кишки человека объемом 27 мм3, который затем подшили с помощью лигатуры к толстой кишке мыши над сделанным раннее разрезом. Процедуру трансплантации завершили послойным ушитием стенки брюшной полости и кожи мыши.
Процедура имплантации была благополучно и без осложнений перенесена мышью-реципиентом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА ОПУХОЛИ ТОЛСТОЙ КИШКИ ЧЕЛОВЕКА В СЛЕПУЮ КИШКУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2020 |
|
RU2727868C1 |
| Способ исследования PDX-модели колоректального рака | 2024 |
|
RU2835140C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА НЕЙРОЭНДОКРИННОЙ ОПУХОЛИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА В ПОДЖЕЛУДОЧНУЮ ЖЕЛЕЗУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2019 |
|
RU2725273C1 |
| СПОСОБ ОПТИМАЛЬНОГО ДОСТУПА К АБДОМИНАЛЬНОМУ ОТДЕЛУ ПИЩЕВОДА ИММУНОДЕФИЦИТНЫХ МЫШЕЙ ПРИ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА ОПУХОЛИ ПИЩЕВОДА ЧЕЛОВЕКА | 2018 |
|
RU2709835C1 |
| Способ доступа к телу желудка иммунодефицитных мышей при ортотопической трансплантации фрагмента опухоли желудка человека | 2022 |
|
RU2790950C1 |
| Способ создания ксенографта рака пищевода внутригрудной локализации на иммунодефицитных мышах | 2020 |
|
RU2738308C1 |
| СПОСОБ СОЗДАНИЯ МОДЕЛИ РАКА ПЕЧЕНИ НА ИММУНОДЕФИЦИТНЫХ МЫШАХ | 2023 |
|
RU2799132C1 |
| Способ индуцирования роста аденокарциномы ободочной кишки человека в органах экспериментальных животных | 2023 |
|
RU2799251C1 |
| СПОСОБ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ КУЛЬТУРЫ ОПУХОЛЕВЫХ КЛЕТОК ПИЩЕВОДА ЧЕЛОВЕКА В ШЕЙНЫЙ ОТДЕЛ ПИЩЕВОДА ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2019 |
|
RU2713798C1 |
| Способ выбора оптимального доступа для ортотопической трансплантации фрагмента опухоли рака яичника человека в яичник самки иммунодифицитной мыши | 2020 |
|
RU2740423C1 |

Изобретение относится к медицине, а именно к экспериментальной онкологии. Производят рассечение кожи, мышц и тканей брюшной стенки пояснично-крестцовой области спины вдоль оси туловища на расстоянии 3 мм от позвоночника. Разрез протяженностью 10 мм начинают на расстоянии 7 мм от основания хвоста. Расширяя при помощи анатомических пинцетов операционную рану, визуализируют прямую кишку. На расстоянии 5 мм от места перехода нисходящего отдела толстой кишки в прямую кишку производят продольное рассечение серозно-мышечного слоя толстой кишки на протяжении 3 мм. При помощи лигатуры фиксируют фрагмент опухоли толстой кишки человека объемом 27 мм3 над сделанным ранее разрезом, послойно ушивают стенку брюшной полости и кожу мыши. Способ позволяет создать ортотопическую пациентоподобную модель рака нисходящего отдела толстой кишки, наиболее точно повторяющую характеристики опухолей нисходящего отдела толстой кишки человека и необходимую для проведения доклинических исследований механизмов онкогенеза и новых терапевтических средств и методов. 1 пр., 3 ил.
Способ трансплантации фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки иммунодефицитных мышей, включающий наркоз мышей, послойное рассечение кожи, мышц и тканей брюшной стенки, отличающийся тем, что производят рассечение кожи, мышц и тканей брюшной стенки пояснично-крестцовой области спины вдоль оси туловища на расстоянии 3 мм от позвоночника, разрез протяженностью 10 мм начинается на расстоянии 7 мм от основания хвоста, расширяя при помощи анатомических пинцетов операционную рану, визуализируют прямую кишку, на расстоянии 5 мм от места перехода нисходящего отдела толстой кишки в прямую кишку производят продольное рассечение серозно-мышечного слоя толстой кишки на протяжении 3 мм, при помоши лигатуры фиксируют фрагмент опухоли толстой кишки человека объемом 27 мм3 над сделанным раннее разрезом, послойно ушивают стенку брюшной полости и кожу мыши.
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА ОПУХОЛИ ТОЛСТОЙ КИШКИ ЧЕЛОВЕКА В СЛЕПУЮ КИШКУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2020 |
|
RU2727868C1 |
| CN 0110150228 A, 23.08.2019 | |||
| КИТ О.И | |||
| и др | |||
| Методы создания ортотопических моделей рака толстой кишки человека на иммунодефицитных животных, Вопросы онкологии, 2019, том 65, 2, с.303-307 | |||
| HIROSHIMA YUKIHIKO et al | |||
| Successful fluorescence-guided surgery on human colon cancer patient-derived orthotopic xenograft mouse | |||
Авторы
Даты
2021-08-12—Публикация
2020-12-02—Подача