Область техники.
Настоящее изобретение относится к слитным белкам гормона роста человека длительного действия, в которых физиологически активная молекула гормона роста соединена с аминокислотными последовательностями, обеспечивающими замедление выведения из организма, термическую и структурную устойчивость.
Предшествующий уровень техники.
Рекомбинантный гормон роста человека (ГРЧ) используется для терапии низкорослости у детей (гипофизарный нанизм), синдроме Тернера и дефиците гормона у взрослых. Данная терапия носит заместительный характер, т.к. при дефиците гормона роста в организме снижается уровень эндогенного ГРЧ. В связи с тем, что ГРЧ крайне нестабилен в организме пациента, терапия предусматривает ежедневные инъекции в высоких дозах в течение длительного времени. Подобная терапия крайне неудобна для пациентов. В настоящее время актуальной задачей является создания препаратов ГРЧ пролонгированного действия, что приведет к улучшению качества жизни пациентов и улучшению терапевтических эффектов лечения.
Выведение ГРЧ из организма происходит по двум механизмам. Первый представляет собой почечный клиренс, в котором ГРЧ выводится из кровотока почечной клубочковой фильтрацией. Почечный клиренс ГРЧ хорошо описан в литературе и составляет 25-53% от общего клиренса ГРЧ. Вторым механизмом является рецептор-опосредованный клиренс в тканях и органах, в первую очередь в печени, где происходит рецептор-опосредованный эндоцитоз с последующей лизисомной деградацией гормона.
Для уменьшения почечного клиренса фармацевтических белков широко используется метод пегелирования. Пегелированные производные ГРЧ не подвержены клубочковой фильтрации, однако эффективно связываются с рецептором и подвергаются эндоцитозу. Кроме того, хорошо известны побочные действия пегелированных производных ГРЧ, в первую очередь это липоатрофия в месте введения препарата. Липоатрофия - это медицинский термин, применяемый для описания локализованной потери жировой ткани. Этология липоатрофии предположительно объясняется прямым липолитическим эффектом высоких доз ГРЧ. Такие высокие концентрации возникают в месте инъекций вязких растворов пегелированных ГРЧ. Большинство крупных фармацевтических производителей приняли решение о прекращении программ клинических исследований пегелированных производных ГРЧ.
Проблемы, выявленные при разработке пегелированных аналогов ГРЧ, привели к необходимости поиска других путей пролонгирования гормона в организме человека. Патент US 9211342 защищает производное ГРЧ, устойчивое к деградации в плазме. Устойчивость достигается путем введения в последовательность молекулы как минимум одной дополнительной дисульфидной связи. В результате гормон приобретает более жесткую структуру, не подверженную разворачиванию и сворачиванию в связи с характерным для ГР реакцией тиол-дисульфидного обмена. Дополнительно вводятся точечные мутации, уменьшающие агрегацию белка. Похожая идея, но с другими мутациями описана в патенте CN 104812776. Патенты KR 20140141874 и US 9187546 защищают метод получения гипер-гликозилированного производного ГРЧ. Для этого в последовательность введены соответствующие точечные мутации, а сам ГРЧ экспрессирован в клетках млекопитающих, способных гликозилировать продукты гетерологической экспрессии. Следует отметить, что сами по себе устойчивые производные ГРЧ не могут рассматриваться как действительно эффективные пролонгированные молекулы. В последующем эти молекулы могут быть встроены в микрочастицы, такое объединение должно дать хороший синергитический эффект для получения пролонгированных препаратов гормона.
В патентах US 9061067 и US 8841249 описаны способы введения точечных мутаций с тем, чтобы по этим точкам присоединять гидрофобные или алифатические углеводороды. Как известно, такие низкомолекулярные соединения обладают высокой аффинностью к сывороточному альбумину. После инъекции, производные ГРЧ с такими хвостами взаимодействуют с альбумином, повышая время жизни препарата в крови. Однако от рецепторного клиренса такие препараты избавить не могут, в результате не удается достигать уменьшения инъекций до одной в неделю.
Для замедления рецептор-опосредованного выведения разработаны несколько вариантов ГРЧ, в которых гормон конъюгирован с крупными белковыми молекулами, таким как альбумин (TV-1106, NNC0195-0092), несмысловые протяженные полипептидные цепи VRS-317 (проводится фаза 3 клинических исследований), MOD-4023 (проводится фаза 2/3 клинических исследований)). Такая модификация снижает связывание с рецептором в 10-15 раз, В патенте US 8470559 описано производное, содержащее комплекс ГР и фрагмент его цитоплазматического рецептора. Такое производное обладает пониженной биологической активностью и поэтому плохо выводится рецепторным механизмом почечного клиренса. Наконец, патент US 9371369 защищает производное ГРЧ, в котором ГРЧ слит с молекулой, состоящей из очень протяженной неприродной аминокислотной последовательности. Протяженный фрагмент уменьшает аффинность производного ГР к своему рецептору в 20 раз, поэтому уменьшается специфический рецепторный клиренс и соответственно увеличивается время жизни аналога ГР в организме человека. Можно рассматривать это как своеобразную попытку депонирования молекулы ГР в организме. Уменьшение сродства к рецептору уменьшает и биологическую активность препаратов, что приводит к увеличению дозы вводимого препарата. Повышение дозы приводит к локальной концентрации активного гормона, что может вызывать побочные действия на организм, например уже упоминавшуюся липоатрофию. В патентах CN 102875683, US 9061072 и RU 2473554 описаны производные ГРЧ, соединенные с фрагментами молекул иммуноглобулинов человека. В патенте US 8304386 описано производное ГР, соединенное в единую молекулу с фрагментом бета-цепи хорионического гонадотропина человека. В патенте US 8470559 описано производное, содержащее комплекс ГРЧ и фрагмент его цитоплазматического рецептора. Такое производное обладает высокой молекулярной массой и пониженным сродством к мембранно-связанным рецепторам ГРЧ и поэтому плохо выводится рецепторным механизмом почечного клиренса.
Методам физического депонирования нативного ГРЧ посвящено много как научных работ, так и патентов. Многочисленные исследования показали, что продолжительное введение малых доз в течение суток дает такой же биологический эффект, как однократное введение большой дозы один раз в день. На основании этих исследований был разработан депонирующийся препарат на основе гормона роста Nutropin Depot, получивший разрешение FDA к применению. Данный препарат снят с производства, в связи со сложностью технологии получения (по объяснению фирмы производителя Genetech Inc, США). В настоящее время разрабатывается депонирующийся препарат LB03002 (фирмы LGLifeSciences, Корея), который допущен к третьей фазе клинических исследований. Разработчики препарата использует ту же технологию, что и при создании Nutropin Depot. Для данного препарата возможны проблемы, как и для его предшественника. Патент WO 2002030990 описывает метод получения химически сшитых амидных производных гиалуроновой кислоты, которая является основным компонентом синовиальной жидкости хряща. Препарат является полностью совместимым с организмом и полностью биодеградируемым. На основе этих частиц получен единственный разрешенный в настоящее время лекарственный препарат ГР пролонгированного действия. Однако для этого потребовалось почти 20 лет, что связано с технической сложностью получения частиц одинакового размера, устойчивых к деградации длительное время и поддерживающие концентрацию ГР на физиологически приемлемом уровне. Патент US 8313767 защищает метод получения пролонгированного ГР путем осаждения рекомбинантного белка внутри пор гидроксиапатитных частиц определенного размера. Получение частиц гидроксиапатита технологически просто и экономически выгодно. Иммобилизация ГР на частицах проводится с использованием хорошо изученной реакции гормона с ионами цинка. Ионы цинка хорошо стабилизируют димер ГР в порах матрицы и медленно высвобождают его с поверхности. Важным показателем качества депонированных препаратов ГР является процентное содержание гормона в грамме микрочастиц. Одно из самых высоких процентных содержаний заявлено в патенте CN 103976982. Микрочастицы получены на основе сополимера, разветвленного ПЭГ и полиэфира, процент содержания составил более 80%. Другими показателями качества депо-ГР являются размер частиц и вязкость вводимого препарата. Патент US 8729015 описывает микрокапсулы на основе липидных композиций. Липидные композиции очень пластичны, мелкие и позволяют использовать иглы тонкого диаметра. Патент KR 20170043890 защищает способ депонирования, в котором депо возникает после введения в тело пациента. Используется полимер на основе декстранов, который обладает способностью затвердевать при температуре тела, захватывая в свой состав молекулы ГР. Медленное разрушение декстрана приводит к медленному, без скачков, повышению концентрации ГР в крови.
Заявителем разработан аналог ГРЧ, сочетающий две возможности пролонгации -увеличение молекулярного веса для уменьшения почечной фильтрации и депонирование для снижения рецепторного клиренса. Лекарственное средство способно, за счет уникальной аминокислотной последовательности, депонироваться в организме и постепенно высвобождаться, а наличие в структуре димеризующего фрагмента и человеческого теоредоксина, увеличивающих молекулярный вес, позволяет поддерживать в течение длительного времени необходимую концентрацию для достижения биологического эффекта.
Рекомбинантный аналог ГРЧ получен путем экспрессии в клетках E.coli, разработаны методики очистки данного продукта. Первичная структура и гомогенность подтверждена ВЭЖХ. Разработанный белок обладает улучшенной фармакокинетикой и сохраняет биологическую активность нативного ГРЧ.
Рекомбинантный ГРЧ имеет уникальную структуру и содержит три функциональные области: область, гомологичную аминокислотной последовательности гормона роста человека, область, увеличивающую термо-стабильносить и функциональную устойчивость молекулы, область, способствующую димеризации и область, обеспечивающую сродство с мембраной клетки.
В качестве фрагмента, улучшающего термо-стабильносить и функциональную устойчивость, использована аминокислотная последовательность тиоредоксина человека. Его положительные свойства широко исследованы в научной литературе.
В качестве димеризующего фрагмента использована последовательность лейциновой молнии. Лейциновая молния (leucine zipper) является общим трехмерным структурным мотивом в белках и имеет такое название потому, что лейцины находятся в каждом седьмом положении аминокислотного фрагмента, составляя тем самым домен димерзации двух альфа-спиралей. Такие структуры присутствуют и прокариотах и в эукариотах и являются одним из важнейших элементов белок-белковых взаимодействий.
Изучение связывания белков с холестерином в клеточных мембранах привело к установлению последовательностей, взаимодействующих с холестерином клеточных мембран. Консенсусные последовательности содержат мотив Leu/Val-X(l-5)-Tyr-X(l-5)-Arg/Lys. Существует множество последовательностей, узнающих мембранный холестерин, и любая из них может быть использована в предлагаемой последовательности.
Разработанный пептид существует в виде димера, поэтому он более стабилен при введении и имеет улучшенную фармакокинетику и превышает таковую для нативного гормонат более чем в 500 раз. На стабильность гормона в организме оказывает влияние и его мембрано-связывающая область. Данная область обеспечивает кратковременное связывание белка с кластерами холестерина клеточных мембран, способствуя депонированию ГРЧ.
Техническим результатом, достигаемым при реализации данного изобретения, является повышение эффективности гормональной терапии и уменьшение частоты инъекций при курсовом лечении.
Изобретение иллюстрируют Фиг. 1-3:
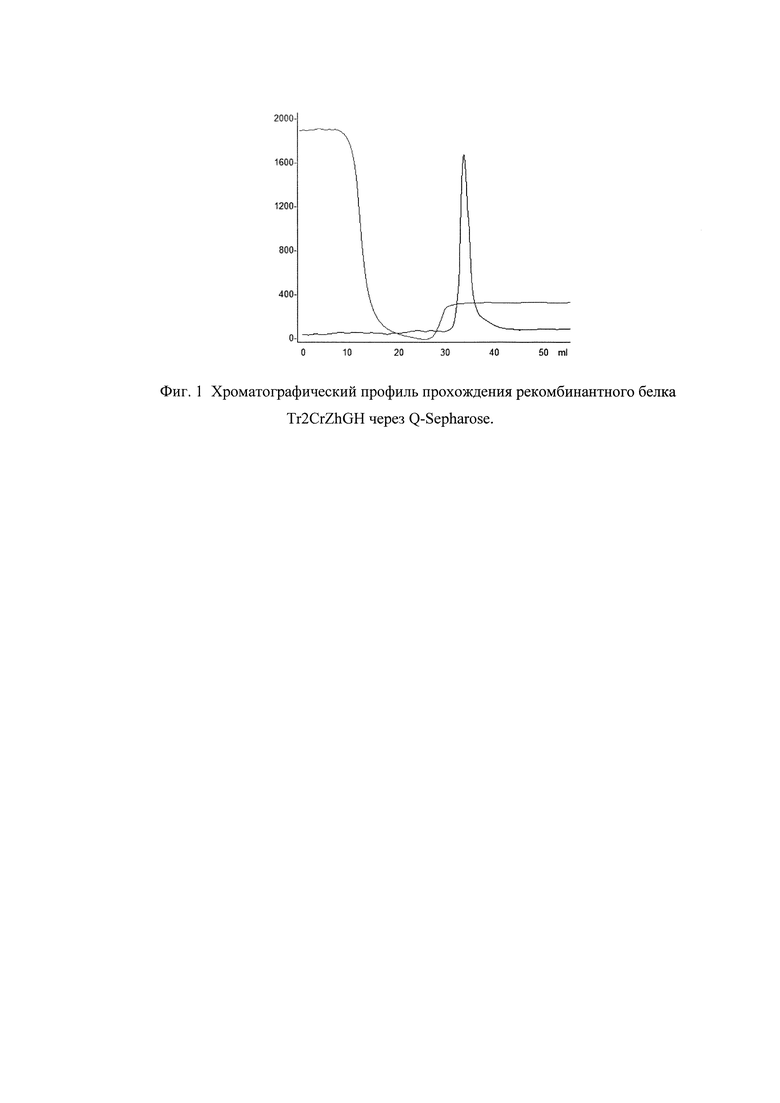
Фиг. 1. Хроматографический профиль прохождения рекомбинантного белка Tr2CrZhGH через Q-Sepharose.
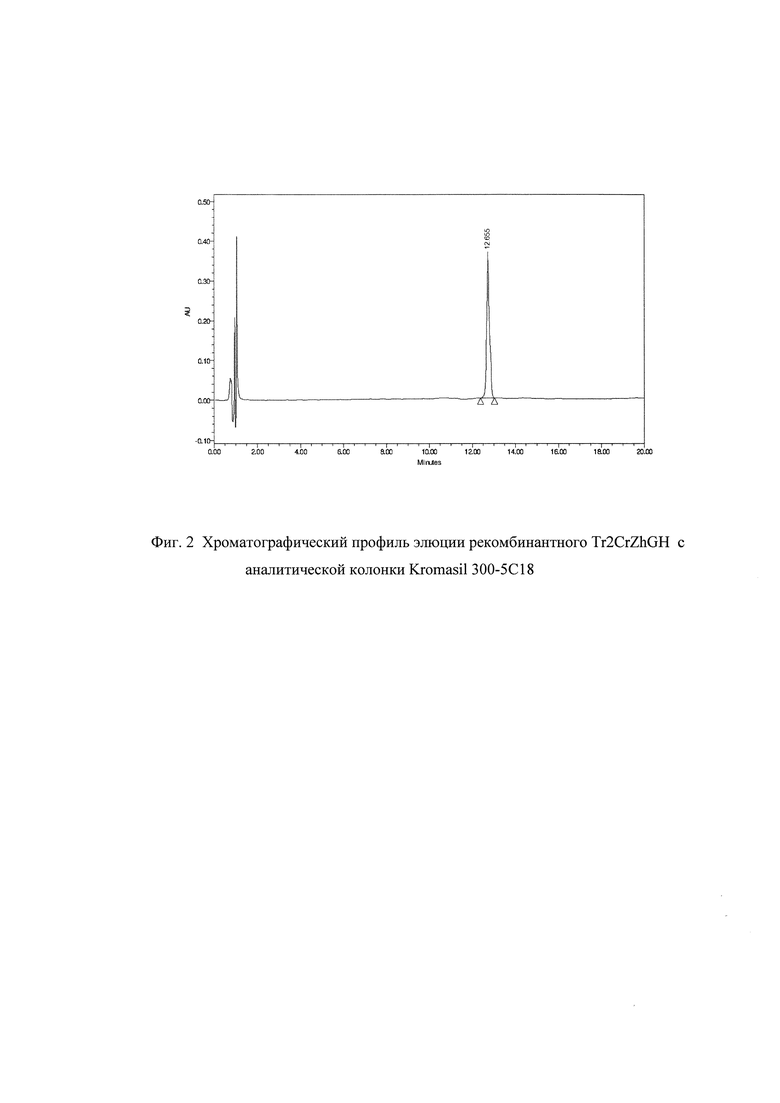
Фиг. 2. Хроматографический профиль элюции рекомбинантного Tr2CrZhGH с аналитической колонки Kromasil 300-5С18
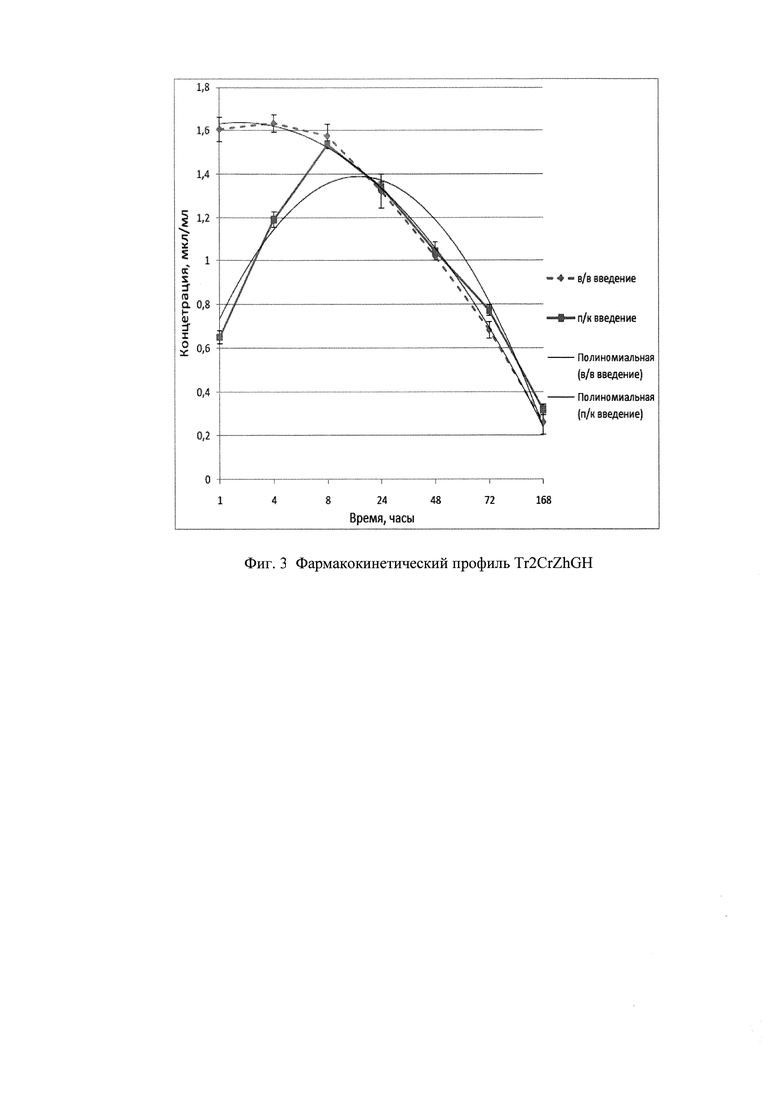
Фиг. З. Фармакокинетический профиль Tr2CrZhGH
Примеры осуществления изобретения:
1. Получение штамма-продуцента рекомбинантного белка Tr2CrZhGH.
Для получения рекомбинантного белка была создана генетическая конструкция на основе плазмиды рЕТ30а, которая содержит ген SEQ ID: 2, кодирующий данный рекомбинантный белок.
Плазмидой трансфецировали клетки E.coli штамма BL21(DE3). Трансформированные клетки рассевали на чашку Петри с LB-агаром, содержащим 25 мг/мл канамицина и инкубировали 16 часов при 37С.24 единичные колонии инкубировали 10 часов в 1 мл LB, содержащим 25 мг/мл канамицина. По 50 мкл культур клеток вносили в 0,5 мл LB, содержащим 25 мг/мл канамицина, инкубировали 2 часа и индуцировали экспрессию белка rec-МР, добавлением IPTG до 1 мкМ. Матричные культуры хранили на -80С до окончания анализа клонов. Наличие рекомбинантного белка анализировали электрофорезом в ПААГ. Один клон, продуцирующий наибольшее количество продукта, использовали в качестве штамма-продуцента.
2. Получение и хроматографическая очистка Tr2CrZhGH.
Клетки штамма-продуцента пересевали в культуральную колбу с 200 мл LB, содержащим 25 мг/мл канамицина. Культура выращивалась на шейкере при 280 об/мин при температуре 37С до достижения оптической плотности значения OD585=0,8E. Индукция экспрессии белка проводилась добавлением IPTG до концентрации 1 mM. Культура дополнительно культивировалась 4 часа, далее клетки осаждались центрифугированием при 5000g. Осадок клеток лизировали в 8М мочевине и обрабатывали на ультразвуковом дезинтеграторе. Лизат клеток центрифугировали при 20000g 2 часа. Супернатант фильтровали через колонку с SPQ-Sepharose. Фракцию, не связавшуюся с данным сорбентом, хроматографировали на Q-Sepharose в градиенте NaCl (стартовый буфер: 20 mM TrisHCl рН 8.8, 20 mM NaCl, итоговый буфер 20 mM TrisHCl рН 8.8, 400 mM NaCl). Хроматографический профиль представлен на Фиг. 1. Фракции, содержащие целевой продукт, объединяли и диализовали в 0,9% NaCl, далее повторно хроматографировали на SP-Sepharose. Чистоту продукта анализировали методом ВЭЖХ (Фиг. 2.).
3. Изучение фармакокинетики рекомбинантного белка Tr2CrZhGH.
В исследовании было использовано 125 самцов мышей ICR и 6 самцов кроликов NZW. Мышам ЛС Tr2CrZhGH вводили подкожно в трех экспериментальных дозах 1 мг/кг, 5 мг/кг и 10 мг/кг. Минимальную дозу 1 мг/кг вводили однократно или еженедельно в течение 4 недель. Дозы 5 мг/кг и 10 мг/кг вводили однократно. Кроликам препарат вводили однократно внутривенно (краевая вена уха) или подкожно в дозе 2 мг/кг.
Максимальная концентрация при однократном подкожном введении мышам достигается в течение четырех часов после инъекции, после чего концентрация медленно снижалась с периодом полувыведения около 63 часов. При всех использованных дозах введения препарат в течение эксперимента (семь суток) препарат сохранялся в кровотоке. Учитывая длительное время полувыведения, время полного выведения препарата может, вероятно, быть очень продолжительным и потенциально препарат может быть обнаружен в крови спустя длительное время.
Максимальная концентрация при подкожном введении препарата кроликам достигается в течение восьми часов после инъекции, после чего концентрация медленно снижалась с периодом полувыведения около 69 часов. Максимальная концентрация при внутривенном введении регистрировалась через 4 часа после инъекции, после чего концентрация медленно снижалась с периодом полувыведения около 63 часов. Профиль выведения приведен на Фиг. 3.
Перечень последовательностей.
<110> ФГБУ Институт биологии и развития им. Н.К. Кольцова РАН
<120> Новый рекомбинантный аналог гормона роста пролонгированного действия.
<160> NUMBER OF SEQ ID NOS: 1
<210> SEQ ID NO 1
<211> 326
<212> AA (amino acid)
<213> artificial
<400> SEQUENCE 1:
MVKQIESKTKFQEALDAAGDKLVVVDFSATWCGPCKMIKPFFHSASEKYSNVIFLEDVDDCQDVASECEVKCMPTFQFFKKGQKVGEFSGANKEKLEATINELVGGSGGSKGGGSGGGKSGGGSGGKLLSGSSGGSGGGGSAMGSSHHHHHHRAFLEKENALLRQEVVALRQELSHLRAVLSRYQAEGGSGGGSGGSGGGSSGSGSGGKEGVLYVGSKTKSGGSGSGSGGGSFTTFTVTKYWFYRLLSALFGIPMALIWGIYFAILSFLHSGSGGSFPTIPLSRLFDNAMLRAHRLHQLAFDTYQEFEEAYIPKEQKYSFLQNPQTSLCFSESIPTPSNREETQQKSNLELLRISLLLIQSWLEPVQFLRSVFANSLVYGASDSNVYDLLKDLEEGIQTLMGRLEDGSPRTGQIFKQTYSKFDTNSHNDDALLKNYGLLYCFRKDMDKVETFLRIVQCRSVEGSCGF
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ СВЯЗАННЫХ С ГОРМОНОМ РОСТА ЗАБОЛЕВАНИЙ У ЧЕЛОВЕКА | 2014 |
|
RU2689336C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ СВЯЗАННЫХ С ГОРМОНОМ РОСТА ЗАБОЛЕВАНИЙ У ЧЕЛОВЕКА | 2019 |
|
RU2802215C2 |
| ПЭГИЛИРОВАННЫЕ СОЕДИНЕНИЯ РЕКОМБИНАНТНОГО ГОРМОНА РОСТА ЧЕЛОВЕКА | 2009 |
|
RU2530714C9 |
| ГИБРИДНЫЙ БЕЛОК НА ОСНОВЕ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА ЧЕЛОВЕКА, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННЫМ ДЕЙСТВИЕМ (ВАРИАНТЫ), И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2515914C1 |
| СЛИТЫЕ БЕЛКИ ГОРМОНА РОСТА | 2008 |
|
RU2473554C2 |
| КОМПОЗИЦИЯ СТАБИЛИЗИРОВАННОГО ГОРМОНА РОСТА И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 1997 |
|
RU2191029C2 |
| ГИБРИДНЫЙ БЕЛОК, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННЫМ ДЕЙСТВИЕМ, НА ОСНОВЕ РЕКОМБИНАНТНОГО ИНТЕРФЕРОНА АЛЬФА-2 ЧЕЛОВЕКА (ВАРИАНТЫ), СПОСОБ ЕГО ПОЛУЧЕНИЯ И ШТАММ Saccharomyces cerevisiae ДЛЯ ОСУЩЕСТВЛЕНИЯ ЭТОГО СПОСОБА (ВАРИАНТЫ) | 2013 |
|
RU2515913C1 |
| ГОРМОН РОСТА, МОДИФИЦИРОВАННЫЙ ДВУХЦЕПОЧЕЧНЫМ ПОЛИЭТИЛЕНГЛИКОЛЕМ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2008 |
|
RU2488598C2 |
| ПРИМЕНЕНИЕ АНТИТЕЛА ДЛЯ ЛЕЧЕНИЯ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ У ПАЦИЕНТА С НЕАДЕКВАТНЫМ ОТВЕТОМ НА ИНГИБИТОР TNF-АЛЬФА | 2008 |
|
RU2489166C2 |
| ЛЕЧЕНИЕ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ У ПАЦИЕНТА С НЕАДЕКВАТНЫМ ОТВЕТОМ НА ИНГИБИТОР TNF-АЛЬФА | 2004 |
|
RU2358762C9 |
Изобретение относится к области биотехнологии, конкретно к получению рекомбинантного гормона роста человека, и может быть использовано в медицине для терапии заболеваний, связанных с дефицитом гормона роста человека. Рекомбинантный гормон роста имеет уникальную структуру и содержит четыре функциональные области: область, гомологичную аминокислотной последовательности гормона роста человека, область, увеличивающую термостабильносить и функциональную устойчивость молекулы, область, способствующую димеризации молекулы, и область, обеспечивающую сродство с мембраной клетки. Изобретение обеспечивает получение гормон роста человека рекомбинантным путем в клетках E. coli, который обладает улучшенной фармакокинетикой - пролонгированным действием и сохраняет биологическую активность нативного гормона роста. 2 н.п. ф-лы, 3 ил., 3 пр.
1. Рекомбинантный полипептид, обладающий агонистической активностью в отношении рецептора гормона роста человека, характеризующийся тем, что имеет аминокислотную последовательность SEQ ID NO: 1.
2. Фармацевтическая композиция для терапии пролонгированным гормоном роста человека на основе рекомбинантного полипептида SEQ ID NO: 1 для подкожного, внутримышечного или ректального введения.
| EP 2968451 A1, 20.01.2016 | |||
| RU 2016143415 A, 03.05.2018 | |||
| Способ получения гибридного белка, состоящего из рекомбинантного белка аналога интерферона гамма, конъюгированного с олигосахаридом | 2016 |
|
RU2656140C2 |
| MULLER S | |||
| et al., Spliceosomal peptide P140 for immunotherapy of systemic lupus erythematosus: results of an early phase II clinical trial, Arthritis & Rheumatism: Official Journal of the American College of Rheumatology, 2008, V | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2021-08-12—Публикация
2019-09-26—Подача