Область техники, к которой относится изобретение
Настоящее раскрытие относится к фармацевтической комбинации антитела к CD19 и ингибитора тирозинкиназы Брутона (ВТК) для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Предпосылки изобретения
В-клетки - это лимфоциты, которые играют большую роль в гуморальном иммунном ответе. Они продуцируются в костном мозге большинства млекопитающих и составляют 5-15% циркулирующего лимфоидного пула. Основная функция В-клеток состоит в создании антител к различным антигенам, и они являются неотъемлемым элементом адаптивной иммунной системы.
Вследствие их критической роли в регулировании иммунной системы расстройство регуляции В-клеток связано с различными нарушениями, такими как лимфомы и лейкозы. Среди таких нарушений находятся неходжкинская лимфома (НХЛ), хронический лимфоцитарный лейкоз (ХЛЛ) и острый лимфобластный лейкоз (ОЛЛ).
НХЛ - это гетерогенная группа злокачественных новообразований, возникающих из лимфоцитов. В Соединенных Штатах (США) заболеваемость оценивается в 65000/год с числом смертельных случаев примерно 20000 (по данным Американского онкологического общества, 2006 г., и сводной статистики рака SEER). Болезнь встречается во всех возрастных группах, обычно ее начало наблюдается у взрослых старше 40 лет, причем заболеваемость растет с возрастом. НХЛ характеризуется клональной пролиферацией лимфоцитов, которые накапливаются в лимфатических узлах, крови, костном мозге и селезенке, хотя может быть вовлечен любой крупный орган. В настоящее время системой классификации, используемой патологоанатомами и лечащими врачами, является Классификация опухолей Всемирной организации здравоохранения (ВОЗ), по которой НХЛ различают как новообразования прекурсорных и зрелых В-клеток или Т-клеток. PDQ (база данных для врачебных запросов) в настоящее время делит НХЛ на индолентную (медленно прогрессирующую) или агрессивную форму на входе в клинические испытания. Индолентная группа НХЛ состоит в основном из фолликулярных подтипов, малой лимфоцитарной лимфомы, MALT (слизистой оболочки лимфоидной ткани) и маргинальной зоны; в число пациентов с индолентной формой входит примерно 50% вновь диагностированных пациентов с В-клеточной НХЛ. Агрессивная форма НХЛ включает пациентов с гистологическим диагнозом преимущественно диффузной крупноклеточной В-клеточной лимфомы (DLBL, DLBCL или DLCL) (у 40% всех вновь диагностированных пациентов наблюдается диффузная крупноклеточная форма), лимфомы Беркитта и лимфомы из клеток мантии. Клиническое течение НХЛ сильно варьируется. Основной детерминантой клинического течения является гистологический подтип. Большинство индолентных форм НХЛ считаются неизлечимыми. Изначально пациенты реагируют либо на химиотерапию, либо на терапию антителами, и у большинства из них произойдет рецидив заболевания. Исследования, проведенные до настоящего времени, не продемонстрировали улучшения выживаемости при раннем лечении. В случае пациентов без выраженных симптомов принято «наблюдать и выжидать», пока у пациента не появятся симптомы или болезнь не станет прогрессировать. С течением времени заболевание может принять более агрессивную гистологическую форму. Средняя выживаемость составляет 8-10 лет, и пациенты с индолентной формой часто получают 3 или более курсов лечения в ходе лечебной фазы их заболевания. Так сложилось, что первоначальное лечение больного с симптоматической индолентной НХЛ состоит из комбинированной химиотерапии. Наиболее часто применяемые средства включают: циклофосфамид, винкристин и преднизолон (CVP); или циклофосфамид, адриамицин, винкристин, преднизолон (CHOP). Примерно 70-80% пациентов будут реагировать на их первоначальную химиотерапию, продолжительность ремиссий длится порядка 2-3 лет. В конечном итоге у большинства пациентов произойдет рецидив заболевания. Разработка и клиническое использование антитела к CD20 - ритуксимаба - обеспечило значительное улучшение реакции и выживаемости. В настоящее время стандартное лечение для большинства пациентов состоит из ритуксимаба + CHOP (R-CHOP) или ритуксимаба + CVP (R-CVP). Для начального лечения НХЛ одобрен интерферон в комбинации с алкилирующими средствами, но в США он широко не применяется. Было показано, что терапия ритуксимабом эффективна при многих типах НХЛ, и в настоящее время он одобрен в качестве лечения первой линии как для индолентой формы (фолликулярной лимфомы), так и агрессивной НХЛ (диффузной крупноклеточной В-клеточной лимфомы). Однако для монклонального антитела (mAb) к CD20 есть серьезные ограничения, включая первичную невосприимчивость (50% ответов у пациентов с рецидивом индолентной формы), приобретенную невосприимчивость (50% ответов при повторном лечении), редкий полный ответ (2% полной ремиссии в популяции с рецидивом заболевания) и продолжающаяся картина рецидива. И наконец, многие В-клетки не экспрессируют CD20, и поэтому многие В-клеточные расстройства не поддаются лечению антителами к CD20.
Кроме НХЛ существуют несколько других типов лейкозов, которые возникают вследствие расстройства регуляции В-клеток. Хронический лимфоцитарный лейкоз (также известный как «хронический лимфоидный лейкоз» или «ХЛЛ») - это тип лейкоза взрослого возраста, который вызван ненормальным накоплением В-лимфоцитов. При ХЛЛ злокачественные лимфоциты могут выглядеть нормальными и зрелыми, но они не способны эффективно действовать против инфекций. ХЛЛ является наиболее часто встречающейся формой лейкоза у взрослых. У мужчин ХЛЛ развивается, как правило, в два раза чаще, чем у женщин. Однако основным фактором риска является возраст. Свыше 75% новых случаев заболевания выявляют у пациентов в возрасте старше 50 лет. Каждый год выявляется более 10000 случаев заболевания, и смертность составляет почти 5000 в год (по данным Американского онкологического общества, 2006 г., и сводной статистики рака SEER). ХЛЛ является неизлечимой болезнью, но в большинстве случаев прогрессирует медленно. Многие люди с ХЛЛ многие годы ведут нормальный и активный образ жизни. Вследствие своего замедленного изначального развития ХЛЛ на ранних стадиях не лечат, поскольку считается, что раннее лечение ХЛЛ не улучшает выживаемость или качество жизни. Вместо этого проводят наблюдение за состоянием больного с течением времени. Первоначальное лечение ХЛЛ варьируется в зависимости от точного диагноза и прогрессирования болезни. Для лечения ХЛЛ применяют десятки средств. Схемы комбинированной химиотерапии, такой как FCR (флударабин, циклофосфамид и ритуксимаб), и BR (ибрутиниб и ритуксимаб) эффективны как при вновь выявленном ХЛЛ, так и при рецидивирующем заболевании. Пересадка аллогенного костного мозга (стволовых клеток) редко используется в качестве лечения ХЛЛ первой линии вследствие связанного с ней риска.
Другим типом лейкоза является острый лимфобластный лейкоз (ОЛЛ), также известный как острый лимфоцитарный лейкоз. ОЛЛ характеризуется свехпродуцированием и продолжающимся увеличением числа злокачественных и незрелых белых кровяных телец (также называемых лимфобластами) в костном мозге. «Острый» относится к недифференцированному, незрелому состоянию циркулирующих лимфоцитов («бластов»), и эта болезнь быстро прогрессирует, и при отсутствии лечения продолжительность жизни составляет недели или месяцы. ОЛЛ особенно характерен для детского периода и достигает своего максимума к возрасту 4-5 лет. Особенно смертность от этого заболевания высока для детей в возрасте 12-16 лет. В настоящее время считается, что по меньшей мере 80% ОЛЛ детского возраста излечимо. Каждый год выявляется почти 4000 случаев заболевания, и смертность составляет почти 1500 в год (по данным Американского онкологического общества, 2006 г., и сводной статистики рака SEER).
Молекула человеческого CD19 представляет собой рецептор на клеточной поверхности с отличающейся структурой, экспрессируемый на поверхности В-клеток человека, включая, но не ограничиваясь ими, предшественники В-клеток, В-клетки на ранней стадии развития (т.е., незрелые В-клетки), зрелые В-клетки при окончательной дифференциации в клетки плазмы и злокачественные В-клетки. CD19 экспрессируется в большинстве случаев пре-В-клеточных острых лимфобластнных лейкозов (ОЛЛ), неходжкинских лимфом, В-клеточных хронических лимфоцитарных лейкозов (ХЛЛ), пролимфоцитарных лейкозов, лейкозов ворсистых клеток, острых недифференцированных лимфоцитарных лейкозов и некоторых острых лимфобластных лейкозов с нулевым фенотипом (Nadler et al, J. Immunol., 131:244-250 (1983), Loken et al, Blood, 70:1316-1324 (1987), Uckun et al, Blood, 71:13- 29 (1 988), Anderson et al, 1984. Blood, 63:1424-1433 (1 984), Scheuermann, Leuk. Lymphoma, 18:385-397(1995)). Тот факт, что CD19 экспрессируется на клетках плазмы, также позволяет предположить, что он может экспрессироваться на дифференцированных В-клеточных опухолях, таких как множественная миелома, плазмацитомы, опухоли Вальденстрема (Grossbard et al., Br. J. Haematol, 102:509- 15(1 998); Treon et al, Semin. Oncol, 30:248-52(2003)).
Поэтому антиген CD 19 представляет собой цель для иммунотерапии при лечении неходжкинской лимфомы (включая каждый подтип, описанный в данном документе), хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Были продемонстрированы некоторые CD19 терапии. Три пациента с ХЛЛ на поздней стадии получали Т-клетки, экспрессирующие химерный антигенный рецептор (CAR) к CD19, включая как CD3-4, так и 4-ВВ костимулирующий домен. Публикация Kalos et al., Т cells with Chimeric Antigen Receptors Have Potent Antitumor Effects and Can Establish Memory in Patients with Advanced Leukemia, Science Translational Medicine, vol. 3, no. 95 (10 августа 2011 г.), которая включена в данный документ во всей своей полноте ссылкой. В публикации Sadelain et al., The promise and potential pitfalls of chimeric antigen receptors, Current Opinion in Immunology, Elsevier, vol. 21, no. 2, 2 April 2009, которая включена в данный документ во всей своей полноте ссылкой, также описаны химерные антигенные рецепторы (CAR) к CD19. В публикации Neither Kalos et al. nor Sadelain et al., однако, описано антитело, специфичное к CD19, в сочетании с ингибитором тирозинкиназы Брутона (ВТК), как проиллюстрировано в данном документе.
Применение антитела CD19 при неспецифических В-клеточных лимфомах обсуждается в публикации W02007076950 (US 2007154473), обе из которых включены в данный документ во всей своей полноте ссылкой, а также вскользь упоминается ибрутиниб в длинном перечне потенциальных компонентов для комбинации, но в этом документе не приводится иллюстрируемое здесь антитело и не предполагается наличие синергического действия от комбинации в лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза в отличие от того, как это проиллюстрировано в данном документе.
Применение антител CD19 в ХЛЛ, НХЛ и ОЛЛ описано в публикации Scheuermann et al., CD19 Antigen in Leukemia and Lymphoma Diagnosis and Immunotherapy, Leukemia and Lymphoma, Vol. 18, 385-397 (1 995), которая включена в данный документ во всей своей полноте ссылкой, но в ней не предложена комбинация, проиллюстрированная в данном документе.
Дополнительные антитела, специфичные к CD19, описаны в публикациях W02005012493 (US 7109304), W02010053716 (USI 2/266,999) (Immunomedics); W02007002223 (US US 8097703) (Medarex); W02008022152 (12/377,251) и W02008150494 (Xencor), W02008031056 (USI I /852, 1 06) (Medimmune); WO 2007076950 (US 11/648505) (Merck Patent GmbH); WO 2009/052431 (USI 2/253895) (Seattle Genetics); and W02010095031 (12/710,442) (Glenmark Pharmaceuticals), W02012010562 и W02012010561 (International Drug Development), W0201 1 147834 (Roche Glycart) и WO 2012/156455 (Sanofi), которые включены в данный документ во всей своей полноте ссылкой.
Комбинации антител, специфичных к CD19, и других средств описаны в публикациях W02010151341 (US 13/377,514) (The Feinstein Institute); US 5686072 (University of Texas) и WO 2002022212 (PCT/US 01/29026) (IDEC Pharmaceuticals), W02013/024097 (14/126928) (MorphoSys AG) и W02013/024095 (14/127217) (MorphoSys AG), которые включены в данный документ во всей своей полноте ссылкой.
В продажу поступают некоторые ингибиторы тирозинкиназы Брутона. Ибрутиниб, также известный как PCI-32765 и поступающий в продажу под названием имбрувика, представляет собой лекарство против рака, нацеленное на В-клеточные злокачественные новообразования. Ибрутиниб описан в патентах США №№7514444, 8008309, 869771, 8735403, 8957079 и 8754090, которые включены в данный документ во всей своей полноте ссылкой.
Испытания ибрутиниба проводили в комбинации с ритуксимабом (антителом к CD20). Burger et al., Lancet Oncol., 2014 September, 15(19): 1090-1099. Потенциально ибрутиниб подавляет активность ADCC некоторых антител CD20 in vitro. Duong et al., mAbs, Jan/Feb 2015, 192-198 и Kohrt et al., Blood, 2014, 123:1957-1960.
Очевидно, что несмотря на недавний прогресс в обнаружении и разработке противоопухолевых средств, многие формы рака, в которые вовлечены опухоли, экспрессирующие CD19, по-прежнему имеют плохой прогноз. Поэтому существует потребность в усовершенствованных способах лечения таких форм рака.
Краткое описание
Ни в каком из документов предшествующего уровня техники, ни в их комбинации не предполагается наличие синергического действия комбинации приведенных антител и ибрутиниба в лечении неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
В одном аспекте настоящее изобретение относится к синергической комбинации антитела, специфичного к CD19, и ингибитора тирозинкиназы Брутона (ВТК). Такие комбинации полезны при лечении В-клеточных злокачественных новообразований, таких как неходжкинская лимфома, хронический лимфоцитарный лейкоз и/или острый лимфобластный лейкоз.
Считается, что модели in vitro показывают, как определенные соединения или комбинации соединений будут вести себя в ходе применения у людей.
Клетки МЕС-1 в такой модели in vitro показывают, как комбинация будет работать в ходе лечения хронического лимфоидного лейкоза (ХЛЛ) у людей. Клетки-Ramos в такой модели in vitro показывают, как комбинация будет работать в ходе лечения неходжкинской лимфомы (НХЛ) у людей. Клетки МЕС-1 (DSMZ# АСС497) представляют собой клеточную линию хронического В-клеточного лейкоза. Клетки-Ramos (АТСС номер CPL-1596) - это человеческие клетки лимфомы Беркитта.
Кроме того, при комбинировании соединений in vitro предполагается, что они будут иметь только совокупное воздействие. Неожиданно изобретателями было обнаружено, что комбинация определенного антитела, специфичного к CD19, и ибрутиниба опосредовала синергический уровень специфического клеточного уничтожения in vitro по сравнению с одним только антителом и одним только ибрутинибом. В частности, изобретателями было обнаружено, что комбинация MOR00208 и ибрутиниба опосредовала синергический уровень специфического клеточного уничтожения in vitro в случае клеток МЕС-1 по сравнению с одним только антителом и одним только ибрутинибом.
Кроме того, и также неожиданно, изобретателями было обнаружено, что комбинация определенного антитела, специфичного к CD19, и ибрутиниба имела определенные функциональные характеристики по сравнению с одним только антителом и одним только ибрутинибом.
В целом, комбинация названного антитела к CD19 и ибрутиниба продемонстрировала синергическое поведение в моделях, относящихся к ХЛЛ. Поскольку ХЛЛ относится к В-клеточным расстройствам, и CD19 свехэкспрессируется на В-клетках, названная комбинация будет иметь такой же механизм действия и должна проявлять синергическое действие в лечении других В-клеточных расстройств, например, ОЛЛ и НХЛ.
Поэтому комбинация названных антитела, специфичного к CD19, и ибрутиниба должна быть эффективной при лечении людей в случаях неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. Ожидаемая действенность комбинации антитела, специфичного к CD 19, и ибрутиниба будет подтверждена в клинических исследованиях.
Поскольку механизмы действия ибрутиниба и других ингибиторов тирозинкиназы Брутона (ВТК) похожи, поскольку все они работают путем подавления протеинкиназного ВТК фермента, который играет решающую роль в развитии В-клеток, считается, что синергия также будет наблюдаться при лечении людей с выявленными неходжкинской лимфомой, хроническим лимфоцитарным лейкозом и/или острым лимфобластным лейкозом комбинацией названного антитела к CD19 и ингибитора тирозинкиназы Брутона (ВТК), отличающегося от ибрутиниба.
Поскольку названное антитело к CD19 и другие антитела к CD19 связываются с CD19, считается, что синергия также будет наблюдаться при лечении людей с выявленными неходжкинской лимфомой, хроническим лимфоцитарным лейкозом и/или острым лимфобластным лейкозом комбинацией названного любого антитела к CD19 и ингибитора тирозинкиназы Брутона (ВТК), например, ибрутинибом.
Один аспект настоящего раскрытия включает в себя синергическую комбинацию, где антитело, специфическое к CD19, содержит участок HCDR1 последовательности SYVMH (SEQ ID NO: 1) участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2) участок HCDR3 последовательности GTYYYGTRVFDY (SEQ ID NO: 3) участок LCDR1 последовательности RSSKSLQNVNGNTYLY (SEQ ID NO: 4) участок LCDR2 последовательности RMSNLNS (SEQ ID NO: 5) участок LCDR3 последовательности MQHLEYPIT (SEQ ID NO: 6) и ибрутиниб. В предпочтительных аспектах комбинацию применяют для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Описание графических материалов
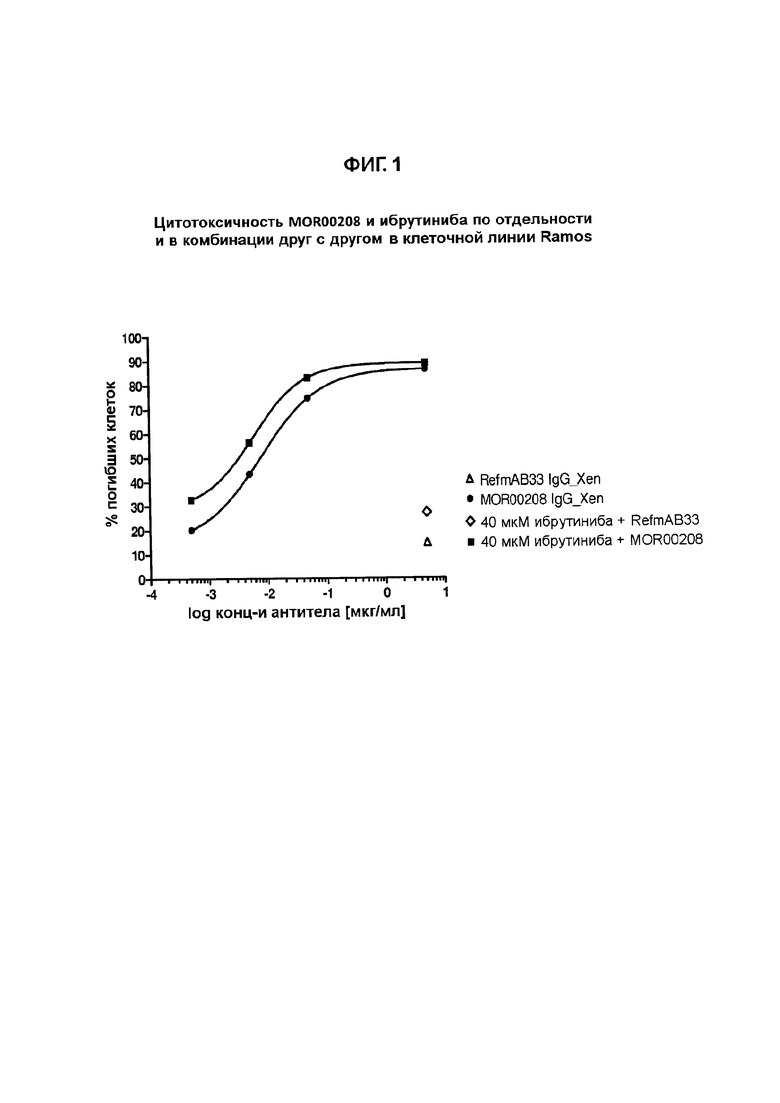
На Фигуре 1 показано цитотоксическое действие MOR00208 и ибрутиниба по отдельности и в комбинации друг с другом на клетки-Ramos. Клетки-Ramos обрабатывали 40 мкМ ибрутиниба 24 часа.
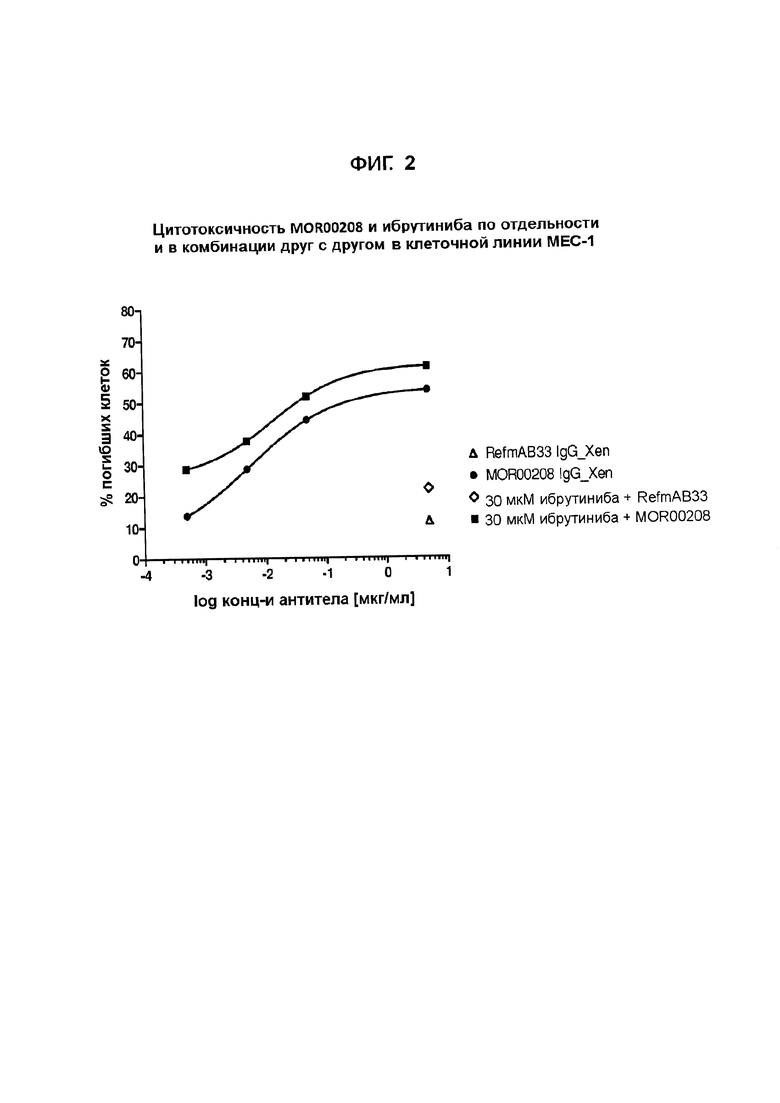
На Фигуре 2 показано цитотоксическое действие MOR00208 и ибрутиниба по отдельности и в комбинации друг с другом на клетки МЕС-1. Клетки МЕС-1 обрабатывали 30 мкМ ибрутиниба 24 часа.
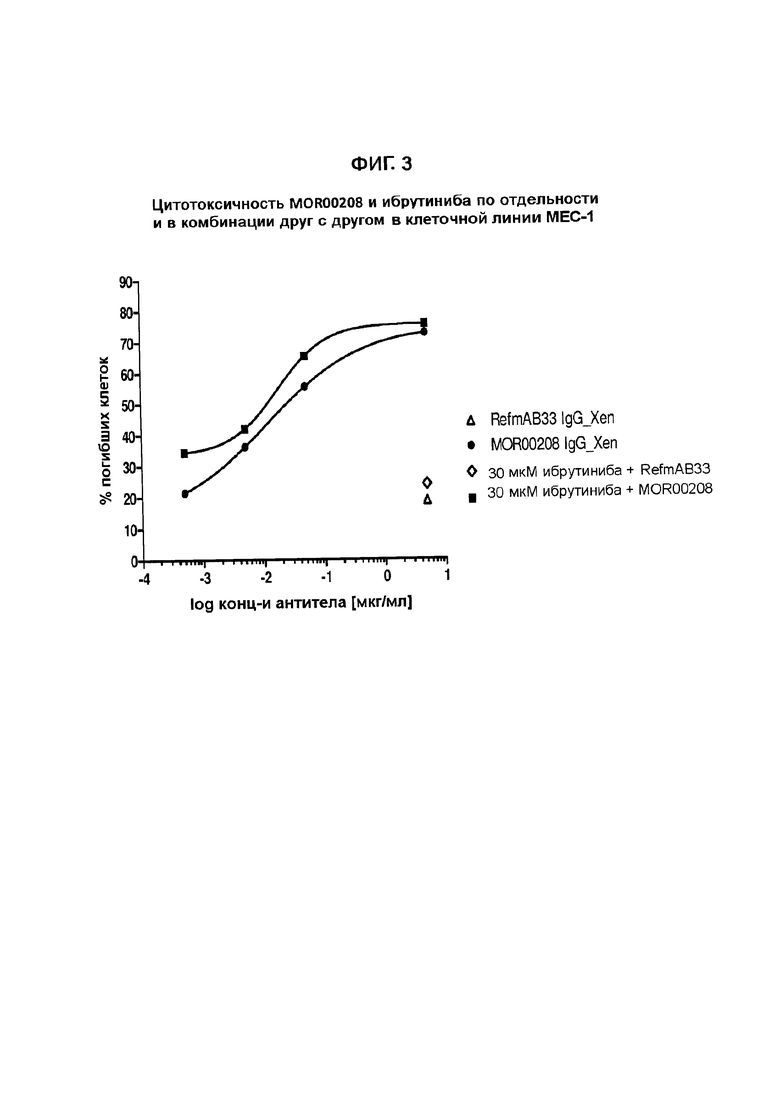
На Фигуре 3 показано цитотоксическое действие MOR00208 и ибрутиниба по отдельности и в комбинации друг с другом на клетки МЕС-1. Клетки МЕС-1 обрабатывали 30 мкМ ибрутиниба 24 часа.
На Фигуре 4 показана аминокислотная последовательность вариабельных доменов MOR00208.
На Фигуре 5 показана аминокислотная последовательность Fc участков MOR00208.
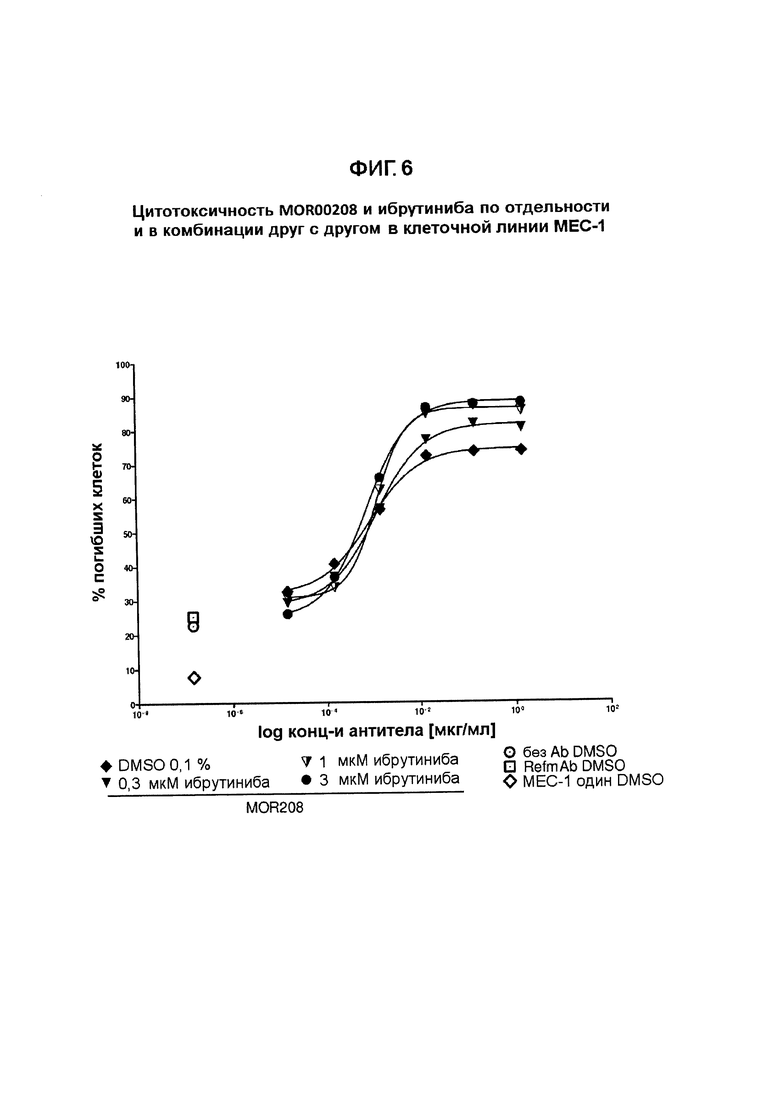
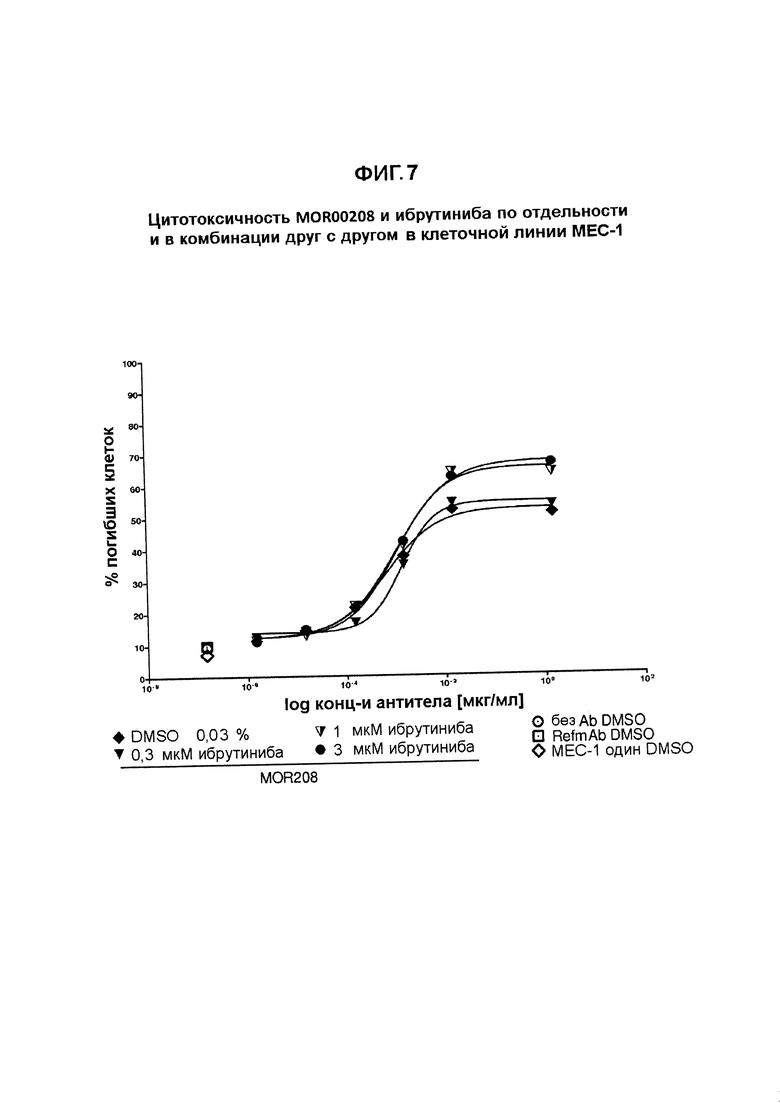
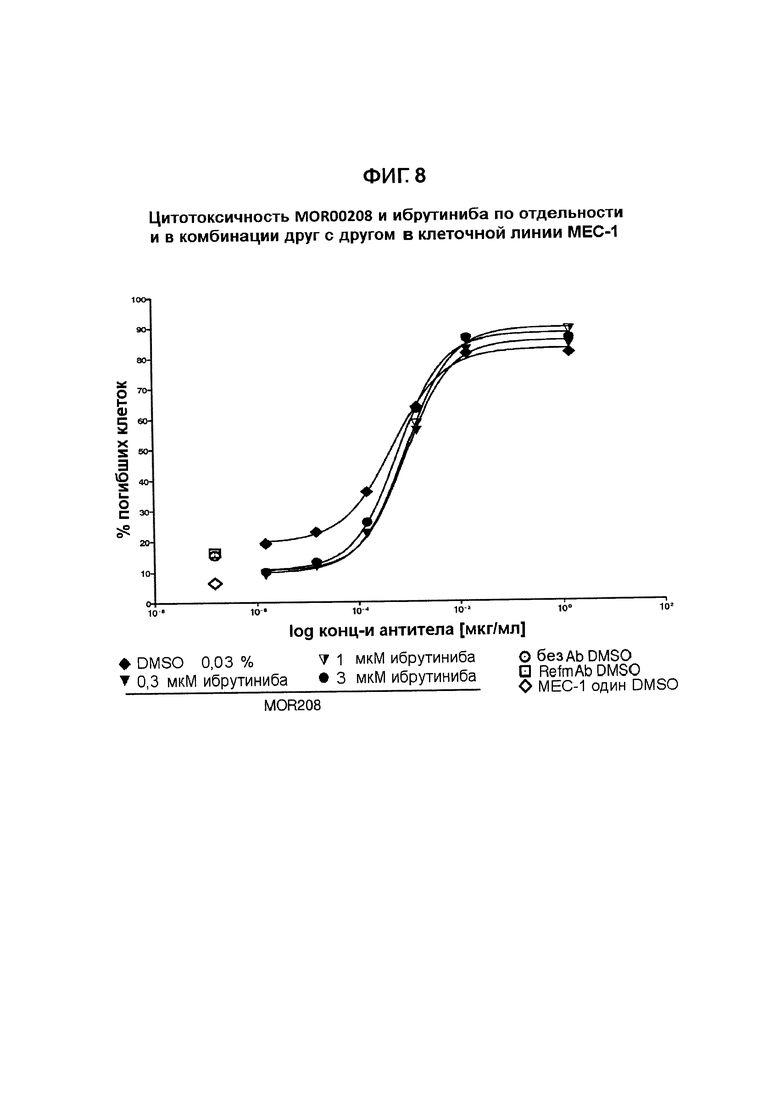
На Фигурах 6-8 показана цитотоксичность MOR00208 и ибрутиниба по отдельности и в комбинации друг с другом в клеточной линии МЕС-1.
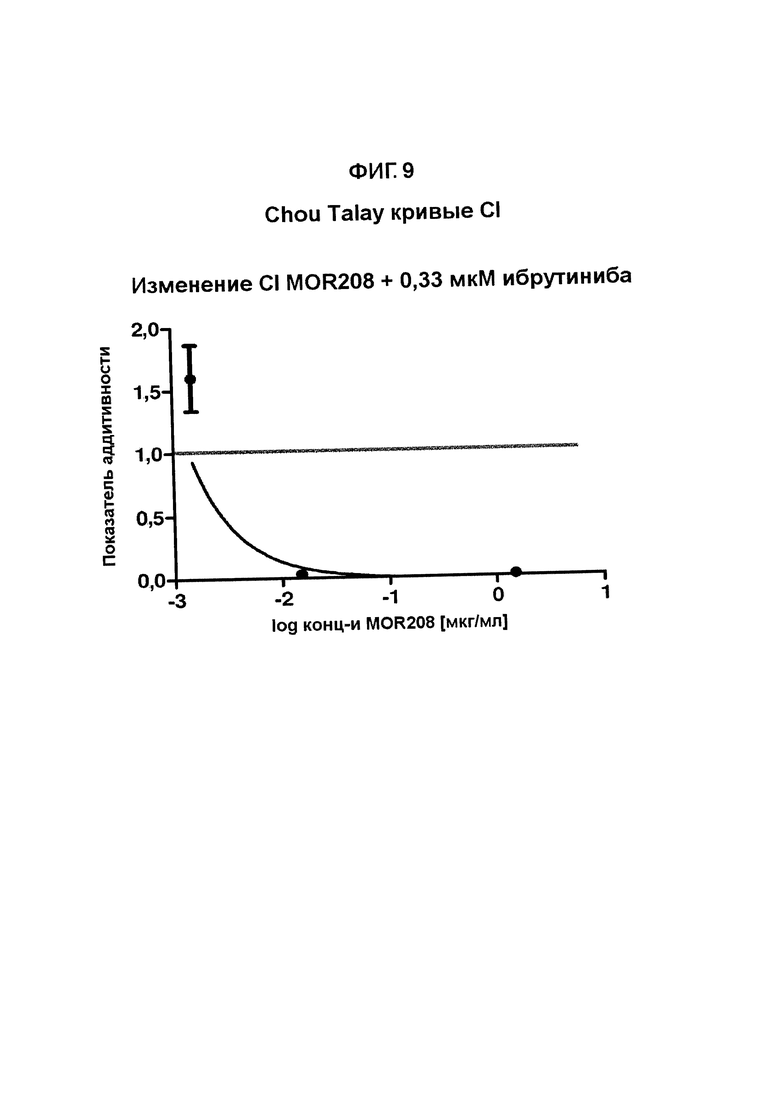
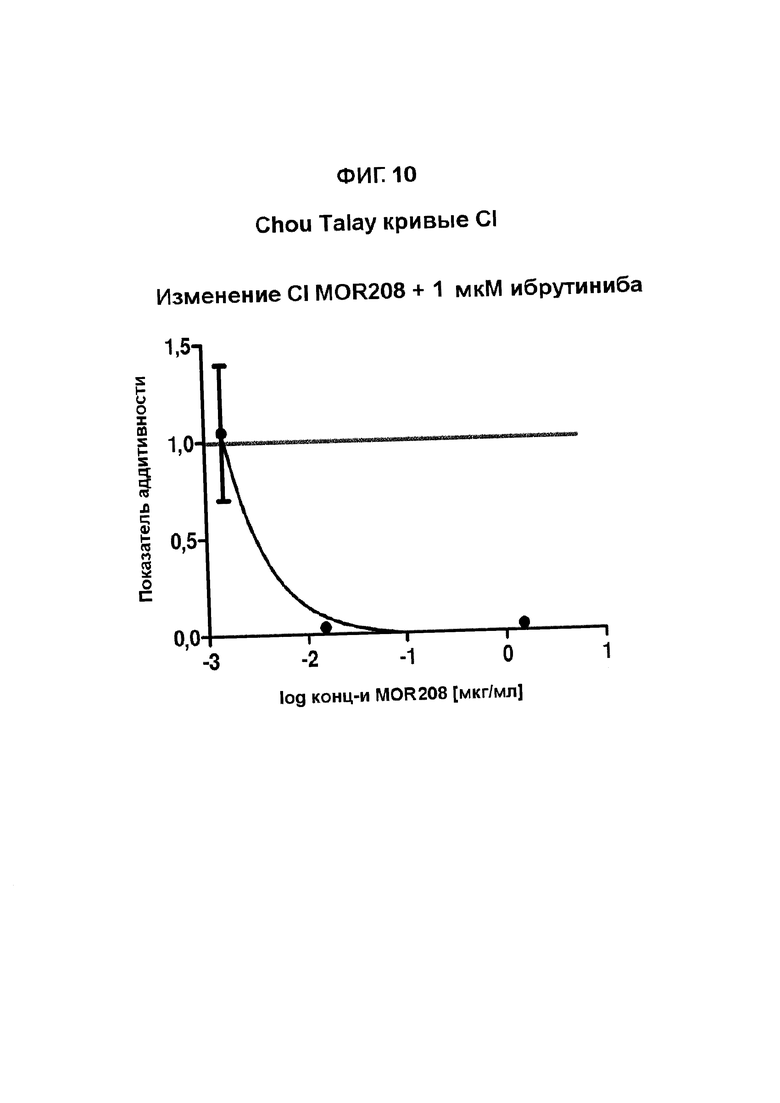
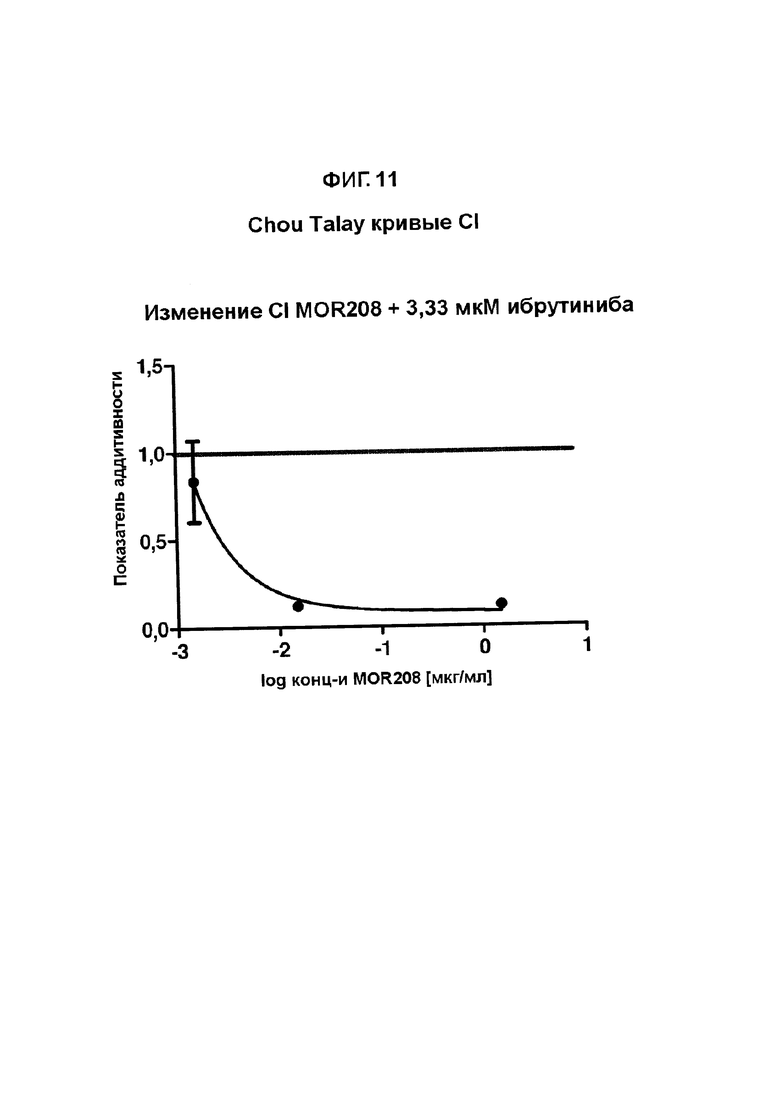
На Фигурах 9-11 показаны кривые показателя аддитивности Chou-Talay для комбинации MOR00208 и ибрутиниба в клеточной линии МЕС-1.
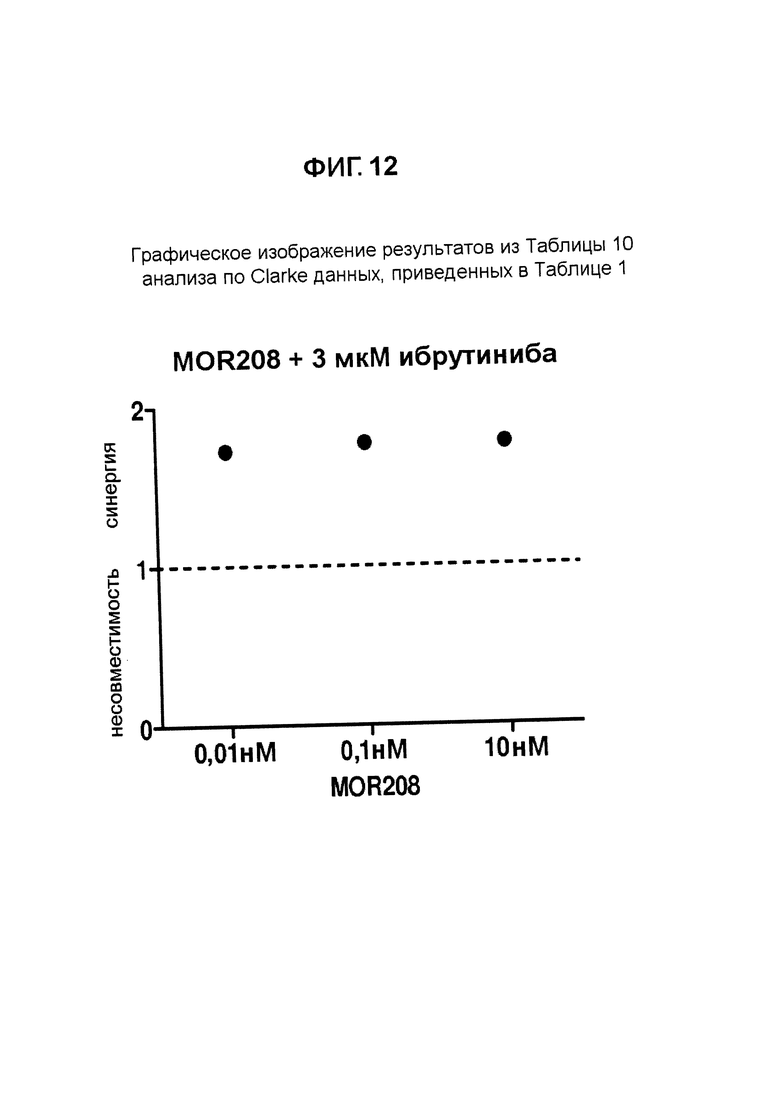
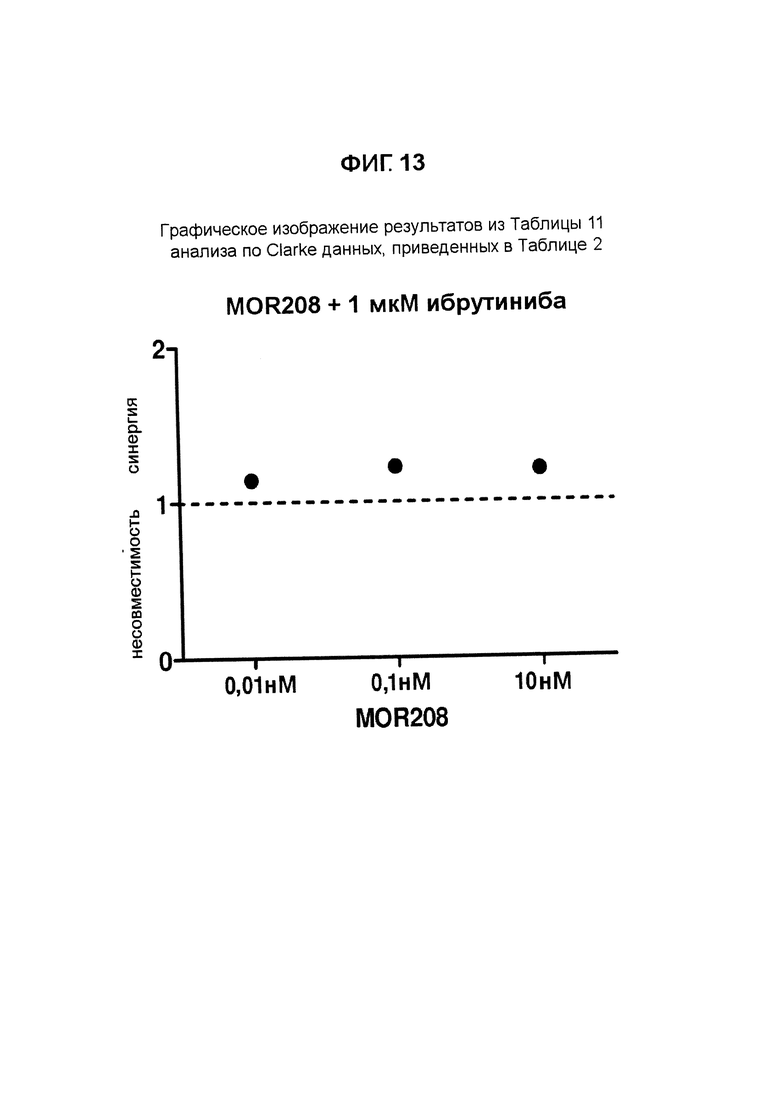
На Фигурах 12-20 показаны расчеты по Clarke et al. синергии MOR00208 и ибрутиниба в комбинации друг с другом в клеточной линии МЕС-1.
Подробное описание изобретения
«Синергия», «синергизм» или «синергический» означают больше, чем ожидаемый суммарный эффект комбинации. «Синергия», «синергизм» или «синергический» эффект комбинации определены в данном документе с помощью способов в публикации Chou et al., Clarke et al. and/or Webb et al. См. Ting-Chao Chou, Theoretical Basis, Experimental Design, and Computerized Simulation of Synergism and Antagonism in Drug Combination Studies, Pharmacol Rev 58:621-681 (2006), которая включена в данный документ во всей своей полноте ссылкой. Также см. публикацию Clarke et al., Issues in experimental design and endpoint analysis in the study of experimental cytotoxic agents in vivo in breast cancer and other models, Breast Cancer Research and Treatment 46:255-278 (1997), которая включена в данный документ во всей своей полноте ссылкой. Также см. публикацию Webb, J.L. (1963) Enzyme and Metabolic Inhibitors, Academic Press, New York, которая включена в данный документ во всей своей полноте ссылкой.
Термин "антитело" означает моноклональные антитела, включая любой изотип, такой как IgG, IgM, IgA, IgD и IgE. Антитело IgG состоит из двух идентичных тяжелых цепей и двух идентичных легких цепей, которые соединены дисульфидными связями. Каждая тяжелая и легкая цепь содержит константную область и вариабельную область. Каждая вариабельная область содержит три сегмента, называемых «участками, определяющими комплементарность» («CDR») или «гипервариабельными участками», которые в первую очередь отвечают за связывание с эпитопом антигена. На них ссылаются как CDR1, CDR2 и CDR3, нумеруя последовательно от N-конца. Более консервативные фрагменты вариабельных участков за пределами CDR называют «каркасными участками». «Фрагменты антитела» означают фрагменты Fv, scFv, dsFv, Fab, Fab', F(ab')2 или другой фрагмент, который содержит по меньшей мере один вариабельную тяжелую или легкую цепь, каждая из которых содержит CDR и каркасные участки.
"Ингибитор тирозинкиназы Брутона (ВТК)" представляет собой класс лекарственных средств, которые действуют путем подавления протеинкиназного ВТК фермента, который играет решающую роль в развитии В-клеток. В частности, ВТК содержит домен РН, который связывает фосфатидилинозитол (3,4,5)-трифосфат (PIP3). Связывание PIP3 стимулирует Btk к фосфорилированию фосфолипазы С, которая, в свою очередь, гидролизует PIP2 - фосфатидилинозитол - на два вторичных мессенджера - инозитолтрифосфат (IP3) и диацилглицерин (DAG), которые затем продолжают модулировать активность белков ниже по каскаду во время передачи сигналов В-клеток.
Ингибиторы тирозинкиназы Брутона (ВТК) включают в себя ибрутиниб. Ибрутиниб поступает в продажу от Pharmacyclics, Inc and Johnson & Johnson's Janssen Pharmaceutical (торговое название - имбрувика (Imbruvica), также называемая PCI-32765). Ибрутиниб в настоящее время рекомендован для лечения пациентов с лимфомой из клеток мантии (MCL), которые получили по крайней мере одну предшествующую терапию, хроническим лимфоцитарным лейкозом (ХЛЛ), которые получили по меньшей мере одну предшествующую терапию, хроническим лимфоцитарным лейкозом с делецией 17р и макроглобулинемией Вальденстрема. Ибрутиниб имеет следующую формулу: 1-[(3R)-3-[4-амино-3(4-феноксифенил)-1Н-пиразоло[3,4-d]пиримидин-1-ил]-1-пиперидил]-2-пропен-1-он, со следующей структурой:
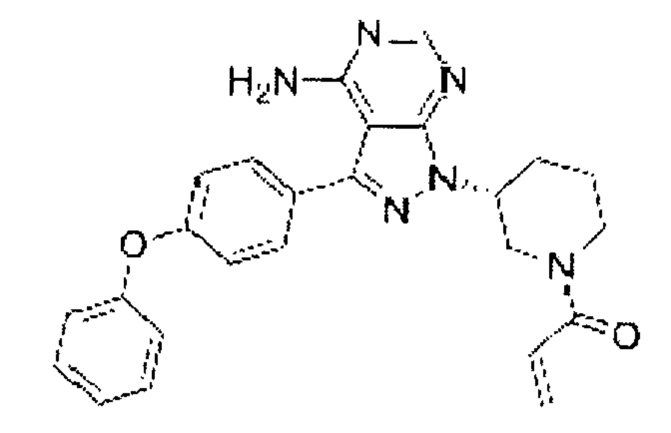
Ибрутиниб представляет собой малую молекулу-ингибитор ВТК. Ибрутиниб образует ковалентную связь с цистеиновым остатком в активном сайте ВТК, что приводит к подавлению ферментной активности ВТК. ВТК представляет собой сигнальную молекулу путей рецептора В-клеточного антигена (BCR) и цитокинового рецептора. Роль ВТК в передаче сигналов через рецепторы поверхности В-клетки приводит к активации путей, необходимых для направленной миграции В-клеток, хемотаксиса и адгезии. Неклинические исследования показывают, что ибрутиниб подавляет злокачественную пролиферацию В-клеток и выживаемость in vivo, а также миграцию клеток и адгезию к субстрату in vitro.
Дополнительно ингибиторы тирозинкиназы Брутона (ВТК) включают в себя:
ACP-196 (Acerta Pharma BV), который описан в публикации WO 2012170976 (заявка на патент США №14/112428), WO 2013010380 (заявка на патент США №14/233478) и WO 2014113932 (заявка на патент США №14/160587), все из которых включены в данный документ во всей своей полноте ссылкой;
BGB-3111 (BeiGene, Co., Ltd.) и СС-292 Evans et al. 2013
"VH" относится к вариабельной области тяжелой цепи иммуноглобулина антитела или фрагмента антитела. "VL" относится к вариабельной области легкой цепи иммуноглобулина антитела или фрагмента антитела.
Термин "CD19" относится к белку, известному как CD19, имеющему следующие синонимы: В4, В-лимфоцитарный антиген CD19, В-лимфоцитарный поверхностный антиген В4, CVID3, дифференцировочный антиген CD19, MGCI 2802 и Т-клеточный поверхностный антиген Leu-12.
Аминокислотная последовательность человеческого CD19:

"MOR00208" представляет собой антитело к CD19. Аминокислотная последовательность вариабельных доменов представлена на Фигуре 4. Аминокислотная последовательность Fc участков тяжелой и легкой цепей MOR00208 представлена на Фигуре 5. "MOR00208" и "XmAb 5574" используются в качестве синонимов для описания антитела, показанного на Фигурах 4 и 5. Антитело MOR00208 описано в заявке на патент США за порядковым номером 12/377251, которая включена в данный документ во всей своей полноте ссылкой.
В заявке на патент США за порядковым номером 12/377251 описано антитело, названное 4G7 Н1.52 Hybrid S239D/I332E / 4G7 L1.155 (позднее названное MOR00208), как указано ниже:


Дополнительные антитела, специфичные к CD19, описаны в патенте США №7109304 (Immunomedics), который включен в данный документ во всей своей полноте ссылкой; заявке на патент США за порядковым номером 11/917750 (Medarex), которая включена в данный документ во всей своей полноте ссылкой; заявке на патент США за порядковым номером 11/852106 (Medimmune), которая включена в данный документ во всей своей полноте ссылкой; заявке на патент США за порядковым номером 11/648505 (Merck Patent GmbH), которая включена в данный документ во всей своей полноте ссылкой; патенте США №7968687 (Seattle Genetics), который включен в данный документ во всей своей полноте ссылкой; заявке на патент США за порядковым номером 12/710442 (Glenmark Pharmaceuticals), которая включена в данный документ во всей своей полноте ссылкой.
"Fc участок" означает константный участок антитела, который у людей может относиться к подклассу IgG1, 2, 3, 4 или другим подклассам. Последовательности человеческих Fc участков можно узнать на сайте IMGT, Human IGH C-REGIONs, http://www.imgt.org/IMGTrepertoire|Proteins /protein/human/IGH/IGHC/Hu_IGHCallgenes.html (найдено 16 мая 2011 г.).
"RefmAb33" представляет собой антитело со следующей аминокислотной последовательностью:
Тяжелая цепь, включая Fc участок:


Легкая цепь, включая Fc участок:

RefmAb33 специфичен к RSV и используется в качестве изотипического контроля, поскольку он имеет такой же Fc участок как и MOR00208.
"Комбинация" означает более чем один компонент, например, соединение, такое как антитело и ибрутиниб.
Настоящее раскрытие также относится к комбинациям, фармацевтическим препаратам и фармацевтическим композициям, содержащим описанные комбинации. Два компонента синергической комбинации данного изобретения, например, антитело, специфическое к CD19, и ибрутиниб, можно вводить вместе, одновременно, отдельно или последовательно, как физически, так и во времени.
В настоящее время ибрутиниб принимают перорально при дозировании один раз в день. В настоящее время MOR00208 вводят внутривенно при дозировании либо раз в неделю, либо один раз в две недели.
Предпочтительно, чтобы введение обоих препаратов позволяло обоим лекарственным средствам проявлять свое действие в патенте одновременно. Например, если MOR208 дозируют еженедельно, а ибрутиниб дозируют ежедневно, то активные вещества обоих лекарственных средств присутствуют в пациенте одновременно. В одном варианте осуществления ибрутиниб принимают до и/или отдельно от введения антитела, специфичного к CD19, например, MOR00208.
«Одновременно» означает, что два компонента вводят в момент времени, когда оба компонента (лекарственные средства) проявляют свое действие в пациенте в одно и то же время. Под «синергизмом» подразумевается, что оба лекарственных средства проявляют свое действие в пациенте в одно и то же время.
«Вводятся вместе» может означать, что они вводятся в одно и то же время.
Эти два компонента могут быть составлены в различных фармацевтических композициях. Фармацевтическая композиция включает активный агент, например, антитело, для терапевтического применения у людей. Фармацевтическая композиция может включать приемлемые носители или вспомогательные вещества.
«Вводимый», «введение» или «прием» включают, но не ограничиваются этим, доставку в форме инъекции, такой как, например, внутривенный, внутримышечный, внутрикожный или подкожный путь, или через слизистую оболочку, например, в виде назального спрея или аэрозоля для ингаляции, или в качестве усваиваемых в пищеварительном тракте раствора, капсулы или таблетки.
«Терапевтически эффективное количество» соединения или комбинации относится к количеству, достаточному для излечения, облегчения или частичного прекращения клинических проявлений данного заболевания или расстройства и его осложнений. Количество, эффективное для конкретной терапевтической цели, будет зависеть от тяжести заболевания или травмы, а также от веса и общего состояния субъекта. Понятно, что подходящую дозу можно определить, используя обычные эксперименты, путем построения таблицы значений и тестирования различных точек в таблице; все из этих приемов являются обычными навыками подготовленного врача или клинического ученого.
"CDR" в данном документе определены, как либо у Chothia et al., либо у Kabat et al. См. публикацию Chothia С, Lesk AM. (1987) Canonical structures for the hypervariable regions of immunoglobulins. J Mol Biol., 196(4):901-17, которая включена в данный документ во всей своей полноте ссылкой. См. публикацию Kabat Е.А, Wu Т.Т., Perry Н.М., Gottesman KS. and Foeller C. (1991). Sequences of Proteins of Immunological Interest. 5th edit., NIH Publication no. 91-3242, US Dept. of Health and Human Services, Washington, DC, которая включена в данный документ во всей своей полноте ссылкой.
«Перекрестно конкурирует» означает способность антитела или другого связывающего агента препятствовать связыванию других антител или связывающих агентов с CD19 в стандартном анализе конкурентного связывания. Способность или степень, с которой антитело или фрагмент антитела может препятствовать связыванию другого антитела или фрагмента антитела с CD19, и, таким образом, когда о нем можно сказать, что оно перекрестно конкурирует в соответствии с данным изобретением, можно определить, используя стандартный анализ конкурентного связывания. В одном подходящем количественном анализе используется технология Biacore (например, если использовать прибор BIAcore 3000 (Biacore, Uppsala, Sweden)), который может измерять степень взаимодействия, используя технологию поверхностного плазмонного резонанса. Другой количественный анализ для измерения перекрестной конкуренции использует подход, основанный на ELISA. Процесс с высокой пропускной способностью для "биннинга эпитопов" антител, основанный на их перекрестной конкуренции, описан в международной патентной заявке № WO 2003/48731.
Термин «эпитоп» включает в себя любую детерминанту белка, способную специфически связываться с антителом или иным образом взаимодействовать с молекулой. Эпитопные детерминанты обычно состоят из химически активных поверхностных скоплений молекул, таких как боковые цепи аминокислот или углеводов или Сахаров, и могут иметь специфические свойства 3-х мерных структур, а также определенные свойства, обусловленные наличием электрического заряда. Эпитоп может быть «линейным» или «конформационным». Термин «линейный эпитоп» относится к эпитопу со всеми точками взаимодействия между белком и взаимодействующей молекулой (такой как антитело), расположенными линейно вдоль первичной аминокислотной последовательности белка (непрерывной). Термин «конформационный эпитоп» относится к эпитопу, в котором прерывистые аминокислоты объединяются в трехмерную конформацию. В конформационном эпитопе точки взаимодействия расположены по аминокислотным остаткам на белке, которые отделены друг от друга.
«Связывается с тем же эпитопом, что и» означает способность антитела или другого связывающего агента связываться с CD19 и иметь тот же эпитоп, что и описываемое антитело. Эпитопы описываемого антитела и других антител к CD19 могут быть определены с использованием стандартных методов картирования эпитопов. Методы картирования эпитопов, широко известные в области техники, включают Протоколы картирования эпитопов (Epitope Mapping Protocols) в публикации Methods in Molecular Biology, Vol. 66 (Glenn E. Morris, Ed., 1996) Humana Press, Totowa, New Jersey. Например, линейные эпитопы можно определять путем, например, одновременного синтеза большого количества пептидов на твердых подложках, пептидов, соответствующих частям молекулы белка, и взаимодействия пептидов с антителами, в то время как пептиды все еще связаны с подложками. Такие методики известны в уровне техники и описаны, например, в патенте США №708871; публикациях Geysen et al, (1984) Proc. Natl. Acad. Sci. USA 8:3998-4002; Geysen et al, (1985) Proc. Natl. Acad. Sci. USA 82:78-182; Geysen et al, (1986) Mol. Immunol. 23:709-715. Аналогичным образом, конформационные эпитопы легко идентифицируются путем определения пространственной конформации аминокислот, такого как, например, обмен водорода / дейтерия, рентгеновская кристаллография и двумерный ядерный магнитный резонанс. См., например, Epitope Mapping Protocols, выше. Антигенные области белков также могут быть идентифицированы с использованием стандартных графиков антигенности и гидрофобное™, таких как рассчитанные с использованием, например, программного обеспечения Omiga версия 1.0, которое можно получить у Oxford Molecular Group.В этой компьютерной программе используется способ Hopp/Woods, Норр et al, (1981) Proc. Natl. Acad. Sci USA 78:3824-3828 для определения профилей антигенности, и методика Kyte-Doolittle, Kyte et al, (1982) J.M01. Biol. 157: 105-132 для построения графиков гидрофобности.
Варианты осуществления
В одном аспекте настоящего раскрытия описана фармацевтическая комбинация, включающая антитело, специфическое к CD19, и ингибитор тирозинкиназы Брутона (ВТК) для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. В вариантах осуществления комбинация является синергической.
В данном документе, комбинация названного антитела к CD19 и ибрутиниба продемонстрировала синергическое поведение в моделях in vitro, относящихся к ХЛЛ. Поскольку ХЛЛ относится к В-клеточному расстройству, и CD19 свехэкспрессируется на В-клетках, названная комбинация должна иметь такой же механизм действия и должна проявлять синергическое действие в лечении других В-клеточных расстройств, например, ОЛЛ и НХЛ. Поэтому комбинация названных антитела, специфичного к CD19, и ибрутиниба должна быть эффективной при лечении людей в случаях неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. Ожидаемая действенность комбинации антитела, специфичного к CD19, и ибрутиниба будет подтверждена в клинических исследованиях.
Испытания проводили на клетках МЕС-1 (DSMZ# АСС497) - клеточной линии хронического В-клеточного лейкоза. Клетки МЕС-1 в такой модели in vitro показывают, как комбинация будет работать в ходе лечения хронического лимфоидного лейкоза (ХЛЛ) у людей. Значения индекса Chou однозначно указывают на синергизм комбинации MOR00208 и ибрутиниба для специфического уничтожения клеток МЕС-1 по сравнению с одним только MOR00208 и только одним ибрутинибом.
Были оценены дополнительные клеточные линии: Клетки-Ramos (АТСС номер CRL-1596) - человеческие клетки лимфомы Беркитта. HG-3 (DSMZ#ACC765) и СИ (DSMZ#ACC773) - клеточная линия хронического лимфоцитарного лейкоза. Su-DHL 6 (DSMZ#ACC572), U2932 (DSMZ#ACC633) и OCI-LY7 (DSMZ#ACC688) - клеточная линия диффузной крупноклеточной В-клеточной лимфомы (DLBCL). JVM-2 (АТСС® CRL3002) -клеточная линия лимфомы из клеток мантии. BALL-1 (DSMZ#ACC742) - клеточная линия острого лимфобластного лейкоза.
Клетки-Ramos в такой модели in vitro показывают, как комбинация будет работать в ходе лечения неходжкинской лимфомы (НХЛ) у людей. Клетки HG-3 и СП в такой модели in vitro показывают, как комбинация будет работать в ходе лечения хронического лимфоидного лейкоза (ХЛЛ) у людей. Клетки Su-DHL 6, U2932 и OCI-LY7 в такой модели in vitro показывают, как комбинация будет работать в ходе лечения неходжкинской лимфомы у людей. Клетки JVM-2 в такой модели in vitro показывают, как комбинация будет работать в ходе лечения неходжкинской лимфомы у людей. Клетки BALL-1 в такой модели in vitro показывают, как комбинация будет работать в ходе лечения острого лимфобластного лейкоза у людей.
В целом, комбинация названного антитела к CD19 и ибрутиниба продемонстрировала синергическое поведение в моделях, относящихся к ХЛЛ.
Поэтому комбинация названных антитела, специфичного к CD19, и ибрутиниба должна быть эффективной при лечении людей в случаях неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза.
Поскольку механизм действия ибрутиниба и других ингибиторов тирозинкиназы Брутона (ВТК) похожи, поскольку все они работают путем подавления протеинкиназного ВТК фермента, который играет решающую роль в развитии В-клеток, считается, что синергия также будет наблюдаться при лечении людей с выявленными неходжкинской лимфомой, хроническим лимфоцитарным лейкозом и/или острым лимфобластным лейкозом комбинацией названного антитела к CD19 и ингибитора тирозинкиназы Брутона (ВТК), отличающегося от ибрутиниба.
Поскольку названное антитело к CD19 и другие антитела к CD19 связываются с CD19, считается, что синергия также будет наблюдаться при лечении людей с выявленными неходжкинской лимфомой, хроническим лимфоцитарным лейкозом и/или острым лимфобластным лейкозом комбинацией названного любого антитела к CD19 и ингибитора тирозинкиназы Брутона (ВТК), где антитело к CD19 представляет собой, например, описанное в публикациях заявок на патент США за номером 12/377251 (Xencor), W02005012493, W02010053716 (Immunomedics), W02007002223 (Medarex), W02008022152 (Xencor), W02008031056 (Medimmune), WO 2007/076950 (Merck Patent GmbH), WO 2009/052431 (Seattle Genetics) и W02010095031 (Glenmark Pharmaceuticals), все из которых включены в данный документ во всей своей полноте ссылкой.
В вариантах осуществления антитело, специфическое к CD19, включает в себя антитело, которое перекрестно конкурирует с антителом, содержащим участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности 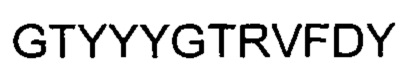 (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности 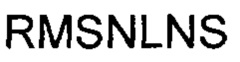 (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6).
(SEQ ID NO: 6).
В вариантах осуществления антитело, специфическое к CD19, включает в себя антитело, которое связывается с тем же эпитопом, что и антитело, содержащее участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности 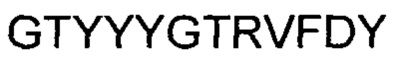 (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности RMSNLNS (SEQ ID NO: 5), участок LCDR3 последовательности MQHLEYPIT (SEQ ID NO: 6).
(SEQ ID NO: 4), участок LCDR2 последовательности RMSNLNS (SEQ ID NO: 5), участок LCDR3 последовательности MQHLEYPIT (SEQ ID NO: 6).
В вариантах осуществления антитело, специфическое к CD19, включает в себя участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности  (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности  (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6).
(SEQ ID NO: 6).
В вариантах осуществления антитело, специфическое к CD19, включает в себя вариабельную тяжелую цепь последовательности 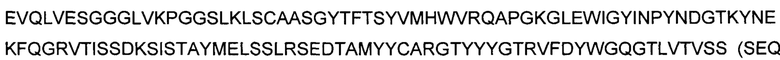
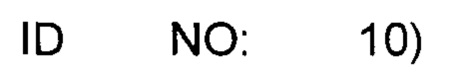 и вариабельную легкую цепь последовательности
и вариабельную легкую цепь последовательности 
В некоторых вариантах осуществления указанное антитело содержит константный домен тяжелой цепи последовательности

В вариантах осуществления антитело, специфическое к CD19, включает в себя константный домен легкой цепи последовательности

В вариантах осуществления ингибитор тирозинкиназы Брутона (ВТК) представляет собой ибрутиниб.
В вариантах осуществления компоненты комбинации - антитело, специфическое к CD19, и ибрутиниб - вводят отдельно. В одном варианте осуществления ибрутиниб принимают до введения антитела, специфичного к CD19.
В вариантах осуществления компоненты комбинации вводят в момент времени, когда оба компонента (лекарственные средства) проявляют свое действие в пациенте в одно и то же время. Под «синергизмом» подразумевается, что оба лекарственных средства проявляют свое действие в пациенте в одно и то же время. В вариантах осуществления компоненты комбинации вводят вместе, одновременно, отдельно или последовательно, как физически, так и во времени. В вариантах осуществления компоненты комбинации вводят одновременно.
В вариантах осуществления комбинация представляет собой фармацевтическую композицию. В вариантах осуществления комбинация включает в себя приемлемый носитель. В вариантах осуществления комбинацию вводят в эффективном количестве.
В другом аспекте синергическая комбинация антитела, специфичного к CD19, содержащего участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности  (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности 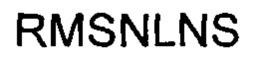 (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6) и ибрутиниба способна опосредовать уничножение клеток МЕС-1 с помощью ADCC в присутствии выделенных человеческих РВМС с действенностью, которая по меньшей мере вдвое, втрое, вчетверо или впятеро лучше действенности одного только ибрутиниба.
(SEQ ID NO: 6) и ибрутиниба способна опосредовать уничножение клеток МЕС-1 с помощью ADCC в присутствии выделенных человеческих РВМС с действенностью, которая по меньшей мере вдвое, втрое, вчетверо или впятеро лучше действенности одного только ибрутиниба.
Один аспект настоящего раскрытия включает в себя синергическую комбинацию антитела, специфичного к CD19, содержащего участок HCDR1 последовательности  (SEQ ID NO: 1), участок HCDR2 последовательности
(SEQ ID NO: 1), участок HCDR2 последовательности  (SEQ ID NO: 2), участок HCDR3 последовательности
(SEQ ID NO: 2), участок HCDR3 последовательности 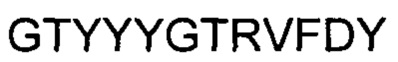 (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности 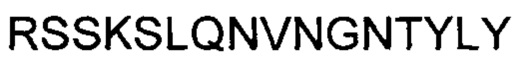 (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности 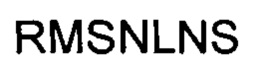 (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6) и ибрутиниб для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. В вариантах осуществления неходжкинскую лимфому выбирают из группы, состоящей из фолликулярной лимфомы, малой лимфоцитарной лимфомы, лимфоидной ткани слизистых оболочек, лимфомы маргинальной зоны, диффузной крупноклеточной В-клеточной лимфомы, лимфомы Беркитта и лимфомы из клеток мантии.
(SEQ ID NO: 6) и ибрутиниб для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза. В вариантах осуществления неходжкинскую лимфому выбирают из группы, состоящей из фолликулярной лимфомы, малой лимфоцитарной лимфомы, лимфоидной ткани слизистых оболочек, лимфомы маргинальной зоны, диффузной крупноклеточной В-клеточной лимфомы, лимфомы Беркитта и лимфомы из клеток мантии.
В вариантах осуществления неходжкинская лимфома представляет собой фолликулярную лимфому. В вариантах осуществления неходжкинская лимфома представляет собой малую лимфоцитарную лимфому. В вариантах осуществления неходжкинская лимфома представляет собой лимфоидную ткань слизистых оболочек. В вариантах осуществления неходжкинская лимфома представляет собой лимфому маргинальной зоны. В вариантах осуществления неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому. В вариантах осуществления неходжкинская лимфома представляет собой лимфому Беркитта. В вариантах осуществления неходжкинская лимфома представляет собой лимфому из клеток мантии.
В вариантах осуществления комбинация предназначена для лечения хронического лимфоцитарного лейкоза. В вариантах осуществления комбинация предназначена для лечения острого лимфобластного лейкоза.
Другой аспект включает в себя способ лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза у лица, нуждающегося в лечении; этот способ включает в себя введение антитела, специфичного к CD19, и ингибитора тирозинкиназы Брутона (ВТК). В вариантах осуществления способа антитело, специфичное к CD19, содержит участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности  (SEQ ID NO: 2), участок HCDR3 последовательности
(SEQ ID NO: 2), участок HCDR3 последовательности 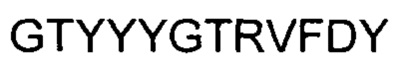 (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности  (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6). В вариантах осуществления способа антитело включает в себя описываемое антитело, специфичное к CD19. В вариантах осуществления способа ингибитор тирозинкиназы Брутона (ВТК) представляет собой ибрутиниб.
(SEQ ID NO: 6). В вариантах осуществления способа антитело включает в себя описываемое антитело, специфичное к CD19. В вариантах осуществления способа ингибитор тирозинкиназы Брутона (ВТК) представляет собой ибрутиниб.
Другой аспект включает в себя применение антитела, специфичного к CD19, где указанное антитело содержит участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности  (SEQ ID NO: 3), участок LCDR1 последовательности
(SEQ ID NO: 3), участок LCDR1 последовательности  (SEQ ID NO: 4), участок LCDR2 последовательности
(SEQ ID NO: 4), участок LCDR2 последовательности 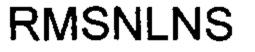 (SEQ ID NO: 5), участок LCDR3 последовательности
(SEQ ID NO: 5), участок LCDR3 последовательности  (SEQ ID NO: 6) в производстве лекарства для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза в виде синергической комбинации с ибрутинибом.
(SEQ ID NO: 6) в производстве лекарства для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза в виде синергической комбинации с ибрутинибом.
Примеры
Пример 1: Цитотоксичность клеток МЕС-1 при использовании MOR00208 и ибрутиниба по отдельности и в комбинации друг с другом
Материалы
Исследуемые клеточные линии: Клетки МЕС-1 (DSMZ №АСС497). Исследуемые клеточные линии: клеточная линия хронического В-клеточного лейкоза; JVM-2 (АТСС® CRL-3002) - клеточная линия лимфомы из клеток мантии; клетки-Ramos (АТСС №CRL-1596), клетки человеческой лимфомы Беркитта; HG-3 (DSMZ № АСС765) и Cll (DSMZ №АСС773) - клеточная линия хронического лимфоцитарного лейкоза; Su-DHL 6 (DSMZ № АСС572), U2932 (DSMZ № АСС633) и OCI-LY7 (DSMZ № АСС688) - клеточная линия диффузной крупноклеточной В-клеточной лимфомы (DLBCL); JVM-2 (АТСС® CRL-3002) - клеточная линия лимфомы из клеток мантии; и BALL-1 (DSMZ № АСС742) - клеточная линия острого лимфобластного лейкоза.
Условия культивирования клеточных линий в соответствии с инструкциями производителя.
Клеточная среда: Iscove's Modified Dulbecco's Medium (IMDM), Invitrogen, Кат. №: 31980-048; RPMI1640, Invitrogen, Кат. №: 31870-074; RPMI1640, GlutaMAX, Invitrogen, Кат. №: 35050-38 Партия №: 1504647; FCS: Sigma Кат. №: F7524 Партия №: 1 1 1M3396.
NK: RPMI1640, с GlutaMAXTM, Invitrogen, Кат. №: 31870-074, 10% FCS; Biocoll: Biochrome AG Кат. №: L6115 Партия №: 0034D; набор MACS NK для выделения клеток: Miltenyi Biotec Кат. №: 130-092-657 Партия №: 51501301 15; Ibrutinib: Selleck Chem Партия №: S2680; FCS: Sigma Кат. №: F7524 Партия №: 1 1 1M3396; и RefmAb33 (анти-RSV) с таким же Fc участком, как и у MOR00208.
Методы
Цитотоксичность MOR00208 и ибрутиниба поодиночке и в комбинации друг с другом исследовали на клеточной линии МЕС-1 (ХЛЛ). Цитотоксичность MOR00208 и ибрутиниба поодиночке и в комбинации друг с другом исследовали на следующих клеточных линиях: JVM-2, Ramos, HG-3, Cll, Su-DHL 6, U2932, OCI-LY7, JVM-2 и BALL-1.
Ибрутиниб представляет собой ковалентный ингибитор тирозинкиназы Брутона, который должен прекращать пролиферацию клеток в целевых клеточных линиях. MOR00208 нацелено на CD19 и способствует гибели клеток-мишеней посредством ADCC. Гибель клеток-мишеней измеряют, используя следующие параметры: Ибрутиниб в интервале концентраций от 0,033 до 33 мкМ, в частности, при 0,3 мкМ, 1,0 мкМ и 3,0 мкМ; MOR00208 в интервале концентраций от 0,001 до 10 нМ, в частности, при 0,01 нМ, 0,1 нМ, и 10 нМ, и комбинация MOR00208 и ибрутиниба. В качестве контролей используется следующее: только клетки RefmAb33 или NK. В группе ибрутиниба, а также в группе комбинации MOR00208 + ибрутиниб клетки-мишени предварительно обрабатывают ибрутинибом в течение 7 дней до проведения аналитических измерений ADCC. Клетки-мишени подсчитывают и окрашивают, используя CFSE в конечной концентрации 1 мкг/мл. В случае клеток-мишеней, обрабатываемых DMSO, выбрано соотношение действующее начало : мишень (Е : Т), равное 2:1, что соответствует плотности клеток, равной 5×105/мл. Воздействие на пролиферацию клеток-мишеней, оказываемое обработкой ибрутинибом, было учтено с помощью подгонки соотношения Е : Т для клеток, обработанных ингибитором. NK клетки подсчитывали и приводили к 1×106/мл. Количественный анализ гибели клеток-мишеней выполняли следующим образом: использовали 96-луночные планшеты, в каждую лунку вносили 100 мкл суспензии клеток-мишеней, а затем в каждую лунку вносили 100 мкл клеточной суспензии NK клеток, получая соотношение Е : Т, равное 2:1. Антитела разбавляли средой до концентрации в пределах 10-0,001 нМ. Клетки центрифугировали и пеллеты из клеток-мишеней:действующего начала повторно суспендировали в 100 мкл среды, содержащей антитело или в соответствующем контрольном растворе. Анализируемые суспензии инкубировали в течение 4 часов в CO2-инкубаторе при 37°С. После 10 мин инкубирования на льду в каждую лунку вносили 50 мкл раствора DAPI (конечная концентрация - 1 мкг/мл) и инкубировали на льду в течение 10 мин. Измерение гибели клеток проводили, используя FACS-Verse. Погибшие клетки-мишени дали положительный результат в отношении DAPI.
Предварительные эксперименты согласно методам, описанным выше, выполняли как на клетках МЕС-1, так и на RAMOS-клетках. На Фигурах 1-3 показаны результаты предварительных экспериментов.
Данные
В целом проводили три эксперимента, чтобы определить влияние на ADCC в клетках МЕС-1 со стороны комбинации MOR00208 и ибрутиниба. Кривые ADCC в зависимости от дозы для экспериментов 1-3 показаны на Фигурах 6-8.
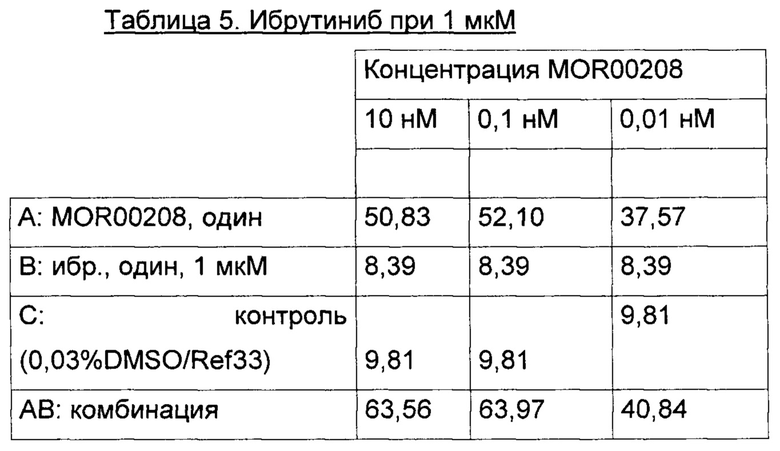
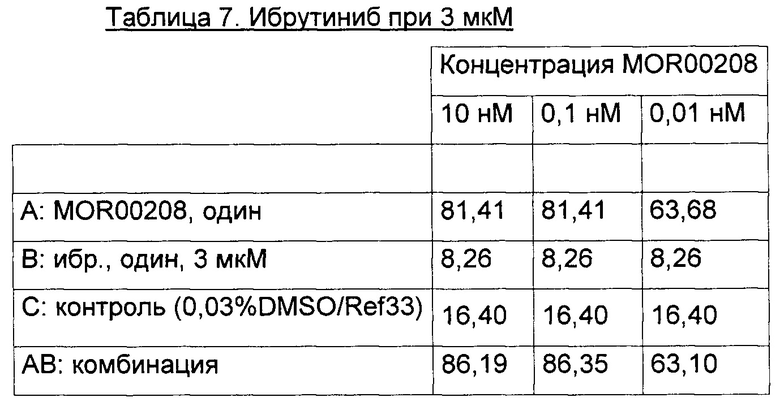
Процент (%) погибших клеток (исходные данные) для экспериментов 1-3 приведены в Таблицах 1-9 ниже.
Эксперимент 1:
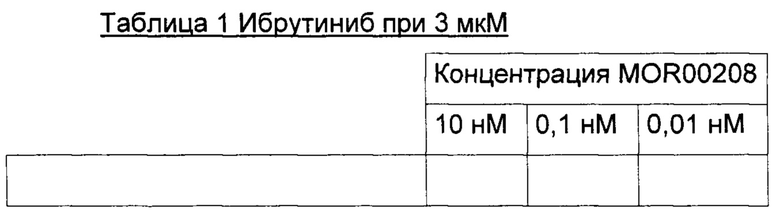

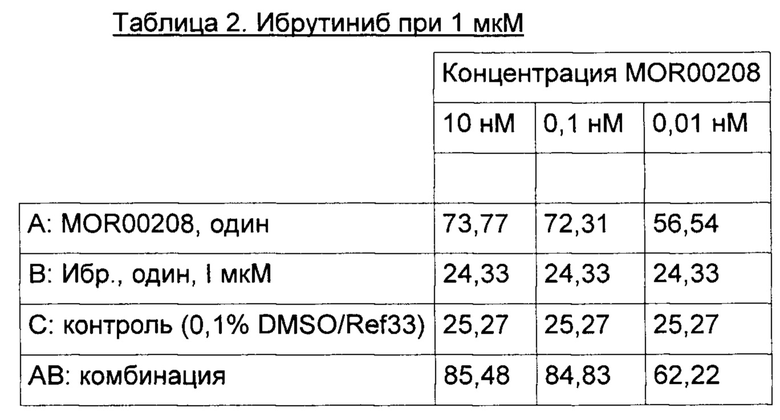
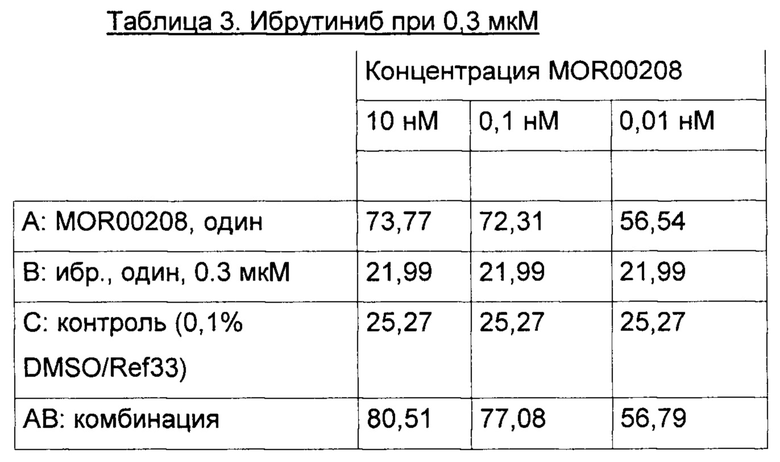
Эксперимент 2:
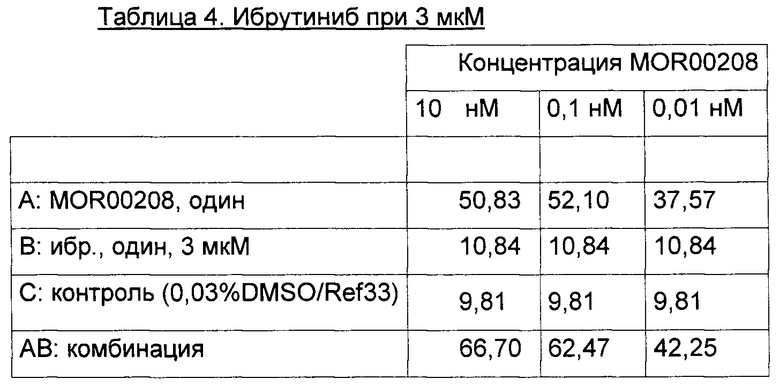
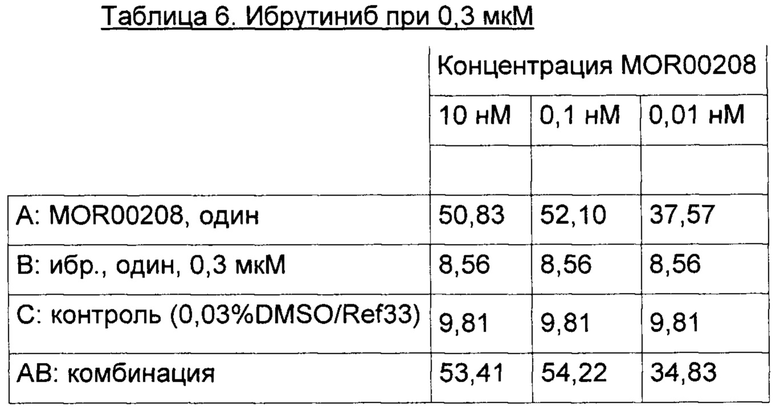
Эксперимент 3:

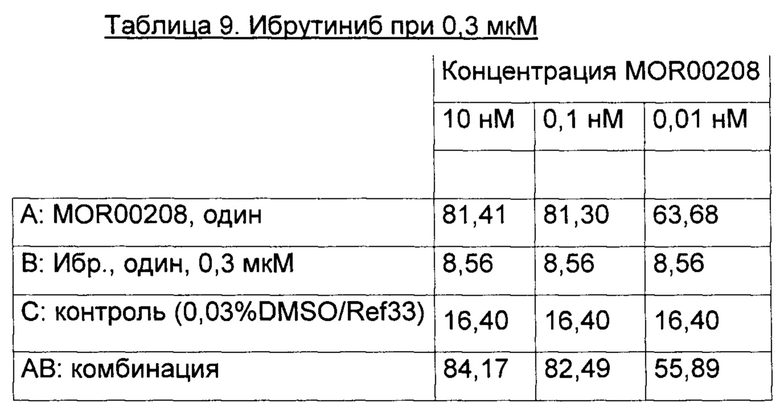
Расчет синергизма
Исходные данные (% мертвых клеток) анализируют следующим образом: 1) из исходных данных (% мертвых клеток), вычитают фон (контроли), что дает специфическое уничтожение для каждой обрабатываемой группы; затем 2) значения для специфического уничтожения нормализуют, принимая значение для комбинации MOR00208+ибрутиниб равным 1.
Расчет показателя аддитивности (CI) выполняют с целью определения синергии комбинации описываемого антитела к CD19 и ибрутиниба в сравнении с одним только MOR00208 и одним только ибрутинибом. Такие вычисления приведены в публикации Ting-Chao Chou, Theoretical Basis, Experimental Design, and Computerized Simulation of Synergism and Antagonism in Drug Combination Studies, Pharmacol Rev 58:621-681 (2006), которая включена в данный документ во всей своей полноте ссылкой, и Chou ТС, Talalay Р, Quantitative analysis of dose-effect relationships: the combined effects of multiple drugs or enzyme inhibitors. Adv Enzyme Regul 22: 27-55 (1984), которая включена в данный документ во всей своей полноте ссылкой. Способы Chou-Talalay выполняют с использованием метода Cl-isobol (метода изоболограмм с показателем аддитивности).
Уравнение средней эффективной дозы
Уравнение средней эффективной дозы дает понятие о действии ингибитора (такого как лекарственное средство) в виде Fa/Fu=(D/D50)^m, где D представляет собой дозу, Fa и Fu представляют собой часть системы, находящуюся под воздействием и не находящуюся под воздействием дозы D (Fa+Fu=1); D50 представляет собой дозу, оказывающую средний эффект (например, IC50, ED50, LD50). Постоянная m определяет форму кривой доза-эффект.
Мы используем GraphPad Prism для выполнения расчета нелинейной регрессии для оценки параметров m и D50.
Метод CI-isobol (метод изоболограмм с показателем аддитивности)
Метод CI-isobol дает количественную оценку синергизма между лекарственными средствами. Показатель аддитивности (CI) устанавливают из данных доза-эффект лечения одним лекарственным средством и комбинированного лечения. Значение CI меньше 1 указывает на синергизм; CI=1 указывает на аддитивный эффект; и CI>1 указывает на несовместимость. Взаимодействие лекарственных средств (синергизм или несовместимость) тем более выражены, чем больше значение CI отличается от 1.
Формально показатель аддитивности (CI) комбинированного лечения лекарственными средствами определяется как
CI=D1/Dx1+D2/Dx2
Здесь D1 и D2 представляют собой дозы лекарственного средства 1 и лекарственного средства 2 в комбинации, соответственно; a Dx1, и Dx2 - это дозы при лечении только одним лекарственным средством 1 и лекарственным средством 2, которые дадут такой же эффект, что и комбинация. Дозы Dx1 и Dx2 нужно оценивать по данным доза-эффект лечения одним лекарственным средством. По существу, уравнение средней эффективной дозы подгоняется к данным каждого лекарственного средства. Из уравнения средней эффективной дозы лекарственного средства мы можем установить дозу (т.е. D), необходимую для получения эффекта (воздействия) (т.е. Fa, Fu). Чем дальше лежит точка от аддитивной линии, чем больше разница между 1 и ее Cl, тем сильнее ее эффект (синергизм или несовместимость).
Результаты
Кривые показателя Chou показаны на Фигурах 9-11. Данные трех экспериментов (при одинаковых концентрациях) объединяли для получения одной кривой для каждой концентрации ибрутиниба.
Значения индекса Chou однозначно указывают на синергизм комбинации MOR00208 и ибрутиниба для специфического уничтожения клеток МЕС-1 по сравнению с одним только MOR00208 и только одним ибрутинибом.
Следовательно, комбинация MOR00208 и ибрутиниба также будет проявлять синергизм при лечении неходжкинской лимфомы (НХЛ), хронического лимфоидного лейкоза (ХЛЛ) и острого лимфобластного лейкоза (ОЛЛ) у людей.
Дополнительные анализы
Другой подход к расчету и сравнению воздействий от агентов поодиночке с тем, когда они применяются в комбинации - это концепция дробного продукта, впервые описанная автором Webb JL. в "Enzymes and metabolic inhibitors" в 1963 г. В этом методе анализа учитывается, что эффект от нескольких лекарственных средств может быть направлен против одной и той же части клеток при условии, что эти эффекты не являются взаимоисключающими, что приложимо к MOR00208 и ибрутинибу, и поэтому измеряемый комбинированный эффект будет меньше, чем теоретическая сумма одиночных эффектов. Концепция дробного продукта утверждает, что когда два лекарственных средства убивают 50%-ную часть клеток-мишеней, эффект в комбинации будет только 75% (применяемое уравнение: 1-(1-0,5)×(1-0,5)=0,75), а не ожидаемые 100%, поскольку только 50% клеток-мишеней по-прежнему остаются жизнеспособными и восприимчивы к одному из двух лекарственных средств.
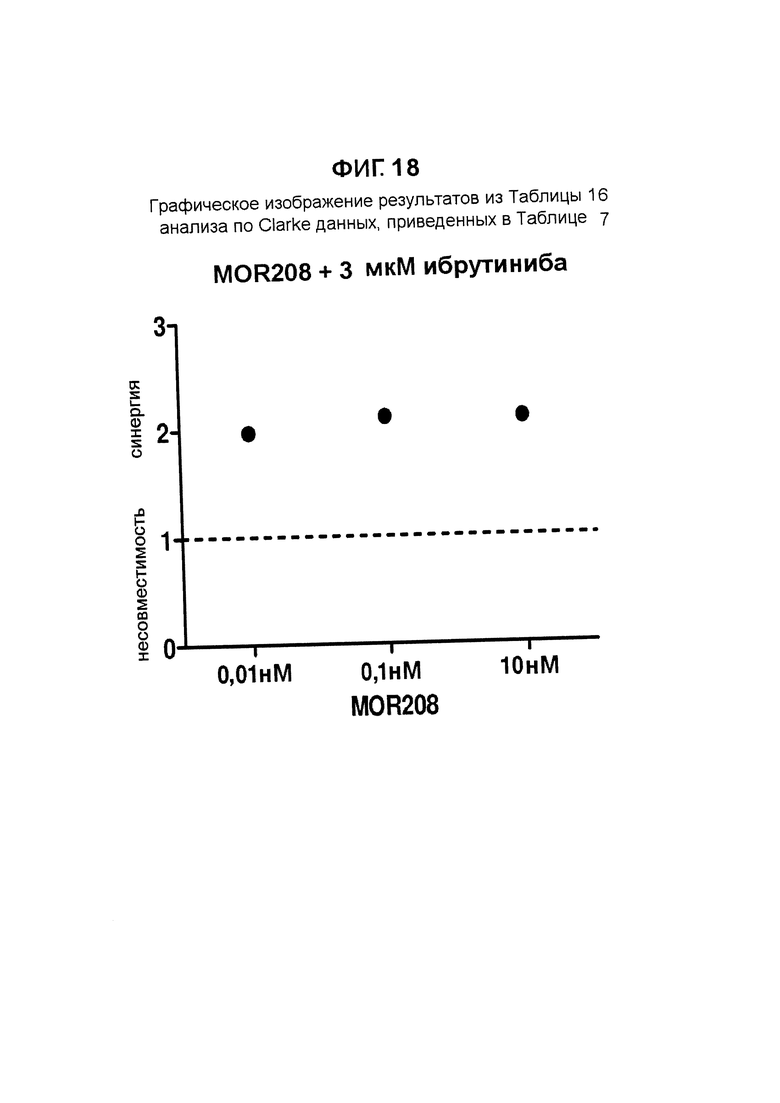
Другой подход к расчету и сравнению воздействий от агентов поодиночке с тем, когда они применяются в комбинации - это подход, описанный у Clarke et al., Issues in experimental design and endpoint analysis in the study of experimental cytotoxic agents in vivo in breast cancer and other models, Breast Cancer Research and Treatment 46:255-278 (1997), которая включена в данный документ во всей своей полноте ссылкой.
% мертвых клеток (исходные данные) из Таблицы 1-16 анализировали следующим образом:
Несовместимые (АВ)/С<(А/С)×(В/С)
Аддитивные (АВ)/С=(А/С)×(В/С)
Синергичные (АВ)/С>(А/С)×(В/С)
где А - обработка одним MOR00208; В - обработка одним ибрутинибом; С - ответ контролей на DMSO + RefMab33; АВ - комбинированная обработка с А и В.
Эксперимент 1
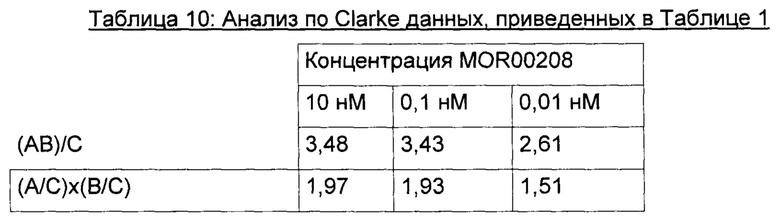
Результат данного анализа по Clarke данных, приведенных в Таблице 1, также представлен графически на Фигуре 12.
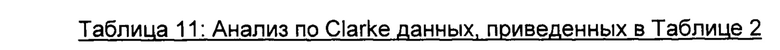

Результат данного анализа по Clarke данных, приведенных в Таблице 2, также представлен графически на Фигуре 13.
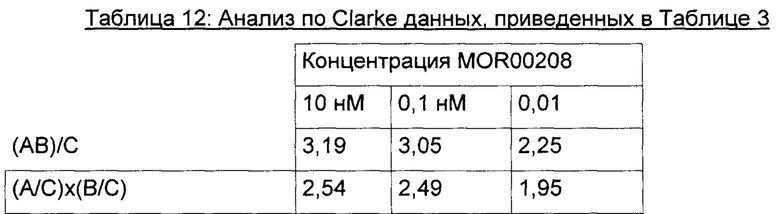
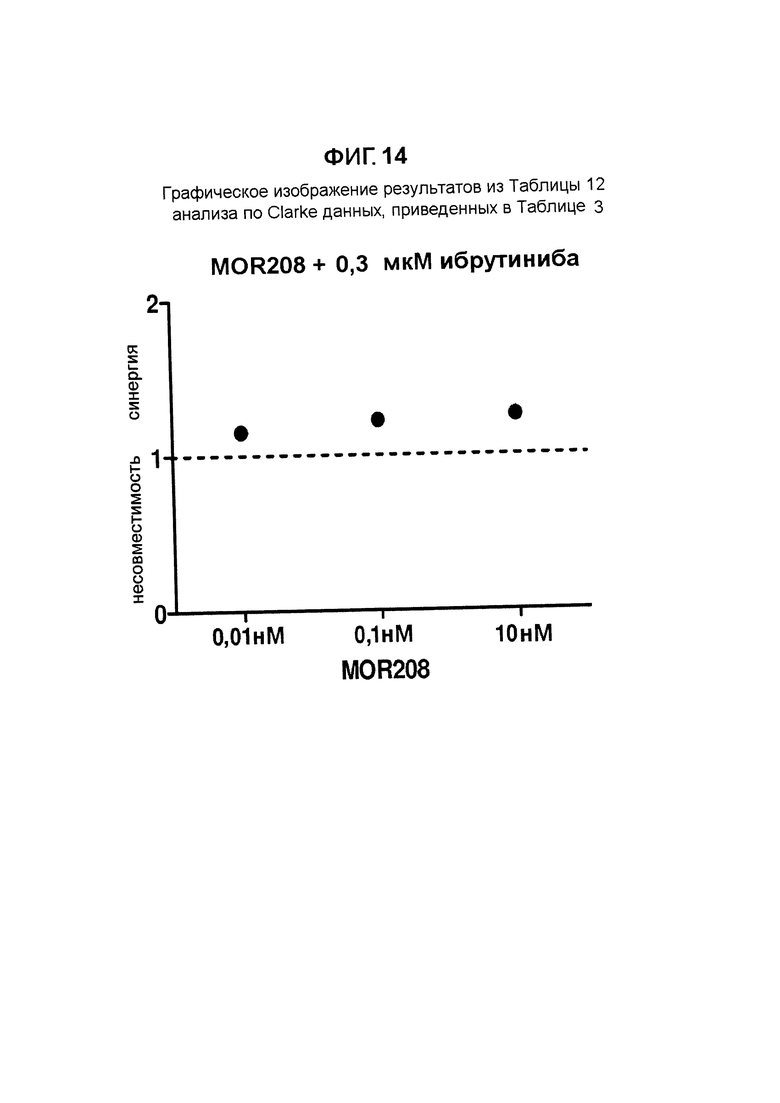
Результат данного анализа по Clarke данных, приведенных в Таблице 3, также представлен графически на Фигуре 14.
Эксперимент 2
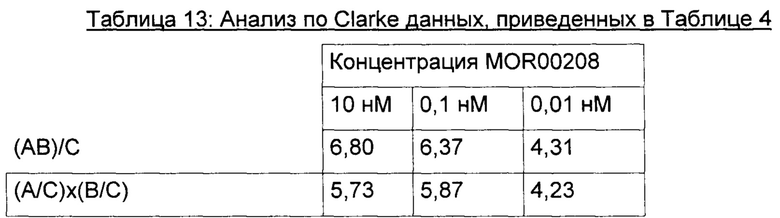
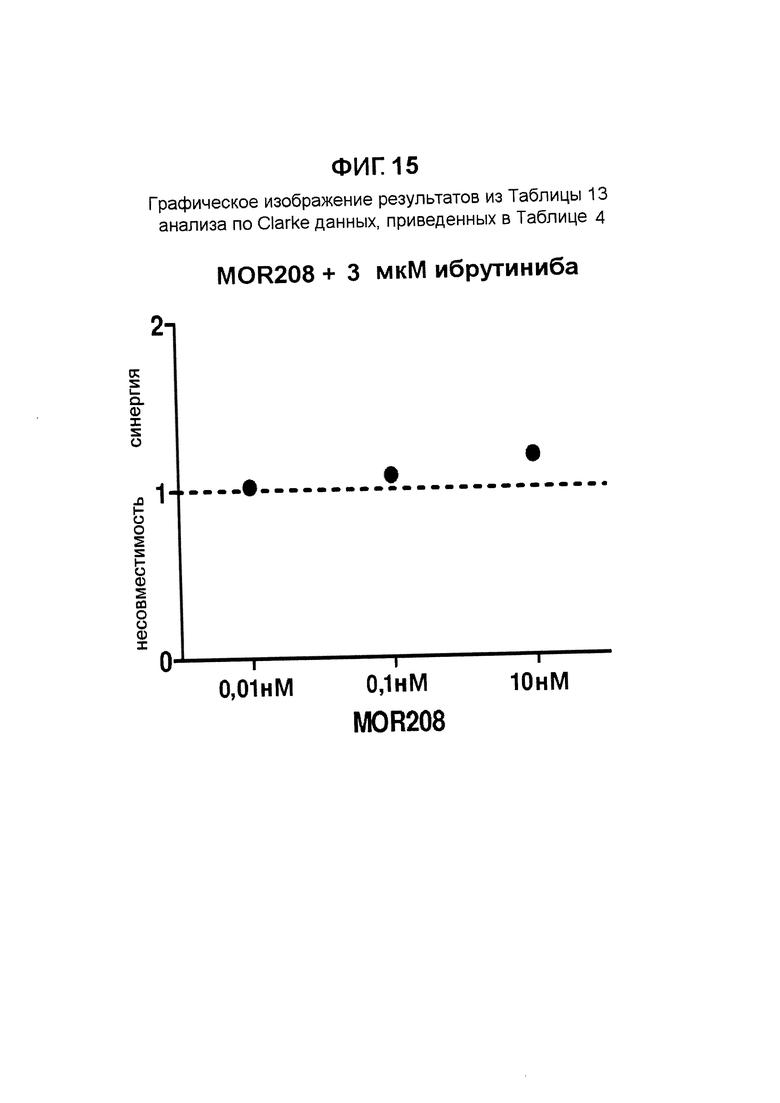
Результат данного анализа по Clarke данных, приведенных в Таблице 4, также представлен графически на Фигуре 15.
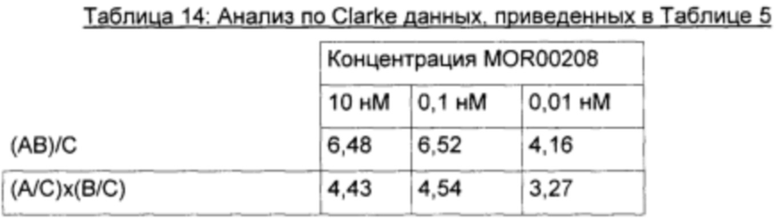
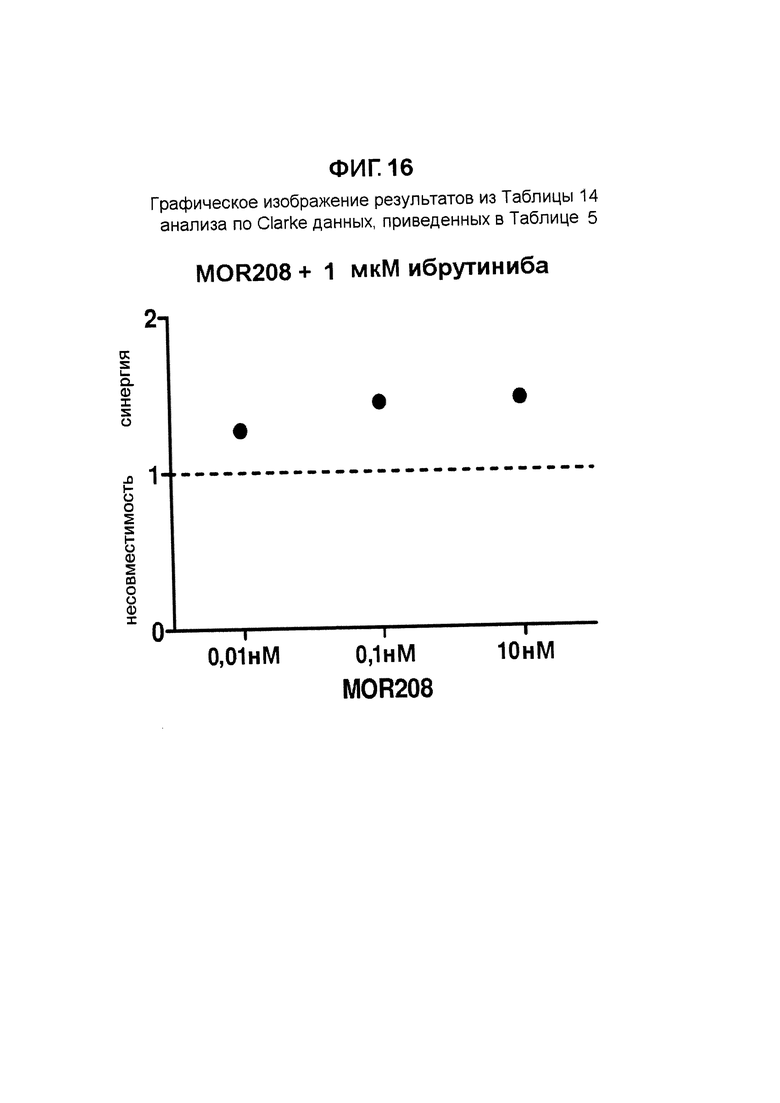
Результат данного анализа по Clarke данных, приведенных в Таблице 5, также представлен графически на Фигуре 16.
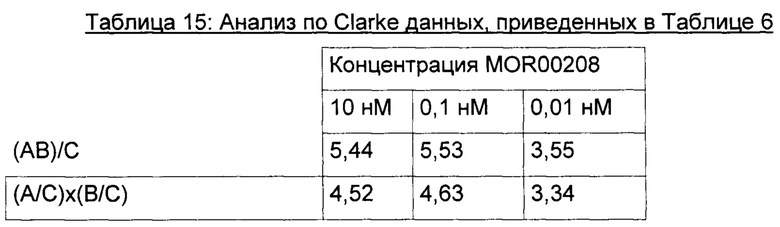
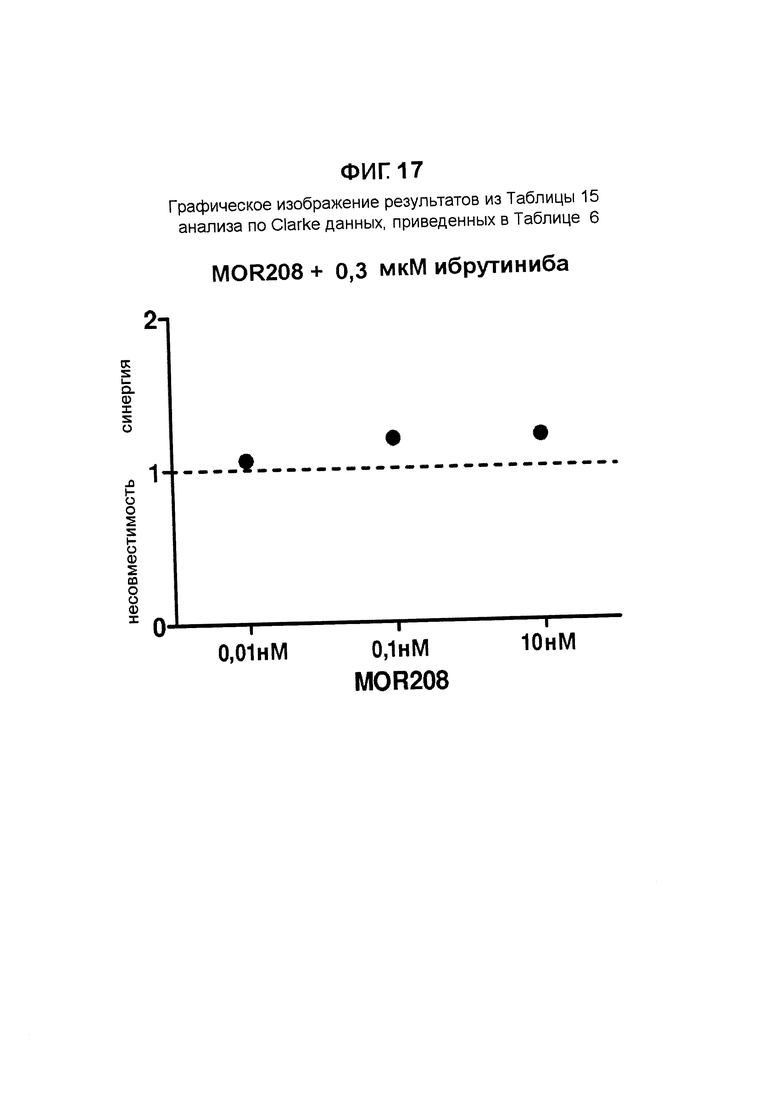
Результат данного анализа по Clarke данных, приведенных в Таблице 6, также представлен графически на Фигуре 17.
Эксперимент 3
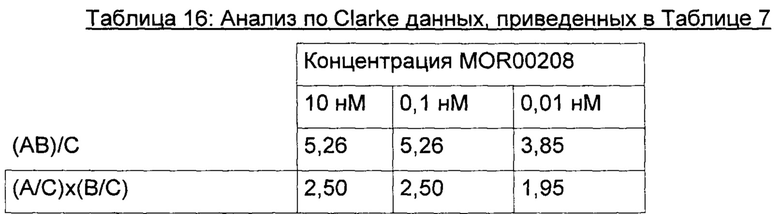
Результат данного анализа по Clarke данных, приведенных в Таблице 7, также представлен графически на Фигуре 18.
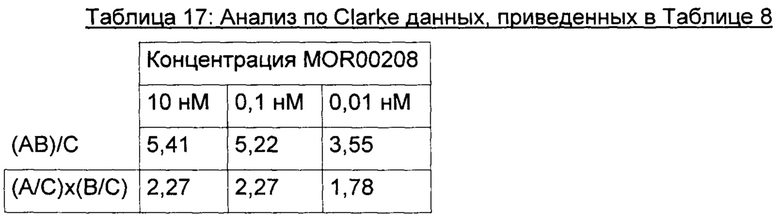
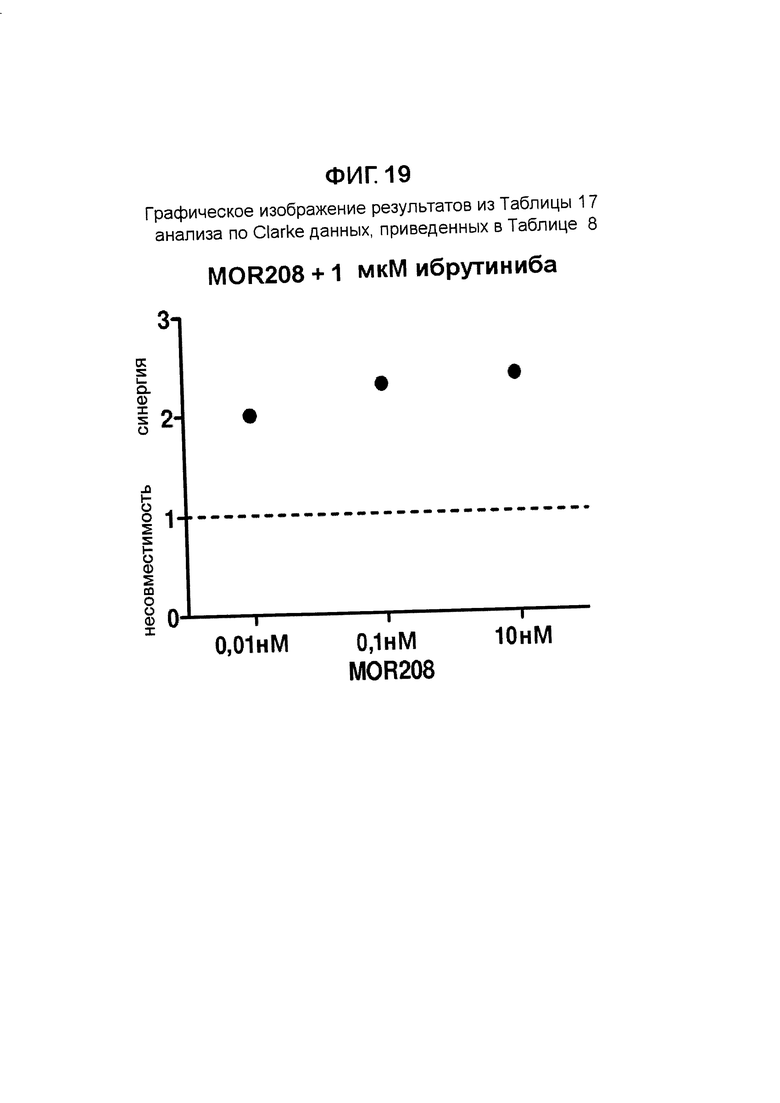
Результат данного анализа по Clarke данных, приведенных в Таблице 8, также представлен графически на Фигуре 19.

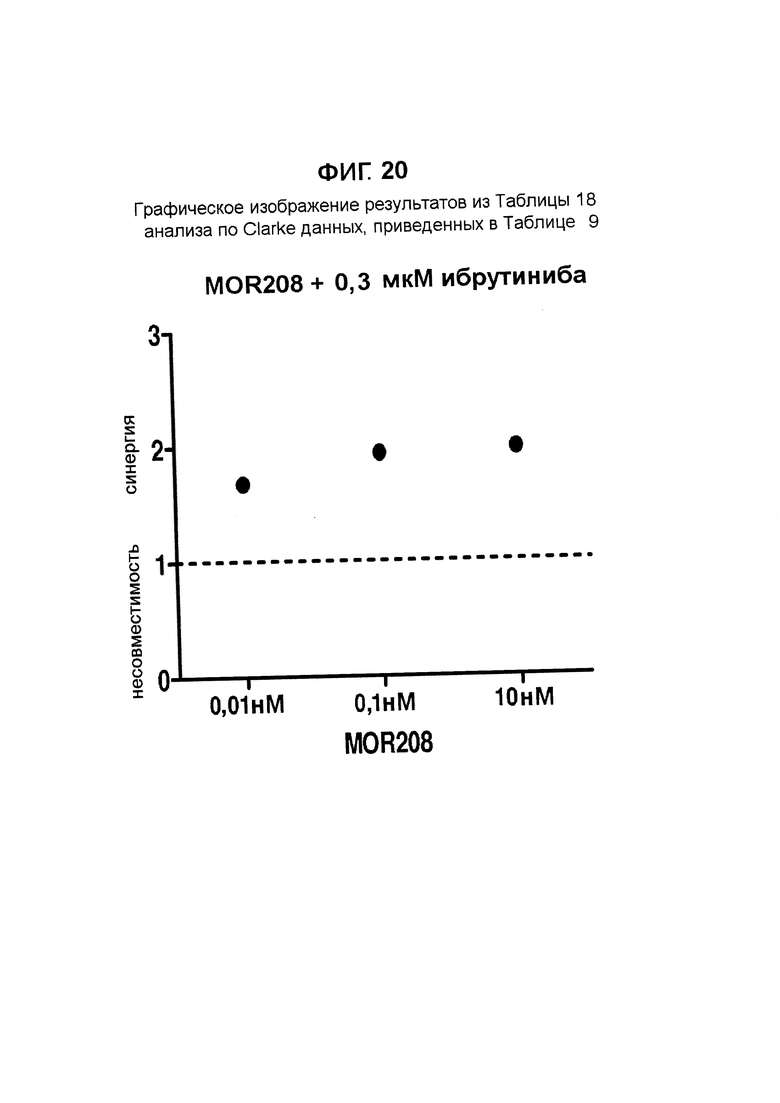
Результат данного анализа по Clarke данных, приведенных в Таблице 9, также представлен графически на Фигуре 20.
Результаты анализа по Clarke
Эксперименты 1-3 при каждой концентрации продемонстрировали явную синергию комбинации MOR00208+ибрутиниб при использовании методов по Clarke et al. Методы по Clarke et al., однако, демонстрируют синергизм несмотря на небольшое число экспериментов, где активность ибрутиниба была ниже, чем в контрольном эксперименте.
Следует понимать, что описание, конкретные примеры и данные с указанием примерных вариантов осуществления приведены в качестве иллюстрации и не предназначены для ограничения настоящего изобретения. Различные изменения и модификации в соответствии с настоящим изобретением станут очевидными для специалиста в данной области техники из обсуждения, раскрытия и данных, содержащихся в настоящем документе, и поэтому рассматриваются как часть изобретения.
--->
SEQUENCE LISTING
<110> MorphoSys AG
<120> Combinations and uses thereof
<130> MS230
<150> EP15196860.9
<151> 2015-11-27
<150> EP15169124.3
<151> 2015-05-26
<160> 15
<170> BiSSAP 1.0
<210> 1
<211> 5
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 1
Ser Tyr Val Met His
1 5
<210> 2
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 2
Asn Pro Tyr Asn Asp Gly
1 5
<210> 3
<211> 12
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 3
Gly Thr Tyr Tyr Tyr Gly Thr Arg Val Phe Asp Tyr
1 5 10
<210> 4
<211> 16
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 4
Arg Ser Ser Lys Ser Leu Gln Asn Val Asn Gly Asn Thr Tyr Leu Tyr
1 5 10 15
<210> 5
<211> 7
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 5
Arg Met Ser Asn Leu Asn Ser
1 5
<210> 6
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 6
Met Gln His Leu Glu Tyr Pro Ile Thr
1 5
<210> 7
<211> 556
<212> PRT
<213> Homo sapiens
<220>
<223> CD19
<400> 7
Met Pro Pro Pro Arg Leu Leu Phe Phe Leu Leu Phe Leu Thr Pro Met
1 5 10 15
Glu Val Arg Pro Glu Glu Pro Leu Val Val Lys Val Glu Glu Gly Asp
20 25 30
Asn Ala Val Leu Gln Cys Leu Lys Gly Thr Ser Asp Gly Pro Thr Gln
35 40 45
Gln Leu Thr Trp Ser Arg Glu Ser Pro Leu Lys Pro Phe Leu Lys Leu
50 55 60
Ser Leu Gly Leu Pro Gly Leu Gly Ile His Met Arg Pro Leu Ala Ile
65 70 75 80
Trp Leu Phe Ile Phe Asn Val Ser Gln Gln Met Gly Gly Phe Tyr Leu
85 90 95
Cys Gln Pro Gly Pro Pro Ser Glu Lys Ala Trp Gln Pro Gly Trp Thr
100 105 110
Val Asn Val Glu Gly Ser Gly Glu Leu Phe Arg Trp Asn Val Ser Asp
115 120 125
Leu Gly Gly Leu Gly Cys Gly Leu Lys Asn Arg Ser Ser Glu Gly Pro
130 135 140
Ser Ser Pro Ser Gly Lys Leu Met Ser Pro Lys Leu Tyr Val Trp Ala
145 150 155 160
Lys Asp Arg Pro Glu Ile Trp Glu Gly Glu Pro Pro Cys Leu Pro Pro
165 170 175
Arg Asp Ser Leu Asn Gln Ser Leu Ser Gln Asp Leu Thr Met Ala Pro
180 185 190
Gly Ser Thr Leu Trp Leu Ser Cys Gly Val Pro Pro Asp Ser Val Ser
195 200 205
Arg Gly Pro Leu Ser Trp Thr His Val His Pro Lys Gly Pro Lys Ser
210 215 220
Leu Leu Ser Leu Glu Leu Lys Asp Asp Arg Pro Ala Arg Asp Met Trp
225 230 235 240
Val Met Glu Thr Gly Leu Leu Leu Pro Arg Ala Thr Ala Gln Asp Ala
245 250 255
Gly Lys Tyr Tyr Cys His Arg Gly Asn Leu Thr Met Ser Phe His Leu
260 265 270
Glu Ile Thr Ala Arg Pro Val Leu Trp His Trp Leu Leu Arg Thr Gly
275 280 285
Gly Trp Lys Val Ser Ala Val Thr Leu Ala Tyr Leu Ile Phe Cys Leu
290 295 300
Cys Ser Leu Val Gly Ile Leu His Leu Gln Arg Ala Leu Val Leu Arg
305 310 315 320
Arg Lys Arg Lys Arg Met Thr Asp Pro Thr Arg Arg Phe Phe Lys Val
325 330 335
Thr Pro Pro Pro Gly Ser Gly Pro Gln Asn Gln Tyr Gly Asn Val Leu
340 345 350
Ser Leu Pro Thr Pro Thr Ser Gly Leu Gly Arg Ala Gln Arg Trp Ala
355 360 365
Ala Gly Leu Gly Gly Thr Ala Pro Ser Tyr Gly Asn Pro Ser Ser Asp
370 375 380
Val Gln Ala Asp Gly Ala Leu Gly Ser Arg Ser Pro Pro Gly Val Gly
385 390 395 400
Pro Glu Glu Glu Glu Gly Glu Gly Tyr Glu Glu Pro Asp Ser Glu Glu
405 410 415
Asp Ser Glu Phe Tyr Glu Asn Asp Ser Asn Leu Gly Gln Asp Gln Leu
420 425 430
Ser Gln Asp Gly Ser Gly Tyr Glu Asn Pro Glu Asp Glu Pro Leu Gly
435 440 445
Pro Glu Asp Glu Asp Ser Phe Ser Asn Ala Glu Ser Tyr Glu Asn Glu
450 455 460
Asp Glu Glu Leu Thr Gln Pro Val Ala Arg Thr Met Asp Phe Leu Ser
465 470 475 480
Pro His Gly Ser Ala Trp Asp Pro Ser Arg Glu Ala Thr Ser Leu Gly
485 490 495
Ser Gln Ser Tyr Glu Asp Met Arg Gly Ile Leu Tyr Ala Ala Pro Gln
500 505 510
Leu Arg Ser Ile Arg Gly Gln Pro Gly Pro Asn His Glu Glu Asp Ala
515 520 525
Asp Ser Tyr Glu Asn Met Asp Asn Pro Asp Gly Pro Asp Pro Ala Trp
530 535 540
Gly Gly Gly Gly Arg Met Gly Thr Trp Ser Thr Arg
545 550 555
<210> 8
<211> 450
<212> PRT
<213> Artificial sequence
<220>
<223> Heavy chain RefMab33
<400> 8
Gln Val Thr Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Met Ser Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Asp Ile Trp Trp Asp Asp Lys Lys His Tyr Asn Pro Ser
50 55 60
Leu Lys Asp Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Val Leu Lys Val Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Asp Met Ile Phe Asn Phe Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Asp Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg
290 295 300
Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Glu Glu
325 330 335
Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 9
<211> 213
<212> PRT
<213> Artificial sequence
<220>
<223> Light chain RefMab33
<400> 9
Asp Ile Gln Met Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ser Ala Ser Ser Arg Val Gly Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
65 70 75 80
Asp Phe Ala Thr Tyr Tyr Cys Phe Gln Gly Ser Gly Tyr Pro Phe Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 10
<211> 121
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 10
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Ser Ser Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Tyr Tyr Gly Thr Arg Val Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 11
<211> 112
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 11
Asp Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ser Ser Lys Ser Leu Gln Asn Val
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Gln Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Asn Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Ile Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 12
<211> 330
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Asp Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Glu Glu Lys Thr Ile Ser Lys Thr Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
225 230 235 240
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 13
<211> 107
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 13
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 14
<211> 451
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 14
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Lys Tyr Asn Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Ser Ser Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr Tyr Tyr Tyr Gly Thr Arg Val Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Asp Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe
290 295 300
Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Glu
325 330 335
Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro Gly Lys
450
<210> 15
<211> 219
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic construct
<400> 15
Asp Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ser Ser Lys Ser Leu Gln Asn Val
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Gln Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Asn Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Ile Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Комбинация антитела CD19 с ингибитором BCL-2 и пути ее применения | 2017 |
|
RU2756405C2 |
| Лечебный подход, предназначенный для лечения комбинацией антитела к CD19 и венетоклакса | 2018 |
|
RU2802812C2 |
| Комбинации и их использование | 2016 |
|
RU2767063C2 |
| БЕЛОК, СВЯЗЫВАЮЩИЙСЯ С NKG2D, CD16 И С ОПУХОЛЕСПЕЦИФИЧЕСКИМ АНТИГЕНОМ | 2018 |
|
RU2826991C2 |
| Составы на основе антитела к CD19 | 2017 |
|
RU2748024C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО РЕЦЕПТОРА АНТИГЕНА ПРОТИВ CD19 | 2015 |
|
RU2815417C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ВВЕДЕНИЯ ДОЗ АЛЛОГЕННЫХ T-КЛЕТОК С ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ | 2018 |
|
RU2776322C2 |
| АНТИТЕЛО ПРОТИВ CD79B, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2817143C2 |
| КЛЕТКА | 2015 |
|
RU2768019C2 |


Настоящее изобретение относится к области иммунологии. Предложено применение синергической комбинации антитела к CD19 и ибрутиниба. Кроме того, рассмотрен способ лечения. Данное изобретение может найти дальнейшее применение в терапии неходжкинской лимфомы, хронического лимфоцитарного лейкоза и острого лимфобластного лейкоза, экспрессирующих CD19. 2 н. и 34 з.п. ф-лы, 20 ил., 18 табл., 1 пр.
1. Применение синергической комбинации, включающей в себя антитело, специфичное к CD19, где указанное антитело содержит участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности GTYYYGTRVFDY (SEQ ID NO: 3), участок LCDR1 последовательности RSSKSLQNVNGNTYLY (SEQ ID NO: 4), участок LCDR2 последовательности RMSNLNS (SEQ ID NO: 5) и участок LCDR3 последовательности MQHLEYPIT (SEQ ID NO: 6), и ибрутиниб, для лечения неходжкинской лимфомы, хронического лимфоцитарного лейкоза и/или острого лимфобластного лейкоза, экспрессирующих CD19.
2. Применение согласно п. 1, где антитело содержит вариабельную тяжелую цепь последовательности EVQLVESGGGLVKPGGSLKLSCAASGYTFTSYVMHWVRQAPGKGLEWIGYINPYNDGTKYNEKFQGRVTISSDKSISTAYMELSSLRSEDTAMYYCARGTYYYGTRVFDYWGQGTLVTVSS (SEQ ID NO: 10) и вариабельную легкую цепь последовательности DIVMTQSPATLSLSPGERATLSCRSSKSLQNVNGNTYLYWFQQKPGQSPQLLIYRMSNLNSGVPDRFSGSGSGTEFTLTISSLEPEDFAVYYCMQHLEYPITFGAGTKLEIK (SEQ ID NO: 11).
3. Применение согласно п. 1 или 2, где антитело содержит константный домен тяжелой цепи последовательности ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPDVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKALPAPEEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 12).
4. Применение согласно любому одному из предыдущих пунктов, где антитело содержит константный домен легкой цепи последовательности RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC. (SEQ ID NO: 13).
5. Применение согласно любому одному из предыдущих пунктов, где указанное антитело, специфичное к CD19, и ибрутиниб вводят отдельно.
6. Применение согласно любому одному из предыдущих пунктов, где ибрутиниб вводят до введения антитела, специфичного к CD19.
7. Применение согласно любому одному из пп. 1-5, где указанное антитело, специфичное к CD19, и ибрутиниб вводят одновременно.
8. Применение согласно любому одному из предыдущих пунктов, где указанное антитело, специфичное к CD19, и ибрутиниб вводят в момент времени, когда оба лекарственные средства проявляют свое действие в пациенте в одно и то же время.
9. Применение согласно любому одному из предыдущих пунктов для лечения хронического лимфоцитарного лейкоза.
10. Применение согласно любому одному из пп. 1-8 для лечения острого лимфобластного лейкоза.
11. Применение согласно любому одному из пп. 1-8 для лечения неходжкинской лимфомы.
12. Применение согласно п. 11, где неходжкинская лимфома представляет собой фолликулярную лимфому.
13. Применение согласно п. 11, где неходжкинская лимфома представляет собой малую лимфоцитарную лимфому.
14. Применение согласно п. 11, где неходжкинская лимфома представляет собой лимфоидную ткань слизистых оболочек.
15. Применение согласно п. 11, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому.
16. Применение согласно п. 11, где неходжкинская лимфома представляет собой лимфому Беркитта.
17. Применение согласно п. 11, где неходжкинская лимфома представляет собой лимфому из клеток мантии.
18. Применение согласно п. 11, где неходжкинская лимфома представляет собой лимфому маргинальной зоны.
19. Способ лечения заболевания, выбранного из группы, состоящей из неходжкинской лимфомы, хронического лимфоцитарного лейкоза и острого лимфобластного лейкоза, экспрессирующих CD19, у лица, нуждающегося в лечении, включающий в себя введение терапевтически эффективного количества антитела, специфичного к CD19, где указанное антитело содержит участок HCDR1 последовательности SYVMH (SEQ ID NO: 1), участок HCDR2 последовательности NPYNDG (SEQ ID NO: 2), участок HCDR3 последовательности GTYYYGTRVFDY (SEQ ID NO: 3), участок LCDR1 последовательности RSSKSLQNVNGNTYLY (SEQ ID NO: 4), участок LCDR2 последовательности RMSNLNS (SEQ ID NO: 5) и участок LCDR3 последовательности MQHLEYPIT (SEQ ID NO: 6), и терапевтически эффективного количества ибрутиниба.
20. Способ согласно п. 19, где антитело содержит вариабельную тяжелую цепь последовательности EVQLVESGGGLVKPGGSLKLSCAASGYTFTSYVMHWVRQAPGKGLEWIGYINPYNDGTKYNEKFQGRVTISSDKSISTAYMELSSLRSEDTAMYYCARGTYYYGTRVFDYWGQGTLVTVSS (SEQ ID NO: 10) и вариабельную легкую цепь последовательности DIVMTQSPATLSLSPGERATLSCRSSKSLQNVNGNTYLYWFQQKPGQSPQLLIYRMSNLNSGVPDRFSGSGSGTEFTLTISSLEPEDFAVYYCMQHLEYPITFGAGTKLEIK (SEQ ID NO: 11).
21. Способ согласно п. 19 или 20, где антитело содержит константный домен тяжелой цепи последовательности ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPDVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKALPAPEEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 12).
22. Способ согласно любому одному из пп. 19-21, где антитело содержит константный домен легкой цепи последовательности RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC. (SEQ ID NO: 13).
23. Способ согласно любому одному из пп. 19-22, где указанное антитело, специфичное к CD19, и ибрутиниб вводят отдельно.
24. Способ согласно любому одному из пп. 19-23, где ибрутиниб вводят до введения антитела, специфичного к CD19.
25. Способ согласно любому одному из пп. 19-22, где указанное антитело, специфичное к CD19, и ибрутиниб вводят одновременно.
26. Способ согласно любому одному из пп. 19-25, где указанное антитело, специфичное к CD19, и ибрутиниб вводят в момент времени, когда оба лекарственные средства проявляют свое действие в пациенте в одно и то же время.
27. Способ согласно любому одному из пп. 19-26, где заболевание представляет собой хронический лимфоцитарный лейкоз.
28. Способ согласно любому одному из пп. 19-26, где заболевание представляет собой острый лимфобластный лейкоз.
29. Способ согласно любому одному из пп. 19-26, где заболевание представляет собой неходжкинскую лимфому.
30. Способ согласно п. 29, где неходжкинская лимфома представляет собой фолликулярную лимфому.
31. Способ согласно п. 29, где неходжкинская лимфома представляет собой малую лимфоцитарную лимфому.
32. Способ согласно п. 29, где неходжкинская лимфома представляет собой лимфоидную ткань слизистых оболочек.
33. Способ согласно п. 29, где неходжкинская лимфома представляет собой диффузную крупноклеточную В-клеточную лимфому.
34. Способ согласно п. 29, где неходжкинская лимфома представляет собой лимфому Беркитта.
35. Способ согласно п. 29, где неходжкинская лимфома представляет собой лимфому из клеток мантии.
36. Способ согласно п. 29, где неходжкинская лимфома представляет собой лимфому маргинальной зоны.
| HORTON H.M | |||
| et al | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Способ получения смеси хлоргидратов опийных алкалоидов (пантопона) из опийных вытяжек с любым содержанием морфия | 1921 |
|
SU68A1 |
| Приспособление к токарному или т.п. станку для нарезания зубчатых колес и других работ | 1927 |
|
SU8049A1 |
| WOYACH J.A | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2021-09-24—Публикация
2016-05-25—Подача