ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области техники по обработке медицинских снимков, в частности, к способу и системе идентификации границ печени.
УРОВЕНЬ ТЕХНИКИ
В медицинской практике часто требуется идентификация границ ткани печени по современным медицинским снимкам, включая ультразвуковую визуализацию, магнитно-резонансную томографию (МРТ визуализация), компьютерную томографию (КТ) и т.д., для локализации области исследования печени, например, для исследования эластичности печени, и цветную Допплеровскую ультразвуковую сонографию печени.
В настоящее время границы ткани печени в основном определяются вручную. Однако выбор границ печени вручную в соответствии с информацией о ткани печени требует, чтобы оператор был очень хорошо знаком со структурой ткани печени и визуальной информацией, чтобы можно было точно выбрать границу ткани печени, что требует от оператора максимальных усилий. В то же время относительно длительное время определения границ печени вручную может привести к низкой эффективности диагностики.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является предложение способа и системы для идентификации границ печени для увеличения эффективности определения границ печени.
В одном из аспектов настоящее изобретение предлагает способ идентификации границ печени, содержащий:
получение информации о ткани печени для идентифицируемой ткани печени;
идентификацию границы ткани печени в информации о ткани печени по характерным свойствам ткани печени, соответствующим информации о ткани печени, и характерным свойствам границы ткани печени в соответствии с информацией о ткани печени при помощи технологии обработки изображений или технологии обработки сигналов; и
вывод информации о местоположении идентифицированной границы ткани печени.
В другом аспекте настоящее изобретение предлагает систему идентификации границы печени, содержащую устройство получения информации, устройство идентификации границы печени и устройство отображения границы печени, где устройство получения информации сконфигурировано для получения информации о ткани печени для идентифицируемой ткани печени; устройство идентификации границы печени сконфигурировано для идентификации границы ткани печени в информации о ткани печени по характерным свойствам ткани печени, соответствующим информации о ткани печени, и характерным свойствам границы ткани печени, соответствующим информации о ткани печени, при помощи технологии обработки изображений или технологии обработки сигналов; а устройство отображения границы печени сконфигурировано для вывода информации о местоположении идентифицированной границы ткани печени.
Способ и система идентификации границ печени, представленные в вариантах осуществления настоящего изобретения, могут эффективно определить область границы. Согласно способу идентификации границы печени, представленному в вариантах осуществления настоящего изобретения, получают информацию о ткани печени для идентифицируемой ткани, а затем применяется технология обработки изображений или технология обработки сигнала для идентификации границы ткани печени по характерным свойствам сигнала ткани печени и ее границы. За счет использования описанного способа граница ткани печени может быть идентифицирована автоматически, и может быть увеличена эффективность идентификации границы ткани печени.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры, описанные здесь, предназначены для обеспечения дальнейшего понимания вариантов осуществления настоящего изобретения и, скорее, представляют собой часть, а не ограничение, вариантов осуществления настоящего изобретения. На фигурах:
на ФИГ. 1 показана блок-схема для реализации способа идентификации границы печени в первом варианте осуществления настоящего изобретения;
на ФИГ. 2 показана блок-схема для реализации способа идентификации границы печени во втором варианте осуществления настоящего изобретения;
на ФИГ. 3 показано схематичное изображение, иллюстрирующее результат идентификации границы ткани печени на основе ультразвукового сигнала М-типа во втором варианте осуществления настоящего изобретения;
на ФИГ. 4 показана блок-схема для реализации способа идентификации границы печени в третьем варианте осуществления настоящего изобретения;
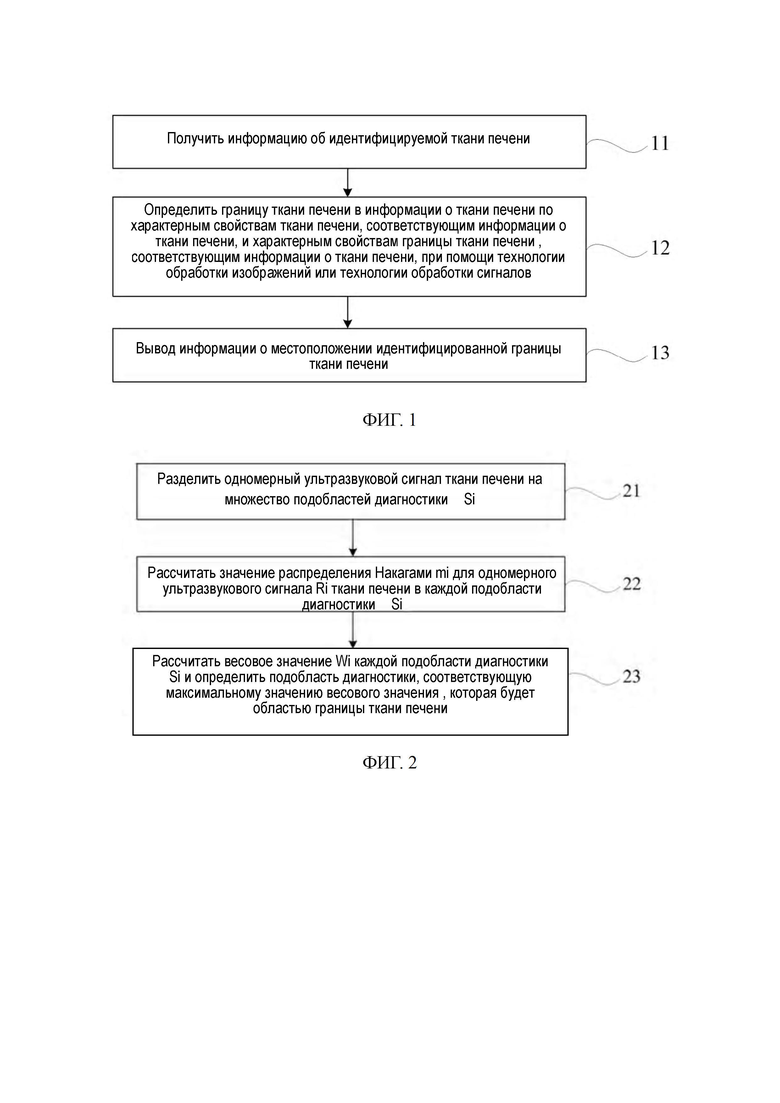
на ФИГ. 5 показано схематичное изображение, иллюстрирующее результат идентификации границы на основе ультразвукового изображения B-типа ткани печени в третьем варианте осуществления настоящего изобретения;
на ФИГ. 6 показана блок-схема реализации способа идентификации границы печени в четвертом варианте осуществления настоящего изобретения;
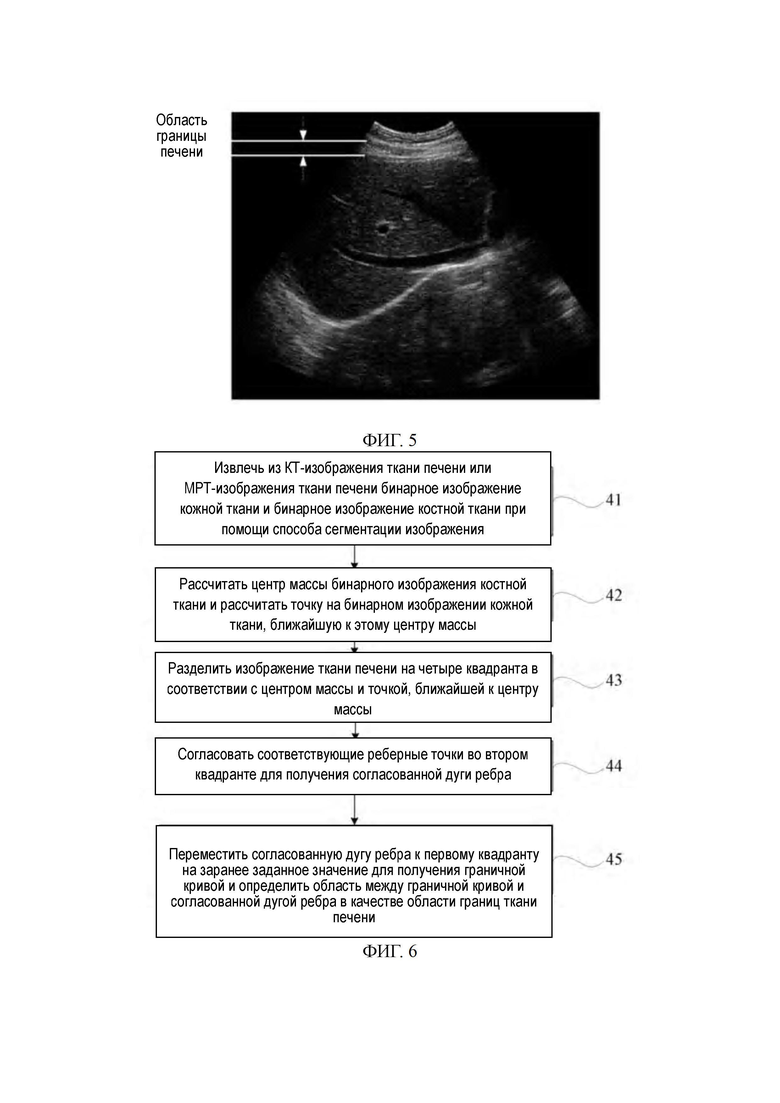
на ФИГ. 7 показано схематичное изображение, иллюстрирующее результат идентификации границы на основе КТ-изображения ткани печени в четвертом варианте осуществления настоящего изобретения;
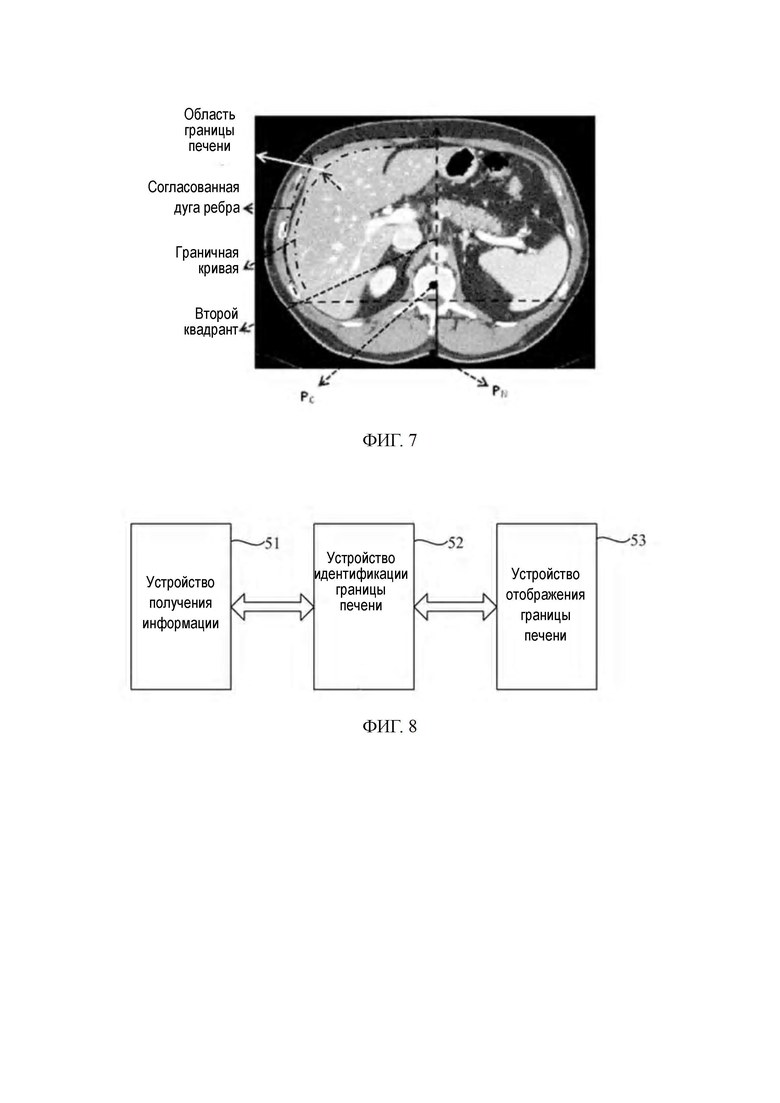
на ФИГ. 8 показано схематичное изображение структуры системы идентификации границы печени, представленной в пятом варианте осуществления настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ
Здесь варианты осуществления настоящего изобретения будут раскрыты более полно и исчерпывающе совместно с сопутствующими чертежами и конкретными вариантами осуществления изобретения. Следует понимать, что эти конкретные варианты осуществления изобретения, раскрытые здесь, использованы только для объяснения вариантов осуществления настоящего изобретения, но не имеют ограничительного характера. Дополнительно следует также учитывать, что для содействия раскрытию на чертежах показаны только части соответствующих вариантов осуществления настоящего изобретения, но не все содержание.
Первый вариант осуществления изобретения.
На ФИГ. 1 представлена блок-схема реализации способа идентификации границы печени в первом варианте осуществления настоящего изобретения. Способ может быть выполнен системой идентификации границ печени. Как показано на ФИГ. 1, процесс реализации включает в себя.
Шаг 11: получение информации о ткани печени для ткани печени, которая должна быть идентифицирована.
Информация о ткани печени может быть ультразвуковым сигналом А-типа ткани печени, ультразвуковым сигналом М-типа ткани печени, ультразвуковым изображением B-типа ткани печени, КТ-изображением ткани печени или МРТ-изображением ткани печени.
Согласно информации о ткани печени можно получить тип информации о ткани печени. Т. е. типом информации о ткани печени может быть ультразвуковой сигнал, например, ультразвуковой сигнал А-типа ткани печени, ультразвуковой сигнал М-типа ткани печени, или двухмерное ультразвуковое изображение, например, ультразвуковое изображение B-типа ткани печени, или трехмерное изображение, например, КТ-изображение ткани печени или МРТ-изображение ткани печени.
Шаг 12: идентифицируют границы ткани печени в информации о ткани печени по характерным признакам этой ткани, соответствующим информации о ткани печени, и по характерным признакам границы ткани печени, соответствующим информации о ткани печени, при помощи технологии обработки изображений или технологии обработки сигналов.
Если информация о ткани печени представляет собой ультразвуковой сигнал ткани печени, то используют технологию обработки сигнала для идентификации границы ткани печени по характерным свойствам ткани печени и границы ткани печени, соответствующим ультразвуковому сигналу ткани печени; если информация о ткани печени представляет собой двухмерное ультразвуковое изображение или трехмерное изображение, используют технологию обработки изображений для идентификации границы ткани печени по характерным свойствам этой ткани и ее границы, соответствующим двухмерному ультразвуковому изображению или трехмерному ультразвуковому изображению ткани печени.
Если информация о ткани печени представляет собой одномерный ультразвуковой сигнал ткани печени, двухмерное ультразвуковое изображение ткани печени или трехмерное ультразвуковое изображение ткани печени, идентификация границы ткани печени в информации о ткани печени в соответствии с характерными свойствами ткани печени, соответствующими информации о ткани печени, и характерным свойствам границы ткани печени, соответствующим информации о ткани печени, при помощи технологии обработки изображения или технологии обработки сигналов, может, в частности, содержать: разделение информации о ткани печени на множество подобластей диагностики; расчет значения характерного параметра информации о ткани печени в каждой подобласти диагностики; и идентификацию границы ткани печени по значениям характерного параметра в информации о ткани печени в подобластях диагностики.
Шаг 13: вывод информации о местоположении идентифицированной границы ткани печени.
Вывод информации о местоположении идентифицированной границы ткани печени может содержать: вывод координат местоположения идентифицированной границы ткани печени; и/или воспроизведение изображения идентифицированной границы ткани печени. Т. е. могут быть выведены: только координаты местоположения идентифицированной границы ткани печени, или может быть воспроизведено только изображение идентифицированной границы ткани печени, или могут быть выведеныа не только координаты местоположения идентифицированной границы ткани печени, но также может быть выведено изображение идентифицированной границы ткани печени при выводе информации о местоположения идентифицированной границы ткани печени.
Согласно способу идентификации границы ткани печени, представленному в первом варианте осуществления настоящего изобретения, граница ткани печени может быть идентифицирована автоматически и эффективно по характерным свойствам ткани печени и ее границы, соответствующим информации о ткани печени, где такая информация может быть ультразвуковым сигналом А-типа, отражающим одномерную информацию о структуре ткани печени, или ультразвуковым сигналом М-типа, отражающим одномерную динамическую информацию о структуре ткани, или ультразвуковым изображением B-типа, отражающим двухмерную структуру ткани печени, или КТ- или МРТ-изображением, отражающим трехмерную структуру ткани печени.
Второй вариант осуществления изобретения:
Второй вариант осуществления является частной оптимизацией, адресованной шагу 12 в первом варианте осуществления настоящего изобретения. Способ применим к одномерному ультразвуковому сигналу ткани печени. На ФИГ. 2 представлена блок-схема реализации способа идентификации границы печени во втором варианте осуществления настоящего изобретения, и на ФИГ. 3 показано схематичное изображение, иллюстрирующее результат идентификации границы на основе ультразвукового сигнала М-типа ткани печени во втором варианте осуществления настоящего изобретения. В сочетании с ФИГ. 2 и 3 способ включает в себя.
Шаг 21: разделение одномерного ультразвукового сигнала ткани печени на множество подобластей диагностики Si.
Одномерный ультразвуковой сигнал ткани печени может быть ультразвуковым сигналом А-типа ткани печени или ультразвуковым сигналом М-типа ткани печени. Предполагая, что один ультразвуковой сигнал содержит n точек выборки и соответствующая глубина сканирования ультразвукового сигнала ткани печени равна d (в мм), то известно, что каждый 1 мм глубины содержит n/d точек. Эти n точек выборки разделены на множество подобластей диагностики Si, где подобласть диагностики Si соответствует глубине сканирования di, где i - целое число, глубина сканирования di может быть средним значением глубины или конечным значением глубины подобласти диагностики Si, и последующее описание будет основано на конечном значении.
Например, n точек выборки образцов разделены на множество подобластей диагностики Si с шагом z. Информацию о самой нижней части изображения, полученного с помощью ультразвуковой визуализации (что соответствует самой нижней части глубины сканирования), можно игнорировать, так как самая нижняя часть изображения обычно не содержит какой либо цели для диагностики. В этом случае i=1, 2,…,[d/z]-1, где z - протяженность сегмента подобласти диагностики (в мм), и [] обозначает округление до целого. В этом случае каждый сегмент подобласти диагностики содержит [zn/d] точек выборки, соответственно. Например, когда глубина сканирования d ультразвукового сигнала составляет 20 мм и шаг z составляет 3 мм, то n точек отбора образцов разделяется на [d/z]-1=6 подобластей диагностики S1~S6, где S1 соответствует сегменту 0~3 мм, S2 соответствует сегменту 3~6 мм, ..., S6 соответствует сегменту 15~18 мм, а самую нижнюю часть изображения (соответствующую части 18~20 мм) не принимают во внимание, так как она обычно не содержит цели для диагностики.
Шаг 22: расчет значения распределения Накагами mi для одномерного ультразвукового сигнала Ri ткани печени в каждой подобласти диагностики Si
Статистическая модель Накагами - это тип технологии для ультразвуковой характеристики ткани. В частности, значение распределения Накагами mi рассчитывают для одномерного ультразвукового сигнала Ri, соответствующего изображению ткани печени в каждой подобласти диагностики Si, в соответствии со следующей формулой:
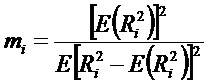
где плотность распределения вероятностей для распределения Накагами:
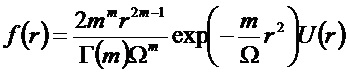
где E(.) - функция среднего значения, Г(.) обозначает гамма-функцию, Ω=E(r2), U(.) обозначает единичную ступенчатую функцию, m - значение распределения Накагами, r - зависимая переменная функции распределения вероятностей f(r), r≥0, m≥0; и для каждой подобласти диагностики Si mi представляет собой значение m в области Si, и Ri - значение огибающей ультразвукового сигнала.
Когда значение m находится в диапазоне (0, 1), ультразвуковой сигнал ткани печени следует предварительному распределению Рэлея. Когда значение m равно 1, отраженный ультразвуковой сигнал следует распределению Рэлея. Когда значение m больше 1, отраженный ультразвуковой сигнал следует последующему распределению Рэлея (пост-Рэлеевское распределение).
Шаг 23: расчет весового значения Wi для каждой подобласти диагностики Si согласно приведенной ниже формуле и определение подобласти диагностики, соответствующей максимальному весовому значению, которая будет областью границ ткани печени:
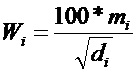
где di - глубина сканирования, соответствующая подобласти обнаружения диагностики Si, и также может быть средним значением глубины или конечным значением глубины подобласти диагностики Si. Весовые значения Wi соответствующих подобластей диагностики, проверяют, чтобы выбрать подобласть диагностики, соответствующую максимальному весовому значению, которая будет областью границ ткани печени, достигая таким образом автоматического позиционирования границы ткани печени.
Способ идентификации границы печени, представленный во втором варианте осуществления настоящего изобретения, может обеспечить реализацию автоматического позиционирования границы ткани печени в режиме реального времени посредством ультразвуковых сигналов А-типа или М-типа ткани печени. Кроме того, данный алгоритм имеет низкий уровень сложности, что может обеспечить более высокую эффективность идентификации границы ткани печени, и, тем самым, автоматическое позиционирование границы ткани печени в режиме реального времени.
Третий вариант осуществления изобретения:
Третий вариант осуществления является частной оптимизацией, адресованной шагу 12 в первом варианте осуществления настоящего изобретения. Способ применим к двухмерному ультразвуковому сигналу ткани печени. На ФИГ. 4 показана блок-схема реализации способа идентификации границы печени в третьем варианте осуществления настоящего изобретения, и на ФИГ. 5 показано схематичное изображение, иллюстрирующее результат идентификации границы на основе ультразвукового изображения B-типа ткани печени в третьем варианте осуществления настоящего изобретения. В сочетании с ФИГ. 4 и 5 способ содержит.
Шаг 31: разделение двухмерного ультразвукового изображения ткани печени на множество прямоугольных подобластей диагностики Rij, где i и j - натуральные числа, обозначающие номер строки и столбца соответствующей подобласти диагностики.
Двухмерное ультразвуковое изображение ткани печени может быть ультразвуковым изображением B-типа ткани печени. Исходя из допущения о том, что размер ультразвукового изображения B-типа составляет w*h, где w - ширина двухмерного ультразвукового изображения ткани печени, h - высота двухмерного ультразвукового изображения ткани печени (единица измерения для w и h - пиксели), и соответствующая глубина сканирования - d (в мм), то в 1 мм глубины линии сканирования в направлении по глубине содержится h/d пикселей. Ультразвуковое изображение B-типа размером w*h разделяется на множество прямоугольных подобластей диагностики Rij.
Например, ультразвуковое изображение B-типа размером w*h разделяется на множество квадратных подобластей диагностики Rij с длиной стороны z. Аналогично первому варианту осуществления информацию о самой нижней части изображения, образованной с использованием ультразвуковой визуализации (что соответствует самой нижней части глубины сканирования), и ее краях в поперечном направлении можно игнорировать, так как самая нижняя часть и края обычно не содержат объект тестирования, где
i=1, 2, …, 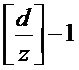
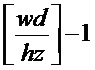
где z - длина стороны квадратной подобласти диагностики (в мм), и [] обозначает округление до целого. В этом случае ширина и высота каждой квадратной подобласти обнаружения Rij составляет [zh/d] пикселей.
Шаг 32: расчет весового значения Wij каждой подобласти диагностики Rij и определение подобласти диагностики, соответствующей максимальному значению весового значения, которая будет областью границ ткани печени. Для уменьшения количества расчетов можно рассчитать весовые значения только половины подобластей диагностики. Например, двухмерное ультразвуковое изображение может быть разделено на две части по центральной линии, и рассчитываются только весовые значения Wkj (k=imax/2) подобластей диагностики Rkj в верхней половине двухмерного ультразвукового изображения для поиска граничной подобласти над центральной линией. Полная граничная область может затем быть найдена за счет расширения граничной подобласти в направлении по ширине (т. е. в поперечном направлении). В этом случае весовые значения Wkj могут быть рассчитаны по следующей формуле:
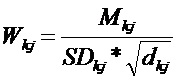
где Mkj - среднее значение градации серого двухмерного ультразвукового изображения ткани печени в подобласти диагностики Rkj, SDkj - стандартное отклонение градации серого двухмерного ультразвукового изображения ткани печени в подобласти диагностики Rkj, и dkj - глубина сканирования, соответствующая подобласти диагностики Rkj. Как известно из k=imax/2, 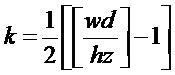
Область границы печени имеет большее среднее значение градации серого, так как огибающая области печени представлена на ультразвуковом изображении B-типа как однородный эхосигнал высокого уровня. Дополнительно стандартное отклонение градации серого относительно низкое, так как огибающая области печени на ультразвуковом изображении B-типа выглядит однородной. Чтобы избежать черных фоновых областей с двух сторон веерообразного ультразвукового изображения B-типа, полученного в результате сканирования конвексным датчиком, поиск необходимо начинать с подобласти диагностики на центральной линии ультразвукового изображения B-типа и если подобласть диагностики Rk1 имеет наибольшее весовое значение среди серии областей диагностики Rkj, подобласть диагностики Rk1 определяется как граница ткани печени.
Способ идентификации границы печени, представленный в третьем варианте осуществления, может обеспечить реализацию автоматического позиционирования границы ткани печени в режиме реального времени с использованием ультразвукового изображения B-типа ткани печени. Данный алгоритм имеет низкий уровень сложности, что может обеспечить более высокую эффективность при идентификации границы ткани печени, и, тем самым, дает возможность автоматического позиционирования границы ткани печени в режиме реального времени.
Четвертый вариант осуществления изобретения:
Четвертый вариант осуществления является частной оптимизацией, адресованной шагу 12 в первом варианте осуществления настоящего изобретения. Способ применим к трехмерному ультразвуковому сигналу ткани печени. На ФИГ. 6 представлена блок-схема реализации способа идентификации границы печени в четвертом варианте осуществления настоящего изобретения, и на ФИГ. 7 показано схематичное изображение, иллюстрирующее результат идентификации границы на основе КТ-изображения ткани печени в четвертом варианте осуществления настоящего изобретения. В сочетании с ФИГ. 6 и 7 способ содержит.
Шаг 41: извлечение из КТ-изображения ткани печени или из МРТ-изображения ткани печени бинарного изображения кожной ткани и бинарного изображения костной ткани при помощи способа сегментации изображения.
Процесс начинается с извлечения бинарного изображения кожной ткани. Бинарное изображение кожной ткани извлекается с использованием способа сегментации изображения (например, способ сегментации с ростом области) и взятия пикселя изображении с координатами (0, 0) в качестве исходной точки, где критерий разрастания области соответствует КТ-значению для воздуха [-1024,-500] HU (единицы Хаунсфилда).
Затем способ переходит к извлечению бинарного изображения костей, включая бинарное изображение позвоночника и бинарное изображение ребер. Пороговая сегментация выполняется для всего изображения на основе порогового диапазона [350,1024] ед. Х. для извлечения бинарного изображения костной ткани.
Шаг 42: расчет центра массы бинарного изображения костной ткани и расчет точки на бинарном изображении кожной ткани, ближайшей к центру массы.
Расчет центра массы PC бинарного изображения костной ткани. Центр массы позвоночника PC берется за центр массы бинарного изображения костной ткани, так как ребра обычно распределены симметрично слева и справа от позвоночника, и позвоночник занимает относительно большую часть на изображении костной ткани.
Приняв центр массы PC позвоночника за начальную точку, найти точку на бинарном изображении кожной ткани, ближайшую к центру массы PC, обозначенную PN.
Шаг 43: разделение изображения ткани печени на четыре квадранта в соответствии с упомянутыми центром массы и точкой, ближайшей к центру массы.
При разделении изображения ткани печени на четыре квадранта с использованием центра массы PC и точки PN, ближайшей к центру массы, за вертикальную ось берется прямая линия, проходящая через центр массы PC и точку PN, ближайшую к центру массы PC, а прямая линия, проходящая через центр массы PC и перпендикулярная вертикальной оси, принята за горизонтальную ось. Большинство частей печени расположены во втором квадранте.
Шаг 44: согласование соответствующих реберных точек во втором квадранте для получения согласованной дуги ребра.
Согласованную дугу ребра получают за счет согласования соответствующих точек ребер во втором квадранте с использованием В-сплайновой кривой или кривой для кожной ткани.
Шаг 45: перемещение согласованной дуги ребра в направлении первого квадранта с использованием заранее заданного значения для того, чтобы получить граничную кривую, и определение области между этой граничной кривой и сопряженной дугой ребра в качестве граничной области тканей печени.
Поскольку дуга ребра находится рядом с капсулой печени, дуга ребра перемещается вовнутрь на заранее заданное значение и принимается за граничную кривую, а область между этой граничной кривой и сопряженной дугой ребра определяется как граничная область тканей печени.
Заранее заданное значение может составлять 5 мм.
Способ идентификации границы печени, представленный в четвертом варианте осуществления настоящего изобретения, может обеспечить реализацию автоматического позиционирования границы ткани печени в режиме реального времени за счет КТ- изображения или МРТ-изображения ткани печени. Кроме того, данный алгоритм имеет низкий уровень сложности, что может обеспечить более высокую эффективность идентификации границы ткани печени, и, тем самым, автоматическое позиционирование границы ткани печени в режиме реального времени.
Пятый вариант осуществления изобретения.
На ФИГ. 8 показана блок-схема, иллюстрирующая систему идентификации границы печени в пятом варианте осуществления настоящего изобретения. Как показано на ФИГ. 8, система идентификации границы печени, раскрытая в данном варианте осуществления, может содержать устройство 51 получения информации, устройство 52 идентификации границы печени и устройство 53 отображения границы печени, при этом устройство 51 получения информации сконфигурировано, чтобы получить информацию о ткани печени для ткани печени, которую необходимо идентифицировать; устройство 52 идентификации границы печени сконфигурировано для идентификации границы ткани печени в информации о ткани печени по характеристическим параметрам ткани печени, соответствующим информации о ткани печени, этой ткани и характеристическим параметрам границы ткани печени соответствующим информации о ткани печени, при помощи технологии обработки изображений или технологии обработки сигналов; и устройство 53 отображения границы печени сконфигурировано для вывода информации о положении идентифицированной границы ткани печени.
Если информация о ткани печени представляет собой одномерный ультразвуковой сигнал ткани печени, двухмерное ультразвуковое изображение ткани печени или трехмерное ультразвуковое изображение ткани печени, устройство 52 идентификации границы печени может содержать: блок разделения области, выполненный с возможностью разделения информации о ткани печени на множество подобластей диагностики; и блок идентификации границы, выполненный с возможностью расчета значения характеристических параметров информации о ткани печени в каждой из подобластей диагностики и идентификации границы ткани печени по значениям характеристических параметров информации о ткани печени в подобластях диагностики.
Если информация о ткани печени представляет собой одномерный ультразвуковой сигнал ткани печени, блок идентификации границы может содержать: первый субблок вычисления значения характеристических параметров, выполненный с возможностью расчета значения mi распределения Накагами для одномерного ультразвукового сигнала Ri ткани печени в каждой подобласти диагностики Si; и первый субблок определения границы, выполненный с возможностью расчета весового значения Wi каждой подобласти диагностики Si по приведенной ниже формуле и определения подобласти диагностики, соответствующей максимальному значению весового значения, как области границ ткани печени:
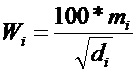
где di - глубина сканирования, соответствующая подобласти диагностики Si.
Если информация о ткани печени представляет собой двухмерное ультразвуковое изображение ткани печени, то блок разделения области, в частности, выполнен с возможностью разделения двухмерного ультразвукового изображения ткани печени на множество прямоугольных подобластей диагностики Rij; блок определения границы может быть, в частности, выполнен с возможностью расчета весового значения Wkj каждой подобласти диагностики Rkj по приведенной ниже формуле и определения подобласти диагностики Rij, соответствующей максимальному значению весового значения, как области границ ткани печени:
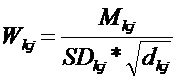
где Mkj - среднее значение градации серого двухмерного ультразвукового изображения ткани печени в подобласти диагностики Rkj, SDkj - стандартное отклонение градации серого двухмерного ультразвукового изображения ткани печени в подобласти диагностики Rkj, и dkj - глубина сканирования, соответствующая подобласти диагностики Rkj и k=imax/2.
Если информация о ткани печени представляет собой КТ-изображение ткани печени или МРТ-изображение ткани печени, устройство 52 для идентификации границы печени может, в частности, содержать: блок получения бинарного изображения, выполненный с возможностью извлечения из КТ-изображения ткани печени или из МРТ-изображения ткани печени бинарного изображения кожной ткани и бинарного изображения костной ткани при помощи способа сегментации изображения; блок определения характеристической точки, выполненный с возможностью расчета центра массы бинарного изображения костной ткани; и расчета точки на бинарном изображении кожной ткани, ближайшей к этому центру массы; блок разделения изображения, выполненный с возможностью разделения изображения ткани печени на четыре квадранта в соответствии с этим центром массы и этой точкой, ближайшей к центру массы; блок согласования кривой, выполненный с возможностью согласования каждой точки ребер во втором квадранте для получения согласованной дуги ребра; и блок определения граничной области, выполненный с возможностью перемещения согласованной дуги ребра в сторону первого квадранта на заранее установленное значение для получения граничной кривой области; и определение области между этой граничной кривой области и согласованной дугой ребра как граничной области ткани печени.
Согласно способу идентификации границы печени, представленному в пятом варианте осуществления настоящего изобретения, граница ткани печени может быть идентифицирована автоматически и эффективно по характерным свойствам границы ткани печени, соответствующим информации о ткани печени, где информация о ткани печени может быть ультразвуковым сигналом А-типа, отражающим одномерную информацию о структуре ткани печени, или ультразвуковым изображением М-типа или ультразвуковым сигналом М-типа, отражающим одномерную динамическую информацию о структуре ткани, или ультразвуковым изображением B-типа, отражающим двухмерную структуру ткани, или КТ- или МРТ-изображением, отражающим трехмерную структуру ткани печени.
Выше раскрыты только предпочтительные варианты осуществления настоящего изобретения, но не имеющие ограничительного характера. Различные изменения могут быть внесены в варианты осуществления настоящего изобретения специалистами в данной области техники. Любые и все модификации, эквивалентные замещения, улучшения и т.д. в рамках объема и принципа вариантов осуществления настоящего изобретения должны входить в объем охраны вариантов осуществления настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ И СИСТЕМА ИДЕНТИФИКАЦИИ ГРАНИЦЫ ПЕЧЕНИ | 2015 |
|
RU2707032C2 |
| Способ и устройство для выбора области диагностики и система диагностики для определения эластичности | 2015 |
|
RU2695619C2 |
| КОЛИЧЕСТВЕННЫЙ АНАЛИЗ ПЕРФУЗИИ | 2010 |
|
RU2541175C2 |
| АВТОМАТИЧЕСКОЕ ПОСЛЕДОВАТЕЛЬНОЕ ПЛАНИРОВАНИЕ МР-СКАНИРОВАНИЯ | 2009 |
|
RU2533626C2 |
| ТЕРАПЕВТИЧЕСКАЯ СИСТЕМА НА ОСНОВЕ СФОКУСИРОВАННОГО УЛЬТРАЗВУКА | 2005 |
|
RU2366475C2 |
| СИСТЕМЫ И СПОСОБЫ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИК ЦЕНТРАЛЬНОЙ ОСИ КОСТИ НА ОСНОВАНИИ ТРЕХМЕРНОГО АНАТОМИЧЕСКОГО ИЗОБРАЖЕНИЯ | 2016 |
|
RU2703699C1 |
| СЕГМЕНТАЦИЯ ТКАНЕЙ ЧЕЛОВЕКА НА КОМПЬЮТЕРНОМ ИЗОБРАЖЕНИИ | 2017 |
|
RU2654199C1 |
| УЛЬТРАЗВУКОВОЕ ИЗМЕРЕНИЕ ОБЪЕМНОГО ПОТОКА ДЛЯ ПЛАНИРОВАНИЯ АБЛЯЦИИ | 2013 |
|
RU2651875C2 |
| УЛЬТРАЗВУКОВАЯ СИСТЕМА И СПОСОБ ОБНАРУЖЕНИЯ СКОЛЬЖЕНИЯ ЛЕГКОГО | 2017 |
|
RU2740257C2 |
| ИСПОЛЬЗОВАНИЕ КОЛЛЕКЦИИ ПЛАНОВ ДЛЯ РАЗРАБОТКИ НОВЫХ ЗАДАЧ ОПТИМИЗАЦИИ | 2010 |
|
RU2566974C2 |

Группа изобретений относится к области медицины, а именно лучевой диагностике, и может быть использована для определения области границ печени. Способ включает получение визуализации компьютерной томографии (КТ-визуализации) или визуализации магниторезонансной томографии (МРТ-визуализации) ткани печени. Извлекают бинарную визуализацию кожной ткани и бинарную визуализацию костной ткани при помощи способа сегментации изображения. Определяют центр массы бинарной визуализации костной ткани и точку на бинарной визуализации кожной ткани, ближайшую к центру массы. Делят изображение ткани печени на четыре квадранта в соответствии с центром массы и точкой, ближайшей к центру массы. Согласовывают каждую реберную точку во втором квадранте и получают кривую согласования ребер. Перемещают кривую согласования ребер к первому квадранту и получают граничную кривую. Определяют область границы печени, как область между граничной кривой и кривой согласования ребер. Выводят информацию о местоположении идентифицированной области границы печени. Система определения области границы печени содержит устройство получения информации, устройство определения границы печени и устройство отображения границы печени, при этом возможно выполнение указанного способа. Способ и система обеспечивают автоматическое определение области границ печени за счет применения технологии обработки изображений. 2 н. и 2 з.п. ф-лы, 8 ил.
1. Способ определения области границы печени, характеризующийся тем, что он включает:
получение информации о ткани печени для ткани печени, которая должна быть идентифицирована, при этом информация о ткани печени представляет собой визуализацию компьютерной томографии (КТ-визуализации) или визуализацию магниторезонансной томографии (МРТ-визуализации) ткани печени;
извлечение из КТ-визуализации ткани печени или из МРТ-визуализации ткани печени бинарной визуализации кожной ткани и бинарной визуализации костной ткани при помощи способа сегментации изображения;
расчет центра массы PC бинарной визуализации костной ткани и расчет точки PN на бинарной визуализации кожной ткани, ближайшей к центру массы PC;
разделение КТ-визуализации или МРТ-визуализации ткани печени на четыре квадранта в соответствии с центром массы и точкой, ближайшей к центру массы;
согласование каждой реберной точки во втором квадранте с использованием внутреннего края реберного среза посредством сплайновой кривой или кривой для кожной ткани для получения кривой согласования ребер; и
перемещение кривой согласования ребер к первому квадранту для получения граничной кривой, и определение области между граничной кривой и кривой согласования ребер в качестве области границы печени,
вывод информации о местоположении идентифицированной области границы печени.
2. Способ по п. 1, отличающийся тем, что выводимая информация о положении определенной области границы печени содержит:
вывод координат определенной области границы печени; и/или
отображение визуализации определенной области границы печени.
3. Система определения области границы печени, отличающаяся тем, что содержит: устройство получения информации, устройство определения границы печени и устройство отображения границы печени, при этом
устройство получения информации выполнено с возможностью получения визуализации компьютерной томографии (КТ-визуализации) или визуализации магниторезонансной томографии (МРТ-визуализации) определяемой ткани печени;
устройство определения границы печени выполнено с возможностью извлечения из КТ-визуализации ткани печени или МРТ-визуализации ткани печени бинарной визуализации кожной ткани и бинарной визуализации костной ткани при помощи способа сегментации изображения, расчета центра массы PC бинарной визуализации костной ткани и расчета точки PN на бинарной визуализации кожной ткани, ближайшей к центру массы PC, разделения КТ-визуализации или МРТ-визуализации ткани печени на четыре квадранта в соответствии с центром массы и точкой, ближайшей к центру массы, согласования каждой реберной точки во втором квадранте с использованием внутреннего края реберного среза посредством сплайновой кривой или кривой для кожной ткани для получения кривой согласования ребер, перемещения кривой согласования ребер к первому квадранту для получения граничной кривой и определения области между кривой области границ и кривой согласования ребер в качестве области границы печени,
устройство отображения границы печени, выполненное с возможностью вывода информации о положении определенной области границы печени.
4. Система по п. 3, отличающаяся тем, что устройство отображения границы печени содержит:
блок вывода местоположения, выполненный с возможностью вывода координат идентифицированной области границы печени; и/или
блок отображения изображения, выполненный с возможностью отображения изображения идентифицированной области границы печени.
| СПОСОБ ОПРЕДЕЛЕНИЯ РАЗМЕРОВ И ГЛУБИНЫ ЗАЛЕГАНИЯ АНАТОМО-МОРФОЛОГИЧЕСКИХ СТРУКТУР В ЖИВОЙ БИОЛОГИЧЕСКОЙ ТКАНИ ПРИ ЕЕ ОБСЛЕДОВАНИИ С ПОМОЩЬЮ ОПТИКО-КОГЕРЕНТНОЙ ТОМОГРАФИИ | 2009 |
|
RU2407426C1 |
| US 7519209 B2, 14.04.2009 | |||
| US 7702153 B2, 20.04.2010 | |||
| НЕДЗЬВЕДЬ А.М | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Таврический вестник информатики и математики | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Ребристый каток | 1922 |
|
SU121A1 |
| CAMPADELLI P | |||
| et al | |||
| Liver segmentation from computed tomography scans: | |||
Авторы
Даты
2021-10-05—Публикация
2015-08-10—Подача