Изобретение относится к области химии, в частности к синтезу химических соединений - полиметилсилоксанов (гидрогелей метилкремниевой кислоты), и может быть использован в медицине и ветеринарии как сорбент, который имеет селективные свойства.
Известны полиметилсесквиоксаны общей химической формулы:
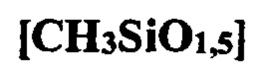
описывающие ряд веществ, в том числе и гидрогель метилкремниевой кислоты, который представляется общей формулой:
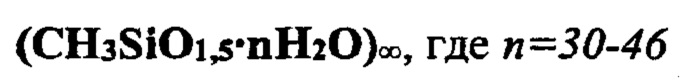
Данные соединения представляют собой сетчатые полимеры сложной топологии, окруженные гидратной оболочкой. Основным способом их получения является проведение поликонденсации с щелочной фазы.
Исходя из структурного представления этих полимеров, следует учесть, что они содержат остаточные несконденсированные гидроксогрупы (ОН-группы) и обобщающая брутто-формула полимера в линейной форме (без учета гидратной оболочки) имеет вид:
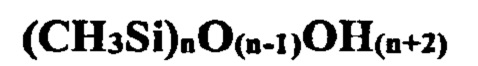
по мере прохождения поликонденсации происходит разветвление полимера с образованием промежуточной структуры вида:
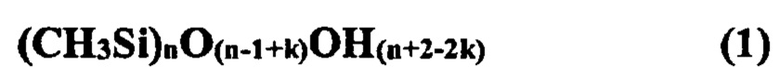
где 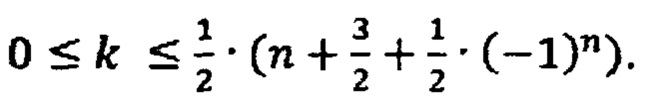
Очевидно, что:
при k=0 полимер представляет собой форму с преимущественно линейной топологией. Существование полимера в данной форме больше присуще щелочным растворам;
при 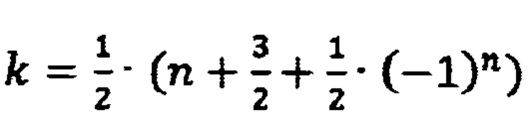 полимер представляет собой форму с циклической топологией, полностью сконденсированную, без содержания ОН-групп. Данная форма полимера присуща ксерогелей метилкремниевой кислоты;
полимер представляет собой форму с циклической топологией, полностью сконденсированную, без содержания ОН-групп. Данная форма полимера присуща ксерогелей метилкремниевой кислоты;
при 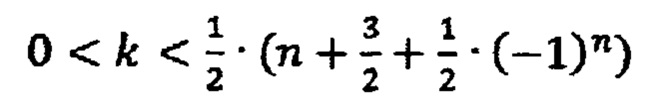 полимер представляет собой форму с промежуточной между линейной и циклической, топологией. Собственно, данная форма и присуща группе соединений под общим названием гидрогель метилкремниевой кислоты.
полимер представляет собой форму с промежуточной между линейной и циклической, топологией. Собственно, данная форма и присуща группе соединений под общим названием гидрогель метилкремниевой кислоты.
Поликонденсация ОН-групп предельной линейной структуры (k=0) описывается химическим уравнением вида:
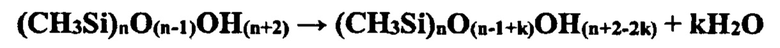
Приведенная реакция представляет собой процесс внутримолекулярной поликонденсации и сопровождается циклизацией молекулы.
Рост цепи полимера на примере поликонденсационного взаимодействия двух молекул со структурами промежуточных топологий (m≤n и 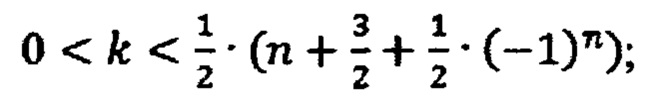
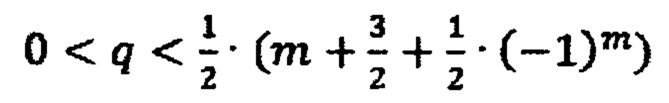 выражается в виде химического уравнения:
выражается в виде химического уравнения:
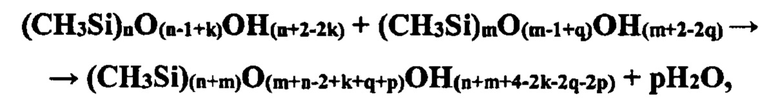
где:
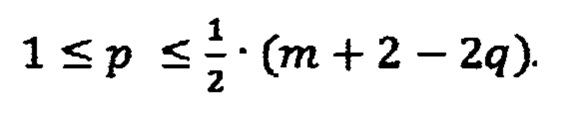
Известен способ получения гидрогеля метилкремниевой кислоты, который включает приготовление рабочей смеси из метилтриэтоксисилана и органического растворителя, приготовление гидролитических смеси с соляной кислоты и воды очищенной, изготовление щелочного раствора, гидролиз метилтриэтоксисилана в присутствии кислотного катализатора с последующей щелочной обработкой, выдержкой реакционной массы, измельчения полученного алкогелю метилкремниевой кислоты, его последующее отмывание водой, очищенной до образования гидрогеля метилкремниевой кислоты. При изготовлении рабочей смеси как органический растворитель применяют водный раствор этанола с объемной долей спирта этилового от 60 до 96,5%, а количественное объемное соотношение метилтриэтоксисилана и органического растворителя в виде водного раствора этанола составляет (1-1,2):(2-2,7) соответственно, при этом метилтриэтоксисилан применяют с массовой долей основного вещества не менее 98%, а гидролиз метилтриэтоксисилан осуществляют при объемном соотношении рабочей смеси и гидролитических смеси (3-3,5):(0,7-1,5) соответственно, при этом время введения гидролитических смеси в реакционную массу составляет 30-40 минут, а выдержку полученной реакционной массы осуществляют в течение 3-3,5 часов при значении рН не менее 3, и после окончания гидролиза метилтриэтоксисилана в полученную реакционную массу вводят щелочной раствор, который имеет температуру 16-30 0 с, после чего полученный алкогидрогель метилкремниевой кислоты выдерживают для созревания в течение не менее 7,5 часов, при этом процесс вызревания алкогидрогеля метилкремниевой кислоты осуществляют до получения полупродукта бесцветного с легкой опалесценцией, а отмывание измельченного алкогидрогелю метилкремниевой кислоты осуществляют путем введения в него воды, очищенной со скоростью 2-4 л в час [UA №90988, C08G 77/00, 2010].
Известный способ имеет следующие недостатки.
Для полного отщепления етоксигруп необходимым условием является наличие сильно щелочной среды (для полного протекания реакции омыления концентрация щелочи должна быть не менее 5 моль/л) и повышенная температура реакционной смеси (не менее 60°С). Применение кислот на стадии проведения поликонденсации для спиртовых растворов приводит к образованию побочного продукта - диэтилового эфира. Так как продукт имеет адсорбционные свойства, он адсорбирует как продукты реакций, так и спирт этиловый из среды растворителя. Конечный продукт, полученный по этому способу, содержит в составе примеси: спирт этиловый, диэтиловый эфир и неомыленных етоксисилан. Удаление этих примесей из продукта требует больших затрат воды очищенной и не может быть проведено полностью в соотвествии с приведенными в способе получения условиями.
Известен способ получения сорбента на основе гидрогеля метилкремниевой кислоты общей формулы {(CH3SiO1,5)⋅mH2O}n, где m - количество молекул воды в звене {(CH3SiO1,5)⋅mH2O}, n - количество звеньев {(CH3SiO1,5)⋅mH2O} в гидрогеле, при котором из исходного вещества в присутствии сильной кислоты в среде спирта получают гидрогель путем гидролиза с последующей поликонденсацией в щелочной среде, который выдерживают и измельчают, и промывают полученный продукт до нейтральной реакции, при этом сильную кислоту используют в концентрации от 0,5% до 1,2%, а щелочной реагент для осуществления реакции поликонденсации используют в концентрации от 20% до 27% [UA №72402, C08G 77/04, 2012].
Так же, как в предыдущем случае, применение кислот на стадии проведения поликонденсации для спиртовых растворов приводит к образованию побочного продукта - диетиловго эфира. Так как продукт имеет адсорбционные свойства, он адсорбирует как продукты реакций, так и спирт этиловый из среды растворителя. Конечный продукт, полученный по этому способу, содержит в составе примеси: спирт этиловый и диэтиловый эфир. Удаление этих примесей из продукта также требует больших затрат воды очищенной и не может быть проведено полностью в соответствии с приведенными в способе получения условиями.
Известно способ получения гидрогеля метилкремниевой кислоты, согласно которому проводят процесс поликонденсации раствора метилсиликонат натрия (или калия) концентрации от 1,75 до 2,30 моль/л путем добавления к нему раствора сильной кислоты до образования гидрогеля, который после выдержки в течение 30 - 90 мин (созревание) измельчают и затем активируют действием разбавленного раствора сильной кислоты концентрации от 0,04 до 0,15 г⋅екв/л с последующим отмыванием водой до нейтральной реакции [RU №94008432 A1, C08G 77/02. 1995].
Сформированный гель обрабатывают разбавленными растворами сильных кислот (стадия активации), что приводит к окончательной конденсации гидроксогруп и, тем самым, приводит к потере свойств супрамолекулярных структур и потери конформационной подвижности.
Ближайшим к заявляемого изобретения, является способ получения сорбента на основе гидрогеля метилкремниевой кислоты общей формулы: {(CH3SiO1,5)⋅nH2O}∞, включающий добавление к раствору метилсиликонату натрия или калия раствора сильной кислоты до образования продукта с последующим выдерживанием, измельчением, активированием продукта путем добавления разбавленного раствора сильной кислоты и отмыванием продукта до нейтральной реакции, при этом используют раствор метилсиликонату натрия или калия в концентрации 2,35-2,95 моль/ли, варьируя значения коэффициента n до 495, получают различные конечные формы сорбента с выборочными сорбционными свойствами относительно высокомолекулярных веществ с молекулярной ной массой 10000-500000 Д и более [UA №82774, C08G 77/00, 2008].
Указанный способ имеет следующие недостатки.
Так как одним из компонентов смеси является сильная кислота, а другим -щелочной раствор метилсиликонату натрия, образуется соль сильной щелочи и сильной кислоты, которая не производит протекционного влияния на ОН-группы (растворы таких солей имеют близкую к нейтральной кислотность). В этом случае преобразования в системе целиком зависят от соотношения щелочной составляющей, которая уменьшается по мере проведения синтеза и сильнокислотний составляющей.
Проведение реакции в приведенных условиях делает невозможным управление ее течением и приводит к получению продукта, который неоднороден по физическим и химическим показателям, что затрудняет его стандартизацию.
Применение на стадиях получения продукта разбавленных растворов сильных кислот приводит к образованию низкомолекулярных фракций продукта, которые способствуют уменьшению адсорбционной способности, которая позиционируется для него как основная характеристика. Согласно требованиям надлежащих практик фармацевтических производств, образования низкомолекулярных фракций следует рассматривать как сопутствующие примеси с позиций целостности состава активного фармацевтического ингредиента, которым является гидрогель метилкремниевой кислоты.
В масштабах промышленного производства образуются сточные воды, которые содержат растворенные и взвешенные вещества на уровнях многократного превышения предельно допустимых концентраций, что требует создания отдельных комплексов очистки и создает проблемы дальнейшей утилизации.
Известно гидрогель метилкремниевой кислоты с высокой сорбционной емкостью и селективностью в отношении среднемолекулярных токсичных метаболитов (ентерогель - супер) формулы:
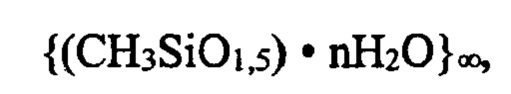
где n = 44-49, характеризующиеся сорбционной емкостью по Конго-красному 3,3-4,6 мг/г [RU №94 008 432 A1, C08G 77/02, 1995].
Такой гидрогель имеет сугубо сорбционные свойства с низкой селективностью.
Ближайшим к заявляемому гидрогелю является гидрогель метилкремниевой кислоты как сорбент среднемолекулярных метаболитов формулы
{(CH3Si01,5) ⋅ nH20} ∞, где n = 44-49, що характеризующиеся сорбционной емкостью по Конго-красному 3,3-4,6 мг/г [RU №2111979 C1, C08G 77/02, 1998].
Указанный гидрогель, как и предыдущий аналог, имеет сугубо сорбционные свойства с низкой селективностью, неоднородный по физическим и химическим показателям, что затрудняет его стандартизацию. Кроме того, применение разбавленных растворов сильных кислот приводит к образованию низкомолекулярных фракций продукта (сопутствующих примесей), которые способствуют уменьшению адсорбционной способности, позиционируемой для него как основная характеристика.
В основу изобретения поставлена задача создания способа получения гидрогеля метилкремниевой кислоты со свойствами супрамолекулярных структур, который был высокотехнологичным, экономически выгодным и экологичным.
Вторая задача, поставленная в основу изобретения, - это получение гидрогеля, который должен был бы иметь развитые селективные адсорбционные свойства и дополнительно - свойства супрамолекулярных структур для возможности его использования в медицине и ветеринарии как индивидуального вещества с терапевтическими свойствами, а также как матрицы для комплексных составов с функциями управляемого и/или пролонгированного высвобождения, и/или целевой доставки вещества.
Поставленную задачу решают тем, что в способе получения гидрогеля метилкремниевой кислоты со свойствами супрамолекулярных структур, в котором используют раствор метилсиликонату натрия, согласно изобретению через раствор метилсиликонату натрия, загруженный в реактор, пропускают газообразный кислый агент для осуществления барботажа, образовавшийся продукт флотируют в горловине реактора, после окончания процесса продукт выгружают из реактора, вакуумируют для удаления остаточного газа и отмывают водой, очищенной до значений рН-6,5-7,0 без остаточных количеств анионов, получая гидрогель метилкремниевой кислоты со свойствами супрамолекулярных структур, который описывается формулой:
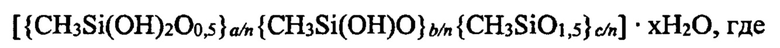
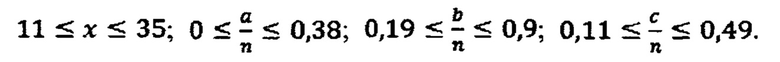
Время барботажа составляет 45 минут, скорость барботажа 333 мл газообразного агента в минуту.
Как газообразный кислый агент могут использовать углекислый газ, который подают через нижний клапан реактора, проводя процесс в замкнутой системе.
Как газообразный кислый агент могут использовать углекислый газ, который подают через верхний клапан реактора, проводя процесс в открытой системе.
Как газообразный кислый агент могут использовать оксид серы (IV) - SO2.
Как газообразный кислый агент могут использовать сероводород - H2S.
Как газообразный кислый агент могут использовать оксид серы (VI) - SO3.
Как газообразный кислый агент могут использовать хлороводород - HCl.
Раствор метилсиликонату натрия могут подавать по каплям через гребенку по гидрофобной поверхности желоба, размещенной в среде газообразного кислого агента, в течение 20 минут.
Вторую поставленную задачу решают получением способом по п. 1 гидрогеля метилкремниевой кислоты со свойствами супрамолекулярных структур, который описывается формулой: 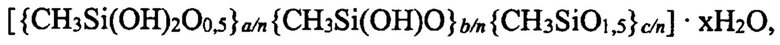 где
где
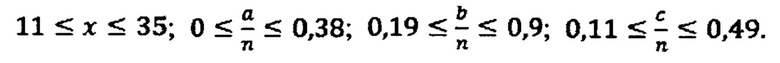
По сравнению с прототипом способ заявляемого является управляемым, высокотехнологичным, экологичным, экономически выгодным.
Полученный гидрогель метилкремниевой кислоты имеет развитые селективные адсорбционные свойства и дополнительно - свойства супрамолекулярных структур, что позволяет использовать его в медицине и ветеринарии как индивидуальное вещество с терапевтическими свойствами, а также в качестве матрицы для комплексных составов с функциями управляемого и/или пролонгированного высвобождения, и/или целевой доставки вещества.
Раствор соли, образованной в результате взаимодействия слабой кислоты и сильного основания осуществляет протекционную функцию несконденсированных гидроксогруп, поскольку кислотность растворов подобных солей щелочная. Полимер характеризуется как подвижный конформационно передорганизованный.
Реакция протекает в трехфазной системе: исходной жидкой, временной газовой и твердой, что формируется. Разветвления полимера в газовой фазе не затруднено противодействием сил вязкости жидкой среды. Итоговый полимер получается с меньшим размером ячейки сетки, что определяет выраженность селективных свойств.
Сформированный гель не обрабатывают кислыми растворами, что не вызывает окончательной конденсации гидроксогруп и позволяет сформировать свойства супрамолекулярных структур и определяет конформационную подвижность. Полученный продукт имеет сорбционные свойства с высокой селективностью и имеет свойства супрамолекулярных структур.
В масштабах промышленной реализации заявленного способа, образованные растворы соли в сточных водах (например, карбонат натрия) не требуют создания дополнительного комплекса по обезвреживанию отходов и их дальнейшего использования или утилизации, что делает технологический процесс экономически выгодным и экологичным.
Изучение особенностей формирования сетчатых полимеров силоксановой группы привело к созданию химической формулы, описывающей одновременно с химическим составом также и топологическую составляющую веществ.
Формирования сетчатой структуры на примере полиметилсилоксанов обусловлено присутствием в составе полимера трех основных фрагментов (Таблица 1):
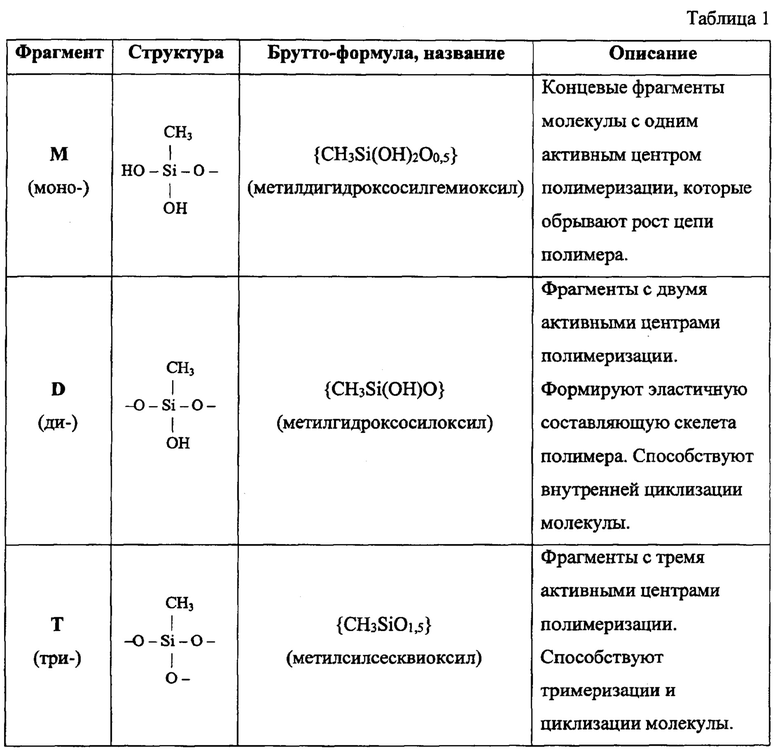
Обобщением приведенного выше является изобретенная химическая формула вида:
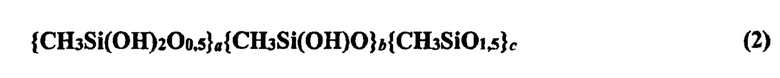
Данная формула уже описывает топологию молекулы полимера в части количественной меры коэффициентов а, b, с
Взаимосвязь формул (1) та (2):
n=а+b+с
k=0,5(с-а)+1
Также формулу (2) можно записать в виде брутто-формы формулы (1) вида:
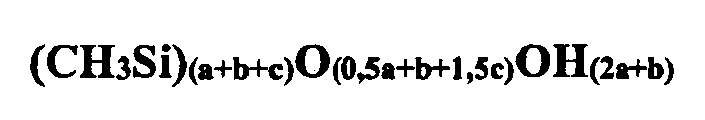
Химическая формула (2) описывает все возможные структуры полиметилсилоксанов. Следует учесть, что с позиций особенностей образования и свойств силоксановой связи недопустимыми [Силоксановая связь. Воронков М.Г., Милешкевич В.П., Южелевский Ю.А. Новосибирск, «Наука», 1976, 413 с.] являются структуры и фрагменты вида:
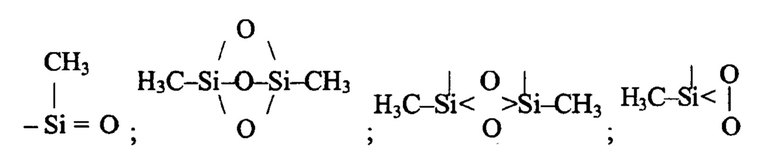
Ввиду сложности экспериментального определения молекулярных масс сетчатых полимеров, было предложено использовать химическую формулу (2) в приведенном виде, а именно:
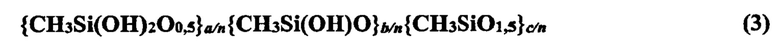
Химическая формула (3) является обобщением химических формул (1) и (2).
Запись данной формулы удобно осуществлять, используя указанные в таблице 1 коды фрагментов. Тогда соединение может быть представлено формулой вида:

или в приведенном виде:

В таблице 2 приведены основные преобразования молекул формулы (4) в процессе поликонденсаций на примере молекул с формулами MaDbTc та MxDyTz.


Изобретена формула описания структур сетчатых полимеров полиорганосилоксаны известного ранее вида [RSiO1,5] имеет вид:
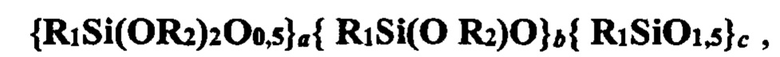
где R1 = CH3, С2Н5, СН2 = СН тому подобное; R2 = H, СН3, С2Н5 и другие
Моделирование молекул и расчеты параметров молекул с размером цепи до 50 звеньев в различных конформациях осуществляли в среде программного комплекса HyperChem 8.09 с применением полуэмпирического квантово-химического метода AMI (расширенный метод Хюккеля), используя в основе теории взаимодействия системы заряженных частиц. Следующую оптимизацию данной системы проводили путем минимизации энергии и ее градиента (скорости изменения энергии) по алгоритму Полака-Рибьера.
Межмолекулярное и внутримолекулярное взаимодействие моделировали на примерах систем, содержащих гидратное окружение, и/или исходные реагенты (точка времени «ноль» к вступлению во взаимодействие), и/или промежуточные продукты реакции и/или продукты реакции поликонденсации.
Оценку геометрических параметров целевых молекул и моделирования самого процесса поликонденсации на основе развитых теорий вероятностных характеристик взаимодействий Флори, Фриша и Степто [P. Flory, Principles of Polymer Chemistry, Cornell University Press, Ithaca, N.Y., 1953] осуществляли путем создания макросов в среде Microsoft Excel с последующей визуализацией топологии полученных систем на основании рандомизации преобразований согласно таблице 2.
Обработку геометрических характеристик молекул проводили путем сопоставления различий нормированных координат атомов кремния в модельных молекулах в присутствии гидратного окружения и без него. Визуализацию полученных данных осуществляли методом нахождения точки, равноудаленной от геометрических координат атомов модели молекулы. В дальнейшем по набору расстояний от равноудаленной точки до атомов молекулы строили топологию молекулы в полярных координатах.
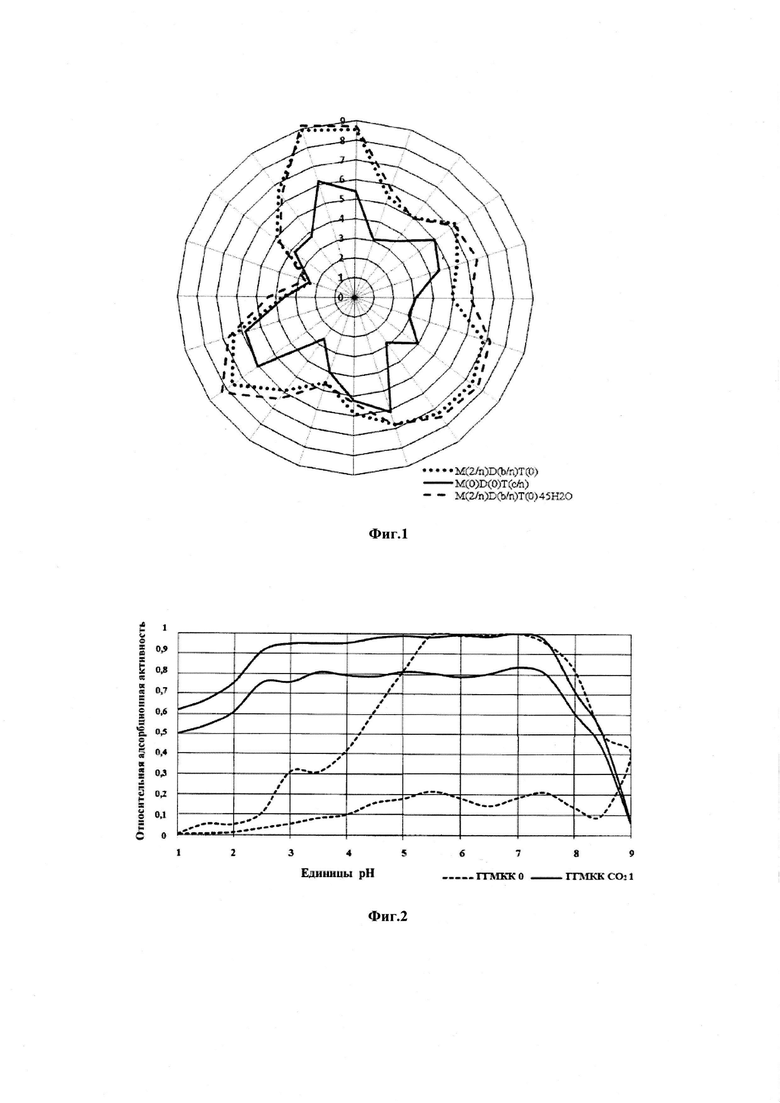
На Фиг. 1 представлен пример топограммы молекул с равным количеством звеньев: полностью циклической 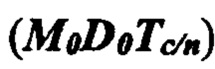 , исходной линейной формы
, исходной линейной формы 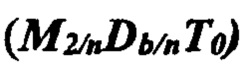 и линейной формы с гидратной оболочкой
и линейной формы с гидратной оболочкой 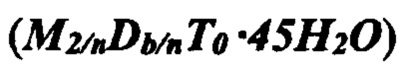 .
.
Как видно из фиг. 1, наличие ОН-групп существенно влияет на конформацию молекулы, а наличие гидратной оболочки не существенного влияет на изменение конформации молекулы.
Общим выводом представленных данных является тот факт, что ОН-группы молекулы как раз и определяют конформационную подвижность молекулы, и изменение определенных условий, провоцирующих как внутримолекулярную, так и межмолекулярную поликонденсацию ОН-групп, приводит к проявлению или отсутствию супрамолекулярных свойств вещества в целом.
Поведение модельной молекулы с гидратной окружением, с разным количеством молекул воды в полостях и вне полостей структур, натолкнуло на позиционирование поведения вещества (гидрогеля метилкремниевой кислоты) в роли надмолекулярных или супрамолекулярных структур по типу «хозяин» относительно веществ, присутствующих в пространстве между молекулами по типу «гость». Дополнительно были промоделированы системы, содержащие различные по химической природе «гостей».
Практическое подтверждение моделей и теории осуществляли с применением разработанных методов исследований и аппаратными методами термогравиметрии, криоскопии, амперометрического титрования, титрования воды по методу К. Фишера, ПК, УФ-ВИД-спектроскопии.
Исследования проводились как на образцах гидрогеля метилкремниевой кислоты, полученных по способу прототипа и на образцах веществ, полученных по заявленному способу.
Исследование свойств полученных веществ по заявленному способу привело к открытию неожиданных эффектов, неизвестных ранее и подтвердило описанную выше гипотезу. Это позволяет позиционировать полученные вещества в дополнение к веществам с адсорбционными свойствами как вещества с супрамолекулярной структурой, обладающие свойствами типа «хозяин-гость» как предорганизованого конформационно подвижного «хозяина» [Супрамолекулярная химия. Пер. с англ.: в 2 т. / Джонатан В. Стыд, Джерри Л. Этвуд. - М.: ИКЦ «Академкнига», 2007].
Условием предорганизованости структуры вещества, полученной по заявленному способу является жесткость его каркаса. В таком случае вещество позиционируется как «хозяин», настроенный на конкретного «гостя» и определяет селективность «хозяина».
Жесткость каркаса обеспечивается наличием в молекуле максимального количества Т-фрагментов, исходя из представленного в таблице 1 и формулах (4) и (5).
С другой стороны, конформационная подвижность молекулы обеспечивается максимальным содержанием ОН-групп. Эластичность и подвижность молекулы обеспечивают D-фрагменты.
Для соответствия условии конформационно подвижной предорганизованой структуры необходимо, чтобы максимальными были значения коэффициентов b/n и c/n в формулах веществ (3) и (5).
Теоретически предъявленным условиям отвечают вещества химических формул (3) и (5) с коэффициентами, значения которых соответствует условию:
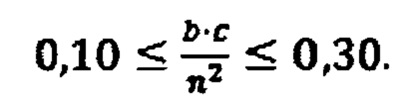
В таком случае диапазоны изменения коэффициентов химической формулы (5) будут:
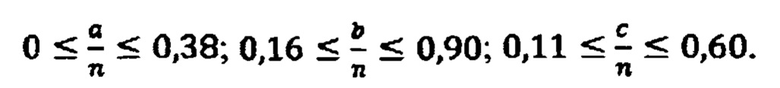
Расчетное содержание ОН-групп соединения составит от 16% до 24%.
Практически добиться условий жесткости каркаса (предорганизованости) и максимальной его конформационной подвижности можно за счет протекции ОН-групп формирующегося полимера, и/или за счет применения фазового перехода в среде формирования молекулы.
В прототипе используют в синтезе стадию обрыва цепи, влиянием слабых растворов сильных кислот, что не приводит к протекции ОН-групп, а наоборот провоцирует их поликонденсацию к равновесной стадии. В результате это приводит к образованию жесткой предорганизованой структуры, которая не имеет свойств типа «хозяин» - «гость», а имеет селективность только за счет адсорбционной емкости создаваемых пор.
Исследование исходных растворов метилсиликонату натрия на предмет определения молекулярных масс растворенных полимеров методом криоскопии исходного и разбавленных растворов привело к выводам о наличии в растворе набора фрагментов с от 4 до 8 мерных звеньев. Проведенное моделирование механики молекул подтверждает их подавляющую линейную структуру. Также причиной линейности молекул является тот факт, что раствор полимера находится в сильно щелочной среде и насыщен ОН-группами щелочи-растворителя.
На основании проведенных исследований, время гелеобразования гидрогелей, полученных по способу прототипа с использованием раствора сильной кислоты различных объемов, путем прилива до фиксированного объема метилсиликоната натрия имеет экспоненциальную зависимость от мольного соотношения компонентов. Это свидетельствует о ходе реакции гелеобразования по радикально-цепному типа, так как гелеобразование происходит и при о наличии малых количеств сильной кислоты. Стадии гелеобразования предложено описывать так:
1. Нейтрализация щелочи до равновесной концентрации;
2. Наращивание длины полимера за счет межмолекулярного взаимодействия (межмолекулярная поликонденсация) полимеров под действием Н+-ионов;
3. Циклизация и тримеризация полимера (конформационная перед организацией скелета);
4. Обрыв цепи;
5. В случае наличия достаточного количества Н+-ионов - внутренне молекулярная поликонденсация (потеря конформационной подвижности молекулы за счет увеличения жесткости скелета). Наступление микросинерезису.
Для сохранения оптимальной конформационной подвижности молекулы необходимым условием является введение стадии протекции ОН-групп молекулы.
За счет того, что в способе получения, описанном в прототипе, одним из компонентов смеси является сильная кислота, а другим - щелочной раствор метилсиликоната натрия, образуется соль сильного щелочи и сильной кислоты, которая не производит протекционного влияния на ОН-гругаты (растворы таких солей имеют близкую к нейтральной кислотность). В этом случае преобразования в системе целиком зависят от соотношения щелочной составляющей, которая уменьшается по мере проведения синтеза и сильнокислотной составляющей.
Данного недостатка удалось избежать в заявленном способе.
Известно, что раствор метилсиликоната натрия содержит катион щелочного металла, поэтому для получения слабой соли, которая могла бы способствовать протекционному воздействию на ОН-группы молекулы, необходимо использовать или кислоты со слабыми анионами, или газообразные кислотные ангидриды.
- Среди большого количества веществ, отвечающих условиям, описанным выше, авторы остановились на использовании газообразных кислых агентов, таких как:
- углекислый газ - CO2;
- оксид серы (IV) - SO2;
- оксид серы (VI) - SO3;
- сероводород - H2S;
- хлороводород - HCl.
Гидрогели метилкремниевой кислоты, полученные по изложенным ниже примерам, подвергались комплексу исследований и неожиданно имели свойства супрамолекулярных соединений.
Анализ полученных данных приводит к выводу, что предпосылкой получения супрамолекулярных структур являются:
- наличие протекционной для ОН-групп составляющей в системе, а протекционное действие оказывает образуемый раствор карбоната натрия (в случае синтеза с применением углекислого газа); сульфита натрия (в случае синтеза с применением оксида серы (IV); сульфида натрия (в случае синтеза с применением сероводорода);
- наличие фазового перехода «газ-жидкость». При этом за счет присутствия газовой фазы циклизация и тримеризация молекулы проходит легче, в отличие от такого же процесса в жидкой фазе (противодействие оказывает вязкость жидкости, которя на порядок больше, чем у газов).
За счет использования при синтезе гидрогелей газообразных слабых кислот и ангидридов слабых кислот в газообразном состоянии выполняются обе предпосылки, что позволило получить образцы с выраженными супрамолекулярная свойствами. При использовании оксида серы (VI) и хлороводорода выполняется лишь вторая предпосылка, и супрамолекулярнисть образцов менее выражена.
Примеры получения гидрогеля метилкремниевой кислоты с супрамолекулярная свойствами:
Пример 1. Получение гидрогеля метилкремниевой кислоты с супрамолекулярная свойствами.
Через 200 мл раствора метилсиликоната натрия (CNaOH = 3,2М; w(ПМС) = 180 г/л) пропустили углекислый газ суммарным объемом 15 литров. Время барботажа - 45 минут. Скорость барботажа 333 млСО2/мин. Способ подачи - через нижний клапан реактора. Процесс проводили в замкнутой системе. Образующийся продукт флотировался в горловине реактора. После окончания процесса, продукт выгружали из реактора, вакуумировали для удаления остаточного газа и отмывали водой, очищенной до значений рН 6,5-7,0 и отсутствия остаточных количеств анионов. Выход продукта 219 г (67% по содержанию полиметилсилоксана в метилсиликонате натрия).
Далее по тексту код образца по примеру - ГГМКК СО2 1
Пример 2. Соотношение исходных компонентов как в примере 1. Способ подачи -через верхний клапан реактора. Процесс проводили в открытой системе. Образующийся продукт флотировался в горловине реактора. Дальнейшие действия, как в примере 1. Выход продукта 232 г (71% по содержанию полиметилсилоксана в метилсиликонате натрия).
Далее по тексту код образца по примеру - ГГМКК СО2 2
Пример 3. Емкость кубической формы объемом 20 литров была заполнена на  углекислым газом. В емкость предварительно был помещен эластичный фторопластовый желоб с бортиками, замкнутый в кольцо, оборудованный поперечными желобками, расположенными под углом 45° в горизонтальной плоскости к основному основном желобу. Конструкция надета на два вала, образуя бесконечную конвейерную ленту. Один из валов был подключен через редуктор к электродвигателю. Угол наклона к емкости составил 15-30°. Линейная скорость движения желобу снизу вверх составляла от 30 до 60 см/мин. Подача раствора метилсиликоната осуществлялась по каплям через гребенку с 6 дюз. Общий объем метилсиликоната натрия - 200 мл. Время осуществления процесса - 20 минут. Скольжение капель метилсиликоната натрия по гидрофобной поверхности желоба в атмосфере СО2 под действием силы тяжести приводит к перемешиванию капли и к дальнейшему ее застыванию. За счет противодействия линейной скорости движения желоба, процесс проходит в условиях, максимально приближенных к свободному падению капли в атмосфере СО2. Дальнейшие действия с продуктом, как в примере 1. Выход продукта 238 г (73% по содержанию полиметилсилоксана в метилсиликонате натрия).
углекислым газом. В емкость предварительно был помещен эластичный фторопластовый желоб с бортиками, замкнутый в кольцо, оборудованный поперечными желобками, расположенными под углом 45° в горизонтальной плоскости к основному основном желобу. Конструкция надета на два вала, образуя бесконечную конвейерную ленту. Один из валов был подключен через редуктор к электродвигателю. Угол наклона к емкости составил 15-30°. Линейная скорость движения желобу снизу вверх составляла от 30 до 60 см/мин. Подача раствора метилсиликоната осуществлялась по каплям через гребенку с 6 дюз. Общий объем метилсиликоната натрия - 200 мл. Время осуществления процесса - 20 минут. Скольжение капель метилсиликоната натрия по гидрофобной поверхности желоба в атмосфере СО2 под действием силы тяжести приводит к перемешиванию капли и к дальнейшему ее застыванию. За счет противодействия линейной скорости движения желоба, процесс проходит в условиях, максимально приближенных к свободному падению капли в атмосфере СО2. Дальнейшие действия с продуктом, как в примере 1. Выход продукта 238 г (73% по содержанию полиметилсилоксана в метилсиликонате натрия).
Далее по тексту код образца по примеру - ГГМКК СО2 3
Пример 4-6. Использованное оборудование и ведения процессов, как описано в примерах 1-3 с той разницей, что в качестве газа использовался оксид серы (IV) - SO2
Выходы продуктов составляли: 228 г (71%); 222 г (68%); 231 г (70%), соотвественно.
Далее по тексту коды образцов по примерам - ГГМКК SO2 4, ГГМКК SO2 5, ГГМКК SO2 6, соотвественно.
Пример 7-9. Использованное оборудование и ведения процессов, как описано в примерах 1-3 с той разницей, что в качестве газа использовался сероводород - H2S
Выходы продуктов составляли: 230 г (67%); 228 г (70%); 220 г (66%), соотвественно.
Далее по тексту коды образцов по примерам - ГГМКК H2S 7, ГГМКК H2S 8, ГГМКК H2S 9, соотвественно.
Пример 10-12. Использованное оборудование и ведения процессов, как описано в примерах 1-3 с той разницей, что в качестве газа использовался оксид серы (VI) - SO3
Выходы продуктов составляли: 242 г (69%); 230 г (68%); 245 г (71%), соотвественно.
Далее по тексту коды образцов по примерам - ГГМКК SO3 10, ГГМКК SO3 11, ГГМКК SO3 12, соотвественно.
Пример 13-15. Использованное оборудование и ведения процессов, как описано в примерах 1-3 с той разницей, что в качестве газа использовался газообразный хлороводород - HCl
Выходы продуктов составляли: 234 г (72%); 236 г (72%); 237 г (68%), соотвественно.
Далее по тексту коды образцов по примерам - ГГМКК HCl 13, ГГМКК HCl 14, ГГМКК HCl 15, соотвественно.
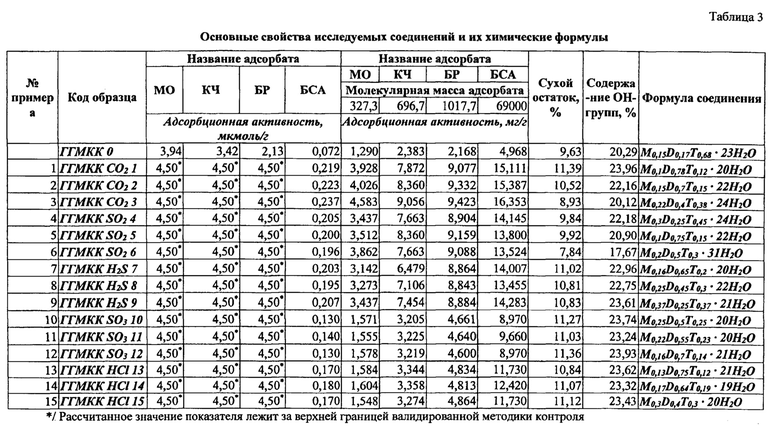
Экспериментальная часть. Гидрогели метилкремниевой кислоты, полученные с известными способами [UA №№82774, C08G 77/00, 2008] (код образца ГГМКК 0) и полученные по способу в примерах 1-15 подлежали исследованию на предмет:
- адсорбционной активности;
- типа структуры;
- наличие свойств по типу «хозяин» - «гость», присущих супрамолекулярным структурам
Адсорбционную активность образцов изучали с применением методик, описанных в [АНД к РП № UA / 2341/01/01 «Гидрогель метилкремниевой кислоты, гель (субстанция) для производства нестерильных лекарственных форм». Заявитель ЗАО «Экологоохранная фирма« КРЕОМА-ФАРМ », Киев, 2004, 10 с].
Как адсорбат использовали: водные растворы индикаторов метилового оранжевого (МО), конго красного (КК), бенгальского розового (БР) и белка - бычьего сывороточного альбумина V (БСА). Для раствора БСА УФ-ВИД-спектрофотометрию проводили для биуретового комплексу после обработки аликвоты раствора белка биуретовым реактивом. При применении приведенной методики контроля адсорбционной активности в отношении образцов, полученных по примерам 1-9 показатели достигали больших значений. Учитывая то, что производители проводят валидацию достоверности полученных данных за пределами номинального значения не более 140% [Государственная Фармакопея Украины / Государственное предприятие «Научно-экспертный центр фармакопейный центр». - 1-е изд. - Дополнение 2. - Харьков: Государственное предприятие «Научно-экспертный центр фармакопейный центр», 2008. - 620 с.], то рабочая способность методики с достоверными значениями составляет 4,50 мкмоль/ч. В случае получения завышенных данных, авторы патента принимали показатели адсорбционной активности в единицах измерения мкмоль/г в виде показателя вида: «больше 4,50 мкмоль/г». Параллельно проводили вычисления значений показателя адсорбционной активности, используя единицы измерения мг/г. Полученные данные показателей адсорбционной активности приведены в таблице 3.
Типы структуры образцов изучали с применением ИК-спектрометрии и смешанного метода определения воды.
Для проведения ИК-спектрометрии предварительно навески образцов помещали в вазелиновое масло и диспергировали до образования однородной суспензии. Образовавшуюся смесь помещали в нагревательной шкафы, нагревали до 150°С и выдерживали при этой температуре в течение 1:00 для полного удаления воды из гидрогеля. После остывания смеси ее повторно диспергировали. Для всех подготовленных образцов осуществляли запись ИК-спектра на ИК-Фурье спектрометре типа IRAffinity-1S. Параллельно осуществляли запись ПК-спектра чистого вазелинового масла для дальнейшего вычитания его из основного спектра.
Описанная методика подготовки проб позволяет изучить непосредственную структуру исследуемого образца с минимальными потерями первичных характеристик, которые теряются при обычном нагреве образцов за счет поликонденсации ОН-групп при нагревании.
Обработку полученных ИК-спектров проводили с применением Фурье преобразований спектров с акцентом на области значений волновых чисел в диапазонах 1200-1000 см-1 (Si-O-Si - связь) и 800-650 см-1 (Скелетные колебания молекулы). В случаях наличия подавляющего числа Т-фрагментов в молекулах наблюдается как увеличение интенсивности линий поглощения в диапазоне 800-650 см-1, так и смещение положения линии в границах диапазона. Для установления зависимости интенсивности от концентрации Т-фрагментов, образцы дополнительно обрабатывали растворами хлористоводородной кислоты различных концентраций, провоцируя поликонденсацию гидрогеля и образования Т-фрагментов согласно схем, приведенных в таблице 2. Точкой отсчета показателя интенсивности на ИК-спектре брали ее значение для полностью обезвоженных образцов (формула M0D0T1).
Для расчета содержания ОН-групп в молекулах применяли смешанный способ определения воды: термогравиметрию и титрование воды по методу К.Фишера. Термогравиметрический способ определения воды применяли, исходя из общепринятых методик проведения подобного контроля. Результаты определения общего количества воды были отправными для дальнейшего расчета состава образцов.
Титрования воды по методу К. Фишера проводили на подготовленных образцах. Подготовка образцов заключалась в предварительном смешивании гидрогеля метилкремниевой кислоты с различными количествами метиловго спирта с известным содержанием воды. Смешивание проводили с применением весового метода. За счет того, что при смешивании с гидрогелем метиловый спирт изначально растворяется в воде гидратной оболочки и частично провоцирует сольватное замещение и поликонденсацию ОН-групп, использование различных соотношений метилового спирта и гидрогеля в экстраполяции на нулевое содержание метилового спирта дает возможность расчета содержания ОН-групп в образце. Итоговое значение содержания ОН-групп в образцах проводили путем вычитания из массы воды, полученной термогравиметрическим методом, массы воды, полученной экстраполяцией на нулевое содержание метилового спирта при титровании воды по методу К.Фишера с последующим умножением результата на два. Результаты расчетов приведены в таблице 3.
В ходе проведенных исследований гидрогели, полученные с известными способами [UA №82774] преимущественно описываются формулами с диапазонами коэффициентов: 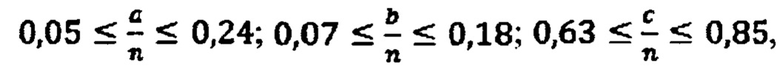 имеют соотношение D- и Т-фрагментов от 0,06 до 0,11 и содержание ОН-групп от 12 до 26%. Гидрогели, полученные по способу описываются формулами с диапазонами коэффициентов:
имеют соотношение D- и Т-фрагментов от 0,06 до 0,11 и содержание ОН-групп от 12 до 26%. Гидрогели, полученные по способу описываются формулами с диапазонами коэффициентов: 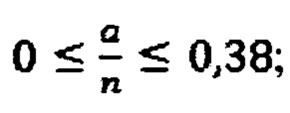
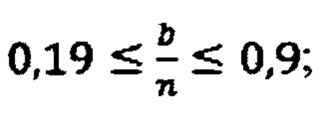
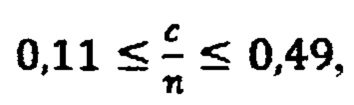 имеют соотношение D- и Т-фрагментов от 0,10 до 0,15 и содержание ОН-групп от 20 до 24%.
имеют соотношение D- и Т-фрагментов от 0,10 до 0,15 и содержание ОН-групп от 20 до 24%.
На основании проведенных исследований обобщающая химическая формула гидрогелей метилкремниевой кислоты, полученных по примерам 1-15 имеет вид:
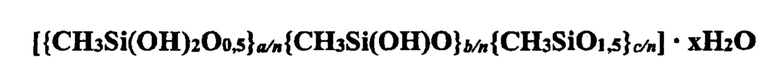
или в сокращенном виде:
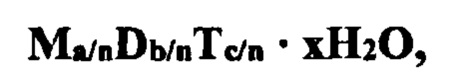
где
11 ≤ х ≤ 35;
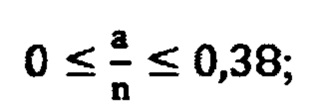
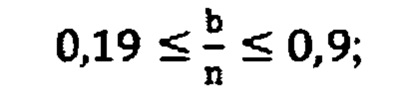
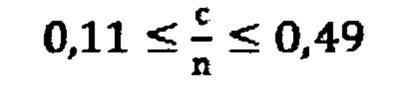
Изучение супрамолекулярных свойств проводили, руководствуясь следующими принципами:
1. Подбор условий изменения конформации молекул гидрогелей. Другими словами - подбор «ключа» для запирания / отпирания «гостя» в «хозяина» [Супрамолекулярная химия. Пер. с англ.: в 2 т./ Джонатан В. Стыд, Джерри Л. Этвуд. - М.: ИКЦ «Академкнига», 2007].
2. Проверка прочности образованного комплекса. Другими словами - «устойчивость к взлому»;
3. Распознавание конкретного «гостя» как свойство селективности.
Для проверки поведения гидрогелей типа «хозяин» - «гость» предварительно делали запись УФ-ВИД-спектров поглощения для эквивалентных растворов указанных веществ (МО, КЧ, БР, БСА) при рН среды в диапазоне от 1,0 до 9,0 и обратно - от 9,0 до 1,0 для растворов адсорбата кроме БСА, и при рН среды в диапазоне от 3,0 до 8,0 и обратно - от 9,0 до 1,0 для растворов БСА. Диапазон температур растворов варьировали от 40 до 60°С для растворов БСА и в диапазоне от 40 до 80°С для растворов других адсорбатов.
Исследование свойств гидрогелей типа «хозяин» - «гость» проводили путем первоначального добавления в систему, содержащую гидрогель и раствор адсорбата, хлористоводородной кислоты в количестве, достаточном для достижения раствором значений рН на уровне 1,0.
Дальнейшее изучение свойств проводили:
- при изменении рН среды путем добавления растворов гидроксида натрия;
- при разведении раствора адсорбата декантациями водой очищенной;
- при нагревании и выдержке при повышенных температурах.
Для возможности сопоставления адсорбционных активностей образцов различных гидрогелей, предварительно измеренную адсорбционную активность в единицах мг/г нормирующих в диапазоне шкалы от 0 до 1 (0-100%).
Изменение относительной адсорбционной активности гидрогелей в зависимости от рН среды представлена на фиг. 2.
Как видно из фиг. 2, образцы гидрогелей, полученных по заявленному способу обладают супрамолекулярным, частично возобновляемой свойством по типу «хозяин» - «гость». В данном случае замыкания «гостя» происходит при достаточно низких значениях рН среды и продолжается в течение значений рН в пределах до 8,5 единиц. Также неожиданным оказалось способность образцов повторно проявлять подобные эффекты. Учитывая то, что значение рН достаточно близки к рН среды человеческого желудка и кишечника, проявления открытых свойств будут полезны с медицинской точки зрения.
Проведение исследований с разведением исходных растворов адсорбатов декантациями водой очищенной и изменением температуры проводили для исключения возможных проявлений у образцов свойств только адсорбционной составляющей.
Образцы гидрогелей, полученных по способу заявляемого обнаружили типичное поведение супрамолекулярных структур по типу «хозяин» - «гость» как передорганизованого конформационно подвижного «хозяина».
Декантации водой очищенной проводили с замером оптической плотности раствора и пересчетом концентрации адсорбата. Гидрогели, полученные по способу заявляемого по мере проведения декантациями водой очищенной частично десорбировали адсорбат в пределах 20-30% (МО, КЧ, БР) и 35-50% (БСА) и по мере изменения рН раствора вели себя подобно графику на фиг. 2.
Нагрев растворов и выдержка при температурах в диапазоне от 40 до 60 (80) ° С не вызывают явных изменений показателей.
| название | год | авторы | номер документа |
|---|---|---|---|
| АДСОРБЕНТ ПОЛИМЕТИЛСИЛОКСАНА ПОЛИГИДРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2761627C1 |
| ГИДРОГЕЛИ МЕТИЛКРЕМНЕВОЙ КИСЛОТЫ КАК АДСОРБЕНТЫ СРЕДНЕМОЛЕКУЛЯРНЫХ МЕТАБОЛИТОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2111979C1 |
| АДСОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2293744C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОГЕЛЕЙ | 2012 |
|
RU2618329C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА НА ОСНОВЕ ГИДРОГЕЛЯ МЕТИЛКРЕМНИЕВОЙ КИСЛОТЫ | 2014 |
|
RU2693695C2 |
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ, СПОСОБНЫЙ К ОБРАЗОВАНИЮ ГИДРОГЕЛЯ, И ГИДРОГЕЛЬ | 2005 |
|
RU2298022C2 |
| Способ получения гидрогеля | 1979 |
|
SU1011052A3 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГИДРОГЕЛЯ | 2016 |
|
RU2641111C1 |
| СПОСОБ ПОПЕРЕЧНОГО СШИВАНИЯ ГИАЛУРОНОВОЙ КИСЛОТЫ, СПОСОБ ПРИГОТОВЛЕНИЯ ИНЪЕКЦИОННОГО ГИДРОГЕЛЯ, ГИДРОГЕЛЬ И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2683286C2 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОПОРИСТЫХ ФОРМОУСТОЙЧИВЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ С ИСПОЛЬЗОВАНИЕМ МИКРОВОЛНОВОГО ИЗЛУЧЕНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2715198C1 |
Изобретение относится к синтезу полиметилсилоксанов (гидрогелей метилкремниевой кислоты). Предложен способ получения гидрогеля метилкремниевой кислоты взаимодействием раствора метилсиликоната натрия с газообразным кислым агентом, который барботируют через раствор метилсиликоната натрия. Образовавшийся продукт флотируют в горловине реактора, потом выгружают из реактора, вакуумируют для удаления остаточного газа и отмывают водой. Предложен также гидрогель, полученный указанным способом. Технический результат – предложенный способ высокотехнологичен и экономически выгоден, а полученные заявленным способом гидрогели имеют повышенную селективность адсорбционных свойств и свойства супрамолекулярных структур. 2 н. и 8 з.п. ф-лы, 2 ил., 3 табл., 15 пр.
1. Способ получения гидрогеля метилкремниевой кислоты со свойствами супрамолекулярных структур, согласно которому используют раствор метилсиликоната натрия, отличающийся тем, что через раствор метилсиликоната натрия, загруженный в реактор, пропускают газообразный кислый агент для осуществления барботажа, образовавшийся продукт флотируют в горловине реактора, после окончания процесса продукт выгружают из реактора, вакуумируют для удаления остаточного газа и отмывают водой, очищенной до значений рН 6,5-7,0 без остаточных количеств анионов, получая гидрогель метилкремниевой кислоты со свойствами супрамолекулярных структур, который описывается формулой:
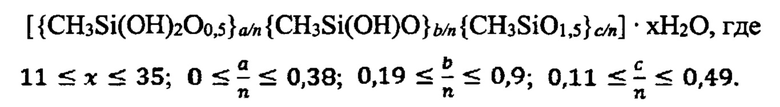
2. Способ по п. 1, отличающийся тем, что время барботажа составляет 45 минут, скорость барботажа - 333 мл газообразного агента в минуту.
3. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют углекислый газ, который подают через нижний клапан реактора, проводя процесс в замкнутой системе.
4. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют углекислый газ, который подают через верхний клапан реактора, проводя процесс в открытой системе.
5. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют оксид серы (IV) - SO2.
6. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют сероводород - H2S.
7. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют оксид серы (VI) - SO3.
8. Способ по п. 1, отличающийся тем, что как газообразный кислый агент используют хлороводород - HCl.
9. Способ по п. 1, отличающийся тем, что метилсиликонат натрия подают по каплям через гребенку по гидрофобной поверхности желоба, размещенной в среде газообразного кислого агента, в течение 20 минут.
10. Гидрогель метилкремниевой кислоты со свойствами супрамолекулярных структур, который описывается формулой:
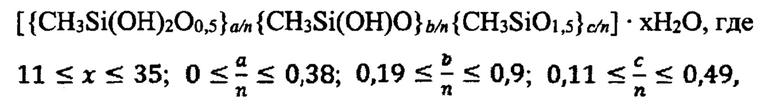
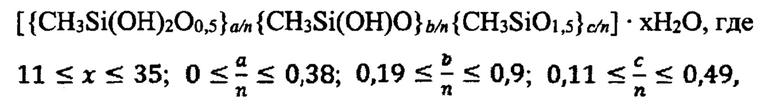
полученный способом по п. 1.
| Самоцентрирующееся приспособление для правильной установки на станке колес крестьянского хода в целях их обработки | 1928 |
|
SU12985A1 |
| ГИДРОГЕЛИ МЕТИЛКРЕМНЕВОЙ КИСЛОТЫ КАК АДСОРБЕНТЫ СРЕДНЕМОЛЕКУЛЯРНЫХ МЕТАБОЛИТОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2111979C1 |
Авторы
Даты
2021-10-06—Публикация
2018-07-09—Подача