Изобретение относится к области медицины, а именно к гинекологии, и может быть использовано для создания экспериментальной модели аденомиоза на крысах линии Wistar.
Известен способ создания экспериментальной модели аденомиоза, в котором новорожденным самкам мышей линии CD 1 в возрасте от 1 до 5 дней вводили перорально тамоксифен (1 мг /кг) (n=27) или эстрадиол (0,1 мг/кг) (n=24). Матки мышей были получены на 2, 5, 10, 15 и 42 дни после рождения. Далее исследовали срезы гистологическим и иммуногистохимическим методами: после воздействия тамоксифена во всех матках отмечались признаки аденомиоза уже на 10-й день - внутренний миометрий был с истончением, отсутствием непрерывности и дезорганизацией. В группе животных, получавших эстрадиол, аденомиоз не наблюдался - все слои матки были развиты нормально, но гипертрофированы, а внутренний миометрий сохранил круговое строение [Mehasseb М.K., Bell S.C., Habiba M.A. The effects of tamoxifen and estradiol on myometrial differentiation and organization during early uterine development in the CD1 mouse // Reproduction (Cambridge, England). 2009. Vol.138. №2. P. 341-350].
Известно исследование Parrott E. и соавт., в котором мышам вводили эстрадиол, тамоксифен, цитрат торемифена или гидрохлорид ралоксифенасо 2 по 5 день после рождения и исследовали гистологические срезы матки на 6, 42 и 90 день. Данные исследования показали, что краткосрочное введение новорожденным мышам тамоксифена и торемифена приводит к созданию модели аденомиоза у значительной части животных к 3-месячному возрасту (на 90 день). Авторы отметили, что уже через 6 дней от рождения матки мышей, получавших тамоксифен и торемифен, но не ралоксифен и эстрадиол, были лишены нормальной дифференцировки слоев гладкой мускулатуры [Parrott Е., Butterworth М., Green A., White I. N., Greaves P. Adenomyosis-a result of disordered stromal differentiation // The American journal of pathology. 2001. Vol. 159. №2. P. 623-630].
Известно исследование Green A.R. и соавт., в котором для создания модели аденомиоза перорально вводили мышам со 2 по 5 день после рождения тамоксифен и ралоксифен, а затем исследовали экспрессию фактора роста нервов (NGF) и родственных ему рецепторов в клетках матки 6-дневных животных. Известно, что во время терминальной миогенной дифференцировки происходит подавление NGF. Результаты исследования продемонстрировали повышение экспрессии фактора роста нервов в 18 раз в просветном эпителии и 25-кратное его повышение во всей матке после введения тамоксифена, что не наблюдалось при введении ралоксифена. Исследование показывает, что за счет подавления NGF регулируется дифференцировка мезенхимальных клеток в миоциты и что раннее нарушение этого процесса играет ключевую роль в развитии аденомиоза [Green A.R., Edwards R.E., Greaves P., White I.N.H. Comparison of the effect of oestradiol, tamoxifen and raloxifene on nerve growth factor-alpha expression in specific neonatal mouse uterine cell types using laser capture microdissection // Journal of molecular endocrinology. 2003. Vol. 30. №LP. 1-12].
Недостатком описанных способов является сложность выполнения эксперимента на новорожденных мышах, отсутствие сведений о точных и экономичных схемах создания экспериментальной модели, характеризующейся высокой воспроизводимостью, об оптимальных сроках выведения животных из эксперимента, связанных с экономическими затратами.
Российских исследований по созданию экспериментальной модели аденомиоза в литературных источниках не обнаружено.
Техническим результатом изобретения является создание высоковоспроизводимой экспериментальной модели аденомиоза на крысах линии Wistar впервые, повышение воспроизводимости способа, более простое и удобное его исполнение по сравнению с мышами, сокращение материальных затрат на проведение эксперимента и длительное содержание животных, разработка точной схемы введения тамоксифена для индукции аденомиоза и определение оптимальных сроков выведения крыс из эксперимента.
Указанный технический результат достигается в способе создания экспериментальной модели аденомиоза на крысах линии Wistar, характеризующемся тем, что новорожденным самкам вводят блокатор рецепторов эстрогенов тамоксифен в дозе 1 мг препарата / 1 кг веса животного перорально однократно со 2 по 5 день неонатального периода и выводят из эксперимента на 30 день после рождения.
Для проведения эксперимента были использованы новорожденные самки крыс линии Wistar. Исследований по созданию экспериментальной модели аденомиозана крысах линии Wistar в литературных источниках не обнаружено.
Для получения аденомиоза крысам вводили блокатор рецепторов эстрогенов (тамоксифен 20 мг) из расчета 1 мг препарата /1 кг веса животного 1 раз в день. По причине лучшей переносимости использовали пероральное, а не подкожное введение препарата [Mehasseb М.K., Bell S.C., Habiba М.А. The effects of tamoxifen and estradiol on myometrial differentiation and organization during early uterine development in the CD1 mouse // Reproduction (Cambridge, England). 2009. Vol. 138. №2. P. 341-350].
Новорожденные крысы были разделены на 4 основные группы для определения наиболее оптимальной схемы введения тамоксифена:
1-я основная группа (n=6) получала препарат со 2 по 5 день постэмбрионального развития (Р2-Р5) один раз в день.
Во 2 основной группе крыс (n=8) препарат применялся с 3 по 8 день жизни (Р3-Р8) один раз в день.
3 основная группа животных (n=7) получала курс тамоксифена дважды: с 3 по 8 день (Р3-Р8) и с 25 по 29 день жизни (Р25-Р29).
4 группа - контрольная, состояла из 5 крыс, которые получали воду без препарата.
Выведение животных из эксперимента проводилось на Р16, Р30 или Р90. Для микроскопического исследования материал (влагалище, матка и яичники) фиксировали в 10% формалине, осуществляли проводку биологического материала и окрашивали гематоксилином и эозином.
По результатам гистологического исследования, в 1 группе аденомиоз наблюдался у всех крыс (n=6): у двух крыс на Р16, у четырех - на Р30. Во 2 группеаденомиоз также был диагностирован у всех животных (n=8): у 6 животных на Р30 и у двух крыс на Р90. В 3 группе аденомиоз был подтвержден у 6 из 7 животных (85,7%), при этом 4 крысы были выведены из эксперимента на Р30 и 3 - на Р90. Аденомиоз не был выявлен у одной крысы, выведенной из эксперимента на Р30, что возможно, связано с техническими трудностями, возникшими при проведении эксперимента.
Таким образом, у 95,2% (20 из 21) крыс из основных групп был гистологически верифицирован аденомиоз, что не отличается от ожидаемого результата, который составляет 100% (р>0,05). В контрольной группе животных (n=5), которых вывели из эксперимента через 90 дней, аденомиоз не наблюдался. Таким образом, на Р90 у животных, принимавших тамоксифен (n=5), аденомиоз развивался, в отличие от контроля, в 100% случаев (р=0,0079). У крыс, вошедших в основную группу, аденомиоз гистологически характеризовался наличием желез эндометрия в миометрий, в отдельных случаях с небольшим количеством стромы эндометрия. Другой особенностью было нарушение концентрических и продольных полос гладких мышц миометрия: вместо регулярных концентрических слоев гладкомышечных клеток у крыс основной группы были обнаружены переплетенные утолщенные полосы гладкомышечных клеток, перемежающиеся со слоями коллагена. Во многих из этих измененных зон наблюдалось наличие полиморфно-ядерных лейкоцитов и эозинофилов, которые отсутствовали у животных контрольной группы.
В связи с тем, что в основной группе на Р30 процент животных с развившимся аленомиозом (92,85%) статистически значимо не отличался от процента животных с аденомиозом, выведенных из эксперимента на Р90 (100%), целесообразно проводить исследование с выводом животных из эксперимента на Р30 (р>0,05). Несмотря на то, что статистически значимых отличий в проценте животных с развившимся аденомиозом на Р16 и Р30 выявлено не было (р>0,05), небольшая выборка исследований, проведенных на Р16 не позволяет рекомендовать выведение животных из эксперимента на этот день.
Способ иллюстрируется фиг. 1-4, где:
на фиг. 1 - макропрепарат матки с влагалищем и яичниками крысы контрольной группы, выведенной из эксперимента на 90 день. Вес препарата 3 г;
на фиг. 2 - макропрепарат матки с влагалищем и яичниками крысы основной группы, получавшей тамоксифен со 2 по 5 день, выведенной из эксперимента на 90 день. Матка увеличена, стенки синюшного цвета. Вес препарата 4,5 г;
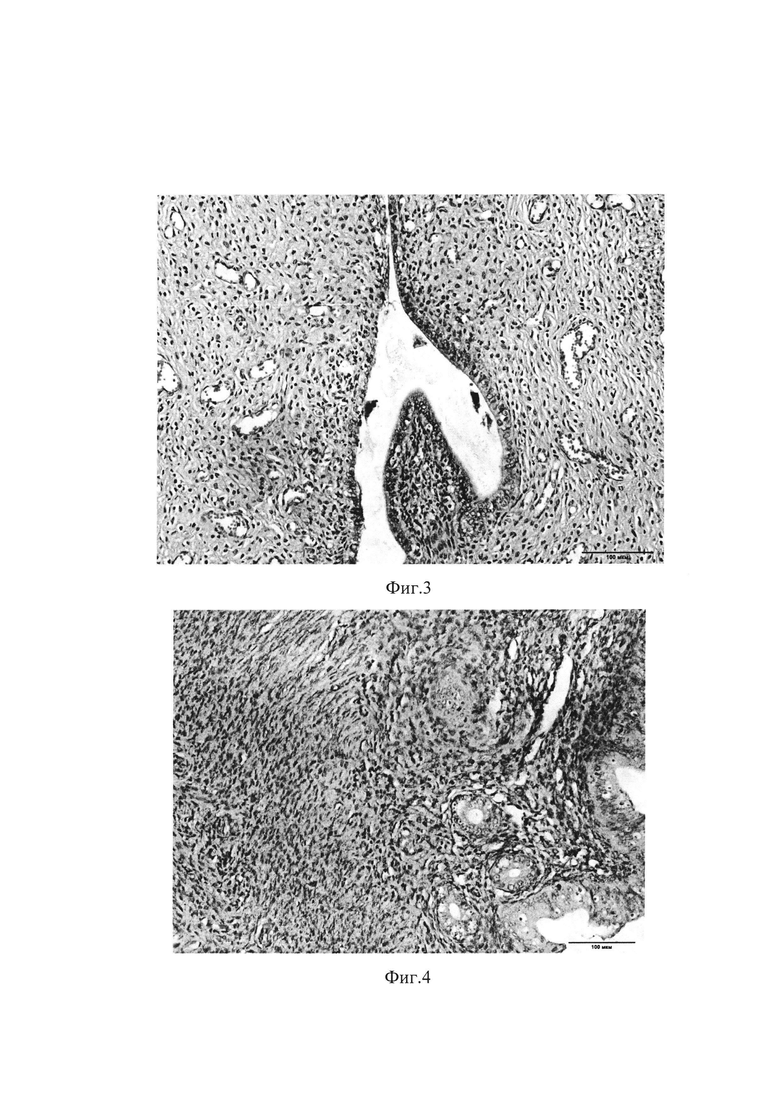
на фиг. 3 - гистологический препарат матки крысы контрольной группы (х200), выведенной из эксперимента на 30 сутки, окраска гематоксилином и эозином. Регулярные концентрические слои гладкомышечных клеток, отсутствие желез и стромы эндометрия в миометрий;
на фиг. 4 - гистологический препарат матки крысы основной 1-ой группы (х200), выведенной из эксперимента на 30 сутки, окраска гематоксилином и эозином. В миометрий визуализируются железы эндометрия, миометрий представлен переплетенными утолщенными полосами гладкомышечных клеток, перемежающимися со слоями коллагена.
Заявляемый способ обеспечивает создание высоковоспроизводимой модели аденомиоза на крысах линии Wistar, более простой и удобной по сравнению с мышами; требует меньших материальных затрат благодаря возможности выведения животных из эксперимента на 30 день постэмбрионального развития, когда выраженность заболевания достаточна и подтверждается при морфологическом исследовании, а также позволяет экономить время и средства благодаря однократному введению тамоксифена по сравнению с нецелесообразным двукратным.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МЕДИКАМЕНТОЗНОГО ЛЕЧЕНИЯ АДЕНОМИОЗА НА ОСНОВАНИИ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ У КРЫС ЛИНИИ WISTAR | 2022 |
|
RU2779227C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ РАКА ЯИЧНИКА В ЭКСПЕРИМЕНТЕ У КРЫС | 2020 |
|
RU2743219C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ В ЭКСПЕРИМЕНТЕ | 2012 |
|
RU2533739C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА В ЭКСПЕРИМЕНТЕ У КРЫС | 2023 |
|
RU2816983C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА НА ОСНОВАНИИ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ У КРЫС | 2019 |
|
RU2711615C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОСТРЕЗЕКЦИОННОЙ ГИПОКАЛЬЦЕМИИ | 2014 |
|
RU2573381C2 |
| Способ формирования модели врожденной диафрагмальной грыжи у плодов крыс с применением нитрофена «ЭКУМ» | 2022 |
|
RU2801603C1 |
| РЕНТГЕНОКОНТРАСТНОЕ СРЕДСТВО | 2011 |
|
RU2448732C1 |
| Способ создания ортотопической модели рака эндометрия | 2024 |
|
RU2818464C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ЗАДЕРЖКИ РАЗВИТИЯ ПЛОДА | 2023 |
|
RU2808475C1 |

Изобретение относится к области медицины, а именно к гинекологии. Способ создания экспериментальной модели аденомиоза на крысах линии Wistar характеризуется тем, что новорожденным самкам вводят блокатор рецепторов эстрогенов тамоксифен в дозе 1 мг препарата / 1 кг веса животного перорально однократно со 2 по 5 день неонатального периода и выводят из эксперимента на 30 день после рождения. Изобретение обеспечивает высоковоспроизводимую модель аденомиоза на крысах линии Wistar, сокращение материальных затрат, позволяет оптимизировать сроки выведения животных из эксперимента при достаточной выраженности заболевания, экономить время и средства при однократном введении тамоксифена по сравнению с нецелесообразным двукратным. 4 ил.
Способ создания экспериментальной модели аденомиоза на крысах линии Wistar, характеризующийся тем, что новорожденным самкам вводят блокатор рецепторов эстрогенов тамоксифен в дозе 1 мг препарата / 1 кг веса животного перорально однократно со 2 по 5 день неонатального периода и выводят из эксперимента на 30 день после рождения.
| СПОСОБ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА НА ОСНОВАНИИ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ У КРЫС | 2019 |
|
RU2711615C1 |
| ЗОРИНА В.Н | |||
| и др | |||
| БЕЛКИ СЕМЕЙСТВА МАКРОГЛОБУЛИНОВ ПРИ АДЕНОМИОЗЕ И МИОМЕ ТЕЛА МАТКИ / Медицинская иммунология, 2015, т | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЧЕРТЕЖЕЙ ДЛЯ ОДНООБРАЗНОЙ РАСКРОЙКИ ПРЕДМЕТОВ ОДЕЖДЫ | 1919 |
|
SU287A1 |
| MEHASSEB M.K | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2021-12-13—Публикация
2021-04-12—Подача