ЗАЯВЛЕНИЕ ОБ ЭЛЕКТРОННОЙ ПОДАЧЕ ПЕРЕЧНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Перечень последовательностей в текстовом формате ASCII, предоставленный в соответствии с 37 CFR. § 1.821 под названием "80783_ST25.txt", размером 15179 байт, созданный 4 апреля 2016 г. и поданный с помощью EFS-WEB, предоставлен вместо бумажной копии. Данный перечень последовательностей тем самым включен в описание данного документа с помощью ссылки с целью его раскрытий.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к кормовым композициям для животных и способам их применения для увеличения привеса у животных.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Корма для животных можно разделить на две группы: (1) концентраты или комбикорма и (2) грубые корма. Концентраты или комбикорма имеют высокую энергетическую ценность, включая жиры, зерновые злаки (ячмень, кукуруза, овес, рожь, пшеница) и побочные продукты их переработки, молотые жмыхи с высоким содержанием белка или жмыхи (сои, рапса, семян хлопка, арахиса и т.п.) и побочные продукты переработки сахарной свеклы, сахарного тростника, сырья животного происхождения и рыбного сырья, которые могут быть получены в виде гранул или крошки. Концентраты или комбикорма могут быть полнорационными, поскольку они способны обеспечить все суточные потребности в пище, или они способны обеспечить часть рациона с дополнением чем-либо еще, что может обеспечить пищевой рацион. Грубый корм включает пастбищные травы, виды сена, силос, корнеплоды, солому и сухой корм из стеблей кукурузы (стебли кукурузы).
Корм составляет наибольшие издержки при выращивании животных для производства продуктов питания. Таким образом, настоящее изобретение относится к композициям и способам повышения эффективности усвояемости корма животным, за счет чего снижаются издержки производства.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте настоящего изобретения предусматривается кормовая композиция для животных, содержащая микробную α-амилазу. В некоторых аспектах микробная α-амилаза содержит полипептид, характеризующийся по меньшей мере 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5.
В другом аспекте настоящего изобретения предусматривается кормовая композиция для животных, содержащая растительный материал, где растительный материал содержит экспрессируемую гетерологичную α-амилазу. В некоторых конкретных вариантах осуществления экспрессируемая гетерологичная α-амилаза кодируется нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержит полипептид, характеризующийся по меньшей мере приблизительно 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1.
В настоящем изобретении дополнительно предусматривается кормовая композиция для животных, содержащая растительный материал из трансгенного растения или части растения, который содержит рекомбинантную α-амилазу, кодируемую нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержащую полипептид, характеризующийся по меньшей мере приблизительно 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1.
В других аспектах в настоящем изобретении предусматривается кукурузный рацион, содержащий растительный материал из трансгенного растения кукурузы или части растения, стабильно трансформированных рекомбинантной α-амилазой, кодируемой нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5. В дополнительных аспектах настоящего изобретения предусматривается кормовая композиция для животных, содержащая кукурузный рацион по настоящему изобретению.
В дополнительном аспекте в настоящем изобретении предусматривается способ увеличения среднесуточного привеса животного, включающий скармливание указанному животному кормовой композиции для животных по настоящему изобретению, при этом среднесуточный привес животного увеличивается на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки.
В дополнительном аспекте настоящего изобретения предусматривается способ увеличения скорости роста (привеса) животного, включающий скармливание указанному животному кормовой композиции для животных по настоящему изобретению, при этом скорость роста животного увеличивается на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки.
В дополнительном аспекте настоящего изобретения предусматривается способ сокращения количества суток, необходимого для достижения требуемого веса у животного, включающий скармливание указанному животному кормовой композиции для животных по настоящему изобретению, за счет чего сокращается количество суток, необходимое для достижения требуемого веса.
В других аспектах предусматривается способ повышения эффективности усвояемости корма животным, при этом способ включает скармливание указанному животному кормовой композиции для животных по настоящему изобретению в количестве, эффективном для повышения эффективности усвояемости корма указанным животным.
Вышеуказанные и другие аспекты настоящего изобретения далее будут описаны более подробно, принимая во внимание другие варианты осуществления, описанные в данном документе. Следует понимать, что настоящее изобретение можно осуществлять в различных формах, и его не следует рассматривать как ограниченное вариантами осуществления, изложенными в данном документе. Наоборот, такие варианты осуществления представлены для того, чтобы данное раскрытие было подробным и полным и полностью передавало объем настоящего изобретения специалисту в данной области техники.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если контекст не указывает иное, то в частности предполагается, что различные признаки настоящего изобретения, описанные в данном документе, можно применять в любой комбинации.
Более того, настоящим изобретением также предполагается, что в некоторых вариантах осуществления настоящего изобретения любой признак или комбинацию признаков, изложенных в данном документе, можно исключить или опустить. С целью иллюстрации, если в описании утверждается, что композиция содержит компоненты А, В и С, то это, в частности, предполагает, что любое из А, В или С или их комбинацию можно опустить и отклонить по отдельности или в любой комбинации.
Если не указано иное, все технические и научные термины, применяемые в данном документе, имеют то же значение, которое обычно понятно специалисту в области техники, к которой относится настоящее изобретение. Терминология, применяемая в данном документе при описании настоящего изобретения, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения настоящего изобретения.
Как предполагается, применяемые в описании настоящего изобретения и прилагаемой формуле изобретения формы единственного числа также включают формы множественного числа, если контекст явно не указывает иное.
Как применяется в данном документе, "и/или" относится к любой и всем возможным комбинациям одного или нескольких соответствующих перечисленных элементов и охватывает их, а также к отсутствию комбинаций при интерпретации в качестве альтернативы ("или").
Термин "приблизительно", применяемый в данном документе при упоминании измеряемой величины, такой как дозировка, количество или период времени и т.п., предназначен для охвата изменений определенного количества на ±20%, ±10%, ±5%, ±1%, ±0,5% или даже ±0,1% (например, количества привеса или предоставляемого корма).
Применяемые в данном документе фразы, такие как "от X до Y" и "от приблизительно X до Y", следует интерпретировать как включающие X и Y. Применяемые в данном документе фразы, такие как "от приблизительно X до Y", означают "от приблизительно X до приблизительно Y". Применяемые в данном документе фразы, такие как "приблизительно X-Y", означают "от приблизительно X до приблизительно Y."
Применяемые в данном документе термины "содержат", "содержит" и/или "содержащий" указывают на присутствие определенных признаков, целых чисел, стадий, действий, элементов и/или компонентов, но не исключают присутствие или добавление одного или нескольких других признаков, целых чисел, стадий, действий, элементов, компонентов и/или их групп.
Применяемая в данном документе переходная фраза "состоящий главным образом из" означает, что объем пункта формулы изобретения следует интерпретировать как охватывающий определенные вещества или стадии, перечисленные в пункте формулы изобретения, а также таковые, которые существенно не влияют на основную и новую характеристику(-и) заявляемого изобретения. Таким образом, термин "состоящий главным образом из", в случае если он применяется в пункте формулы настоящего изобретения, не предназначен для интерпретации как эквивалент термину "содержащий".
Настоящее изобретение относится к композициям и способам повышения эффективности усвояемости корма животным, за счет чего снижаются издержки производства. Авторы настоящего изобретения сделали неожиданное открытие того, что у животных, которым скармливали кормовую композицию для животных, содержащую микробную α-амилазу, может наблюдаться увеличение среднесуточного привеса или скорости роста, повышение эффективности усвояемости корма или требоваться сокращенное количество суток для достижения требуемого веса по сравнению с животными, которым не скармливали указанную кормовую композицию.
Соответственно, в одном аспекте настоящего изобретения предусматривается кормовая композиция для животных, содержащая микробную α-амилазу. В дополнительных аспектах настоящего изобретения микробная α-амилаза содержит полипептид, характеризующийся по меньшей мере 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, характеризующейся по меньшей мере 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5. В некоторых вариантах осуществления α-амилаза является жидкой. Таким образом, в некоторых вариантах осуществления настоящего изобретения кормовая композиция для животных по настоящему изобретению может представлять собой добавку, содержащую жидкую микробную α-амилазу, которую можно добавлять к корму, предоставляемому животному.
В другом аспекте в настоящем изобретении предусматривается кормовая композиция для животных, содержащая растительный материал, где растительный материал содержит экспрессируемую гетерологичную α-амилазу. В некоторых конкретных вариантах осуществления экспрессируемая рекомбинантная α-амилаза кодируется нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержит полипептид, характеризующийся по меньшей мере приблизительно 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1. Таким образом, в дополнительных вариантах осуществления настоящего изобретения предусматривается кормовая композиция для животных, содержащая растительный материал из трансгенного растения или части растения, который содержит рекомбинантную α-амилазу, кодируемую нуклеотидной последовательностью, характеризующейся по меньшей мере приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержащую полипептид, характеризующийся по меньшей мере приблизительно 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1.
В конкретных вариантах осуществления трансгенное растение или часть растения могут содержать от приблизительно 1 до приблизительно 100% по весу растительного материала. Таким образом, например, трансгенное растение или часть растения могут содержать приблизительно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% по весу растительного материала, и т.п., или любой диапазон в указанных пределах. Таким образом, в некоторых вариантах осуществления растительный материал может предусматривать один или несколько различных типов растений. Таким образом, например, растительный материал может происходить из растения, в котором экспрессируется рекомбинантная или гетерологичная (например, микробная) α-амилаза. В других вариантах осуществления растительный материал содержит, состоит главным образом из или состоит из материала из растения, в котором экспрессируется рекомбинантная или гетерологичная (например, микробная) α-амилаза, и материала из растения, в котором указанная рекомбинантная или гетерологичная α-амилаза не экспрессируется (например, товарного растения). Таким образом, в некоторых вариантах осуществления, если растительный материал содержит материал из растения, в котором экспрессируется рекомбинантная или гетерологичная (например, микробная) α-амилаза, и материал из растения, в котором указанная рекомбинантная или гетерологичная α-амилаза не экспрессируется (например, товарного растения), то материал из растения, в котором экспрессируется рекомбинантная или гетерологичная (например, микробная) α-амилаза, может содержать от приблизительно 1% до приблизительно 99% по весу растительного материала, и материал из растения, не экспрессирующего указанную рекомбинантную или гетерологичную α-амилазу, может содержать от приблизительно 99% до приблизительно 1% по весу растительного материала.
В дополнительных вариантах осуществления растительный материал может составлять от приблизительно 5% до приблизительно 100% по весу кормовой композиции для животных. Таким образом, например, растительный материал может составлять приблизительно 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% по весу кормовой композиции для животных, и т.п., и/или любой диапазон в указанных пределах.
Корм для животных по настоящему изобретению может быть в любой форме, пригодной для настоящего изобретения. Таким образом, в некоторых вариантах осуществления форма корма для животных может представлять собой без ограничения гранулы, в том числе один или несколько типов смешанных зерен (т.е. смешанное зерно), смесь зерна и гранул, силос, ядра сухого плющения, хлопья из ядер, полученные при воздействии пара, цельные ядра, грубодробленые ядра (например, грубодробленое ядро кукурузы), кукурузу с высокой влажностью и/или любую их комбинацию. В некоторых вариантах осуществления корм для животных может содержать другие компоненты, в том числе без ограничения грубодробленые ядра, влажную зерновую барду, сухую зерновую барду, кукурузный силос, добавки/жидкие добавки, корм на основе кукурузной клейковины и/или измельченное сено.
Применяемый в данном документе термин "растительный материал" включает в себя любую часть растения, в том числе без ограничения эндосперм, эмбрионы (зародыш), перикарп (оболочка отрубей), ножку (корневой чехлик), пыльцу, яйцеклетки, семена (зерно), листья, цветки, ветки, стебли, плоды, ядра, колосья, початки, шелуху, цветоножки, корни, корневые кончики, пыльники, клетки растения, в том числе клетки растения, которые являются интактными в растениях и/или частях растений, протопласты растений, ткани растений, клетки растения из тканевых культур, каллусы растений, скопления клеток растения и т.п. Кроме того, "клетка растения", как применяется в данном документе, относится к структурной и физиологической единице растения, которая содержит клеточную стенку, а также может относиться к протопласту. Клетка растения по настоящему изобретению может находиться в форме выделенной единичной клетки, или может представлять собой клетку из культуры, или может быть частью более высокоорганизованной единицы, такой как, например, ткань растения или орган растения. "Протопласт" представляет собой выделенную клетку растения без клеточной стенки или только с частями клеточной стенки. Таким образом, в некоторых вариантах осуществления настоящего изобретения трансгенное растение или часть растения, которые содержат рекомбинантную α-амилазу, кодируемую нуклеотидной последовательностью по настоящему изобретению, содержат клетку, которая содержит указанную рекомбинантную α-амилазу, кодируемую нуклеотидной последовательностью по настоящему изобретению, где клетка представляет собой клетку любого растения или части растения, в том числе без ограничения клетку корня, клетку листа, клетку тканевой культуры, клетку семени, клетку цветка, клетку плода, клетку пыльцы и т.п. В иллюстративных вариантах осуществления растительный материал может представлять собой семя или зерно.
Растительный материал может происходить из любого растения. В некоторых вариантах осуществления растительный материал происходит из растения, в котором может экспрессироваться рекомбинантная или гетерологичная (например, микробная) α-амилаза. Кроме того, как обсуждалось в данном документе, в других вариантах осуществления растительный материал может представлять собой смесь растительного материала из растения, в котором экспрессируется рекомбинантная или гетерологичная (например, микробная) α-амилаза, и из растения, в котором указанная рекомбинантная или гетерологичная α-амилаза не экспрессируется (например, товарного растения). Таким образом, в иллюстративных вариантах осуществления растительный материал может представлять собой смесь растительного материала из обычного "товарного" растения (например, товарной кукурузы) и растительного материала из трансгенного растения по настоящему изобретению, экспрессирующего рекомбинантную или гетерологичную α-амилазу.
Таким образом, в некоторых вариантах осуществления растительный материал может происходить из растения кукурузы, растения сорго, растения пшеницы, растения ячменя, растения ржи, растения овса, растения риса и/или растения проса. В иллюстративных вариантах осуществления растительный материал может происходить из растения кукурузы. В других вариантах осуществления растительный материал может представлять собой семя или зерно из растения кукурузы. В конкретных вариантах осуществления растительный материал может представлять собой растение кукурузы, предусматривающее трансформант кукурузы 3273 (см. патент США №8093453).
В некоторых вариантах осуществления в настоящем изобретении предусматривается "общий смешанный рацион", содержащий растительный материал из трансгенного растения кукурузы или части растения, стабильно трансформированных рекомбинантной α-амилазой, кодируемой нуклеотидной последовательностью, характеризующейся приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержащей полипептид, характеризующийся по меньшей мере 80%) идентичностью с аминокислотной последовательностью под SEQ ID NO: 1. Как применяется в данном документе, "общий смешанный рацион" может означать суточную норму корма для отдельного животного, который включает, например, растительный материал из трансгенного растения кукурузы или части растения (например, ядра кукурузы, грубодробленое зерно кукурузы и т.п.), добавки и дополняющие вещества (например, витамины и минералы) и/или "грубые корма" (например, пастбищные травы, виды сена, силос, корнеплоды, солому и сухой корм из стеблей кукурузы (стебли кукурузы)).
В некоторых вариантах осуществления растительный материал из трансгенного растения кукурузы или части растения составляет от приблизительно 1% до приблизительно 100% по весу общего смешанного рациона. Таким образом, например, трансгенное растение или часть растения могут составлять приблизительно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% по весу растительного материала, и т.п., и/или любой диапазон в указанных пределах.
В других вариантах осуществления предусматривается кормовая композиция для животных, которая содержит общий смешанный рацион по настоящему изобретению. В некоторых вариантах осуществления общий смешанный рацион может составлять от приблизительно 5% до приблизительно 100% по весу кормовой композиции для животных. Таким образом, например, общий смешанный рацион может составлять приблизительно 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%о, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%), 99%, 100% по весу кормовой композиции для животных и т.п. или любой диапазон в указанных пределах. В иллюстративных вариантах осуществления общий смешанный рацион составляет приблизительно 50% кормовой композиции для животных.
В еще одних дополнительных вариантах осуществления настоящего изобретения предусматривается кукурузный рацион, содержащий растительный материал из трансгенного растения кукурузы или части растения, стабильно трансформированных рекомбинантной α-амилазой, кодируемой нуклеотидной последовательностью, характеризующейся приблизительно 80% идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, или содержащей полипептид, характеризующийся по меньшей мере 80% идентичностью с аминокислотной последовательностью под SEQ ID NO: 1. Как применяется в данном документе, "кукурузный рацион" означает суточную норму кукурузы для отдельного животного.
В некоторых вариантах осуществления растительный материал из трансгенного растения кукурузы или части растения составляет от приблизительно 1% до приблизительно 100% по весу кукурузного рациона. Таким образом, например, трансгенное растение или часть растения могут содержать приблизительно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% по весу растительного материала, и т.п., и/или любой диапазон в указанных пределах.
В других вариантах осуществления предусматривается кормовая композиция для животных, которая содержит кукурузный рацион по настоящему изобретению. В некоторых вариантах осуществления кукурузный рацион может составлять от приблизительно 5% до приблизительно 100% по весу кормовой композиции для животных. Таким образом, например, кукурузный рацион может составлять приблизительно 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% по весу кормовой композиции для животных и т.п. и/или любой диапазон в указанных пределах. В иллюстративных вариантах осуществления кукурузный рацион составляет приблизительно 50% кормовой композиции для животных.
В некоторых вариантах осуществления общий смешанный рацион может предусматривать влажный корм из кукурузной клейковины, содержание которого может составлять от приблизительно 10% до приблизительно 40% по весу кормовой композиции для животных. В дополнительных вариантах осуществления общий смешанный рацион может предусматривать влажный корм из кукурузной клейковины, содержание которого может составлять приблизительно 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40% по весу кормовой композиции для животных.
В других вариантах осуществления общий смешанный рацион может предусматривать модифицированную зерновую барду с растворимыми веществами, содержание которой может составлять от приблизительно 5% до приблизительно 25% по весу кормовой композиции для животных. В дополнительных вариантах осуществления общий смешанный рацион может предусматривать модифицированную зерновую барду с растворимыми веществами, содержание которой может составлять приблизительно 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25% по весу кормовой композиции для животных.
В дополнительных вариантах осуществления общий смешанный рацион может предусматривать влажную зерновую барду с растворимыми веществами, содержание которой может составлять от приблизительно 5% до приблизительно 25% по весу кормовой композиции для животных. В дополнительных вариантах осуществления общий смешанный рацион может предусматривать влажную зерновую барду с растворимыми веществами, содержание которой может составлять приблизительно 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25% по весу кормовой композиции для животных.
Различные нуклеиновые кислоты или белки, характеризующиеся гомологией, в данном документе называются "гомологами". Термин "гомолог" включает гомологичные последовательности от одного и того же вида и других видов, а также ортологичные последовательности от одного и того же вида и других видов. Выражение "гомология" относится к уровню сходства между двумя или более последовательностями нуклеиновых кислот и/или аминокислотными последовательностями, выраженному в виде процента идентичности по положениям (т.е. сходства или идентичности последовательностей). Гомология также относится к представлению о сходных функциональных свойствах различных нуклеиновых кислот или белков. Таким образом, композиции и способы по настоящему изобретению дополнительно включают гомологи нуклеотидных последовательностей и полипептидных последовательностей по настоящему изобретению (например, SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5). Как применяется в данном документе, "ортологичный" относится к гомологичным нуклеотидным последовательностям и/или аминокислотным последовательностям у различных видов, которые возникли от общего предкового гена в процессе видообразования. Гомолог по настоящему изобретению характеризуется значительной идентичностью последовательности (например, 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, и/или 100% к SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 или SEQ ID NO: 5.
Гомолог SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5 может использоваться с любой кормовой композицией или способом по настоящему изобретению, отдельно или в комбинации друг с другом, и/или с SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5.
Как применяется в данном документе, "идентичность последовательностей" относится к степени инвариантности двух оптимально выровненных последовательностей полинуклеотидов или пептидов по всему окну выравнивания компонентов, например, нуклеотидов или аминокислот. "Идентичность" можно легко вычислить с помощью известных способов, включая без ограничения те, что описаны в Computational Molecular Biology (Lesk, A.M., ed.) Oxford University Press, New York (1988); Biocomputing: Informatics and Genome Projects (Smith, D.W., ed.) Academic Press, New York (1993); Computer Analysis of Sequence Data, Part I (Griffin, A.M., and Griffin, H.G., eds.) Humana Press, New Jersey (1994); Sequence Analysis in Molecular Biology (von Heinje, G., ed.) Academic Press (1987); и Sequence Analysis Primer (Gribskov, M. and Devereux, J., eds.) Stockton Press, New York (1991).
Применяемые в данном документе термины "процент идентичности последовательностей" или "процент идентичности" относятся к процентной доле идентичных нуклеотидов в линейной последовательности полинуклеотида в эталонной ("запрашиваемой") молекуле полинуклеотида (или ее комплементарной нити) по сравнению с тестируемой ("испытуемой") молекулой полинуклеотида (или ее комплементарной нитью), в случае если две последовательности оптимально выровнены. В некоторых вариантах осуществления "процент идентичности" может относиться к процентной доле идентичных аминокислот в аминокислотной последовательности.
Фраза "в значительной степени идентичные", применительно к двум молекулам нуклеиновой кислоты, нуклеотидным последовательностям или белковым последовательностям, относится к двум или более последовательностям или подпоследовательностям, которые по меньшей мере на приблизительно 70%, по меньшей мере на приблизительно 75%, по меньшей мере на приблизительно 80%, по меньшей мере на приблизительно 81%, по меньшей мере на приблизительно 82%, по меньшей мере на приблизительно 83%, по меньшей мере на приблизительно 84%, по меньшей мере на приблизительно 85%, по меньшей мере на приблизительно 86%, по меньшей мере на приблизительно 87%, по меньшей мере на приблизительно 88%, по меньшей мере на приблизительно 89%, по меньшей мере на приблизительно 90%, по меньшей мере на приблизительно 95%, по меньшей мере на приблизительно 96%, по меньшей мере на приблизительно 91%, по меньшей мере на приблизительно 98% или по меньшей мере на приблизительно 99% идентичны нуклеотидам или аминокислотным остаткам при сравнении и выравнивании на максимальное соответствие, которое измеряют с помощью одного из следующих алгоритмов сравнения последовательностей, описанных в данном документе и известных из уровня техники, или с помощью визуального просмотра. В некоторых вариантах осуществления настоящего изобретения значительная идентичность существует в пределах области последовательностей, длина которой составляет по меньшей мере от приблизительно 50 остатков до приблизительно 200 остатков, от приблизительно 50 остатков до приблизительно 150 остатков и т.п. Таким образом, в некоторых вариантах осуществления по настоящему изобретению значительная идентичность существует в пределах области последовательностей, длина которой составляет по меньшей мере приблизительно 50, приблизительно 60, приблизительно 70, приблизительно 80, приблизительно 90, приблизительно 100, приблизительно 110, приблизительно 120, приблизительно 130, приблизительно 140, приблизительно 150, приблизительно 160, приблизительно 170, приблизительно 180, приблизительно 190, приблизительно 200 остатков или больше. В дополнительном варианте осуществления последовательности в значительной степени идентичны по всей длине кодирующих областей. Кроме того, в иллюстративных вариантах осуществления в значительной степени идентичные нуклеотидные или белковые последовательности выполняют, по сути, ту же функцию (например, α-амилазная активность). Таким образом, в некоторых конкретных вариантах осуществления последовательности являются в значительной степени идентичными в пределах по меньшей мере приблизительно 150 остатков и обладают α-амилазной активностью.
При сравнении последовательностей одна последовательность обычно выступает в качестве эталонной последовательности, с которой сравнивают тестируемые последовательности. При применении алгоритма сравнения последовательностей тестируемые и эталонные последовательности вводят в компьютер, при необходимости задают координаты подпоследовательности и задают программные параметры алгоритма сравнения последовательностей. Затем с помощью алгоритма сравнения последовательностей на основе заданных программных параметров вычисляют процентную идентичность последовательностей для тестируемой(-ых) последовательности(-ей) относительно эталонной последовательности.
Оптимальное выравнивание последовательностей для выравнивания в окне сравнения хорошо известно специалистам в данной области техники и может проводиться с помощью инструментов, таких как алгоритм поиска локальной гомологии Смита-Уотермана, алгоритм выравнивания областей гомологии Нидлмана-Вунша, способ поиска сходства по Пирсону-Липману, и необязательно с помощью компьютеризированных путей реализации данных алгоритмов, таких как GAP, BESTFIT, FASTA и TFASTA, доступных как часть GCG® Wisconsin Package® (Accelrys Inc., Сан-Диего, Калифорния). "Доля идентичности" для выровненных сегментов тестируемой последовательности и эталонной последовательности представляет собой число идентичных компонентов, которые являются общими для двух выровненных последовательностей, разделенное на общее число компонентов в сегменте эталонной последовательности, т.е. всей эталонной последовательности или меньшей определенной части эталонной последовательности. Процентная идентичность последовательностей представлена как доля идентичности, умноженная на 100. Сравнение одной или нескольких полинуклеотидных последовательностей может проводиться с полноразмерной полинуклеотидной последовательностью или ее частью либо с более длинной полинуклеотидной последовательностью. Для целей настоящего изобретения "процент идентичности" может быть также определен с применением BLASTX версии 2.0 для транслируемых нуклеотидных последовательностей и BLASTN версии 2.0 для полинуклеотидных последовательностей.
Программное обеспечение для проведения анализов BLAST общедоступно благодаря Национальному центру биотехнологической информации. Данный алгоритм предусматривает изначальную идентификацию пар последовательностей с наибольшим сходством (HSP) путем идентификации коротких "слов" длиной W в запрашиваемой последовательности, которые либо совпадают, либо удовлетворяют некоторому положительному пороговому баллу Т при выравнивании со "словом" такой же длины в последовательности из базы данных. Т называется пороговым показателем соседнего "слова" (Altschul et al., 1990). Эти исходные совпадения соседних "слов" выступают в качестве затравки для начала поисков с целью обнаружения более длинных HSP, содержащих их. Затем совпадения "слов" продлеваются в обоих направлениях вдоль каждой последовательности до тех пор, пока может увеличиваться совокупный показатель выравнивания. Совокупные показатели рассчитывают с применением, в случае нуклеотидных последовательностей, параметров М (балл-вознаграждение, начисляемый за пару совпадающих остатков; всегда >0) и N (штрафной балл, начисляемый за несовпадающие остатки; всегда <0). В случае аминокислотных последовательностей, для расчета совокупного показателя применяют матрицу замен. Продление совпадений "слов" в каждом направлении прекращается, когда совокупный показатель выравнивания снижается на величину X от его максимального достигнутого значения, при этом совокупный показатель падает до нуля или ниже вследствие накопления одного или нескольких выравниваний остатков с отрицательными показателями, либо в случае достижения конца одной из последовательностей. Параметры W, Т и X алгоритма BLAST определяют чувствительность и скорость выравнивания. В программе BLASTN (для нуклеотидных последовательностей) по умолчанию используется длина "слова" (W), равная 11, ожидаемое значение (Е), равное 10, пороговое значение, равное 100, М=5, N=-4 и сравнение обеих нитей. Для аминокислотных последовательностей в программе BLASTP по умолчанию используется длина "слова" (W), равная 3, ожидаемое значение (Е), равное 10, а также матрица замен BLOSUM62 (см. Henikoff & Henikoff, Proc Natl Acad. Sci USA 89: 10915 (1989)).
В дополнение к расчету процентной идентичности последовательностей алгоритм BLAST также выполняет статистический анализ сходства между двумя последовательностями (см., например, Karlin & Altschul, Proc. Nat'l. Acad. Sci. USA 90: 5873-5787 (1993)). Одной мерой сходства, предоставляемой алгоритмом BLAST, является наименьшая суммарная вероятность (P(N)), являющаяся показателем вероятности, согласно которому совпадения между двумя нуклеотидными или аминокислотными последовательностями будут наблюдаться случайным образом. Например, тестируемая последовательность нуклеиновой кислоты считается подобной эталонной последовательности, если наименьшая суммарная вероятность при сравнении тестируемой нуклеотидной последовательности с эталонной нуклеотидной последовательностью составляет от менее приблизительно 0,1 до менее приблизительно 0,001. Таким образом, в некоторых вариантах осуществления настоящего изобретения наименьшая суммарная вероятность при сравнении тестируемой нуклеотидной последовательности с эталонной нуклеотидной последовательностью составляет менее приблизительно 0,001.
Две нуклеотидные последовательности также могут считаться в значительной степени идентичными, если две последовательности гибридизируются друг с другом при жестких условиях. В некоторых иллюстративных вариантах осуществления две нуклеотидные последовательности, которые считаются в значительной степени идентичными, гибридизируются друг с другом при очень жестких условиях.
"Жесткие условия гибридизации" и "жесткие условия отмывки при гибридизации" в контексте экспериментов по гибридизации нуклеиновых кислот, таких как Саузерн- и Нозерн-гибридизация, зависят от последовательности и отличаются при разных параметрах окружающей среды. Расширенное руководство по гибридизации нуклеиновых кислот можно найти в Tijssen Laboratory Techniques in Biochemistry and Molecular Biology-Hybridization with Nucleic Acid Probes, часть 1, глава 2 "Overview of principles of hybridization and the strategy of nucleic acid probe assays" Elsevier, New York (1993). Как правило, условия гибридизации и отмывки высокой жесткости выбирают так, чтобы температура была приблизительно на 5°С ниже точки плавления (Tm) для конкретной последовательности при определенных ионной силе и значении рН.
Значение Tm представляет собой температуру (при определенных ионной силе и значении рН), при которой 50% целевой последовательности гибридизируется с точно совпадающим зондом. Для очень жестких условий выбирают температуру, равную Tm для конкретного зонда. Примером жестких условий гибридизации для гибридизации комплементарных последовательностей нуклеотидов, которые имеют более 100 комплементарных остатков на фильтре при Саузерн- или Нозерн-блоттинге, является 50% формамид с 1 мг гепарина при 42°С, при этом гибридизацию проводят в течение ночи. Примером условий отмывки высокой жесткости является 0,15 М NaCl при 72°С в течение приблизительно 15 минут. Примером жестких условий отмывки является отмывка с помощью 0,2х SSC при 65°С в течение 15 минут (описание буфера SSC см. в Sambrook ниже). Часто с целью избавления от фонового сигнала зонда отмывке в условиях высокой жесткости предшествует отмывка в условиях низкой жесткости. Примером условий отмывки средней жесткости для дуплекса, например с более чем 100 нуклеотидами, является 1x SSC при 45°С в течение 15 минут. Примером условий отмывки низкой жесткости для дуплекса, например с более чем 100 нуклеотидами, является 4-6х SSC при 40°С в течение 15 минут. Для коротких зондов (например, длиной от приблизительно 10 до 50 нуклеотидов) жесткие условия обычно предусматривают концентрации солей, составляющие менее чем приблизительно 1,0 М ионов Na, как правило концентрации, составляющие приблизительно 0,01-1,0 М ионов Na (или других солей) при рН 7,0-8,3, а также температуру, как правило равную по меньшей мере приблизительно 30°С. Жесткие условия также могут быть достигнуты с добавлением дестабилизирующих средств, таких как формамид. В целом, соотношение сигнал-шум, в 2 (или более) раза превышающее наблюдаемое для несвязанного зонда при конкретном гибридизационном анализе, указывает на выявление специфической гибридизации. Нуклеотидные последовательности, которые не гибридизируются друг с другом в жестких условиях, все еще являются в значительной степени идентичными, если белки, которые они кодируют, в значительной степени идентичны. Это может происходить, например, если копия нуклеотидной последовательности создана с применением максимальной вырожденности кодонов, допускаемой генетическим кодом.
Ниже приводятся примеры комплексов условий гибридизации/отмывки, которые можно применять для клонирования гомологичных нуклеотидных последовательностей, являющихся в значительной степени идентичными эталонным нуклеотидным последовательностям (например, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5). В одном варианте осуществления эталонная нуклеотидная последовательность гибридизируется с "тестируемой" нуклеотидной последовательностью в 7% додецилсульфате натрия (SDS), 0,5 М NaPO4, 1 мМ EDTA при 50°С с отмывкой в 2Х SSC, 0,1% SDS при 50°С. В другом варианте осуществления эталонная нуклеотидная последовательность гибридизируется с "тестируемой" нуклеотидной последовательностью в 7% додецилсульфате натрия (SDS), 0,5 М NaPO4, 1 мМ EDTA при 50°С с отмывкой в 1X SSC, 0,1% SDS при 50°С или в 7% додецилсульфате натрия (SDS), 0,5 М NaPO4, 1 мМ EDTA при 50°С с отмывкой в 0,5Х SSC, 0,1% SDS при 50°С. В еще одних вариантах осуществления эталонная нуклеотидная последовательность гибридизируется с "тестируемой" нуклеотидной последовательностью в 7% додецилсульфате натрия (SDS), 0,5 М NaPO4, 1 мМ EDTA при 50°С с отмывкой в 0,1Х SSC, 0,1% SDS при 50°С или в 7% додецилсульфате натрия (SDS), 0,5 М NaPO4, 1 мМ EDTA при 50°С с отмывкой в 0,1Х SSC, 0,1% SDS при 65°С.
В конкретных вариантах осуществления дополнительным свидетельством того, что две нуклеотидные последовательности или две полипептидные последовательности в значительной степени идентичны, может быть то, что белок, кодируемый первой нуклеиновой кислотой, характеризуется иммунологической перекрестной реактивностью с белком, кодируемым второй нуклеиновой кислотой, или специфически с ним связывается. Таким образом, в некоторых вариантах осуществления полипептид может быть в значительной степени идентичным второму полипептиду, например, если два полипептида отличаются только консервативными заменами.
Соответственно, в некоторых вариантах осуществления настоящего изобретения предусматриваются нуклеотидные последовательности, характеризующиеся значительной идентичностью последовательности с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5. "Значительная идентичность последовательности" или "значительное сходство последовательности" означают идентичность или сходство с другой нуклеотидной последовательностью по меньшей мере на приблизительно 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, и/или 100%. Таким образом, в дополнительных вариантах осуществления "значительная идентичность последовательности" или "значительное сходство последовательности" означают идентичность или сходство с другой нуклеотидной последовательностью в диапазоне от приблизительно 70% до приблизительно 100%, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 81% до приблизительно 100%, от приблизительно 82% до приблизительно 100%, от приблизительно 83% до приблизительно 100%, от приблизительно 84% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 86% до приблизительно 100%, от приблизительно 87% до приблизительно 100%, от приблизительно 88% до приблизительно 100%, от приблизительно 89% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 91% до приблизительно 100%, от приблизительно 92% до приблизительно 100%, от приблизительно 93% до приблизительно 100%, от приблизительно 94% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 96% до приблизительно 100%, от приблизительно 97% до приблизительно 100%, от приблизительно 98%о до приблизительно 100% и/или от приблизительно 99% до приблизительно 100%. Следовательно, в некоторых вариантах осуществления нуклеотидная последовательность по настоящему изобретению представляет собой нуклеотидную последовательность, которая характеризуется значительной идентичностью последовательности с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 или SEQ ID NO: 5 и кодирует полипептид, обладающий α-амилазной активностью. В некоторых вариантах осуществления нуклеотидная последовательность по настоящему изобретению представляет собой нуклеотидную последовательность, которая характеризуется 80% - 100% идентичностью последовательности с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 или SEQ ID NO: 5 и кодирует полипептид, обладающий α-амилазной активностью. В иллюстративных вариантах осуществления нуклеотидная последовательность по настоящему изобретению представляет собой нуклеотидную последовательность, которая характеризуется 95% идентичностью последовательности с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 или SEQ ID NO: 5 и кодирует полипептид, обладающий α-амилазной активностью.
В некоторых вариантах осуществления полипептид по настоящему изобретению содержит, состоит главным образом из или состоит из аминокислотной последовательности, которая по меньшей мере на приблизительно 70%, например, по меньшей мере на 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и/или 100% идентична аминокислотной последовательности под SEQ ID NO: 1 и обладает α-амилазной активностью.
В некоторых вариантах осуществления полипептидная или нуклеотидная последовательность могут представлять собой вариант с консервативной модификацией. Как применяется в данном документе, "вариант с консервативной модификацией" относится к полипептидным и нуклеотидным последовательностям, содержащим отдельные замены, делеции или добавления, за счет которых изменяется, добавляется или удаляется одна аминокислота или нуклеотид или небольшая процентная доля аминокислот или нуклеотидов в последовательности, при этом изменение приводит в результате к замене аминокислоты на химически сходную аминокислоту. Таблицы консервативных замен, обеспечивающих функционально сходные аминокислоты, являются хорошо известными из уровня техники.
Как применяется в данном документе, вариант полипептида с консервативной модификацией является биологически активным, и следовательно обладает требуемой активностью эталонного полипептида (например, α-амилазной активностью), как описано в данном документе. Вариант может возникать в результате, например, генетического полиморфизма или действий человека. Биологически активный вариант эталонного полипептида может характеризоваться по меньшей мере приблизительно 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 91%, 98%, 99%, или большей идентичностью или сходством последовательности (например, от приблизительно 40% до приблизительно 99% или большей идентичностью или сходством последовательности и любым диапазоном в указанных пределах) с аминокислотной последовательностью эталонного полипептида, как определено с помощью программ для выравнивания последовательностей и параметров, описанных в других местах в данном документе. Активный вариант может отличаться от последовательности эталонного полипептида всего лишь 1-15 аминокислотными остатками, всего лишь 1-10, например 6-10, всего лишь 5, всего лишь 4, 3, 2 или даже 1 аминокислотным остатком.
В популяции могут существовать встречающиеся в природе варианты. Эти варианты можно идентифицировать с помощью хорошо известных методик молекулярной биологии, таких как полимеразная цепная реакция (ПЦР) и гибридизация, как описано ниже. Нуклеотидные последовательности, полученные синтетическим путем, например последовательности, полученные с помощью сайт-направленного мутагенеза или ПЦР-опосредованного мутагенеза, которые кодируют полипептид по настоящему изобретению, также включены в качестве вариантов. Замены, добавления или делеции одного или нескольких нуклеотидов или аминокислот можно вводить в нуклеотидную или аминокислотную последовательность, раскрытые в данном документе, таким образом, что замены, добавления или делеции вводятся в кодируемый белок. Добавления (вставки) или делеции (усечения) можно осуществлять в N-концевой или С-концевой областях нативного белка или в одном или нескольких участках нативного белка. Аналогично, замену одного или нескольких нуклеотидов или аминокислот можно осуществлять в одном или нескольких участках нативного белка.
Например, консервативные аминокислотные замены можно осуществлять по одному или нескольким предсказанным остаткам предпочтительно несущественных аминокислот. Остаток "несущественной" аминокислоты представляет собой остаток, который можно изменить в последовательности белка дикого типа без изменения биологической активности, тогда как "существенная" аминокислота является необходимой для биологической активности. "Консервативная аминокислотная замена" является такой, при которой аминокислотный остаток замещают аминокислотным остатком со сходной боковой цепью. Семейства аминокислот, остатки которых имеют сходные боковые цепи, известны из уровня техники. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислотными боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярными боковыми цепями (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), разветвленными в бета-положении боковыми цепями (например, треонин, валин, изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Такие замены не могут быть осуществлены в отношении консервативных аминокислотных остатков или в отношении аминокислотных остатков, которые находятся в консервативном мотиве, при этом такие остатки являются существенными для активности белка.
Например, варианты аминокислотной последовательности эталонного полипептида можно получить посредством мутации нуклеотидной последовательности, кодирующей фермент. Можно осуществлять рекомбинантную экспрессию полученных в результате мутантов у растений и проводить скрининг в отношении тех, у которых сохраняется биологическая активность, с помощью анализа α-амилазной активности с применением способов, хорошо известных из уровня техники. Способы мутагенеза и изменений нуклеотидной последовательности хорошо известны из уровня техники. См., например, Kunkel (1985) Proc. Natl. Acad. Sci. USA 82:488-492; Kunkel et al. (1987) Methods in Enzymol. 154:367-382; и Techniques in Molecular Biology (Walker & Gaastra eds., MacMillan Publishing Co. 1983) и ссылки, процитированные там; а также патент США №4873192. Ясно, что мутации, осуществленные в ДНК, кодирующей вариант, не должны приводить к нарушению рамки считывания, и в результате них предпочтительно не будут формироваться комплементарные области, которые могут образовать вторичную структуру мРНК. См. публикацию европейской патентной заявки №75444. Рекомендации относительно соответствующих аминокислотных замен, которые не влияют на биологическую активность белка, представляющего интерес, можно найти в модели Dayhoff et al. (1978) Atlas of Protein Sequence and Structure (Национальный фонд биомедицинских исследований, Вашингтон, округ Колумбия), включенной в данный документе с помощью ссылки.
Делеции, вставки и замены в полипептидах, описанных в данном документе, как предполагается, не будут приводить к радикальным изменениям в отношении характеристик полипептида (например, активности полипептида). Однако, если сложно предсказать точный эффект замены, делеции или вставки до ее осуществления, то специалист в данной области техники поймет, что эффект можно оценивать с помощью обычных скрининговых анализов, которыми можно осуществлять скрининг в отношении определенных активностей полипептида, представляющих интерес (например, α-амилазной активности).
В некоторых вариантах осуществления композиции по настоящему изобретению могут содержать активные фрагменты полипептида. Как применяется в данном документе, "фрагмент" означает часть эталонного полипептида, которая сохраняет полипептидную активность α-амилазы. Фрагмент также означает часть молекулы нуклеиновой кислоты, кодирующей эталонный полипептид. Активный фрагмент полипептида можно получить, например, путем выделения части молекулы нуклеиновой кислоты, кодирующей полипептид, который экспрессирует кодируемый фрагмент полипептида (например, с помощью рекомбинантной экспрессии in vitro), и оценки активности фрагмента. Молекулы нуклеиновой кислоты, кодирующей такие фрагменты, могут состоять из по меньшей мере приблизительно 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 800, 900, 1000, 1100, 1200, 1300, 1400, 1500, 1600, 1700, 1800, 1900, 2000, 2100, или 2200 смежных нуклеотидов, или любого диапазона в указанных пределах, или вплоть до числа нуклеотидов, присутствующих в полноразмерной молекуле нуклеиновой кислоты, кодирующей полипептид. Как таковые, полипептидные фрагменты могут состоять из по меньшей мере приблизительно 50, 60, 70, 80, 90, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 525, 550, 525, 550, 600, 625, 650, 675, или 700 смежных аминокислотных остатков, или любого диапазона в указанных пределах, или вплоть до общего числа аминокислотных остатков, присутствующих в полноразмерном полипептиде. Таким образом, в некоторых вариантах осуществления настоящего изобретения предусматривается полипептид, содержащий, состоящий главным образом из или состоящий из по меньшей мере приблизительно 150 смежных аминокислотных остатков полипептида по настоящему изобретению (например, SEQ ID NO: 1) и обладающий α-амилазной активностью.
Термины "экспрессируют", "экспрессирует", "экспрессируемый" или "экспрессия" и т.п., применяемые в данном документе в отношении молекулы нуклеиновой кислоты и/или нуклеотидной последовательности (например, РНК или ДНК), указывают на то, что молекула нуклеиновой кислоты и/или нуклеотидная последовательность транскрибируется и необязательно транслируется. Таким образом, молекула нуклеиновой кислоты и/или нуклеотидная последовательность могут экспрессировать или продуцировать полипептид, представляющий интерес, или функциональную нетранслируемую РНК.
"Гетерологичная" или "рекомбинантная" нуклеотидная последовательность представляет собой нуклеотидную последовательность, в природных условиях не связанную с клеткой-хозяином, в которую ее вводят, в том числе не встречающиеся в природе множественные копии нуклеотидной последовательности, встречающейся в природе.
"Нативная" или "дикого типа" нуклеиновая кислота, нуклеотидная последовательность, полипептид или аминокислотная последовательность относятся к встречающейся в природе или эндогенной нуклеиновой кислоте, нуклеотидной последовательности, полипептиду или аминокислотной последовательности. Таким образом, например, "мРНК дикого типа" представляет собой мРНК, которая встречается в природе в организме или является эндогенной по отношению к нему. "Гомологичная" последовательность нуклеиновой кислоты представляет собой нуклеотидную последовательность, в природных условиях связанную с клеткой-хозяином, в которую ее вводят.
Также применяемые в данном документе термины "нуклеиновая кислота", "молекула нуклеиновой кислоты", "нуклеотидная последовательность" и "полинуклеотид" могут применяться взаимозаменяемо и охватывают как РНК, так и ДНК, в том числе кДНК, геномную ДНК, мРНК, синтетическую (например, химически синтезированную) ДНК или РНК и химерные ДНК и РНК. Термины "полинуклеотид", "нуклеотидная последовательность" или "нуклеиновая кислота" относятся к цепи нуклеотидов без учета длины цепи. Нуклеиновая кислота может быть двухнитевой или однонитевой. Если нуклеиновая кислота однонитевая, то она может представлять собой смысловую нить или антисмысловую нить. Нуклеиновую кислоту можно синтезировать с применением аналогов или производных олигонуклеотидов (например, инозина или фосфотиоатных нуклеотидов). Такие олигонуклеотиды можно применять, например, для получения нуклеиновых кислот с измененными свойствами спаривания оснований или повышенной устойчивостью к нуклеазам. В настоящем изобретении дополнительно предусматривается нуклеиновая кислота, которая является комплементарной (что может означать как полную комплементарность, так и частичную комплементарность) нуклеиновой кислоте, нуклеотидной последовательности или полинуклеотиду по настоящему изобретению. Молекулы нуклеиновых кислот и/или нуклеотидные последовательности, предусмотренные в данном документе, приводятся в данном документе в направлении от 5'- к 3'- концу, слева направо, и обозначаются с применением стандартного кода для обозначения символов нуклеотидов, как установлено правилами США для изложения последовательностей, §§1.821-1.825 раздела 37 CFR и стандартом ST.25 Всемирной организации интеллектуальной собственности (WIPO).
В некоторых вариантах осуществления рекомбинантные молекулы нуклеиновых кислот, нуклеотидные последовательности и полипептиды по настоящему изобретению являются "выделенными". "Выделенная" молекула нуклеиновой кислоты, "выделенная" нуклеотидная последовательность или "выделенный" полипептид представляют собой молекулу нуклеиновой кислоты, нуклеотидную последовательность или полипептид, которые посредством вмешательства человека существует отдельно от своей естественной среды, а следовательно не являются природными продуктами. Выделенная молекула нуклеиновой кислоты, нуклеотидная последовательность или полипептид могут находиться в очищенной форме, т.е. быть по меньшей мере частично отделенными от по меньшей мере некоторых других компонентов встречающегося в природе организма или вируса, например, структурных компонентов клетки или вируса или других полипептидов или нуклеиновых кислот, обычно обнаруживаемых связанными с полинуклеотидом. В иллюстративных вариантах осуществления выделенная молекула нуклеиновой кислоты, выделенная нуклеотидная последовательность и/или выделенный полипептид являются чистыми по меньшей мере на приблизительно 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или больше.
В других вариантах осуществления выделенная молекула нуклеиновой кислоты, нуклеотидная последовательность или полипептид могут существовать в среде, не являющейся естественной, например, такой как рекомбинантная клетка-хозяин. Таким образом, например, в отношении нуклеотидных последовательностей, термин "выделенная" означает то, что она отделена от хромосомы и/или клетки, в которой она встречается в природе. Полинуклеотид также является выделенным, если он отделен от хромосомы и/или клетки, в которой он встречается в природе, и затем встроен в генетическое окружение, хромосому и/или клетку, в которых он в природе не встречается (например, другую клетку-хозяина, другие регуляторные последовательности и/или другое положение в геноме по сравнению с таковыми обнаруживаемыми в природе). Соответственно, рекомбинантные молекулы нуклеиновой кислоты, нуклеотидные последовательности и кодируемые ими полипептиды являются "выделенными", поскольку они посредством вмешательства человека существуют отдельно от их естественной среды и, следовательно, не являются природными продуктами, однако в некоторых вариантах осуществления они могут быть введены в рекомбинантную клетку-хозяина и существовать в ней.
В некоторых вариантах осуществления нуклеотидные последовательности и/или молекулы нуклеиновой кислоты по настоящему изобретению могут быть функционально связаны с различными промоторами для экспрессии в клетках-хозяевах (например, клетках растения). Как применяется в данном документе, "функционально связанный с", при упоминании первой последовательности нуклеиновой кислоты, которая функционально связана со второй последовательностью нуклеиновой кислоты, означает ситуацию, в которой первая последовательность нуклеиновой кислоты находится в функциональной взаимосвязи со второй последовательностью нуклеиновой кислоты. Например, промотор функционально связан с кодирующей последовательностью, если промотор влияет на транскрипцию или экспрессию кодирующей последовательности.
"Промотор" ДНК является нетранслируемой последовательностью ДНК, расположенной выше кодирующей области, которая содержит сайт связывания для РНК-полимеразы и инициирует транскрипцию ДНК. "Промоторная область" может также включать другие элементы, которые действуют в качестве регуляторов экспрессии генов. Промоторы могут включать, например, конститутивные, индуцируемые, регулируемые во времени, регулируемые в процессе развития, регулируемые химическими веществами, тканепредпочтительные и тканеспецифичные промоторы для применения при получении рекомбинантных молекул нуклеиновой кислоты, т.е. химерных генов. В определенных аспектах "промотор", пригодный в соответствии с настоящим изобретением, представляет собой промотор, способный инициировать транскрипцию нуклеотидной последовательности в клетке растения.
"Химерный ген" представляет собой рекомбинантную молекулу нуклеиновой кислоты, в которой промотор или другая регуляторная нуклеотидная последовательность функционально связаны с нуклеотидной последовательностью, которая кодирует мРНК или которая экспрессируется в виде белка, таким образом, что регуляторная нуклеотидная последовательность способна регулировать транскрипцию или экспрессию ассоциированной нуклеотидной последовательности. Регуляторная нуклеотидная последовательность химерного гена обычно не является функционально связанной с ассоциированной нуклеотидной последовательностью, встречающейся в природе.
Выбор промотора будет меняться в зависимости от временных и пространственных требований для экспрессии, а также в зависимости от клетки-хозяина, подлежащей трансформации. Таким образом, например, экспрессия нуклеотидной последовательности может иметь место в любом растении и/или части растения (например, в листьях, в цветоножках или стеблях, в колосьях, в соцветиях (например, колосках, метелках, початках и т.п.), в корнях, семенах и/или проростках и т.п.). Не смотря на то, что многие промоторы из двудольных растений, как было показано, функционируют у однодольных и наоборот, в идеальном случае для экспрессии у двудольных растений выбирают промоторы двудольных, а промоторы однодольных выбирают для экспрессии у однодольных. Однако не существует каких-либо ограничений в отношении происхождения выбранных промоторов; при этом достаточно, чтобы они являлись функциональными в отношении управления экспрессией нуклеотидных последовательностей в требуемой клетке.
Промоторы, пригодные в соответствии с настоящим изобретением, включают без ограничений промоторы, которые управляют экспрессией нуклеотидной последовательности конститутивно, промоторы, которые управляют экспрессией при индукции, и промоторы, которые управляют экспрессией тканеспецифически или специфически по отношению к развитию. Эти различные типы промоторов хорошо известны из уровня техники.
Примеры конститутивных промоторов включают без ограничений промотор вируса цеструма (cmp) (патент США №7166770), промотор гена актина-1 риса (Wang et al. (1992) Mol. Cell Biol. 12:3399-3406; а также патент США №5641876), промотор CaMV 35S (Odell et al. (1985) Nature 313:810-812), промотор CaMV 19S (Lawton et al. (1987) Plant Mol. Biol. 9:315-324), промотор гена nos (Ebert et al. (1987) Proc. Natl. Acad. Sci USA 84:5745-5749), промотор гена Adh (Walker et al. (1987) Proc. Natl. Acad. Sci. USA 84:6624-6629), промотор гена сахарозосинтазы (Yang & Russell (1990) Proc. Natl. Acad. Sci. USA 87:4144-4148) и промотор гена убиквитина. Конститутивный промотор, полученный из гена убиквитина, накапливается во многих типах клеток. Убиквитиновые промоторы были клонированы из нескольких видов растений для применения у трансгенных растений, например, у подсолнечника (Binet et al., 1991. Plant Science 79: 87-94), маиса (Christensen et al., 1989. Plant Molec. Biol. 12: 619-632) и арабидопсиса (Norris et al. 1993. Plant Molec. Biol. 21:895-906). Убиквитиновый промотор маиса (UbiP) был разработан в трансгенных системах однодольных, и его последовательность и векторы, сконструированные для трансформации однодольных растений, раскрыты в патентной публикации ЕР 0342926. Дополнительно, кассеты экспрессии с промотором, описанные в McElroy et al. (Mol. Gen. Genet. 231: 150-160 (1991)) можно легко модифицировать для экспрессии нуклеотидных последовательностей, и они являются особенно подходящими для применения у однодольных хозяев.
В некоторых вариантах осуществления можно применять тканеспецифичные/тканепредпочтительные промоторы. Тканеспецифичные или тканепредпочтительные профили экспрессии включают без ограничения профили экспрессии, специфичные или предпочтительные в отношении зеленых тканей, специфичные или предпочтительные в отношении корня, специфичные или предпочтительные в отношении стебля и специфичные или предпочтительные в отношении цветка. Промоторы, подходящие для экспрессии в зеленой ткани, включают множество промоторов, которые осуществляют регуляцию генов, участвующих в фотосинтезе, и многие из них были клонированы как из однодольных, так и из двудольных. В одном варианте осуществления промотор, пригодный в соответствии с настоящим изобретением, представляет собой промотор РЕРС маиса из гена фосфоенолкарбоксилазы (Hudspeth & Grula, Plant Molec. Biol. 12:579-589 (1989)). Неограничивающие примеры тканеспецифичных промоторов включают промоторы, связанные с генами, кодирующими запасные белки семян (такие как β-конглицинин, круциферин, напин и фазеолин), зеин (например, гамма-зеин), или белки масляных телец (такие как олеозин), или белки, вовлеченные в биосинтез жирных кислот (в том числе ацилпереносящий белок, стеароил-АСР-десатуразу и десатуразы жирных кислот (fad 2-1)), и другими нуклеиновыми кислотами, экспрессируемыми в ходе эмбрионального развития (такими как Все4, см., например, Kridl et al. (1991) Seed Sci. Res. 1:209-219; а также патент ЕР №255378). Тканеспецифичные или тканепредпочтительные промоторы, пригодные для экспрессии нуклеотидных последовательностей у растений, в частности маиса, включают без ограничения промоторы, которые управляют экспрессией в корне, сердцевине стебля, листе или пыльце. Такие промоторы раскрыты, например, в публикации согласно РСТ WO 93/07278, которая включена в данный документ с помощью ссылки во всей своей полноте. Другие неограничивающие примеры тканеспецифичных или тканепредпочтительных промоторов включают промотор гена рибулозо-1,5-бифосфаткарбоксилазы хлопчатника, раскрытый в патенте США №6040504; промотор гена сахаросинтазы риса, раскрытый в патенте США №5604121; промотор, специфичный в отношении корня, описанный de Framond (FEBS 290:103-106 (1991); ЕР 0452269, выданный Ciba-Geigy); промотор, специфичный в отношении стебля, описанный в патенте США №5625136 (выданный Ciba-Geigy), и который управляет экспрессией гена trpA маиса; и промотор вируса цеструма, вызывающего желтую курчавость листьев, раскрытый в публикации согласно РСТ WO 01/73087, все из которых включены в данный документ с помощью ссылки.
Дополнительные примеры тканеспецифичных/тканепредпочтительных промоторов включают без ограничения промоторы, специфичные в отношении корня, RCc3 (Jeong et al. Plant Physiol. 153:185-197 (2010)) и RB7 (патент США №5459252), промотор гена лектина (Lindstrom et al. (1990) Der. Genet. 11:160-167; и Vodkin (1983) Prog. Clin. Biol. Res. 138:87-98), промотор гена алкогольдегидрогеназы 1 кукурузы (Dennis et al. (1984) Nucleic Acids Res. 12:3983-4000), S-аденозил-L-метионинсинтетазы (SAMS) (Vander Mijnsbrugge et al. (1996) Plant and Cell Physiology, 37(8): 1108-1115), промотор генов светособирающего комплекса кукурузы (Bansal et al. (1992) Proc. Natl. Acad. Sci. USA 89:3654-3658), промотор гена белка теплового шока кукурузы (O'Dell et al. (1985) EMBO J. 5:451-458; и Rochester et al. (1986) EMBO J. 5:451-458), промотор гена малой субъединицы RuBP-карбоксилазы гороха (Cashmore, "Nuclear genes encoding the small subunit of ribulose-1,5-bisphosphate carboxylase" стр. 29-39 в: Genetic Engineering of Plants (Hollaender ed., Plenum Press 1983; и Poulsen et al. (1986) Mol. Gen. Genet. 205:193-200), промотор гена маннопинсинтазы Ti-плазмиды (Langridge et al. (1989) Proc. Natl. Acad. Sci. USA 86:3219-3223), промотор гена нопалинсинтазы Ti-плазмиды (Langridge et al. (1989), выше), промотор гена халконизомеразы петунии (van Tunen et al. (1988) EMBO J. 7:1257-1263), промотор гена богатого глицином белка 1 фасоли (Keller et al. (1989) Genes Dev. 3:1639-1646), промотор усеченной CaMV 35S (O'Dell et al. (1985) Nature 313:810-812), промотор гена пататина картофеля (Wenzler et al. (1989) Plant Mol. Biol. 13:347-354), промотор из клеток корней (Yamamoto et al. (1990) Nucleic Acids Res. 18:7449), промотор гена зеина маиса (Kriz et al. (1987) Mol. Gen. Genet. 207:90-98; Langridge et al. (1983) Cell 34:1015-1022; Reina et al. (1990) Nucleic Acids Res. 18:6425; Reina et al. (1990) Nucleic Acids Res. 18:7449; и Wandelt et al. (1989) Nucleic Acids Res. 17:2354), промотор гена глобулина-1 (Belanger et al. (1991) Genetics 129:863-872), cab-промотор гена α-тубулина (Sullivan et al. (1989) Mol. Gen. Genet. 215:431-440), промотор гена РЕРСазы (Hudspeth & Grula (1989) Plant Mol. Biol. 12:579-589), промоторы, связанные с комплексами R-генов (Chandler et al. (1989) Plant Cell 1:1175-1183), и промоторы гена хальконсинтазы (Franken et al. (1991) EMBOJ. 10:2605-2612).
Особенно пригодными для экспрессии, специфичной в отношении семян, является промотор вицилина гороха (Czako et al. (1992) Mol. Gen. Genet. 235:33-40; a также специфичные в отношении семян промоторы, раскрытые в патенте США №5625136. В некоторых вариантах осуществления промотор может представлять собой промотор, специфичный в отношении эндосперма, в том числе без ограничения промотор гамма-зеина маиса или промотор ADP-gpp маиса.
Промоторы, применимые для экспрессии в зрелых листьях, представляют собой промоторы, которые включаются при наступлении старения, такие как промотор SAG из Arabidopsis (Gan et al. (1995) Science 270:1986-1988).
Кроме того, можно применять промоторы, являющиеся функциональными в пластидах. Неограничивающие примеры таких промоторов включают промотор 5'-UTR гена 9 бактериофага Т3 и другие промоторы, раскрытые в патенте США №7579516. Другие промоторы, пригодные в соответствии с настоящим изобретением, включают без ограничения промотор малой субъединицы S-E9 RuBP-карбоксилазы и промотор гена ингибитора трипсина Кунитца (Kti3).
В некоторых вариантах осуществления настоящего изобретения можно применять индуцируемые промоторы. Таким образом, например, промоторы, регулируемые химическими веществами, можно применять для модуляции экспрессии гена в растении посредством применения экзогенного химического регулятора. Регуляция экспрессии нуклеотидных последовательностей посредством промоторов, регулируемых химическими веществами, обеспечивает синтез полипептидов по настоящему изобретению только тогда, когда культурные растения обрабатывают индуцирующими химическими веществами. В зависимости от цели промотор может представлять собой промотор, индуцируемый химическим веществом, при этом применение химического вещества индуцирует экспрессию гена, или промотор, подавляемый химическим веществом, при этом применение химического вещества подавляет экспрессию гена.
Промоторы, индуцируемые химическими веществами, известны из уровня техники и включают без ограничения промотор In2-2 маиса, который активируется антидотами бензолсульфонамидных гербицидов, промотор GST маиса, который активируется гидрофобными электрофильными соединениями, применяемыми в качестве предвсходовых гербицидов, и промотор PR-1a табака, который активируется салициловой кислотой (например, системы PR1a), стероидзависимые промоторы (см., например, промотор, индуцируемый глюкокортикоидами, в Schena et al. (1991) Proc. Natl. Acad. Sci. USA 88, 10421-10425 и McNellis et al. (1998) Plant J. 14, 247-257) и промоторы, индуцируемые тетрациклинами и подавляемые тетрациклинами (см., например, Gatz et al. (1991) Mol. Gen. Genet. 227, 229-237 и патенты США №№5814618 и 5789156), промоторы системы Lac-penpeccopa, промоторы системы, индуцируемой медью, промоторы системы, индуцируемой салицилатом (например, системы PR1a), промоторы, индуцируемые глюкокортикоидами (Aoyama et al. (1997) Plant J. 11:605-612), и промоторы системы, индуцируемой экдизоном.
Другие неограничивающие примеры индуцируемых промоторов включают промоторы, индуцируемые ABA и тургорным давлением, промотор гена белка, связывающегося с ауксином (Schwob et al. (1993) Plant J. 4:423-432), промотор УДФ-глюкозофлавоноидгликозилтрансферазы (Ralston et al. (1988) Genetics 119:185-197), промотор ингибитора протеиназы MPI (Cordero et al. (1994) Plant J. 6:141-150) и промотор глицеральдегид-3-фосфатдегидрогеназы (Kohler et al. (1995) Plant Mol. Biol. 29:1293-1298; Martinez et al. (1989) J Mol. Biol. 208:551-565; и Quigley et al. (1989) J Mol. Evol. 29:412-421). Также включены системы, индуцируемые бензолсульфонамидом (патент США №5364780) и индуцируемые спиртами (публикации Международных заявок на патенты №№WO 97/06269 и WO 97/06268), и промоторы гена глутатион-S-трансферазы. Аналогично можно применять любой из индуцируемых промоторов, описанных в Gatz (1996) Current Opinion Biotechnol. 7:168-172 и Gatz (1997) Annu. Rev. Plant Physiol. Plant Mol. Biol. 48:89-108. Другие индуцируемые химическими веществами промоторы, пригодные для управления экспрессией нуклеотидных последовательностей по настоящему изобретению у растений, раскрыты в патенте США №5614395, включенном в данный документ с помощью ссылки во всей своей полноте. Химическое индуцирование экспрессии генов также подробно изложено в опубликованной заявке ЕР 0332104 (выданной Ciba-Geigy) и патенте США №5614395. В некоторых вариантах осуществления промотор для химического индуцирования может представлять собой промотор PR-1а табака.
Полипептид по настоящему изобретению может нацеливаться или не нацеливаться на участок внутри растения посредством применения сигнальной последовательности. Известно, что многочисленные сигнальные последовательности влияют на экспрессию или нацеливание полинуклеотида на конкретный участок/ткань или за пределами конкретного участка/ткани. Подходящие сигнальные последовательности и промоторы, обеспечивающие нацеливание, известны из уровня техники и включают без ограничения те, которые приведены в данном документе (см. например патент США №7919681). Примеры мишеней включают без ограничения вакуоль, эндоплазматический ретикулум (ER), хлоропласт, амилопласт, крахмальную гранулу, клеточную стенку, семя или конкретную ткань, например, эндосперм. Таким образом, нуклеотидная последовательность, кодирующая полипептид по настоящему изобретению (например, SEQ ID NO: 1), может быть функционально связана с сигнальной последовательностью для нацеливания и/или сохранения полипептида в участке внутри растения. В некоторых вариантах осуществления сигнальная последовательность может представлять собой N-концевую сигнальную последовательность из waxy, N-концевую сигнальную последовательность из гамма-зеина, крахмалсвязывающего домена или С-концевого крахмалсвязывающего домена. В дополнительных вариантах осуществления сигнальная последовательность может представлять собой сигнальную последовательность ER, последовательность удерживания ER, сигнальную последовательность ER и дополнительную последовательность удерживания ER. Таким образом, в некоторых вариантах осуществления настоящего изобретения полипептиды α-амилазы могут быть слиты с одной или несколькими сигнальными последовательностями (и/или нуклеотидные последовательности, кодирующие указанные полипептиды, могут быть функционально связаны с нуклеотидными последовательностями, кодирующими указанные сигнальные последовательности).
Как применяется в данном документе, "кассета экспрессии" означает молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, представляющую интерес (например, нуклеотидную последовательность под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5), при этом указанная нуклеотидная последовательность функционально связана по меньшей мере с регуляторной последовательностью (например, промотором). Таким образом, в некоторых вариантах осуществления настоящего изобретения предусматриваются кассеты экспрессии, сконструированные для экспрессии нуклеотидной последовательности под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5. Таким образом, например, один или несколько промоторов растений, функционально связанных с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5 или нуклеотидной последовательностью, характеризующейся значительной идентичностью с нуклеотидной последовательностью под SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4 и/или SEQ ID NO: 5, могут быть предоставлены в кассете экспрессии с целью экспрессии в организме или его клетке (например, растении, части растения и/или клетке растения).
Кассета экспрессии, содержащая нуклеотидную последовательность, представляющую интерес, может быть химерной, что означает, что по меньшей мере один из ее компонентов является гетерологичным по отношению по меньшей мере к одному из ее остальных компонентов. Кассета экспрессии также может представлять собой таковую, которая встречается в природе, но которая была получена в рекомбинантной форме, пригодной для гетерологичной экспрессии. Однако обычно кассета экспрессии является гетерологичной по отношению к хозяину, т.е. конкретная последовательность нуклеиновой кислоты в кассете экспрессии не встречается в клетке-хозяине в природных условиях, а должна быть введена в клетку-хозяина или предка клетки-хозяина с помощью трансформации.
В дополнение к промоторам, функционально связанным с нуклеотидной последовательностью, подлежащей экспрессии, кассета экспрессии может также включать другие регуляторные последовательности. Как применяется в данном документе, "регуляторная последовательность" означает нуклеотидную последовательность, расположенную выше (5'-некодирующие последовательности), в пределах и/или ниже (3'-некодирующие последовательности) кодирующей последовательности, и/или которая влияет на транскрипцию, процессинг или стабильность РНК или трансляцию связанной кодирующей последовательности. Регуляторные последовательности включают без ограничения промоторы, энхансеры, интроны, лидерные последовательности, регулирующие трансляцию, сигналы терминации и сигнальные последовательности полиаденилирования. В некоторых вариантах осуществления кассета экспрессии также может включать в себя нуклеотидные последовательности, кодирующие сигнальные последовательности, функционально связанные с полинуклеотидной последовательностью по настоящему изобретению.
Для целей настоящего изобретения регуляторные последовательности или области могут являться нативными/аналогичными в отношении растения, части растения и/или клетки растения, и/или регуляторные последовательности могут являться нативными/аналогичными в отношении других регуляторных последовательностей. В качестве альтернативы, регуляторные последовательности могут являться гетерологичными в отношении растения (и/или части растения и/или клетки растения) и/или друг друга (т.е. регуляторных последовательностей). Таким образом, например, промотор может являться гетерологичным, если он функционально связан с полинуклеотидом от вида, отличного от вида, от которого получили полинуклеотид. В качестве альтернативы, промотор может также являться гетерологичным в отношении выбранной нуклеотидной последовательности, если промотор происходит от одного и того же/аналогичного вида, от которого получен полинуклеотид, но один или оба (т.е. промотор и/или полинуклеотид) в значительной степени модифицированы по сравнению со своей исходной формой и/или геномным локусом, и/или промотор не является нативным промотором в отношении функционально связанного полинуклеотида.
Как известно, ряд нетранслируемых лидерных последовательностей, полученных от вирусов, усиливают экспрессию генов. В частности, было показано, что лидерные последовательности вируса табачной мозаики (TMV, "ω-последовательность"), вируса хлоротической пятнистости маиса (MCMV) и вируса мозаики люцерны (AMV) являются эффективными в усилении экспрессии (Gallie et al. (1987) Nucleic Acids Res. 15:8693-8711; и Skuzeski et al. (1990) Plant Mol. Biol. 15:65-79). Другие лидерные последовательности, известные из уровня техники, включают без ограничения лидерные последовательности пикорнавирусов, такие как лидерная последовательность 5'-некодирующей области вируса энцефаломиокардита (EMCV) (Elroy-Stein et al. (1989) Proc. Natl. Acad. Sci. USA 86:6126-6130); лидерные последовательности потивирусов, такие как лидерная последовательность вируса гравировки табака (TEV) (Allison et al. (1986) Virology 154:9-20); лидерная последовательность вируса карликовой мозаики маиса (MDMV) (Allison et al. (1986), выше); лидерная последовательность белка, связывающегося с тяжелой цепью иммуноглобулинов человека (BiP) (Macejak & Samow (1991) Nature 353:90-94); нетранслируемая лидерная последовательность мРНК белка оболочки AMV (РНК 4 AMV; Jobling & Gehrke (1987) Nature 325:622-625); лидерная последовательность вируса табачной мозаики TMV (Gallie et al. (1989) Molecular Biology of RNA 237-256) и лидерная последовательность MCMV (Lommel et al. (1991) Virology 81:382-385). См. также Della-Cioppa et al. (1987) Plant Physiol. 84:965-968.
Кассета экспрессии также необязательно может содержать участок терминации транскрипции и/или трансляции (т.е. участок терминации), который является функциональным у растений. Разнообразные терминаторы транскрипции доступны для применения в кассетах экспрессии, и они отвечают за терминацию транскрипции за пределами представляющей интерес гетерологичной нуклеотидной последовательности и правильное полиаденилирование мРНК. Участок терминации может быть нативным в отношении участка инициации транскрипции, может быть нативным в отношении функционально связанной нуклеотидной последовательности, представляющей интерес, может быть нативным в отношении растения-хозяина или может быть получен из другого источника (например, быть чужеродным или гетерологичным в отношении промотора, представляющей интерес нуклеотидной последовательности, растения-хозяина или любой их комбинации). Надлежащие терминаторы транскрипции включают без ограничения терминатор 35S CAMV, терминатор гена tml, терминатор гена нопалинсинтазы и/или терминатор гена rbcs-E9 гороха. Их можно применять как у однодольных, так и у двудольных растений. В дополнение, можно применять терминатор транскрипции, нативный в отношении кодирующей последовательности.
Кассета экспрессии по настоящему изобретению также может включать нуклеотидную последовательность селектируемого маркера, который можно применять для отбора трансформированного растения, части растения и/или клетки растения. Как применяется в данном документе, "селектируемый маркер" означает нуклеотидную последовательность, которая при экспрессии придает отличительный фенотип растению, части растения и/или клетке растения, экспрессирующим данный маркер, и, таким образом, позволяет отличать такие трансформированные растения, части растений и/или клетки растений от тех, которые не имеют маркера. Такая нуклеотидная последовательность может кодировать либо селектируемый, либо подвергаемый скринингу маркер в зависимости от того, придает ли маркер признак, по которому можно провести отбор с помощью химических средств, например, путем применения селективного средства (например, антибиотика, гербицида и т.п.), или от того, является ли маркер просто признаком, который можно идентифицировать посредством наблюдения или тестирования, например, путем скрининга (например, признаком, определяемым в R-локусе). Разумеется, существует много примеров подходящих селектируемых маркеров, которые известны из уровня техники и могут применяться в кассетах экспрессии, описанных в данном документе.
Примеры селектируемых маркеров включают без ограничения нуклеотидную последовательность, кодирующую neo или nptII, которые придают устойчивость к канамицину, G418 и т.п. (Potrykus et al. (1985) Mol. Gen. Genet. 199:183-188); нуклеотидную последовательность, кодирующую bar, который придает устойчивость к фосфинотрицину; нуклеотидную последовательность, кодирующую измененную 5-енолпирувилшикимат-3-фосфатсинтазу (EPSP), которая придает устойчивость к глифосату (Hinchee et al. (1988) Biotech. 6:915-922); нуклеотидную последовательность, кодирующую нитрилазу, такую как bxn от Klebsiella ozaenae, которая придает устойчивость к бромоксинилу (Stalker et al. (1988) Science 242:419-423); нуклеотидную последовательность, кодирующую измененную ацетолактатсинтазу (ALS), которая придает устойчивость к имидазолинону, сульфонилмочевине или другим ALS-ингибирующим химическим веществам (европейская патентная заявка №154204); нуклеотидную последовательность, кодирующую устойчивую к метотрексату дигидрофолатредуктазу (DHFR) (Thillet et al. (1988) J. Biol. Chem. 263:12500-12508); нуклеотидную последовательность, кодирующую далапондегалогеназу, которая придает устойчивость к далапону; нуклеотидную последовательность, кодирующую маннозо-6-фосфатизомеразу (также называемую фосфоманнозоизомеразой (PMI)), которая придает способность к метаболизму маннозы (патенты США №5767378 и №5994629); нуклеотидную последовательность, кодирующую измененную антранилатсинтазу, которая придает устойчивость к 5-метилтриптофану; и/или нуклеотидную последовательность, кодирующую hph, который придает устойчивость к гигромицину. Специалист в данной области техники способен выбрать подходящий селектируемый маркер для применения в кассете экспрессии по настоящему изобретению.
Дополнительные селектируемые маркеры включают без ограничения нуклеотидную последовательность, кодирующую β-глюкуронидазу или uidA (GUS), который кодирует фермент, для которого известны различные хромогенные субстраты; нуклеотидную последовательность R-локуса, которая кодирует продукт, регулирующий продуцирование антоцианиновых пигментов (красного цвета) в тканях растений (Dellaporta et al., "Molecular cloning of the maize R-nj allele by transposon-tagging with Ac," pp. 263-282 в: Chromosome Structure and Function: Impact of New Concepts, 18th Stadler Genetics Symposium (Gustafson & Appels eds., Plenum Press 1988)); нуклеотидную последовательность, кодирующую β-лактамазу, фермент, для которого известны различные хромогенные субстраты (например, PAD АС, хромогенный цефалоспорин) (Sutcliffe (1978) Proc. Natl. Acad. Sci. USA 75:3737-3741); нуклеотидную последовательность, кодирующую xylE, который кодирует катехолдиоксигеназу (Zukowsky et al. (1983) Proc. Natl. Acad. Sci. USA 80:1101-1105); нуклеотидную последовательность, кодирующую тирозиназу, фермент, способный окислять тирозин до DOPA и допахинона, который, в свою очередь, конденсируется с образованием меланина (Katz et al. (1983) J. Gen. Microbiol. 129:2703-2714); нуклеотидную последовательность, кодирующую β-галактозидазу, фермент, для которого существуют хромогенные субстраты; нуклеотидную последовательность, кодирующую люциферазу (lux), которая обеспечивает выявление с помощью биолюминесценции (Ow et al. (1986) Science 234:856-859); нуклеотидную последовательность, кодирующую экворин, который может быть использован в обнаружении чувствительной к кальцию биолюминесценции (Prasher et al. (1985) Biochem. Biophys. Res. Comm. 126:1259-1268); или нуклеотидную последовательность, кодирующую зеленый флуоресцентный белок (Niedz et al. (1995) Plant Cell Reports 14:403-406). Специалист в данной области техники способен выбрать подходящий селектируемый маркер для применения в кассете экспрессии по настоящему изобретению.
В других аспектах настоящего изобретения предусматривается способ увеличения скорости роста (привеса) или среднесуточного привеса животного, при этом способ включает скармливание указанному животному кормовой композиции для животных по настоящему изобретению, при этом скорость роста животного или среднесуточный привес животного увеличиваются на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки по сравнению со скоростью роста контрольного животного, которому не предоставляли кормовую композицию для животных по настоящему изобретению. Таким образом, в некоторых вариантах осуществления увеличение скорости роста или среднесуточного привеса может составлять приблизительно 0,05, 0,06, 0,07, 0,08, 0,09, 0,1, 0,1, 0,125, 0,15, 0,175, 0,2, 0,225, 0,25, 0,275, 0,3, 0,325, 0,35, 0,375, 0,4, 0,425, 0,45, 0,475, 0,5, 0,525, 0,55, 0,575, 0,6, 0,625, 0,65, 0,675, 0,7, 0,725, 0,75, 0,775, 0,8, 0,825, 0,85, 0,875, 0,9, 0,925, 0,95, 0,975, 1, 1,25, 1,5, 1,75, 2, 2,25, 2,5, 2,75, 3, 3,25, 3,5, 3,75, 4, 4,1, 4,2, 4,21, 4,22, 4,23, 4,24, 4,25, 4.26, 4,27, 4,28, 4,29, 4,3, 4,31, 4,32, 4,33, 4,34, 4,35, 4,36, 4,37, 4,38, 4,39, 4,4, 4,41, 4,42, 4,43, 4,44, 4,45, 4,46, 4,47, 4,48, 4,49, 4,5, 4,75, 5, 5,25, 5,5, 5,75, 6, 6,25, 6,5, 6,75, 7, 7,25, 7,5, 7,75, 8, 8,25, 8,5, 8,75, 9, 9,25, 9,5, 9,75, 10 фунтов/сутки, и т.п., и/или любой диапазон в указанных пределах. В некоторых конкретных вариантах осуществления увеличение скорости роста или среднесуточного привеса может составлять от приблизительно 0,05 фунта/сутки до приблизительно 0,5 фунта/сутки. В дополнительных вариантах осуществления увеличение скорости роста или среднесуточного привеса может составлять приблизительно 0,1 фунт/сутки по сравнению с ростом контрольного животного, которому не предоставляли указанную кормовую композицию для животных.
В еще одних аспектах настоящего изобретения предусматривается способ сокращения количества суток, необходимого для достижения требуемого веса у животного, при этом способ включает скармливание указанному животному кормовой композиции для животных по настоящему изобретению, за счет чего сокращается количество суток, необходимое для достижения требуемого веса, по сравнению с количеством суток, необходимым для достижения такого же требуемого веса у контрольного животного, которому не скармливали указанную кормовую композицию для животных.
Как применяется в данном документе, "требуемый вес" или "требуемый предубойный вес" могут означать живой вес или вес парной туши. Таким образом, например, для крупного рогатого скота требуемый живой вес может составлять от приблизительно 950 до приблизительно 1600 фунтов, и требуемый вес парной туши может составлять от приблизительно 700 до приблизительно 1000 фунтов.
Перед поступлением на откормочную площадку, крупный рогатый скот проводит большую часть своей жизни пасясь на пастбище или пастбищном угодье, и затем его транспортируют на откормочную площадку для завершающего откорма, где ему скармливают зерно и другие кормовые концентраты. Как правило, крупный рогатый скот поступает на откормочную площадку с весом, составляющим от приблизительно 600 до приблизительно 750 фунтов. В зависимости от веса при помещении, условий питания и требуемого предубойного веса, период пребывания на откормочной площадке может находиться в диапазоне от приблизительно 90 суток до приблизительно 300 суток. Средний прирост может составлять от приблизительно 2,5 до приблизительно 5 фунтов в сутки.
Соответственно, в другом аспекте настоящего изобретения количество суток, необходимое для достижения требуемого веса у животного, которому скармливали кормовые композиции для животных по настоящему изобретению, может сокращаться на величину от приблизительно 1 суток до приблизительно 30 суток по сравнению с контрольным животным, которому не скармливали указанную кормовую композицию для животных. В некоторых вариантах осуществления количество суток, необходимое для достижения требуемого веса у животного, которому скармливали кормовые композиции для животных по настоящему изобретению, может сокращаться на величину от приблизительно 1 суток до приблизительно 25 суток, от приблизительно 1 суток до приблизительно 20 суток, от приблизительно 5 суток до приблизительно 20 суток, от приблизительно 5 суток до приблизительно 15 суток и т.п., по сравнению с контрольным животным, которому не скармливали указанную кормовую композицию для животных. Таким образом, в некоторых вариантах осуществления количество суток, необходимое для достижения требуемого веса у животного, которому скармливали кормовую композицию для животных по настоящему изобретению, может сокращаться на приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 суток, и т.п., и/или любой диапазон в указанных пределах.
В других аспектах настоящего изобретения предусматривается способ повышения эффективности усвояемости корма животным, при этом способ включает скармливание указанному животному кормовой композиции для животных по настоящему изобретению в количестве, эффективном для повышения эффективности усвояемости корма указанным животным по сравнению с контрольным животным, которому не скармливали указанную кормовую композицию для животных.
Эффективность усвояемости корма можно рассчитать как прирост веса тела животного на количество предоставленного корма. В некоторых вариантах осуществления вес тела представляет собой предубойный вес тела перед убоем. В дополнительных вариантах осуществления предоставленный корм представляет собой количество корма, которое предоставляется в течение периода от приблизительно 90 суток до приблизительно 300 суток. Таким образом, в некоторых вариантах осуществления предоставленный корм представляет собой количество корма, которое предоставляется в течение периода от приблизительно 100 суток до приблизительно 275 суток, от приблизительно 125 суток до приблизительно 250 суток, от приблизительно 150 суток до приблизительно 225 суток, от приблизительно 180 суток до приблизительно 200 суток и т.п.
Соответственно, в некоторых вариантах осуществления период времени (количество суток), за который измеряют привес, составляет 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 213, 214, 215, 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254, 255, 256, 257, 258, 259, 260, 261, 262, 263, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285, 286, 287, 288, 289, 290, 291, 292, 293, 294, 295, 296, 297, 298, 299, 300 суток, и т.п., и/или любой диапазон в указанных пределах.
В дополнительных аспектах настоящего изобретения кормовая ценность кукурузы для животного повышается на величину от приблизительно 1% до приблизительно 25% по сравнению с контрольным животным, которому не скармливали указанную кормовую композицию для животных. Кормовая ценность кукурузы равняется разнице коэффициента кормоотдачи от кормовой композиции по настоящему изобретению и коэффициента кормоотдачи у контрольного животного, которому не скармливали указанную кормовую композицию, деленной на коэффициент кормоотдачи у указанного контрольного животного, которому не скармливали указанную кормовую композицию, с разделением всего на процентное содержание кукурузы в указанной кормовой композиции. Соответственно, в некоторых вариантах осуществления повышение кормовой ценности кукурузы может составлять приблизительно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19%, 20%, 21%, 22%, 23%, 24%, 25%, и т.п., и/или любой диапазон в указанных пределах. В конкретных вариантах осуществления повышение кормовой ценности кукурузы составляет от приблизительно 1% до приблизительно 10% по сравнению с контролем. В иллюстративном варианте осуществления повышение пищевой ценности составляет приблизительно 5% по сравнению с контролем.
В дополнительных аспектах настоящего изобретения эффективность усвояемости корма животным повышается на величину от приблизительно 0,005 до приблизительно 0,1 по сравнению с контрольным животным, которому не скармливали указанную кормовую композицию для животных. Соответственно, в некоторых вариантах осуществления повышение эффективности усвояемости корма может составлять приблизительно 0,005, 0,006, 0,007, 0,008, 0,009,0,01, 0,011, 0,012, 0,013, 0,014, 0,015, 0,016, 0,017, 0,018, 0,019, 0,02, 0,021, 0,022, 0,023, 0,024, 0,025, 0,026, 0,027, 0,028, 0,029, 0,03, и т.п., и/или любой диапазон в указанных пределах. В конкретных вариантах осуществления повышение эффективности усвояемости корма составляет от приблизительно 0,005 до приблизительно 0,01 по сравнению с контролем. В иллюстративном варианте осуществления повышение эффективности усвояемости корма составляет приблизительно 0,06 по сравнению с контролем. Эффективность усвояемости корма, также известная как "G:F", представляет собой среднесуточный прирост, разделенный на потребление сухого вещества в сутки животным.
В некоторых вариантах осуществления животному скармливают от приблизительно 1 фунта до приблизительно 30 фунтов кормовой композиции для животных по настоящему изобретению в пересчете на одно животное в сутки. Соответственно, в некоторых вариантах осуществления животному скармливают приблизительно 1 фунт, 2 фунта, 3 фунта, 4 фунта, 5 фунтов, 6 фунтов, 7 фунтов, 8 фунтов, 9 фунтов, 10 фунтов, 11 фунтов, 12 фунтов, 13 фунтов, 14 фунтов, 15 фунтов, 16 фунтов, 17 фунтов, 18 фунтов, 19 фунтов, 20 фунтов, 21 фунт, 22 фунта, 23 фунта, 24 фунта, 25 фунтов, 26 фунтов, 27 фунтов, 28 фунтов, 29 фунтов, 30 фунтов кормовой композиции для животных по настоящему изобретению в пересчете на одно животное в сутки, и т.п., и/или любой диапазон в указанных пределах. В некоторых вариантах осуществления животному скармливают от приблизительно 9 фунтов до приблизительно 21 фунта кормовой композиции для животных по настоящему изобретению в пересчете на одно животное в сутки. В некоторых вариантах осуществления животному можно скармливать кормовую композицию для животных по настоящему изобретению ad libitum, или от приблизительно одного раза до приблизительно трех раз в сутки (например, 1, 2, 3), или в любой их комбинации.
Кормовую композицию для животных по настоящему изобретению можно скармливать любому животному, например, сельскохозяйственному животному, животному зоопарка, лабораторному животному и/или домашнему животному. В некоторых вариантах осуществления животное может представлять собой без ограничения представителя бычьих (например, домашний крупный рогатый скот (коровы (например, молочной и/или мясной породы)), бизона, буйвола), представителя лошадиных (например, лошадь, осла, зебру и т.п.), представителя птичьих (например, курицу, перепела, индейку, утку и т.п.; например, домашнюю птицу), овцу, козу, антилопу, свинью (например, домашнюю свинью), представителя собачьих, кошачьих, грызунов (например, мышь, крысу, морскую свинку); кролика, рыбу и т.п. В некоторых вариантах осуществления животное может представлять собой корову. В некоторых вариантах осуществления животное может представлять собой домашнюю птицу. В других вариантах осуществления животное может представлять собой курицу. В дополнительных вариантах осуществления животное может представлять собой домашнюю свинью. В еще одних вариантах осуществления животное может представлять собой свинью.
В дополнительных вариантах осуществления настоящего изобретения предусматривается способ увеличения объема надоя молока от молочного животного (например, коровы, козы и т.п.), включающий скармливание указанному молочному животному кормовой композиции для животных по настоящему изобретению, при этом объем надоя молока от указанного животного увеличивается на величину от приблизительно 5% до приблизительно 200% по сравнению с объемом надоя молока от контрольного животного, которому не предоставляли указанную кормовую композицию для животных по настоящему изобретению. В некоторых вариантах осуществления увеличение объема молока происходит в течение периода времени от приблизительно 1 до приблизительно 72 часов. В других вариантах осуществления объем надоя молока от указанного животного увеличивается на величину от приблизительно 25% до приблизительно 175%, от приблизительно 50% до приблизительно 150% и т.п. В дополнительных вариантах осуществления объем надоя молока от указанного животного увеличивается на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 100%, 105%, 110%, 115%, 120%, 125%, 130%, 135%, 140%, 145%, 150%, 155%, 160%, 165%, 170%, 175%, 180%, 185%, 190%, 195% и/или 200% по сравнению с контрольным животным, которому не скармливали кормовую композицию для животных по настоящему изобретению.
Применяемыми в данном документе терминами "увеличение", "увеличивающий", "увеличенный", "усиливать", "усиленный", "усиливающий" и "усиление" (и их грамматическими вариантами) описывают увеличение среднесуточного привеса животного или скорости роста (привеса) животного за счет скармливания указанному животному кормовой композиции для животных по настоящему изобретению, при этом среднесуточной привес или скорость роста животного увеличиваются на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки, или повышение эффективности усвояемости корма животным за счет скармливания указанному животному кормовой композиции для животных по настоящему изобретению в количестве, эффективном для повышения эффективности усвояемости корма указанным животным. Данное увеличение среднесуточного привеса, скорости роста (привеса) или эффективности усвояемости корма животным можно наблюдать посредством сравнения среднесуточного привеса, скорости роста (привеса) или повышения эффективности усвояемости корма животным с животным, которому не скармливали кормовую композицию для животных по настоящему изобретению (т.е. контролем).
Применяемыми в данном документе терминами "уменьшать", "уменьшенный", "уменьшающий", "уменьшение", "снижать", "подавлять" и "сокращать" (и их грамматическими вариантами) описывают, например, уменьшение или сокращение количества суток, необходимого для достижения требуемого веса у животного по сравнению с контролем (например, контрольным животным, которому не скармливали кормовую композицию для животных).
Настоящее изобретение более конкретно описано в следующих примерах, которые предназначены только для иллюстрации, поскольку для специалистов в данной области техники будут очевидны их многочисленные модификации и вариации.
ПРИМЕРЫ
Эксперимент 1
Триста кроссбредных быков (исходный BW=658±36 фунтов) использовали в испытании на откормочной площадке для завершающего откорма в сельскохозяйственном научно-исследовательском центре UNL (ARDC) возле Мида, Небраска. Крупному рогатому скоту скармливали рацион в ограниченном количестве, составляющем 2% от BW, который состоял из 32% влажной кукурузной барды с растворимыми веществами, 32% люцернового сена, 32% кукурузы сухого плющения и 4% добавки (основа DM), в течение пяти дней перед началом эксперимента. В 0 и 1-й день регистрировали значения исходного веса в пределах двух дней, которые усредняли и использовали в качестве исходного BW. Быков разделяли на блоки по BW в блоки с легким, средним и тяжелым BW (n=3, 2 и 1 повторности загонов, соответственно), стратифицированным по BW, и распределяли случайным образом в один из 30 загонов, при этом к загонам случайным образом распределяли один из пяти рационов для обработки. Насчитывалось 10 поголовий/загон и 6 повторностей/обработка. Рационы для обработки включали: 1) коммерческий источник кукурузы (CON), 2) тестируемую кукурузу Enogen (SYN), 3) смесь 50:50 CON и SYN, 4) CON с влажным кормом на основе кукурузной клейковины (CON-SB) и 5) SYN с влажным кормом на основе кукурузной клейковины (SYN-SB) в схеме рандомизированных блоков (таблица 1). Быков адаптировали к рационам завершающего откорма в течение 21-дневного периода, при этом кукурузой замещали люцерновое сено, тогда как включение кукурузного силоса, влажной кукурузной барды с растворимыми веществами (WDGS) и добавки оставалось таким же во всех рационах. В рационах, содержащих влажный корм на основе кукурузной клейковины (Sweet Bran® (Cargill); SB), концентрация оставалась такой же во всех зерновых рационах для адаптации. Рационы составляли с удовлетворением или превосхождением требований NRC в отношении белка и минералов. Конечные рационы завершающего откорма обеспечивал 360 мг/бык в сутки румензина (30 г/тонна DM) и 90 мг/бык в сутки тилана (9 г/тонна DM). Быков имплантировали в 1-й день с помощью Revalor-XS.
Всех быков собирали в коммерческой скотобойне (Greater Omaha Pack, Омаха, Небраска) на 173-й день. Конечный живой BW определяли в день убоя и применяли 4% поправку на потерю веса для расчета убойного выхода. Корм, обеспечиваемый на 173-й день, составлял 50% DMI предыдущего дня, и проводили взвешивание в 4:00 после полудня. Быков затем перевозили и содержали до убоя на следующий день. Вес парной туши и показатели печени регистрировали в день убоя. Толщину жира, область LM и степень мраморности согласно оценке USDA регистрировали через 48 ч. охлаждения. Конечный BW, ADG и F:G рассчитывали с применением HCW, скорректированного к общему убойному выходу 63%.
Эксперимент 2
Двести сорок кроссбредных быков (исходный BW=634±34 фунтов) использовали в испытании на откормочной площадке для завершающего откорма в центре сельскохозяйственных исследований и внедрения достижений в Панхандле UNL (PHREC) возле Скотсблаффа, Небраска. Протоколы ограниченного кормления крупного рогатого скота и определения исходного BW являлись такими же как в эксп. 1. Быков разделяли на блоки по BW в блоки с легким, средним и тяжелым BW, стратифицированным по BW, и распределяли случайным образом в один из 24 загонов, при этом к загонам случайным образом распределяли один из четырех рационов для обработки. Насчитывалось 10 поголовий на загон и 6 повторностей на обработку. Рационы для обработки включали: 1) CON, 2) SYN, 3) смесь и 4) CON с ферментом (Amaize; Alltech, Inc.), добавленным к рациону при норме 5 г/бык в сутки (NZ; таблица 2). Процедуры ограниченного кормления, взвешивания, разделения на блоки, имлантирования и адаптации к зерну являлись такими же как в эксп. 1. Быков в блоках с тяжелым, средним и легким BW собирали в коммерческой скотобойне (Cargill Meat Solutions, Форт Морган, Колорадо) на 148, 169 и 181-й день (соответственно). В последний день быков удерживали от корма и взвешивали в 8:00 до полудня перед перевозкой и убоем в тот же день. Данные анализировали по схеме рандомизированных блоков с блоком исходного BW в качестве фиксированного результата и загоном в качестве экспериментальной единицы.
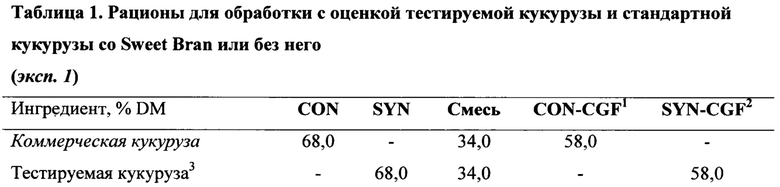
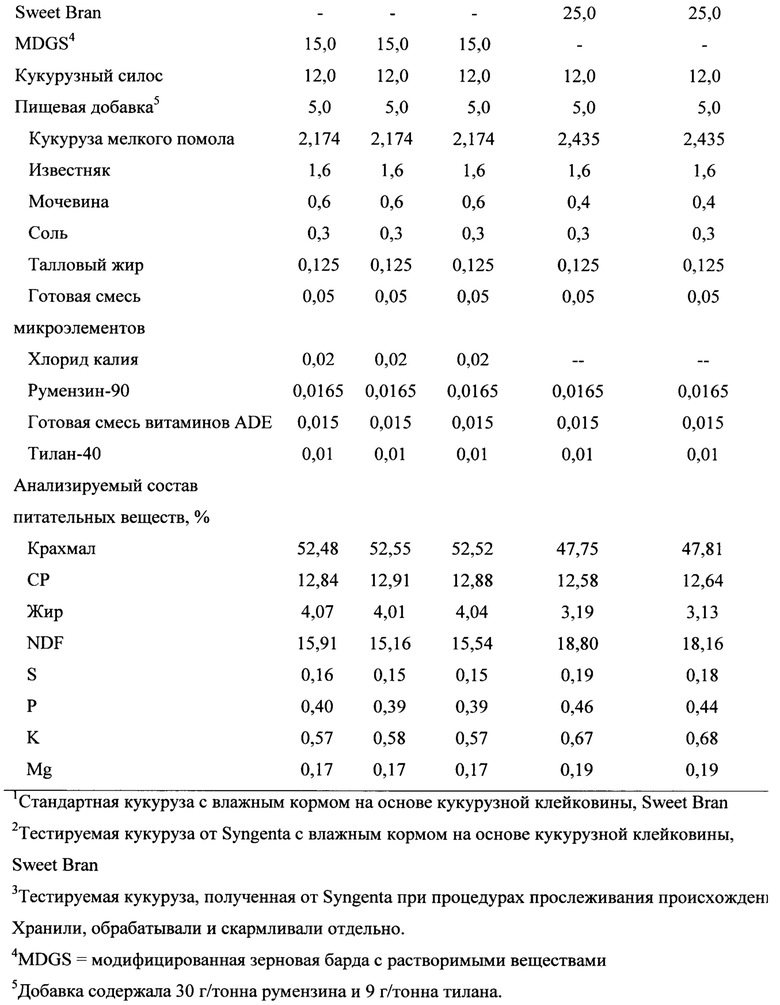
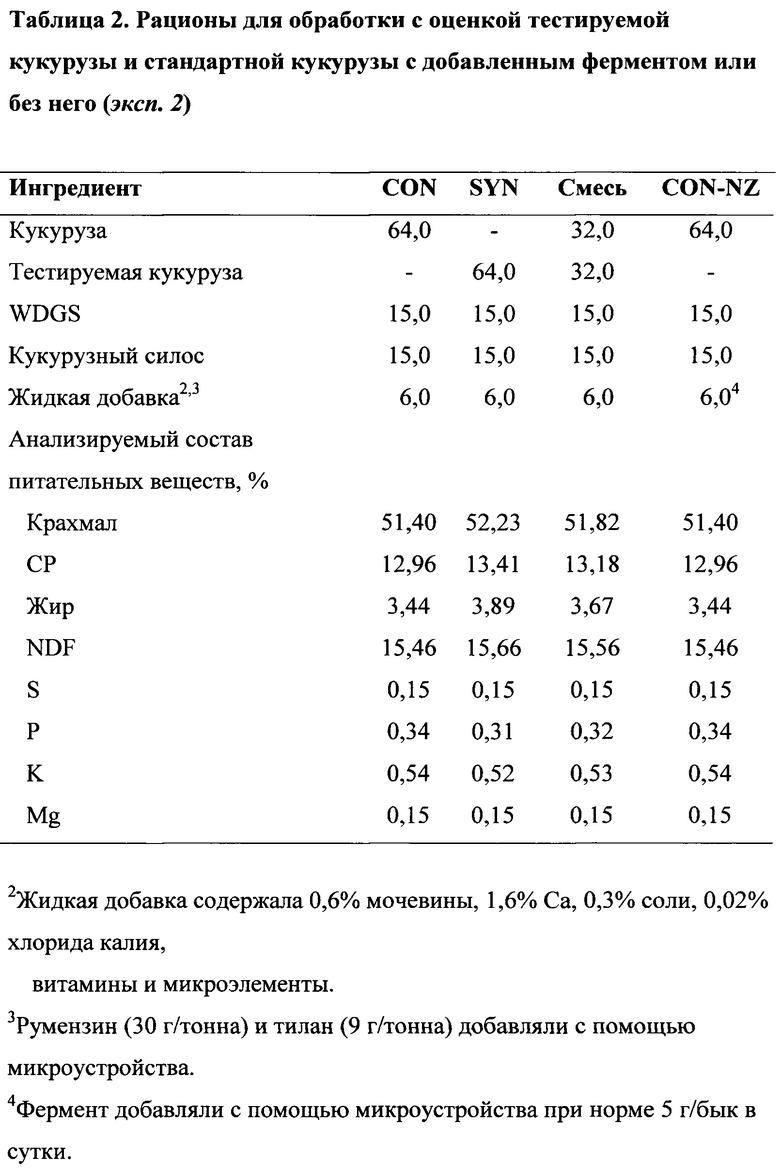

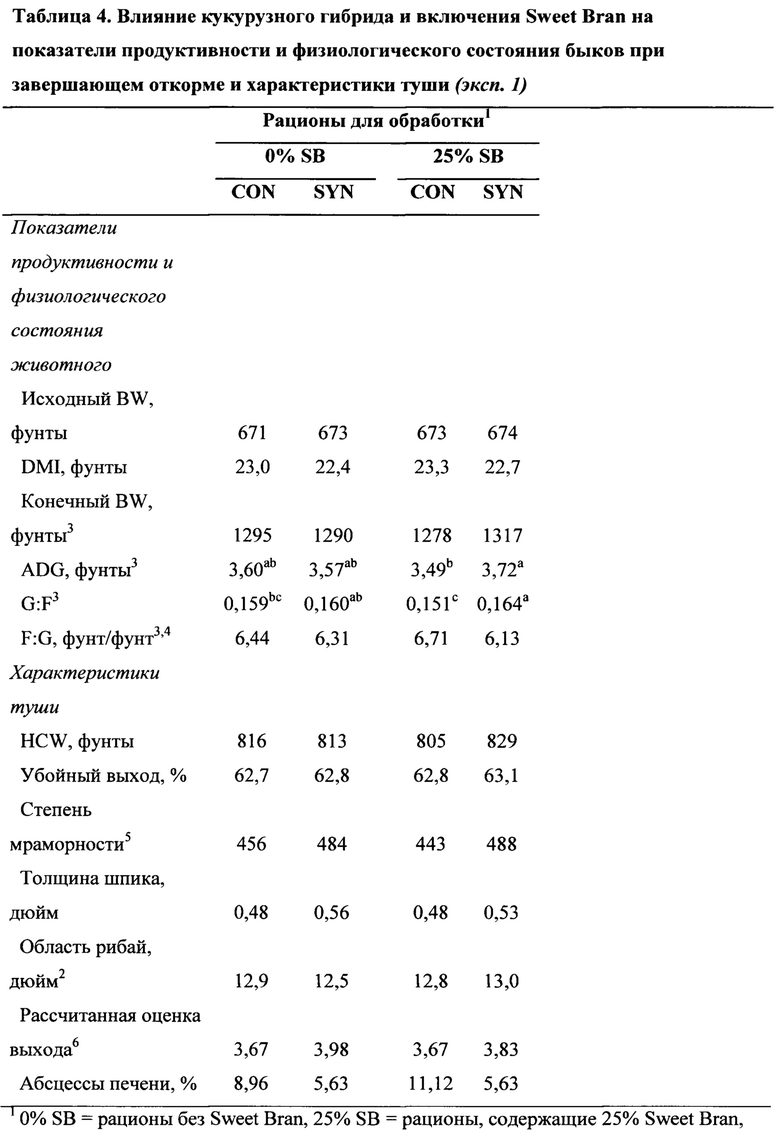



Эксперимент 3
Испытание по завершающем откорме длительностью 173 дня проводили с использованием некоторого количества кроссбредных быков (исходный BW (вес тела)=685±46 фунтов) по схеме рандомизированных блоков. Быкам скармливали рацион в ограниченном количестве, составляющем 2% от BW, который состоял из 47,5% люцернового сена, 47,5% влажного корма на основе кукурузной клейковины и 5% добавки (основа DM (сухое вещество)), в течение пяти дней перед началом эксперимента. В 0 и 1-й день регистрировали значения исходного веса в пределах двух дней и усредняли для определения исходного BW. Наряду с измерением исходного BW в 1-й день, быков имплантировали с помощью Revalor-XS. Быков разделяли на блоки по BW в блоки с легким и тяжелым BW, стратифицированные по BW и распределяли случайным образом в загон. К загонам затем случайным образом распределяли рацион для обработки с 8 поголовьями/загон и 6 повторностями/обработка.
Рационы для обработки (таблица 6) согласовывали с факторами, в том числе тестируемой кукурузой или контролем (Enogen или отличный от Enogen) и типом побочного продукта (MDGS (модифицированная зерновая барда с растворимыми веществами) или Sweet Bran). Побочные продукты, используемые в этом испытании, обеспечивали либо в качестве источника белка (18% MDGS), либо в качестве средств контроля ацидоза (35% SB (Sweet Bran® (Cargill))). Быков адаптировали к рационам завершающего откорма в течение 21-дневного периода, при этом кукурузой замещали люцерновое сено, тогда как включение соргового силоса, Sweet Bran или MDGS и добавки оставалось таким же во всех рационах. Рационы составляли с удовлетворением или превосхождением требований NRC в отношении белка и минералов. Конечные рационы завершающего откорма обеспечивал 330 мг/бык в сутки румензина (30 г/тонна DM) и 90 мг/бык в сутки тилана (8,18 г/тонна DM).
Всех быков собирали на 174-й день в коммерческой скотобойне (Greater Omaha Pack, Омаха, Небраска). Корм, обеспечиваемый на 173-й день, составлял 50% DMI предыдущего дня, и проводили взвешивание в 4:00 после полудня. Быков затем перевозили в коммерческую скотобойню и содержали до убоя на следующий день. Значения веса парной туши и показатели печени регистрировали в день убоя, при этом характеристики туши, такие как толщина жира на 12-ом ребре, область LM и степень мраморности согласно оценке USDA, регистрировали через 48 ч. охлаждения. Оценку выхода рассчитывали с применением уравнения для YG согласно USDA [YG=2,5+2,5 (толщина жира, дюйм) - 0,32 (область LM, дюйм2)+0,2 (жир КРН, %)+0,0038 (HCW, фунт)]. Конечный BW, ADG (среднесуточный прирост) и G:F (соотношение прироста к корму) рассчитывали с применением HCW (вес парной туши), скорректированного к общему убойному выходу 63%.
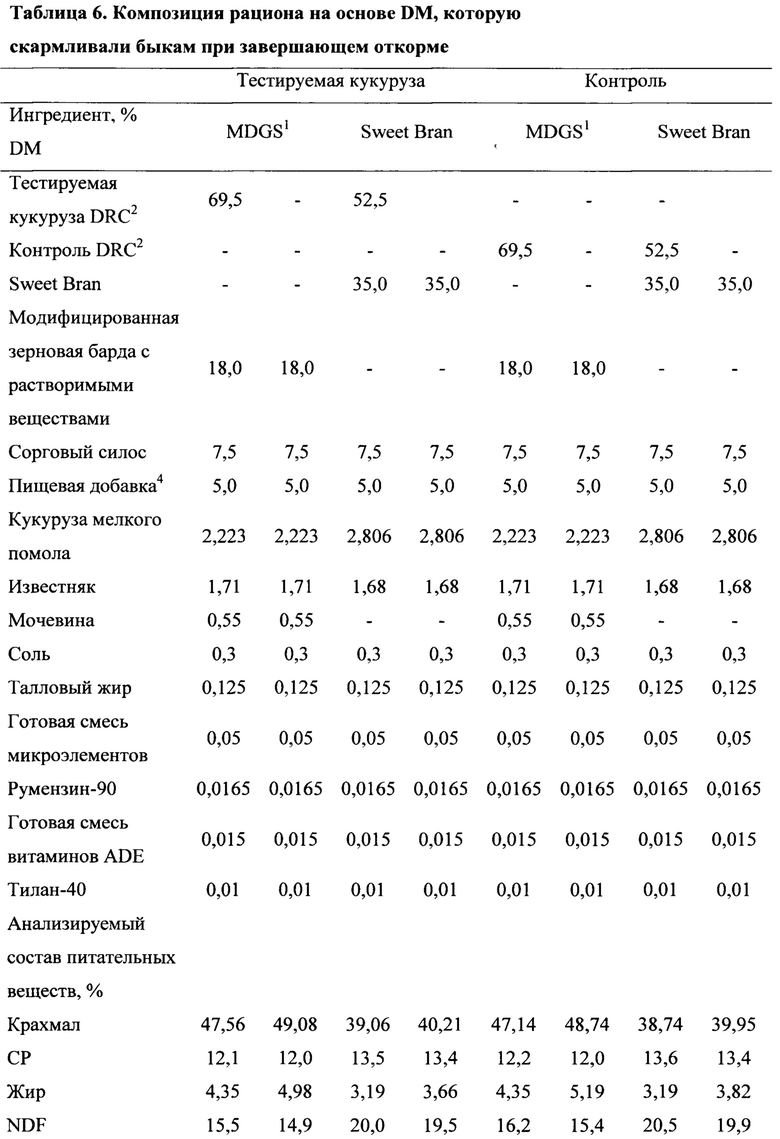

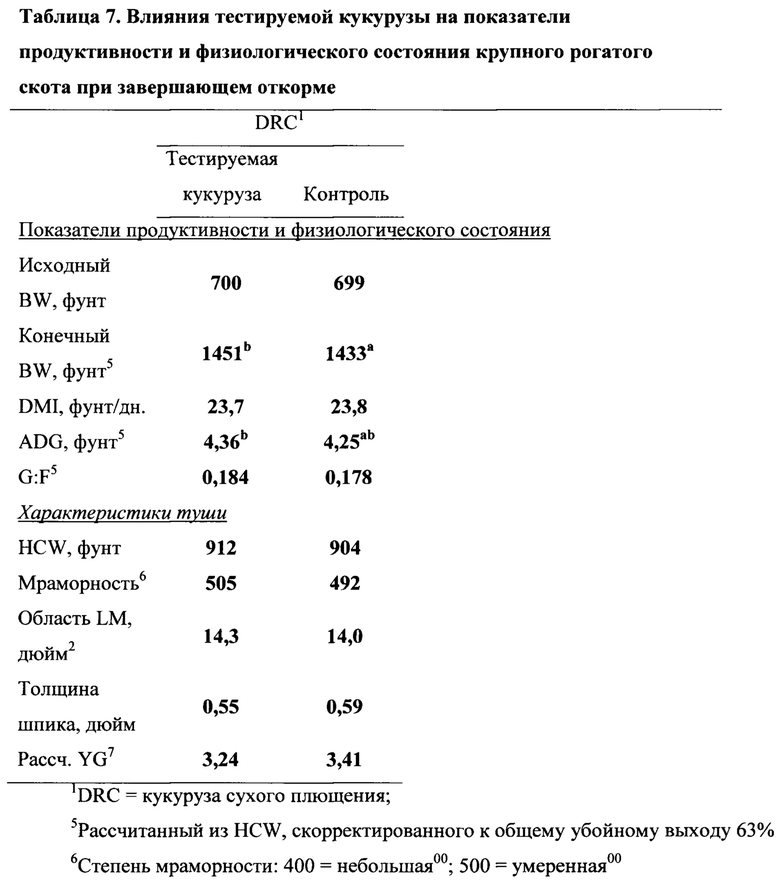

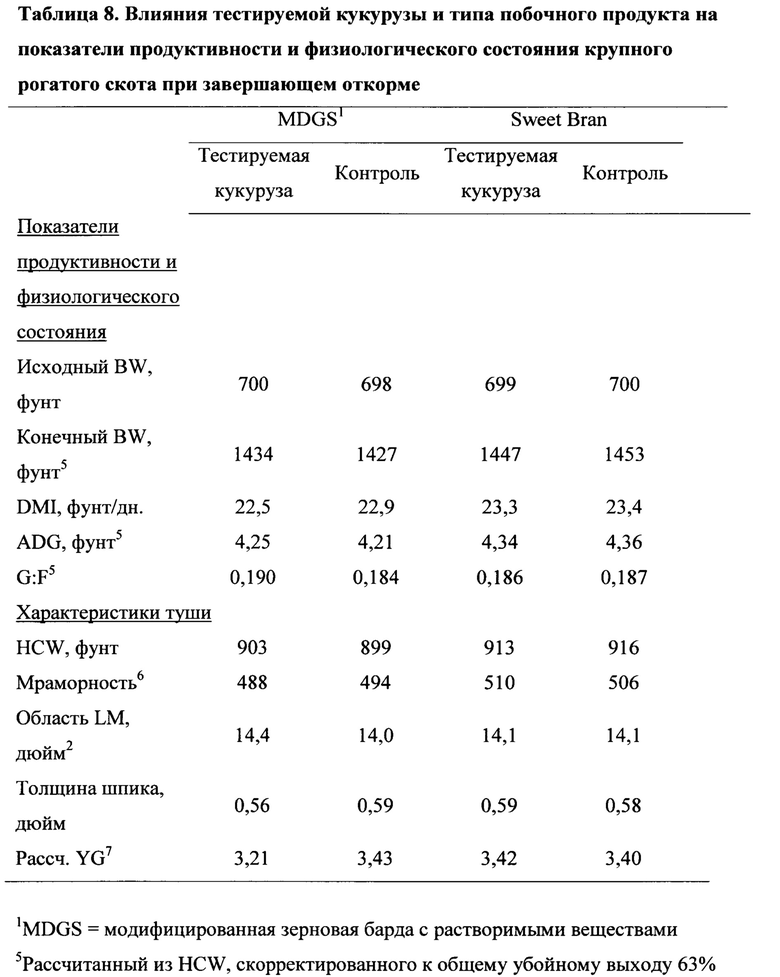
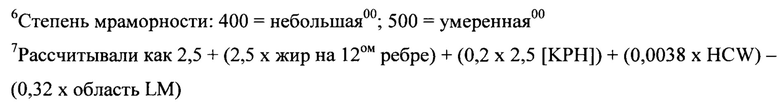
Вышеизложенное является иллюстрацией настоящего изобретения и не подразумевает его ограничение. Настоящее изобретение определяется следующей формулой изобретения, при этом в нее включены также и эквиваленты пунктов формулы изобретения.
Все публикации, заявки на патенты, патенты и другие ссылки, цитируемые в данном документе, включены с помощью ссылки во всей своей полноте для объяснения идей, относящихся к предложению и/или абзацу, в котором приведена данная ссылка.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SYNGENTA PARTICIPATIONS AG
Iragavarapu, Tammiraj Kumar
Witherspoon, David
<120> КОРМОВЫЕ КОМПОЗИЦИИ ДЛЯ ЖИВОТНЫХ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 80783-WO-REG-ORG-P-1
<150> US 62/145,587
<151> 2015-04-10
<160> 5
<170> PatentIn версия 3.5
<210> 1
<211> 436
<212> БЕЛОК
<213> Искусственная
<220>
<223> синтетический
<400> 1
Met Ala Lys Tyr Leu Glu Leu Glu Glu Gly Gly Val Ile Met Gln Ala
1 5 10 15
Phe Tyr Trp Asp Val Pro Ser Gly Gly Ile Trp Trp Asp Thr Ile Arg
20 25 30
Gln Lys Ile Pro Glu Trp Tyr Asp Ala Gly Ile Ser Ala Ile Trp Ile
35 40 45
Pro Pro Ala Ser Lys Gly Met Ser Gly Gly Tyr Ser Met Gly Tyr Asp
50 55 60
Pro Tyr Asp Tyr Phe Asp Leu Gly Glu Tyr Tyr Gln Lys Gly Thr Val
65 70 75 80
Glu Thr Arg Phe Gly Ser Lys Gln Glu Leu Ile Asn Met Ile Asn Thr
85 90 95
Ala His Ala Tyr Gly Ile Lys Val Ile Ala Asp Ile Val Ile Asn His
100 105 110
Arg Ala Gly Gly Asp Leu Glu Trp Asn Pro Phe Val Gly Asp Tyr Thr
115 120 125
Trp Thr Asp Phe Ser Lys Val Ala Ser Gly Lys Tyr Thr Ala Asn Tyr
130 135 140
Leu Asp Phe His Pro Asn Glu Leu His Ala Gly Asp Ser Gly Thr Phe
145 150 155 160
Gly Gly Tyr Pro Asp Ile Cys His Asp Lys Ser Trp Asp Gln Tyr Trp
165 170 175
Leu Trp Ala Ser Gln Glu Ser Tyr Ala Ala Tyr Leu Arg Ser Ile Gly
180 185 190
Ile Asp Ala Trp Arg Phe Asp Tyr Val Lys Gly Tyr Gly Ala Trp Val
195 200 205
Val Lys Asp Trp Leu Asn Trp Trp Gly Gly Trp Ala Val Gly Glu Tyr
210 215 220
Trp Asp Thr Asn Val Asp Ala Leu Leu Asn Trp Ala Tyr Ser Ser Gly
225 230 235 240
Ala Lys Val Phe Asp Phe Pro Leu Tyr Tyr Lys Met Asp Ala Ala Phe
245 250 255
Asp Asn Lys Asn Ile Pro Ala Leu Val Glu Ala Leu Lys Asn Gly Gly
260 265 270
Thr Val Val Ser Arg Asp Pro Phe Lys Ala Val Thr Phe Val Ala Asn
275 280 285
His Asp Thr Asp Ile Ile Trp Asn Lys Tyr Pro Ala Tyr Ala Phe Ile
290 295 300
Leu Thr Tyr Glu Gly Gln Pro Thr Ile Phe Tyr Arg Asp Tyr Glu Glu
305 310 315 320
Trp Leu Asn Lys Asp Lys Leu Lys Asn Leu Ile Trp Ile His Asp Asn
325 330 335
Leu Ala Gly Gly Ser Thr Ser Ile Val Tyr Tyr Asp Ser Asp Glu Met
340 345 350
Ile Phe Val Arg Asn Gly Tyr Gly Ser Lys Pro Gly Leu Ile Thr Tyr
355 360 365
Ile Asn Leu Gly Ser Ser Lys Val Gly Arg Trp Val Tyr Val Pro Lys
370 375 380
Phe Ala Gly Ala Cys Ile His Glu Tyr Thr Gly Asn Leu Gly Gly Trp
385 390 395 400
Val Asp Lys Tyr Val Tyr Ser Ser Gly Trp Val Tyr Leu Glu Ala Pro
405 410 415
Ala Tyr Asp Pro Ala Asn Gly Gln Tyr Gly Tyr Ser Val Trp Ser Tyr
420 425 430
Cys Gly Val Gly
435
<210> 2
<211> 1308
<212> ДНК
<213> Искусственная
<220>
<223> синтетический
<400> 2
atggccaagt acctggagct ggaggagggc ggcgtgatca tgcaggcgtt ctactgggac 60
gtcccgagcg gaggcatctg gtgggacacc atccgccaga agatccccga gtggtacgac 120
gccggcatct ccgcgatctg gataccgcca gcttccaagg gcatgtccgg gggctactcg 180
atgggctacg acccgtacga ctacttcgac ctcggcgagt actaccagaa gggcacggtg 240
gagacgcgct tcgggtccaa gcaggagctc atcaacatga tcaacacggc gcacgcctac 300
ggcatcaagg tcatcgcgga catcgtgatc aaccacaggg ccggcggcga cctggagtgg 360
aacccgttcg tcggcgacta cacctggacg gacttctcca aggtcgcctc cggcaagtac 420
accgccaact acctcgactt ccaccccaac gagctgcacg cgggcgactc cggcacgttc 480
ggcggctacc cggacatctg ccacgacaag tcctgggacc agtactggct ctgggcctcg 540
caggagtcct acgcggccta cctgcgctcc atcggcatcg acgcgtggcg cttcgactac 600
gtcaagggct acggggcctg ggtggtcaag gactggctca actggtgggg cggctgggcg 660
gtgggcgagt actgggacac caacgtcgac gcgctgctca actgggccta ctcctccggc 720
gccaaggtgt tcgacttccc cctgtactac aagatggacg cggccttcga caacaagaac 780
atcccggcgc tcgtcgaggc cctgaagaac ggcggcacgg tggtctcccg cgacccgttc 840
aaggccgtga ccttcgtcgc caaccacgac acggacatca tctggaacaa gtacccggcg 900
tacgccttca tcctcaccta cgagggccag cccacgatct tctaccgcga ctacgaggag 960
tggctgaaca aggacaagct caagaacctg atctggattc acgacaacct cgcgggcggc 1020
tccactagta tcgtgtacta cgactccgac gagatgatct tcgtccgcaa cggctacggc 1080
tccaagcccg gcctgatcac gtacatcaac ctgggctcct ccaaggtggg ccgctgggtg 1140
tacgtcccga agttcgccgg cgcgtgcatc cacgagtaca ccggcaacct cggcggctgg 1200
gtggacaagt acgtgtactc ctccggctgg gtctacctgg aggccccggc ctacgacccc 1260
gccaacggcc agtacggcta ctccgtgtgg tcctactgcg gcgtcggc 1308
<210> 3
<211> 2223
<212> ДНК
<213> Искусственная
<220>
<223> синтетический
<400> 3
atggccaagt acctggagct ggaggagggc ggcgtgatca tgcaggcgtt ctactgggac 60
gtcccgagcg gaggcatctg gtgggacacc atccgccaga agatccccga gtggtacgac 120
gccggcatct ccgcgatctg gataccgcca gcttccaagg gcatgtccgg gggctactcg 180
atgggctacg acccgtacga ctacttcgac ctcggcgagt actaccagaa gggcacggtg 240
gagacgcgct tcgggtccaa gcaggagctc atcaacatga tcaacacggc gcacgcctac 300
ggcatcaagg tcatcgcgga catcgtgatc aaccacaggg ccggcggcga cctggagtgg 360
aacccgttcg tcggcgacta cacctggacg gacttctcca aggtcgcctc cggcaagtac 420
accgccaact acctcgactt ccaccccaac gagctgcacg cgggcgactc cggcacgttc 480
ggcggctacc cggacatctg ccacgacaag tcctgggacc agtactggct ctgggcctcg 540
caggagtcct acgcggccta cctgcgctcc atcggcatcg acgcgtggcg cttcgactac 600
gtcaagggct acggggcctg ggtggtcaag gactggctca actggtgggg cggctgggcg 660
gtgggcgagt actgggacac caacgtcgac gcgctgctca actgggccta ctcctccggc 720
gccaaggtgt tcgacttccc cctgtactac aagatggacg cggccttcga caacaagaac 780
atcccggcgc tcgtcgaggc cctgaagaac ggcggcacgg tggtctcccg cgacccgttc 840
aaggccgtga ccttcgtcgc caaccacgac acggacatca tctggaacaa gtacccggcg 900
tacgccttca tcctcaccta cgagggccag cccacgatct tctaccgcga ctacgaggag 960
tggctgaaca aggacaagct caagaacctg atctggattc acgacaacct cgcgggcggc 1020
tccactagta tcgtgtacta cgactccgac gagatgatct tcgtccgcaa cggctacggc 1080
tccaagcccg gcctgatcac gtacatcaac ctgggctcct ccaaggtggg ccgctgggtg 1140
tacgtcccga agttcgccgg cgcgtgcatc cacgagtaca ccggcaacct cggcggctgg 1200
gtggacaagt acgtgtactc ctccggctgg gtctacctgg aggccccggc ctacgacccc 1260
gccaacggcc agtacggcta ctccgtgtgg tcctactgcg gcgtcggcac atcgattgct 1320
ggcatcctcg aggccgacag ggtcctcacc gtcagcccct actacgccga ggagctcatc 1380
tccggcatcg ccaggggctg cgagctcgac aacatcatgc gcctcaccgg catcaccggc 1440
atcgtcaacg gcatggacgt cagcgagtgg gaccccagca gggacaagta catcgccgtg 1500
aagtacgacg tgtcgacggc cgtggaggcc aaggcgctga acaaggaggc gctgcaggcg 1560
gaggtcgggc tcccggtgga ccggaacatc ccgctggtgg cgttcatcgg caggctggaa 1620
gagcagaagg gccccgacgt catggcggcc gccatcccgc agctcatgga gatggtggag 1680
gacgtgcaga tcgttctgct gggcacgggc aagaagaagt tcgagcgcat gctcatgagc 1740
gccgaggaga agttcccagg caaggtgcgc gccgtggtca agttcaacgc ggcgctggcg 1800
caccacatca tggccggcgc cgacgtgctc gccgtcacca gccgcttcga gccctgcggc 1860
ctcatccagc tgcaggggat gcgatacgga acgccctgcg cctgcgcgtc caccggtgga 1920
ctcgtcgaca ccatcatcga aggcaagacc gggttccaca tgggccgcct cagcgtcgac 1980
tgcaacgtcg tggagccggc ggacgtcaag aaggtggcca ccaccttgca gcgcgccatc 2040
aaggtggtcg gcacgccggc gtacgaggag atggtgagga actgcatgat ccaggatctc 2100
tcctggaagg gccctgccaa gaactgggag aacgtgctgc tcagcctcgg ggtcgccggc 2160
ggcgagccag gggttgaagg cgaggagatc gcgccgctcg ccaaggagaa cgtggccgcg 2220
ccc 2223
<210> 4
<211> 3285
<212> ДНК
<213> Aspergillus shirousami
<400> 4
gccaccccgg ccgactggcg ctcccagtcc atctacttcc tcctcaccga ccgcttcgcc 60
cgcaccgacg gctccaccac cgccacctgc aacaccgccg accagaagta ctgcggcggc 120
acctggcagg gcatcatcga caagctcgac tacatccagg gcatgggctt caccgccatc 180
tggatcaccc cggtgaccgc ccagctcccg cagaccaccg cctacggcga cgcctaccac 240
ggctactggc agcaggacat ctactccctc aacgagaact acggcaccgc cgacgacctc 300
aaggccctct cctccgccct ccacgagcgc ggcatgtacc tcatggtgga cgtggtggcc 360
aaccacatgg gctacgacgg cgccggctcc tccgtggact actccgtgtt caagccgttc 420
tcctcccagg actacttcca cccgttctgc ttcatccaga actacgagga ccagacccag 480
gtggaggact gctggctcgg cgacaacacc gtgtccctcc cggacctcga caccaccaag 540
gacgtggtga agaacgagtg gtacgactgg gtgggctccc tcgtgtccaa ctactccatc 600
gacggcctcc gcatcgacac cgtgaagcac gtgcagaagg acttctggcc gggctacaac 660
aaggccgccg gcgtgtactg catcggcgag gtgctcgacg tggacccggc ctacacctgc 720
ccgtaccaga acgtgatgga cggcgtgctc aactacccga tctactaccc gctcctcaac 780
gccttcaagt ccacctccgg ctcgatggac gacctctaca acatgatcaa caccgtgaag 840
tccgactgcc cggactccac cctcctcggc accttcgtgg agaaccacga caacccgcgc 900
ttcgcctcct acaccaacga catcgccctc gccaagaacg tggccgcctt catcatcctc 960
aacgacggca tcccgatcat ctacgccggc caggagcagc actacgccgg cggcaacgac 1020
ccggccaacc gcgaggccac ctggctctcc ggctacccga ccgactccga gctgtacaag 1080
ctcatcgcct ccgccaacgc catccgcaac tacgccatct ccaaggacac cggcttcgtg 1140
acctacaaga actggccgat ctacaaggac gacaccacca tcgccatgcg caagggcacc 1200
gacggctccc agatcgtgac catcctctcc aacaagggcg cctccggcga ctcctacacc 1260
ctctccctct ccggcgccgg ctacaccgcc ggccagcagc tcaccgaggt gatcggctgc 1320
accaccgtga ccgtgggctc cgacggcaac gtgccggtgc cgatggccgg cggcctcccg 1380
cgcgtgctct acccgaccga gaagctcgcc ggctccaaga tatgctcctc ctccaagccg 1440
gccaccctcg actcctggct ctccaacgag gccaccgtgg cccgcaccgc catcctcaac 1500
aacatcggcg ccgacggcgc ctgggtgtcc ggcgccgact ccggcatcgt ggtggcctcc 1560
ccgtccaccg acaacccgga ctacttctac acctggaccc gcgactccgg catcgtgctc 1620
aagaccctcg tggacctctt ccgcaacggc gacaccgacc tcctctccac catcgagcac 1680
tacatctcct cccaggccat catccagggc gtgtccaacc cgtccggcga cctctcctcc 1740
ggcggcctcg gcgagccgaa gttcaacgtg gacgagaccg cctacgccgg ctcctggggc 1800
cgcccgcagc gcgacggccc ggccctccgc gccaccgcca tgatcggctt cggccagtgg 1860
ctcctcgaca acggctacac ctccgccgcc accgagatcg tgtggccgct cgtgcgcaac 1920
gacctctcct acgtggccca gtactggaac cagaccggct acgacctctg ggaggaggtg 1980
aacggctcct ccttcttcac catcgccgtg cagcaccgcg ccctcgtgga gggctccgcc 2040
ttcgccaccg ccgtgggctc ctcctgctcc tggtgcgact cccaggcccc gcagatcctc 2100
tgctacctcc agtccttctg gaccggctcc tacatcctcg ccaacttcga ctcctcccgc 2160
tccggcaagg acaccaacac cctcctcggc tccatccaca ccttcgaccc ggaggccggc 2220
tgcgacgact ccaccttcca gccgtgctcc ccgcgcgccc tcgccaacca caaggaggtg 2280
gtggactcct tccgctccat ctacaccctc aacgacggcc tctccgactc cgaggccgtg 2340
gccgtgggcc gctacccgga ggactcctac tacaacggca acccgtggtt cctctgcacc 2400
ctcgccgccg ccgagcagct ctacgacgcc ctctaccagt gggacaagca gggctccctg 2460
gagatcaccg acgtgtccct cgacttcttc aaggccctct actccggcgc cgccaccggc 2520
acctactcct cctcctcctc cacctactcc tccatcgtgt ccgccgtgaa gaccttcgcc 2580
gacggcttcg tgtccatcgt ggagacccac gccgcctcca acggctccct ctccgagcag 2640
ttcgacaagt ccgacggcga cgagctgtcc gcccgcgacc tcacctggtc ctacgccgcc 2700
ctcctcaccg ccaacaaccg ccgcaactcc gtggtgccgc cgtcctgggg cgagacctcc 2760
gcctcctccg tgccgggcac ctgcgccgcc acctccgcct ccggcaccta ctcctccgtg 2820
accgtgacct cctggccgtc catcgtggcc accggcggca ccaccaccac cgccaccacc 2880
accggctccg gcggcgtgac ctccacctcc aagaccacca ccaccgcctc caagacctcc 2940
accaccacct cctccacctc ctgcaccacc ccgaccgccg tggccgtgac cttcgacctc 3000
accgccacca ccacctacgg cgagaacatc tacctcgtgg gctccatctc ccagctcggc 3060
gactgggaga cctccgacgg catcgccctc tccgccgaca agtacacctc ctccaacccg 3120
ccgtggtacg tgaccgtgac cctcccggcc ggcgagtcct tcgagtacaa gttcatccgc 3180
gtggagtccg acgactccgt ggagtgggag tccgacccga accgcgagta caccgtgccg 3240
caggcctgcg gcgagtccac cgccaccgtg accgacacct ggcgc 3285
<210> 5
<211> 1320
<212> ДНК
<213> Искусственная
<220>
<223> синтетический
<400> 5
atggcgaagc acttggctgc catgtgctgg tgcagcctcc tagtgcttgt actgctctgc 60
ttgggctccc agctggccca atcccaggtc ctcttccagg ggttcaactg ggagtcgtgg 120
aagaagcaag gtgggtggta caactacctc ctggggcggg tggacgacat cgccgcgacg 180
ggggccacgc acgtctggct cccgcagccg tcgcactcgg tggcgccgca ggggtacatg 240
cccggccggc tctacgacct ggacgcgtcc aagtacggca cccacgcgga gctcaagtcg 300
ctcaccgcgg cgttccacgc caagggcgtc cagtgcgtcg ccgacgtcgt gatcaaccac 360
cgctgcgccg actacaagga cggccgcggc atctactgcg tcttcgaggg cggcacgccc 420
gacagccgcc tcgactgggg ccccgacatg atctgcagcg acgacacgca gtactccaac 480
gggcgcgggc accgcgacac gggggccgac ttcgccgccg cgcccgacat cgaccacctc 540
aacccgcgcg tgcagcagga gctctcggac tggctcaact ggctcaagtc cgacctcggc 600
ttcgacggct ggcgcctcga cttcgccaag ggctactccg ccgccgtcgc caaggtgtac 660
gtcgacagca ccgcccccac cttcgtcgtc gccgagatat ggagctccct ccactacgac 720
ggcaacggcg agccgtccag caaccaggac gccgacaggc aggagctggt caactgggcg 780
caggcggtgg gcggccccgc cgcggcgttc gacttcacca ccaagggcgt gctgcaggcg 840
gccgtccagg gcgagctgtg gcgcatgaag gacggcaacg gcaaggcgcc cgggatgatc 900
ggctggctgc cggagaaggc cgtcacgttc gtcgacaacc acgacaccgg ctccacgcag 960
aactcgtggc cattcccctc cgacaaggtc atgcagggct acgcctatat cctcacgcac 1020
ccaggaactc catgcatctt ctacgaccac gttttcgact ggaacctgaa gcaggagatc 1080
agcgcgctgt ctgcggtgag gtcaagaaac gggatccacc cggggagcga gctgaacatc 1140
ctcgccgccg acggggatct ctacgtcgcc aagattgacg acaaggtcat cgtgaagatc 1200
gggtcacggt acgacgtcgg gaacctgatc ccctcagact tccacgccgt tgcccctggc 1260
aacaactact gcgtttggga gaagcacggt ctgagagttc cagcggggcg gcaccactag 1320
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| УСОВЕРШЕНСТВОВАННЫЕ КОРМОВЫЕ КОМПОЗИЦИИ ДЛЯ ЖИВОТНЫХ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2830148C1 |
| УСОВЕРШЕНСТВОВАННЫЕ КОРМОВЫЕ КОМПОЗИЦИИ ДЛЯ ЖИВОТНЫХ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2804140C2 |
| СПОСОБЫ ПРИМЕНЕНИЯ ТЕРМОСТАБИЛЬНЫХ СЕРИНОВЫХ ПРОТЕАЗ | 2017 |
|
RU2771261C2 |
| ПОЛИПЕПТИДЫ С ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2005 |
|
RU2393224C2 |
| ГЕН АХМ1554, КОДИРУЮЩИЙ ДЕЛЬТА-ЭНДОТОКСИН, И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2755282C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2017 |
|
RU2765722C2 |
| ГЛЮКОАМИЛАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2802790C2 |
| ПОЛИПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ, И ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ | 2006 |
|
RU2415150C2 |
| ПОЛИПЕПТИДЫ, ОБЛАДАЮЩИЕ АНТИМИКРОБНОЙ АКТИВНОВНОСТЬЮ, И ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ | 2006 |
|
RU2512525C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2016 |
|
RU2745306C2 |
Настоящее изобретение относится к биотехнологии и сельскому хозяйству и представляет собой применение материала из трансгенного растения кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влажности или любую их комбинацию, в качестве корма для животных, в котором материал из трансгенного растения кукурузы содержит рекомбинантную альфа-амилазу, где указанная рекомбинантная α-амилаза содержит полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3. Изобретение позволяет увеличить скорость привеса животных, увеличить объем надоя молока и повысить эффективность усвояемости корма. 8 н. и 15 з.п. ф-лы, 8 табл., 3 пр.
1. Применение материала из трансгенного растения кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влажности или любую их комбинацию, в качестве корма для животных, в котором материал из трансгенного растения кукурузы содержит рекомбинантную α-амилазу, где указанная рекомбинантная α-амилаза содержит полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3.
2. Применение по п. 1, где рекомбинантная α-амилаза не нацелена на ее субстрат.
3. Применение по п. 2, где рекомбинантная α-амилаза нацелена на органеллу, выбранную из группы, состоящей из хлоропласта, вакуоли, цитоплазмы, апопласта и эндоплазматического ретикулума.
4. Применение по любому из пп. 1-3, где кукуруза представляет собой трансформант кукурузы 3272.
5. Применение по любому из пп. 1-4, где животное представляет собой сельскохозяйственное животное, животное зоопарка и/или домашнее животное.
6. Способ увеличения среднесуточного привеса животного, включающий скармливание указанному животному эффективного количества материала трансгенной кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влаги или любую их комбинацию, при этом материал трансгенной кукурузы содержит рекомбинантную α-амилазу, и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3, при этом среднесуточный привес животного увеличивается на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки по сравнению с контрольным животным, которого не кормили указанным материалом трансгенной кукурузы.
7. Способ увеличения скорости роста (привеса) животного, включающий скармливание указанному животному эффективного количества материала трансгенной кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влаги или любую их комбинацию, при этом материал трансгенной кукурузы содержит рекомбинантную α-амилазу, и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3, при этом скорость роста животного увеличивается на величину от приблизительно 0,05 фунта/сутки до приблизительно 10 фунтов/сутки по сравнению с контрольным животным, которого не кормили указанным материалом трансгенной кукурузы.
8. Способ сокращения количества суток, необходимого для достижения требуемого веса у животного, включающий скармливание указанному животному эффективного количества материала трансгенной кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влаги или любую их комбинацию, при этом материал трансгенной кукурузы содержит рекомбинантную α-амилазу, и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3, за счет чего сокращается количество суток, необходимое для достижения требуемого веса, по сравнению с контрольным животным, которого не кормили указанным материалом трансгенной кукурузы.
9. Способ по п. 8, где количество суток, необходимое для достижения требуемого веса у животного, сокращается на величину от приблизительно 1 дня до приблизительно 20 дней.
10. Способ повышения эффективности усвояемости корма животным, включающий скармливание указанному животному эффективного количества материала трансгенной кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влаги или любую их комбинацию, при этом материал трансгенной кукурузы содержит рекомбинантную α-амилазу, и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3, по сравнению с контрольным животным, которого не кормили указанным материалом трансгенной кукурузы.
11. Способ по п. 10, где эффективность усвояемости корма животным повышается на величину от приблизительно 1% до приблизительно 25%.
12. Способ по любому из пп. 6-11, где животному скармливают от приблизительно 1 фунта до приблизительно 30 фунтов кормовой композиции для животных в сутки.
13. Способ по любому из пп. 6-12, где животному скармливают кормовую композицию для животных от приблизительно одного раза до приблизительно трех раз в сутки.
14. Способ по любому из пп. 6-13, где животное представляет собой млекопитающее, птицу или рыбу.
15. Способ по п. 14, где млекопитающее является представителем бычьих, овцой, козой или свиньей.
16. Способ по п. 14, где птица представляет собой курицу, индейку, перепела или утку.
17. Способ увеличения объема надоя молока от молочного животного, включающий скармливание указанному молочному животному эффективного количества материала трансгенной кукурузы, включающего кукурузные гранулы, кукурузное зерно, кукурузный силос, кукурузные ядра сухого плющения, хлопья из обработанных паром кукурузных ядер, цельные кукурузные ядра, грубодробленые кукурузные ядра, кукурузу с высоким содержанием влаги или любую их комбинацию, при этом материал трансгенной кукурузы содержит рекомбинантную α-амилазу, и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной с нуклеотидной последовательностью SEQ ID NO: 2 и/или SEQ ID NO: 3, при этом объем надоя молока от указанного молочного животного увеличивается на величину от приблизительно 5% до приблизительно 200% по сравнению с объемом надоя молока от контрольного животного, которого не кормили указанным материалом трансгенной кукурузы.
18. Способ по п. 17, где молочное животное представляет собой корову или козу.
19. Кукурузный силос, содержащий материал трансгенной кукурузы, где материал трансгенной кукурузы содержит рекомбинантную α-амилазу и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3.
20. Хлопья из обработанных паром ядер трансгенной кукурузы, где материал трансгенной кукурузы содержит рекомбинантную α-амилазу и где указанная рекомбинантная α-амилаза включает полипептид, по меньшей мере на 80% идентичный аминокислотной последовательности SEQ ID NO: 1, или полипептид, кодируемый нуклеотидной последовательностью, по меньшей мере на 80% идентичной нуклеотидной последовательности SEQ ID NO: 2 и/или SEQ ID NO: 3.
21. Силос кукурузы по п. 19 или хлопья из обработанных паром ядер трансгенной кукурузы по п. 20, в которых рекомбинантная α-амилаза не нацелена на ее субстрат.
22. Силос кукурузы или хлопья из обработанных паром ядер трансгенной кукурузы по п. 21, где рекомбинантная α-амилаза нацелена на органеллу, выбранную из группы, состоящей из хлоропласта, вакуоли, цитоплазмы, апопласта и эндоплазматического ретикулума.
23. Силос кукурузы по п. 19 или хлопья из обработанных паром ядер трансгенной кукурузы по п. 20, в которых силос кукурузы или ядра трансгенной кукурузы содержат трансформант кукурузы 3272.
| US 20030135885 A1, 17.07.2003 | |||
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТСОДЕРЖАЩЕГО ГРАНУЛЯТА ДЛЯ ЖИВОТНЫХ, ФЕРМЕНТСОДЕРЖАЩИЙ ГРАНУЛЯТ ДЛЯ ЖИВОТНЫХ, КОРМОВАЯ КОМПОЗИЦИЯ И СПОСОБ СТИМУЛИРОВАНИЯ РОСТА ЖИВОТНОГО | 2003 |
|
RU2348175C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КОРМОВ | 2013 |
|
RU2533001C2 |
| Гальванический элемент | 1928 |
|
SU10246A1 |
| МУЛЬТИЭНЗИМНАЯ КОМПОЗИЦИЯ ДЛЯ ЖИВОТНОВОДСТВА | 1993 |
|
RU2073715C1 |
| US 7557262 B2, 07.07.2009. | |||
Авторы
Даты
2021-12-15—Публикация
2016-04-08—Подача