Область техники, к которой относится изобретение
Это изобретение относится к терпенам и к их применению. В частности, изобретение относится к серрулатановым дитерпенам и к применению этих соединений при лечении заболеваний и нарушений, таких как рак.
В настоящем изобретении приводятся ссылки на различные публикации путем указания первого автора и года опубликования. Полные ссылки на эти публикации в порядке их появления в описании изобретения представлены в разделе "Ссылки" непосредственно перед формулой изобретения.
Уровень техники
Вторичные метаболиты растений являются основным источником лекарственных веществ, которые представляют собой соединения-прототипы для создания и разработки лекарственных препаратов.
Растения продуцируют смолы и экссудаты, содержащие вторичные метаболиты, для защиты бутонов цветов и почек листьев от бактерий и грибков, а также от повреждающего воздействия солнечного света. Соответственно, соединения, содержащиеся в смолах и экссудатов растений, часто обладают противомикробной активностью и антиоксидантной активностью/активностью по захвату свободных радикалов. Рабочие домашние медоносные пчелы (Apis mellifera) собирают растительные смолы/экссудаты молодых побегов и почек с определенных деревьев и кустарников. Полученную смесь называют прополисом или так называемым пчелиным клеем. Прополис представляет собой сложное смолообразное вещество, являющееся богатым источником биологически-активных веществ. Он используется пчелами в смеси с воском для герметизации трещин и отверстий в их ульях и в качестве дезинфицирующего средства для защиты от микробных инфекций. Лечебные свойства прополиса используются человеком с древних времен.
В настоящее время прополис производится в значительных количествах в качестве природного лечебного средства и широко используется в косметических препаратах. Однако в настоящий момент его применение в медицине в основном ограничено, так как химический состав прополиса изменяется в широком диапазоне в результате того, что медоносные пчелы собирают мед из разных растительных источников или из смеси растительных источников. Состав прополиса зависит от окружающей растительности, к которой пчелы имеют доступ, и, соответственно, различия в растительности могут приводить к различиям в составах прополиса. Например, известно, что в европейском прополисе основными фармакологически активными соединениями являются флавоноиды, в кубинском и венесуэльском прополисе основными веществами являются полипренилированные бензофеноны, а в бразильском прополисе преобладают пренилированные производные коричной кислоты.
Признание того, что вырабатываемый медоносными пчелами прополис имеет растительное происхождение, предполагает размещение ульев в соответствующих благоприятных местах, в результате чего можно производить прополис из одного растительного источника, получая лекарственные препараты высокого качества и с высокой активностью.
Лечебная уникальность прополиса определяется способностью медоносных пчел избирательно его собирать, поскольку они могут распознавать природные материалы, которые являются относительно неполярными и обладают свойствами антибиотиков. Сообщалось, что типичным источником прополиса являются экссудаты листовых почек и цветочных бутонов, которые характеризуются высокой антибиотической активностью при защите роста нежной растительной ткани от нападения микроорганизмов. Также сообщалось, что медоносные пчелы собирают прополис из экссудатов тканей поврежденных или пораженных болезнью растений. Такие источники могут содержать повышенные количества антибиотиков, вырабатываемых растениями в ответ на повреждения или на нападения насекомых, микроорганизмов и вирусов.
Лечебные свойства прополиса связаны с биологической активностью отдельных растительных смол/экссудатов. В ранее проведенных исследованиях не было выяснено, собирают ли пчелы растительный материал, известный как прополис, или имеет место метаболическая модификация или дополнение в результате воздействия на материал пчел. Однако, очевидно, что нет доказательств того, что медоносные пчелы добавляют значительное количество материала, так же как нет убедительных доказательств наличия метаболической трансформации. Поэтому, необходимо более глубоко представлять себе специфику состава прополиса в конкретных географических областях, для того чтобы иметь возможность как можно более эффективно использовать прополис для разработки новых средств для лечения заболеваний и нарушений, таких как рак.
Сущность изобретения
В исследовании, в результате которого создано настоящее изобретение, был проведен анализ образцов прополиса, собранных на острове Кенгуру (Южная Австралия). Неожиданно, авторы изобретения обнаружили, что в отличие от других видов прополиса, которые обычно содержат в качестве активных компонентов флавоноиды, прополис с острова Кенгуру из растений рода Myoporum, в частности, Myoporum insulare, содержит серрулатановые дитерпены. Поэтому, настоящее изобретение относится к соединениям, выделенным из смол/экссудатов листьев и листовых почек растения Myoporum insulare, из прополиса, полученного из этого растения, и к применению этих соединений.
Myoporum insulare представляет собой кустарник, встречающийся на гребнях гор и береговых обрывах в Австралии. Обиходные названия включают boobialla, природный можжевельник и, в Западной Австралии, черничное дерево. Myoporum представляет собой род из приблизительно 30 видов, из которых шестнадцать встречаются в Австралии. Myoporum insulare обитает в различных местах и может представлять собой густой или разреженный кустарник или небольшое дерево до 6 метров высотой. Листья имеют форму от ланцетовидной до эллиптической, длину 30-100 мм и ширину 10-20 мм с глянцевым зеленым цветом. Цветки появляются группами до 8 штук в пазухах листьев в конце весны и летом, и они обычно имеют белый цвет или иногда бледно-розовый.
Авторы изобретения выделили пять основных соединений, а именно, соединения 1-5, из прополиса, полученного из Myoporum insulare. Соединения 1-5 показаны в таблице 1. Общепринятая нумерация для серрулатановых соединений показана применительно к соединению 1. Как правило, серрулатановые дитерпены имеют (1R,4S)-конфигурацию (Ghisalberti, 1994).
При окислении соединения 1 образуется его производное, соединение 6. Кроме того, что касается получения производных, то соединения могут быть подвергнуты ацилированию, алкилированию, алкенилирование или бензоилированию по трем свободным гидроксильным группам. Например, соединения 1 и 2 могут быть ацетилированы с получением производных 7 и 8, в то время как бензоилирование может давать производные 9 и 10.
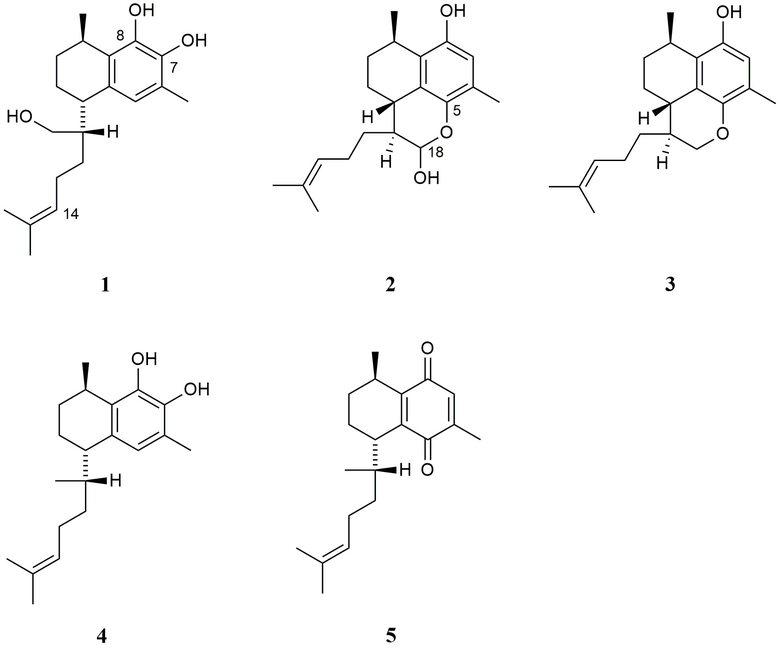
Таблица 1. Типичные серрулатановые дитерпиноидные соединения.
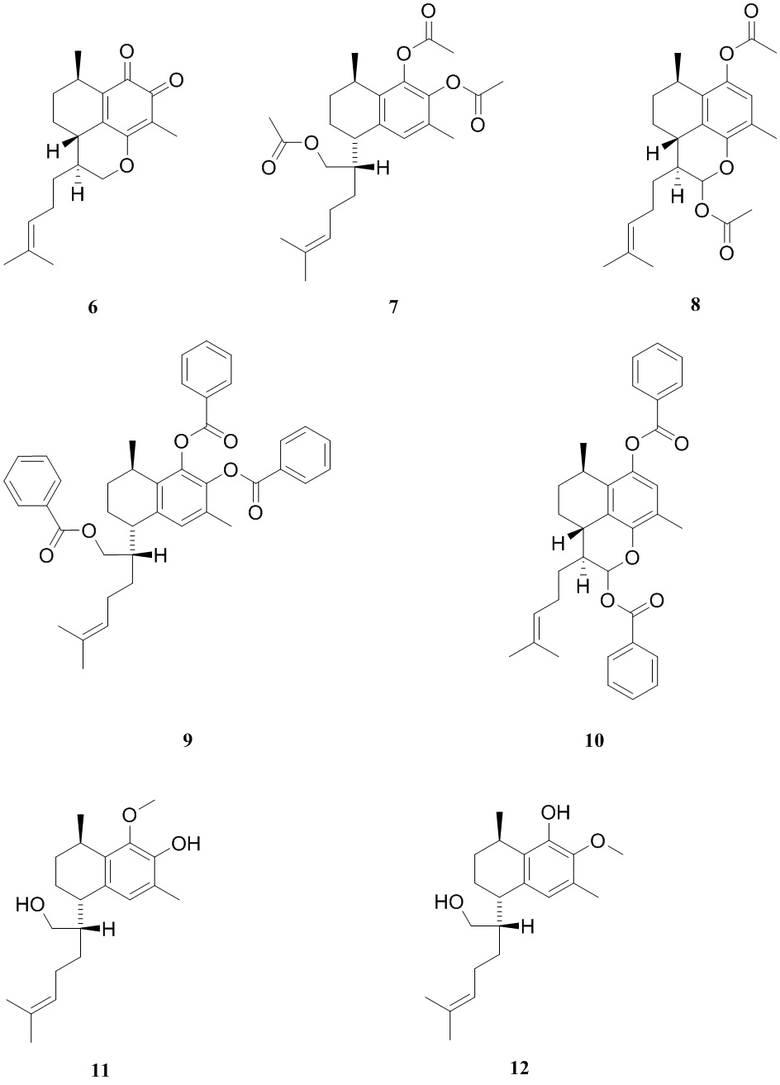
Таблица 2. Серрулатановые дитерпиноидные производные.
Типичные соединения оценивали на их фармакологическую активность, и было обнаружено, что они могут применяться при модулировании ряда заболеваний или нарушений. Например, было обнаружено, что соединения ингибируют пролиферацию раковых клеток и демонстрируют ингибирование, с активностью в диапазоне от умеренной до высокой, различных мишеней, связанных с раковой патологией. Это указывает на то, что серрулатановые дитерпеновые соединения по настоящему изобретению могут применяться в качестве терапевтических средств, например, для лечения рака. Поэтому, описанные в изобретении серрулатановые дитерпены представляют большой интерес в качестве соединений-прототипов для поиска и разработок новых лекарственных средств и как биологический инструментарий для дальнейшего понимания патофизиологии заболеваний и нарушений, таких как рак.
Соответственно, в первом аспекте, предлагается способ лечения рака, где способ включает введение терапевтически эффективного количества соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата, или фармацевтической композиции, включающей указанные соединения, субъекту, нуждающемуся в этом,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
Согласно второму аспекту, предлагается применение соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при приготовлении лекарственного препарата для лечения рака.
Согласно третьему аспекту, предлагается применение соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при лечении рака.
Согласно четвертому аспекту, предлагается соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
для применения при лечении рака.
Согласно пятому аспекту, предлагается соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
Согласно шестому аспекту, предлагается фармацевтическая композиция, включающая соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват согласно пятому аспекту и фармацевтически приемлемое вспомогательное вещество.
Согласно седьмому аспекту, предлагается фармацевтическая композиция, включающая соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват согласно пятому аспекту или их смесь и фармацевтически приемлемое вспомогательное вещество.
Согласно восьмому аспекту, предлагается соединение, которое определено в пятом аспекте, выделенное из прополиса, где прополис образуется из растений рода Myoporum.
Согласно девятому аспекту, предлагается соединение, которое определено в пятом аспекте, выделенное из смолы, камеди или экссудата растения рода Myoporum.
Согласно десятому аспекту, предлагается способ лечения заболевания или нарушения, где способ включает введение терапевтически эффективного количества соединения согласно пятому аспекту или композиции согласно шестому или седьмому аспекту.
Согласно одиннадцатому аспекту, предлагается применение соединения согласно пятому аспекту при приготовлении лекарственного препарата для лечения заболевания или нарушения.
Согласно двенадцатому аспекту, предлагается соединение согласно пятому аспекту или композиция согласно шестому аспекту или седьмому аспекту при лечении заболевания или нарушения.
Согласно тринадцатому аспекту настоящего изобретения, предлагается соединение согласно пятому аспекту или композиция согласно шестому аспекту или седьмому аспекту для применения при лечении заболевания или нарушения.
Краткое описание чертежей
На фигуре 1 приведен типичный спектр 1H ЯМР (400 МГц, CDCl3) 4:1 смеси монометилированных продуктов (соединений 11 и 12).
На фигуре 2 приведен типичный спектр 13C ЯМР (100 МГц, CDCl3) 4:1 смеси монометилированных продуктов (соединений 11 и 12).
На фигурах 3-6 приведены примеры кривых связывания для соединения 1 с эпигенетическими мишенями.
На фигуре 3 показана кривая связывания с ASH1L(h) бромодоменом.
На фигуре 4 показана кривая связывания с CECR2(h) бромодоменом.
На фигуре 5 показана кривая связывания с SP140 (h) бромодоменом.
На фигуре 6 показана кривая связывания с UHRF1(108-286) (h).
На фигуре 7 графически представлены данные по связыванию 5-липоксигеназы для соединения 1 (голубые кружки, IC50=2,31 мкМ) и референсного соединения NGA (красные квадратики, IC50=0,64 мкМ).
На фигуре 8 графически представлены данные по связыванию липидной пероксидазы для соединения 1 (голубые кружки, IC50=1,47 мкМ) и референсного соединения N-пропилгаллата (красные квадратики, IC50=165 мкМ).
На фигуре 9 графически представлены данные по связыванию моноаминоксидазы (MAO-A) для соединения 1 (голубые кружки, IC50=6,74 мкМ) и референсного соединения клоргилина (красные квадратики, IC50=1,43 нM).
На фигуре 10 графически представлены данные по транскрипционному ответу и связыванию NF-κB для соединения 1 (голубые кружки, IC50=1,36 мкМ) и референсного соединения циклоспорина A (красные квадратики, IC50=0,029 мкМ).
На фигуре 11 графически представлены данные по пролиферативному ответу при обработке линии клеток MDA-MB-415 с помощью соединения 1.
На фигуре 12 графически представлены данные по пролиферативному ответу при обработке линии клеток RKO-AS45-1 с помощью соединения 1.
На фигуре 13 графически представлены данные по пролиферативному ответу при обработке линии клеток SW480 с помощью соединения 1.
На фигуре 14 графически представлены данные по пролиферативному ответу при обработке линии клеток 639-V с помощью соединения 1.
На фигуре 15 графически представлены данные по пролиферативному ответу при обработке линии клеток Hs 729 с помощью соединения 1.
На фигуре 16 графически представлены данные по пролиферативному ответу при обработке линии клеток Hs 852.T с помощью соединения 1.
На фигуре 17 графически представлены данные по пролиферативному ответу при обработке линии клеток HCT-8 с помощью соединения 1.
На фигуре 18 графически представлены данные по пролиферативному ответу при обработке линии клеток IM-9 с помощью соединения 1.
На фигуре 19 графически представлены данные по пролиферативному ответу при обработке линии клеток HREC с помощью соединения 1 при проведении исследования пролиферации нормальных клеток, используя OncoPanelТМ.
Далее описаны конкретные варианты осуществления изобретения. Следует иметь в виду, что эти варианты осуществления являются только иллюстрациями и не ограничивают объем изобретения.
Подробное описание изобретения
В изобретении раскрывается способ лечения рака, где способ включает введение терапевтически эффективного количества соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата, или фармацевтической композиции, включающей указанные соединения, субъекту, нуждающемуся в этом,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если соединение представляет собой соединение формулы (Ia):
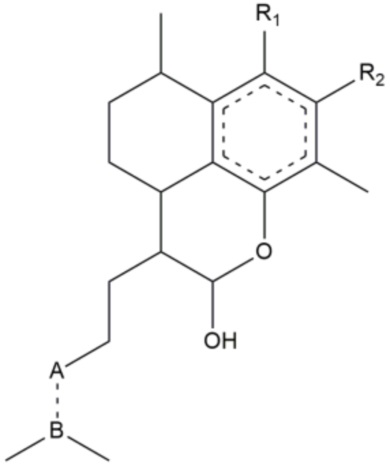
(Ia).
Предпочтительно, если соединение представляет собой соединение формулы (Ib):

(Ib).
Предпочтительно, если соединение представляет собой соединение формулы (Ic):
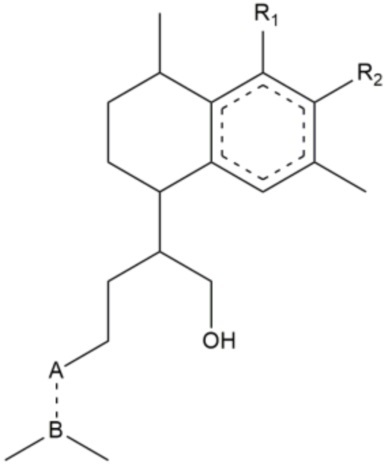
(Ic).
Предпочтительно, если соединение представляет собой соединение формулы (Id):

(Id).
Предпочтительно, если соединение представляет собой соединение формулы (Ie):

(Ie).
Предпочтительно, если соединение представляет собой соединение формулы (If):

(If).
Предпочтительно, если соединение представляет собой соединение формулы (Ig):

(Ig).
Предпочтительно, если соединение представляет собой соединение формулы (Ih):

(Ih).
Предпочтительно, если соединение представляет собой соединение формулы (Ii):

(Ii).
Предпочтительно, если A---B обозначает CH=C.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
, ,
, ,
,
 ,
,  ,
,
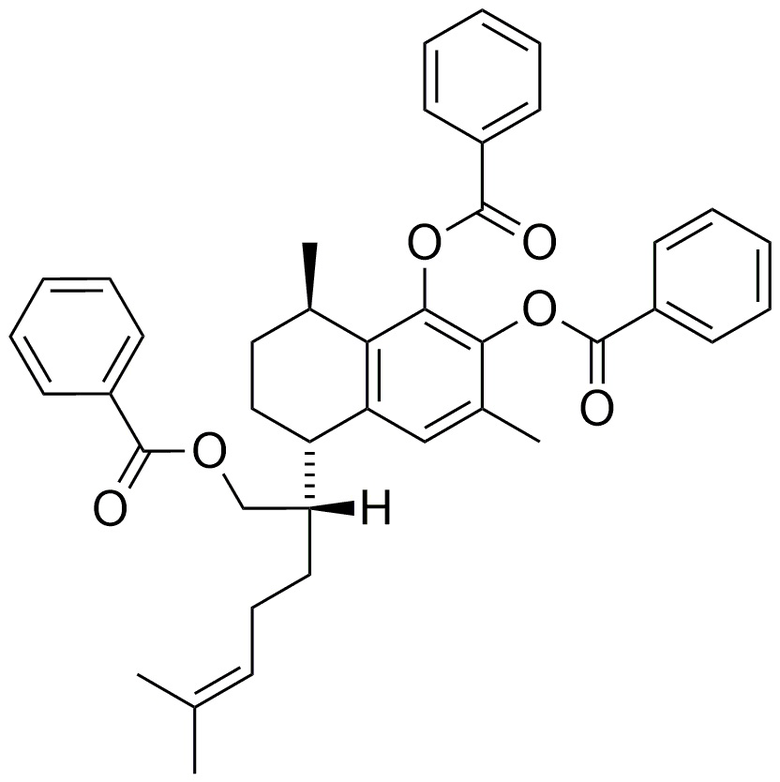 ,
,  ,
,
 и
и 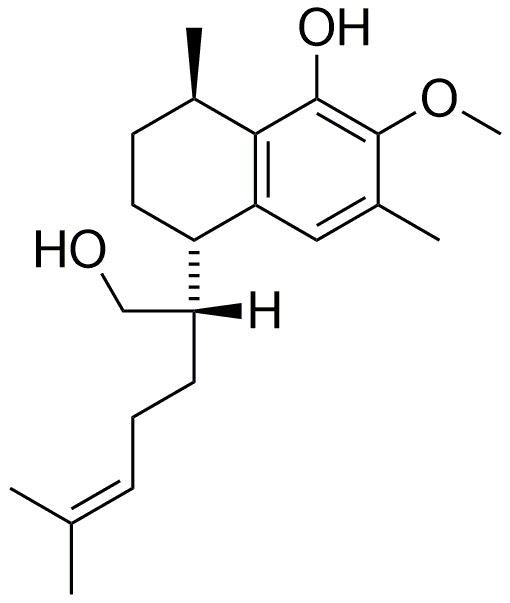 .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
, ,
, ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и  .
.
Соединение предпочтительно представляет собой
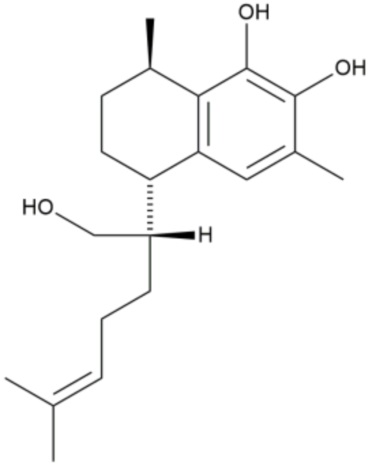 .
.
Предпочтительно, если соединение представляет собой
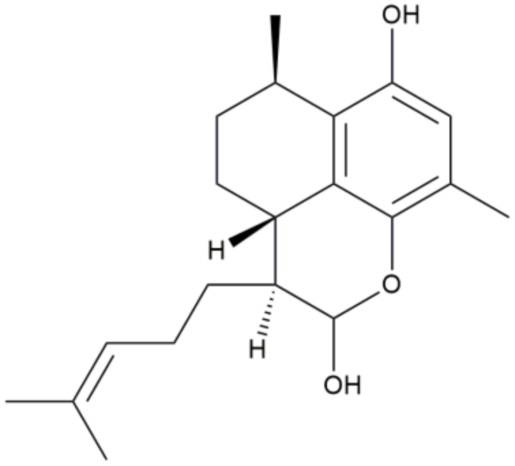 .
.
Соединение предпочтительно представляет собой
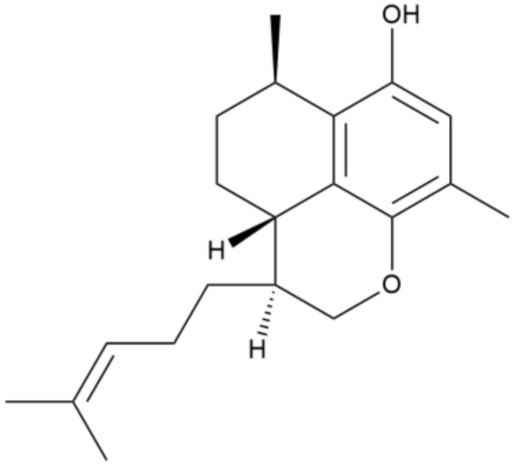 .
.
Предпочтительно, если соединение представляет собой
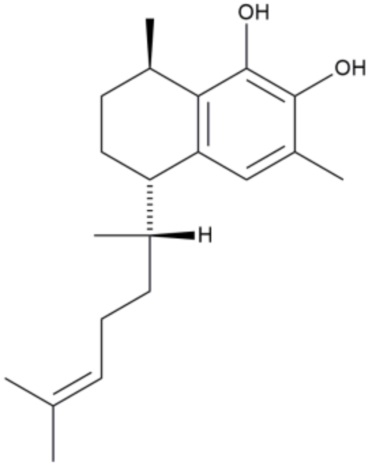 .
.
Соединение предпочтительно представляет собой
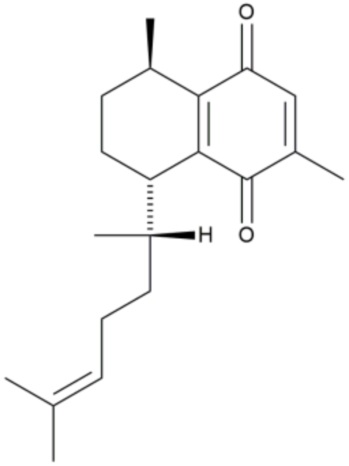 .
.
Предпочтительно, если соединение представляет собой
 .
.
Предпочтительно, чтобы рак представлял собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
Предпочтительно, чтобы рак центральной нервной системы представляет собой глиому. Предпочтительно, чтобы рак центральной нервной системы представлял собой медуллобластому. Предпочтительно, чтобы рак центральной нервной системы представлял собой нейробластому.
Предпочтительно, чтобы рак легких представлял собой немелкоклеточный рак легких. Предпочтительно, чтобы рак легких представлял собой мелкоклеточный рак легких.
Предпочтительно, чтобы карцинома представляла собой аденосквамозную карциному или сквамозную карциному.
Предпочтительно, чтобы саркома представляла собой липосаркому, рабдомиосаркому или фибросаркому. Предпочтительно, чтобы саркома представляла собой саркому мягких тканей. Предпочтительно, чтобы саркома мягких тканей представляла собой остеосаркому мягких тканей.
Предпочтительно, чтобы лимфома представляла собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
Несмотря на то, что, в случае применения для лечения, описанные в изобретении соединения или их фармацевтически приемлемая соль или сольват могут быть введены в терапевтически эффективном количестве в виде самого по себе химического вещества в чистом виде, тем не менее, в первом аспекте настоящего изобретения, активный ингредиент вводят в виде фармацевтической композиции. Поэтому, настоящее изобретение также предусматривает фармацевтическую композицию, включающую соединение формулы (I) - (Ii) или его фармацевтически приемлемую соль или сольват и фармацевтически приемлемое вспомогательное вещество. Вспомогательное вещество должно быть приемлемым в смысле его совместимости с другими ингредиентами композиции и безопасности для реципиента.
При необходимости, соединения по настоящему изобретению, включающие соединения формулы (I) - (Ii), могут быть в форме фармацевтически приемлемой соли и/или могут быть введены в форме фармацевтически приемлемой соли.
Используемый в изобретении термин "фармацевтически приемлемая соль" относится к солям, которые являются безопасными с точки зрения их токсического действия при системном введении. Фармацевтически приемлемые соли могут быть выбраны из солей щелочных или щелочноземельных металлов, включающих, натрий, литий, калий, кальций, магний и другие подобные металлы, а также нетоксичных катионов аммония, четвертичного аммония и амина, включающих, но этим не ограничивая, аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин, триэтаноламин и другие подобные катионы.
Используемый в изобретении термин "фармацевтически приемлемое вспомогательное вещество" относится к твердому или жидкому наполнителю, носителю, разбавителю или инкапсулирующему веществу, которые можно безопасно использовать при введении. В зависимости от конкретного способа введения, может быть использован целый ряд хорошо известных носителей. Эти носители или вспомогательные вещества могут быть выбраны из группы, включающей сахара, крахмалы, целлюлозу и ее производные, солод, желатин, тальк, сульфат кальция, растительные масла, синтетические масла, полиолы, альгиновую кислоту, забуференные фосфатом растворы, эмульгаторы, изотонический раствор и апирогенную воду.
Используемый в изобретении термин "сольват" относится к комплексу с переменной стехиометрией, образованному растворенным веществом (в этом изобретении, соединением формулы (I) - (Ii) или его солью или физиологически функциональным производным) и растворителем. Применительно к настоящему изобретению, такие растворители не должны отрицательно влиять на биологическую активность растворенного вещества. Примеры подходящих растворителей включают, но этим не ограничивая, воду, метанол, этанол и уксусную кислоту. В частности, используемый растворитель является фармацевтически приемлемым растворителем. Примеры подходящих фармацевтически приемлемых растворителей включают, но этим не ограничивая, воду, этанол, уксусную кислоту, глицерин, жидкие полиэтиленгликоли и их смеси. Конкретным примером растворителя является вода.
Введение соединений формулы (I) - (Ii) может быть осуществлено в форме "пролекарства". Пролекарство представляет собой неактивную форму соединения, которая превращается in vivo в активную форму. Подходящие пролекарства включают эфиры, фосфонатные эфиры и другие подобные эфиры активной формы соединения.
Следует иметь в виду, что помимо указанных конкретно выше ингредиентов, композиции могут включать и другие вещества, традиционно используемые при приготовлении данного типа композиции.
Соединения по настоящему изобретению могут применяться для лечения заболеваний у человека или животного. В одном примере, субъектом лечения является млекопитающее, включая человека, лошадь, собаку, кошку, овцу, корову или примата. В другом примере, субъектом лечения является человек. В еще одном примере, субъект лечения не является человеком. Термины "субъект" и "пациент" используются в изобретении взаимозаменяемо.
Используемый в изобретении термин "эффективное количество" обозначает количество лекарственного средства или фармацевтического препарата, которое позволяет получить биологический или лечебный ответ ткани, системы, животного или человека, который стремится достигнуть, например, исследователь или лечащий врач.
Кроме того, термин "терапевтические эффективное количество" обозначает любое количество, которое, по сравнению с соответствующим субъектом, который не получал такого количества, приводит к улучшению результатов лечения, выздоровлению или облегчению заболевания, нарушения или побочного эффекта, или к уменьшению скорости развития заболевания или нарушения. Термин также включает в рамках области его применения количества, которые являются эффективными для усиления нормальной физиологической функции. Термин также включает в рамках области его применения количества, которые являются эффективными для предотвращения возникновения заболевания, нарушения или побочного эффекта.
Используемый в изобретении термин "лечение" относится к защите от симптома или подавлению симптома, к лечению симптома, замедлению проявления симптома, снижению тяжести развития симптома и/или снижению числа или типов симптомов, от которых страдает индивидуум, по сравнению со случаем, когда индивидууму не вводят фармацевтическую композицию, включающую соединение по изобретению. Термин также включает в рамках области его применения предотвращение возникновения заболевания, нарушения или побочного эффекта. Термин "лечение" включает в себя и паллиативное лечение.
Противоопухолевой эффект соединений по настоящему изобретению может быть достигнут при использовании монотерапии или комбинированной терапии, то есть, когда два или более серрулатановых дитерпеноидов могут вводиться в комбинации. Терапия может также включать введение смеси двух или более серрулатановых дитерпеноидов. Кроме того, терапия может включать введение одного или более других веществ и/или лекарственных средств. Такое объединенное лечение может быть достигнуто путем одновременного, последовательного или раздельного применения индивидуальных компонентов лечения. В области лекарственной терапии злокачественных опухолей, обычной практикой является использование комбинации различных форм лечения страдающего от рака пациента, такой как комбинация хирургического вмешательства, радиационной терапии и/или химиотерапии. В частности, известно, что лучевая терапия или лечение с помощью антиангиогенных и/или снижающих проницаемость сосудов средств может увеличивать количество гипоксической ткани внутри опухоли. Поэтому, эффективность соединений по настоящему изобретению может быть повышена за счет объединенного лечения с использованием радиационной терапии и/или антиангиогенного средства.
Индивидуальные компоненты таких комбинаций могут быть введены раздельно в различные моменты времени в процессе проведения терапии или одновременно в разделенных или одной лекарственных формах. Поэтому, следует иметь в виду, что настоящее изобретение охватывает все такие режимы одновременного или чередующегося лечения, и термин "введение" следует интерпретировать соответствующим образом. Следует иметь в виду, что возможные варианты комбинаций соединений по этому изобретению с другими противоопухолевыми средствами включает, по существу, любую комбинацию с любой фармацевтической композицией, применяемой для лечения рака.
В случае объединения в одной и той же лекарственной форме, следует иметь в виду, что эти два соединения должны быть стабильными и совместимыми друг с другом и другими компонентами лекарственной формы, и их можно приготовить в такой форме для введения. В случае приготовления раздельных лекарственных форм, они могут быть приготовлены в виде любой подходящей лекарственной формы, желательно, такими методами, которые хорошо известны для таких соединений.
Фармацевтические композиции по настоящему изобретению могут быть приготовлены для соответствующего способа введения, например, для перорального (включая буккальный или сублингвальный), ректального, назального, местного (включая буккальный, сублингвальный или трансдермальный), вагинального или парентерального (включая подкожный, внутримышечный, внутривенный или интрадермальный) способа. Поэтому, фармацевтические композиции по изобретению могут быть приготовлены, например, в форме таблеток, капсул, порошков, гранул, пастилок, кремов или жидких препаратов, таких как пероральные или стерильные парентеральные растворы или суспензии. Такие фармацевтические композиции могут быть приготовлены любым известным в фармацевтике методом, например, путем смешения активного ингредиента с носителем (носителями) или вспомогательным веществом (веществами). Такие фармацевтические композиции могут быть приготовлены в форме покрытых энтеросолюбильной оболочкой гранул, таблеток или капсул, применяемых для введения, и в форме фармацевтических композиций с отсроченным высвобождением.
Когда соединение используют в комбинации со вторым терапевтическим средством, обладающим активностью в отношении этого же заболевания, доза каждого соединения может отличаться от дозы, при которой соединение используют при монотерапии. Соответствующие дозы могут быть легко определены специалистами в этой области.
Кроме того, в изобретении раскрывается применение соединения формулы (I),

(I)
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при приготовлении лекарственного препарата для лечения рака.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если соединение представляет собой соединение формулы (Ia):

(Ia).
Предпочтительно, если соединение представляет собой соединение формулы (Ib):

(Ib).
Предпочтительно, если соединение представляет собой соединение формулы (Ic):

(Ic).
Предпочтительно, если соединение представляет собой соединение формулы (Id):

(Id).
Предпочтительно, если соединение представляет собой соединение формулы (Ie):

(Ie).
Предпочтительно, если соединение представляет собой соединение формулы (If):

(If).
Предпочтительно, если соединение представляет собой соединение формулы (Ig):

(Ig).
Предпочтительно, если соединение представляет собой соединение формулы (Ih):

(Ih).
Предпочтительно, если соединение представляет собой соединение формулы (Ii):

(Ii).
Предпочтительно, если A---B обозначает CH=C.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и  .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Предпочтительно, чтобы рак представлял собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
Предпочтительно, чтобы рак центральной нервной системы представлял собой глиому. Предпочтительно, чтобы рак центральной нервной системы представлял собой медуллобластому. Предпочтительно, чтобы рак центральной нервной системы представлял собой нейробластому.
Предпочтительно, чтобы рак легких представлял собой немелкоклеточный рак легких. Предпочтительно, чтобы рак легких представлял собой мелкоклеточный рак легких.
Предпочтительно, чтобы карцинома представляла собой аденосквамозную карциному или сквамозную карциному.
Предпочтительно, чтобы саркома представляла собой липосаркому, рабдомиосаркому или фибросаркому. Предпочтительно, чтобы саркома представляла собой саркому мягких тканей. Предпочтительно, чтобы саркома мягких тканей представляла собой остеосаркому мягких тканей.
Предпочтительно, чтобы лимфома представляла собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
В изобретении также раскрывается применение соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при лечении рака.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если:
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если соединение представляет собой соединение формулы (Ia):

(Ia).
Предпочтительно, если соединение представляет собой соединение формулы (Ib):

(Ib).
Предпочтительно, если соединение представляет собой соединение формулы (Ic):

(Ic).
Предпочтительно, если соединение представляет собой соединение формулы (Id):

(Id).
Предпочтительно, если соединение представляет собой соединение формулы (Ie):

(Ie).
Предпочтительно, если соединение представляет собой соединение формулы (If):

(If).
Предпочтительно, если соединение представляет собой соединение формулы (Ig):

(Ig).
Предпочтительно, если соединение представляет собой соединение формулы (Ih):

(Ih).
Предпочтительно, если соединение представляет собой соединение формулы (Ii):

(Ii).
Предпочтительно, если A---B обозначает CH=C.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и 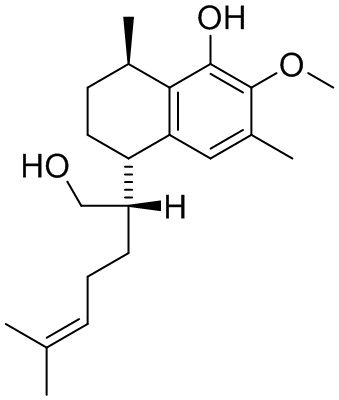 .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и  .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Предпочтительно, чтобы рак представлял собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
Предпочтительно, чтобы рак центральной нервной системы представлял собой глиому. Предпочтительно, чтобы рак центральной нервной системы представлял собой медуллобластому. Предпочтительно, чтобы рак центральной нервной системы представлял собой нейробластому.
Предпочтительно, чтобы рак легких представлял собой немелкоклеточный рак легких. Предпочтительно, чтобы рак легких представлял собой мелкоклеточный рак легких.
Предпочтительно, чтобы карцинома представляла собой аденосквамозную карциному или сквамозную карциному.
Предпочтительно, чтобы саркома представляла собой липосаркому, рабдомиосаркому или фибросаркому. Предпочтительно, чтобы саркома представляла собой саркому мягких тканей. Предпочтительно, чтобы саркома мягких тканей представляла собой остеосаркому мягких тканей.
Предпочтительно, чтобы лимфома представляла собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
В изобретении также раскрывается соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
для применения при лечении рака.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если соединение представляет собой соединение формулы (Ia):

(Ia).
Предпочтительно, если соединение представляет собой соединение формулы (Ib):

(Ib).
Предпочтительно, если соединение представляет собой соединение формулы (Ic):

(Ic).
Предпочтительно, если соединение представляет собой соединение формулы (Id):

(Id).
Предпочтительно, если соединение представляет собой соединение формулы (Ie):

(Ie).
Предпочтительно, если соединение представляет собой соединение формулы (If):

(If).
Предпочтительно, если соединение представляет собой соединение формулы (Ig):

(Ig).
Предпочтительно, если соединение представляет собой соединение формулы (Ih):

(Ih).
Предпочтительно, если соединение представляет собой соединение формулы (Ii):

(Ii).
Предпочтительно, если A---B обозначает CH=C.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
, и
и  .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Предпочтительно, чтобы рак представлял собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
Предпочтительно, чтобы рак центральной нервной системы представлял собой глиому. Предпочтительно, чтобы рак центральной нервной системы представлял собой медуллобластому. Предпочтительно, чтобы рак центральной нервной системы представлял собой нейробластому.
Предпочтительно, чтобы рак легких представлял собой немелкоклеточный рак легких. Предпочтительно, чтобы рак легких представлял собой мелкоклеточный рак легких.
Предпочтительно, чтобы карцинома представляла собой аденосквамозную карциному или сквамозную карциному.
Предпочтительно, чтобы саркома представляла собой липосаркому, рабдомиосаркому или фибросаркому. Предпочтительно, чтобы саркома представляла собой саркому мягких тканей. Предпочтительно, чтобы саркома мягких тканей представляла собой остеосаркому мягких тканей.
Предпочтительно, чтобы лимфома представляла собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
В изобретении также раскрывается соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
Предпочтительно, если соединение представляет собой соединение формулы (Ia):

(Ia).
Предпочтительно, если соединение представляет собой соединение формулы (Ib):

(Ib).
Предпочтительно, если соединение представляет собой соединение формулы (Ic):

(Ic).
Предпочтительно, если соединение представляет собой соединение формулы (Id):

(Id).
Предпочтительно, если соединение представляет собой соединение формулы (Ie):

(Ie).
Предпочтительно, если соединение представляет собой соединение формулы (If):

(If).
Предпочтительно, если соединение представляет собой соединение формулы (Ig):

(Ig).
Предпочтительно, если соединение представляет собой соединение формулы (Ih):

(Ih).
Предпочтительно, если соединение представляет собой соединение формулы (Ii):

(Ii).
Предпочтительно, если A---B обозначает CH=CH.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
Соединение предпочтительно выбирать из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
Предпочтительно, если соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и  .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
Соединение предпочтительно представляет собой
 .
.
Предпочтительно, если соединение представляет собой
 .
.
В изобретении также раскрыта фармацевтическая композиция, включающая описанное в изобретении соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват и фармацевтически приемлемое вспомогательное вещество.
В изобретении также раскрыта фармацевтическая композиция, включающая описанное в изобретении соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват, или их смесь, и фармацевтически приемлемое вспомогательное вещество.
Раскрытые выше соединения или фармацевтические композиции предпочтительно применять в качестве лекарственного препарата.
Раскрытые выше соединения или фармацевтические композиции предпочтительно применять в терапии.
Также раскрывается описанное выше соединение, выделенное из прополиса, где источником прополиса являются растения рода Myoporum. Предпочтительно, чтобы источником прополиса являлось растение Myoporum insulare.
Также раскрывается описанное выше соединение, выделенное из смолы, камеди или экссудата растения рода Myoporum. Предпочтительно, чтобы соединение выделяли из смолы, камеди или экссудата растения Myoporum insulare.
Также раскрывается способ лечения заболевания или нарушения, где способ включает введение терапевтически эффективного количества описанных в изобретении соединения или композиции.
Также раскрывается применение описанного в изобретении соединения при приготовлении лекарственного препарата для лечения заболевания или нарушения.
Также в изобретении раскрывается применение описанных в изобретении соединения или композиции при лечении заболевания или нарушения.
Также в изобретении раскрывается описанные в изобретении соединение или композиция для применения при лечении заболевания или нарушения.
Предпочтительно, чтобы заболевание или нарушение выбирали из группы, состоящей из острого коронарного синдрома, связанного с возрастом заболевания или нарушения, аллергического заболевания или связанного с ним состояния, болезни Альцгеймера, атеросклероза, аутоиммунного заболевания, бактериальной инфекции, рака, деменции, депрессивного синдрома или связанного с ним состояния, диабета, дислипидемии, гиперлипидемии, гипертензии, ихтиоза, иммунопатологического заболевания, метаболического заболевания или нарушения, неврологического заболевания или нарушения, ожирения, болезни Паркинсона, боли, ревматоидного артрита и кожного заболевания или нарушения.
Заболевание или нарушение предпочтительно представляет собой рак.
Предпочтительно, чтобы рак представлял собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
Предпочтительно, чтобы рак центральной нервной системы представлял собой глиому. Предпочтительно, чтобы рак центральной нервной системы представлял собой медуллобластому. Предпочтительно, чтобы рак центральной нервной системы представлял собой нейробластому.
Предпочтительно, чтобы рак легких представлял собой немелкоклеточный рак легких. Предпочтительно, чтобы рак легких представлял собой мелкоклеточный рак легких.
Предпочтительно, чтобы карцинома представляла собой аденосквамозную карциному или сквамозную карциному.
Предпочтительно, чтобы саркома представляла собой липосаркому, рабдомиосаркому или фибросаркому. Предпочтительно, чтобы саркома представляла собой саркому мягких тканей. Предпочтительно, чтобы саркома мягких тканей представляла собой остеосаркому мягких тканей.
Предпочтительно, чтобы лимфома представляла собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
Кожное заболевание или нарушение предпочтительно выбирают из группы, состоящей из экземы, псориаза, акне, рубца, воспаления, ожога, солнечного ожога, повреждения кожи и раздражения кожи.
Типичные соединения оценивали на их фармакологическую активность, и было обнаружено, что они могут применяться при модулировании ряда заболеваний или нарушений. Например, было обнаружено, что соединения ингибируют пролиферацию раковых клеток и демонстрируют ингибирование, с активностью в диапазоне от умеренной до высокой, различных мишеней, связанных с раковой патологией. Дополнительное обсуждение активности соединения представлено ниже в примерах.
Примеры вариантов осуществления
1. Способ лечения рака, где способ включает введение терапевтически эффективного количества соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата, или фармацевтической композиции, включающей указанные соединения, субъекту, нуждающемуся в этом,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
2. Применение соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при приготовлении лекарственного препарата для лечения рака.
3. Применение соединения формулы (I),

(I)
его геометрического изомера, стереоизомера, фармацевтически приемлемой соли или сольвата,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
при лечении рака.
4. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
5. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
6. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
7. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
8. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
9. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
10. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ia):

(Ia).
11. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ib):

(Ib).
12. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ic):

(Ic).
13. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Id):

(Id).
14. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ie):

(Ie).
15. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (If):

(If).
16. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ig):

(Ig).
17. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ih):

(Ih).
18. Способ согласно примеру варианта осуществления 1 или применение согласно примеру варианта осуществления 2 или примеру варианта осуществления 3, где соединение представляет собой соединение формулы (Ii):

(Ii).
19. Способ или применение согласно любому одному из примеров вариантов осуществления 1-16, где A---B обозначает CH=C.
20. Способ согласно любому одному из примеров вариантов осуществления 1-19 или применение согласно любому одному из примеров вариантов осуществления 2-19, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
21. Способ или применение согласно примеру варианта осуществления 20, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
22. Способ или применение согласно примеру варианта осуществления 21, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
23. Способ или применение согласно примеру варианта осуществления 22, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
, и
и  .
.
24. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
25. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
26. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
27. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
28. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
29. Способ или применение согласно примеру варианта осуществления 23, где соединение представляет собой
 .
.
30. Способ согласно любому одному из примеров вариантов осуществления 1-29 или применение согласно любому одному из примеров вариантов осуществления 2-29, где рак представляет собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
31. Способ или применение согласно примеру варианта осуществления 30, где рак центральной нервной системы представляет собой глиому.
32. Способ или применение согласно примеру варианта осуществления 30, где рак центральной нервной системы представляет собой медуллобластому.
33. Способ или применение согласно примеру варианта осуществления 30, где рак центральной нервной системы представляет собой нейробластому.
34. Способ или применение согласно примеру варианта осуществления 30, рак легких представляет собой немелкоклеточный рак легких.
35. Способ или применение согласно примеру варианта осуществления 30, где рак легких представляет собой мелкоклеточный рак легких.
36. Способ или применение согласно примеру варианта осуществления 30, где карцинома представляет собой аденосквамозную карциному или сквамозную карциному.
37. Способ или применение согласно примеру варианта осуществления 30, где саркома представляет собой липосаркому, рабдомиосаркому или фибросаркому.
38. Способ или применение согласно примеру варианта осуществления 30, где саркома представляет собой саркому мягких тканей.
39. Способ или применение согласно примеру варианта осуществления 38, где саркома мягких тканей представляет собой остеосаркому мягких тканей.
40. Способ согласно примеру варианта осуществления 30, где лимфома представляет собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
41. Соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH.
42. Соединение формулы (I),

(I)
его геометрический изомер, стереоизомер, фармацевтически приемлемая соль или сольват,
где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил, OC(O)C4-5алкадиенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC4-5алкадиенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или OC(O)C4-5алкадиенил; и
A---B обозначает CH=C или CH2-CH,
для применения при лечении рака.
43. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph, OC(O)C2-5алкенил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC2-5алкенил, OC(O)C1-5алкил, OC(O)Ph или OC(O)C2-5алкенил; и
A---B обозначает CH=C или CH2-CH.
44. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил, OC(O)Ph или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph; и
A---B обозначает CH=C или CH2-CH.
45. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой CH2, CHOH или C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
где X представляет собой CH2, CHOH или C(O), R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
46. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой CH2;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
47. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой CHOH;
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
48. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где
X представляет собой C(O);
R1 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R2 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
R3 независимо представляет собой H, OH, OC1-5алкил, OC(O)C1-5алкил или =O;
и не более чем один из R1, R2 и R3 может представлять собой H;
R4 представляет собой H, OH, OC1-5алкил, OCH2Ph, OC(O)C1-5алкил или OC(O)Ph;
или X и R3 образуют шестичленное эфирное кольцо или лактоновое кольцо, или шестичленное кольцо, содержащее углеродный атом в полуацетальной форме или углеродный атом в ацетальной форме, где R4 представляет собой соответственно OH или OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
49. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ia):

(Ia).
50. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ib):

(Ib).
51. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ic):

(Ic).
52. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Id):

(Id).
53. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ie):

(Ie).
54. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (If):

(If).
55. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ig):

(Ig).
56. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ih):

(Ih).
57. Соединение согласно примеру варианта осуществления 41 или примеру варианта осуществления 42, где соединение представляет собой соединение формулы (Ii):

(Ii).
58. Соединение согласно любому одному из примеров вариантов осуществления 41-57, где A---B обозначает CH=C.
59. Соединение согласно любому одному из примеров вариантов осуществления 41-58, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
60. Соединение согласно примеру варианта осуществления 59, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 и
и  .
.
61. Соединение согласно примеру варианта осуществления 60, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 и
и  .
.
62. Соединение согласно примеру варианта осуществления 61, где соединение выбирают из группы, состоящей из
 ,
,  ,
,  ,
,
 ,
,  и
и  .
.
63. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
64. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
65. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
66. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
67. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
68. Соединение согласно примеру варианта осуществления 62, где соединение представляет собой
 .
.
69. Соединение согласно любому одному из примеров вариантов осуществления 42-68, где рак представляет собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
70. Соединение согласно примеру варианта осуществления 69, где рак центральной нервной системы представляет собой глиому.
71. Соединение согласно примеру варианта осуществления 69, где рак центральной нервной системы представляет собой медуллобластому.
72. Соединение или применение согласно примеру варианта осуществления 69, где рак центральной нервной системы представляет собой нейробластому.
73. Соединение согласно примеру варианта осуществления 69, где рак легких представляет собой немелкоклеточный рак легких.
74. Соединение согласно примеру варианта осуществления 69, где рак легких представляет собой мелкоклеточный рак легких.
75. Соединение согласно примеру варианта осуществления 69, где карцинома представляет собой аденосквамозную карциному или сквамозную карциному.
76. Соединение согласно примеру варианта осуществления 69, где саркома представляет собой липосаркому, рабдомиосаркому или фибросаркому.
77. Соединение согласно примеру варианта осуществления 69, где саркома представляет собой саркому мягких тканей.
78. Соединение согласно примеру варианта осуществления 77, где саркома мягких тканей представляет собой остеосаркому мягких тканей.
79. Соединение согласно примеру варианта осуществления 69, где лимфома представляет собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
80. Фармацевтическая композиция, включающая соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68 и фармацевтически приемлемое вспомогательное вещество.
81. Фармацевтическая композиция, включающая соединение, его геометрический изомер, стереоизомер, фармацевтически приемлемую соль или сольват согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68, или их смесь, и фармацевтически приемлемое вспомогательное вещество.
82. Соединение согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68, или фармацевтическая композиция согласно примеру варианта осуществления 80 или примеру варианта осуществления 81 для применения в качестве лекарственного препарата.
83. Соединение согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68 или фармацевтическая композиция согласно примеру варианта осуществления 80 или примеру варианта осуществления 81 для применения в терапии.
84. Соединение, определяемое в любом одном из примеров вариантов осуществления 42-68, выделенное из прополиса, где прополис образуется из растений рода Myoporum.
85. Соединение согласно примеру варианта осуществления 84, где прополис образуется из растения Myoporum insulare.
86. Соединение, определяемое в примере варианта осуществления 41 или в любом одном из примеров вариантов осуществления 43-68, выделенное из смолы, камеди или экссудата растения рода Myoporum.
87. Соединение согласно примеру варианта осуществления 86, выделенное из смолы, камеди или экссудата растения Myoporum insulare.
88. Способ лечения заболевания или нарушения, где способ включает введение терапевтически эффективного количества соединения согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43 и 68 или композиции согласно примеру варианта осуществления 80 или примеру варианта осуществления 81.
89. Применение соединения согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68 при приготовлении лекарственного препарата для лечения заболевания или нарушения.
90. Применение соединения согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68 или композиции согласно примеру варианта осуществления 80 или примеру варианта осуществления 81 при лечении заболевания или нарушения.
91. Соединение согласно примеру варианта осуществления 41 или любому одному из примеров вариантов осуществления 43-68 или композиция согласно примеру варианта осуществления 80 или примеру варианта осуществления 81 для применения при лечении заболевания или нарушения.
92. Способ согласно примеру варианта осуществления 88 или применение согласно примеру варианта осуществления 89 или примеру варианта осуществления 90 или соединение согласно примеру варианта осуществления 91, где заболевание или нарушение выбирают из группы, состоящей из острого коронарного синдрома, связанного с возрастом заболевания или нарушения, аллергического заболевания или связанного с ним состояния, болезни Альцгеймера, атеросклероза, аутоиммунного заболевания, бактериальной инфекции, рака, деменции, депрессивного синдрома или связанного с ним состояния, диабета, дислипидемии, гиперлипидемии, гипертензии, ихтиоза, иммунопатологического заболевания, метаболического заболевания или нарушения, неврологического заболевания или нарушения, ожирения, болезни Паркинсона, боли, ревматоидного артрита и кожного заболевания или нарушения.
93. Способ или применение, или соединение согласно примеру варианта осуществления 92, где заболевание или нарушение представляет собой рак.
94. Способ или применение, или соединение согласно примеру варианта осуществления 93, где рак представляет собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
95. Способ или применение, или соединение согласно примеру варианта осуществления 94, где рак центральной нервной системы представляет собой глиому.
96. Способ или применение, или соединение согласно примеру варианта осуществления 94, где рак центральной нервной системы представляет собой медуллобластому.
97. Способ или применение, или соединение согласно примеру варианта осуществления 94, где рак центральной нервной системы нейробластому.
98. Способ или применение, или соединение согласно примеру варианта осуществления 94, где рак легких представляет собой немелкоклеточный рак легких.
99. Способ или применение, или соединение согласно примеру варианта осуществления 94, где рак легких представляет собой мелкоклеточный рак легких.
100. Способ или применение, или соединение согласно примеру варианта осуществления 94, где карцинома представляет собой аденосквамозную карциному или сквамозную карциному.
101. Способ или применение, или соединение согласно примеру варианта осуществления 94, где саркома представляет собой липосаркому, рабдомиосаркому или фибросаркому.
102. Способ или применение, или соединение согласно примеру варианта осуществления 94, где саркома представляет собой саркому мягких тканей.
103. Способ или применение, или соединение согласно примеру варианта осуществления 102, где саркома мягких тканей представляет собой остеосаркому мягких тканей.
104. Способ или применение, или соединение согласно примеру варианта осуществления 94, где лимфома представляет собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
105. Способ или применение, или соединение согласно примеру варианта осуществления 92, где кожное заболевание или нарушение выбирают из группы, состоящей из экземы, псориаза, акне, рубца, воспаления, ожога, солнечного ожога, повреждения кожи и раздражения кожи.
Примеры
Для лучшего понимания предмета изобретения, далее будет приведено описания ряда примеров.
Экспериментальная часть
Материалы
Медоносных пчел, замеченных за сбором прополиса с деревьев и кустарников boobialla (Myoporum insulare), отлавливали и помещали в пластиковые пробирки, закрывали их крышками и замораживали. Отсекали и объединяли фрагменты задних лапок пчел с захваченным на них прополисом. Собирали образцы растений и высушивали их при 40°C в вентилируемом сушильном шкафу (Thermoline, NSW Australia) в течение нескольких дней, для того чтобы предоставить контрольные образцы с целью их идентификации специалисту в области ботаники доценту Марри Хенвуд (Murray Henwood), работающей с коллекцией гербария John Ray Herbarium в Сиднейском университете (University of Sydney, Sydney, Australia), и регистрировали их как подлинные образцы растения Myoporum insulare под номером Duke-131202-01. До анализа или дальнейшей обработки, извлеченную из образцов растений смолу хранили при -20°С.
Прополис был получен на местах для пасеки с присутствием от 1 до 10 колоний европейской медоносной пчелы (Apis mellifera ligustica) в стандартных 10-рамочных ящичных ульях, в каждом из которых устанавливали прополисный холстик под крышкой улья. Образцы прополиса собирали и предоставляли несколько пчеловодов из восьми мест для пасеки, расположенных в разных частях острова Кенгуру в Южной Австралии (Kangaroo Island, South Australia). Эти места находились в непосредственной близости от Hanson Bay, Vivonne Bay, Flour Cask Bay, Island Beach, Kingscote, Brownlow, Rainy Creek и Eleanor River. Известно, что эти места являются местом обитания растения Myoporum insulare на острове Кенгуру. В результате было получено 23 образца прополиса, которые, согласно данным анализа методами ТСХ и 1Н ЯМР, содержали, по меньшей мере, 90% прополиса из растения Myoporum insulare. До последующего анализа и обработки образцов прополиса, их хранили при -20°С.
Пластины для тонкослойной хроматографии с предварительно нанесенным слоем силикагеля 60 F254 и силикагеля 60H для использования при хроматографии при пониженном давлении в короткой колонке с нормальной фазой (NPSCVC) приобретали у фирмы Merck. Пластины для тонкослойной хроматографии (ТСХ) визуализировали с помощью излучения лампы Minerallight UVGL-58, Multiband УФ-2544/366.
Все химические реагенты, использовавшиеся для выделения и синтеза, включая дейтерированные растворители для ЯМР, такие как d-хлороформ, d4-метанол и d6-диметилсульфоксид, приобретали у фирмы Novachem Pty Ltd (Collingwood, Vic, Australia). Растворители, включающие гексан, дихлорметан, этилацетат, изопропанол, этанол, метанол и уксусную кислоту, были аналитической степени чистоты и приобретались у фирмы Chem Supply, Gillman, SA, Australia.
Общие методы
Для испарения фракции растворителя использовали роторный испаритель Rotavapor model R-114 с температурой воды в водяной бане в диапазоне 40-60˚C. Использовали вакуумный насос V-700 или диафрагменный насос Vacuubrand MD 4C NT (Vacuubrand GMBH, Wertheim, Germany) с регулятором вакуума V-800 или V-850. Окончательную сушку проводили в сушильном шкафу Napco 5831 (NAPCO, Salt Lake City, USA), используя вакуумный насос DirectTorr (Sargent-Welch, Buffalo, USA).
Изократную аналитическую высокоэффективную жидкостную хроматографию (ВЭЖХ) проводили на системе Shimadzu UFLC, насос LC-20AD, автодозатор SIL-20A HT, на колонке Hewlett-Packard, NUCLEOSIL 100 C18, 5 мкм, 4 мм × 125 мм, объем вводимой пробы 20 мкл, элюировали при расходе 1 мл/мин и детектировали при длине волны 230 нм с помощью детектора в ультрафиолетовой и видимой области (Shimadzu SPD-20A). Колонку элюировали смесью метанол-вода-уксусная кислота (65:34,8:0,2).
Градиентную аналитическую HPLC проводили на системе Shimadzu Nexera X2 LC-30AD, автодозатор SIL-30, на колонке Hewlett-Packard, NUCLEOSIL 100 C18, 5 мкм, 4 мм × 125 мм, объем вводимой пробы 10 мкл, элюировали при расходе 1 мл/мин и детектировали при длине волны 320 нм с помощью детектора на диодной матрице SPD-M30A в ультрафиолетовой и видимой области. Колонку элюировали с помощью градиентной системы, приготовленной из метанола (фаза A) и смеси метанол:вода:уксусная кислота (40:59,8:0,2) (фаза B). Градиент растворителей применяли следующим образом: 0-2 минуты: 32-50% A, 2-9 минут: 50-90% A, 9-12 минут: 90-100% A, 12-14 минут: 100% A, и наконец 14-15 мин: 100-32% A, поддерживаемый в течение 5 минут.
Анализы методом 1H и 13C ядерного магнитного резонанса (ЯМР) проводили на системе Varian 400 МГц с автодозатором SMS (Palo Alto, California, USA). Химические сдвиги (δ) пиков в спектрах ЯМР регистрировали в частях на миллион (ppm) относительно тетраметилсилана (Si(CH3)4, TMS). Данные 1H ЯМР приводятся в виде химического сдвига (δ), относительного интеграла, мультиплетности (условные сокращенные обозначения: с=синглет, д=дуплет, т=триплет, тд=триплет дуплетов, кв=квартет, дд=дуплет дуплетов, ддд=дуплет дуплета дуплетов, уш.с=уширенный синглет, уш.т=уширенный триплет), константы взаимодействия (J в Гц) и отнесения. Данные 13C ЯМР приводятся в виде химического сдвига (δ) и отнесения.
В случае использования масс-спектрометрии низкого разрешения с ионизацией электрораспылением (ESI-MS), образцы анализировали с помощью системы тандемной масс-спектроскопии (MS/MS) с ионной ловушкой Finnigan Polaris (Finnigan Corporation, San Jose, USA), используя систему обработки данных Xcalibur 1,2, в режимах ионизации электрораспылением (ESI) отрицательных и положительных ионов, используя метод инфузии.
Данные масс-спектрометрии высокого разрешения с ионизацией электрораспылением (ESI-MS) регистрировали на масс-спектрометре Bruker Daltonics Apex Ultra Fourier Transform Ion Cyclotron Resonance 7 Tesla в подразделении масс-спектрометрии химического факультета Сиднейского университета (School of Chemistry, The University of Sydney).
Определение химических характеристик образцов растений и прополиса методом 1H-ЯМР
Поросль молодых листьев (25 г), заднюю ножку пчел (0,01 г) и прополис из улья (1,0 г) подвергали экстракции дихлорметаном при комнатной температуре в течение 15 минут. Экстракты фильтровали, сушили при пониженном давлении и анализировали методом 1H-ЯМР и ВЭЖХ. Было обнаружено, что образцы содержат серрулатановые дитерпены. Затем отбирали образцы прополиса и растений для выделения из них компонентов.
Получение экстракта смолы растения Myoporum insulare
Собирали свежие молодые листья и верхушки молодых побегов с нескольких деревьев Myoporum insulare. До обработки в течение 5 дней, листья хранили в пластиковых пакетах на льду. Для извлечения наружной смолы/экссудата, листья и верхушки побегов (4 кг) смешивали с дихлорметаном (4 литра) и, после отстаивания в течение 1 часа, дихлорметановый экстракт фильтровали, и дихлорметан удаляли из фильтрата испарением при пониженном давлении, используя роторный испаритель, с получением коричневой частично отвердевшей высушенной смолы (12,5 г, выход 0,31%).
Выделение и идентификация серрулатановых дитерпенов из прополиса растения Myoporum insulare с острова Кенгуру.
Общий метод
Прополис (100 г) подвергали экстракции дихлорметаном при комнатной температуре при перемешивании в течение 1 часа. Экстракт очищали хроматографией при пониженном давлении в короткой колонке с нормальной фазой (NPSCVC). Для элюирования компонентов, которые анализировали методом ТСХ и ЯМР, использовали ступенчатый градиент подвижной фазы (2×100 мл), состоящий из дихлорметана (DCM) и этилацетата (EtOAc) при 0, 1, 2, 4, 8, 10, 15, 20, 50 и 100%. При необходимости, проводили дополнительную очистку соединений тем же самым методом NPSCVC с различными подвижными фазами, состоящими или из гексана и EtOAc, или из гексана и изопропанола. Структуры и идентификацию этих чистых соединений охарактеризовывали методами 1H- и 13C-ЯМР и масс-спектрометрии, включая масс-спектрометрию высокого разрешения. При необходимости, проводили более подробные структурные анализы выделенного соединения методом 2D-ЯМР, используя градиентную гетероядерную когерентность множественных связей (GHMBC). Было обнаружено, что основным серрулатановым дитерпеноидом является 7,8,18-тригидроксисеррулат-14-ен (1).
Выделенные серрулатановые дитерпены из растения Myoporum insulare.
7,8,18-тригидроксисеррулат-14-ен (1)

Желтоватая жидкость, выход 50 мг, [α]D20 -27,3° (C=1,0, CHCl3). УФ (CH3OH) λmax нм (log ε) 279 (3,37) и 320 (2,49). ИК (ν): 3381, 2924, 2864, 1625, 1581, 1448 см-1. HRESIMS: 341,2089 m/z [M+Na]+ (рассчитано 341,2087) C20H30O3. 1H ЯМР (400 МГц, CDCl3) δ: 6,56, (1H, с, H-5), 5,04 (1H, уш.т, J= 7,0 Гц, H-14), 3,63 (2H, д, J= 6,2 Гц, H-18), 3,07 (1H, пентет д, J= 6,8, 1,6 Гц, H-1), δ 2,76 (1H, тд, J= 5,6, 2,6 Гц, H-4), 2,20 (3H, с, H-19), 1,99 (1H, м, H-13A), 1,90 (1H, м, H-13B), 1,90 (1H, м, H-3A), 1,86 (1H, м, H-2A), 1,83 (1H, м, H-11), 1,68 (3H, с, H-16), 1,66 (1H, м, H-2B), 1,58 (3H, с, H-17), 1,51 (1H, м, H-3B), 1,25 (1H, м, H-12A), 1,36 (2H, м, H-12B), 1,21 (3H, д, J= 7,0 Гц, H-20). 13C ЯМР (100 МГц, CDCl3) δ: 15,54 (C-19), 17,68 (C-17), 20,51 (C-2), 21,11 (C-20), 25,70 (C-16), 26,16 (C-13), 26,47 (C-3), 26,98 (C-1), 29,85 (C-12), 37,91 (C-4), 45,45 (C-11), 64,38 (C-18), 121,31 (C-6), 122,00 (C-5), 124,43 (C-14), 127,18 (C-9), 130,70 (C-10), 131,75 (C-15), 139,74 (C-7), 141,61 (C-8).
5,18-эпоксисеррулат-14-ен-8,18-диол (2)

Красная жидкость, выход 84 мг, [α]D20 -21,5° (C=1,0, CHCl3). УФ (CH3OH) λmax нм (log ε) 293 (3,36) и 334 (2,91). ИК (ν): 3327, 2970, 2926, 2860, 1647, 1558, 1448, 1043см-1. HRESIMS: 315,1970 m/z [M-H]- (рассчитано 315,1966).C20H28O3. 1H ЯМР (400 МГц, CDCl3) δ 6,48 (1H, с, H-7), 5,59 (1H, уш.с, H-18), 5,14 (1H, уш.т, J= 7,0 Гц, H-14), 3,11 (1H, секстет, J= 7,6, H-1), 2,54 (1H, тд, J= 11,4, 3,6 Гц, H-4), 2,25 (1H, м, H-2A), 2,20 (1H, м, H-13A), 2,13 (3H, с, H-19), 2,09 (1H, м, H-13B), 2,08 (1H, м, H-3A), 1,69 (1H, м, H-12A), 1,70 (3H, с, H-16), 1,63 (3H, с, H-17), 1,52 (1H, м, H-11), 1,41 (1H, м, H-2B), 1,28 (3H, д, J= 6,9 Гц, H-20), 1,27 (1H, м, H-12B), 1,05 (1H, м, H-3B). 13C ЯМР (100 МГц, CDCl3) δ 15,88 (C-19), 17,75 (C-17), 22,89 (C-20), 25,36 (C-13), 25,70 (C-16), 26,62 (C-3), 27,79 (C-1), 28,90 (C-12), 31,75 (C-2), 31,99 (C-4), 40,48 (C-11), 91,88 (C-18), 115,94 (C-7), 122,94 (C-6), 124,09 (C-14), 124,29 (C-10), 125,21 (C-9), 131,99 (C-15), 141,71 (C-5), 146,85 (C-8).
5,18-эпокси-8-гидроксисеррулат-14-ен (3)
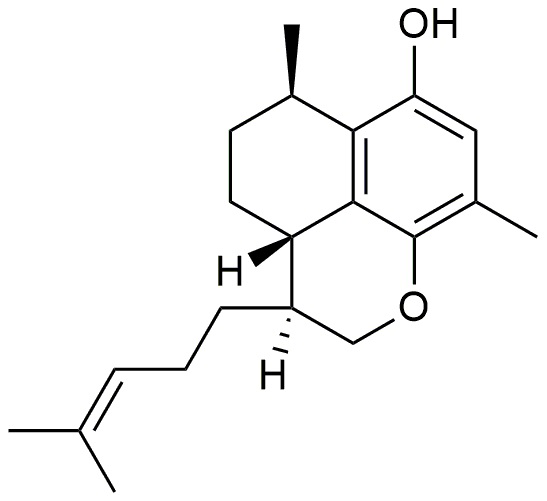
Жидкость с блестящим желтым цветом, выход 87 мг, [α]D20 -8,9° (C=1,0, CHCl3). УФ (CH3OH) λmax нм (log ε) 296 (3,55) и 334 (2,66). ИК (ν): 3502, 2922, 2856, 1622, 1597, 1421, 1230 см-1. HRESIMS: 301,21635 m/z [M+H]+ (рассчитано 301,21621) C20H28O2. 1H ЯМР (400 МГц, CDCl3) δ: 6,46 (1H, с, H-7), 5,13 (1H, уш.т, J= 6,9 Гц, H-14), 4,35 (1H, дд, J= 10,5, 3,7 Гц, H-18A), 3,70 (1H, т, J= 10,8 Гц, H-18B), 3,13 (1H, секстет, J= 7,4 Гц, H-1), 2,31 (1H, м, H-4), 2,24 (1H, м, H-2A), 2,16(1H, м, H-13A), 2,15 (1H, м, H-3A), 2,12 (3H, с, H-19), 2,02 (1H, м, H-13B), 1,74 (1H, м, H-12A), 1,70 (3H, с, H-16), 1,63 (3H, с, H-17), 1,55, (1H, м, H-11), 1,40 (1H, м, H-2B), 1,28 (3H, д, J= 7,0 Гц, H-20), 1,18 (1H, м, H-12B), 1,06 (1H, тд, J= 12,2, 4,4 Гц, H-3B). 13C ЯМР (100 МГц, CDCl3) δ: 15,82 (C-19), 17,73 (C-17), 23,12 (C-20), 25,44 (C-13), 25,70 (C-16), 26,97 (C-3), 27,61 (C-1), 29,97 (C-12), 31,47 (C-2), 37,17 (C-11), 39,00 (C-4), 69,52 (C-18), 115,79 (C-7), 122,64 (C-6), 124,12 (C-14), 124,26 (C-9), 125,70 (C-10), 131,99 (C-15), 145,27 (C-5), 146,16 (C-8).
7,8-дигидроксисеррулат-14-ен (4)

Желтоватая жидкость, выход 56 мг, [α]D20 -21,1° (C=1,0, CHCl3). УФ (CH3OH) λmax нм (log ε) 278 (3,36) и 329 (2,95). ИК (ν): 3396, 2954, 2924, 2868, 1635, 1577, 1456 см-1. HRESIMS: 325,21413 m/z [M+Na]+ (рассчитано 325,21380) C20H30O2. 1H ЯМР (400 МГц, CDCl3) δ 6,53 (1H, с, H-5), 5,00 (1H, уш.т, J= 7,0 Гц, H-14), 3,06 (1H, пентет д, J= 6,7, 2,8 Гц, H-1), 2,53 (1H, тд, J= 5,5, 3,4 Гц, H-4), 2,22 (3H, с, H-19), 2,00 (1H, м, H-13A), 1,95 (1H, м, H-2A), 1,84 (1H, м, H-11), 1,82 (1H, м, H-3A), 1,80 (1H, м, H-13B), 1,70 (1H, м, H-3B), 1,67 (3H, с, H-16), 1,59 (3H, с, H-17), 1,48 (1H, м, H-2B), 1,29 (1H, м, H-12A), 1,12 (3H, д, J= 6,8 Гц, H-20), 1,05 (1H, м, H-12B), 0,95 (3H, д, J=6,8,H-18). 13C ЯМР (100 МГц, CDCl3) δ: 15,53 (C-19), 17,62 (C-17), 18,66 (C-18), 19,63 (C-3), 21,10 (C-20), 25,71 (C-16), 26,25 (C-13), 27,1 (C-1), 27,43 (C-2), 33,35 (C-12), δ 37,8 (C-11), δ 41,88 (C-4), δ 120,50 (C-6), δ 122,46 (C-5), δ 124,96 (C-14), δ 127,09 (C-9), δ 131,10 (C-15), δ 131,90 (C-10), δ 139,19 (C-7), δ 140,93 (C-8).
Серрулат-14-ен-5,8-дион (5)
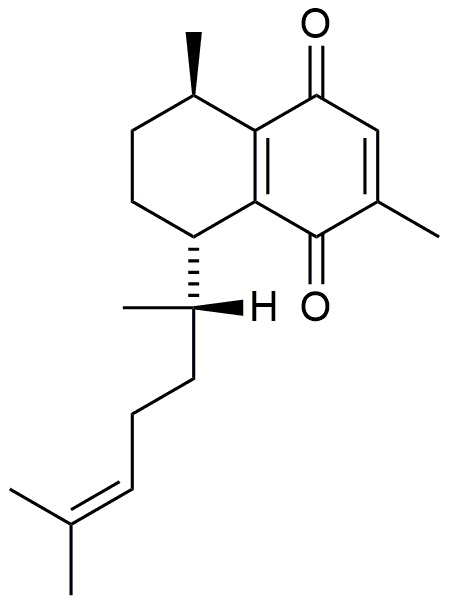
Светло-оранжевая жидкость, выход 30 мг. 1H ЯМР (400 МГц, CDCl3) δ 6,68 (1H, с, H-5), 5,02 (1H, уш.т, J= 7,1 Гц, H-14), 2,85 (1H, м, H-1), 2,20 (1H, м, H-4), 2,12 (1H, м, H-3A), 2,03 (1H, м, H-13A), 1,95 (3H, с, H-19), 1,88 (1H, м, H-11), 1,85 (1H, м, H-13B), 1,69 (1H, м, H-2A), 1,67 (3H, с, H-16), 1,58 (3H, с, H-17), 1,34 (1H, м, H-2B), 1,30 (1H, м, H-12A), 1,20 (1H, м, H-3B), 1,12 (1H, м, H-12B), 1,07 (6H, д, J= 6,9 Гц, H-18 и H-20). 13C ЯМР (100 МГц, CDCl3) δ 15,21 (C-19), 17,69 (C-17), 18,67 (C-20), 18,75 (C-18), 20,55 (C-3), 25,71 (C-16), 26,10 (C-13), 26,56 (C-1), 26,59 (C-2), 33,41 (C-12), 34,9 (C-11), 43,83 (C-4), 124,13 (C-14), 132,00 (C-15), 135,36 (C-6), 140,04 (C-7), 140,70 (C-9), 150,13 (C-10), 179,85 (C-5), 181,55 (C-8).
5,18-эпоксисеррулат-14-ен-7,8-дион (6)

Пурпурная жидкость, выход 50 мг, HRESIMS: 315,19573 m/z [M+H]+ (рассчитано 315,19547) C20H26O3. 1H ЯМР (400 МГц, CDCl3) δ 5,07 (1H, уш.т, J= 6,8 Гц, H-14), 4,49 (1H, дд, J= 11,0, 3,8 Гц, H-18A), 3,86 (1H, т, J= 11,1 Гц, H-18B), 2,82 (1H, м, H-1), 2,14 (1H, м, H-4), 2,15 (1H, м, H-2A), 2,13 (1H, м, H-3A), 2,09 (1H, м, H-13A), 1,97 (1H, м, H-13B), 1,81 (3H, с, H-19), 1,76 (1H, м, H-12A), 1,74 (1H, м, H-11), 1,71 (3H, с, H-16), 1,63 (3H, с, H-17), 1,23 (1H, м, H-2B), 1,19 (1H, м, H-12B), 1,13 (3H, д, H-20) 1,11 (1H, м, H-3B). 13C ЯМР (100 МГц, CDCl3) δ 7,57 (C-19), 17,78 (C-17), 21,67 (C-20), 24,66 (C-13), 25,32 (C-3), 25,71 (C-16), 28,74 (C-1), 29,15 (C-12), 30,77 (C-2), 37,07 (C-11), 40,09 (C-4), 71,85 (C-18), 114,44 (C-6), 123,06 (C-14), 132,87 (C-15), 139,43 (C-9), 149,67(C-10), 162,76 (C-5), 179,38 (C-7), 181,91 (C-8).
Было обнаружено, что соединение 6 образуется в результате окисления соединения 1.
Ацетилирование серрулатановых дитерпенов
7,8,18-триацетилоксисеррулат-14-ен (7)
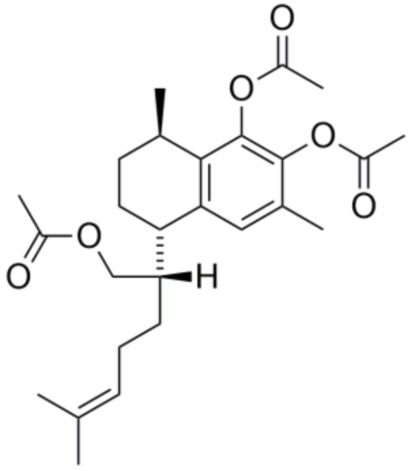
Серрулатан (1) (400 мг) растворяли в уксусном ангидриде (1 мл) и в осушенном пиридине (1 мл) и перемешивали при комнатной температуре в течение ночи (Davisetal.,1999). Реакционную смесь гасили дистиллированной водой (30 мл) и экстрагировали дихлорметаном (3×40 мл). Дихлорметановый раствор экстрагировали водным 0,1 M раствором хлористоводородной кислоты (30 мл) для удаления остаточных следов пиридина. Дихлорметановые растворы сушили над Na2SO4, фильтровали и концентрировали на роторном испарителе с получением желтого маслянистого остатка. И наконец, используя хроматографию при пониженном давлении в короткой колонке с нормальной фазой (NPSCVC) с дихлорметаном и этилацетатом (от 100:0 до 90:10 по объему), очищали и выделяли соединение (7) (434 мг, 77%) в виде бледно-желтого масла, выход 27 мг. HRESIMS: 467,2404 m/z [M+Na]+ (рассчитано 467,2206). C26H36O6.1H ЯМР (400 МГц, CDCl3) δ 6,92 (1H, с, H-5), 4,97 (1H, уш.т, J=7,1 Гц, H-14), 4,11 (2H, д, J= 6,3 Гц, H-18), 2,92 (1H, м, H-1), 2,88 (1H, м, H-4), 2,31 (3H, с, H-26), 2,29 (3H, с, H-24), 2,14 (3H, с, H-19), 2,12 (1H, м, H-11), 2,06 (3H, с, H-22), 1,99 (1H, м, H-13A), 1,87 (1H, м, H-13B), 1,87 (1H, м, H-3A), 1,87 (1H, м, H-2A), 1,68 (1H, м, H-3B), 1,66 (3H, с, H-16), 1,54 (3H, с, H-17), 1,50 (1H, м, H-2B), 1,33 (1H, м, H-12A), 1,23 (1H, м, H-12B), 1,15 (3H, д, J= 7,0 Гц, H-20). 13C ЯМР (100 МГц, CDCl3) δ 16,08 (C-19), 17,60 (C-17), 19,16 (C-3), 20,36 (C-24), 20,51 (C-26), 20,97 (C-22), 21,45 (C-20), 25,68 (C-16), 26,11 (C-13), 26,96 (C-2), 27,58 (C-1), 28,32 (C-12), 36,92 (C-4), 41,92 (C-11), 65,88 (C-18), 123,94 (C-14), 128,09 (C-5), 128,31 (C-6), 132,04 (C-15), 139,26 (C-7), 140,56 (C-8), 134,06 (C-9), 137,11 (C-10), 168,1 (C-23), 168,34 (C-25), 171,18 (C-21).
5,18-эпоксисеррулат-14-ен-8,18-диацетат (8)

Для ацетилирования соединения (2), 80 мг серрулатана (2) растворяли в уксусном ангидриде (1 мл) и в осушенном пиридине (1 мл) и перемешивали при комнатной температуре в течение ночи, и, с помощью того же самого метода обработки и используя хроматографию при пониженном давлении в короткой колонке с гексаном и этилацетатом (от 100:0 до 80:20 по объему), очищали и выделяли соединение (8) (57,8 мг, 58%). Жидкость красного цвета, выход 18 мг, HRESIMS: m/z 423,2143 [M+Na]+ рассчитано 423,2142. C24H32O5. 1H ЯМР (400 МГц, CDCl3) δ: 6,69 (1H, с, H-7), 6,53 (1H, д, J= 1,7 Гц, H-18), 5,08 (1H, уш.т, J= 6,5 Гц, H-14), 2,96 (1H, секстет, J= 7,4 Гц, H-1), 2,54 (1H, тд, J= 11,6, 3,8 Гц, H-4), 2,3 (3H, с, H-24), 2,19 (1H, м, H-13A), 2,19 (1H, м, H-2A), 2,14 (3H, с, H-19), 2,12 (1H, м, H-3A), 2,09 (3H, с, H-22), 2,02, (1H, м, H-13B), 1,70 (1H, м, H-12A), 1,69 (3H, с, H-16), 1,62 (3H, с, H-17), 1,65 (1H, м, H-11), 1,42 (1H, м, H-2B), 1,30 (1H, м, H-12B), 1,23 (3H, д, J= 6,8 Гц, H-12), 1,10 (1H, м, H-3B).13C ЯМР (100 МГц, CDCl3) δ: 15,88 (C-19), 17,68 (C-17), 21,09 (C-22), 21,23 (C-24), 22,78 (C-20), 25,15 (C-13), 25,70 (C-16), 26,22 (C-3), 28,26 (C-1), 28,29 (C-12), 31,41 (C-2), 32,3 (C-4), 38,93 (C-11), 90,18 (C-18), 41,92 (C-11), 122,53 (C-7), 123,48 (C-14), 123,77 (C-10), 123,96 (C-6), 130,9 (C-9), 132,57 (C-15), 142,44 (C-8), 145,63 (C-5), 170,05 (C-23), 170,19 (C-21).
Метилирование серрулатановых дитерпенов
8-метокси-7,18-дигидроксисеррулат-14-ен (11) и 7-метокси-8,18-дигидроксисеррулат-14-ен (12)

Соединение 1 (140 мг) обрабатывали диазометаном (избытком относительно эквивалентного количества) в диэтиловом эфире при температуре от 0°C до комнатной температуры в течение ночи с получением неидентифицированной смеси 4: 1 (1H-ЯМР монометилированных продуктов 11 и 12 (35 мг, 88% чистота, определенная методом ВЭЖХ).
Соединения 11 и 12
Желтое масло. Масс-спектр (в режиме положительных ионов) m/z=333,2 (12%, (M+H)+), 315,2 (100%, (M+H-H2O)+), 205,2 (18%, (M+H-C8H16O)+). Анализ методом ВЭЖХ: длина волны 210 нм, диапазон частот 4; колонка SorbTech C18AQ, 2,1×50 мм, 3 мкм; время удерживания 7,474 мин; подвижная фаза ацетонитрил/муравьиная кислота/вода; градиентный метод 5-95% CAN+0,1% муравьиной кислоты в воде+0,1% муравьиная кислота через 14 минут, выдержка при 95% CAN+муравьиная кислота в течение 4 мин. УФmax, 275 нм и 210 нм, плечо при 225 нм. Анализ методом 1H-ЯМР указывал на неидентифицированную смесь 4:1 соединений 11 и 12 (взаимозаменяемые мажорный и минорный изомеры). 1H ЯМР (400 МГц, CDCl3) δ: 6,74 (1H, с, H-5)[минорный], 6,56, (1H, с, H-5)[мажорный], 5,78 (1H, OH)[мажорный], 5,57 (1H, OH)[минорный], 5,01 (1H, уш.т, J= 6,3 Гц, H-14), 3,78 (3H, с, CH3O)[минорный], 3,77 (3H, с, CH3O)[мажорный], 3,63 (2H, м, H-18), 3,14 (1H, м, H-1)[мажорный], 3,07 (1H, м, H-1)[минорный], δ 2,81 (1H, м, H-4), 2,25 (3H, с, H-19)[мажорный], 2,21 (3H, с, H-19)[минорный], 2,0-1,8 (5H, м, H-13, H-3A, H-2A, H-11), 1,7-1,6 (1H, м, H-2B), 1,66 (3H, уш.с, H-16), 1,55 (3H, уш.с, H-17), 1,52-1,46 (1H, м, H-3B), 1,35-1,23 (2H, м, H-12), 1,21 (3H, д, J= 6,8 Гц, H-20)[мажорный] 1,20 (3H, д, J= 6,8 Гц, H-20)[минорный]. 13C ЯМР (100 МГц, CDCl3) δ: 15,50 (C-19)[минорный], 15,77 (C-19)[мажорный], 17,62 (C-17), 20,22 (C-2)[мажорный], 20,44 (C-2)[минорный], 21,08 (C-20)[мажорный], 22,22 (C-20)[минорный], 25,66 (C-16), 26,27 (C-13), 26,81 (C-3), 27,14 (C-1)[мажорный], 27,87 (C-1)[минорный], 29,14 (C-12)[минорный], 29,26 (C-12)[мажорный], 37,53 (C-4)[минорный], 37,55 (C-4)[мажорный], 45,43 (C-11)[минорный], 45,53 (C-11)[мажорный], 60,64 (OCH3)[мажорный], 60,89 (OCH3)[минорный], 64,17 (C-18)[мажорный], 64,30 (C-18)[минорный], 121,89 (C-5), 124,55 (C-14), 126,39, 126,70, 127,69, 130,42, 131,63, 131,66, 133,17, 135,11, 143,15, 144,85, 145,26, 146,27.
На фигуре 1 и фигуре 2 приведены спектры 1H ЯМР (400 МГц, CDCl3) и 13C ЯМР (100 МГц, CDCl3) 4:1 смеси соединений 11 и 12.
Оценка биологической активности серрулатановых терпеновых соединений
Биологическую активность in vitro серрулатановых дитерпенов 1-3 оценивали путем проведения исследований эпигенетики (таблица 3 -12). В таблице 3 приведены условия эксперимента, использовавшиеся при исследованиях эпигенетического связывания. В таблице 4 представлены результаты ингибирующего действия соединений 1-3 на связывание эпигенетически взаимодействующих белковых модулей. В таблицах 5-8 приведены типичные данные по ингибированию для соединения 1 на примере связывания эпигенетических мишеней (таблица 5: ASH1L (h) бромодомен; таблица 6: CECR2(h) бромодомен; таблица 7: SP140 (h) бромодомен; таблица 8: UHRF1(108-286) (h)). Соответствующие кривые связывания для данных, представленных в таблицах 5-8, приведены на фигурах 3-6. В таблице 9 представлены значения IC50, полученные из кривых зависимости ингибирования от концентрации для соединений 1 и 2 для связывания эпигенетически взаимодействующих белковых модулей при сравнении с референсными соединениями.-. В таблице 10 приведены данные по ингибированию соединениями 1-3 при концентрации 10 мкМ эпигенетических ферментов при сравнении с референсными соединениями. -
В таблице 11 приведены значения IC50, полученные из кривых зависимости ингибирования от концентрации для соединений 1, 2 и 4, при ингибировании эпигенетических ферментов при сравнении с референсными соединениями. В таблице 12 представлены данные по фармакологической активности соединений 1-3. Дитерпены оценивали также на их in vitro фармакологическую активность (таблицы 13-16). В таблице 13 приведены методы фармакологического исследования. В таблице 14 представлены данные по фармакологической активности соединений 1-3 при концентрации 10 мкМ. В таблице 15 представлены данные по активности соединения 1 и референсных соединений IC50 (мкM) в отношении 5-липоксигеназы, липидной пероксидазы и моноаминоксидазы (MAO-A). В таблице 16 приведены данные по воздействию соединений 1-4 на усваивание 2-деокси-D-глюкозы в мышечных клетках.
В таблице 17 приведены дозозависимый эффект и величины IC50 при исследовании фармакологической активности типичных серрулатановых дитерпенов.
Исследовали воздействие дитерпенов 1-4 и смолы растения Myoporum insulare на жизнеспособность клеток (таблица 18).
Исследовали воздействие дитерпенов 1, 2, 4 и смолы растения Myoporum insulare на пролиферацию раковых клеток с использованием OncoPanel (таблица 19 - таблица 29). В таблице 21 приведены результаты исследования пролиферации клеток с использованием Oncopanel для соединений 11 и 12.
Эпигенетические исследования
Исследования эпигенетического связывания проводились компанией Eurofins CEREP (France). Условия проведения исследований, включающие такие параметры, как ферменты, источник ферментов, субстрат, концентрация субстрата, лиганд, концентрация лиганда, метка, инкубация, метод детектирования и референсное соединение и концентрация, подробно приведены в таблице 3. Кроме того, также приведены соответствующие литературные ссылки. Метод детектирования AlphaScreen относится к гомогенному анализу люминесценции, усиленной за счет эффекта близости, который используется для исследования биомолекулярных воздействий (смотрите публикацию Ullman et al. 1994). Методы анализа LANCE и LanthaScreen основаны на принципе переноса энергии флуоресценции с разрешением во времени (TR-FRET) и описаны, например, в публикации Ma et al. 2008.
Величины IC50 (концентрация, вызывающая полумаксимальное ингибирование контрольной удельной активности) определяли методом нелинейной регрессии графических зависимостей ингибирования от концентрации, построенных на основе среднего значения двух определений с помощью аппроксимации кривой по уравнению Хилла. Концентрации, используемые для получения графической зависимости ингибирования от концентрации, составляли 30, 3, 0,3, 0,03 и 0,003 мкM.
Таблица 3. Условия проведения исследования эпигенетического связывания
Результаты анализов связывания представлены ниже в таблице 4.
Таблица 4. Ингибирующее действие соединений 1-3 при концентрации 10 мкМ на связывание эпигенетически взаимодействующих белковых модулей при сравнении с референсными соединениями.
A% ингибирования контрольного специфического связывания
NA Не применялось
Данные по типичному ингибирующему действию соединения 1 на связывание примеров эпигенетических мишеней приведены в таблицах 5-8.
Таблица 5. ASH1L (h) бромодомен
Таблица 6. CECR2(h) бромодомен кривая связывания
Таблица 7. SP140 (h) бромодомен кривая связывания
Таблица 8. UHRF1(108-286) (h) кривая связывания.
Таблица 9. Величины IC50, рассчитанные из кривых зависимости ингибирования от концентрации, для соединений 1 и 2 в случаи связывании эпигенетически взаимодействующих белковых модулей при сравнении с референсными соединениями.
IC50 (мкM)
Таблица 10. Ингибирующее действие соединений 1-3 при концентрации 10 мкМ на активность эпигенетических ферментов при сравнении с референсными соединениями.
N-метил-трансфераза (h)
N-метил-трансфераза (h)
S-метил-трансфераза (h)
А Контрольные величины % ингибирования
Таблица 11. Величины IC50, рассчитанные из кривых зависимости ингибирования от концентрации, для соединений 1, 2 и 4 в случае ингибирования эпигенетических ферментов при сравнении с референсными соединениями.
IC50 (мкM
Результаты: эпигенетические мишени, заболевания и рак
Эпигенетические модификации могут играть определенную роль в развитии ряда заболеваний. Эпигенетическая регуляция вызывает иерархическую ковалентную модификацию ДНК и белков, которые образуют упаковку, такую как гистоны. Регуляция ДНК происходит путем метилирования и деметилирования на цитозиновых остатках. Метилирование ДНК опосредуется представителями семейства ДНК-метилтрансферазы (DNMT1, DNMT3A и DNMT3B), в то время как деметилирование опосредуется семейством с транслокацией десятой-одиннадцатой хромосом (TET1-3). Помимо метилирования и деметилирования, регуляция гистона также происходит в результате ацетилирования и деацетилирования. Ключевые белки, которые опосредуют эпигенетический сигнальный путь в результате ацетилирования и метилирования гистонов, включают гистон-ацетилтрансферазы (HATs), гистон-деацетилазы (HDMs), протеин-метилтрансферазы (PMTs), включающие лизин-метилтрансферазы (KMTs) протеин-аргинин-метилтрансферазы (PRMTs), и бромодоменсодержащие белки, и белки, которые связывают метилированные гистоны (Arrowsmith et al., 2012; Plass et al., 2013; Tough et al., 2014; Biggar и Li, 2015).
Бромодоменсодержащие белки
Соединение 1 демонстрировало значительную ингибирующую активность в отношении многих из бромодоменсодержащих белков (таблица 10), в частности, ASH1L, CECR2, EP300, KAT2A, PHIP(2), SP140, SMARCA2, TAF1(2), ATAD2A, BRD2(1), BRD4(2) и CREBBP. Соединение 2 демонстрировало значительную ингибирующую активность в отношении BRD2(1). В недавно проведенных исследованиях обнаружена непосредственная связь бромодомен (BRD)-содержащих белков с большим числом заболеваний человека, в том числе с раком (Taverna et al., 2007; Prinjha et al., 2012; Biggar и Li, 2015). Наиболее исследованным представителем BRD-содержащих белков (BCPs) в качестве мишеней для лекарственных средств является семейство белков BET. В настоящее время, известно несколько ингибиторов BET, проходящих различные стадии клинических испытаний, включающие RVX-208, I-BET 762, OTX 015, CPI-0610 и TEN-010 (смотрите таблицу 14 в публикации Tough et al., 2014).
Кроме того, было показано, что JQ1 и I-BET взаимодействуют с NF-κB и индуцируют апоптоз при лейкозе, резистентном к действию лекарственных средств (Ciceri et al., 2014). NF-κB играет центральную роль при воспалении и недиагностируемом воспалении, и имеет непосредственное отношение ко многим болезненным состояниям, в том числе к раку.
Было показано, что некоторые бромодоменсодержащие белки, включающие ASH1L, ATAD2A/B, BAZ2A/B, CECR2, EP300, KAT2A, PHIP(2), PB1, SMARCA2/4, BRD2/4 и CREBBP, характеризуются повышенной регуляцией при многих типах рака (Tough et al., 2014; Fu et al., 2015). Следовательно, BRDs являются терапевтическими мишенями при раке. Была выяснена связь между BRD-содержащими доменами и развитием ряда чрезвычайно агрессивных опухолей, содержащих BRD4-NUT и BRD3-NUT. Были выявлены CREBBP мутации при рецидивирующем остром лимфобластном лейкозе, и они очень часто имеют место при диффузной В-крупноклеточной лимфоме и фолликулярной лимфоме, лимфоме Ходжкина. CREBBP и родственный HAT сильно экспрессируют при прогрессирующей стадии рака предстательной железы, и была выявлена зависимость выживаемости пациентов от уровней экспрессии. ATAD2 характеризуется повышенной экспрессией в более чем 70% случаев опухолей молочной железы, и более высокие уровни белка коррелируют с плохим прогнозом общей выживаемости и обострением болезни (Ciro et al., 2009). ATAD2B характеризуется избыточной экспрессией при глиобластоме и олигодендроглиоме, а также при карциноме молочной железы (Krakstad et al., 2015). BRD4 связан с развитием рака шейки матки (Weidner-Glunde et al.; 2010).
Соединение 1 демонстрировало высокую ингибирующую активность в отношении домена PHD (гомологичного домена растительных организмов), содержащего домен белков SP140, TRIM 33, UHRF1 (108-286)).
Метилтрансферазы
Соединение 1 являлось сильным ингибитором фермента лизин- метилтрансферазы G9a, в то время как соединения 2 и 3 имели более слабое ингибирующее действие (таблица 10). G9a представляет собой мультипотентный регулятор экспрессии генов, который, как было показано, избыточно экспрессирует при многих различных типах рака (более подробную информацию можно найти в обзорах Shankar et al., 2013; Casciello et al., 2015). Соединения 1-3 сильно ингибируют активность PRMT4 и умеренно ингибируют активность PRMT6. Разрегулируемая экспрессия и активность PRMT было обнаружена при различных типах рака, и было показано, что PRMT1-5 и 7 избыточно экспрессируют или же способствуют образованию опухолей, в то время как PRMT8 и 9 непосредственно не связана с онкогенезом (Fuhrmann et al., 2015). PRMT4 (CARM1) является необходимым для транскрипционного фактора NFκB экспрессии таргетных генов. В еще одном исследовании была обнаружена связь между PRMT4 и активностью p300 ацетилтрансферазы при NFκB рекрутменте и активации генов.
Деметилазы
Соединение 1 демонстрировало значительную ингибирующую активность в отношении многих из ферментов лизин-деметилаз (таблица 10), в частности, JARID1A, JARID1B, JMJD1A, JMJD2B, JMJD2E, JMJD3 и UTX. Аберантную экспрессию и мутации лизин-деметилаз связывают с различными типами рака (Hojfeldt et al., 2013; Tough et al., 2014). Было показано, что мутации лизин-деметилаз, включающих FBXL10, JMJD2A, JMJDB, JMJD2C, JARID1B и PHF2, избыточно экспрессируются при опухолях молочной железы, толстой кишки, легких, представительной железы, мочевого пузыря и при других опухолях; функциональная значимость избыточной экспрессии JMJD2C дополнительно подтверждается присутствием гена JMJD2C внутри амплифицированного участка хромосомы при множественных раках (Xiang et al., 2007; Couvelard et al., 2008; Roesch et al., 2010; He et al., 2011a; Berry и Janknecht, 2013; Kogure et al., 2013; Tzatsos et al., 2013).
Гистон-ацетилтрансферазы
Серрулатановые дитерпены демонстрировали значительную ингибирующую активность в отношении гистон-ацетилтрансфераз CREBBP и MYST4 (таблица 10). Аберрантное регулирование активности гистон-ацетилтрансферазы связывали с многими различными патогенетическими состояниями, включающими различные типы рака, нейродегенеративные нарушения и метаболические, респираторные, воспалительные и сердечно-сосудистые заболевания (Adcock and Lee, 2006; Avvakumov and Cote, 2007; Grabiec et al., 2008; Ghizzo et al., 2011, Iyer et al., 2011; Pirooznia and Elefant, 2013).
Таблица 12. Исследования стимуляции ферментов и клеток с помощью соединений 1-3 при концентрации 10 мкM
IC50 (мкM
Фармакологические исследования
In vitro фармакологические исследования проводились научной исследовательской организацией Eurofins PanLab (Taiwan) с использованием параметров, представленных в таблице 13, с указанием ссылок на соответствующие литературные данные.
Таблица 13. Методы фармакологического исследования.
(время/температура)
MgCl2, 1 мМ EDTA, 0,1% BSA
80,0 г подвздошная кишка
(время/температура)
(время/температура)
(время/температура)
(время/температура)
1 мМ CaCl2, 0,2% BSA
(время/температура)
MgCl2, 1 мМ EDTA, 0,1% BSA
(время/температура)
5 мМ MgCl2, 0,5% BSA, 0,1% NaN3
(время/температура)
(время/температура)
1 мМ MgCl2, 0,2% BSA
(время/температура)
1 мМ CaCl2, 0,2% BSA
(время/температура)
(время/температура)
мМ MgCl2, 137 мМ NaCl
(время/температура)
(время/температура)
мМ MgCl2, 137 мМ NaCl
(время/температура)
1,2 мМ CaCl2, 5 мМ KCl, 1,2 мМ MgSO4, 138 мМ NaCl
(время/температура)
(время/температура)
0,54 мМ MgCl2, 30,6 мкM SAM
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
2 мМ EDTA, 0,2 мг/мл BSA
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
MgCl2, 0,1% BSA
(время/температура)
(время/температура)
(время/температура)
(время/температура)
1 мМ NADP, 4 мМ EDTA, 2 мМ DTT,
0,6 Ед/мл G-6-P-DH
(время/температура)
(время/температура)
(время/температура)
(время/температура)
0,1 мМ EDTA
(время/температура)
(время/температура)
100
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
(время/температура)
1% FBS
(время/температура)
1% FBS
(время/температура)
Результаты фармакологических исследований приведены в таблице 14.
Таблица 14. Фармакологическая активность соединений 1-3 при 10 мкМ.
Фармакологические исследования: дополнительные исследования липоксигеназы, липидной пероксидазы и моноаминоксидазы
Дополнительные in vitro фармакологические исследования проводились научной исследовательской организацией Eurofins Panlabs Ltd. (Taiwan) с использованием параметров, представленных в таблице 3, с указанием ссылок на соответствующие литературные данные.
Для соединения 1 при исследовании 5-липоксигеназы, липидной пероксидазы и моноаминоксидазы MAO-A assays, концентрации для построения графических зависимостей ингибировании от концентрации составляли 10, 3, 1, 0,3, 0,01, 0,03 и 0,01 мкM (таблица 15).
Таблица 15. Активность соединения 1 в отношении 5-липоксигеназы, липидной пероксидазы и моноаминоксидазы (MAO-A) IC50 (мкМ) и референсных соединений
1
IC50 мкM
IC50 мкM
Соединения 1-3 являются ингибиторами окисления липидов с высокой и умеренно высокой активностью (таблицы 14 и 15). Поэтому, они могут применяться для блокирования воспаления, вызванного окислительным повреждением при раке.
5-Липоксигеназа промотирует окисление липидов и продуцирует лейкотриены. Соединения 1-3 являются ингибиторами 5-липоксигеназы с высокой и умеренно высокой активностью (таблицы 14 и 15). Поэтому, они могут применяться для блокирования воспаления, вызванного окислительным повреждением и воспалительной патофизиологией при раке.
12-Липоксигеназа промотирует окисление липидов и продуцирует лейкотриены. Соединения 1-3 являются ингибиторами 5-липоксигеназы с умеренной активностью (таблица 14). Поэтому, они могут применяться для блокирования воспаления, вызванного окислительным повреждением и воспалительной патофизиологией при раке.
Соединение 1 является сильным ингибитором моноаминоксидазы A и B (таблицы 14 и 15). Поэтому, оно может применяться для блокирования окислительного повреждения, вызванного окислением моноаминов, и в качестве антидепрессанта.
Соединения 1-3 ингибируют связывание радиолиганда с H1- и H2-гистаминовыми рецепторами (таблица 14). Поэтому, они могут применяться для блокирования воспаления, вызванного гистамином, что обуславливает противовоспалительное действие, которое является целесообразным при лечении рака.
Соединение 1 ингибировало активность тиоредоксинредуктазы (таблица 14). Ингибирование активности тиоредоксинредуктазы может быть использовано для селективного усиления окислительного стресса в раковых клетках, уменьшая при этом окислительный стресс в нормальных клетках.
Соединение 1 ингибировало активность миелопероксидазы (таблица 14). Ингибирование активности миелопероксидазы может быть использовано для селективного уменьшения окислительного стресса в иммуноцитах при проведении противораковой терапии.
Кривые, демонстрирующие связывание соединения 1 с 5-липоксигеназой, липидной пероксидазой и моноаминоксидазой (MAO-A), представлены на фигурах 7-9.
Фармакологические исследования: усвоение 2-деокси-D-глюкозы в мышечных клетках
Таблица 16. Действие соединений 1-4 при концентрации 10 мкМ на усвоение 2-деокси-D-глюкозы в мышечных клетках.
1
2
3
4
* антагонист - ингибирование вызванного инсулином усвоения 2-DG
Фармакологические исследования: адгезия и транскрипционный ответ
Таблица 17. Эффект дозы и величины IC50 для фармакологической активности типичных серрулатановых дитерпенов.
1
2
3
Ядерный фактор каппа-В (NF-κB) сначала был открыт в качестве фактора в ядре В-лимфоцитов, который связывается с энхансером каппа легкой цепи иммуноглобулина и который также является лимфоидно специфическим (Sen and Baltimore, 1986). Семейство NF-κB включает RelA/p65, NF-κB1 p50/p105, NF-κB2 p52/p100, C Rel и RelB. Эти белки содержат N-терминальный домен гомологии Rel (RHD), который ответственен за связывание с ДНК и другими белками и перенос лидерской последовательности ядер (NLS). NF-κB белки функционируют в качестве димерного транскрипционного фактора, который регулирует экспрессию генов, влияющих на широкий диапазон биологических процессов, включающих врожденный и приобретенный иммунитет, воспаление, стрессовые реакции, развитие В-клеток и лимфоидный органогенез (Pantano et al., 2006; Brigelius-Fohê и Fohê 2011; Ghosh et al., 2012; Akdis et al., 2017).
Было показано, что NF-κB играет различные и комплексные роли при раке и иммуномодуляции (Perkins, 2012; Sethi et al., 2012; Parri and Chiarugi, 2013; D'Ignazio et al., 2015). Исходя из значительной ингибирующей активности в отношении NF-κB (IC50 0,69 мкМ) и цитокинов (IC50 6,6, 8,8, 4,3, 8,9 мкМ, для IL1β, IL-6, IL10, TNFα, соответственно), соединение 1 может теоретически влиять на экспрессию упомянутых выше биологических процессов, а также на модуляцию иммунных ответов. В подтверждение этих результатов, геномный анализ с использованием с использованием панели раковых клеток OncoPanel™ фирмы Eurofins показал, что соединение 1 скапливалось вблизи ABT-199, ингибитора BCL-2 домена BH3. ABT-199 блокировал антиапоптозное действие BCL-2, приводя к программированной гибели клеток. Помимо противоопухолевого действия лекарственного средства BCL 2, были предложены миметики BH3 применительно к иммуномодуляции (Ludwig et al., 2016). В совокупности, действие соединения 1 могло бы быть нацелено на гибель раковых клеток, а также на иммуномодуляцию. На фигуре 10 представлены данные для соединения 1 по транскрипционному ответу и связыванию в отношении NF-κB.
In vitro исследование воздействия серрулатановых терпенов на жизнеспособность клеток
Проводили оценку четырех серрулатановых дитерпенов, а именно, соединений 1-4, и смолы растения Myoporum insulare на их способность in vitro ингибировать клеточный рост в 43 линиях раковых клеток и в одной линии нормальных клеток, результаты которой представлены в таблице 19. Продолжительность исследования составляет 72 часа (три дня).
Методика in vitro исследования жизнеспособности клеток
Исследования жизнеспособности клеток проводились компанией Eurofins PanLab (Taiwan). Исследования основываются на хорошо известном принципе, что жизнеспособность (выживаемость) клеток может быть оценена путем определения внутриклеточных уровней аденозинтрифосфата (ATP) с помощью биолюминесценции в метаболически активных клетках (Xia, M et al. 2008). Исследования проводят путем высевания клеток в двух планшетах (T0 и T72). В момент времени "ноль" собирают клетки из планшета (T0), обрабатывают их и инкубируют в течение 72 часов (трех дней) до того момента, когда будет произведен сбор клеток из планшета T72. Определяют внутриклеточные уровни ATP и регистрируют количество жизнеспособных клеток.
Результаты исследования жизнеспособности клеток для соединений 1 и 4 и экстракта смолы/экссудата растения Myoporum insulare на 43 линиях раковых клеток и 1 линии нормальных клеток представлены в таблице 18.
Таблица 18. Ингибирование клеточного роста при концентрации 10,5 мкг/мл смолы растения Myoporum insulare и 10 мкM соединений 1-4.
Результаты исследования жизнеспособности клеток
При концентрации 10 мкM, соединение 1 демонстрировало сильное снижение жизнеспособности клеток (от -80 до -100%) на 20 линиях раковых клеток. Умеренное снижение жизнеспособности клеток (от -40 до -80%) наблюдалось в случае 12 линий раковых клеток и слабое воздействие на жизнеспособность клеток обнаруживалось в случае 4 линий клеток. Ингибирование роста наблюдалось в случае оставшихся клеточных линий.
При концентрации 10 мкM, соединение 2 демонстрировало слабое снижение жизнеспособности клеток (-35%) на лейкозных клетках HL-60 и отсутствие значимого эффекта на оставшихся клеточных линиях. При концентрации 10 мкM, соединение 3 демонстрировало отсутствие значимого эффекта на всех 44 клеточных линиях. При концентрации 10 мкM, соединение 4 демонстрировало сильное снижение жизнеспособности клеток (от -82 до -94%) на шести клеточных линиях лимфомы, лейкоза и рак головного мозга: Ramos и H33HJ-JA1 (лимфома); HL-60 (TB), MOLT-4 и MV-411 (лейкоз) и SK-N-MC (головной мозг). Соединение 4 проявляло селективность без значимого снижения роста эндотелиальных клеток HUVEC (линия нормальных клеток).
При концентрации 10,5 мкг/мл, смола растения Myoporum insulare демонстрировала сильное снижение жизнеспособности клеток (от -80 до -100%) на четырех линиях раковых клеток: SW-620 (толстая кишка), Ramos (лимфома), и MV-411 и MOLT4 (лейкоз). Умеренное снижение жизнеспособности клеток (от -40 до -80%) наблюдалось на шести линиях раковых клеток: MCF-7, MCF7 AdrR, MDA-MB-468 (молочная железа), H33HJ-JA1 (лимфома), SK-MEL-5 (меланома) и MES-SA (матка). Слабое снижение жизнеспособности клеток (от -5 до -38%) наблюдалось на пяти клеточных линиях: K-562 (лейкоз), OVCAR-3 (яичник), LNCaP (предстательная железа), MDA-MB-231 (молочная железа) и A375 (кожа). Отсутствие значимого эффекта наблюдалось на эндотелиальных клетках (линия нормальных клеток).
Исследование пролиферации клеток на панели раковых клеток OncoPanelТМ
Исследование пролиферации клеток на панели раковых клеток OncoPanelТМ дает возможность измерить пролиферативный ответ в линиях раковых клеток на обработку лекарственными средствами с помощью одновременной многопараметрической флуоресцентной визуализации или биолюминесценции. В то время как продолжительность проведения описанного выше исследования жизнеспособности клеток составляет три дня, продолжительность проведения исследования на панели раковых клеток OncoPanelТМ составляет 10 дней.
Методика эксперимента
Клетки выращивали в среде RPMI 1640, 10% FBS, 2 мМ L-алагил-L-глутамин, 1 мМ Na пируват или в специальной среде. Клетки высевали в 384-луночных планшетах и инкубировали в увлажненной атмосфере с 5% CO2 при 37°C. На следующий день после посева клеток добавляли соединения. Одновременно, приготавливали планшет с необработанными клетками с моментом времени ноль. После инкубации в течение 10 дней, клетки фиксировали и окрашивали с целью флуоресцентной визуализации ядер. На 7 день после посева, питательные среды заменяли, и в планшеты повторно вводили испытуемое соединение.
Соединения последовательно разбавляли с полулогарифмической величиной шага от наивысшей концентрации испытуемого соединения, указанной выше в таблице, и проводили исследование при 10 концентрациях с максимальной концентрацией DMSO при исследовании 0,1%. Автоматизированную флуоресцентную микроскопию проводили с использованием установки для одновременной многопараметрической флуоресцентной визуализации ImageXpress Micro XL фирмы Molecular Devices, и изображения получали с помощью 4X объектива. Регистрировали 16-битные изображения в формате TIFF и анализировали их с помощью программного обеспечения MetaXpress 5.1.0.41.
Анализ данных
Пролиферацию клеток измеряли по интенсивности флуоресценции введенного в ядро красителя. Результат выражают в форме относительного числа клеток, где измеренную интенсивность ядра пересчитывают в процент контроля (POC), используя следующую формулу:
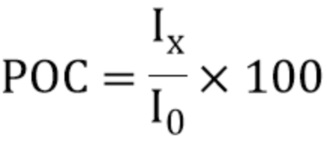
где Ix представляет собой интенсивность ядра при концентрации x, и I0 представляет собой среднее значения интенсивности ядра в лунках с необработанной средой.
Параметры клеточного ответа рассчитывали с использованием нелинейной регрессии для сигмоидальной одноцентровой модели доза-эффект:
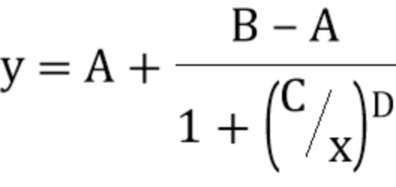
где y представляет собой эффект, измеренный при концентрации x, A и B представляют собой нижний и верхний пределы величины эффекта, C представляет собой концентрацию для медианы измеренных величин эффекта (EC50), и D представляет собой угловой коэффициент Хилла (Fallahi-Sichani, M., S. et al. 2013).
Необработанные планшеты с временем ноль использовали для определения числа удвоений в течение периода времени исследования, используя формулу:

где N представляет собой число клеток в необработанных лунках в момент времени окончания исследования, и NT0 представляет собой число клеток в момент добавления соединения.
Число клеток IC50 представляет собой концентрацию испытуемого соединения при 50% максимально возможного эффекта. EC50 представляет собой концентрацию испытуемого соединения в точке перегиба кривой или при половине величины действенного эффекта (параметр C при подборе аппроксимирующей кривой). GI50 представляет собой концентрацию, необходимую для снижения наблюдаемого роста наполовину (посредине между максимумом кривой и величиной времени ноль). Область активности представляет собой оценку интегрированной площади над кривой (Barretina, J. G. et al. 2012). Значения области активности изменяются в пределах 0-10, где значение ноль указывает на отсутствие ингибирования пролиферации при все концентрациях, а значение 10 указывает на полное ингибирование пролиферации при всех концентрациях. В редких случаях, могут наблюдаться значения < 0 или > 10. В этих случаях, значения < 0 следует считать эквивалентными 0, а значения > 10 следует считать эквивалентными 10.
Подбор аппроксимирующей кривой, вычисления и генерирование отчета осуществляли с использованием машины редуцирования пользовательских данных и программного обеспечения на основе MathIQ (AIM).
Результаты исследования пролиферации клеток на панели раковых клеток OncoPanelТМ (OncoPanelТМ, Eurofins PanLab, USA, на 280 линиях раковых клеток человека) для соединений 1, 2 и 4 представлены ниже в таблице 19. В таблицах 21-28 приведены типичные данные по пролиферативному ответу (таблица 21: MDA-MB-415; таблица 22: RKO-AS45-1; таблица 23: SW480; таблица 24: 639-V; таблица 25: Hs 729; таблица 26: Hs 852.T; таблица 27: HCT-8; таблица 28: IM-9), и результаты по пролиферации клеток для смолы растения Myoporum insulare приведены ниже в таблице 29.
Таблица 19. Результаты исследования пролиферации клеток на панели раковых клеток OncoPanelТМ для соединений 1, 2 и 4.
(мкM)
(RA 1)
Таблица 20. Результаты исследования антипролиферативной активности соединений 11 и 12 с использованием панели раковых клеток OncoPanel™.
Таблица 21. Типичные данные по пролиферативному ответу в случае обработки клеток линии MDA-MB-415 с помощью соединения 1
Данные, приведенные в таблице 21, графически представлены на фигуре 11.
Таблица 22. Типичные данные по пролиферативному ответу в случае обработки клеток линии RKO-AS45-1 с помощью соединения 1
Данные, приведенные в таблице 22, графически представлены на фигуре 12.
Таблица 23. Типичные данные по пролиферативному ответу в случае обработки клеток линии SW480 с помощью соединения 1
Данные, приведенные в таблице 23 графически представлены на фигуре 13.
Таблица 24. Типичные данные по пролиферативному ответу в случае обработки клеток линии 639-V с помощью соединения 1
Данные, приведенные в таблице 24, графически представлены на фигуре 14.
Таблица 25. Типичные данные по пролиферативному ответу в случае обработки клеток линии Hs 729 с помощью соединения 1
Данные, приведенные в таблице 25 графически представлены на фигуре 15.
Таблица 26. Типичные данные по пролиферативному ответу в случае обработки клеток линии Hs 852.T с помощью соединения 1
Данные, приведенные в таблице 26, графически представлены на фигуре 16.
Таблица 27. Типичные данные по пролиферативному ответу в случае обработки клеток линии HCT-8 с помощью соединения 1
Данные, приведенные в таблице 27, графически представлены на фигуре 17.
Таблица 28. Типичные данные по пролиферативному ответу в случае обработки клеток линии IM-9 с помощью соединения 1
Данные, приведенные в таблице 28, графически представлены на фигуре 18.
Таблица 29. Результаты исследования пролиферации клеток на панели раковых клеток OncoPanelТМ для экстракта смолы растения Myoporum insulare.
A 14 июля 2016 года; B 22 августа 2016 года; C 22 сентября 2016 года; D 5 октября 2016 года
Для соединения 1, наблюдался широкий спектр активности в отношении 280 типов клеток, с активностью от очень высокой до высокой (GI50=0,006-2,98 мкM) в отношении 174 клеточных линий. Очень высокая активность наблюдалась в отношении линий клеток почек SK-NEP-1 (GI50=0,00618 мкM) и лейкоза J-RT3-T3-5 (GI50=0,0101 мкM). Умеренно высокая активность наблюдалась (GI50=0,11 мкM) в отношении линии клеток лейкоза KG-1. Умеренно высокая активность (GI50=0,4-1,0 мкM) наблюдалась в отношении следующих клеточных линий: 2 линии клеток молочной железы KPL-1, MDA-MB-453; 3 линии клеток миеломы IM-9, RPMI8226, SKO-007; 3 линии клеток меланомы A7, COLO829, RPMI-7951; 7 линий клеток мягкой ткани HOS (остеосаркомы), KHOS-240S (остеосаркомы), SW1353 (остеосаркомы), A204 (саркомы), HT-1080 (саркомы), RD (саркомы), SW 872 (саркомы); 2 линии клеток мелкоклеточной карциномы легкого DMS53, SHP-77; а также Colo 201 (толстой кишки); FaDu (головы и шеи), 769-P (почки), HepG2 (печени), и AGS (желудка). Сильная активность была продемонстрирована (GI50=1-2,98 мкM) в отношении 149 клеточных линий: 16 линий клеток меланомы, 15 линий клеток лимфомы, 9 линий клеток женских урогениталий, 14 линий клеток мягкий тканей (саркомы), 16 линий клеток толстой кишки, 12 линий клеток лейкоза, 8 линий клеток немелкоклеточной карциномы легкого, 8 линий клеток поджелудочной железы, 9 линий клеток молочной железы, 10 линий клеток ЦНС, 8 линий клеток мочевого пузыря, 5 линий клеток почки, 4 линий клеток головы и шеи, 4 линий клеток железы внутренней секреции, 1 линии клеток миеломы, 3 линий клеток печени, 2 линий клеток мелкоклеточной карциномы легкого, 2 линий клеток предстательной железы, 2 линий клеток желудка и 1 линии клеток яичка.
Для соединения 2, наблюдался узкий спектр активности в отношении 280 типов клеток, с активностью от высокой до сильной (GI50=0,06-2,96 мкM) в отношении 10 клеточных линий. Высокая активность наблюдалась в отношении линии клеток почек SK-NEP-1 (GI50=0,0606 мкM). Сильная активность (GI50=1-2,96 мкM) наблюдалась в отношении следующих клеточных линий: 5 линий клеток лейкоза J-RT3-T3-5, Jurkat, MOLT-3, NALM-6, TF-1; 2 линий клеток миеломы RPMI8226, SKO-007; 1 линии клеток мягкой ткани RD (саркомы). Для соединения 2, активности в отношении Jurkat, MOLT-3, NALM-6, TF-1 (лейкоз) и SKO-007 (миелома) по величине были аналогичными величине для соединения 1.
Для соединения 4, наблюдался узкий спектр активности в отношении 280 280 типов клеток, с активностью от умеренно высокой до сильной (GI50=0,68-2,92 мкM) в отношении 12 клеточных линий. Одна сильная активность (GI50=0,684 мкM) наблюдалась в отношении линии клеток A204 (саркомы мягких тканей), по величине аналогичная величине, наблюдаемой для соединения 1. Сильная активность (GI50=1,23-2,92 мкM) для соединения 4 наблюдалась в отношении следующих клеточных линий: 5 линий клеток лимфомы (Daudi, DOHH-2, GA-10, L-428, ST486); 2 линий клеток лейкоза (MX1, NALM-6); также для линии клеток T47D (молочная железа), линии клеток CEM-C1 (лейкоз), линии клеток A-673 (саркома мягких тканей). Активность в отношении этих клеточных линий является сопоставимой по величине с соединением 1, однако, соединение 4 демонстрирует сильную активность в отношении линии клеток лейкоза J-RT3-T3-5 (GI50=2,71 мкM), которая приблизительно в 270 раз меньше, чем очень высокая активность, наблюдавшаяся для соединения 1 (GI50=0,0101 мкM) в отношении этой клеточной линии.
Экстракт смолы растения демонстрировал сильную активность (GI50=0,11 -1,03 мкг/мл) в отношении 24 клеточных линий: 4 линий клеток саркомы мягких тканей (A204, HT-1080, RD, SW 872); 4 линий клеток меланомы (A7, COLO829, Hs695T, RPMI-7951); 3 линий клеток миеломы (IM-9, RPMI8226, SKO-007); 2 линий клеток молочной железы (KPL-1, MDA-MB-453); 2 линий клеток лимфомы (DOHH-2, SU-DHL-5); 2 линий клеток мелкоклетчатой карциномы (DMS53, SHP-77); 2 линий клеток лейкоза (Jurkat, NALM-6) и также линии клеток мочевого пузыря (UM-UC-3); толстой кишки (SW480); щитовидной железы (CGTH-W-1); головы и шеи (FaDu) и желудка (AGS). Для линии клеток меланомы Hs695T, в расчете на массу, экстракт смолы растения (GI50=0,11 μмкг/мл) имел активность приблизительно в 3 раза выше, чем активность соединения 1 (GI50=0,37 μмкг/мл) в отношении этой конкретной линии клеток. При сравнении в расчете по массе в отношении всех других клеточных линий, экстракт растения имел более низкую активность, чем соединение 1.
В целом, соединение 1 обеспечивает широкий спектр противораковой активности в отношении широкого спектра клеточных линий. Соединение 2 демонстрирует специфичность в отношении линии клеток предстательной железы LNCaP, а также специфическую активность в отношении линии клеток SK-NEP-1 (почки), Jurkat, MOLT-3, NALM-6, TF-1 (лейкоз) и SKO-007, RPMI8226 (миеломы), аналогичную величине для соединения 1. Соединение 4 демонстрировало активность, от умеренно высокой до сильной (GI50=0,68-2,92 мкM), в отношении узкого диапазона клеточных линий (12 из 280) по сравнению с соединением 1 (174 из 280).
Таблица 30. Число типов раковых клеток рак для уровней ингибирующей активности роста для соединений 1, 2 и 4
Таблица 31. Число типов раковых клеток рак для уровней ингибирующей активности роста для экстракта растения Myoporum insulare
Ингибирование активации толл-подобного рецептора 4 (TLR4) на мононуклеарах периферической крови человека (PBMC's).
Цель исследования
Оценка способности соединения ингибировать активацию толл-подобного рецептора 4 (TLR4) на мононуклеарах периферической крови человека (PBMC's).
Протокол проведения эксперимента
Проводили оценку способности соединения 1 ингибировать TLR4 в PBMC's человека, измеряемую по выделению специфических цитокинов. Оценку проводила компания Eurofins Panlabs Inc., St Charles, Missouri, USA.
Протокол исследования ингибирования TLR4
a) Криосохраненные BMC's человека размораживали до жидкого состояния.
b) Разбавляли клетки до соответствующей плотности (1×105 клеток на лунку) и высевали в 96-луночных полипропиленовых планшетах, содержащих 150 мкл на лунку культуральной среды (RPMI 1640, 10% термоинактивированная FBS, 1% пенициллин/стрептомицин, 2 мМ L-глутамин).
c) Инкубировали клетки при 37°C, 5% CO2 в течение 1 часа перед добавлением испытуемых соединений или контрольных соединений.
d) Растворяли испытуемые соединения в DMSO с получением исходных раствором, и затем дополнительно разбавляли с помощью среды культуры клеток. Положительный контроль, LPS (from S. minnesota R595), ресуспендировали в не содержащей эндотоксин воде при 0,5 мг/мл с получением рабочих исходных растворов. Дексаметазон использовали в качестве референсного контрольного соединения.
e) Соединения и контрольные соединения, включая соответствующие контрольные среды, добавляли к PBMC's в объемах 10 мкл и инкубировали в течение 1 часа при 37°C, 5% CO2. Соединения подвергали испытанию два раза при конечных концентрациях исследования 10, 3, 1, 0,3, 0,1, и 0,03 мкM. В лунки для контрольной среды просто добавляли 10 мкл соответствующей среды.
f) После 1 часа инкубации, 40 мкл разбавленного рабочего исходного LPS (липополисахарида) добавляли в лунки с испытуемым соединением и в лунки с контрольным соединением с получением конечных объемов для исследования 200 мкл. Планшеты инкубировали в течение 24 часов при 37°C, 5% CO2.
g) Планшеты центрифугировали при 200 x g в течение 10 минут. Надосадочные жидкости клеточной культуры собирали и хранили при -80°C до тех пор, пока их не подвергали анализу.
h) Уровни цитокина в каждом образце определяли, используя методику фирмы Luminex в соответствии с протоколом фирмы-производителя.
Донор PBMC: Человеческий донор 1 (лот # 100)
Результаты и обсуждение
Стимуляция PBMC's человека с помощью LPS в течение 24 часов характеризовалась измеряемым выделением соответствующих цитокинов внутри ожидаемых диапазонов. В противоположность этому, дексаметазон ингибировал LPS-стимулированное выделение цитокинов из PBMC's человека, также внутри ожидаемых диапазонов. Соединение 1 проявляло поддающееся измерению ингибирование LPS-индуцированного выделения специфических цитокинов из PBMC's человека после стимуляции на протяжении 24 часов.
Как видно из результатов, приведенных в таблице 32, соединение 1 оказывало ингибирующее действие, от умеренного до сильного, в отношении секреции всех цитокинов при наивысшей испытуемой концентрации, характеризуясь измеренными величинами IC50 4,3 мкM, 6,6 мкM, 8,8 мкM и 8,9 мкM для IL-10, IL-1β, IL-6 и TNFα, соответственно. (Величины IC50 не могли быть измерены для IL-8 и MIP-1α.)
Таблица 32. Активность соединения 1 в отношении конкретных LPS-индуцированных цитокинов
Исследования с помощью панели BioPrint
Исследование с помощью панели BioPrint (проводимое компанией Eurofins Cerep, France) позволяет получать набор свойств, который обеспечивает достижение двойной цели, оценивая безопасность при воздействии на мишени с известными требованиями по безопасности, а также обеспечивая достаточно подробный набор свойств для поиска соединений с аналогичными свойствами.
Методика
Соединение 1 подвергали испытаниям при 10 мкM. Для соединения 1 при 10 мкM, исследования агониста радиолиганда для контрольного специфического ингибирования, представляющего интерес с точки зрения биологической активности или безопасности, проводятся при следующих условиях:
Семейство GPCR: аденозин A3 (h), 92%; адренергический альфа 2C (h), 92%; каннабиоид CB2 (h), 71%; холецистокинин CCK1 (CCKA) (h), 81%; дофамин D1 (h), 67%; дофамин D3 (h), 85%; гистамин H1 (h), 64%; мелатонин MT1 (ML1A) (h), 91%.
Транспортеры: транспортер норэпинефрина (h), 76%.
Нестероидные ядерные рецепторы: PPARgamma (h), 91%.
Для соединения 1 при 10 мкM, ферментативные исследования для контрольного специфического ингибирования, представляющего интерес с точки зрения биологической активности или безопасности, проводятся при следующих условиях:
AA метаболизм: COX1 (h), 81%; COX2 (h), 74%.
Связывание соединения рассчитывали, как % ингибирования связывания радиоактивно-меченного лиганда, специфического для каждой мишени. Активность соединения по ингибированию ферментов рассчитывали, как % ингибирования активности контрольного фермента. Считается, что результаты, характеризующие ингибирование или стимуляцию выше чем 50%, представляют значимые эффекты испытуемых соединений.
Результаты
Результаты соединения 1 по ингибированию контрольного специфического связывания с рецепторами приведены в таблице 33, а результаты по ингибированию контрольного специфического связывания ферментов в ферментативных и клеточных исследованиях приведены в таблице 34.
Таблица 33. Результаты исследования соединения 1 при 10 мкМ с помощью панели BioPrint на ингибирование контрольного специфического связывания с рецепторами.
1
IC50 (мкM)
5-HT (h) (антагонист радиолиганд)
Таблица 34. Результаты исследования на ферментах и клетках соединения 1 при 10 мкМ с помощью панели BioPrint на ингибирование контрольного специфического связывания ферментов
1
IC50 (мкM)
In vitro токсичность: исследование токсичности на панели нормальных клеток
В исследовании пролиферации нормальных клеток с помощью набора OncoPanelТМ (Eurofins Panlabs Inc., St Charles, Missouri, USA) определяется пролиферативный ответ нормальных клеток на воздействие лекарственного средства методом одновременной многопараметрической флуоресцентной визуализации.
Методика
Нормальные клетки (смотрите описание в таблице 35) выращивали в специально подобранной среде для каждого типа клеток. Клетки высевали в 384-луночных планшетах и инкубировали в увлажненной атмосфере 5% CO2 при 37°C. На следующий день после посева клеток добавляли соединения (информация в таблице 36). Одновременно, в момент времени ноль приготавливали планшеты с необработанными клетками. После 3 дней инкубации, клетки фиксировали и окрашивали для флуоресцентной визуализации ядер.
Таблица 35. Описание клеток, используемых при исследовании токсичности на панели нормальных клеток
Таблица 36. Информация по соединениям, используемым при исследовании токсичности на панели нормальных клеток
масса
Соединения последовательно разбавляли с полулогарифмическим шагом от наивысшей испытуемой концентрации, указанной выше в таблице, и исследовали при 10 концентрациях при максимальной концентрации DMSO в исследованиях 0,1%.
Методика эксперимента и вычисления являются такими же, как в случае описанного выше исследования пролиферации клеток на панели OncopanelТМ при инкубации в течение 10 дней.
Результаты
В таблице 37 приведены данные по активности соединения 1 (EC50 IC50 и GI50 (мкМ)) в сравнении с референсным соединением паклитакселом. С целью сравнения, в таблице 38 представлены данные по другим референсным соединениям.
Таблица 37. Активность соединения 1 (EC50 IC50 и GI50 (мкМ)) при сравнении с паклитакселом
Таблица 38. Активность дополнительных референсных соединений
В таблице 39 представлены типичные данные по ответу при исследовании пролиферации нормальных клеток линии HREC под воздействием соединения 1 с использованием OncoPanelТМ.
Таблица 39. Воздействие соединения 1 на HREC
Данные, приведенные в таблице 39, графически представлены на фигуре 19.
Обсуждение
Соединение 1 и референсные соединения, паклитаксел, циклогексимид, карбонилцианид 3-хлорфенил-гидразона(CCCP) и стауроспорин, подвергали испытанию на 4 типах нормальных клеток, CCD 841 CoN, HMEC, HREC и Wi38. В итоге, соединение 1 демонстрировало относительно низкую токсичность в отношении всех 4 клеточных линий. Паклитаксел характеризовался низкой токсичностью в отношении клеточной линии HMEC и высокой токсичностью в отношении трех других клеточных линий. На основе средней величины GI50 для 4 линий нормальных клеток, порядок токсичности может быть представлен в следующем виде: стауроспорин > паклитаксел > циклогексимид > CCCP > соединение 1.
In vitro токсичность: исследование ADME-токсичности (токсичности при всасывании, распределении, метаболизме и выведении)
Исследование ADME-токсичности соединений 1, 2 и 4 проводила компания Eurofins Panlabs Inc, St Charles, MO, USA, используя CYP (цитохром Р450)
Методика
Мониторинг ингибирования цитохрома P450 проводили с использованием детектирования методом ВЭЖХ-УФ/видимая область и ВЭЖХ-тандемная масс-спектроскопия. Регистрировали площади пиков, соответствующих метаболиту каждого субстрата. Затем рассчитывали процент контрольной активности путем сравнения площади пика, полученного в присутствии испытуемого соединения, и площади пика, полученного в отсутствии испытуемого соединения. Затем, рассчитывали процент ингибирования для каждого соединения путем вычитания процента контрольной активности из 100. Определяли величины IC50 (концентрацию, вызывающую полумаксимальное ингибирование контрольных величин) методом нелинейного регрессионного анализа кривой концентрация-эффект, используя для аппроксимации уравнение Хилла [Dierks, E.A. et al. (2001)].
Результаты
Таблица 40. Ингибирование CYPs соединениями 1, 2 и 4 при сравнении с референсными соединениями
Заключение о результатах
Фермент - субстраты
CYP1A (субстрат фенацетина)
Соединения 1, 2 и 4 являются сильными ингибиторами при 10 мкM (63-92%). Исходя из определенных величин IC50, которые равны < 10, соединения 1, 2 и 4 являются более сильными ингибиторами, чем референсный стандарт фурафиллин (IC50 16 мкM). Соединения 1 и 2 демонстрировали умеренное ингибирование при 1 мкM (28% и 38%, соответственно).
CYP2B6 (субстрат бупропиона)
Соединения 1, 2 и 4 являются относительно слабыми ингибиторами (13-16% при 1 мкM) по сравнению с референсным соединением клопидогрелем (IC50 0,39 мкM).
CYP2C8 (субстрат паклитаксела)
Соединения 1, 2 и 4 являются относительно слабыми ингибиторами (12-24% при 1 мкM) по сравнению с референсным соединением монтелукастом (IC50 0,57 мкM).
CYP2C9 (субстрат диклофенака)
Соединение 1 являлось очень слабым ингибитором при 1 мкM (5%) и соединения 2 и 4 являлись относительно слабыми ингибиторами (20 и 31%) по сравнению с референсным соединением сульфафеназолом (IC50 0,28 мкM).
CYP2C19 (субстрат омепразола)
Соединения 1, 2 и 4 являются умеренно сильными ингибиторами (25-37% при 1 мкM) с активностью, сравнимой с оксибутинином (IC50 6,7 мкM).
CYP2D6 (субстрат декстрометорфана)
Соединения 1, 2 и 4 являются относительно слабыми ингибиторами (12-21% при 1 мкM) по сравнению с референсным соединением хинидином (IC50 0,12 мкM).
CYP3A (субстрат мидазолама)
Соединения 1, 2 и 4 являются относительно слабыми ингибиторами (15-16% при 1 мкM) по сравнению с референсным соединением кетоконазолом (IC50 0,18 мкM).
CYP3A (субстрат тестостерона)
Соединения 1, 2 и 4 являются относительно слабыми ингибиторами (7-20% при 1 мкM) по сравнению с референсным соединением кетоконазолом (IC50 0,18 мкM).
In vivo токсичность: максимально переносимая доза (MTD) соединения 1 для мышей
Два исследования проводились компанией Eurofins Panlabs Taiwan, Ltd. Целью исследования 1 являлась оценка возможных побочных эффектов соединения 1 в чистом виде, или в комбинации с карбоплатином в эксперименте по определению максимально переносимой дозы (MTD). Целью исследования 2 является последующий эксперимент, проводимый при возрастающих дозах.
Информация об используемых в исследовании лекарственной среде и объеме вводимой дозы приведена в таблице 41. В таблице 42 и таблице 43 представлены результаты исследования 1 по наблюдаемой смертности и массе тела. Что касается исследования 2, то в таблице 44 и таблице 45 приведены результаты по наблюдаемой смертности и массе тела, а поведенческие, симптоматические, то есть, неврологические и вегетативные проявления при применении соединения 1 в чистом виде, или в комбинации с карбоплатином, приведены в таблице 46 и таблице 47. Соответствующие проявления в случае введения лекарственных сред приведены в таблице 48 и таблице 49.
Таблица 41. Информация об используемых в исследовании лекарственной среде и объеме вводимой дозы в исследованиях по определению максимально переносимой дозы (MTD)
(мг/мл)
(мг/кг)
Испытуемое вещество и схема дозирования
Соединение 1 растворяли в 10% Tween 20/90% PBS или 20% Tween 20/80% PBS для интраперитонеальных (IP) инъекций. Соединение 1 вводили в чистом виде или в комбинации с карбоплатином при объеме вводимой дозы 10 или 20 мл/кг для каждого вещества.
Исследование 1
При исследовании смертности, испытуемое вещество (соединение 1; 100 мг/кг) в чистом виде или в комбинации с карбоплатином (8,75, 17,5 или 35 мг/кг, применяемым в этот же день) вводили мышам путем интраперитонеальной (IP) инъекции с целью оценки возможных побочных эффектов в эксперименте по определению максимально переносимой дозы (MTD). Мышей объединяли в группу, содержащую 3 самки мышей линии NOD/SCID в возрасте 6-7 недель. Смертность регистрировали через 30 минут и снова через 3, 24, 48 и 72 часов после введений соединения.
При исследовании массы тела, испытуемое вещество (соединение 1; 100 мг/кг) в чистом виде или в комбинации с карбоплатином (8,75, 17,5, применяемым в этот же день) вводили группе из 3 самок мышей линии NOD/SCID в возрасте 6-7 недель. Массу тела каждого животного измеряли и регистрировали ежедневно в течение 3 дней.
Соединение 1 в чистом виде не проявляло значимых нежелательных побочных действий и считалось переносимым. Все испытуемые животные выживали в течение 72 часов периода наблюдения (таблица 42). Однако соединение 1 в комбинации с карбоплатином вызывало тонус конечностей, от легкого до умеренного, и приводило к 33% смертности через 72 часа после дозирования, указывая на то, что уровень дозы плохо переносился животными (таблица 42).
Затем в эксперименте по определению максимально переносимой дозы (MTD) исследовали соединение 1 в комбинации с более низкими дозами карбоплатина (8,75 и 17,5 мг/кг). Соединение 1, вводимое с двумя дозами карбоплатина в один и тот же день, вызывало абдоминальный тонус, от легкого до умеренного, в течение первых 30 минут введения (таблица 44 и таблица 45). Однако в течение всего времени проведения эксперимента у испытуемых животных не наблюдались случаи смерти и потери массы тела, указывая на то, что уровни доз были переносимыми для животных (таблица 44 и таблица 45).
Таблица 42. Максимально переносимая доза (MTD) у мышей (исследование 1, стадия 1 и 2)
35 мг/кг
10 мл/кг
17,5 мг/кг
8,75 мг/кг
Примечание:
a 10% Tween 20/90% PBS
b 0,9% NaCl
Таблица 43. Максимально переносимая доза (MTD) у мышей (исследование 1, стадия 2)
1
2
17,5 мг/кг
8,75 мг/кг
Примечание:
a 10% Tween 20/90% PBS
b 0,9% NaCl
Исследование 2
Последующее исследование максимально переносимой дозы (MTD) проводили с целью оценки нежелательных побочных эффектов при возрастающих дозах испытуемого соединения (соединения 1) в чистом виде или в комбинации с карбоплатином (17,5 мг/кг) при интраперитонеальном введении (IP) в группе из 3 самок мышей линии NOD/SCID в возрасте 6-7 недель.
При исследовании смертности, возрастающие дозы соединения 1 (200 мг/кг) в чистом виде или в комбинации с карбоплатином (17,5 мг/кг, применяемым в этот же день) вводили группе из трех самок мышей линии NOD/SCID в возрасте 6-7 недель путем интраперитонеальной (IP) инъекции. Смертность регистрировали через 30 минут и снова через 3, 24, 48 и 72 часов после введений соединения.
При исследовании массы тела, возрастающие дозы (200 мг/кг) испытуемого вещества (соединения 1) в чистом виде или в комбинации с карбоплатином (17,5 мг/кг, применяемым в этот же день) вводили группе из 3 самок мышей линии NOD/SCID в возрасте 6-7 недель путем интраперитонеальной (IP) инъекции. Массу тела каждого животного измеряли и регистрировали ежедневно в течение 3 дней.
Введение соединения 1 (200 мг/кг) в чистом виде и в комбинации с карбоплатином (17,5 мг/кг) приводило к 33-100% смертности, но не вызывало заметной потери массы тела в течение периода времени исследования (таблица 30 и таблица 31).
Таблица 44. Максимально переносимая доза (MTD) у мышей (исследование 2)
10 мл/кг
17,5 мг/кг
Примечание:
a 20% Tween 20/80% PBS
b 0,9% NaCl
Таблица 45. Максимально переносимая доза (MTD) у мышей (исследование 2; стадия 1 и 2)
1
2
10 мл/кг
17,5 мг/кг
Примечание:
a 20% Tween 20/80% PBS
b 0,9% NaCl
Для исследования поведенческих, симптоматических, то есть, неврологических и вегетативных проявлений, испытуемое вещество (соединение 1; 200 мг/кг) в чистом виде или в комбинации с карбоплатином (17,5 мг/кг, применяемым в этот же день) вводили путем интраперитонеальной инъекции (IP) группе из 3 самок мышей линии NOD/SCID в возрасте 6-7 недель. Затем животных обследовали на присутствие острых токсических симптомов и вегетативных эффектов в течение 30 минут после введения первой дозы.
При введении соединения 1 в чистом виде и в комбинации с карбоплатином наблюдались резко выраженные поведенческие эффекты, такие как пониженная ответная реакция на испуг, на прикосновение, реакция ушами и пониженная способность запоминания расположения предметов (смотрите таблицу 46). При введении соединения 1 наблюдались пониженные неврологические проявления, такие как спонтанная деятельность, распрямление тела, атаксия и низкое положение конечностей (таблица 46). В качестве вегетативного проявления наблюдалась гипотермия (пониженная температура тела) (таблица 47).
Таблица 46. Поведенческие и неврологические проявления у мышей при введении соединения 1 (исследование 2; стадия 1)
Таблица 47. Вегетативные проявления у мышей при введении соединения 1 (исследование 2; стадия 1)
Таблица 48. Поведенческие и неврологические проявления у мышей при введении лекарственных сред (исследование 2; стадия 1)
Таблица 49. Вегетативные проявления у мышей при введении лекарственных сред (исследование 2; стадия 1)
Примечание для таблиц 46-49
a 20% Tween 20/80% PBS
b 0,9% NaCl
-: отсутствие эффектов
±: эффекты от легких до умеренных
+: эффекты в тяжелой форме
Inc.: повышенный
Dec.: пониженный
Spont.: спонтанный
C.: хронический
T.: тонический
C-T: хронический-тонический
↓: низкий
D: глубокий
In vivo противораковая активность: соединение 1 и гемцитабин
In vivo исследование показывает, что соединение 1 является эффективным в комбинации с гемцитабином. Дизайн клинического исследования подробно описан ниже и в таблице 50. Результаты исследования, которые приведены в таблице 51 и таблице 52, позволяют сделать вывод о наличии синергетического эффекта. Монотерапия и комбинированные терапии хорошо переносились животными.
Таблица 50. Дизайн клинического исследования ксенотрансплантата клеток MIA PaCa-2 опухоли поджелудочной железы у самок "голых" (nu/nu) мышей
мг/мл
(самки)
qwk x 3c
q4d x 4d
qwk x 3c
+
Гемцитабин
+
IP
+
8
+
80, q4d x 4d
a Самкам "голых" (nu/nu) мышей в возрасте 7-8 недель имплантируют 1×107 клетки MIA PaCa-2 (0,2 мл/мышь) и начинают дозирование, когда средний объем опухоли в группе достигает ~80-150 мм3.
b Среда для испытуемого вещества (10% Tween 20/90% физиологический раствор)
c Дозы вводят 1 раз в неделю на протяжении 3 недель.
d Дозы вводят 1 раз каждые четыре дня (суммарно четыре введения).
Массу тела и объемы опухоли регистрируют два раза в неделю, начиная со дня 1 и продолжая до момента окончания исследования.
Ингибирование роста опухоли (%TGI) определяют два раза в неделю в течение периода времени дозирования по формуле: %TGI=(1 -[(T -T0)/(C -C0)]) × 100, где T=средний объем опухоли в подвергаемой обработке группе, T0=средний объем опухоли в подвергаемой обработке группе на момент начала исследования, C=средний объем опухоли в контрольной группе, и C0=средний объем опухоли в контрольной группе на момент начала исследования.
Предполагается проведение исследования в течение 28 дней или до тех пор, пока объем опухоли в отрицательной контрольной группе не достигает 2000 мм3, в зависимости от того, что наступит раньше.
Затем определяют TGI, полученные в исследовании данные могут быть пересчитаны в величину замедления роста опухоли (TGD).
Животные должны быть выведены из эксперимента, если/когда:
1. Потеря веса составляет > 25%
2. Наблюдается тяжелая форма изъязвления опухоли
ПРЕДПОЛАГАЕМЫЕ СРОКИ И ПОСЛЕДОВАТЕЛЬНОСТЬ ВЫПОЛНЕНИЯ ИССЛЕДОВАНИЯ
Поставка животных: в течение одного месяца после получения испытуемых соединений
Имплантация опухолевых клеток: в течение двух недель после доставки животных
Дозирование: приблизительно через 1-2 недели после имплантации опухолевых клеток
ТРЕБУЕМОЕ КОЛИЧЕСТВО ОБРАЗЦА
Соединение 1 150 мг, гемцитабин 256 мг.
ПРОТОКОЛ
Ксенотрансплантат клеток MIA PaCa-2 опухоли поджелудочной железы
Методика: используются группы (8) самок мышей линии nu/nu (возраст 7-8 недель), выведенных в изоляторе для животных (клетки с индивидуальной вентиляцией (IVC)) в свободных от специфической патогенной микрофлоры (SPF) условиях при температуре 22 ± 2°C. Жизнеспособные клетки линии MIA PaCa-2 опухоли поджелудочной железы человека (ATCC CRL-1420) (1,0×107 в 0,2 мл) инъецируют подкожно в правый бок экспериментальных мышей. При достижении объемов опухолей ~80-150 мм3 (приблизительно через 8-10 дней после имплантации), животных случайным образом разбивают на группы по восемь особей, и начинают проводить введения дозы испытуемых соединений и/или среды (обозначается как день 1). Испытуемые соединения вводят, как подробно описано в разделе "Дизайн клинического исследования" (таблица 50). Объемы опухолей и массы тел измеряют и регистрируют два раза в неделю в течение периода времени проведения исследования. Все животные находятся под постоянным наблюдением. Эксперимент прекращают, когда средняя величина объема опухоли в отрицательной контрольной группе достигает 2000 мм3 или через 28 дней, в зависимости от того, что наступит раньше.
Объем опухоли (мм3) рассчитывают по формуле для вытянутого эллипсоида: длина (мм) x [ширина (мм)]2×0,5. Ингибирование роста опухоли (%TGI) будет определяться два раза в неделю в течение периода дозирования по формуле: %TGI=(1 -[(T -T0)/(C -C0)]) x 100, где T=средний объем опухоли в подвергаемой обработке группе, T0=средний объем опухоли в подвергаемой обработке группе на момент начала исследования, C=средний объем опухоли в контрольной группе, и C0=средний объем опухоли в контрольной группе на момент начала исследования [Mohammed et al. 1998].
Все аспекты этого исследования, включая содержание животных, проведение экспериментов и захоронение животных, проводятся в полном соответствии с "Руководством по содержанию и использованию лабораторных животных" ("Guide for the Care и Use of Laboratory Animals: Eighth Edition" (2011)) в виварии для лабораторных животных, официально аккредитованном Международной ассоциацией по аттестации и аккредитации содержания лабораторных животных (AAALAC).
Таблица 51. Изменение объема опухоли в ксенотрансплантатной модели опухолевых клеток MIA PaCa-2 поджелудочной железы в качестве ответа на введение соединения 1 в чистом виде или в комбинации с гемцитабином.
Исследование ксенотрансплантата клеток MIA PaCa-2 опухоли поджелудочной железы
WO#1060729 (AB67928) Самки мышей линии nu/nu
(мг/кг)
(способ введения)
QWK x 3
IP
Q4D x 4
IP
QWK x 3
IP
+
гемцитабин
QWK x 3
IP
+
80 мг/кг
Q4D x 4
IP
Таблица 52. Изменение массы тела в ксенотрансплантатной модели опухолевых клеток MIA PaCa-2 поджелудочной железы в качестве ответа на введение соединения 1 в чистом виде или в комбинации с гемцитабином.
Исследование # 581500 ксенотрансплантата клеток MIA PaCa-2 опухоли поджелудочной железы
WO#1060729 (AB67928) Самки мышей линии nu/nu
(мг/кг)
(способ введения)
1
4
8
11
15
QWK x 3
IP
Q4D x 4
IP
QWK x 3
IP
+
гемцитабин
QWK x 3
IP
+
80 мг/кг
Q4D x 4
IP
Для специалистов в этой области является очевидным, что могут быть предложены многочисленные варианты и/или модификации изобретения, которое представлено конкретными вариантами осуществления, без отклонения от объема подробно описанного изобретения. Поэтому, со всех точек зрения следует считать, что настоящие варианты осуществления являются иллюстрациями и не ограничивают объем изобретения.
Цитируемая литература
Ghisalberti EL (1994) The phytochemistry of the Myoporaceae. Phytochemistry, 35: 7-33.
Davis RA, Caroll AR, Pierens GK (1999). New lamellarin alkaloids from the Australian ascidian, Didemnum chartaceum. J. Nat. Prod., 62(3), 419-24.
Ullman EF, Kirakossian H, Singh S, Wu ZP, Irvin BR, Pease JS, Switchenko AC, Irvine JD, Dafforn A, Skold CN (1994) Luminescent oxygen channeling immunoassay: Measurement of particle binding kinetics by chemiluminescence. Proc. Natl. Acad. Sci. USA Vol. 91, 5426-5430.
Ma H, Deacon S, Horiuchi K (2008). The challenge of selecting protein kinase assays for lead discovery optimization. Expert Opin Drug Discov. 3(6): 607-621.
Filippakopoulos, P., Picaud S, Mangos M, Keates T, Lambert JP, Barsyte-Lovejoy D, Felletar I, Volkmer R, Müller S, Pawson T, Gingras AC, Arrowsmith CH, Knapp S. (2012) Histone recognition and large-scale structural analysis of the human bromodomain family. Cell, 149(1): 214-31.
Filippakopoulos, P. and S. Knapp (2012) The bromodomain interaction module. FEBS Lett, 586(17): 2692-704.
Philpott, M., Yang J, Tumber T, Fedorov O, Uttarkar S, Filippakopoulos P, Picaud S, Keates T, Felletar I, Ciulli A, Knapp S, Heightman TD (2011) Bromodomain-peptide displacement assays for interactome mapping and inhibitor discovery. Mol Biosyst, 7(10): 2899-908.
Kaustov, L., Ouyang H, Amaya M, Lemak A, Nady N, Duan S, Wasney GA, Li Z, Vedadi M, Schapira M, Min J, Arrowsmith CH (2011) Recognition and specificity determinants of the human cbx chromodomains. J Biol Chem 286(1): 521-9.
Kim, J., Daniel J, Espejo A, Lake A, Krishna M, Xia L, Zhang Y, Bedford MT (2006) Tudor, MBT and chromo domains gauge the degree of lysine methylation. EMBO Rep, 7(4): 397-403.
Org, T., Chignola F, Hetényi C, Gaetani M, Rebane A, Liiv I, Maran U, Mollica L, Bottomley MJ, Musco G, Peterson P (2008) The autoimmune regulator PHD finger binds to non-methylated histone H3K4 to activate gene expression. EMBO Rep, 9(4): 370-6.
Venturini, L., You J, Stadler M, Galien R, Lallemand V, Koken MH, Mattei MG, Ganser A, Chambon P, Losson R, de Thé H. (1999) TIF1gamma, a novel member of the transcriptional intermediary factor 1 family. Oncogene, 18(5): 1209-17.
Xie, S., J. Jakoncic, and C. Qian (2012) UHRF1 double tudor domain and the adjacent PHD finger act together to recognize K9me3-containing histone H3 tail. J Mol Biol, 415(2): 318-28.
Adams-Cioaba, M.A., Li Z, Tempel W, Guo Y, Bian C, Li Y, Lam R, Min J. (2012) Crystal structures of the Tudor domains of human PHF20 reveal novel structural variations on the Royal Family of proteins. FEBS Lett, 586(6): 859-65.
Hayashi-Takanaka Y, Yamagata K, Wakayama T, Stasevich TJ, Kainuma T, Tsurimoto T, Tachibana M, Shinkai Y, Kurumizaka H, Nozaki N, Kimura H (2011) Nucleic Acids Res. 39(15): 6475-88.
Kubicek, S. et al. (2007), Mol.Cell. 25:473-481.
Ken-ichi Noma and Shiv I. S. Grewal (2002), Proc Natl Acad Sci U S A. December 10; 99 (Suppl 4): 16438-16445.
Rotili, D. and Mai, A. (2011), Genes & Cancer, 2: 663-679.
Chowdhury, R. et al. (2011), Eur. Mol. Biol. Org., 12: 463-469.
Nottke, A. et al. (2009), Development, 136:879-889.
Kristensen, L.H. et al. (2012), FEBS Journal, 279:1905-1914.
Heightman T. D. (2011), Current Chemical Genomics, 5: 62-71.
King O.N.F. et al. (2010), PLoS ONE, 5:1-12.
Hong, S. et al. (2007), PNAS., 104:18439-18444.
Pradhan, S. et al. (1999), J. Biol. Chem., 274: 33002-33010.
Suetake I, Shinozaki F, Miyagawa J, Takeshima H, Tajima S. (2004), J Biol Chem. 279(26): 27816-23.
Aoki, A. et al. (2001), Nucleic. Acids. Res., 29: 3506-3512.
Zhang, H. et al. (2012), J Biol Chem., 287(9):6573-81.
Strahl, B.D. and C.D Allis (2000) The language of covalent histone modifications. Nature, 403(6765): 41-5.
Michan, S. and Sinclair, D. (2007), Biochem. J., 404: 1-13.
Michishita, E. et al. (2008), Nature, 452, 492-496.
Kim, W. and Kim, J.E. (2013), J. Physiol.Pharmacol., 64(5):531-534.
An S1, Yeo KJ, Jeon YH, Song JJ. (2011), J Biol Chem. 286(10): 8369-74.
Yost, J.M. et al. (2011), Curr. Chem. Genomics, 5: 72-84.
Shen, X, Liu, Y. et al. (2008), Mol. Cell., 32: 491-502
Nayak, V. et al. (2011), Nucleus, 1:2.
Jiang H1, Lu X, Shimada M, Dou Y, Tang Z, Roeder RG. (2013), Nat Struct Mol Biol., 10:1156-63.
Ali M1, Hom RA1, Blakeslee W1, Ikenouye L1, Kutateladze TG2. (2014), Biochim Biophys Acta. ;1843(2):366-71.
Allali-Hassani A1, Kuznetsova E1, Hajian T1, Wu H1, Dombrovski L1, Li Y1, Gräslund S1, Arrowsmith CH2, Schapira M3, Vedadi M4.(2014), J Biomol Screen.; 19 (6):928-935.
Selvi B.R. et al. (2010), Biochim Biophys Acta., 1799(10-12): 810-28.
Munoz-Fuentes, V. et al. (2011), PLoS ONE, 6: 1-7.
Cheng, D. et al. (2004), J. Biol. Chem., 279: 23892-23899.
Li, K.K. et al. (2012), Med Res Rev. 32(4):815-67.
Selvi, B. R. et al. (2010), J. Biol. Chem., 285: 7143-7152.
Yost, J.M. et al. (2011), Curr. Chem. Genomics, 5: 72-84.
Iberg, A.N. et al. (2007), J. Biol. Chem., 283: 3006-3010.
Zurita-Lopez CI1, Sandberg T, Kelly R, Clarke SG. (2012), J Biol Chem. 287(11):7859-70.
Lee, J. et al. (2005), The journal of biological chemistry, vol. 280, 38: 32890-32896.
Du, H.-N. et al. (2008), Gene Dev., 22: 2786-2798
Schultz, D.C. et al. (2002), Genes Dev., 16: 919-932.
Kang, H.B. et al. (2009), FEBS LETT 583: 1880-1886.
Sabbattini P, Canzonetta C, Sjoberg M, Nikic S, Georgiou A, Kemball-Cook G, Auner HW, Dillon N. (2007), EMBO J. 26(22):4657-69.
Preuss U, Landsberg G, Scheidtmann KH. (2003), Nucleic Acids Res., 31(3):878-85.
Han A, Lee KH, Hyun S, Lee NJ, Lee SJ, Hwang H, Yu J. (2011), Bioorg Med Chem., 19(7):2373-7.
Baek SH. (2011), Mol Cell., 42(3):274-84
Barnett, S.F. et al. (2005), Biochem. J., 385: 399-408.
Misaghi, S. et al. (2009), Mol. Cell. Biol. 29: 2181-2192.
Horton, R.A. et al. (2007), Anal. Biochem., 360:138-143.
Hu, M. et al. (2005), The EMBO Journal 24, 3747-3756.
Ye Y. et al. (2011), EMBO reports, 12: 350-357.
Tian, X. et al. (2011), Assay and Drug Dev. Technol., 9:165-173.
Arrowsmith CH, Bountra C, Fish PV, Lee K, Schapira M (2012) Epigenetic protein families: a new frontier for drug discovery. Nature Reviews Drug Discovery, 11, 384-400.
Plass C, Pfister SM, Lindroth AM, Bogatyrova O, Claus R and Lichter P. (2013). Mutations in regulators of the epigenome and their connections to global chromatin patterns in cancer. Nature Reviews Genetics 14: 765-780.
Taverna SD, Li H, Ruthenburg AJ, Allis CD, Patel DJ. (2007) How chromatin-binding modules interpret histone modifications: lessons from professional pocket pickers Nature Structural & Molecular Biology 14, 1025-1040.
Prinjha RK, Witherington J, Lee K. (2012) Place your BETs: the therapeutic potential of bromodomains Trends in Pharmacological Sciences 33, 3, 146-153.
Biggar KL, Li SS-C. (2015) Non-histone protein methylation as a regulator of cellular signalling and function. Nature Rev Mol Cell Biol, 16, 5-17.
Tough DF, Lewis HD, Rioja I, Lindon MJ, Prinjha RK (2014). Epigenetic pathways targets for the treatment of disease: accelerating progress in the development of pharmacological tools: IUPHAR Review 11. Br J Pharmacol 171: 4981-5010
Ciceri P, Müller S, O'Mahony A, Fedorov O, Filippakopoulos P, Hunt JP, Lasater EA, Pallares G, Picaud S, Wells C, Martin S, Wodicka LM, Shah NP, Treiber DK, Knapp S (2014) Dual kinase-bromodomain inhibitors for rationally designed polypharmacology. Nature Chemical Biology, 10, 305-312.
Fu L, Tian M, Li X, Li J-J, Huang J L, Zhang Y, Liu B. (2015). Inhibition of BET bromodomains as a therapeutic strategy for cancer drug discovery. Oncotarget. 2015 Mar 20; 6(8): 5501-5516.
Ciro M, Prosperini E, Quarto M, Grazini U, Walfridsson J, McBlane F, Nucifero P, Pacchiana G, Capra M, Christensen J, Helin K. (2009) ATAD2 is a novel cofactor for MYC, overexpressed and amplified in aggressive tumors. Cancer Res., 69: 8491-8498.
Krakstad C, Tangen IL, Hoivik EA, Halle MK, Berg A, Werner HM, Salvesen, HB. (2015) ATAD2 overexpression links to enrichment of B-MYB-translational signatures and development of aggressive endometrial carcinoma. Oncotarget, 6: 28440-28452.
Weidner-Glunde M, Ottinger M, Schulz TF. (2010) WHAT do viruses BET on? Front Biosci. 15: 537-549.
Blus BJ, Wiggins K, S. (2011) Epigenetic virtues of chromodomains. Critical Reviews in Biochemistry and Molecular Biology. 46, 6, 507-526
Cyr AR, Dormann FE. The redox basis of epigenetic modifications: from mechanism to functional consequences. (2011) Antioxidant & Redox Signaling, 15(2), 551-589.
Copeland RA, Solomon ME, Richon VM. (2009) Protein methyl transferase as a target class for drug discovery. Nat. Rev. Drug Discovery, 8, 724-732.
Shankar RS, Bahirvani AG, Rao VK, Bharathy N, Ow JR, Taneja R. (2013) G9a a multipotent regulator of gene expression. Epigenetics, 8:1, 16-22.
Casciello F, Winloch K, Gannon F, Lee JS. (2015) Functional role of G9a histone methyltransferase in cancer. Front. Immunol., 6:487-498.
Fuhrmann J, Clancy KW, Thompson PR. (2015) Chemical biology of protein arginine modifications in epigenetic regulation. Chem Rev., 115, 5413-5461.
Højfelt JW, Agger K, Helin K. (2013) Histone lysine demethylases as targets for anticancer therapy. Nat. Rev. Drug Discov. 917.
Xiang Y, Zhu Z, Han G, Ye X, Xu B, Peng Z et al. (2007). JARID1B is a histone H3 lysine 4 demethylase up-regulated in prostate cancer. Proc Natl Acad Sci USA 104: 19226-19231.
Couvelard A, Deschamps L, Rebours V, Sauvanet A, Gatter K, Pezzella F et al. (2008). Overexpression of the oxygen sensors PHD-1, PHD-2, PHD-3, and FIH is associated with tumor aggressiveness in pancreatic endocrine tumors. Clin Cancer Res 14: 6634-6639.
Roesch A, Fukunaga-Kalabis M, Schmidt EC, Zabierowski SE, Brafford PA, Vultur A et al. (2010). A temporarily distinct subpopulation of slow-cycling melanoma cells is required for continuous tumor growth. Cell 141: 583-594.
He J, Nguyen AT, Zhang Y (2011). KDM2b/JHDM1b, an H3K36me2-specific demethylase, is required for initiation and maintenance of acute myeloid leukemia. Blood 117: 3869-3880.
Berry WL, Janknecht R (2013). KDM4/JMJD2 histone demethylases: epigenetic regulators in cancer cells. Cancer Res 73: 2936-2942.
Kogure M, Takawa M, Cho H-S, Toyokawa G, Hayashi K, Tsunoda T et al. (2013). Deregulation of the histone demethylase JMJD2A is involved in human carcinogenesis through regulation of the G1/S transition. Cancer Lett 336: 76-84.
Tzatsos A, Paskaleva P, Ferrari F, Deshpande V, Stoykova S, Contino G et al. (2013). KDM2B promotes pancreatic cancer via polycomb dependent and -independent transcriptional programs. J Clin Invest 123: 727-739.
Adcock IM, Lee KY (2006). Abnormal histone acetylase and deacetylase expression and function in lung inflammation. Inflamm Res 55: 311-321.
Avvakumov N, Cote J (2007). The MYST family of histone acetyltransferases and their intimate links to cancer. Oncogene 26: 5395-5407.
Grabiec A, Tak P, Reedquist K (2008). Targeting histone deacetylase activity in rheumatoid arthritis and asthma as prototypes of inflammatory disease: should we keep our HATs on? Arthritis Res Ther 10: 226.
Ghizzoni M, Haisma HJ, Maarsingh H, Dekker FJ (2011). Histone acetyltransferases are crucial regulators in NF-kB mediated inflammation. Drug Discov Today 16: 504-511.
Iyer A, Fairlie DP, Brown L (2011). Lysine acetylation in obesity, diabetes and metabolic disease. Immunol Cell Biol 90: 39-46.
Pirooznia SK and Elefant F (2013). Targeting specific HATs for neurodegenerative disease treatment: translating basic biology to therapeutic possibilities. Front Cell Neurosci 7: 30.
Lee, S., et al., (2001) Combined angiotensin converting enzyme inhibition and angiotensin AT(1) receptor blockade up-regulates myocardial AT(2) receptors in remodeled myocardium post-infarction. Cardiovasc Res, 51(1): 131-9.
Rubin, B., Laffan RJ, Kotler DG, O'Keefe EH, Demaio DA, Goldberg ME (1978) SQ 14,225 (D-3-mercapto-2-methylpropanoyl-l-proline), a novel orally active inhibitor of angiotensin I-converting enzyme. J Pharmacol Exp Ther, 204(2): 271-80.
Bunning, P., B. Holmquist, and J.F. Riordan, Substrate specificity and kinetic characteristics of angiotensin converting enzyme. Biochemistry, 1983. 22(1): p. 103-10.
Hesselgesser, J., et al., Identification and characterization of small molecule functional antagonists of the CCR1 chemokine receptor. J Biol Chem, 1998. 273(25): p. 15687-92.
Gong, X., Gong W, Kuhns DB, Ben-Baruch A, Howard OM, Wang JM (1997) Monocyte chemotactic protein-2 (MCP-2) uses CCR1 and CCR2B as its functional receptors. J Biol Chem, 272(18): 11682-5.
Combadiere, C., Salzwedel K, Smith ED, Tiffany HL, Berger EA, Murphy PM (1998) Identification of CX3CR1. A chemotactic receptor for the human CX3C chemokine fractalkine and a fusion coreceptor for HIV-1. J Biol Chem, 273(37): 23799-804.
Grob, P.M., David E, Warren TC, DeLeon RP, Farina PR, Homon CA. (1990) Characterization of a receptor for human monocyte-derived neutrophil chemotactic factor/interleukin-8. J Biol Chem, 265(14): 8311-6.
Ahuja, S.K. and P.M. Murphy (1996) The CXC chemokines growth-regulated oncogene (GRO) alpha, GRObeta, GROgamma, neutrophil-activating peptide-2, and epithelial cell-derived neutrophil-activating peptide-78 are potent agonists for the type B, but not the type A, human interleukin-8 receptor. J Biol Chem, 271(34): 20545-50.
Valenzuela-Fernandez, A., Planchenault T, Baleux F, Staropoli I, Le-Barillec K, Leduc D, Delaunay T, Lazarini F, Virelizier JL, Chignard M, Pidard D, Arenzana-Seisdedos F. (2002) Leukocyte elastase negatively regulates Stromal cell-derived factor-1 (SDF-1)/CXCR4 binding and functions by amino-terminal processing of SDF-1 and CXCR4. J Biol Chem, 277(18): 15677-89.
Dittadi, R., et al., Radioligand binding assay of epidermal growth factor receptor: causes of variability and standardization of the assay. Clin Chem, 1990. 36(6): p. 849-54.
Muller-Enoch, D., E. Seidl, and H. Thomas, [6.7-Dihydroxycoumarin (Aesculetin) as a substrate for catechol-o-methyltransferase (author's transl)]. Z Naturforsch C, 1976. 31(5-6): 280-4.
Tietge, U.J., Pratico D, Ding T, Funk CD, Hildebrand RB, Van Berkel T, Van Eck M. (2005). Macrophage-specific expression of group IIA sPLA2 results in accelerated atherogenesis by increasing oxidative stress. J Lipid Res, 46(8): 1604-14.
Montalibet, J., K.I. Skorey, and B.P. Kennedy (2005) Protein tyrosine phosphatase: enzymatic assays. Methods 35(1): 2-8.
Sun, Z.Y. and Z.H. Tu, A novel in vitro model to screen steroid 5 alpha-reductase inhibitors against benign prostatic hyperplasia. Methods Find Exp Clin Pharmacol, 1998. 20(4): p. 283-7.
Becker, K., Gromer, S., Schirmer, R.H., Müller, S. (2000) Thioredoxin reductase as a pathophysiological factor and drug target. Eur J Biochem, 267(20): 6118-25.
Hatano, T., et al. (1990). Effects of interaction of tannins with co-existing substances. VII. Inhibitory effects of tannins and related polyphenols on xanthine oxidase. Chem Pharm Bull (Tokyo), 38(5): 1224-9.
De Backer et al., (1993). Genomic cloning, heterologous expression and pharmacological characterization of a human histamine H1 receptor. Biochem Biophys Res Commun 197(3): 1601-1608.
Ruat et al., (1990). Reversible and irreversible labeling and autoradiographic localization of the cerebral histamine H2 receptor using [125I]iodinated probes. Proc Natl Acad Sci USA. 87(5): 1658-1662.
Krueger et al., (2005). G protein-dependent pharmacology of histamine H3 receptor ligands: evidence for heterogeneous active state receptor conformations. J Pharmacol Exp Ther. 314(1): 271-281.
Liu et al., (2001). Comparison of human, mouse, rat, and guinea pig histamine H4 receptors reveals substantial pharmacological species variation. J Pharmacol Exp Ther. 299(1): 121-130.
Kubo and Strott, (1987). Differential activity of 3-hydroxy-3-methylglutaryl coenzyme A reductase in zones of the adrenal cortex. Endocrinology. 120:214-221.
Pufahl et al., (2007). Development of a fluorescence-based enzyme assay of human 5-lipoxygenase. Anal Biochem. 364(2): 204-212.
Mansuy et al., (1986). A new potent inhibitor of lipid peroxidation in vitro and in vivo, the hepatoprotective drug anisylditholthione. Biochem Biophys Res Comm. 135:1015-1021.
Romano et al., (1993). Lipoxin synthase activity of human platelet 12-lipoxygenase. Biochem J. 296: 127-133.
Urban et al., (1991). Comparative membrane locations and activities of human monoamine oxidases expressed in yeast. FEBS Lett. 286(1-2): 142-146.
Svensson et al., (1987). Peroxidase and peroxidase-oxidase activities of isolated human myeloperoxidase. Biochem J. 242:673-680.
Yamamoto et al., (2006). A nonradioisotope, enzymatic assay for 2-deoxyglucose uptake in L6 skeletal muscle cells cultured in a 96-well microplate. Anal Biochem. 351(1):139-45.
Cobb, R.R., et al.,(1992) Functional expression of soluble ICAM-1 by baculovirus-infected Sf9 cells. Biochem Biophys Res Commun, 185(3): 1022-33.
Stoltenborg, J.K., Tsao PW, George HJ, Bouchard PJ, Wexler EJ, Hausner EA (1994). A fluorescent cellular adhesion assay using insect cell produced human VCAM1. J Immunol Methods, 175(1): 59-68.
Lenardo, M.J. and D. Baltimore (1989) NF-kappa B: a pleiotropic mediator of inducible and tissue-specific gene control. Cell, 58(2): 227-9.
Sen R., Baltimore D. (1986). Multiple nuclear factors interact with immunoglobulin enhancer sequences. Cell, 46, 705-716.
Pantano C., Reynaert N.L., van der Vliet A.V., Janssen-Heininger Y.M.W. (2006). Redox-sensitive kinasesof the nuclear factor κB signalling pathway. Antioxidants & Redox Signaling 8(9-10), 1791-1807.
Brigelius-Flohê R., Flohê L. (2011). Basic principle and emerging concepts in redox control of transcription factors. Antioxidants & Redox Signaling, 15(8), 2335-2380.
Ghosh G., Wang V.Y-F., Huang D-B., Fusco A. (2015). NF-κB regulation: lessons from structures. Immunol. Rev. 246(1), 36-58.
Akdis M., Aab A., Altunbulakli C., Azkur K., Costa R.A., Crameri R., Duan S., Eiwegger T., Eljaszewicz A., Ferstl R., Frei R., Garbani M., Globinska A., Hess L., Huitema C., Kubo T., Komlosi Z., Konieczna P., Kovacs N., Kucuksezer U.C., Meyer N., Morita H., Olzhausen J., O'Mahony L., Perzer M., Prati M., Rabane A., Rhyner C., Rinaldi A., Sokolowska M., Stanic B., Sugita K., Treis A., van der Veen W., Wanke K., Wawrzyniak M., Wawrzyniak P., Wirz O.F., Zakzuk J.S, Akdis C.A. (2016). Interleukins (from IL-1 to IL-38), interferons, transforming growth factor β, and TNF-α: receptors, functions, and role in diseases. Fundamentals of allergy and Immunology, 138, 4, 984-1010.
Perkins N.D. (2012). The diverse and complex roles of NF-κB subunits in cancer. Nature Reviews Cancer, 12, 121-133.
Sethi G., Shanmugam M.K., Ramachandran L., Kumar A.P., Tergaonkar V. (2012). Multifacet link between cancer and inflammation. Biosci. Rep. 32, 1-15.
Parri M., Chiarugi P. (2013). Redox molecular machines involved in tumour progression. Antioxidants & Redox Signaling, 19(15), 1828-1846.
D'Ignazio L., Bandarra D., Rocha S. (2016). NF-κB cross talk in immune responses. FEBS Journal 283, 413-424.
Ludwig L.M., Nassin M.L., Hadji A., Labelle, J.L. (2016). Killing two cells with one stone: Pharmacologic BCL-2 family targeting for cancer cell death and immune modulation. Frontiers in Peadiatrics, Vol 4, Artcle 135, page 1-13.
Xia, M, Huang R, Witt KL, Southall N, Fostel J, Cho MH, Jadhav A, Smith CS, Inglese J, Portier CJ, Tice RR, Austin CP (2008) Compound cytotoxicity profiling using quantitative high-throughput screening. Environ Health Perspect. 116(3):284-91.
Fallahi-Sichani, M., S. Honardejad, L.M. Heiser, J.W. Gray, and P.K. Sorger (2013). Metrics other than potency reveal systematic variation in responses to cancer drugs. Nat. Chem. Biol. 9: 708-714.
Barretina, J., G. Caponigro, N. Stransky, K. Venkatesan, A.A. Margolin, et al. (2012). The Cancer Cell Line Encyclopedia enables predictive modelling of anticancer drug sensitivity. Nature 483: 603-607.
Dierks EA, Stams KR, Lim HK, Cornelius G, Zhang H, Ball SE (2001). A method for the simultaneous evaluation of the activities of seven major human drug-metabolizing
cytochrome P450s using an in vitro cocktail of probe substrates and fast gradient liquid chromatography tandem mass spectrometry. Drug Metab. Dispos., 29: 23-29.
Mohammad R.H., Dugan, M.C., Mohamed, A.N., Almatchy, V.P., Flake, T.M., Dergham, S.T., Shields, A.F., Al-Katib, A.A., Vaitkevicius, V.K. and Sarkar, F.H (1998). Establishment of a human pancreatic tumor xenograft model: Potential application for preclinical evaluation of novel therapeutic agents. Pancreas 16:19-25.
"Guide for the Care and Use of Laboratory Animals: Eighth Edition" (2011), The National Academies Press, Washington, DC.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ТРИЖДЫ НЕГАТИВНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ И РАКА ЯИЧНИКА | 2019 |
|
RU2776897C2 |
| ЦИАНОТИЕНОТРИАЗОЛОДИАЗЕПИНЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2750164C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2762111C1 |
| СЕЛЕКТИВНЫЕ И ОБРАТИМЫЕ ИНГИБИТОРЫ УБИХИТИН-СПЕЦИФИЧЕСКОЙ ПРОТЕАЗЫ 7 | 2012 |
|
RU2622640C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2609018C2 |
| КОМБИНАЦИОННАЯ ТЕРАПИЯ С ПРИМЕНЕНИЕМ ДИАРИЛЬНЫХ МАКРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 2018 |
|
RU2784853C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ C-C ХЕМОКИНОВОГО РЕЦЕПТОРА 4 (CCR4) И ОДНОГО ИЛИ БОЛЕЕ ИНГИБИТОРОВ КОНТРОЛЬНЫХ ТОЧЕК | 2019 |
|
RU2810717C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2015 |
|
RU2805949C2 |
| ПЕПТИДЫ ГЛЮКАГОНОВОГО СУПЕРСЕМЕЙСТВА, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ ОТНОСИТЕЛЬНО ЯДЕРНЫХ ГОРМОНАЛЬНЫХ РЕЦЕПТОРОВ | 2011 |
|
RU2604067C2 |
| ХИРАЛЬНЫЕ ДИАРИЛЬНЫЕ МАКРОЦИКЛЫ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2728579C2 |
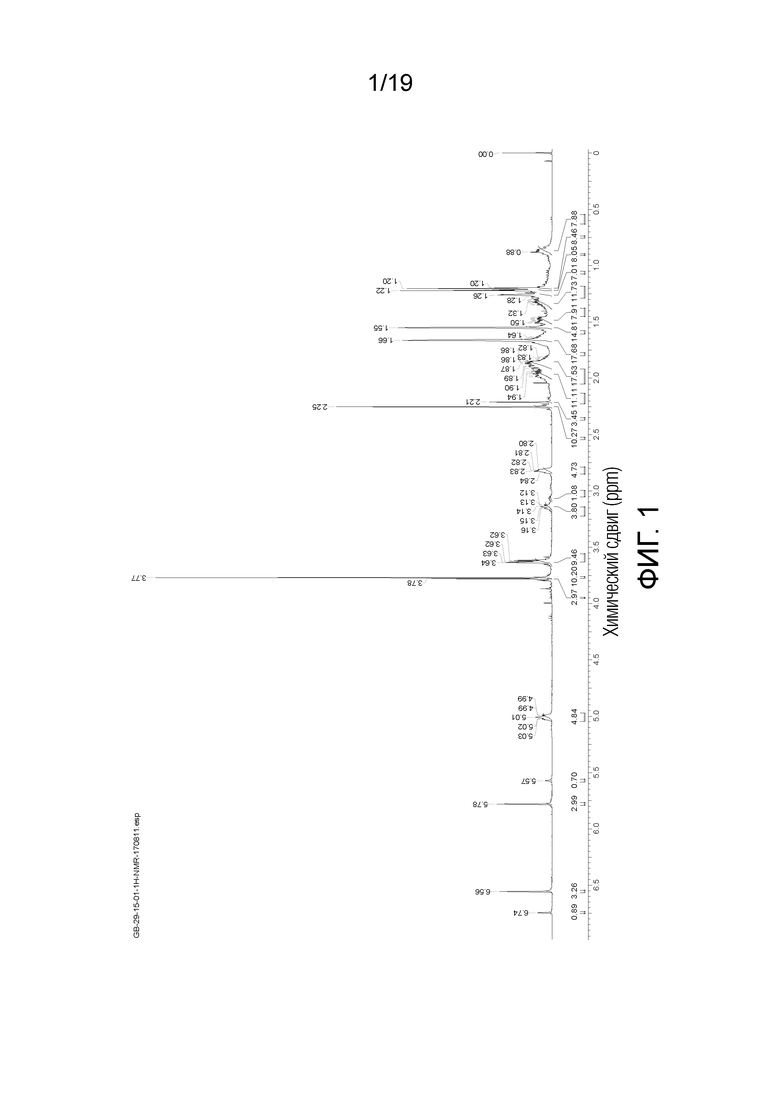

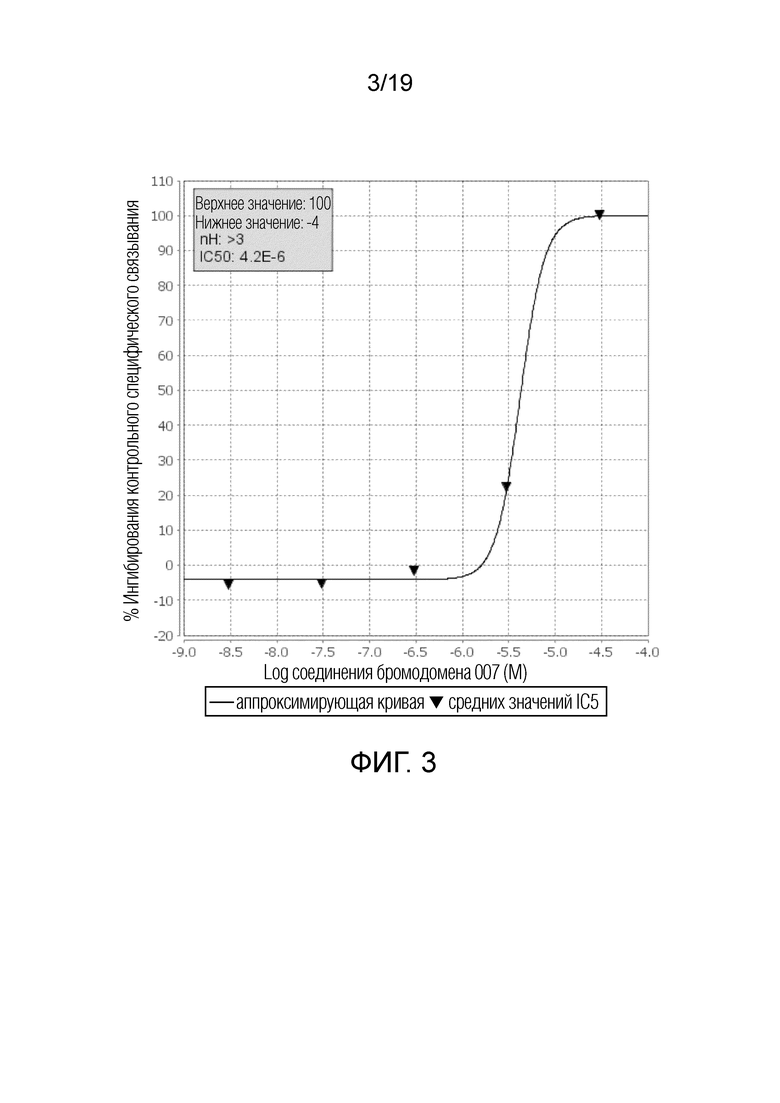
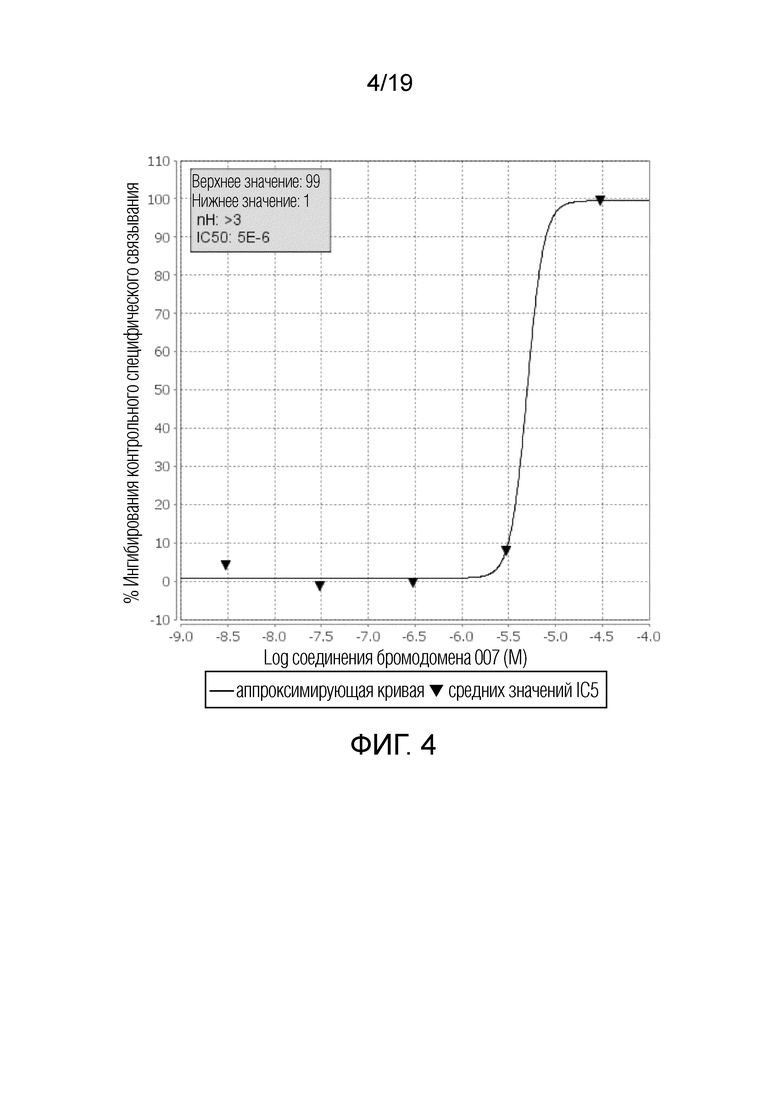
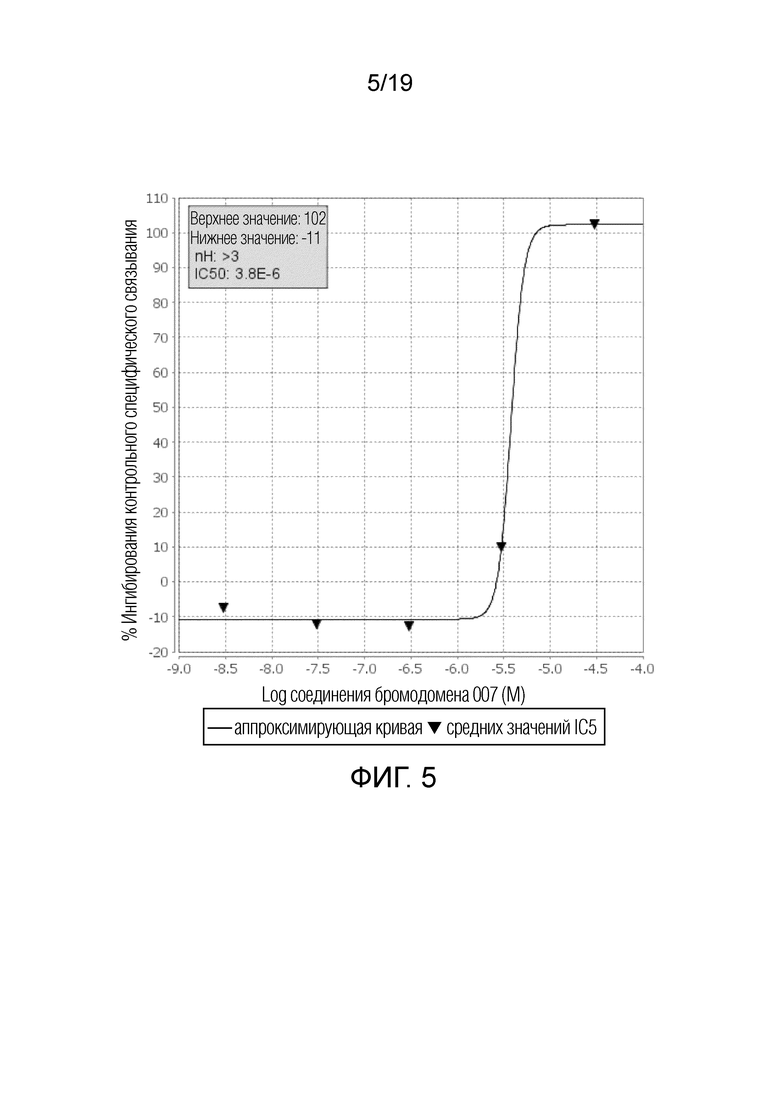
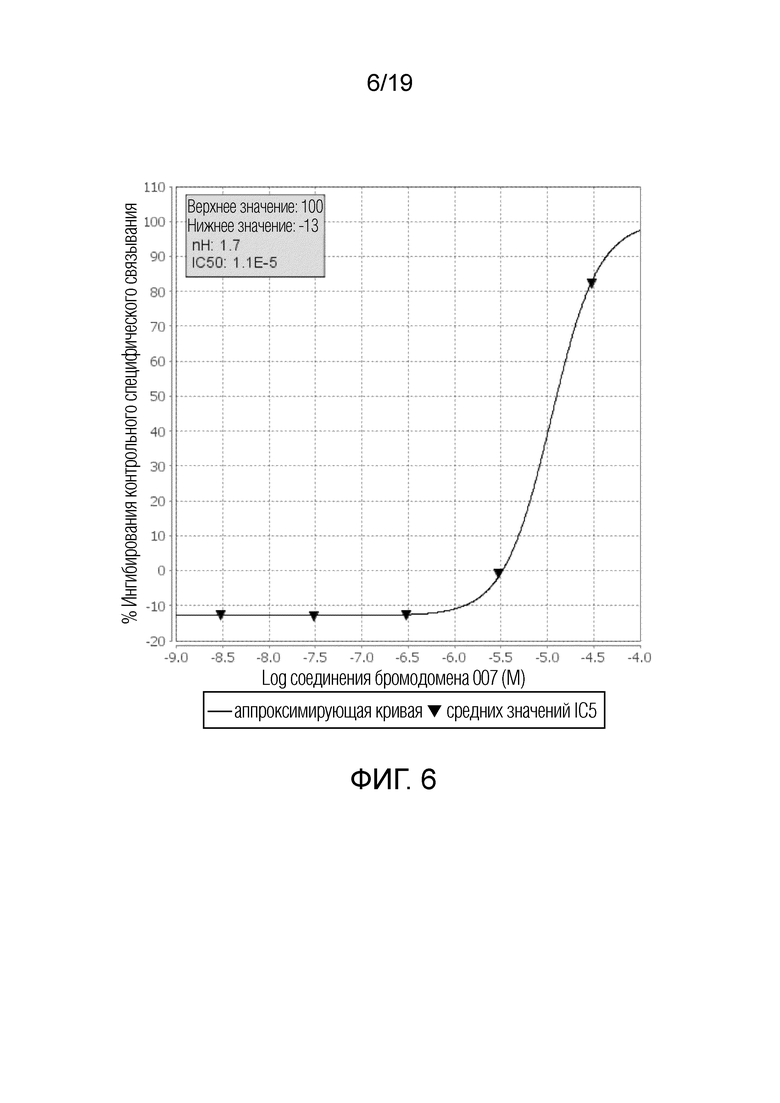
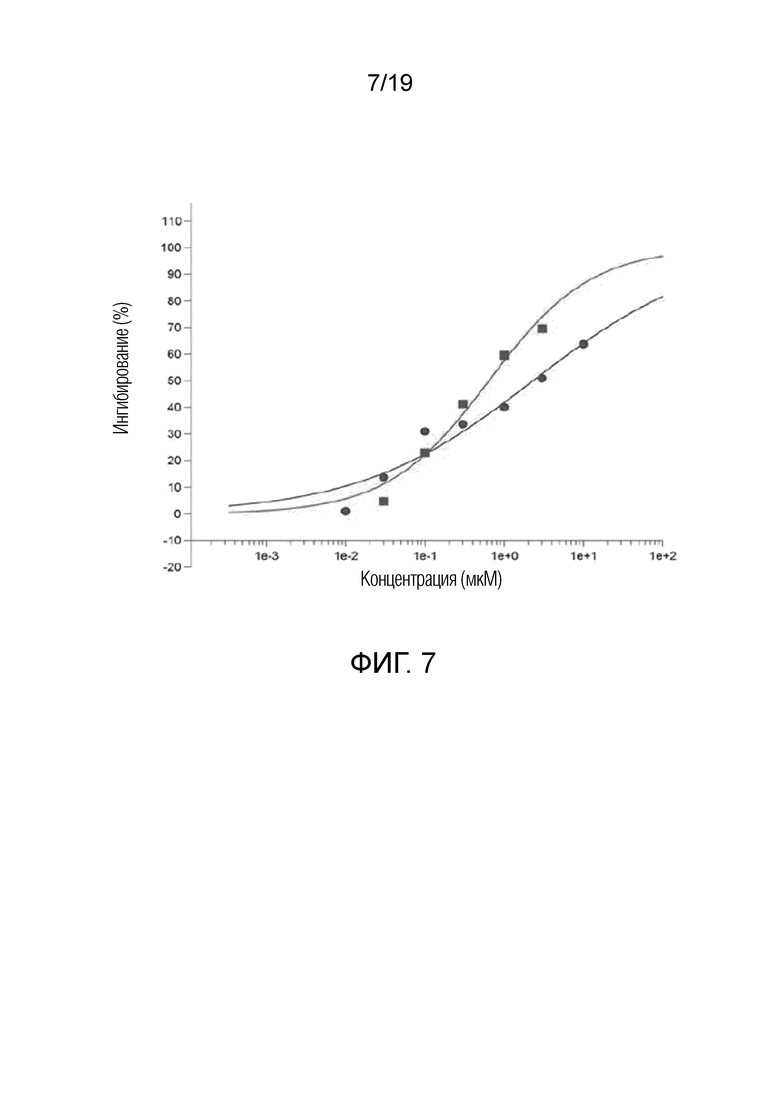
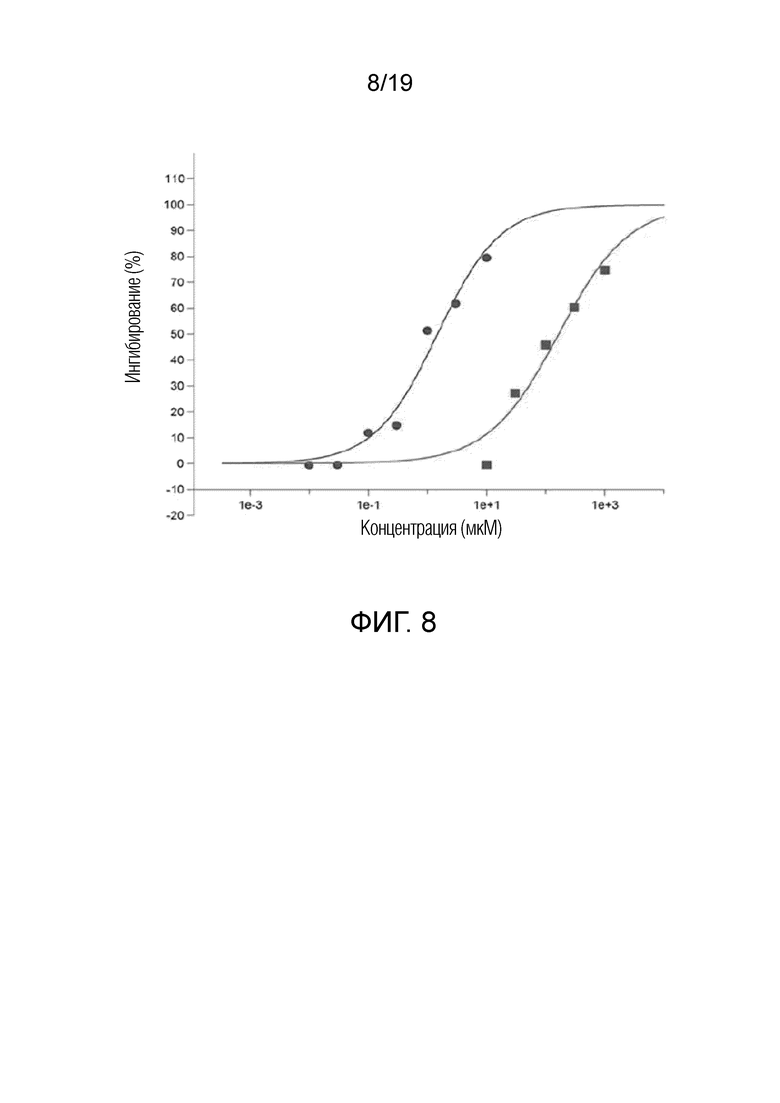





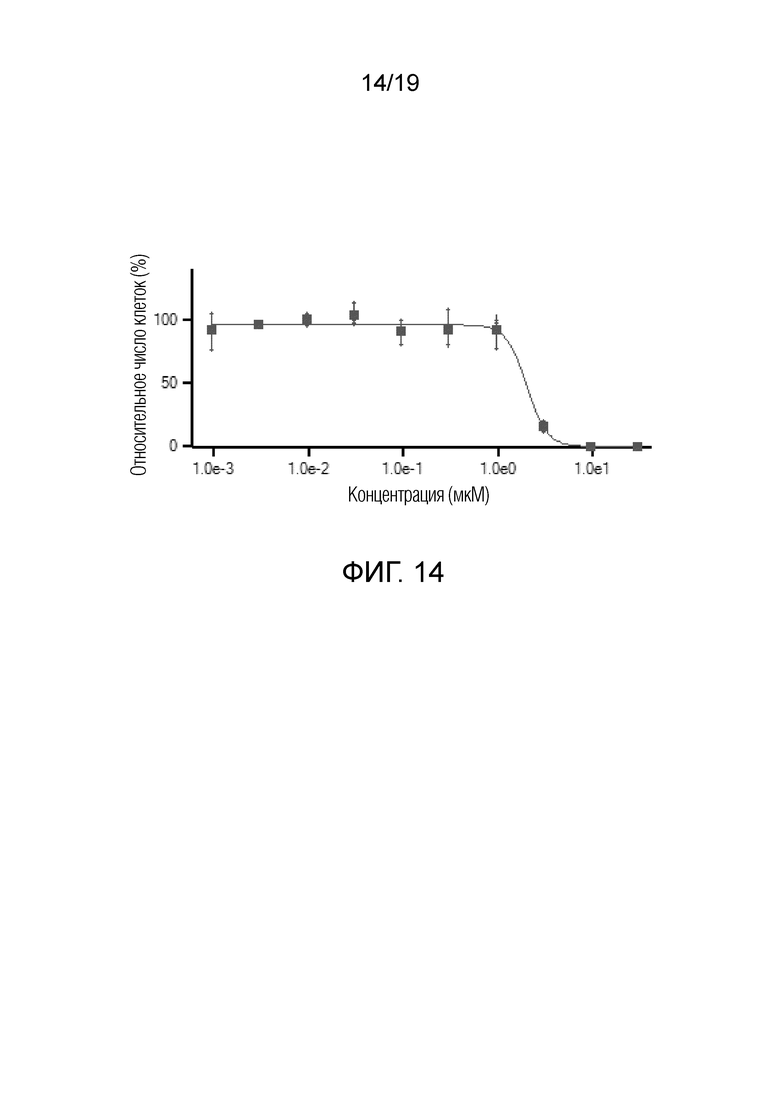
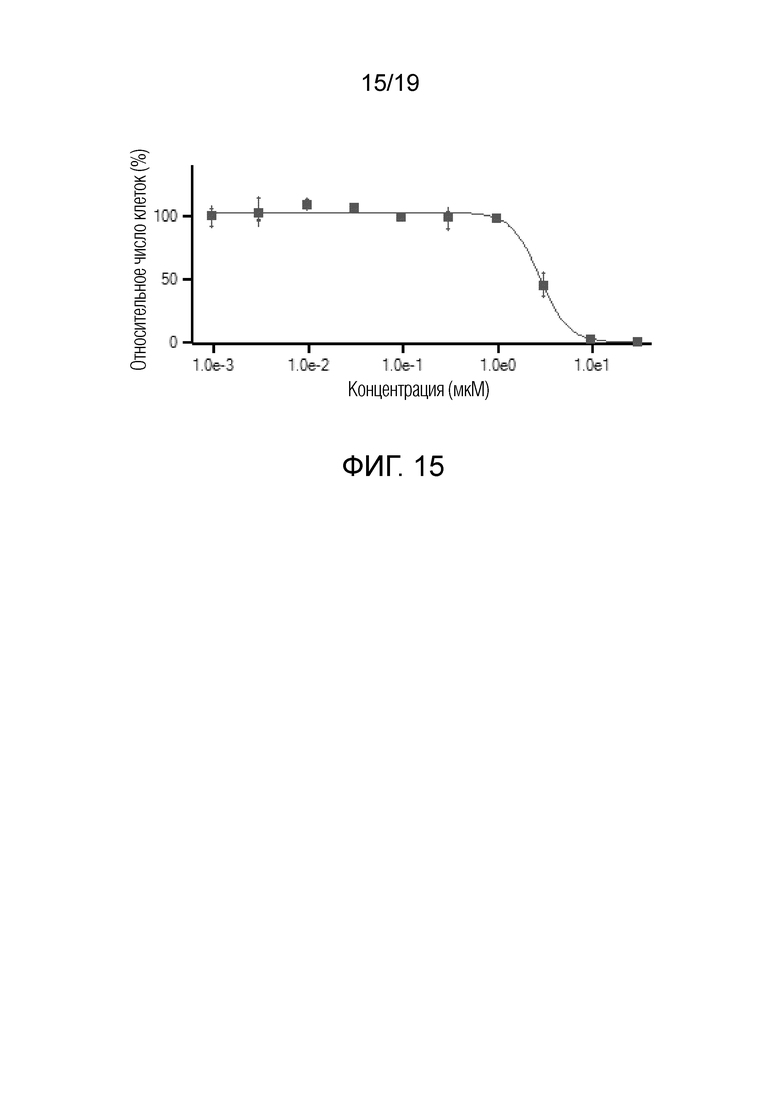




Изобретение относится к способу лечения рака, где способ включает введение терапевтически эффективного количества соединения формулы (I)

(I),
его фармацевтически приемлемой соли или сольвата, или фармацевтической композиции, включающей указанные соединения, субъекту, нуждающемуся в этом. В формуле (I): X представляет собой CH2; R1 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; R2 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; R3 представляет собой H; R4 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; и A---B обозначает CH=C или CH2-CH. Также предложены соединение формулы (I), его применение для лечения рака и кожного заболевания или нарушения, фармацевтическая композиция, включающая соединение формулы (I). Изобретение позволяет получить серрулатановые дитерпены формулы (I), которые могут применяться при лечении рака и кожного заболевания или нарушения. 13 н. и 23 з.п. ф-лы, 19 ил., 52 табл.
1. Способ лечения рака, где способ включает введение терапевтически эффективного количества соединения формулы (I)

(I),
его фармацевтически приемлемой соли или сольвата или фармацевтической композиции, включающей указанные соединения, субъекту, нуждающемуся в этом,
где в формуле (I):
X представляет собой CH2;
R1 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R2 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R3 представляет собой H;
R4 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
2. Способ по п. 1, где соединение представляет собой соединение формулы (Ic)

(Ic).
3. Способ по п. 1 или 2, где A---B обозначает CH=C.
4. Способ по любому одному из пп. 1-3, где соединение выбирают из группы, состоящей из
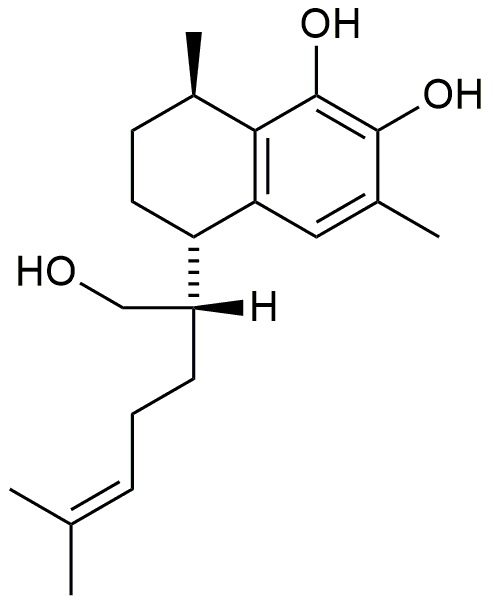 ,
,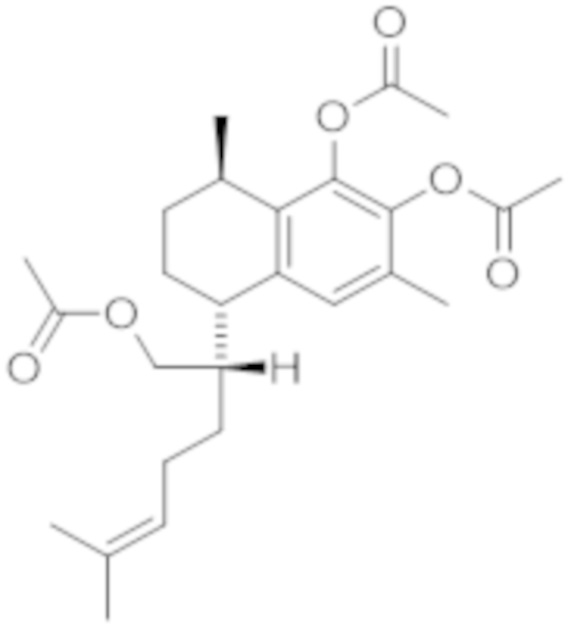 ,
,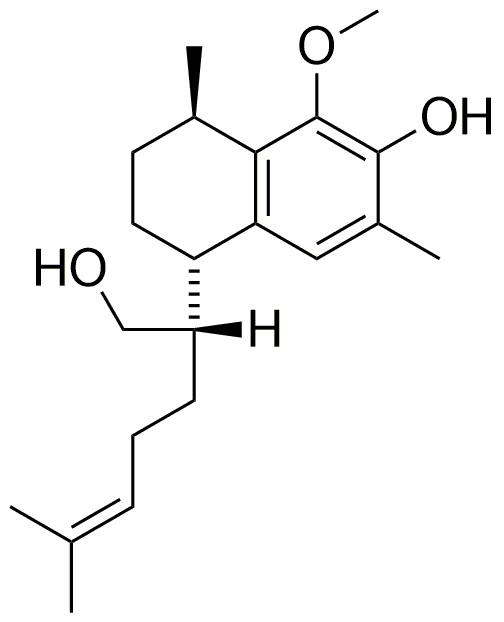 и
и  .
.
5. Способ по п. 4, где соединение представляет собой
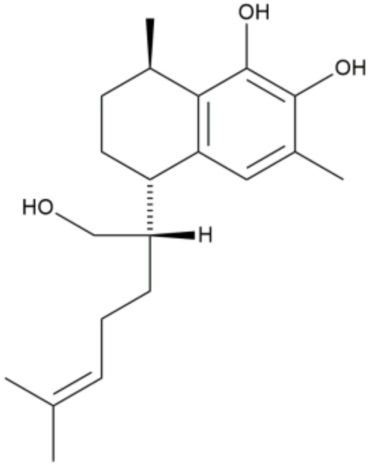 .
.
6. Способ по любому одному из пп. 1-5, где рак представляет собой рак мочевого пузыря, рак костей, рак головного мозга, рак молочной железы, рак центральной нервной системы, рак надпочечников, рак плаценты, рак яичек, рак шейки матки, рак толстой кишки, рак почки, рак головы и шеи, миелома, лейкоз, рак печени, рак легких, меланому, рак яичников, рак поджелудочной железы, рак предстательной железы, рак кожи, рак желудка, рак щитовидной железы, рак матки, карциному, лимфому, саркому, рак глаза, рак пищевода, рак желчного протока или рак вульвы.
7. Способ по п. 6, где рак центральной нервной системы выбран из группы, состоящей из глиомы, медуллобластомы и нейробластомы.
8. Способ по п. 6, где рак легких представляет собой немелкоклеточный рак легких или мелкоклеточный рак легких.
9. Способ по п. 6, где карцинома представляет собой аденосквамозную карциному или сквамозную карциному.
10. Способ по п. 6, где саркома представляет собой липосаркому, рабдомиосаркому, фибросаркому или саркому мягких тканей.
11. Способ по п. 6, где саркома мягких тканей представляет собой остеосаркому мягких тканей.
12. Способ по п. 6, где лимфома представляет собой лимфому Беркитта, лимфому Ходжкина или неходжкинскую лимфому.
13. Применение соединения формулы (I)

(I),
его фармацевтически приемлемой соли или сольвата,
где в формуле (I):
X представляет собой CH2;
R1 представляет собой OH, OC1-5алкил или OC4-5алкадиенил;
R2 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R3 представляет собой H;
R4 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH,
при приготовлении лекарственного препарата для лечения рака.
14. Применение соединения формулы (I)

(I),
его фармацевтически приемлемой соли или сольвата,
где X представляет собой CH2;
R1 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R2 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R3 представляет собой H;
R4 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH,
при лечении рака.
15. Соединение формулы (I)

(I),
его фармацевтически приемлемая соль или сольват,
где X представляет собой CH2;
R1 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R2 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил;
R3 представляет собой H;
R4 представляет собой OH, OC1-5алкил или OC(O)C1-5алкил; и
A---B обозначает CH=C или CH2-CH.
16. Соединение по п. 15, где соединение представляет собой соединение формулы (Ic)

(Ic).
17. Соединение по любому одному из пп. 15, 16, где A---B обозначает CH=C.
18. Соединение по любому одному из пп. 15-17, где соединение выбирают из группы, состоящей из
 ,
, ,
,  и
и  .
.
19. Выделенное соединение
 .
.
20. Фармацевтическая композиция для лечения рака, включающая терапевтически эффективное количество соединения, его фармацевтически приемлемой соли или сольвата по любому одному из пп. 15-19 и фармацевтически приемлемое вспомогательное вещество.
21. Фармацевтическая композиция для лечения кожного заболевания или нарушения, включающая терапевтически эффективное количество соединения, его фармацевтически приемлемой соли или сольвата по любому одному из пп. 15-19 или их смесь и фармацевтически приемлемое вспомогательное вещество.
22. Соединение по любому одному из пп. 15-19 для применения в качестве лекарственного средства для лечения рака.
23. Соединение по любому одному из пп. 15-19 для применения в качестве лекарственного средства для лечения кожного заболевания или нарушения.
24. Соединение по любому одному из пп. 15-19, выделенное из прополиса, где прополис образуется из растений рода Myoporum.
25. Соединение по п. 24, где прополис образуется из растения Myoporum insulare.
26. Соединение по любому одному из пп. 15-19, выделенное из смолы, камеди или экссудата растения рода Myoporum.
27. Соединение по п. 26, выделенное из смолы, камеди или экссудата растения Myoporum insulare.
28. Способ лечения рака, где способ включает введение терапевтически эффективного количества соединения по любому одному из пп. 15-19 или композиции по п. 20.
29. Способ лечения кожного заболевания или нарушения, где способ включает введение терапевтически эффективного количества соединения по любому одному из пп. 15-19 или композиции по п. 21.
30. Способ по п. 29, где кожное заболевание или нарушение выбирают из группы, состоящей из экземы, псориаза, акне, рубца, воспаления, ожога, солнечного ожога, повреждения кожи и раздражения кожи.
31. Применение соединения по любому одному из пп. 15-19 при приготовлении лекарственного средства для лечения рака.
32. Применение соединения по любому одному из пп. 15-19 при приготовлении лекарственного средства для лечения кожного заболевания или нарушения.
33. Применение по п. 32, где кожное заболевание или нарушение выбирают из группы, состоящей из экземы, псориаза, акне, рубца, воспаления, ожога, солнечного ожога, повреждения кожи и раздражения кожи.
34. Применение соединения по любому одному из пп. 15-19 или композиции по п. 20 при лечении рака.
35. Применение соединения по любому одному из пп. 15-19 или композиции по п. 21 при лечении кожного заболевания или нарушения.
36. Применение по п. 35, где кожное заболевание или нарушение выбирают из группы, состоящей из экземы, псориаза, акне, рубца, воспаления, ожога, солнечного ожога, повреждения кожи и раздражения кожи.
| US 20020091093 A1, 11.07.2002 | |||
| RODRIGUES I.I | |||
| et al., New pseudopterosin and seco-pceudopterosin diterpene glycosides from two Colombian isolates of Pseudopterogorgia elisabethae and their diverse biological activities, Journal of Natural Products, 2004, v | |||
| Приспособление для получения кинематографических стерео снимков | 1919 |
|
SU67A1 |
| Автоматическое переключающее приспособление для паровозных инжекторов, работающих свежим и мятым паром | 1924 |
|
SU1672A1 |
| ABELL A.D | |||
| et al., The structure of a stable serrulatane | |||
Авторы
Даты
2021-12-21—Публикация
2017-09-07—Подача