Изобретение относится к медицине, а именно к онкологии, и может быть использовано в качестве средства, обладающего противоопухолевым действием и может быть использовано при производстве противоопухолевых лекарственных средств.
Злокачественные новообразования являются одной из главных проблем стоящей перед медициной в настоящее время. Ежегодно свыше 5 млн. человек в мире погибает от этой патологии. Вследствие этого актуальной задачей является поиск новых соединений, обладающих выраженным противоопухолевым действием.
В качестве ближайших аналогов по действию могут быть указаны такие производные хиназолина, являющиеся ингибиторами рецептора эпидермального фактора роста человека (РЭФР), как гефитиниб и эрлотиниб (см. Hu, M; Ye, W; Li, J; Zhong, G; He, G; Xu, Q; Zhang, Y Synthesis and evaluation of salicylanilide derivatives as potential epidermal growth factor receptor inhibitors. Chem. Biol. Drug Des. 85:280-9 (2015)). Молекулы данных препаратов связываются с активным центром рецептора-фермента тирозинкиназы РЭФР и ингибируют его, что приводит к подавлению роста некоторых раковых клеток.
В качестве ближайших аналогов по действию и по химической структуре могут быть указаны, такие антиметаболиты, как препараты фторурацил, фторофур и цитарабин (см. Граник В.Г. Основы медицинской химии. - М.: Вузовская книга, 2001 - 384 с.). Эти препараты в виде метаболитов внедряются в ДНК, что приводит к нарушению целостности её структуры и цитостатическому действию. В зарубежной литературе опубликованы работы, в которых сообщается о противоопухолевой активности конденсированных производных пиримидина проявляющих цитостатическое действие посредством ингибирования CDK2 (см. Srinivasulu Cherukupalli Synthesis, anticancer evalution, and molecular docking studies of some novel 4,6-disubstitutedpyrazolo[3,4-d]pyrimidinesascyclin-dependent kinase 2 (CDK2) inhibitors / Srinivasulu Cherukupalli, Balakumar Chandrasekaran, Vladimir Krystof [et all] - Bioorganic Chemistry 79 (2018) 46-59).
Среди ближайших аналогов по структуре производных пиримидин-4(1Н)-она, обнаружено немало соединений, обладающих психотропной (см. Срадомский В.В., Климонтова Е.С., Рябухин Ю.И. Молекулярные механизмы психотропного действия триметидона, Хим.-фармац. журн. - 1997. - Т. 28. - №1 - С. 9-10), противовоспалительной (см. Кодониди И.П., Новиков О.О., Кулешова С.А., Рябухин Ю.И., Шатохин С.С., Ивченко А.В., Кодониди М.И., Жилина О.М. Синтез новых n- гидроксифенильных и толильных производных пиримидин-4(1н)-она, обладающих противовоспалительной активностью. Фармация и фармакология. 2017. Т. 5. № 6. С. 556-567), антиоксидантной (см. Е.В. Петрова, Э.Т. Оганесян, И.П. Кодониди. Сравнительная антиоксидантная и антигипоксическая активность нового производного 1,4-дигидро-4-оксопиримидина - соединения PDMpT.HCl и мексидола. Экспериментальная и клиническая фармакология. - 2013. - №6. - С. 38-40) церебропротекторной активностью (см. Патент на изобретение RU 2711613, опубл.17.01.2020. Бюл. №2) и низкой токсичностью. Техническим результатом данного изобретения является создание новых производных лабданоидов (Iа, б), обладающих способностью к подавлению роста опухолевых клеток человека. Новые соединения получают путем химической модификации доступного растительного метаболита Pinus sibirica R. Mayr. - ламбертиановой кислоты (VI), которая легко выделяется из лесопромышленного продукта - кедровой живицы или из хвои кедра, являющейся многотоннажным отходом лесосеки (см. Толстикова Т.Г., Сорокина И.В., Долгих М.П., Харитонов Ю.В., Чернов С.В., Шульц Э.Э., Толстиков Г.А. Химико-фармацевтический журнал. - 2004. - Т. 38. - С. 13-15). Физико-химические константы новых, впервые полученных соединений приведены в примерах 1, 2.
Технический результат - создание нового эффективного средства с цитостатической активностью, обладающего противоопухолевым действием.
Технический результат достигается натриевой солью 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида формулы (I).
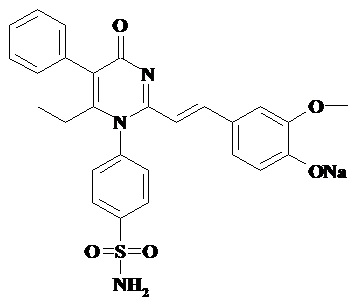 I
I
Способ получения натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида (I) основан на взаимодействии 4-(2-метил-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил)-бензсульфамида (II) с 4-гидрокси-3-метоксибензальдегидом в ледяной уксусной кислоте с дальнейшим переводом полученного продукта в его натриевую соль. Этот процесс осуществляется взаимодействием вещества (1) с метилатом натрия.
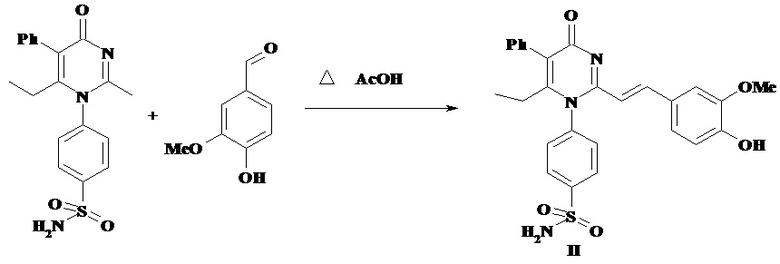
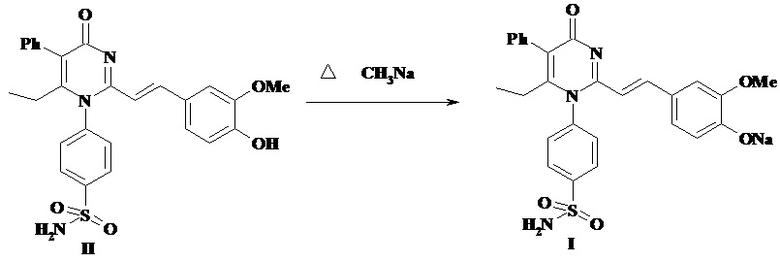
Новое соединение проявляет выраженную противоопухолевую активность.
Ниже приведен пример синтеза натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида.
Стадия 1
4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамид
Суспензию 3,69 г (0,01 моль) 4-(2-метил-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил)-бензсульфамида растворяют в 7 мл ледяной уксусной кислоты при нагревании. Затем добавляют 1,52 г (0,01 моль) 4-гидрокси-3-метоксибензальдегида и кипятят 3 часа. Выделяют 90 мл диэтилового эфира при охлаждении. Выход: 76% - 3,82 г. Вещество представляет собой желтый кристаллический порошок без запаха. Растворим в этаноле и пропаноле-2, нерастворим в диэтиловом эфире и воде. Температура плавления 201-202°С (из метанола). Rf = 0,78 (этанол).
УФ-спектр, λmax, нм: 202, 253, 362.
ИК-спектр, ν, см-1: 3416, 3265, 1631, 1603, 1585, 1560, 1034.
1H ЯМР (400 МГц), δ, м.д. в DMSO-d6: 0,68-0,72 (т, J = 7.4 Гц, 3H, СH3), 1,73-2,09 (м, 2H, CH2), 3,69 (с, 3H, О-CH3), 5,85-5,89 (д, J = 15.6 Гц, 1H, CH=), 6,73-6,90 (м, 3H, ArH), 7,26-7,45 (м, 5H, ArH), 7,63 (с, 2H, NH2), 7,74-7,93 (м, 3H, 2ArH, 1CH=), 8,06-8,09 (дд, J = 8.5, 2.9 Гц, 2H, ArH), 9,64 (с, 1H, OH).
Молекулярная масса: 503,5. Брутто формула: C27H25N3O5S
Элементный состав:
Найдено, %: С: 63,1% H: 5, 3% N: 8,5% O: 15,2% S: 6,0%.
Вычислено, %: C: 64,4% H: 5% N: 8,3% O: 15,9% S: 6,4%.
Стадия 2
Натриевая соль 4-{2-[2-(4-гидроксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида
В 400 мл метанола при нагревании 5,03 г (0,01 моль) 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида растворяют при одновременном добавлении 0,81 г (0,015 моль) метилата натрия. Полученный раствор доводят до кипения и упаривают до 50 мл. Реакционную среду охлаждают до комнатной температуры и выделяют продукт реакции добавлением 100 мл диэтилового эфира. Выход соли составляет 66 % (3,46 г). Вещество представляет собой оранжевый порошок без запаха. Растворим в воде, этаноле, метаноле, пропаноле-2, диметилформамиде, не растворим в диэтиловом эфире. Температура плавления 298-300°С с разложением (из этанола). Rf = 0,81 (этанол).
УФ-спектр, λmax, нм: 203, 255, 364.
ИК-спектр, ν, см-1: 1631, 1587, 1027.Спектр 1H ЯМР (400 МГц), δ, м.д. в DMSO-d6: 0,68-0,72 (т, J = 7.4 Гц, 3H, СH3); 1,69-2,06 (м, 2H, CH2); 3,51 (с, 3H, О-CH3); 5,23-5,30 (т, J = 14.6 Гц, 1H, CH=), 6,03-6,05 (д, J = 8.3 Гц, 1H, ArH), 6,36-6,38 (д, J = 10.1, 1H, ArH), 6,63 (с, 1H, ArH); 7,24-7,43 (м, 5H, ArH), 7,62-7,70 (м, 5H, ArH, NH2), 7,98-8,00 (д, J = 8.0 Гц, 2H, ArH), 8,51 (с, 1H, OH).
Молекулярная масса: 525,3.
Брутто формула: C27H24N3O5SNa.
Элементный состав:
Найдено, %: С: 60,5% H: 4, 3% N: 7,6% O: 14,8% S: 6,0% Na: 4,7%.
Вычислено, %: C: 61,7% H: 4,6% N: 8,0% O: 15,2% S: 6,1% Na: 4,4%.
Натриевая соль 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида обладает выраженным противоопухолевым действием. Исследование противоопухолевого действия вещества проводили на самцах мышей линии С57BL/6. Было сформировано 2 группы: основная (n = 9) - мыши, получавшие исследуемое вещество, и контрольная (n = 9) - мыши, получавшие воду для инъекции, в том же объёме, что и мыши основной группы. Животным подкожно в подлопаточную область справа перевивали меланому В16/F10 в объёме 0,5 мл, в разведении 1:10.
Через 24 часа после перевивки вводили вещество: натриевую соль 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида (формулы I) внутримышечно в дозе 0,375 мг на мышь (250мг/80кг), предварительно растворив в 0,1 мл воды для инъекции, по схеме: 5 дней - введение, 2 дня - перерыв в течение всей жизни животного. Фиксировали динамику веса экспериментальных животных и динамику роста подкожных опухолей.
В основной и контрольной группах динамика веса животных была идентичной. Выход опухолей у мышей, получавших натриевую соль 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида, происходил в одни и те же сроки, что и в контроле - в среднем через неделю после перевивки. В тоже время на фоне приёма тестируемого вещества у мышей регистрировались бóльшие, чем в контроле: средняя продолжительность жизни - в 1,6 раза (р<0,05); минимальная продолжительность жизни – на 11 дней; максимальная продолжительность жизни – на 23 дня (см. Табл. 1).
Таблица 1
Выход опухоли и продолжительность жизни мышей самцов (сутки) под влиянием вещества I
±2.96
±4.67
±2.53
±0.96
Примечание: * - статистическая значимость отличий относительно контрольных значений (р<0,05).
Средний объём опухолей на фоне приёма натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида был меньше контрольных значений: на 11 сутки - в 77,0 раз, на 14 сутки - в 19,2 раза, на 18 сутки - в 7,5 раза, на 21 сутки - в 4,5 раза, на 25 сутки - в 4,3 раза (см. Табл. 2).
Таблица 2
Динамика роста опухолей у мышей самцов под влиянием вещества I
Примечание: * - статистическая значимость отличий относительно контрольных значений (р<0,05).
Показатель торможения роста опухолей (ПТРО) у мышей, получавших натриевую соль 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида, был высоким на протяжении всего периода наблюдения, начиная с 4 суток и до 28 суток от 99,9 до 76,2 (см. Табл. 3). ПТРО = (К - Оп)/К × 100, где К - средний объем опухолей у животных контрольной группы, Оп - средний объем опухолей у животных опытной группы.
Таблица 3
Показатель торможения роста опухолей (%) (ПТРО) у мышей самцов под влиянием вещества I
Таким образом натриевая соль 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида обладает выраженной цитостатической активностью, в результате которой происходит торможение роста подкожных опухолей меланомы В16/F10, что способствует увеличению продолжительности жизни экспериментальных животных.
Настоящее изобретение относится к области медицины, а именно онкологии, и раскрывает применение натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида, формулы I, в качестве средства, обладающего противоопухолевым действием при меланоме. Техническим результатом настоящего изобретения является выраженная цитостатическая активность натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида, формулы I, которая обладает противоопухолевым действием при меланоме.
1 з.п. ф-лы, 3 табл.
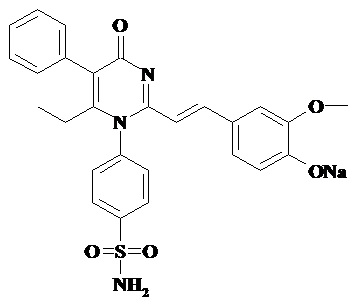 I
I
1. Применение натриевой соли 4-{2-[2-(4-гидрокси-3-метоксифенил)-винил]-6-этил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида формулы I в качестве средства, обладающего противоопухолевым действием при меланоме.
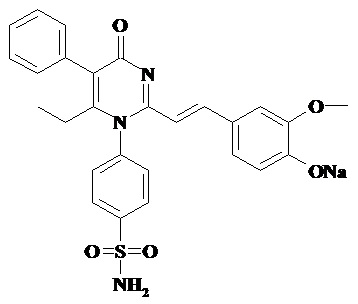 I
I
2. Применение по п. 1 для изготовления фармацевтической композиции.
| WO 2013043232 A2, 28.03.2013 | |||
| ПИРИМИДИНСУЛЬФАМИДЫ И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ ЭНДОТЕЛИАЛЬНЫХ РЕЦЕПТОРОВ | 2003 |
|
RU2329255C2 |
| DMITRY I | |||
| POZDNYAKOV et al., The Administration of the New Pyrimidine Derivative—4-{ 2-[2-(3,4-Dimethoxyphenyl)-Vinyl]-6-Ethyl-4-Oxo-5-Phenyl-4H-Pyrimidine-1-Il} Benzsulfamide Restores the Activity of Brain Cells in Experimental Chronic Traumatic Encephalopathy by Maintaining Mitochondrial | |||
Авторы
Даты
2022-01-11—Публикация
2021-03-26—Подача