Ацетилсалициловая кислота, известная под торговым названием Аспирин, используется в терапии более 100 лет. В частности, о-ацетилсалициловая кислота широко используется в качестве болеутоляющего, жаропонижающего или противоревматического средства, а также в качестве нестероидного противовоспалительного средства при артрите, невралгии или миалгии.
К сожалению, ацетилсалициловая кислота имеет ограниченную растворимость в воде, что ограничивает скорость ее всасывания и, следовательно, формы ее потенциального применения. Было обнаружено, что некоторые соли ацетилсалициловой кислоты демонстрируют значительно улучшенную скорость всасывания. В частности, соли ацетилсалициловой кислоты с основными аминокислотами, особенно лизином, демонстрируют значительно улучшенную скорость всасывания.
Следовательно, обычно в качестве соли ацетилсалициловой кислоты применяют лизинат ацетилсалициловой кислоты [также называемый ацетилсалицилатом лизина). Эта соль известна уже более 60 лет. Ее использовали в нескольких фармацевтических композициях и способах применения. Преимуществом лизината ацетилсалициловой кислоты является высокая устойчивость при пероральном применении, а также повышенная скорость увеличения уровня в крови по сравнению с ацетилсалициловой кислотой, применяемой отдельно.
Еще одной важной солью является ацетилсалицилат лизина ⋅ глицин [LASAG; также называемый ацетилсалицилат D,L-лизина ⋅ глицин), который проявляет дополнительные полезные свойства. Регулируя размер частиц LASAG, можно регулировать важные параметры, такие как скорость растворения (также называемая интенсивностью растворения).
Синтез лизината ацетилсалициловой кислоты и LASAG был предметом нескольких попыток оптимизации. К сожалению, различные способы синтеза имеют некоторые незначительные или существенные недостатки. Обычно используемый в настоящее время способ синтеза включает избыток лизина и использование затравочных кристаллов лизината ацетилсалициловой кислоты. Недостатком использования затравочных кристаллов является больший риск загрязнения конечного продукта.
Некоторые другие способы синтеза лизината ацетилсалициловой кислоты не требуют применения затравочных кристаллов, но характеризуются низким выходом по сравнению со способами с применением затравочных кристаллов (например, выход примерно 70% по сравнению с выходом от 90 до 95%).
Следовательно, существует потребность в новом и улучшенном способе синтеза, который не требует применения затравочных кристаллов, но сохраняет высокий выход лизината ацетилсалициловой кислоты. Кроме того, существует потребность в синтезе LASAG, который позволяет легко получать частицы LASAG с определенными и небольшими размерами частиц.
Краткое описание изобретения
Настоящее изобретение относится к способу получения лизината ацетилсалициловой кислоты, необязательно ацетилсалицилата лизина ⋅ глицина, включающему следующие стадии:
a) обеспечение раствора ацетилсалициловой кислоты в этаноле;
b) обеспечение водного раствора лизина;
c) объединение растворов со стадий а) и b) с получением смеси;
d) необязательно перемешивание полученной смеси;
e) добавление ацетона к смеси;
f) инкубирование смеси с обеспечением возможности образования продукта лизината ацетилсалициловой кислоты;
g) выделение продукта лизината ацетилсалициловой кислоты;
причем ацетилсалициловую кислоту используют в избытке по отношению к лизину и
причем к смеси не добавляют затравочные кристаллы; и необязательно
h) обеспечение перекристаллизованного глицина; где глицин перекристаллизован с помощью следующих стадий:
h1) растворение глицина в воде;
h2) добавление ацетона к раствору глицина;
h3) перемешивание полученной смеси до получения осадка;
i) объединение перекристаллизованного глицина со стадии h) с продуктом стадии g) - лизинатом ацетилсалициловой кислоты - с получением частиц ацетилсалицилата лизина ⋅ глицина (LASAG).
В предпочтительном варианте реализации настоящего изобретения полученные частицы - и, в частности, частицы LASAG, полученные на стадии i), - имеют медианный размер частиц менее 40 мкм, и 90% частиц имеют размер частиц 110 мкм или менее.
Краткое описание чертежей Фиг. 1: Схема реакции получения лизината ацетилсалициловой кислоты.
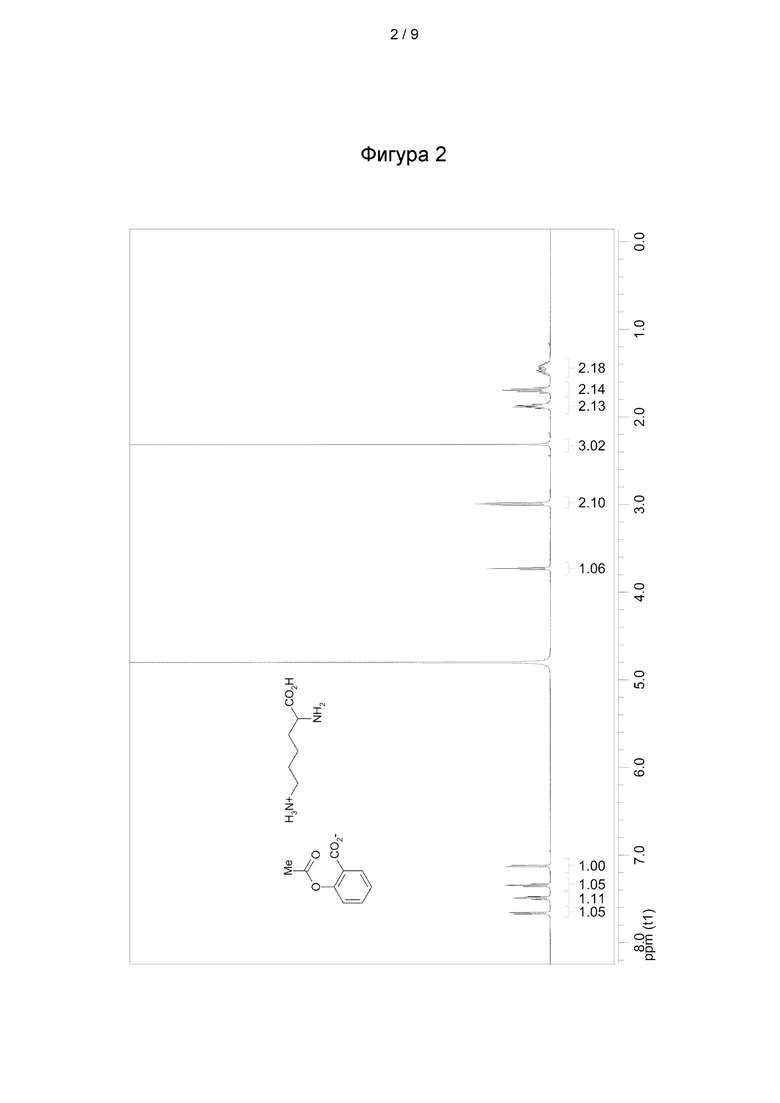
Фиг. 2: 1Н-ЯМР анализ лизината ацетилсалициловой кислоты, полученного способом согласно настоящему изобретению.
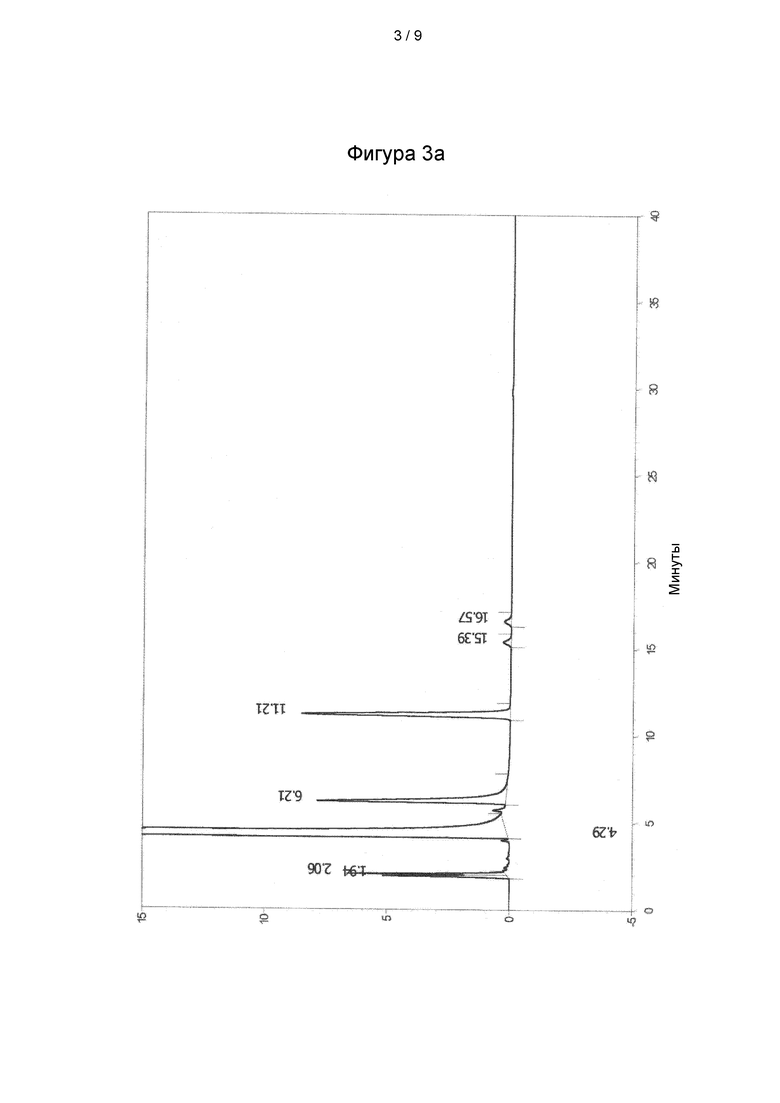
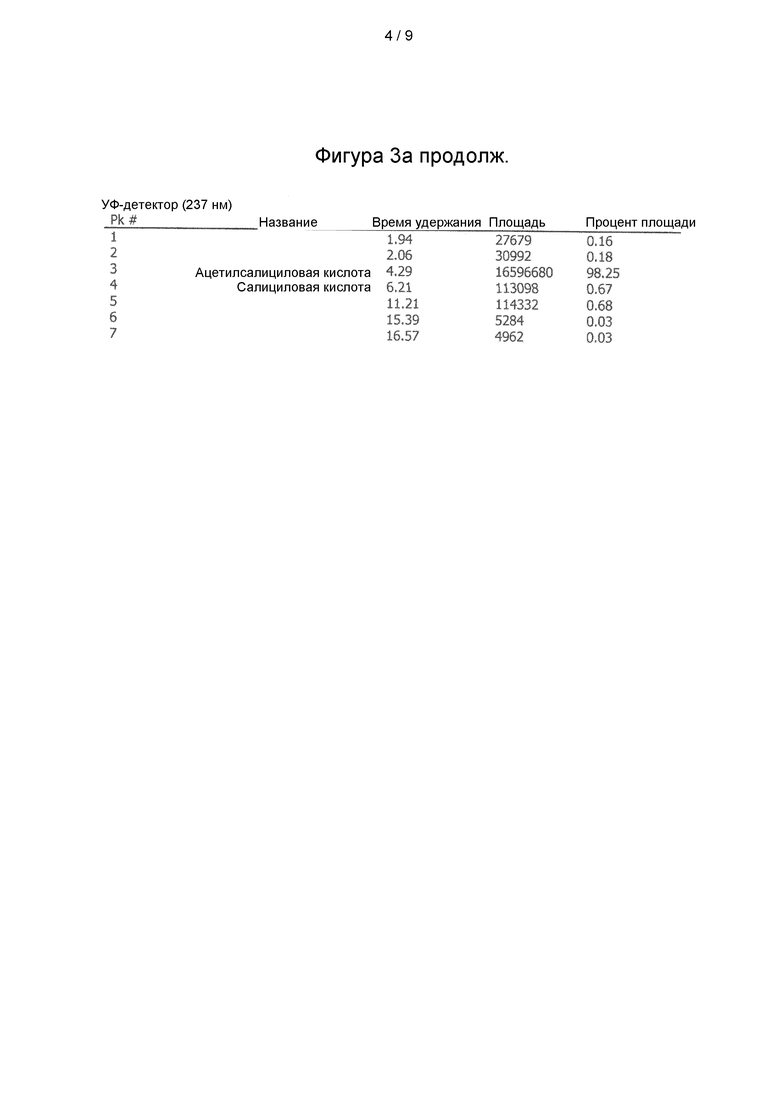
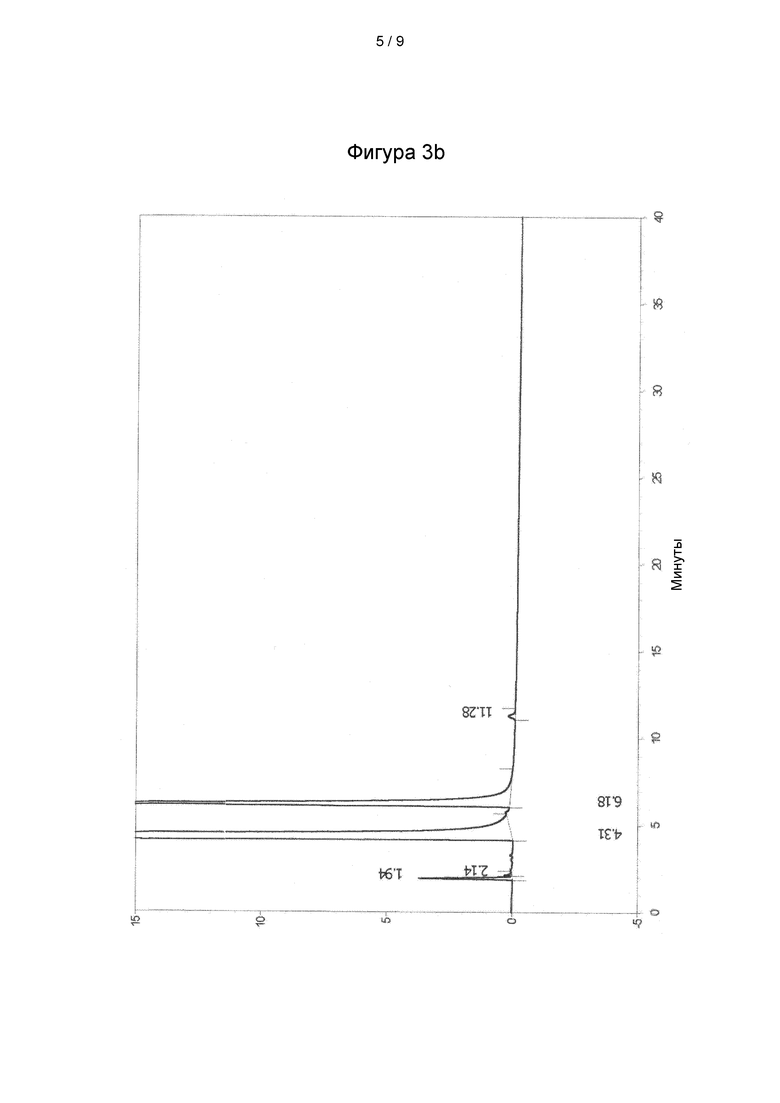
Фиг. 3: ВЭЖХ-МС анализ а) образца лизината ацетилсалициловой кислоты, полученного в соответствии со способом согласно настоящему изобретению, и b) образца коммерчески доступного лизината ацетилсалициловой кислоты.
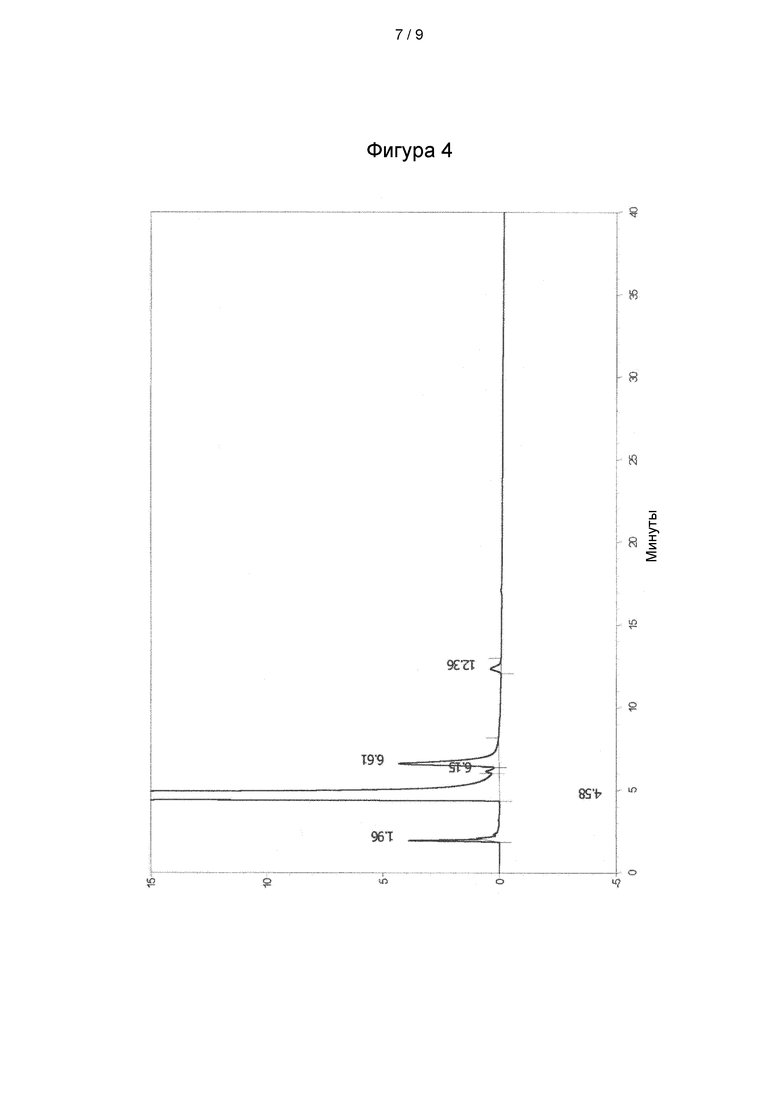
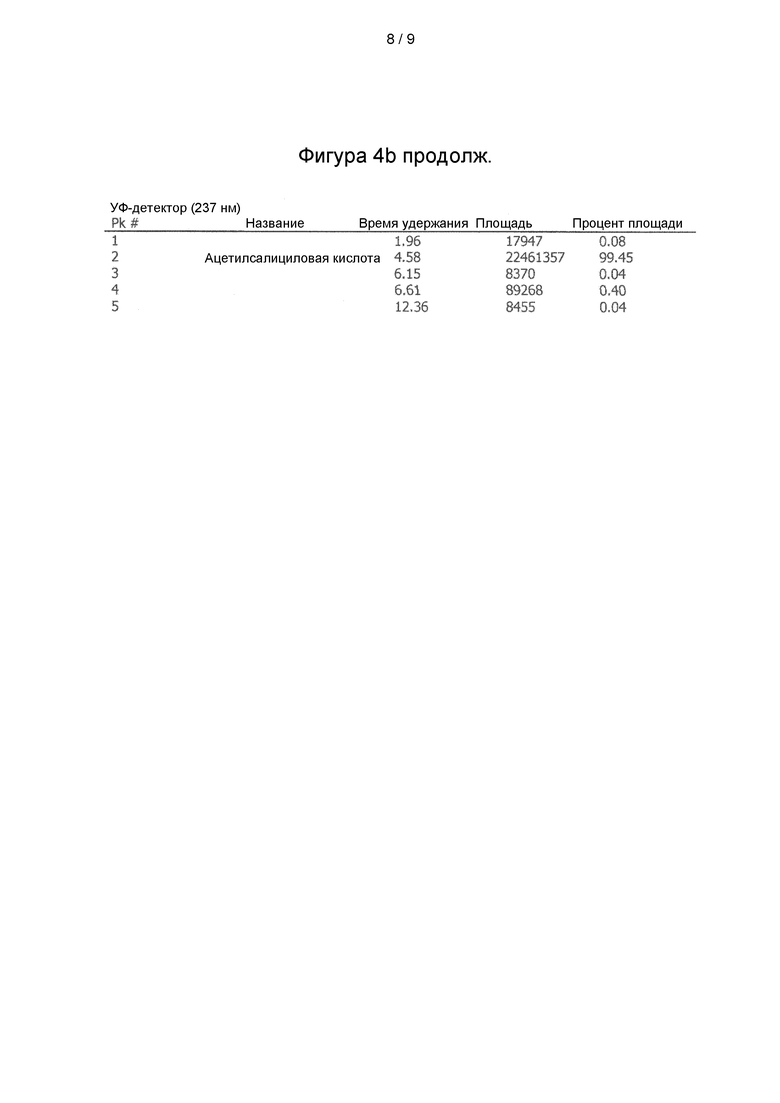
Фиг. 4: ВЭЖХ-МС анализ а) образца лизината ацетилсалициловой кислоты, полученного в большом масштабе в соответствии со способом согласно настоящему изобретению.
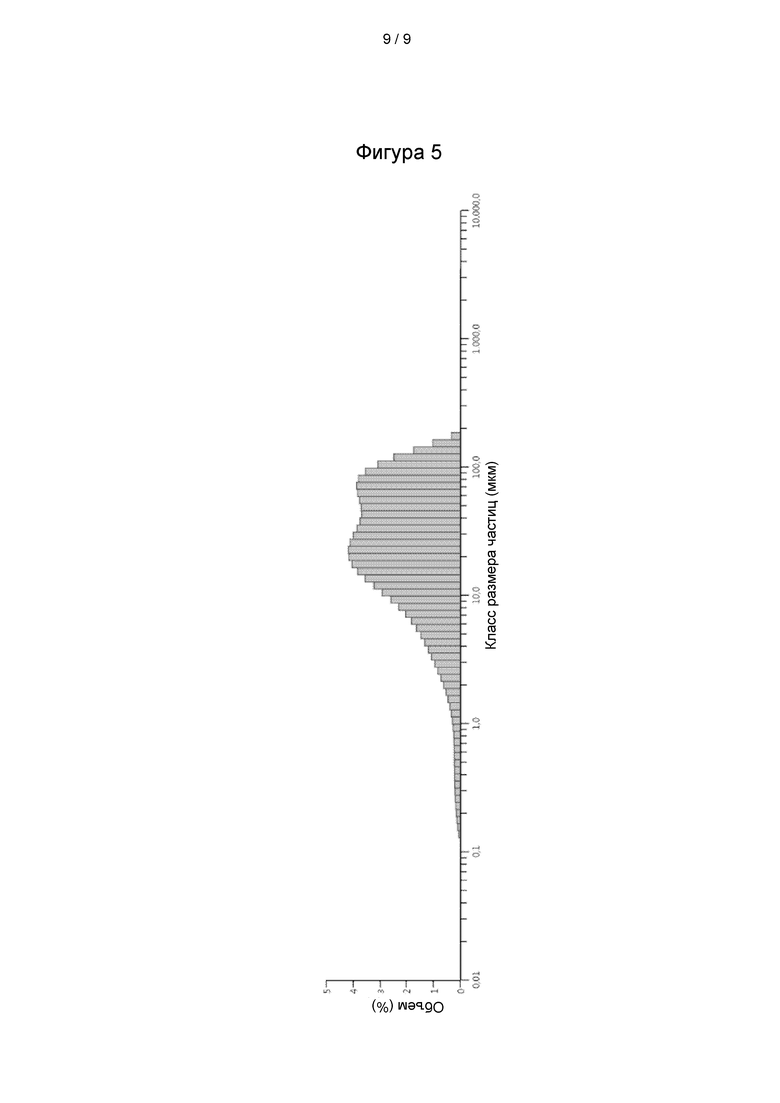
Фиг. 5: Распределение по размеру частиц образца LASAG, полученного в соответствии со способом согласно настоящему изобретению.
Подробное описание изобретения
Авторы изобретения разработали улучшенный способ получения лизината ацетилсалициловой кислоты, который обеспечивает очень высокие выходы (≥90%) без необходимости применения затравочных кристаллов. Указанный способ дополнительно обеспечивает значительно сокращенное время образования продукта. Дополнительная модификация этого способа позволяет получать ацетилсалицилат лизина ⋅ глицин с определенным и малым размером частиц.
Соответственно, в первом аспекте, настоящее изобретение относится к способу получения лизината ацетилсалициловой кислоты, необязательно ацетилсалицилата лизина ⋅ глицина, включающему следующие стадии:
а) обеспечение раствора ацетилсалициловой кислоты в этаноле;
b) обеспечение водного раствора лизина;
c) объединение растворов со стадий а) и b) с получением смеси;
d) необязательно перемешивание полученной смеси;
e) добавление ацетона к смеси;
f) инкубирование смеси с обеспечением возможности образования продукта лизината ацетилсалициловой кислоты;
g) выделение продукта лизината ацетилсалициловой кислоты;
причем ацетилсалициловую кислоту используют в избытке по отношению к лизину и
причем к смеси не добавляют затравочные кристаллы; и необязательно следующие дальнейшие стадии:
h) обеспечение перекристаллизованного глицина; где глицин перекристаллизован с помощью следующих стадий:
h1) растворение глицина в воде;
h2) добавление ацетона к раствору глицина;
h3) перемешивание полученной смеси до получения осадка;
i) объединение перекристаллизованного глицина со стадии h) с продуктом стадии g) - лизинатом ацетилсалициловой кислоты - с получением частиц ацетилсалицилата лизина ⋅ глицина (LASAG).
Способ может включать до двух необязательных стадий:
g1) промывание выделенного продукта и/или
j) стерилизация выделенного продукта.
Во втором аспекте настоящее изобретение относится к лизинату ацетилсалициловой кислоты и, необязательно, ацетилсалицилату лизина ⋅ глицину (LASAG), полученным описанным выше способом(-ами) в соответствии с первым аспектом настоящего изобретения.
Указанный способ, в частности, подходит для получения частиц LASAG с определенным размером частиц. Термин «размер частиц» в контексте настоящего изобретения относится к диаметру частиц, измеренному с помощью лазерной дифракции; например, с использованием лазерного дифрактометра Mastersizer 3000 (Malvern Instruments), оборудованного модулем для сухих порошков. Таким образом, термины «размер частиц» и «диаметр частиц» могут использоваться в настоящем описании как синонимы. Что касается измерений размера частиц, все проценты, представленные в настоящем описании (такие как «по меньшей мере 90% частиц имеют размер частиц…»), следует понимать как объемные проценты.
Предпочтительно частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 100 мкм, предпочтительно менее 80 мкм, более предпочтительно менее 50 мкм, в частности, предпочтительно менее 40 мкм и особенно предпочтительно менее 30 мкм. В другом предпочтительном варианте реализации по меньшей мере 90% частиц LASAG, полученных на стадии i), имеют размер частиц менее 200 мкм, предпочтительно менее 175 мкм, более предпочтительно менее 150 мкм, еще более предпочтительно менее 130 мкм, в частности, предпочтительно менее 120 мкм и особенно предпочтительно менее 110 мкм. В еще одном предпочтительном варианте реализации не более 10% частиц LASAG, полученных на стадии i), имеют размер частиц менее 1 мкм, предпочтительно менее 2 мкм, более предпочтительно менее 3 мкм.
В конкретном варианте реализации настоящего изобретения частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 50 мкм, и по меньшей мере 90% частиц имеют размер частиц 150 мкм или менее. В предпочтительном варианте реализации частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 40 мкм, и по меньшей мере 90% частиц имеют размер частиц 130 мкм или менее. В более предпочтительном варианте реализации частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 30 мкм, и по меньшей мере 90% частиц имеют размер частиц 110 мкм или менее. Например, в одном из других предпочтительных вариантов реализации частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 30 мкм, по меньшей мере 90% частиц имеют размер частиц 110 мкм или менее, и не более 10% частиц имеют размер частиц 3 мкм или менее.
Под ацетилсалициловой кислотой в контексте настоящего изобретения предпочтительно понимают о-ацетилсалициловую кислоту.
Стадии а) и b), обеспечение ацетилсалициловой кислоты в этаноле и обеспечение водного раствора лизина, могут быть выполнены при любой температуре. Растворы могут быть обработаны любым требуемым или желаемым способом. В предпочтительном варианте реализации по меньшей мере один указанный раствор стадий а) и/или b) предварительно обрабатывали с целью стерилизации указанных растворов перед использованием. В одном варианте реализации настоящего изобретения по меньшей мере один из растворов стадии а) и/или b) подвергали стерилизующему фильтрованию.
В некоторых вариантах реализации настоящего изобретения растворы стадий а) и/или b) могут содержать дополнительные добавки, такие как, например, глицин.
Полученные растворы могут быть предварительно обработаны перед использованием. Предварительная обработка включает любую обработку растворов перед использованием в способе. Некоторые способы предварительной обработки предполагают, что раствор нагревали, охлаждали или замораживали перед использованием в способе. В некоторых вариантах реализации по меньшей мере один из растворов нагревали или охлаждали. В других вариантах реализации по меньшей мере один из растворов облучали. В других вариантах реализации несколько различных способов предварительной обработки комбинировали для по меньшей мере одного раствора.
Растворы стадий а) и b) должны содержать достаточно чистые соединения и быть приготовлены на основе растворителей фармацевтической степени чистоты. Соединения ацетилсалициловая кислота и лизин предпочтительно являются по меньшей мере по существу чистыми, более предпочтительно имеют по меньшей мере фармацевтическую степень чистоты, наиболее предпочтительно по существу не содержат примесей.
Растворы стадии а) и/или b) могут содержать близкие концентрации соединений или содержать различные концентрации соединений. В одном предпочтительном варианте реализации настоящего изобретения раствор стадии а) предпочтительно содержит примерно от 8 до 12% (масс/об.) ацетилсалициловой кислоты. В предпочтительном варианте реализации настоящего изобретения раствор содержит примерно от 9 до 11% (масс/об.) ацетилсалициловой кислоты. Наиболее предпочтительно раствор содержит примерно от 9 до 10% (масс/об.) ацетилсалициловой кислоты.
Раствор, содержащий лизин, предпочтительно имеет более высокую концентрацию, чем раствор, содержащий ацетилсалициловую кислоту. В одном варианте реализации настоящего изобретения водный раствор, содержащий лизин, со стадии b) содержит примерно от 25 до 40% (масс/об.) лизина. В предпочтительном варианте реализации настоящего изобретения водный раствор стадии b) содержит примерно от 30 до 35% (масс/об.) лизина. Наиболее предпочтительно водный раствор стадии b) содержит примерно от 32 до 33% (масс/об.) лизина.
Предпочтительно лизин используют в форме свободного основания. Даже если можно использовать лизин в форме соли, например, в форме гидрохлорида лизина, предпочтительно использовать лизин в форме моногидрата лизина.
Не имеет значения, какой стереоизомер лизина используют. Также можно использовать смесь стереоизомеров. В одном варианте реализации настоящего изобретения используют D-лизин. В предпочтительном варианте реализации используют L-лизин. В альтернативном варианте реализации настоящего изобретения используют D,L-лизин.
Для способа важно, чтобы в конечной смеси молярное количество ацетилсалициловой кислоты превышало молярное количество лизина. Предпочтительно использовать небольшой избыток ацетилсалициловой кислоты по отношению к лизину. В одном варианте реализации настоящего изобретения ацетилсалициловую кислоту используют по меньшей мере в 1,05-кратном молярном избытке по отношению к лизину. Предпочтительно ацетилсалициловую кислоту используют по меньшей мере в 1,07-кратном молярном избытке, и более предпочтительно ацетилсалициловую кислоту используют по меньшей мере в 1,1-кратном молярном избытке.
В одном конкретном варианте реализации настоящего изобретения ацетилсалициловую кислоту и лизин используют в молярном отношении примерно от 1 до 0,95. В более предпочтительном варианте реализации настоящего изобретения ацетилсалициловую кислоту и лизин используют в молярном отношении примерно от 1 до 0,90.
В некоторых вариантах реализации любой из растворов стадии а) или b) может дополнительно содержать глицин. Например, раствор, содержащий лизин, стадии b) может дополнительно содержать глицин. В альтернативном варианте реализации глицин получают в виде отдельного раствора. Если глицин добавляют в отдельный раствор, предпочтительно, чтобы глицин получали в растворе примерно от 75 до 85% (об./об.) этанола. В одном варианте реализации количество глицина в конечном сухом продукте находится в диапазоне от 8 до 12 масс. % или примерно 10% (масс/масс).
Если добавляют раствор глицина, указанный раствор предпочтительно добавляют в то же время, когда объединяют растворы стадий а) и b), или одновременно с добавлением ацетона или вскоре после него.
В некоторых вариантах реализации, если в конечном продукте желательно наличие глицина, то есть твердой формы лизината ацетилсалициловой кислоты, глицин также можно добавлять на более поздней стадии и в твердой форме; например, перекристаллизованный глицин, как описано выше на необязательной стадии h).
Обычно предпочтительно, чтобы объем этанольного раствора стадии а) превышал объем водного раствора стадии b). Предпочтительно объем этанольного раствора стадии а) является по меньшей мере примерно в 2 раза, предпочтительно по меньшей мере примерно в 3 раза, более предпочтительно примерно в 4 раза большим, чем объем водного раствора стадии b).
Стадии а) и b) могут быть выполнены в любом порядке.
Стадия с), объединение растворов с получением смеси, может быть выполнена любым подходящим способом. Предпочтительно растворы объединяют медленно, при необходимости перемешивая образующуюся смесь. В идеальном варианте смесь начнет кристаллизоваться в процессе перемешивания. В предпочтительном варианте реализации растворы объединяют путем добавления раствора стадии b) к раствору стадии а), в то время как раствор и образующуюся смесь перемешивают. Предпочтительно растворы объединяют в течение менее чем одного часа, более предпочтительно в течение менее чем 30 минут, более предпочтительно в течение менее чем 15 минут, еще более предпочтительно в течение менее чем 10 минут, наиболее предпочтительно в течение менее чем 5 минут.
Затем смесь могут необязательно перемешивать в течение определенного периода времени. Предпочтительно смесь хранят менее 24 часов, предпочтительно смесь перемешивают менее 12 часов, более предпочтительно менее 6 часов, еще более предпочтительно смесь перемешивают менее 3 часов, более предпочтительно менее 1 часа. В другом предпочтительном варианте реализации смесь перемешивают менее 15 минут.
После объединения растворов на стадии с) и необязательного перемешивания к смеси добавляют ацетон. Предпочтительно количество добавляемого ацетона имеет примерно такой же объем, что и имеющаяся смесь, более предпочтительно добавляют немного меньшее количество. В одном варианте реализации объем добавленного ацетона соответствует примерно от 1 до 1,2 объема этанольного раствора стадии а). В предпочтительном варианте реализации объем ацетона соответствует примерно от 1,05 до 1,15 объема этанольного раствора стадии а). Наиболее предпочтительно объем ацетона соответствует примерно 1,1 объема этанольного раствора стадии а).
Добавление ацетона должно привести к получению перенасыщенной смеси, что приводит к улучшенной и более быстрой кристаллизации с более высокими выходами. Соответственно, количество используемого ацетона должно быть достаточным для обеспечения перенасыщения смеси.
В предпочтительном варианте реализации настоящего изобретения ацетон добавляют после начала кристаллизации, то есть после получения первичного осадка. Обычно первичный осадок должен образовываться без использования затравочных кристаллов в течение 10 минут или менее. В нескольких вариантах реализации настоящего изобретения первичный осадок образуется в течение пяти минут.
Основным преимуществом способа согласно настоящему изобретению является то, что не требуется затравочных кристаллов для достижения высокой чистоты продукта после короткого времени образования продукта, даже в промышленном масштабе. Другие способы, используемые в промышленном масштабе, требуют использования затравочных кристаллов или, в других случаях, приводят к значительно более низким выходам, чем способ согласно настоящему изобретению.
После добавления ацетона смесь следует инкубировать с обеспечением возможности образования кристаллов лизината ацетилсалициловой кислоты. Еще одним преимуществом способа является то, что для способа согласно настоящему изобретению не требуется длительного времени инкубирования. Высокие выходы продукта достигаются менее чем за три часа времени инкубирования. Смесь можно перемешивать или не перемешивать во время инкубирования и образования кристаллов. В предпочтительном варианте реализации настоящего изобретения смесь перемешивают во время инкубирования.
Смесь можно инкубировать столько, сколько необходимо. Однако преимуществом настоящего изобретения является короткое время инкубирования. В одном варианте реализации настоящего изобретения смесь инкубируют в течение примерно трех часов или менее, предпочтительно в течение примерно двух часов или менее, более предпочтительно в течение примерно одного часа или менее. В наиболее предпочтительном варианте реализации смесь инкубируют в течение примерно 30 минут.
В конкретном предпочтительном варианте реализации настоящего изобретения смесь инкубируют в течение примерно менее чем одного часа и перемешивают во время инкубирования.
После инкубирования осажденный продукт следует выделить. Подходит любой способ, который позволяет отделить осажденный продукт от жидкого раствора.
Предпочтительно продукт выделяют путем фильтрования или центрифугирования. В наиболее предпочтительном варианте реализации настоящего изобретения продукт выделяют путем фильтрования.
Как уже было указано выше, продукт может быть необязательно промыт на необязательной стадии g1) для удаления примесей. Предпочтительно продукт промывают ацетоном. Более предпочтительно продукт несколько раз промывают ацетоном. В одном варианте реализации настоящего изобретения выделенный продукт промывают по меньшей мере один раз, предпочтительно по меньшей мере два раза, более предпочтительно по меньшей мере три раза.
После выделения и промывания продукта продукт может быть необязательно высушен. В контексте настоящего изобретения термин «сушка» относится к удалению остатков растворителя, предпочтительно удалению избытка воды, этанола и ацетона. Растворители могут быть удалены любым подходящим способом, однако сушка при комнатной температуре в течение некоторого времени или лиофилизация продукта является предпочтительной. В контексте настоящего описания термин «комнатная температура» относится к диапазону 20±5°С.
В конкретном варианте реализации настоящего изобретения способ включает добавление глицина для получения ацетилсалицилата лизина ⋅ глицина. В этом случае способ включает получение глицина, предпочтительно перекристаллизованного глицина.
В одном варианте реализации настоящего изобретения перекристаллизацию глицина проводят путем растворения глицина в воде. Предпочтительно глицин растворяют в деионизированной воде.
В предпочтительном варианте реализации глицин растворяют в воде с получением 20% (масс/об.) раствора.
Предпочтительно глицин растворяют примерно при комнатной температуре. В некоторых вариантах реализации настоящего изобретения раствор глицина нагревают или охлаждают до 20 или 21°С. В одном варианте реализации температуру раствора доводят до 20°С. В другом варианте реализации настоящего изобретения температуру раствора доводят до 21°С.
После растворения глицина и, необязательно, установления указанной температуры добавляют ацетон для осаждения глицина. Предпочтительно ацетон добавляют медленно; более предпочтительно ацетон добавляют по каплям. Смесь предпочтительно перемешивают во время добавления ацетона.
В предпочтительном варианте реализации добавление ацетона проводят с контролем температуры. В более предпочтительном варианте реализации температура смеси во время добавления ацетона не превышает 30°С.
В одном варианте реализации настоящего изобретения добавляют избыток ацетона по сравнению с количеством глицина. В предпочтительном варианте реализации к раствору глицина добавляют по меньшей мере в 2 раза больший объем ацетона, более предпочтительно к раствору глицина добавляют по меньшей мере в четыре раза больший объем ацетона.
В некоторых вариантах реализации настоящего изобретения смесь дополнительно перемешивают после добавления ацетона.
Затем осажденный и перекристаллизованный глицин собирают и сушат. В некоторых вариантах реализации осажденный глицин промывают ацетоном перед сушкой. Предпочтительно глицин сушат при комнатной температуре. В некоторых вариантах реализации перекристаллизованный глицин сушат на воздухе при комнатной температуре и при атмосферном давлении. В некоторых вариантах реализации перекристаллизованный глицин сушат под вакуумом.
После перекристаллизации глицин объединяют с лизинатом ацетилсалициловой кислоты, полученным на стадии g). Глицин может быть объединен путем смешивания соединений, предпочтительно в твердой форме. Авторы изобретения неожиданно обнаружили, что стадия перекристаллизации h) улучшает способность лизината ацетилсалициловой кислоты (или ацетилсалицилата лизина) и перекристаллизованного глицина смешиваться; например, обеспечивает улучшение однородности полученной смеси, а также предотвращение разделения образовавшейся смеси (например, во время последующих операций обработки, таких как заполнение саше или флаконов, или во время хранения). Не желая ограничиваться какой-либо теорией, в настоящее время полагают, что улучшенное поведение при смешивании обусловлено или по меньшей мере частично обусловлено уменьшенной разницей в плотности между лизинатом ацетилсалициловой кислоты и перекристаллизованным глицином (по сравнению с глицином, который не подвергали перекристаллизации перед смешиванием).
В одном варианте реализации твердые соединения смешивают и перемешивают, предпочтительно при комнатной температуре. В предпочтительном варианте реализации соединения смешивают без применения дополнительного нагрева. В другом предпочтительном варианте реализации соединения смешивают при атмосферном давлении.
Последняя стадия (то есть стадия i) позволяет определить окончательную композицию LASAG. Количество глицина в конечном продукте (LASAG) можно легко контролировать. В некоторых вариантах реализации глицин добавляют в количестве примерно 10 масс. % от количества лизината ацетилсалициловой кислоты. В некоторых вариантах реализации количество глицина составляет примерно до 20 масс. % от количества лизината ацетилсалициловой кислоты.
После смешивания ацетилсалицилат лизина * глицин (LASAG) может быть далее приготовлен любым необходимым способом. В некоторых вариантах реализации LASAG может быть спрессован в таблетки; в альтернативных вариантах реализации LASAG может применяться в порошкообразной форме.
Как упомянуто выше, способ, в частности, подходит для получения частиц LASAG с определенным размером частиц. Предпочтительно частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 100 мкм, предпочтительно менее 80 мкм, более предпочтительно менее 50 мкм, в частности, предпочтительно менее 40 мкм и особенно предпочтительно менее 30 мкм. В другом предпочтительном варианте реализации по меньшей мере 90% частиц LASAG, полученных на стадии i), имеют размер частиц менее 200 мкм, предпочтительно менее 175 мкм, более предпочтительно менее 150 мкм, еще более предпочтительно менее 130 мкм, в частности, предпочтительно менее 120 мкм и особенно предпочтительно менее 110 мкм. В еще одном предпочтительном варианте реализации не более 10% частиц LASAG, полученных на стадии i), имеют размер частиц менее 1 мкм, предпочтительно менее 2 мкм, более предпочтительно менее 3 мкм.
В конкретном варианте реализации настоящего изобретения частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 50 мкм, и по меньшей мере 90% частиц имеют размер частиц 150 мкм или менее. В предпочтительном варианте реализации частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 40 мкм, и по меньшей мере 90% частиц имеют размер частиц 130 мкм или менее. В более предпочтительном варианте реализации частицы LASAG, полученные на стадии i), имеют медианный размер частиц менее 30 мкм, и по меньшей мере 90% частиц имеют размер частиц 110 мкм или менее.
Стадии способа а) - h) могут быть выполнены в стерильных условиях. В этом случае все используемые соединения должны быть стерильными и подходящими для фармацевтического применения. В качестве альтернативы, способ может не быть выполнен в стерильных условиях, и фармацевтический продукт впоследствии стерилизуют на необязательной стадии j). В предпочтительном варианте реализации продукт необязательно стерилизуют на стадии j) с использованием облучения.
Преимуществом способа, разработанного авторами изобретения, является независимость указанного способа от температуры. В отличие от других способов, этот способ обеспечивает высокие выходы за короткое время при комнатной температуре.
В контексте настоящего изобретения термин «комнатная температура» относится к температуре в диапазоне от 20 до 30°С. Предпочтительно термин «комнатная температура» относится к температуре в диапазоне от 23 до 27°С. Например, термин «комнатная температура» может относиться к температуре примерно 25°С.
В одном конкретном варианте реализации настоящего изобретения все стадии способа выполняют при примерно одинаковой температуре. Предпочтительно способ осуществляют при комнатной температуре. В альтернативном варианте реализации способ осуществляют при комнатной температуре или ниже, предпочтительно при 20°С или ниже. В другом варианте реализации способ осуществляют при температуре 15°С или ниже, предпочтительно при 10°С или ниже, более предпочтительно при 5°С или ниже. В одном конкретном варианте реализации способ выполняют при 0°С или ниже.
В альтернативных вариантах реализации стадии способа выполняют при различных температурах. Способ работает и обеспечивает значительно улучшенный выход, даже если одну или несколько последовательных стадий выполняют при различных температурах.
В частности, стадии а) и b) полностью независимы от температуры. Тем не менее, предпочтительно, чтобы растворы стадии а) и/или b) получали при комнатной температуре или ниже, или чтобы их оставляли для охлаждения до комнатной температуры или ниже перед выполнением стадии с).
В одном варианте реализации настоящего изобретения растворы стадий а) и/или b) получают при комнатной температуре. В альтернативном варианте реализации настоящего изобретения растворы стадии а) и/или b) получают при температуре ниже комнатной. В предпочтительном варианте реализации растворы стадии а) и/или b) получают при температуре примерно 20°С или ниже, предпочтительно при температуре 15°С или ниже, более предпочтительно при температуре 10°С или ниже, еще более предпочтительно при температуре 5°С или ниже. В конкретном варианте реализации настоящего изобретения растворы стадии а) и/или b) получают при температуре 0°С или ниже.
Стадии с) и d), объединения и, необязательно, перемешивания растворов, предпочтительно выполняют при той же температуре, которую имеет по меньшей мере один из растворов стадии а) или b). Однако каждая из стадий с) или d) может быть выполнена при различной температуре. Предпочтительно стадии с) и/или d) выполняют при комнатной температуре. В одном варианте реализации стадии с) и/или d) выполняют при комнатной температуре или ниже. В конкретном варианте реализации настоящего изобретения стадии с) и/или d) выполняют при 20°С или ниже, предпочтительно при 15°С или ниже, более предпочтительно при 10°С или ниже, еще более предпочтительно при 5°С или ниже. В одном конкретном варианте реализации стадии с) и/или d) выполняют при 0°С или ниже.
Добавление ацетона на стадии е) предпочтительно выполняют при той же температуре, что и стадии с) и d), или при той же температуре, что и стадию инкубирования е). В одном варианте реализации стадию е) выполняют при комнатной температуре или ниже. В альтернативном варианте реализации стадию е) выполняют при 20°С или ниже, предпочтительно при 15°С или ниже, более предпочтительно при 10°С или ниже, наиболее предпочтительно при 5°С или ниже. В одном конкретном варианте реализации стадию е) выполняют при 0°С или ниже.
В одном варианте реализации настоящего изобретения стадию инкубирования f) выполняют при комнатной температуре. В альтернативном варианте реализации настоящего изобретения стадию инкубирования f) выполняют при температуре ниже комнатной температуры. В предпочтительном альтернативном варианте реализации стадию инкубирования выполняют при температуре, равной или 20°С ниже, более предпочтительно при 15°С или ниже, еще более предпочтительно при 10°С или ниже, и наиболее предпочтительно при 5°С или ниже. В конкретном альтернативном варианте реализации настоящего изобретения стадию инкубирования выполняют при 0°С или ниже.
Стадию выделения g) и необязательную стадию промывания g1) предпочтительно выполняют при той же или близкой температуре, что и стадию инкубирования. Однако, если используют другую температуру, смесь и продукт могут адаптировать или не адаптировать к новой температуре. Например, если стадию f) выполняли при 5°С, а выделение выполняют при комнатной температуре, смесь, содержащую продукт, могут нагревать или не нагревать до комнатной температуры перед выделением.
Стадии g) и h) могут быть выполнены при одинаковой или различной температуре. В предпочтительном варианте реализации стадии g) и/или h) выполняют при комнатной температуре или ниже. В альтернативном варианте реализации стадии g и/или h) выполняют при 20°С или ниже, предпочтительно при 15°С или ниже, более предпочтительно при 10°С или ниже, наиболее предпочтительно при 5°С или ниже. В конкретном варианте реализации стадии g) и/или h) выполняют при 0°С или ниже.
Необязательная стадия стерилизации может быть выполнена при любой подходящей температуре.
Примеры
Пример 1: Получение лизината ацетилсалициловой кислоты
Лизинат ацетилсалициловой кислоты получали в соответствии со схемой реакции, показанной на фиг. 1.
1 г ацетилсалициловой кислоты растворяли в 11 мл этанола и 0,82 г моногидрата D,L-лизина растворяли в 2,5 мл Н2О. Два полученных раствора смешивали при перемешивании. Примерно через 5 минут образовывался осадок белого цвета. Суспензию дополнительно перемешивали в течение 30 минут, после чего добавляли 12 мл ацетона, и полученную смесь дополнительно инкубировали.
Осадок собирали путем фильтрования, промывали ацетоном и анализировали с помощью ЯМР и ВЭЖХ-МС. Выход составил 1,429 г лизината ацетилсалициловой кислоты (88%). Увеличение масштаба в 7 раз привело к выходу в 91%.
1Н-ЯМР (D20, 300 МГц, фигура 2): δ =1,44 (шир., 2Н, -СН2-), 1,70 (шир., 2Н, -СН2-), 1,87 (шир., 2Н, -СН2-), 2,32 (s, 3Н, Me), 3,00 (t, 2Н, -СН2-, 3J=4,5 Гц), 3,73 (t, 2Н, -СН2-, 3J=4,2 Гц), 7,12 (dd, 1Н, Н-3, 3J1=4,8 Гц, 3J2=0,6 Гц), 7,34 (dt, 1Н, Н-5, 3J1=4,5 Гц, 3J2=0,6 Гц), 7,49 (dt, 1Н, Н-4, 3J1=4,8 Гц, 3J2=0,9 Гц), 7,66 (dd, 1Н, Н-6, 3J1=4,8 Гц, 3J2=0,9 Гц).
Анализ ВЭЖХ-МС подтвердил чистоту, сопоставимую с коммерчески доступными продуктами (фигуры 3а и 3b).
Пример 2: Получение лизината ацетилсалициловой кислоты в большем масштабе партии
Лизинат ацетилсалициловой кислоты получали в соответствии с той же схемой реакции, что и в примере 1, но в большем масштабе.
135 граммов ацетилсалициловой кислоты смешивают с 1,5 литрами этанола. После образования прозрачного раствора быстро добавляли 117,14 г моногидрата D,L-лизина, растворенного в 340 мл деионизированной воды. Через 2 минуты образуется осадок белого цвета. Суспензию продолжают интенсивно перемешивать. Через 0,5 часа к смеси добавляют 1,8 литра ацетона и продолжают перемешивание в течение еще 0,5 часа. Затем осадок белого цвета отфильтровывают, промывают 800 мл ацетона и сушат в вакууме при нагревании до 45°С на водяной бане.
Выход составил 222,62 г лизината ацетилсалициловой кислоты (95%).
1H-ЯМР (D2O, 300 МГц): δ =1,44 (шир., 2Н, -СН2-), 1,70 (шир., 2Н, -СН2-), 1,87 (шир., 2Н, -СН2-), 2,32 (s, 3Н, Me), 3,00 (t, 2Н, -СН2-, 3J=4,5 Гц), 3,73 (t, 2Н, -СН2-, 3J=4,2 Гц), 7,12 (dd, 1Н, Н-3, 3J1=4,8 Гц, 3J2=0,6 Гц), 7,34 (dt, 1Н, Н-5, 3J1=4,5 Гц, 3J2=0,6 Гц), 7,49 (dt, 1Н, Н-4, 3J1=4,8 Гц, 3J2=0,9 Гц), 7,66 (dd, 1Н, Н-6, 3J1=4,8 Гц, 3J2=0,9 Гц).
Анализ ВЭЖХ-МС подтвердил чистоту, сопоставимую с коммерчески доступными продуктами (фигура 4).
Пример 3: Перекристаллизация глицина 10 граммов глицина растворяли в 50 мл деионизированной воды. Полученный раствор нагревали до 21°С, и затем к раствору глицина по каплям добавляли 200 мл ацетона при перемешивании. Добавление ацетона проводили с такой скоростью, чтобы температура смеси ацетон/вода не превышала 30°С. После добавления ацетона полученную суспензию дополнительно перемешивали в течение 60 минут. Затем осадок собирали путем фильтрования, промывали 30 мл ацетона и сушили на воздухе с получением 9,29 г перекристаллизованного глицина.
В альтернативном примере 10 граммов глицина растворяли в 50 мл деионизированной воды. Полученный раствор нагревали до 20°С, а затем отфильтровывали через пористый стеклянный фильтр. Затем к 200 мл ацетона по каплям добавляли полученный фильтрат при перемешивании. Добавление водного раствора проводили с такой скоростью, чтобы температура смеси ацетон/вода не превышала 30°С. После добавления полученную суспензию дополнительно перемешивали в течение 20 минут. Осадок собирали путем фильтрования, промывали 20 мл ацетона и сушили на воздухе с получением 9,62 г перекристаллизованного глицина.
Пример 4: Получение частиц ацетилсалицилата лизина ⋅ глицина (LASAG).
Лизинат ацетилсалициловой кислоты и перекристаллизованный глицин получали, как описано выше.
28,03 грамма лизината ацетилсалициловой кислоты и 2,80 грамма глицина помещали в круглодонную колбу объемом 500 мл. Смесь перемешивали на роторном испарителе без подводимого тепла или пониженного давления в течение 1 часа 25 минут с получением желаемой смеси. Количество глицина в полученной смеси составляет от 8 до 12 масс. %.
На фиг. 5 показано распределение частиц по размерам (PSD) образца LASAG, полученного способом согласно настоящему изобретению. Размер частиц измеряли с помощью лазерной дифракции, в частности, с использованием лазерного дифрактометра Mastersizer 3000 (Malvern Instruments), оборудованного модулем для сухих порошков. Можно видеть, что большинство частиц имеет размер частиц менее 100 мкм, и только примерно 5,5 об. % частиц имеют размер частиц выше 100 мкм.
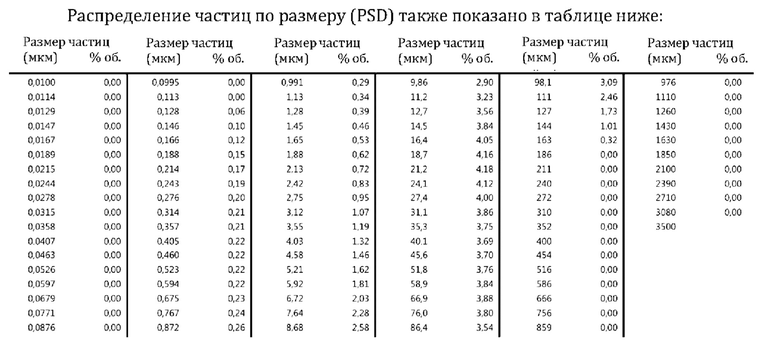
Медианный размер частиц, измеренный для этого образца LASAG, составляет 24,5 мкм, и 90% частиц имеют размер частиц 93,3 мкм или менее (то есть Dv(90)=93,3 мкм).
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАБИЛЬНЫЙ БИОЛОГИЧЕСКИ АКТИВНЫЙ КОМПЛЕКС СОЛЕЙ О-АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ С ОСНОВНЫМИ АМИНОКИСЛОТАМИ И ГЛИЦИНА | 2006 |
|
RU2433995C2 |
| ПРИМЕНЕНИЕ СОЛИ АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ | 2009 |
|
RU2524304C2 |
| Ингалируемые порошковые составы альгинатных олигомеров | 2015 |
|
RU2708397C1 |
| СОЛЮБИЛИЗИРОВАННЫЙ ИБУПРОФЕН | 2006 |
|
RU2403033C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИТОЗАНА С НИЗКИМ СОДЕРЖАНИЕМ ЭНДОТОКСИНА | 2014 |
|
RU2747702C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИТОЗАНА С НИЗКИМ СОДЕРЖАНИЕМ ЭНДОТОКСИНА | 2014 |
|
RU2751231C2 |
| КЛАСТЕР НА ОСНОВЕ ЦИРКОНИЯ В КАЧЕСТВЕ АКТИВНОГО ВЕЩЕСТВА АНТИПЕРСПИРАНТА И ДЕЗОДОРАНТА | 2018 |
|
RU2749186C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛПРОПИОНОВОЙ КИСЛОТЫ | 1993 |
|
RU2133733C1 |
| Средство, проявляющее антиагрегационную активность | 2019 |
|
RU2727508C1 |
| СОЕДИНЕНИЯ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ КРАСИТЕЛИ, ПОЛУЧЕННЫЕ ИЗ ГЕНИПИНА ИЛИ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ГЕНИПИН | 2014 |
|
RU2687413C2 |

Настоящее изобретение относится к способу получения частиц ацетилсалицилата лизина ⋅ глицина, включающему стадии a) обеспечение раствора ацетилсалициловой кислоты в этаноле; b) обеспечение водного раствора лизина; c) объединение растворов со стадий (a) и (b) с получением смеси; d) перемешивание полученной смеси; е) добавление ацетона к смеси; f) инкубирование смеси с обеспечением возможности образования продукта лизината ацетилсалициловой кислоты; g) выделение продукта лизината ацетилсалициловой кислоты; причем ацетилсалициловую кислоту используют в избытке по отношению к лизину и причем к смеси не добавляют затравочные кристаллы; и h) обеспечение перекристаллизованного глицина, где глицин перекристаллизован с помощью следующих стадий: h1) растворение глицина в воде; h2) добавление ацетона к раствору глицина; h3) перемешивание полученной смеси до получения осадка; i) объединение перекристаллизованного глицина со стадии (h) с продуктом стадии (g) лизинатом ацетилсалициловой кислоты с получением частиц ацетилсалицилата лизина ⋅ глицина (LASAG). 14 з.п. ф-лы, 9 ил., 1 табл., 4 пр.
1. Способ получения частиц ацетилсалицилата лизина ⋅ глицина, включающий стадии:
a) обеспечение раствора ацетилсалициловой кислоты в этаноле;
b) обеспечение водного раствора лизина;
c) объединение растворов со стадий (a) и (b) с получением смеси;
d) перемешивание полученной смеси;
е) добавление ацетона к смеси;
f) инкубирование смеси с обеспечением возможности образования продукта лизината ацетилсалициловой кислоты;
g) выделение продукта лизината ацетилсалициловой кислоты;
причем ацетилсалициловую кислоту используют в избытке по отношению к лизину и
причем к смеси не добавляют затравочные кристаллы; и
h) обеспечение перекристаллизованного глицина; где глицин перекристаллизован с помощью следующих стадий:
h1) растворение глицина в воде;
h2) добавление ацетона к раствору глицина;
h3) перемешивание полученной смеси до получения осадка;
i) объединение перекристаллизованного глицина со стадии (h) с продуктом стадии (g) лизинатом ацетилсалициловой кислоты с получением частиц ацетилсалицилата лизина ⋅ глицина (LASAG).
2. Способ по п. 1, в котором частицы, полученные на стадии (i), имеют медианный размер частиц менее 40 мкм, и в котором по меньшей мере 90% частиц, полученных на стадии (i), имеют размер частиц менее 110 мкм.
3. Способ по п. 1, в котором по меньшей мере стадии способа (с) - (f) и/или (h) и (i) выполняют при комнатной температуре или ниже.
4. Способ по п. 1, в котором стадию инкубирования (f) выполняют при 10 °С или менее.
5. Способ по п. 1, в котором выделение на стадии (g) выполняют путем фильтрования.
6. Способ по п. 1, в котором выделение на стадии (g) выполняют путем центрифугирования.
7. Способ по п. 1, в котором раствор ацетилсалициловой кислоты, полученный на стадии (а), содержит примерно от 8 до 12% (масс./об.), предпочтительно примерно от 9 до 10% (масс./об.) ацетилсалициловой кислоты.
8. Способ по п. 1, в котором водный раствор лизина, полученный на стадии (b), содержит примерно от 30 до 35% (масс./об.) лизина.
9. Способ по п. 1, в котором водный раствор лизина, полученный на стадии (b), дополнительно содержит растворенный глицин, и в котором концентрация глицина в растворе необязательно составляет от 2 до 20% (масс./об.).
10. Способ по п. 1, в котором водный раствор лизина, полученный на стадии (b), получают из моногидрата лизина.
11. Способ по п. 1, в котором ацетилсалициловую кислоту и лизин используют в молярном отношении от 1 до 0,9 или в отношении от 1 до 0,95.
12. Способ по п. 1, дополнительно включающий стадию:
g1) промывание выделенного продукта.
13. Способ по п. 12, в котором стадия очистки включает промывание продукта ацетоном.
14. Способ по п. 1, в котором указанный способ осуществляют в стерильных условиях.
15. Способ по п. 1, в котором указанный способ осуществляют в нестерильных условиях, и указанный способ включает дополнительную стадию:
j) стерилизация продукта облучением.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| СТАБИЛЬНЫЙ БИОЛОГИЧЕСКИ АКТИВНЫЙ КОМПЛЕКС СОЛЕЙ О-АЦЕТИЛСАЛИЦИЛОВОЙ КИСЛОТЫ С ОСНОВНЫМИ АМИНОКИСЛОТАМИ И ГЛИЦИНА | 2006 |
|
RU2433995C2 |
Авторы
Даты
2022-01-18—Публикация
2017-12-22—Подача