Группа изобретений относится к медицине, а именно к фармацевтической химии и фармакологии, и может быть использована для создания новых лекарственных средств профилактики тромбоза и тромбоэмболических осложнений.
Известно, что в качестве антиагрегационных средств последнего поколения разрешены к клиническому применению препараты L-цистеинамид, N6-(аминоиминометил)-N2-(3-меркапто-1-оксопропил)-b-лизилглицил-b-α-аспартил-L-триптофи-L-пропил-,циклический(1-6)-дисульфид («Интегрилин», Glaxo Operations UK Limited, Великобритания), N-(бутилсульфаонил)-4-[4-(4-пиперидин)бутокси]-α-фенилаланина моно-гидрохлорид моногидрат (Тирофибан, «Аграстат», Correvio, Великобритания), F(ab')2 фрагменты мышиных моноклональных антител FRaMon против рецептора фибриногена тромбоцитов - ГП IIb-IIIa («Монафрам®», ЗАО «Фрамон», Россия) [см. Holmes L.E. A randomized trial assessing the impact of three different glycoprotein IIb/IIIa antagonists on glycoprotein IIb/IIIa platelet receptor inhibition and clinical endpoints in patients with acute coronary syndromes / L.E. Holmes, R. Gupta, S. Rajendran, J. Luu, J.K. French, CP. Juergens // Cardiovasc. Ther. - 2016, N21. doi: 10.1111/1755-5922.12203].
Однако несмотря на то, что данные соединения по результатам клинических исследований оказываются наиболее эффективными в условиях интервеционной кардиологии, применение их ограничено по причине высокой стоимости, развития аутоиммунных реакций [см. Patrono, С.Antiplatelet agents for the treatment and prevention of atherothrombosis / C. Patrono, F. Andreotti, H. Arnesen // European Heart Journal. - 2011. - Vol. 32. - P. 2922-2932].
Наиболее близким аналогом изобретения является DL-лизина ацетилсалицилат, введение раствора которого показало устойчивое торможение агрегации тромбоцитов после приема внутрь в течение 5 минут (почти полное подавление агрегации); аналогичные результаты были получены через 30 минут после приема аспирина [см. Болотова Т.В. и др. Синтез ацетилсалицилатов аминокислот - Бутлеровские сообщения. №3, том 49. 2017 - С. 114-118].
Тем не менее недостатком прототипа является то, что он не проявляет антиагрегационную активность при агрегации тромбоцитов, индуцированной коллагеном.
Задачей изобретения является расширение арсенала биологически активных веществ, проявляющих антиагрегационную активность.
Технический результат - получение средств, проявляющих антиагрегационную активность, расширение спектра их антиагрегационной активности.
Сущность изобретения: применение L-пролина (L-пролиния ацетилсалицилата) или L-тирозина (L-тирозиния ацетилсалицилата) общей формулы:

в качестве средства, проявляющего антиагрегационную активность.
Исследованиями авторов установлено, что соединения Ia и Ib в изо-эквимолярных концентрациях подавляют агрегацию при АДФ-индуцированной агрегации тромбоцитов на 14,3% и 15,3% соответственно, что по уровню соответствует ацетилсалициловой кислоте.
Однако соединение Ia и Ib проявляют антиагрегационную активность и при агрегации тромбоцитов, индуцированной коллагеном, что свидетельствует о более широком спектре антиагрегационной активности. Медианы подавления агрегации для соединения Ia и Ib при коллаген-индуцированной агрегации тромбоцитов составляют 12,1% и 14,7% соответственно.
Таким образом, соединения Ia и Ib оказывают выраженную антиагрегационную активность, превосходящую по уровню и спектру известный препарат, - ацетилсалициловую кислоту.
Соединения Ia и Ib синтезировали следующим образом.
Растворимые соли соединений Ia и Ib получали путем взаимодействия ацетилсалициловой кислоты и L-пролина или L-тирозина в мольном соотношении 1:1. К раствору соответствующей аминокислоты в воде прибавляли суспензию ацетилсалициловой кислоты в ацетоне в соотношении 1: 2, при перемешивании при температуре 20-30°С, при этом наблюдали образование осадка, который растворяли добавлением небольшого количества ацетона. Реакционную смесь выдерживали при перемешивании при той же температуре, до полного растворения ацетилсалициловой кислоты и образования прозрачного раствора. Контроль за ходом реакции осуществляли методом ТСХ (в системе этанол - вода -1:1). По завершении реакции раствор стерилизовали методом бактериальной фильтрации, добавляли ацетон стерилизованный методом бактериальной фильтрации. Полученный раствор охлаждали при температуре от 0° до 6°С в течение 20 ч до образования кристаллов. Выпавшие кристаллы отфильтровывали, промывали стерильным ацетоном (3×3 мл) и сушили при 25°С (30 мм рт.ст.).
Пример 1. Синтез L-Пролиния ацетилсалицилата (Ia).
К раствору 0,92 г L-пролина 115,13 (0,008 моль) в 4 мл воды добавляли суспензию 1,44 г ацетилсалициловой кислоты (0,008 моль) в 3,2 мл ацетона. Полученную смесь перемешивали при комнатной температуре, при этом образовался осадок, который растворяли добавлением 6 мл ацетона. Реакционную смесь выдерживали при этой же температуре. Контроль протекания реакции проводили методом ТСХ (подвижная фаза этанол /вода - 1/1). Затем раствор стерилизовали методом бактериальной фильтрации.
К стерильному раствору реакционной смеси добавляли 15 мл ацетона, стерилизованного методом бактериальной фильтрации. После перемешивания полученный раствор охлаждали при температуре от 0° до 6°С в течение 20 ч до образования кристаллов. Выпавшие кристаллы отфильтровывали, промывали стерильным ацетоном (3×5 мл) и сушили при 25°С (30 мм рт.ст.).
Выход 1,69 г (72%). т. пл. 98-100°С (из водного ацетона). Rf 0,61 (этанол /вода - 1/1).
Элементный анализ. Найдено, %: С 56,8; Н 5,5; N 4,5. C14H17NO6. Вычислено, %: С 57,0 Н 5,8 N 4,7.
Заявляемое соединение представляет собой белое кристаллическое вещество, растворимое в воде, в водном ацетоне, смеси этанол вода 1:1, формулы:
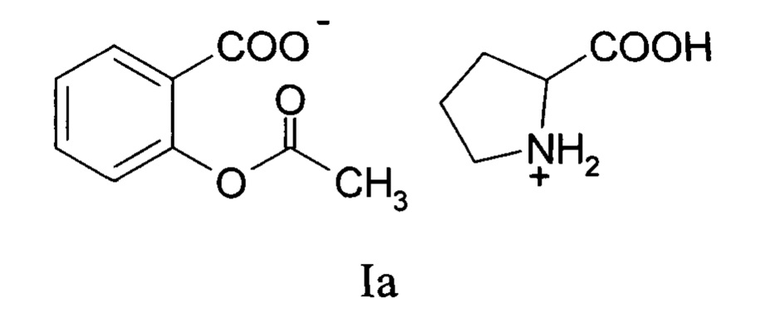
ИК Спектр, ν, см-1:2585 (СООН, Pro, С-С, вал.), 1749 (СООН, Pro, С=O, вал.), 1723 (AcSal, O-(O)СН3, вал.), 1676 (O(O)ССН3, AcSal, С=O, вал.), 1604 (Ar AcSal, С=С, вал.).
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1.85 (2Н, м, СН2(4)); 2.00 (2Н, м, СН2(3)); 2.25 (3Н, д, J=2.5 Гц, СН3); 3,4 (2Н, м, СН2(5)); 4.2 (Н, м, СН(2)); 6.85 (1Н, м, С5Н); 7.3 (1Н, м, С3Н); 7.65 (1Н, т, J=1.5 Гц, С4Н); 7.9 (1Н, д, J=1.5 Гц, С6Н); 8.5 (1H,NH2+).
Пример 2. Синтез L-Тирозиния ацетилсалицилата (Ib).
К раствору 0,6 г тирозина (0,003 моль) в 2 мл воды добавляли суспензию 0,59 г ацетилсалициловой кислоты (0,003 моль) в 3,4 мл ацетона. Полученную смесь перемешивали при комнатной температуре, при этом образовался осадок, который растворяли добавлением 12 мл ацетона. Реакционную смесь выдерживали при этой же температуре. Контроль протекания реакции проводили методом ТСХ (подвижная фаза этанол /вода -1/1). Затем раствор стерилизовали методом бактериальной фильтрации.
К стерильному раствору реакционной смеси добавляли 15 мл ацетона, стерилизованного методом бактериальной фильтрации. После перемешивания полученный раствор охлаждали при температуре от 0° до 6°С в течение 20 ч до образования кристаллов. Выпавшие кристаллы отфильтровывали, промывали стерильным ацетоном (3×3 мл) и сушили при 25°С (30 мм рт.ст.).
Выход 0,45 г (38%),т. пл. 250°С. (из водного ацетона).
Элементный анализ. Найдено, %: С 59,8; Н 4,8; N 3,7. C18H18NO6
Вычислено, %: С 60,0; Н 5,0; N 3,9.
ИК Спектр, ν, см-1: 3192 (NH3+, вал.), 1730 (СООН, Tyr, С=O, вал,), 1628 (О-С(О)СН3, AcSal, С=O, вал.), 1615 ν(COO-, AcSal, С=O, вал.), 1605 (Ar, AcSal, C=C вал.), 1585 δ(Ar, AcSal C=C, деф.).
Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 2.37 с. (3Н, 3СН3), J=3.2 Гц; 2.39 с. (3Н, СН3); 3.04 м. (2Н, СН2, СН3), J=9,2 Гц; 4.29 т.(1Н, СН), J=6.5 Гц; 6.56 м. (2Н, СН3), J=3.3 Гц; 6.96 м. (3Н, СН3), J=6.4 Гц; 7.56 т.д. (1Н, СН3), J=9.0 Гц; 7.83 д.д. (1Н, СН3), J=6.1 Гц; 7.88 м. (2Н, СН3), J=6.3 Гц; 8.62 с. (1Н, NH3+); 9.18 с. (1Н, СН3).
Заявляемое соединение представляет собой белое кристаллическое вещество, растворимое в воде, в водном ацетоне, смеси этанол вода 1:1, формулы:
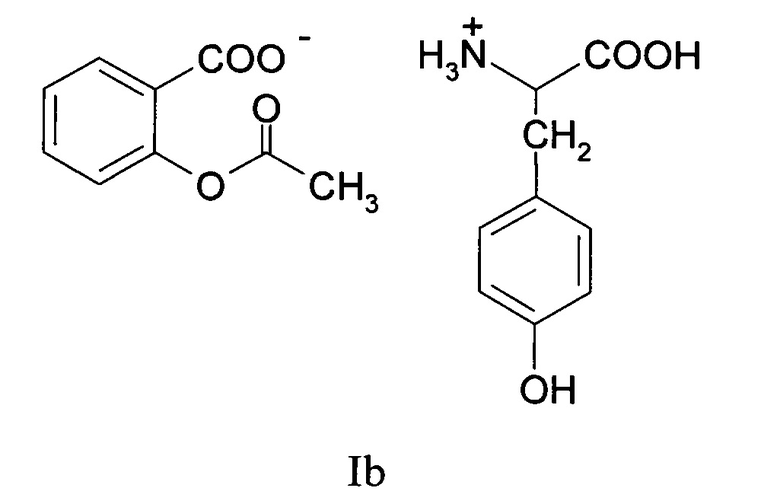
Пример 3. Антиагрегационная активность соединений Ia и Ib. Антиагрегационная активность соединений Ia и Ib исследовалась следующим образом. Эксперименты в условиях in vitro выполнены на крови здоровых доноров-мужчин в возрасте 18-24 лет. Общее количество доноров составило 68 человек. Забор крови проводился из кубитальной вены с использованием систем вакуумного забора крови BD Vacutainer® (Becton Dickinson and Company, США). В качестве стабилизатора венозной крови использовался 3,8% раствор цитрата натрия в соотношении 9:1.
Все тесты проводились на обогащенной и обедненной тромбоцитами плазмах. Образцы богатой тромбоцитами плазмы получали центрифугированием цитратной крови при 1000 об/мин в течение 10 минут, бестромбоцитарной плазмы - при 3000 об/мин в течение 20 минут. В работе использовалась центрифуга ОПН-3.02 (ОАО ТНК "ДАСТАН", Киргизия).
Исследование влияния на агрегацию тромбоцитов проводили по методу Born (Born G.G.V.Nature (London). – 1962 - V. 194.) на агрегометре "Thromlite-1006A" (Россия) и лазерном анализаторе агрегации тромбоцитов "Биола 230LA" (ООО НПФ «БИОЛА», Россия). Определение антиагрегационной активности исследуемых веществ и препаратов сравнения проводили в конечной концентрации 2×10-3 моль/л. В качестве препарата сравнения использовали ацетилсалициловую кислоту («Ацетилсалициловая кислота», Фармацевтическая фабрика Шандонг Ксинхуа Фармасьютикал Ко., ЛТД, Китай). В качестве индукторов агрегации использовали аденозиндифосфат (АДФ) в концентрации 20 мкг/мл и коллаген в концентрации 5 мг/мл производства "Технология-Стандарт" (Россия, г. Барнаул).
Результаты исследования обработаны с применением статистического пакета Statistica 10,0 (StatSoft Inc, США). Проверку на нормальность распределения фактических данных выполняли с помощью критерия Шапиро-Уилка. Выявлено, что вид распределения полученных данных отличается от нормального, поэтому при дальнейшей работе использовались непараметрические методы. Данные представлены в виде медианы, 25 и 75 процентилей. Дисперсионный анализ проводили с помощью критерия Краскела-Уоллиса. Критический уровень значимости р для статистических критериев принимали равным 0,05.
По результатам исследования установлено, что ацетилсалициловая кислота в скрининговой концентрации 2×10-3 моль/л проявила выраженную антиагрегационную активность лишь на одном индукторе агрегации: при АДФ-индуцированной агрегации регистрировалась антиагрегационная активность равная 13,5%, при коллаген-индуцированной агрегации тромбоцитов активность не проявлялась.
Соединения Ia и Ib в изоэквимолярных концентрациях подавляли агрегацию АДФ-индуцированной агрегации тромбоцитов на 14,3% и 15,3%) соответственно, что по уровню соответствует ацетилсалициловой кислоте. Однако соединения Ia и Ib проявляют антиагрегационную активность и при агрегации тромбоцитов, индуцированной коллагеном, что свидетельствует о более широком спектре антиагрегационной активности. Медианы подавления агрегации для соединений Ia и Ib при коллаген-индуцированной агрегации тромбоцитов составляют 12,1% и 14,7% соответственно (таблица).
Таким образом, соединения Ia и Ib оказывают выраженную антиагрегационную активность, превосходящую по уровню и спектру аналоговый препарат - ацетилсалициловую кислоту.
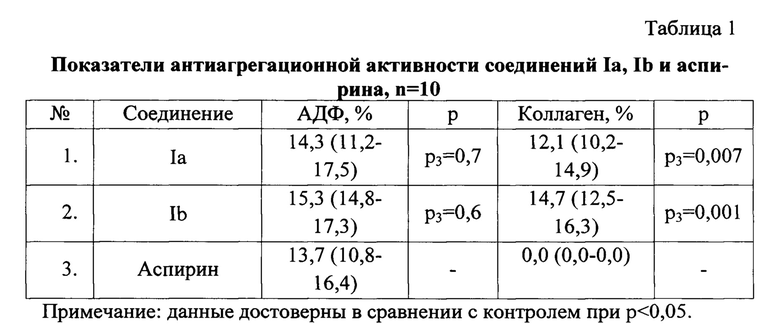
Уровень статистической значимости различий в сравнении аспирином.
| название | год | авторы | номер документа |
|---|---|---|---|
| Производные 1-(3,5-ди-трет-бутил-4-гидроксибензил)изатина, обладающие антиагрегационной активностью | 2023 |
|
RU2822271C1 |
| L-аланиния ацетилсалицилат, проявляющий антикоагуляционную активность | 2019 |
|
RU2703513C1 |
| Производные триазола, проявляющие антиагрегационную активность | 2021 |
|
RU2770405C1 |
| ЦИКЛОГЕКСИЛАММОНИЕВАЯ СОЛЬ [3-МЕТИЛ-1-Н-ПРОПИЛ-7-(1-ОКСОТИЕТАНИЛ-3)КСАНТИНИЛ-8-ТИО]УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩАЯ АНТИТРОМБОТИЧЕСКУЮ АКТИВНОСТЬ | 2011 |
|
RU2459826C1 |
| N'-ПИРИДИН-4-ИЛМЕТИЛЕН-2-[6-МЕТИЛ-4-(ТИЕТАН-3-ИЛОКСИ)ПИРИМИДИН-2-ИЛТИО]АЦЕТОГИДРАЗИД, ОБЛАДАЮЩИЙ АНТИАГРЕГАЦИОННОЙ И АНТИКОАГУЛЯЦИОННОЙ АКТИВНОСТЬЮ | 2024 |
|
RU2825129C1 |
| Средство с антиагрегационной активностью и способ его получения | 2021 |
|
RU2778686C1 |
| Антиагрегационное и антиоксидантное средство | 2023 |
|
RU2808474C1 |
| Способ получения антиагрегационного и антиоксидантного средства | 2023 |
|
RU2819387C1 |
| ПРИМЕНЕНИЕ 5,7-ДИГИДРОКСИ-6,8-ДИМЕТИЛФЛАВАНОНА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2812630C1 |
| СОЛИ [3-МЕТИЛ-1-Н-ПРОПИЛ-7-(1,1-ДИОКСОТИЕТАНИЛ-3)КСАНТИНИЛ-8-ТИО]УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ПРОАГРЕГАНТНУЮ АКТИВНОСТЬ | 2011 |
|
RU2459825C1 |
Изобретение относится к химии и медицине, а именно к фармацевтической химии и фармакологии, и может быть использовано для создания новых лекарственных средств профилактики тромбоза и тромбоэмболических осложнений. Сущность изобретения: применение L-пролина (L-пролиния ацетилсалицилата) или L-тирозина (L-тирозиния ацетилсалицилата) общей формулы, приведенной ниже, в качестве средства, проявляющего антиагрегационную активность. Соединения по изобретению проявляют антиагрегационную активность, превосходящее ацетилсалициловую кислоту (см. табл. 1).

3 пр., 1 табл.
Применение L-пролина (L-пролиния ацетилсалицилата) или L-тирозина (L-тирозиния ацетилсалицилата) общей формулы:
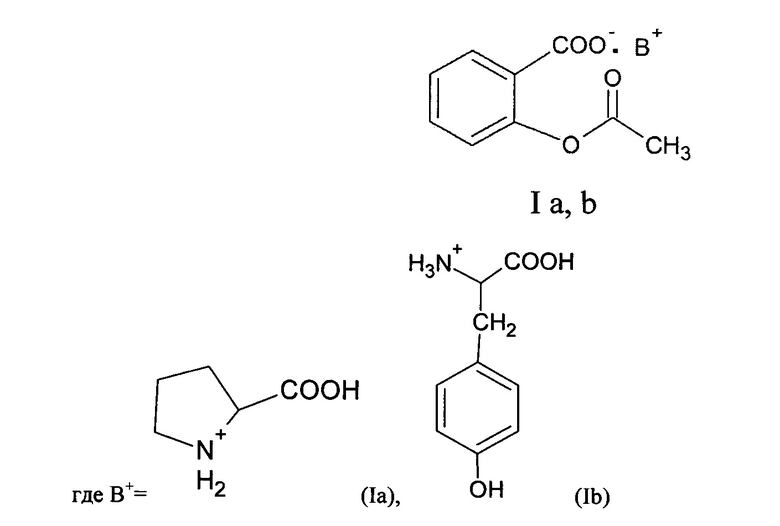
в качестве средства, проявляющего антиагрегационную активность.
| Болотова Т.В | |||
| и др | |||
| "Синтез ацетилсалицилатов аминокислот" Бутлеровские сообщения, 3, 49, 2017, 31.03.2017, с | |||
| Способ получения борнеола из пихтового или т.п. масел | 1921 |
|
SU114A1 |
Авторы
Даты
2020-07-22—Публикация
2019-02-18—Подача