Изобретение относится к медицине, в частности к экспериментальной фармакологии.
Прототипом заявленного решения является способ коррекции неврологического статуса солями гамма-оксимасляной кислоты при моделировании травматического повреждения головного мозга у крыс (Литвинов А.А. Церебропротекторные свойства солей гамма-оксимасляной кислоты и некоторые аспекты механизма их действия: дис. к-та фарм. наук: 14.03.06 / А.А. Литвинов. – Волгоград, 2015. – 196 с. (90-99). Механизм их действия заключается в том, что являясь производными ГАМК (гамма-аминомаслянной кислоты), которая является естественным медиатором, оказывают влияние на дофаминергическую и ГАМК-ергическую системы, обладают антигипоксическим действием, снижают интенсивность процессов перекисного окисления липидов и повышение активности ключевых ферментов антиоксидантной системы, таких как супероксиддисмутазы, каталазы. Помимо этого соли ГОМК приводят к усилению утилизации глюкозы мозгом и снижению скорости и степени агрегации тромбоцитов (Литвинов А.А. Церебропротекторные свойства солей гамма-оксимасляной кислоты и некоторые аспекты механизма их действия: дис. … к-та фарм. наук: 14.03.06 / А.А. Литвинов. – Волгоград, 2015. – 196 с. (29-33, 160-167).
Вторичные повреждения головного мозга при травматическом повреждении могут достигать 2/3 от общей зоны поражения [Zhang X., Satchell M.A., Clark R.S.B., Nathaniel P.D., Kochanek P.M., GrahamS.H.Apoptosis // In:Clark R.S.B, Kochanek P.M., editor. In Brain Injury. Boston: Kluwer Academic Publishers. – 2001. – Р. 199–230] и [Robertson G., Crocker S., Nicholson D.Neuroprotection by the inhibition of apoptosis // BrainPathol. – 2000. – Vol. 10, № 2. – P. 283-292]. Основными факторами, определяющими степень вторичного повреждения нервной ткани при травматическом повреждении головного мозга, являются эксайтотоксичность (токсическое влияние высокого содержания «возбуждающих» аминокислот), воспаление, образование реактивных свободных радикалов кислорода, активация перекисного окисления липидов и запуск механизмов «программируемой» гибели клеток (апоптоза):
1. Кабанов А.А. Нейропротекция при травмах центральной нервной системы // Лечебное дело. – 2011. – №2. – С.59-68.
2. Крылов В.В., Пурас Ю.В. Патофизиологические механизмы вторичного повреждения мозга при черепно-мозговой травме // Неврологический журнал. – 2013. – № 4. – С.4-7.
3. Мороз В.В., Кармен Н.Б., Маевский Е.И. Механизмы вторичного повреждения нейронов при тяжелой черепно-мозговой травме (часть 2) // Общая реаниматология. – 2011. – VII, 5. – С.42-45.
Неотъемлемой частью эксайтотоксичности является перегрузка клетки кальцием, образование свободных радикалов, открытие метахондриальной макропоры через которые выходят протеолитические ферменты апоптоза.
Поэтому способ коррекции неврологического статуса солями гамма-оксимасляной кислоты при моделировании травматического повреждения головного мозга у крыс является не удовлетворительным.
Задачей изобретения является создание эффективного способа коррекции неврологического дефицита при экспериментальной модели травматического повреждения головного мозга (а именно черепно-мозговой травмы - ЧМТ), включающего использование нового производного этилтиадиазола - 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноата (лабораторный шифр ЛХТ 12-18).
Синтез нового соединения осуществляли путем взаимодействия эквимолярных количеств 2-амино-5-этил-1,3,4-тиодиазола с N-ацетил-аминоэтановой кислотой.
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником, загружают 65 мл пропанола-2. Затем при перемешивании постепенно добавляют 2,58 г (0,02 м) 2-амино-5-этил-1,3,4-тиодиазола, к раствору постепенно добавляют 2,34 г (0,02 м)N-ацетил-аминоэтановой кислоты. Реакционную массу перемешивают при 45-50°С в течение 30 минут. Полученный раствор фильтруют, в вакууме отгоняют пропанол-2, полученный осадок перекристаллизовывают из смеси пропанола-2:ацетон (9:1). Осадок сушат до постоянной массы. Получают 3,98 г (81%) белого кристаллического порошка с Т плав. = 159 — 161°C.
Найдено, %: С 39,01; Н 5,76; N 22,77; S 12,98
C8H14N4SO3 м.м. 246,29
Вычислено, %: С 39,02; Н 5,73; N 22,75;S 13,02; О 19,48
ИК, ν, см-1: 3405, 3210 (NH). 2970, 2890 (СН), 2420 (N+), 1590 (C=N), 1560 (COO-).
УФ: 0,002% раствор в воде максимум поглощения при 238±2 нм.
ТСХ: на пластинах Silicagel УФ 254 в системе растворителей этанол:хлороформ:аммиак-3:1:1 (одно пятно).
Задача решается предложенным способом коррекции патологии при экспериментальной модели травматического повреждения головного мозга - ЧМТ, с использованием 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноата, который вводили курсом 3 суток, в дозе 50 мг/кг, однократно, первый раз - за 30 мин до моделирования патологии, с последующим введением в течение 2-х суток в одно и тоже время.
Это приводит к выраженной коррекции неврологического дефицита при моделируемой патологии.
Техническим результатом предлагаемого изобретения является коррекции неврологического дефицита новым производным этилтиадиазола2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноатом при травматическом повреждении головного мозга - ЧМТ, который вводили в дозе 50 мг/кг курсом 3 дня, первый раз - за 30 мин до моделирования патологии, обладающего антиоксидантной и антигипоксической активностью и блокирующем активацию свободнорадикальных процессов, а также перекисного окисления липидов клеточных мембран, при острых нарушений регионального и общего кровообращения. Способ приводит к выраженной коррекции последствий травматического повреждения головного мозга.
СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ
Травматическое повреждение головного мозга (ЧМТ) вызвали у крыс мужского пола с массой тела 270±20 г [Соколова Т.Ф., Редькин Ю.В. Способ нанесения дозированной закрытой черепно-мозговой травмы у белых крыс // Вопросы нейрохирургии. – 1986. – №2. – С. 68–6]. В работе была воспроизведена техника моделирования черепно-мозговой травмы у крыс при помощи метода свободного падения груза массой 155 грамм с высоты 0,6 м. Установка содержит стойку, которая состоит из полой трубы длинной 1,1 м, зажатой в штативе в вертикальном положении. У нижнего края трубы располагается боек со стопором. В полость трубы на заданную высоту размещали груз. Локализацию удара осуществляли согласно анатомии головного мозга у крыс. Место осуществления удара локализировалось в лобно-теменно-височной области левого полушария ГМ. Голову грызуна жестко не закрепляли. Данная модель позволяет воспроизвести модель ЧМТ максимально приближенную к аналогичной у человека.
Воспроизводилась травма, соответствующая средней степени тяжести (по шкале оценки McGraW в модификации И.В. Ганнушкиной, 2,5-5,5 балла) 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноата (ВНЦ БАВ, Россия, Старая Купавна). Производное этилтиадиазола – ЛХТ 12-18 вводили в дозе 50 мг/кг (подбор дозы осуществлялся экспериментальным путем), курсом 3 дня, первый раз - за 30 мин до моделирования патологии. Вещество растворяли с помощью 1% крахмального раствора и вводили внутрижелудочно через металлический зонд с гладкой оливой на конце. Далее осуществляли моделирование патологии.
Спустя сутки после моделирования ЧМТ запускали оценку показателей неврологического дефицита по шкале McGraW в модификации И.В. Ганнушкиной и по шкале mNSS 1-е, 2-е, 3-е и 7-е сутки после травматического повреждения головного мозга.
Шкала McGraw в модификации И.В. Ганнушкиной представлена перечнем проявлений неврологических нарушений. Анализируемые показатели суммировались. В зависимости от итоговой суммы, неврологический дефицит можно обозначить по-разному: сумма баллов 0,5-2,0 соответствует легкой степени дефицита; 2,5-5,0 – средней степени тяжести; 5,5-10 тяжелой степени неврологического дефицита. Оценка производилась на 1, 3 и 7 сутки эксперимента.
Таблица 1
Шкала оценки неврологического дефицита по McGraw в модификации И.В. Ганнушкиной (1996)

Для оценки неврологического дефицита через 48 ч после моделирования ЧМТ был проведен модифицированный тест оценки неврологического дефицита. Шкала mNSS – (modified neurologicalseverityscore) – это особая система интерпретации неврологического дефицита при имеющейся травме ГМ. Она используется для оценки моторного, сенсорного, балансового и рефлекторного поведения животных [Chen J., Sanberg P.R., Li Y. Et al. Intravenous administration of human umbilical cord blood reduces behavioral deficits after stroke in rats. Stroke. 2001; 32: 2682-2688. doi: 10.1161/hs1101.098367]. Согласно данной неврологической шкале выполняли подвешивание грызунов за хвост (чтобы определить наличие парезов и параличей), оценивали двигательную активность в домашней клетке (для регистрации нарушений походки и стереотипных движений) и особенности передвижения на горизонтальной балке (для проведения оценки координации движений), проверяли сохранность основных рефлексов (стартл-рефлекс, рефлекс наружного слухового прохода, роговичный рефлекс). Результаты исследования по определению неврологического дефицита формулировали исходя из суммы баллов, набранных в каждом тесте. Более высокий балл указывает на более тяжелую травму. Суммарное количество баллов в диапазоне от 1 - 6 указывает на наличие ЧМТ легкой степени тяжести, от 7 до 12 - средней, а сумма баллов 13-18 показывает наличие тяжелой ЧМТ.
Таблица 2
Модифицированная шкала тяжести неврологической симптоматики mNSS

При статистической обработке данных рассчитывается среднее значение, величину стандартного отклонения. Различия считаются достоверными при p<0,05.
ПРИМЕР КОНКРЕТНОГО ВЫПОЛНЕНИЯ.
Оценку влияния ЛХТ 12-18 в дозе 50 мг/кг на неврологический дефицит животных после моделирования черепно-мозговой травмы исследовали с применением балльной шкалы McGraw в модификации И.В. Ганнушкиной и шкалы оценки неврологического дефицита mNSS.
У животных интактной группы наблюдали отсутствие неврологического дефицита. За контроль принимали группу животных с патологией без фармакологической коррекции. В данной группе в 1 сутки отмечался неврологический дефицит средней степени тяжести - 4,04 балла, с тенденцией к ухудшению степени тяжести до тяжелой к 7-м суткам до 6,08 балла.
Спустя 1 сутки после моделирования патологии тяжелую степень неврологического дефицита регистрировали в группе контроля (4,04 балла). В группе крыс с применением ЛХТ 12-18 неврологический дефицит был легкой степени тяжести (2,96 балла).
На 3 сутки эксперимента в контрольной группе наблюдали ухудшение неврологического статуса. В группе с применением ЛХТ 12-18(2,73балла) ухудшения неврологического дефицита не наблюдалось.
На 7-е сутки эксперимента наблюдали снижение показателей неврологического дефицита в группе с коррекцией ЛХТ 12-18 (2,46 балла).
Введение крысам исследуемого соединения ЛХТ 12-18 в условиях экспериментальной ЧМТ приводило к выраженному уменьшению выраженности неврологического дефицита у крыс по отношению к контролю. Статистически значимо (p<0,05) регистрировали снижение степени тяжести неврологического дефицита группы животных с применением ЛХТ 12-18 в дозе 50 мг/кг в сравнении с группой контроля (таблица 3).
Таблица 3
Влияние ЛХТ 12-18 на тяжесть неврологического дефицита у крыс по шкале McGraw в модификации И.В. Ганнушкиной (1996) (по среднему значению балла в группе) (n=13)
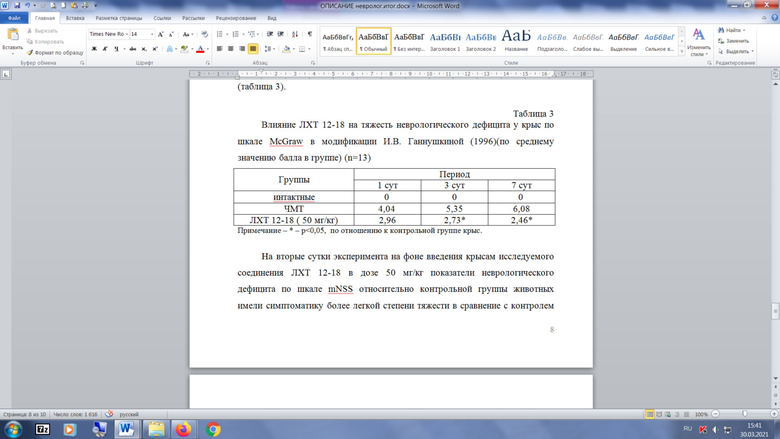
На вторые сутки эксперимента на фоне введения крысам исследуемого соединения ЛХТ 12-18 в дозе 50 мг/кг показатели неврологического дефицита по шкале mNSS относительно контрольной группы животных имели симптоматику более легкой степени тяжести в сравнение с контролем (p<0,05) (таблица 4). Крысы группы с применением ЛХТ 12-18 обладали более выраженными моторными навыками в сравнение с животными контрольной группы.
Таблица 4
Влияние ЛХТ 12-18 на тяжесть неврологического дефицита у крыс по шкале тяжести неврологической симптоматики mNSS (по среднему значению балла в группе) (n=13)
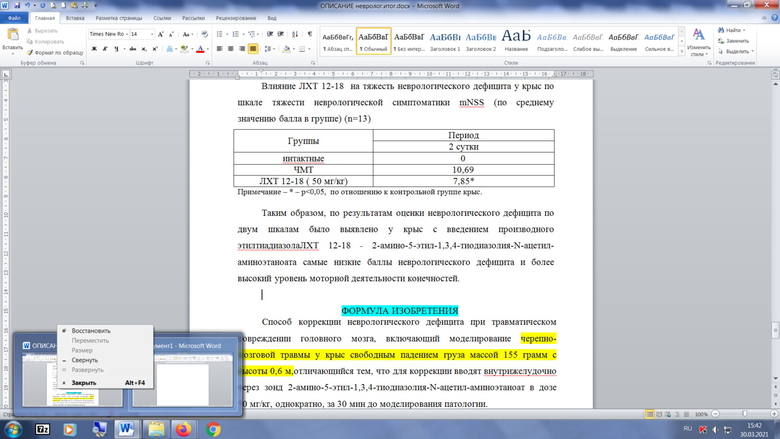
Таким образом, по результатам оценки неврологического дефицита по двум шкалам было выявлено у крыс с введением производного этилтиадиазола ЛХТ 12-18 - 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноата который вводили в дозе 50 мг/кг курсом 3 дня, первый раз - за 30 мин до моделирования патологии, самые низкие баллы неврологического дефицита и более высокий уровень моторной деятельности конечностей.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ коррекции неврологического дефицита 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноатом при травматическом повреждении головного мозга | 2021 |
|
RU2758433C1 |
| Способ коррекции поведенческого статуса 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноатом при травматическом повреждении головного мозга | 2021 |
|
RU2756325C1 |
| Способ коррекции поведенческого статуса 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноатом при повреждении головного мозга | 2021 |
|
RU2763012C1 |
| Способ коррекции неврологического дефицита при травматическом повреждении головного мозга | 2021 |
|
RU2758245C1 |
| Способ коррекции морфологических изменений при травматическом повреждении головного мозга | 2021 |
|
RU2758545C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ | 2018 |
|
RU2696203C1 |
| Способ коррекции неврологического статуса 2-этил-6-метил-3- гидрокси пиридиния-N-ацетиламиноацетатом при повреждении головного мозга вследствие внутримозгового кровоизлияния в эксперименте | 2022 |
|
RU2786315C1 |
| Способ коррекции ишемии головного мозга субстанцией рапиталама в эксперименте | 2019 |
|
RU2711906C1 |
| Способ лечения черепно-мозговой травмы и средство для его осуществления | 2023 |
|
RU2826364C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИШЕМИИ ГОЛОВНОГО МОЗГА | 2017 |
|
RU2642961C1 |
Изобретение относится к медицине, в частности к экспериментальной фармакологии. Способ коррекции неврологического дефицита при травматическом повреждении головного мозга включает моделирование черепно-мозговой травмы у крыс свободным падением груза массой 155 грамм с высоты 0,6 м. Для коррекции патологии вводят внутрижелудочно через зонд 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноат, курсом 3-е суток, в дозе 50 мг/кг, однократно, первый раз за 30 мин до моделирования патологии, с последующим введением в течение 2-х суток. Способ приводит к выраженной коррекции последствий травматического повреждения головного мозга. 4 табл., 1 пр.
Способ коррекции неврологического дефицита при травматическом повреждении головного мозга, включающий моделирование черепно-мозговой травмы у крыс свободным падением груза массой 155 г с высоты 0,6 м, характеризующийся тем, что для коррекции патологии вводят внутрижелудочно через зонд 2-амино-5-этил-1,3,4-тиодиазолия-N-ацетил-аминоэтаноат, курсом 3-е суток, в дозе 50 мг/кг, однократно, первый раз - за 30 мин до моделирования патологии, с последующим введением в течение 2-х суток.
| Способ коррекции ишемии головного мозга субстанцией рапиталама в эксперименте | 2019 |
|
RU2711906C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ | 2018 |
|
RU2696203C1 |
| МАРТЫНОВА О.В | |||
| и др., Исследование нейродинамических нарушений у крыс при черепно-мозговой травме / Научные результаты биомедицинских исследований, 2019,т.5, N.3 | |||
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| МАРТЫНОВА О.В | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2022-03-15—Публикация
2021-05-28—Подача