Изобретение относится к производным целлюлозы, а также к сульфатированным полисахаридам и гибридным макромолекулярным антиоксидантам, проявляющим биологическую активность и способу их получения. Изобретение может быть использовано для создания эффективных лекарственных препаратов комбинированного действия для купирования патологических свободно-радикальных процессов, приводящих к дисфункции клеток крови и сердечно-сосудистой системы.
Известно, что патооксидантные процессы вызывают и сопровождают хронические нарушения микроциркуляции крови и лимфы. Вызванные ими патологии микроциркуляции приводят к тяжелым заболеваниям сердечно-сосудистой системы, когнитивным и другим нарушениям, являются наиболее распространенными причинами смертности и инвалидности в мире. Известно также о влиянии интенсификации свободно-радикальных процессов на дисфункцию эндотелия сосудов, роль которого существенна в общем гемостазе. Поэтому эффективная терапия при рассматриваемых патологиях должна включать подход с использованием комбинированных лекарственных препаратов, обладающих органопротекторными, эндотелийпротекторными и антиоксидантными свойствами. Для профилактики и лечения повреждений микрососудов и обменных процессов в них перспективны водорастворимые макромолекулы с привитыми антиоксидантами.
Наиболее востребованный тип структур при создании гибридных полимерных антиоксидантов - это фенолы различного строения, тем или иным методом конъюгированные с макромолекулярными носителями. Усиление антиоксидантных свойств фенолов может быть достигнуто введением алкильных групп в арильную структуру. Многие из эффективных синтетических антиоксидантов данного типа (алкилфенолов) отличаются доступностью, безопасностью, отсутствием цвета и запаха [Koltover V.K. Antioxidant biomedicine: from free radical chemistry to systems biology mechanisms. Russian Chemical Bulletin, International Edition. 2010. 59(1). 37-42. https://doi.org/10.1007/s11172-010-0042-2]. Фенолы с объемными алкильными заместителями представляют собой, как правило, гидрофобные соединения. Одним из методов их гидрофилизации и создания препаратов с заданной активностью и способностью к циркуляции в кровяном русле является конъюгирование с водорастворимыми полимерами, прежде всего с полисахаридами. Установлено повышение стабильности и активности иммобилизованных на полимерной платформе алкилфенолов, снижение их токсичности по сравнению с низкомолекулярными предшественниками, отмечен эффект создания высоких локальных концентраций. Конъюгированные с полисахаридами антиоксиданты проявляют антирадикальную активность и способны регулировать процессы перекисного окисления липидов (ПОЛ) в клеточных мембранах [Filippov S.K., Sergeevaa O. Yu., Vlasov P.S. et al. Modified hydroxyethyl starch protects cells from oxidative damage. Carbohydrate Polymers. 2015. 134. 314-323. https://doi.org/10.1016/j.carbpol.2015.07.062; Власов П.С., Сергеева О.Ю., Домнина Н.С., Чукичева И.Ю., Буравлев Е.В., Кучин А.В. Макромолекулярные антиоксиданты на основе полисахаридов и производных 2,6-диизоборнил-4-метилфенола // Химия природных соединений. 2012. 4. 481-484].
Известны способы получения полимерных антиоксидантов на основе полисахаридов с привитыми алкилфенолами для биомедицинского применения. В патенте [RU 2273483] описывается водорастворимый полимерный антиоксидант - плазмозаменитель, способ поддержания уровня артериального давления и процессов антиоксидантной защиты в организме при острой кровопотере. Фрагмент пространственно-затрудненного фенола - β-(4-гидркоси-3,5-дитретбутилфенил)-пропионил или β-(4-гидрокси-3,5-дитрет.бутилфенил)-α-(N-бензоиламино)-акрилоил. В качестве нейтральных полисахаридов-носителей использованы модифицированный крахмал или пуллулан, известные как плазмозаменители. Содержание алкилфенолов не превышало для модифицированного гидроксиэтилированного крахмала 10 мас.%, а для модифицированного пуллулана 12 мас.%. Цель данной разработки - купировать негативные последствия высокой концентрации свободных радикалов, приводящих к некробиотическим изменениям тканей при острой кровопотере.
Нейтральные полисахариды и алкилфенолы использованы несколькими исследовательскими группами для синтеза полимерных антиоксидантов на их основе. Получены конъюгаты декстрана, гидроксиэтилкрахмала и диалкилоксиарилов различных типов. Предложено применение гибридного макромолекулярного антиоксиданта на основе декстрана ((1→6)-α-D-глюкан) с молекулярной массой 40 кДа и дигидрокверцетина в качестве гемореологического средства [Патент RU 2473348]. В патентах [RU 2497828, RU 2619934, RU 2347561] описывается водорастворимый конъюгат гидроксиэтилкрахмала, модифицированный фрагментами Диборнола™ (2,6-диизоборнил-4-метилфенола). Диборнол - терпенофенол, антиоксидант из группы алкилзамещенных фенолов - проявляет выраженную биологическую активность и эффективно ингибирует последствия патогенных оксидантных процессов - снижает вязкость крови и агрегацию эритроцитов, оказывает антитромбоцитарное и антитромбогенное действие и предотвращает развитие тромбофильного состояния и ретромбозы в органах при терапии.
Природные и синтетические сульфатированные полисахариды представляют собой перспективную платформу для создания полимерных антиоксидантов с конъюгированными диалкилфенолами, с дальнейшей возможностью применения в изделиях, контактирующих с человеком, а также в области медицины. Это связано с тем, что сами по себе природные и синтетические сульфатированные полисахариды проявляют широкий спектр биологической активности: антикоагулянтную, противовирусную, гиполипидемическую, демонстрируют противовоспалительные и антиоксидантные свойства [Zhang Q., Lin D., Yao S. Review on biomedical and bioengineering applications of cellulose sulfate. Carbohydrate Polymers. 2015. 132. 311-322. https://doi.org/10.1016/j.carbpol.2015.06.041].
Сульфат целлюлозы (СЦ) - наиболее исследуемый в ряду искусственных сульфатированных полисахаридов. Причинами такого интереса к нему являются разнообразие свойств и доступность полисахарида-основы. После введения сульфатных групп в макромолекулу целлюлозы получают водорастворимый полисахарид, способный к модификации реологии растворов, образованию пленок и обладающий разнообразной биологической активностью. Перспектива модификации СЦ диалкилфенолами состоит в возможности получения полиэлектролитных платформ, обладающих свойствами биоантиоксидантов. Так, ранее продемонстрирована противовоспалительная активность ионных конъюгатов, синтезированных на основе смешанного эфира СЦ [Chukicheva I. Yu., Buravlev E.V., Torlopov M.A., Vikharev Yu. B., Anikina L.V., Grishko V.V. Ionic Conjugates of Sulfate Carboxymethyl Cellulose with Dialkylaminomethyl Derivatives of 2-lsobornyl-4-Methylphenol: Synthesis and Study of Anti-Inflammatory and Analgesic Activity. Russian Journal of Bioorganic Chemistry. 2012. 38 (6). 647-651. https://doi.org/10.1134/S1068162012040048].
В описании патента [RU 2174985], выбранного за прототип, описываются различные анионные полисахариды, модифицированные ковалентно присоединенными антиоксидантами, в том числе из группы алкилфенолов, а именно ди-трет-бутилфенолами. В качестве полисахаридов-носителей предлагается использовать, в том числе сульфатированные полисахариды, такие как гепарин, хондроитинсульфат, гепарансульфат, кератансульфат. Модифицированные таким образом полисахариды предлагается использовать для лечения суставов млекопитающих, для ускорения заживления хронических ран и язв, предотвращения послеоперационных спаек. В примере указывается, что при синтезе натриевые соли кислых полисахаридов могут быть превращены метилтрикаприламмониевые соли для увеличения растворимости в органических растворителях. После реакции прививки антиоксиданта, тетраалкиламмониевую соль, модифицированного антиоксидантом, можно снова превратить в натриевую форму ионным обменом. Однако в данном патенте не приведены сведения, подтверждающие антиоксидантную активность синтезированных соединений. Среди предлагаемых для конъюгирования структур низкомолекулярных антиоксидантов в описываемом изобретении нет диалкилфенолов с терпеновыми заместителями, а среди анионных полимеров нет сульфатированных производных целлюлозы. Макромолекулярные антиоксиданты, полученные путем конъюгирования Диборнола и анионных, в том числе сульфатированных полисахаридов, ранее описаны не были.
Технический результат состоит в получении сульфатированного полисахарида в нескольких вариантах состава и его реализация в качестве биологически активного средства. Новое соединение имеет низкую цитотоксичность, повышенную эффективность в купировании деструктивных изменений компонентов крови, вызванных патологическими процессами, обладает высокой антиоксидантной, мембранопротекторной активностью, заключающейся в способности эффективно защищать клетки крови в условиях острого окислительного стресса.
Технический результат достигается тем, что получено новое соединение - сульфатированный полисахарид структуры I с ковалентно присоединенным фрагментом 2,6-диизоборнил-4-метилфенола структуры II
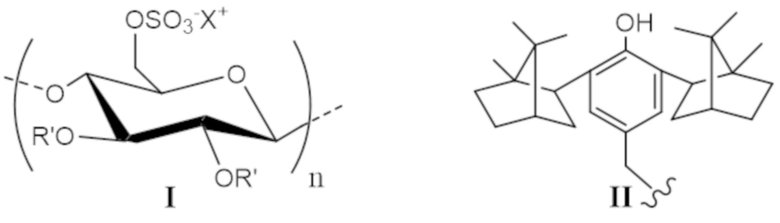
где: R' = структура II;
X = Na+ или (Bu)4N+.
Полученный сульфатированный полисахарид с содержанием фрагмента II от 0,3 мас.% до 5,8 мас.% может быть использован в качестве средства, обладающего антирадикальной, антиоксидантной и мембранопротекторной активностью, заключающейся в способности эффективно защищать клетки крови в условиях острого окислительного стресса, а также для защиты сердечно-сосудистой системы.
Способ получения сульфатированного полисахарида, указанного выше, заключается в том, что свободные гидроксильные группы сульфата целлюлозы в виде тетрабутиламмониевой соли O-алкилируют 4-бромометил-2,6-диизоборнилфенолом, при этом для получения натриевой формы структуры I осуществляют ионный обмен.
Сульфат целлюлозы - полисахарид для синтеза заявляемого полимерного антиоксиданта представляет собой производное целлюлозы, содержащее одну или более сульфатных групп в статистическом мономерном звене в виде натриевой или тетрабутиламмониевой соли. Введенный в структуру сульфата целлюлозы терпенофенол представляет собой фрагмент 2,6-диизоборнил-4-метилфенола (4-метилоксиметил-2,6-ди(1,7,7-триметилбицикло [2.2.1] гептан-2-ил)фенола, который связан с полимерной цепью простой эфирной связью. Фрагменты терпенофенола связаны, по меньшей мере, с одной гидроксильной группой полисахарида. Способ получения включает О-алкилирование тетрабутиламмониевых солей сульфата целлюлозы бромопроизводным Диборнола (4-бромометил-2,6-ди-изоборнилфенолом - 4-бромометил-2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)фенолом).
Анализ известного технического уровня не выявил технических решений с совокупностью признаков по реализации вышеописанного результата, что свидетельствует о соответствии заявляемого технического решения критериям «новизна», «изобретательский уровень».
Настоящее изобретение осуществляется следующим образом.
Пример 1. Общий способ получения заявляемого полимерного антиоксиданта на основе сульфата целлюлозы в виде амфифильной тетрабутиламмониевой соли
Тетрабутиламмониевую соль СЦ (7,50 г) растворяли в 75 мл ДМСО. К раствору добавляли заданное количество 4-бромометил-2,6-диизоборнилфенола (ДБ-Br), предварительно растворенного в ДМСО. Реакционную смесь перемешивали при температуре 35°C в течение 6 ч в атмосфере аргона. Для выделения и очистки полимер осаждали в диоксане (600 мл), затем отделяли и дважды промывали диоксаном. Для дополнительной очистки от низкомолекулярных компонентов, полимер переосаждали из хлороформа в диоксан, подсушивали в вакууме, затем растворяли в воде и лиофилизировали; показатель полидисперсности Mw/Mn=4,1. Элементный анализ (%) для образца, содержащего 5,8 мас.% фрагментов Диборнола (%): N 3,04; C 55,70; H 9,17; S 6,34.
Ниже представлена заявляемая структура макромолекулы, полимерный антиоксидант (в вариантах состава) на основе сульфата целлюлозы (структура I) с привитыми фрагментами 2,6-диизоборнил-4-метилфенола (Диборнол™, структура II), которая подтверждена данными ЯМР-, ИК- и УФ- спектроскопии.
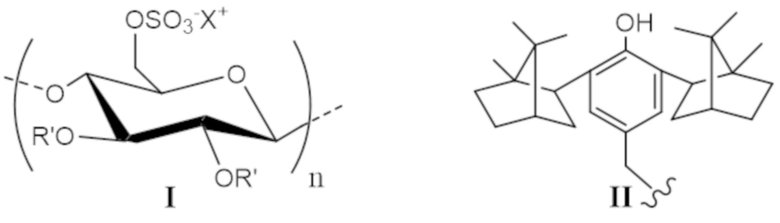
R' = структура II
X = Na+ или (Bu)4N+.
Пример 2. По способу, приведенному в примере 1, варьированием соотношения алкилирующий агент (ДБ-Br) - сульфат целлюлозы, получен заявляемый полимерный антиоксидант (в вариантах состава) с различным содержанием ковалентно связанного терпенофенольного фрагмента, что иллюстрирует таблица 1
Таблица 1
Пример 3. Получение заявляемого полимерного антиоксиданта (в вариантах содержания Диборнола)
Для получения Na-солей полимеров из тетрабутиламмониевых солей водный 2%-й раствор соответствующих тетрабутиламмониевых солей заявляемого полимерного антиоксиданта элюировали через колонку с ионообменной смолой КУ-2Na (длина 60 см, диаметр 2 см) со скоростью 1,0 мл/ч.
Элементный анализ (%) для образца, содержащего 5,8 мас.% фрагментов Диборнола (%): N 0,1; C 28,72; H 2,9; S 13,25.
Пример 4. Антирадикальная активность заявляемого полимерного антиоксиданта (в вариантах состава и содержания Диборнола)
Результаты исследования антирадикальной активности (АРА) исходной СЦ (в вариантах солеобразующих катионов) и продуктов его модификации фрагментами Диборнола представлены в виде гистограмм на фигуре 1 - антирадикальная активность модифицированных полисахаридов при концентрациях 0,5 и 2,5 мг/мл (А - натриевые соли, Б - тетрабутиламмониевые соли). Здесь и далее: Na, ТБА - обозначение натриевой и тетрабутилаамониевой соли полимера соответственно; число в шифре образца - содержание фрагментов Диборнола (мас.%). Например, СЦТБА-ДБ-5,0 - образец сульфата целлюлозы в виде тетрабутиламмониевой соли, с привитыми фрагментами Диборнола в количестве 5,0 мас.%.
Из приведенных данных следует, что заявляемые полимерные антиоксиданты проявляют АРА. Наиболее высокой АРА отличался исходный полимер СЦNа. Конъюгат СЦNа-ДБ-5,0 несколько превосходил по активности исходный полимер, тогда как образцы с более низким содержанием диалкилфенола (СЦNа-ДБ-3,0 и СЦNа-ДБ-0,8), напротив, существенно уступали исходному полимеру. Высокая АРА отмечена и для СЦТБА. Однако введение в ее молекулу фрагментов Диборнола (конъюгаты СЦТБА-ДБ-5,0, СЦТБА-ДБ-3,0, СЦТБА-ДБ-0,8) привело к неоднозначному эффекту - при концентрации 0,5 мг/мл АРА усиливалась, тогда как при 2,5 мг/мл - снижалась. Следовательно, способность исследованных соединений взаимодействовать со стабильным хромоген-радикалом 2,2-дифенил-1-пикрилгидразила (ДФПГ) обусловлено, главным образом, свойствами самого сульфатированного полисахарида, а протекторные свойства заявляемого полимерного антиоксиданта зависят не только от введения терпенофенольных соединений, но и от полисахаридной составляющей.
Пример 5. Мембранопротекторная и антиоксидантная активность заявляемого полимерного антиоксиданта (в вариантах состава и содержания Диборнола)
О мембранопротекторной активности соединений судили по их способности защищать эритроциты от разрушения (гемолиза) в условиях Н2О2-индуцированного окислительного стресса. Антиоксидантную активность коньюгатов оценивали по их способности ингибировать окисление нативного гемоглобина (oxyHb) до метгемоглобина (metHb) и феррилгемоглобина (ferrylHb), а также предотвращать накопление вторичных продуктов ПОЛ (ТБК-АП), образующихся вследствие интенсификации свободнорадикальных процессов в мембранах эритроцитов. Результаты исследования мембранопротекторной активности заявляемых полимерных антиоксидантов (в вариантах состава) с использованием метода индуцированного гемолиза, представлены в виде гистограмм на фиг. 2 и 3. На фиг. 2 представлено влияние соединений на основе Na-соли сульфата целлюлозы на степень Н2О2-индуцированного гемолиза эритроцитов через 1-5 ч инкубации. На фиг. 3 - влияние соединений на основе тетрабутиламмониевой соли сульфата целлюлозы на степень Н2О2-индуцированного гемолиза эритроцитов через 1-5 ч инкубации. Влияние полимеров на содержание вторичных продуктов ПОЛ (ТБК-АП) и соотношение окисленных и нативных форм гемоглобина в эритроцитах под воздействием H2O2 приведено в таблице 2.
Таблица 2
Полученные результаты достоверно указывают на то, что в концентрации 0,5 мг/мл все заявляемые полимерные антиоксиданты в виде натриевых солей практически полностью защищали эритроциты от гибели под воздействием Н2О2 и статистически значимо снижали окисление нативного гемоглобина до мет- и феррилгемоглобина (таблица 2). Полимер-основа этой группы полимеров (СЦNа) также проявляет и собственную мембранопротекторную активность, но более низкую в сравнении с конъюгатами, содержащими Диборнол.
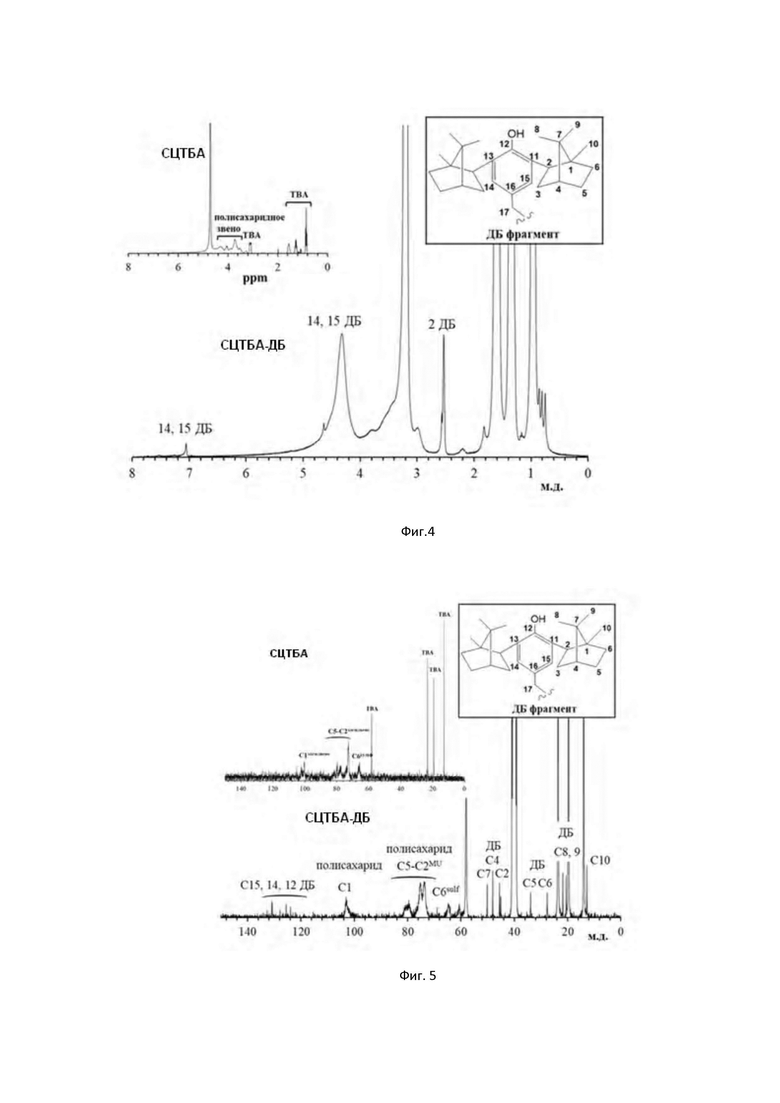
Высокой мембранопротекторной активностью отличаются и коньюгаты на основе СЦТБА-ДБ. В отличие от предыдущей группы соединений (СЦNа-ДБ), они хорошо ингибируют Н2О2-индуцированный гемолиз (фиг. 2, 3) не только в высокой (0,5 мг/мл), но и в низкой (0,05 мг/мл) концентрации, а также статистически значимо снижают окисление оксигемоглобина и накопление вторичных продуктов ПОЛ (таблица 2). Отметим, что в данном случае у полимера-основы (СЦТБА) мембранопротекторная активность не зафиксирована (фиг. 3). При снижении концентрации соединений на порядок (до 0,05 мг/мл) только конъюгаты с терпенофенольными фрагментами показали статистически значимую мембранопротекторную активность и способность ингибировать окисление нативного гемоглобина (таблица 2). СЦ без привитых фрагментов Диборнола не обладает такими свойствами в низких концентрациях. На фиг. 4 представлены данные, подтверждающие структуру и чистоту заявляемого соединения, ЯМР 1H спектр СЦТБА-ДБ (ω=5,8) и СЦТБА (врезка). На фиг. 5 представлены данные - ЯМР 13С спектр СЦТБА-ДБ (ω=5,8) и СЦТБА (врезка).
Для исследования структуры сульфатированных полисахаридов с целью уменьшения мешающего влияния солеобразующих тетрабутиламмониевых фрагментов дополнительно использованы соответствующие натриевые соли, полученные методом ионного обмена из СЦТБА и СЦТБА-ДБ.
В ЯМР 13С спектрах СЦТБА и СЦТБА-ДБ присутствуют сигналы 100,2; 79,6; 74,1; 77,3; 72,6 и 64,8 м.д., соответствующие С1-С6 атомам статистического мономерного звена (фиг. 5 (врезка и основная)). Введение сульфатных групп в структуру полисахарида приводит к смещению сигналов химического сдвига для этерифицированного атома С6 в область более сильного поля, что свидетельствует о полном замещении первичных спиртовых групп на сернокислые в принятых. Сигналы в области 70-76 м.д. соответствуют атомам С2, С3 и С5 ангидроглюкозного звена, в области 76-78 м.д. атомам С4 и С4', указывающим на проявление эффекта сульфатирования атома С3 ангидроглюкозного звена. Сигнал в области 102,2 м.д. характерен для атома С1, а для атома С1 в звеньях, испытывающих влияние С6 сульфатированной группы, наблюдается смещение в сторону слабого поля (сигнал C1ME, 102,7 м.д.). В ЯМР 13С спектрах синтезированных конъюгатов СЦТБА-ДБ (фиг. 5) дополнительно наблюдаются сигналы, характерные для конъюгированного с полимером терпенофенола. Для алкильной части конъюгированных фрагментов ДБ присутствуют характерные сигналы: пик 12,8 м.д. (С10); 20,6; 21,8 м.д. (C8, C9); 27,7; 33,9 м.д. (С5); 45,1-50,2 м.д. (С3, C2, C4, C7); 123,9-130,9 м.д. (Ar). Группа сигналов 13,9; 19,7; 23,6; 58,1 соответствует атомам углерода бутильных радикалов при атоме азота солеобразующей группы, которые не подверглись ионному обмену.
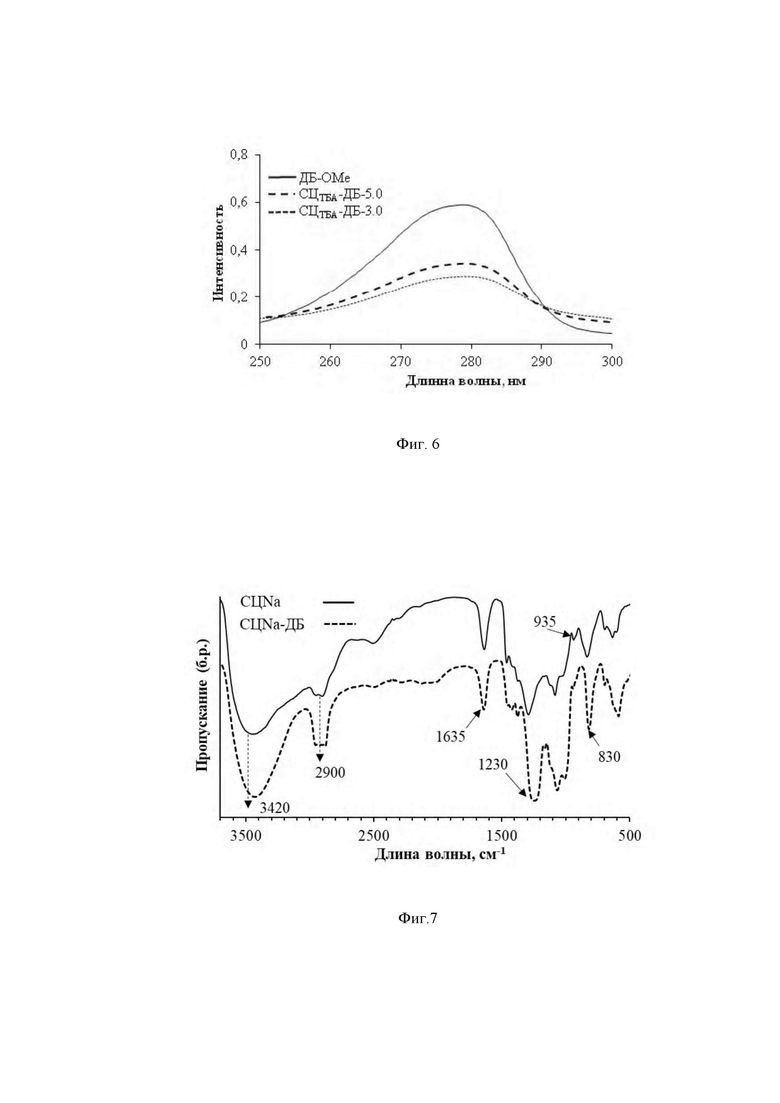
Количественное определение ароматического фрагмента в полимерном антиоксиданте осуществляли с использованием модельного соединения - 2,6-диизоборнил-4-метилоксиметилфенола (ДБ-OMe). В интервале частот 200-320 нм наблюдается максимум поглощения модельного соединения и фрагмента Диборнола, конъюгированного с СЦ. На фиг. 6 представлены УФ-спектры СЦТБА-ДБ с различным содержанием фрагмента Диборнола и модельного вещества ДБ-OMe (этанол / вода 3:2). Макромолекула исходного сульфата целлюлозы в данном диапазоне не поглощает.
На фиг. 7 представлен ИК спектр полимера антиоксиданта на основе СЦ (СЦNа и СЦNа-ДБ-3,0). В ИК спектрах CЦNa присутствуют полосы поглощения, характерные для этого полимера, в частности 1230 и 830 см-1, соответствующие колебаниям C-OSO3 и S-O связей. Последняя полоса наиболее характерна для сложноэфирных сульфатных групп. В спектре также присутствуют полосы поглощения в области 3420 см-1 (колебания гидроксильных групп), 2900 см-1 (алкильные группы) в случае СЦNа-ДБ в этой области также поглощают терпеновые структуры в составе алкилфенола (фиг. 7).
Методы анализа структуры и биологической активности in vitro.
Спектры ЯМР 13С и 1H регистрировали на приборе «Bruker Avance II 300» (рабочая частота 75 и 300 МГц) DMSO-d6 и D2O, концентрация образца 5-8%, температура 30°C; время релаксации 3,5 с.
ИК спектры записывали на ИК-Фурье-спектрометре IR Prestige 21 «Shimadzu» в таблетках с KBr в диапазоне длин волн 400-4000 см-1.
Элементный анализ осуществляли на приборе EA-1110 фирмы «CE instruments».
УФ спектры регистрировали на приборе UV-1700 (Shimadzu) в растворе этанол/вода (3:2 v/v). Содержание присоединенных фрагментов диалкилфенола (ωДБ, масс %) в смешанных эфирах определяли по калибровочной шкале. В качестве стандарта для ее построения использован (ДБ-OMe) (молярный коэффициент поглощения ε=1904 л∙моль-1∙см-1, λmax= 282 нм).
Молекулярную массу (ММ) образцов СЦ определяли с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Для анализа использовали хроматографическую систему «Shimadzu» (Япония): насос LC-20AD, термостат CTO-10AS, рефрактометр RID-10A, колонка Shodex OHpac SB804 HG (8 мм ×30 см). Элюирование проводили 0,15 М NaCl при 40°С со скоростью потока 0,3 см3/мин. Для калибровки колонки использовали образцы сульфатированных пуллуланов с ММ в диапазоне 1,3⋅103 - 8,0⋅103.
Антирадикальную активность соединений оценивали по их способности взаимодействовать со стабильным хромоген-радикалом 2,2-дифенил-1-пикрилгидразила (ДФПГ). Исследуемые соединения вносили в водный раствор ДФПГ в концентрациях 0,5 и 2,5 мг/мл, перемешивали, через 30 мин измеряли оптическую плотность раствора при λ=517 нм с использованием спектрофотометра ThermoSpectromicGenesys 20 (США). Степень ингибирования рассчитывали в процентах по отношению к оптической плотности раствора ДФПГ, не содержащего исследуемых соединений [Sevgi K., Tepe B., Sarikurkcu C. Antioxidant and DNA damage protection potentials of selected phenolic acids. Food and Chemical Toxicology. 2015. 77. 12-21. https://doi.org/10.1016/j.fct.2014.12.006].
Для оценки токсичности, антиоксидантной и мембранопротекторной активности соединений использовали 0,5% (v/v) суспензию эритроцитов лабораторных мышей в фосфатно-солевом буфере (PBS, рН 7,4). Исследуемые вещества предварительно растворяли в PBS. Токсичность соединений оценивали (in vitro) по их способности индуцировать гемолиз. Растворы соединений вносили в суспензию эритроцитов и инкубировали при 37°С в течение 5 ч в термостатируемом шейкере Biosan ES-20 (Латвия). Контрольные образцы содержали соответствующий объем PBS. О наличии цитотоксичности судили по степени гемолиза эритроцитов через 1, 3 и 5 ч инкубации.
Мембранопротекторную и антиоксидантную активность определяли по степени ингибирования Н2О2-индуцированного гемолиза, торможения накопления вторичных продуктов ПОЛ и окисления оксигемоглобина в эритроцитах. С этой целью спустя 30 мин после внесения в суспензию эритроцитов растворов исследуемых соединений (итоговые концентрации 0,05 и 0,5 мг/мл) инициировали гемолиз раствором пероксида водорода (0,006%). Затем реакционную смесь инкубировали в термостатируемом шейкере при медленном перемешивании и 37°С в течение 5 ч. Каждый час из инкубационной среды отбирали аликвоту, центрифугировали 5 мин (1600 g), степень гемолиза определяли по содержанию гемоглобина в супернатанте на спектрофотометре ThermoSpectromic Genesys 20 (США) при λ 524 нм [Takebayashi J., Chen J., Tai A. Advanced Protocols in Oxidative Stress II, Methods in Molecular Biology / Ed. Armstrong D. New York; Dordrecht; Heidelberg; London: Humana Press, 2010. 594. 287-296. https://doi.org/10.1007/978-1-60761-411-1_20]. Процент гемолиза рассчитывали по отношению к полному гемолизу образца. Содержание вторичных продуктов ПОЛ, реагирующих с 2-тиобрабитуровой кислотой (ТБК-АП), определяли с использованием спектрофотометра ThermoSpectromic Genesys 20 (США) при λ=532 нм, для расчетов использовали коэффициент экстинкции 1,56×105 M–1см–1 [Asakawa T., Matsushita S. Coloring conditions of thiobarbituric acid test for detecting lipid hydroperoxides. Lipids. 1980. 15. 137-140. https://doi.org/10.1007/BF02540959; Buege J. A., Aust S. D. In Methods in Enzymology; Fleischer, S., Packer, L., Eds.; Academic Press: San Diego, CA, 1978. 52, 302-310. https://doi.org/10.1016/S0076-6879(78)52032-6]. Для оценки накопления продуктов окисления гемоглобина после завершения инкубации аликвоту суспензии эритроцитов подвергали полному гемолизу, центрифугировали с целью осаждения теней эритроцитов и анализировали спектр поглощения в интервале 540-630 нм, используя спектрофлуориметр «Флюорат-02-Панорама» (Люмэкс, Санкт-Петербург). Содержание различных форм гемоглобина (oxyHb, metHb и ferrylHb) рассчитывали с учетом соответствующих коэффициентов экстинкции [Van den Berg J. J. M., Op den Kamp J.A. F., Lubin B .H., Roelofsen B., Kuypers F. A. Kinetics and site specificity of hydroperoxide-induced oxidative damage in red blood cells. Free Radical Biol. Med. 1992. 12. 487-498. https://doi.org/10.1016/0891-5849(92)90102-M]. Каждый эксперимент проводили в 4-6 повторностях. Статистическую обработку данных осуществляли с помощью пакета программ Microsoft Office Excel 2007.
| название | год | авторы | номер документа |
|---|---|---|---|
| СЕРОСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ 2,6-ДИИЗОБОРНИЛФЕНОЛА | 2014 |
|
RU2568437C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,6-ДИИЗОБОРНИЛФЕНОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2516699C2 |
| ω-(Гидроксиарил)алкилсульфиды на основе 2-изоборнил-6-метил-4-пропилфенола | 2016 |
|
RU2616618C1 |
| ГИДРОФИЛЬНЫЙ КОНЪЮГАТ ПРОИЗВОДНОГО КРАХМАЛА И 2,6-ДИИЗОБОРНИЛ-4-МЕТИЛФЕНОЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2619934C2 |
| Антиагрегационное и антиоксидантное средство | 2023 |
|
RU2808474C1 |
| Способ получения антиагрегационного и антиоксидантного средства | 2023 |
|
RU2819387C1 |
| Гибридные терпенофенолы с изоборнильным и 1-фенилэтильным или 1-фенилпропильным заместителями и их применение в качестве средства, обладающего антирадикальной, антиоксидантной и мембранопротекторной активностью | 2016 |
|
RU2642062C2 |
| ГИДРОФИЛЬНЫЙ КОНЪЮГАТ ГИДРОКСИЭТИЛКРАХМАЛА И 2,6-ДИИЗОБОРНИЛ-4-МЕТИЛФЕНОЛА | 2012 |
|
RU2497828C1 |
| 2,6-ДИИЗОБОРНИЛФЕНОЛЫ | 2011 |
|
RU2502719C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2701739C1 |

Изобретение относится к производным целлюлозы. Предложен сульфатированный полисахарид структуры I с ковалентно присоединённым фрагментом 2,6-диизоборнил-4-метилфенола структуры II. Причем R' = структура II; X = Na+, (Bu)4N+. Способ получения сульфатированного полисахарида предусматривает O-алкилирование свободных гидроксильных групп сульфата целлюлозы в виде тетрабутиламмониевой соли 4-бромометил-2,6-диизоборнилфенолом путем растворения тетрабутиламмониевой соли сульфата целлюлозы в ДМСО. Затем к раствору добавляют 4-бромометил-2,6-диизоборнилфенол, предварительно растворенный в ДМСО, реакционную смесь перемешивают при температуре 35°C в течение 6 ч в атмосфере аргона. Для выделения и очистки полимер осаждают в диоксане. Затем отделяют и дважды промывают диоксаном, для дополнительной очистки от низкомолекулярных компонентов полимер переосаждают из хлороформа в диоксан, подсушивают в вакууме, затем растворяют в воде и лиофилизируют. При необходимости получения Na-солей полимеров из тетрабутиламмониевых солей водный 2%-й раствор тетрабутиламмониевых солей полученного полимера элюируют через колонку с ионообменной смолой КУ-2Na длиной 60 см и диаметром 2 см со скоростью 1,0 мл/ч. Также предложено применение сульфатированнного полисахарида с содержанием фрагмента II от 0,3 мас.% до 5,8 мас.% в качестве средства, обладающего антирадикальной, антиоксидантной и мембранопротекторной активностью, заключающейся в способности эффективно защищать клетки крови в условиях острого окислительного стресса, а также для защиты сердечно-сосудистой системы. Изобретение направлено на получение соединения с низкой цитотоксичностью, антирадикальной, антиоксидантной и мембранопротекторной активностью, заключающейся в способности эффективно защищать клетки крови в условиях острого окислительного стресса. 3 н.п. ф-лы, 2 табл., 5 пр., 7 ил.
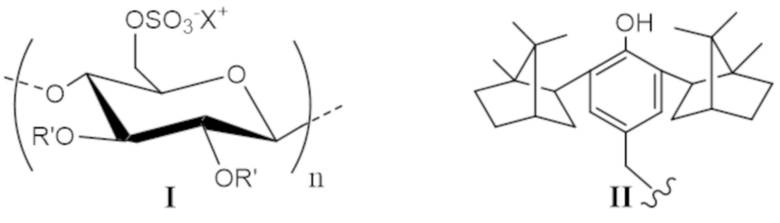
1. Сульфатированный полисахарид структуры I на основе целлюлозы с ковалентно присоединённым фрагментом 2,6-диизоборнил-4-метилфенола структуры II
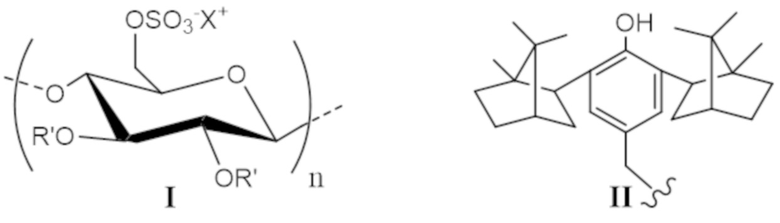
где: R' = структура II;
X = Na+ или (Bu)4N+.
2. Способ получения сульфатированного полисахарида по п.1, предусматривающий O-алкилирование свободных гидроксильных групп сульфата целлюлозы в виде тетрабутиламмониевой соли 4-бромометил-2,6-диизоборнилфенолом путем растворения тетрабутиламмониевой соли сульфата целлюлозы в ДМСО, затем к раствору добавляют 4-бромометил-2,6-диизоборнилфенол, предварительно растворенный в ДМСО, реакционную смесь перемешивают при температуре 35°C в течение 6 ч в атмосфере аргона, для выделения и очистки полимер осаждают в диоксане, затем отделяют и дважды промывают диоксаном, для дополнительной очистки от низкомолекулярных компонентов полимер переосаждают из хлороформа в диоксан, подсушивают в вакууме, затем растворяют в воде и лиофилизируют, при необходимости получения Na-солей полимеров из тетрабутиламмониевых солей водный 2%-й раствор тетрабутиламмониевых солей полученного полимера элюируют через колонку с ионообменной смолой КУ-2Na длиной 60 см и диаметром 2 см со скоростью 1,0 мл/ч.
3. Применение сульфатированнного полисахарида по п.1 с содержанием фрагмента II от 0,3 мас.% до 5,8 мас.% в качестве средства, обладающего антирадикальной, антиоксидантной и мембранопротекторной активностью, заключающейся в способности эффективно защищать клетки крови в условиях острого окислительного стресса, а также для защиты сердечно-сосудистой системы.
| ПОЛИСАХАРИД С ПРИВИТЫМ АНТИОКСИДАНТОМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2174985C2 |
| ГИДРОФИЛЬНЫЙ КОНЪЮГАТ ГИДРОКСИЭТИЛКРАХМАЛА И 2,6-ДИИЗОБОРНИЛ-4-МЕТИЛФЕНОЛА | 2012 |
|
RU2497828C1 |
| ГИДРОФИЛЬНЫЙ КОНЪЮГАТ ПРОИЗВОДНОГО КРАХМАЛА И 2,6-ДИИЗОБОРНИЛ-4-МЕТИЛФЕНОЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2619934C2 |
| ВОДОРАСТВОРИМЫЙ ПОЛИМЕРНЫЙ АНТИОКСИДАНТ, ПЛАЗМОЗАМЕНИТЕЛЬ С АНТИОКИСЛИТЕЛЬНОЙ И АНТИРАДИКАЛЬНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) И СПОСОБ ПОДДЕРЖАНИЯ УРОВНЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ И ПРОЦЕССОВ АНТИОКСИДАНТНОЙ ЗАЩИТЫ В ОРГАНИЗМЕ ПРИ ОСТРОЙ КРОВОПОТЕРЕ | 2004 |
|
RU2273483C2 |
| Способ получения водорастворимого линейного полисахарида | 1981 |
|
SU981322A1 |
Авторы
Даты
2022-03-16—Публикация
2021-02-15—Подача