Изобретение относится к области органического синтеза, а именно к способам получения соединения, которое может быть использовано в медицинской практике в качестве средства, обладающего антиагрегационным и антиоксидантным действием.
Известны средства, обладающие антиагрегационным действием [Патент РФ 2453312, Средство, проявляющее антиагрегантную и антитромбогенную активности / Спасов А.А. и др.], [Патент РФ 2440814, Средство, обладающее антитромбогенной активностью / Спасов А.А. и др.], [Патент РФ 2594254, Средство, обладающее церебропротекторным, эндотелиопозитивным и антитромботическим действием / Берестовицкая В.М. и др.], [Патент РФ 2459826, Циклогексиламмониевая соль [3-метил-1-н-пропил-7-(1-оксотиетанил-3)ксантинил-8-тио] уксусной кислоты, проявляющая антитромботическую активность, Губаева Р.А.], [Патент РФ 2640579, Гидрохлориды 1-алкил-3-метил-8-пиперазино-7-(тиетанил-3)ксантина, проявляющие антитромботический эффект посредством блокирования рецепторов тромбоцитов гп IIb-IIIa / Халиуллин Ф.А. и др.], [Патент РФ 2662308, Средство для лечения и профилактики тромбоза / Камилов Ф.Х и др.].
Известны средства, обладающие антиоксидантным действием [Патент РФ 2767207, Сульфатированный полисахарид на основе целлюлозы с привитым терпенофенолом, способ его получения и средство, обладающее антирадикальной, антиоксидантной и мембранопротекторной активностью/ Торлопов М. А. и др.].
В настоящее время не вызывает сомнения важность свободнорадикальных реакций окисления липидов мембран в регуляции клеточного метаболизма. Вместе с тем чрезмерная интенсификация процессов перекисного окисления липидов (ПОЛ) ассоциирована с развитием разнообразных заболеваний, включая атеросклероз, сахарный диабет, ишемическую болезнь сердца, артрит, нарушения микроциркуляции крови и лимфы и др. Известно и о влиянии интенсификации свободнорадикальных процессов на дисфункцию эндотелия сосудов, роль которого существенна в общем гемостазе.
Сердечно-сосудистые заболевания составляют основную причину смертности во всем мире. Среди сердечно-сосудистых заболеваний ведущие место занимают ишемическая болезнь сердца и ишемические инсульты, развитие которых обусловлено атеросклеротическим поражением кровеносных сосудов. Атеросклероз приводит к повреждению стенки сосуда и активации тромбоцитов, что вызывает образование тромба и прекращение кровотока в жизненно важных органах.
Тромбообразование обусловлено адгезией и агрегацией тромбоцитов и активацией плазменных прокоагулянтов на их фосфолипидной поверхности. Эти изменения индуцируются различными физиологическими и патологическими агентами, вызывающими активацию специфических клеточных рецепторов, что приводит к нарушению клеточной асимметричности, появлению мезоморфных структур. Поэтому поиск веществ, способствующих воздействию на эти процессы и позволяющих их корректировать, является основной задачей создания принципиально новых лекарственных препаратов.
Модификация природных терпенов путем введения серосодержащих биологически активных фрагментов позволяет получить лекарственное средство нового типа, обладающие антикоагуляционным и антиоксидантным действием.
Известен структурный аналог предлагаемого соединения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол, обладающий антиагрегационным действием [Патент РФ 2522198, 2-({[(1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил]метил}сульфинил)этановая кислота, обладающая антиагрегационным действием / Никитина Л.Е. и др.].
Известен структурный аналог предлагаемого соединения, 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола, обладающий антиоксидантным действием [Melekhin A.K., Sudarikov D.V., Shevchenko O.G., Rubtsova S.A., Kuchin A.V. New S-monoterpenylcysteines // Chem. Nat. Compd. 2018, 54, 281–285].
Предлагаемое соединение структурной формулы I, 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол, ранее было описано в работах (Nikitina L. E., Startseva V. A., Dieva S. A., Vakulenko I. A., Shamov G. A. Reaction of β-pinene and thiols in the presence of Lewis acids // Chem. Nat. Compd. 2006, 42, 178–181; Firdaus M., Montero de Espinosa L., Meier M.A.R. Terpene-based renewable monomers and polymers via thiol–ene additions. Macromolecules, 2011, 44, 7253–7262), но его антиагрегационные и антиоксидантные свойства не исследованы.

Наиболее близким аналогом способа получения соединения I является способ, заключающийся в реакции присоединения 2-меркаптоэтанола к β-пинену. Выход целевого продукта с применением указанного способа составлял 87% (Nikitina L. E., Startseva V. A., Dieva S. A., Vakulenko I. A., Shamov G. A. Reaction of β-pinene and thiols in the presence of Lewis acids // Chem. Nat. Compd. 2006, 42, 178–181). Неселективность данной реакции затрудняет выделение продуктов вследствие их близкой хроматографической подвижности.
Технический результат состоит в разработке нового, более эффективного способа получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола формулы I, обеспечивающего повышение выхода целевого продукта до 95% без образования побочных продуктов (без побочных стереоизомерных соединений). Полученное новым способом чистое соединение формулы I, позволяет провести оценку эффективности на модели «агрегация-дезагрегация», дать точную оценку пригодности в качестве лекарственного средства для лечения заболеваний крови, связанных с окислительно-восстановительным равновесием и сворачиваемостью крови, что в свою очередь позволяет проводить клинические исследования.
Технический результат способа получения достигается тем, что способ получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола формулы I
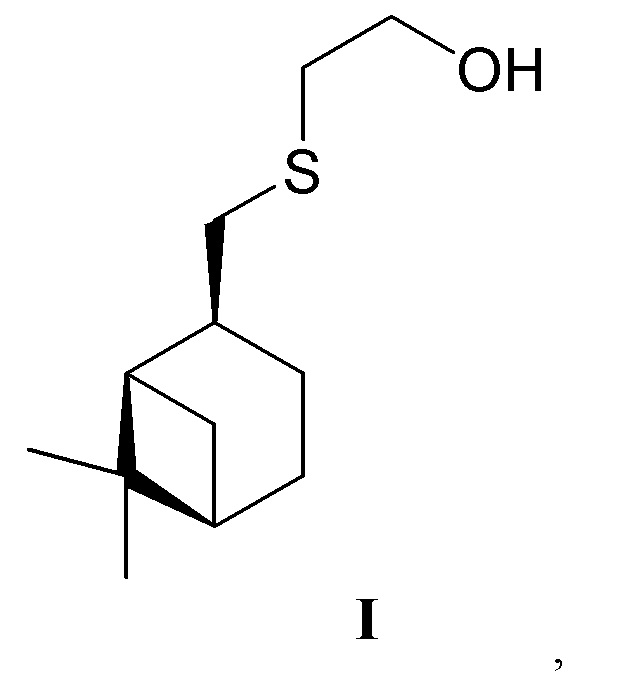
обладающего антиагрегационной и антиоксидантной активностью, включающий выделение целевого продукта методом колоночной хроматографии, согласно изобретения, способ осуществляют путем взаимодействия цис-миртантиола с 2-бромэтанолом в присутствии карбоната цезия (Cs2CO3) и иодида тетрабутиламмония (TBAI) при нагревании смеси в среде инертного газа, при этом осуществляют бимолекулярное нуклеофильное замещение брома в 2-бромэтаноле цис-миртантиолом, процесс ведет до полного расходования цис-миртантиола.
Заявленный способ получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола осуществляется следующим образом.
Предлагаемый новый способ получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола (соединение I) основан на реакции цис-миртантиола с 2-бромэтанолом в присутствии карбоната цезия (Cs2CO3) и иодида тетрабутиламмония (TBAI). Выход соединения I при реализации нового способа составляет 95%, при этом никаких побочных продуктов, стереоизомерных соединений не образуются.
Пример 1. (пример осуществления способа)
В 50 мл этанола растворяли 1,7 г (10 ммоль) (1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил-тиола (цис-миртантиол), затем добавляли 3.9 г (12 ммоль) карбоната цезия (Cs2CO3), 4.4 г (12 ммоль) иодида тетрабутиламмония (TBAI) и 0,86 мл (12 ммоль) 2-бромэтанола (ρ = 1,75 г/мл). Реакционную смесь нагревали в среде инертного газа в течение 48 ч. Контроль за протеканием реакции осуществляли методом тонкослойной хроматографии. По окончании реакции проводили экстракцию хлороформом. Продукты реакции (схема выделяли методом колоночной хроматографии на силикагеле (0,06–0,2 мм) используя в качестве элюента смесь петролейный эфир : этилацетат (2 : 1). Выход 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола в данных условиях составил 95%.
2-((1S,2R,5S)-6,6-Диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол – вязкая бесцветная жидкость, растворимая как в полярных так и неполярных органических растворителях, не растворима в воде.
Получение 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанил-этанола на основе цис-миртантиола приведено на схеме 1.

ИК-спектр регистрировали на ИК-Фурье-спектрометре Shimadzu IR Prestige 21. ИК-спектр, ν, см–1: 1051 (CH2–OH), 1457 (CH2, CH3), 2950 (C–H), 3387 (OH).
Спектры ЯМР 1H и 13C регистрировали на спектрометре Bruker Avance-300 (300.17 МГц для 1Н и 75.48 МГц для 13С) в растворе CDCl3. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 0.89 (д, 1Н, J = 7.5 Гц, Н7а), 0.99 (c, 3H, Н9), 1.19 (с, 3H, Н8), 1.43–1.59 (м, 1H, Н4а), 1.80–1.96 (м, 3H, Н3, Н5), 1.98–2.07 (м, 2H, Н1, Н4b), 2.20 (квин, 1Н, J = 7.5 Гц, H2), 2.29–2.38 (м, 2H, Н7b, ОН), 2.53–2.63 (м, 2H, Н10), 2.69 (т, 2Н, J = 5.9 Гц, SCH2), 3.69 (т, 2H, J = 6.1 Гц, CH2O). Спектр ЯМР 13С (CDCl3, δ, м.д.): 22.04 (C4), 23.19 (C9), 26.08 (C3), 27.94 (C8), 33.30 (C7), 35.42 (CH2S), 38.62 (C6), 38.91 (C10), 41.12 (C5), 41.26 (C2), 45.50 (C1), 60.18 (CH2OH). Найдено, %: С 67.18; Н 10.40; S 14.79. C12H22OS. Вычислено, %: С 67.24; Н 10.34; S 14.96.
Авторами проведены экспериментальные исследования и установлена антиагрегационная активность и антиоксидантная активность 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола, что позволяет полученное новым способом соединение применять в качестве лекарственного средства.
Эксперименты в условиях in vitro выполнены на крови здоровых доноров-мужчин в возрасте 18–24 лет. Общее количество доноров составило 12 человек. Забор крови для исследования соединений в отношении системы гемостаза проводился из кубитальной вены с использованием систем вакуумного забора крови BD Vacutainer® (Becton Dickinson and Company, США). В качестве стабилизатора венозной крови использовался 3,8% раствор цитрата натрия в соотношении 9:1. Все тесты проводились на обогащенной и обедненной тромбоцитами плазмах. Образцы богатой тромбоцитами плазмы получали центрифугированием цитратной крови при 1000 об/мин в течение 10 минут, бестромбоцитарной плазмы – при 3000 об/мин в течение 20 минут. В работе использовалась центрифуга ОПН-3.02 (ОАО ТНК «ДАСТАН», Киргизия).
Активность соединения I, полученного новым способом показана на следующих примерах.
Пример 2. Антиагрегационная активность 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола.
Исследование влияния на агрегацию тромбоцитов проводили по методу Born (Born G.G.V.Nature (London). – 1962 . – V. 194.) на агрегометре «АТ-02» (НПФ «Медтех», Россия). В качестве индукторов агрегации использовали аденозиндифосфат (АДФ) в концентрации 20 мкг/мл и коллаген в концентрации 5 мг/мл производства «Технология-Стандарт» (Россия). Проводили оценку максимальной амплитуды агрегации, скорости агрегации, время достижения максимальной амплитуды и дезагрегацию в присутствии изучаемых соединений при агрегации тромбоцитов, индуцированной АДФ. При коллаген-индуцированной агрегации тромбоцитов оценивали латентный период, во время которого происходит активация фосфолипазы С (что приводит к образованию вторичных посредников, вследствие чего развивается секреция тромбоцитарных гранул и синтез тромбоксана А2).
Тромбоэластографию (ТЭГ) проводили на аппарате TEG 5000 (Haemoscope Corporation, США). При анализе тромбоэластограмм определяли общую тенденцию коагуляции (R), функциональную активность тромбоцитов и фибриногена (МА, Angle), активность фибринолиза (CLT) и физико-механические свойства образовавшихся сгустков (G). В качестве активаторов ТЭГ использовали 0.2 М раствор CaCl2 (Innovin®, Dade Behring, Германия).
Определение антиагрегационной активности по методу Born и тромбоэластография исследуемых веществ и препаратов сравнения проводили в конечной концентрации 2×10–3 М.
Предлагаемое вещество по химической природе не имеет аналогов среди антиагрегационных лекарственных препаратов. Поэтому в качестве препарата сравнения, согласно с рекомендациями «Руководства по доклиническому изучению новых фармакологических веществ» (Руководство по проведению доклинических исследований лекарственных средств. Часть первая. – М.: Гриф и К, 2012. – 944 с.), выбрали ацетилсалициловую кислоту, как наиболее эффективное антиагрегационное средство, используемое в настоящее время в клинической практике («Ацетилсалициловая кислота», Фармацевтическая фабрика Шандонг Ксинхуа Фармасьютикал Ко., ЛТД, Китай).
Результаты исследования обработаны с применением статистического пакета Statistica 10.0 (StatSoft Inc, США). Проверку на нормальность распределения фактических данных выполняли с помощью критерия Шапиро-Уилка. Выявлено, что вид распределения полученных данных отличается от нормального, поэтому при дальнейшей работе использовались непараметрические методы. Данные представлены в виде медианы, 25 и 75 процентилей. Дисперсионный анализ проводили с помощью критерия Краскела-Уоллиса. Критический уровень значимости р для статистических критериев принимали равным 0.05.
По результатам исследования оценки влияния соединения (I) на систему гемостаза тромбоэластографией установлено, что 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол проявляет антиагрегационную активность на уровне ацетилсалициловой кислоты, действуя на функциональную активность тромбоцитов (МА) и коагуляционный компонент системы гемостаза (R), что приводит к формированию неполноценного фибринового сгустка (G) и не влияет на фибринолитическую активность (показатель CLT не изменялся). Показатели тромбоэластографии 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол и ацетилсалициловой кислоты, Ме (0.25–0.75) приведены в таблице 1.
(10.3–15.6)
(40.1–49.4)
(54.2–61.2)
(4.5–8.1)
(35.4–42.4)
(12.5–15.3)
(30.2–34.7)**, †
(37.4–42.9)*
(3.1–3.9)**
(35.1–38.7)
(11.2–14.4)
(36.2–38.7)*
(31.2–38.1)**
(3.1–4.6)*
(36.7–39.4)
Показатели антиагрегационной активности 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола в сравнении с ацетилсалициловой кислотой представлены в таблице 2, Ме (0.25–0.75).
(11.2–15.3)*,††,##
(11.2–16.7)*,†
(6.1–11.7)*,††,#
(16.4–21.5)*,†,#
(1.1–2.6)††
(10.8–16.4)*,††
(7.6–12.3)*,††
(8.7–13.4)*,††
Установлено, что 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанил-этанол более эффективно удлинял реакцию высвобождения тромбоцитов при коллаген-индуцированной агрегации тромбоцитов и снижал максимальную амплитуду агрегации на уровне ацетилсалициловой кислоты.
Пример 3. Антиоксидантная активность 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола.
Антиоксидантную активность соединений оценивали (in vitro) по способности ингибировать процессы ПОЛ в липидах головного мозга лабораторных мышей (Acker C.I., Brandão R., Rosário A.R., Nogueira C.W. Antioxidant effect of alkynylselenoalcohol compounds onliver and brain of rats in vitro // Environ. Toxicol. Pharmacol. 2009, 28, 280–287; Stefanello S.T., Prestes A.S., Ogunmoyole T., Salman S.M., Schwab R.S., Brender C.R., Dornelles L., Rocha J.B.T., Soares F.A.A. Evaluation of in vitro antioxidant effect of new mono and diselenides // Toxicol. in Vitro. 2013, 27, 1433–1439.
Головной мозг гомогенизировали (10%) в физиологическом растворе (pH = 7.4) и центрифугировали в течение 10 мин, затем отбирали супернатант (S1), содержащий липиды. Исследуемое соединение вносили в супернатант в виде раствора в ацетоне (итоговые концентрации 100 мкМ и 1 мМ). Через 30 мин инициировали ПОЛ внесением свежеприготовленного FeCl2 и аскорбиновой кислоты (Chawla R., Arora R., Kumar R., Sharma A. et al. Antioxidant activity of fractionated extracts of rhizomes of high-altitude Podophyllum hexandrum: role in radiation protection // Mol. Cell. Biochem. 2005, 273, 193–208; Kim J.-S. Preliminary evaluation for comparative antioxidant activity in the water and ethanol extracts of dried citrus fruit (Citrus unshiu) peel using chemical and biochemical In Vitro assays // Food Nutr. Sci. 2013, 4, 177–188). Образцы инкубировали в течение часа при 37°C и медленном перемешивании. Содержание вторичных продуктов ПОЛ, реагирующих с 2-тиобарбитуровой кислотой (ТБК-АП), определяли с использованием спектрофотометра ThermoSpectromic Genesys 20 (США) при λ = 532 нм, для расчетов использовали коэффициент экстинкции 1.56×105 M–1см–1 (Asakawa T., Matsushita S. Coloring conditions of thiobarbituric acid test for detecting lipid hydroperoxides // Lipids. 1980, 15, 137–140; Buege J. A., Aust S. D. In Methods in Enzymology; Fleischer, S., Packer, L., Eds.; Academic Press: San Diego, CA, 1978, 52, 302–310).
Для оценки антиоксидантной и мембранопротекторной активности образца использовали 0.5% (v/v) суспензию эритроцитов лабораторных мышей в фосфатно-солевом буфере (PBS, рН 7.4). Мембранопротекторную и антиоксидантную активность определяли по степени ингибирования Н2О2-индуцированного гемолиза, торможения накопления вторичных продуктов ПОЛ и окисления оксигемоглобина в эритроцитах. С этой целью спустя 30 мин после внесения в суспензию эритроцитов растворов исследуемых соединений (итоговая концентрация 100 мкМ) инициировали гемолиз раствором пероксида водорода (0.006%) либо AAPH (2,2'-azobis(2-amidinopropane) dihydrochloride, 3 мM). Затем реакционную смесь инкубировали в термостатируемом шейкере при медленном перемешивании и 37°С в течение 5 ч. Каждый час из инкубационной среды отбирали аликвоту, центрифугировали 5 мин (1600 g), степень гемолиза определяли по содержанию гемоглобина в супернатанте на спектрофотометре ThermoSpectromic Genesys 20 (США) при λ 524 нм (Takebayashi J., Chen J., Tai A. Advanced protocols in oxidative stress II, methods in molecular biology / Ed. Armstrong D. New York; Dordrecht; Heidelberg; London: Humana Press, 2010, 594, 287–296). Процент гемолиза рассчитывали по отношению к полному гемолизу образца. Содержание вторичных продуктов ПОЛ, реагирующих с 2-тиобарбитуровой кислотой (ТБК-АП), определяли спектрофотометрически, как указано выше. Для оценки накопления продуктов окисления гемоглобина после завершения инкубации аликвоту суспензии эритроцитов подвергали полному гемолизу, центрифугировали с целью осаждения теней эритроцитов и анализировали спектр поглощения в интервале 540–630 нм, используя спектрофлуориметр «Флюорат-02-Панорама» (Люмэкс, Санкт-Петербург). Содержание различных форм гемоглобина (oxyHb, metHb и ferrylHb) рассчитывали с учетом соответствующих коэффициентов экстинкции (Van den Berg J.J. M., Op den Kamp J.A. F., Lubin B .H., Roelofsen B., Kuypers F. A. Kinetics and site specificity of hydroperoxide-induced oxidative damage in red blood cells // Free Radical Biol. Med. 1992, 12, 487–498). Каждый эксперимент проводили в 3–8 повторностях. Статистическую обработку данных и построение диаграмм осуществляли с помощью пакета программ Microsoft Office Excel 2007 и Statistica 6.0. Экспериментальные данные представлены в виде средних арифметических значений с указанием стандартной ошибки среднего. Статистическую значимость различий оценивали по критерию Манна–Уитни. Критический уровень значимости р для статистических критериев принимали равным 0.05.
Пример 4. Антиоксидантная активность в субстрате, содержащем липиды головного мозга животных (неклеточная модель).
О наличии антиоксидантной способности судили по способности образца ингибировать накопление вторичных продуктов ПОЛ в субстрате, содержащем легкоокисляемые липиды головного мозга лабораторных животных. В концентрации 1 мМ 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол I эффективно ингибировал как спонтанную, так и индуцированную внесением Fe2+/аскорбат деградацию полиненасыщенных жирных кислот липидов головного мозга (фиг. 1), что следовало из снижения концентрации вторичных продуктов ПОЛ (ТБК-АП) в субстрате (уровень статистической значимости различий р = 0.004). По способности ингибировать накопление вторичных продуктов ПОЛ соединение I сопоставимо с ранее изученным (–)-цис-вербенолом и превосходит большинство других исследованных бициклических монотерпеновых спиртов: ((–)-неоизовербанол, (+)-3α,4α-карандиол, (–)-3β,4α-карандиол, (+)-3β,4β-карандиол, (–)-2α,3α-пинандиол, (–)-2α,3β-пинандиол, (–)-3α,4β-пинандиол, пинокамфеол, (±)-2-экзо-10-эндо-камфандиол, (–)-изокаранол-4, (–)-цис-миртанол, (–)-транс-миртанол, (–)-миртенол) (Nikitina L.E., Lisovskaya S.A., Startseva V.A., Frolova L.L., Kutchin A.V., Shevchenko O.G., Ostolopovskaya O.V., Pavelyev R.S., Khelkhal M.A., Gilfanov I.R., et al. Biological activity of bicyclic monoterpene alcohols. BionanoSci. 2021, 11, 970–976).
На фиг. 1 представлено Влияние 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанил-этанола I (100 мкМ и 1 мМ) на концентрацию ТБК-АП в субстрате на основе гомогената головного мозга. Концентрацию ТБК-АП измеряли спустя 1 ч после внесения Fe2+/аскорбат. К – контрольный образец, не содержащий исследуемого соединения 1, И – интактный образец, в котором не инициировали ПОЛ.
Пример 5. Мембранопротекторная и антиоксидантная активность.
Исследование мембранопротекторной и антиоксидантной активности 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола на живых клетках проводили при концентрации 100 мкМ.
О мембранопротекторной активности судили по способности образца защищать эритроциты от разрушения (гемолиза) в условиях Н2О2- либо ААРН-индуцированного окислительного стресса. Антиоксидантную активность оценивали по их способности ингибировать окисление нативного гемоглобина (oxyHb) до метгемоглобина (metHb) и феррилгемоглобина (ferrylHb), а также предотвращать накопление вторичных продуктов ПОЛ (ТБК-АП), образующихся вследствие интенсификации свободнорадикальных процессов в мембранах эритроцитов.
2-((1S,2R,5S)-6,6-Диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол I показал способность не только ингибировать ПОЛ в неклеточной среде (фиг. 2), но и защищать эритроциты от гибели в условиях острого окислительного стресса, индуцированного Н2О2 (p = 0.007) либо ААРН (p = 0.004) (фиг. 2). Указанное соединение статистически значимо снижало накопление в клетках вторичных продуктов ПОЛ и ингибировало окисление в них нативного оксигемоглобина (oxyHb) до мет- (metHb) и феррил- (ferrylHb) форм под воздействием Н2О2 (табл. 3).
На фиг. 2 представлено влияние 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанил-этанола I (100 мкМ) на уровень Н2О2- и ААРН-индуцированного гемолиза эритроцитов через 1–5 ч инкубации. В таблице 3 показано влияние 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола I (100 мкМ) на содержание вторичных продуктов ПОЛ (ТБК-АП) и соотношение окисленных и нативной форм гемоглобина в эритроцитах в условиях окислительного стресса, инициированного внесением H2O2.
Полученные результаты указывают на то, что 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанол обладает антиоксидантной активностью, что проявляется в способности тормозить процессы ПОЛ в неклеточной среде, содержащей животные липиды, а также ингибировать Н2О2- и ААРН-индуцированный гемолиз эритроцитов, снижать накопление в клетках вторичных продуктов ПОЛ и предотвращать окисление в них нативного оксигемоглобина.
Примеры использования 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метил-сульфанилэтанола (соединения I).
Из представленного исследования следует, что отличительной особенностью полученного соединения I является его способность избирательно блокировать агрегацию тромбоцитов, вызываемую коллагеном, который является более сильным индуктором, чем АДФ. Известно, что активация коллаген-зависимых рецепторов приводит к увеличению внутриклеточной концентрации ионов кальция за счет поступления их из окружающей среды. Это вызывает изменение структуры клеточной мембраны тромбоцитов, и она приобретает тромбогенные свойства, что в свою очередь приводит к активации плазменного гемостаза.
Таким образом, соединение, полученное заявленным способом, в отличие от используемых антиагрегационных препаратов не только блокирует агрегацию тромбоцитов, но и ингибирует плазменный гемостаз, а также обладает мембранопротекторным и антиоксидантным действием. Поэтому способ получения соединения может оказаться перспективным для разработки принципиально новых препаратов, используемых для профилактики и лечения тромбофилии. Обнаруженные и описанные биологические свойства соединения I могут быть использованы в медицинской практике для создания препаратов для лечения заболеваний крови, связанных с окислительно-восстановительным равновесием и сворачиваемостью крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| Антиагрегационное и антиоксидантное средство | 2023 |
|
RU2808474C1 |
| 2-(1S,2R,5S)-6,6-ДИМЕТИЛБИЦИКЛО[3.1.1]ГЕПТ-2ИЛ]МЕТИЛ}СУЛЬФИНИЛ)ЭТАНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ АНТИАГРЕГАЦИОННЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2522198C2 |
| Применение пинанилсульфида с метилмеркаптоацетатным фрагментом - метил 2-({ [(1S, 2R, 5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил]метил} тио)ацетата, обладающий ингибирующим действием на активацию тромбоцитов | 2015 |
|
RU2671567C2 |
| Кумарины с бициклическими монотерпеновыми заместителями | 2019 |
|
RU2707103C1 |
| Сульфатированный полисахарид на основе целлюлозы с привитым терпенофенолом, способ его получения и средство, обладающее антирадикальной, антиоксидантной и мембранопротекторной активностью | 2021 |
|
RU2767207C1 |
| Хиральные цис-миртанилсульфонамиды на основе (-)-β-пинена | 2021 |
|
RU2765749C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2,6-ДИИЗОБОРНИЛФЕНОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2516699C2 |
| Сульфопроизводные на основе бета-пинена и способ их получения | 2019 |
|
RU2708617C1 |
| Хиральные трифторметилированные монотерпеновые тиоацетаты и тиолы на основе миртеналя | 2020 |
|
RU2743302C1 |
| ХИРАЛЬНЫЕ МИРТАНИЛСУЛЬФОНАМИДЫ | 2019 |
|
RU2725878C1 |

Изобретение относится к области органического синтеза, а именно к способу получения соединения, которое может быть использовано в медицинской практике в качестве средства, обладающего антиагрегационным и антиоксидантным действием. Раскрывается способ получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола формулы I путем взаимодействия цис-миртантиола с 2-бромэтанолом в присутствии карбоната цезия (Cs2CO3) и иодида тетрабутиламмония (TBAI) при нагревании смеси в среде инертного газа до полного расходования цис-миртантиола. Использование изобретения позволяет повысить выход целевого соединения до 95%. 2 ил. 3 табл., 5 пр.

Способ получения 2-((1S,2R,5S)-6,6-диметилбицикло[3.1.1]гепт-2-ил)метилсульфанилэтанола формулы I

обладающего антиагрегационной и антиоксидантной активностью, включающий выделение целевого продукта методом колоночной хроматографии, отличающийся тем, что способ осуществляют путем взаимодействия цис-миртантиола с 2-бромэтанолом в присутствии карбоната цезия (Cs2CO3) и иодида тетрабутиламмония (TBAI) при нагревании смеси в среде инертного газа, при этом осуществляют бимолекулярное нуклеофильное замещение брома в 2-бромэтаноле цис-миртантиолом, процесс ведут до полного расходования цис-миртантиола.
| Nikitina, Liliya & Startseva, V | |||
| & Dieva, S | |||
| & Vakulenko, I | |||
| & Shamov, Grigory | |||
| Reaction of β-pinene and thiols in the presence of Lewis acids | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ получения кодеина | 1922 |
|
SU178A1 |
| Firdaus, Maulidan & Espinosa, Lucas & Meier, Michael | |||
| Terpene-Based Renewable Monomers and Polymers via Thiol-Ene Additions | |||
| Macromolecules, 2011, | |||
Авторы
Даты
2024-05-20—Публикация
2023-10-25—Подача