Настоящее изобретение относится к способу создания оптических окон прозрачности слизистой оболочки десны в ультрафиолетовой (УФ) области электромагнитного спектра, в частности к способу повышения прозрачности таких тканей и может быть использовано в медицине для лечения и ранней диагностики стоматологических заболеваний, в частности хронического рецидивирующего афтозного стоматита, герпесного стоматита, для профилактики и лечения вирусной инфекции ротоглотки и др.
При взаимодействии излучения с биологическими тканями наблюдаются в основном такие эффекты как поглощение, отражение и рассеяние, которые в различной степени вносят существенный вклад при диагностике заболеваний, исследовании здоровых и патологических биотканей, при разработке фототермических и светотерапевтических процедур и т.д. Совершенствование оптических систем в последние десятилетия, открытие лазерных и светодиодных источников, широкое использование компьютеров, микропроцессоров и разработка новых технологий получения трехмерных изображений позволили сделать следующий значительный шаг в технологии визуализации тканей на клеточном и субклеточных уровнях.
Благодаря значительному развитию оптических и, в частности, лазерных методов, используемых, как для неинвазивной медицинской диагностики, так и для фототерапии, актуальной является проблема, связанная с увеличением глубины проникновения излучения в биологические ткани, которая решается с помощью применения иммерсионных просветляющих агентов, в том числе и гиперосмотических, таких как глицерин, пропиленгликоль (см. например, патент РФ 2633494, МПК G01N 21/01, опубл. 12.10.2017).
Иммерсионный метод повышения прозрачности ткани в настоящее время является предпочтительным, поскольку воздействие, применяемое для замены тканевой воды на биологически совместимый агент, является временным и обратимым. Эти действия в идеале могут сделать ткань полностью прозрачной, что было продемонстрировано на органах мелких животных. Обратимость этого метода может быть обеспечена за счет естественной или вспомогательной регидратации, в зависимости от того, находится ли ткань в состоянии in vivo или ex vivo.
Был изучен целый ряд иммерсионных агентов и определен их потенциал для расширения окон прозрачности в видимом и ближнем ИК диапазонах для различных тканей и крови. Наиболее распространенные иммерсионные агенты представляют собой сахара, такие как глюкоза, фруктоза, сахароза, маннитол; спирты, такие как глицерин; органические растворители, такие как диметилсульфоксид (ДМСО), пропиленгликоль; или коммерческие рентгеноконтрастные агенты, такие как Тразограф™ или Омнипак™. Когда эти агенты наносят или в них погружают такие ткани, как кожа, мышечная ткань, склера или ткани желудочного тракта, то наблюдается увеличение коллимированного пропускания ткани (Tc) и достигается лучший контраст оптических изображений, полученных из более глубоких слоев ткани. Таким образом, метод иммерсионного оптического просветления позволяет расширять оптические окна прозрачности ткани, которые дают возможность диагностировать и лечить патологии с помощью света. До недавнего времени такие окна наблюдались только в видимой и ближней инфракрасной области спектра.
Недавние исследования показывают, что, когда биологические ткани анализируются во время воздействия иммерсионных агентов, окно прозрачности, расположенное между длинами волн 600 и 1000 нм, становится более широким и эффективным, что хорошо видно по поведению коллимированного пропускания ткани Tc в этой области. Некоторые недавние обзорные статьи подтверждают растущее число публикаций и исследований, проводимых в этой области исследований за последние 20 лет, что указывает на эффективность этого метода для улучшения глубинной визуализации тканей и для его применения в сочетании с методами неинвазивной диагностики и лечения с использованием света.
На эту тему опубликован ряд патентов:
Известен способ увеличения светопропускания в биологической ткани, включающий временную замену тканевой воды жидкостью, показатель преломления которой близок к показателям межклеточных/внутриклеточных компонентов, вследствие чего создается переходное окно для улучшения пропускания света для терапевтических и /или диагностических применений (см. патент US 6275726, МПК A61B 3/12, опубл. 14.08.2001). Способ позволяет усилить пропускания биологической ткани в спектральной области между видимым и ближним инфракрасным диапазоном при использовании иммерсионных агентов.
Известен ряд изобретений, описывающих различные иммерсионные агенты и способы их получения (см. CN 102749231, CN 101487775, CN 104568553, CN 1063900138).
Однако все эти изобретения направлены на обеспечение роста прозрачности тканей в видимой и ближней инфракрасной области в области уже существующих окон прозрачности с помощью иммерсионных агентов, причем ни один из них не рассматривает метод иммерсионного просветления в УФ-диапазоне.
Наиболее близким к предлагаемому является способ оптического просветления биологических тканей, который включает пропитывание ткани биологически совместимым иммерсионным агентом для создания оптических окон прозрачности в ультрафиолетовый (УФ) области электромагнитного спектра (см. заявку на изобретение PT115371, МПК G01N-001/28, опубл. 14.09.20).
Однако, данный способ освещает образование двух окон прозрачности при иммерсии слизистой в гиперосмотических агентах и не предусматривает применение в ротовой полости.
Техническая проблема заключается в разработке способа оптического просветления слизистой полости рта за счет использования иммерсионного агента, обеспечивающего создание окон прозрачности слизистой полости рта путем исследования количественных кинетических характеристик коэффициентов полного пропускания.
Технический результат заключается в создании трех окон прозрачности в ультрафиолетовой области спектра с положением центра первого окна прозрачности (200±3) нм с шириной на уровне половинной интенсивности (38±7) нм, второго окна -(283±4) нм с шириной (39±8) нм и третьего окна - (344±13) нм с шириной (72±5) нм.
Для достижения технического результата в способе оптического просветления биологических тканей, включающем пропитывание ткани биологически совместимым иммерсионным агентом для создания оптических окон прозрачности в ультрафиолетовой области электромагнитного спектра, согласно изобретению, в качестве иммерсионного агента используют смесь глицерина с пропиленгликолем в концентрациях масс. %, 30/70 или 50/50 или в сочетании с водой 55/35/10, которой пропитывают слизистую ткань полости рта в течение 8 -15 минут.
Для обеспечения дополнительного комфорта и увеличения скорости диффузии иммерсионного агента, иммерсионный агент предварительного нагревают до температуры, равной температуре биологической ткани 37-39°С.
Изобретение поясняется чертежами, где представлены:
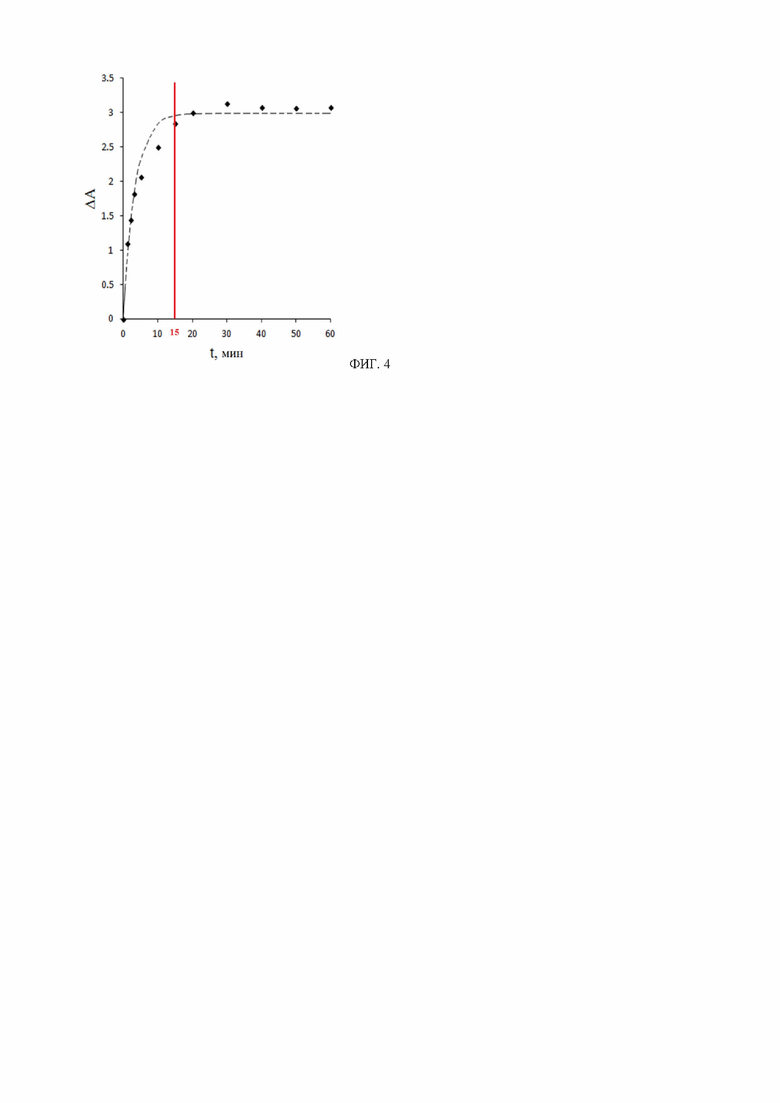
на фиг. 1 - спектры поглощения гемоглобина - HbH, оксигемоглобина - HbO2, дезоксигемоглобина - HbH, метгемоглобина - HbMet, карбоксигемоглобина - HbCO, которые обнаружены в исходном образце слизистой десны (как эндогенные хромофоры);
на фиг. 2 - спектры слизистой десны: а- диффузного отражения, б - полного пропускания, с провалами на характерных линиях поглощения оксигемоглобина; R - коэффициент диффузного отражения; Т - коэффициент полного пропускания;
на фиг. 3 - выявленные окна прозрачности в УФ области спектра при иммерсии слизистой десны в смеси глицерина и пропиленгликоля: а - в диапазоне от 200 до 800 нм, б - в диапазоне от 200 до 400 нм;
на фиг. 4 - кинетика разности эффективной оптической плотности (ΔА) процесса иммерсии слизистой десны свиньи смесью глицерина и пропиленгликоля; A=-logR эффективная оптическая плотность; ΔА - разница между начальным значением эффективной оптической плотности А и значением А в текущий момент времени.
Способ осуществляется следующим образом.
Готовят смеси иммерсионного агента пропиленгликоля и глицерина в соотношении 30/70 или 50/50 или в сочетании с водой 55/35/10. В качестве агентов могут быть использованы готовые смеси - вейпы соответствующего состава.
Каждой смесью пропитывают стерильный бинт и делают аппликации каждой из смесей в течение 8-15 минут на всю слизистую оболочку полости рта (СОПР).
В результате проведенных процедур образуются окна прозрачности, которые можно использовать для проведения диагностических, профилактических и терапевтически процедур в ультрафиолетовом диапазоне.
Положение окон прозрачности находили по 5 параллельным измерениям in vitro. Измеренные спектры полного пропускания слизистой десны после полной иммерсии в смеси оценивали по увеличению полного пропускания и по правилам статистики определяли границы увеличенных областей (окон прозрачности). Максимальное значение в коэффициентах полного пропускания также усредняли и называли центром окна прозрачности.
С оптической точки зрения ткань слизистой десны можно отнести к оптически мутным средам, в которых наряду с поглощением наблюдается сильное рассеяние света. При распространении оптического излучения в ткани хромофоры - вещества эндогенного или экзогенного происхождения, способны поглощать энергию излучения (фотоны). Основными хромофорами биотканей являются вода, белки и липиды, гемоглобин, поглощение которых играет важную роль в определении оптических свойств ткани и, особенно, в определении глубины проникновения излучения в ткань. Для мягких тканей вода является наиболее важными эндогенными хромофорами, однако пропускание воды в измеренном диапазоне 350-800 нм незначительно и начинает влиять в диапазоне 1200-2500 нм. Таким образом, слизистую оболочку десны можно отнести к волокнистым тканям, оптические свойства которых определяются в основном коллагеновыми и аргирофильными волокнами и гемоглобином в ткани десны.
На фиг. 1 показаны спектры поглощения гемоглобина и его форм. В области от 350 до 650 нм форма спектра диффузного отражения (СДО) достаточно хорошо коррелирует с формой спектра пропускания десны, т.к. в этом диапазоне длин волн форма спектров определяется сильными полосами поглощения оксигемоглобина и влиянием рассеяния света на основных рассеивателях слизистой десны - коллагеновых и эластиновых волокнах (см. фиг. 2, а, б).
На СДО и спектрах пропускания хорошо видны провалы, соответствующие полосам поглощения оксигемоглобина на длинах волн 415, 542 и 576 нм. Наличие сильных полос поглощения уменьшает как число прошедших, так и обратно рассеянных фотонов в пределах полос поглощения. Начиная с 650 нм и далее до 800 нм, влияние полос поглощения гемоглобина уже не существенно, спектры полного пропускания и обратного отражения формируются в основном за счет рассеяния, поскольку вклад полос поглощения всех хромофоров мягких тканей в этой области минимален, что соответствует их «терапевтическому окну прозрачности» и свет в этой области проходит в ткани на большую глубину.
Основным источником рассеяния света в биотканях является неоднородность показателя преломления за счет различия его значений для компонентов биотканей, т.е. митохондрий, ядер, других органелл и цитоплазмы клеток; или для внутритканевой жидкости и структурных элементов соединительной (фиброзной) ткани (коллагеновых и эластиновых волокон). При введении в биоткань иммерсионной жидкости, имеющей показатель преломления больший, чем у внутритканевой жидкости, происходит частичное замещение внутритканевой жидкости иммерсионным агентом, что вызывает выравнивание показателей преломления рассеивателей (например, коллагеновых волокон) ткани и окружающей их среды, и, как следствие, значительное снижение светорассеяния [D. Jing, Y. Yi, W. Luo, S. Zhang, Q. Yuan, J. Wang, E. Lachika, Z. Zhao, and H. Zhao, Tissue clearing and its application to bone and dental tissues, J. Dent. Res. 98(6), 621-631 (2019). doi: 10.1177/0022034519844510.]. Авторами [Genin, V.D. Optical clearing of the gastric mucosa using 40%-glucose solution / V.D. Genin, E.A. Genina, S.V. Kapralov et al. // Journal of Biomedical Photonics & Engineering. - 2019. - Vol. 5 (3). - P. 030302.] исследовалась кинетика коллимированного пропускания слизистой оболочки желудка под действием водного 40% раствора глюкозы. Было установлено, что применение данного просветляющего агента увеличивает глубину проникновение света от 5% до 15%, в зависимости от выбранного спектрального диапазона. Изменение кинетики коллимированного пропускания твердой мозговой оболочки человека in vitro в диапазоне 400-700 нм 40% раствора глюкозы описано в [Башкатов, А.Н. Определение коэффициента диффузии глюкозы в твердой мозговой оболочке человека / А.Н. Башкатов, Э.А. Генина, В.В. Тучин // Известия Саратовского университета, Новая серия, Серия Физика. - 2018. - Т. 18 (1). - С. 32-45.]. Определен коэффициент проницаемости твердой мозговой оболочки для глюкозы, равный (1.3±0.13)·10-4 см/с, что увеличивает значения коллимированного пропускания и способствует просветлению биоткани. При исследовании оптических свойств слизистой прямой кишки в диапазоне от 200 до 1000 нм, обработанной водно-глицериновыми растворами, авторами [Carneiro, I. A robust ex vivo method to evaluate the diffusion properties of agents in biological tissues / I. Carneiro, S. Carvalho, R. Henrique et al. // J. Biophoton. - 2019. - Vol. 12 (4). - P. e201800333.] было установлено формирование «динамических» окон прозрачности биоткани с высокой эффективностью в УФ области спектра, которые образуются при иммерсионном просветлении и только на время действия просветляющего агента. Обработка колоректальной слизистой создает два новых оптических окна с пиками эффективности пропускания при 230 нм и 300 нм, что открывает возможность разработки клинических процедур для постановки диагноза или лечения в ультрафиолетовом диапазоне.
Для создания корректных методик с оптимальным режимом использования потенциально высокотравматичного лазерного излучения, сеансов фотодинамических процедур и физиотерапевтического светолечения, а также при проведении диагностических процедур, основанных на количественном определении концентрации контрастного агента внутри нормальных и патологически измененных биотканей (томографические, флуоресцентные методы и др.), актуальным является вопрос определения проницаемости биоткани к тому или иному препарату и коэффициента диффузии агента в биологической ткани.
Поскольку структура биологических тканей сложна, и процессы диффузии различных лекарственных составов и веществ имеют нелинейные решения, определение количественных кинетических характеристик - важная и актуальная биофизическая задача.
Пример.
Были проведены исследования ex vivo по иммерсии тканей слизистой свободной десны человека (полученные после хирургических вмешательств с получением письменного согласия пациентов на работу с их биоматериалом) и прикрепленной десны свиньи ex vivo смесью глицерина и пропиленгликоля в различных соотношениях.
Для измерения коэффициентов полного пропускания образцов тканей в спектральном диапазоне 200-800 нм использовали двухлучевой спектрофотометр Shimadzu UV-2550 (Япония) с интегрирующей сферой. Источником излучения служила галогенная лампа с фильтрацией излучения в исследуемом спектральном диапазоне. Предельное разрешение спектрометра составляло 0.1 нм. Спектры были нормализованы перед измерениями с использованием эталонного отражателя BaSO4, который обладает лучшими свойствами в УФ. Все измерения проводились при комнатной температуре (~25°С) и нормальном атмосферном давлении. Каждый образец исследуемой ткани фиксировали в специальной рамке с окном 0.5×0.5 см и фиксировали в кварцевой кювете так, чтобы образец ткани прижимался к стенке кюветы и подвергался оптическому измерению. Чтобы измерить спектры полного пропускания (СПП), кварцевая кювета с образцом ткани была установлена непосредственно перед интегрирующей сферой, собирая все излучение, прошедшее через образец ткани. Диаметр светового пучка, падающего на образец, составлял 3 мм. Перед измерениями кварцевую кювету с фиксированным образцом заполняли физиологическим раствором, чтобы увлажнить образец и приблизить результаты измерений к ex vivo. Затем кювету наполняли смесью просветляющих агентов и проводили регистрацию спектров полного пропускания до прекращения изменений.
Проведенные исследования выявили, что при иммерсии ткани слизистой десны просветляющими смесями появляются три дополнительных оптических окна в УФ области спектра: положение центра первого окна прозрачности составило (200±3) нм с шириной на уровне половинной интенсивности (38±7) нм; положение центра второго окна составило (283±4) нм с шириной (39±8) нм; и положение третьего окна составило (344±13) нм с шириной (72±5) нм (см. фиг. 3, а, б).
Как видно из фиг 4 , значительный рост показателя ΔА наблюдается в интервале от 0 до 8 минут, незначительный рост данного показателя наблюдается в интервале от 8 до 15 минут, после чего рост показателя не наблюдается, что объясняется практически полным насыщением десны просветляющим агентом. Таким образом, верхняя граница временного интервала ограничена 15 минутами, а нижняя 8 минутами.
Эффективность оптического просветления оценивалась по формуле:
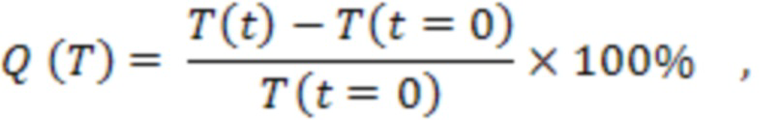
где Q - эффективность оптического просветления;
T - полное пропускание ткани.
t - время взаимодействия биоткани с агентом.
Эффективность оптического просветления (ОП) тканей десны при иммерсии смесью глицерина GL и пропиленгликоля PG в различных соотношениях представлена в таблице.
(30/70/0)
54
218
59
43
48
(55/35/10)
(50/50/0)
Положение центра первого окна прозрачности составило (200±3) нм с шириной на уровне половинной интенсивности (38±7) нм; положение центра второго окна составило (283±4) нм с шириной (39±8) нм; положение третьего окна составило (344±13) нм с шириной (72±5) нм.
Первое окно имеет наибольшую эффективность при иммерсии слизистой десны со смесью PG/GL/W (55/35/10) с максимальной эффективностью оптического просветления до 1309±54%. Эффективность оптического просветления у второго окна наибольшая у смеси PG/GL/W (50/50/0) и достигает 1200±78 %. Третье окно прозрачности в УФ области достигает наибольших значений при иммерсии слизистой десны со смесью PG/GL/W (50/50/0) и достигает 1352±79%.
Таким образом, заявляемый способ оптического просветления слизистой полости рта создает три окна прозрачности в УФ области спектра, что позволит его использовать для эффективной диагностики, профилактики и терапии в стоматологии. В частности, способ позволит осуществлять иммерсионное просветление совместно с одним из терапевтических методов, использующих ультрафиолетовые лучи в диапазоне 200-400 нм.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОЗДАНИЯ ОПТИЧЕСКИХ ОКОН ПРОЗРАЧНОСТИ БИОЛОГИЧЕСКИХ ТКАНЕЙ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ В УЛЬТРАФИОЛЕТОВОЙ ОБЛАСТИ | 2019 |
|
RU2745614C1 |
| СПОСОБ ФОТОТЕРАПИИ ХРОНИЧЕСКОГО РЕЦИДИВИРУЮЩЕГО АФТОЗНОГО СТОМАТИТА | 2021 |
|
RU2768593C1 |
| Способ определения фазы цикла яичников | 2023 |
|
RU2826570C1 |
| СПОСОБ ВИЗУАЛИЗАЦИИ БИОЛОГИЧЕСКИХ ТКАНЕЙ И/ИЛИ ОРГАНОВ | 2019 |
|
RU2735463C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКОГО ИЗОБРАЖЕНИЯ МЕЖФАЛАНГОВЫХ СУСТАВОВ И ОПТИЧЕСКИЙ СЕНСОР ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2018 |
|
RU2697594C1 |
| Биосенсор для неинвазивного оптического мониторинга патологии биологических тканей | 2016 |
|
RU2633494C2 |
| СПОСОБ ИССЛЕДОВАНИЯ СОСТОЯНИЯ КОЖИ МЕТОДОМ ОПТИЧЕСКОЙ КОГЕРЕНТНОЙ ТОМОГРАФИИ | 2007 |
|
RU2387365C2 |
| СПОСОБ ЛАЗЕРНОЙ БИОМОДУЛЯЦИИ И ПОВЫШЕНИЯ ПРОНИЦАЕМОСТИ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2019 |
|
RU2740123C1 |
| СПОСОБ ЛАЗЕРНОЙ ГИПЕРТЕРМИИ ОПУХОЛЕЙ ПРИ ВВЕДЕНИИ ПЛАЗМОННО-РЕЗОНАНСНЫХ НАНОЧАСТИЦ С ПРИМЕНЕНИЕМ ТЕХНИКИ ИММЕРСИОННОГО ОПТИЧЕСКОГО ПРОСВЕТЛЕНИЯ | 2022 |
|
RU2800156C1 |
| МЯГКАЯ ДИАФРАГМА ДЛЯ ЛАЗЕРОВ | 1998 |
|
RU2157034C2 |
Изобретение относится к медицине, а именно к стоматологии, и может быть использовано для оптического просветления слизистой оболочки десны для лечения и ранней диагностики стоматологических заболеваний. Способ включает пропитывание ткани биологически совместимым иммерсионным агентом для создания оптических окон прозрачности в ультрафиолетовой области электромагнитного спектра. В качестве иммерсионного агента используют смесь глицерина с пропиленгликолем в концентрациях, масс. %, 30/70 или 50/50 или в сочетании с водой 55/35/10, которой пропитывают слизистую ткань полости рта в течение 8-15 мин. Использование изобретения позволяет создать три окна прозрачности в ультрафиолетовой области спектра с положением центра первого окна прозрачности 200±3 нм с шириной на уровне половинной интенсивности 38±7 нм, второго окна - 283±4 нм с шириной 39±8 нм и третьего окна - 344±13 нм с шириной 72±5 нм. 1 з.п. ф-лы, 4 ил., 1 табл., 1 пр.
1. Способ оптического просветления биологических тканей, включающий пропитывание ткани биологически совместимым иммерсионным агентом для создания оптических окон прозрачности в ультрафиолетовой области электромагнитного спектра, отличающийся тем, что в качестве иммерсионного агента используют смесь глицерина с пропиленгликолем в концентрациях, масс. %, 30/70 или 50/50 или в сочетании с водой 55/35/10, которой пропитывают слизистую ткань полости рта в течение 8-15 мин.
2. Способ по п.1, отличающийся тем, что иммерсионный агент предварительного нагревают до температуры, равной температуре биологической ткани 37-39°С.
| СПОСОБ ВИЗУАЛИЗАЦИИ БИОЛОГИЧЕСКИХ ТКАНЕЙ И/ИЛИ ОРГАНОВ | 2019 |
|
RU2735463C1 |
| Биосенсор для неинвазивного оптического мониторинга патологии биологических тканей | 2016 |
|
RU2633494C2 |
| CN 102749231B, 09.07.2012 | |||
| CARNEIRO I | |||
| et al | |||
| A robust ex vivo method to evaluate the diffusion properties of agents in biological tissues // J | |||
| Biophoton | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| - Vol | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| - P | |||
| e201800333, реферат | |||
| JING D | |||
| et al | |||
| Tissue clearing and its application to bone and dental tissues, J | |||
| Dent | |||
Авторы
Даты
2022-03-24—Публикация
2021-07-12—Подача