ОБЛАСТЬ ТЕХНИКИ
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент Австралии №2017900385 (поданной 8 февраля 2017), содержание которой включено во всей полноте в настоящую заявку.
Настоящее изобретение относится к лечению или предупреждению инфекции, вызванной вирусом гриппа. В частности, настоящее изобретение относится к противовирусным соединениям и их применению в лечении или предупреждении инфекции, вызванной вирусом гриппа.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Любое обсуждение известного уровня техники по всему описанию изобретения не следует рассматривать как признание того, что такой известный уровень техники является широко известным или образует часть обычных известных знаний в этой области.
Грипп представляет собой одно из нескольких наиболее распространенных инфекционных заболеваний, плохо контролируемых современной медициной. Бремя гриппа является тяжелым, согласно оценкам Всемирной Организации Здравоохранения, 5-10% взрослых и 20-30% детей населения Земли (3-5 миллионов человек) поражается в ежегодных эпидемиях, вызывающих от 250000 до 500000 смертей в год.
Симптомы гриппозной инфекции могут быть от умеренных до тяжелых. Самые распространенные симптомы включают: высокую температуру, насморк, боль в горле, мышечные боли, головную боль, кашель и слабость. Осложнения, ассоциированные с гриппом, включают пневмонию, бронхит, инфекции носовых пазух и инфекции уха. Другие возможные серьезные осложнения, вызываемые гриппом, могут включать воспаление сердца, головного мозга или мышц и функциональную недостаточность многих органов. Инфекция дыхательных путей может вызывать экстремальную воспалительную реакцию организма и может приводить к сепсису. Грипп также может усугубить хронические проблемы со здоровьем. Например, люди, страдающие астмой, могут переносить приступы астмы в то время, как они имеют грипп, и люди с хроническим заболеванием сердца могут переносить ухудшение этого состояния, вызванное гриппом.
Грипп вызывается вирусом семейства Orthomyxoviridae, и существует три типа вирусов гриппа, которые поражают людей, называющиеся тип А, тип В и тип С. Эти вирусы гриппа обычно приводят к похожим симптомам, но типы вируса не связаны в антигеном отношении, в результате чего инфекция от одного типа не обеспечивает иммунитет против другого. Вирусы гриппа А и В вызывают сезонные эпидемии почти каждую зиму. Возникновение нового и совершенно непохожего вируса гриппа А с инфицированием людей может вызвать пандемию гриппа. Инфекции гриппа типа С обычно вызывают умеренную респираторную заболеваемость и не считаются причиной эпидемий.
Вирус гриппа А можно разделить на разные подтипы согласно генетическим вариантам двух разных белков поверхности вируса: гемагглютинина (НА/Н в подтипе) и нейраминидазы (NA/N в подтипе). Существует 16 разных НА и 9 NA, которые различаются серологически. Вирусы гриппа В не делятся на подтипы, но могут быть разделены на линии. Распространяющиеся в настоящее время вирусы гриппа В принадлежат одной из двух линий: B/Yamagata и B/Victoria. Также существуют варианты и конкретные изоляты штамма гриппа определяют по стандартной системе условных обозначений, описывающих тип вируса, происхождение хозяина, географическое происхождение, порядковый номер выделения, год выделения и подтипы НА и NA для гриппа А.
При появлении нового штамма вируса гриппа, население имеет незначительную нативную устойчивость, и существующие противогриппозные вакцины часто имеют ограниченную эффективность, так как они обычно активны против конкретных вирусов гриппа А и В, которые отличаются от вирусов возникшего штамма. Этот феномен приводит к эпидемиям, которые случаются регулярно. Кроме того, вирусы гриппа претерпевают постепенное антигенное варьирование (антигенный дрейф), которое понижает уровень иммунологической устойчивости против обновленной инфекции. Пандемии случаются каждые два десятилетия и происходят вследствие резкого изменения (антигенного сдвига) у подтипов вирусных НА и NA.
Вакцины против гриппа, содержащие убитые штаммы типов А и В вируса, распространяющегося в настоящее время, имеются в продаже, но имеют процент успеха в предупреждении инфекции только от 50 до 60%. Стандартные вакцины против гриппа должны модернизироваться каждый год для противодействия новым вариантам вируса. Кроме того, любой предлагаемый иммунитет является кратковременным. По этой причине вакцины не могут предупреждать или ограничивать пандемию, если распространяющиеся штаммы продолжают дрейфовать значительно или возникает другой подтип. Вместе с тем, противовирусные агенты будут решающими для первоначального контроля и защиты против возникающей пандемии.
Одобрены два класса противовирусных препаратов для клинического использования против гриппа человека:
• Ингибитор нейраминидазы - включая осельтамивир, занамивир и перамивир.
• Ингибитор ионных каналов М2 - включая амантадин и римантадин. Эти медицинские препараты активны против вируса гриппа А, но не против вируса гриппа В из-за структурно отличающихся каналов М2.
Осельтамивир стал предпочтительным выбором ингибитора нейраминидазы для правительств и организаций в их подготовках к возможным пандемиям гриппа благодаря пероральной его доставке. Запасы осельтамивира были использованы в 2009 г во время пандемии гриппа A H1N1 (Nguyen-Van-Tam et al., Clin Microbiol Infect, 2015. 21: 222-22). Однако клиническая эффективность ингибитора нейраминидазы, такого как осельтамивир, все еще подвергается полемике. Недавние доклады показали, что осельтамивир снижает время до облегчения симптомов гриппа у взрослых только до 16,8 часа (Jefferson et al., Cochrane Database Syst Rev 2014;4) и не снижает значительно частоту пневмонии, серьезных осложнений, госпитализаций или смертей (Nguyen-Van-Tam et al., Clin Microbiol Infect, 2015. 21: 222-225). Кроме того, было показано, что применение осельтамивира повышает риск побочных эффектов, таких как тошнота, рвота, психиатрические эффекты и явления, связанные с почками, у взрослых и рвота у детей (Jefferson et al., Cochrane Database Syst Rev 2014;4).
До 2007 устойчивость к ингибитору нейраминидазы среди вирусов гриппа обычно была низкой, приблизительно 1% (Ilyushina et al., Antivir Res, 2006. 70(3): 121-131; Stiver, CMAJ, 2003. 168(1):49-57). Однако Центр по контролю и профилактике болезней сообщал в 2007-2008, что грипп A(H1N1) показал возникновение и распространение по всему миру устойчивости к осельтамивиру. Устойчивые к осельтамивиру вирусы гриппа А, несущие мутацию H275Y NA, возникли в результате генетического дрейфа и медикаментозного лечения. С возникновения этого штамма вируса гриппа, устойчивого к осельтамивиру, имеет место беспокойство, что замещение H275Y может генерировать будущую пандемию или даже фиксироваться в вирусном геноме. Это ставит под сомнение целесообразность создания резервных запасов ингибитора нейраминидазы (Nguyen-Van-Tam et al., Clin Microbiol Infect, 2015. 21: 222-225) и заостряет внимание на необходимости непрерывно отслеживать чувствительность к противовирусным лекарственных средствам, и выдвигает на первый план изыскание новых лекарственных средств против вируса гриппа (Samson, et al. Antiviral Res. 2013, 98(2): 174-85).
В отличие от ингибитора нейраминидазы, амантадин и римантадин являются недорогими и широкодоступными. Амантадин представляет собой производное адамантана, который эффективно подавляет репликацию вируса гриппа A (Davies et al., Science, 1964. 144: 862-863). Лекарственное средство подавляет репликацию путем непосредственного связывания с белком М2 вируса гриппа в мембране оболочки и блокирования активности его Н+-проводящих ионных каналов, которая важна для репликации вируса (Sugrue & Hay, Virology, 1991. 180: 617-624; Pinto et al., Cell, 1992. 69: 517-528; Schroeder et al., J Gen Virol, 1994. 75: 3477-3484). В более высоких концентрациях амантадин также опосредованным путем повышает эндосомальный рН, что изменяет чувствительную к рН конформацию гемагглютинина, уменьшая высвобождение инфекционных вирусных частиц (Daniels et al., Cell, 1985. 40: 431-439; Steinhauer et al., Proc Natl Acad Sci, 1991. 88: 11525-11529).
Однако амантадин и римантадин эффективны только против гриппа А, и устойчивые к лекарственному средству варианты могут быть легко получены путем культивирования вируса в присутствии этих агентов (Cochran et al., Ann NY Acad Sci, 1965. 130(1): 432-439; Appleyard, J Gen Virol, 1977. 36: 249-255). Устойчивость к амантадину и римантадину вырабатывается в результате мутаций в трансмембранной области М2, которая сохраняет активность ионных каналов, при этом снижая способности лекарственных средств подавлять репликацию вируса. Встречаемость устойчивых к амантадину штаммов вируса гриппа А, обнаруженных распространяющимися у населения, повысилась от 0,4% в 1995 до 12,3% в 2003-2004 (Bright et al., Lancet. 2005. 366, 1175-1181). В изолятах из Азии 61% штаммов имели мутации, которые придают устойчивость к амантадину.
Существует потребность в новых противовирусных препаратах, которые являются эффективными в лечении разнообразных подтипов и штаммов гриппа, в частности подтипов и штаммов гриппа, которые являются устойчивыми к современным препаратам.
Задача настоящего изобретения заключается в преодолении или улучшении по меньшей мере одного из недостатков известного уровня техники или в предложении полезной альтернативы.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Ранее было продемонстрировано, что, N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамид (BIT225) имеет только ограниченную активность против виропорина М2 гриппа А и не считается подходящим для лечения гриппа (Jalily et al., MolPharm, 2016. 90: 80-95). Однако настоящая заявка неожиданно показывает, что BIT225 имеет активность против разнообразных подтипов и штаммов вируса гриппа. Важно, было обнаружено, что BIT225 обладает активностью против подтипов и штаммов, которые являются устойчивыми к амантадину.
Химическая структура BIT225 показана ниже:
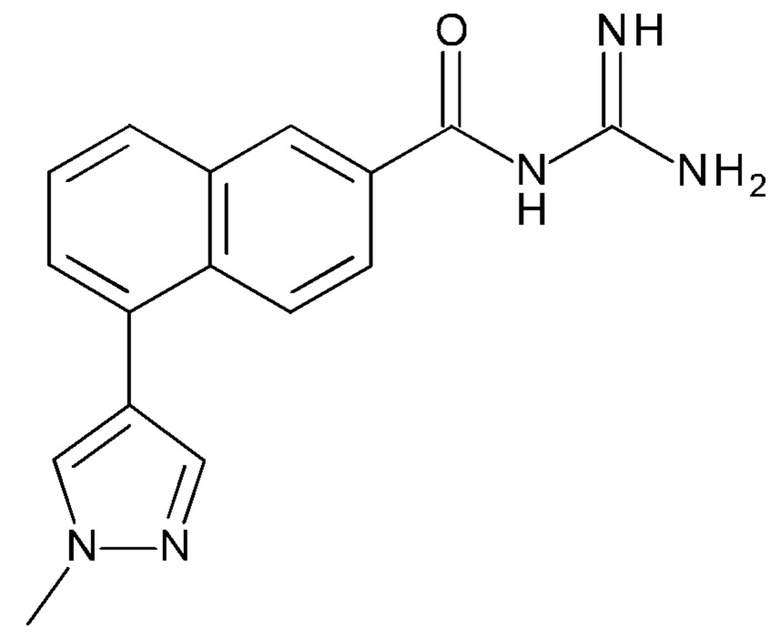
BIT225 также может называться N-карбамимидоил-5-(1-метилпиразол-4-ил)нафталин-2-карбоксамидом или 5-(1-метилпиразол-4-ил)2-нафтоилгуанидином.
Настоящее изобретение главным образом относится к применению BIT225, или его фармацевтически приемлемой соли, в лечении или предупреждении гриппа, в подавлении репликации вируса гриппа, в снижении степени тяжести, интенсивности или продолжительности осложнений или симптомов, ассоциированных с гриппом, или в снижении титра вируса гриппа.
Согласно одному аспекту в настоящем изобретении предложен способ лечения или предупреждения инфекции, вызванной вирусом гриппа, у субъекта, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли.
Согласно другому аспекту в настоящем изобретении предложен способ подавления репликации вируса гриппа у субъекта, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли.
Согласно другому аспекту в настоящем изобретении предложен способ снижения степени тяжести, интенсивности или продолжительности осложнений или симптомов, ассоциированных с инфекцией, вызванной вирусом гриппа, у субъекта, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли.
Согласно другому аспекту в настоящем изобретении предложен способ снижения титра вируса гриппа у субъекта, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли.
Согласно другому аспекту в настоящем изобретении предложено применение N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли для изготовления лекарственного средства для лечения или предупреждения инфекции, вызванной вирусом гриппа.
Согласно другому аспекту в настоящем изобретении предложено применение N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для подавления репликации вируса гриппа.
Согласно другому аспекту в настоящем изобретении предложено применение N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для снижения степени тяжести, интенсивности или продолжительности осложнений или симптомов, ассоциированных с инфекцией, вызванной вирусом гриппа.
Согласно другому аспекту в настоящем изобретении предложено применение N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для снижения титра вируса гриппа.
Согласно другому аспекту в настоящем изобретении предложена композиция, содержащая N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль, для применения в способе лечения или предупреждения инфекции, вызванной вирусом гриппа, у субъекта.
Согласно другому аспекту в настоящем изобретении предложена композиция, содержащая N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль, для применения в способе подавления репликации вируса гриппа у субъекта.
Согласно другому аспекту в настоящем изобретении предложена композиция, содержащая N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль, для применения в способе снижения степени тяжести, интенсивности или продолжительности осложнений или симптомов, ассоциированных с инфекции, вызванной вирусом гриппа, у субъекта.
Согласно другому аспекту в настоящем изобретении предложена композиция, содержащая N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль, для применения в способе снижения титра вируса гриппа у субъекта.
В некоторых воплощениях вирус гриппа выбран из вируса гриппа А, вируса гриппа В и вируса гриппа С.
В некоторых воплощениях вирус гриппа представляет собой вирус гриппа А с хозяином любого происхождения (человеческий, свиной, куриный, конский и так далее).
В некоторых воплощениях вирус гриппа А выбран из подтипов H1N1, H1N2, H2N2, H3N2, H3N8, H5N1, H5N2, H5N3, H5N6, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H7N9, H9N2 и H10N7.
В некоторых воплощениях вирус гриппа А выбран из подтипов H1N1, H3N2 и H5N1.
В некоторых воплощениях вирус гриппа представляет собой вирус гриппа В любой линии.
В некоторых воплощениях вирус гриппа В выбран из линий B/Yamagata и B/Victoria.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят посредством пути, выбранного из перорального, назального, внутривенного, внутрибрюшинного, ингаляционного и местного.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят ежедневно.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят два раза в сутки.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят в дозировке от примерно 100 мг до примерно 600 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально и вводят в дозировке примерно 600 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально и вводят в дозировке примерно 200 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально и вводят в дозировке примерно 100 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально и вводят ежедневно.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально и вводят два раза в сутки.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально один раз в сутки в дозировке примерно 200 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально два раза в сутки в дозировке примерно 200 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально один раз в сутки в дозировке примерно 100 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят перорально два раза в сутки в дозировке примерно 100 мг.
В некоторых воплощениях N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамид или его фармацевтически приемлемую соль вводят в комбинации с одним или более дополнительных противовирусных агентов.
В некоторых воплощениях дополнительные противовирусные агенты выбирают из занамивира, осельтамивира и перамивира.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
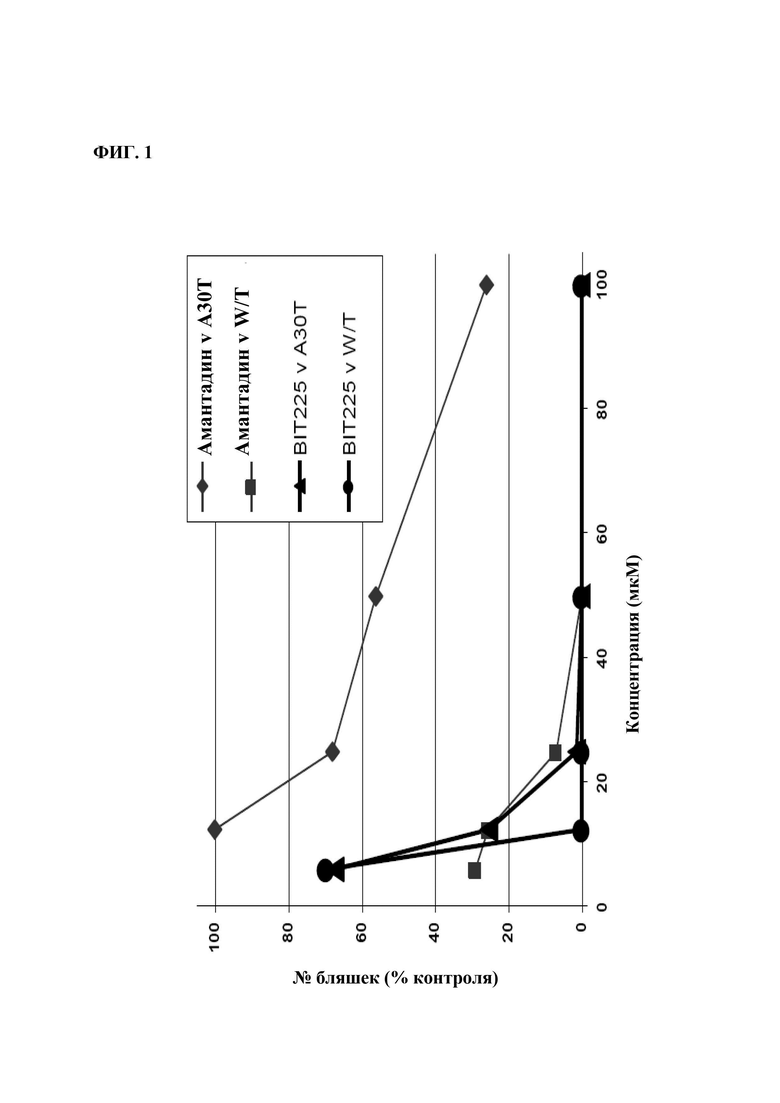
Фиг. 1: На этой Фиг. демонстрируется ЕС50 для BIT225, которая равнялась приблизительно 10 мкМ по сравнению как с вирусом дикого типа, так и с мутантным вирусом А30Т с соответствующими значениями ЕС90 12 мкМ и 18 мкМ. Это резко контрастирует с большим сдвигом чувствительности к лекарственному средству амантадину, вызванным мутацией А30Т в М2.
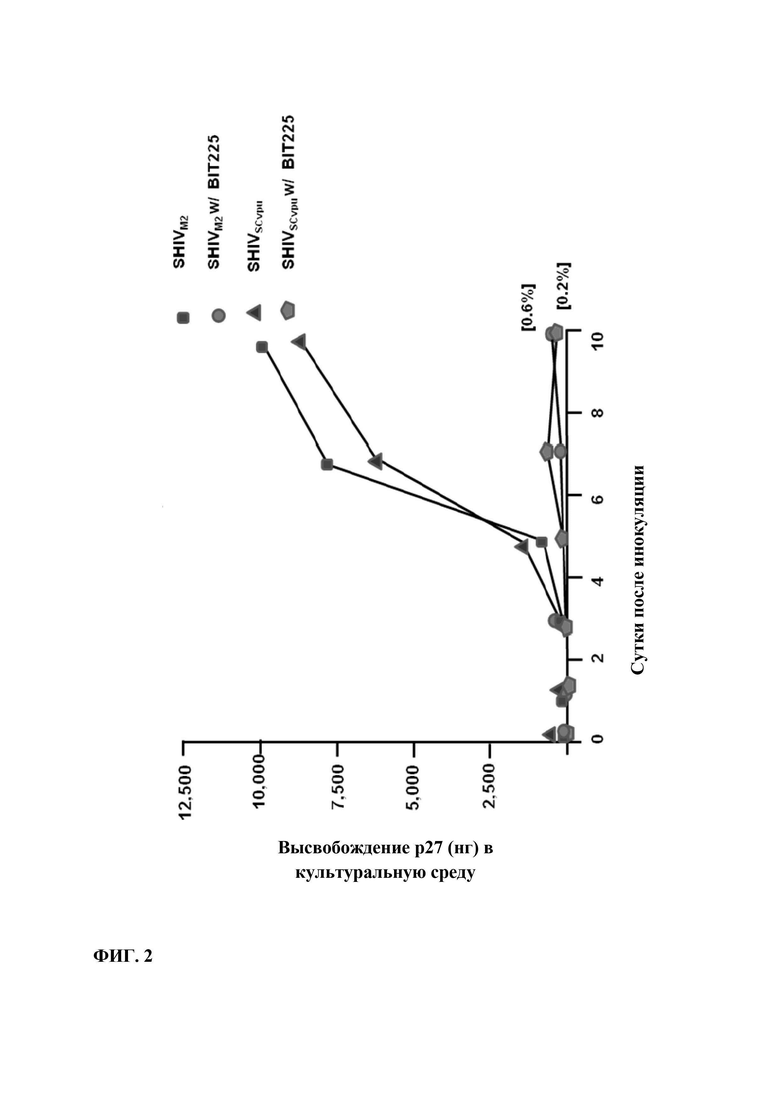
Фиг. 2: На этой Фиг. показано подавление посредством BIT225 репликации в Т-клеточной линии (С8166) химерного вируса SHIV-1M2 и SHIV-1SCVpu, которая экспрессирует последовательности ионных каналов М2 гриппа А или Vpu HIV-1, соответственно. Обработка 10 мкМ BIT225 снижала количество вируса, высвобождаемого в супернатант клеточной культуры, которое измеряли по вирусному белку р27. Контроли, обработанные одним носителем-растворителем(DMSO), показаны для сравнения
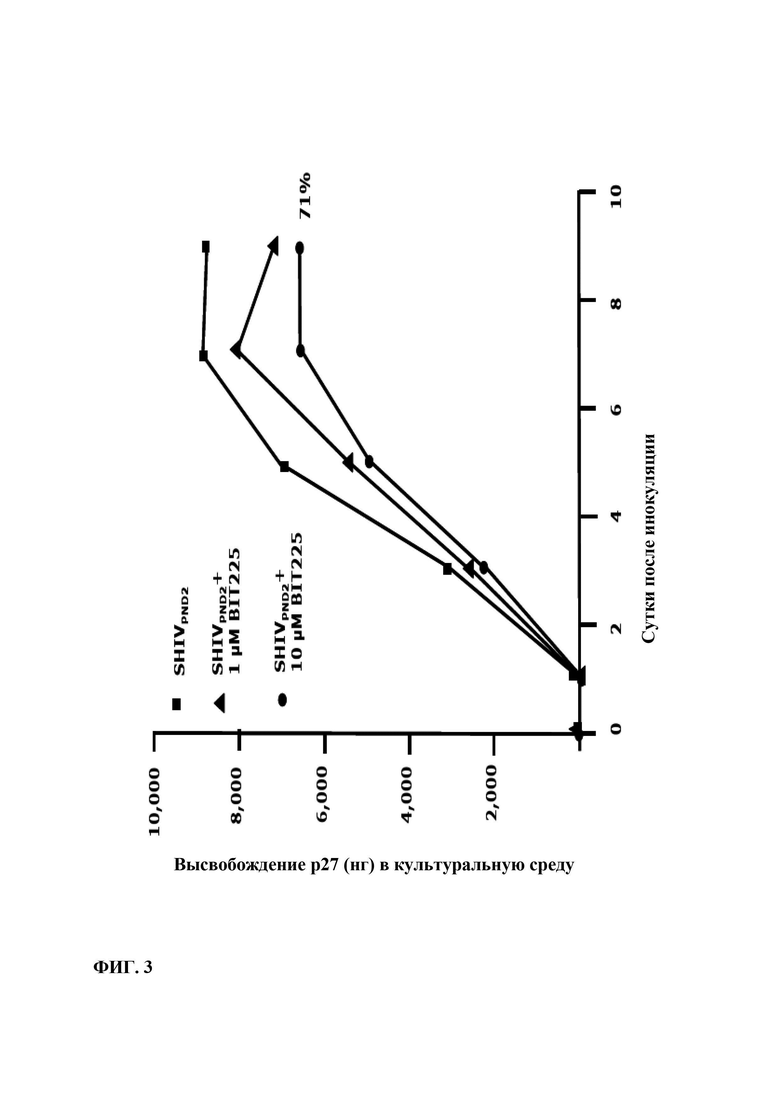
Фиг. 3: На этой Фиг. показано, что обработка посредством 10 мкМ BIT225 мутантного вируса SHIV-1PND2 с нефункциональным ионным каналом Vpu не снижала значительно репликацию вируса.
ОПРЕДЕЛЕНИЯ
В соответствии с определениями, изложенными ниже, в описании и формуле настоящего изобретения использовалась следующая терминология. Также следует понимать, что терминология, используемая в данном описании изобретения, предназначена только для цели описания конкретных воплощений изобретения и не предназначена для ограничения. Все технические и научные термины, используемые в данном описании изобретения, имеют одно и то же значение, которое обычно понятно специалисту обычной квалификации в области техники, к которой принадлежит изобретение, если не установлено иное.
В контексте настоящего изобретения слова "содержит", "содержащий" и тому подобные следует истолковывать в смысле как включающие в себя, в противоположность значению "исключающий", то есть в смысле "включающий, но без ограничения".
Термины "предпочтительный" и "предпочтительно" относятся к воплощениям изобретения, которые могут давать определенные преимущества в определенных условиях. Однако другие воплощения также могут быть предпочтительными в таких же или других условиях. Кроме того, перечисление одного или более предпочтительных воплощений не означает, что другие воплощения не являются полезными, и не предполагает исключения других воплощений из объема изобретения.
Термин "вирус гриппа" при использовании в данном описании изобретения относится к РНК вирусу семейства Orthomyxoviridae, включаюшему грипп А, грипп В и грипп С и их мутанты. Вирус гриппа А, рассматриваемый в данном описании изобретения, включает те вирусы, которые имеют два антигенных гликолизированных фермента на своей поверхности: нейраминидазу и гемагглютинин. Различные подтипы вируса гриппа А, которые можно лечить, применяя вещества и способы по заявленному изобретению, включают, но без ограничения, H1N1, H1N2, H2N2, H3N2, H3N8, H5N1, H5N2, H5N3, H5N6, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H7N9, H9N2 и H10N7. Вирус гриппа В включает, но без ограничения, линии B/Yamagata и B/Victoria.
При использовании в данном описании изобретения термин "грипп" или "инфлюэнца" относится к инфекционному заболеванию, вызванному вирусом гриппа.
Термин "симптом(ы)" при использовании в данном описании изобретения, относится к признакам или показателям того, что субъект страдает от конкретного состояния или заболевания. Например, симптомы, ассоциированные с гриппозной инфекцией, при использовании в данном описании изобретения относятся к признакам или показателям того, что субъект инфицирован вирусом гриппа. Симптомы, связанные с гриппом, рассматриваемые в данном описании изобретения, включают, но без ограничения, повышение температуры, головную боль, упадок сил/слабость, мышечную боль, воспаление суставов, раздраженные слезящиеся глаза, недомогание, тошноту и/или рвоту, дрожь, озноб, боль в груди, чихание и респираторные симптомы (то есть воспаленные слизистые мембраны дыхательных путей, чувство жжения за грудиной, выделения из носа, першение/боль в горле, сухой кашель, потеря чувства запаха).
Симптомы, ассоциированные с гриппа инфекции, могут начинаться в течение от 24 до 48 часов после инфицирования и могут начинаться внезапно. Озноб или ощущение познабливания часто являются первым признаком гриппа. Повышение температуры является обычным в течение первых нескольких суток, и температура может подниматься до 39°С. Во многих случаях субъекты чувствуют себя настолько больными, что остаются в постели надолго; субъекты часто ощущают ломоту и боли во всем теле, наиболее выраженные в спине и ногах.
При использовании в данном описании изобретения термин "осложнение(я)" относится к патологическому процессу или явлению, возникающего во время заболевания или состояния, которое не является неотъемлемой частью заболевания или состояния; которое может быть результатом заболевания/состояния или независимых случаев. Таким образом, термин осложнение(я) относится к медицинским/клиническим проблемам, которые наблюдаются у субъектов с диагностированной гриппозной инфекцией. Одно из осложнений гриппозной инфекции заключается в том, что гриппозная инфекция может сделать хронические проблемы со здоровьем еще хуже. Например, осложнения, ассоциированные с гриппозной инфекцией, включают, без ограничения, энцефалит, бронхит, трахеит, миозит, ринит, синусит, астму, бактериальные инфекции (а именно бактериальная инфекция Streptococcus aureus, бактериальная инфекция Haemophilus influenzae, бактериальная инфекция Staphylococcal pneumonia), осложнения сердечной деятельности (а именно предсердную фибрилляцию, миокардит, перикардит), синдром Рейе, неврологические осложнения (а именно спутанность сознания, судороги, психоз, неврит, синдром Гийена-Барре, кому, поперечный миелит, энцефалит, энцефаломиелит), синдром токсического шока, миозит, миоглобинурию и почечную недостаточность, круп, средний отит, вирусные инфекции (а именно вирусную пневмонию), фиброз легкого, облитерирующий бронхиолит, бронхоэктаз, обострения астмы, обострения хронической обструктивной болезни легких, абсцесс легкого, эмпиему, аспергиллез легких, миозит и миоглобинемию, сердечную недостаточность, и внутриутробная смерть плода до и после 28 недель беременности у беременных женщин, повышенную перинатальную смертность у беременных женщин и врожденные аномалии развития при родах.
При использовании в данном описании изобретения термин "эффективное количество" в контексте введения лекарственного средства субъекту относится к количеству лекарственного средства, которое имеет профилактический и/или терапевтический эффект(ы). В некоторых воплощениях "эффективное количество" в контексте введения лекарственного средства субъекту относится к количеству лекарственного средства, которое является достаточным для достижения одного, двух, трех, четырех или более следующих эффектов: (1) снижение или улучшение степени тяжести инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (2) снижение продолжительности инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (3) предупреждение развития инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (4) вызывание ослабления симптомов инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (5) предупреждение развития или начала инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (6) предупреждение рецидива инфекции, вызванной вирусом гриппа, заболевания или симптома, связанного с ним; (7) снижение или предупреждение распространения вируса гриппа от одной клетки к другой клетке, от одной ткани к другой ткани или от одного органа к другому органу; (9) предупреждение или снижение распространения вируса гриппа от одного субъекта к другому субъекту; (10) снижение функциональной недостаточности органа, связанной с инфекцией, вызванной вирусом гриппа; (11) снижение случаев госпитализации субъекта; (12) снижение продолжительности госпитализации; (13) повышение выживаемости субъекта с инфекцией, вызванной вирусом гриппа, или заболеванием, связанным с ней; (14) ликвидация инфекции, вызванной вирусом гриппа, или заболевания, связанного с ней; (15) подавление или снижение репликации вируса гриппа; (16) подавление или снижение поступления вируса гриппа в клетку(и)-хозяина; (18) подавление или снижение репликации генома вируса гриппа; (19) подавление или снижение синтеза белков вируса гриппа; (20) подавление или снижение сборки частиц вируса гриппа; (21) подавление или снижение высвобождения частиц вируса гриппа из клетки(ок)-хозяина; (22) снижение титра вируса гриппа; и/или (23) усиление или улучшение профилактического(их) или терапевтического(их) эффекта(ов) другой терапии.
В некоторых воплощениях эффективное количество не вызывает полную защиту от заболевания вирусом гриппа, но имеет результатом более низкий титр или пониженное количество вируса гриппа по сравнению с субъектом, не подвергавшемуся лечению. В некоторых воплощениях эффективное количество имеет результатом 0,5-кратное, 1-кратное, 2-кратное, 4-кратное, 6-кратное, 8-кратное, 10-кратное, 15-кратное, 20-кратное, 25-кратное, 50-кратное, 75-кратное, 100-кратное, 125-кратное, 150-кратное, 175-кратное, 200-кратное, 300-кратное, 400-кратное, 500-кратное, 750-кратное, или 1000-кратное или большее снижение титра вируса гриппа по сравнению с субъектом, не подвергавшемуся лечению. В некоторых воплощениях эффективное количество вызывает снижение соотношения титр/объем или массы образца вируса гриппа по сравнению с субъектом, не подвергавшемуся лечению, приблизительно на 1 log или более, приблизительно 2 log или более, приблизительно 3 log или более, приблизительно 4 log или более, приблизительно 5 log или более, приблизительно 6 log или более, приблизительно 7 log или более, приблизительно 8 log или более, приблизительно 9 log или более, приблизительно 10 log или более, 1-3 log, 1-5 log, 1-8 log, 1-9 log, 2-10 log, 2-5 log, 2-7 log, 2 log - 8 log, 2-9 log, 2-10 log 3-5 log, 3-7 log, 3-8 log, 3-9 log, 4-6 logs, 4-8 log, 4-9 log, 5-6 log, 5-7 log, 5-8 log, 5-9 log, 6-7 log, 6-8 log, 6-9 log, 7-8 log, 7-9 log или 8-9 log. Преимущества снижения титра, количества или совокупного груза вируса гриппа включают, но без ограничения, менее тяжелые симптомы инфекции, меньшее количество симптомов инфекции и снижение продолжительности заболевания, ассоциированного с инфекцией.
"Одновременное введение", "введение одновременно", "совместное введение", "совместно введенные" и тому подобные при использовании в данном описании изобретения включают введение BIT225, или его фармацевтически приемлемой соли, и вместе с ним одного или более дополнительных противовирусных лекарственных средств способом, подходящим для лечения гриппозной инфекции или для лечения симптомов/осложнений, связанных с гриппозной инфекцией. В соответствии с описанием изобретения, одновременное введение включает в себя предоставление субъекту BIT225 или его фармацевтически приемлемой соли и одного или более дополнительных противовирусных лекарственных средств в виде отдельных соединений, таких как, например, отдельные фармацевтические композиции, вводимые последовательно, одновременно или в различные моменты времени. Предпочтительно, если BIT225 или его фармацевтически приемлемая соль и один или более дополнительных противовирусных лекарственных средств вводят раздельно, то они не вводятся так отдаленно по времени друг от друга, чтобы BIT225, или его фармацевтически приемлемую соль, и один или более дополнительных противовирусных лекарственных средств не могли взаимодействовать. BIT225, или его фармацевтически приемлемую соль, и один или более дополнительных противовирусных лекарственных средств можно вводить в любом порядке. В одном воплощении BIT225, или его фармацевтически приемлемую соль, можно вводить раньше (например на 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 16 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель до), одновременно с или вслед за (например на 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 16 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель после) введения субъекту одного или более дополнительных противовирусных лекарственных средств. Согласно заявленному изобретению одновременное введение также включает предложение одного или более дополнительных противовирусных лекарственных средств в смеси с BIT225 или его фармацевтически приемлемой солью, такой как фармацевтическая композиция.
Дополнительная противовирусная терапия по изобретению включает вакцинации или противовирусные препараты, такие как ингибитор нейраминидазы или гемагглютинина, или препараты, которые модулируют иммунную систему или факторы клетки-хозяина. Предполагаемые противовирусные лекарственные средства для применения в соответствии с заявленным изобретением включают, но без ограничения, амантадин, римантадин, рибавирин, идоксуридин, трифлуридин, видарабин, ацикловир, ганцикловир, фоскарнет, зидовудин, диданозин, перамивир, залцитабин, ставудин, фамцикловир, осельтамивир, занамивир и валацикловир.
В сходных воплощениях субъекту с диагностированной гриппозной инфекцией можно вводить BIT225 или его фармацевтически приемлемую соль одновременно с другими лекарственными препаратами, полезными в лечении симптомов, ассоциированных с гриппозной инфекцией. Например, субъекту с диагностированной гриппозной инфекцией можно вводить средства против кашля, муколитики, отхаркивающие средства, жаропонижающие средства, анальгетики или назальные противоотечные средства одновременно с BIT225 или его фармацевтически приемлемой солью.
При использовании в данном описании изобретения термин "инфекция" означает внедрение, размножение и/или присутствие вируса в клетке или у субъекта. В одном воплощении инфекция представляет собой "активную" инфекцию, то есть инфекцию, при которой вирус реплицируется в клетке или у субъекта. Такая инфекция характеризуется распространением вируса в другие клетки, ткани и/или органы из клеток, тканей и/или органов, изначально инфицированных вирусом. Инфекция также может представлять собой латентную инфекцию, то есть инфекцию, при которой вирус является пассивным.
При использовании в данном описании изобретения выражение "лечение инфекции, вызванной вирусом гриппа" означает улучшение, смягчение или облегчение по меньшей мере одного симптома или биологического последствия инфекции, вызванной вирусом гриппа, у субъекта, и/или уменьшение или снижение титра вируса гриппа, нагрузки, репликации или пролиферации у субъекта после воздействия вируса гриппа. Выражение "лечение инфекции, вызванной вирусом гриппа" также включает сокращение периода времени, в течение которого у субъекта проявляется по меньшей мере один симптом или биологическое последствие инфекции, вызванной вирусом гриппа, после инфицирования вирусом гриппа. Способы лечения инфекции, вызванной вирусом гриппа, по настоящему изобретению включают введение фармацевтической композиции по настоящему изобретению субъекту после того, как субъекта был инфицирован вирусом гриппа и/или после того как у субъекта проявляется или диагностируется один или более симптомов или биологических последствий инфекции, вызванной вирусом гриппа.
При использовании в данном описании изобретения выражение "предупреждение инфекции, вызванной вирусом гриппа" означает предупреждение по меньшей мере одного симптома или биологического последствия инфекции, вызванной вирусом гриппа, у субъекта, и/или подавление или ослабления степени, в которой вирус гриппа способен поступать, распространяться и/или репродуцировать внутри/между клетками организма животного. Выражение "предупреждение инфекции, вызванной вирусом гриппа" также включает снижение подверженности субъекта по меньшей мере одному симптому или биологическому последствию инфекции, вызванной вирусом гриппа. Способы предупреждения инфекции, вызванной вирусом гриппа, (то есть профилактика) включают введение а фармацевтической композиции по настоящему изобретению субъекту до того, как субъект инфицируется вирусом гриппа и/или до того, как у субъекта проявляется один или более симптомов или биологических последствий инфекции, вызванной вирусом гриппа. Способы предупреждения инфекции, вызванной вирусом гриппа, могут включать введение фармацевтической композиции по настоящему изобретению субъекту в определенный период времени или сезон года (например в течение периода 1 -2 месяца незадолго до того времени, в которое обычно обнаруживается максимальная численность индивидуумов, подвергающихся инфекции, вызванной вирусом гриппа), или до поездки субъекта в климатические условия или подвергания климатическим условиям с высокой частотой инфекции, вызванной вирусом гриппа, и/или до воздействия на субъекта других субъектов, которые инфицированы вирусом гриппа.
При использовании в данном описании изобретения термины "репликация", "вирусная репликация" и "репликация вируса" в контексте вируса относятся к одной, или более или всем стадиям жизненного цикла вируса, которые вызывают размножение вируса. Стадии жизненного цикла вируса включают, но без ограничения, прикрепление вируса к поверхности клетки-хозяина, проникновение или поступление в клетку-хозяина (например посредством рецепторно-опосредованного эндоцитоза или мембранного слияния), «раздевание» (процесс, посредством которого вирусный капсид удаляется и разлагается под действием ферментов вируса или ферментов хозяина, таким образом высвобождая геномную нуклеиновую кислоту вируса), репликацию генома, синтез вирусной информационной РНК (мРНК), синтез вирусного белка и сборку рибонуклеопротеиновых комплексов вируса для репликации генома, сборку вирусных частиц, посттрансляционную модификацию вирусных белков и высвобождение из клетки-хозяина посредством лизиса или почкования и приобретение фосфолипидной оболочки, которая содержит встроенные вирусные гликопротеины. В некоторых воплощениях термины "репликация", "вирусная репликация" и "репликация вируса" относятся к репликации вирусного генома. В других воплощениях термины "репликация", "вирусная репликация" и "репликация вируса" относятся к синтезу вирусных белков.
При использовании в данном описании изобретения, термин "титр" в контексте вируса относится к количеству вирусных частиц, присутствующих в данном объеме крови или другой биологической жидкости или массе ткани или органа. Также можно использовать термины "вирусная нагрузка" и "вирусный груз".
При использовании в данном описании изобретения термин "субъект" используют для обозначения животного (например птиц, рептилий и млекопитающих). В конкретном воплощении, субъект представляет собой птицу. В другом воплощении субъект представляет собой млекопитающее, включая неприматов (например верблюда, осла, зебру, корову, свинью, лошадь, козу, овцу, кошку, собаку, крысу и мышь) и приматов (например обезьяну, шимпанзе и человека). В некоторых воплощениях субъект представляет собой нечеловекоподобное животное. В некоторых воплощениях субъект представляет собой сельскохозяйственное животное или домашнее животное. В другом воплощении субъект представляет собой человека. В другом воплощении субъект представляет собой младенца. В другом воплощении субъект представляет собой ребенка. В другом воплощении субъект представляет собой взрослого человека. В другом воплощении субъект представляет собой пожилого человека. В другом воплощении субъект представляет собой недоношенного младенца.
Пути введения включают, но без ограничения, внутривенный, внутрибрюшинный, подкожный, внутричерепной, внутрикожный, внутримышечный, внутриглазной, внутриоболочечный, внутрицеребральный, интраназальный, трансмукозальный, или перорально путем инфузии, ректально, посредством капельницы для внутривенного вливания, пластыря и импланта. Пероральные пути являются особенно предпочтительными.
Композиции, подходящие для инъекционного применения, включают стерильные водные растворы (когда водорастворимые) и стерильные порошки для экстемпорального получения стерильных инъекционных растворов. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгиколь и тому подобное), их подходящие смеси и растительные масла. Предотвращение действия микроорганизмов может осуществляться, например, посредством различных антибактериальных и противогрибковых агентов, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты, тиомерсала и тому подобного. Во многих случаях, предпочтительно включать изотонические агенты, например, сахара или хлорид натрия. Пролонгированная абсорбция инъекционных композиций может осуществляться, например, посредством использования в композициях агентов, замедляющих абсорбцию, например, моностеарата алюминия и желатина.
Стерильные инъекционные растворы получают путем включения активных соединений в необходимом количестве в подходящий растворитель с целым рядом других ингредиентов, приведенных выше, при необходимости, с последующей, например, стерилизацией фильтрованием или стерилизацией посредством других подходящих способов. Также рассматриваются дисперсии, и они могут быть получены путем включения различных стерилизованных активных ингредиентов в стерильную среду доставки, которая содержит основную дисперсионную среду и необходимые другие ингредиенты из ингредиентов, приведенных выше. В случае стерильных порошков для приготовления стерильных инъекционных растворов, предпочтительный способ получения включает вакуумную сушку и способ лиофилизации, что дает порошок активного ингредиента плюс любой дополнительный желательный ингредиент из предварительно стерилизованного фильтрованием раствора.
Когда активные ингредиенты соответствующим образом защищены, они могут быть введены перорально, например, с инертным разбавителем или с усваиваемым съедобным носителем, или они могут быть помещены в твердую или мягкую капсулу с желатиновой оболочкой, или они могут быть спрессованы в таблетки. Для перорального терапевтического введения активное соединение может быть включено с эксципиентами и применяться в форме проглатываемых таблеток, защечных таблеток, троше, капсул, эликсиров, суспензий, сиропов, облаток и тому подобного. Такие композиции и препараты должны содержать по меньшей мере 0,01% масс, более предпочтительно 0,1% масс, еще более предпочтительно 1% масс, активного соединения. Конечно, процентное содержание композиций и препаратов может варьироваться и для удобства может быть равным от примерно 1 до примерно 99%, более предпочтительно от примерно 2 до примерно 90%, еще более предпочтительно от примерно 5 до примерно 80% масс, единицы. Количество активного соединения в таких терапевтически полезных композициях является таким, чтобы была получена подходящая дозировка. Предпочтительные композиции или препараты по настоящему изобретению получают так, чтобы пероральная форма единичной дозы содержала от примерно 0,1 нг и 2000 мг активного соединения.
Таблетки, троше, пилюли, капсулы и тому подобные также могут содержать компоненты, которые перечислены выше: связующее вещество, такое как камедь, аравийская камедь, кукурузный крахмал или желатин; эксципиенты, такие как гидрофосфат кальция; разрыхлитель, такой как кукурузный крахмал, картофельный крахмал, альгиновая кислота и тому подобное; смазывающее вещество, такое как стеарат магния; и подсластитель, такой как сахароза, лактоза или сахарин, может быть добавлен или корригент, такой как мята перечная, масло гаультерии или вишневый корригент. Когда единичная дозированная форма представляет собой капсулу, она может содержать, в дополнение к веществам приведенного выше типа, жидкий носитель. Различные другие вещества могут присутствовать в качестве покрытий или для иной модификации физической формы единицы дозирования. Например, таблетки, пилюли или капсулы могут быть покрыты шеллаком, сахаром или тем и другим. Сироп или эликсир может содержать активное соединение, сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консервантов, краску и корригент, такой как вишневый или апельсиновый корригент.Любое вещество, используемое в получении любой формы единичной дозы, должно быть фармацевтически чистым и по существу нетоксичным в используемых количествах. Кроме того, активное(ые) соединение(я) можно включать в препараты и композиции с замедленным высвобождением.
Настоящее изобретение также распространяется на формы, подходящие для местного применения, такие как кремы, лосьоны и гели. В таких формах, компоненты могут быть добавлены или модифицированы для помощи в преодолении поверхностного барьера.
Способы изготовления форм единичной дозы и местных препаратов легко доступны специалисту в данной области техники из руководств, таких как Pharmaceutical Handbook, 19ое издание (Edited by Ainley Wade), The Pharmaceutical Press London; CRC Handbook of Chemistry and Physics (edited by Robert C. Weast), CRC Press Inc.; Goodman and Gilman's The Pharmacological basis of Therapeutics, 9oe издание, McGraw Hill; Remington: The Science and Practice of Pharmacy, 19oe издание (edited by Joseph P. Remington and Alfonso R. Gennaro), Mack Publishing Co.
Термин "фармацевтически приемлемая соль" при использовании в данном описании изобретения относится к любой соли BIT225, которая является фармацевтически приемлемой и не снижает значительно или подавляет активность BIT225. Подходящие примеры включают соли присоединения кислоты с органической или неорганической кислотой, такие как ацетат, тартрат, трифторацетат, лактат, малеат, фумарат, цитрат, метанат, сульфонат, сульфат, фосфат, нитрат или хлорид.
Фармацевтически приемлемые носители и/или разбавители включают любой и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и замедляющие абсорбцию агенты и тому подобные. Применение таких сред и агентов для фармацевтически активных веществ хорошо известно в данной области техники. Кроме случаев, когда какая-либо общепринятая среда или агент несовместимы с активным ингредиентом, их применение в терапевтических композициях рассматривается. Вспомогательные активные ингредиенты также могут быть включены в композиции.
Особенно эффективно готовить парентеральные композиции в форме единичной дозы для облегчения введения и единообразия дозирования. Форма единичной дозы при использовании в данном описании изобретения относится к физически обособленным единицам, подходящим в качестве однократных доз для субъектов, подлежащих лечению; где каждая единица содержит заранее установленное количество активного вещества, вычисленное для получения желательного терапевтического эффекта, в ассоциации с необходимым фармацевтическим носителем. Требования к новым формам единичных доз по изобретению диктуются ими и непосредственно зависят от (а) уникальных характеристик активного вещества и конкретного терапевтического эффекта, который должен быть получен, и (б) ограничений, свойственных области техники приготовления лекарственных средств.
Эффективные количества, рассматриваемые в настоящем изобретении, будут варьироваться в зависимости от степени тяжести состояния и здоровья и возраста реципиента. В общих чертах, эффективные количества могут варьироваться от 0,01 нг/кг массы тела до примерно 100 мг/кг массы тела. Эффективные количества включают от примерно 100 мг до примерно 600 мг, в частности, примерно 100 мг, примерно 150 мг, примерно 200 мг, примерно 250 мг, примерно 300 мг, примерно 350 мг, примерно 400 мг, примерно 450 мг, примерно 500 мг, примерно 550 мг или примерно 600 мг.
За исключением рабочих примеров, или когда показано иным образом, все числа, выражающие количества ингредиентов или условий реакции, используемые в данном описании изобретения, следует понимать как уточненные во всех случаях посредством термина "примерно".
Перечисление диапазона числовых значений, с включением концов, включает все числа, включенные в этот диапазон (например 1-5 включает 1, 1,5, 2, 2,75, 3, 3,80, 4, 5 и так далее).
ПРЕДПОЧТИТЕЛЬНОЕ ВОПЛОЩЕНИЕ ИЗОБРЕТЕНИЯ
Хотя изобретение было описано со ссылкой на конкретные воплощения, подробно описанные в данном описании изобретения, другие воплощения могут достигать таких же или подобных результатов. Вариации и модификации изобретения будут очевидны специалисту в данной области техники и изобретение предназначено для охвата всех таких модификаций и эквивалентов.
Настоящая заявка основана на неожиданном обнаружении того, что BIT225 имеет активность против разнообразных подтипов и штаммов вируса гриппа. Важно, было обнаружено, что BIT225 имеет активность в отношении подтипов и штаммов, которые являются устойчивыми к амантадину.
В настоящем изобретении предложены способы и композиции (такие как фармацевтические композиции) для лечения или предупреждения гриппа.
В настоящем изобретении предложены вещества и способы предупреждения и/или лечения вирусных инфекций. Более точно, в заявленном изобретении предложены вещества и способы предупреждения гриппозной инфекции; лечение/уменьшение интенсивности симптомов, ассоциированных с гриппозными инфекциями; и/или предупреждении/замедление начала осложнений, ассоциированных с гриппозными инфекциями.
В настоящем изобретении предложен способ лечения или предупреждения инфекции, вызванной вирусом гриппа, у субъекта, где способ включает введение субъекту эффективного количества BIT225 или его фармацевтически приемлемой соли.
В настоящем изобретении также предлагается способ подавления репликации вируса гриппа у субъекта, включающий введение субъекту эффективного количества BIT225 или его фармацевтически приемлемой соли.
В настоящем изобретении дополнительно предложен способ снижения степени тяжести, интенсивности или продолжительности осложнений или симптомов, ассоциированных с инфекцией, вызванной вирусом гриппа, у субъекта, включающий введение субъекту эффективного количества BIT225 или его фармацевтически приемлемой соли.
В изобретении дополнительно предложен способ понижения титра вируса гриппа у субъекта, включающий введение субъекту эффективного количества BIT225 или его фармацевтически приемлемой соли.
Настоящее изобретение дополнительно описано посредством следующих неограничивающих примеров.
ПРИМЕРЫ
Получение BIT225
Смесь 5-бром-2-нафтойной кислоты (2,12 г, 8,44 ммоль), 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразола (1,84 г, 8,86 ммоль) и тетракис(трифенилфосфин)палладия(0) (502 мг, 0,435 ммоль) в 250 мл круглодонной колбе вакуумировали и продували азотом (три цикла). Ацетонитрил (40 мл) и 2М водный карбонат натрия (10 мл) добавляли к смеси с помощью шприца и смесь нагревали с обратным холодильником в атмосфере азота в течение 22 часов. Реакционную смесь оставляли охлаждаться перед добавлением 1М водной соляной кислоты (30 мл) и затем экстрагировали ее этилацетатом (3×50 мл). Объединенные органические слои сушили (MgSO4), фильтровали и концентрировали в вакууме с получением неочищенного продукта (2,98 г после воздушной сушки). Это неочищенное вещество растворяли в горячем этаноле (150 мл) и фильтровали, пока горячий, для удаления желтой примеси (120 мг). Фильтрат концентрировали в вакууме и остаток перекристаллизовывали из дихлорметана (30 мл) с получением 5-(1-метил-1H-пиразол-4-ил)-2-нафтойной кислоты в виде белого твердого вещества (724 мг, 34%). Дополнительную порцию 5-(1-метил-1H-пиразол-4-ил)-2-нафтойной кислоты (527 мг, 25%) получали из концентрированных маточных растворов путем перекристаллизации из дихлорметана (20 мл).
Оксалилхлорид (1,1 мл, 13 ммоль) добавляли к раствору 5-(1-метил-1H-пиразол-4-ил)-2-нафтойной кислоты (1,19 г, 4,71 ммоль) в безводном дихлорметане (200 мл (который добавляли порциями во время реакции для эффективного растворения)), содержащем диметилформамид (2 капли), в атмосфере азота и смесь перемешивали при комнатной температуре в течение 4,25 часов. Затем реакционную смесь нагревали в течение 1 часа при 40°С перед концентрацией при пониженном давлении. Полученный неочищенный хлорангидрид суспендировали в безводном тетрагидрофуране (50 мл) и эту смесь добавляли по каплям к раствору гуанидингидрохлорида (2,09 г, 21,9 ммоль) в 2М водном гидроксиде натрия (15 мл, 30 ммоль) и затем реакционную смесь перемешивали в течение 30 минут. Органическую фазу отделяли и водную фазу экстрагировали хлороформом (3×30 мл) с последующим экстрагированием с этилацетатом (3×30 мл). Объединенные органические экстракты промывали последовательно 1М водным гидроксидом натрия (60 мл) и водой (40 мл), затем сушили (Na2SO4) и концентрировали в вакууме с получением стекловидного твердого вещества (1,45 г после сушки в глубоком вакууме). Указанное твердое вещество растворяли в дихлорметане, который затем оставляли медленно испаряться с получением BIT225 в виде желтого твердого вещества (1,15 г, 83%).
Штаммы вируса
Определяли активность BIT225 в отношении следующих штаммов вируса:
• Грипп A/New Caledonia/20/99 (H1N1). Новейший клинический изолят, используемый в самой последней вакцине (CDC);
• Грипп A/Panama/2007/99 (H3N2). Новейший клинический изолят, используемый в самой последней вакцине (CDC);
• Грипп B/Hong Kong/330/02. Новейший клинический изолят, используемый в самой последней вакцине (CDC);
• Грипп A/NWS/33 (H1N1). Широко известный лабораторный штамм (KW. Cochran, Univ. Michigan).
Все вирусные штаммы тестировали в присутствии трипсина, хотя в некоторых исследованиях вирус A/NWS/33 использовали без трипсина.
Анализ противовирусной активности:
Быстрый скрининговый анализ
В анализе стандартного цитопатического эффекта (СРЕ) используют 18-часовой монослой (80-100% сливания) подходящих клеток, среду удаляют и добавляют каждую из концентраций тестируемого соединения или плацебо, с последующим добавлением в течение 15 минут вируса или разведения вируса. Две лунки используют для каждой концентрации соединения как для противовирусного исследования, так и тестирования цитотоксичности. Планшет герметично закрывают и инкубируют в течение стандартного периода времени, необходимого для индуцирования почти максимального СРЕ вируса. Затем планшет окрашивают нейтральным красным посредством способа, описанного ниже, и процент поглощения, показывающий жизнеспособные клетки, считывают на автоматическом микропланшетном ридере при двухлучевых длинах волн 405 и 540 нм с разницей, взятой для устранения фона. Определяют приблизительную концентрацию подавления вируса, 50% предельного значения (ЕС50) и концентрацию подавления клеток, 50% предельного значения (СС50), из которых вычисляют общий индекс селективности: SI=(CC50)/(EC50). Подтверждающее тестирование SI от 3 или более возбудителей.
Подавление цитопатического действия вируса (СРЕ)
Этот анализ, определение в 96-луночных плоскодонных микропланшетах, используют для первоначального оценивания противовирусного действия всех новых тестируемых соединений. В этом тесте подавления СРЕ четыре разведения log10 каждого тестируемого соединения (например 1000, 100, 10, 1 мкг/мл) добавляют в 3 лунки, содержащие клеточный монослой и в течение 5 минут добавляют вирус, планшет герметично закрывают, инкубируют при 37°С. СРЕ считывают при помощи микроскопа, когда необработанные инфицированные контроли проявляют от 3 до 4+ СРЕ (приблизительно от 72 до 120 часов). Известное лекарственное средство в качестве положительного контроля оценивают параллельно с тестируемыми лекарственными средствами в каждом прогоне анализа. Последующее тестирование с соединениями, обнаруженными активными в первоначальных скрининг-тестах, прогоняют таким же образом, за исключением того, что 8 половинных разведений log10 каждого соединения используют в 4 лунках, содержащих клеточный монослой на разведение.
Данные выражают в виде 50% эффективных концентраций (ЕС50).
Повышение поглощения нейтрального красного красителя
Этот анализ проводят для подтверждения подавления СРЕ, наблюдаемого в первоначальном тесте, и используют те же самые 96-луночные микропланшеты после оценивания СРЕ. Нейтральный красный добавляют в среду; клетки не повреждаются вирусом, впитавшим значительно большее количество красителя, что считывается на компьютеризированном автоматическом микропланшетном ридере. Используют способ, который описан у McManus (McManus, Арр Environ Microbiol, 1976. 31(1): 35-38). ЕС50 определяют по поглощению красителя.
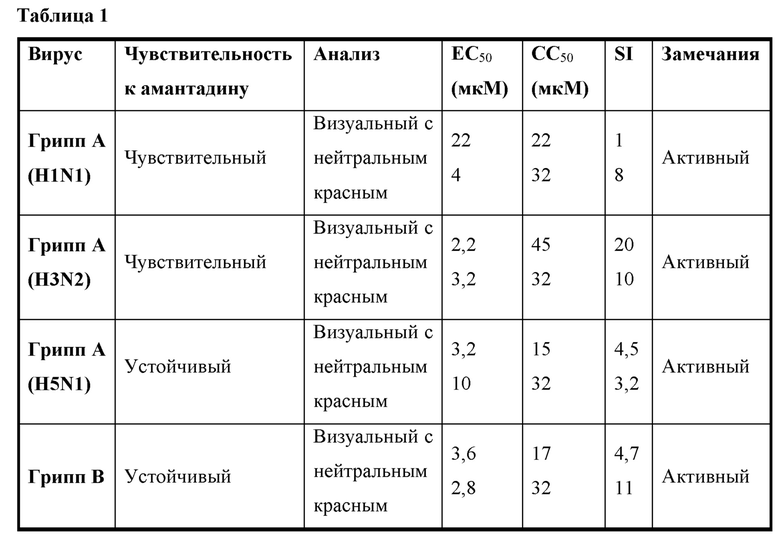
BIT225 имеет противовирусную активность как против чувствительных, так и против устойчивых к амантадину вирусов. Эта активность широкого спектра и, в частности, эта активность против гриппа В делает его важным противовирусным соединением. Данные противовирусной активности в отношении гриппа А и В для BIT225 в клетках Мадин-Дарби почек собак (MDCK) обобщены в Таблице 1.
Имеющиеся в продаже противовирусные агенты обычно не имеют противовирусной активности против гриппа В.
Анализ бляшкообразования в зависимости от дозы
Активность BIT225 против вируса гриппа А подтверждали посредством in vitro анализа дозозависимого сокращения бляшек в клетках Мадин-Дарби почек собак (MDCK). В этих экспериментах использовали лабораторный штамм PR8 и устойчивый к амантадину вариант вируса создавали посредством мутирования гена М2 для кодирования треонина в позиции 30 вместо аланина в последовательности. Мутантный вирус АЗОТ известен как PR8 4С.
Анализ бляшек выполняли, как описано в Haydenet al. (Hayden et al., Antimicrob Agents Chemother, 1980. 17(5): 865-870), используя 1×103 БОЕ (бляшкообразующих единиц) рекомбинантных вирусов PR8 в 150 мкл сред для инфицирования монослоев клеток MDCK.
Такое разведение вируса дает приблизительно 100 бляшек в необработанных контрольных лунках. BIT225 растворяли в DMSO и добавляли к средам в указанных конечных концентрациях. Контроли токсичности показывали отсутствие токсических эффектов BIT225 в клетках MDCK вплоть до 100 мкМ.
Фиг. 1 иллюстрирует, что BIT225 способен снижать вирусную репликацию как чувствительных, так и устойчивых к амантадину вирусов PR8. ЕС50 для BIT225 равнялась приблизительно 10 мкМ по сравнению как с вирусом дикого типа, так и мутантным вирусом А30Т, с соответствующими значениями ЕС90 12 мкМ и 18 мкМ. Это резко контрастирует с большим сдвигом чувствительности к лекарственному средству амантадину, вызванным мутацией А30Т в М2.
Исследования химерного вируса
Эксперименты проводили для изучения действия BIT225 на репликацию в Т-клеточной линии (С8166) химерных вирусов SHIV-1M2 и SHIV-1SCVpu, которые экспрессируют последовательности ионных каналов М2 гриппа А или Vpu HIV-1, соответственно. Обработка 10 мкМ BIT225 снижала количество вируса, высвобождаемого в супернатант клеточной культуры, которое измеряли по вирусному белку р27 (Фиг. 2). Контроли, обработанные одним носителем-растворителем (DMSO (диметилсульфоксид)) показаны для сравнения.
Однако обработка 10 мкМ BIT225 мутантного вируса SHIV-1PND2 с нефункциональным ионным каналом Vpu не снижает значительно репликацию вируса (Фиг. 3).
В целом, эти результаты показывают, что подавление ионных каналов Vpu или М2 представляет собой возможный механизм действия BIT225 в отношении гриппа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИИ ВИЧ-1 | 2020 |
|
RU2827716C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ ПОЛИМЕРАЗЫ | 2011 |
|
RU2599013C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ МОДУЛЯТОРЫ СИНТЕЗА ЛИПИДОВ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ РАКА И ВИРУСНЫХ ИНФЕКЦИЙ | 2015 |
|
RU2766087C2 |
| СТАБИЛИЗАТОРЫ ТУЧНЫХ КЛЕТОК ЛЕЧЕНИЯ ГИПЕРЦИТОКИНЕМИИ И ВИРУСНОЙ ИНФЕКЦИИ | 2017 |
|
RU2760682C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ ПОЛИМЕРАЗЫ | 2011 |
|
RU2718690C2 |
| 6,13,13-ТРИМЕТИЛ-6,8,9,12-ТЕТРАГИДРО-6,9-МЕТАНОАЗЕПИНО[2,1-b]ХИНАЗОЛИН-10(7Н)-ОН В КАЧЕСТВЕ ИНГИБИТОРА ВИРУСОВ ГРИППА А | 2017 |
|
RU2664331C1 |
| ПРОТИВОВИРУСНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО В ВИДЕ КАПСУЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2633085C2 |
| МАТЕРИАЛЫ И СПОСОБЫ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ С ПОМОЩЬЮ СОЕДИНЕНИЯ ЦИСТЕАМИНА | 2006 |
|
RU2431476C2 |
| НОВЫЕ СОСТАВЫ 2-(ИМИДАЗОЛ-4-ИЛ)-ЭТАНАМИДА ПЕНТАНДИОВОЙ-1,5 КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2782532C2 |
| НОВЫЕ СОСТАВЫ 2-(ИМИДАЗОЛ-4-ИЛ)-ЭТАНАМИДА ПЕНТАНДИОВОЙ-1,5 КИСЛОТЫ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2791902C2 |
Группа изобретений относится к области фармацевтической химии и представляет собой способ лечения инфекции, вызванной вирусом гриппа А или В, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли. Также изобретение относится к применению N-карбамимидоил-5-(1-метил-1Н-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения инфекции, вызванной вирусом гриппа A или B. Технический результат – создание противовирусного средства на основе N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамида (BIT225) для лечения инфекции, вызванной вирусом гриппа А или В, устойчивого к адамантадину. 2 н. и 6 з.п. ф-лы, 3 ил., 1 табл., 1 пр.
1. Способ лечения инфекции, вызванной вирусом гриппа A, или инфекции, вызванной вирусом гриппа B, у субъекта, включающий введение субъекту эффективного количества N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли.
2. Способ по п. 1, где репликация вируса гриппа подавляется.
3. Способ по п. 1 или 2, где титр вируса гриппа понижается.
4. Способ по любому из пп. 1-3, где вирус гриппа A выбран из подтипов H1N1, H1N2, H2N2, H3N2, H3N8, H5N1, H5N2, H5N3, H5N6, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H7N9, H9N2 и H10N7.
5. Способ по п. 4, где вирус гриппа A выбран из подтипов H1N1, H3N2 и H5N1.
6. Применение N-карбамимидоил-5-(1-метил-1H-пиразол-4-ил)-2-нафтамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения инфекции, вызванной вирусом гриппа A, или инфекции, вызванной вирусом гриппа B.
7. Применение по п. 6, где репликация вируса гриппа подавляется.
8. Применение по п. 6 или 7, где титр вируса гриппа понижается.
| Jalily P.H | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Molecular Pharmacology, 2016, 90 (2), pp.80-95 | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| Прибор для отбора из нефтехранилищ нефти с приспособлением для одновременного определения высоты налива и отстоя воды | 1929 |
|
SU22336A1 |
Авторы
Даты
2022-03-30—Публикация
2018-02-07—Подача