Заявление о приоритете
[0001] Настоящая заявка испрашивает приоритет предварительной заявки США, серийный номер 62/385021, поданной 8 сентября 2016 г., полное содержание которой включено в настоящий документ посредством ссылки.
Область техники, к которой относится изобретение
[0002] Настоящее изобретение относится к способам лечения гиперцитокинемии и вирусных инфекций и других нарушений, связанных с гиперцитокинемией, с использованием соединения, стабилизирующего тучные клетки, необязательно в комбинации с противовирусным средством или другим терапевтическим средством. Изобретение также относится к композициям и дозированным формам, содержащим средства, стабилизирующие тучные клетки, необязательно с противовирусным средством или другим терапевтическим средством.
Предпосылки создания изобретения
[0003] Тучные клетки представляют собой уникальные гемопоэтические клетки, которые находятся только в тканях, а не в кровотоке. Они являются стражами, постоянно находящимися в поисках инвазивных организмов, токсичных молекул и повреждения ткани. Когда тучные клетки сталкиваются с такими патогенами или повреждениями, они высвобождают поток медиаторов; эти медиаторы представляют собой смесь низкомолекулярных эффекторов (таких как гистамин), протеаз, липидных сигнальных молекул (простагландинов) и цитокинов. Процесс высвобождения этих медиаторов обычно называется «дегрануляцией».
[0004] Высвобождение медиаторов посредством дегрануляции приводит к привлечению широкого спектра иммунных клеток к участку высвобождения медиатора для борьбы с нарушителем. Этот процесс также вызывает локализованное воспаление для ограничения движения любой инфекции или токсина. Контролируемый воспалительный ответ на чужеродные вещества позволяет организму предотвращать распространение токсинов в соседние ткани, ограничивая повреждение в одной области, и является желательным. После того, как токсин был нейтрализован, нормальным ответом для организма является начало активного разрешения воспалительной реакции (ROI). Это приводит к выходу рекрутированных иммунных клеток из поврежденной ткани, ремоделированию ткани, уменьшению отека и, наконец, полному заживлению.
[0005] В некоторых случаях это нормальное развитие ответа пропорционального воспалительного ответа не приводит к устранению нарушения. Это может привести либо к хроническому состоянию воспаления, либо к чрезмерно сильной реакции медиаторов, которая непропорциональна явлению инвазии. Последняя ситуация была названа «цитокиновым штормом» или гиперцитокинемией. Чрезвычайно высокий уровень воспалительных цитокинов и медиаторов, который не устранен, вреден для хозяина и может привести к смерти, особенно если быстропротекающая реакция происходит в легких. Наиболее повреждающие аспекты и симптомы многих заболеваний являются прямым результатом гиперцитокинемии, в отличие от нарушений от исходного заболевания.
[0006] Современные способы лечения состояний, которые вызывают гиперцитокинемию, обычно не делают ничего для улучшения непрерывного продуцирования медиаторов воспаления, которые сохраняют это состояние. Эти состояния обычно лечат с помощью вмешательств, нацеленных на патоген, вызывающий ответ, или с помощью антагонистов к одному конкретному медиатору воспаления. В то время как очень важно для патогенных микроорганизмов быть нейтрализованными, при большинстве заболеваний, которые вызывают гиперцитокинемию, проблема заключается не в патогене, а в чрезмерно сильной реакции организма на патоген, вызываемой дюжиной или более медиаторами воспаления.
[0007] Тем не менее, подавление иммунной системы само по себе недостаточно для лечения этих состояний. На самом деле, есть доказательства того, что в некоторых случаях лечение пациентов кортикостероидами для уменьшения воспаления повышает смертность. Кортикостероиды являются очень мощными супрессорами врожденной и адаптивной иммунной системы. «Отключение» всех аспектов иммунного ответа во время инфекции не допускает клиренс патогена. Таким образом, необходимо найти баланс между чрезмерно сильным иммунным ответом и слишком малым ответом.
[0008] Вирусы гриппа представляют собой родственные серии вирусов в семействе Orthomyxoviridae. Были описаны три типа (типы A, B или C), и все они являются отрицательно полярными одноцепочечными сегментированными РНК-вирусами. Типы A и B являются значимыми с медицинской точки зрения для здоровья человека, причем тип A является причиной более тяжелого заболевания. Вирусы типа А обычно встречаются у диких птиц и лишь в редких случаях вызывают заболевания у их хозяина. Подтипы гриппа А обычно вызывают волны заболеваний гриппом человека по всему миру с далеко идущими последствиями для здоровья и экономики. В США ежегодно около 30000 человек умирают от гриппа или осложнений, вызванных гриппозной инфекцией. Оценки экономического воздействия в США превышают прямые затраты на медицинское обслуживание и потерю работы более 80 миллиардов долларов в год. Грипп обычно заражает людей через дыхательные пути, хотя есть также сообщения о том, что инфекция может попасть через глаза.
[0009] Грипп индуцирует быстрый цитокиновый ответ у людей, обычно обнаруживаемый в течение нескольких часов после заражения. Важно отметить, что тяжесть каждого случая гриппа напрямую связана с уровнями индуцированных цитокинов. Это хорошо известно специалистам в данной области и было задокументировано по многим различным штаммам гриппа. Что особенно поражает в заболевании, вызванном гриппом, так это то, что тяжесть заболевания зависит от штамма вируса и индивидуума. Например, большинство ежегодных случаев гриппа вызваны штаммом H1N1. В то время как многие люди инфицированы, тяжесть заболевания колеблется от отсутствия симптомов до смерти. В нормальный сезон сезонного гриппа H1N1 в США около 20% населения болеют (60 миллионов человек), 200000 из них госпитализируют и около 30000 человек умирают каждый год (около 0,05% смертности). При вспышках с участием высокопатогенных штаммов вируса (например, H5N1) от 30% до 60% случаев заканчиваются смертельным исходом. Хотя это указывает на то, что вирус является основной причиной тяжести заболевания, причина, по которой у людей проявляется более тяжелое или смертельное заболевание, одинакова для любого штамма: тяжелобольные люди имеют чрезвычайно высокие уровни цитокинов, независимо от штамма вируса. Таким образом, проблема на самом деле не в самом вирусе, а в реакции организма на вирус. При более вирулентных штаммах большая часть людей будет испытывать гиперцитокинемию. Тем не менее, эта гиперцитокинемия ничем не отличается от той, которая наблюдается у небольшой части людей, испытывающих те же симптомы от менее вирулентного штамма.
[0010] Было показано, что стабилизаторы тучных клеток, такие как кетотифен и кромолин (хромогликат натрия), ингибируют дегрануляцию тучных клеток и вызванное этим высвобождение медиаторов, таких как гистамин, фактор некроза опухоли (TNF-α), простагландины, лейкотриены, интерлейкины и другие цитокины. Эти эффекты не могут быть ограничены тучными клетками и могут иметь более широкий эффект снижения высвобождения воспалительных цитокинов во многих типах клеток. Эти соединения, однако, не влияют на адаптивную иммунную систему и позволяют выводить из организма антигены на основе антител, по существу, как обычно. Оба эти соединения используются для лечения хронических заболеваний. Кромолин был обнаружен и использовался в качестве ингаляционного лечения астмы. Кетотифен был открыт как H1-антигистаминное средство и широко используется в составах глазных капель для лечения воспаления глаз. Он также был разработан в качестве перорального лечения астмы, хотя это, кажется, занимает несколько недель, чтобы оказать существенное влияние на хроническую астму. Было показано, что кетотифен и в меньшей степени кромолин увеличивают выживаемость мышей в модели инфекция гриппа (Hu et al., Mast Cell-Induced Lung Injury in Mice Infected with H5N1 Influenza Virus, J. Virol. 86(6):3347 (2012); Han et al., The therapeutic effects of sodium cromoglycate against influenza A virus H5N1 in mice, Influenza and Other Respiratory Viruses 10(1):57 (2016)). В случае кетотифена его комбинировали с осельтамивиром, и влияние на выживаемость увеличивалось, когда соединения объединяли.
[0011] Настоящее изобретение преодолевает недостатки в данной области, предоставляя композиции и способы лечения гиперцитокинемии и связанных с ней нарушений.
Сущность изобретения
[0012] Настоящее изобретение относится к разработке способов лечения для подавления гиперцитокинемии с целью успешного вмешательства в случаях цитокинового шторма. Настоящее изобретение обеспечивает более эффективный способ, способствующий уравновешиванию ингибирования слишком сильного иммунного ответа организма и обеспечения слишком малого ответа для обеспечения лечения, которое позволяет решать обе проблемы: исходное состояние, на которое реагирует организм (то есть инфекция) и возникающая в результате гиперцитокинемия. Это может быть достигнуто с помощью режима терапии, который подавляет врожденную иммунную систему и позволяет адаптивной иммунной системе устранять причинный патогенный микроорганизм. Альтернативно, лечение, которое подавляет врожденную иммунную систему, может быть объединено с лечением, чтобы помочь устранить проникшие частицы (например, противовирусное соединение).
[0013] Соответственно, в качестве одного аспекта изобретение предоставляет способ лечения, облегчения или профилактики гиперцитокинемии у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики гиперцитокинемии. В некоторых вариантах осуществления способ дополнительно включает введение субъекту дополнительного терапевтического средства, например, противовирусного средства.
[0014] Изобретение, кроме того, относится к способу лечения, облегчения или профилактики вирусной инфекции, связанной с гиперцитокинемией, у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики вирусной инфекции. В некоторых вариантах осуществления способ дополнительно включает введение субъекту дополнительного терапевтического средства, например, противовирусного средства.
[0015] Изобретение, кроме того, относится к способу лечения, облегчения или профилактики нарушения, связанного с гиперцитокинемией, у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики нарушения. В некоторых вариантах осуществления способ дополнительно включает введение субъекту дополнительного терапевтического средства, например, противовирусного средства.
[0016] Изобретение, кроме того, относится к способу лечения, облегчения или профилактики лихорадки у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики лихорадки. В некоторых вариантах осуществления способ дополнительно включает введение субъекту дополнительного терапевтического средства, например, жаропонижающего средства.
[0017] Изобретение также относится к фармацевтической композиции, включающей норкетотифен и фармацевтически приемлемый носитель и, необязательно, дополнительное терапевтическое средство.
[0018] Изобретение дополнительно относится к фармацевтической композиции, включающей кетотифен, дополнительное терапевтическое средство и фармацевтически приемлемый носитель.
[0019] Изобретение, кроме того, относится к лекарственным формам, включающим фармацевтические композиции по изобретению.
[0020] Настоящее изобретение более подробно поясняется на чертежах в настоящем документе и в описании, приведенном ниже.
Краткое описание чертежей
[0021] На фиг. 1 показаны расчетные уровни кетотифена в сыворотке у субъекта при нескольких различных режимах дозирования.
Подробное описание изобретения
[0022] Настоящее изобретение может быть воплощено в различных формах и не должно рассматриваться как ограниченное вариантами осуществления, изложенными в настоящем документе. Скорее, эти варианты осуществления предоставлены для того, чтобы настоящее раскрытие было полным и завершенным и полностью передавало объем изобретения специалистам в данной области техники. Например, признаки, проиллюстрированные в отношении одного варианта осуществления, могут быть включены в другие варианты осуществления, а признаки, проиллюстрированные в отношении конкретного варианта осуществления, могут быть удалены из этого варианта осуществления. Кроме того, многочисленные вариации и дополнения к вариантам осуществления, предложенным в настоящем документе, будут очевидны для специалистов в данной области техники в свете настоящего раскрытия, которые не отходят от настоящего изобретения.
[0023] Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое обычно понимают специалисты в области техники, к которой относится настоящее изобретение. Терминология, используемая в описании изобретения в настоящем документе, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения изобретения.
[0024] Если контекст не указывает на иное, специально подразумевается, что различные признаки изобретения, описанные в настоящем документе, могут использоваться в любой комбинации.
[0025] Кроме того, настоящее изобретение также предусматривает, что в некоторых вариантах осуществления изобретения любой признак или комбинация признаков, изложенных в настоящем документе, могут быть исключены или опущены.
[0026] Чтобы проиллюстрировать, если в описании указано, что комплекс включает компоненты A, B и C, специально предусмотрено, что любой из A, B или C или их комбинации могут быть опущены и отклонены по отдельности или в любой комбинации.
[0027] Все публикации, заявки на патенты, патенты и другие ссылки, упомянутые в настоящем документе, включены в настоящий документ посредством ссылки в полном объеме.
[0028] Как используется в настоящем документе, формы единственного числа могут означать один или более чем один. Например, клетка может означать одну клетку или множество клеток.
[0029] Так же, как используется в настоящем документе, «и/или» относится и охватывает любые и все возможные комбинации одного или нескольких связанных перечисленных элементов, а также отсутствие комбинаций при интерпретации в альтернативном варианте («или»).
[0030] Кроме того, термин «примерно», как используется в настоящем документе, когда он относится к измеряемой величине, такому как количество соединения или средства по настоящему изобретению, доза, время, температура и тому подобное, предназначен для охвата изменений, составляющих±20%,±10%,±5%,±1%,±0,5%, или даже±0,1% от указанного количества.
[0031] Термин «состоит по существу из» (и грамматических вариантов) применительно к композициям по настоящему изобретению означает, что композиция может включать дополнительные компоненты, если дополнительные компоненты не изменяют композицию существенным образом. Термин «существенно измененная» применительно к композиции относится к увеличению или снижению терапевтической эффективности композиции, по меньшей мере, приблизительно на 20% или более по сравнению с эффективностью композиции, состоящей из перечисленных компонентов.
[0032] Под терминами «лечить» или «лечение» (и их грамматическими вариациями) подразумевается, что тяжесть состояния субъекта снижается, по меньшей мере, частично улучшается или стабилизируется и/или что достигается некоторое облегчение, смягчение, уменьшение или стабилизация по меньшей мере одного клинического симптома и/или имеется задержка в прогрессировании заболевания или нарушения.
[0033] Термины «предотвращать», «предотвращение» и «профилактика» (и их грамматические вариации) относятся к предотвращению и/или задержке начала заболевания, нарушения и/или клинического(их) симптома(ов) у субъекта и/или уменьшению тяжести начала заболевания, нарушения и/или клинического симптома(ов) относительно того, что было бы в отсутствие способов по настоящему изобретению. Предотвращение может быть полным, например, полное отсутствие заболевания, нарушения и/или клинического симптома(ов). Предотвращение также может быть частичным, так что возникновение заболевания, нарушения и/или клинического симптома(ов) у субъекта и/или тяжесть начала и/или периода времени симптомов меньше, чем было бы в отсутствие настоящего изобретения.
[0034] «Эффективное для лечения» или «терапевтически эффективное» количество, как используется в настоящем документе, представляет собой количество, которое является достаточным для обеспечения некоторого улучшения или пользы для субъекта. В качестве альтернативы указано, что «эффективное для лечения» количество представляет собой количество, обеспечивающее некоторое облегчение, смягчение, уменьшение или стабилизацию по меньшей мере одного клинического симптома у субъекта. Специалистам в данной области должно быть понятно, что терапевтические эффекты не должны быть полными или излечивающими, если обеспечивается некоторая польза субъекту.
[0035] Используемое в настоящем документе «эффективное для профилактики» количество представляет собой количество, которое является достаточным для профилактики и/или задержки начала заболевания, нарушения и/или клинических симптомов у субъекта и/или для уменьшения и/или задержки тяжести начала заболевания, нарушения и/или клинических симптомов у субъекта относительно того, что было бы в отсутствие способов по настоящему изобретению. Специалистам в данной области должно быть понятно, что степень профилактики не обязательно должна быть полной, если обеспечивается некоторая польза субъекту.
[0036] Как используется в настоящем документе, термин «гиперцитокинемия», также известный как «цитокиновый шторм» или «цитокиновый каскад», относится к иммунной реакции, состоящей из положительной обратной связи между цитокинами и клетками, секретирующими медиатор, что приводит к высоко повышенным уровням различных цитокинов. Во время гиперцитокинемии уровни одного или нескольких цитокинов в сыворотке и/или органах могут быть повышены, например, по меньшей мере, в 5 раз выше уровня, наблюдаемого у здорового субъекта или у здоровой популяции, например, по меньшей мере, в 10 раз или в 100 раз выше. Симптомы гиперцитокинемии могут включать высокую температуру, отек и покраснение, сильную усталость и тошноту.
[0037] «Нарушение, связанное с гиперцитокинемией» относится к любому нарушению, при котором гиперцитокинемия является одним из его симптомов или побочных эффектов во время по меньшей мере одной стадии нарушения.
[0038] «Вирусная инфекция, связанная с гиперцитокинемией» относится к любой вирусной инфекции, при которой гиперцитокинемия является одним из ее симптомов или побочных эффектов во время по меньшей мере одной стадии инфекции.
[0039] «Грипп», как используется в настоящем документе, определяется как заболевание, связанное с положительным диагностическим тестом на грипп.
[0040] «Гриппоподобное заболевание», как используется в настоящем документе, определяется как симптомы лихорадки (температура 37,8°C или выше) и кашля и/или ангины без известной причины.
[0041] «Синдром системной воспалительной реакции (SIRS)» или «сепсис» определяется наличием двух или более следующих клинических проявлений: (а) температура тела выше 38°С или 36°С; (b) частота сердечных сокращений более 90 в минуту; (c) частота дыхания более 20 в минуту или PACO2 ниже 32 мм рт.ст.; (d) количество лейкоцитов более 12000 клеток/л или менее 4000 клеток/л или более 10% незрелых (палочкоядерные нейтрофилы) форм.
[0042] «Фармацевтически приемлемый», как используется в настоящем документе, означает вещество, которое не является биологически или иным образом нежелательным, то есть вещество может быть введено индивидууму вместе с композициями по настоящему изобретению, не вызывая существенных вредных биологических эффектов или взаимодействия вредным образом с любым из других компонентов композиции, в которой оно содержится. Естественно выбирать это вещество таким образом, чтобы минимизировать любое разложение активного ингредиента и минимизировать любые неблагоприятные побочные эффекты у субъекта, которые хорошо известны специалистам в данной области (см., например, Remington's Pharmaceutical Science; 21st ed. 2005). Типичные фармацевтически приемлемые носители для композиций по настоящему изобретению включают, но не ограничиваются ими, стерильную апирогенную воду и стерильный апирогенный физиологический раствор.
[0043] «Одновременно» означает достаточно близкое по времени для получения комбинированного эффекта (то есть одновременно может происходить в то же самое время, или это могут быть два или несколько событий, протекающих за короткий период времени до или после друг друга). В некоторых вариантах осуществления введение двух или нескольких соединений «одновременно» означает, что два соединения вводят достаточно близко во времени, чтобы присутствие одного изменяло биологические эффекты от другого. Два соединения могут быть введены в одинаковых или разных лекарственных формах или последовательно. Одновременное введение может быть осуществлено путем смешивания соединений перед введением или путем введения соединений в двух разных лекарственных формах, например, в один и тот же момент времени, но в разных анатомических точках или с использованием разных путей введения.
[0044] Настоящее изобретение предназначено для лечения физиологического повреждения (вызванного любыми путями) и индуцированной гиперцитокинемии. Это достигается путем лечения острого состояния соединением, стабилизирующим тучные клетки, которое уменьшает высвобождение медиаторов из тучных клеток. Эти соединения также могут быть эффективными в снижении высвобождения медиаторов из клеток других типов. Конечным эффектом является снижение чрезмерно повышенной реакции врожденной иммунной системы, что позволяет адаптивной иммунной системе решить начальную проблему, приводящую к гиперцитокинемии. Эти соединения также могут быть объединены с соединением, специфическим для заболевания. Специфическое для заболевания соединение нацелено на первоначальное повреждение, но повреждение все еще может индуцировать или продолжать индуцировать сильный цитокиновый ответ. Соединение, стабилизирующее тучные клетки, уменьшает высвобождение медиаторов, уменьшая гиперцитокинемию. Уменьшение острой воспалительной реакции предотвращает дополнительное повреждение, вызванное неконтролируемым воспалением. Комбинированный подход к лечению гораздо более эффективен, чем единственное лечение, поскольку он направлен как на вредное повреждение (например, инфекцию), так и на еще более вредный цитокиновый ответ.
[0045] Хотя некоторые соединения, стабилизирующие тучные клетки, использовали в прошлом в качестве общих противовоспалительных средств, настоящее изобретение отличается от предыдущих применений, поскольку оно включает лечение острых воспалительных состояний в отличие от хронических состояний (например, SIRS против астмы). Кроме того, настоящее изобретение включает лечение симптомов, вызванных возбудителями инфекции, такими как вирусы, в отличие от аллергических реакций на сезонные аллергены.
[0046] Одним из наиболее распространенных состояний, которые могут вызвать гиперцитокинемию, является инфекция гриппа. Грипп имеет огромную смертность и оказывает влияние на мир каждый год, вызывая в среднем более 30000 смертей в год в США. Хотя существуют вакцины от сезонного гриппа, они имеют ограничения в том, что их эффективность зависит от выбора правильных штаммов задолго до наступления сезона гриппа, чтобы обеспечить время для производства. Доступные противовирусные терапии также ограничены в своей эффективности, поскольку вирус способен мутировать и становиться устойчивым ко всем известным в настоящее время противовирусным препаратам. Даже если вирус, инфицирующий пациента, чувствителен к используемому противовирусному препарату, ингибирование распространения вируса не лечит основной фактор риска гриппа; индуцированную гиперцитокинемию.
[0047] Тучные клетки являются резидентными часовыми, которые обнаруживают и реагируют на первоначальную инфекцию вирусом гриппа. Распознавание вируса тучными клетками осуществляется паттерн-распознающими рецепторами и приводит к быстрой дегрануляции, высвобождая множество цитокинов (Graham et al., J. Immunol. 190: 4676 (2013)). Это высвобождение медиаторов вызывает первые респондеры иммунной системы, включая Т-клетки, для атаки инфекции. Тучные клетки продолжают выделять цитокины, которые распространяются системно и продолжают привлекать больше иммунных клеток к инфекции. Эти привлеченные клетки также высвобождают цитокины для усиления иммунного ответа. Результатом может стать самоусиливающаяся петля, что усиливает ответ непропорционально инфекции. Острые симптомы, которые ощущаются при гриппе, вызваны медиаторами, а не нарушением, вызванным вирусом. Если не принять меры, эта воспалительная реакция вызывает повреждение тканей в легких и снижает функцию легких, обеспечивая в то же время идеальную среду для роста бактерий, что приводит к пневмонии. Если не принять меры, воспалительная реакция в легких может привести к острому респираторному дистресс-синдрому (ОРДС) и смерти.
[0048] Лечение пациента противовирусными препаратами не остановит этот самоусиливающийся цикл. На самом деле, к тому времени, когда пациент испытывает симптомы, это составляет по меньшей мере 48 часов после начала инфекции. Активная репликация вируса гриппа в результате проникновения в клетку начинается через 6 часов после заражения клетки и продолжается в течение нескольких дней. К тому времени, когда инфекция обнаружена и начато противовирусное лечение, уже наблюдается высокая вирусная нагрузка и сильный иммунный ответ: пациент уже в самом конце пути, ведущему к цитокиновому шторму. Таким образом, одной лишь остановки вируса на данном этапе недостаточно для лечения физиологического состояния пациентов, инфицированных гриппом.
[0049] Таким образом, один аспект изобретения относится к способу лечения, облегчения или профилактики гиперцитокинемии у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики гиперцитокинемии. В некоторых вариантах осуществления гиперцитокинемия обусловлена заболеванием, нарушением или состоянием у субъекта. В определенных вариантах осуществления заболевание, нарушение или состояние не является астмой, конъюнктивитом или мастоцитозом. В некоторых вариантах осуществления заболевание, нарушение или состояние представляет собой вирусную инфекцию, например, респираторную вирусную инфекцию, например, грипп. В некоторых вариантах осуществления заболевание, нарушение или состояние не является инфекцией гриппа.
[0050] Другой аспект изобретения относится к способу лечения, облегчения или профилактики нарушения, связанного с гиперцитокинемией, у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики нарушения.
[0051] Примеры клинических диагнозов, которые связаны с острой гиперцитокинемией, включают, без ограничения, вирусные инфекции, такие как грипп, гриппоподобное заболевание, синдром системной воспалительной реакции (от инфекционных или неинфекционных причин) или сепсис.
[0052] В некоторых вариантах осуществления способы осуществляются у субъектов, у которых диагностирована гиперцитокинемия. В других вариантах осуществления способы осуществляются у субъектов, у которых не диагностирована гиперцитокинемия, но диагностированы или имеются подозрения на наличие заболевания, расстройства или состояния, связанного с гиперцитокинемией, и для которых настоящие способы должны быть полезными. Как видно из этого списка клинических диагнозов, документированное повышение цитокинов не требуется для выявления пациентов, которые могли бы извлечь выгоду из этого лечения. На самом деле специалистам в данной области понятно, что обнаружение повышенного системного уровня цитокинов не всегда обнаруживается у пациентов, у которых цитокиновый шторм вызывает неблагоприятные эффекты. Локальная концентрация цитокинов, особенно в жизненно важных органах, более конкретно в легких, имеет большее значение, чем уровень цитокинов, обнаруживаемый в циркулирующей плазме. Таким образом, с практической точки зрения, опираясь на клинические диагнозы, такие как перечисленные выше, которые не измеряют цитокины, а скорее фокусируются на симптомах или известных причинах повышенного уровня цитокинов (таких как положительный тест на грипп), являются более эффективными при идентификации пациентов, которые извлекут выгоду из настоящее изобретение.
[0053] Другой аспект изобретения относится к способу лечения, облегчения или профилактики вирусной инфекции, связанной с гиперцитокинемией, у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики вирусной инфекции. В некоторых вариантах осуществления вирусная инфекция представляет собой респираторную вирусную инфекцию, например, грипп.
[0054] Как правило, первичная вирусная инфекция или реактивированный латентный вирус вызывает устойчивый цитокиновый ответ у пациентов. Это особенно опасно при респираторных вирусах, но другие также могут индуцировать опасные уровни цитокинов. В этих случаях уменьшение величины гиперцитокинемии является полезным, независимо от того, какой вирус вызывает ответ. Даже в тех случаях, когда симптомы не являются опасными для жизни, повышение уровня цитокинов вызывает симптомы, и они могут быть облегчены путем лечения соединением, стабилизирующим тучные клетки. Примеры вирусов, для которых этот метод лечения может быть полезен, включают, но не ограничиваются ими, грипп, парагрипп, норовирус, ВИЧ, парвовирус, вирус Синдбис, вирус денге, аденовирус, вирус Эпштейна-Барр (EBV), респираторно-синцитиальный вирус (RSV), вирус коровьей оспы, метапневмовирус, риновирус, цитомегаловирус (CMV), вирусы гепатита (все типы), вирус простого герпеса (все типы), вирус папилломы, коронавирус SARS, коронавирус MERS, вирус Западного Нила, вирус желтой лихорадки и другие. В некоторых вариантах вирус не является гриппом.
[0055] Дополнительный аспект изобретения относится к способу лечения, облегчения или профилактики лихорадки у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики лихорадки. В некоторых вариантах осуществления лихорадка связана с респираторной вирусной инфекцией, например, гриппом. В некоторых вариантах осуществления лихорадка связана с вирусной инфекцией или другим нарушением, связанным с гиперцитокинемией. В некоторых вариантах осуществления жаропонижающее действие соединения, стабилизирующего тучные клетки, приводит к снижению температуры тела по меньшей мере на 1°C, например, на 2°C, 3°C, 4°C, 5°C, или более.
[0056] В некоторых вариантах осуществления способы по изобретению дополнительно включают введение субъекту дополнительного терапевтического средства от заболевания, расстройства или состояния. В некоторых вариантах осуществления дополнительное терапевтическое средство представляет собой противовирусное средство, например, противогриппозное средство. Примеры противогриппозных средств включают, без ограничения, римантадин, амантадин, осельтамивир (Тамифлю (Tamiflu®)), ланинамивир (Inavir®), занамивир (Relenza®), перамивир (Rapivab®), тамифосфор, фавипиравир, VX-787, AL794, S-033188, AB103, TCAD Combo, Avi-7100, флуфивиртид-3, флуконазол (FluCide®), рибавирин (виразол), ингибиторы эндонуклеазы, ингибиторы матрицы M1, антитела к вирусным белкам, Vis-410, нитазоксанид, NT-300, флудаза, алферон, PUR003, EV-077, сурфаксин и хомспера. В одном варианте осуществления противогриппозное средство представляет собой осельтамивир. Лечение осельтамивиром для инфицированных пациентов составляет дозу по 75 мг два раза в день в течение 5 дней. Это обеспечивает терапевтическую дозу системно в течение периода времени, который считается подходящим для большинства случаев гриппа А и В. В некоторых вариантах осуществления дополнительное терапевтическое средство представляет собой жаропонижающее средство, такое как ибупрофен, напроксен, кетопрофен, нимесулид, аспирин и другие нестероидные противовоспалительные лекарственные средства и ацетаминофен. В некоторых вариантах осуществления дополнительное терапевтическое лекарственное средство представляет собой средство, используемое для лечения SIRS или сепсиса, например, антианафилактические средства, такие как эпинефрин, стероиды и дифенгидрамин, или антиоксиданты, такие как селен, глутамин, витамин Е и эйкозапентаеновая кислота.
[0057] Соединением, стабилизирующим тучные клетки, может быть любое соединение, стабилизирующее тучные клетки, известное в данной области. Примеры соединений, стабилизирующих тучные клетки, включают, без ограничения, кетотифен, норкетотифен, кромолин, недокромил, кверцетин, пемироласт, олопатадин, эбастин и каребастин. В некоторых вариантах осуществления способов по изобретению соединение, стабилизирующее тучные клетки, представляет собой кетотифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления способов по изобретению соединение, стабилизирующее тучные клетки, представляет собой норкетотифен или его фармацевтически приемлемую соль. В некоторых вариантах осуществления соединение, стабилизирующее тучные клетки, представляет собой комбинацию кетотифена или его фармацевтически приемлемой соли и норкетотифена или его фармацевтически приемлемой соли.
[0058] Соединение, стабилизирующее тучные клетки, и дополнительное терапевтическое средство можно вводить субъекту в одной и той же композиции или в отдельных композициях, например, вводить одновременно. Дополнительное терапевтическое средство может быть доставлено субъекту по другому режиму или другим путем по сравнению с соединением, стабилизирующим тучные клетки. Дополнительным терапевтическим средством может быть любое средство, которое приносит пользу субъекту.
[0059] Способы по настоящему изобретению также могут быть объединены с физическими методами лечения, которые, как известно в данной области, эффективны для лечения заболевания, нарушения или состояния. Физические методами лечения могут включать, без ограничения, хирургическое вмешательство (например, удаление ткани), трансплантацию костного мозга или цельных органов, плазмаферез, модуляцию (увеличение или уменьшение) температуры субъекта или ткани или органа у субъекта, или любую их комбинацию.
[0060] Соединения по изобретению могут вводиться субъекту по мере необходимости для лечения заболевания, нарушения или состояния. Соединение можно вводить непрерывно или периодически. В одном варианте осуществления соединение вводят субъекту более одного раза в день или один раз каждые 1, 2, 3, 4, 5, 6 или 7 дней. В другом варианте осуществления соединение вводят субъекту не чаще, чем один раз в неделю, например, не чаще, чем один раз каждые две недели, один раз в месяц, один раз каждые два месяца, один раз каждые три месяца, один раз каждые четыре месяца, один раз каждые пять месяцев, один раз в шесть месяцев или дольше. В дополнительном варианте осуществления соединение вводят с использованием двух или нескольких различных схем, например, сначала более часто (например, для повышения до определенного уровня, например, один раз в день или более) и затем менее часто (например, один раз в неделю или менее). В других вариантах осуществления соединение может быть введено по любой схеме прерывистого введения. В одном примере соединение может вводиться не чаще, чем раз в три дня, каждые четыре дня, каждые пять дней, каждые шесть дней, каждые семь дней, каждые восемь дней, каждые девять дней или каждые десять дней или больше. Введение может продолжаться в течение одной, двух, трех или четырех недель или одного, двух или трех месяцев или дольше. Необязательно, после периода отдыха соединение можно вводить по той же или другой схеме. Период отдыха может составлять одну, две, три или четыре недели или дольше, в зависимости от фармакодинамического воздействия соединения на субъекта.
[0061] Изучение уровней цитокинов периферической крови у инфицированных пациентов показывает, что повышенные уровни циркулирующих в крови цитокинов, особенно IP10 и IL-6, присутствуют в течение нескольких часов после заражения с пиком между 2 и 4 днями после заражения. Симптомы обычно появляются примерно через 2 дня после заражения. Уровень цитокинов повышается до гораздо более высоких уровней у пациентов с более тяжелыми симптомами и остается повышенным. Из-за различий в степени тяжести и течении инфекции от человека к человеку, комбинированная терапия может проводиться первоначально в течение 5 дней, и затем продолжена до тех пор, пока симптомы значительно разрешаться по отношению к исходному уровню.
[0062] Соединения по изобретению могут быть доставлены субъекту любым подходящим путем, например пероральным, ректальным, буккальным (например, подъязычным), вагинальным, парентеральным (например, подкожным, внутримышечным, интрадермальным или внутривенным), местным (т.е. как на поверхности кожи, так и на слизистых оболочках, включая поверхности дыхательных путей), назальной и/или пероральной ингаляцией и трансдермальным введением.
[0063] Когда противовирусное средство вводят путем ингаляции (например, занамивир), соединение, стабилизирующее тучные клетки, и противовирусное средство могут быть объединены в ингаляторе для одновременной доставки. Преимущество этого подхода заключается в доставке обоих активных соединений непосредственно к месту инфекции, что потенциально сокращает время, необходимое для достижения терапевтических уровней в инфицированных клетках, и, следовательно, повышает эффективность. Дополнительным преимуществом использования соединения, стабилизирующего тучные клетки (например, кетотифен с ингаляционным противовирусным препаратом), является его эффективность для лечения астмы. Одной из проблем для безопасности с занамивиром является появление побочных эффектов у пациентов с астмой и хронической обструктивной болезнью легких. Возможно, что противовоспалительные свойства соединений, стабилизирующих тучные клетки, таких как кетотифен, могут уменьшить эти осложнения и увеличить популяцию, в которой можно использовать ингаляционный противовирусный препарат.
[0064] Могут быть разработаны некоторые новые противовирусные методы лечения, которые требуют только одной дозы. Двумя примерами, находящимися в процессе разработки, являются моноклональное антитело против гриппа или ингибитор кэп-зависимой эндонуклеазы. В сочетании с такими методами лечения, к лечению может быть добавлено соединение, стабилизирующее тучные клетки, и оно может быть доставлено в течение нескольких дней, вероятно, более 3 дней, чтобы уменьшить влияние гиперцитокинемии. Подход, основанный на микросферах с временным высвобождением, может также использоваться для одновременной доставки соединения, стабилизирующего тучные клетки, и обеспечения его присутствия в течение продолжительного времени, даже при использовании только одной дозы. Shiny et al. (Int. J. Pharm. Investig. 3(3):119 (2013)) является примером подхода для непрерывной доставки до 30 дней.
[0065] Некоторые вирусные заболевания могут вызывать тяжелые симптомы, требующие госпитализации. Пациентам в стационаре может быть целесообразно проводить терапию внутривенно. Для этой цели противовирусное средство и соединение, стабилизирующее тучные клетки, можно вводить через ВВ, обеспечивая дозировку обоих препаратов в течение необходимого периода времени. Таким образом, тяжелобольные пациенты, которые не могут глотать лекарства, смогут получать лечение этой комбинацией лекарственных средств.
[0066] Соединения вводят субъекту в дозе, эффективной для лечения расстройства. Эффективная доза будет зависеть от многих факторов, включая пол, возраст, массу и общее физическое состояние субъекта, тяжесть заболевания, конкретное соединение или композицию, которую вводят, продолжительность лечения, характер любого параллельного лечения, используемый носитель и подобные факторы в пределах знаний и опыта специалистов в данной области. При необходимости эффективное количество для лечения в любом отдельном случае может быть определено специалистом в данной области с помощью ссылок на соответствующие тексты и литературу и/или с использованием рутинных экспериментов (см., например, Remington, The Science and Practice of Pharmacy (21st ed. 2005)). В одном варианте осуществления соединение, стабилизирующее тучные клетки, вводят в дозе от около 0,001 до около 500 мг/кг массы тела, например, около 0,001, 0,005, 0,01, 0,05, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400 или 500 мг/кг или в любом диапазоне в нем. В некоторых случаях доза может быть еще ниже, например, до 0,0005 или 0,0001 мг/кг или ниже. В некоторых случаях доза может быть даже выше, например, до 20, 50, 100, 500 или 1000 мг/кг или выше. Для кетотифена диапазон доз может составлять от около 0,001 мг/кг до около 40 мг/кг, например, от около 0,01 мг/кг до около 20 мг/кг, например, около 0,001, 0,005, 0,01, 0,05, 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 15, 20, 25, 30, 35 или 40 мг/кг или в любом диапазоне в нем. Для норкетотифена диапазон доз может составлять от около 0,001 мг/кг до около 500 мг/кг, например, от около 0,01 мг/кг до около 200 мг/кг, например, около 0,001, 0,005, 0,01, 0,05, 0,1, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, or 100, 150, 200, 250, 300, 350, 400, 450 или 500 мг/кг или в любом диапазоне в нем. Настоящее изобретение охватывает каждый поддиапазон в пределах указанных диапазонов и количеств. Эти дозы могут вводиться один раз в день или более одного раза в день, например, 2, 3 или 4 раза в день.
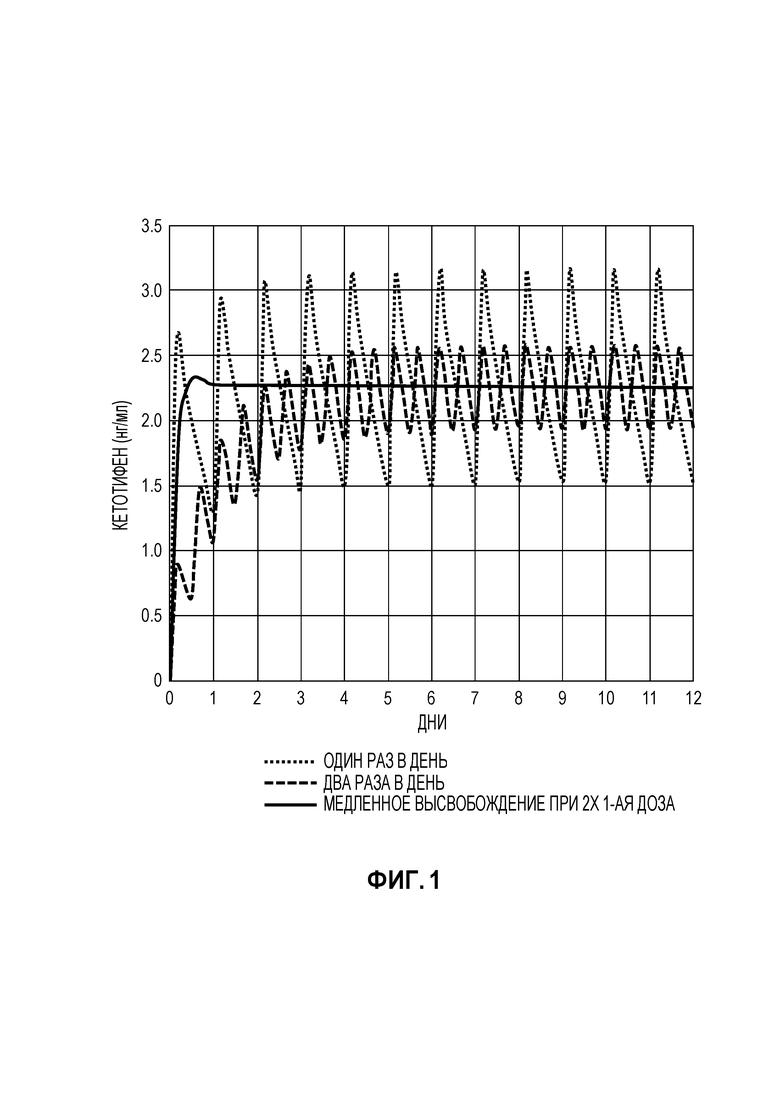
[0067] Поскольку симптомы гриппа обычно не появляются в течение одного или двух дней после заражения, желательно, чтобы системные терапевтические уровни соединения, стабилизирующего тучные клетки, и дополнительного терапевтического средства были получены быстро, чтобы предотвратить как распространение вируса, так и накопление более высокого уровня цитокины. Для достижения этого способом, который обеспечит легкое соблюдение пациентом режима, может быть предпочтительной форма введения с замедленным высвобождением. На фиг. 1 показаны уровни в сыворотке, вычисленные для кетотифена в дозе 4 мг в день в нескольких различных режимах дозирования на основании опубликованных фармакокинетических данных.
[0068] Два раза в день дозирование при 2 мг на дозу является текущим подходом, используемым для нарушений работы тучной клетки. Для достижения устойчивого уровня около 2 нг/мл требуется не менее 2,5 дней. Если дозировка 4 мг/день принимается за одну дозу, она быстро превышает уровень устойчивого состояния, но каждый день общий уровень значительно понижается и падает ниже 2 нг/мл. Если метод с замедленным высвобождением используется с первой дозой, удвоенной до 8 мг, уровень 2 нг/мл достигается быстро, общий уровень не становится слишком высоким и поддерживается постоянная доза выше 2 нг/мл. Таким образом, использование метода с временным высвобождением, необязательно с увеличенной начальной дозой, позволяет быстро увеличивать системные уровни лекарственного средства, которые поддерживаются на протяжении всего лечения.
[0069] Одним из свойств многих вирусов, включая грипп, является то, что они вызывают большое воспаление и секреты из носа. Может быть выгодно доставлять эту комбинацию противовирусного средства и соединения, стабилизирующего тучные клетки, с использованием интраназального пути (например, путем назальной инстилляции и/или назальной ингаляции), доставляя соединение, стабилизирующее тучные клетки, непосредственно в придаточные пазухи носа. Придаточные пазухи носа богаты сосудистой сетью, что позволяет эффективно абсорбировать многие лекарственные средства, используя этот способ. Фактически, было показано, что кетотифен является более биодоступным при интраназальной доставке у кроликов, чем любой другой путь. Дополнительное преимущество стабилизатора тучных клеток, такого как кетотифен, заключается в его антигистаминных свойствах, позволяющих быстро и эффективно снизить выраженность носовых симптомов.
[0070] Некоторые лекарственные средства доставляются подкожно или внутримышечно для обеспечения доступности соединений, которые нелегко абсорбируются другими путями введения. Этот метод также имеет преимущество в скорости и практичности в больницах, кабинетах врачей, аптеках и дома. Существует множество доступных автоинжекторных систем, которые облегчают самостоятельное введение терапевтических доз комбинации по изобретению. В этом случае соединения могут быть смешаны в одной камере, если они совместимы, или может быть использована двухкамерная система для хранения противовирусного соединения и соединения, стабилизирующего тучные клетки, в отдельных отделениях до дозирования. Поскольку вполне вероятно, что режим дозирования будет составлять несколько дней, система, которая позволяет осуществлять многократное дозирование с одного устройства (или «ручки»), повысит удобство и соответствие необходимому режиму введения.
[0071] Для некоторых пациентов (включая детей) глотание таблеток или пилюль является трудным или невозможно. В этих случаях может быть выгодно доставлять комбинацию по изобретению в жидкой лекарственной форме для перорального применения. Эта лекарственная форма может доставлять комбинацию лекарственного средства по механизму замедленного высвобождения или по любому другому желаемому профилю доставки. Это также может быть выполнено с использованием суппозитория для внутриректальной доставки.
[0072] Настоящее изобретение находит применение в исследованиях, а также в ветеринарии и медицине. Подходящими субъектами обычно являются млекопитающие. Термин «млекопитающее», как используется в настоящем документе, включает, но не ограничивается этим, людей, приматов (кроме человека), крупный рогатый скот, овец, коз, свиней, лошадей, кошек, собак, кроликов, грызунов (например, крыс или мышей) и т.п. Человек включает новорожденных, детей, подростков, взрослых и пожилых людей.
[0073] В конкретных вариантах осуществления субъект представляет собой человека, у которого имеется гиперцитокинемия или нарушение, связанное с гиперцитокинемией, например, вирусные инфекции, такие как грипп, гриппоподобное заболевание, синдром системной воспалительной реакции, или сепсис, или лихорадка. В других вариантах осуществления субъект представляет собой человека, подверженного риску развития гиперцитокинемии или нарушения, связанного с гиперцитокинемией, например, субъекта, который подвергался воздействию вируса или живет или работает с субъектом, у которого, как известно, имеется вирусная инфекция. Когда вирус, подобный гриппу, заражает человека, обнаруживаемое увеличение системы цитокинов начинается через несколько часов после заражения. Хотя связанное с этим локальное воспаление может служить для ограничения распространения вируса, в большинстве случаев системное увеличение цитокинов мало что делает для предотвращения распространения инфекции и, вероятно, замедляет выведение вируса адаптивной иммунной системой. Кроме того, скопившиеся жидкости от воспаления способствуют распространению вируса через чихание и кашель. Полученные микрокапельки позволяют вирусным частицам оставаться в аэрозоле в течение продолжительного времени, что позволяет ему более эффективно распространяться. Способы по изобретению можно использовать профилактически для уменьшения симптомов у любого инфицированного и уменьшения распространения вируса. В других вариантах осуществления субъект, используемый в способах по изобретению, представляет собой животную модель гиперцитокинемии или нарушения, связанного с гиперцитокинемией.
[0074] Субъект может быть субъектом, «нуждающимся» в способах по настоящему изобретению, например, нуждающимся в терапевтических и/или профилактических эффектах способов изобретения.
[0075] В некоторых вариантах осуществления субъект находится в группе повышенного риска вирусной инфекции, например, инфекции гриппа. К ним относятся, но не ограничиваются ими, пожилые люди, очень молодые люди, беременные женщины, пациенты с ослабленным иммунитетом и этнические группы, которые подвергаются более высокому риску (например, американские эскимосы, коренные американцы). Кроме того, очень вирулентные штаммы гриппа вызвали более тяжелые заболевания у здоровых людей в возрасте от 20 до 50 лет (пандемический штамм 2009 года является самым последним примером), и этот режим, вероятно, будет более эффективным в этой группе для вирулентного штамма.
[0076] Еще один аспект изобретения относится к фармацевтической композиции, содержащей норкетотифен и фармацевтически приемлемый носитель. Фармацевтическая композиция может дополнительно включать дополнительное терапевтическое средство, например, противовирусное средство, например, противогриппозное средство, например, осельтамивир.
[0077] Другой аспект изобретения относится к фармацевтической композиции, включающей кетотифен, дополнительное терапевтическое средство и фармацевтически приемлемый носитель. В некоторых вариантах осуществления, дополнительное терапевтическое средство представляет собой противовирусное средство, например, противогриппозное средство, например, осельтамивир.
[0078] Дополнительный аспект изобретения относится к лекарственной форме, включающей фармацевтическую композицию по изобретению. Лекарственная форма может быть любой лекарственной формой, известной в данной области, которая подходит для способов по настоящему изобретению. Лекарственная форма может представлять собой, без ограничения, твердую или жидкую пероральную лекарственную форму, лекарственную форму для назальной и/или пероральной ингаляции, лекарственную форму для внутривенного введения, лекарственную форму для трансдермального или мукозального введения (например, пластырь), лекарственную форму для инъекций (например, подкожной или внутримышечной), лекарственную форму для имплантации (например, рассасывающуюся лекарственную форму или устройство, такое как насос) или лекарственную форму для внутриглазного введения.
[0079] Соединения по настоящему изобретению (например, соединения, стабилизирующие тучные клетки, такие как кетотифен и норкетотифен), включают все их фармацевтически приемлемые солевые формы. Примеры таких солей включают соли, полученные из фармацевтически приемлемых неорганических и органических кислот и оснований. Примеры подходящих солей кислот включают, без ограничения, ацетат, адипат, альгинат, аспартат, бензоат, бутират, цитрат, фумарат, гликолят, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, малонат, метансульфонат, никотинат, нитрат, оксалат, пальмоат, пектинат, персульфат, гидроксинаптоат, пивалат, пропионат, салицилат, сукцинат, сульфат, тартрат, тиоцианат, тозилат и ундеканоат. Другие кислоты, такие как щавелевая кислота, которые сами по себе не являются фармацевтически приемлемыми, могут быть использованы при получении солей, полезных в качестве промежуточных соединений при получении соединений по изобретению и их фармацевтически приемлемых кислотно-аддитивных солей.
[0080] Соли, полученные из соответствующих оснований, включают, без ограничения, соли щелочных металлов (например, натрия, калия), щелочноземельных металлов (например, магния и кальция), аммония и N-(алкил)4+.
[0081] Соединения по изобретению включают соединения, имеющие кватернизацию любой основной азотсодержащей группы в них.
[0082] Обсуждение в настоящем документе для простоты приведено без ссылки на стереоизомерию. Специалистам в данной области понятно, что соединения по изобретению могут включать один или несколько асимметричных центров и, таким образом, могут встречаться в виде рацематов и рацемических смесей, отдельных оптических изомеров, индивидуальных диастереомеров и диастереомерных смесей. Все такие изомерные формы этих соединений явным образом включены в настоящее изобретение.
[0083] Аналогичным образом, соединения по изобретению, содержащие двойную связь, могут существовать в форме геометрических изомеров, которые могут быть легко разделены и восстановлены с помощью обычных процедур. Такие изомерные формы входят в объем настоящего изобретения.
[0084] Если не указано иное, подразумевается, что структуры, изображенные в настоящем документе, также включают соединения, которые отличаются только присутствием одного или нескольких изотопно обогащенных атомов. Например, соединения, имеющие настоящие структуры, где водород заменен на дейтерий или тритий или углерод заменен на 13С- или 14С-обогащенный углерод, входят в объем настоящего изобретения. Такие соединения являются полезными, например, в качестве аналитических инструментов или зондов в биологических анализах.
[0085] Кроме того, соединения по изобретению включают пролекарства соединений, которые превращаются в активное соединение in vivo. Например, соединение можно модифицировать для увеличения клеточной проницаемости (например, путем этерификации полярных групп), и затем превратить в активное соединение с помощью клеточных ферментов. Способы маскировки заряженных или реакционноспособных фрагментов в качестве пролекарства известны специалистам в данной области (см., например, P. Korgsgaard-Larsen and H. Bundgaard, A Textbook of Drug Design and Development, Reading U.K., Harwood Academic Publishers, 1991).
[0086] Термин «пролекарство» относится к соединениям, которые быстро превращаются in vivo с образованием исходного соединения приведенной выше формулы, например, путем гидролиза в крови, см., например, T. Higuchi and V. Stella, Prodrugs as Novel delivery Systems, Vol. 14 of the A.C.S. Symposium Series and in Edward B. Roche, ed., Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press, 1987, оба из которых включены в настоящее описание в качестве ссылки. См. также патент США No. 6680299. Примеры пролекарств включают такие пролекарства, которые в результате метаболизма in vivo в организме пациента превращаются в активное лекарственное средство, обладающее активностью соединений, описанных в настоящем документе, причем пролекарство является сложным эфиром спирта или карбоксильной группы, если такая группа присутствует в соединении; амидом аминогруппы или группы карбоновой кислоты, если такие группы присутствуют в соединении; уретаном аминогруппы, если такая группа присутствует в соединении; ацеталем или кеталем спиртовой группы, если такая группа присутствует в соединении; N-основанием Манниха или имином аминогруппы, если такая группа присутствует в соединении; или основанием Шиффа, оксимом, ацеталем, сложным эфиром енола, оксазолидином или тиазолидином карбоксильной группы, если такая группа присутствует в соединении, как описано, например, в патенте США No. 6680324 и патенте США No. 6680322.
[0087] Термин «фармацевтически приемлемое пролекарство» (и подобные термины), как используется в настоящем описании, относится к таким пролекарствам соединений по настоящему изобретению, которые в рамках здравого медицинского суждения подходят для использования в контакте с тканями человека и/или других животных без чрезмерной токсичности, раздражения, аллергического ответа и тому подобного, соразмерных с разумным соотношением риск/польза и эффективны для их предполагаемого использования, а также, когда это возможно, к цвиттерионным формам соединений по изобретению.
[0088] Соединения по изобретению, описанные выше, могут быть составлены для введения в фармацевтическом носителе в соответствии с известными методиками. См., например, Remington, The Science And Practice of Pharmacy (21st ed. 2005). При изготовлении фармацевтической композиции по изобретению соединение обычно смешивают, в частности, с приемлемым носителем. Носитель должен, конечно, быть приемлемым в смысле совместимости с любыми другими ингредиентами в составе и не должен быть опасным для пациента. Носитель может быть твердым или жидким, или и тем, и другим, и может быть составлен с соединением в виде стандартной дозы лекарственной формы, например, таблетки, которая может содержать от 0,01% или 0,5% до 95% или 99% по массе соединения. Одно или несколько соединений могут быть включены в лекарственные формы по изобретению, которые могут быть получены любым из хорошо известных методов фармации, включающих смешивание компонентов, необязательно включающих один или несколько вспомогательных ингредиентов.
[0089] Лекарственные формы по изобретению включают формы, подходящие для перорального, ректального, местного, буккального (например, подъязычного), вагинального, парентерального (например, подкожного, внутримышечного, внутрикожного или внутривенного), местного (то есть как через кожу, так и через слизистую оболочку, включая дыхательные пути) введения, назальной и/или пероральной ингаляции и трансдермального введения, хотя наиболее подходящий способ в любом конкретном случае будет зависеть от природы и тяжести состояния, подлежащего лечению, и от природы конкретного активного соединения, которое используется.
[0090] Лекарственные формы, подходящие для перорального введения, могут быть представлены в отдельных единицах, таких как капсулы, саше, пастилки или таблетки, каждая из которых содержит заранее определенное количество активного соединения; в виде множества частиц, порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; или в виде эмульсии масло-в-воде или вода-в-масле. Такие лекарственные формы могут быть получены любым подходящим способом фармации, который включает стадию объединения соединения и подходящего носителя (который может содержать один или несколько вспомогательных ингредиентов, как указано выше). Как правило, лекарственные формы по изобретению получают путем равномерного и тщательного смешивания соединения с жидким или тонкоизмельченным твердым носителем или с обоими, и затем, если необходимо, формования полученной смеси. Например, таблетка может быть получена прессованием или формовкой порошка или гранул, содержащих соединение, необязательно с одним или несколькими дополнительными ингредиентами. Прессованные таблетки могут быть получены путем прессования в подходящей машине соединения в сыпучей форме, такой как порошок или гранулы, необязательно смешанных со связующим веществом, смазочным материалом, инертным разбавителем и/или поверхностно-активным/диспергирующим средством(ами). Формованные таблетки могут быть получены путем формования в подходящей машине порошкообразного соединения, увлажненного инертным жидким связующим.
[0091] Термин «таблетка», как используется в настоящем документе, включает, но не ограничивается ими, таблетки с немедленным высвобождением (IR), таблетки с замедленным высвобождением (SR), таблетки с пролонгированным высвобождением (ER), матричные таблетки, многослойные таблетки, многослойные матричные таблетки, таблетки с отсроченным высвобождением и таблетки с прерывистым высвобождением, любые или все из которых могут быть необязательно покрыты одним или несколькими материалами для покрытия, включая полимерные материалы для покрытий, такие как кишечнорастворимые покрытия, контролирующие скорость покрытия, полупроницаемые покрытия и тому подобное. Термин «таблетка» также включает осмотические системы доставки, в которых лекарственное соединение объединено с осмотическим агентом (и, необязательно другими эксципиентами) и покрыто полупроницаемой мембраной, причем полупроницаемая мембрана определяет отверстие, через которое лекарственное соединение может быть высвобождено. Таблетированные твердые лекарственные формы, которые могут быть полезны при осуществлении изобретения, включают формы, выбранные из группы, состоящей из таблеток IR, таблеток SR, таблеток ER, таблеток IR с покрытием, таблеток SR с покрытием, таблеток ER с покрытием, матричных таблеток, матричных таблеток, покрытых оболочкой, многослойных таблеток, многослойных таблеток с покрытием, многослойных матричных таблеток и многослойных матричных таблеток, покрытых оболочкой. В некоторых вариантах осуществления таблетированная лекарственная форма представляет собой таблетированную лекарственную форму с энтеросолюбильным покрытием. В некоторых вариантах осуществления таблетированная лекарственная форма представляет собой таблетированную лекарственную форму, покрытую кишечнорастворимой оболочкой, с замедленным высвобождением.
[0092] Термин «капсула», как используется в настоящем документе включает, но не ограничивается ими, IR-капсулы, SR-капсулы, ER-капсулы, IR-капсулы с покрытием, SR-капсулы с покрытием и ER-капсулы, включая капсулы с отсроченным высвобождением. Капсулы могут быть заполнены порошками, гранулами, мультичастицами, таблетками, полутвердыми веществами или жидкостями. В некоторых вариантах осуществления инкапсулированная лекарственная форма представляет собой инкапсулированную лекарственную форму, покрытую кишечнорастворимой оболочкой. В некоторых вариантах осуществления инкапсулированная лекарственная форма представляет собой инкапсулированную лекарственную форму, покрытую кишечнорастворимой оболочкой, с замедленным высвобождением. Капсулы могут быть изготовлены из твердого желатина, мягкого желатина, крахмала, целлюлозных полимеров или других материалов, известных в данной области техники.
[0093] Термин «лекарственная форма в виде множества частиц» означает множество дискретных частиц, микрочастиц, наночастиц, шариков, мини-таблеток и их смесей или комбинаций. Если лекарственная форма для перорального применения представляет собой капсулу, состоящую из множества частиц, можно использовать твердые или мягкие желатиновые капсулы или капсулы из других материалов для вмещения множества частиц. В некоторых вариантах осуществления пакет-саше может быть подходящим образом использован для вмещения множества частиц. В некоторых вариантах осуществления лекарственная форма, состоящая из множества частиц, может быть покрыта слоем, содержащим контролирующий скорость полимерный материал. В некоторых вариантах осуществления лекарственная форма для перорального введения, состоящая из множества частиц, в соответствии с изобретением может содержать смесь двух или более совокупностей частиц, шариков или мини-таблеток, имеющих различные характеристики высвобождения in vitro и/или in vivo. Например, лекарственная форма для перорального применения, состоящая из множества частиц, может включать смесь компонента с немедленным высвобождением и компонента с отсроченным высвобождением, содержащуюся в подходящей капсуле.
[0094] В некоторых вариантах осуществления изобретения лекарственная форма, состоящая из множества частиц, и одного или нескольких вспомогательных эксципиентов, может быть спрессована в форму таблетки, такую как многослойная таблетка. В некоторых вариантах осуществления многослойная таблетка может включать два слоя, включающие одинаковые или различные уровни одного и того же активного ингредиента, имеющего одинаковые или различные характеристики высвобождения. В некоторых вариантах осуществления многослойная таблетка может содержать различные активные ингредиенты в каждом слое. Такая таблетка, однослойная или многослойная, может быть необязательно покрыта полимером с контролируемым высвобождением для того, чтобы обеспечить дополнительные свойства контролируемого высвобождения. В некоторых вариантах осуществления лекарственная форма, состоящая из множества частиц, заключает в себе капсулу, содержащую мини-таблетки с отсроченным высвобождением быстрого проявления. В некоторых вариантах осуществления лекарственная форма, состоящая из множества частиц, заключает в себе капсулу с отсроченным высвобождением, содержащую мини-таблетки с немедленным высвобождением. В некоторых вариантах осуществления лекарственная форма, состоящая из множества частиц, заключает в себе капсулу, содержащую гранулы с отсроченным высвобождением. В некоторых вариантах осуществления лекарственная форма, состоящая из множества частиц, заключает в себе капсулу с отсроченным высвобождением, содержащую гранулы с мгновенным высвобождением.
[0095] Лекарственные формы, подходящие для трансбуккального (подъязычного) введения, включают таблетки для рассасывания, включающие соединение в ароматизированной основе, обычно в сахарозе и аравийской камеди или трагаканте; и пастилки, включающие соединение в инертной основе, такой как желатин и глицерин или сахароза и аравийская камедь.
[0096] Лекарственные формы по настоящему изобретению, подходящие для парентерального введения, включают стерильные водные и неводные инъекционные растворы соединения, причем эти препараты предпочтительно являются изотоническими по отношению к крови предполагаемого реципиента. Эти препараты могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают лекарственную форму изотонической с кровью предполагаемого реципиента. Водные и неводные стерильные суспензии могут включать суспендирующие агенты и загустители. Лекарственные формы могут быть представлены в однодозовых (например, в шприце или другом инъекционном устройстве) или в многодозовых контейнерах, например, в герметичных ампулах и флаконах, и могут храниться в сублимированном (лиофилизированном) состоянии, требующем только добавления стерильного жидкого носителя, например, физиологического раствора или воды для инъекций непосредственно перед использованием. Экстемпоральные инъекционные растворы и суспензии могут быть приготовлены из стерильных порошков, гранул и таблеток ранее описанного типа. Например, в одном аспекте настоящего изобретения предоставляется инъецируемая стабильная стерильная композиция, содержащая одно или несколько соединений, в стандартной лекарственной форме в герметичном контейнере. Соединение предоставляется в форме лиофилизата, который способен к восстановлению подходящим фармацевтически приемлемым носителем с образованием жидкой композиции, подходящей для ее инъекции субъекту. Стандартная лекарственная форма обычно содержит от около 0,001 мг до около 10 г соединения. Когда соединение является по существу нерастворимым в воде (например, когда оно конъюгировано с липидом), достаточное количество эмульгирующего агента, которое является физиологически приемлемым, может быть использовано в достаточном количестве для эмульгирования соединения в водном носителе. Одним из таких полезных эмульгирующих агентов является фосфатидилхолин.
[0097] Лекарственные формы, подходящие для ректального введения, предпочтительно представлены в виде однодозовых суппозиториев. Они могут быть получены путем смешивания соединения с одним или несколькими обычными твердыми носителями, например, маслом какао, и затем формования полученной смеси.
[0098] Лекарственные формы, подходящие для местного нанесения на кожу, предпочтительно принимают форму мази, крема, лосьона, пасты, геля, спрея, аэрозоля или масла. Носители, которые могут быть использованы, включают вазелин, ланолин, полиэтиленгликоли, спирты, трансдермальные усилители и комбинации двух или более из них.
[0099] Лекарственные формы, подходящие для трансдермального введения, могут быть представлены в виде дискретных пластырей, приспособленных для того, чтобы оставаться в тесном контакте с эпидермисом реципиента в течение длительного периода времени. Лекарственные формы, подходящие для трансдермального введения, также могут быть доставлены с помощью ионофореза (см., например, Pharm. Res. 3:318 (1986)) и обычно принимают форму необязательно забуференного водного раствора соединения. Подходящие составы включают цитрат или бис/трис-буфер (рН 6) или этанол/воду и включают от 0,1 до 0,2 М активного ингредиента.
[0100] Другие фармацевтические композиции могут быть получены из соединений, раскрытых в настоящем документе, таких как эмульсии на водной основе. В таком случае композиция будет включать достаточное количество фармацевтически приемлемого эмульгирующего агента для эмульгирования желаемого количества соединения. Особенно полезные эмульгаторы включают фосфатидилхолины и лецитин.
[0101] В дополнение к соединению, фармацевтические композиции могут содержать другие добавки, такие как рН-регулирующие добавки. В частности, применимые рН-регулирующие агенты включают кислоты, такие как хлористоводородная кислота, основания или буферы, такие как лактат натрия, ацетат натрия, фосфат натрия, цитрат натрия, борат натрия или глюконат натрия. Кроме того, композиции могут содержать микробиологические консерванты. Применимые микробиологические консерванты включают метилпарабен, пропилпарабен и бензиловый спирт. Микробиологический консервант, как правило, использовали в том случае, если состав помещали в сосуд, предназначенный для многодозового применения. Другие добавки, которые хорошо известны в данной области, включают, например, агенты для уменьшения вязкости, пеногасители, антиоксиданты (например, аскорбилпальмитат, бутилгидроксианизол (ВНА), бутилгидрокситолуол (ВНТ) и токоферолы, например, α-токоферол (витамин) E)), консерванты, хелатирующие агенты (например, EDTA и/или EGTA), модуляторы вязкости, вспомогательные вещества (например, сахар, такой как сахароза, лактоза и/или маннит), ароматизаторы, красители, отдушки, замутнители, суспендирующие агенты, связующие вещества, наполнители, смягчители, смазывающие вещества и их смеси. Количество таких добавок может быть легко определено специалистом в данной области в соответствии с конкретными желаемыми свойствами.
[0102] Добавка также может включать загуститель. Подходящими загустителями могут быть те, которые известны и применяются в данной области, включая, например, фармацевтически приемлемые полимерные материалы и неорганические загустители. Примеры загустителей для использования в настоящих фармацевтических композициях включают полиакрилатные смолы и полиакрилат-сополимерные смолы, например, смолы на основе полиакриловой кислоты и полиакриловой кислоты/метакриловой кислоты; целлюлозы и производные целлюлозы, включая: алкилцеллюлозы, например, метил-, этил- и пропилцеллюлозы; гидроксиалкилцеллюлозы, например, гидроксипропилцеллюлозы и гидроксипропилалкилцеллюлозы, такие как гидроксипропилметилцеллюлозы; ацилированные целлюлозы, например, ацетаты целлюлозы, ацетатфталлаты целлюлозы, ацетатсукцинаты целлюлозы и фталлаты гидроксипропилметилцеллюлозы; и их соли, такие как натрий-карбоксиметилцеллюлоза; поливинилпирролидоны, включая, например, сополимеры поли-N-винилпирролидонов и винилпирролидонов, такие как винилпирролидон-винилацетатные сополимеры; поливиниловые смолы, например, включая поливинилацетаты и спирты, а также другие полимерные вещества, включая трагакантовую камедь, гуммиарабик, альгинаты, например, альгиновую кислоту, и ее соли, например, альгинаты натрия; и неорганические загустители, такие как атапульгит, бентонит и силикаты, включая гидрофильные продукты диоксида кремния, например, алкилированные (например, метилированные) силикагели, в частности, коллоидный диоксид кремния. Такие загустители, как описано выше, могут быть включены, например, для обеспечения эффекта замедленного высвобождения. Однако, когда предполагается пероральное введение, использование загустителей, как указано выше, обычно не требуется и, как правило, менее предпочтительно. С другой стороны, использование загустителей показано, например, там, где предусмотрено местное применение.
[0103] Кроме того, настоящее изобретение относится к липосомальным составам соединений, раскрытых в настоящем документе. Технология образования липосомальных суспензий хорошо известна в данной области. Когда соединение находится в форме водорастворимого вещества, то используя обычную липосомальную технологию, она же может быть включена в липидные везикулы. В таком случае, благодаря растворимости соединения в воде, соединение будет по существу захвачено гидрофильным центром или ядром липосом. Используемый липидный слой может быть любой обычной композиции и может содержать холестерин или не содержать холестерин. Если представляющее интерес соединение является нерастворимым в воде, то снова используя обычную технологию образования липосом, соединение может быть по существу захвачено в гидрофобный липидный бислой, который образует структуру липосомы. В любом случае, получаемые липосомы могут быть уменьшены в размере, при помощи использовании стандартных методов обработки ультразвуком и гомогенизации. Липосомальные составы, содержащие соединение, раскрытое в настоящем описании, могут быть лиофилизированы для получения лиофилизата, который может быть восстановлен фармацевтически приемлемым носителем, таким как вода, для регенерации липосомальной суспензии.
[0104] В определенных вариантах осуществления лекарственная форма представляет собой лекарственную форму с замедленным высвобождением. Лекарственная форма может иметь период полураспада по меньшей мере 24 часа. В некоторых вариантах осуществления лекарственная форма с замедленным высвобождением будет обеспечивать более медленное высвобождение лекарственного средства в течение 24-часового периода времени, так что постоянный ограниченный диапазон лекарственного средства доступен системно в течение 24 часов. В определенных вариантах осуществления, как показано в примере на фиг.1, уровень соединения в сыворотке поддерживается выше 2 нг/мл на протяжении всего периода лечения, но в то же время не поднимается выше 2,5 нг/мл. Лекарственная форма может содержать и/или покрываться контролирующим скорость полимерным материалом, например, гидроксипропилметилцеллюлозой, полимером акриловой или метакриловой кислоты или их соответствующими эфирами, или сополимерами акриловой или метакриловой кислоты или их соответствующими эфирами.
[0105] В любом из вышеупомянутых вариантов осуществления покрытие с контролируемым высвобождением (например, кишечнорастворимое покрытие) может быть нанесено на конечную лекарственную форму (капсула, таблетка, многослойная таблетка и т.д.). Покрытие с контролируемым высвобождением обычно может содержать контролирующий скорость полимерный материал, как определено выше. Характеристики растворения такого материала для покрытия могут зависеть от рН или не зависеть от рН.
[0106] Термин «контролирующий скорость полимерный материал», как используется в настоящем документе, включает гидрофильные полимеры, гидрофобные полимеры и смеси гидрофильных и/или гидрофобных полимеров, которые способны контролировать или замедлять высвобождение соединения из лекарственной формы по настоящему изобретению. Подходящие контролирующие скорость полимерные материалы включают материалы, выбранные из группы, состоящей из гидроксиалкилцеллюлозы, такой как гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза; поли(этилен)оксида; алкилцеллюлозы, такой как этилцеллюлоза и метилцеллюлоза; карбоксиметилцеллюлозы; гидрофильных производных целлюлозы; полиэтиленгликоля; поливинилпирролидона; ацетата целлюлозы; ацетобутирата целлюлозы; ацетатфталата целлюлозы; ацетат-тримеллитата целлюлозы; поливинилацетат фталата; фталата гидроксипропилметилцеллюлозы; сукцината гидроксипропилметилцеллюлозы; поливинилацетальдиэтиламино ацетата; поли(алкилметакрилат) и поли(винилацетат). Другие подходящие гидрофобные полимеры включают полимеры и/или сополимеры, полученные из акриловой или метакриловой кислоты и их соответствующих сложных эфиров, зеин, воски, шеллак и гидрогенизированные растительные масла. Особенно полезными в практике осуществления настоящего изобретения являются полимеры полиакриловой кислоты, полиакрилата, полиметакриловой кислоты и полиметакрилата. Некоторые из этих полимеров (например, полиметакрилатные полимеры) можно использовать в качестве полимеров с отсроченным высвобождением для контроля места высвобождения лекарственного средства.
[0107] Вышеизложенное является иллюстративным для настоящего изобретения, и это не следует рассматривать как его ограничение. Настоящее изобретение определено следующей формулой изобретения с эквивалентами формулы изобретения, которые в нее включены. Все публикации, патентные заявки, патенты, патентные публикации и любые другие ссылки, цитируемые в настоящем документе, включены в качестве ссылки во всей их полноте для идей, относящихся к предложению и/или параграфу, в котором представлена ссылка.
Группа изобретений относится к области медицины и предназначена для лечения, облегчения или профилактики гиперцитокинемии у субъекта, нуждающегося в этом, и включает введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики гиперцитокинемии, где соединение, стабилизирующее тучные клетки, представляет собой норкетотифен или его фармацевтически приемлемую соль. Также представлены способ лечения, облегчения или профилактики нарушения, связанного с гиперцитокинемией, и способ лечения, облегчения или профилактики лихорадки у субъекта. Техническим результатом группы изобретений является обеспечение более эффективного способа, способствующего уравновешиванию ингибирования слишком сильного иммунного ответа организма и обеспечения слишком малого ответа для обеспечения лечения, которое позволяет решать обе проблемы: исходное состояние, на которое реагирует организм (то есть инфекция), и возникающая в результате гиперцитокинемия. 3 н. и 20 з.п. ф-лы, 1 ил.
1. Способ лечения, облегчения или профилактики гиперцитокинемии у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики гиперцитокинемии, где соединение, стабилизирующее тучные клетки, представляет собой норкетотифен или его фармацевтически приемлемую соль.
2. Способ по п.1, где гиперцитокинемия обусловлена заболеванием, нарушением или состоянием у субъекта.
3. Способ по п. 2, где заболевание, нарушение или состояние не является астмой, конъюнктивитом или мастоцитозом.
4. Способ по п. 2 или 3, где заболевание, нарушение или состояние представляет собой вирусную инфекцию.
5. Способ по п. 4, где вирусная инфекция представляет собой вирусную инфекцию гриппа.
6. Способ по любому из пп. 2-5, дополнительно включающий введение субъекту дополнительного терапевтического средства от заболевания, нарушения или состояния.
7. Способ по п.6, где дополнительное терапевтическое средство представляет собой противовирусное средство.
8. Способ по п.7, где дополнительное терапевтическое средство представляет собой противогриппозное средство.
9. Способ по п.8, где противогриппозное средство представляет собой осельтамивир.
10. Способ лечения, облегчения или профилактики нарушения, связанного с гиперцитокинемией, у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики нарушения, где соединение, стабилизирующее тучные клетки, представляет собой норкетотифен или его фармацевтически приемлемую соль.
11. Способ по п. 10, где нарушение представляет собой вирусную инфекцию, гриппоподобное заболевание, синдром системной воспалительной реакции или сепсис.
12. Способ по п. 11, где вирусная инфекция представляет собой вирусную инфекцию гриппа.
13. Способ по любому из пп.10-12, дополнительно включающий введение субъекту дополнительного терапевтического средства.
14. Способ по п. 13, где дополнительное терапевтическое средство представляет собой противовирусное средство.
15. Способ по п. 14, где дополнительное терапевтическое средство представляет собой противогриппозное средство.
16. Способ по п. 15, где противогриппозное средство представляет собой осельтамивир.
17. Способ лечения, облегчения или профилактики лихорадки у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного или профилактически эффективного количества соединения, стабилизирующего тучные клетки, таким образом, для лечения, облегчения или профилактики лихорадки, где соединение, стабилизирующее тучные клетки, представляет собой норкетотифен или его фармацевтически приемлемую соль.
18. Способ по п. 17, дополнительно включающий введение субъекту дополнительного терапевтического средства.
19. Способ по п. 18, где дополнительное терапевтическое средство представляет собой жаропонижающее средство.
20. Способ по любому из пп. 6-9, 13-16, 18 или 19, где соединение, стабилизирующее тучные клетки, и дополнительное терапевтическое средство вводят в одной и той же композиции.
21. Способ по любому из пп. 6-9, 13-16, 18 или 19, где соединение, стабилизирующее тучные клетки, и дополнительное терапевтическое средство вводят в отдельных композициях.
22. Способ по любому из пп. 1-21, дополнительно включающий физический метод лечения субъекта.
23. Способ по п. 22, где физический метод лечения представляет собой хирургическое вмешательство, трансплантацию, плазмаферез, модуляцию температуры или любую их комбинацию.
| GRAHAM C | |||
| AMY et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| GRAHAM C | |||
| AMY et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| US 6207684 B1, 27.03.2001 | |||
| US 6207684 B1, | |||
Авторы
Даты
2021-11-29—Публикация
2017-09-07—Подача