Изобретение относится к области медицины, в частности к пульмонологии, и может быть использовано для оценки вероятности формирования хронических заболеваний легких у детей в исходе бронхолегочной дисплазии (БЛД).
Известен способ оценки исходов БЛД посредством ультразвукового исследования легких [Клиническое значение ультразвукового исследования легких в прогнозировании исходов бронхолегочной дисплазии / И.Е. Колтунов, А.В. Горбунов, М.В. Дегтярева, О.Ф. Выхристюк, А.В. Ерохина // Педиатрия. – 2019. – Т. 98, №2. – С. 88–93]. Способ позволяет оценить исходы БЛД в неонатальном периоде (тяжесть течения заболевания, риск развития летального исхода) на основании визуализации изменений легочной ткани при ультразвуковом исследовании (ателектазы, в том числе повторные, обширные зоны уплотнения легочной ткани, интерстициальная легочная эмфизема). Достоинством данного способа является возможность оценки объема поражения легочной ткани у тяжелых нетранспортабельных пациентов, а также отсутствие лучевой нагрузки. Недостатками данного способа являются необходимость обучения врачей функциональной диагностики, отсутствие возможности оценить долгосрочные респираторные последствия БЛД.
Предложен способ (№ 2480753 C1, 27.04.2013, RU), позволяющий оценивать тяжести течения бронхолегочной дисплазии на фоне гастроэзофагеального рефлюкса у новорожденных детей, находящихся на искусственной вентиляции легких. В качестве прогностического критерия используют активность пепсина, выделяемого из трахеобронхиального аспирата. Достоинством способа является ранняя диагностика гастроэзофагеального рефлюкса и своевременное проведение лечения, что снижает риск развития хронической бронхолегочной патологии и инвалидизации. Недостатками способа является необходимость инвазивного вмешательства для забора трахеобронхиального аспирата, катамнез охватывает только первый год жизни ребенка, когда отмечается течение БЛД и говорить о респираторных последствиях заболевания не правомочно, прогнозирование исходов БЛД без учета данных о течении заболевания на амбулаторном этапе.
Известен способ диагностики исходов БЛД в составе программы для ЭВМ RU 2018611614, 02.02.2018. Заложенная в основе программы нейронная сеть обрабатывает три блока вводных параметров: состояние здоровья матери, анамнез, течение беременности и родов (30 показателей); состояние здоровья новорожденного ребенка (15 показателей); социально-бытовые условия семьи (5 показателей). По результатам анализа программа оценивает вероятность развития церебральной лейкомаляции, внутричерепных кровоизлияний, гидроцефалии, некротизирующего энтероколита, бронхолегочной дисплазии, ретинопатии недоношенных в периоде новорожденности, а также прогнозирует исход (частичное или полное выздоровление, летальный исход). Недостатком данного способа является большой объем данных на входе нейронной сети, прогнозирование исходов БЛД без учета данных о течении заболевания на амбулаторном этапе.
Наиболее близким к предлагаемому способу является способ, описанный Ю.В. Сороколатом [Сороколат Ю.В. Способы прогноза течения бронхолегочной дисплазии у детей в возрасте года / Ю.В. Сороколат // ScienceRise. – 2015. – Т. 12, №3(17). – С. 56-59]. На основании проспективного анализа особенностей течения БЛД у детей с периода новорожденности до трех лет определены предикторы повозрастного течения и исходов заболевания. Для каждого из предикторов установлены прогностические коэффициенты и прогностическая информативность градации показателей. Данными предикторами являются тяжесть БЛД и характер клинического течения заболевания в первые 6 месяцев жизни, пол больного, анамнестические данные (длительность интенсивной терапии, лечение сурфактантом, гестационная зрелость и оценка по шкале Апгар), учитывается сопутствующая патология.
Данный способ принимается за прототип. Недостаток прототипа: применение данного алгоритма прогноза динамики течения БЛД возможно у детей не старше 1 года жизни (оптимально – 6 и 12 месяцы жизни).
Задача - разработка прогностической модели для оценки респираторных последствий БЛД у детей старше 3 лет.
Бронхолегочная дисплазия (БЛД) является многофакторным заболеванием, в патогенезе которого доказана роль окислительного стресса. Частота БЛД в настоящее время остается высокой вследствие совершенствования методик выхаживания недоношенных новорожденных. Формирование БЛД и ее последующая трансформация в старшем возрасте в хроническую патологию органов дыхания существенно снижает качество жизни детей, что требует совершенствования походов к лечению заболевания и профилактике его исходов.
Респираторные последствия БЛД оцениваются при достижении больным возраста 3 лет. По мере роста ребенка может наступать клиническое выздоровление, однако у значительной доли больных диагностируются заболевания органов дыхания, такие как рецидивирующий бронхит, хронический бронхит, облитерирующий бронхиолит, бронхиальная астма, эмфизема легких, пневмосклероз или бронхоэктазы [Овсянников Д.Ю. Бронхолегочная дисплазия: естественное развитие, исходы и контроль [текст] / Д.Ю. Овсянников // Педиатрия. – 2011. – Т. 90, №1. – С. 141-150]. Объективные критерии, позволяющие с высокой вероятностью предсказать риск развития того или иного клинического исхода, в настоящее время отсутствуют. Разработка способа прогнозирования респираторных последствий БЛД позволить персонифицировать программу диспансерного наблюдения детей, страдающих БЛД, и своевременно проводить превентивное лечение, направленное на уменьшение риска неблагоприятного исхода.
В основу способа положены результаты ретроспективного исследования данных катамнеза и одномоментной оценки текущего состояния респираторного здоровья 60 детей в возрасте от 3 до 17 лет (медиана 5,0 лет, нижний квартиль 4,0 года, верхний – 6,0 лет), перенесших БЛД.
При диспансерном осмотре детей с БЛД для формирования прогноза исхода заболевания учитывается пол больного, оцениваются такие данные анамнеза как характер респираторной поддержки в периоде новорожденности, объем, длительность и регулярность медикаментозной терапии на этапе реанимации и на амбулаторном этапе, наследственный анамнез по заболеваниям органов дыхания. Дополнительно оценивается концентрация глутатиона (окисленного или восстановленного) в сыворотке крови.
Положительными прогностическими характеристиками обладают такие параметры как мужской пол, неинвазивная вентиляция легких методом постоянного положительного давления через носовые канюли, терапия ингаляционными глюкокортикостероидами на этапе реанимации и/или амбулаторно.
Снижают вероятность благоприятного исхода женский пол, искусственная вентиляция легких, отягощенная наследственность по атопии и патологии легких, а также концентрация глутатиона выше 10 перцентиля.
Указанные предикторы подвергаются бинарному кодированию, присваиваются значения коэффициентов при указанных предикторах согласно Фиг. 1. Характеристика предикторов благоприятного исхода БЛД.
Далее вычисляется сумма векторов предикторов x
x = 1,06A-1,27B+1,44C+0,67D-0,79E-0,60F
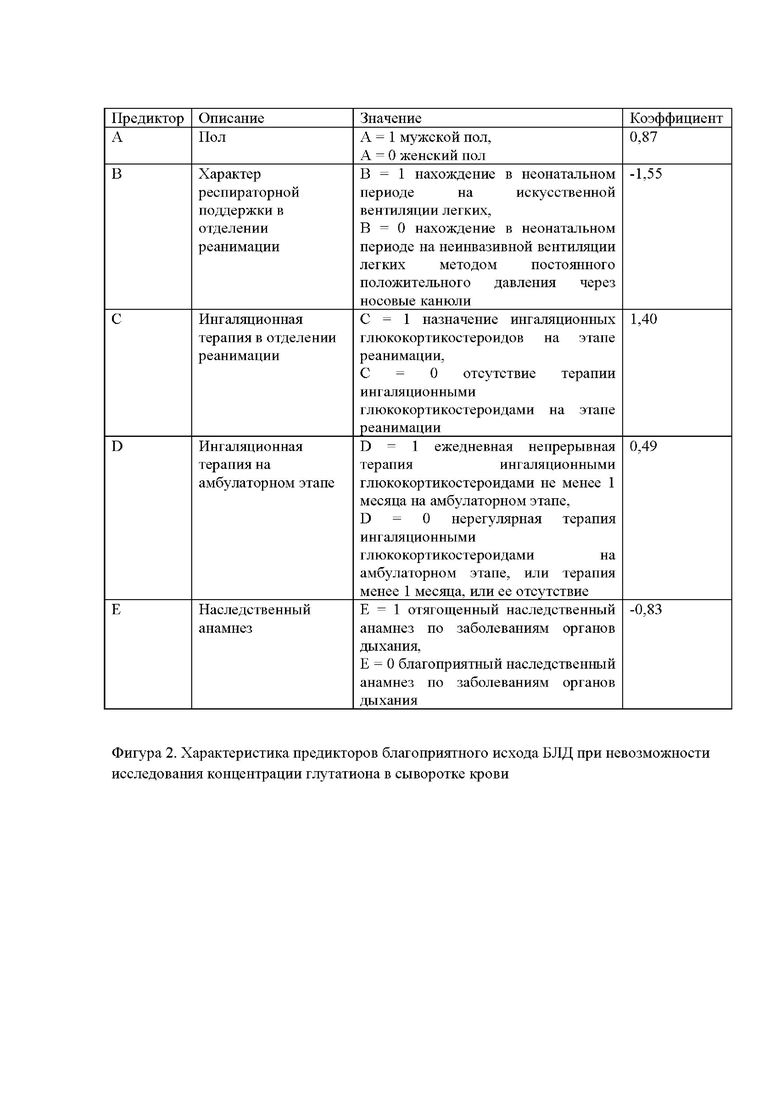
При отсутствии технической возможности оценить концентрацию глутатиона в сыворотке крови используются значения коэффициентов при предикторах согласно Фиг. 2. Характеристика предикторов благоприятного исхода БЛД при невозможности исследования концентрации глутатиона в сыворотке крови.
В данной ситуации сумма векторов предикторов x
x = 0,87A-1,55B+1,40C+0,49D-0,83E
Далее определяется вероятность благоприятного исхода Y (%) по формуле
Y = (1 / (1+e-x))*100%
где e - основание натурального логарифма, x – сумма векторов предикторов.
С целью оптимизации практического применения способа расчеты выполняют с помощью компьютерной программы, осуществляющей вычисления и размещенной на машиночитаемом носителе.
Как показывают расчеты, у детей в случае развития хронической патологии легких после перенесенной БЛД медиана вероятности выздоровления составляет 32%, в группе пациентов с клиническим выздоровлением – 54%. Исходя из вышеизложенного, в группу высокого риска формирования хронической патологии органов дыхания в исходе БЛД следует относить детей со значением Y≤50%, однако необходимо учитывать, что данный метод является скрининговым и может применяться в качестве вспомогательного средства при принятии решений о тактике диспансерного наблюдения детей с БЛД.
Качество разработанной математической модели отражает ROC-кривая, площадь под которой составляет 0,74, что свидетельствует о «хорошем» качестве полученной математической модели. Чувствительность предложенного метода комплексной оценки респираторных последствий БЛД у детей старшего возраста составляет 71,8%, специфичность – 57,1%.
Разработанный способ повышает точность диагностики респираторных последствий БЛД у детей старше 3 лет.
Клинический пример №1
Мальчик К., 7 лет. Рожден на сроке гестации 26 недель с массой 660 г. В связи с клиническими проявлениями респираторного дистресс-синдрома находился на искусственной вентиляции легких 39 дней, на протяжении 76 дней нуждался в дополнительной подаче кислорода. Выставлен диагноз бронхолегочной дисплазии средней степени тяжести. Терапия ингаляционными стероидами начата на этапе реанимации, продолжена амбулаторно регулярно; суммарная длительность терапии 6 месяцев. Эпизоды острых респираторных заболеваний 2-3 раза в год, без явлений бронхиальной обструкции. Проявлений бронхиальной гиперреактивности нет. Отягощена наследственность по атопическим заболеваниям – у матери аллергический ринит. При лабораторном обследовании уровень восстановленного глутатиона составил 0,916 мкмоль/л, что было менее 10 перцентиля.
По результатам комплексного обследования выставлен диагноз - Клиническое выздоровление. БЛД в анамнезе.
Вероятность формирования хронической патологии органов дыхания в исходе БЛД с учетом заявленных значений предикторов составила 24,8%, что свидетельствовало о низком риске развития хронической патологии органов дыхания в исходе БЛД у данного больного.
Клинический пример №2
Девочка К., 3 года. Рождена на сроке гестации 28 недель с массой 894 г. В связи с клиническими проявлениями респираторного дистресс-синдрома находилась на искусственной вентиляции легких 11 дней, на протяжении 41 дня нуждалась в дополнительной подаче кислорода. Выставлен диагноз бронхолегочной дисплазии легкой степени тяжести. Терапия ингаляционными стероидами проводилась на этапе реанимации, прекращена при снятии с искусственной вентиляции легких, амбулаторно назначалась трижды после эпизодов обострения БЛД, длительностью 10-14 дней. Эпизоды острых респираторных заболеваний 4-6 раз в год, с оральными хрипами, иногда отмечается участие вспомогательной мускулатуры. Мокроту откашливает плохо, эпизоды закашливания. Отягощена наследственность по атопическим заболеваниям – у старшей сестры аллергический ринит, у отца поллиноз. При лабораторном обследовании уровень окисленного глутатиона составил 6,036 мкмоль/л, что было более 10 перцентиля.
По результатам комплексного обследования выставлен диагноз - Рецидивирующий бронхит. БЛД в анамнезе.
Вероятность формирования хронической патологии органов дыхания в исходе БЛД с учетом заявленных значений предикторов составила 77,2%, что свидетельствовало о высоком риске развития хронической патологии органов дыхания в исходе БЛД у данного больного.
Вывод. Таким образом, применение предложенного способа позволяет выделять группу высокого риска формирования хронической патологии органов дыхания в исходе БЛД, однако необходимо учитывать, что данный метод является скрининговым. Данный способ может применяться в качестве вспомогательного средства при принятии решений о тактике диспансерного наблюдения детей с БЛД.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У НОВОРОЖДЕННЫХ С ОЧЕНЬ НИЗКОЙ И ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА ПРИ РОЖДЕНИИ | 2009 |
|
RU2416388C1 |
| СПОСОБ ПРОФИЛАКТИКИ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У НОВОРОЖДЕННЫХ С ОЧЕНЬ НИЗКОЙ И ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА ПРИ РОЖДЕНИИ | 2012 |
|
RU2504395C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДОВ ВРОЖДЕННОЙ ПНЕВМОНИИ У ГЛУБОКОНЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ | 2013 |
|
RU2543343C1 |
| СПОСОБ КОМПЛЕКСНОЙ МЕДИКАМЕНТОЗНОЙ ПРОФИЛАКТИКИ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ | 2010 |
|
RU2432953C1 |
| СПОСОБ ОЦЕНКИ СТЕПЕНИ ТЯЖЕСТИ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ | 2008 |
|
RU2401066C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У ДЕТЕЙ С ВРОЖДЕННОЙ ПНЕВМОНИЕЙ | 2010 |
|
RU2439569C1 |
| Способ прогнозирования развития бронхолегочной дисплазии (БЛД) у недоношенных новорожденных | 2024 |
|
RU2840880C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ ТЯЖЕЛОЙ СТЕПЕНИ У НЕДОНОШЕННЫХ ДЕТЕЙ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА В НЕОНАТАЛЬНОМ ПЕРИОДЕ | 2017 |
|
RU2649830C1 |
| Способ прогнозирования риска прогрессирования очагового пневмофиброза у детей с хроническими неспецифическими заболеваниями легких | 2023 |
|
RU2816053C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ БРОНХОЛЕГОЧНОЙ ДИСПЛАЗИИ У НЕДОНОШЕННЫХ ДЕТЕЙ С ЭКСТРЕМАЛЬНО НИЗКОЙ МАССОЙ ТЕЛА ПРИ РОЖДЕНИИ | 2012 |
|
RU2514013C2 |

Изобретение относится к области медицины, а именно к пульмонологии, и может быть использовано для прогнозирования респираторных последствий бронхолегочной дисплазии у детей старше 3 лет. Проводят оценку таких анамнестических данных как пол больного и характер респираторной поддержки. Дополнительно учитывают проводимую терапию ингаляционными стероидами на этапе отделения реанимации и амбулаторно, наследственный анамнез по атопическим заболеваниям органов дыхания и определяют концентрацию глутатиона в сыворотке крови. На основании совокупности полученных данных устанавливают вероятность формирования хронической патологии органов дыхания в исходе бронхолегочной дисплазии Y по формуле Y = 100% - (1 / (1+e-x))*100%, где е – основание натурального логарифма, x – сумма векторов предикторов, равная 1,06А-1,27В+1,44С+0,67D-0,79Е-0,60F, где A – пол ребенка: мужской пол – 1 балл, женский пол – 0 баллов; B – характер респираторной поддержки в отделении реанимации: нахождение в неонатальном периоде на искусственной вентиляции легких – 1 балл, нахождение в неонатальном периоде на неинвазивной вентиляции легких методом постоянного положительного давления через носовые канюли – 0 баллов; C - ингаляционная терапия в отделении реанимации: назначение ингаляционных глюкокортикостероидов на этапе реанимации – 1 балл; отсутствие терапии ингаляционными глюкокортикостероидами на этапе реанимации – 0 баллов; D - ингаляционная терапия на амбулаторном этапе: ежедневная непрерывная терапия ингаляционными глюкокортикостероидами не менее 1 месяца на амбулаторном этапе – 1 балл; нерегулярная терапия ингаляционными глюкокортикостероидами на амбулаторном этапе, или терапия менее 1 месяца, или ее отсутствие – 0 баллов; E - наследственный анамнез по атопическим заболеваниям органов дыхания: отягощенный наследственный анамнез по атопическим заболеваниям органов дыхания – 1 балл, благоприятный наследственный анамнез по атопическим заболеваниям органов дыхания – 0 баллов; F - концентрация глутатиона в сыворотке крови: концентрация окисленного глутатиона выше 2,0 мкмоль/л и/или концентрация восстановленного глутатиона выше 4,0 мкмоль/л – 1 балл, концентрация окисленного глутатиона ниже 2,0 мкмоль/л и/или концентрация восстановленного глутатиона ниже 4,0 мкмоль/л – 0 баллов. При значении Y больше или равном 50% у ребенка прогнозируют риск формирования хронической патологии органов дыхания в исходе бронхолегочной дисплазии. Способ обеспечивает повышение точности прогноза респираторных последствий бронхолегочной дисплазии у детей старше 3 лет за счет комплексной оценки данных катамнеза и одномоментной оценки текущего состояния респираторного здоровья детей, перенесших бронхолегочную дисплазию. 2 ил., 2 пр.
Способ прогнозирования респираторных последствий бронхолегочной дисплазии у детей старше 3 лет, включающий оценку таких анамнестических данных как пол больного и характер респираторной поддержки, отличающийся тем, что дополнительно учитывают проводимую терапию ингаляционными стероидами на этапе отделения реанимации и амбулаторно, наследственный анамнез по атопическим заболеваниям органов дыхания и определяют концентрацию глутатиона в сыворотке крови, далее на основании совокупности полученных данных устанавливают вероятность формирования хронической патологии органов дыхания в исходе бронхолегочной дисплазии Y по формуле Y = 100% - (1 / (1+e-x))*100%, где e – основание натурального логарифма, x – сумма векторов предикторов, равная 1,06A-1,27B+1,44C+0,67D-0,79E-0,60F, где
A - пол ребенка: мужской пол – 1 балл, женский пол – 0 баллов;
B - характер респираторной поддержки в отделении реанимации: нахождение в неонатальном периоде на искусственной вентиляции легких – 1 балл, нахождение в неонатальном периоде на неинвазивной вентиляции легких методом постоянного положительного давления через носовые канюли – 0 баллов;
C - ингаляционная терапия в отделении реанимации: назначение ингаляционных глюкокортикостероидов на этапе реанимации – 1 балл; отсутствие терапии ингаляционными глюкокортикостероидами на этапе реанимации – 0 баллов;
D - ингаляционная терапия на амбулаторном этапе: ежедневная непрерывная терапия ингаляционными глюкокортикостероидами не менее 1 месяца на амбулаторном этапе – 1 балл; нерегулярная терапия ингаляционными глюкокортикостероидами на амбулаторном этапе, или терапия менее 1 месяца, или ее отсутствие – 0 баллов;
E - наследственный анамнез по атопическим заболеваниям органов дыхания: отягощенный наследственный анамнез по атопическим заболеваниям органов дыхания – 1 балл, благоприятный наследственный анамнез по атопическим заболеваниям органов дыхания – 0 баллов;
F - концентрация глутатиона в сыворотке крови: концентрация окисленного глутатиона выше 2,0 мкмоль/л и/или концентрация восстановленного глутатиона выше 4,0 мкмоль/л – 1 балл, концентрация окисленного глутатиона ниже 2,0 мкмоль/л и/или концентрация восстановленного глутатиона ниже 4,0 мкмоль/л – 0 баллов;
причем при значении Y больше или равном 50% у ребенка прогнозируют риск формирования хронической патологии органов дыхания в исходе бронхолегочной дисплазии.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ФОРМИРОВАНИЯ БРОНХОЛЕГОЧНОЙ ПАТОЛОГИИ У ДЕТЕЙ, НАХОДИВШИХСЯ НА ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЕГКИХ В НЕОНАТАЛЬНОМ ПЕРИОДЕ | 2013 |
|
RU2531346C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРОГРЕССИРОВАНИЯ ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2008 |
|
RU2382597C1 |
| КУРМАШЕВА Е.И | |||
| Персонифицированная диагностика заболеваний органов дыхания у детей, рожденных недоношенными, и стратификация риска нежелательных исходов | |||
| Автореф | |||
| диссер | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| ПАВЛИНОВА Е.Д | |||
| и др | |||
| Отдаленные респираторные последствия заболеваний органов дыхания, возникших в | |||
Авторы
Даты
2022-04-18—Публикация
2020-12-01—Подача