Область применения изобретения
Настоящее изобретение относится к дозированной форме пастилки. Настоящее изобретение также относится к способу получения дозированной формы пастилки и способам ослабления симптомов у человека при введении дозированной формы пастилки. Дозированная форма пастилки, которая может содержать один или более терапевтически активных агентов, особенно полезна при лечении симптомов кашля и простуды, включая, помимо прочего, кашель, заложенность носа и боль в горле.
Предпосылки создания изобретения
Лекарственные препараты, предназначенные для перорального приема, обычно поставляются в твердой форме в виде таблеток, капсул, пилюль, карамелей или гранул. Как правило, быстро распадающиеся таблетки используются для введения лекарственных средств в тех случаях, когда использование таблетки для проглатывания целиком нецелесообразно, например, для детей. Исследованием быстро распадающихся таблеток занималось несколько специалистов в данной области (см., например, патенты США № 6106861 и 6024981 и заявка PCT № WO 99/47126).
Описана двухкомпонентная дозированная форма, сочетающая в себе применение быстро распадающейся таблетки, содержащей фармацевтически активный агент с более медленно распадающейся леденцовой оболочкой. Дозированная форма обеспечивает как преимущество быстрой доставки фармацевтически активного агента, содержащегося в части быстро распадающейся таблетки, так и преимущество более медленного распада части леденцовой оболочки, которая может содержать второй фармацевтически активный агент.
Дозированную форму, составляющую предмет настоящего изобретения, можно применять для лечения, например, боли в горле, которая характеризуется ощущением боли или раздражения горла или глотки, как правило, вызванного острым фарингитом. Боль в горле чаще всего вызвана вирусной инфекцией. Боль в горле также может быть вызвана стрептококковой инфекцией, опухолями, гастроэзофагеальным рефлюксным заболеванием, мононуклеозом и аллергиями.
Боль в горле может развиваться по многим причинам, включая вирусную или бактериальную инфекцию, или общую или сезонную аллергию. Часто связанная с инфекцией обычная или сезонная аллергия включает некоторую степень заложенности носа или пазух. Эта заложенность, как правило, относится к стеканию слизи из носоглотки, при этом слизь, образующаяся на поверхности слизистой оболочки носа или слизистой оболочки пазух, стекает в верхнюю часть пищевода. Накопление носовой слизи в верхней части пищевода также стимулирует глотательный рефлекс, часто связанный с болью в горле. Глотательный рефлекс приводит кислую слизь в относительно постоянный контакт с областью горла. Кислотный характер слизи слизистой оболочки пазух или слизистой оболочки полости носа разъедает эпителиальную ткань горла, таким образом подвергая нижележащую ткань воздействию кислой слизи. Нервные окончания в расположенной ниже ткани, контактирующие с кислой слизью, вызывают то, что идентифицируют как дискомфорт или боль, связанную с болью в горле. Чем сильнее воспалена слизистая оболочка носа или слизистая оболочка носовых пазух, тем больше образуется кислой слизи, тем больше эрозия и тем сильнее боль и дискомфорт, связанные с болью в горле.
Боль в горле можно лечить различными дозированными формами или средствами. Обычные дозированные формы включают спреи для горла, пастилки и таблетки или жидкости, вводимые перорально, причем все они могут содержать активные ингредиенты. Спреи и пастилки, как правило, содержат местные анальгетики или ментол для облегчения боли в горле. Таблетки или жидкости, вводимые перорально, как правило, содержат системно действующие активные ингредиенты от боли, кашля и/или простуды; включая, например, ацетаминофен, НПВС, противозастойные средства и/или средства от кашля. В некоторых случаях данные продукты содержат вещества, создающие ощущение прохлады, которые также способствуют облегчению боли или приданию ощущения облегчения боли.
Одним из основных недостатков таких продуктов является отсутствие немедленного эффекта и/или короткая продолжительность действия. Во многих случаях спреи или жидкости не обеспечивают дополнительное облегчение боли, поскольку композицию глотают почти сразу же при введении.
Сохраняется потребность в композициях и способах, которые безопасны и эффективны для лечения, ослабления или уменьшения тяжести боли в горле. Такая композиция должна работать быстро и обеспечивать превосходное облегчение боли в горле в течение продолжительного периода времени.
В патенте США № 4260596 описана съедобная дозированная форма, имеющая внешнюю оболочку и жидкую или гелевую сердцевину, которая может содержать терапевтически эффективное количество лекарственного средства.
В патенте США № 4517205 описан соосажденный двухкомпонентный леденец, имеющий часть карамельной оболочки и сердцевину, которая может быть мягкой, а также способ изготовления такого леденца.
В патенте США № 5302394 описан способ изготовления лекарственных леденцов из декстрометорфана в непрерывной системе.
В патентах США № 5549906, 5662920, и 6280761 описана никотиновая пастилка для прекращения курения.
В патенте США № 5614207 описана пастилка против сухости рта, содержащая основу пастилки, смягчающее средство, увлажнитель и фармацевтически приемлемый подкислитель для стимулирования слюноотделения.
В патенте США № 5616340 описана пастилка на основе леденца, содержащая антацид, полученная способом, совместимым с непрерывным способом производства.
В патенте США № 5871781 описано устройство для изготовления съедобных единиц, которые могут содержать активные компоненты и способны растворяться во рту в течение нескольких секунд.
В опубликованной заявке на патент США № 20050019376 описана дозированная форма, содержащая по меньшей мере один активный ингредиент, кондитерскую композицию и по меньшей мере одну грань, причем относительное стандартное отклонение массы дозированной формы составляет менее 1%.
В опубликованной заявке на патент США № 20050142199 описана фармацевтическая дозированная форма, содержащая сердцевину таблетки, содержащую фармацевтически активный ингредиент, и покрытие, покрывающее по меньшей мере 25% площади поверхности сердцевины таблетки, причем покрытие образуется в результате осаждения порошка, содержащего плавкие частицы, и сплавления частиц с образованием покрывающей пленки.
В опубликованной заявке на патент США № 20050238695 описана органолептически привлекательная пастилка.
В опубликованной заявке на патент США № 20070087053 описана многокомпонентная композиция для лечения сухости рта, которая содержит первую часть, которая быстро распадается в полости рта и высвобождает соединение, стимулирующее слюноотделение, в комбинации с буферной системой на основе шипучей органической кислоты, и вторую часть, которая высвобождает в полость рта смягчающее средство в течение нескольких минут.
В опубликованной заявке на патент США № 2008286340 описан оральный состав, содержащий никотин и по меньшей мере одну аминокислоту в количестве, эффективном для буферизации состава.
В опубликованной заявке на патент США № 20090004248 описана дозированная форма, содержащая как часть распадающейся таблетки, так и леденцовую часть, причем: (i) часть распадающейся таблетки содержит по меньшей мере один фармацевтически активный агент, а (ii) леденцовая часть покрывает по меньшей мере 20% поверхности части распадающейся таблетки, и при этом время распадаемости леденцовой части по меньшей мере в десять раз больше времени распадаемости части распадающейся таблетки. В ссылке описано изготовление дозированной формы, которая содержит леденцовую часть и часть распадающейся таблетки, включающее помещение прессованной таблетки в форму, которая покрывает грани таблетки, и впрыскивание текучей леденцовой смеси для окружения поверхности таблетки. В ссылке также описано получение дозированной формы, содержащей два слоя, которое включает помещение прессованной таблетки плоской гранью на поверхность леденца, содержащего ПЭГ 3350; и нагревание полученной дозированной формы таким образом, что ПЭГ 3350 плавится и создает адгезию между поверхностями таблетки и леденца.
В опубликованной заявке на патент США № 20090011079 раскрыто кондитерское изделие с твердым покрытием, имеющее потребляемую, мягкую, обогащенную, жевательную сердцевину с высоким содержанием сухих веществ, инкапсулированную в твердом потребляемом покрытии, и способ изготовления обогащенного кондитерского изделия.
В опубликованной заявке на патент США № 20100124560 описана многокомпонентная интраоральная дозированная форма, в состав которой входит по меньшей мере один быстро распадающийся компонент и по меньшей мере один медленно распадающийся компонент, причем время распадаемости медленно распадающегося компонента по меньшей мере в два раза превышает время распадаемости быстро распадающегося компонента. В ссылке описано изготовление двухкомпонентной дозированной формы, которое включает прессование двух частей смешанного материала в таблетки с помощью прямого прессования. В ссылке также описано изготовление двухкомпонентной дозированной формы, которое включает дозирование расплавленной части таблетки поверх охлажденной леденцовой части.
В опубликованных заявках на патенты США № WO2013103318 и 20160095818 описаны фармацевтические дозированные формы, которые содержат сердцевину, покрытую по меньшей мере одним пленочным покрытием. Сердцевина содержит по меньшей мере один АФИ, причем одно или более органолептически неприятное ощущение активного фармацевтического ингредиента (АФИ) снижают за счет компонентов пленочного покрытия.
В заявке на патент США № 8865204 раскрыта пастилка, полученная способом, который включает формирование порошковой смеси, содержащей аморфный углеводный полимер, в желаемую форму и приложение радиочастотной энергии к форме в течение достаточного периода времени для размягчения или расплавления аморфного углеводного полимера для сплавления формы с образованием пастилки.
Сохраняется потребность в получении дозированной формы пастилки и эффективном, коммерчески доступном способе получения такой дозированной формы.
Целью настоящего изобретения является обеспечение эффективного способа получения двухкомпонентной дозированной формы, который легко адаптируется к коммерческому производству.
Дозированную форму можно изготовить на коммерческом производственном уровне, имеющую часть сердцевины, которая отличается от части оболочки по функции, и, при необходимости, по текстуре, аромату и оптическим характеристикам, таким как цвет и светопередача. Более того, настоящее изобретение позволяет специалистам–практикам удобно включать активный ингредиент в привлекательный, органолептически приятный, леденцовый кондитерский продукт.
Изложение сущности изобретения
Данное изобретение относится к дозированной форме, которая содержит как часть распадающейся таблетки, так и часть леденцовой оболочки.
Прочие отличительные особенности и преимущества настоящего изобретения будут понятны из подробного описания изобретения и формулы изобретения.
Краткое описание графических материалов
На Фиг. 1–8 представлены фотографии дозированных форм, изготовленных в соответствии с данным изобретением.
Подробное описание изобретения
Считается, что специалист в данной области, основываясь на представленном в настоящем документе описании, сможет использовать настоящее изобретение в самом полном объеме. Представленные ниже конкретные варианты осуществления следует рассматривать исключительно как иллюстративные, которые ни в коей мере не ограничивают остальную часть описания.
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют общепринятое значение, понятное любому обычному специалисту в данной области, к которой относится настоящее изобретение. Кроме того, все публикации, заявки на патенты, патенты и другие материалы, упомянутые в настоящем документе, включены в настоящий документ путем ссылки. В настоящем документе все процентные значения представляют собой весовое процентное содержание, если не указано иное. Кроме того, все указанные в настоящем документе диапазоны предполагают включение любых комбинаций значений между двумя конечными значениями включительно.
В настоящем документе термин «активный», «активный агент» или «активный ингредиент» используется в широком смысле и может охватывать любой материал, который обеспечивает терапевтический эффект. Например, активный агент или активный ингредиент может представлять собой фармацевтический препарат, нутрицевтический препарат, витамин, диетическую добавку, питательное вещество, лекарственную траву, продукт питания, диетический продукт, пищевую, минеральную, добавку, агент для ухода за полостью рта или ароматизатор (создающее ощущение вещество) или т.п., а также их комбинации.
«Дозированная форма» относится к любой композиции, предназначенной для содержания конкретного заранее определенного количества (дозы) определенного ингредиента и, например, активного ингредиента, как определено в настоящем документе. Подходящими дозированными формами могут быть фармацевтические системы доставки лекарственных средств и системы для доставки минеральных веществ, витаминов и других питательных веществ, агентов для ухода за полостью рта, ароматизаторов и т.п. В особенно предпочтительном варианте осуществления дозированная форма представляет собой систему доставки фармацевтически активного ингредиента для перорально введения в желудочно–кишечный тракт человека.
«Быстрый распад»: В одном варианте осуществления часть быстро распадающейся таблетки соответствует критериям таблетки для рассасывания в полости рта (ODTS), определенном в Руководстве Управления по контролю за качеством пищевых продуктов и медикаментов, декабрь 2008 года. В одном варианте осуществления часть быстро распадающейся таблетки соответствует двойному определению таблеток для рассасывания в полости рта, включая следующие критерии: 1) твердая таблетка – это таблетка, которая содержит медицинские вещества и которая быстро, как правило, в течение нескольких секунд, распадается при помещении на язык, а также 2) может рассматриваться как твердая композиция для перорального применения, которая быстро распадается в полости рта, и время ее распадения in vitro составляет приблизительно 30 секунд или менее на основе результатов теста на распадение, указанного в Фармакопее США (USP 24 NF 29) для конкретного медицинского вещества или веществ.
Термин «терапевтический эффект» означает любой эффект или действие активного ингредиента, предназначенное для диагностики, лечения, излечения, облегчения или предотвращения заболевания, либо воздействие на структуру или любую функцию тела.
Соответствующие вещества, создающие ощущения, которые могут быть использованы в настоящем изобретении, включают ментол, ароматизаторы мяты и мяты перечной, фруктовые ароматизаторы, шоколад, ваниль, ароматизаторы жевательной резинки, кофейные ароматизаторы, ликерные ароматизаторы и комбинации вышеуказанного и т.п.
Терапевтически эффективное количество активного ингредиента или ингредиентов может быть легко определено специалистом в данной области техники.
Часть распадающейся таблетки
Дозированная форма, составляющая предмет настоящего изобретения, содержит часть распадающейся таблетки. Часть распадающейся таблетки содержит один или более фармацевтически активных агентов и необязательно содержит один или более прессуемых эксципиентов, эксципиентов, набухающих при контакте с водой, шипучих пар и других ингредиентов.
В одном варианте осуществления часть распадающейся таблетки выполнена с возможностью растворения в полости рта после ее помещения на язык в течение менее приблизительно 60 секунд, например менее приблизительно 45 секунд, например менее приблизительно 30 секунд, например менее приблизительно 15 секунд.
Прессуемый эксципиент
В одном варианте осуществления часть распадающейся таблетки также содержит один или более прессуемых эксципиентов. Термин «прессуемый эксципиент» обозначает ингредиент, который может быть спрессован в таблетку без добавления других связующих веществ. В одном варианте осуществления прессуемый эксципиент может присутствовать в форме гидрата и может быть выбран из числа органических соединений, таких как моногидрат декстрозы, мальтодекстрин, моногидрат лактозы и декстрин, а также из числа неорганических соединений, таких как дигидрат двухосновного фосфата кальция, дигидрат двухосновного фосфата натрия, гептагидрат двухосновного фосфата натрия, додекагидрат двухосновного фосфата натрия, моногидрат одноосновного фосфата натрия и дигидрат одноосновного фосфата натрия. В одном из вариантов осуществления часть распадающейся таблетки содержит прессуемый эксципиент, выбранный из группы, в состав которой входят: изомальт, моногидрат декстрозы, мальтодекстрин, моногидрат лактозы, декстрин, маннит, мальтит, лактит, сорбит, ксилит, эритрит, сахароза и лактоза. В одном варианте осуществления часть распадающейся таблетки включает полиглицитол, смесь, состоящую, главным образом, из мальтита и сорбита и меньших количеств гидрогенизированных олигонуклеотидов и полисахаридов и мальтротиита. Полиглицитол также известен как гидрогенизированный гидролизат крахмала.
Эксципиент, набухающий при контакте с водой
В одном из вариантов осуществления часть распадающейся таблетки также содержит один или более эксципиентов, набухающих при контакте с водой. Термин «эксципиент, набухающий при контакте с водой» обозначает материал, который набухает или впитывает жидкость при контакте с жидкой средой и таким образом способствует распадению спрессованной таблетки. Эксципиент, набухающий при контакте с водой, может быть выбран из числа супердезинтеграторов, таких как кросповидон, кроскармеллоза, натрия гликолят крахмала, соединений на основе целлюлозы, таких как микрокристаллическая целлюлоза, крахмалы, альгиновая кислота, и неорганических клеев, таких как бентонит, аттапульгит и алюмосиликат магния. В одном из вариантов осуществления эксципиент, набухающий при контакте с водой, по меньшей мере частично гидратирован и выбран из группы, состоящей из натрия гликолят крахмала, кросповидона, кроскармеллозы, микрокристаллической целлюлозы, крахмалов, гидроксипропилцеллюлозы и альгиновой кислоты.
Шипучая пара
В одном из вариантов осуществления часть распадающейся таблетки также включает одну или несколько шипучих пар. В одном варианте осуществления шипучая пара содержит один элемент, выбранный из группы, состоящей из бикарбоната натрия, бикарбоната калия, карбоната кальция, карбоната магния и карбоната натрия; и один элемент, выбранный из группы, состоящей из лимонной кислоты, яблочной кислоты, фумаровой кислоты, винной кислоты, фосфорной кислоты и альгиновой кислоты.
Могут быть использованы полоксамеры. Например, Lutrol® F 127 является растворимым в воде, этаноле (95%) и изопропаноле. Не нерастворим в эфире, парафине и жирных маслах. Lutrol F–127 используется преимущественно в качестве загустителя и гелеобразующего агента, но также в качестве соэмульгатора и усилителя консистенции в кремах и жидких эмульсиях. Он также используется в качестве солюбилизатора для некоторых активных веществ, таких как нифедипин, напроксен и фентконазол, а также эфирных масел в фармацевтических и косметических композициях. Lutrol® F 127 подходит для разработки активных веществ, которые демонстрируют пониженную растворимость из–за нейтрализации.
Прочие ингредиенты
Часть распадающейся таблетки может содержать другие традиционные ингредиенты, включая наполнители; стандартные сухие связующие вещества, например поливинилпирролидон; подсластители, такие как аспартам, ацесульфам калия, сукралоза и сахарин; смазочные средства, такие как стеарат магния, стеариновая кислота, тальк и воски; консерванты; ароматизаторы; разрыхлители; антиоксиданты; активные вещества, такие как лимонная кислота, яблочная кислота, винная кислота, аскорбиновая кислота и фумаровая кислота; ПАВ и красители. Часть распадающейся таблетки может содержать полиэтиленгликоль (ПЭГ), полиэфирное соединение, имеющее структуру H−(O−CH2−CH2)n−OH.
Изготовление
Часть распадающейся таблетки может изготавливаться при помощи разнообразных методов изготовления таблетки. Традиционные способы производства таблеток включают прямое прессование («сухое смешивание»), сухую грануляцию с последующим прессованием и влажную грануляцию с последующим прессованием. Другие способы включают использование технологии прессования роликами, такой как роликовый пресс или опускной ролик, или технологий формования, литья или экструзии. Эти способы хорошо известны в данной области техники и подробно описаны, например, в Lachman, et al., The Theory and Practice of Industrial Pharmacy, Chapter 11(3rd Ed. 1986).
В одном варианте осуществления часть распадающейся таблетки формируют способом прямого прессования, который включает непосредственно прессование смеси фармацевтически активного агента, прессуемого эксципиента, эксципиента, набухающего при контракте с водой, и любых других подходящих необязательных ингредиентов. После смешивания предварительно определенный объем частиц заполняют в полость пресс–формы роликового таблеточного пресса, который непрерывно поворачивается как часть «пресс–формы» из положения заполнения в положение прессования. Частицы сжимаются между верхним пуансоном и нижним пуансоном в положение выталкивания, при котором полученная часть распадающейся таблетки выталкивается из полости пресс–формы с помощью нижнего пуансона и направляется в желоб выталкивания при помощи неподвижной панели «отбора».
Множество слоев
В одном варианте осуществления часть распадающейся таблетки имеет множество слоев, каждый из которых содержит по меньшей мере один ингредиент, который отличается от другого. В одном варианте осуществления часть распадающейся таблетки содержит два слоя, причем первый слой содержит первый фармацевтически активный агент, а второй слой содержит второй фармацевтически активный агент, который отличается от первого фармацевтически активного агента.
В одном варианте осуществления как первый слой, так и второй слой расположены на поверхности дозированной формы.
В одном варианте осуществления первый слой двухслойной части распадающейся таблетки содержит первый ароматизатор, а второй слой содержит другой второй ароматизатор для последовательной подачи ароматического профиля.
В одном варианте осуществления первый слой двухслойной части распадающейся таблетки содержит один активный ингредиент с быстрым высвобождением, а второй слой содержит активный ингредиент, такой же или отличающийся от первого активного ингредиента, который доставляется способом модифицированного высвобождения.
Часть леденцовой оболочки
Дозированная форма, составляющая предмет настоящего изобретения, содержит часть леденцовой оболочки. В одном варианте осуществления часть леденцовой оболочки содержит один или более сахаров, выбранных из группы, состоящей из изомальта, сахарозы, лактозы, декстрозы, кукурузного сиропа, лактита и ликазина.
В одном варианте осуществления леденцовая часть содержит фармацевтически активный агент. В одном варианте осуществления часть леденцовой оболочки содержит фармацевтически активный агент, который отличается от фармацевтически активного агента, содержащегося в части распадающейся таблетки.
Часть леденцовой оболочки можно изготовить различными способами, включая, помимо прочего, равномерную прокатку, обжаривание и последующую резку и штамповку, а также заливку в формы. Эти формы могут быть изготовлены из металла, резины, смолы или пластика.
Прессованные сахарные пастилки изготавливают с помощью методик таблетирования и прессования, известных в данной области техники для изготовления таблеток, хотя их прессуют при уровне твердости выше, чем традиционно применяемый для жевательных, распадающихся таблеток или таблеток для проглатывания, т.е. выше приблизительно 15 кг, и изготавливают с возможностью медленного растворения в полости рта.
Фармацевтически активный агент
Дозированная форма, составляющая предмет настоящего изобретения, включает по крайней мере один фармацевтически активный агент. Под «фармацевтически активным агентом» подразумевают агент (например, соединение), который разрешен или одобрен Управлением по контролю за качеством пищевых продуктов и лекарственных средств США, Европейским агентством по лекарственным средствам или любым из их правопреемников в качестве средства для перорального лечения патологического состояния или заболевания. Применяемые фармацевтически активные агенты включают, но не ограничиваются ими, обезболивающие, противовоспалительные и антигистаминные средства, антибиотики (например, антибактериальные, противовирусные и противогрибковые агенты), антидепрессанты, противодиабетические, спазмолитические, средства, подавляющие аппетит, бронходилятаторы, сердечно–сосудистые лекарственные агенты (например, статины), агенты для лечения центральной нервной системы, средства от кашля, деконгестанты, диуретики, отхаркивающие средства, агенты для лечения заболеваний желудочно–кишечного тракта, анестетики, муколитические средства, мышечные релаксанты, средства для лечения остеопороза, стимулирующие средства, никотинсодержащие средства и успокоительные средства.
Примеры приемлемых агентов, применяемых для лечения заболеваний желудочно–кишечного тракта, включают в себя, помимо прочего, антациды, такие как алюминийсодержащие активные ингредиенты (например, карбонат алюминия, гидроксид алюминия, карбонат дигидроксиалюминия натрия и фосфат алюминия), бикарбонатсодержащие активные ингредиенты, висмутсодержащие активные ингредиенты (например, алюминат висмута, карбонат висмута, субкарбонат висмута, субгаллат висмута и субнитрат висмута), кальцийсодержащие активные ингредиенты (например, карбонат кальция), глицин, магнийсодержащие активные ингредиенты (например, магалдрат, алюмосиликаты магния, карбонат магния, глицинат магния, гидроксид магния, оксид магния и трисиликат магния), фосфатсодержащие активные ингредиенты (например, фосфат алюминия или фосфат кальция), калийсодержащие активные ингредиенты (например, бикарбонат калия), натрийсодержащие активные ингредиенты (например, бикарбонат натрия) и силикаты; слабительные препараты, такие как размягчающие стул слабительные средства (например, докузат) и слабительные стимулирующего действия (например, бисакодил); антагонисты H2–рецепторов, такие как фамотидин, ранитидин, циметадин и низатидин; ингибиторы протонного насоса, такие как омепразол и лансопразол; желудочно–кишечные цитопротекторы, такие как сукрафлат и мизопростол; желудочно–кишечные прокинетики, такие как прукалоприд; антибиотики, активные в отношении H. pylori, такие как кларитромицин, амоксициллин, тетрациклин и метронидазол; противодиарейные средства, такие как субсалицилат висмута, каолин, дифеноксилат и лоперамид; гликопирролат; анальгетики, такие как мезаламин; противорвотные средства, такие как ондансетрон, циклизин, дифенгидрамин, дименгидринат, меклизин, прометазин и гидроксизин; бактерии–пробиотики, включающие, помимо прочего, лактобациллы; лактазу, рацекадотрил; антифлатуленты, такие как полидиметилсилоксаны (например, диметикон и симетикон, включая описанные в патентах США № 4906478, 5275822 и 6103260); их изомеры и фармацевтически приемлемые соли и пролекарства (например, сложные эфиры).
Примеры приемлемых анальгетиков, противовоспалительных и жаропонижающих агентов включают, помимо прочего, нестероидные противовоспалительные препараты (НПВП), такие как бензидамин, производные пропионовой кислоты (например, ибупрофен, напроксен, кетопрофен, флурбипрофен, фенбуфен, фенопрофен, индопрофен, флупрофен, пирпрофен, карпрофен, оксапрозин, пранопрофен и супрофен), и ингибиторы циклооксигеназы (ЦОГ), такие как целекоксиб; ацетаминофен; ацетилсалициловую кислоту; производные уксусной кислоты, такие как индометацин, диклофенак, сулиндак и толметин; производные фенаминовой кислоты, такие как мефенаминовая кислота, меклофенаминовая кислота и флуфенаминовая кислота; производные дифенилкарбоновой кислоты, такие как дифлунизал и флуфенизал; и оксикамы, такие как пироксикам, судоксикам, изоксикам и мелоксикам; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Примеры антигистаминных и противозастойных средств включают в себя, помимо прочего, бромфенирамин, хлорциклизин, дексбромфенирамин, бромгексан, фениндамин, фенирамин, пириламин, тонзиламин, приполидин, эфедрин, фенилэфрин, псевдоэфедрин, фенилпропаноламин, хлорфенирамин, декстрометорфан, дифенгидрамин, доксиламин, астемизол, терфенадин, фексофенадин, нафазолин, оксиметазолин, монтелукаст, пропилгекседрин, трипролидин, клемастин, акривастин, прометазин, оксомемазин, меквитазин, буклизин, бромгексин, кетотифен, терфенадин, эбастин, оксатомид, ксилометазолин, лоратадин, дезлоратидин и цетиризин; их изомеры и их фармацевтически приемлемые соли и сложные эфиры.
Примеры противокашлевых и отхаркивающих агентов включают, помимо прочего, дифенгидрамин, декстрометорфан, носкапин, клофедианол, ментол, бензонатат, этилморфон, кодеин, ацетилцистеин, карбоцистеин, амброксол, алкалоиды красавки обыкновенной, собренол, гваякол, амброксол и гвайфенезин; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Примеры мышечных релаксантов включают в себя, помимо прочего, циклобензаприн, хлорзоксазон, метаксалон, орфенадрин и метокарбамол; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Примеры стимуляторов включают в себя, помимо прочего, кофеин.
Примеры седативных средств включают в себя, помимо прочего, снотворные средства, такие как антигистаминные препараты (например, дифенгидрамин), эсзопиклон и золпидем; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Примеры средств для подавления аппетита включают в себя, помимо прочего, фенилпропаноламин, фентермин и диэтилкатинон; их изомеры и их фармацевтически приемлемые соли и пролекарства
Примеры анестетиков (например, при лечении боли в горле) включают, помимо прочего, диклонен, бензокаин и пектин; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Примеры приемлемых статинов включают в себя, помимо прочего, аторвастин, розувастатин, флувастатин, ловастатин, симвастатин, аторвастатин, правастатин; их изомеры и их фармацевтически приемлемые соли и пролекарства.
В одном варианте осуществления фармацевтически активный агент, содержащийся в части распадающейся таблетки, выбирают из фенилэфрина, декстрометорфана, амброксола, псевдоэфедрина, ацетаминофена, ибупрофена, кетопрофена, лоперамида, фамотидина, карбоната кальция, симетикона и ментола; их изомеры и их фармацевтически приемлемые соли и пролекарства.
В одном варианте осуществления фармацевтически активный агент, содержащийся в части леденцовой оболочки, выбирают из фенилэфрина, декстрометорфана, амброксола, псевдоэфедрина, хлорфенимидина, метатомола, хлопадинола, аскорбиновой кислоты, ментола, пектина, дициклона и бензокаина; их изомеры и их фармацевтически приемлемые соли и пролекарства.
Как описано выше, фармацевтически активные агенты настоящего изобретения могут также присутствовать в форме фармацевтически приемлемых солей, таких как кислотные/анионные или основные/катионные соли. Фармацевтически приемлемые кислотные/анионные соли включают в себя, помимо прочего, ацетат, бензолсульфонат, бензоат, бикарбонат, битартрат, бромид, эдетат кальция, камзилат, карбонат, хлорид, цитрат, дигидрохлорид, эдетат, эдисилат, эстолат, эзилат, фумарат, глицептат, глюконат, глутамат, гликолиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, иодид, изетионат, лактат, лактобионат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, памоат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, субацетат, сукцинат, сульфат, таннат, тартрат, теоклат, тозилат и триэтиодид. Фармацевтически приемлемые основные/катионные соли включают в себя, помимо прочего, соли алюминия, бензатин, соли кальция, хлоропрокаин, холин, диэтаноламин, этилендиамин, соли лития, соли магния, меглумин, соли калия, прокаин, соли натрия и соли цинка.
Как описано выше, фармацевтически активные агенты настоящего изобретения также могут присутствовать в форме пролекарств фармацевтически активных агентов. В целом такие пролекарства будут представлять собой функциональные производные фармацевтически активного агента, которые легко преобразуются in vivo в необходимый фармацевтически активный агент. Стандартные процедуры отбора и получения приемлемых производных пролекарств описаны, например, в Design of Prodrugs, ed. H. Bundgaard, Elsevier, 1985. Помимо солей настоящее изобретение предусматривает использование сложных эфиров, амидов и других защищенных или производных форм описанных соединений.
Если фармацевтически активные агенты в соответствии с настоящим изобретением имеют по меньшей мере один хиральный центр, следовательно, они могут существовать в виде энантиомеров. Если фармацевтически активные агенты обладают двумя и более хиральными центрами, они могут дополнительно существовать в виде диастереомеров. Следует понимать, что все такие изомеры и их смеси входят в объем настоящего изобретения. Более того, подразумевается, что некоторые кристаллические формы фармацевтически активных агентов могут существовать в виде полиморфов, которые включены в настоящее изобретение. Кроме того, некоторые фармацевтически активные агенты могут приводить к образованию сольватов с водой (например, гидратов) или обычными органическими растворителями, и подразумевается, что такие сольваты также входят в объем настоящего изобретения.
В одном варианте осуществления изобретения фармацевтически активный агент или агенты присутствуют в дозированной форме в терапевтически эффективном количестве, что представляет собой количество, которое вызывает желаемый терапевтический эффект при пероральном применении и может быть легко определено специалистом. Как известно в данной области техники, при определении таких количеств необходимо принимать во внимание вводимый фармацевтически активный агент, его характеристики биодоступности, режим дозирования, возраст и массу пациента, а также другие факторы.
Фармацевтически активный агент может присутствовать в различных формах. Например, фармацевтически активный агент может быть диспергирован на молекулярном уровне, например быть расплавленным внутри дозированной формы, или может быть в форме частиц, которые, в свою очередь, могут быть покрыты или не покрыты оболочкой. Если фармацевтически активный агент присутствует в форме частиц (с покрытием или без него), то средний размер частиц, как правило, составляет от приблизительно 1 до приблизительно 2000 мкм (например, от приблизительно 1 до приблизительно 1000 мкм). В одном варианте осуществления такие частицы представляют собой кристаллы со средним размером частиц от приблизительно 1 до приблизительно 300 мкм. В другом варианте осуществления частицы представляют собой гранулы или пеллеты со средним размером частиц от приблизительно 50 до приблизительно 2000 мкм, как например, от приблизительно 50 до приблизительно 1000 мкм, как например, от приблизительно 100 до приблизительно 800 мкм.
Если фармацевтически активный агент имеет неприятный вкус, то на него можно нанести маскирующее вкус покрытие, известное в данной области. Примеры приемлемых маскирующих вкус покрытий описаны в патенте США № 4,851,226, в патенте США № 5,075,114 и патенте США № 5,489,436. Также можно использовать доступные в продаже фармацевтически активные агенты для маскирования вкуса. Например, частицы ацетаминофена, инкапсулированные в оболочку из этилцеллюлозы или других полимеров при помощи процесса коацервации, могут использоваться в рамках настоящего изобретения. Инкапсулированный при помощи коацервации ацетаминофен может быть приобретен на коммерческих условиях у компании Eurand America, Inc. (Вандалия, штат Огайо) или у компании Circa Inc. (Дэйтон, штат Огайо).
Перед нанесением покрытия (например, покрытия для модифицированного высвобождения или маскирования вкуса) фармацевтически активный агент может присутствовать в чисто кристаллической или гранулированной форме. Технологии гранулирования могут использоваться с целью улучшения характеристик сыпучести или размера частиц фармацевтически активного агента для облегчения его прессования или последующего покрытия оболочкой. Приемлемые связующие вещества для выполнения гранулирования включают в себя, помимо прочего, крахмал, поливинилпирролидон, полиметакрилаты, гидроксипропилметилцеллюлозу и гидроксипропилцеллюлозу. Частицы, включающие фармацевтически активный(–ые) агент(–ы), можно получить при помощи когрануляции фармацевтически активного(–ых) агента(–ов) с приемлемыми частицами субстрата посредством любых известных в данной области способов гранулирования. Примеры такого способа гранулирования включают, помимо прочего, влажное гранулирование с высокой скоростью сдвига и гранулирование в «кипящем слое», такое как ротационное гранулирование в «кипящем слое», детали которого описаны в The Theory and Practice of Industrial Pharmacy, 3rd edition, Chapter 11, Lachman, Leon et. al., 1986.
В одном варианте осуществления фармацевтически активный агент покрывают комбинацией нерастворимого в воде пленкообразующего полимера (такого как, помимо прочего, ацетат целлюлозы или этилцеллюлоза) и растворимого в воде полимера (такого как, помимо прочего, повидон, полиметакриловые сополимеры, доступные в продаже под торговым названием Eudragit E–100 от Rohm America, и гидроксипропилцеллюлоза). В данном варианте осуществления соотношение нерастворимого в воде пленкообразующего полимера и растворимого в воде полимера составляет от приблизительно 50 до приблизительно 95 процентов от количества нерастворимого в воде полимера и от приблизительно 5 до приблизительно 50 процентов от растворимого в воде полимера, причем весовое процентное содержание покрытия по массе частицы с покрытием для маскирования вкуса составляет от приблизительно 5 процентов до приблизительно 40 процентов.
В одном варианте осуществления один или более фармацевтически активных ингредиентов или часть фармацевтически активного ингредиента могут быть связаны с ионообменной смолой в части распадающейся таблетки или в части леденцовой оболочки для маскирования вкуса фармацевтически активного ингредиента или доставки фармацевтически активного агента путем модифицированного высвобождения.
В одном варианте осуществления фармацевтически активный агент способен растворяться при приведении в контакт с текучей средой, такой как вода, желудочная кислота, кишечная текучая среда или т.п. В одном варианте осуществления характеристики растворимости фармацевтически активного вещества, входящего в состав части распадающейся таблетки, соответствуют спецификациям Фармакопеи США (USP) на таблетки, содержащие фармацевтически активный агент, с быстрым высвобождением. Например, для таблеток ацетаминофена в USP 24 уточняется, что в фосфатном буфере с pH 5,8, используя USP аппарат 2 (с лопастями) при 50 оборотов/мин, по крайней мере 80% ацетаминофена, содержащегося в дозированной форме, высвобождается из нее в течение 30 минут после приема, а для таблеток ибупрофена в USP 24 уточняется, что в фосфатном буфере с pH 7,2, при использовании USP аппарата 2 (с лопастями) при 50 оборотов/мин, по крайней мере 80% ибупрофена, содержащегося в дозированной форме, высвобождается из нее в течение 60 минут после приема дозы. См. USP 24, 2000 Version, 19–20 и 856 (1999). В другом варианте осуществления характеристики растворимости фармацевтически активного агента модифицированы, например контролируются, поддерживаются, расширяются, замедляются, пролонгируются, задерживаются и т.п.
Агент, индуцирующий слюноотделение
В одном варианте осуществления часть распадающейся таблетки, часть леденцовой оболочки или обе части содержат один или более агентов, индуцирующих слюноотделение. Примеры приемлемых агентов, индуцирующих слюноотделение, включают, помимо прочего, агонисты мускариновых ацетилхолиновых рецепторов (такие как пилокарпин и всасывающий агент, поставляемый компанией International Flavors and Fragrances под торговым названием SN12011), связующие вещества, такие как арилалкиламины (например, N, N–двузамещенные фенилалкиламины, в которых алкил содержит от приблизительно 1 до приблизительно 8 атомов углерода), N, N двузамещенные–2–фенилциклопропиламины, спирооксатиолан–хиннуклидин, корень Heliopsis longpipes, а также ингибиторы холинэстеразы. В одном варианте осуществления часть распадающейся таблетки и/или часть леденцовой оболочки содержит агент, индуцирующий слюноотделение, в количестве от приблизительно 0,1% до приблизительно 10% по массе соответствующей части.
Дозированные формы с двумя частями
В одном варианте осуществления часть леденцовой оболочки содержит фармацевтически активный агент, который отличается от фармацевтически активного агента, содержащегося в части распадающейся таблетки.
В одном варианте осуществления дозированная форма имеет многослойную структуру, причем часть распадающейся таблетки представляет собой один слой, а часть леденцовой оболочки представляет собой другой слой. В одном варианте осуществления поверхность первого слоя имеет выпуклую форму, а поверхность второго слоя имеет вогнутую форму.
В одном варианте осуществления фармацевтически активный агент, содержащийся в части распадающейся таблетки, выбирают из группы, состоящей из фенилэфрина, декстрометорфана, амброксола, псевдоэфедрина, ацетаминофена, ибупрофена, кетопрофена, лоперамида, фамотидина, кальция карбоната, симетикона и ментола, а также их фармацевтически приемлемых солей или пролекарств.
В одном варианте осуществления фармацевтически активный агент, содержащийся в части леденцовой оболочки, выбирают из группы, состоящей из фенилэфрина, декстрометорфана, амброксола, псевдоэфедрина, хлорфенирамина, метокарбомала, клофедианола, аскорбиновой кислоты, ментола, пектина, диклонина и бензокаина, а также их фармацевтически приемлемых солей или пролекарств.
Испытание на распадаемость
Для определения распада части леденцовой оболочки и части распадающейся таблетки можно использовать тест на разрушение для «таблеток без покрытия» в соответствии с USP30–NF25(с применением воды в качестве иммерсионной жидкости). Вкратце, одну единицу дозирования помещают в каждую из шести стеклянных трубок корзинки прибора, при этом воду (температура которой поддерживается на уровне 37±2°C) используют в качестве иммерсионной жидкости. За время распадаемости принимают среднее из десяти результатов измерения времени, необходимого для полного распада соответствующей части таблетки. В одном варианте осуществления время распадаемости части распадающейся таблетки составляет менее приблизительно 30 с. В другом варианте осуществления время распадаемости части распадающейся таблетки составляет менее приблизительно 15 с.
Испытание на твердость
Твердость является термином, используемым в данной области и характеризующим усилие, требуемое для разлома таблетки по диаметру, измеряется, например, при помощи прибора для определения твердости Schleuniger по методу, описанному, например, в Leiberman et al., Pharmaceutical Dosage Forms – Tablets, Volume 2, 2nd ed., Marcel Dekker Inc., 1990, pp. 213–217, 327–329. Для проведения испытания на твердость одну таблетку помещают в стальную камеру прибора, определяющего твердость таблеток, и стальной поршень оказывает давление на дозированную форму до тех пор, пока она не сломается. Применяемая сила измеряется как твердость. Обычно тестируют 5 образцов таблеток для определения среднего значения твердости, выраженного в килограмм–силах.
Сладость
В настоящем документе термин «коэффициент сладости» представляет собой термин, используемый для описания уровня сладости части распадающейся таблетки, части леденцовой оболочки или всей дозированной формы по отношению к сахарозе. Сахароза, определяемая в качестве стандарта, имеет коэффициент сладости, равный 1. Например, коэффициенты сладости нескольких известных подсластителей перечислены ниже:
В одном варианте осуществления часть распадающейся таблетки и/или часть леденцовой оболочки дозированной формы, составляющей предмет настоящего изобретения, имеет коэффициент сладости менее приблизительно 0,6. Если требуется более высокая сладость, добавление подслащивающего агента может увеличить сладость дозированной формы до по меньшей мере приблизительно 0,9, например, по меньшей мере приблизительно 1,0, по меньшей мере приблизительно 1,5 или по меньшей мере приблизительно 2,0.
Применение дозированной формы
В одном варианте осуществления настоящего изобретения заявляется метод лечения патологического состояния, а именно метод, включающий пероральное применение вышеописанной дозированной формы, причем эта форма включает дозу фармацевтически активного агента, эффективную для лечения данного патологического состояния. Примеры таких заболеваний включают в себя, помимо прочего, боль (такую как головные боли, мигрени, боли в горле, спазмы, боли в спине и миалгии), лихорадочные состояния, воспаление, патологические состояния верхних дыхательных путей (такие как кашель и заложенность носоглотки), инфекции (такие как бактериальные и вирусные инфекции), депрессию, сахарный диабет, ожирение, патологии сердечно–сосудистой системы (такие состояния, как повышение уровня холестерина, триглицеридов и артериального давления), расстройства желудочно–кишечного тракта (такие как тошнота, диарея, синдром раздраженного кишечника и повышенное газообразование), нарушения сна, остеопороз, а также никотиновую зависимость.
В одном варианте осуществления способ предназначен для лечения расстройств верхних дыхательных путей, причем фармацевтически активный агент выбирают из группы, состоящей из фенилэфрина, цетиризина, лоратадина, фексофенадина, дифенгидрамина, декстрометорфана, хлорфенирамина, хлофедианола и псевдоэфедрина, а часть леденцовой оболочки содержит фармацевтически активный агент, выбранный из группы, состоящей из ментола, диклонина, пектина и бензокаина.
Примеры
Конкретные варианты осуществления настоящего изобретения проиллюстрированы представленными ниже примерами. Настоящее изобретение не ограничено установленными ограничениями, изложенными в данных примерах.
Определенная форма
Форма настоящего изобретения включает медленно распадающуюся часть леденцовой оболочки и быстро распадающуюся часть. Часть леденцовой оболочки содержит резервуар, который удерживает быстро распадающуюся часть. Быстро распадающаяся часть имеет по меньшей мере одну поверхность, которая распадается при контакте с жидкой средой. В одном варианте осуществления быстро распадающаяся часть является пористой.
Горячее в холодное
В одном варианте осуществления формируют пористую таблетку, пористую таблетку помещают в полость формы и наносят горячую расплавленную карамель поверх пористой таблетки.
Холодное плюс горячее
В одном варианте осуществления часть леденцовой оболочки изготавливают за один этап и дают охладиться до температуры окружающей среды. В данном варианте осуществления смесь из горячих материалов, содержащую быстро распадающуюся часть, можно добавить к части леденцовой оболочки и дать ей остыть для создания единой дозированной формы с двумя частями.
Смесь горячих материалов может быть добавлена с использованием нескольких типов способов, включая дозирование или экструзию. Другим способом добавления смеси горячего материала является создание деформируемой сердцевины или таблетки. Деформируемую сердцевину добавляют к части леденцовой оболочки, причем к сердцевине применяют давление и/или тепло для заполнения предварительно определенного пространства в пределах части леденцовой оболочки. Деформируемую сердцевину можно добавлять либо в горячем, либо в холодном состоянии (при температуре окружающей среды).
Холодное плюс холодное
В одном варианте осуществления часть леденцовой оболочки изготавливают за один этап и дают охладиться до температуры окружающей среды. Если быстро распадающийся компонент добавляют к части леденцовой оболочки и обеспечивают его прикрепление, он должен быть запаян или посажен на место. В одном варианте осуществления деформируемую сердцевину добавляют в холодном состоянии, как указано выше. В другом варианте осуществления часть порошка добавляют в заданное пространство или лунку и запаивают на месте. В одной из версий данного варианта осуществления быстро распадающаяся часть содержит плавкий материал, который запаивается при охлаждении и позволяет быстро распадающейся части оставаться в заданном пространстве без отделения. Если он запаивается при охлаждении, после добавления холодной смеси (при температуре окружающей среды) в заданное пространство может быть добавлен этап нагрева.
Кроме того, быстро распадающаяся часть может быть запаяна на месте путем перемещения нагревательного устройства над его поверхностью. Нагревательное устройство может представлять собой отдельное устройство, такое как излучающий нагреватель, или твердое контактное устройство, такое как проводящий скребковый брусок или проводящий ролик нагревателя, который находится в непосредственном контакте с дозированной формой для создания уплотнения на одной поверхности части быстро распадающейся таблетки. Эта процедура помогает предотвратить отсоединение части быстро распадающейся таблетки от части леденцовой оболочки, в то же время сохраняя свойства быстрого распада у части быстро распадающейся таблетки.
Примеры
Для дополнительной иллюстрации композиций и способов настоящего изобретения предложены следующие примеры. Настоящее изобретение не ограничивается описанными примерами.
Пример 1. Часть леденцовой оболочки
1. Готовили раствор красителя, содержащий 10 г очищенной воды, 10 г гидрогенизированного гидролизата крахмала (Stabilite® SD301 и 0,001 г FD&C Green № 32.
1 Коммерчески доступный от Ingredion Incorporated, Бриджуотер, штат Нью–Джерси. Stabilite® SD30 представляет собой полиглицитол в форме, высушенной распылительной сушкой. Он представляет собой порошок с низкой сладостью, который имеет более высокую молекулярную массу и более низкую гигроскопичность, чем типичные продукты полиглицитола. Типичное распределение полиглицитола выглядит следующим образом: HP1 (сорбит), 2% по сухой массе; HP2 (мальтит), 6% по сухой массе; HP3 +, 92% по сухой массе. HP представляет собой степень распределения полиолов, от полиола с более низкой молекулярной массой до полиола с более высокой молекулярной массой. HP1 с низкой молекулярной массой (сорбит), HP3 с более высокой молекулярной массой.
2 FD&C Green № 3, № CAS 2353–45–9, представляет собой синевато–зеленый пищевой краситель, обеспечивающий темно– зеленый оттенок при применении. Цвет главным представляет собой динатриевую соль N–этил–N–[4–[[4–[этил[(3–сульфофенил)метил]амино]фенил](4–гидрокси–2–сульфофенил)метилен]–2,5–циклогексадиен–1–илиден]–3–сульфобензен–метанаминиум гидроксид. Он растворим в воде, в основном растворим в этаноле и нерастворим в растительных маслах.
2. Часть леденцовой оболочки готовили следующим образом. 44,41 г изомальта (коммерчески доступного под названием galenIQ™ 9903) и 5,59 г раствора красителя нагревали до 150°С и перемешивали и выдерживали при 150 °С в течение 10–15 минут до выпаривания воды. Полученную часть леденцовой оболочки помещали в форму при температуре 140–145 °C и применяли 3/8 дюймовый металлический стержень для создания резервуара для быстрой растворяющей части, пока часть леденцовой оболочки оставалась горячей. Части леденцовой оболочки давали остыть. Часть леденцовой оболочки имела сплошную нижнюю поверхность с прилегающими боковыми стенками и заданным резервуаром.
Пример 2. Быстро распадающийся наполнитель с использованием ксилита, ПЭГ и гидрогенизированного гидролизата крахмала
Таблица 1. Наполнитель для пастилки
таб.
масс.
3 Коммерчески доступный от Beneo GmbH. galenIQ™ 990 представляет собой фармацевтически пригодный изомальт для применения в карамельной массе пастилки. Свойства включают растворимость 25 г/100 г раствора при 20°С в воде; узкое распределение частиц по размерам; высокую химическую и температурную стабильность; низкую гигроскопичность – снижение адсорбции влаги; и высокую температуру перехода леденца.
4 Коммерчески доступный от Roquette America, Inc. XYLISORB® представляет собой торговое название Roquette для целого ряда порошков ксилита, которые могут быть использованы в различных фармацевтических и косметических составах. Xylisorb 100DC. 100 мкм, также содержит 5% декстринов.
5 ПЭГ 4000 PF. Измельченный ПЭГ от Clariant.
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 1)
1. Материалы из таблицы 1 были добавлены в сосуд, пригодный для нагревания. Добавку A Xylisorb® 100DC и добавку B Xylisorb® добавляли по отдельности в разное время.
2. Материалы нагревали до 90°C, после чего ксилит расплавлялся, указывая на то, что это он не будет наиболее желательным технологическим материалом для создания быстро растворяющейся части. Более низкая температура плавления ксилита, используемого в данном примере, не благоприятствовала данной процедуре. Данную форму ксилита можно использовать в качестве наполняющего материала основы при использовании с более низкотемпературным процессом, например, если поместить его в охлажденную леденцовую часть и обработать только поверхностным теплом.
Пример 3. Быстро распадающийся наполнитель с использованием мальтита, ПЭГ и мальтодекстрина
Таблица 2. Наполнитель для пастилки
таб.
масс.
6 Коммерчески доступный от Roquette America, Inc. SweetPearl® P90 представляет собой сыпучий подсластитель с мелким размером частиц, который получают из природных соединений пшеницы и кукурузы. SweetPearl® представляет собой мальтит от Roquette и часто используется в выпечке и шоколаде.
7 Коммерчески доступные от Grain Processing Corporation, Маскетайн, штат Айова, MALTRIN QD® (быстро диспергируемые) мальтодекстрины являются мягкими, минимально сладкими, белыми, сыпучими углеводными порошками, которые имеют высокую скорость растворения и отличную прочность частиц, полученными из кукурузы происхождения США. Они представляют собой продукты с различными профилями длины полимеров, которые обеспечивают широкий диапазон характеристик вязкости и растворимости. ТРЕБОВАНИЯ СТАНДАРТА: • Декстрозный эквивалент 9,0–12,0; • Влажность, % 6,0 макс.; • Зола (сульфатированная), % 0,5 макс.; • рН (20% раствор) 4,0–5,1; • Насыпная плотность (упакованная), фунт/куб фт. 16,0–24,0; • Размер частицы, % в диапазоне; • 20 сетка 90,0 мин; • 200 сетка 10,0 макс.; • Количество аэробных чашек, КОЕ/г; 100 макс.; • Дрожжи/форма, КОЕ/г 100 макс.; • E. coli отрицательный/10 г; • Salmonella отрицательный/25 г; МАРКИРОВОЧНАЯ ИНФОРМАЦИЯ УГЛЕВОДОВ: • DP1 (глюкоза) граммов на 100 граммов 1; • DP2 (мальтоза) граммов на 100 граммов 3; ** Информация об углеводах представлена «как есть». СТЕПЕНЬ ПОЛИМЕРИЗАЦИИ (ПРОФИЛЬ DP): • DP1–7, % 30; • DP8–25, % 35; • DP26–40, % 1; • Больше DP40, % 34.
Часть A. Процедура смешивания и нагревания материалов
Материалы, указанные в таблице 2, комбинировали следующим образом:
1. Первую часть (добавка А) мальтита, ароматизатора и сукралозы
смешивали в сосуде
2. Вторую часть (добавка B) мальтита, полиэтиленгликоля и смеси, полученной
на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Мальтодекстрин добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на часть леденцовой оболочки из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Этот наполнитель имел достаточную прочность сцепления, чтобы оставаться в части леденцовой оболочки дозированной формы.
Пример 4. Быстро распадающийся наполнитель с использованием мальтита, ПЭГ и крахмала
Таблица 3. Состав наполнителя для пастилки
таб.
масс.
Часть A. Процедура смешивания и нагревания материалов
Материалы, указанные в таблице 3, комбинировали следующим образом:
8 Коммерчески доступный от Ingredion Incorporated, Бриджуотер, штат Нью–Джерси. Модифицированный пищевой крахмал ULTRA–SPERSE M представляет собой высокопроизводительный, набухающий в холодной воде (CWS) крахмал, полученный из восковой кукурузы. Он проявляет отличную дисперсию и придает более высокую консистенцию, прозрачность и гладкость по сравнению с традиционными предварительно клейстеризованными крахмалами.
1. Первую часть (добавка А) мальтита, ароматизатора и сукралозы смешивали в сосуде.
2. Вторую часть (добавка B) мальтита, полиэтиленгликоля и смеси, полученной на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Крахмал Ultrasperse® M добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Данная смесь обеспечивала однородную текстуру.
Пример 5. Быстро распадающийся наполнитель с использованием мальтита, полоксамера и крахмала
Таблица 4. Наполнитель для пастилки
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 4)
Материалы, указанные в таблице 4, комбинировали следующим образом:
9 Коммерчески доступный от BASF North America. Блок–сополимеры Lutrol F представляют собой синтетические сополимеры окиси этилена и окиси пропилена, представленные следующей химической структурой:
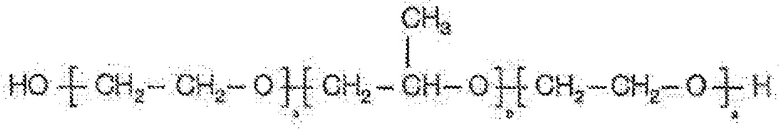
Полоксамер представляет собой 407, a представляет собой 101 и b представляет собой 56.
1. Первую часть (добавка А) мальтита, ароматизатора и сукралозы смешивали в сосуде.
2. Вторую часть (добавка B) мальтита, Lutrol и смеси, полученной на стадии один,
добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Крахмал Ultrasperse® M добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Этот наполнитель был более хрупким, чем формулы, в которых используется полиэтиленгликоль, и подвержен выпадению из формы. В этом примере в качестве замены полиэтиленгликоля использовали Lutrol, но он не обеспечивал достаточную прочность сцепления.
Пример 6. Быстро распадающийся наполнитель с использованием гидрогенизированного гидролизата крахмала и ПЭГ
Таблица 5. Наполнитель для пастилки
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 5)
Материалы, указанные в таблице 5, комбинировали следующим образом:
1. Первую часть гидрогенизированного гидролизата крахмала (добавка А), ароматизатора и сукралозы смешивали в сосуде
2. Вторую часть гидрогенизированного гидролизата крахмала (добавка B) и смеси, полученной на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Полиэтиленгликоль добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Этот наполнитель был более хрупким, чем формулы, в которых используется мальтит, и подвержен выпадению из формы. Несмотря на то, что этот наполнитель был утрамбован под некоторым давлением, он не обеспечивал достаточную прочность сцепления.
Пример 7. Быстро распадающийся наполнитель с использованием эритритола и ПЭГ
Таблица 6. Состав наполнителя для пастилки
масс.
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 6)
Материалы, указанные в таблице 6, комбинировали следующим образом:
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 6)
Материалы, указанные в таблице 6, комбинировали следующим образом:
1. Первую часть (добавка А) эритритола, ароматизатора и сукралозы смешивали в сосуде.
10 Коммерчески доступный от Jungbunzlauer Suisse AG, Базель, Швейцария. ERYLITE®, кат. № CAS 149–32–6, представляет собой сыпучий подсластитель с калорийностью, близкой к нулю. Химически он представляет собой четырехуглеродный сахарный спирт (полиол). ERYLITE® получают путем микробной ферментации углеводного субстрата. ERYLITE представляет собой белое кристаллическое вещество без запаха или порошок высокой чистоты. ERYLITE встречается в самых разнообразных продуктах, в том числе во многих фруктах и грибах, а также в ферментированных пищевых продуктах, таких как сыр, вино, пиво и соевый соус. Его подслащивающий профиль очень близок к сахарозе, а его сладость составляет до 60–70% сладости сахарозы.
2. Вторую часть (добавка B) эритритола и смеси, полученной на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Полиэтиленгликоль добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Этот наполнитель имел лучшие характеристики прочности и разрушения и имел более однородную текстуру, чем мальтит, из–за меньшего размера частиц. Прочность позволяла ему оставаться в части леденцовой оболочки. Меньший размер частиц мальтита также может иметь аналогичную текстуру.
Пример 8. Быстро распадающийся наполнитель с использованием эритритола, ксилита и никотина
Таблица 7. Состав наполнителя для пастилки
a. Коммерчески доступный от Jungbunzlauer Suisse AG
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 7)
Материалы, указанные в таблице 7, комбинировали следующим образом:
1. Первую часть (добавка А) эритритола, ксилисорба, диоксида титана и FD&C Blue № 1 смешивали в сосуде.
2. Добавляли дигидрат диартрата никотина и смешивали вручную.
11 Коммерчески доступный от Roquette. XYLISORB® представляет собой торговое название Roquette для целого ряда порошков ксилита, которые могут быть использованы в различных фармацевтических и косметических составах. Частицы XYLISORB® 300 имеют средний диаметр, равный 300 мкм.
3. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
4. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте.
Пример 9. Быстро распадающийся наполнитель с использованием мальтита, ПЭГ и гидрогенизированного гидролизата крахмала
Таблица 8. Состав наполнителя для пастилки
масс.
Часть A. Процедура смешивания и нагревания материалов
Материалы, указанные в таблице 8, комбинировали следующим образом:
1. Первую часть мальтита (добавка А), ароматизатора и сукралозы смешивали в сосуде.
2. Вторую часть мальтита (добавка B), полиэтиленгликоля и смеси, полученной на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Гидрогенизированный гидролизат крахмала добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Твердая масса оставалась в дозированной форме без выпадения.
Пример 10. Быстро распадающийся наполнитель с использованием ксилита, полоксамера и крахмала
Таблица 9. Состав наполнителя для пастилки
Часть A. Процедура смешивания и нагрева материалов (с использованием формулы из таблицы 9)
Материалы, указанные в таблице 9, комбинировали следующим образом:
1. Первую часть Xylisorb® (добавка А), ароматизатора и сукралозы смешивали в сосуде.
2. Вторую часть Xylisorb® (добавка B), полиэтиленгликоля, Lutrol и смеси, полученной на стадии один, добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
3. Ultrasperse добавляли в пластиковый пакет и перемешивали путем переворачивания в течение 2 минут.
4. Полученную смесь нагревали до 90°C при ручном перемешивании на горячей плите.
5. Нагретую смесь переносили на леденцовую часть из примера 1 при небольшом нажатии на верхнюю поверхность и охлаждали на месте. Твердая масса оставалась в дозированной форме без выпадения.
Приведенные выше примеры не предназначены для ограничения объема настоящего изобретения, который может быть определен в формуле изобретения. В частности, специалисту в данной области известны различные эквиваленты и заменители, применимые в вышеизложенном описании, и они будут попадать в объем изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДОЗИРОВАННОЙ ФОРМЫ С ПОКРЫТИЕМ | 2017 |
|
RU2771159C2 |
| ТВЕРДАЯ НИКОТИНСОДЕРЖАЩАЯ ДОЗИРОВАННАЯ ФОРМА СО СНИЖЕННЫМ НЕПРИЯТНЫМ ОРГАНОЛЕПТИЧЕСКИМ ВОЗДЕЙСТВИЕМ | 2013 |
|
RU2623018C2 |
| ТВЕРДЫЕ ЧАСТИЦЫ СИМЕТИКОНА И ИХ ДОЗИРОВАННАЯ ФОРМА | 2018 |
|
RU2790260C2 |
| РАСПАДАЮЩАЯСЯ В ПОЛОСТИ РТА ЛЕКАРСТВЕННАЯ ФОРМА | 2008 |
|
RU2482839C2 |
| ЖИДКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МУКОАДГЕЗИВНЫЙ АГЕНТ | 2017 |
|
RU2773140C2 |
| СОСТОЯЩАЯ ИЗ МНОГИХ ЧАСТЕЙ ВНУТРИРОТОВАЯ ЛЕКАРСТВЕННАЯ ФОРМА С ОРГАНОЛЕПТИЧЕСКИМИ СВОЙСТВАМИ | 2010 |
|
RU2490010C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТАБЛЕТОК С ИСПОЛЬЗОВАНИЕМ РАДИОЧАСТОТНОГО ИЗЛУЧЕНИЯ И ЧАСТИЦ С ПОГЛОЩАЮЩИМ ПОКРЫТИЕМ | 2015 |
|
RU2712267C2 |
| СПОСОБ ОБЕСПЕЧЕНИЯ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ ЭФФЕКТОВ УХОДА ЗА ПОЛОСТЬЮ РТА | 2017 |
|
RU2783120C2 |
| РАСПАДАЮЩИЕСЯ В ПОЛОСТИ РТА ТВЕРДЫЕ ДОЗИРОВАННЫЕ ФОРМЫ, СОДЕРЖАЩИЕ ПРОГЕСТИН, И СПОСОБЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ УКАЗАННЫХ ДОЗИРОВАННЫХ ФОРМ | 2007 |
|
RU2465907C2 |
| ДОЗИРОВАННАЯ ФОРМА ТАБЛЕТКИ ДЛЯ РАССАСЫВАНИЯ, СОСТОЯЩАЯ ИЗ ДВУХ ЧАСТЕЙ | 2008 |
|
RU2466719C2 |
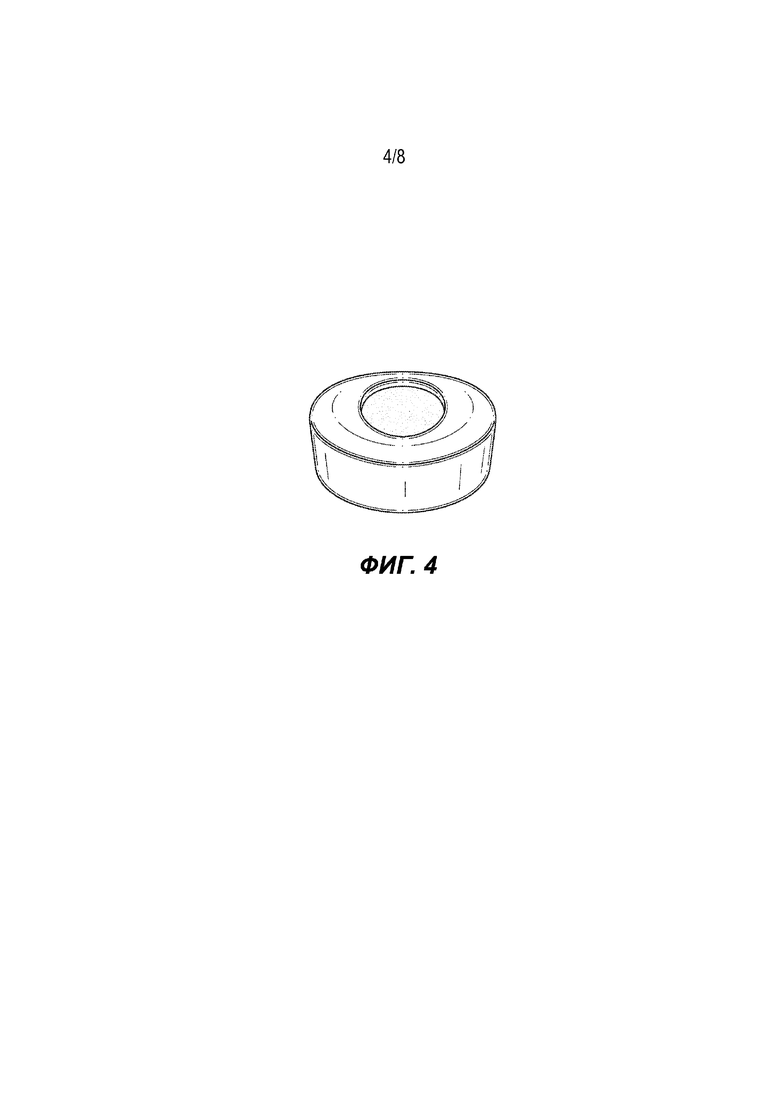
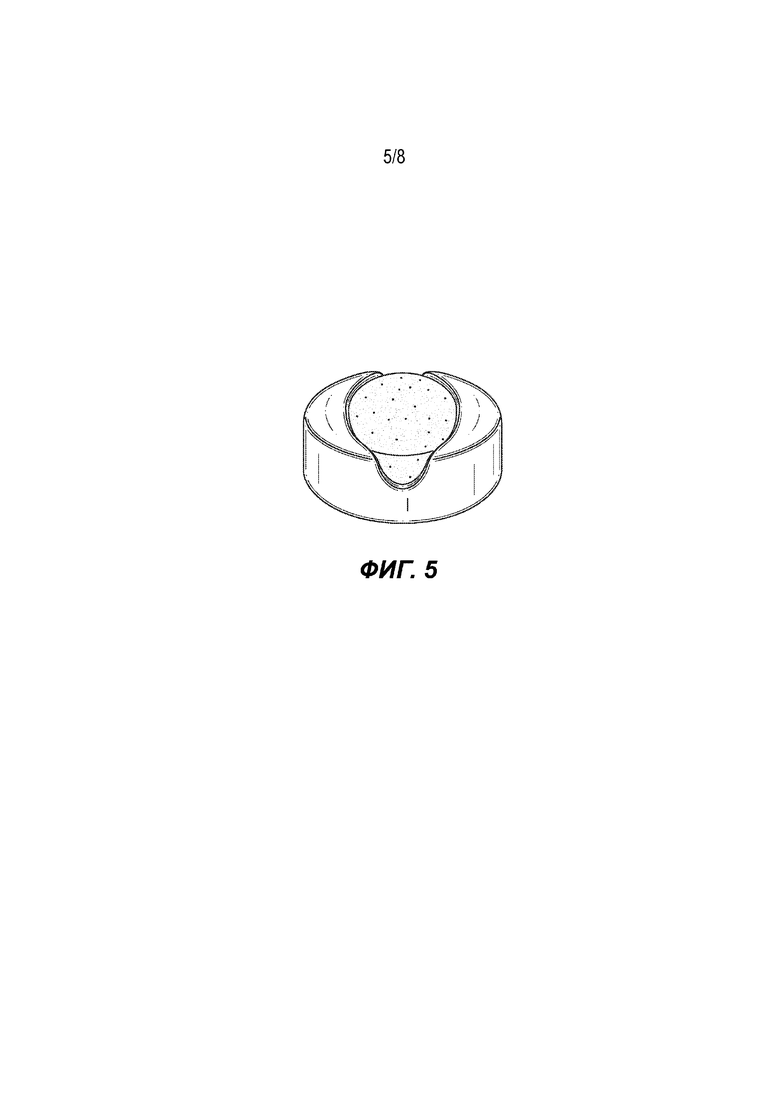
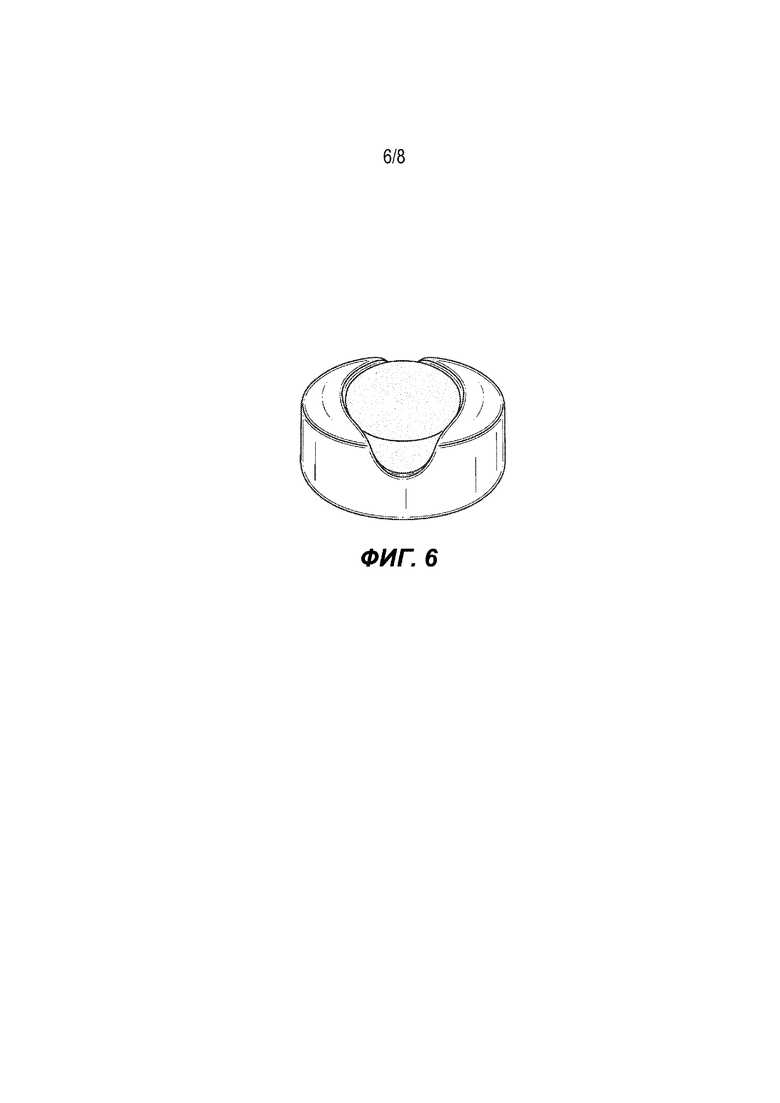
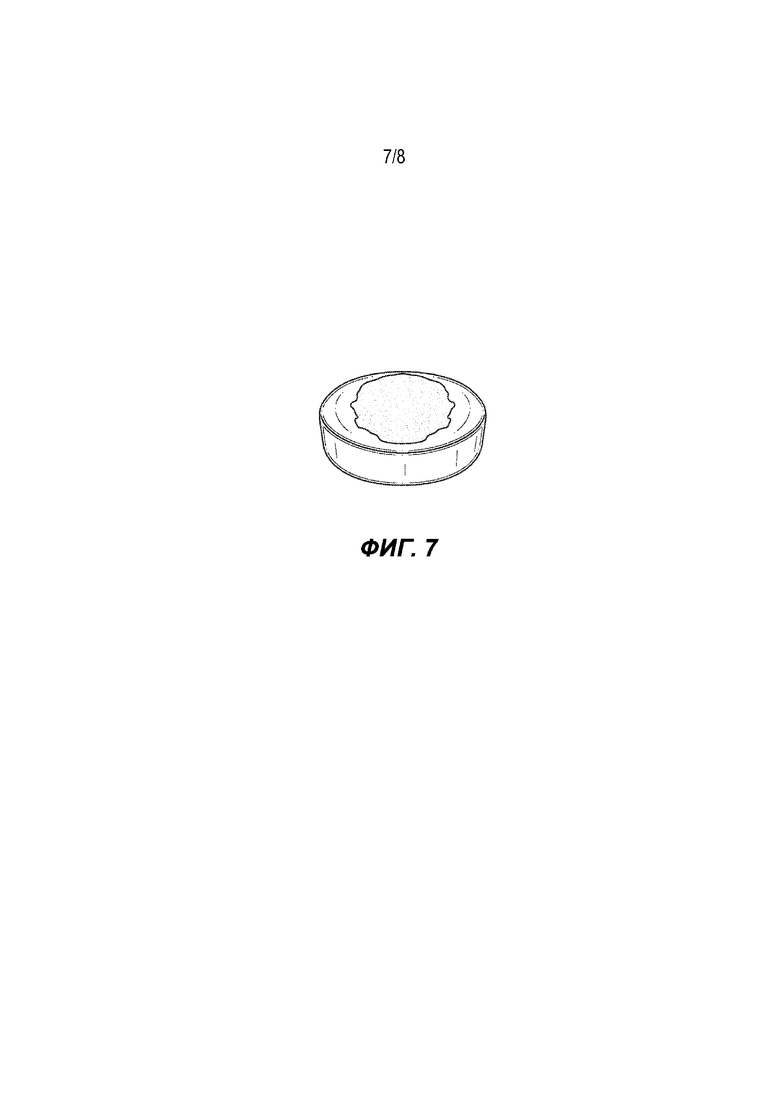
Настоящее изобретение относится к области фармации, а именно к способу получения дозированной формы пастилки, где дозированная форма пастилки содержит: часть распадающейся таблетки; и часть леденцовой оболочки, содержащая резервуар, который удерживает быстро распадающуюся часть; причем часть распадающейся таблетки содержит по меньшей мере один фармацевтически активный ингредиент; и где способ включает: изготовление части леденцовой оболочки за одну стадию и предоставление возможности ей остыть до температуры окружающей среды; создание деформируемой сердцевины или таблетки, содержащей распадающуюся часть таблетки; добавление деформируемой сердцевины или таблетки к части леденцовой оболочки; и применение небольшого нажатия к деформируемой сердцевине или таблетке для заполнения заранее определенного пространства в пределах части леденцовой оболочки; и запаивание на месте. Техническим результатом настоящего изобретения является обеспечение эффективного способа получения двухкомпонентной дозированной формы, который легко адаптируется к коммерческому производству. 5 з.п. ф-лы, 8 ил., 9 табл., 10 пр.
1. Способ получения дозированной формы пастилки, где дозированная форма пастилки содержит:
часть распадающейся таблетки; и
часть леденцовой оболочки, содержащая резервуар, который удерживает быстро распадающуюся часть;
причем часть распадающейся таблетки содержит по меньшей мере один фармацевтически активный ингредиент; и
где способ включает:
изготовление части леденцовой оболочки за одну стадию и предоставление возможности ей остыть до температуры окружающей среды;
создание деформируемой сердцевины или таблетки, содержащей распадающуюся часть таблетки;
добавление деформируемой сердцевины или таблетки к части леденцовой оболочки; и
применение небольшого нажатия к деформируемой сердцевине или таблетке для заполнения заранее определенного пространства в пределах части леденцовой оболочки; и
запаивание на месте.
2. Способ по п. 1, отличающийся тем, что часть леденцовой оболочки содержит по меньшей мере один фармацевтически активный ингредиент.
3. Способ по п. 1, отличающийся тем, что часть распадающейся таблетки содержит по меньшей мере два эксципиента, выбранных из группы, состоящей из полоксамера, полиэтиленгликоля, сахара, крахмала и гидролизата крахмала.
4. Способ по п. 1, отличающийся тем, что часть распадающейся таблетки содержит множество слоев.
5. Способ по п. 4, отличающийся тем, что часть распадающейся таблетки содержит два слоя, причем первый слой содержит первый фармацевтически активный ингредиент, и при этом второй слой содержит второй фармацевтически активный ингредиент.
6. Способ по п. 5, отличающийся тем, что первый слой и второй слой расположены на поверхности дозированной формы.
| ДОЗИРОВАННАЯ ФОРМА ТАБЛЕТКИ ДЛЯ РАССАСЫВАНИЯ, СОСТОЯЩАЯ ИЗ ДВУХ ЧАСТЕЙ | 2008 |
|
RU2466719C2 |
| US 2010124560 A, 20.05.2010 | |||
| US 20170035656 A1, 09.02.2017 | |||
| РАСПАДАЮЩАЯСЯ В ПОЛОСТИ РТА ЛЕКАРСТВЕННАЯ ФОРМА | 2008 |
|
RU2482839C2 |
| WO 2010044736 A1, 22.04.2010. | |||
Авторы
Даты
2022-05-12—Публикация
2018-01-25—Подача