Настоящее изобретение охватывает новые хинолиновые производные общей формулы (I), как описано и определено в описании настоящего изобретения, способы получения указанных соединений, промежуточные соединения, полезные для получения указанных соединений, фармацевтические композиции и комбинации, содержащие указанные соединения, и применение указанных соединений для получения фармацевтических композиций для контроля, лечения и/или профилактики заболеваний, в частности для контроля, лечения и/или профилактики инфекций, вызванных гельминтами, в частности инфекций, вызванных желудочно-кишечными и внекишечными нематодами, у животных и людей, составы, содержащие такие соединения, и способы контроля, лечения и/или профилактики инфекций, вызванных гельминтами, в частности, инфекций, вызванных желудочно-кишечными и внекишечными нематодами, у животных и людей, в которых указанные соединения применяются в качестве единственного агента или в сочетании с другими активными ингредиентами.
Уровень техники
Возникновение резистентности против всех коммерчески доступных антигельминтных агентов, как оказалось, является увеличивающейся проблемой в области ветеринарной медицины. Широкое использование антигельминтных агентов для управления борьбы с нематодами привело к значительному выбору высокорезистентных популяций гельминтов. Поэтому распространение сопротивления против всех классов антигельминтных лекарственных средств угрожает эффективной борьбе с гельминтами у крупного рогатого скота, коз, овец и лошадей. Кроме того, успешная профилактика дирофиляриоза сердца у собак, которая в настоящее время опирается исключительно на использование макроциклических лактонов, находится под угрозой, так как потеря эффективности для множества макроциклических лактонов была описана для некоторых областей Соединенных штатов Америки - особенно в тех областях, где проблема заражения сердечным гельминтом высока. Наконец, экспериментальные исследования инфекции с личинками Dirofilaria immitis из предполагаемой области случаев потери эффективности в Lower Mississippi Дельта подтвердили in vivo существование резистентности к макроциклическому лактону.
Хотя резистентность человеческих гельминтов к антигельминтным агентам в настоящее время является редкой, распространение антигельминтной резистентности в ветеринарной области, как упоминалось ранее, необходимо учитывать при лечении гельминтоза у человека. Продолжительные терапии с регулярным введением доз против филяриоза могут приводить к высокорезистентным генотипам, и резистентности уже были описаны для определенных антигельминтных агентов (например, празиквантел, бензимидазол и никлозамид).
Поэтому срочно требуются преодоляющие резистентность антигельминтные агенты с новыми молекулярными режимами действия.
Задача настоящего изобретения состоит в предоставление соединений, которые могут использоваться в качестве антигельминтных агентов в медицине, особенно ветеринарии, обладающих удовлетворительной или улучшенной антигельминтной активностью против широкого спектра гельминтов, особенно при относительно низких дозах, для контроля, лечения и/или профилактики инфекций, вызванных гельминтами, у животных и людей, предпочтительно без каких-либо неблагоприятных токсических эффектов для организма, подлежащего лечению.
Определенные хинолинкарбоксамиды описаны в JP 2008-214323 А в качестве агентов, подходящих для лечения и/или профилактики кожных заболеваний, таких как обыкновенные угри, дерматит или тому подобное.
В WO 2017103851 описаны хинолин-3-карбоксамиды в качестве H-PGDS ингибиторов, полезных для лечения атеросклероза, псориаза, синусита и мышечной дистрофии Дюшенна.
Однако в уровне техники не описываются новые хинолиновые производные общей формулы (I) согласно настоящему изобретению, как описано и определено в описании настоящего изобретения.
Было обнаружено, и это составляет основу настоящего изобретения, что соединения согласно настоящему изобретению имеют удивительные и предпочтительные свойства.
В частности, было обнаружено, что соединения согласно настоящему изобретению эффективно взаимодействуют с Slo-1 кальций-зависимыми калиевыми каналами нематод. Это взаимодействие характеризуется достижением паралич а/ингибирования, в частности, желудочно-кишечных нематод, не паразитирующих нематод и филярий, для которых данные приводятся в части экспериментов по биологической активности. Поэтому соединения согласно настоящему изобретению могут использоваться в качестве антигельминтных агентов для контроля, лечения и/или профилактики инфекций, вызванных желудочно-кишечными и внекишечных гельминтных, в частности желудочно-кишечных и внекишечных инфекций, вызванных нематодами, включая филярий.
Описание изобретения
Первым объектом настоящего изобретения являются соединения общей формулы (I):
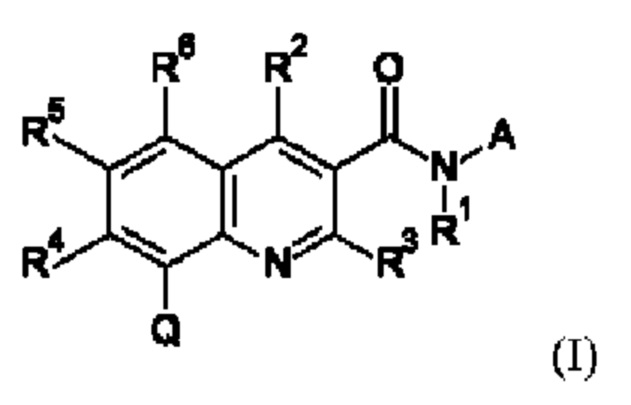
в которой:
А представляет собой А1 или А2,
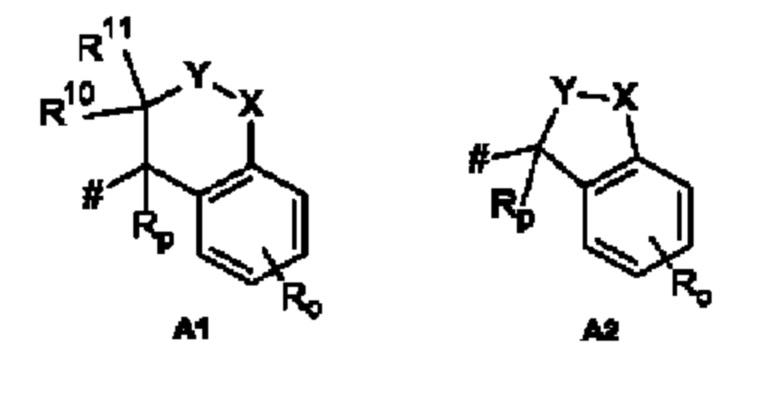
о представляет собой 0, 1, 2, 3 или 4,
R выбирают из группы, состоящей из водорода, галогена, циано, нитро, -ОН, C1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, C1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, S(О)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, -S(O)-С1-С4-галогеналкила и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, S, и N-R9, где по меньшей мере один из X и Y представляет собой CR7R8, или
X, Y образуют вместе член кольца, выбранный из группы, состоящей из -С(О)-O-, -C(O)-NR9-, -S(O)-NR9-, -SO2-NR9- и -SO2-O-,
R1 выбирают из фуппы, состоящей из водорода, циано, -СНО, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, С3-С6-галогенциклоалкила, имеющего от 1 до 5 атомов галогена, С3-С4-алкенила, С3-С4-алкинила, С1-С4-алкокси-С1-С4-алкила, С3-С6-циклоалкил-С1-С3-алкила, циано-С1-С4-алкила, -NH-С1-С4-алкила, -N(С1-С4-алкила)2, NH2-С1-С4-алкила-, С1-С4-алкила-NH-С1-С4-алкила-, (C1-С4-алкила)2N-С1-С4-алкила-, С1-С4-алкил-С(O)-, С1-С4-галогеналкил-С(O)-, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси-С(O)-, бензилокси-С(О)-, С1-С4-алкокси-С1-С4-алкил-С(O)-, -SO2-С1-С4-алкила, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенил-С1-С4-алкила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R2 выбирают из группы, состоящей из
водорода, галогена, циано, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(О)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-С6-алкила, С3-С6-циклоалкила, С2-С4-алкенила, С3-С6-циклоалкенила, С2-С4-алкинила или фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-алкил-С(О)-, С1-С4-алкокси-С(O)-, -C(O)-NH2, -C(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(С(O)-С1-С4-алкила), -N(С1-С4-алкил)(С(O)-С1-С4-алкила), -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-C4-алкила, С1-С4-алкил-С(O)--, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-алкокси-С1-С4-алкила-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и 4-10-ти членного гетероциклоалкила,
R3 представляет собой водород или С1-С4-алкил,
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С3-С6-циклоалкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси-С1-С4-алкила, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-С(O)-, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила,
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С3-С6-циклоалкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси-С1-С4-алкила, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,С1-С4-алкил-С(O)-, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила,
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С3-С6-циклоалкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси-С1-С4-алкила, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-С(O)-, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила,
R7 выбирают из группы, состоящей из водорода, -ОН, фтора, C1-С4-алкила и С1-С4-алкокси,
R8 выбирают из группы, состоящей из водорода, -ОН, фтора, C1-C4-алкила и С1-С4-алкокси,
или R7 и R8 вместе образуют оксо группу (=O),
или R7 и R8 образуют, вместе с атомом углерода, с которым они связаны, 3-6-ти членное кольцо, выбранное из группы, состоящей из С3-С6-циклоалкила и 3- 6-ти членного гетероциклоалкила,
R9 выбирают из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и С1-С4-алкокси,
R10 выбирают из группы, состоящей из водорода, -ОН, С1-С4-алкила и С1-С4-алкокси,
R11 выбирают из группы, состоящей из водорода, С1-С4-алкила и С1-С4-алкокси,
или R10 и R11 образуют, вместе с атомом углерода, с которым они связаны, 3-6-ти членное кольцо, выбранное из группы, состоящей из С3-С6-циклоалкила и 3- 6-ти членного гетероциклоалкила,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -ОН, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(-C(O)-C1-С4-алкила), -N(С1-С4-алкил)(-С(O)-С1-С4-алкила), С1-С4-алкокси, С1-С4-алкокси-С(О)-;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, -N(С1-С4-алкила)(-С(O)-С1-С4-алкила), C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
-NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4-алкила, C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Q выбирают из группы, состоящей из 6-ти или 10-ти членного арила и 5-10-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, выбранными из группы, состоящей из галогена, SF5, циано, -СНО, нитро, оксо, С1-С4-алкила, С1-С4-гидроксиалкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, С1-С4-алкокси, С3-С6-циклоалкил-С1-С4-алкокси, циано-С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH-SO2-(С1-С4-алкила), -N(SO2-[С1-С4-алкил])(С1-С4-алкила), (С1-С4-алкоксиимино)-С1-С4-алкила, 4-6-ти членного гетероциклила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -СН2-O-(С1-С4-алкила), -СН2-NH(С1-С4-алкила), -СН2-N(С1-С4-алкила)2, метила, замещенного 4-6-ти членным гетероциклилом, который сам по себе необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -СН2-S-(С1-С4-алкила), -СН2-S(O)-(С1-С4-алкила), -СН2-SO2-(С1-С4-алкила), -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(С1-С4-алкила), -S-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -CONH(С1-С4-алкила), -CONH(С3-С6-циклоалкила), -NHCO(С1-С4-алкила), -NHCO(C3-C6-циклоалкила), -NHCO(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена,
где когда Y представляет собой О, S или N-R9, ни один из R7, R8, R10 и R11 не представляет собой -ОН, и где когда X представляет собой О, S или N-R9, ни один из R7 и R8 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
Определения
Термин «замещенный» означает, что один или более атомов водорода при обозначенном атоме или группе замещены заместителем, выбранным из указанной группы, при условии, что нормальная валентность обозначенного атома в существующих условиях не будет превышена. Допускаются комбинации заместителей и/или переменных.
Термин «необязательно замещенный» означает, что количество заместителей может быть равным или отличным от нуля. Если не указано иное, возможно, что необязательно замещенные группы замещены таким большим количеством необязательных заместителей, которые могут быть присоединены путем замещения атома водорода атомом, не являющимся водородом, при любой доступном атоме углерода или атоме азота. Как правило, число необязательных заместителей, если они присутствуют, может быть 1, 2, 3, 4 или 5, в частности 1, 2 или 3.
Как применено в описании настоящего изобретения, термин «один или более», например, в определении заместителей соединений общей формулы (I) согласно настоящему изобретению, означает «1, 2, 3, 4 или 5, особенно 1, 2, 3 или 4, более конкретно 1, 2 или 3, еще более конкретно 1 или 2".
Как применяется в описании настоящего изобретения, оксо-заместитель представляет собой атом кислорода, который связан с атомом углерода или атомом серы через двойную связь.
Термин «заместитель в кольце» означает заместитель, присоединенный к ароматическому или неароматическому кольцу, который замещает доступный атом атома в кольце.
Если сложный заместитель состоит из более чем одной части, например, (С1-С4-алкокси) -(С1-С4-алкил)-, положение данной части может находиться в любом подходящем положении указанного сложного заместителя, то есть С1-С4--алкокси часть может быть присоединена к любому атому углерода С1-С4--алкильной части указанной (С1-С4--алкокси)-(С1-С4--алкильной) группы. Дефис в начале или в конце такого сложного заместителя указывает точку присоединения указанного сложного заместителя к остальной части молекулы. Если кольцо, содержащее атомы углерода и необязательно один или более гетероатомов, таких как атом азота, атом кислорода или атом серы, например, замещено заместителем, возможно, указанный заместитель может быть связан в любом подходящем положении указанного кольца, с подходящим атомом углерода и/или подходящим гетероатомом.
Как применяется в настоящей заявке, положение, через которое соответствующий заместитель соединен с остальной частью молекулы, может в показанной структуре быть изображено знаком «решетка» (#) или пунктирной линией в указанном заместителе.
Термин «содержащий» при использовании в описании настоящего изобретения включает «состоящий из».
Если в описании настоящего изобретения любой признак сопровождается «как указано в описании настоящего изобретения», это означает, что он может упоминаться в любом месте в описании настоящего изобретения.
Термины, упомянутые в описании настоящего изобретения, имеют следующие значения:
Термин "атом галогена" означает атом фтора, хлора, брома или иода, в частности атом фтора, хлора или брома.
Термин "C1-С6-алкила" означает линейную или разветвленную, насыщенную, одновалентную углеводородную группу, имеющую 1, 2, 3, 4, 5 или 6 атомов углерода. Термин "С1-С4-алкил" означает линейную или разветвленную, насыщенную, одновалентную углеводородную группу, имеющую 1, 2, 3, или 4 атома углерода, например, метальную, этильную, н-пропильную, изопропильную, н-бутильную, втор-бутыльную, изобутильную или трет-бутильную группу, или их изомер. В частности, указанная группа имеет 1, 2 или 3 атома углерода ("С1-С3-алкил"), например, метальная, этильная, н-пропильная или изопропильная группа.
Термин "С1-С4-гидроксиалкил" означает линейную или разветвленную, насыщенную, одновалентную углеводородную группу, в которой термин "С1-С4-алкил" определен выше, и в которой 1 или 2 атома водорода замещены гидрокси группой, например, гидроксиметильная, 1-гидроксиэтильная, 2-гидроксиэтильная, 1,2-дигидроксиэтильная, 3-гидроксипропильная, 2-гидроксипропильная, 1-гидроксипропильная, 1-гидроксипропан-2-ильная, 2-гидроксипропан-2-ильная, 2,3-дигидроксипропильная, 1,3-дигидроксипропан-2-ильная, 3-гидрокси-2-метил-пропильная, 2-гидрокси-2-метил-пропильная, 1-гидрокси-2-метил-пропильная группа.
Термин "-NH(С1-С4-алкил)" или "-N(С1-С4-алкил)2" означает линейную или разветвленную, насыщенную, одновалентную группу, в которой термин "С1-С4-алкил" имеет значение, как указано выше, например, метиламино, этиламино, н-пропиламино, изопропиламино, N,N-диметиламино, N-метил-N-этиламино или N,N-диэтиламино группа.
Термин "-S-С1-С4-алкил", "-S(O)-С1-С4-алкил" или "-SO2-С1-С4-алкил" означает линейную или разветвленную, насыщенную группу, в которой термин "С1-С4-алкил" имеет значение, как указано выше, например, метилсульфанильная, этилсульфанильная, н-пропилсульфанильная, изопропилсульфанильная, н-бутилсульфанильная, втор-бутилсульфанильная, изобутилсульфанильная или трет-бутилсульфанильная группа, метилсульфинильная, этилсульфинильная, н-пропилсульфинильная, изопропилсульфинильная, н-бутилсульфинильная, втор-бутилсульфинильная, изобутилсульфинильная или трет-бутилсульфинильная группа, или метилсульфонильная, этилсульфонильная, н-пропилсульфонильная, изопропилсульфонильная, н-бутилсульфонильная, втор-бутилсульфонильная, изобутилсульфонильная или трет-бутилсульфонильная группа.
Термин "С1-С4-галогеналкил" означает линейную или разветвленную, насыщенную, одновалентную углеводородную группу, в которой термин "С1-С4-алкил" имеет значение, как указано выше, и в которой один или более атомов водорода замещены, одинаково или различно, атомом галогена. В частности, указанный атом галогена представляет собой атом фтора. Более конкретно, все указанные атомы галогена представляют собой атомы фтора ("C1-С4-фторалкил"). Указанная С1-С4-галогеноалкильная группа представляет собой, например, фторметил, дифторметил, трифторметил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, пентафторэтил, 3,3,3-трифторпропил или 1,3-дифторпропан-2-ил.
Термин "С1-С4-алкокси" означает линейную или разветвленную, насыщенную, одновалентную группу формулы (С1-С4-алкил)-O-, в которой термин "С1-С4-алкил" имеет значение, как указано выше, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси, изобутокси или трет-бутокси группа, или их изомер.
Термин "С1-С4-галогеналкокси" означает линейную или разветвленную, насыщенную, одновалентную С1-С4-алкокси группу, как указано выше, в которой один или более из атомов водорода замещены, одинаково или различно, атомом галогена. В частности, указанный атом галогена представляет собой атом фтора. Указанная С1-С4-галогеноалкокси группа представляет собой, например, фторметокси, дифторметокси, трифторметокси, 2,2,2-трифторэтокси или пентафторэтокси.
Термин "С2-С4-алкенил" означает линейную или разветвленную, одновалентную углеводородную группу, которая содержит одну двойную связь, и которая имеет 2, 3 или 4 атома углерода. Указанная С2-С4-алкенильная группа представляет собой, например, этенильная (или "винильная"), проп-2-ен-1-ильная (или "аллильная"), проп-1-ен-1-ильная, бут-3-енильная, бут-2-енильная, бут-1-енильная, проп-1-ен-2-ильная (или "изопропенильная"), 2-метилпроп-2-енильная, 1-метилпроп-2-енильная, 2-метилпроп-1-енильная или 1-метилпроп-1-енильная группа. В частности, указанная группа представляет собой аллил.
Термин "С2-С4-алкинил" означает линейную одновалентную углеводородную группу, которая содержит одну тройную связь, и которая содержит 2, 3 или 4 атома углерода. Указанная С2-С4-алкинильная группа представляет собой, например, этинильную, проп-1-инильную, проп-2-инильную (или "пропаргильную"), бут-1-инильную, бут-2-инильную, бут-3-инильную или 1-метилпроп-2-инильную, группу. В частности, указанная алкинильную группа представляет собой проп-1-инил или проп-2-инил.
Термин "С3-С6-циклоалкил" означает насыщенное, одновалентное, моноциклическое углеводородное кольцо, которое содержит 3, 4, 5 или 6 атома углерода ("С3-С6-циклоалкил"). Указанная С3-С6-циклоалкильная группа представляет собой, например, моноциклическое углеводородное кольцо, например, циклопропильная, циклобутильная, циклопентильная или циклогексильная группа.
Термин "С3-С6-галогенциклоалкил" означает насыщенное, одновалентное, моноциклическое углеводородное кольцо, в котором термин "С3-С6-циклоалкил" имеет значение, как указано выше, и в котором один или более атомов водорода замещены, одинаково или различно, атомом галогена. В частности, указанный атом галогена представляет собой атом фтора или хлора. Указанная С3-С6-галогеноциклоалкильная группа представляет собой, например, моноциклическое углеводородное кольцо, замещенные одним или двумя атомами фтора или хлора, например, 1-фтор-циклопропильная, 2-фторциклопропильная, 2,2-дифторциклопропильная, 2,3-дифторциклопропильная, 1-хлорциклопропильная, 2-хлорциклопропильная, 2,2-дихлорциклопропильная, 2,3-дихлор циклопропильная, 2-фтор-2-хлорциклопропильная и 2-фтор-3-хлорциклопропильная группа.
Термин "бензо-С5-Сб-циклоалкил" означает моновалентное, бициклическое углеводородное кольцо, где насыщенное, моновалентное, моноциклическое углеводородное кольцо, которое содержит 5 или 6 атомов углерода ("С5-С6-циклоалкил"), аннелировано с фенильным кольцом. Указанная бензо-С5-С6-циклоалкильная группа представляет собой, например, бициклическое углеводородное кольцо, например, индан (т.е. 2,3-дигидро-1H-инден) или тетралин (т.е. 1,2,3,4-тетрагидронафталиновая) группа.
Термин "спироциклоалкил" означает насыщенную, моновалентную бициклическую углевоодродную группу, в которой два кольца делят один общий кольцевой атом углерода, и где указанная бициклическая углеводородная группа содержит 5, 6, 7, 8, 9, 10 или 11 атомов углерода, причем возможно указанная спироциклоалкильная группа присоединена к остатку молекулы через любой один из атомов углерода, за исключением спиро атома углерода. Указанная спироциклоалкильная группа представляет собой, например, спиро[2.2]пентил, спиро[2.3]гексил, спиро[2.4]гептил, спиро[2.5]октил, спиро[2.6]нонил, спиро[3.3]гептил, спиро[3.4]октил, спиро[3.5]нонил, спиро[3.6]децил, спиро[4.4]нонил, спиро[4.5]децил, спиро[4.6]ундецил или спиро[5.5]ундецил.
Термин "гетероциклоалкил" означает моноциклический или бициклический, насыщенный или частично насыщенный гетероцикл с 4, 5, 6, 7, 8, 9 или 10 кольцевыми атомами в общем ("4-10-ти членная гетероциклоалкильная" группа), в частности 4, 5 или 6 кольцевыми атомами ("4-6-ти членная гетероциклоалкильная," группа), которая содержит один или два идентичных или различных кольцевых гетероатомов из ряда N, О и S, причем, возможно, указанная гетероциклоалкильная группа присоединена к остатку молекулы через любой один из атомов углерода, за исключением спиро атома углерода, или, если присутствует, атома азота.
Указанная гетероциклоалкильная группа, без ограничения к этому, может представлять собой 4-ти членное кольцо, такое как азетидинил, оксетанил или тиетанил, например; или 5-ти членное кольцо, такое как тетрагидрофуранил, оксоланил, 1,3-диоксоланил, тиоланил, пирролидинил, имидазолидинил, пиразолидинил, 1,1диоксидотиоланил, 1,2-оксазолидинил, 1,3-оксазолидинил, 1,3-тиазолидинил или 1,2,4-тиазолидинил, например; или 6-ти членное кольцо, такое как тетрагидропиранил, тетрагидротиопиранил, пиперидинил, морфолинил, дитианил, тиоморфолинил, пиперазинил, оксанил, 1,3-диоксанил, 1,4-диоксанил или 1,2-оксазинанил, например; или 7--ми членное кольцо, такое как азепанил, 1,4-диазепанил или 1,4-оксазепанил, например; или бициклическое 7-ми членное кольцо, такое как 6-окса-3-азабицикло[3.1.1]гептан, например; или бициклическое 8-ми членное кольцо, такое как 5,6-дигидро-4Н-фуро[2,3-с]пиррол или 8-окса-3-азабицикло[3.2.1]октан, например; или бициклическое 9-ми членное кольцо, такое как октагидро-1Н-пирроло[3,4-b]пиридин, 1,3-дигидро-изоиндол, 2,3-дигидро-индол или 3,9-диокса-7-азабицикло[3.3.1]нонан, например; или бициклическое 10-ми членное кольцо, такое как декагидрохинолин или 3,4-дигидроизохинолин, например.
Термин "гетероспироциклоалкил" означает бициклический, насыщенный гетероцикл с 6, 7, 8, 9, 10 или 11 кольцевыми атомами в общем, в котором два кольца делят один общий атом углерода, где "гетероспироциклоалкил" содержит один или два идентичных или различных кольцевых гетероатома из ряда: N, О, S; причем, возможно, указанная гетероспироциклоалкильная группа присоединена к остатку молекулы через любой один из атомов углерода, за исключением спиро атома углерода, или, если присутствует, атома азота.
Указанная гетероспироциклоалкильная группа представляет собой, например, азаспиро[2.3]гексил, азаспиро[3.3]гептил, оксаазаспиро[3.3]гептил, тиаазаспиро[3.3]гептил, оксаспиро[3.3]гептил, оксазаспиро[5.3]нонил, оксазаспиро[4.3]октил, оксазаспиро[2.5]октил, азаспиро[4.5]децил, оксазаспиро [5.5] ундецил, диазаспиро [3.3] гептил, тиазаспиро [3.3] гептил, тиазаспиро[4.3]октитл, азаспиро[5.5]ундецил, или один из других гомологичных вриантов, таких как спиро[3.4]-, спиро[4.4]-, спиро[2.4]-, спиро[2.5]-, спиро[2.6]-, спиро[3.5]-, спиро[3.6]-, спиро[4.5]- и спиро[4.6]-.
Термин "6- или 10-ти членный арил" означает моновалентное, моноциклическое или бициклическое ароматическое кольцо, имеющее 6 или 10 кольцевых атомов углерода, например, фенильную или нафтильную группу.
Термин "гетероарил" означает моновалентное, моноциклическое, бициклическое или трициклическое ароматическое кольцо, имеющее 5, 6, 9 или 10 кольцевых атомов ("5-10-ти членная гетероарильная" группа), в частности 5 или 6 кольцевых атомов ("5- 6-ти членная гетероарильная" группа), которая содержит по меньшей мере один кольцевой гетероатом и необязательно один, два или три других кольцевых гетероатомов из ряда: N, О и/или S, и которая связана через кольцевой атом углерода или необязательно через кольцевой атом азота (если допускается валентностью).
Указанная гетероарильная группа может представлять собой 5-ти членную гетероарилую группу, такую как, например, тиенил, фуранил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, оксадиазолил, триазолил, тиадиазолил или тетразолил; или 6-ти членную гетероарильную группу, такую как, например, пиридинил, дигидропиридинил, пиридазинил, пиримидинил, тетрагидропиримидинил, пиразинил или триазинил.
Термин "гетероциклил" означает гетероцикл, выбранный из группы, состоящей из гетероциклоалкила и гетероарила. В частности, термин "4-6-ти членный гетероциклил" означает гетероцикл, выбранный из группы, состоящей из 4-6-ти членный гетероциклоалкил, и 5- 6-ти членного гетероарила.
В общем случае и, если не указано иное, гетероарильные или гетероариленовые группы включают все их возможные изомерные формы, например: таутомеры и позиционные изомеры относительно точки соединения с остальной частью молекулы. Таким образом, для некоторых иллюстративных неограничивающих примеров термин пиридинил включает пиридин-2-ил, пиридин-3-ил и пиридин-4-ил; или термин тиенил включает тиен-2-ил и тиен-3-ил.
Термин "С1-С4", как применяется в описании настоящего изобретения, например, в контексте определения "С1-С4-алкил", "С1-С4-галогеноалкил", "С1-С4-гидроксиалкил", "С1-С4-алкокси" или "С1-С4-галогеноалкокси" означает алкильную группу, имеющую конечное число атомов углерода от 1 до 4, т.е. 1, 2, 3 или 4 атома углерода.
Кроме того, как применяется в настоящей заявке, термин "С3-С6", как применяется в описании настоящего изобретения, например, в контексте определения "С3-С6-циклоалкил" или С3-С6-галогенциклоалкил, означает циклоалкильную группу, имеющую конечное число атомов углерода от 3 до 6, т.е. 1, 2, 3, 4, 5 или 6 атомов углерода.
Когда задан диапазон значений, указанный диапазон охватывает каждое значение и поддиапазон в указанном диапазоне.
Например:
"С1-С4" охватывает С1, С2, С3, С4, С1-С4, С1-С3, С1-С2, С2-С4, С2-С3, и С3-С4;
"С2-С6" охватывает С2, С3, С4, С5, С6, C2-C6, C2-C5, С2-С4, С2-С3, C3-C6, C3-C5, С3-С4, C4-C6, С4-С5, и С5-С6;
"С3-С4" охватывает С3, С4, и С3-С4;
"С3-С10" охватывает С3, С4, С5, С6, С7, С8, С9, С10, С3-С10, С3-С9, С3-С8, С3-С7, С3-С6, С3-С5, С3-С4, С4-С10, С4-С9, С4-С8, С4-С7, C4-C6, С4-С5, С5-С10, С5-С9, С5-С8, С5-С7, С5-С6, C6-С10, С6-С9, C6-C8, С6-С7, С7-С10, С7-С9, С7-С8, С8-С10, С8-С9 и С9-С10;
"С3-С8" охватывает С3, С4, С5, С6, С7, С8, С3-С8, С3-С7, С3-С6, С3-С5, С3-С4, С4-С8, С4-С7, С4-С6, С4-С5, С5-С8, С5-С7, С5-С6, С6-С8, С6-С7 и С7-С8;
"С3-С6" охватывает С3, С4, С5, С6, С3-С6, С3-С5, С3-С4, С4-С6, С4-С5, и С5-С6;
"С4-С8" охватывает С4, С5, С6, С7, С8, С4-С8, С4-С7, С4-С6, С4-С5, С5-С8, С5-С7, С5-С6, С6-С8, С6-С7 и С7-С8;
"С4-С7" охватывает С4, С5, С6, С7, С4-С7, С4-С6, С4-С5, С5-С7, С5-С6 и С6-С7; "С4-С6" охватывает С4, С5, С6, C4-C5, C4-C5 и С5-С6;
"С5-С10" охватывает С5, C6, С7, C8, С9, С10, С5-С10, С5-С9, C5-C8, С5-С7, С5-С6, С6-С10, С6-С9, C6-C8, С6-С7, С7-С10, С7-С9, С7-С8, С8-С10, С8-С9 и С9-С10;
"C6-C10" охватывает C6, С7, C8, С9, С10, C6-С10, С6-С10, С6-C9, С6-С7, С7-С10, С7-С9, С7-С8, C8-С10, C8-C9 и С9-С10.
Как применяется в описании настоящего изобретения, термин "уходящая группа" означает атом или группу атомов, которая замещается в ходе химической реакции в виде стабильной группы, взятой вместе со связывающими электронами. В частности, такая уходящая группа выбрана из группы, содержащей: галогенид, в частности фторид, хлорид, бромид или иодид, (метилсульфонил)окси, [(трифторметил)сульфонил]окси, [(нонафторбутил)сульфонил]окси, (фенилсульфонил)окси, [(4-метилфенил)сульфонил]окси, [(4-бромфенил)сульфонил]окси, [(4-нитрофенил)сульфонил]окси, [(2-нитрофенил)сульфонил]окси, [(4-изопропилфенил)сульфонил]окси, [(2,4,6-триизопропилфенил)сульфонил]окси, [(2,4,6-триметилфенил)сульфонил]окси, [(4-трет-бутилфенил)сульфонил]окси и [(4-метоксифенил)сульфонил]окси.
Оксо заместитель в контексте настоящего изобретения означает атом кислорода, который связан с атомом углерода через двойную связь.
Для соединений общей формулы (I) возможно существование в виде изотопных вариантов. Поэтому настоящее изобретение включает один или более изотопных вариантов соединений общей формулы (I), в частности дейтерий-содержащие соединения общей формулы (I).
Термин "изотопный вариант" соединения или реагента определяется как соединение, проявляющее не существующую в природе долю одного или более изотопов, которые составляют такое соединение.
Термин "изотопный вариант соединения общей формулы (I)" определяется как соединение общей формулы (I), проявляющее не существующую в природе долю одного или более изотопов, которые составляют такое соединение.
Выражение "не существующая в природе доля" означает долю такого изотопа, которая выше, чем его содержание в природе. Содержания в природе изотопов, применяемые в этом контексте, описаны в "Isotopic Compositions of the Elements 1997", Pure Appl. Chem., 70(1), 217-235, 1998.
Примеры таких изотопов включают стабильные и радиоактивные изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, хлора, брома и иода, как например 2Н (дейтерий), 3Н (тритий), 11C, 13С, 14С, 15N, 17O, 18O, 32Р, 33Р, 33S, 34S, 35S, 36S, 18F, 36Cl, 82Br, 123I, 124I, 125I, 129I, 131I, соответственно.
В отношении лечения и/или профилактики нарушений, указанных в настоящей заявке, изотопный вариант (варианты) соединений общей формулы (I) предпочтительно содержат дейтерий ("дейтерий-содержащие соединения общей формулы (I)"). Изотопные варианты соединений общей формулы (I), в которых один или более радиоактивных изотопов, таких как 3Н или 14С, включены, полезны, например, при исследованиях распределения лекарственного средства и/или субстрата в тканях. Эти изотопы, в частности, предпочтительны из-за легкости их включения и обнаружения. Позитронно-активные изотопы, такие как 18F или 11С, могут быть включены в соединение общей формулы (I). Эти изотопные варианты соединения общей формулы (I) полезны для применений in vivo визуализации. Дейтерий-содержащие и 13С-содержащие соединения общей формулы (I) могут применяться в анализах масс-спектрометрии в контексте преклинических или клинических исследований.
Изотопные варианты соединений общей формулы (I) обычно могут быть получены способами, известными специалисту в данной области, такими как описанные в схемах и/или примерах в описании настоящего изобретения, путем замещения реагента на изотопный вариант указанного реагента, предпочтительно на дейтерий-содержащий реагент. В зависимости от желаемых сайтов дейтерирования, в некоторых случаях дейтерий из D2O может быть включен либо непосредственно в соединения, либо в реагенты, которые полезны для синтеза таких соединений. Дейтерий в виде газа также является полезным реагентом для включения дейтерия в молекулы. Каталитическое дейтерирование олефиновых связей и ацетильных связей представляет собой быстрый путь для включения дейтерия. Катализаторы на основе металлов (то есть Pd, Pt, и Rh) в присутствии дейтерия в виде газа могут быть использованы для непосредственного обмена дейтерия на водород в функциональных группах, содержащих углеводороды. Различные дейтерированные реагенты и синтетические строительные блоки коммерчески доступны от таких компаний, таких как, например, C/D/N Isotopes, Quebec, Canada; Cambridge Isotope Laboratories Inc., Andover, MA, USA; и CombiPhos Catalysts, Inc., Princeton, NJ, USA.
Термин "дейтерий-содержащее соединение общей формулы (I)" определяется как соединение общей формулы (I), в которых один или более атомов водорода замещены одним или более атомами дейтерия, и в которых содержание дейтерия в таком дейтерированном положении соединения общей формулы (I) выше, чем содержание дейтерия в природе, которое составляет около 0.015%. В частности, в дейтерий-содержащем соединении общей формулы (I) содержание дейтерия в каждом дейтерированном положении соединения общей формулы (I) составляет более 10%, 20%, 30%, 40%, 50%, 60%, 70% или 80%, предпочтительно более 90%, 95%, 96% или 97%, даже более предпочтительно более 98% или 99% в указанном положении (положениях). Понятно, что содержание дейтерия в каждом дейтерированном положении не зависит от содержания дейтерия в другом дейтерированном положении (положениях).
Селективное включение одного или более атомов дейтерия в соединение общей формулы (I) может изменять физико-химические свойства (такие как, например, кислотность [С.L. Perrin, et al., J. Am. Chem. Soc., 2007, 129, 4490], основность [С.L. Perrin et al., J. Am. Chem. Soc., 2005, 127, 9641], липофильность [В. Testa et al., Int. J. Pharm., 1984, 19(3), 271]) и/или метаболический профиль молекулы и может приводить к изменениям соотношения родоначального соединения и метаболитов или количеств образованных метаболитов. Такие изменения могут приводить к определенным терапевтическим преимуществам и следовательно могут быть предпочтительны в некоторых применениях. Уменьшенные скорости метаболизма и выключение метаболизма, при которых соотношение метаболитов изменяется, описаны (А.Е. Mutlib et al., Toxicol. Appl. Pharmacol., 2000, 169, 102).
Эти изменения при воздействии родоначального лекарственного средства и метаболитов могут иметь важные последствия в отношении фармакодинамики, переносимости и эффективности дейтерий-содержащего соединения общей формулы (I). В некоторых случаях замещение на дейтерий уменьшает или исключает образование нежелательного или токсичного метаболита и усиливает образование желаемого метаболита (например, Nevirapine: А.М. Sharma et al., Chem. Res. Toxicol., 2013, 26, 410; Efavirenz: A.E. Mutlib et al., Toxicol. Appl. Pharmacol., 2000, 169, 102). В других случаях основной эффект дейтерирования состоит в уменьшении скорости системного клиренса. В результате биологический период полувыведения соединения увеличивается. Потенциальные клинические преимущества будут включать способность поддерживать подобное системное воздействие с уменьшенными пиковыми уровнями и повышенными остаточными уровнями. Это может привести к снижению побочных эффектов и повышению эффективности, в зависимости от конкретного фар мако кинетического/фармакодинамического взаимоотношения конкретного соединения. ML-337 (С.J. Wenthur et al., J. Med. Chem., 2013, 56, 5208) и Odanacatib (K. Kassahun et al., WO 2012/112363) являются примерами этого эффекта дейтерия. Сообщалось также о других случаях, при которых сниженные скорости метаболизма приводят к увеличению воздействия лекарственного средства без изменения скорости системного клиренса (например, Rofecoxib: F. Schneider et al., Arzneim. Forsch. / Drug. Res., 2006, 56, 295; Telaprevir: F. Maltais et al., J. Med. Chem., 2009, 52, 7993). Дейтерированные лекарственные средства, демонстрирующие этот эффект, могут иметь уменьшенные требования дозировки (например, меньшее количество доз или более низкая доза для достижения желаемого эффекта) и/или могут приводить к снижению метаболических нагрузок.
Соединение общей формулы (I) может иметь множество потенциальных сайтов воздействия на метаболизм. Для оптимизации вышеописанных эффектов по физико-химическим свойствам и метаболический профиль могут быть выбраны дейтерий-содержащие соединения общей формулы (I), имеющие определенную модель одного или более дейтерий-водородного обмена (обменов). В частности, атом(ы) дейтерия дейтерий-содержащего соединения (соединений) общей формулы (I) присоединяется/присоединяются к атому углерода и/или располагается/располагаются в тех положениях соединения общей формулы (I), которое являются сайтами воздействия на метаболизирующие ферменты, такие как, например, цитохром Р450.
Если в описании настоящего изобретения используется множественная форма слова соединения, соли, полиморфы, гидраты, сольваты и тому подобное, это означает также одно соединение, соль, полиморф, изомер, гидрат, сольват или тому подобное.
Под «стабильным соединением» или «стабильной структурой» понимается соединение, которое является достаточно устойчивым, чтобы выдержать выделение до полезной степени чистоты из реакционной смеси и состава в эффективный терапевтический агент.
Соединения согласно настоящему изобретению необязательно содержат один или более асимметричных центров, в зависимости от расположения и природы различных желаемых заместителей. Возможно, что в конфигурации присутствует один или более асимметричных атома углерода (R) или (S), что может привести к рацемическим смесям в случае одного асимметричного центра, и диастереомерным смесям в случае множества асимметричных центров. В некоторых случаях возможно, что асимметрия также присутствует из-за ограниченного вращения вокруг данной связи, например, центральной связи, примыкающей к двум замещенным ароматическим кольцам указанных соединений.
Предпочтительными соединениями являются соединения, которые обеспечивают более желательную биологическую активность. Отделенные, чистые или частично очищенные изомеры и стереоизомеры, или рацемические или диастереомерные смеси соединений согласно настоящему изобретению также включены в объем настоящего изобретения. Очистка и разделение таких материалов могут быть выполнены стандартными методами, известными в данной области техники.
Предпочтительными изомерами являются те, которые обеспечивают более желательную биологическую активность. Эти отделенные, чистые или частично очищенные изомеры или рацемические смеси соединений согласно настоящему изобретению также включены в объем настоящего изобретения. Очистка и разделение таких материалов могут быть выполнены стандартными методами, известными в данной области техники.
Оптические изомеры могут быть получены путем разделения рацемических смесей в соответствии с обычными способами, например, путем образования диастереоизомерных солей с использованием оптически активной кислоты или основания или образования ковалентных диастереомеров. Примерами подходящих кислот являются винная, диацетилвинная, дитолуоилвинная и камфоросульфоновая кислота. Смеси диастереоизомеров могут быть разделены на их отдельные диастереомеры на основе их физических и/или химических различий с помощью способов, известных в данной области, например, путем хроматографии или фракционной кристаллизации. Оптически активные основания или кислоты затем высвобождаются из отделенных диастереомерных солей. Различные способы разделения оптических изомеров включают применение хиральной хроматографии {например, ВЭЖХ колонки с применением хиральной фазы), с или без обычной дериватизации, необязательно выбранной для максимизации разделения энантиомеров. Стабильные ВЭЖХ колонки с применением хиральной фазы являются коммерчески доступными, такие как произведенные компанией Daicel, например, Chiracel OD и Chiracel OJ, например, среди многих других, которые все доступны для выбора рутинным путем. Ферментативные разделения, с или без дериватизации, также применяются. Оптически активные соединения согласно настоящему изобретению могут подобным образом быть получены посредством хиральных синтезов, применяя оптически активные исходные вещества.
Чтобы различать различные типы изомеров друг от друга, делается ссылка на Правила IUPAC часть Е (Pure Appl Chem 45, 11-30, 1976).
Настоящее изобретение включает все возможные стереоизомеры соединений согласно настоящему изобретению, в виде отдельных стереоизомеров, или в виде любой смеси указанных стереоизомеров, например, (R) - или (S) - изомеров в любом соотношении. Выделение одного стереоизомера, например, одного энантиомера или одного диастереомера соединения согласно настоящему изобретению, достигается с помощью любого подходящего способа из уровня техники, такого как хроматография, особенно хиральная хроматография, например.
Кроме того, соединения согласно настоящему изобретению могут существовать в виде таутомеров. Например, любое соединение согласно настоящему изобретению, которое содержит модель замещения, приводящую к α-СН-- составляющей при хинолине, которая имеет повышенную СН-кислотность, может существовать в виде таутомера 1,4-дигидрохинолина или даже смеси в любом количестве двух таутомеров, а именно:
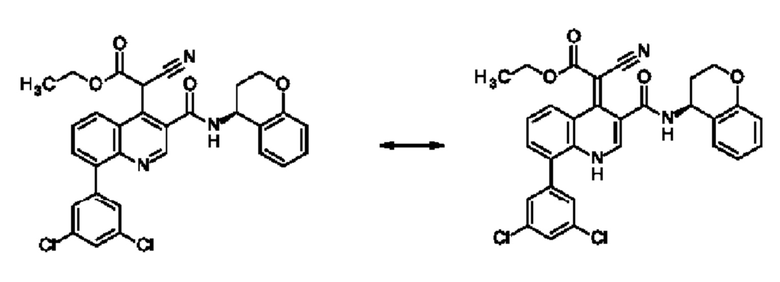
Настоящее изобретение включает все возможные таутомеры соединений согласно настоящему изобретению в виде отдельных таутомеров, или в виде любой смеси указанных таутомеров, при любом соотношении.
Кроме того, соединения согласно настоящему изобретению могут существовать как N-оксиды, которые определяются тем, что по меньшей мере один атом азота соединений согласно настоящему изобретению окислен. Настоящее изобретение включает все такие возможные N-оксиды.
Настоящее изобретение также охватывает полезные формы соединений согласно настоящему изобретению, такие как метаболиты, гидраты, сольваты, пролекарства, соли, в частности фармацевтически приемлемые соли и/или сопреципитаты.
Соединения согласно настоящему изобретению могут существовать в виде гидрата или в виде сольвата, когда соединения согласно настоящему изобретению содержат полярные растворители, в частности воду, метанол или этанол, например, в качестве структурного элемента кристаллической решетки соединений. Количество полярных растворителей, в частности воды, может находиться при стехиометрическом или нестехиометрическом соотношении. В случае стехиометрических сольватов, например, гидрата, геми-, (полу-), моно-, сескви-, ди-, три-, тетра-, пента- и т.д. сольваты или гидраты, соответственно, возможны. Настоящее изобретение включает все такие гидраты или сольваты.
Кроме того, соединения согласно настоящему изобретению могут существовать в свободной форме, например, в виде свободного основания или в виде свободной кислоты, или в виде цвиттериона, или могут существовать в форме соли. Указанной солью может быть любая соль, либо органическая, либо неорганическая аддитивная соль, в частности любая фармацевтически приемлемая органическая или неорганическая аддитивная соль, которая стандартным образом применяется в фармацевтике, или которая применяется, например, для выделения или очистки соединений согласно настоящему изобретению.
Термин "фармацевтически приемлемая соль" относится к неорганической или органической соли кислотного добавления соединения согласно настоящему изобретению. Например, смотрите S.М. Berge, et at. "Pharmaceutical Salts," J. Pharm. Sci. 1977, 66, 1-19.
Подходящая фармацевтически приемлемая соль соединений согласно настоящему изобретению может представлять собой, например, соль кислотного добавления соединения согласно настоящему изобретению, несущего атом азота в цепи или в кольце, например, которое является достаточно основным, как например соль кислотного добавления с неорганической кислотой или "минеральной кислотой", такой как соляная, бромистоводородная, иодистоводородная, серная, сульфаминовая, бисерная, фосфорная или азотная кислота, например, или с органической кислотой, такой как муравьиная, уксусная, ацетоуксусная, пировиноградная, трифторуксусная, пропионовая, масляная, гексановая, гептановая, ундекановая, лауриновая, бензойная, салициловая, 2- (4-гидроксибензоил)-бензойная, камфорная, коричная, циклопентанпропионовая, диглюконовая, 3-гидрокси-2-нафтойная, никотиновая, памовая, пектиновая, 3-фенапропионовая, пивалиновая, 2-гидроксиэтансульфоновая, итаконовая, трифторметансульфоновая, додецилсульфоновая, этансульфоновая, бензолсульфоновая, пара-толуолсульфоновая, метансульфоновая, 2-нафталинсульфоновая, нафталиндисульфоновая, камфорсульфоновая, лимонная, винная, стеариновая, молочная, щавелевая, малоновая, янтарная, яблочная, адипиновая, альгиновая, малеиновая, фумаровая, D-глюконовая, миндальная, аскорбиновая, глюкогептановая, глицерофосфорная, аспарагиновая, сульфосалициловая или тиоциановая кислота, например.
Кроме того, другой подходящей фармацевтически приемлемой солью соединения согласно настоящему изобретению, которое является достаточно кислотным, является соль щелочного металла, например соль натрия или калия, соль щелочноземельного металла, например кальция, магния или стронция, или соль алюминия или цинка, или аммониевая соль, производная от аммиака или от органического первичного, вторичного или третичного амина, имеющего от 1 до 20 атома углерода, как например этиламин, диэтиламин, триэтиламин, этилдиизопропиламин, моноэтаноламин, диэтаноламин, триэтаноламин, дициклогексиламин, диметиламиноэтанол, диэтиламиноэтанол, трис(гидроксиметил)аминометан, прокаин, дибензиламин, N-метилморфолин, аргинин, лизин, 1,2-этилендиамин, N-метилпиперидин, N-метил-глюкамин, N,N-диметил-глюкамин, N-этил-глюкамин, 1,6-гександиамин, глюкозамин, саркозин, серинол, 2-амино-1,3-пропандиол, 3-амино-1,2-пропандиол, 4-амино-1,2,3-бутантриол, или соль с четвертичным ионом аммония, имеющую от 1 до 20 атомов углерода, как например тетраметиламмоний, тетраэтиламмоний, тетра(н-пропил)аммоний, тетра(н-бутил)аммоний, N-бензил-N,N,N-триметиламмоний, холин или бензалконий.
Специалистам в данной области техники также понятно, что кислотные аддитивные соли заявленных соединений могут быть получены реакцией соединений с подходящей неорганической или органической кислотой с помощью любого из ряда известных способов. Альтернативно, соли щелочных и щелочноземельных металлов кислотных соединений согласно настоящему изобретению получают путем взаимодействия соединений согласно настоящему изобретению с соответствующим основанием с помощью множества известных способов.
Настоящее изобретение включает все возможные соли соединений согласно настоящему изобретению в виде отдельных солей, или в виде любой смеси указанных солей, в любом соотношении.
В описании настоящего изобретения, в частности в Экспериментальной части, для синтеза промежуточных соединений и примеров согласно настоящему изобретению, когда соединение упоминается в форме соли с соответствующим основанием или кислотой, точный стехиометрический состав указанной солевой формы, в виде, полученным посредством соответствующего способа получения и/или очистки, в большинстве случаев неизвестен.
Если не указано иное, суффиксы в химических названиях или структурных формулах, относящихся к солям, такие как «гидрохлорид», «трифторацетат», «натриевая соль» или «х HCl», «х CF3COOH», «х Na+», например, означают форму соли, где стехиометрия формы соли не уточняется.
Это относится аналогичным образом к случаям, когда промежуточные соединения или примерные соединения или их соли были получены посредством описанных способов получения и/или очистки, в виде сольватов, таких как гидраты, с (если определено) неизвестным стехиометрическим составом.
Кроме того, настоящее изобретение включает все возможные кристаллические формы, или полиморфы соединений согласно настоящему, изобретению либо в виде отдельного полиморфа, либо в виде смеси более одного полиморфа, при любом соотношении.
Кроме того, настоящее изобретение также включает пролекарства соединений согласно настоящему изобретению. Термин «пролекарства» в контексте настоящего изобретения означает соединения, которые сами по себе могут быть биологически активными или неактивными, но превращаются (например, метаболически или гидролитически) в соединения согласно настоящему изобретению во время их пребывания в организме.
В соответствии со вторым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (Т), выше, в которой:
А представляет собой А1 или А2,
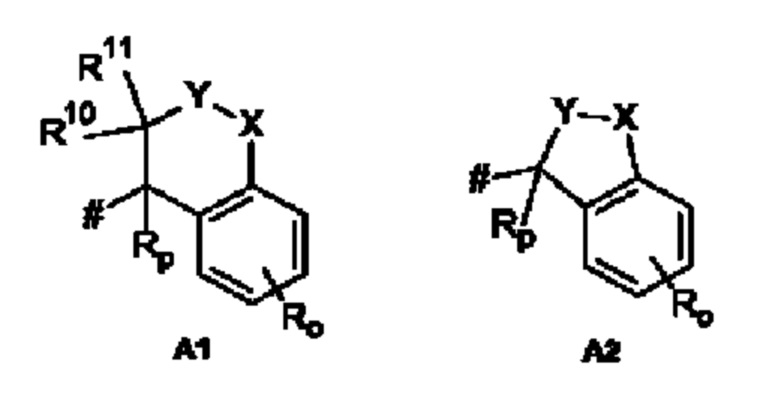
о представляет собой 0, 1, 2, 3 или 4,
R выбирают из группы, состоящей из водорода, галогена, циано, нитро, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(C1-С4-алкила), -N[(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-C1-С4-галогеналкила, -S(O)-С1-С4-галогеналкила и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, S, и N-R9, где по меньшей мере один из X и Y представляет собой CR7R8, или
X, Y образуют вместе член кольца, выбранный из группы, состоящей из -С(О)-О-, -C(O)-NR9-, -S(O)-NR9-, -SO2-NR9- и -SO2-О-,
R1 выбирают из группы, состоящей из водорода, циано, -СНО, -ОН, С1-С4-алкила, C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, С3-С6-галогенциклоалкила, имеющего от 1 до 5 атомов галогена, С3-С4-алкенила, С3-С4-алкинила, С1-С4-алкокси-С1-С4-алкила, С3-С6-циклоалкил-С1-С3-алкила, циано-С1-С4-алкила, -NH-С1-С4-алкила, -N(С1-С4-алкила)2, NH2-С1-С4-алкила-, С1-С4-алкила-NH-С1-С4-алкила-, (C1-С4-алкила)2N-С1-С4-алкила-, С1-С4-алкил-С(O)-, С1-С4-галогеналкил-С(O)-, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси-С(O)-, бензилокси-С(О)-, С1-С4-алкокси-С1-С4-алкил-С(O)-, -SO2-С1-С4-алкила, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенил-С1-С4-алкила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R2 выбирают из группы, состоящей из
водорода, галогена, циано, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(О)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-С6-алкила, С3-С6-циклоалкила, С2-С4-алкенила, С3-С6-циклоалкенила, С2-С4-алкинила или фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-алкил-С(О)-, С1-С4-алкокси-С(O)-, -C(O)-NH2, -C(O)-NH(C1-C4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(С(O)-С1-С4-алкила), -Н(С1-С4-алкил)(С(O)-С1-С4-алкила), -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)г, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-алкил-С(O)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-алкокси-С1-С4-алкила-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,-SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и 4-10-ти членного гетероциклоалкила,
R3 представляет собой водород или С1-С4-алкил,
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R7 выбирают из группы, состоящей из водорода, -ОН, фтора, С1-С4-алкила и С1-С4-алкокси,
R8 выбирают из группы, состоящей из водорода, -ОН, фтора, С1-С4-алкила и С1-С4-алкокси,
или R7 и R8 вместе образуют оксо группу (=O),
R9 выбирают из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и С1-С4-алкокси,
R10 выбирают из группы, состоящей из водорода, -ОН, С1-С4-алкила и С1-С4-алкокси,
R11 выбирают из группы, состоящей из водорода, С1-С4-алкила и С1-С4-алкокси,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -ОН, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(-C(O)-C1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, -N(С1-С4-алкил)-(-С(O)-С1-С4-алкила), С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными
из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
-NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-С2алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена;
фенила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными
из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -C(O)-NH(C1-C4-алкила), -C(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
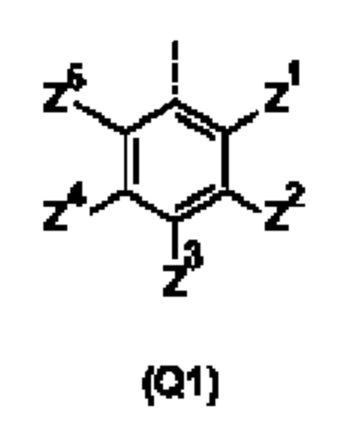
в которой:
Z1, Z2, Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, SF5, циано, -ОНО, нитро, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, С1-С4-алкокси, С3-С6-циклоалкил-С1-С4-алкокси, циано-C1-C4-алкокси, С1-С4-галогеналкокси, имеющнго от 1 до 5 атомов галогена, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH-SO2-(С1-С4-алкила), -N(SO2-[С1-С4-алкил])(С1-С4-алкила), (C1-C4-алкоксиимино)-С1-С4-алкила, 4-6-ти членного гетероциклила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -СН2-O-(С1-С4-алкила), -СН2-NH(С1-С4-алкила), -СН2-N(C1-С4-алкила)2, метила, замещенного 4-6-ти членным гетероциклилом, который сам по себе необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -СН2-S-(С1-С4-алкила), -СН2-S(O)-(С1-С4-алкила), -СН2-SO2-(С1-С4-алкила), -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(C1-C4-алкила), -S-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -CONH(С1-С4-алкила), -CONH(С3-С6-циклоалкила), -NHCO(С1-С4-алкила), -NHCO(С3-С6-циклоалкила), -NHCO(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они связаны, 5-ти или 6-ти членное насыщенное или частично насыщенное гетероциклическое кольцо, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых может быть необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, SF5, циано, СНО, нитро, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, C1-С4-алкокси, С3-С6-циклоалкил-С1-С4-алкокси, циано-С1-С4-алкокси, С1-С4-алкокси-С(O)-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH-SO2-(С1-С4-алкил), -N(SO2-[С1-С4-алкил])(С1-С4-алкила), (C1-C4-алкоксиимино)-С1-С4-алкила, 4-6-ти членного гетероциклоалкила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, метила или циано, -СН2-O-(С1-С4-алкила), -СН2-NH(С1-С4-алкила), -СН2-N(С1-С4-алкила)2, метила, замещенного 4-6-ти членным гетероциклоалкилом, который сам по себе необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, метила или циано, -СН2-S-(С1-С4-алкила), -СН2-S(O)-(С1-С4-алкила), -СН2-SO2-(С1-С4-алкила), -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(C1-C4-алкила), -S-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -CONH(С1-С4-алкила), -CONH(С3-С6-циклоалкила), NHCO(С1-С4-алкила), -NHCO(С3-С6-циклоалкила), -NHCO(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Z2 и Z3 образуют вместе с атомами углерода, с которыми они связаны, 5-ти или 6-ти членное насыщенное или частично насыщенное гетероциклическое кольцо, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z1, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, SF5, циано, СНО, нитро, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, C1-С4-алкокси, С3-С6-циклоалкил-С1-С4-алкокси, циано-С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, -NH-SO2-(С1-С4-алкила), -N(SO2-[C1-С4-алкил])(С1-С4-алкила), (С1-С4-алкоксиимино)-С1-С4-алкилаа, 4-6-ти членного гетероциклоалкила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, метила или циано, -СН2-O-(С1-С4-алкила), -СН2-NH(С1-С4-алкила), -СН2-N(С1-С4-алкила)2, метила, замещенного 4-6-ти членным гетероциклоалкилом, который сам по себе необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, метила или циано, -СН2-S-(С1-С4-алкила), -СН2-S(O)-(С1-С4-алкила), -СН2-SO2-(С1-С4-алкила), -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(С1-С4-алкила), -S-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -CONH(С1-С4-алкила), -CONH(С3-С6-циклоалкила), -NHCO(С1-С4-алкила), -NHCO(С3-С6-циклоалкила), -NHCO(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q2)
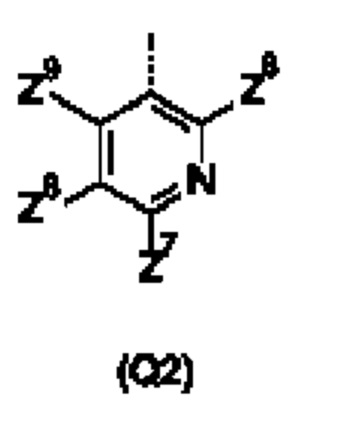
в которой:
Z6, Z7, Z8 и Z9 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой пиримидиновое кольцо формулы (Q3)
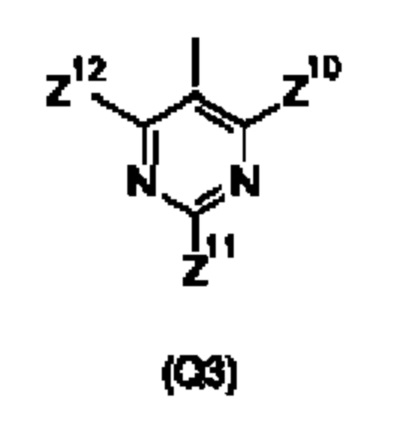
в которой:
Z10, Z11 и Z12 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
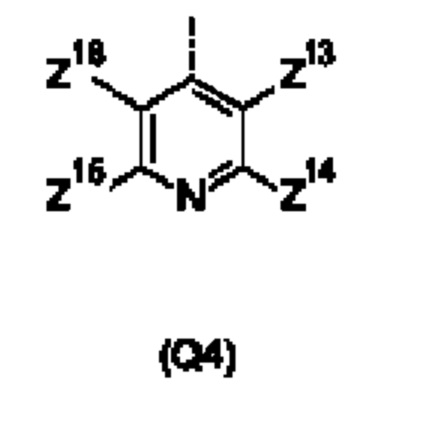
в которой:
Z13, Z14, Z15, Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С1-С4-гидроксиалкила, NH2, -NH(С1-С4-алкил), -N(С1-С4-алкил)2, -NH-CO-C1-С4-алкил, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, C1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(С1-С4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
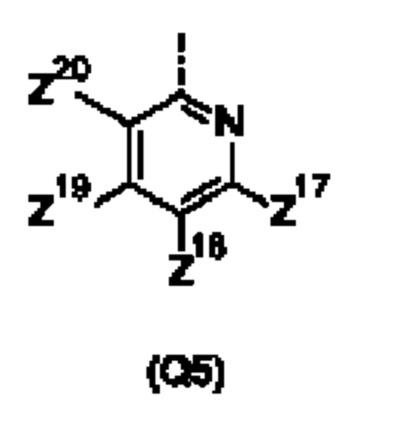
в которой:
Z17, Z18, Z19 и Z20 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющнго от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
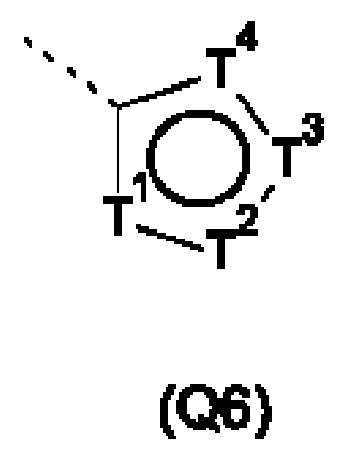
в которой:
Т1-Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1-Т4 представляет собой О, не более чем один из Т1-Т4 представляет собой S, не более чем один из Т1-Т4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, и
каждый Z22 независимо выбран из группы, состоящей из водорода, C1-C4-алкила, C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкил-C3-C6-циклоалкила, C1-C4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
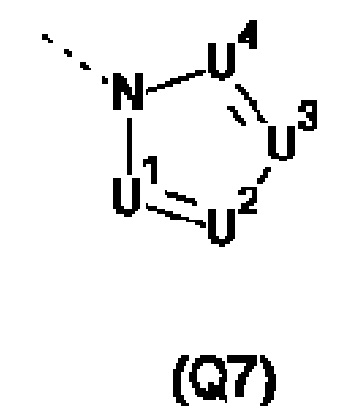
в которой:
U1-U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1-U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
где когда Y представляет собой О, S или N-R9, ни один из R7, R8, R10 и R11 не представляет собой -ОН, и где когда X представляет собой О, S или N-R9, ни один из R7 и R8 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с третьим вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
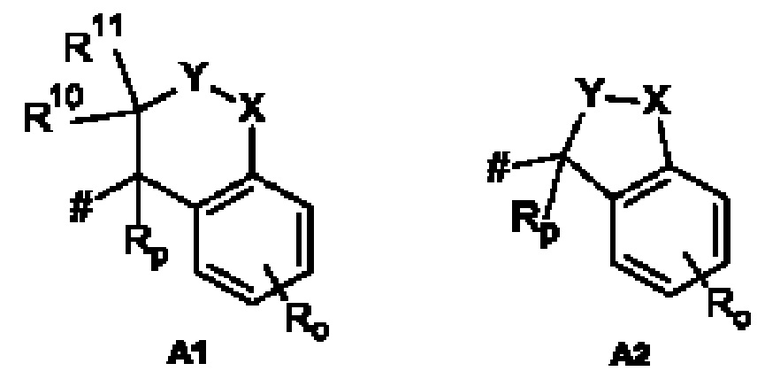
о представляет собой 0, 1 или 2,
R выбирают из группы, состоящей из галогена, C1-C4-алкила и C1-C4-алкокси, циано, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, S, и N-R9, где по меньшей мере один из X и Y представляет собой CR7R8,
R1 выбирают из группы, состоящей из водорода, С1-С4-алкила, C3-C6-циклоалкила, C3-С4-алкенила, C3-С4-алкинила, С1-С4-алкокси-С1-С4-алкила, C3-C6-циклоалкил-C1-C3-алкила, циано-С1-С4-алкила,
R2 выбирают из группы, состоящей из
водорода, галогена, циано, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(О)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
С1-С4-алкила, С3-С6-циклоалкила, С2-С4-алкенила, С3-С6-циклоалкенила, С2-С4-алкинила или фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(C(O)-C1-C4-алкила), -N(С1-С4-алкил)(С(O)-С1-С4-алкила), -S-С1-С4-алкила, -S(O)-C1-C4-алкила, -SO2-С1-С4-алкила, -S-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, C1-С4-алкила, C1-C4-алкил-С(О)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-алкокси-С1-С4-алкила-, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-C6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R3 представляет собой водород или С1-С4-алкил,
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2,
R7 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R8 выбирают из группы, состоящей из водорода и С1-С4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН, С1-С4-алкила и С1-С4-алкокси,
R11 представляет собой водород,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-С1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, C3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, -N(С1-С4-алкил)-(-С(O)-С1-С4-алкила), С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-C6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -SO2-C1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкил, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
фенил, бензо-С5-C6-циклоалкил, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклический или бициклический гетероцикл, выбранный из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
C1-C4-алкила, C3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-C6-циклоалкила; и гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
R15 выбирают из группы, состоящей из водорода;
C1-C4-алкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
Q представляет собой замещенное фенильное кольцо формулы (Q1)
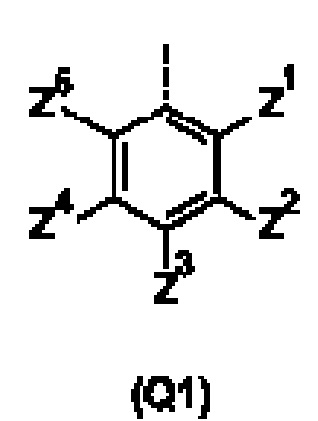
в которой:
Z1, Z2, Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, C1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, 4-6-ти членного гетероциклила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(С1-С4-алкила), или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они связаны, 5-или 6-членный гетероциклоалкил, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-алкокси-С(О)-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, или
Z2 и Z3 образуют вместе с атомами углерода, с которыми они связаны, 5-ти или 6-ти членное насыщенное или частично насыщенное гетероциклическое кольцо, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z1, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q2)
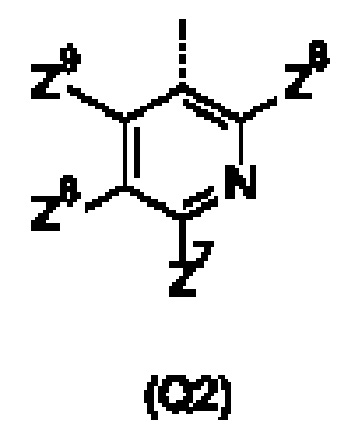
в которой:
Z6, Z7, Z8 и Z9 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -NH(С1-С4-алкила)2, или
Q представляет собой пиримидиновое кольцо формулы (Q3)
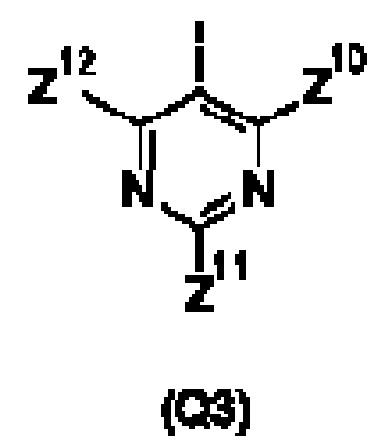
в которой:
Z10, Z11 и Z12 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-C4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
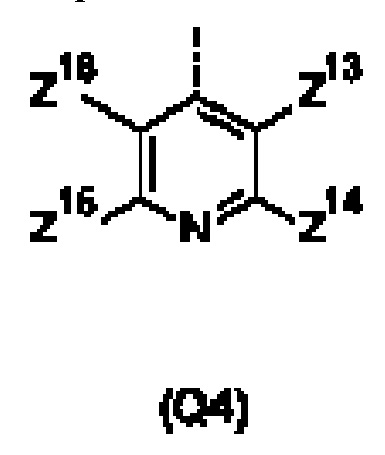
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С1-С4-гидроксиалкила, NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH-СО-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-C6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
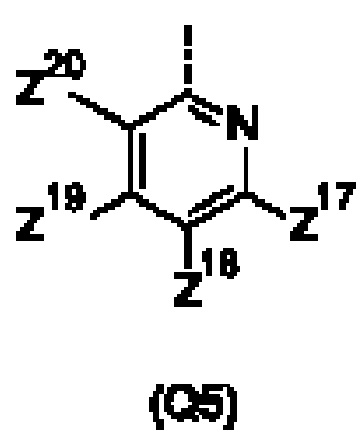
в которой:
Z17, Z18, Z19 и Z20 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
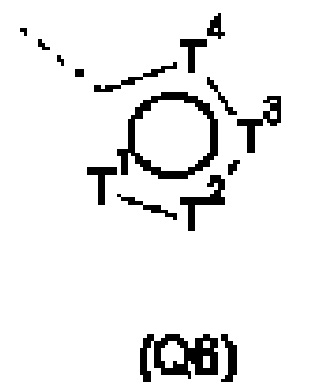
в которой:
T1-T4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1-Т4 представляет собой О, не более чем один из Т1-Т4 представляет собой S, не более чем один из T1-T4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-C3-C6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
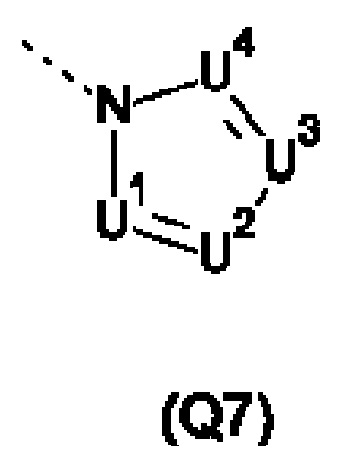
в которой:
U1-U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1-U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
где когда Y представляет собой О, S или N-R9, R10 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с четвертым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
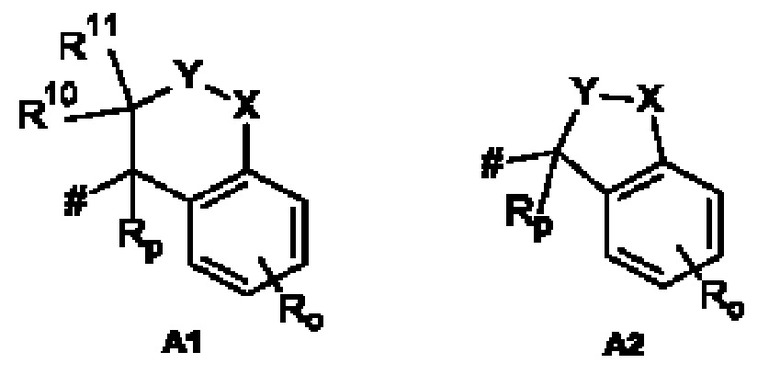
о представляет собой 0, 1 или 2,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X выбирают из группы, состоящей из CR7R8, О, S, и N-R9,
Y представляет собой CR7R8 или О,
R1 представляет собой водорода или С1-С4-алкил,
R2 выбирают из группы, состоящей из водорода, галогена, -C(O)-N(C1-C4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-С4-алкила, C3-C6-циклоалкила, С2-С4-алкенила или C3-C6-циклоалкенила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(O)- и -C(O)-NH2, С1-С4-алкокси, -NH2, -N(С1-С4-алкила)2, -N(С1-С4-алкил)(С(O)-С1-С4-алкила); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила, и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, -СООН, C1-C4-алкокси-С(O)-, -C(O)-NH2, C1-C4-алкила, С1-С4-алкил-С(O)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси-С1-С4-алкила-, С1-С4-алкокси-С1-С4-алкила-, -NH2, -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R3 представляет собой водород или C1-C4-алкил,
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH2,
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси,
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
R7 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R8 выбирают из группы, состоящей из водорода и C1-C4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН и С1-С4-алкила,
R11 представляет собой водород,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-С1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, C3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, С1-C4-алкила, С1-С4-алкокси, С3-С6-циклоалкила, -NH2, -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и С1-С4-алкокси;
фенила и бензо-С5-C6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
С1-С4-алкила, С3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, С1-С4-алкила, С1-С4-алкокси и C3-C6-циклоалкила; и
4-10-ти членного гетероциклоалкила,
R15 выбирают из группы, состоящей из водорода;
C1-C4-алкила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из -ОН и -СООН; и
6-ти членного гетероарила,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
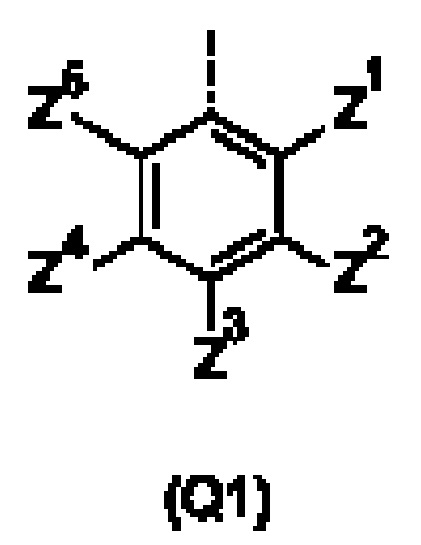
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, С1-С4-алкокси, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, -ОН, C1-С4-алкила, C1-С4-алкокси, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -S-(С1-С4-алкила) и 4-6-ти членного гетероциклоалкила, и
Z3 выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, и -N(С1-С4-алкила)2, или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они соединены, 5-ти членный гетероциклоалкил или 5-ти членный гетероарил, каждый из которых может быть необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо,
Z3 и Z5 представляют собой водород, и
Z4 выбирают из группы, состоящей из водорода и С1-С4-алкокси-С(O)-, или
Q представляет собой пиридиновое кольцо формулы (Q4)
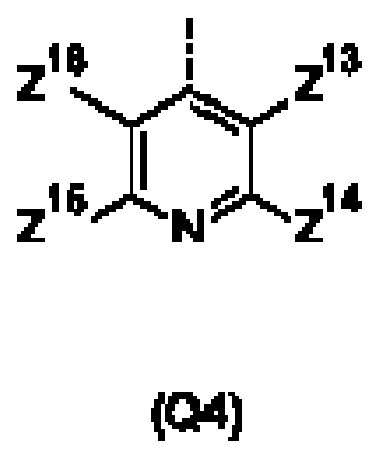
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-алкокси, С1-С4-гидроксиалкила, NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -NH-CO-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-С6-циклоалкила, -NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
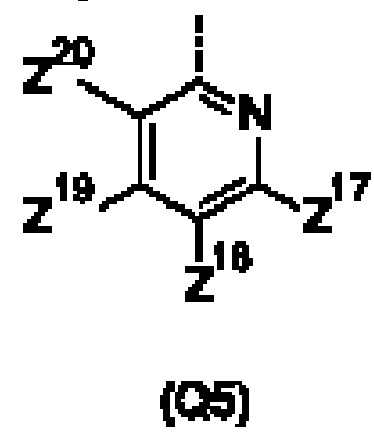
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой галоген, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
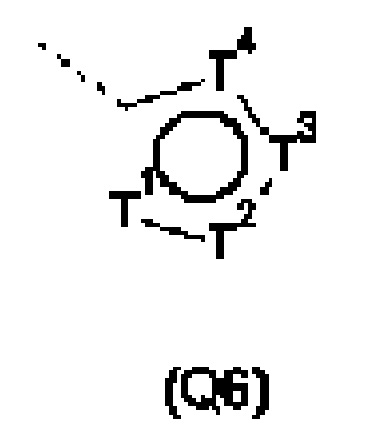
в которой:
Т1-Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1-Т4 представляет собой О, не более чем один из Т1-Т4 представляет собой S, не более чем один из Т1-Т4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-C3-C6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
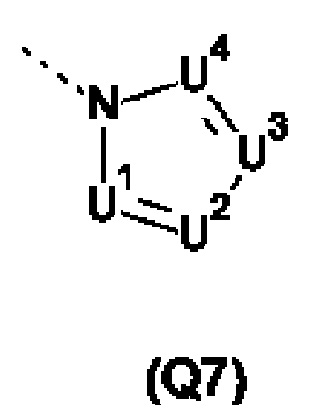
в которой:
U1-U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1-U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с пятым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
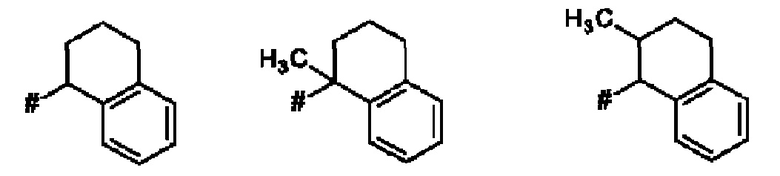
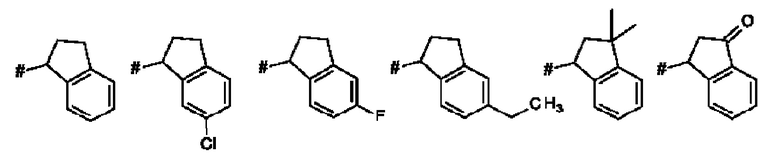
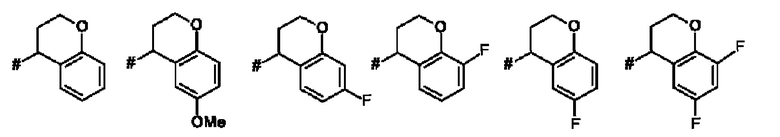
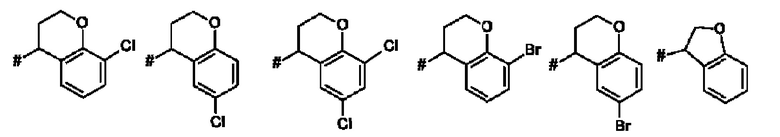
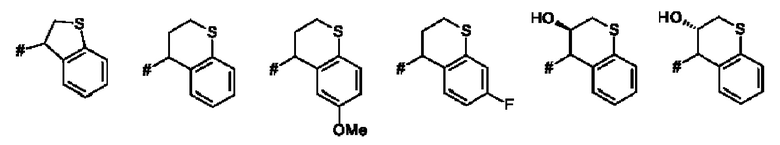

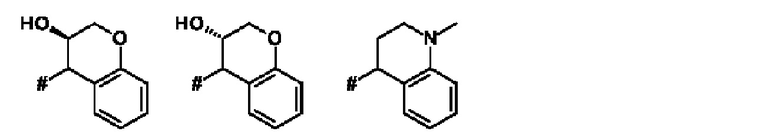
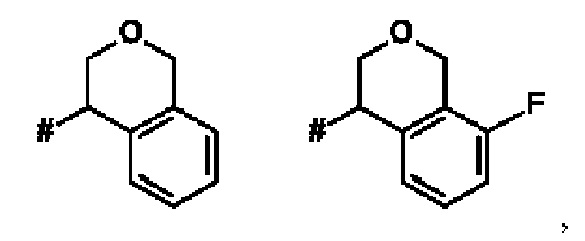
R1 представляет собой водород или метил,
R2 выбирают из группы, состоящей из
водорода, хлора, иода, -C(O)-N(CH3)2,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклобутила, циклопентила, циклогексила, этенила, пропенила, циклопентенила, циклогексенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из -ОН, циано, этокси-С(О)-, -С(O)-NH2, метокси, NH2, N(CH3)2, N(CH3)(C(O)CH3); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, оксетана, пирролидина, тетрагидрофурана, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропирана, тетрагидропиридина, дигидро-2H-пирана, 1,2-оксазолидина, 1,2-оксазина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидро-индола, 1,3-дигидро-изоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло[3.1.1]гептана, 8-окса-3-азабицикло[3.2.1]октана, тиофена, имидазола, пиразола, 1,2,4-триазола, 1,2,3-триазола, 1,2,3,4-тетразола, пиридина, дигидропиридина, пиримидина, тетрагидропиримидина, 4-окса-7-азаспиро[2.5]октана, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, циано, -ОН, оксо, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, метила, метил-С(О)-, дифторметила, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R3 представляет собой водород или метил,
R4 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, метокси, трифторметила, трифторметокси и NH2,
R5 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, метокси и трифторметила,
R6 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила и метокси,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-метила), метокси;
метила, этила, пропила, изопропила, бутила, изобутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, -C(O)-NMe2, -NH-С(O)-метил, метил, метокси, циклопропил, -NH2, NMe2, S-метил, S(O)-метил, SO2-метил, и (EtO)2Р(=O)-;
гетероциклил-метила, гетероциклил-этила, где гетероциклильный заместитель выбирают из группы, состоящей из оксетана, тетрагидрофурана, тетрагидропирана, пирролидина, морфолина, пиразола, имидазола, 1, 2, 4-оксадиазола, пиридина, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, хлора, -ОН, оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического или бициклического гетероцикла, выбранного из группы оксетана, тиетана, пирролидина, морфолина, тетрагидропирана, пиридина и пиразола, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, -ОН, оксо, метила;
R14 выбирают из группы, состоящей из
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, метила, метокси и циклопентила; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбирают из группы, состоящей из
метила и этила, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -ОН и -СООН; и
пиридина,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
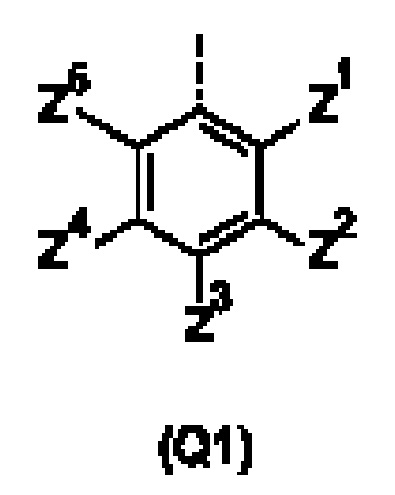
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила, трифторметила и метокси,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
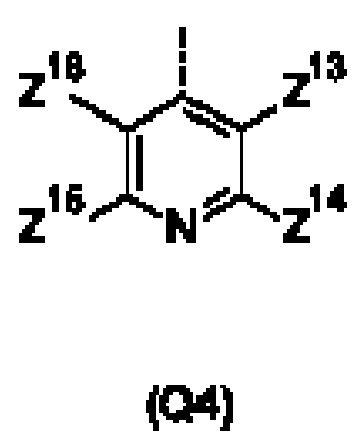
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, этокси, изопропокси, гидроксиметила, NH2, -NHMe -NMe2, -NH-C(O)-Me, морфолинила, или
Q представляет собой пиридиновое кольцо формулы (Q5)
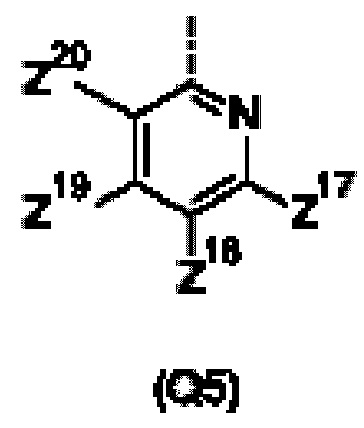
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой фтор, хлор, или
Q выбирают из группы, состоящей из
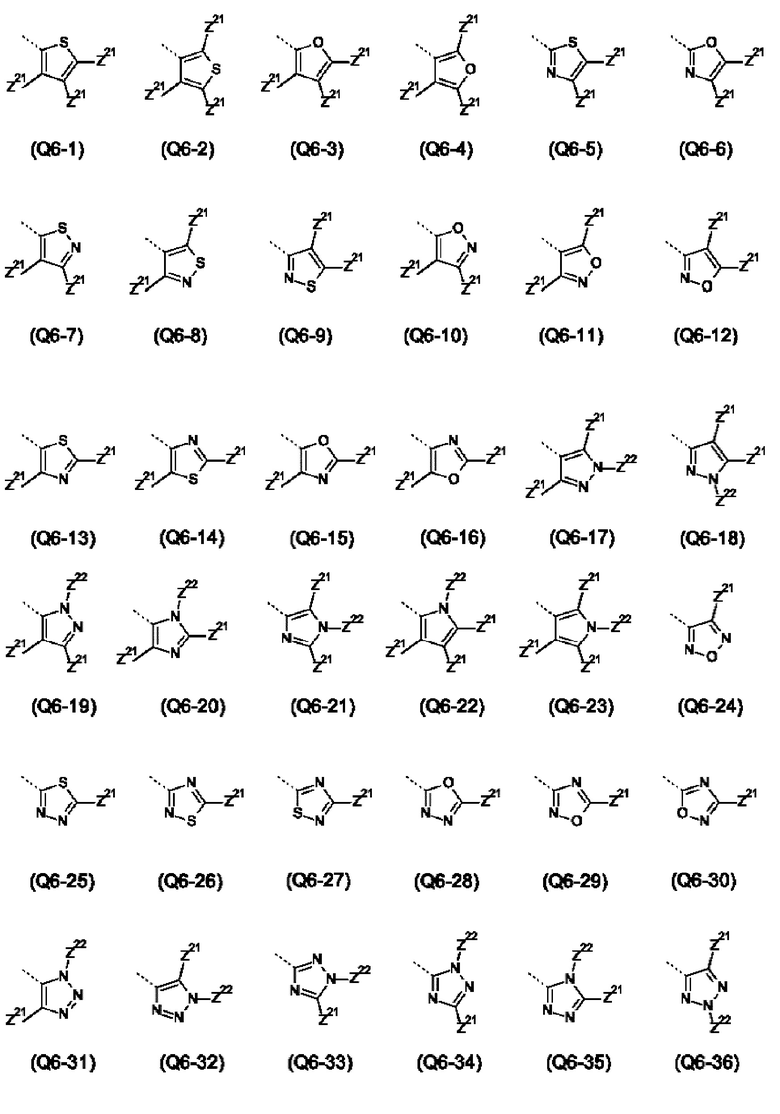
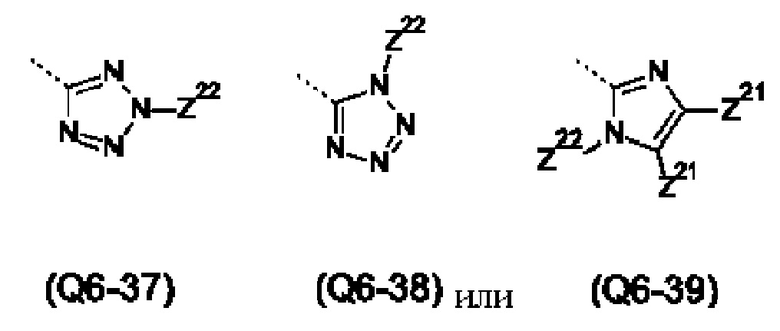
в которой:
каждый Z независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, метокси и
Z22 представляет собой водород, метил, или
Q выбирают из группы, состоящей из
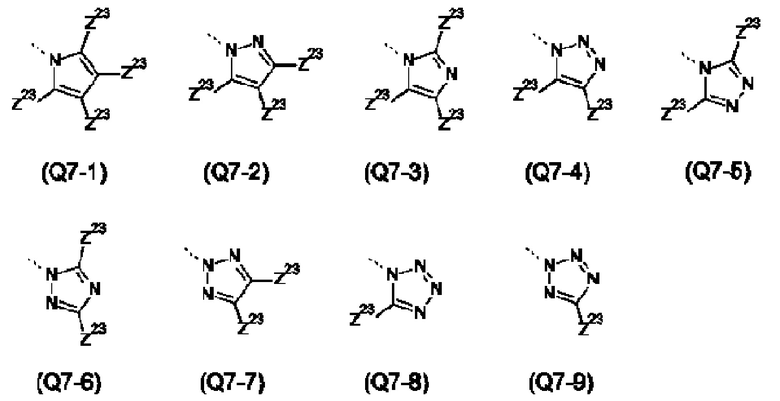
в которой:
каждый Z23 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, метокси, или
Q выбирают из группы, состоящей из
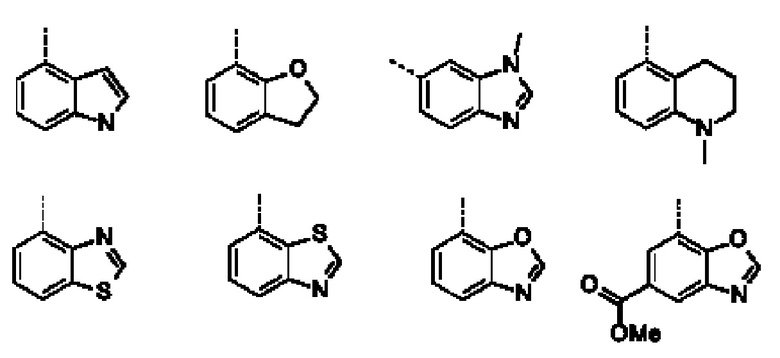
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с шестым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
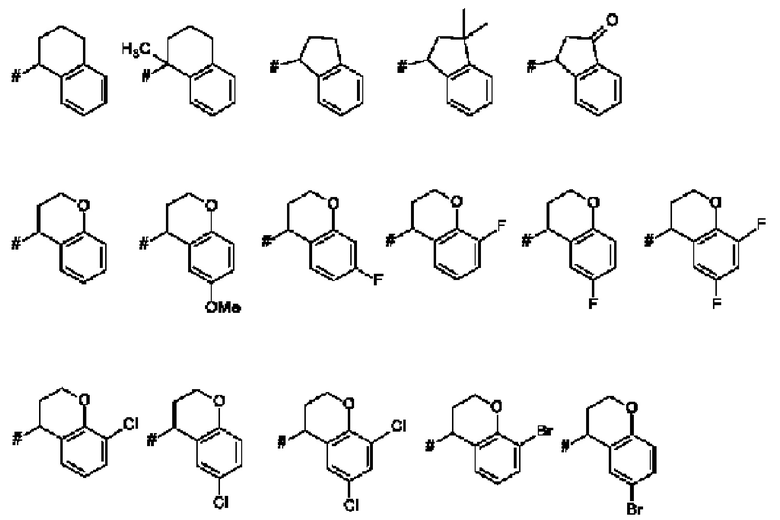
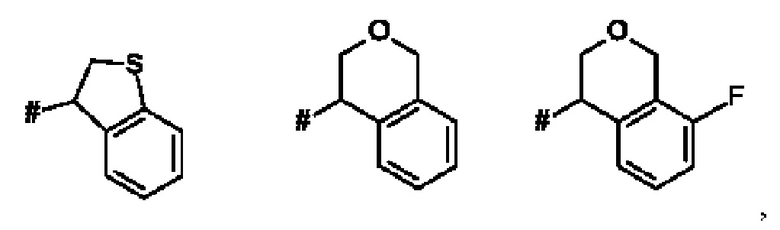
R1 представляет собой водород или метил,
R2 выбирают из группы, состоящей из
хлора, иода, -С(O)-N(СН3)2,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклобутила, циклопентила, этенила, пропенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из -ОН, циано, этокси-С(О)-, -C(O)-NH2, метокси, NH2, N(CH3)2, N(CH3)(C(O)CH3); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, оксетана, пирролидина, тетрагидрофурана, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропирана, дигидро-2H-пирана, 1,2-оксазолидина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидро-индола, 1,3-дигидро-изоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло[3.1.1]гептана, 8-окса-3-азабицикло[3.2.1]октана, тиофена, имидазола, пиразола, 1,2,3-триазола, 1,2,3,4-тетразола, пиридина, дигидропиридина, пиримидина, тетрагидропиримидина, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, оксо, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, метила, метил-С(О)-, дифторметила, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R3 представляет собой водород или метил,
R4 выбирают из группы, состоящей из водорода, хлора, фтора, метила, метокси и трифторметила,
R5 выбирают из группы, состоящей из водорода, хлора, фтора, -ОН, циано, метила, трифторметокси и NH2,
R6 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила и метокси,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-метила), метокси;
метила, этила, пропила, изопропила, бутила, изобутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, -C(O)-NMe2, -NH-С(O)-метила, метила, метокси, циклопропила, -NH2, -NMe2, SO2-метила и (EtO)2Р(=O)-;
гетероциклил-метила, гетероциклил-этила, где гетероциклильный заместитель выбирают из группы, состоящей из оксетана, тетрагидрофурана, тетрагидропирана, пирролидина, пиразола, имидазола, 1,2,4-оксадиазола, морфолина, пиридина, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического или бициклического гетероцикла, выбранного из группы оксетана, морфолина, тетрагидропирана, пиридина и пиразола;
R14 выбирают из группы, состоящей из
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, метила, метокси и циклопентила; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбирают из группы, состоящей из
метила и этила, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -ОН и -СООН; и
пиридина,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
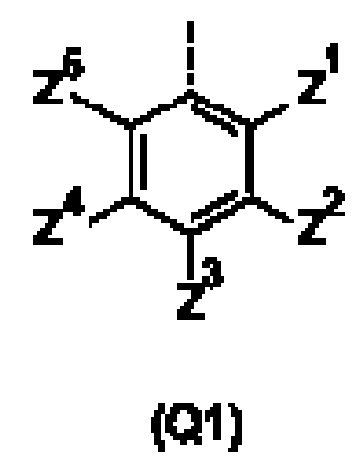
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила, метокси и трифторметила,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
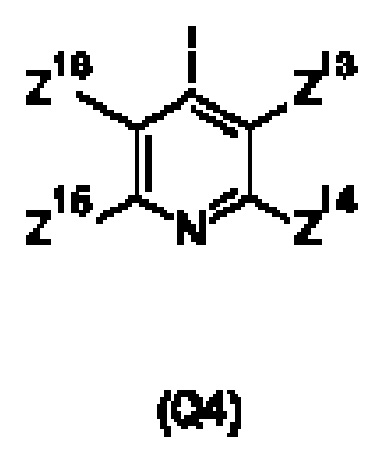
в которой:
Z14 и Z15 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, этокси, изопропокси, гидроксиметил, NH2, морфолинила и
Z13 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила, метокси, или
Q представляет собой пиридиновое кольцо формулы (Q5)
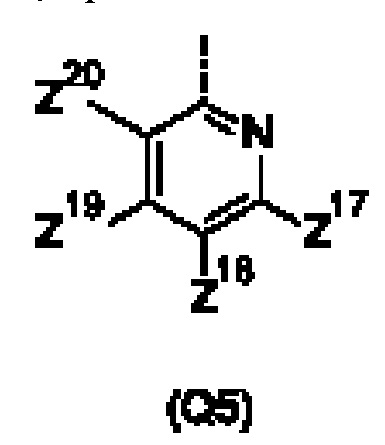
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой фтор, или
Q выбирают из группы, состоящей из
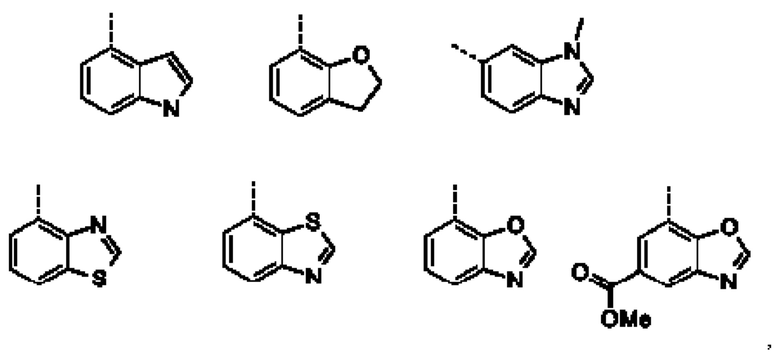
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с седьмым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
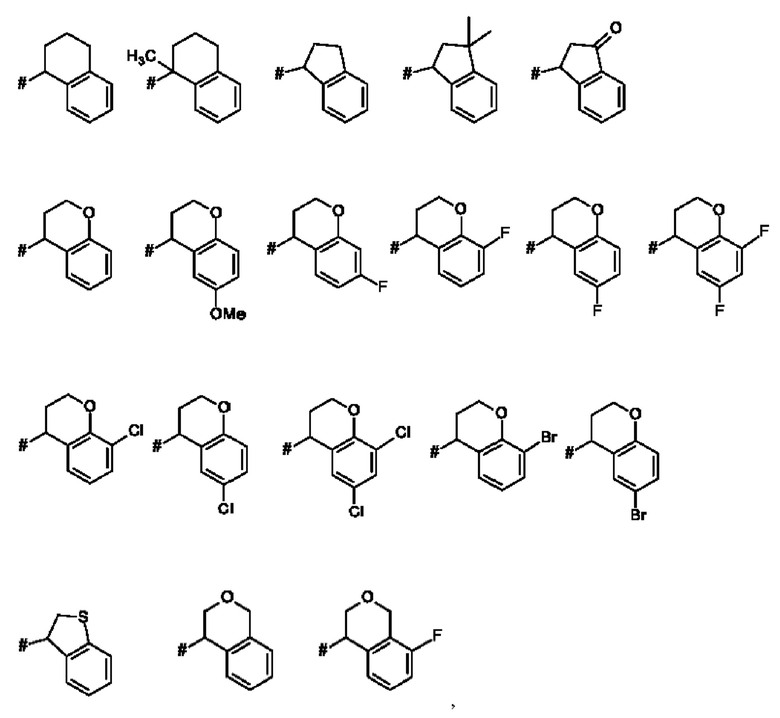
R1 представляет собой водорода или метил,
R2 выбирают из группы, состоящей из водорода, (1S)-2,3-дигидро-1Н-инден-1-иламино, (2,3-дифторбензил)окси, (2-ацетамидоэтил)амино, (2-амино-2-оксоэтил)амино, (2-аминоэтил)амино, (2-карбоксиэтил)сульфанила, (2-этокси-2-оксоэтил)(метил)амино, (2-гидроксиэтил)(метил)амино, (2-гидроксиэтил)амино, гидроксиметила, метоксиметила, 2-гидроксиэтила, (2-гидроксиэтил)окси, (2-гидроксиэтил)сульфанила, (2-метокси-2-оксоэтил)амино, (3-метокси-3-оксопропил)-метиламино, (2-метоксиэтил)(метил)амино, (2-метоксиэтил)амино, (2-метоксиэтил)окси, (2R)-2-(гидроксиметил)пирролидин-1-ила, (2R)-2-(метоксикарбонил)пирролидин-1-ила, (2R)-2-(метоксиметил)пирролидин-1-ила, (2R)-2-(трет-бутоксикарбонил)пирролидин-1-ила, (2R)-2-карбоксилатопирролидин-1-ила, (2R)-2-карбоксипирролидин-1-ила, (2R,6S)-2,6-диметилморфолин-4-ила, 2-(трифторметил)морфолин-4-ила, (2rac)-2-карбоксипирролидин-1-ила, (2S)-2-(этоксикарбонил)пирролидин-1-ила, (2S)-2-(гидроксиметил)пирролидин-1-ила, (2S)-2-(метоксикарбонил)пирролидин-1-ила, (2S)-2-(метоксиметил)пирролидин-1-ила, (2S)-2-(трет-бутоксикарбонил)пирролидин-1-ила, (2S)-2-карбамоилпирролидин-1-ила, (2S)-2-карбоксипирролидин-1-ила, (2S)-2-метил-2,3-дигидро-1H-индол-1-ила, (2S)-2-метилморфолин-4-ила, (2-трет-бутокси-2-оксоэтил)(метил)амино, (2-трет-бутокси-2-оксоэтил)амино, 2,2-дифторэтил(метил)амино, (3,3,3-трифторпропил)амино, (3,3-диметилбутил)окси, (3-амино-3-оксопропил)(метил)амино, (3-амино-3-оксопропил)амино, (3-фторбензил)окси, (3-метокси-3-метилбутил)окси, (3-метоксибензил)окси, (3R)-3-(гидроксиметил)пирролидин-1-ила, (3R)-3-(метоксикарбонил)пирролидин-1-ила, (3R)-3-аминопирролидин-1-ила, (3R)-3-карбоксипирролидин-1-ила, (3R)-3-гидроксипирролидин-1-ила, (3R)-пирролидин-3-илокси, (3rac,4rac)-3-амино-4-фторпирролидин-1-ила, (3S)-3-(диметиламино)пирролидин-1-ила, (3S)-3-(гидроксиметил)пирролидин-1-ила, (3S)-3-(метоксикарбонил)пирролидин-1-ила, (3S)-3-гидроксипирролидин-1-ила, (карбоксилатометил)амино, (карбоксиметил)(метил)амино, (карбоксиэтил)амино, (циклопентилметил)окси, (циклопропилметил)(метил)амино, (пиридин-2-илметил)амино, (rac)-3-гидроксипирролидин-1-ила, [(1R,3S)-3-амино-2,2-диметилциклопропил]амино, [(2R)-1-гидроксибутан-2-ил]амино, [(2S)-1-амино-1-оксопропан-2-ил]амино, [(5-метил-1,2,4-оксадиазол-3-ил)метил]амино, [(диэтоксифосфорил)метил](метил)амино, [2-(1Н-пиразол-1-ил)этил]амино, 2-(1Н-имидазол-1-ил)этиламино, 2-(1Н-имидазол-1-ил)этил-метиламино, [2-(циклопропиламино)этил]амино, [2-(диметиламино)этил]амино, [2-(пирролидин-1-ил)этил]амино, [3-(диметиламино)-3-оксопропил]амино, 1,1-диоксидотиоморфолин-4-ила, 1,2-оксазолидин-2-ила, 1,3-дигидро-2Н-изоиндол-2-ила, 1-циано-2-этокси-2-оксоэтила, 1Н-1,2,3-триазол-1-ила, 1H-имидазол-1-ила, 1Н-пиразол-1-ила, 1Н-пиразол-4-ил, 1H-пиразол-4-иламино, 2,2-диметилморфолин-4-ил, 2,2-диметилпирролидин-1-ила, 2,4-диметил-3,5-диоксо-1,2,4-триазолидин-1-ила, 2-ацетилгидразино, 2-амино-2-оксоэтила, 2Н-1,2,3-триазол-2-ила, 1H-тетразол-5-ила, 3-(пирролидин-1-ил)азетидин-1-ила, 3,3-дифторазетидин-1-ила, 3,3-дифторпирролидин-1-ила, 3,4-дигидроизохинолин-2(1Н)-ила, 3,9-диокса-7-азабицикло[3.3.1]нон-7-ила, 3-фторазетидин-1-ила, 3-гидроксиазетидин-1-ила, 3-метилазетидин-1-ила, 3-оксопиразолидин-1-ила, 1-(дифторметил)-1Н-пиразол-4-ила, 4-(трифторметил)-1Н-пиразол-1-ила, 1-метил-пиперидин-4-ила, 4-фторпиперидин-1-ила, 4,4-дифторпиперидин-1-ила, 4-ацетилпиперазин-1-ила, 4-оксоимидазолидин-1-ила, 6-окса-3-азабицикло[3.1.1]гепт-3-ила, 8-окса-3-азабицикло[3.2.1]окт-3-ила, амино, анилино, азетидин-1-ила, бензил(метил)амино, бис(2-метоксиэтил)амино, хлора, иода, цианометила, циклобутил(метил)амино, циклопентилокси, циклопропила, циклобутила, циклопентила, циклопропил(этил)амино, циклопропил(метил)амино, циклопропиламино, диэтиламино, диметиламино, диметиламинокарбонила, аминометила, 2-аминоэтила, (диметиламино)метила, 2-(диметиламино)этила, [ацетил(метил)амино]метила, этенила, этила, этил(2-метоксиэтил)амино, этиламино, этилокси, этилсульфанил, этилсульфинила, этилсульфонила, этил(метил)амино, изобутил(метил)амино, изопропил(метил)амино, изопропила, изопропилокси, метокси(метил)амино, метоксиамино, метил, метил(2-метилсульфонилэтил)амино, метил-оксолан-3-ил]метил]амино, метил(оксан-4-илметил)амино, метил(1-фенилэтил)амино, метил(2,2,2-трифторэтил)амино, оксетан-3-илметиламино, метил(оксетан-3-ил)амино, метил(фенил)амино, метил[2-(2-оксопирролидин-1-ил)этил]амино, метил[2-(морфолин-4-ил)этил]амино, метиламино, метилокси, метилсульфанила, морфолин-4-ила, морфолин-4-иламино, нитрилометила, проп-1-ен-2-ила, пропила, пропиламино, пиридин-4-ила, пиридин-2-илсульфанила, пиридин-4-иламино, пирролидин-1-ила, пирролидин-3-ила, оксетан-3-ила, тетрагидрофуран-3-ила, 3,6-дигидро-2Н-пиран-4-ила, тетрагидропиран-4-ила, тетрагидро-2Н-пиран-4-иламино, тетрагидро-2Н-пиран-4-илокси, 2-аминопиримидин-5-ила, 1,3-диметил-2,4-диоксо-1,2,3,4-тетрагидропиримидин-5-ила, 3-фтор-2-оксо-1,2-дигидропиридин-5-ила, 2-оксо-1,2-дигидропиридин-5-ила, 3-тиенила и тиоморфолин-4-ила,
R3 представляет собой водород или метил,
R4 выбирают из группы, состоящей из водорода, хлора, фтора, -ОН, циано, метила, метокси, трифторметила, трифторметокси и NH2,
R5 выбирают из группы, состоящей из водорода, хлора, фтора, -ОН, циано, метила, метокси и трифторметила,
R6 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила и метокси,
Q выбирают из группы, состоящей из фенила, 1,3-бензотиазол-4-ила, 1,3-бензотиазол-7-ила, 1,3-бензоксазол-7-ила, 1H-индол-4-ила, 1-метил-1Н-бензимидазол-6-ила, 2,5-бис(трифторметил)фенила, 2,3,4-трифторфенила, 2,3,5-трихлорфенила, 2,3,5-трифторфенила, 2,3,6-трифторфенила, 2,3-дихлорфенила, 2,3-дихлор-5-цианофенила, 2,3-дихлор-5-гидроксифенила, 2,3-дигидро-1-бензофуран-7-ила, 2,3-дифторфенила, 2,4,5-трифторфенила, 2,4,6-трифтор-3-метоксифенила, 2,4-дифтор-S-гидроксифенила, 2,4-дифтор-S-метоксифенила, 2,5-дихлорфенила, 2-хлор-5-цианофенила, 2-хлор-5-метилфенила, 2,5-дифтор-4-метоксифенила, 2,6-дифторфенила, 2-хлор-6-метилпиридин-4-ила, 3-метилпиридин-4-ила, 2,6-диметилпиридин-4-ила, 2-хлор-3-фторфенила, 2-хлор-4-(диметиламино)фенила, 2-хлор-4-фторфенила, 2-хлор-5-фторфенила, 2-хлор-6-фторфенила, 2-хлорфенила, 2-хлорпиридин-4-ила, 3-хлорпиридин-4-ила, 2,3-дихлорпиридин-4-ила, 2,5-дихлорпиридин-4-ила, 2,6-дихлорпиридин-4-ила, 3,5-дихлорпиридин-4-ила, 2,6-дифторпиридин-4-ила, 3,5-дифторпиридин-4-ила, 2-хлор-3-фторпиридин-4-ила, 2-цианопиридин-4-ила, 3-хлор-2-метоксипиридин-4-ила, 5-хлор-2-метоксипиридин-4-ила, 5-фтор-2-метоксипиридин-4-ила, 5-фтор-2-изопропилоксипиридин-4-ила, 2,3-диметоксипиридин-4-ила, 2,6-диметоксипиридин-4-ила, 2-фтор-5-метилфенила, 3-фтор-5-метилфенила, 2-фтор-3-(трифторметокси)фенила, 2-фтор-3-(трифторметил)фенила, 5-фтор-2-(трифторметил)фенила, 3-циано-5-метилфенила, 2-фторпиридин-4-ила, 2-этокси-5-фторпиридин-4-ила, 2-(гидроксиметил)пиридин-4-ила, 2-метилупиридин-4-ила, 2-метоксипиридин-4-ила, 3-метоксипиридин-4-ила, 2-аминопиридин-4-ила, 2-морфолин-4-илпиридин-4-ила, 3-(диметиламино)-2,4-дифторфенила, 3-(диметиламино)фенила, 3-(метиламино)фенила, 3-(трифторметил)фенила, 3-(трифторметокси)фенила, 3,4,5-трифторфенила, 3,4-дихлор-5-(диметиламино)фенила, 3,4-дихлорфенила, 3,4-дифтор-2-метоксифенила, 3,4-дифторфенила, 3,5-дихлор-4-(диметиламино)фенила, 3,5-дихлор-4-фторфенила, 3,5-дихлорфенила, 3,5-дифторфенила, 4-(дифторметокси)-3,5-дифторфенила, 2,5-диметилфенила, 3,5-диметилфенила, 3-трет-бутил-5-метилфенила, 5-трет-бутил-2-хлор-3-метилфенила, 3-хлор-2-фтор-5-метилфенила, 3-хлор-2-фторфенила, 3-хлор-2-метилфенила, 3-хлор-4-(диметиламино)-5-фторфенила, 3-хлор-4-(диметиламино)фенила, 3-хлор-4-фторфенила, 3-хлор-4-метилфенила, 3-хлор-5-(диметиламино)фенила, 3-хлор-5-(метилсульфанил)фенила, 3-хлор-5-(морфолин-4-ил)фенила, 2-хлор-3-(трифторметил)фенила, 2-метил-5-(трифторметил)фенила, 3-хлор-5-(трифторметил)фенила, 3-хлор-5-этилфенила, 3-хлор-5-фторфенила, 3-хлор-5-метоксифенила, 3-хлор-5-метилфенила, 3-хлорфенила, 3-фтор-2-метилфенила, 3-фтор-4-метоксифенил, 3-фтор-5-метилфенил, 3-фторпиридин-2-ил, 3-фторпиридин-4-ил, 4-хлор-3-(диметиламино)фенила, 4-фтор-3-метоксифенила, 5-(метоксикарбонил)-1,3-бензоксазол-7-ила, 5-хлор-2,4-дифторфенила, 5-хлор-2-фтор-3-метилфенила, 5-хлор-2-фтор-4-метилфенила, 5-хлор-2-фторфенила, 5-хлор-2-метоксифенила, 5-фтор-2-метилфенила, 5-фтор-2-метоксифенила, 5-хлор-1Н-имидазол-2-ила, 3,5-диэтилфенила, 2-хлор-3,5-диэтилфенила, 3-хлор-2-тиенила, 4-хлор-2-тиенила, 5-хлор-2-тиенила, 2,5-дихлор-3-тиенила, 5-фтор-2-тиенила, 5-циано-2-тиенила, 5-циано-4-метил-2-тиенила, 5-метил-2-тиенила, 2,5-диметил-3-тиенила, 5-(трифторметил)-2-тиенила и 2-метил-1,3-тиазол-5-ила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В соответствии с восьмым вариантом выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой A3 или А4
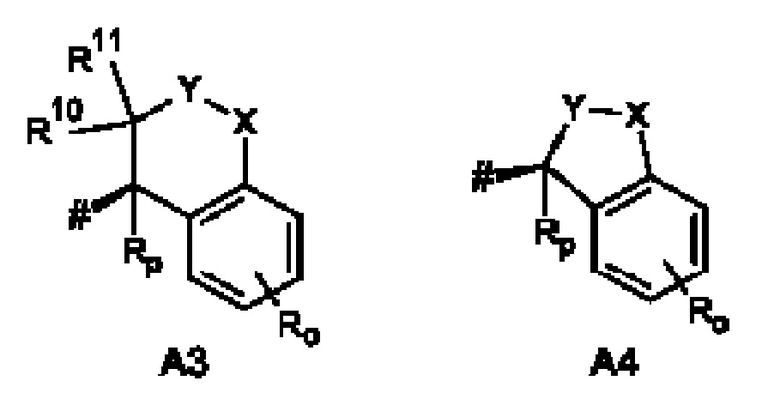
о представляет собой 0 или 1,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X выбирают из группы, состоящей из CR7R8, О, S, и N-R9,
Y представляет собой CR7R8 или О,
R1 представляет собой водород или C1-С4-алкил,
R2 выбирают из группы, состоящей из водорода, галогена, -С(O)-N(С1-С4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-C4-алкила, C3-C6-циклоалкила, С2-С4-алкенила или C3-C6-циклоалкенила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(O)- и -C(O)-NH2 С1-С4-алкокси, -NH2, -N(С1-С4-алкила)2, -N(С1-С4-алкил)(С(O)-С1-С4-алкила), и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила, и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, -СООН, C1-C4-алкокси-С(O)-, -C(O)-NH2, C1-C4-алкила, С1-С4-алкил-С(O)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси-С1-С4-алкила-, С1-С4-алкокси-С1-С4-алкила-, -NH2, -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R3 представляет собой водород или C1-C4-алкил,
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, NH2,
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R7 выбирают из группы, состоящей из водорода и C1-C4-алкила,
R8 выбирают из группы, состоящей из водорода и C1-C4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН и С1-С4-алкила,
R11 представляет собой водорода,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-С1-С4-алкила), C1-C4-алкокси;
C1-C4-алкила, C3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, С1-С4-алкила, С1-С4-алкокси, С3-С6-циклоалкила, -NH2, -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-C4-алкила, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и С1-С4-алкокси;
фенила и бензо-С5-C6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
С1-С4-алкила, C3-C6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, С1-С4-алкила, С1-С4-алкокси и C3-C6-циклоалкила; и
4-10-ти членного гетероциклоалкила,
R15 выбирают из группы, состоящей из
водорода;
C1-C4-алкила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из -ОН и -СООН; и
6-ти членного гетероарила,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
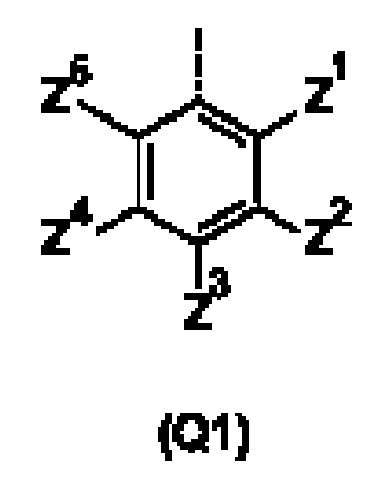
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, C1-C4-алкила, C1-C4-алкокси и С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, -ОН, C1-C4-алкила, C1-C4-алкокси, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -S-(С1-С4-алкила) и 4-6-ти членного гетероциклоалкила, и
Z3 выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, и -N(С1-С4-алкила)2, или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они соединены, 5-ти членный гетероциклоалкил или 5-ти членный гетероарил, каждый из которых может быть необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо,
Z3 и Z5 представляют собой водород, и
Z4 выбирают из группы, состоящей из водорода и С1-С4-алкокси-С(O)-, или
Q представляет собой пиридиновое кольцо формулы (Q4)
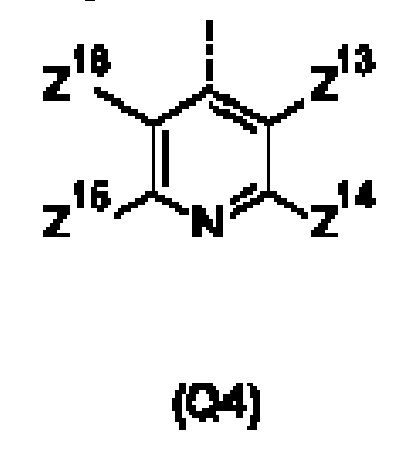
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-алкокси, С1-С4-гидроксиалкила, NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -NH-CO-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, C3-C6-циклоалкила, -NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
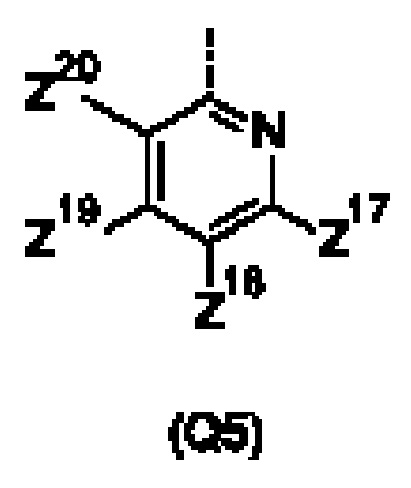
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой галоген, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
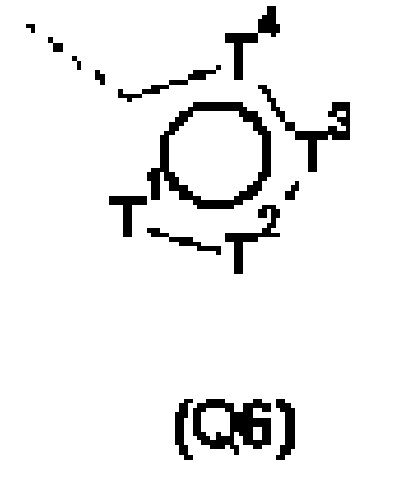
в которой:
Т1-Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1-Т4 представляет собой О, не более чем один из Т1-Т4 представляет собой S, не более чем один из Т1-Т4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-C3-C6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
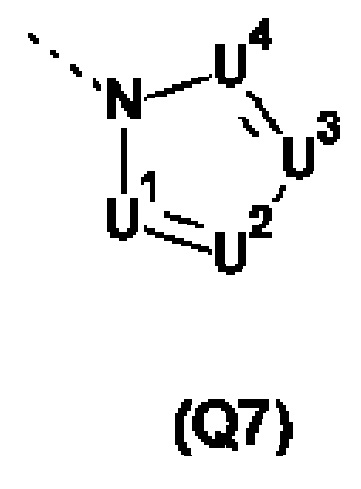
в которой:
U1-U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1-U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
Другие варианты выполнения первого объекта настоящего изобретения:
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
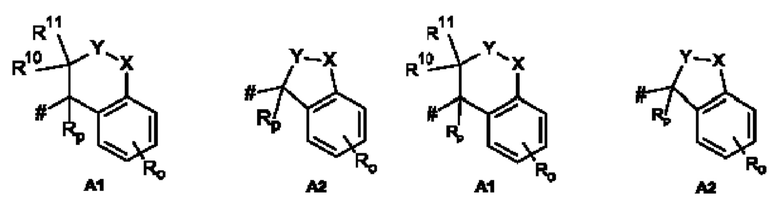
о представляет собой 0, 1 или 2,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси, циано, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp представляет собой водород,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, S, и N-R9, где по меньшей мере один из X и Y представляет собой CR7R8,
R7 выбирают из группы, состоящей из водорода и C1-C4-алкила,
R8 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R9 представляет собой C1-C4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН, С1-С4-алкила и C1-C4-алкокси, и
R11 представляет собой водород,
где когда Y представляет собой О, S или N-R9, R10 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
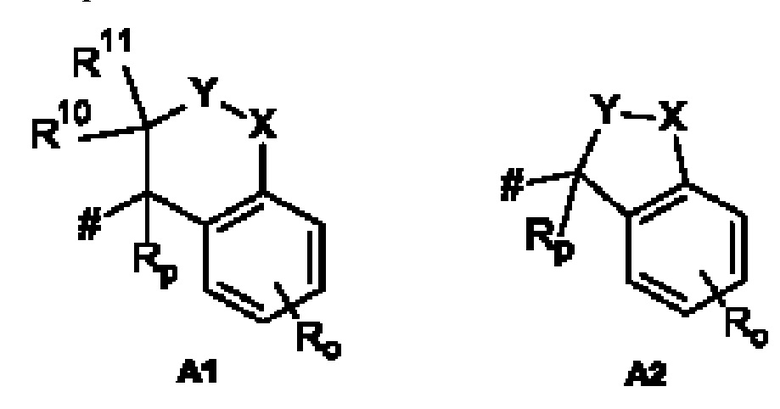
о представляет собой 0, 1 или 2,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси, циано, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp выбирают из группы, состоящей из водорода, C1-C4-алкила,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, S, и N-R9, где по меньшей мере один из X и Y представляет собой CR7R8,
R7 выбирают из группы, состоящей из водорода и С1-C4-алкила,
R8 выбирают из группы, состоящей из водорода и С1-C4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН, C1-C4-алкила и C1-C4-алкокси, и
R11 представляет собой водород,
где когда Y представляет собой О, S или N-R9, R10 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,

о представляет собой 0, 1 или 2,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси, циано, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена,
Rp представляет собой водород,
X, Y независимо друг от друга выбирают из группы, состоящей из CR7R8, О, и S,
где по меньшей мере один из X и Y представляет собой CR7R8,
R7 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R8 выбирают из группы, состоящей из водорода и С1-С4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R10 выбирают из группы, состоящей из водорода, -ОН, С1-С4-алкила и С1-С4-алкокси, и
R11 представляет собой водород,
где когда Y представляет собой О, S или N-R9, R10 не представляет собой -ОН,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
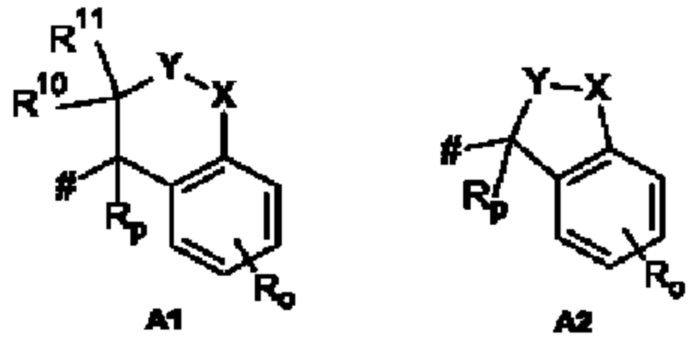
о представляет собой 0 или 1,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси,
Rp представляет собой водород,
X выбирают из группы, состоящей из CR7R8, О, S, и N-R9,
Y представляет собой CR7R8,
R7 выбирают из группы, состоящей из водорода и C1-C4-алкила,
R8 выбирают из группы, состоящей из водорода и C1-C4-алкила,
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН и C1-C4-алкила, и
R11 представляет собой водород,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
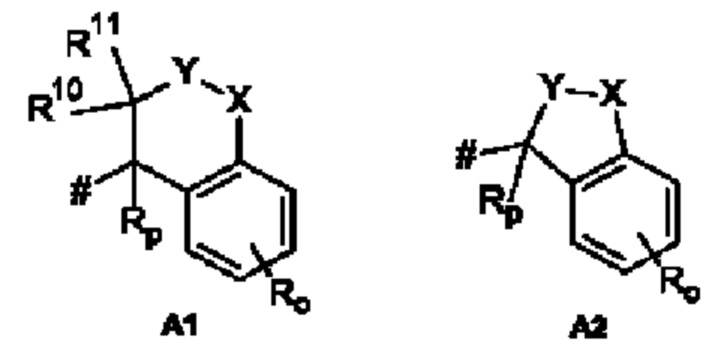
о представляет собой 0 или 1,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и C1-C4-алкокси,
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила,
X выбирают из группы, состоящей из CR7R8, О, S, и N-R9,
Y представляет собой CR7R8 или О,
R7 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R8 выбирают из группы, состоящей из водорода и C1-C4-алкила,
или R7 и R8 вместе образуют оксо группу (=O),
R9 представляет собой С1-С4-алкил,
R10 выбирают из группы, состоящей из водорода, -ОН и C1-C4-алкила, и
R11 представляет собой водород,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А представляет собой А1 или А2,
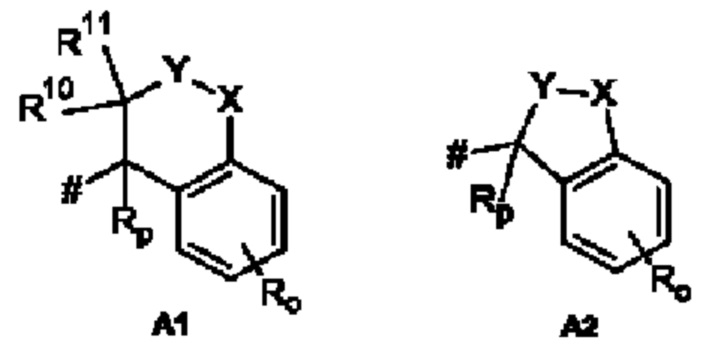
о представляет собой 0 или 1,
R выбирают из группы, состоящей из галогена, С1-С4-алкила и С1-С4-алкокси,
Rp представляет собой водород,
X выбирают из группы, состоящей из CR7R8, О и S,
Y представляет собой CR7R8 или О,
R7 выбирают из группы, состоящей из водорода и С1-С4-алкила,
R8 выбирают из группы, состоящей из водорода и C1-C4-алкила, или R7 и R8 вместе образуют оксо группу (=O),
R10 выбирают из группы, состоящей из водорода, -ОН и C1-C4-алкила, и
R11 представляет собой водород,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
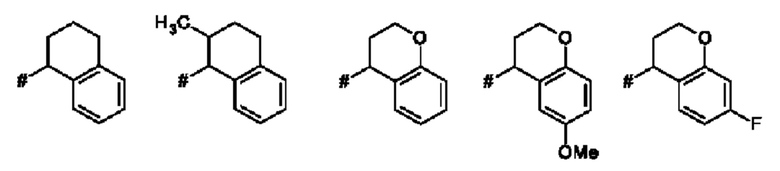
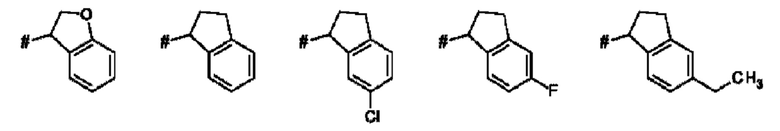
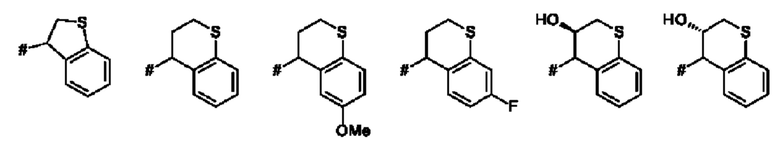
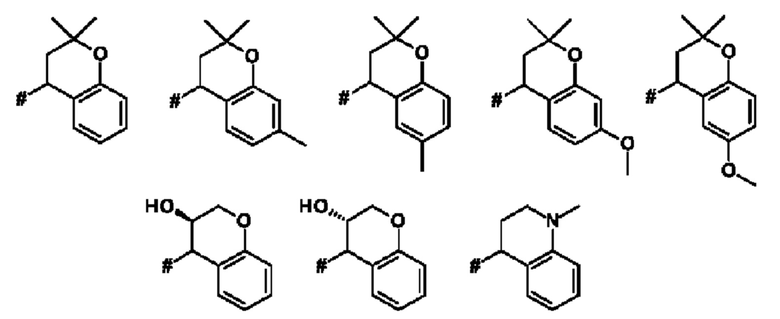
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
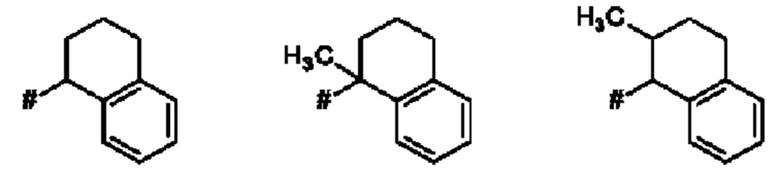
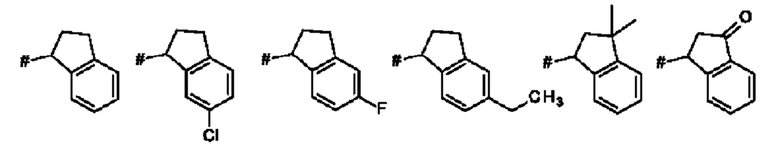
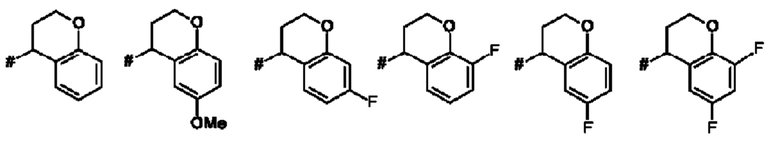
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
А выбирают из группы, состоящей из
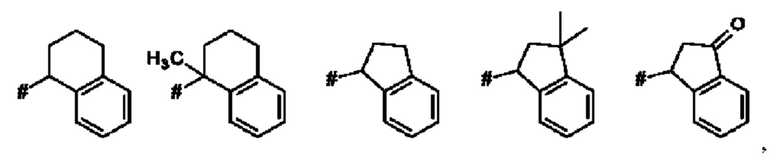
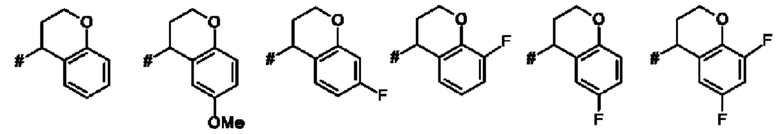
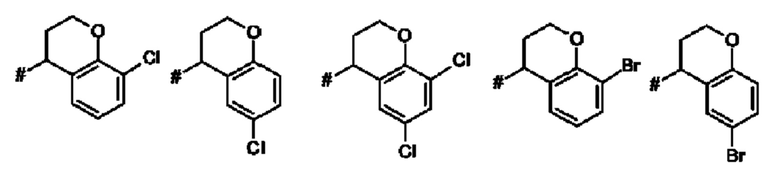
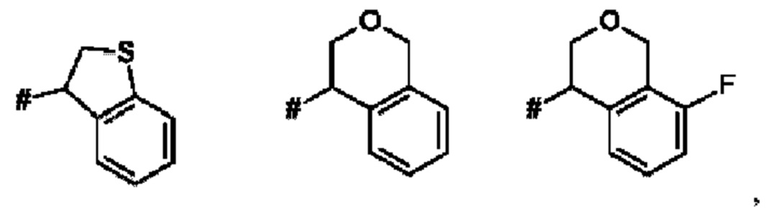
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, галогена, циано, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(О)-NH(C1-С4-алкила), -C(O)-N(C1-С4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-C4-алкила, С3-С6-циклоалкила, С2-С4-алкенила, С3-С6-циклоалкенила, С2-С4-алкинила или фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-C1-C4-алкила, S-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, С1-С4-алкила, С1-С4-алкил-С(О)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-алкокси-С1-С4-алкила-, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-С1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, -N(С1-С4-алкил)-(-С(O)-С1-С4-алкила), С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
фенила, бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила; и
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, галогена, циано, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(О)-NH(С1-С4-алкила), -C(O)-N(C1-C4-алкила)2;
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
С1-С4-алкила, С3-С6-циклоалкила, С2-С4-алкенила, С3-С6-циклоалкенила, С2-С4-алкинила или фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH(C(O)-C1-C4-алкила), -N(С1-С4-алкил)(С(O)-С1-С4-алкила), -S-C1-C4-алкила, -S(O)-C1-C4-алкила, -SO2-С1-С4-алкила, -S-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и -SO2-C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, C1-С4-алкила, C1-C4-алкил-С(О)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-С4-алкокси, гидрокси-С1-С4-алкила, С1-С4-алкокси-С1-С4-алкила-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из
водорода, -NH(-С(O)-С1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, -СООН, С1-С4-алкокси-С(О)-, -C(O)-NH2, -С(O)-NH(С1-С4-алкила), -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, -N(С1-С4-алкил)-(-С(O)-С1-С4-алкила), С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-С1-С4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, -S(O)-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, SO2-С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
фенила, бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила; и
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена;
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, галогена,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
C1-C4-алкила, С3-С6-циклоалкила, С2-С4-алкенила или С3-С6-циклоалкенила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкокси-С(O)- и -C(O)-NH2; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила, и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, С1-С4-алкила, С1-С4-алкил-С(O)-, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси-С1-С4-алкила-, С1-С4-алкокси-С1-С4-алкила-, -NH2, -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из водорода, -NH(-С(O)-С1-С4-алкила), C1-C4-алкокси;
C1-C4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, C1-C4-алкила, С1-С4-алкокси, С3-С6-циклоалкила, -NH2, -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, и С1-С4-алкокси;
фенила и бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, C1-C4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, C1-C4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
C1-C4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, С1-С4-алкила, С1-С4-алкокси и С3-С6-циклоалкила; и
4-10-ти членного гетероциклоалкила,
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из -ОН и -СООН; и
6-ти членного гетероарила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, галогена, -С(O)-N(C1-С4-алкила)2
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
С1-С4-алкила, С3-С6-циклоалкила, С2-С4-алкенила или С3-С6-циклоалкенила, каждый из которых необязательно замещен 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, циано, С1-С4-алкокси-С(O)- и -C(O)-NH2, С1-С4-алкокси, -NH2, -N(С1-С4-алкила)2, -N(С1-С4-алкил)(С(O)-С1-С4-алкила); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из 4-10-ти членного гетероциклоалкила, гетероспироциклоалкила, 5-ти членного гетероарила, и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, С1-С4-алкила, С1-С4-алкил-С(O)-, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси-С1-С4-алкила-, С1-С4-алкокси-С1-С4-алкила-, -NH2, -N(С1-С4-алкила)2, и 4-10-ти членного гетероциклоалкила,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из
водорода, -NH(-С(O)-С1-С4-алкила), С1-С4-алкокси;
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, -СООН, С1-С4-алкокси-С(O)-, -C(O)-NH2, -С(O)-N(С1-С4-алкила)2, -NH-С(O)-С1-С4-алкила, С1-С4-алкила, С1-С4-алкокси, С3-С6-циклоалкила, -NH2, -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, и (С1-С4-алкокси)2Р(=O)-;
гетероциклил-С1-С4-алкила, где гетероциклильный заместитель выбирают из группы, состоящей из 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, -ОН, оксо, C1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, и C1-C4-алкокси;
фенила и бензо-С5-С6-циклоалкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена; и
моноциклического или бициклического гетероцикла, выбранного из группы 4-10-ти членного гетероциклоалкила, 5-ти членного гетероарила и 6-ти членного гетероарила каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, оксо, циано, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
R14 выбирают из группы, состоящей из
С1-С4-алкила, С3-С6-циклоалкила, фенил-С1-С4-алкила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, -ОН, С1-С4-алкила, С1-С4-алкокси и С3-С6-циклоалкила; и
4-10-ти членного гетероциклоалкила,
R15 выбирают из группы, состоящей из
водорода;
С1-С4-алкила, который необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из -ОН и -СООН; и
6-ти членного гетероарила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, хлора,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклогексила, пропенила, циклопентенила, циклогексенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из циано, этокси-С(О)-, и -C(O)-NH2; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, пирролидина, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропиридина, дигидро-2H-пирана, 1,2-оксазолидина, 1,2-оксазина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидро-индола, 1,3-дигидро-изоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло [3.1.1] гептана, 8-окса-3-азабицикло[3.2.1] октана, имидазола, пиразола, 1,2,4-триазола, 1,2,3-триазола, 4-окса-7-азаспиро[2.5]октана, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, циано -ОН, оксо, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, метила, метил-С(О)-, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из
водорода, -NH-С(О)-метила), метокси;
метила, этила, пропила, изопропила, бутила, изобутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, -C(O)-NMe2, -NH-С(O)-метила, метила, метокси, циклопропил, -NH2, NMe2, S-метила, S(O)-метила, SO2-метила, и (EtO)2Р(=O)-;
гетероциклил-метила, гетероциклил-этила, где гетероциклильный заместитель выбирают из группы, состоящей из пирролидина, морфолина, пиразола, 1, 2, 4-оксадиазола, пиридина, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, хлора, -ОН, оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического или бициклического гетероцикла, выбранного из группы оксетана, тиетана, пирролидина, морфолина, тетрагидропирана, пиридина и пиразола, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, -ОН, оксо, метила;
R14 выбирают из группы, состоящей из
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, метила, метокси и циклопентила; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбирают из группы, состоящей из
метила и этила, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -ОН и -СООН; и
пиридина,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R2 выбирают из группы, состоящей из
водорода, хлора, иода, -C(O)-N(CH3)2,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклобутила, циклопентила, циклогексила, этенила, пропенила, циклопентенила, циклогексенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из ОН, циано, этокси-С(О)-, -C(O)-NH2, метокси, NH2, N(CH3)2, N(CH3)(C(O)CH3); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, оксетана, пирролидина, тетрагидрофурана, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропиридина, дигидро-2H-пирана, 1,2-оксазолидина, 1,2-оксазина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидро-индола, 1,3-дигидро-изоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло[3.1.1] гептана, 8-окса-3-азабицикло[3.2.1]октана, тиофена, имидазола, пиразола, 1,2,4-триазола, 1,2,3-триазола, 1,2,3,4-тетразола, пиридина, дигидропиридина, пиримидина, тетрагидропиримидина, 4-окса-7-азаспиро[2.5]октана, каждый из которых необязательно замещен 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, циано -ОН, оксо, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, метила, метил-С(О)-, дифторметила, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R12 и R13 независимо друг от друга выбирают из группы, состоящей из
водорода, -NH(-С(O)-метила), метокси;
метила, этила, пропила, изопропила, бутила, изобутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, -СООН, метокси-С(О)-, этокси-С(О)-, трет-бутокси-С(О)-, -C(O)-NH2, -C(O)-NMe2, -NH-С(O)-метила, метила, метокси, циклопропила, -NH2, NMe2, S-метила, S(O)-метила, SO2-метила, и (EtO)2Р(=O)-;
гетероциклил-метила, гетероциклил-этила, где гетероциклильный заместитель выбирают из группы, состоящей из оксетана, тетрагидрофурана, тетрагидропирана, пирролидина, морфолина, пиразола, имидазола, 1,2,4-оксадиазола, пиридина, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, хлора, -ОН, оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического или бициклического гетероцикла, выбранного из группы оксетана, тиетана, пирролидина, морфолина, тетрагидропирана, пиридина и пиразола, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, хлора, -ОН, оксо, метила;
R14 выбирают из группы, состоящей из
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -ОН, метила, метокси и циклопентил; и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбирают из группы, состоящей из
метил и этил, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -ОН и -СООН; и
пиридин,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Rp представляет собой водород или С1-С4-алкил,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Rp представляет собой водород или метил,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R3 представляет собой водород или С1-С4-алкил,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R3 представляет собой водород или метил,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R4 выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R4 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, NH2,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R4 выбирают из группы, состоящей из водорода, хлора, фтора, циано, метила, метокси и трифторметила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R4 выбирают из группы, состоящей из водорода, хлора, фтора, -ОН, циано, метила, метокси, трифторметила, трифторметокси и NH2,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R5 выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R5 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, C1-C4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R5 выбирают из группы, состоящей из водорода, хлора, фтора и метила, и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R5 выбирают из группы, состоящей из водорода, хлора, фтора, -ОН, циано, метила, метокси и трифторметила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R6 выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R6 выбирают из группы, состоящей из водорода, галогена, -ОН, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R6 выбирают из группы, состоящей из водорода, фтора, хлора и метила,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
R6 выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила и метокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
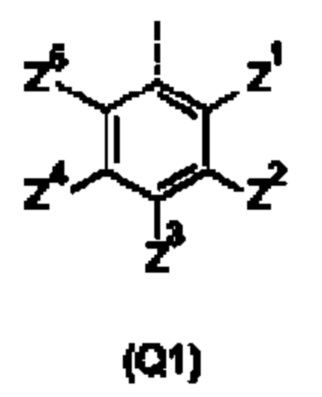
в которой:
Z1, Z2, Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, гидрокси, C1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(С1-С4-алкила), -N(C1-С4-алкила)2, 4-6-ти членного гетероциклила, который необязательно замещен 1 или 2 заместителями, выбранными из группы, состоящей из фтора, хлора, брома, метила и циано, -S-(С1-С4-алкила), -S(O)-(С1-С4-алкила), -SO2-(С1-С4-алкила), или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они связаны, 5-или 6-членный гетероциклоалкил, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z3, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-алкокси-С(О)-, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, или
Z2 и Z3 образуют вместе с атомами углерода, с которыми они связаны, 5-ти или 6-ти членное насыщенное или частично насыщенное гетероциклическое кольцо, 5-ти членный гетероарил или 6-ти членный гетероарил, каждый из которых необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо, и
Z1, Z4, и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q2)
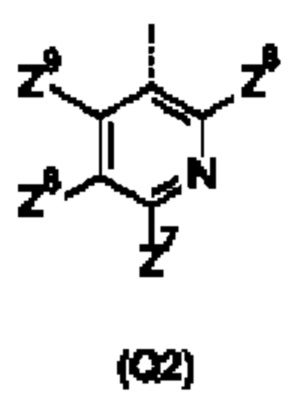
в которой:
Z6, Z7, Z8 и Z9 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(C1-С4-алкила)2, или
Q представляет собой пиримидиновое кольцо формулы (Q3)
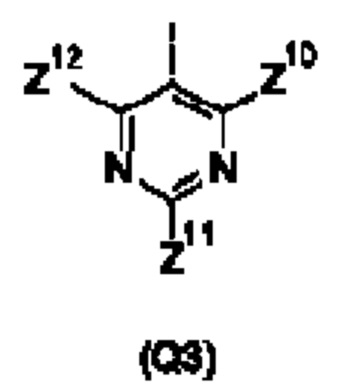
в которой:
Z10, Z11 и Z12 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-C4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
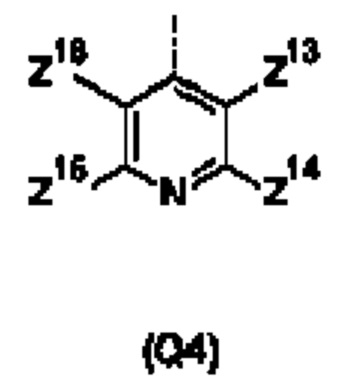
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С1-С4-гидроксиалкила, NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -NH-СО-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-C6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
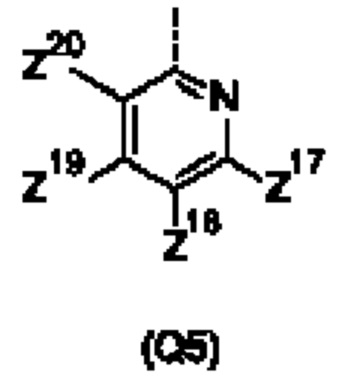
в которой:
Z17, Z18, Z19 и Z20 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -NH(C1-С4-алкила), -N(С1-С4-алкила)2, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
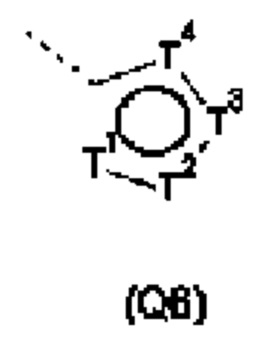
в которой:
T1-Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1 - Т4 представляет собой О, не более чем один из Т1 - Т4 представляет собой S, не более чем один из представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-С3-С6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
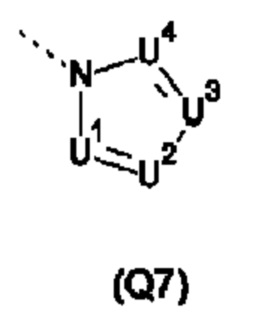
в которой:
U1 - U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1 - U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
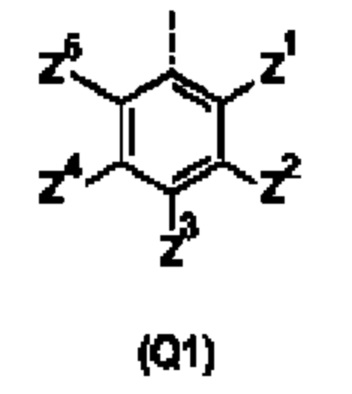
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила и С1-С4-алкокси,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, -ОН, С1-С4-алкила, С1-С4-алкокси, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -S-(С1-С4-алкила) и 4-6-ти членного гетероциклоалкила, и
Z3 выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, С1-С4-алкокси и -N(С1-С4-алкила)2, или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они соединены, 5-ти членный гетероциклоалкил или 5-ти членный гетероарил, каждый из которых может быть необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо,
Z3 и Z5 представляют собой водород, и
Z4 выбирают из группы, состоящей из водорода и С1-С4-алкокси-С(O)-, или
Q представляет собой пиридиновое кольцо формулы (Q4)
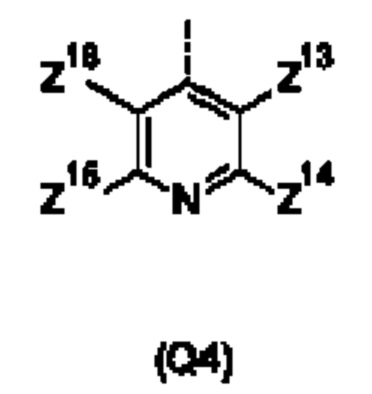
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-алкокси, С1-С4-гидроксиалкила, NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -NH-CO-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
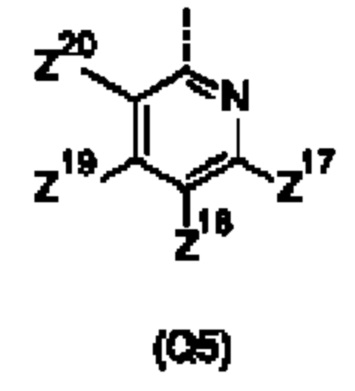
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой галоген, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
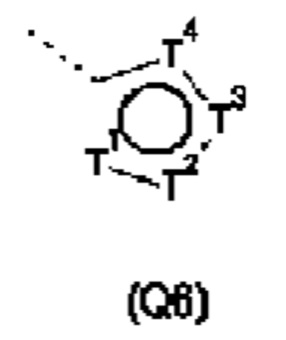
в которой:
Т1 - Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1 - Т4 представляет собой О, не более чем один из Т1 - Т4 представляет собой S, не более чем один из Т1 - Т4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-С3-С6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
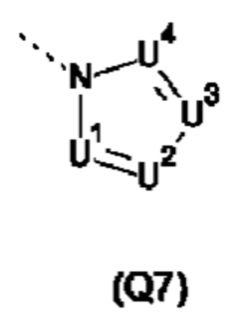
в которой:
U1 - U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1 - U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
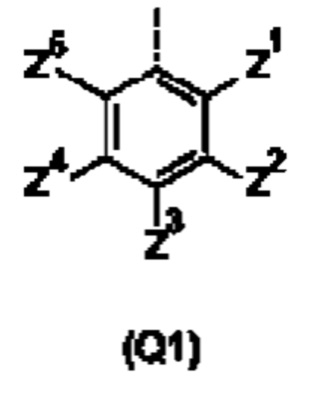
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, С1-С4-алкокси и С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, -ОН, C1-С4-алкила, С1-С4-алкокси, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, -S-(С1-С4-алкила) и 4-6-ти членного гетероциклоалкила, и
Z3 выбирают из группы, состоящей из водорода, галогена, С1-С4-алкила, C1-C4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, и -N(С1-С4-алкила)2, или
Z1 и Z2 образуют вместе с атомами углерода, с которыми они соединены, 5-ти членный гетероциклоалкил или 5-ти членный гетероарил, каждый из которых может быть необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из метила, фтора и оксо,
Z3 и Z5 представляют собой водород, и
Z4 выбирают из группы, состоящей из водорода и С1-С4-алкокси-С(O)-, или
Q представляет собой пиридиновое кольцо формулы (Q4)
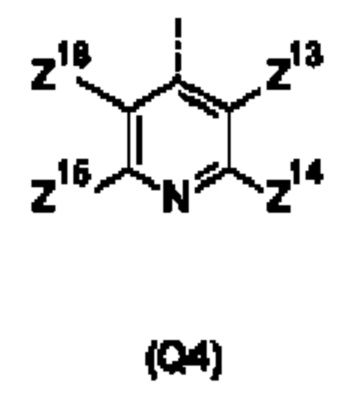
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-алкокси, С1-С4-гидроксиалкила, NH2, -NH(C1-C4-алкила), -N(C1-C4-алкила)2, -NH-CO-С1-С4-алкила, и моноциклических гетероциклов, выбранных из группы 4-7-ми членного гетероциклоалкила или 5-ти членных гетероарилов, имеющих по меньшей мере один атом азота, через который гетероарильное кольцо соединено с пиридиновым кольцом, каждый из которых необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, оксо, тионо, C1-C4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, С1-С4-галогеналкокси, имеющего от 1 до 5 атомов галогена, С3-С6-циклоалкила, -NH2, -NH(С1-С4-алкила), -N(С1-С4-алкила)2, -S-C1-C4-алкила, -S(O)-С1-С4-алкила, -SO2-С1-С4-алкила, -S-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -S(O)-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, -SO2-(C1-C4-галогеналкила), имеющего от 1 до 5 атомов галогена, или
Q представляет собой пиридиновое кольцо формулы (Q5)
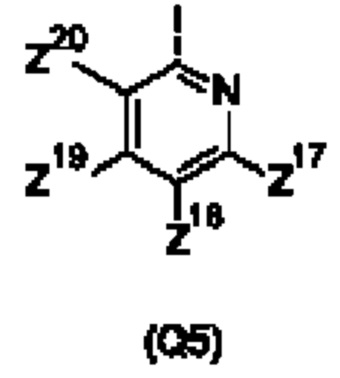
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой галоген, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q6)
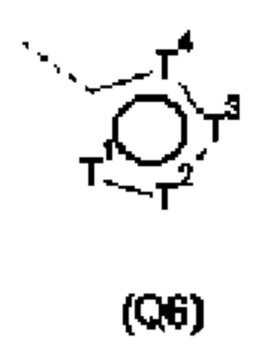
в которой:
Т1 - Т4 независимо друг от друга выбирают из группы, состоящей из N, О, S, C-Z21 и N-Z22, где не более чем один из Т1 - Т4 представляет собой О, не более чем один из Т1 - Т4 представляет собой S, не более чем один из Т1 - Т4 представляет собой N-Z22, и где
каждый Z21 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси, и
каждый Z22 независимо выбран из группы, состоящей из водорода, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкил-С3-С6-циклоалкила, С1-С4-алкокси-С1-С4-алкила, или
Q представляет собой 5-ти членный ароматический гетероцикл формулы (Q7)
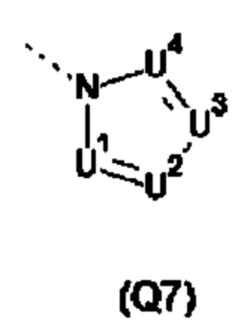
в которой:
U1 - U4 независимо друг от друга выбирают из группы, состоящей из N и C-Z23, где не более чем три из U1 - U4 представляют собой N, и где
каждый Z23 независимо выбран из группы, состоящей из водорода, галогена, циано, С1-С4-алкила, С1-С4-галогеналкила, имеющего от 1 до 5 атомов галогена, С1-С4-алкокси,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
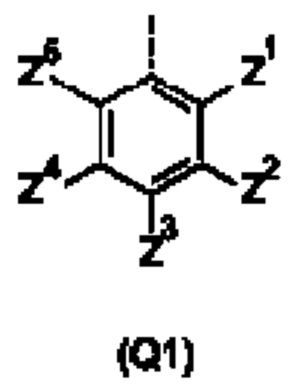
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила и метокси,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, метила, этила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
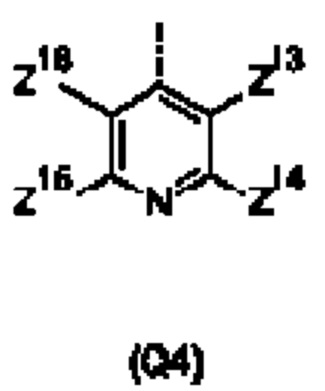
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, этокси, изопропокси, гидроксиметила, NH2, -NHMe -NMe2, -NH-C(O)-Me, морфолинила, или
Q представляет собой пиридиновое кольцо формулы (Q5)
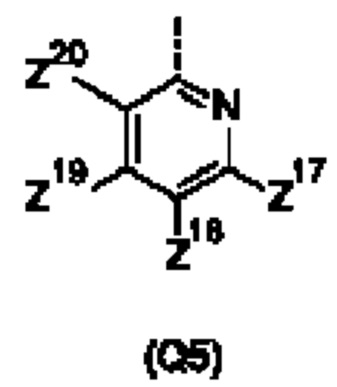
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой фтор, хлора, или
Q выбирают из группы, состоящей из
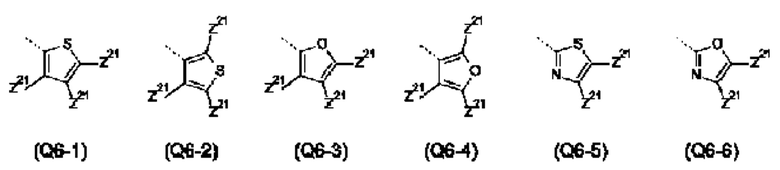
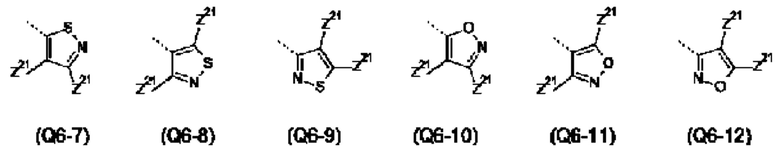
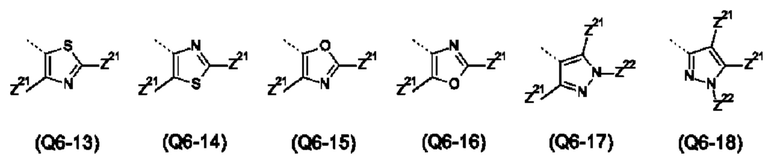
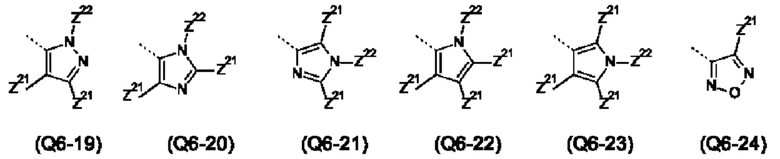
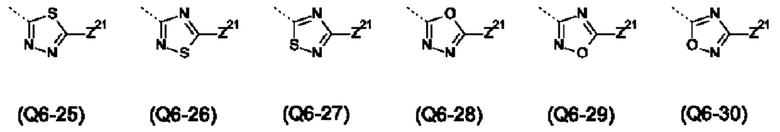
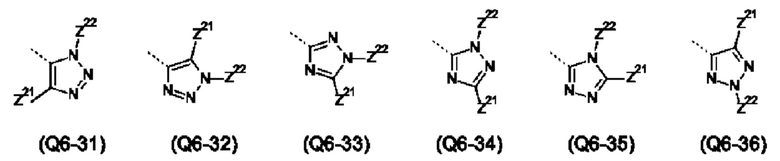
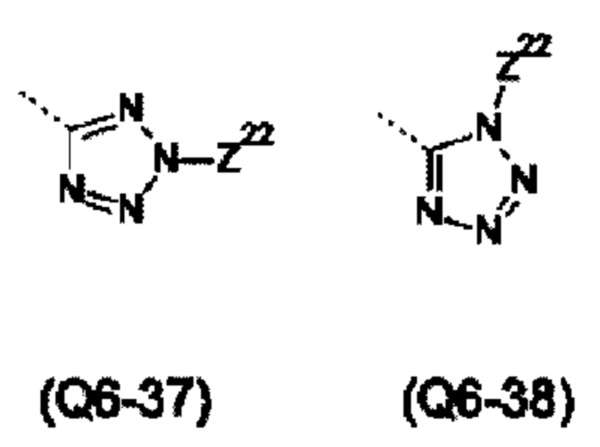
в которой:
каждый Z21 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, метокси и
Z22 представляет собой водород, метил, или
Q выбирают из группы, состоящей из
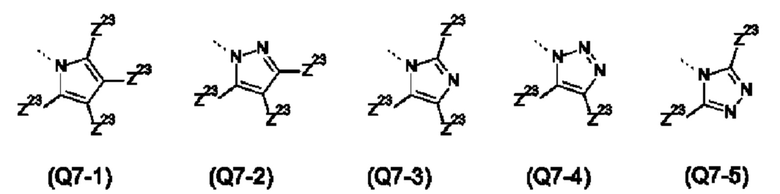
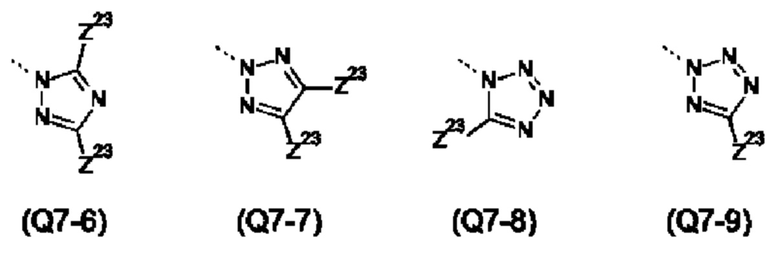
в которой:
каждый Z23 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, метокси, или
Q выбирают из группы, состоящей из
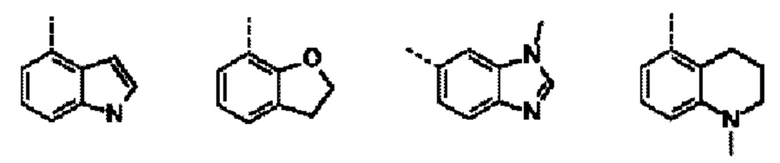
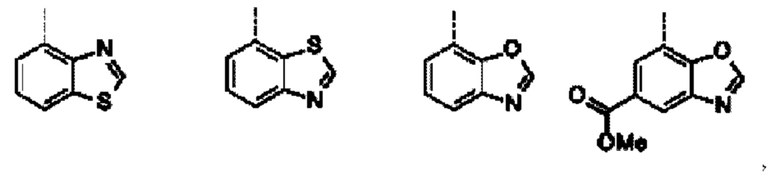
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
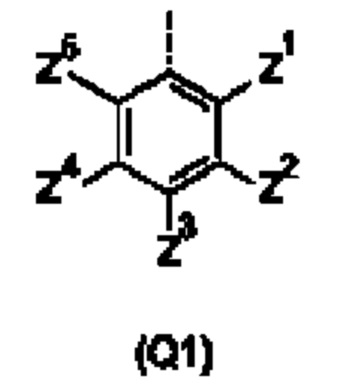
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила, метокси и трифторметила,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
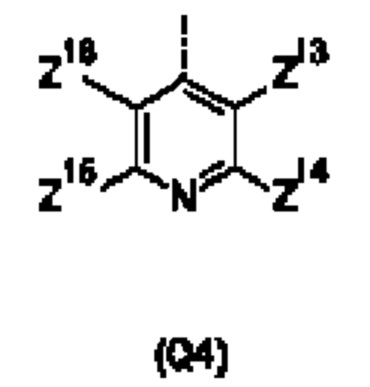
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, этокси, изопропокси, гидроксиметила, NH2, -NHMe -NMe2, -NH-C(O)-Me, морфолинила, или
Q представляет собой пиридиновое кольцо формулы (Q5)
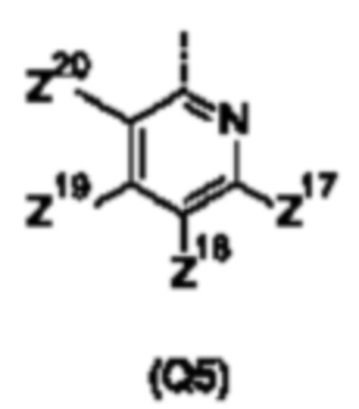
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой фтор, хлор или
Q выбирают из группы, состоящей из
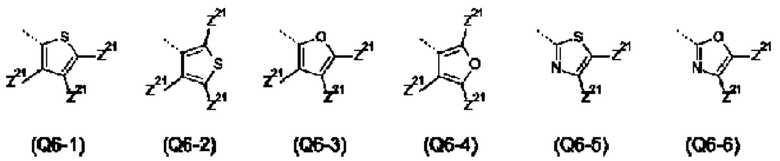
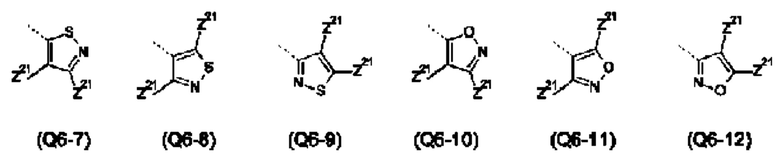
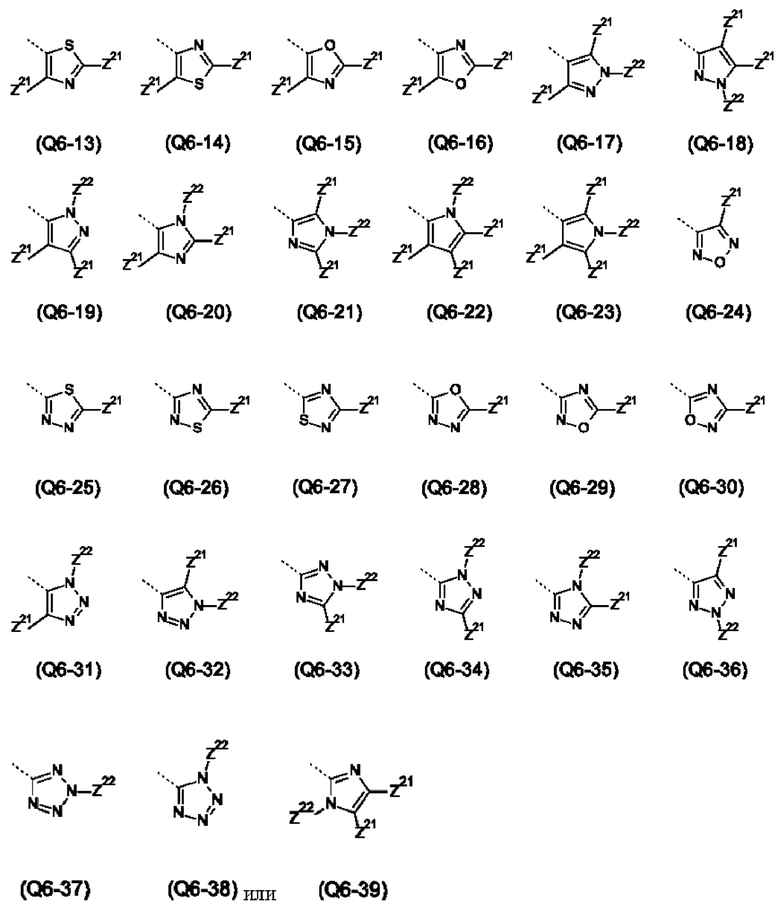
в которой:
каждый Z21 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, метокси и
Z22 представляет собой водород метил, или
Q выбирают из группы, состоящей из
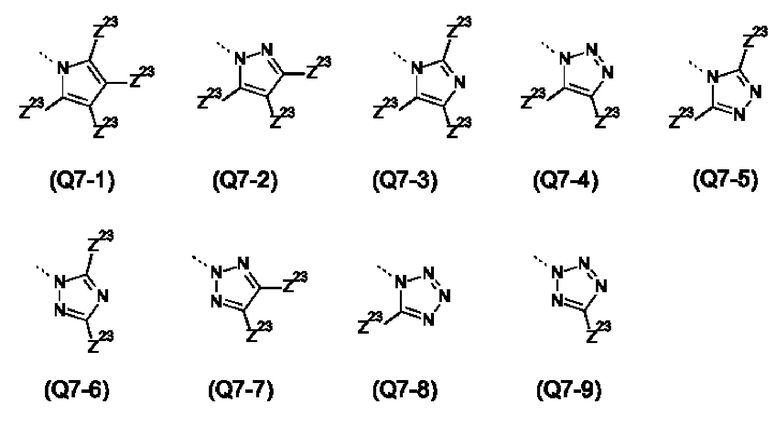
в которой:
каждый Z23 независимо выбран из группы, состоящей из водорода, фтора, хлора, пиано, метила, трифторметила, метокси, или
Q выбирают из группы, состоящей из
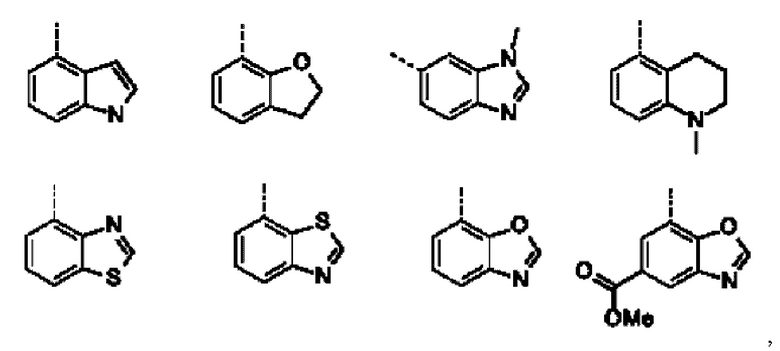
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой:
Q представляет собой замещенное фенильное кольцо формулы (Q1)
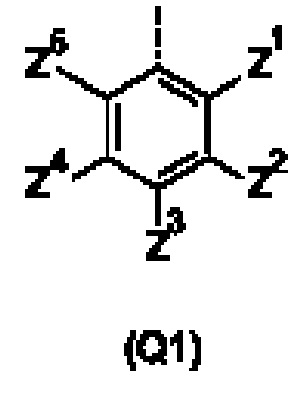
в которой:
Z1 и Z5 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, метила, метокси и трифторметила,
Z2 и Z4 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, -ОН, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
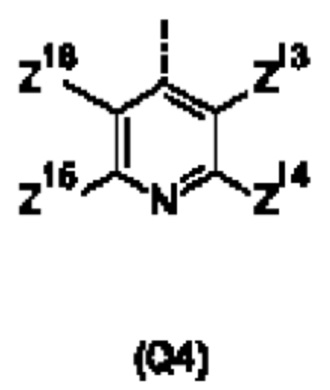
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбирают из группы, состоящей из водорода, фтора, хлора, пиано, метила, метокси, этокси, изопропокси, гидроксиметила, NH2, -NHMe -NMe2, -NH-C(O)-Me, морфолинила, или
Q выбирают из группы, состоящей из
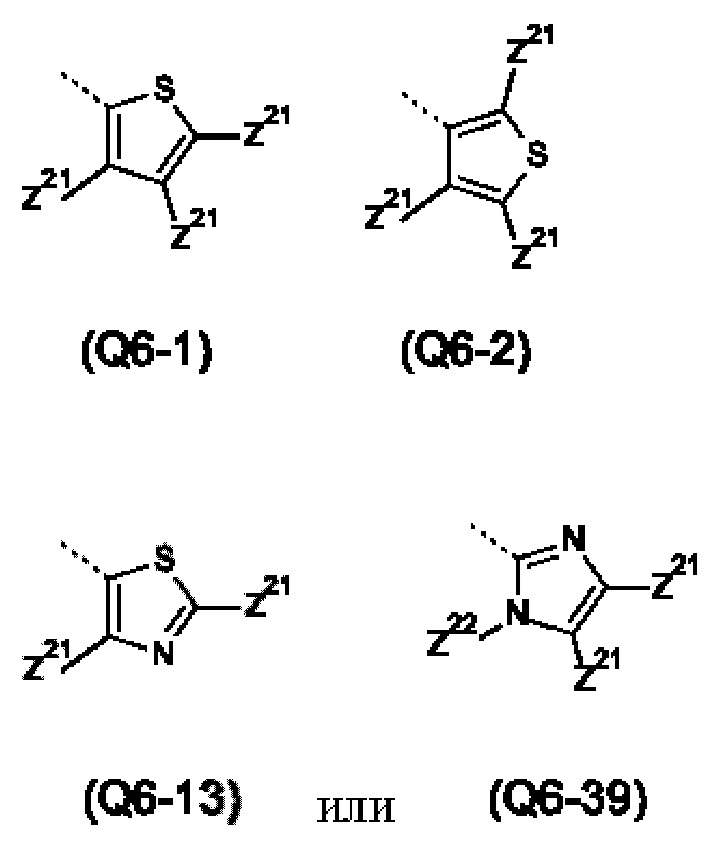
в которой:
каждый Z21 независимо выбран из группы, состоящей из водорода, фтора, хлора, пиано, метила, трифторметила, метокси и
Z22 представляет собой водород, метил, или
Q выбирают из группы, состоящей из
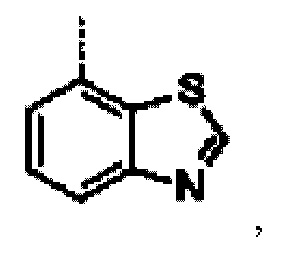
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте выполнения первого объекта настоящего изобретения, настоящее изобретение охватывает соединения общей формулы (I), выше, в которой
А представляет собой A3 или А4
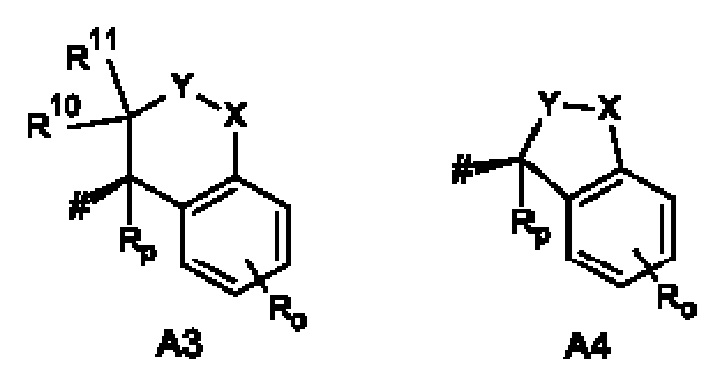
в которой
Rp выбирают из группы, состоящей из водорода, С1-С4-алкила; предпочтительно водорода,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В другом варианте настоящего изобретения в любом или во всех вариантах выполнения настоящего изобретения с первого по восьмой (включая варианты выполнения настоящего изобретения, обозначенные как "другие варианты выполнения первого объекта настоящего изобретения") из определения X и/или Y значение "NR9", как определено выше.
В другом варианте настоящего изобретения в любом или во всех вариантах выполнения настоящего изобретения с первого по восьмой (включая варианты выполнения настоящего изобретения, обозначенные как "другие варианты выполнения первого объекта настоящего изобретения") из определения R2 водород исключен.
В конкретном другом варианте выполнения первого объекта настоящее изобретение охватывает комбинации двух или более из вышеуказанных вариантов выполнения настоящего изобретения, обозначенных как "другие варианты выполнения первого объекта настоящего изобретения".
Настоящее изобретение охватывает любую подкомбинацию в рамках любого варианта выполнения настоящего изобретения или объекта настоящего изобретения соединений общей формулы (I), выше.
Настоящее изобретение охватывает соединения общей формулы (I), которые раскрыты в части Примеры в описании настоящего изобретения, ниже.
Соединения согласно настоящему изобретению общей формулы (I) могут быть получены согласно схемам 1а-е, 2, 3 и 4, как показано в Экспериментальной части настоящего изобретения (Общие методики). Описанные схемы и методики иллюстрируют пути синтеза соединений общей формулы (I) согласно настоящему изобретению и не предназначены для ограничения. Специалисту в данной области ясно, что порядок преобразований, как показано на схемах 1а-е, 2 и 3, может быть модифицирован различными способами. Следовательно, порядок преобразований, приведенный в качестве примера на этих схемах, не является ограничивающим. Кроме того, взаимопревращение любого из заместителей Q, A, R1, R2, R3, R4, R5 или R6 может быть достигнуто до и/или после приведенных примеров преобразований. Эти модификации могут быть такими, как введение защитных групп, отщепление защитных групп, восстановление или окисление функциональных групп, галогенирование, металлирование, замещение или другие реакции, известные специалисту в данной области. Эти преобразования включают те, которые вводят функциональную группу, которая позволяет дальнейшее взаимопревращение заместителей. Соответствующие защитные группы и их введение и отщепление хорошо известны специалисту в данной области (смотрите, например, T.W. Greene и P.G.M. Wuts в Protective Groups in Organic Synthesis, 3rd edition, Wiley 1999). Конкретные примеры описаны в последующих абзацах.
Далее несколько путей получения соединений общей формулы (I) описаны на схемах 1а-е и 2.
В соответствии со вторым объектом, настоящее изобретение охватывает способы получения соединений общей формулы (I), как указано выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1N:
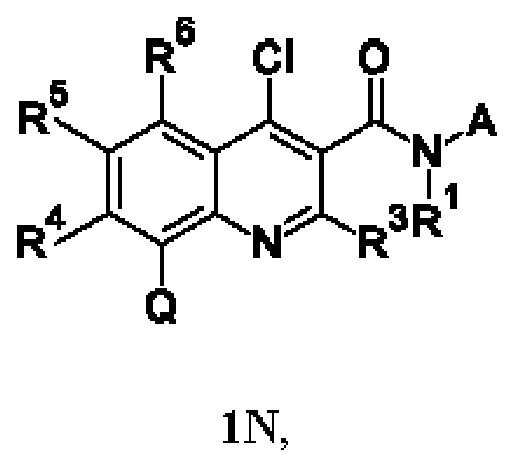
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1F:
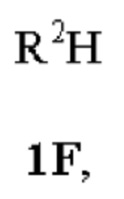
в которой R2 представляет собой NR12R13, OR14, или SR15, каждый как определено для соединения общей формулы (I), как указано выше,
таким образом, получая соединение общей формулы (I):
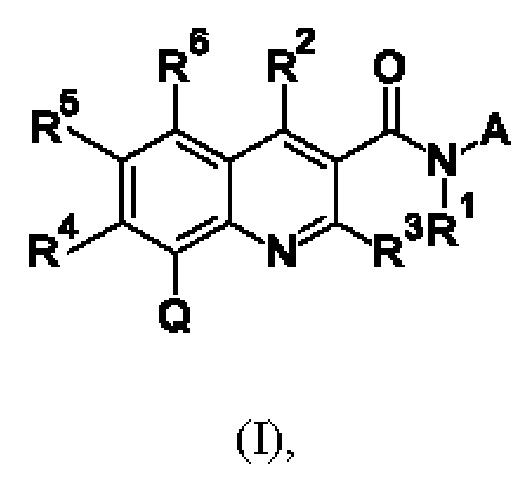
в которой А, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше.
Согласно альтернативному варианту выполнения второго объекта настоящего изобретения, настоящее изобретение охватывает способы получения соединений общей формулы (I), как указано выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1Т:
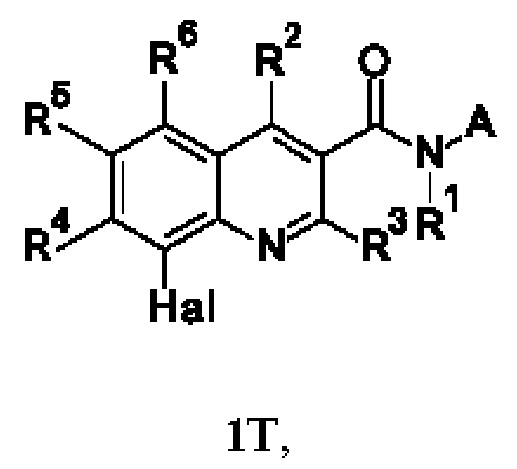
в которой A, R1, R2, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше, и в которой Hal представляет собой галоген, в частности хлор, бром или иод,
в реакцию с соединением общей формулы 1H:
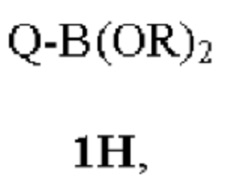
в которой Q имеет значения, как определено для соединения общей формулы (I), как указано выше, и каждый R может по отдельности представлять собой Н или Me, или оба R представляют собой пинаколат,
таким образом, получая соединение общей формулы (I):
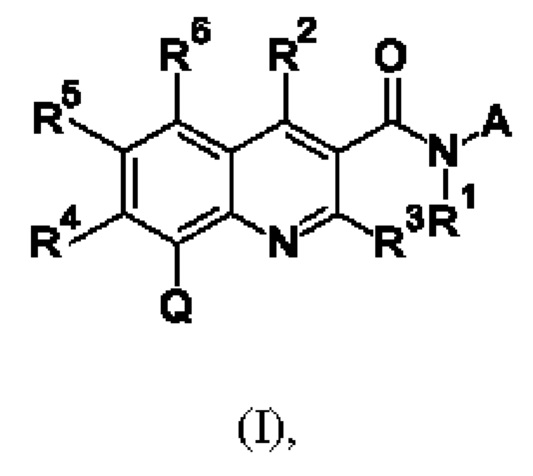
в которой А, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше.
Согласно альтернативному варианту выполнения второго объекта настоящего изобретения, настоящее изобретение охватывает способы получения соединений общей формулы (I), как указано выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1W:
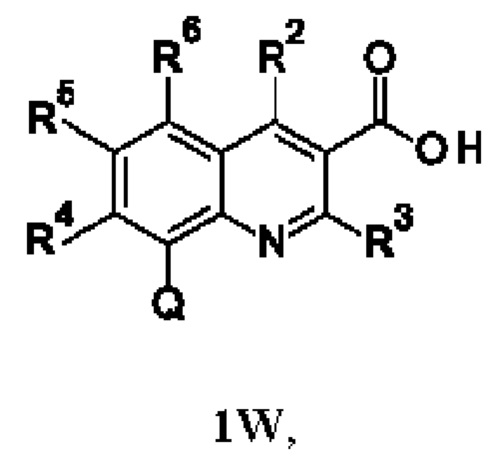
в которой Q, R2, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1М:

в которой R1 и А имеют значения, как определено для соединений общей формулы (I), как указано выше,
таким образом, получая соединение общей формулы (I):
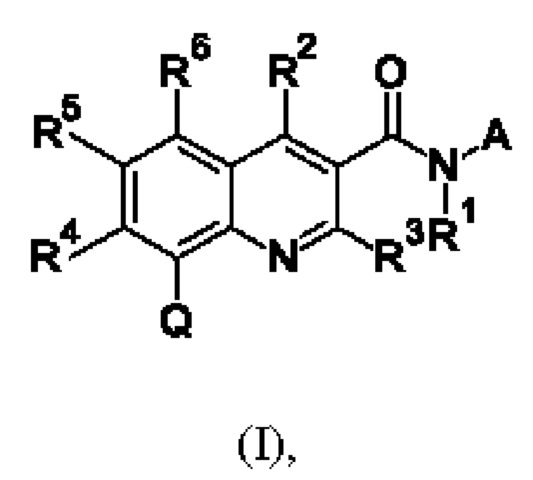
в которой A, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше.
Согласно альтернативному варианту выполнения второго объекта настоящего изобретения, настоящее изобретение охватывает способы получения соединений общей формулы (I), как указано выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1X:
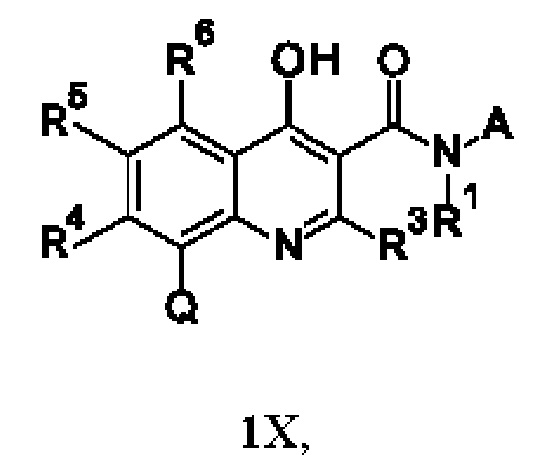
в которой Q, A, R1, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1Y:
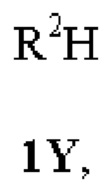
в которой R2 представляет собой OR14, как определено для соединения общей формулы (I), как указано выше,
таким образом, получая соединение общей формулы (I):
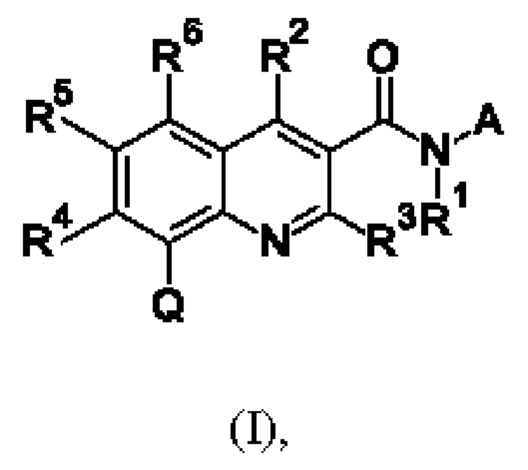
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как указано выше, и R2 представляет собой С1-С4-алкокси, который необязательно замещен, как определено выше.
Согласно альтернативному варианту выполнения второго объекта настоящего изобретения, настоящее изобретение охватывает способы получения соединений общей формулы (1), как указано выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1N:
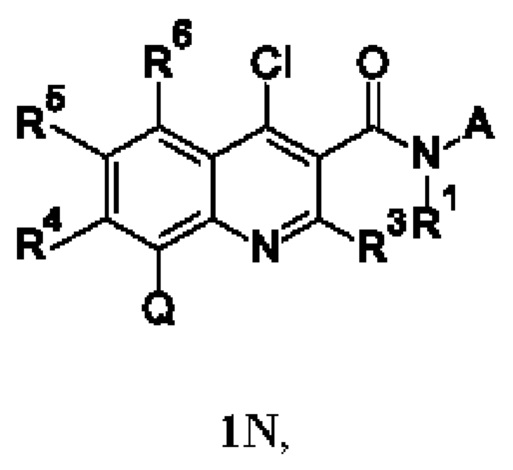
в которой Q, A, R1, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 2А:
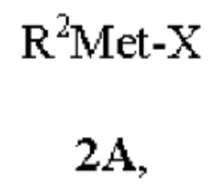
в которой R2 представляет собой C1-C4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, С3-С6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкил, каждый из которых необязательно замещен, как определено для соединения общей формулы (I), как указано выше, Met представляет собой магний или цинк, и X представляет собой хлор, бром или иод,
таким образом, получая соединение общей формулы (I):
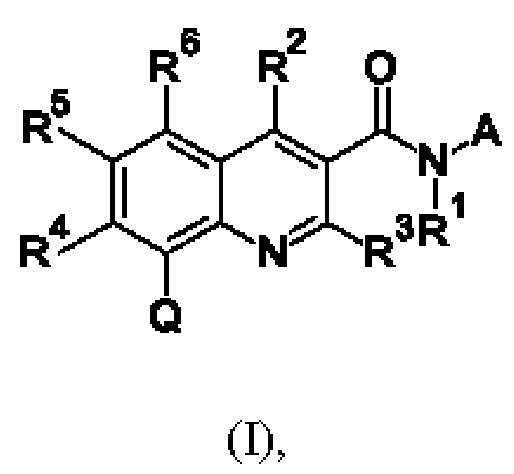
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как указано выше и R2 представляет собой С1-С4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, C3-C6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкила, каждый из которых необязательно замещен, как определено выше.
Третьим объектом настоящего изобретения являются способы получения соединений общей формулы (I), как определено выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1N:
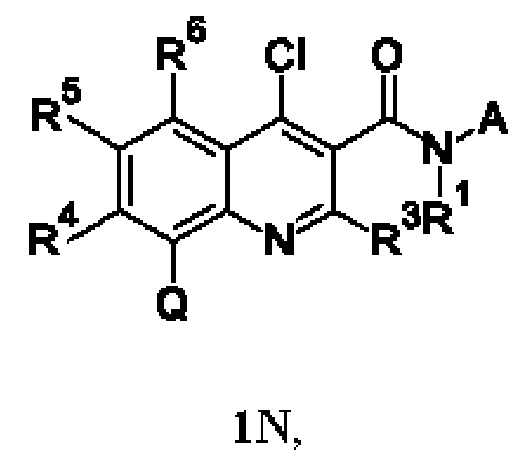
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1F:
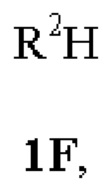
в которой R2 представляет собой NR12R13, OR14, или SR15, каждый как определено для соединения общей формулы (I), как указано выше,
таким образом, получая соединение общей формулы (I):
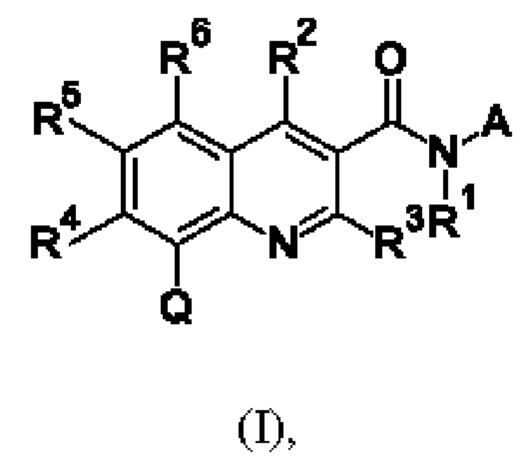
в которой A, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше,
затем необязательно превращения указанного соединения в сольваты, соли и/или сольваты таких солей, применяя соответствующие (i) растворители и/или (ii) основания или кислоты.
В соответствии с альтернативным вариантом выполнения третьего объекта настоящее изобретение охватывает способы получения соединений общей формулы (I), как определено выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1Т:
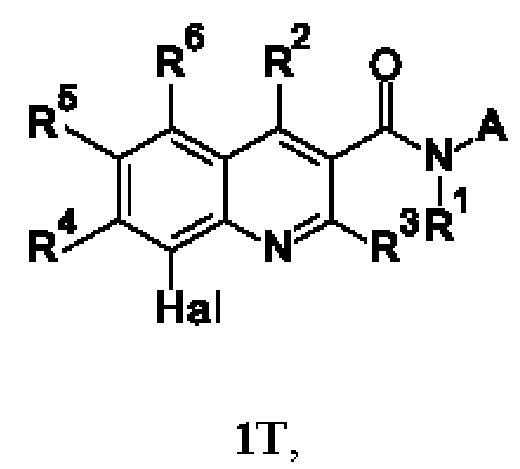
в которой A, R1, R2, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше, и в которой Hal представляет собой галоген, в частности хлор, бром или иод,
в реакцию с соединением общей формулы 1H:
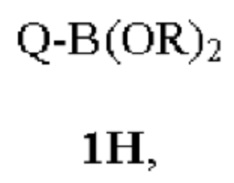
в которой Q имеет значения, как определено для соединения общей формулы (I), как указано выше, и каждый R может по отдельности представлять собой Н или Me, или оба R представляют собой пинаколат,
таким образом, получая соединение общей формулы (I):
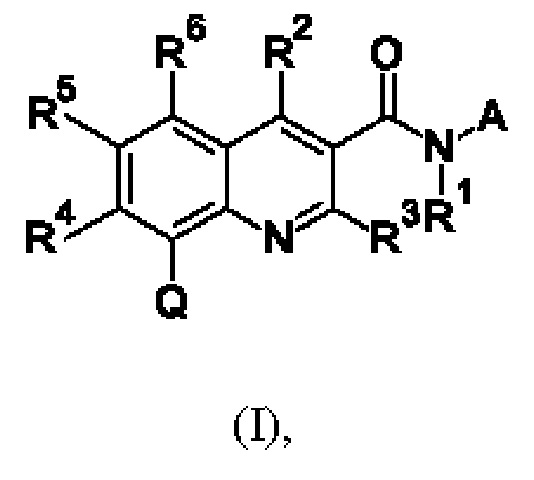
в которой A, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше,
затем необязательно превращения указанного соединения в сольваты, соли и/или сольваты таких солей, применяя соответствующие (i) растворители и/или (ii) основания или кислоты.
В соответствии с альтернативным вариантом выполнения третьего объекта настоящее изобретение охватывает способы получения соединений общей формулы (I), как определено выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1W:
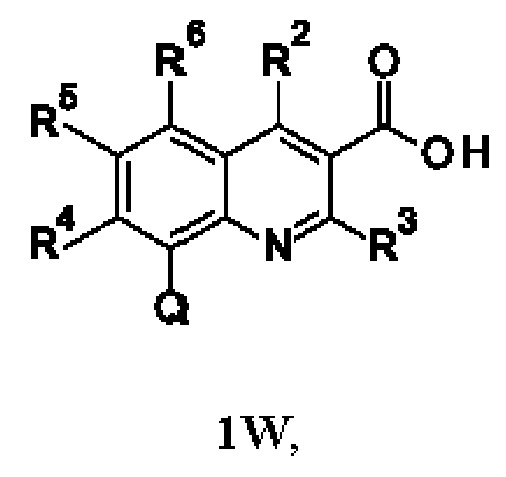
в которой Q, R2, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1М:
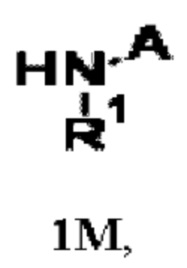
в которой R1 и А имеют значения, как определено для соединений общей формулы (I), как указано выше,
таким образом, получая соединение общей формулы (I):
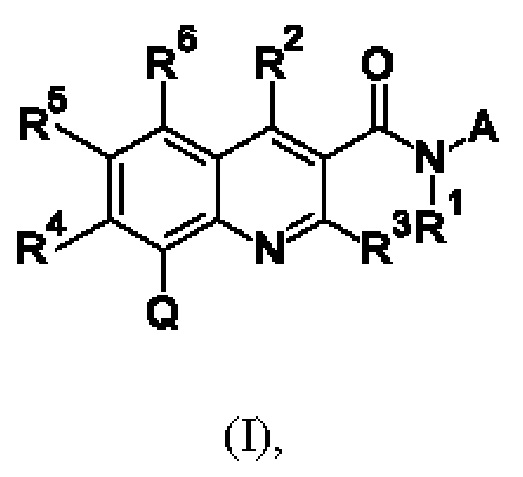
в которой А, R1, R2, R3, R4, R5, R6, и Q имеют значения, как указано выше,
затем необязательно превращения указанного соединения в сольваты, соли и/или сольваты таких солей, применяя соответствующие (i) растворители и/или (ii) основания или кислоты.
В соответствии с альтернативным вариантом выполнения третьего объекта настоящее изобретение охватывает способы получения соединений общей формулы (I), как определено выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1X:
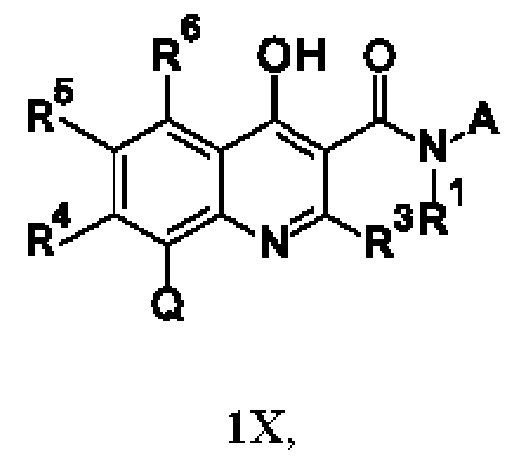
в которой Q, A, R1, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 1Y:
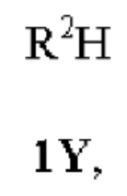
в которой R2 представляет собой OR14, как определено для соединения общей формулы (I), как указано выше, таким образом, получая соединение общей формулы (I):
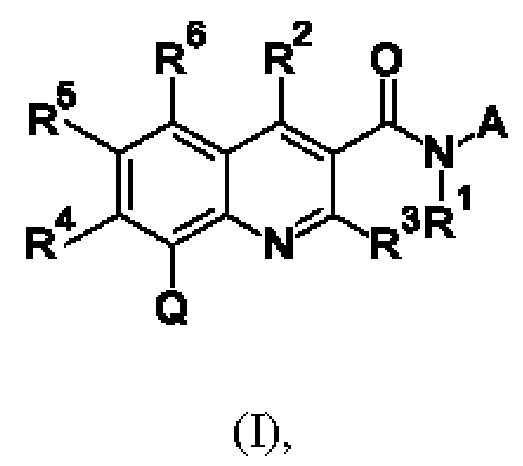
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как указано выше, и R2 представляет собой С1-С4-алкокси, который необязательно замещен, как определено выше,
затем необязательно превращения указанного соединения в сольваты, соли и/или сольваты таких солей, применяя соответствующие (i) растворители и/или (ii) основания или кислоты.
В соответствии с альтернативным вариантом выполнения третьего объекта настоящее изобретение охватывает способы получения соединений общей формулы (I), как определено выше, причем указанные способы включают стадию введения промежуточного соединения общей формулы 1N:
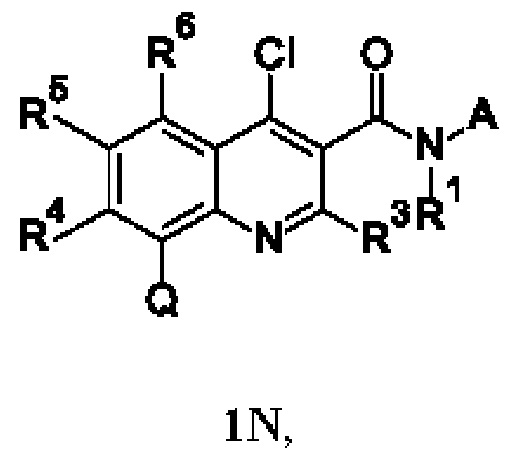
в которой Q, A, R1, R3, R4, R5 и R6 имеют значения, как определено для соединений общей формулы (I), как указано выше,
в реакцию с соединением общей формулы 2А:
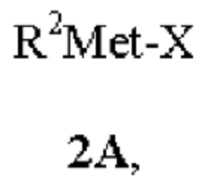
в которой R2 представляет собой С1-С4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, С3-С6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкил, каждый из которых необязательно замещен, как определено для соединения общей формулы (I), как указано выше, Met представляет собой магний или цинк, и X представляет собой хлор, бром или иод,
таким образом, получая соединение общей формулы (I):
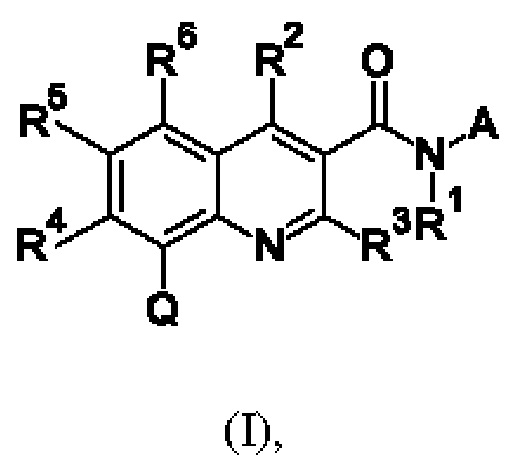
в которой A, R1, R3, R4, R5, R6, и Q имеют значения, как указано выше и R2 представляет собой С1-С4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, С3-С6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкил, каждый из которых необязательно замещен, как определено выше,
затем необязательно превращения указанного соединения в сольваты, соли и/или сольваты таких солей, применяя соответствующие (i) растворители и/или (ii) основания или кислоты.
Настоящее изобретение охватывает способы получения соединений согласно настоящему изобретению общей формулы (I), причем указанные способы включают стадии, как описано в Экспериментальной части в настоящей заявке.
Четвертым объектом настоящего изобретения являются промежуточные соединения, которые полезны для получения соединений общей формулы (I), выше.
В частности, настоящее изобретение охватывает промежуточные соединения общей формулы (II):
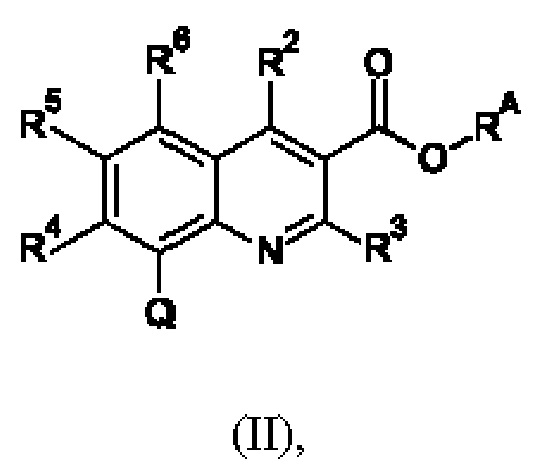
в которой
R представляет собой -ОН или как определено для соединений общей формулы (I) выше,
R3, R4, R5, R6, и Q имеют значения, как определено для соединений общей формулы (I) выше, и
RA представляет собой Н или С1-С4-алкил,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
В частности, настоящее изобретение также охватывает промежуточные соединения общей формулы (III):
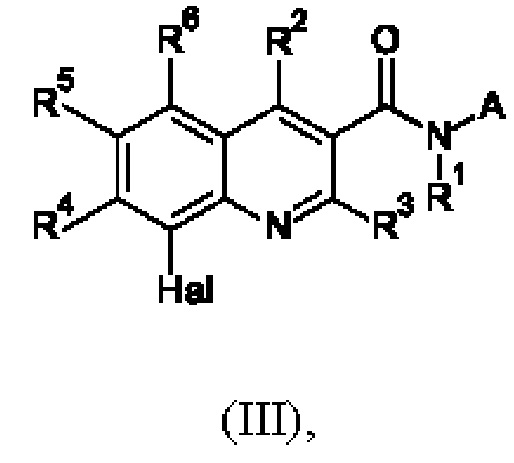
в которой
R2 представляет собой -ОН или как определено для соединений общей формулы (I) выше,
A, R1, R3, R4, R5, и R6 имеют значения, как определено для соединений общей формулы (I) выше, и
Hal представляет собой галоген,
и их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и их соли, и смеси указанных.
Пятым объектом настоящего изобретения является применение указанных промежуточных соединений для получения соединения общей формулы (I), как определено выше.
В частности, настоящее изобретение охватывает применение промежуточных соединений общей формулы (II):
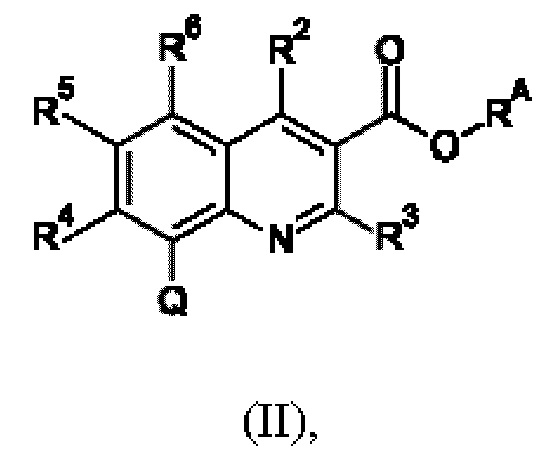
в которой
R2 представляет собой -ОН или как определено для соединений общей формулы (I) выше,
R3, R4, R5, R6, и Q имеют значения, как определено для соединений общей формулы (I) выше, и
RA представляет собой Н или С1-С4-алкил,
для получения соединения общей формулы (I), как определено выше.
В частности, настоящее изобретение также охватывает применение промежуточных соединений общей формулы (III):
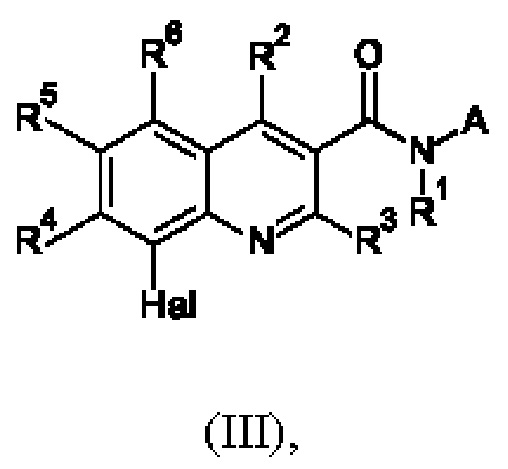
в которой
R2 представляет собой -ОН, как определено для соединений общей формулы (I) выше,
A, R1, R3, R4, R5, и R6 имеют значения, как определено для соединений общей формулы (I) выше, и
Hal представляет собой галоген,
для получения соединения общей формулы (I), как определено выше.
Настоящее изобретение охватывает промежуточные соединения, которые раскрыты в Экспериментальной части в описании настоящего изобретения, ниже.
Соединения общей формулы (I), согласно настоящему изобретению, могут быть превращены в любую соль, предпочтительно фармацевтически приемлемые соли, как описано в настоящей заявке, любым способом, который известен специалисту в данной области техники. Аналогично любая соль соединения общей формулы (I) согласно настоящему изобретению, может быть превращена в свободное соединение любым способом, который известен специалисту в данной области техники.
Соединения общей формулы (I) согласно настоящему изобретению продемонстрировали ценный фармакологический спектр действия, которого нельзя было предсказать. Соединения соответствовали настоящему изобретению, как неожиданно было обнаружено, эффективно взаимодействовать с Slo-1, и поэтому можно использовать указанные соединения для лечения или профилактики заболеваний, особенно гельминтоза, в частности, желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций с нематодами у людей и животных.
Соединения согласно настоящему можно использовать изобретению для контроля, лечения и/или профилактики гельминтоза, в частности желудочно-кишечных и внекишечного гельминтоза. Этот способ включает введение нуждающемуся в этом млекопитающему небольшого количества соединения по настоящему изобретению или его фармацевтически приемлемой соли, изомера, полиморфа, метаболита, гидрата, сольвата или сложного эфира; которые эффективны для лечения нарушения.
В альтернативном варианте этот способ включает введение птицам, а именно птицам клеточного содержания или, в частности, домашней птице, нуждающимся в этом, количества соединения согласно настоящему изобретению или его фармацевтически приемлемой соли, изомера, полиморфа, метаболита, гидрата, сольвата или сложного эфира; которые эффективны для лечения нарушения.
В частности, в области ветеринарной медицины соединения согласно настоящему изобретению подходят с благоприятной токсичностью у теплокровных животных, для борьбы с паразитами, в частности гельминтами, которые встречаются в животноводстве, разведении животных, зоопарке, лаборатории, у экспериментальных и домашних животных. Они активны против всех или конкретных стадий развития паразитов, в частности гельминтов.
Сельскохозяйственные животные включают, например, млекопитающих, таких как овцы, козы, лошади, ослы, верблюды, буйволы, кролики, олени, палевые олени и, в частности, крупный рогатый скот и свиньи; или птиц, таких как индейки, утки, гуси и, в частности, цыплята; или рыб или ракообразных, например, в аквакультуре.
Домашние животные включают, например, млекопитающих, таких как хомяки, морские свинки, крысы, мыши, шиншиллы, хорьки или, в частности, собаки, кошки; птицы клеточного содержания; рептилии; амфибии или аквариумные рыбы.
Настоящее изобретение также обеспечивает способы лечения гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
Эти нарушения хорошо охарактеризованы у животных, и их можно лечить путем введения фармацевтических композиций согласно настоящему изобретению.
Термин «лечить» или «лечение», используемый в описании настоящего изобретения, используется традиционно, например, контроль или уход за субъектом с целью борьбы, облегчения, уменьшения, освобождения, улучшения состояния болезни или нарушения, таких как инфекция, вызванная нематодами. В частности и особенно в области здоровья животных или ветеринарной области, термин «лечить» или «лечение» включает профилактическое, метафилактическое или терапевтическое лечение.
Гельминты, патогенные для человека или животных, включают, например, скребни, нематоды, пентастомы и плоские черви (например, моногенеи, цестоды и трематоды).
Примерные гельминты включают, без какого-либо ограничения:
Моногенеи: например: Dactylogyrus spp., Gyrodactylus spp., Microbothrium spp., Polystoma spp., Troglocephalus spp.
Цестоды: из отряда Pseudophyllidea, например: Bothridium spp., Diphyllobothrium spp., Diplogonoporus spp., Ichthyobothrium spp., Ligula spp., Schistocephalus spp., Spirometra spp.
из отряда Циклофиллиды, например: Andyra spp., Anoplocephala spp., Avitellina spp., Bertiella spp., Cittotaenia spp., Davainea spp., Diorchis spp., Diplopylidium spp., Dipylidium spp., Echinococcus spp., Echinocotyle spp., Echinolepis spp., Hydatigera spp., Hymenolepis spp., Joyeuxiella spp., Mesocestoides spp., Moniezia spp., Paranoplocephala spp., Raillietina spp., Stilesia spp., Taenia spp., Thysaniezia spp., Thysanosoma spp.
Трематоды: из класса дигенетические сосальщики, например: Austrobilharzia spp., Brachylaima spp., Calicophoron spp., Catatropis spp., Clonorchis spp.Collyriclum spp., Cotylophoron spp., Cyclocoelum spp., Dicrocoelium spp., Diplostomum spp., Echinochasmus spp., Echinoparyphium spp., Echinostoma spp., Eurytrema spp., Fasciola spp., Fasciolides spp., Fasciolopsis spp., Fischoederius spp., Gastrothylacus spp., Gigantobilharzia spp., Gigantocotyle spp., Heterophyes spp., Hypoderaeum spp., Leucochloridium spp., Metagonimus spp., Metorchis spp., Nanophyetus spp., Notocotylus spp., Opisthorchis spp., Ornithobilharzia spp., Paragonimus spp., Paramphistomum spp., Plagiorchis spp., Posthodiplostomum spp., Prosthogonimus spp., Schistosoma spp., Trichobilharzia spp., Troglotrema spp., Typhlocoelum spp.
Нематоды: из отряда Trichinellida, например: Capillaria spp., Eucoleus spp., Paracapillaria spp., Trichinella spp., Trichomosoides spp., Trichuris spp.
из отряда Тиленхиды, например: Micronema spp., Parastrongyloides spp., Strongyloides spp.
из отряда Rhabditina, например: Aelurostrongylus spp., Amidostomum spp., Ancylostoma spp., Angiostrongylus spp., Bronchonema spp., Bunostomum spp., Chabertia spp., Cooperia spp., Cooperioides spp., Crenosoma spp., Cyathostomum spp., Cyclococercus spp., Cyclodontostomum spp., Cylicocyclus spp., Cylicostephanus spp., Cylindropharynx spp., Cystocaulus spp., Dictyocaulus spp., Elaphostrongylus spp., Filaroides spp., Globocephalus spp., Graphidium spp., Gyalocephalus spp., Haemonchus spp., Heligmosomoides spp., Hyostrongylus spp., Marshallagia spp., Metastrongylus spp., Muellerius spp., Necator spp., Nematodirus spp., Neostrongylus spp., Nippostrongylus spp., Obeliscoides spp., Oesophagodontus spp., Oesophagostomum spp., Ollulanus spp.; Ornithostrongylus spp., Oslerus spp., Ostertagia spp., Paracooperia spp., Paracrenosoma spp., Parafilaroides spp., Parelaphostrongylus spp., Pneumocaulus spp., Pneumostrongylus spp., Poteriostomum spp., Protostrongylus spp., Spicocaulus spp., Stephanuras spp., Strongylus spp., Syngamus spp., Teladorsagia spp., Trichonema spp., Tricho strongylus spp., Triodontophorus spp., Troglostrongylus spp., Uncinaria spp.
из отряда Спируриды, например: Acanthocheilonema spp., Anisakis spp., Ascaridia spp.; Ascaris spp., Ascarops spp., Aspiculuris spp., Baylisascaris spp., Brugia spp., Cercopithifilaria spp., Crassicauda spp., Dipetalonema spp., Dirofilaria spp., Dracunculus spp.; Draschia spp., Enterobius spp., Filaria spp., Gnathostoma spp., Gongylonema spp., Habronema spp., Heterakis spp.; Litomosoides spp., Loa spp., Onchocerca spp., Oxiuris spp., Parabronema spp., Parafilaria spp., Parascaris spp., Passalurus spp., Physaloptera spp., Probstmayria spp., Pseudofilaria spp., Setaria spp., Skjrabinema spp., Spirocerca spp., Stephanofilaria spp., Strongyluris spp., Syphacia spp., Thelazia spp., Toxascaris spp., Toxocara spp., Wuchereria spp.
Скребни: из отряда Oligacanthorhynchida, например: Macracanthorhynchus spp., Prosthenorchis spp.; из отряда Moniliformida, например: Moniliformis spp.;
из отряда Polymorphida, например: Filicollis spp.; из отряда Echinorhynchida, например: Acanthocephalus spp., Echinorhynchus spp., Leptorhynchoides spp.
Пентастомы: из отряда Porocephalida, например: Linguatula spp.
Соединения согласно настоящему изобретению могут применяться в частности для лечения и предотвращения, т.е. профилактики, гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
Посредством применения соединений согласно настоящему изобретению для борьбы с животными паразитами, в частности гельминтами, предполагается уменьшить или предотвратить болезнь, случаи смерти и снижения производительности (в случае мяса, молока, шерсти, шкур, яиц, меда и тому подобного), так что становится возможным более экономичное и простое разведение животных и достижение лучшего благополучия животных.
Термин «борьба» или «контроль», как применяется в описании настоящего изобретения в отношении области защиты животных, означает, что соединения согласно настоящему изобретению эффективны для снижения частоты возникновения соответствующего паразита у животного, инфицированного такими паразитами, до безобидных уровней. Более конкретно, «борьба», как применяется в описании настоящего изобретения, означает, что соединения согласно настоящему изобретению эффективны для уничтожения соответствующего паразита, ингибирования его роста или ингибирования его пролиферации.
В соответствии с другим объектом, настоящее изобретение охватывает соединения общей формулы (I), как описано выше, или их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и соли, в частности их фармацевтически приемлемые соли, или их смеси, для применения для лечения или профилактики заболеваний, в частности гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
Фармацевтическая активность соединений согласно настоящему изобретению может быть пояснена посредством их взаимодействия с ионным каналом Slo-1.
В соответствии с другим объектом, настоящее изобретение охватывает применение соединений общей формулы (I), как описано выше, или их стереоизомеров, таутомеров, N-оксидов, гидратов, сольватов и солей и, в частности их фармацевтически приемлемых солей, или их смесей, для лечения или профилактики заболеваний, в частности гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
В соответствии с другим объектом, настоящее изобретение охватывает применение соединений общей формулы (I), как описано выше, или их стереоизомеров, таутомеров, N-оксидов, гидратов, сольватов и солей и, в частности их фармацевтически приемлемых солей, или их смесей, в способе лечения или профилактики заболеваний, в частности гельминтоза, особенно желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
В соответствии с другим объектом, настоящее изобретение охватывает применение соединений общей формулы (I), как описано выше, или их стереоизомеров, таутомеров, N-оксидов, гидратов, сольватов и солей и, в частности их фармацевтически приемлемых солей, или их смесей, для получения фармацевтической композиции, предпочтительно лекарственного средства, для профилактики или лечения заболеваний, в частности гельминтоза, особенно желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами.
В соответствии с другим объектом, настоящее изобретение охватывает способ лечения или профилактики заболеваний, в частности гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами, применяя эффективное количество соединения общей формулы (I), как описано выше, или его стереоизомеров, таутомеров, N-оксидов, гидратов, сольватов и солей, в частности его фармацевтически приемлемых солей или их смесей.
В соответствии с другим объектом, настоящее изобретение охватывает соединения общей формулы (I), как описано выше, или их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и соли, в частности их фармацевтически приемлемые соли, или их смеси, для применения в качестве антиэндопаразтарного средства.
В соответствии с другим объектом, настоящее изобретение охватывает соединения общей формулы (I), как описано выше, или их стереоизомеры, таутомеры, N-оксиды, гидраты, сольваты и соли, в частности их фармацевтически приемлемые соли, или их смеси, для применения в качестве антигельминтного средства, в частности для применения в качестве нематицидного средства, платигельминтоцидное средство, акантоцефалицидное средство или пентастомицидное средство.
В соответствии с другим объектом, настоящее изобретение охватывает фармацевтические композиции, в частности ветеринарную композицию, содержащую соединение общей формулы (I), как описано выше, или его стереоизомер, таутомер, N-оксид, гидроксид, сольват, соль, в частности фармацевтически приемлемую соль, или их смесь, и один или более эксципиентов, в частности один или более фармацевтически приемлемых эксципиентов. Можно использовать обычные методики для приготовления таких фармацевтических композиций в соответствующих лекарственных формах.
В соответствии с другим объектом, настоящее изобретение охватывает способ получения фармацевтической композиции, в частности ветеринарной композиции, включающий стадию смешивания соединения общей формулы (I), как описано выше, или его стереоизомера, таутомера, N-оксида, гидроксида, сольвата, соли, в частности фармацевтически приемлемой соли, или их смеси, с одним или более эксципиентами, в частности одним или более фармацевтически приемлемыми эксципиентами.
В соответствии с другим объектом, настоящее изобретение охватывает способ лечения или профилактики заболеваний, в частности гельминтоза, в частности желудочно-кишечного и внекишечного гельминтоза, более конкретно желудочно-кишечных и внекишечных инфекций, вызванных нематодами, с применением фармацевтической композиции, в частности ветеринарной композиции, содержащей эффективное количество соединения общей формулы (I), как описано выше, или его стереоизомеров, таутомеров, N-оксидов, гидратов, сольватов и солей, в частности их фармацевтически приемлемых солей, или их смесей.
Кроме того, настоящее изобретение относится к фармацевтическим композициям, в частности ветеринарным композициям, которые содержат по меньшей мере одно соединение согласно изобретению, обычно вместе с одним или более фармацевтически приемлемыми эксципиентами, и к их применению для вышеупомянутых целей.
Соединения согласно настоящему изобретению могут иметь системную и/или местную активность. С этой целью их можно вводить подходящим образом, например, через пероральный, парентеральный, легочный, назальный, подъязычный, лингвальный, буккальный, ректальный, вагинальный, дермальный, трансдермальный, конъюнктивальный, ушной путь или в виде имплантата или стента. Такое введение может быть проведено профилактически, метафилактически или терапевтически.
Для этих путей введения можно вводить соединения согласно настоящему изобретению в подходящих формах введения.
Для перорального введения можно получить соединения согласно настоящему изобретению в лекарственных формах, известных в данной области техники, которые доставляют соединения согласно настоящему изобретению быстро и/или модифицированным образом, таких как, например, таблетки (таблетки без покрытия или покрытые оболочкой таблетки, например с энтеросолюбильными покрытиями или покрытиями с контролируемым высвобождением, которые растворяются с задержкой или нерастворимы), перорально-распадающиеся таблетки, пленки/пластины, пленки/лиофилизаты, капсулы (например, твердые или мягкие желатиновые капсулы), таблетки с сахарным покрытием, гранулы, пеллеты, жевательные резинки (например мягкие жевательные резинки), порошки, эмульсии, суспензии, аэрозоли или растворы. Можно включать соединения согласно настоящему изобретению в кристаллической и/или аморфизированной и/или растворенной форме в указанные лекарственные формы.
Парентеральное введение может быть осуществлено с предотвращением стадии абсорбции (например, внутривенно, внутриартериально, внутрисердечно, внутриспинально или эндолюмбально) или с включением абсорбции (например, внутримышечно, подкожно, внутрикожно, чрескожно или внутрибрюшинно). Формы введения, которые подходят для парентерального введения, включают, среди прочего, препараты для инъекций и инфузии в виде растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков.
Примерами, подходящими для других путей введения, являются фармацевтические формы для ингаляции (в том числе порошковые ингаляторы, небулайзеры), назальные капли, назальные растворы, назальные спреи; таблетки/пленки/пастилки/капсулы для лингвального, сублингвального или буккального введения; суппозитории; глазные капли, глазные мази, глазные ванны, линзы, ушные капли, ушные аэрозоли, ушные порошки, ушные протирки, ушные тампоны; вагинальные капсулы, водные суспензии (лосьоны, микстуры, требующие взбалтывания), липофильные суспензии, эмульсии, мази, кремы, трансдермальные терапевтические системы (такие как, например, пластыри), молоко, пасты, пены, точечно наносимые средства, пылевидные порошки, имплантаты или стенты.
Соединения согласно настоящему изобретению могут быть включены в указанные формы введения. Это может быть осуществлено известным образом путем смешивания с фармацевтически приемлемыми эксципиентами. Фармацевтически приемлемые эксципиенты включают, среди прочего,
 наполнители и носители (например, целлюлоза, микрокристаллическая целлюлоза (например, Avicel®), лактоза, маннит, крахмал, фосфат кальция (такой как, например, Di-Cafos®)),
наполнители и носители (например, целлюлоза, микрокристаллическая целлюлоза (например, Avicel®), лактоза, маннит, крахмал, фосфат кальция (такой как, например, Di-Cafos®)),
 основания мази (например, вазелин, парафины, триглицериды, воски, шерстный воск, спирты шерстного воска, ланолин, гидрофильная мазь, полиэтиленгликоли),
основания мази (например, вазелин, парафины, триглицериды, воски, шерстный воск, спирты шерстного воска, ланолин, гидрофильная мазь, полиэтиленгликоли),
 основания для суппозиторий (например полиэтиленгликоль, кокосовое масло, твердый жир),
основания для суппозиторий (например полиэтиленгликоль, кокосовое масло, твердый жир),
 растворители (например, вода, этанол, изопропанол, глицерин, пропиленгликоль, жирные масла триглицеридов средней длины цепи, жидкие полиэтиленгликоли, парафины),
растворители (например, вода, этанол, изопропанол, глицерин, пропиленгликоль, жирные масла триглицеридов средней длины цепи, жидкие полиэтиленгликоли, парафины),
 поверхностно-активные вещества, эмульгаторы, диспергирующие средства или смачивающие средства (например, натрия додецилсульфат), лецитин, фосфолипиды, жирные спирты (такие как, например, Lanette®), сложные эфиры сорбитана и жирной кислоты (такие как, например, Span®), полиоксиэтиленовые сложные эфиры сорбитана и жирной кислоты (такие как, например, Tween®), полиоксиэтиленовые глицериды жирной кислоты (такие как, например, Cremophor®), полиоксиэтиленовые сложные эфиры жирной кислоты, полиоксиэтиленовые сложные эфиры жирного спирта, глицериновые сложные эфиры жирной кислоты, полоксамеры (такие как, например, Pluronic®),
поверхностно-активные вещества, эмульгаторы, диспергирующие средства или смачивающие средства (например, натрия додецилсульфат), лецитин, фосфолипиды, жирные спирты (такие как, например, Lanette®), сложные эфиры сорбитана и жирной кислоты (такие как, например, Span®), полиоксиэтиленовые сложные эфиры сорбитана и жирной кислоты (такие как, например, Tween®), полиоксиэтиленовые глицериды жирной кислоты (такие как, например, Cremophor®), полиоксиэтиленовые сложные эфиры жирной кислоты, полиоксиэтиленовые сложные эфиры жирного спирта, глицериновые сложные эфиры жирной кислоты, полоксамеры (такие как, например, Pluronic®),
 буферы, кислоты и основания (например фосфаты, карбонаты, лимонная кислота, уксусная кислота, соляная кислота, раствор гидроксида натрия, аммония карбонат, трометамол, триэтаноламин),
буферы, кислоты и основания (например фосфаты, карбонаты, лимонная кислота, уксусная кислота, соляная кислота, раствор гидроксида натрия, аммония карбонат, трометамол, триэтаноламин),
 изотонические средства (например, глюкоза, хлорид натрия),
изотонические средства (например, глюкоза, хлорид натрия),
 адсорбенты (например, высоко диспергированные диоксиды кремния),
адсорбенты (например, высоко диспергированные диоксиды кремния),
 повышающие вязкость средства, гелеобразоатели, загустители и/или связующие вещества (например, поливинилпирролидон, метилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, карбоксиметилцеллюлоза-натрий, крахмал, карбомеры, полиакриловые кислоты (такие как, например, Carbopol®); альгинаты, желатин),
повышающие вязкость средства, гелеобразоатели, загустители и/или связующие вещества (например, поливинилпирролидон, метилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, карбоксиметилцеллюлоза-натрий, крахмал, карбомеры, полиакриловые кислоты (такие как, например, Carbopol®); альгинаты, желатин),
 дезинтегрирующие средства (например, модифицированный крахмал, карбоксиметилцеллюлоза-натрий, натрия крахмала гликолят (как например, Explotab®), поперечно-сшитый поливинилпирролидон, кроскармеллоза-натрий (как например, AcDiSol®)),
дезинтегрирующие средства (например, модифицированный крахмал, карбоксиметилцеллюлоза-натрий, натрия крахмала гликолят (как например, Explotab®), поперечно-сшитый поливинилпирролидон, кроскармеллоза-натрий (как например, AcDiSol®)),
 регуляторы скорости потока, смазывающие вещества, вещества, способствующие скольжению и смазки, облегчающие выемке изделий из форм (например, стеарат магния, стеариновая кислота, тальк, высоко диспергированные диоксиды кремния (как например, Aerosil®)),
регуляторы скорости потока, смазывающие вещества, вещества, способствующие скольжению и смазки, облегчающие выемке изделий из форм (например, стеарат магния, стеариновая кислота, тальк, высоко диспергированные диоксиды кремния (как например, Aerosil®)),
 покрывающие вещества (например, сахара, шеллак) и пленкообразователи для пленок или диффузионные мембраны, которые растворяются быстро или модифицированным образом (например поливинипирролидоны (такие как, например, Kollidon®), поливиниловый спирт, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, этилцеллюлоза, гидроксипропилметилцеллюлоза фталат, целлюлозы ацетат, целлюлозы ацетат фталат, полиакрилаты, полиметакрилаты, такие как, например, Eudragit®)),
покрывающие вещества (например, сахара, шеллак) и пленкообразователи для пленок или диффузионные мембраны, которые растворяются быстро или модифицированным образом (например поливинипирролидоны (такие как, например, Kollidon®), поливиниловый спирт, гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза, этилцеллюлоза, гидроксипропилметилцеллюлоза фталат, целлюлозы ацетат, целлюлозы ацетат фталат, полиакрилаты, полиметакрилаты, такие как, например, Eudragit®)),
 материалы капсулы (например, желатин, гидроксипропилметилцеллюлоза),
материалы капсулы (например, желатин, гидроксипропилметилцеллюлоза),
 синтетические полимеры (например, полилактиды, полигликолиды, полиакрилаты, полиметакрилаты (такие как, например, Eudragit®), поливинипирролидоны (такие как, например, Kollidon®), поливиниловые спирты, поливинилацетаты, полиэтиленоксиды, полиэтиленгликоли и их сополимеры и блок-сополимеры),
синтетические полимеры (например, полилактиды, полигликолиды, полиакрилаты, полиметакрилаты (такие как, например, Eudragit®), поливинипирролидоны (такие как, например, Kollidon®), поливиниловые спирты, поливинилацетаты, полиэтиленоксиды, полиэтиленгликоли и их сополимеры и блок-сополимеры),
 пластификаторы (например полиэтиленгликоли, пропиленгликоль, глицерин, триацетин, триацетилцитрат, дибутилфталат),
пластификаторы (например полиэтиленгликоли, пропиленгликоль, глицерин, триацетин, триацетилцитрат, дибутилфталат),
 усилители проникновения,
усилители проникновения,
 стабилизаторы (например, антиоксиданты, такие как, например, аскорбиновая кислота, аскорбилпальмитат, натрия аскорбат, бутилгидроксианизол, бутилгидрокситолуол, пропилгаллат),
стабилизаторы (например, антиоксиданты, такие как, например, аскорбиновая кислота, аскорбилпальмитат, натрия аскорбат, бутилгидроксианизол, бутилгидрокситолуол, пропилгаллат),
 консерванты (например, парабены, сорбиновая кислота, тиомерзал, бензалкония хлорид, хлоргексидина ацетат, натрия бензоат),
консерванты (например, парабены, сорбиновая кислота, тиомерзал, бензалкония хлорид, хлоргексидина ацетат, натрия бензоат),
 красители (например, неорганические пигменты, такие как, например, оксиды железа, диоксид титана),
красители (например, неорганические пигменты, такие как, например, оксиды железа, диоксид титана),
 ароматизаторы, подсластители, ароматизаторы и/или средства против запаха.
ароматизаторы, подсластители, ароматизаторы и/или средства против запаха.
Кроме того, настоящее изобретение относится к фармацевтической композиции, которая содержит по меньшей мере одно соединение согласно настоящему изобретению, обычно вместе с одним или более фармацевтически приемлемыми эксципиентами и их применению согласно настоящему изобретению.
В соответствии с другим объектом настоящее изобретение охватывает фармацевтические комбинации, в частности лекарственные средства, содержащие по меньшей мере одно соединение общей формулы (I) согласно настоящему изобретению и по меньшей мере один или более дополнительные активные ингредиенты, в частности для лечения и/или профилактики эндо- и/или эктопаразитарной инфекции.
Термин «эндопаразит» в настоящем изобретении используется, как известно специалистам в данной области, и относится в частности к гельминтам. Термин «эктопаразит» в настоящем изобретении используется, как известно специалистам в данной области, и относится в частности к членистоногим, в частности насекомым или акаридам.
В частности, настоящее изобретение охватывает фармацевтическую комбинацию, в частности ветеринарную комбинацию, которая содержит:
 один или более первых активных ингредиентов, в частности соединений общей формулы (I), как указано выше, и
один или более первых активных ингредиентов, в частности соединений общей формулы (I), как указано выше, и
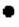 один или более дополнительных активных ингредиентов, в частности один или более эндо- и/или эктопаразитицидов.
один или более дополнительных активных ингредиентов, в частности один или более эндо- и/или эктопаразитицидов.
Термин «комбинация» в настоящем изобретении используется, как известно специалистам в данной области техники, причем указанная комбинация может быть фиксированной комбинацией, нефиксированной комбинацией или набором из частей.
«Фиксированная комбинация» в настоящем изобретении используется, как известно специалистам в данной области, и определяется как комбинация, в которой, например, первый активный ингредиент, такой как одно или более соединений общей формулы (I) согласно настоящему изобретению, и дополнительный активный ингредиент присутствуют вместе в одной единичной дозировке или в одной лекарственной форме. Одним из примеров «фиксированной комбинации» является фармацевтическая композиция, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют в смеси для одновременного введения, например, в составе. Другим примером «фиксированной комбинации» является фармацевтическая комбинация, в которой первый активный ингредиент и другой активный ингредиент присутствуют в одной единице без смешивания.
Нефиксированная комбинация или «набор из частей» в настоящем изобретении используется, как известно специалистам в данной области, и определяется как комбинация, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют в более чем одной единице. Одним из примеров нефиксированной комбинации или набора из частей является комбинация, в которой первый активный ингредиент и дополнительный активный ингредиент присутствуют раздельно. Компоненты нефиксированной комбинации или набора из частей можно вводить раздельно, последовательно, одновременно, в одно и то же время или в хронологическом порядке
Соединения согласно настоящему зрения могут быть введены в виде единственного фармацевтического агента или в сочетании с одним или более другими фармацевтически активными ингредиентами, где комбинация не вызывает неприемлемых побочных эффектов. Настоящее изобретение также охватывает такие фармацевтические комбинации. Например, соединения согласно настоящему изобретению могут быть объединены с известными эктопаразитицидами и/или эндопаразитицидами.
Другие или дополнительные активные ингредиенты, указанные в настоящей заявке под их "общим названием", известны и описаны, например, в справочнике пестицидов ("The Pesticide Manual" 16th Ed., British Crop Protection Council 2012) или могут быть обнаружены в интернете (например, http://www.alanwood.net/pesticides). Классификация основана на принципе системы IRAC, действующей на момент подачи заявки на заявки на патент.
Примерами эктопаразитицидов и/или эндопаразитицидов являются инсектициды, акарициды и нематоциды, и они включают, в частности:
(1) Ингибиторы ацетилхолинэстеразы (AChE), например карбаматы, например, аланикарб, альдикарб, Бендиокарб, Бенфуракарб, Бутокарбоксим, Бутоксикарбоксим, Карбарил, Карбофуран, Карбосульфан, Этиофенкарб, Фенобукарб, Форметанат, Фуратиокарб, изопрокарб, Метиокарб, Метомил, Метолкарб, Оксамил, пиримикарб, пропоксур, тиодикарб, тиофанокс, триазамат, триметакарб, ХМС, и Ксилилкарб; или фосфорорганические соединения, например, ацефат, азаметифос, азинфос-этил, азинфос-метил, Кадузафос, хлорэтоксифос, хлорфенвинфос, хлормефос, хлорпирифос, хлорпирифос-метил, Кумафос, цианофос, деметон-S-метил, диазинон, дихлорвос/DDVP, дикротофос, диметоат, диметилвинфос, дисульфотон, EPN, Этион, Этопрофос, Фамфур, Фенамифос, Фенитротион, Фентион, Фостиазат, гептенофос, Имициафос, изофенфос, изопропил-О-(метоксиаминотио-фосфорил) салицилат, изоксатион, Малатион, Мекарбам, Метамидофос, Метидатион, Мевинфос, Монокротофосфос, Налед, Ометоат, Оксидеметон-метил, Паратион, Паратион-метил, Фентоат, Форат, Фосалон, Фосмет, Фосфамидон, Фоксим, пиримифос-метил, профенофос, пропетамфос, протиофос, пираклофос, пиридафентион, Хиналфос, Сульфотеп, Тебупиримфос, Темефос, Тербуфос, тетрахлорвинфос, тиометон, триазофос, трихлорфон и Вамидотион.
(2) Антагонисты GABA-зависимого хлоридного канала, например циклодиеновые хлорорганические соединения, например, хлордан и Эндосульфан; или фенилпиразолы (фипролы), например, Этипрол и Фипронил.
(3) Модуляторы натриевого канала/Блокаторы потенциал-зависимого натриевого канала, например пиретроиды, например, акринатрин, аллетрин, d-цис-транс Аллетрин, d-транс-аллетрин, Бифентрин, Биоаллетрин, Биоаллетрина S-циклопентенил-изомер, Биоресметрин, циклопротрин, цифлутрин, бета-цифлутрин, цигалотрин, лямбда-цигалотрин, гамма-цигалотрин, циперметрин, альфа-циперметрин, бета-циперметрин, тета-циперметрин, зета-циперметрин, цифенотрин [(1R)-транс-изомеры], дельтаметрин, Эмпентрин [(EZ)-(1R) изомеры), Эсфенвалерат, Этофенпрокс, Фенпропатрин, Фенвалерат, Флуцитринат, Флуметрин, тау-Флувалинат, галфенпрокс, Имипротрин, Кадетрин, Перметрин, Фенотрин [(1R)-транс-изомер), Праллетрин, пиретрин (пиретрум), Ресметрин, Силафлуофен, Тефлутрин, тетраметрин, тетраметрин [(1R) изомеры)], Тралометрин, и Трансфлутрин; или ДДТ; или метоксихлор.
(4) Агонисты никотинового ацетилхолинового рецептора (nAChR), например, неоникотиноиды, например, ацетамиприд, Клотианидин, динотефуран, Имидаклоприд, Нитенпирам, тиаклоприд, и Тиаметоксам; или Никотин; или Сульфоксахлор или флупирадифурон.
(5) Аллостерические модуляторы никотинового ацетилхолинового рецептора (nAChR), такие как например спиносины, например, Спинеторам и Спиносад.
(6) Аллостерические модуляторы глутамат-зависимого хлоридного канала (GluCl), например авермектины/мильбемицины, например, абамектин, Эмамектина бензоат, Лепимектин и Мильбемектин.
(7) Миметики ювенильного гормона, например, аналоги ювенильного гормона, например, гидропрен, Кинопрен и Метопрен; или Феноксикарб; или Пирипроксифен.
(9) Модуляторы органа слуха у насекомых, например, пиметрозин; или Флоникамид.
(10) Ингибиторы роста клещей, например, Клофентезин, гекситиазокс, и Дифловидазин; или Этоксазол.
(12) ингибиторы митохондриального АТФ-синтеза, такие как АТФ-дезинтеграторы, такие как, например; диафентиурон или оловоорганические митициды, например, азоциклотин, цигексатин, и Фенбутатина оксид; или Пропаргит; или тетрадифон.
(13) Средства, разобщающие окислительное фосфорилирование посредством разрушения протонового градиента, например, хлорфенапир, DNOC и Сульфлурамид.
(14) Блокаторы никотинергического ацетилхолинового рецептора, такие как, например, Бенсультап, Картапа гидрохлорид, тиоциклам и Тиосультап-натрий.
(15) Ингибиторы биосинтеза хитина, типа 0, например Бистрифлурон, Хлофлуазурон, дифлубензурон, Флуциклоксурон, Флуфеноксурон, гексафлумурон, Луфенурон, Новалурон, Новифлумурон, Тефлубензурон и Трифлумурон.
(16) Ингибиторы биосинтеза хитина, типа 1, например Бупрофезин.
(17) Ингибиторы линьки (в частности для Двукрылых, т.е. мух), такие как, например, циромазин.
(18) Агонисты рецептора экдизона, например Хромафенозид, галофенозид, метоксифенозид и Тебуфенозид.
(19) Октопаминергические агонисты, такие как, например, амитраз.
(20) Ингибиторы транспорта электронов митохондриального комплекса III, например Гидраметилнон; или Ацехиноцил; или Флуакрипирим.
(21) Ингибиторы транспорта электронов митохондриального комплекса I, например, из группы METI акарицидов, например, Феназахин, Фенпироксимат, пиримидифен, пиридабен, Тебуфенпирад и Толфенпирад; или Ротенон (Деррис).
(22) Блокаторы потенциалзависимого натриевого канала, например, Индоксакарб; или Метафлумизон.
(23) Ингибиторы ацетил-КоА-карбоксилазы, например, производные тетроновой и тетраминовой кислоты, например, Спиродиклофен, Спиромезифен и Спиротетрамат.
(25) Ингибиторы транспорта электронов митохондриального комплекса II, например, бета-кетонитрильная производная, например, циенопирафен и Цифлуметофен, и Карбоксанилид, как например, Пифлубумид.
(28) Модуляторы рианодинового рецептора, такие как, например, диамиды, например, хлорантранилипрол, циантранилипол и флубендиамид,
Другие активные ингредиенты с неизвестным или недоказанным механизмом действие, такие как, например, афидопиропен, афоксоланер, азадирахтин, бенклотиаз, бензоксимат, бифеназат, бромфланилид, бромпропилат, хинометионат, криолит, цикланилипрол, циклоксаприд, цигалодиамид, диклоромезотиаз, дикофол, дифловидазин, флометоквин, флуазаиндолизин, флуенсульфон, флуфенерим, флуфеноксистробин, флуфипрол, флугексафон, флуопирам, флураланер, флуксаметамид, фуфенозид, гуадипир, гептафлутрин, имидаклотиз, ипродион, лотиланер, меперфлутрин, паичонгдинг, пифлубумид, пиридалил, пирифлуквиназон, пириминостробин, сароланер, тетраметилфлутрин, тетранилипрол, тетрахлорантранилипрол, тиоксазафен, трифлумезопирим и иодметан; кроме того, препараты на основе Bacillus firmus (1-1582, BioNeem, Votivo), а также следующие активные соединения: 1-{2-фтор-4-метил-5-[(2,2,2-трифторэтил)сульфинил]фенил}-3-(трифторметил)-1Н-1,2,4-триазол-5-амин (известный из WO 2006/043635) (CAS 885026-50-6), {1'-[(2Е)-3-(4-хлорфенил)проп-2-ен-1-ил]-5-фторспиро[индол-3,4'-пиперидин]-1(2Н)-ил}(2-хлорпиридин-4-ил)метанон (известный из WO 2003/106457) (CAS 637360-23-7), 2-хлор-N-[2-{1-[(2Е)-3-(4-хлорфенил)проп-2-ен-1-ил]пиперидин-4-ил}-4-(трифторметил)фенил]изоникотинамид (известный из WO 2006/003494) (CAS 872999-66-1), 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-метокси-1,8-диазаспиро[4.5]дец-3-ен-2-он (известный из WO 2010052161) (CAS 1225292-17-0), 3-(4-хлор-2,6-диметилфенил)-8-метокси-2-оксо-1,8-диазаспиро[4.5]дец-3-ен-4-ил-этилкарбонат (известный из ЕР 2647626) (CAS-1440516-42-6), 4-(бут-2-ин-1-илокси)-6-(3,5-диметилпиперидин-1-ил)-5-фторпиримидин (известный из WO2004/099160) (CAS 792914-58-0), PF1364 (известный из JP 2010/018586) (CAS-Reg.No. 1204776-60-2), N-[(2Е)-1-[(6-хлорпиридин-3-ил)метил]пиридин-2(1Н)-илиден]-2,2,2-трифторацетамид (известный из WO 2012/029672) (CAS 1363400-41-2), (3Е)-3-[1-[(6-хлор-3-пиридил)метил]-2-пиридилиден]-1,1,1-трифторпропан-2-он (известный из WO 2013/144213) (CAS 1461743-15-6), N-[3-(бензилкарбамоил)-4-хлорфенил]-1-метил-3-(пентафторэтил)-4-(трифторметил)-1Н-пиразол-5-карбоксамид (известный из WO 2010/051926) (CAS 1226889-14-0), 5-бром-4-хлор-N-[4-хлор-2-метил-6-(метилкарбамоил)фенил]-2-(3-хлор-2-пиридил)пиразол-3-карбоксамид (известный из CN103232431) (CAS 1449220-44-3), 4-[5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(цис-1-оксидо-3-тиетанил)бензамид, 4-[5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(транс-1-оксидо-3-тиетанил)бензамид и 4-[(5S)-5-(3,5-дихлорфенил)-4,5-дигидро-5-(трифторметил)-3-изоксазолил]-2-метил-N-(цис-1-оксидо-3-тиетанил)бензамид (известный из WO 2013/050317 А1) (CAS 1332628-83-7), N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид, (+)-N-[3-хлор-1-(3-пиридинил)-1H-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид и (-)-N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)сульфинил]пропанамид (известный из WO 2013/162715 А2, WO 2013/162716 А2, US 2014/0213448 A1) (CAS 1477923-37-7), 5-[[(2Е)-3-хлор-2-пропен-1-ил]амино]-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[(трифторметил)сульфинил]-1Н-пиразол-3-карбонитрил (известный из CN 101337937 A) (CAS 1105672-77-2), 3-бром-N-[4-хлор-2-метил-6-[(метиламино)тиохометил]фенил]-1-(3-хлор-2-пиридинил)-1Н-пиразол-5-карбоксамид, (Liudaibenjiaxuanan, известный из CN 103109816 A) (CAS 1232543-85-9); N-[4-хлор-2-[[(1,1-диметилэтил)амино]карбонил]-6-метилфенил]-1-(3-хлор-2-пиридинил)-3-(фторметокси)-1Н-пиразол-5-карбоксамид (известный из WO 2012/034403 A1) (CAS 1268277-22-0), N-[2-(5-амино-1,3,4-тиадиазол-2-ил)-4-хлор-6-метилфенил]-3-бром-1-(3-хлор-2-пиридинил)-1Н-пиразол-5-карбоксамид (известный из WO 2011/085575 A1) (CAS 1233882-22-8), 4-[3-[2,6-дихлор-4-[(3,3-дихлор-2-пропен-1-ил)окси]фенокси]пропокси]-2-метокси-6-(трифторметил)пиримидин (известный из CN 101337940 A) (CAS 1108184-52-6); (2Е)- и 2(Z)-2-[2-(4-цианофенил)-1-[3-(трифторметил)фенил]этилиден]-N-[4-(дифторметокси)фенил]гидразинкарбоксамид (известный из CN 101715774 А) (CAS 1232543-85-9); циклопропанкарбоновая кислота-3-(2,2-дихлорэтенил)-2,2-диметил-4-(1Н-бензимидазол-2-ил)фениловый сложный эфир (известный из CN 103524422 A) (CAS 1542271-46-4); (4aS)-7-хлор-2,5-дигидро-2-[[(метоксикарбонил)[4-[(трифторметил)тио]фенил]амино]карбонил]индено[1,2-е][1,3,4]оксадиазин-4а(3Н)-карбоновая кислота метиловый сложный эфир (известный из CN 102391261 A) (CAS 1370358-69-2); 6-дезокси-3-O-этил-2,4-ди-О-метил-1-[N-[4-[1-[4-(1,1,2,2,2-пентафторэтокси)фенил]-1Н-1,2,4-триазол-3-ил]фенил]карбамат]-α-L-маннопираноза (известный из US 2014/0275503 A1) (CAS 1181213-14-8); 8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло[3.2.1]октан (CAS 1253850-56-4), (8-anti)-8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло[3.2.1]октан (CAS 933798-27-7), (8-syn)-8-(2-циклопропилметокси-4-трифторметилфенокси)-3-(6-трифторметилпиридазин-3-ил)-3-азабицикло[3.2.1]октан (известный из WO 2007040280 A1, WO 2007040282 A1) (CAS 934001-66-8) и N-[3-хлор-1-(3-пиридинил)-1Н-пиразол-4-ил]-N-этил-3-[(3,3,3-трифторпропил)тио]-пропанамид (известный из WO 2015/058021 A1, WO 2015/058028 A1) (CAS 1477919-27-9) и N-[4-(аминотиоксометил)-2-метил-6-[(метиламино)карбонил]фенил]-3-бром-1-(3-хлор-2-пиридинил)-1H-пиразол-5-карбоксамид (известный из CN 103265527 А) (CAS 1452877-50-7), 5-(1,3-диоксан-2-ил)-4-[[4-(трифторметил)фенил]метокси]-пиримидин (известный из WO 2013/115391 A1) (CAS 1449021-97-9), 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-метокси-1-метил-1,8-диазаспиро[4.5]дец-3-ен-2-он (известный из WO 2010/066780 A1, WO 2011/151146 A1) (CAS 1229023-34-0), 3-(4-хлор-2,6-диметилфенил)-8-метокси-1-метил-1,8-диазаспиро[4.5]декан-2,4-дион (известный из WO 2014/187846 A1) (CAS 1638765-58-8), 3-(4-хлор-2,6-диметилфенил)-8-метокси-1-метил-2-оксо-1,8-диазаспиро[4.5]дец-3-ен-4-ил-карбоновой кислоты сложный этиловый эфир (известный из WO 2010/066780 А1, WO 2011151146 A1) (CAS 1229023-00-0), N-[1-[(6-хлор-3-пиридинил)метил]-2(1H)-пиридинилиден]-2,2,2-трифтор-ацетамид (известный из DE 3639877 А1, WO 2012029672 A1) (CAS 1363400-41-2), [N(E)]-N-[1-[(6-хлор-3-пиридинил)метил]-2(1Н)-пиридинилиден]-2,2,2-трифтор-ацетамид, (известный из WO 2016005276 A1) (CAS 1689566-03-7), [N(Z)]-N-[1-[(6-хлор-3-пиридинил)метил]-2(1Н)-пиридинилиден]-2,2,2-трифтор-ацетамид, (CAS 1702305-40-5), 3-эндо3-[2-пропокси-4-(трифторметил)фенокси]-9-[[5-(трифторметил)-2-пиридинил]окси]-9-азабицикло[3.3.1]нонан (известный из WO 2011/105506 A1, WO 2016/133011 А1) (CAS 1332838-17-1).
Активные ингредиенты с неизвестными или неспецифическими механизмами действия, например, фентрифанил, феноксакрим, циклопрен, хлорбензилат, хлордимеформ, флубензимин, дицикланил, амидофлумет, хинометионат, триаратен, клотиазобен, тетразул, олеат калия, керосин, метоксадиазон, госсиплур, флутензин, бромпропилат, криолит;
Активные ингредиенты из других классов, например, бутакарб, диметилан, клоэтокарб, фосфокарб, пиримифос(-этил), паратион(-этил), метакрифос, изопропил-о-салицилат, трихлорфон, сулпрофос, пропафос, себуфос, пиридатион, Протоат, дихлофентион, деметон-S-метилсульфон, изазофос, цианофенфос, диалифос, карбофенотион, аутатиофос, аромфенвинфос(-метил), азинфос(-этил), хлорпирифос(-этил), фосметилан, иодфенфос, диоксабензофос, формотион, фонофос, флупиразофос, фенсульфотион, этримфос;
Хлорорганические соединения, например, камфехлор, линдан, гептахлор; или фенилпиразолы, например, ацетопрол, пирафлупрол, пирипрол, ванилипрол, сизапронил; или изоксазолин, например, сароланер, афоксоланер, лотиланер, флураланер;
Пиретроиды, например, (цис-, транс-)метофлутрин, профлутрин, флуфенпрокс, флуброцитринат, флубфенпрокс, фенфлутрин, протрифенбут, пирезметрин, RU 15525, тераллетрин, цис-ресметрин, гептафлутрин, биоэтанометрин, биоперметрин, фенпиритрин, цис-циперметрин, цис-перметрин, клоцитрин, цигалотрин (лямбда), хловапортрин, или галогенированные углеводородные соединения (НСН);
неоникотиноиды, например, нитиазин;
дихлормезотиаз, трифлумезопирим;
макроциклические лактоны, например, немадектин, ивермектин, латидектин, моксидектин, селамектин, эприномектин, дорамектин, эмамектинбензоат; милбемициноксим;
Трифен, Эпофенонан, диофенолан;
Биологические вещества, гормоны, феромоны, например, природные продукты, например, турингиенсин, кодлемон или ним-компоненты Codlemon или Neem;
динитрофенолы, например, динокап, динобутон, бинапакрил;
бензоилмочевины, например, флуазурон, пенфлурон,
Амидиновые производные, например, Хлормебуформ, симиазол, демидитраз;
Акарициды для защиты пчел от клещей Варроа, например, органические кислоты, например, муравьиная кислота, щавелевая кислота.
Неограничивающие примеры инсектицидов и акарицидов, представляющих особый интерес для использования для здоровья животных, представляют собой и включают в частности [т.е. Mehlhorn et al Encyclpaedic Reference of Parasitology 4th edition (ISBN 978-3-662-43978-4)]:
Эффекторы на управляемые лигандами хлоридные каналы членистоногих: хлордан, гептахлор, эндокулфан. Диэльдрин, бромциклен, токсафен, линдан, фипронил, пирипрол, сисапронил, афоксоланер, флураланер, сароланер, лотиланер, флюксаметамид, бромфланилид, авермектин, дорамектин, эприномектин, ивермектин, милбемицин, моксидектин, селамектин;
Модуляторы октопаминовых рецепторов членистоногих: амитраз, BTS27271, цимиазол, демидитраз;
Эффекторы натриевых каналов членистоногих, зависящих от напряжения: DDT, метоксихлор, метафлумизон, индоксакарб, цинерин I, цинерин II, джасмолин I, джасмолин II, пиретрин I, пиретрин II, аллетрин, альфациперметрин, биоаллетрин, бетацисфлутрин, цифлутрин, цигалотрин, циперметрин, дельтаметрин, этофенпрокс, фенвалерат, флуцитринат, флуметрин, гальфенпрокс, перметрин, фенотрин, ресметрин, тау-флувалинат, тетраметрин;
Эффекторы никотиновых холинергических синапсов членистоногих (ацетилхолиновая эстераза, ацетилхолиновые рецепторы): бромприпилат, бендиокарб, карбарил, метомил, промацил, пропоксур, азаметифос, хлорфенвинфос, хлорпирифос, кумафос, цитиоат, диазинон, диклорвос, дикротофос, диметоат, этнон, фамфур, фенитротион, фентион, гептенофос, малатион, налед, фосмет, фоксим, фталофос, пропетамфос, темефос, тетрахлорвинфос, трихлорфон, имидаклоприд, нитенпирам, динотефуран, спиносад, спинеторам;
Эффекторы процессов развития членистоногих: циромазин, дицикланил, дифлубензурон, флюазурон, люфенурон, трифлюмурон, феноксикарб, гидропрен, метопрен, пирипроксифен, феноксикарб, гидропрен, S-метопрен, пирипроксифен.
Примерные активные ингредиенты из группы эндопаразитицидов в качестве дополнительного или другого активного ингредиента согласно настоящему изобретению включают, без ограничения, антигельминтно активные соединения и антипротозойно активные соединения.
Антигельминтные агенты включают, например, следующие активные вещества против нематод, трематод и/или цестод:
из класса макроциклических лактонов, например: эприномектин, абамектин, немадектин, моксидектин, дорамектин, селамектин, лепимектин, латидектин, милбемектин, эмамектин, милбемицин;
из класса бензимидазолов и пробензимидазолов, например: оксибендазол, мебендазол, триклабендазол, тиофанат, парбендазол, оксфендазол, нетобимин, фенбендазол, фебантел, тиабендазол, циклобендазол, камбендазол, альбендазолсульфоксид, альбендазол, флубендазол;
из класса депсипетидов, предпочтительно циклических депсипетидов, особенно 24-членных циклических депсипетидов, например: эмодепсид, PF1022A;
из класса тетрагидропиримидинов, например: морантел, пирантел, оксантел;
из класса имидазотиазолов, например: бутамизол, левамизол, тетрамизол;
из класса аминофениламидинов, например: амидантел, диацилированный амидантел (dAMD), трибендимидин;
из класса аминоацетонитрилов, например: монепантел;
из класса парагерквиамидов, например: парагерквиамид, дерквиантел;
из класса салициланилидов, например: трибромсалан, бромксанид, бротианид, клиоксанид, клосантел, никлосамид, оксиклозанид, рафоксанид;
из класса замещенных фенолов, например: нитроксинил, битионол, дикофенол, гексахлорфен, никлофолан, мениклофолан;
из класса органофосфатов, например: трихлорфон, нафталофос, дихлорвос/DDVP, круфомат, коумафос, галоксон;
из класса пиперазинов/хинолинов, например: празиквантел, эпсипрантел; из класса пиперазинов, например: пиперазин, гидроксизин;
из класса тетрациклинов, например: тетрациклин, хлортетрациклин, доксициклин, окситетрациклин, ролитетрациклин;
из различных других классов, например: бунамидин, ниридазол, резорантел, омфалотин, олтипраз, нитросканат, нитроксинил, оксамниквин, миразан, Мирацил, лукантон, гикантон, гетолин, эметин, диэтилкарбамазин, дихлорфен, диамфенетид, клоназепам, бефениум, амосканат, клорсулон;
Активными ингредиентами против простейших согласно настоящему изобретению являются, без ограничения к этому, следующие активные ингредиенты:
из класса триазинов, например: диклазурил, поназурил, летразурил, толтразурил;
из класса полиэфирных ионофоров, например: монензин, салиномицин, мадурамицин, наразин;
из класса макроциклических лактонов, например: милбемицин, эритромицин;
из класса хинолонов, например: энрофлоксацин, прадофлоксацина;
из класса хинолонов, например: энрофлоксацин, прадофлоксацина;
из класса хининов, например: хлороквин;
из класса пиримидинов, например: пириметамин;
из класса сульфонамидов, например: сульфахиноксалин, триметоприм, сульфаклозин;
из класса тиаминов, например: ампролиум;
из класса линкозамидов, например: клиндамицин;
из класса карбанилидов, например: имидокарб;
из класса нитрофуранов, например: нифуртимокс;
из класса алкалоиды хиназолинона, например: галофугинон;
из других классов, например: оксамниквин, паромомицин,
из класса вакцины или антигены микроорганизмов, например: Babesia canis rossi, Eimeria tenella, Eimeria praecox, Eimeria necatrix, Eimeria mitis, Eimeria maxima, Eimeria brunetti, Eimeria acervulina, Babesia canis vogeli, Leishmania infantum, Babesia canis canis, Dictyocaulus viviparus.
Все вышеупомянутые смесительные партнеры могут, если они способны на основании их функциональных групп, необязательно образовывать соли с подходящими основаниями или кислотами.
Основываясь на стандартных лабораторных методах, известных для оценки соединений, полезных для лечения гельминтоза, стандартными испытаниями токсичности и стандартными фармакологическими анализами для определения лечения состояний, указанных выше у животных, и путем сопоставления этих результатов с результатами для известных активных ингредиентов или медикаментов, которые используются для лечения этих состояний, эффективная доза соединений согласно настоящему описанию может быть легко определена для лечения каждого желаемого показания. Количество активного ингредиента, которое должно вводиться при лечении одного из этих состояний, может широко варьироваться в соответствии с такими условиями, как конкретное соединение и применяемая дозированная единица, способ введения, период лечения, возраст и пол подлежащего лечению субъекта, и характер и степень подлежащего лечению состояния.
Общее количество вводимого активного ингредиента обычно будет составлять от около 0,001 мг/кг до около 200 мг/кг массы тела в день и предпочтительно от около 0,01 мг/кг до около 20 мг/кг массы тела в день. Клинически полезные режимы дозирования будут варьироваться от одного до трех раз в день до дозирования один раз в четыре недели. Кроме того, возможен «отдых от лекарственного средства», при котором субъект не получает дозу лекарственного средства в течение определенного периода времени, который является полезным для общего баланса между фармакологическим эффектом и переносимостью. Кроме того, можно проводить лечение длительного действия, когда субъект получает лечение один раз в течение более четырех недель. Единица дозирования может содержать от около 0,5 мг до около 1500 мг активного ингредиента и может вводиться один или более раз в день или менее одного раза в день. Средняя суточная доза для введения путем инъекции, включая внутривенные, внутримышечные, подкожные и парентеральные инъекции, и использования инфузионных методов будет предпочтительно составлять от 0,01 до 200 мг/кг общей массы тела. Средний дневной режим ректального введения дозы будет предпочтительно составлять от 0,01 до 200 мг/кг общей массы тела. Средний дневной режим вагинального введения дозы предпочтительно будет составлять от 0,01 до 200 мг/кг общей массы тела. Средний ежедневный режим местного дозирования предпочтительно будет составлять от 0,1 до 200 мг, вводимых от 1 до 4 раза в день. Трансдермальная концентрация будет предпочтительно такой, которая необходима для поддержания суточной дозы от 0,01 до 200 мг/кг. Средний ежедневной режим дозирования ингаляцией будет предпочтительно составлять от 0,01 до 100 мг/кг общей массы тела.
Конечно, конкретный начальный и продолжающийся режим дозирования для каждого субъекта будет варьироваться в зависимости от характера и тяжести состояния, определяемого лечащим диагностом, активности конкретного используемого соединения, возраста и общего состояния субъекта, времени введения, пути введения, скорости экскреции лекарственного средства, комбинации лекарственных средств и тому подобного. Желаемый способ лечения и количество доз соединения согласно настоящему изобретению или его фармацевтически приемлемой соли или сложного эфира или композиции может быть установлен специалистами в данной области с использованием обычных тестов на лечение.
Экспериментальная часть
Различные аспекты изобретения, описанные в настоящей заявке, проиллюстрированы следующими примерами, которые не предназначены для ограничения настоящего изобретения каким-либо образом.
Эксперименты по тестированию примеров, описанные в настоящей заявке, служат для иллюстрации настоящего изобретения, и настоящее изобретение не ограничивается приведенными примерами.
Экспериментальная часть
Аббревиатуры:

Различные аспекты изобретения, описанные в настоящей заявке, проиллюстрированы следующими примерами, которые не предназначены для ограничения настоящего изобретения каким-либо образом.
Эксперименты по тестированию примеров, описанные в настоящей заявке, служат для иллюстрации настоящего изобретения, и настоящее изобретение не ограничивается приведенными примерами.
Экспериментальная часть - общая часть
Все реагенты, для которых синтез не описан в экспериментальной части, являются либо коммерчески доступными, либо известными соединениями, либо могут быть получены из известных соединений известными способами специалистом в данной области.
Соединения и промежуточные соединения, полученные согласно способам согласно настоящему изобретению, могут потребовать очистки. Очистка органических соединений хорошо известна специалисту в данной области, и может быть несколько способов очистки одного и того же соединения. В некоторых случаях очистка не требуется. В некоторых случаях соединения могут быть очищены путем кристаллизации. В некоторых случаях примеси могут быть исключены с использованием подходящего растворителя. В некоторых случаях соединения могут быть очищены с помощью хроматографии, в частности колоночной флэш-хроматографии, с использованием, например, предварительно заполненных силикагелем картриджей, например, Biotage SNAP картриджи KP-Sil® или KP-NH®, в комбинации со системой Biotage autopurifier (SP4® или Isolera Four®) и элюентами, такими как градиенты гексан/этилацетат или дихлорметан/метанол. В некоторых случаях соединения могут быть очищены препаративной ВЭЖХ с использованием, например, автоочистителя Waters, оснащенного детектором на диодной матрице и/или масс-спектрометром с ионизацией распылением в реальном времени, в сочетании с подходящей предварительно набитой обращеннофазовой колонкой и элюентами, такими как градиент воды и ацетонитрила, который может содержать добавки, такие как трифторуксусная кислота, муравьиная кислота или водный аммиак.
В некоторых случаях способы очистки, как описано выше, могут обеспечить те соединения согласно настоящему изобретению, которые обладают достаточно щелочной или кислотной функциональностью в форме соли, как например, в случае соединения согласно настоящему изобретению, которое является достаточно основным, трифторацетат или формиатную соль, например, или, в случае соединения согласно настоящему изобретению, которое является достаточно кислотным, например, аммониевая соль. Соль этого типа может быть либо превращена в ее свободное основание, либо в свободную кислотную форму, соответственно, различными способами, известными специалисту в данной области, или ее можно использовать в качестве солей в последующих биологических анализах. Следует понимать, что конкретная форма (например, соль, свободное основание и т.д.) соединения согласно настоящему изобретению, как выделено и как описано в настоящей заявке, не необязательно находятся в единственной форме, в которой указанное соединение может быть применено в биологическом анализе для количественной оценки конкретной биологической активности.
Аналитические и хроматографические способы
Аналитическая и препаративная жидкостная хроматография
Аналитическую (UP) LC-MS проводили с помощью различного оборудования, как описано ниже. Массы (m/z) приводятся на основе ионизации электрораспылением из ионизации с электрораспылением положительно заряженных ионов, если не указан отрицательный режим (ESI-).
Способ L0:
Измерение значений logP проводилось согласно директиве EEC 79/831 Приложение V.A8 посредством ВЭЖХ (высокоэффективная жидкостная хроматография) на колонках с обращенной фазой следующими способами:
[a] logP значение определяют посредством измерения LC-UV, в кислотном диапазоне, с 0.1% муравьиной кислотой в воде и ацетонитриле в качестве элюента (линейный градиент от 10% ацетонитрила до 95% ацетонитрила).
[b] logP значение определяют посредством измерения LC-UV, в нейтральном диапазоне, с 0.001 молярным раствором аммония ацетата в воде и ацетонитриле в качестве элюента (линейный градиент от 10% ацетонитрила до 95% ацетонитрила).
Калибровка проводилась с использованием алкан-2-онов с прямой цепью (от 3 до 16 атомов углерода) с известными значениями logP (измерение значений logP с использованием времен удерживания с линейной интерполяцией между последовательными алканонами). Максимальные значения лямбда определялись с использованием УФ-спектров от 200 нм до 400 нм и пиковых значений хроматографических сигналов.
М+1 (или М+Н) означает пик молекулярного иона, плюс или минус 1 a.m.u. (атомная единица массы) соответственно, как наблюдалось при масс-спектрометрии посредством ионизации электрораспылением (ESI + или -).
Способ L1:
Тип устройства: Waters ACQUITY SQD UPLC system; колонка: Waters Acquity UPLC HSS T3 1.8 мкм 50×1 мм; элюент А: 1 л воды + 0.25 мл муравьиной кислоты, элюент В: 1 л ацетонитрила + 0.25 мл муравьиной кислоты; градиент: 0.0 мин 90% А → 1.2 мин 5% А → 2.0 мин 5% А печь: 50°С; поток: 0.40 мл/мин; УФ-обнаружение: 208-400 нм.
Способ L2:
Тип устройства MS: Agilent Technologies 6130 Quadrupole LC-MS; Тип устройства ВЭЖХ: Agilent Technologies 1260 Infinity; колонка: Waters XSelect (C18, 50×2.1 мм, 3.5 мкм); поток: 0.8 мл/мин; температура колонки: 35°С; элюент А: 0.1% муравьиной кислоты в ацетонитриле; элюент В: 0.1% муравьиной кислоты в воде; линейный градиент: t=0 мин 5% А, t=3.5 мин 98% A, t=6 мин 98% А; обнаружение: DAD (220-320 нм); обнаружение: MSD (ESI пол/отр) массовый диапазон: 100-800; обнаружение: ELSD (PL-ELS 2100): поток газа 1.2 мл/мин, температура газа: 70°С, зонд: 50°С.
Способ L3:
Тип устройства MS: Agilent Technologies LC/MSD SL; Тип устройства ВЭЖХ: Agilent Technologies 1100 Series; колонка: Waters XSelect (C18, 50×2.1 мм, 3.5 мкм; поток: 0.8 мл/мин; температура колонки: 25°С; элюент А: 95% ацетонитрила + 5% 10 мм аммония бикарбоната в воде; элюент В: 10 мм аммония бикарбоната в воде рН-9.0; линейный градиент: t=0 мин 5% A, t=3.5 мин 98% А, t=6 мин 98% А; обнаружение: DAD (220-320 нм); обнаружение: MSD (ESI пол/отр) массовый диапазон: 100-800.
Способ L4:
Тип устройства: Waters ACQUITY SQD UPLC System; колонка: Waters Acquity UPLC HSS T3 1.8 мкм 50×1 мм; элюент А: 1 л воды + 0.25 мл 99%-ой муравьиной кислоты, Элюент В: 1 л ацетонитрила + 0.25 мл 99%-ой муравьиной кислоты; градиент: 0.0 мин 95% А→6.0 мин 5% А→7.5 мин 5% А печь: 50°С; поток: 0.35 мл/мин; УФ-обнаружение: 210-400 нм.
Способ L5:
Тип устройства MS: Waters SQD; Устройство ВЭЖХ: Waters UPLC; колонка: Zorbax SB-Aq (Agilent), 50 мм × 2.1 мм, 1.8 мкм; элюент А: вода + 0.025% муравьиной кислоты, элюент В: ацетонитрила (ULC) + 0.025% муравьиной кислоты; градиент: 0.0 мин 98%А - 0.9 мин 25%А - 1.0 мин 5%А - 1.4 мин 5%А - 1.41 мин 98%А - 1.5 мин 98%А; печь: 40°С; поток: 0.600 мл/мин; УФ-обнаружение: DAD; 210 нм.
Способ L6:
Тип устройства MS: Thermo Scientific FT-MS; Тип устройства ВЭЖХ: Thermo Scientific UltiMate 3000; колонка: Waters, HSST3, 2.1×75 мм, С18 1.8 мкм; элюент А: 1 л воды + 0.01% муравьиной кислоты; элюент В: 1 л ацетонитрила + 0.01% муравьиной кислоты; Градиент: 0.0 мин 10% В→2.5 мин 95% В→3.5 мин 95% В; печь: 50°С; Поток: 0.90 мл/мин; УФ-обнаружение: 210 нм / оптимальный путь интегрирования 210-300 нм:
Способ L7:
Тип устройства MS: Waters (Micromass) Quattro Micro; Тип устройства ВЭЖХ: Waters UPLC Acquity; колонка: Waters ВЕН С18 1.7 мкм 50×2.1 мм; элюент А: 1 л воды + 0.01 моль аммония формиата, элюент В: 1 л ацетонитрила; градиент: 0.0 мин 95% А→0.1 мин 95% А→2.0 мин 15% А→2.5 мин 15% А→2.51 мин 10% А→3.0 мин 10% А; печь: 40°С; поток: 0.5 мл/мин; УФ-обнаружение: 210 нм.
Способ L8:
Тип устройства MS: Waters SQD2; Устройство ВЭЖХ: Waters UPLC; колонка: Zorbax SB-Aq (Agilent), 50 мм × 2.1 мм, 1.8 мкм; элюент А: вода + 0.025% муравьиной кислоты, элюент В: ацетонитрила (ULC) + 0.025% муравьиной кислоты; градиент: 0.0 мин 98%А - 0.9 мин 25%А - 1.0 мин 5%А - 1.4 мин 5%А - 1.41 мин 98%А - 1.5 мин 98%А; печь: 40°С; поток: 0.600 мл/мин; УФ-обнаружение: DAD; 210 нм.
Способ L9:
Тип устройства MS: Agilent Technologies LC/MSD SL; Тип устройства ВЭЖХ: Agilent Technologies 1100 Series; колонка: Waters XSelect (C18, 50×2.1 мм, 3.5 мкм; поток: 0.8 мл/мин; температура колонки: 25°С; элюент А: 95% ацетонитрила + 5% аммония бикарбоната в воде; элюент В: 10 мМ аммония бикарбоната в воде рН=9.0; линейный градиент: t=0 мин 5% А, t=3.5 мин 98% A, t=6 мин 98% А; обнаружение: DAD (220-320 нм); обнаружение: MSD (ESI пол/отр) массовый диапазон: 100-800.
Способ L10:
Тип устройства MS: Agilent Technologies 6130 Quadrupole LC-MS; Тип устройства ВЭЖХ: Agilent Technologies 1260 Infinity; колонка: Waters XSelect (C18, 30×2.1 мм, 3.5 мкм); поток: 1 мл/мин; температура колонки: 35°С; элюент А: 0.1% муравьиной кислоты в ацетонитриле; элюент В: 0.1% муравьиной кислоты в воде; линейный градиент: t=0 мин 5% А, t=1.6 мин 98% A, t=3 мин 98% А; обнаружение: DAD (220-320 нм); обнаружение: MSD (ESI пол/отр) массовый диапазон: 100-800; обнаружение: ELSD (PL-ELS 2100): поток газа 1.2 мл/мин, температура газа: 70°С, зонд: 50°С.
Способ L11:
Тип устройства MS: Agilent Technologies LC/MSD SL; Тип устройства ВЭЖХ: Agilent Technologies 1100 Series; колонка: Phenomenex Gemini NX (C18, 50×2.0 mm), 3.0 мкм; поток: 0.8 мл/мин; температура колонки: 25°С; элюент А: 95% ацетонитрила + 5% 10 мМ аммония бикарбоната в воде в ацетонитриле рН=9.0; элюент В: 10 мм аммония бикарбоната в воде рН=9.0; линейный градиент: t=0 мин 5% А, t=3.5 мин 98% А, t=6 мин 98% А; обнаружение: DAD (220-320 нм); обнаружение: MSD (ESI пол/отр) массовый диапазон: 100-800.
Способ L12:
МА устройство: Agilent MS Quad 6150; ВЭЖХ устройство: Agilent 1290; колонка: Waters Acquity UPLC HSS T3 1.8 мкм 50×2.1 мм; элюент А: 1 л воды + 0.25 мл 99% муравьиной кислоты, Элюент В: 1 л ацетонитрила + 0.25 мл 99% муравьиной кислоты; градиент: 0.0 мин 90% А→0.3 мин 90% А→1.7 мин 5% А→3.0 мин 5% А печь: 50°С; поток: 1,20 мл/мин; УФ-обнаружение: 205-305 нм.
Способ M1:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 1.80 с общим временем работы 2.10 мин. Температура колонки была при 45°C с общей скоростью потока 1.20 мл/мин.
Способ М2:
Применяемой колонкой была EVO, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 4.20 с общим временем работы 4.50 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М3:
Применяемой колонкой была CORTECS C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М4:
Применяемой колонкой была CORTECS C18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 45°C с общей скоростью потока 1.00 мл/мин.
Способ М5:
Применяемой колонкой была Kinetex EVO С18, 2.6 мкм; 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М6:
Применяемой колонкой была CORTECS С18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 2.60 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М7:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 2.80 с общим временем работы 3.30 мин. Температура колонки была при 45°C с общей скоростью потока 1.20 мл/мин.
Способ М8:
Применяемой колонкой была CORTECS C18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М9:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 4.20 с общим временем работы 4.50 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М10:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М11:
Применяемой колонкой была CORTECS С18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М12:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М13:
Применяемой колонкой была Ascentis Express С 18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ M14:
Применяемой колонкой была Ascentis Express С 18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент; начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ M15:
Применяемой колонкой была Ascentis Express С 18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 70% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М16:
Применяемой колонкой была CORTECS C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ M17:
Применяемой колонкой была CORTECS C18+ 100А, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.60 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ M18:
Применяемой колонкой была Kinetex EVO С18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ M19:
Применяемой колонкой была Kinetex EVO C18 100А, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.60 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М20:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М21:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.09% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М22:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.09% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М23:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.09% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М24:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М25:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 4.6×50 мм. Применяли линейный градиент, начиная при 90% А (А: 5 мМ NH4HCO3 в воде) и заканчивая при 95% В (В: MeCN) за 1.75 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.80 мл/мин.
Способ М26:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 4.90 с общим временем работы 5.30 мин. Температура колонки была при 45°C с общей скоростью потока 1.50 мл/мин.
Способ М27:
Применяемой колонкой была Poroshell HPH-C18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М28:
Применяемой колонкой была CORTECS C18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 45°C с общей скоростью потока 1.00 мл/мин.
Способ М29:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 4.60 с общим временем работы 5.30 мин. Температура колонки была при 40°C с общей скоростью потока 1.20 мл/мин.
Способ М30:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 2.80 с общим временем работы 3.30 мин. Температура колонки была при 45°C с общей скоростью потока 1.20 мл/мин.
Способ М31:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 4.70 с общим временем работы 5.00 мин. Температура колонки была при 45°C с общей скоростью потока 1.20 мл/мин.
Способ М32:
Применяемой колонкой была CORTECS C18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 5.20 с общим временем работы 5.70 мин. Температура колонки была при 45°C с общей скоростью потока 1.00 мл/мин.
Способ М33:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 2.20 с общим временем работы 2.60 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М34:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.20 мл/мин.
Способ М35:
Применяемой колонкой была CORTECS C18+, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.09% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М36:
Применяемой колонкой была CORTECS C18+ 100А, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 0.1% FA в воде) и заканчивая при 100% В (В: 0.1% FA в MeCN) за 2.60 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М37:
Применяемой колонкой была CORTECS C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.09% FA в воде) и заканчивая при 95% В (В: 0.1% FA в MeCN) за 2.60 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М38:
Применяемой колонкой была CORTECS C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 1.80 с общим временем работы 2.00 мин. Температура колонки была при 45°C с общей скоростью потока 1.00 мл/мин.
Способ М39:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 70% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 5.70 с общим временем работы 6.50 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М40:
Применяемой колонкой была Ascentis Express C18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 60% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 2.70 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М41:
Применяемой колонкой была Kinetex EVO C18, 2.6 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 5 мм NH4HCO3 в воде) и заканчивая при 95% В (В: MeCN) за 1.80 с общим временем работы 2.00 мин. Температура колонки была при 45°C с общей скоростью потока 1.50 мл/мин.
Способ М42:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 1.70 с общим временем работы 2.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.20 мл/мин.
Способ М43:
Применяемой колонкой была Kinetex EVO C18 100А, 2.6 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 90% А (А: 5 мм NH4HCO3 в воде) и заканчивая при 95% В (В: MeCN) за 2.60 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М44:
Применяемой колонкой была НРН-С18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 90% А (А: 5 мм NH4HCO3 в воде) и заканчивая при 100% В (В: MeCN) за 2.60 с общим временем работы 3.00 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ 45:
Применяемой колонкой была Ascentis Express С18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 3.10 с общим временем работы 3.60 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М46:
Применяемой колонкой была Ascentis Express С 18, 2.7 мкм, 2.1×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 100% В (В: 0.05% TFA в MeCN) за 2.10 с общим временем работы 2.60 мин. Температура колонки была при 40°C с общей скоростью потока 1.00 мл/мин.
Способ М47:
Применяемой колонкой была Ascentis Express С18, 2.7 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 95% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 4.20 с общим временем работы 4.50 мин. Температура колонки была при 40°C с общей скоростью потока 1.50 мл/мин.
Способ М48:
Применяемой колонкой была Shim-pack XR-ODS, 2.2 мкм, 3.0×50 мм. Применяли линейный градиент, начиная при 80% А (А: 0.05% TFA в воде) и заканчивая при 95% В (В: 0.05% TFA в MeCN) за 5.00 с общим временем работы 5.60 мин. Температура колонки была при 45°C с общей скоростью потока 1.20 мл/мин.
1H-ЯМР данные
1H-ЯМР данные определили с помощью Bruker Avance 400 (оборудованного проточной ячейкой (объем 60 мкл), или с помощью Bruker AVIII 400, оборудованного 1.7 мм cryo CPTCI зондом, или с помощью Bruker AVIII 400 (400.13 МГц), оборудованного 5 мм зондом, или с помощью Bruker AVII 600 (600.13 МГц), оборудованного 5 мм cryo TCI зондом, или с помощью Bruker AVIII 600 (601.6 МГц), оборудованного 5 мм cryo CPMNP зондом, или с помощью Bruker AVIII 500 (500.13 МГц), оборудованного 5 мм широкополосным зондом или 5 мм Prodigy™ зондом, с тетраметилсиланом в качестве контроля (0.0) и растворителями CD3CN, CDCl3 или D6-ДМСО. Альтернативные 1H- и 13С-ЯМР типы устройств: Bruker DMX300 (1Н-ЯМР: 300 МГц; 13С ЯМР: 75 МГц), Bruker Avance III 400 (1Н-ЯМР: 400 МГц; 13С ЯМР: 100 МГц) или Bruker 400 Ultrashield (1Н-ЯМР: 400 МГц; 13С ЯМР: 100 МГц).
Химические сдвиги (δ) показаны в частях на миллион [ppm]; используются следующие аббревиатуры: s = синглет, d = дублет, t = триплет, q = квартет, m = мультиплет, br. = расширенный; константы связывания приводятся в Герцах [Гц].
Экспериментальная часть - общие методики
Синтез соединений формулы (I) может быть проведен согласно или аналогично следующим схемам (Схема 1а-е, Схема 2 и Схема 3).
Схема 1а
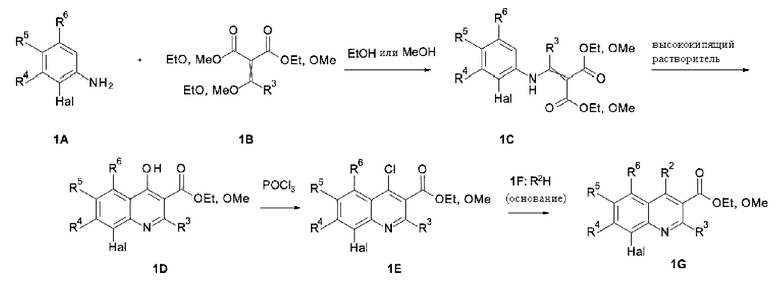
2-Галогена-замещенные анилины 1А (Hal = иод, бром, хлор) являются коммерчески доступными и могут быть легко превращены с помощью (алкоксиметилен)малонатов 1В, растворенных в соответствующем растворителе спирте, предпочтительно в условиях кипения, в (анилинометилен)малонаты 1C, как описано в Monatshefte fuer Chemie, 2015, 146(2), 291-302, или без какого-либо растворителя, как описано в WO 2002004444. Замыкание кольца осуществляли в высококипящих растворителях, предпочтительно в дифениловом простом эфире или ксилоле, с получением гидроксихинолинов 1D, как описано в WO 2013118071. Гидроксихинолины 1D могут быть легко преобразованы в соответствующие соединения хлора 1Е с реагентом хлорирования, предпочтительно с возвращаемым в виде флегмы POCl3, как описано в WO 2013118071.
В зависимости от природы нуклеофила R2H 1F, хинолины хлора 1Е реагируют с 1F в присутствии основания, например, этилата натрия, метилата натрия, калия трет-бутилата, триэтиламин N,N-диизопропил этиламина, диазабициклоундекана, гидрида натрия, гидроксида лития, гидроксида натрия, гидроксида калия, карбоната калия, карбоната цезия, или тому подобного, с получением сложноэфирных промежуточных соединений 1G.
Схема 1b
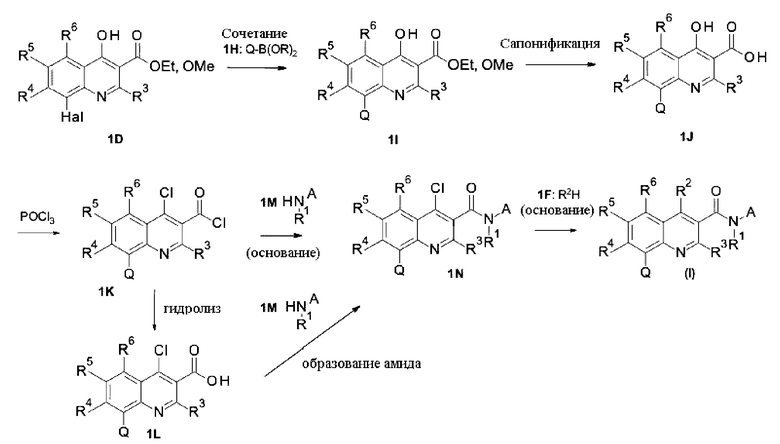
Альтернативно, реакция сочетания Сузуки промежуточных соединений 1D с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат). как описано в Chem. Soc. Rev. 2014, 43, 412-443 или в Tetrahedron 2002, 58 (48), 9633-969, до сложноэфирных промежуточных соединений 1I. Затем, сложноэфирные промежуточные соединения 1I могут быть легко омылены, например, с помощью гидроксида лития, приводя к соответствующим карбоновым кислотам 1J. которые могут быть легко превращены в соответствующие хлориды хлоркарбоновых кислот 1K с реагентом хлорирования, предпочтительно с возвращающимся в виде флегмы POCl3, как описано в WO 2013096151. Промежуточные соединения 1K реагируют в гидролитических условиях с получением хинолонкарбоновых кислот 1L, которые объединяют с коммерчески доступными аминами 1М через реагенты образования амида и дегидратации, например, N-(3-диметиламиноизопропил)-N'-этил-карбодиимид-гидрохлорид (EDC), с получением амидов 1N. Подобные синтезы описаны в Journal of Medicinal Chemistry 2012, 55. 3563-3567 например. Промежуточные соединения 1K могут непосредственно образовывать амиды 1N, так как хлориды карбоновых кислот 1K объединяются с аминами 1М при основных условиях, например, пиридин, триэтиламин или N,N-диизопропил этиламин, как описано в Chemical Biology & Drug Design 2015, 85(5), 549-564.
В зависимости от природы нуклеофила R2H 1F, хинолины хлора 1N реагируют с 1F в присутствии основания, например, этилата натрия, метилата натрия, калия трет-бутилата, триэтиламин N,N-диизопропил этиламина, диазабициклоундекана, гидрида натрия, гидроксида лития, гидроксида натрия, гидроксида калия, карбоната калия, карбоната цезия, или тому подобного, с получением целевых соединений формулы (I).
Схема 1c
Хинолины хлора 1Е могут быть легко омылены, например, с помощью гидроксида лития, приводя к соответствующим карбоксилатам 1O, полученным, например, в виде соли лития, или приводя к карбоновым кислотам 1P после кислотного гидролиза. Затем, промежуточные соединения карбоксамиды 1S получают посредством условий амидного связывания, например, через хлориды карбоновых кислот, образованные из 1P, которые объединяют с аминами 1М в основных условиях, например, пиридин, триэтиламин или N,N-диизопропил этиламин, или через образование амида из карбоновых кислот 1P, которые объединяют с аминами 1М и реагентами дегидратации, например, N-(3-диметиламиноизопропил)-N'-этилкарбодиимид-гидрохлорид (EDC). Подобные синтезы описаны в Journal of Medicinal Chemistry 2012, 55, 3563-3567, например. В зависимости от природы нуклеофила R2H 1F, хинолины хлора 1S реагируют с 1F в присутствии основания, например, этилата натрия, метилата натрия, калия трет-бутилата, триэтиламин N,N-диизопропил этиламина, диазабициклоундекана, гидрида натрия, гидроксида лития, гидроксида натрия, гидроксида калия, карбоната калия, карбоната цезия, или тому подобного, с получением промежуточных соединений карбоксамидов 1T. Реакция сочетания Сузуки промежуточных соединений карбоксамидов 1T с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат), как описано в Chem. Soc. Rev. 2014, 43, 412-443, или в Tetrahedron 2002, 58 (48), 9633-9695, приводит к конечным продуктам формулы (I).
Альтернативно, хинолины хлора 1Е реагируют через реакцию сочетания Сузуки с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат), как описано в Chem. Soc. Rev. 2014, 43, 412-443 или в Tetrahedron 2002, 58 (48), 9633-9695, с обеспечением хинолиновых сложных эфиров карбоновых кислот 1Q, которые могут быть легко омылены, например, с гидроксидом лития, приводя к соответствующей хинолинкарбоновой кислоты 1R. Затем, промежуточные соединения карбоксамиды 1N получают посредством условий амидного связывания, например, через хлориды карбоновых кислот, образованные из 1R, которые объединяются с аминами 1М в основных условиях, например, пиридин, триэтиламин или N,N-диизопропилэтиламин, или через образование амида из карбоновых кислот 1R, которые объединяются с аминами 1М и реагентами дегидратации, например, N-(3-диметиламиноизопропил)-N'-этилкарбодиимид-гидрохлорид (EDC). Подобные синтезы описаны в Journal of Medicinal Chemistry 2012, 55, 3563-3567 например. В зависимости от природы нуклеофила R2H 1F, хинолины хлора 1N реагируют с 1F в присутствии основания, например, этилата натрия, метилата натрия, калия трет-бутилата, триэтиламин N,N-диизопропил этиламина, диазабициклоундекана, гидрида натрия, гидроксида лития, гидроксида натрия, гидроксида калия, карбоната калия, карбоната цезия, или тому подобного, с получением конечных продуктов формулы (I).
Схема 1d
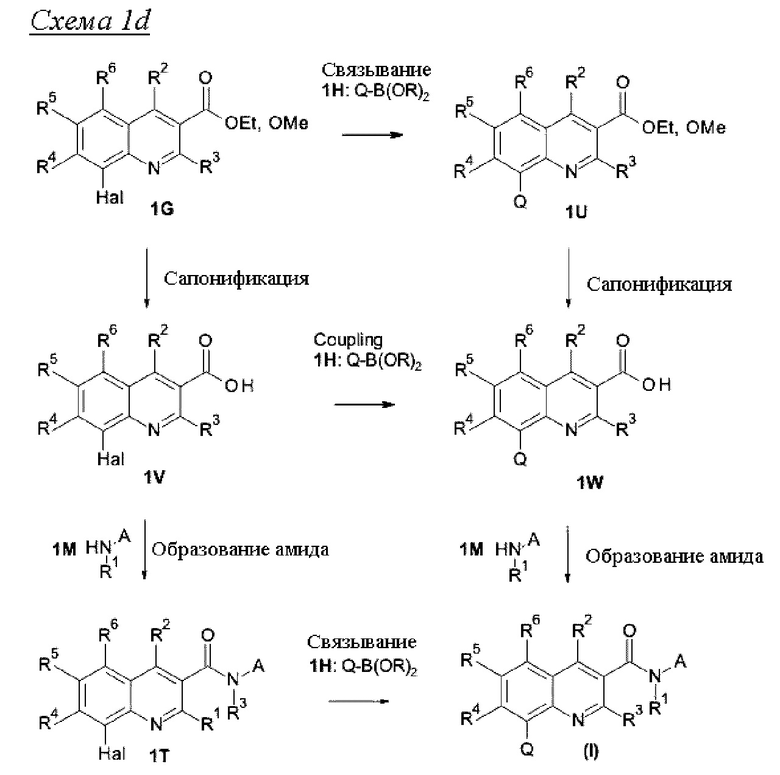
Хинолиновые сложные эфиры карбоновых кислот 1G могут быть превращены через реакцию сочетания Сузуки с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат), как описано в Chem. Soc. Rev. 2014, 43, 412-443 или в Tetrahedron 2002, 58 (48), 9633-9695, с обеспечением хинолиновых сложных эфиров карбоновых кислот 1U, которые могут быть плавно омылены, например, с гидроксидом лития, приводя к соответствующей хинолинкарбоновой кислоте 1W. Затем, конечные продукты формулы (I) получают посредством условий амидного связывания, например, через хлориды карбоновых кислот, образованные из 1W, которые объединяются с аминами 1М при основных условиях, например, пиридин, триэтиламин или N,N-диизопропилэтиламин, или через образование амида из карбоновых кислот 1W, которые объединяются с аминами 1М и реагентами дегидратации, например, N-(3-диметиламиноизопропил)-N'-этилкарбодиимид-гидрохлорид (EDC). Подобные синтезы описаны в Journal of Medicinal Chemistry 2012, 55, 3563-3567, например.
Альтернативно, хинолиновые сложные эфиры карбоновых кислот 1G могут быть омылены сначала и затем превращены через реакцию сочетания Сузуки с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат) в хинолинкарбоновые кислоты 1W или трансформированы в хинолинкарбоксамиды 1T посредством условий амидного связывания, например, через хлориды хннолинкарбоновых кислот, образованные из 1V, которые объединяются с аминамии 1М при основных условиях, например, пиридин, триэтиламин или N,N-диизопропилэтиламин, или через образование амида из хинолонкарбоновых кислот 1V, которые объединяются с аминами 1М и реагентами дегидратации, например, N-(3-диметиламиноизопропил)-N'-этилкарбодиимид-гидрохлорид (EDC). Наконец, хинолинкарбоксамиды 1T могут быть превращены посредством реакции сочетания Сузуки с бороновыми кислотами или бороновыми сложными эфирами 1Н Q-B(OR)2 (R=H; R=Me или R,R = пинаколат), как описано в Chem. Soc. Rev. 2014, 43, 412-443 или в Tetrahedron 2002, 58 (48), 9633-9695, в конечные продукты формулы (I).
Схема 1d'
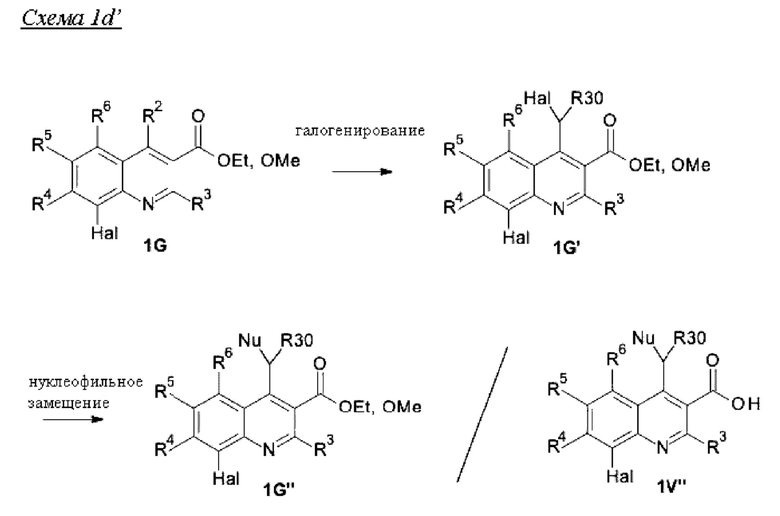
Подгруппа 1G, где R2 представляет собой алкильную группу, такую как метил (R30=Н), может быть галогенирована, например, бромирована посредством агентов бромирования, таких как бром, N-бром-сукцинимид, пиридиния трибромид или фенилтриметиламмония трибромид или бромалкильные производные 1G', как описано в, например, J. Heterocl. Chem. 1981, vol. 18, 925-928, J. Med. Chem., 2009, vol. 52, 3047-3062 or J. Am. Chem. Soc., 1948, 70, 417-418. Такие бромалкильные соединения 1G' могут быть замещены нуклеофилами, такими как амины, спирты или тиолы или их соли, иногда в присутствии основания, согласно стандартным методикам, до конечных насыщенных алкил-хинолинов 1G''. В условиях реакции нуклеофильного замещения сложные эфиры 1G'' могут быть далее превращены в соответствующие кислоты 1V'', или они могут быть выделены и превращены на отдельной стадии гидролиза в кислоты 1V''. Затем, конечные продукты (I) могут быть получены из кислот 1V'' посредством образования амида и связывания группы Q способами, описанными на схеме 1d.
Схема 1e (R2 = необязательно замещенный С1-С4-алкокси)
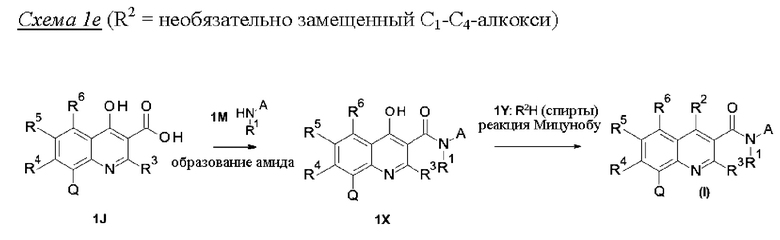
Гидроксихинолоны 1X получают посредством условий амидного связывания, например, через хлориды карбоновых кислот, образованные из 1J, которые объединяются с аминами 1М в основных условиях, например, пиридин, триэтиламин или N,N-диизопропилэтиламин, или через образование амида из карбоновых кислот 1J, которые объединяются с аминами 1М и реагентами дегидратации, например, N-(3-диметиламиноизопропил)-N'-этилкарбодиимид-гидрохлорид (EDC). Подобные синтезы описаны в Journal of Medicinal Chemistry 2012, 55, 3563-3567, например. Конечные продукты формулы (I) получают посредством реакции Мицунобу гидроксихинолонов 1X со спиртами 1Y (R2=C1-С4-алкокси, необязательно замещенный) в присутствии реагентов дегидратации, например, диизопропил-(Е)-диазен-1,2-дикарбоксилат и трифенилфосфин, как описано в Organic & Biomolecular Chemistry 2012, 10(32), 6537-6546.
Схема 2 (R2 = C1-C4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, С3-С6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкил, каждый из которых необязательно замещен, как определено для соединения общей формулы (I), как указано выше)
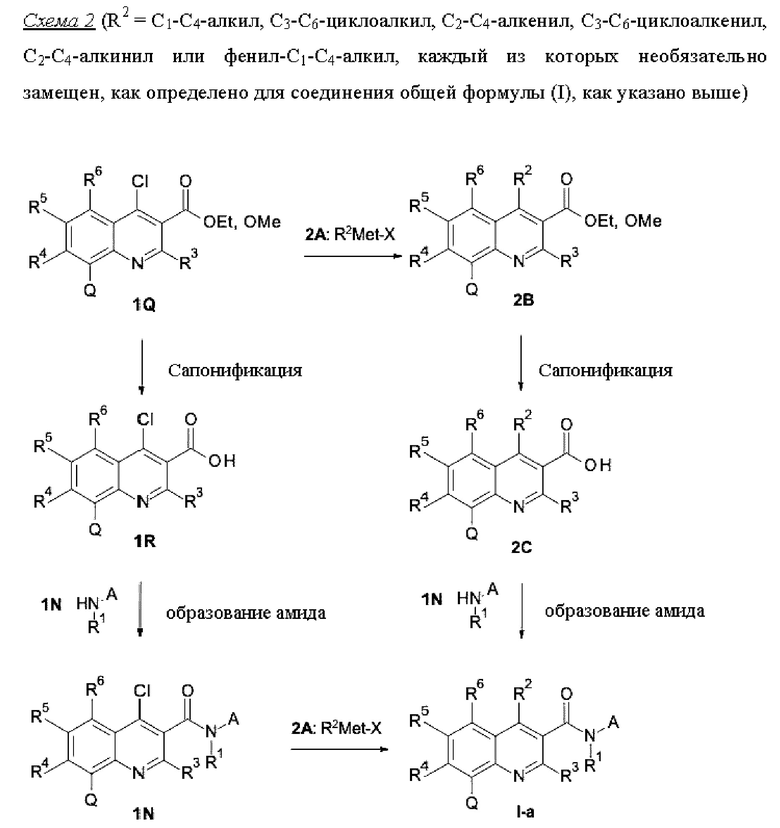
Промежуточные соединения хинолиновых сложных эфиров карбоновых кислот 1Q или хинолонкарбоксамидные промежуточные соединения 1N могут быть превращены с определенными соединениями Гриньяра или металлическими органическими соединениями 2А: С1-С4-алкил-Met-X, С3-С6-циклоалкил-Met-X, С2-С4-алкенил-Vet-Х, С3-С6-циклоалкенил-Met-X, С2-С4-алкинил-Met-Х или фенил-С1-С4-алкил-Met-Х (Met = Мг, Zn; X=I, Br, Cl), вводя С1-С4-алкил, С3-С6-циклоалкил, С2-С4-алкенил, С3-С6-циклоалкенил, С2-С4-алкинил или фенил-С1-С4-алкил, каждый из которых необязательно замещен, как определено для соединения общей формулы (I), как указано выше, как описано в Tetrahedron Letters, 2000, 41(33), 6387-6391, например, в сложноэфирные промежуточные соединения 2В или конечные соединения I-а.
Схема 3 (R3 = C1-C4-алкил)
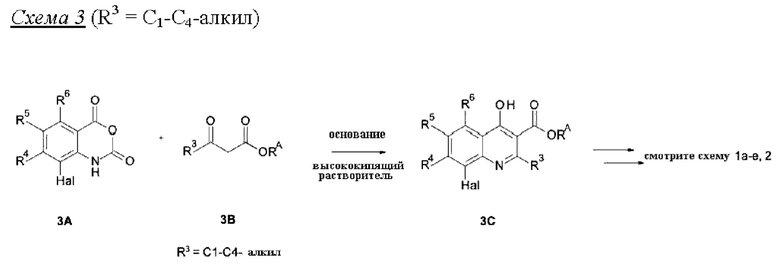
В альтернативном пути получения гидроксильного сложного эфира 3С (R3=C1-С4-алкил, RA = метил, этил или трет.-бутил) применяют коммерчески доступные 2Н-3,1-оксазин-2.4(1Н)-дионы 3А (Hal = иод, бром, хлор) в реакции декарбоксилирования со сложными кетоэфирами 3В (R3=С1-С4-алкил, RA = метил, этил или трет.-бутил) в присутствии основания, например, гидрида натрия в полярных высококипящих растворителях, например, N,N-диметилацетамид, как описано в US 20080306048. Следующие стадии могут быт осуществлены согласно схеме 1а-е или схеме 2.
Схема 4
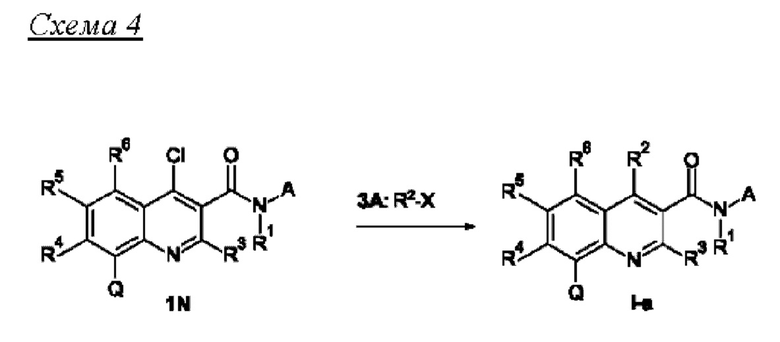
Хинолонкарбоксамидные промежуточные соединения 1N могут быть превращены посредством окислительно-восстановительной реакции под действием света с определенными алкил, циклоалкил и гетероциклоалкил галогенидами или карбоновыми кислотами 3А: С1-С4-алкил-Х, С3-С6-циклоалкил-Х, С3-С6-циклоалкенил-Х, гетероциклоалкил-Х (X=Br, СООН), вводя С1-С4-алкил, С3-C6-циклоалкил, С3-С6-циклоалкенил, гетероциклоалкил, каждый из которых необязательно замещен, как определено для соединения общей формулы (I), как указано выше, как описано в J. Qrg. Chem., 2016, 81 (16), pp 6898-6926 или Chem. Rev., 2013, 113 (7), pp 5322-5363.
Экспериментальная часть - Примеры
Синтез 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(R2)хинолин-3-карбоксамидов (примеры 135, 137, 150, 188, 189, 243, 261, 264, 273).
Стадия 1
8-(3,5-дихлорфенил)-4-гидроксихинолин-3-карбоновая кислота
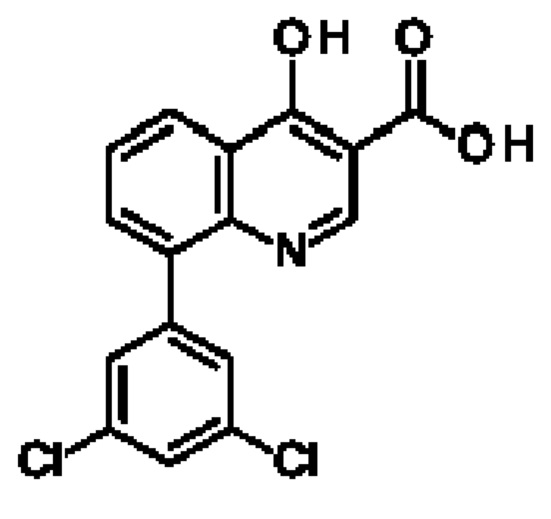
В атмосфере аргона в колбу загрузили этил 8-бром-4-гидрокси-хинолин-3-карбоксилат (15.0 г, 50.7 ммоль) (Gharat, al., WO 2013/118071), 3,5-бензолбороновую кислоту (11.6 г, 60.8 ммоль), карбонат калия (14.0 г, 101 ммоль) 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (1.24 г, 1.52 ммоль) и дегазированную 5:1 смесь диоксана и воды (190 мл). Суспензию перемешивали всю ночь при 70°С. Затем водный раствор гидроксида натрия (5 М, 101 мл, 505 ммоль) добавили, и смесь темного цвета нагревали с возвратом флегмы в течение 6 ч. Затем, горячую воду (110 мл), метанол (70 мл) и активированный уголь (2.5 г) добавили и нагревание с возвратом флегмы продолжали в течение нескольких минут. Смесь отфильтровали горячей, и осадок на фильтре промыли метанолом/водой (1:1). 5 М уксусную кислоту (150 мл, 750 ммоль) добавили медленно при перемешивании к горячему фильтрату до достижения значения рН в интервале 6-7. Еще 90 мл воды добавили, и растворители частично удалили при пониженном давлении. Суспензию охладили при перемешивании до комнатной температуры и позднее до 0°С. Осадок отфильтровали, промыли метанолом/водой (2:1), перемешали в МТВЕ, отфильтровали снова и высушили в вакууме.
Выход: 17.5 г (92% чистота, 95% от теоретического выхода)
LC-MS (Способ L1): Rt=1.02 мин; MS (ESIpos): m/z=334 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (1.06), 0.008 (0.98), 1.909 (9.53), 2.524 (1.24), 2.670 (0.41), 3.162 (0.87), 3.175 (0.89), 3.568 (5.51), 7.609 (2.04), 7.628 (3.44), 7.650 (15.61), 7.654 (16.00), 7.769 (2.83), 7.773 (4.62), 7.778 (2.66), 7.788 (3.38), 7.791 (3.46), 7.806 (2.84), 7.809 (2.66), 7.874 (0.44), 7.879 (0.42), 7.948 (0.51), 7.952 (0.48), 8.364 (3.52), 8.368 (3.54), 8.385 (3.50), 8.388 (3.26), 8.603 (10.14), 12.202 (1.00).
Стадия 2
4-хлор-8-(3,5-дихлорфенил)хинолин-3-карбонилхлорид
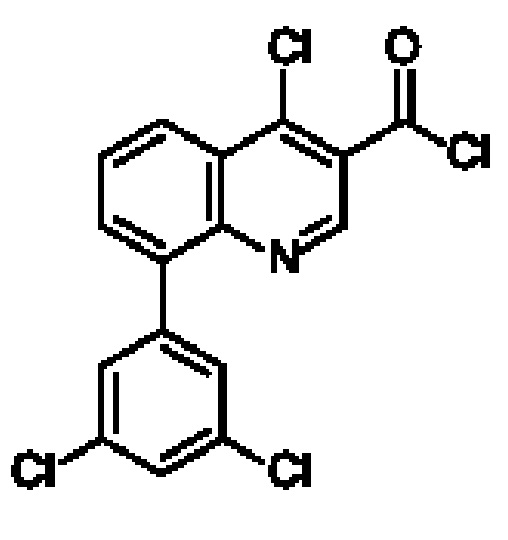
К суспензии 8-(3,5-дихлорфенил)-4-гидроксихинолин-3-карбоновой кислоты (стадия 1) (8.10 г, 24.2 ммоль) 6 хлороформе (48 мл) при перемешивании добавили DMF (4 капли) и оксалилхлорид (40 мл, 460 ммоль) медленно в течение 1 ч при температуре окружающей среды, вызывая значительное газообразование. Затем, смесь медленно нагрели до возврата флегмы и перемешивали при температуре возврата флегмы в течение 3.5 ч. Летучие соединения выпарили при пониженном давлении, и остаток совместно выпарили дважды с сухим дихлорметаном и один раз с сухим THF. Неочищенный продукт (9.0 г, 100%) применяли на следующей стадии.
1H-ЯМР (400 МГц, Хлороформ-d): δ [ppm] = 9.42 (s, 1H), 8.53 (dd, 1H), 7.89-7.95 (m, 1H), 7.80-.87 (m, 1H), 7.53 (d, 2H), 7.46 (t, 1H).
Стадия 3
4-хлор-8-(3,5-дихлорфенил)хинолин-3-карбоновая кислота
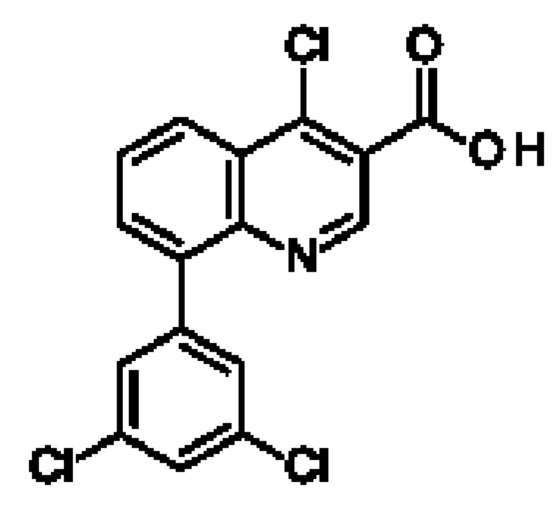
4-хлор-8-(3,5-дихлорфенил)хинолин-3-карбонилхлорид (стадия 2) (5.40 г, 14.6 ммоль) суспендировали в THF (100 мл). Воду (25 мл) и гидрокарбонат натрия (2.0 г, 23.8 ммоль) добавили до поддержания рН 5, и реакционную смесь перемешивали всю ночь при температуре окружающей среды. THF в значительной степени удалили при пониженном давлении при температуры бани, не превышающей 40°С. Ацетонитрил (20 мл) добавили, и органические растворители удалили снова при пониженном давлении. Эту методику повторили, и суспензию охладили до 0°С. Осадок отфильтровали, промыли небольшими объемами ацетонитрила / воды (2:1) и петролейного простого эфира и высушили в вакууме.
Выход: 5.10 г (93% чистота, 92% от теоретического выхода)
LC-MS (Способ L1): Rt=1.16 мин; MS (ESIpos): m/z=352 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (1.29), 0.008 (1.20), 1.760 (0.44), 2.329 (0.64), 2.367 (0.44), 2.524 (2.38), 2.671 (0.63), 2.711 (0.43), 3.601 (0.50), 7.654 (1.72), 7.660 (4.30), 7.664 (6.77), 7.669 (16.00), 7.673 (7.64), 7.804 (1.91), 7.823 (3.49), 7.843 (3.22), 7.887 (3.53), 7.890 (3.71), 7.904 (2.79), 8.354 (3.04), 8.357 (3.11), 8.375 (2.85), 8.378 (2.73), 8.907 (6.32).
Стадия 4а
4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (пример 4)
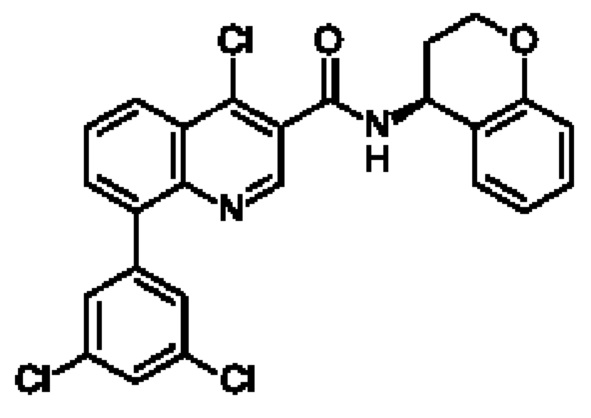
К раствору 4-хлор-8-(3,5-дихлорфенил)хинолин-3-карбоновой кислоты (стадия 3) (7.60 г, 21.6 ммоль) в THF (110 мл) добавили при перемешивании (4S)-хроман-4-амин гидрохлорид (4.4 г, 23.7 ммоль), триэтиламин (12 мл, 86 ммоль) и через 10 мин при температуре окружающей среды раствор 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксида в этилацетате (19 мл, 50% содержание, 32 ммоль), после этого температуру смеси подняли до 36°С. После перемешивания всю ночь при температуре окружающей среды еще (4S)-хроман-4-амин гидрохлорид (0.8 г, 4.3 ммоль), триэтиламин (3 мл, 21.5 ммоль) и раствор 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксида в этилацетате (3.85 мл, 50% content, 6.5 ммоль) добавили, и перемешивание продолжали при температуре окружающей среды в течение еще одной ночи. Затем воду добавили, и большую часть органических растворителей выпарили при пониженном давлении. Образованный осадок отфильтровали и промыли петролейным простым эфиром и высушили в вакууме.
Выход: 10.0 g (94% чистота, 90% от теоретического выхода)
LC-MS (Способ L1): Rt=1.35 мин; MS (ESIpos): m/z=483 [M+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 1.356 (1.31), 1.743 (2.45), 1.752 (3.18), 1.759 (6.79), 1.768 (3.21), 1.776 (2.57), 1.988 (0.51), 2.059 (0.99), 2.066 (1.07), 2.076 (1.22), 2.084 (1.26), 2.093 (1.57), 2.100 (1.38), 2.209 (1.45), 2.221 (1.33), 2.229 (1.27), 2.242 (0.90), 2.366 (0.47), 3.585 (2.47), 3.601 (5.93), 3.617 (2.49), 4.221 (0.89), 4.241 (2.24), 4.249 (1.82), 4.262 (2.18), 4.270 (2.80), 4.279 (2.21), 4.287 (1.82), 4.296 (1.93), 4.315 (0.75), 5.267 (0.91), 5.282 (2.01), 5.301 (2.05), 5.315 (0.88), 6.791 (3.63), 6.811 (4.03), 6.917 (1.84), 6.936 (3.82), 6.955 (2.20), 7.161 (2.03), 7.179 (3.22), 7.199 (1.53), 7.380 (3.39), 7.399 (3.19), 7.680 (16.00), 7.879 (0.46), 7.893 (2.16), 7.912 (3.99), 7.932 (3.43), 8.009 (4.26), 8.026 (2.94), 8.389 (3.75), 8.410 (3.33), 8.962 (9.97), 9.251 (3.23), 9.272 (3.16).
Стадия 4b
4-хлор-8-(3,5-дихлорфенил)-N-[(1S)-2,3-дигидро-1Н-инден-1-ил]хинолин-3-карбоксамид (пример 3)
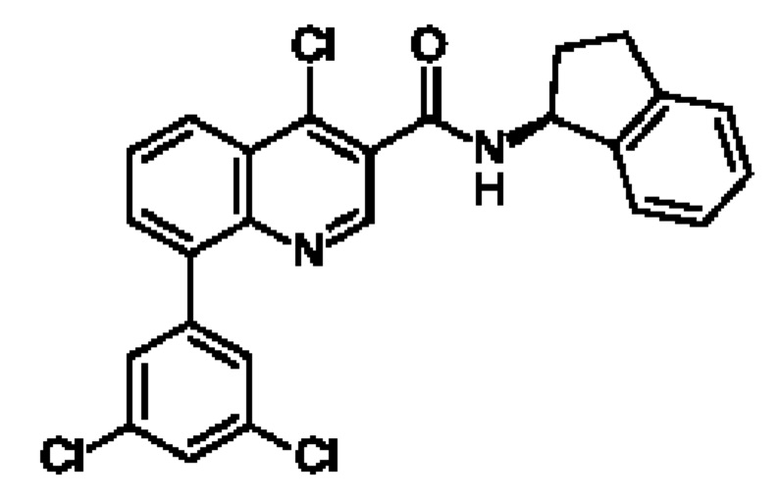
К перемешиваемой смеси 4-хлор-8-(3,5-дихлорфенил)хинолин-3-карбонилхлорида (стадия 2) (480 мг, 1.29 ммоль) в DMF (4 мл) добавили триэтиламин (0.36 мл, 2.6 ммоль) и затем по каплям раствор (1S)-индан-1амина (0.18 мл, 2.6 ммоль) в дихлорметане (1.2 мл) at 0°C. Реакционную смесь перемешивали 1 ч при 0°С, затем нагрели до температуры окружающей среды, и значение рН довели до 5-6 с помощью 1 М уксусной кислоты, с последующим добавлением воды и экстракции с помощью дихлорметаном. Органические фазы отделили и выпарили при пониженном давлении, и осадок очистили посредством колоночной хроматографии на силикагеле (100 г), элюент: циклогексан / этилацетат (9-40%).
Выход: 149 мг (25% от теоретического выхода)
LC-MS (Способ L1): Rt=1.37 мин; MS (ESIpos): m/z=467 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 0.008 (1.33), 1.234 (2.20), 1.397 (0.85), 1.924 (1.63), 1.935 (0.83), 1.946 (1.76), 1.956 (1.90), 1.967 (0.79), 1.977 (1.84), 1.998 (0.66), 2.524 (2.18), 2.567 (0.88), 2.575 (0.77), 2.838 (0.77), 2.859 (1.28), 2.878 (2.28), 2.898 (2.50), 2.918 (1.19), 2.951 (1.54), 2.959 (1.64), 2.973 (1.71), 2.980 (1.81), 2.990 (0.99), 2.999 (0.88), 3.012 (0.86), 3.020 (0.74), 3.070 (1.91), 5.542 (1.02), 5.562 (2.83), 5.582 (2.79), 5.602 (0.92), 7.223 (0.96), 7.232 (4.00), 7.240 (4.95), 7.246 (5.24), 7.254 (7.15), 7.263 (2.96), 7.271 (3.67), 7.281 (2.50), 7.293 (1.17), 7.435 (2.55), 7.446 (2.61), 7.456 (2.00), 7.635 (1.10), 7.665 (0.98), 7.678 (13.08), 7.681 (16.00), 7.686 (7.10), 7.689 (3.73), 7.695 (1.37), 7.700 (0.80), 7.895 (2.06), 7.913 (4.25), 7.934 (3.06), 8.004 (4.66), 8.008 (3.27), 8.022 (3.28), 8.026 (2.07), 8.393 (4.14), 8.396 (2.75), 8.414 (3.73), 8.417 (2.39), 8.962 (10.00), 9.118 (3.31), 9.139 (3.23).
Стадия 5
4-(азетидин-1-ил)-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (пример 135)
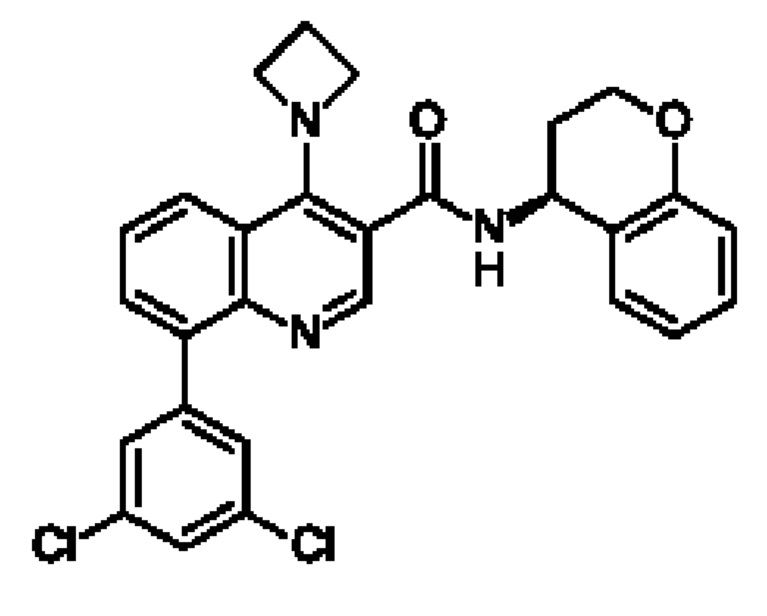
В толстостенном сосуде, подводящем для обработки микроволнами, триэтиламин (84 мкмл, 0.6 ммоль) и азетидин (40 мкмл, 0.6 ммоль) добавили к раствору 4-хлор-8-(3,5-диклорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (стадия 4а) (145 мг, 0.3 ммоль) в N-метилпирролидоне. Сосуд закрыли и нагревали при перемешивании до 100°С в течение 2.5 ч. 5 М муравьиную кислоту (180 мкмл, 0.9 ммоль) и немного ДМСО добавили к смеси темного цвета, и раствор очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота / ацетонитрил).
Выход: 93 мг (62% от теоретического выхода)
LC-MS (Способ L1): Rt=0.89 мин; MS (ESIpos): m/z=504 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (6.30), 0.008 (2.98), 2.004 (1.02), 2.014 (0.94), 2.026 (1.43), 2.041 (1.28), 2.126 (1.31), 2.141 (1.56), 2.373 (2.15), 2.394 (2.92), 2.412 (2.16), 2.433 (1.25), 2.519 (4.80), 2.523 (4.67), 4.243 (3.28), 4.255 (4.75), 4.261 (3.01), 4.270 (2.58), 4.427 (5.50), 4.446 (8.06), 4.466 (4.62), 5.160 (0.92), 5.174 (1.75), 5.194 (1.64), 5.754 (2.42), 6.781 (3.04), 6.785 (3.14), 6.802 (3.39), 6.805 (3.26), 6.887 (1.73), 6.890 (1.66), 6.906 (3.30), 6.909 (2.99), 6.924 (1.93), 6.927 (1.70), 7.142 (1.75), 7.146 (1.77), 7.163 (2.63), 7.180 (1.31), 7.185 (1.20), 7.291 (2.83), 7.311 (2.52), 7.434 (2.40), 7.452 (3.13), 7.455 (2.90), 7.473 (2.61), 7.592 (2.65), 7.597 (4.87), 7.602 (5.82), 7.611 (16.00), 7.616 (8.48), 7.698 (3.62), 7.701 (3.63), 7.716 (3.07), 7.719 (2.82), 8.058 (3.06), 8.061 (3.05), 8.080 (2.76), 8.083 (2.47), 8.430 (11.34), 8.946 (2.94), 8.966 (2.74).
этил N-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2H-хромен-4-илкарбамоил]хинолин-4-ил}-N-метилглицинат (пример 137)
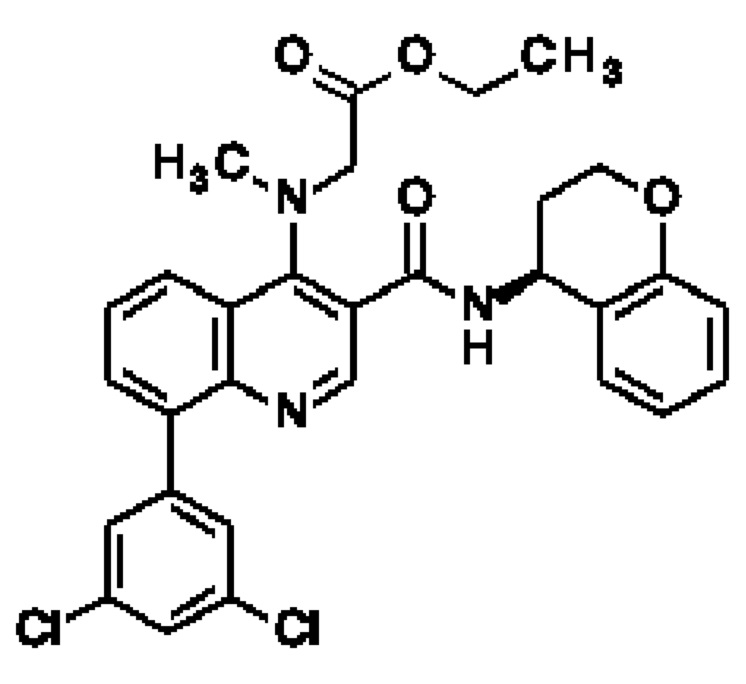
В атмосфере аргона в толстостенный сосуд, подходящий для обработки микроволнами, загрузили 1,4-диаза6ицикло(2.2.2)октан (56 мг, 0.5 ммоль), этил-N-метилглицинатгидрохлорид (1:1) (154 мг, 1.0 ммоль), N,N-диизопропилэтиламин (350 мкмл, 2.0 ммоль), N-метил пирролидон (0.8 мл) и 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2H-хромен-4-ил]хинолин-3-карбоксамид (стация 4а) (242 мг, 0.5 ммоль). Сосуд закрыли, и смесь нагревали при перемешивании при 100°С в течение 3 ч. Дополнительные количества этил-N-метилглицинатгидрохлорида (1:1) (77 мг, 0.5 ммоль), N,N-диизопропилэтиламина (170 мкмл, 1.0 ммоль) добавили, и нагревание продолжали в течение 2 ч. 5 М муравьиную кислоту (0.7 мл, 3.5 ммоль) и ДМСО (3 мл) добавили, и раствор очистили посредством препаративной ВЭЖХ (С18, градиент 0.1% вод. муравьиная кислота / ацетонитрил).
Выход: 150 мг (98% чистота, 52% от теоретического выхода)
LC-MS (Способ L1): Rt=1.38 мин; MS (ESIpos): m/z=564 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (0.78), 0.008 (0.70), 1.199 (4.33), 1.217 (9.13), 1.234 (4.62), 1.356 (0.52), 2.063 (0.43), 2.073 (0.48), 2.084 (0.47), 2.099 (0.71), 2.107 (0.59), 2.114 (0.45), 2.193 (0.49), 2.205 (0.59), 2.216 (0.59), 2.227 (0.52), 2.523 (0.52), 3.049 (12.82), 4.052 (6.68), 4.134 (1.34), 4.152 (4.12), 4.170 (4.04), 4.187 (1.27), 4.255 (1.01), 4.267 (1.21), 4.278 (1.65), 4.282 (1.70), 4.293 (0.97), 5.257 (0.42), 5.271 (0.95), 5.291 (0.95), 5.305 (0.42), 6.792 (1.74), 6.812 (1.94), 6.901 (0.87), 6.919 (1.84), 6.937 (1.07), 7.154 (0.86), 7.157 (0.93), 7.175 (1.47), 7.193 (0.70), 7.196 (0.71), 7.362 (1.56), 7.380 (1.46), 7.645 (16.00), 7.688 (1.26), 7.707 (1.75), 7.728 (1.59), 7.840 (1.89), 7.842 (2.05), 7.857 (1.58), 7.860 (1.56), 8.354 (1.72), 8.357 (1.80), 8.376 (1.63), 8.379 (1.60), 8.757 (6.02), 9.197 (1.69), 9.217 (1.64).
N-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}-N-метилглицин (пример 150)
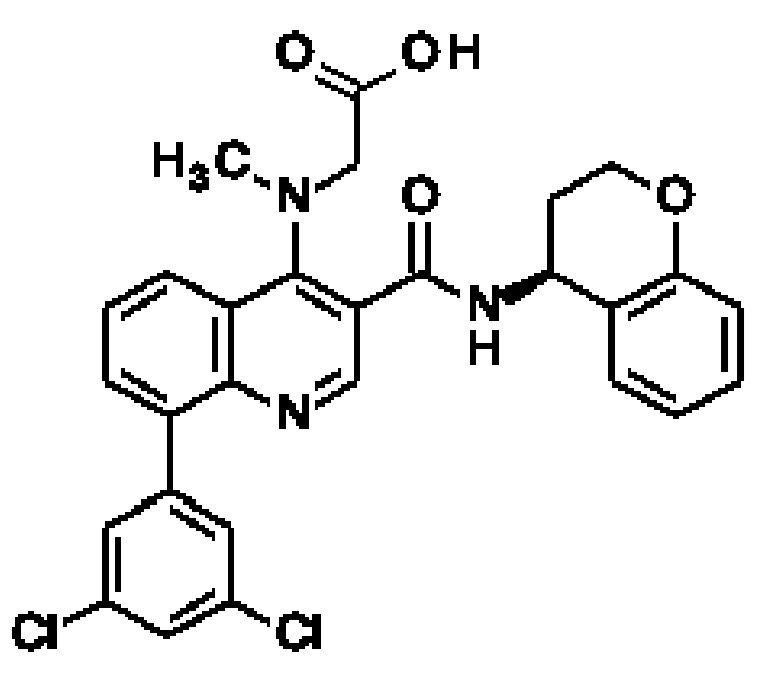
Этил N-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}-N-метилглицинат (из примера 137) (35 мг, 62 мкмоль) перемешали в THF (0.3 мл), этаноле (0.3 мл) и 5 М вод. гидроксиде натрия (50 мкмл, 250 мкмоль) в течение 1.5 ч при температуре окружающей среды. Реакционную смесь подкислили до рН 3 посредством добавления 5 М муравьиной кислоты, и часть растворителей выпарили при пониженном давлении. Образованный осадок отфильтровали, промыли водой и высушил и в вакууме.
Выход: 27 мг (81% от теоретического выхода)
LC-MS (Способ L1): Rt=1.11 мин; MS (ESIpos): m/z=536 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 2.132 (1.28), 2.205 (1.37), 2.328 (0.59), 3.040 (16.00), 3.931 (0.61), 3.975 (4.59), 3.984 (4.71), 4.281 (3.48), 5.309 (1.69), 5.326 (1.68), 6.779 (2.78), 6.799 (3.08), 6.883 (1.42), 6.901 (2.80), 6.920 (1.72), 7.140 (1.56), 7.159 (2.50), 7.175 (1.25), 7.348 (2.66), 7.365 (2.47), 7.643 (14.76), 7.660 (2.25), 7.678 (2.82), 7.699 (1.88), 7.820 (3.02), 7.835 (2.42), 8.139 (1.05), 8.304 (2.56), 8.326 (2.33), 8.755 (6.56).
8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(1H-1,2,3-триазол-1-ил)хинолин-3-карбоксамид (пример 188)
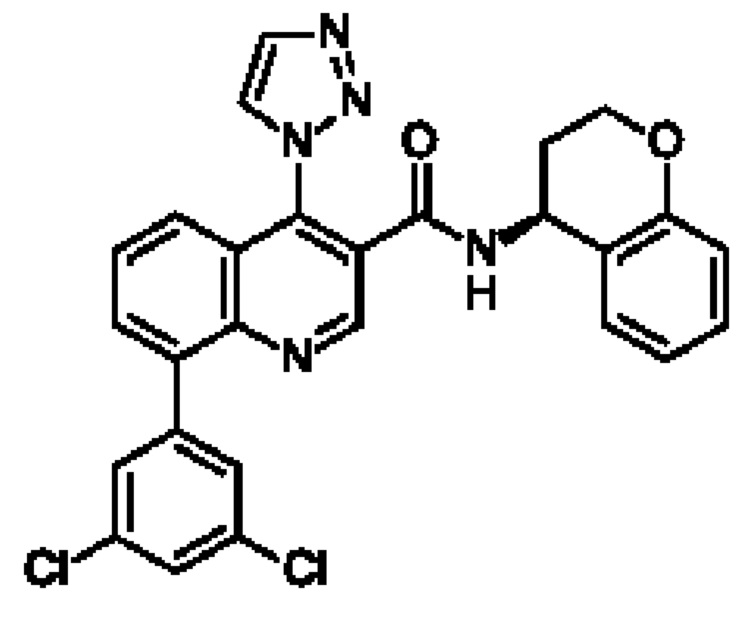
и
8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(2Н-1,2,3-триазол-2-ил)хинолин-3-кар6оксамид (пример 189)
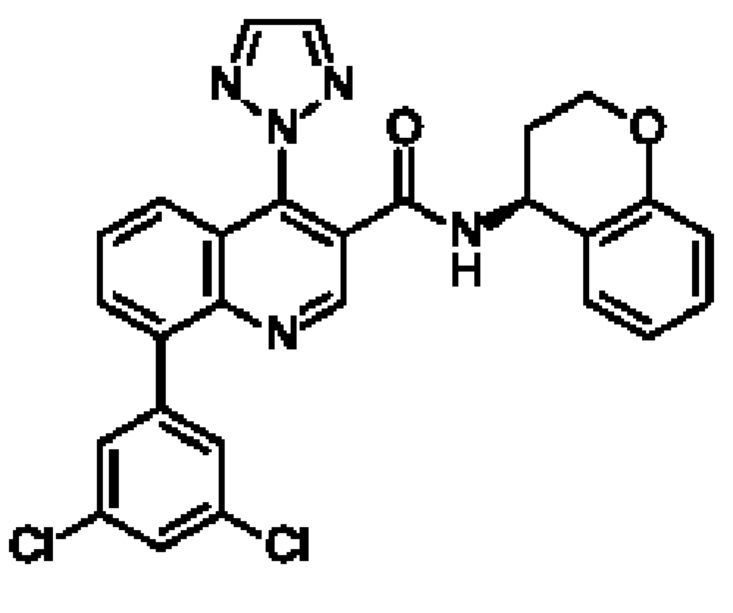
В толстостенный сосуд, подходящий для обработки микроволнами, загрузили 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (стадия 4а) (145 мг, 0.3 ммоль), 1,2,3-триазол (62 мг, 0.9 ммоль), N-метилпирролидон (0.5 мл), триэтиламин (84 мкмл, 0.6 ммоль) и карбонат цезия (98 мг, 0.3 ммоль). Сосуд закрыли, и смесь нагревали при перемешивании при 100°С в течение 2 ч. 5 М муравьиную кислоту (240 мкмл, 1.2 ммоль) и воду (1.5 мл) добавили, и осадок отфильтровали и отбросили. Фильтрат очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота / ацетонитрил).
Выход (пример 188): 23 мг (15% от теоретического выхода)
LC-MS (Способ L1): Rt=1.18 мин; MS (ESIneg): m/z=514 [M-H]-
1H-ЯМР (400 МГц, ДМСО-d6): δ [ppm] = 9.23 (s, 1H), 9.12 (d, 1H), 8.65 (d, 1H), 8.14 (d, 1H), 8.06 (dd, 1H), 7.80-7.88 (m, 1H), 7.68-7.76 (m, 3Н), 7.39-7.46 (m, 1H), 7.10-7.20 (m, 1H), 7.06 (d, 1H), 6.82-6.92 (m, 1H), 6.76 (d, 1H), 4.98-5.09 (m, 1H), 4.18 (td, 1H), 4.00-4.12 (m, 1H), 2.02 (br dd, 1H), 1.73-1.86 (m, 1H).
Выход (пример 189): 73 мг (97% чистота, 46% от теоретического выхода)
LC-MS (Способ L1): Rt=1.27 мин; MS (ESIpos): m/z=516 [M+H]-
1H-ЯМР (400 МГц, ДМСО-d6): Сдвиг [ppm] = 9.12-9.22 (m, 2H), 8.35 (s, 2H), 8.03 (dd, 1H), 7.87-7.96 (m, 1H), 7.78-7.87 (m, 1H), 7.66-7.76 (m, 2H), 7.25 (d, 1H), 7.10-7.19 (m, 1H), 6.88-6.98 (m, 1H), 6.76 (d, 1H), 4.98-5.14 (m, 1H), 4.07-4.29 (m, 2H), 2.02-2.14 (m, 1H), 1.94 (dtd, 1H).
трет-бутил 1-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2H-хромен-4-илкарбамоил]хинолин-4-ил}-L-пролинат (пример 243)
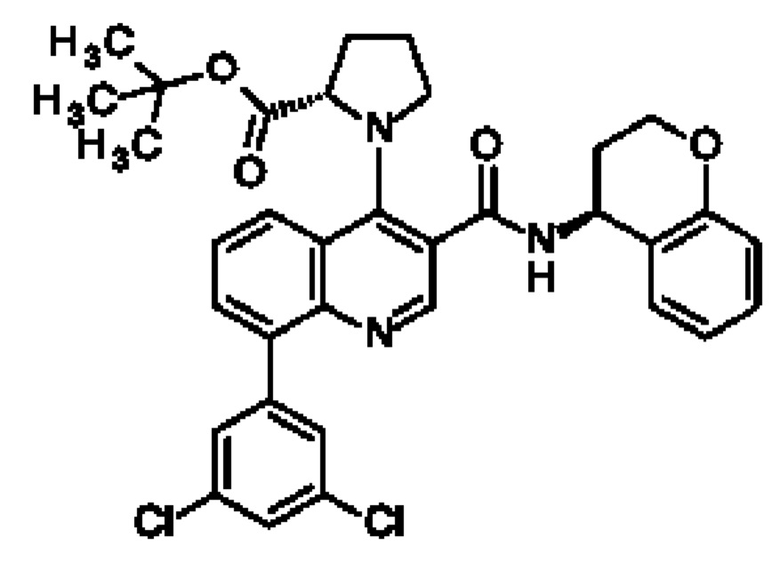
Согласно методике примера 137 указанное в заглавии соединение синтезировали из 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (стадия 4а) (242 мг, 0.5 ммоль) и трет-бутил L-пролината (171 мг, 1.0 ммоль) посредством нагревания при 100°С в течение 3 ч.
Выход: 185 мг (60% от теоретического выхода)
LC-MS (Способ L1): Rt=1.39 мин; MS (BSIpos): m/z=618 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 1.198 (16.00), 1.918 (0.63), 1.932 (0.85), 1.945 (0.51), 4.260 (0.44), 6.788 (0.61), 6.808 (0.69), 6.939 (0.64), 7.186 (0.52), 7.394 (0.55), 7.412 (0.51), 7.638 (5.73), 7.655 (0.62), 7.676 (0.53), 7.815 (0.70), 7.832 (0.56), 8.315 (0.60), 8.334 (0.55), 8.684 (2.06), 9.236 (0.58), 9.257 (0.57).
1-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}-L-пролинат (пример 261)
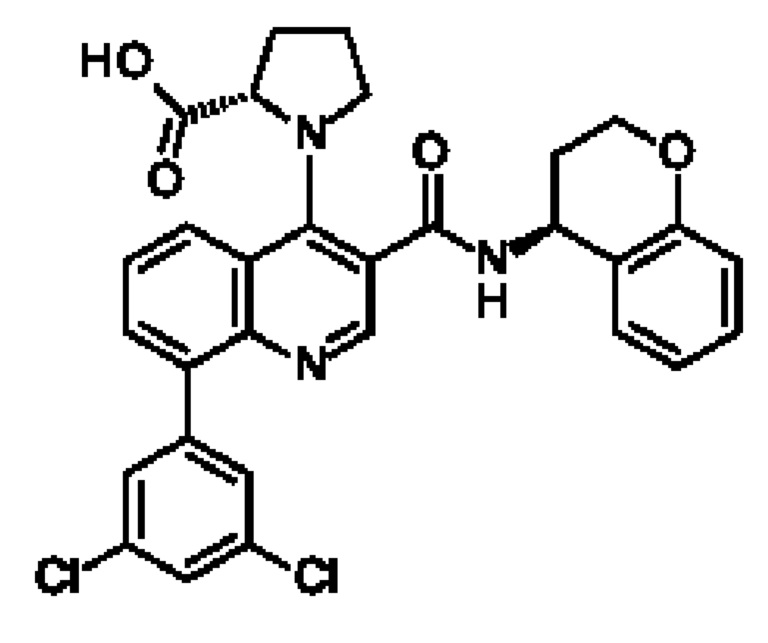
Раствор водорода хлорид в диоксане (1 мл, 4 М) добавили к раствору трет-бутил 1-{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}-L-пролината (из примера 243) (155 мг, 0.25 ммоль) в дихлорметане (0.8 мл) и перемешивали всю ночь при температуре окружающей среды. Летучие соединения удалили при пониженном давлении, и остаток перемешали с дихлорметаном и водой. Отделенную водную фазу экстрагировали дихлорметаном, объединенные органические фазы высушили и выпарили. Остаток очистили посредством препаративной ВЭЖХ (C18, градиент: 0.1% вод. муравьиная кислота / ацетонитрил).
Выход: 52 мг (37% от теоретического выхода)
LC-MS (Способ L1): Rt=0.91 мин; MS (ESIpos): m/z=562 [M+H]+
1H-ЯМР Перечень пиков (500 МГц, ДМСО-d6) δ [ppm]: -0.007 (3.09), 0.006 (1.99), 1.907 (2.42), 2.028 (0.58), 2.033 (0.60), 2.044 (0.71), 2.056 (0.83), 2.166 (0.52), 2.175 (0.71), 2.185 (0.75), 2.193 (0.77), 2.204 (0.50), 2.358 (0.89), 2.361 (1.22), 2.365 (0.93), 2.369 (0.58), 2.392 (0.70), 2.407 (0.71), 2.514 (3.50), 2.518 (3.01), 2.522 (2.34), 2.631 (0.87), 2.635 (1.14), 2.639 (0.81), 3.866 (0.46), 3.878 (1.06), 3.895 (0.91), 4.183 (0.43), 4.188 (0.44), 4.205 (1.12), 4.224 (0.89), 4.229 (0.73), 4.243 (0.75), 4.250 (1.08), 4.262 (0.91), 4.277 (0.46), 4.638 (0.83), 4.649 (1.02), 4.654 (1.33), 4.665 (1.06), 5.254 (0.54), 5.264 (1.14), 5.280 (1.10), 5.291 (0.50), 6.786 (2.22), 6.788 (2.18), 6.802 (2.42), 6.804 (2.32), 6.919 (1.16), 6.921 (1.08), 6.933 (2.26), 6.935 (2.11), 6.948 (1.31), 6.950 (1.18), 7.169 (1.12), 7.172 (1.16), 7.186 (1.76), 7.200 (0.93), 7.203 (0.89), 7.388 (1.80), 7.403 (1.70), 7.629 (1.72), 7.634 (4.02), 7.637 (8.89), 7.639 (16.00), 7.642 (4.87), 7.652 (2.18), 7.654 (1.91), 7.669 (1.82), 7.806 (2.51), 7.809 (2.42), 7.821 (2.05), 7.823 (1.86), 8.303 (1.86), 8.320 (1.72), 8.680 (8.25), 12.586 (0.91).
8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-[(2-гидроксиэтил)сульфанил]хинолин-3-карбоксамид (пример 264)
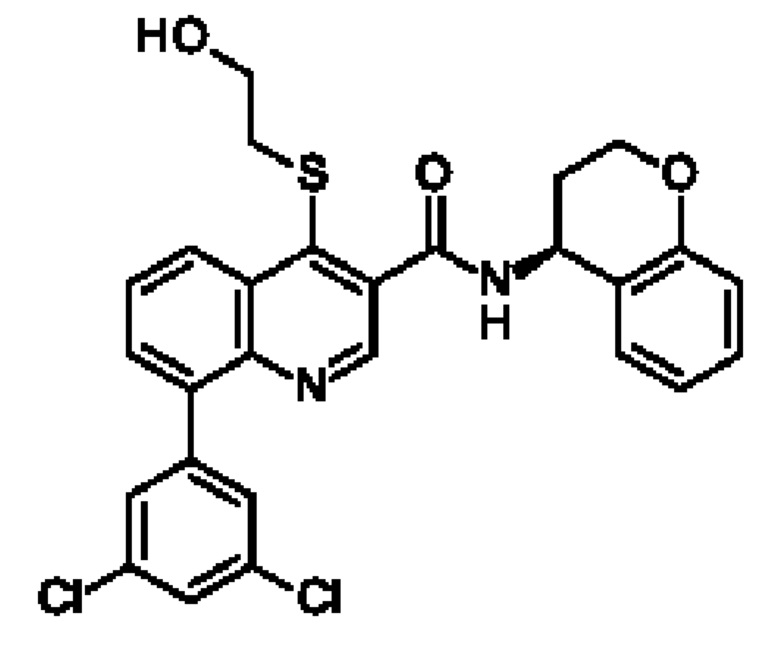
В толстостенный сосуд загрузили 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (стадия 4а) (121 мг, 250 мкмоль), ДМСО (0.3 мл), 2-сульфанилэтанол (39 мг, 500 мкмоль) и триэтиламин (87 мкмл, 630 мкмоль), закрыли и нагревали 2 ч при 100°С. После охлаждения до температуры окружающей среды 5 М муравьиную кислоту (300 мкмл, 1.5 ммоль) добавили, смесь растворили посредством добавления ацетонитрила и очистили посредством препаративной ВЭЖХ (C18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил).
Выход: 95 мг (72% от теоретического выхода)
LC-MS (Способ L1): Rt=1.28 мин; MS (ESIpos): m/z=525 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (2.66), 0.008 (2.57), 2.119 (1.04), 2.128 (0.86), 2.366 (0.82), 2.710 (0.82), 3.060 (2.72), 3.077 (6.64), 3.093 (3.50), 3.287 (2.70), 3.438 (1.04), 3.454 (2.48), 3.468 (3.16), 3.481 (2.10), 3.497 (0.89), 4.254 (1.46), 4.263 (1.26), 4.273 (2.24), 4.282 (2.43), 4.297 (1.35), 4.946 (2.06), 4.960 (4.56), 4.974 (1.99), 5.291 (1.28), 5.310 (1.31), 6.781 (2.41), 6.784 (2.61), 6.802 (2.74), 6.805 (2.88), 6.910 (1.33), 6.913 (1.46), 6.928 (2.63), 6.932 (2.57), 6.947 (1.59), 6.950 (1.53), 7.151 (1.31), 7.156 (1.35), 7.173 (2.21), 7.190 (1.24), 7.194 (1.13), 7.448 (2.17), 7.465 (2.06), 7.627 (1.00), 7.632 (1.04), 7.658 (5.73), 7.662 (16.00), 7.666 (6.68), 7.669 (3.41), 7.675 (1.22), 7.838 (1.93), 7.856 (2.97), 7.859 (2.35), 7.877 (2.92), 7.929 (3.21), 7.932 (3.50), 7.946 (2.21), 7.950 (2.06), 8.624 (2.97), 8.627 (2.97), 8.645 (2.70), 8.649 (2.50), 8.881 (10.45), 9.155 (2.48), 9.175 (2.37).
8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-метоксихинолин-3-карбоксамид (пример 373)
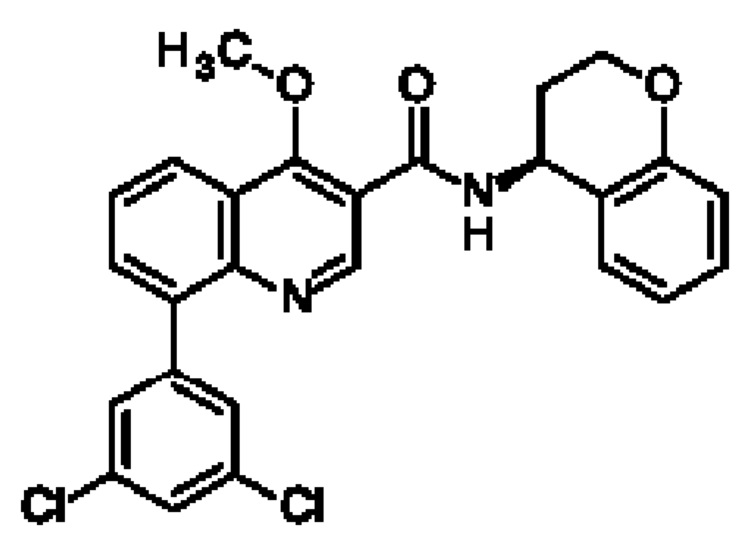
В атмосфере аргона раствор метилата натрия в метаноле (140 мкмл, 5.4 М, 780 мкмоль) добавили по каплям к раствору 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (стадия 4а) (150 мг, 310 мкмоль) в N-метилпирролидоне (1 мл), и смесь перемешивали при температуре окружающей среды в течение 40 мин. Уксусную кислоту (250 мкмл, 5.0 М, 1.2 ммоль) добавили, и смесь очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил).
Выход: 94 мг (63% от теоретического выхода)
LC-MS (Способ L1): Rt=1.39 мин; MS (ESIpos): m/z=479 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 4.172 (16.00), 4.245 (0.90), 4.254 (1.07), 4.269 (1.49), 4.273 (1.51), 4.283 (0.86), 5.274 (0.83), 5.293 (0.83), 5.754 (12.35), 6.793 (1.40), 6.796 (1.53), 6.814 (1.59), 6.816 (1.66), 6.909 (0.74), 6.912 (0.74), 6.928 (1.55), 6.930 (1.54), 6.946 (0.93), 6.949 (0.91), 7.159 (0.76), 7.163 (0.82), 7.180 (1.29), 7.363 (1.33), 7.380 (1.25), 7.650 (0.88), 7.655 (2.07), 7.659 (2.33), 7.670 (7.40), 7.675 (4.39), 7.702 (1.20), 7.720 (1.66), 7.723 (1.57), 7.741 (1.47), 7.886 (1.69), 7.890 (1.80), 7.904 (1.44), 7.908 (1.42), 8.296 (1.61), 8.299 (1.63), 8.317 (1.54), 8.320 (1.45), 8.811 (5.57), 9.192 (1.36), 9.212 (1.34).
Синтез 4-хлор-8-(3,5-диметилфенил)-N-[(1S)-1,2,3,4-тетрагидронафталин-1-ил]хинолин-3-карбоксамида (пример 1).
Стадия 1
этил-4-хлор-8-(3,5-диметилфенил)хинолин-3-карбоксилат
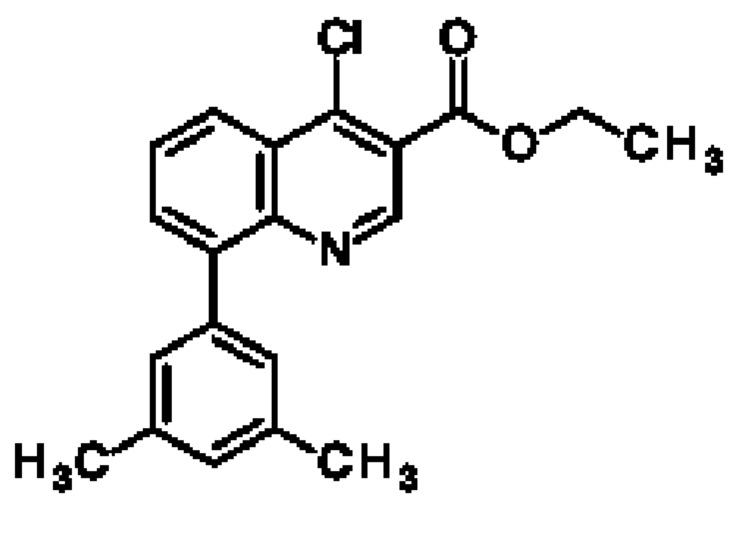
В атмосфере аргона в колбу загрузили этил 8-бром-4-хлорхинолин-3-карбоксилат (330 мг, 1.05 ммоль) (Zask, al. Bioorganic и Medicinal Chemistry Letters, 2003, 1487-1490; Laxmikant, al. US 2013/210844), 3,5-диметилбензолбороновую кислоту (189 мг, 1.26 ммоль) и дегазированную смесь диоксана (6.6 мл) и воду 1.3 мл). Затем карбонат калия (290 мг, 2.10 ммоль) и 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (42.8 мг, 52.5 мкмоль) добавили, и смесь перемешивали всю ночь при 50°С. Реакционную смесь отфильтровали через целит и промыли этилацетатом и водой. Органическую фазу фильтрата промыли водой и соляным раствором, высушили над сульфатом натрия и выпарили при пониженном давлении. Остаток очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил) и хроматографии на силикагеле (циклогексан / этилацетат - 5:1).
Выход: 77.0 мг (21% от теоретического выхода)
LC-MS (Способ L1): Rt=1.43 мин; MS (ESIpos): m/z=340 [M+H]+
ЯМР: 1H-ЯМР (400 МГц, ДМСО-d6): δ [ppm] = 9.13 (s, 1H), 8.42 (dd, 1H), 7.87-7.96 (m, 2H), 7.20 (s, 2H), 7.07 (s, 1H), 4.44 (q, 2H), 2.35 (s, 6H), 1.38 (t, 3H).
Стадия 2
4-хлор-8-(3,5-диметилфенил)хинолин-3-кар6оновая кислота
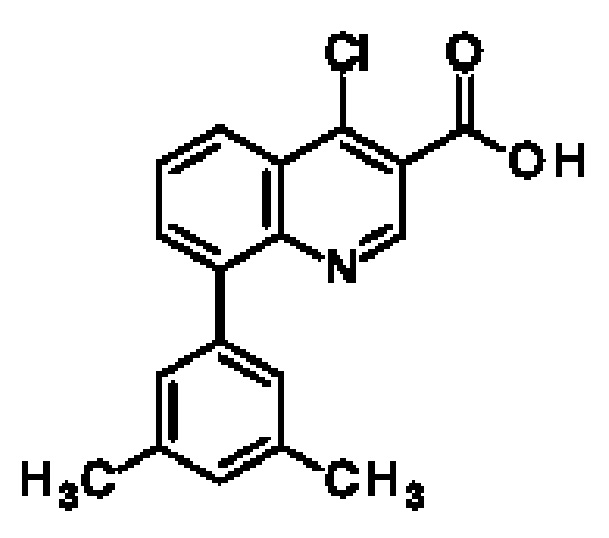
К этил-4-хлор-8-(3,5-диметилфенил)хинолин-3-карбоксилату (стадия 1) (84.0 мг, 247 мкмоль) в 0.5 мл этанола и 0.5 мл THF добавили водный раствор гидроксида натрия (5 M, 150 мкмл, 740 мкмоль), и смесь перемешивали всю ночь при температуре окружающей среды. Растворители удалили при пониженном давлении, остаток растворили в ДМСО и 5 М муравьиной кислоте и очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетон игр ил) с получением твердого вещества грязновато белого цвета.
Выход: 75.0 мг (97% от теоретического выхода).
LC-MS (Способ L1): Rt=1.15 мин; MS (ESIpos): m/z=312 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 2.346 (16.00), 7.062 (1.52), 7.189 (3.52), 7.884 (1.52), 7.895 (1.68), 7.902 (3.49), 8.396 (0.99), 8.403 (0.92), 8.414 (0.88), 8.421 (0.87), 9.116 (2.83).
Стадия 3
4-хлор-8-(3,5-диметилфенил)-N-[(1S)-1,2,3,4-тетрагидронафталин-1-ил]хинолин-3-карбоксамид (пример 1)
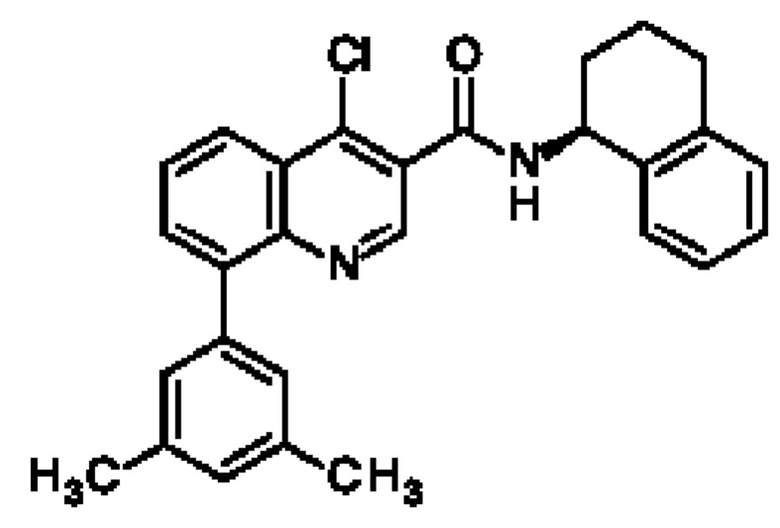
4-Хлор-8-(3,5-диметилфенил)хинолин-3-карбоновую кислоту (стадия 2) (71.0 мг, 228 мкмоль) в 1.2 мл THF обработали (1S)-1,2,3,4-тетрагидронафталин-1-амином (36.9 мг, 251 мкмоль) и триэтиламином (190 мкмл, 1.4 ммоль) и перемешивали при 60°С в течение 10 мин. Затем раствор 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксида в этил ацетате (200 мкмл, 50% содержание, 340 мкмоль) добавили, нагревание прекратили, и смесь перемешивали всю ночь при температуре окружающей среды. Воду и 5 М муравьиную кислоту (0.6 мл) добавили, и растворители удалили при пониженном давлении. Остаток очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил).
Выход: 20.0 мг (20% от теоретического выхода)
LC-MS (Способ L1): Rt=1.42 мин; MS (ESIpos): m/z=441 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (4.41), 0.008 (4.06), 2.342 (16.00), 2.759 (1.07), 7.059 (1.60), 7.111 (0.66), 7.128 (1.05), 7.183 (4.61), 7.195 (1.69), 7.202 (0.82), 7.207 (0.96), 7.422 (0.89), 7.438 (0.75), 7.855 (4.02), 7.865 (2.24), 7.869 (2.26), 8.303 (1.26), 8.314 (1.10), 8.317 (1.07), 8.328 (1.10), 8.874 (5.11), 9.102 (0.96), 9.123 (0.96).
Синтез 8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(морфолин-4-ил)хинолин-3-карбоксамида (пример 52).
Стадия 1
8-бром-4-хлорхинолин-3-карбоновая кислота
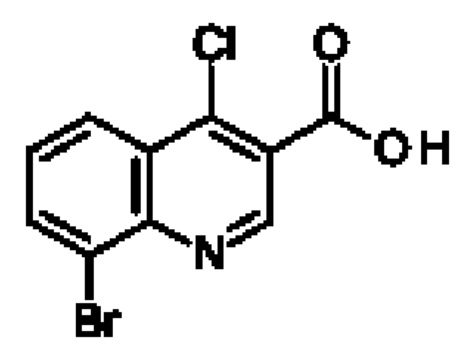
Е суспензии этил-8-бром-4-хлорхинолин-3-карбоксилата (9.44 г, 30.0 ммоль) в THF (65 мл) добавили водный раствор гидроксида натрия (12 мл, 10 М, 120 ммоль), и смесь перемешивали интенсивно при температуре окружающей среды. Через 5 часов, воду (12 мл) добавили, и смесь перемешивали всю ночь при температуре окружающей среды. Супернатант отделили от аморфного осадка, который образовался на стенках колбы, и отбросили. Осадок высушили в вакууме, с получением натриевой соли указанного в заглавии соединения.
LC-MS (Способ L1): Rt=0.70 мин; MS(ESIpos): m/z=285 [М+Н]+
1H-ЯМР (400 МГц, ДМСО-d6): δ [ppm] = 8.98 (s, 1Н), 8.29 (dd, 1H), 8.16-8.23 (m, 1H), 7.64 (t, 1H).
Оставшееся влажное твердое вещество растворили в воде (250 мл) при 60°С, и муравьиную кислоту (57 мл, 5.0 М, 280 ммоль) добавили при интенсивном перемешивании с получением значения рН 3 и образованием осадка. Смесь охладили до температуры окружающей среды, осадок отфильтровали, промыли водой и высушили в вакууме при 40°С.
Выход: 7.0 г (98% чистота, 80% от теоретического выхода)
LC-MS (Способ L1): Rt=0.70 мин; MS(ESIpos): m/z=285 [М+Н]+
1H-ЯМР (400 МГц, ДМСО-d6): δ [ppm] = 14.12 (br s, 1H), 9.25 (s, 1H), 8.42 (d, 1H), 8.36 (d, 1H), 7.75 (t, 1H).
Стадия 2
8-бром-4-хлор-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид
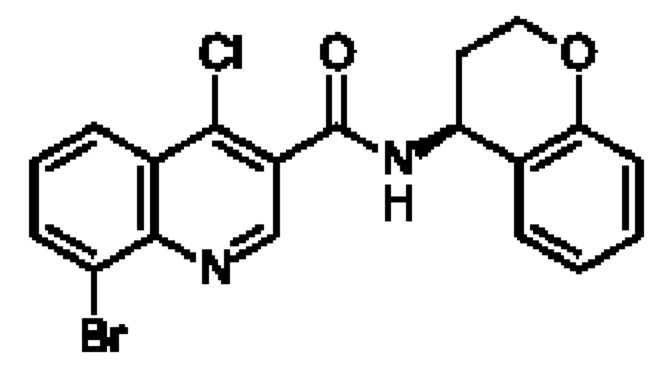
8-Бром-4-хлорхинолин-3-карбоновую кислоту (стадия 1) (7.00 г, 24.4 ммоль) растворили в THF посредством перемешивания на масляной бане 50°С в течение 10 мин. Нагревание прекратили, (4S)-хроман-4-амин гидрохлорид (5.44 г, 29.3 ммоль), N,N-диизопропил-этил-амин (17 мл, 98 ммоль) и раствор 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксида в этилацетате (23 мл, 50% содержание, 39 ммоль) добавили, что вызвало повышение температуры до 45°С. Перемешивание продолжали в течение 30 мин, и воду (300 мл) добавили при непрерывном перемешивании для поддержания осаждения твердого вещества. Осадок собрали, промыли водой и высушили в вакууме.
Выход: 9.50 г (93% от теоретического выхода)
LC-MS (Способ L1): Rt=1.01 мин; MS (ESIneg): m/z=417 [М+Н]-
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 2.047 (0.74), 2.054 (0.99), 2.063 (1.54), 2.070 (1.66), 2.081 (1.85), 2.088 (1.86), 2.097 (2.49), 2.104 (2.18), 2.113 (1.49), 2.120 (1.08), 2.197 (1.06), 2.206 (1.61), 2.218 (2.41), 2.231 (2.17), 2.239 (2.10), 2.252 (1.56), 2.264 (1.01), 2.273 (0.71), 2.328 (0.42), 2.670 (0.47), 4.205 (1.18), 4.212 (1.43), 4.233 (3.76), 4.240 (2.80), 4.253 (3.08), 4.261 (2.42), 4.277 (2.42), 4.285 (3.12), 4.293 (2.75), 4.302 (3.10), 4.313 (1.33), 4.321 (1.40), 4.329 (1.04), 5.266 (1.51), 5.281 (3.35), 5.300 (3.35), 5.315 (1.47), 6.793 (5.60), 6.814 (6.35), 6.922 (2.99), 6.940 (6.44), 6.959 (3.78), 7.162 (3.04), 7.165 (3.11), 7.183 (5.15), 7.201 (2.48), 7.382 (5.42), 7.401 (5.04), 7.713(4.62), 7.733 (8.03), 7.754 (5.29), 8.312 (6.79), 8.324 (8.26), 8.327 (8.69), 8.345 (6.64), 9.042 (16.00), 9.264 (4.77), 9.285 (4.67).
Стадия 3
8-бром-N-[(4S)-3,4-дигидро-2H-хромен-4-ил]-4-(морфолин-4-ил)хинолин-3-карбоксамид
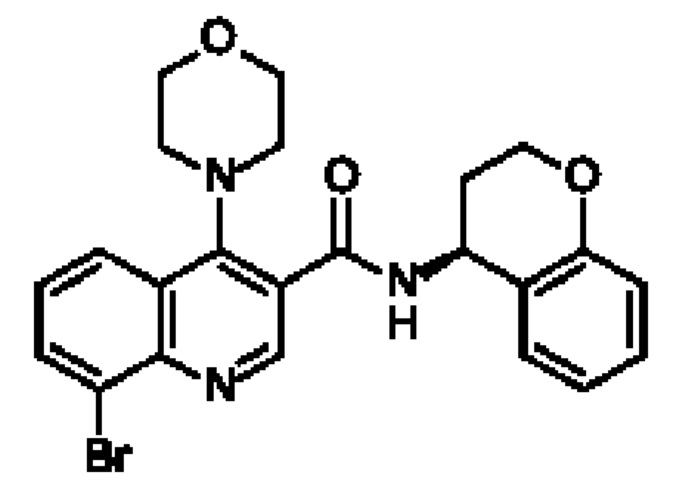
К суспензии 8-бром-4-хлор-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (стадия 2) (9.50 г, 22.7 ммоль) в THF (70 мл), морфолин (6.0 мл, 68 ммоль) и 1,4-диаза6ицикло[2.2.2]октан (2.55 г, 22.7 ммоль) добавили и перемешивали в течение 1.5 ч при температуре бани 80°С. Воду добавили (30 мл), и THF выпарили при пониженном давлении. Больше воды добавили, и суспензию перемешивали сначала при 50°С и затем при температуре окружающей среды. Осадок отфильтровали, промыли водой и высушили в вакууме.
Выход: 10.5 г (98% от теоретического выхода)
LC-MS (Способ L1): Rt=0.92 мин; MS (ESIneg): m/z=466 [M-H]-
1Н-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.149 (0.41), -0.008 (4.42), 0.008 (3.18), 2.041 (0.54), 2.048 (0.76), 2.056 (1.13), 2.063 (1.19), 2.076 (1.30), 2.091 (1.80), 2.098 (1.57), 2.106 (1.11), 2.197 (0.74), 2.206 (1.17), 2.218 (1.70), 2.231 (1.59), 2.240 (1.58), 2.253 (1.13), 2.262 (0.74), 2.274 (0.52), 2.327 (0.60), 2.366 (0.49), 2.523 (2.30), 2.669 (0.66), 2.710 (0.48), 3.217 (0.69), 3.228 (1.18), 3.248 (4.71), 3.258 (11.00), 3.269 (11.28), 3.279 (5.00), 3.842 (8.92), 3.853 (14.13), 3.864 (8.07), 4.214 (0.80), 4.221 (1.01), 4.242 (2.68), 4.249 (2.03), 4.263 (2.41), 4.271 (2.08), 4.276 (2.00), 4.286 (2.44), 4.293 (2.07), 4.302 (2.18), 4.314 (0.86), 4.321 (0.96), 4.329 (0.65), 5.245 (1.10), 5.259 (2.45), 5.279 (2.44), 5.292 (1.06), 6.797 (4.29), 6.815 (4.84), 6.927 (2.26), 6.929 (2.16), 6.946 (4.75), 6.964 (2.87), 7.164 (2.33), 7.167 (2.40), 7.185 (3.85), 7.202 (1.91), 7.206 (1.79), 7.385 (4.05), 7.403 (3.77), 7.499 (3.74), 7.518 (5.40), 7.538 (4.06), 8.123 (4.80), 8.125 (5.04), 8.142 (4.71), 8.144 (4.51), 8.197 (4.92), 8.199 (4.64), 8.218 (4.71), 8.753 (16.00), 9.177 (3.99), 9.197 (3.89).
Стадия 4
8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(морфолин-4-ил)хинолин-3-карбоксамид (пример 52)
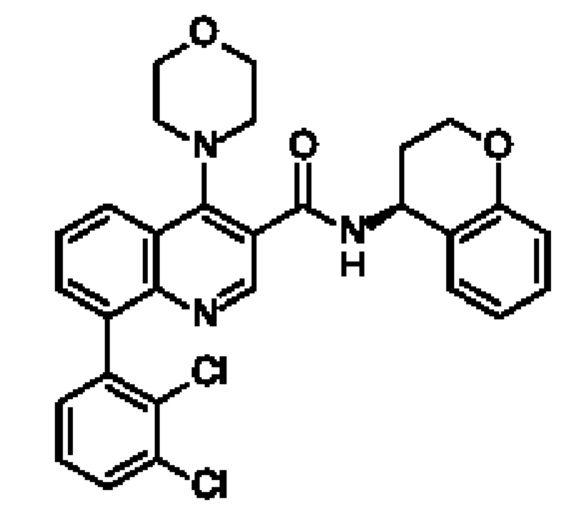
В атмосфере аргона карбонат калия (1.29 г, 9.31 ммоль) растворили в дегазированной 5:1 смеси диоксана и воды (21 мл) посредством обработки ультразвуком. 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (190 мг, 0.23 ммоль) и 8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(морфолин-4-ил)хинолин-3-карбоксамид (стадия 3) (2.18 г, 4.65 ммоль) добавили, а затем 2,3-бензолбороновую кислоту (977 мг, 5.12 ммоль). Сосуд закрыли и перемешивали при температуре бани 80°С в течение 2.5 ч. Воду добавили, и смесь экстрагировали этилацетатом. Органические фазы высушили, и выпарили при пониженном давлении. Остаток очистили посредством колоночной хроматографии на силикагеле (10 г), элюент: циклогексан / этилацетат (15-35%). Полученное твердое вещество перемешали в смеси МТВЕ (30 мл) и метанола (1.5 мл), отфильтровали и высушили в вакууме.
Выход: 2.03 г (82% от теоретического выхода)
LC-MS (Способ L1): Rt=1.13 мин; MS (ESIpos): m/z=534 [M+H]+
1H-ЯМР Перечень пиков (600 МГц, ДМСО-d6) δ [ppm]: 2.056 (0.40), 2.199 (0.43), 2.208 (0.44), 2.214 (0.44), 3.269 (0.65), 3.280 (1.04), 3.289 (1.15), 3.300 (1.36), 3.307 (1.17), 3.321 (0.61), 3.335 (16.00), 4.233 (0.78), 4.237 (0.53), 4.247 (0.59), 4.251 (0.49), 4.261 (0.49), 4.267 (0.62), 4.272 (0.54), 4.278 (0.63), 5.239 (0.42), 5.246 (0.54), 5.260 (0.42), 6.781 (1.24), 6.794 (1.32), 6.911 (0.70), 6.915 (0.74), 6.928 (0.40), 7.150 (0.59), 7.162 (0.96), 7.175 (0.49), 7.310 (0.47), 7.312 (0.47), 7.323 (0.59), 7.324 (0.57), 7.336 (0.53), 7.338 (0.53), 7.348 (0.71), 7.350 (0.72), 7.357 (1.04), 7.370 (0.95), 7.420 (0.46), 7.432 (1.04), 7.445 (1.07), 7.457 (0.42), 7.664 (0.76), 7.676 (1.51), 7.690 (2.57), 7.693 (1.60), 7.704 (2.49), 7.716 (0.68), 8.281 (1.15), 8.283 (1.14), 8.295 (1.07), 8.297 (1.02), 8.588 (1.70), 8.595 (1.82), 9.166 (0.54), 9.180 (1.03), 9.195 (0.56).
Синтез 8-(3-хлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-7-фторхинолин-3-карбоксамида (пример 141).
Стадия 1
этил 8-бром-7-фтор-7-гидроксихинолин-3-карбоксилат
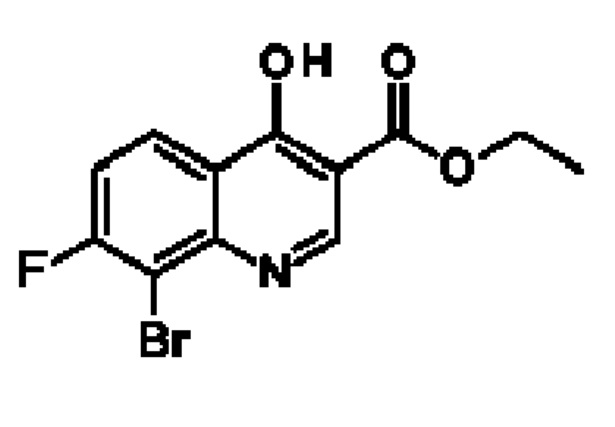
Смесь 2-бром-3-фторанилина (24.89 г, 131 ммоль) и диэтилэтоксиметиленмалоната (28.33 г, 131 ммоль, 26 мл) перемешивали при комнатной температуре в течение 16 ч. Перемешивание продолжали при 250°С под вакуумом (60 мбар) в течение 6 ч. Реакционной смеси позволили охладиться до комнатной температуры. Твердый осадок перемешали в нагреваемом до возврата флегмы этилацетате (400 мл). Осадок отфильтровали и промыли этилацетатом. Твердое вещество перемешали в нагреваемой до возврата флегмы смеси этанола (400 мл) и метанола (40 мл). Горячую суспензию отфильтровали. Твердое вещество промыли этанолом и высушили на воздухе.
Выход: 28.60 г (83 ммоль, 63% от теоретического выхода)
LC-MS (Способ L2): Rt=1.73 мин, m/z=314/316 (М+Н)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 11.78 (s, 1H), 8.45 (s, 1H), 8.22 (m, 1H), 7.50-7.39 (m, 1H), 4.23 (d, J=7.1 Гц, 2Н), 1.28 (t, J=7.1 Гц, 3Н).
Стадия 2
этил 8-бром-4-хлор-7-фторхинолин-3-карбоксилат
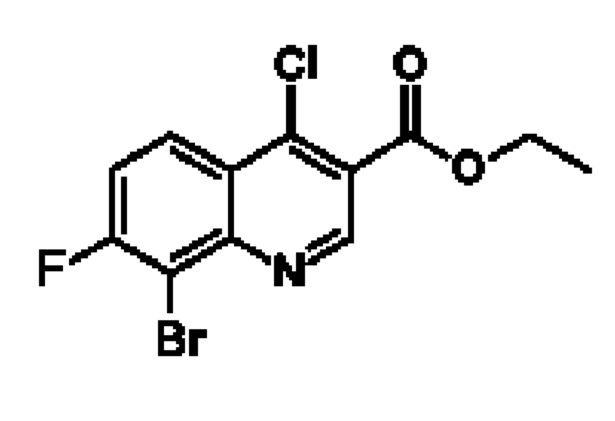
К перемешиваемому оксихлориду фосфора (38.4 г, 250 ммоль, 23 мл) добавили этил 8-бром-7-фтор-4-гидроксихинолин-3-карбоксилат (стадия 1) (23.6 г, 75 ммоль). Полученную суспензию перемешивали при 80°С в течение 1 ч. Смеси позволили охладиться до комнатной температуры и перелили в интенсивно перемешиваемую ледяную воду (100 мл). Полученную смесь оставили отстаиваться на два дня при комнатной температуре. Осадок собрали посредством фильтрации и промыли водой до получения нейтрального фильтрата. Твердые вещества растерли в порошок в смеси диэтилового простого эфира и диизопропилового простого эфира (1:1; 1 л). Твердые вещества отфильтровали. Фильтрат концентрировали в вакууме при 25°С. После совместного выпаривания остатка с толуолом 21.3 г (64 ммоль, 85% от теоретического выхода) указанного в заглавии соединения получили.
Выход: 21.3 г (64 ммоль, 85% от теоретического выхода)
LC-MS (Способ L2): Rt=2.18 мин, m/z=332/334 (М+Н)+
Стадия 3
этил 8-бром-4-(диметиламино)-7-фторхинолин-3-карбоксилат
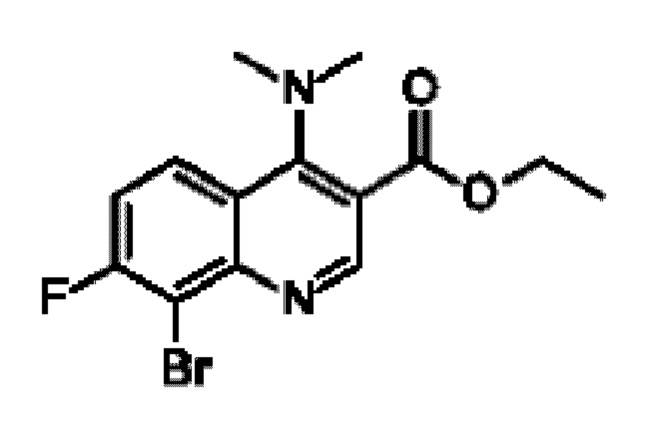
К раствору этил 8-бром-4-хлор-7-фторхинолин-3-карбоксилата (стадия 2) (14.31 г, 43 ммоль) в сухом тетрагидрофуране (150 мл) добавили триэтиламин (8.71 г, 86 ммоль, 12 мл) и диметиламин (2 M в тетрагидрофуране; 48 ммоль, 24 мл). Реакционную смесь перемешивали в течение 16 ч при комнатной температуре. Твердые вещества отфильтровали и промыли тетрагидрофураном. Фильтрат концентрировали в вакууме с получением указанного в названии соединения.
Выход: 12.66 г (37 ммоль, 86% от теоретического выхода)
LC-MS (Способ L2): Rt=1.75 мин, m/z=341/343 (М+Н)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 8.86 (s, 1Н), 8.28 (dd, J=9.4, 6.1 Гц, 1Н),7.63 (dd, J=9.4, 8.2 Гц, 1H),4.39 (q, J=7.1 Гц, 2Н), 3.07 (s, 6Н), 1.36 (t, J=7.1 Гц, 3Н).
Стадия 4
этил 8-бром-4-(диметиламино)-7-фторхинолин-3-карбоксилат гидрохлорид
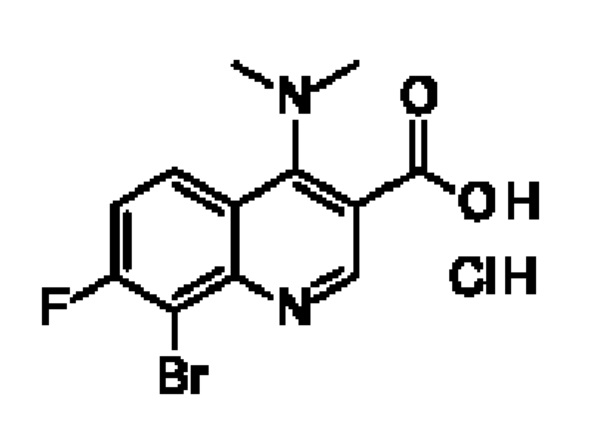
К раствору этил 8-бром-4-(диметиламино)-7-фторхинолин-3-карбоксилата (стадия 3) (14.0 г, 41 ммоль) в тетрагидрофуране (100 мл) добавили раствор моногидрат гидроксида лития (11.5 г, 274 ммоль) в воде (100 мл). Смесь перемешивали в течение 16 ч при 75°С и позволили охладиться до комнатной температуры. Слои разделил, и водный слой экстрагировали тетрагидрофураном (2×150 мл). Объединенные органические слои концентрировали в вакууме, и соляную кислоту (4 М; 100 мл) добавили. Твердое вещество отфильтровали, промыли водой и диэтиловым простым эфиром и высушили на воздухе с получением указанного в названии соединения.
Выход: 10.6 г (30 ммоль, 74% от теоретического выхода)
LC-MS (Способ L2): Rt=1.21 мин, m/z=313/315 (М+Н)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 8.73 (s, 1Н), 8.41 (dd, J=9.4, 5.7 Гц, 1Н), 7.66 (dd, J=9.4, 8.1 Гц, 1Н), 3.35 (s, 6Н) [кислотные протоны не были обнаружены].
Стадия 5
8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-7-фторхинолин-3-карбокеамид
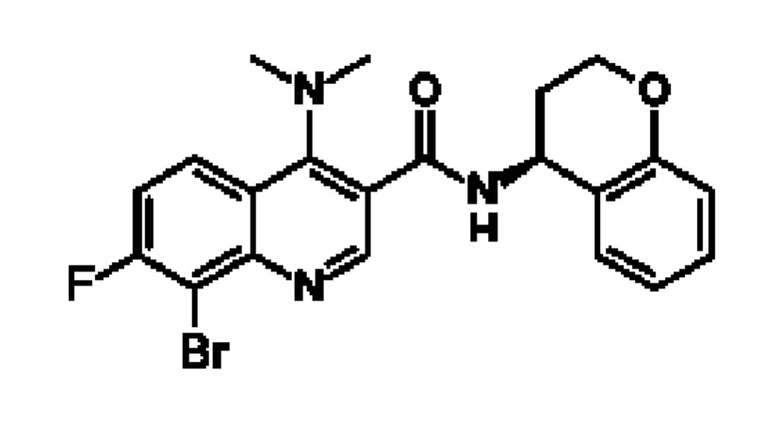
К раствору 8-6ром-4-(диметиламино)-7-фторхинолин-3-карбоновой кислоты гидрохлориду (стадия 4) (2.00 г, 5.7 ммоль) в N,N-диметилформамиде (50 мл) добавили 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфат (2.18 г, 5.7 ммоль) и N,N-диизопропилэтиламин (4.21 г, 32.6 ммоль, 5.7 мл). Смесь перемешивали при комнатной температуре в течение 1 ч. (4S)-Хроман-4-амингидрохлорид (1.06 г, 5.7 ммоль) добавили. Реакционную смесь перемешивали в течение 16 ч при комнатной температуре. Смесь перелили в воду (200 мл). Твердые вещества отфильтровали, промыли водой и высушили в вакууме. После совместного выпаривания с толуолом и этил ацетатом получили указанное в названии соединение.
Выход: 1.90 г (4.3 ммоль, 75% от теоретического выхода)
LC-MS (Способ L2): Rt=1.78 мин, m/z=444/446 (М+Н)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 9.12 (d, J=8.1 Гц, 1H), 8.70 (s, 1H), 8.23 (dd, J=9.4, 6.1 Гц, 1H), 7.59 (dd, J=9.3, 8.3 Гц, 1H),7.37 (d, J=6.8 Гц, 1Н), 7.22-7.14 (m, 1Н), 6.98-6.90 (m, 1H), 6.81 (dd, J=8.2, 1.0 Гц, 1Н), 5.29-5.20 (m, 1Н), 4.34-4.19 (m, 2Н), 3.06 (s, 6Н), 2.27-2.15 (m, 1Н), 2.11-2.00 (m, 1Н).
Стадия 6
8-(3-хлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметил-амино)-7-фторхинолин-3-карбоксамид (пример 141)
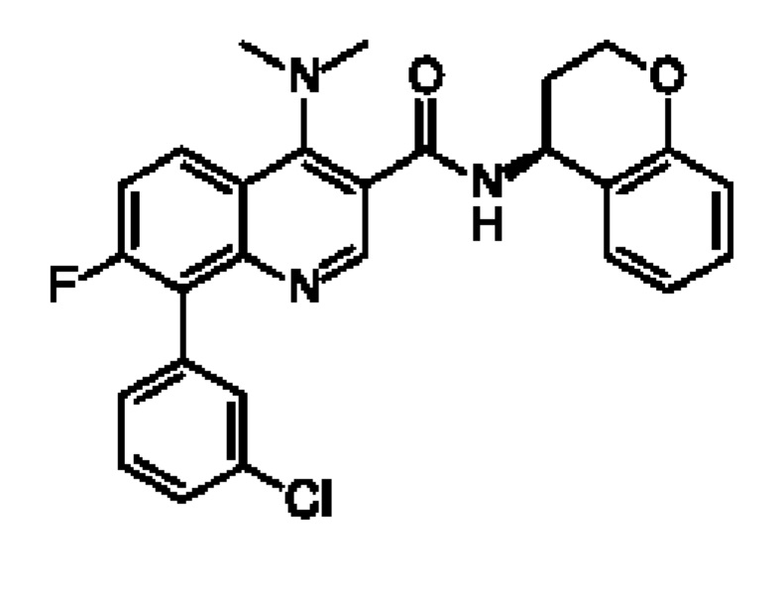
В сосуде с закручивающейся крышкой, объемом 8 мл, к дегазированной (1 мин, азот) смеси 8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-7-фторхинолин-3-карбоксамида (100 мг, 0.225 ммоль), (3-хлорфенил)бороновой кислоты (42 мг, 0.270 ммоль) и карбоната натрия (72 мг, 0.675 ммоль) в смеси тетрагидрофурана (1.30 мл) и воды (0.25 мл) добавили 1,1'-бис(дифенилфосфино)ферроценпалладия(II) дихлорид (3 мг, 0.005 ммоль). Реакционную смесь перемешивали в течение 16 ч при 60°С и охладили до комнатной температуры. Воду (5 мл) добавили, и водный слой экстрагировали дихлорметаном (3×3 мл) посредством фазового разделителя. Растворители удалили в вакууме. Очистка посредством колоночной флэш-хроматографии (гептан, 5%-35% этилацетат) обеспечила указанные в названии соединения.
Выход: 56 мг (0.118 ммоль, 52% от теоретического выхода)
LC-MS (Способ L2): Rt=3.03 мин, m/z=476 (M+H)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 9.08 (d, J=8.2 Гц, 1Н), 8.58 (s, 1Н), 8.27 (dd, J=9.4, 6.2 Гц, 1Н), 7.60 (t, J=9.3 Гц, 1Н), 7.55-7.45 (m, 3Н), 7.43-7.31 (m, 2Н), 7.20-7.12 (m, 1Н), 6.95-6.88 (m, 1H), 6.83-6.76 (m, 1H), 5.28-5.19 (m, 1H), 4.32-4.19 (m, 2H), 3.07 (s, 6H), 2.25-2.14 (m, 1H), 2.09-1.98 (m, 1H).
Синтез 8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоксамида (пример 331).
Стадия 1
этил 8-бром-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоксилат
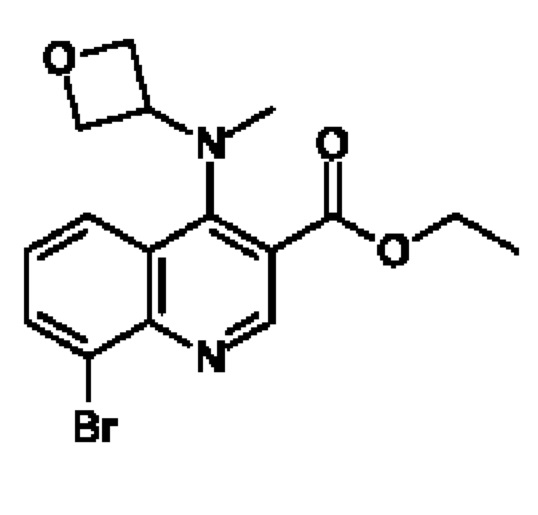
В колбу загрузили этил 8-бром-4-хлорхинолин-3-карбоксилат (1.26 г, 4 ммоль) (Zask, al. Bioorganic и Medicinal Chemistry Letters, 2003, 1487-1490; Laxmikant, al. US 2013/210844), 1-метил-3-оксетанамин (0.42 г, 4 ммоль), N,N-диизопропилэтиламин (0.62 г, 4.8 ммоль) в 40 мл ацетонитрила. Реакционную смесь нагревали с возвратом флегмы в течение 24 часов. Затем растворитель удалили при пониженном давлении, и оставшееся вещество растворили в этил ацетате и дважды промыли водой. Органическую фазу отделили, высушили над сульфатом кальция, отфильтровали, и фильтрат удалили при пониженном давлении. Полученный остаток очистили посредством колоночной хроматографии с обращенной фазой (элюент вода / ацетонитрил градиент).
Выход: 1.2 г (3.2 ммоль, 82% от теоретического выхода)
1Н-ЯМР (400 МГц, ДМСО-d6) δ 8.94 (s, 1Н), 8.20 (d, 1Н), 8.14 (d, 1Н), 7.55 (dd, 1H), 4.72-4.62 (m, 5H, оксетаннл), 4.43-4.38 (q, 2H),3.10 (s,3H), 1.37 (t, 3H).
Стадия 2
этил 8-(2,3-дихлорфенил)-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоксилат
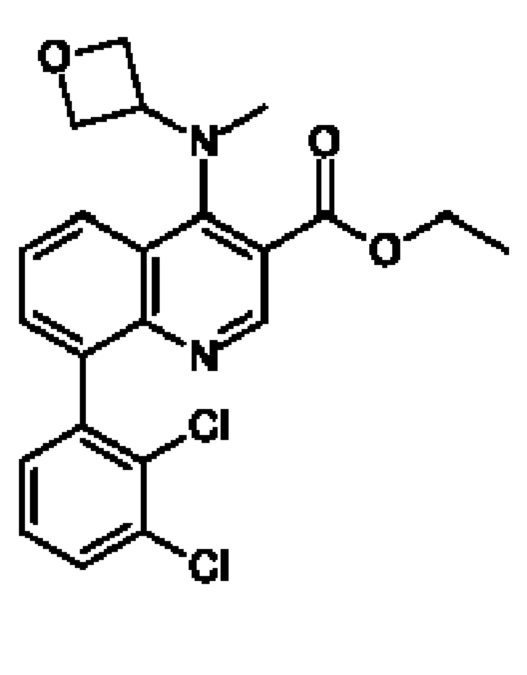
В сосуде, подходящем для обработки микроволнами, к дегазированной (1 мин, аргон) смеси этил 8-бром-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоксилата (стадия 1) (500 мг, 1.37 ммоль), (2,3-дихлорфенил)бороновой кислоты (261 мг, 1.37 ммоль), водного раствора карбоната цезия (2 М, 1.37 мл, 2.74 ммоль) и диоксана (12.5 мл) добавили 1,1'-бис(дифенилфосфино)ферроценпалладия(II) дихлорид (111 мг, 0.14 ммоль). Реакционную смесь обработали в микроволновой печи Biotage в течение 25 минут при 100°С. Реакционную смесь отфильтровали через картридж сульфат натрия / силикагель и очистили посредством обращеннофазовой колоночной хроматографии (элюент вода / ацетонитрила градиент).
Выход: 600 мг (98% от теоретического выхода)
1H-ЯМР (400 МГц, ДМСО-d6) δ 8.77 (s, 1Н), 8.21 (t, 1Н), 7.74 (d, 2Н), 7.71 (d, 1Н), 7.45 (t, 1Н), 7.36 (d, 1Н), 4.76-4.65 (m, 5Н, оксетанил), 4.40-4.34 (q, 2Н), 3.14 (s, 3Н), 1.34 (t, 3Н).
Стадия 3
8-(2,3-дихлорфенил)-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоновая кислота
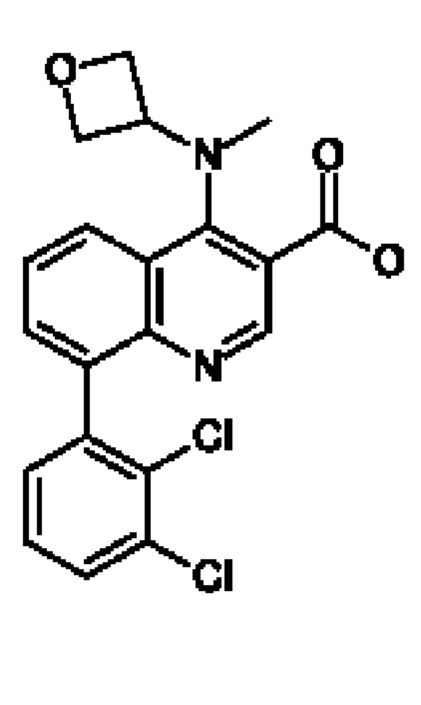
Этил 8-(2,3-дихлорфени)-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоксилат (стадия 2) (580 мг, 1.34 ммоль) растворили в 20 мл диоксана и смешали с LiOH (35.4 мг, 1.48 ммоль) в 5 мл воды. Реакционную смесь нагревали в течение 16 часов при 60°С. Диоксан удалили при пониженном давлении, оставшийся раствор получили в смеси этил ацетата и воды. Водную фазу отделили и обработали 1H HCl до рН 5. Этот подкисленный раствор дважды экстрагировали этил ацетатом, объединенные экстракты высушили, отфильтровали, и растворитель удалили при пониженном давлении. Полученное соединение применяли на следующей стадии без дальнейшей очистки.
Выход: 570 мг (99% от теоретического выхода)
1H-ЯМР (400 МГц, ДМСО-d6) δ 12.00 (bs, 1H, СООН), 8.73 (s, 1Н), 8.24-8.22 (dd, 1Н), 7.23-7.68 (m, 3Н), 7.44 (t, 1Н), 7.37-7.35 (dd, 1Н), 4.76-4.65 (m, 5Н, оксетанил), 3.13 (s, 3Н).
Стадия 4
8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-[метил(оксетан-3-ил)амино]-хинолин-3-карбоксамид (пример 331)
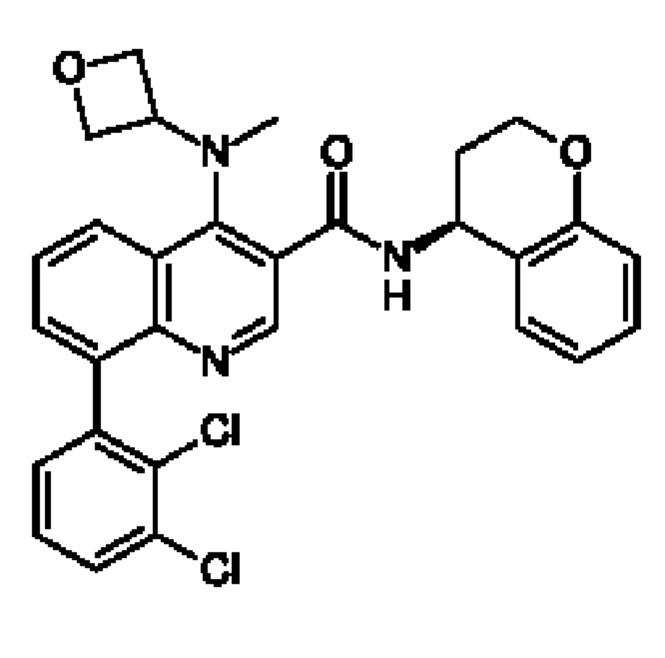
В колбу загрузили 8-(2,3-дихлорфенил)-4-[метил(оксетан-3-ил)амино]хинолин-3-карбоновую кислоту (стадия 3) (260 мг, 0.645 ммоль), (4S)-хроман-4-амин гидрохлорид (131.7 мг, 0.71 ммоль), N,N-диизопропил этиламин (250 мг, 1.93 ммоль), 4-(N,N-диметиламино)пиридин (39.4 мг, 0.32 ммоль), 1-гидрокси-1Н-бензотриазол (43.5 мг, 0.32 ммоль) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (123.6 мг, 0.645 ммоль) в 10 мл дихлорметана. Реакционную смесь перемешивали при температуре окружающей среды всю ночь, затем смешали с водой, фазу дихлорметана отделили, высушили с помощью картриджа сульфат натрия / силикат ель, и растворитель удалили при пониженном давлении. Остаток очистили посредством обращеннофазовой колоночной хроматографии (элюент вода / ацетонитрила градиент) с получением указанного в названии соединения
Выход: 130 мг (0.24 ммоль, 37% от теоретического выхода)
1H-ЯМР Перечень пиков (399,9532 МГц, ДМСО): δ=9.1403 (1.94); 9.1288 (2); 9.1208 (2.32); 9.1103 (1.85); 8.6012 (10.54); 8.4715 (0.58); 8.3155 (1.57); 8.2143 (2.25); 8.1975 (2.56); 8.1729 (1.06); 7.7323 (2.07); 7.7127 (5.31); 7.6894 (10.46); 7.6737 (1.95); 7.4635 (1.67); 7.4521 (1.74); 7.4433 (2.94); 7.4332 (2.77); 7.4235 (2.08); 7.4143 (1.65); 7.3824 (1.86); 7.3618 (4.63); 7.3428 (4.44); 7.3225 (1.63); 7.1895 (1.81); 7.171 (3.64); 7.1535 (2.27); 6.9433 (2.6); 6.9255 (4.32); 6.9084 (2.02); 6.8059 (4.77); 6.7848 (4.45); 6.5782 (0.9); 5.2488 (1.97); 5.237 (2); 4.725 (1.91); 4.697 (7.04); 4.6722 (5.48); 4.6575 (5.6); 4.5955 (1.22); 4.5844 (1.61); 4.2921 (2.17); 4.2752 (3.94); 4.2675 (3.64); 4.2552 (2.23); 4.2471 (2.41); 4.2281 (0.89); 3.3183 (319.34); 3.2701 (0.87); 3.2496 (0.61); 3.1747 (0.71); 3.081 (16); 3.0759 (15.54); 2.9497 (1.08); 2.6703 (8.96); 2.5893 (0.63); 2.5051 (1239.6); 2.5012 (1583.24); 2.4971 (1204.24); 2.3276 (9.3); 2.2832 (0.88); 2.2475 (1.34); 2.2286 (1.72); 2.2205 (1.78); 2.1313 (0.96); 2.074 (5.92); 2.0168 (0.96); 1.2694 (0.87); 1.169 (4.47); 1.0034 (0.71); 0.9887 (0.75); 0.1463 (2.93); -0.0001 (642.47); -0.0792 (0.67); -0.1497 (3.13); -3.3083 (0.55).
Синтез 8-(3,5-дихлорфенил)-N-[(1S)-2,3-дигидро-1Н-инден-1-ил]-4-этоксихинолин-3-кар6оксамида (пример 134).
Стадия 1
8-(3,5-дихлорфенил)-N-[(1S)-2,3-дигидро-1H-инден-1-ил]-4-гидроксихинолин-3-карбоксамид
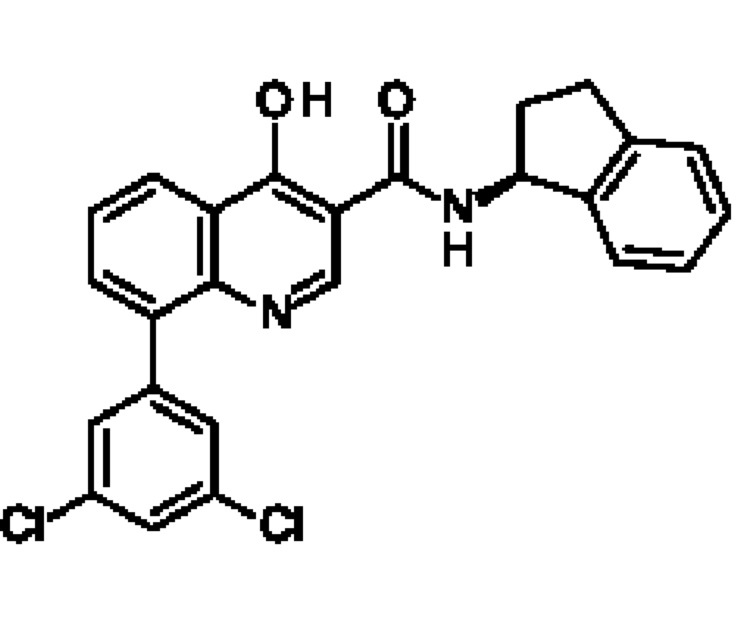
Раствор 8-(3,5-дихлорфенил)-4-гидроксихинолин-3-карбоновой кислоты (5.50 г, 16.5 ммоль) в THF обработали при перемешивании (13)-индан-1-амином (2.5 мл, 20 ммоль) и триметиламином (9.2 мл, 66 ммоль) в течение 10 мин при температуре окружающей среды. Затем раствор 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксида в этилацетате (19.6 мл, 50% содержание, 33 ммоль) добавляли при перемешивании всю ночь при температуре окружающей среды. Воду (100 мл) добавили, и THF выпарили при пониженном давлении. Больше воды и этил ацетата добавили, и смесь очистили посредством фильтрации. Водную фазу экстрагировали этил ацетатом, и объединенные органические фазы высушили и выпарили при пониженном давлении. Осадок очистили посредством колоночной хроматографии на силикагеле (340 г) с циклогексаном / этил ацетатом (15-40%). Две фракции выделили:
Выход: 3.0 г (98% чистота, 40% от теоретического выхода) и 0.69 г (94% чистота, 9% от теоретического выхода)
LC-MS (Способ L1): Rt=1.27 мин; MS (ESIneg): m/z=447 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 1.849 (1.87), 1.868 (2.39), 1.880 (2.59), 1.900 (2.50), 1.921 (1.16), 2.578 (3.74), 2.588 (3.08), 2.841 (1.03), 2.862 (1.82), 2.882 (2.65), 2.902 (3.54), 2.922 (2.00), 2.977 (2.56), 2.990 (2.71), 2.999 (2.71), 3.029 (1.74), 5.474 (1.16), 5.493 (3.52), 5.512 (3.77), 5.531 (1.67), 7.197 (1.27), 7.214 (3.91), 7.233 (6.17), 7.256 (5.56), 7.280 (7.00), 7.298 (9.89), 7.316 (4.52), 7.521 (2.83), 7.540 (5.61), 7.560 (4.06), 7.626 (14.53), 7.631 (16.00), 7.695 (5.87), 7.713 (5.06), 7.804 (5.42), 8.297 (4.58), 8.318 (4.68), 8.611 (4.35), 8.624 (4.69), 10.285 (4.44), 10.304 (4.72), 11.637 (3.53).
Стадия 2
8-(3,5-дихлорфенил)-N-[(1S)-2,3-дигидро-1H-инден-1-ил]-4-этоксихинолин-3-карбоксамид (пример 134)
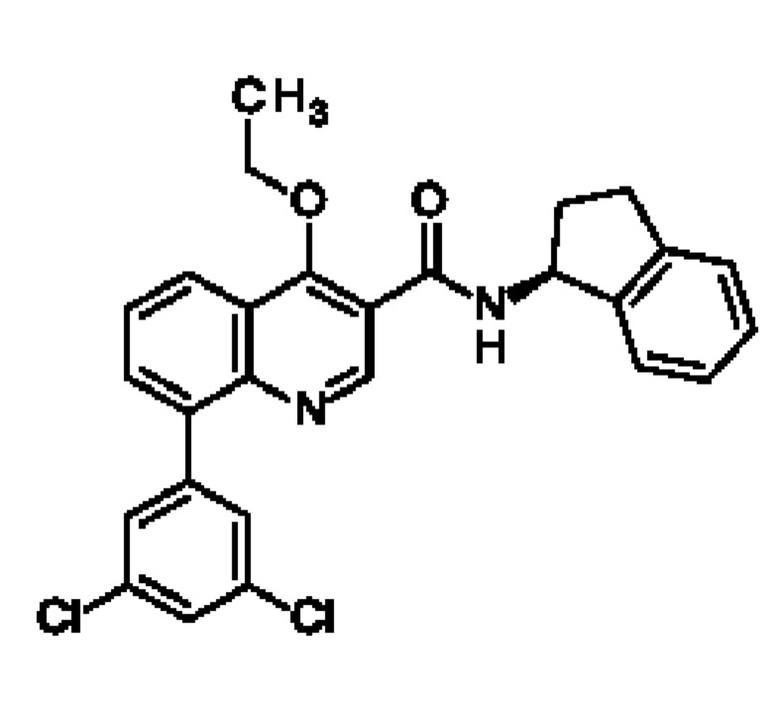
8-(3,5-дихлорфенил)-N-[(1S)-2,3-дигидро-1H-инден-1-ил]-4-гидроксихинолин-3-карбоксамид (стадия 1) (70.0 мг, 156 мкмоль), этанол (27 мкмл, 470 мкмоль), трифенилфосфин (61.3 мг, 234 мкмоль) и диизопропил-(E)-диазен-1,2-дикарбоксилат (46 мкмл, 230 мкмоль) перемешали в THF (1 мл) при температуре окружающей среды в течение 6 ч. 5 М муравьиную кислоту (93 мкмл, 470 мкмоль) добавили, растворитель выпарили, и остаток очистили посредством препаративной ВЭЖХ (CIS, градиент: 0.1% вод. муравьиная кислота/ ацетонитрил).
Выход: 40 мг (92% чистота, 49% от теоретического выхода)
LC-MS (Способ L7): Rt=2.60 мин; MS (ESIpos): m/z=477 [М+Н]+
1H-ЯМР (Перечень пиков) (500 МГц, ДМСО-d6) δ [ppm]: -0.007 (4.15), 0.007 (3.67), 1.235 (1.26), 1.395 (7.56), 1.409 (16.00), 1.423 (7.72), 1.950 (1.18), 1.966 (1.28), 1.975 (1.34), 1.991 (1.30), 2.522 (1.98), 2.853 (1.24), 2.869 (1.51), 2.885 (1.92), 2.901 (0.85), 2.981 (1.03), 2.989 (1.09), 2.999 (1.11), 3.006 (1.07), 3.013 (0.81), 3.286 (5.84), 4.352 (1.51), 4.354 (1.53), 4.366 (4.56), 4.368 (4.83), 4.380 (4.46), 4.383 (4.79), 4.394 (1.38), 4.396 (1.51), 5.533 (0.78), 5.549 (2.29), 5.564 (2.27), 5.580 (0.78), 5.754 (0.91), 7.227 (2.02), 7.231 (3.49), 7.238 (4.46), 7.245 (4.52), 7.249 (3.34), 7.260 (1.11), 7.278 (2.99), 7.290 (1.65), 7.294 (1.20), 7.400 (2.19), 7.406 (2.33), 7.417 (2.00), 7.654 (2.35), 7.658 (5.35), 7.661 (4.98), 7.674 (15.77), 7.678 (10.55), 7.714 (2.52), 7.729 (3.39), 7.731 (3.32), 7.745 (2.97), 7.889 (3.47), 7.891 (3.80), 7.903 (3.01), 7.906 (3.03), 8.304 (3.32), 8.307 (3.57), 8.321 (3.16), 8.324 (3.16), 8.842 (11.93), 8.998 (2.83), 9.015 (2.77).
Синтез 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-этилхинолин-3-карбоксамида (пример 350).
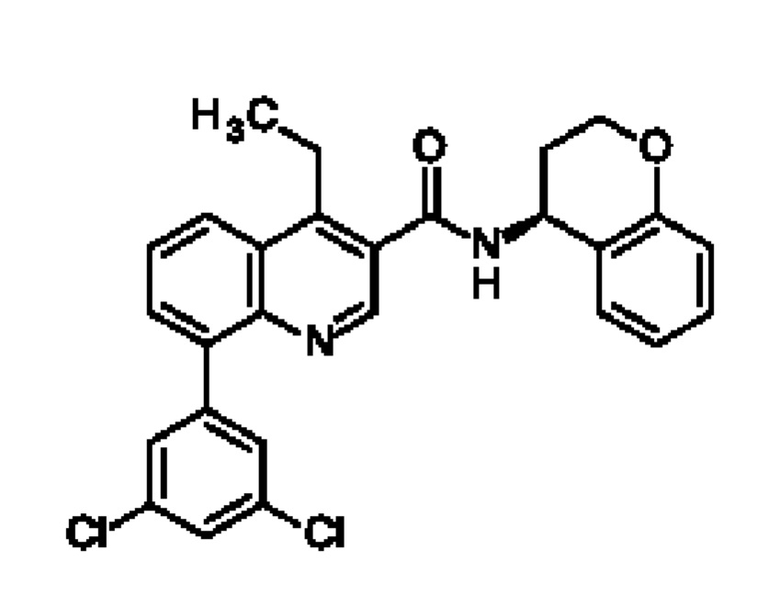
Раствор диэтилцинка в гептане (400 мкмл, 1.0 М, 400 мкмоль) добавили по каплям к смеси 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (стадия 4, пример 4) (97 мг, 200 мкмоль) и 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекса (32.7 мг, 40.0 мкмоль) в диоксане (2 мл) и перемешивали при 90°С всю ночь в атмосфере аргона. 5 М муравьиную кислоту (160 мкмл, 5.0 М, 800 мкмоль) и ДМСО (1 мл) добавили, и отфильтрованную смесь очистили дважды посредством препаративной ВЭЖХ (CIS, градиент: 0.1% вод. муравьиная кислота/ ацетонитрил).
Выход: 52 мг (98% чистота, 53% от теоретического выхода)
LC-MS (Способ L1): Rt=1.35 мин; MS (ESIpos): m/z=477 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 1.303 (2.43), 1.322 (5.61), 1.341 (2.50), 3.252 (2.09), 3.271 (2.06), 4.250 (1.06), 4.259 (1.62), 4.268 (1.95), 4.275 (1.54), 4.284 (1.06), 5.305 (0.92), 5.325 (0.92), 6.783 (1.53), 6.785 (1.66), 6.803 (1.75), 6.806 (1.83), 6.911 (0.78), 6.914 (0.83), 6.930 (1.72), 6.932 (1.71), 6.948 (1.03), 6.951 (1.00), 7.149 (0.86), 7.153 (0.89), 7.170 (1.43), 7.350 (1.48), 7.370 (1.41), 7.652 (16.00), 7.752 (1.09), 7.770 (1.68), 7.791 (1.47), 7.871 (1.93), 7.874 (2.04), 7.889 (1.44), 7.892 (1.42), 8.319 (1.50), 8.322 (1.58), 8.340 (1.43), 8.343 (1.39), 8.839 (5.77), 9.102 (1.60), 9.123 (1.55).
Выделение 8-(3-хлор-5-этилфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-этилхинолин-3-карбоксамида (пример 351).
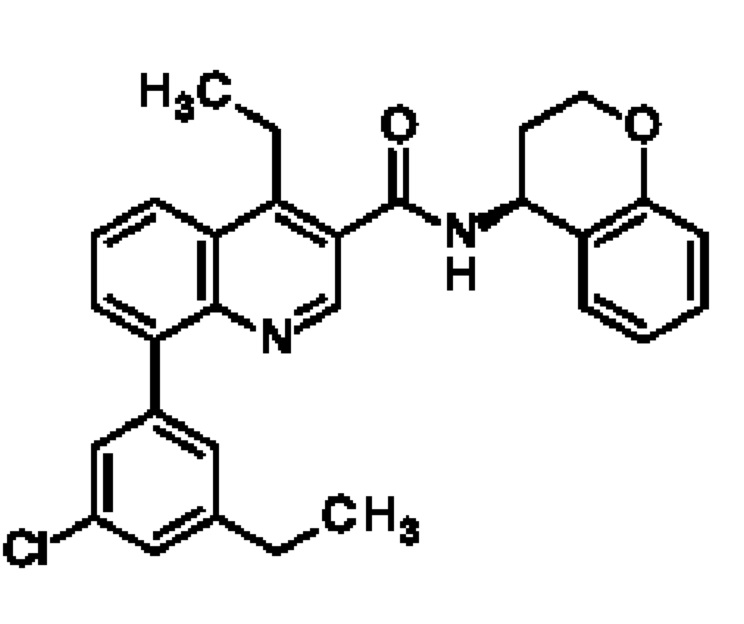
Отделение посредством препративной ВЭЖХ, описанное в примере 350, дало указанное в заглавии соединение в качестве побочного продукта.
Выход: 12 мг (100% чистота, 13% от теоретического выхода)
LC-MS (Способ L1): Rt=1.36 мин; MS (ESIpos): m/z=471 [М+Н]+
1H-ЯМР (400 МГц, ДМСО-d6): δ [ppm]=9.10 (d, 1Н), 8.81 (s, 1Н), 8.29 (dd, 1Н), 7.72-7.83 (m, 2Н), 7.46 (t, 1Н), 7.31-7.40 (m, 3Н), 7.17 (t, 1Н), 6.93 (td, 1Н), 6.79 (dd, 1Н), 5.27-5.35 (m, 1Н), 4.22-4.31 (m, 2Н), 3.21-3.29 (m, 2Н) наслаивается с сигналом воды, 2.64-2.73 (m, 2Н), 2.16-2.26 (m, 1Н), 2.01-2.11 (m, 1Н), 1.32 (t, 3Н), 1.23 (t, 3Н).
Синтез 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(проп-1-ен-2-ил)хинолин-3-карбоксамида (пример 317)
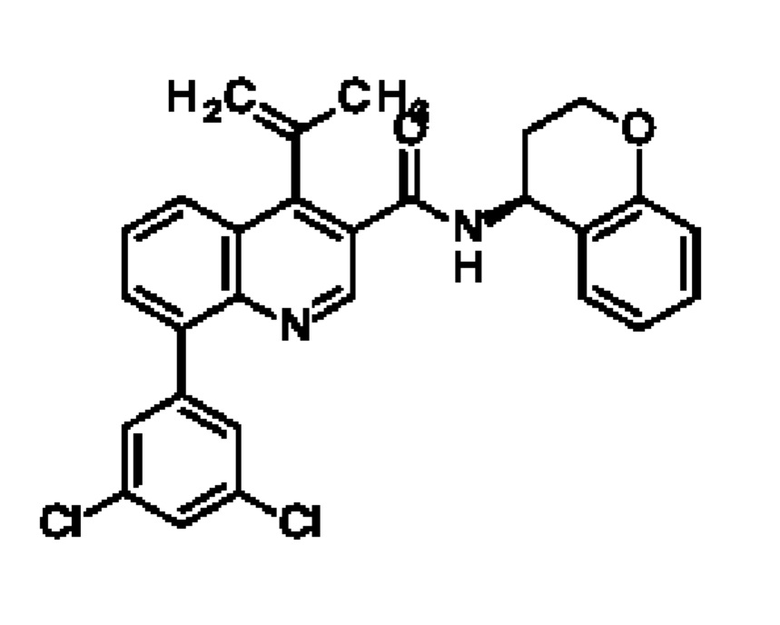
В атмосфере аргона и при непрерывной обработке ультразвуком карбонат калия (571 мг, 4.13 ммоль) растворили в толстостенном сосуде в 5:1 дегазированной смеси диоксана и воды (7.0 мл). 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (84.4 мг, 103 мкмоль) и 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-кар6оксамид (стадия 4, пример 4) (1.00 г, 2.07 ммоль) добавили, а затем 4,4,5,5-тетраметил-2-(проп-1-ен-2-ил)-1,3,2-диоксаборолан (0.49 мл, 4.1 ммоль). Сосуд закрыли, и перемешивали при 80°С в течение 4 ч. 5 М муравьиную кислоту (1.3 мл) и воду добавили и смесь экстрагировали этилацетатом. Органические фазы высушили и выпарили при пониженном давлении. Осадок очистили посредством колоночной хроматографии на силикагеле (50 г, элюент: циклогексан / этил ацетат (7-16%).
Выход: 885 мг (87% от теоретического выхода)
LC-MS (Способ L1): Rt=1.39 мин; MS (ESIpos): m/z=489 [М+Н]+
1H-ЯМР (400МГц, ДМСО-d6): Сдвиг [ppm]=8.88-9.00 (m, 2Н), 8.04 (dd, 1Н), 7.90 (dd, 1Н), 7.76 (dd, 1Н), 7.67 (s, 3Н), 7.32 (br d, 1Н), 7.11-7.22 (m, 1Н), 6.92 (t, 1Н), 6.78 (dd, 1Н), 5.54 (s, 1Н), 5.18-5.30 (m, 1Н), 5.03 (br s, 1Н), 4.16-4.33 (m, 2Н), 2.12-2.26 (m, 4Н), 1.95-2.06 (m, 1Н).
Синтез 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-шопропил-хинолин-3-карбоксамида (пример 359)
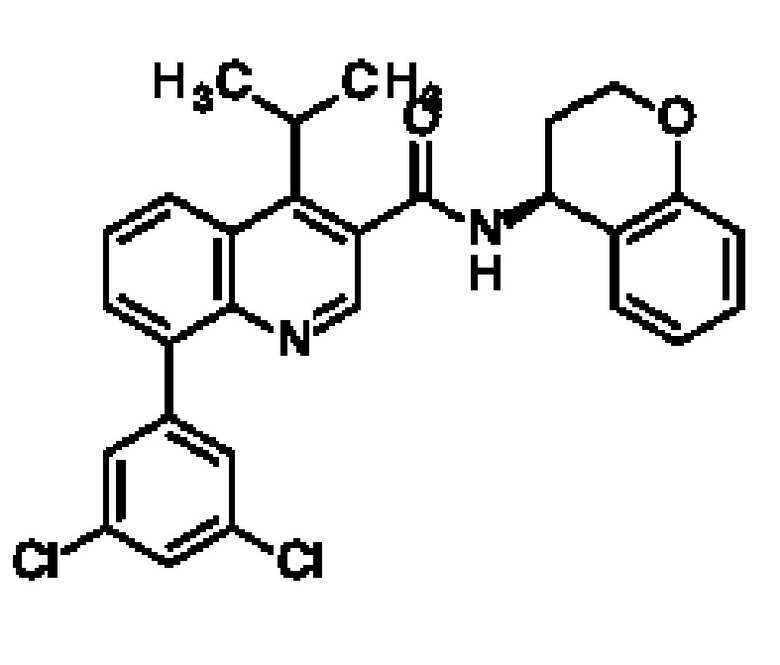
В атмосфере аргона 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(проп-1-ен-2-ил)хинолин-3-карбоксамид (из примера 317) (150 мг, 306 мкмоль) растворили в этилацетате (7 мл) и этаноле (3.5 мл). Pd на активированном угле (44 мг, 10%) добавили, и смесь гидратировали при нормальном давлении при температуре окружающей среды в течение 1.5 ч. Катализатор отфильтровали через целит, промыли смесью этилацетат/этанол (2:1), и фильтрат выпарили при пониженном давлении. Остаток очистили дважды посредством препаративной ВЭЖХ (С 18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил).
Выход: 64 мг (42% от теоретического выхода)
LC-MS (Способ L1): Rt=41 мин; MS (ESIpos): m/z=491 [M+H]+
1H-ЯМР (400 МГц, ДМСО-d6): сдвиг [ppm]=9.12 (d, 1H), 8.76 (s, 1H), 8.45 (d, 1H), 7.85 (d, 1H),7.74 (t, 1Н), 7.61-7.66 (m, 3H), 7.36 (d, 1H), 7.17 (t, 1Н), 6.93 (t, 1H), 6.79 (d, 1Н), 5.25-5.31 (m, 1H), 4.21-4.31 (m, 2H), 3.82-3.92 (m, 1H), 2.21 (td, 1H), 2.06 (ddd, 1H), 1.56 (br d, 3H), 1.53 (br d, 3H).
Синтез этил циано{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}ацетата (пример 354)
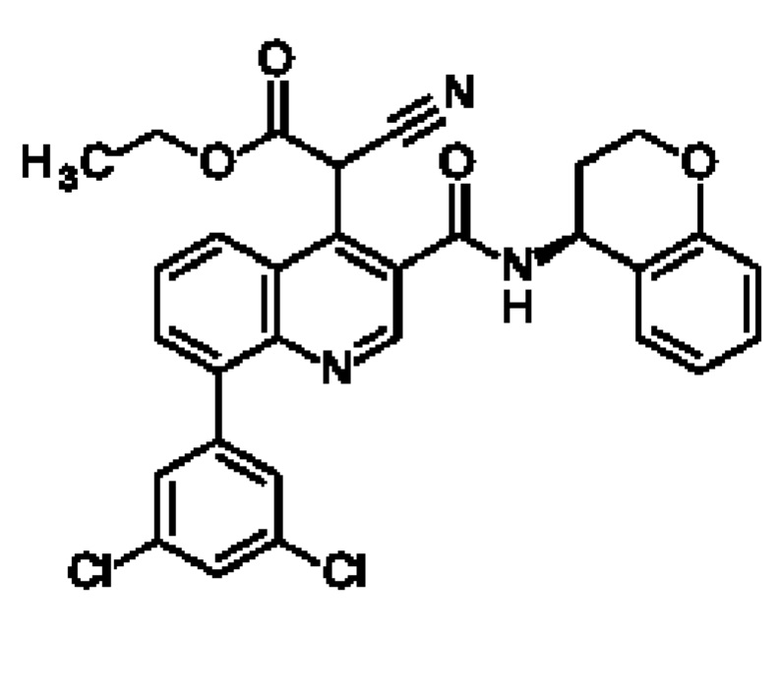
В атмосфере аргона гидрид натрия (165 мг, 60% content, 4.13 ммоль) добавили при 0°С к раствору этил-циан о ацетата (0.44 мл, 4.1 ммоль) в сухом N-метилпирролидоне, перемешивали при температуре окружающей среды в течение 15 мин до прекращения выделения газа. Затем 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (1.00 г, 2.07 ммоль) добавили, и смесь перемешивали при 70°С в течение 3 ч. После охлаждения до температуры окружающей среды 5 М муравьиную кислоту (1.2 мл, 6.2 ммоль) и воду добавили, и смесь экстрагировали два раза этилацетатом. Объединенные органические фазы высушили и выпарили при пониженном давлении. Осадок очистили посредством колоночной хроматографии на силикагеле (100 г) с циклогексаном / этилацетатом (5-50%).
Выход: 650 мг (96% чистота, 54% от теоретического выхода)
LC-MS (Способ L6): Rt=17.46 мин; MS (ESIpos): m/z=560 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (3.55), 0.008 (3.23), 0.146 (0.40), 0.890 (0.44), 1.157 (2.49), 1.175 (7.53), 1.188 (4.41), 1.193 (9.23), 1.205 (8.20), 1.211 (4.25), 1.215 (2.56), 1.223 (4.21), 1.233 (2.01), 1.245 (1.50), 1.250 (2.12), 1.264 (0.77), 1.268 (1.05), 1.988 (9.00), 2.083 (0.45), 2.092 (0.48), 2.104 (0.46), 2.116 (0.65), 2.129 (0.70), 2.163 (1.14), 2.176 (1.60), 2.187 (1.26), 2.327 (0.47), 2.366 (0.41), 2.523 (1.67), 2.669 (0.54), 2.710 (0.46), 3.998 (2.03), 4.002 (0.89), 4.021 (2.14), 4.038 (2.14), 4.056 (0.79), 4.133 (0.51), 4.151 (0.98), 4.168 (0.93), 4.175 (0.83), 4.186 (0.84), 4.193 (1.11), 4.202 (2.21), 4.210 (1.51), 4.219 (4.66), 4.228 (3.20), 4.236 (4.66), 4.246 (3.73), 4.254 (2.15), 4.263 (1.53), 4.272 (0.85), 4.287 (1.21), 4.298 (1.72), 4.309 (1.16), 5.226 (0.78), 5.245 (0.83), 5.266 (0.79), 5.285 (0.73), 6.794 (1.56), 6.804 (5.05), 6.815 (1.91), 6.826 (4.30), 6.837 (0.92), 6.856 (1.42), 6.866 (0.52), 6.875 (0.87), 6.917 (0.71), 6.936 (1.45), 6.955 (0.86), 7.142 (0.96), 7.145 (0.95), 7.163 (1.28), 7.173 (0.83), 7.177 (0.93), 7.194 (1.20), 7.212 (0.58), 7.387 (1.34), 7.408 (1.79), 7.429 (1.14), 7.599 (0.99), 7.603 (1.04), 7.683 (16.00), 7.702 (0.43), 7.875 (1.05), 7.879 (1.00), 7.897 (2.37), 7.914 (1.62), 7.918 (1.55), 8.002 (3.30), 8.019 (2.41), 8.408 (1.18), 8.423 (1.48), 8.443 (1.15), 9.112 (4.72), 9.124 (4.29), 9.517 (1.49), 9.525 (1.44), 9.537 (1.51), 9.544 (1.34).
Синтез 4-(цианометил)-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (пример 355)
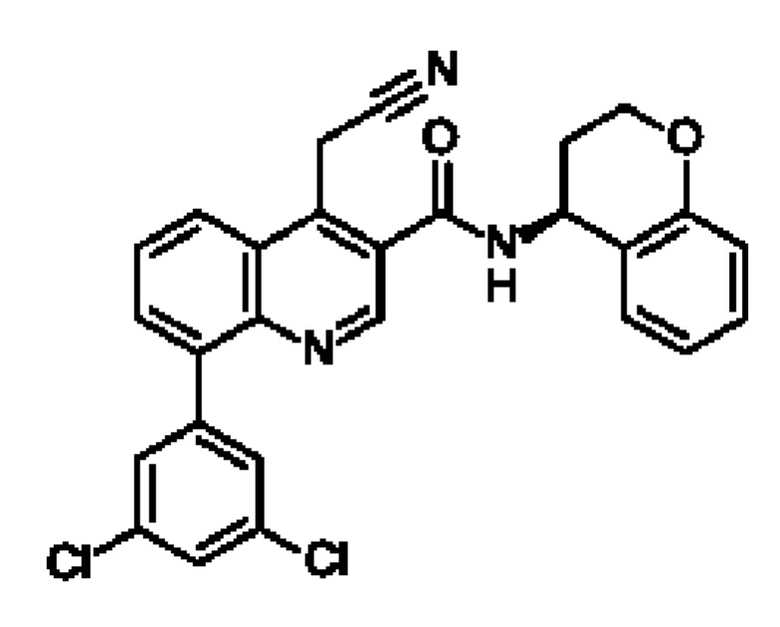
Раствор этил циано{8-(3,5-дихлорфенил)-3-[(4S)-3,4-дигидро-2Н-хромен-4-илкарбамоил]хинолин-4-ил}ацетата (пример 354) (300 мг, 0.54 ммоль) в ДМСО (2.4 мл) обработали хлоридом натрия (63 мг, 1.1 ммоль) и водой (0.24 мл) и нагревали при перемешивании всю ночь при 90°С. Воду (2.5 мл) добавили, осадок отфильтровали, промыли вод ой и высушили в вакууме.
Выход: 250 мг (99% чистота, 95% от теоретического выхода)
LC-MS (Способ L1): Rt=1.24 мин; MS (ESIpos): m/z=488 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: 2.099 (0.43), 2.136 (0.80), 2.145 (0.69), 2.205 (0.64), 2.224 (0.67), 2.239 (0.54), 4.266 (1.68), 4.277 (2.29), 4.711 (6.99), 5.278 (0.45), 5.294 (1.03), 5.312 (1.04), 5.326 (0.45), 6.798 (2.04), 6.818 (2.30), 6.899 (1.01), 6.917 (2.07), 6.936 (1.19), 7.163 (1.04), 7.182 (1.68), 7.200 (0.79), 7.387 (1.76), 7.405 (1.62), 7.677 (16.00), 7.883 (1.06), 7.903 (1.92), 7.922 (1.56), 7.988 (2.46), 8.006 (1.65), 8.417 (1.93), 8.437 (1.73), 9.029 (5.73), 9.379 (1.69), 9.399 (1.68).
Синтез 4-(2-амино-2-оксоэтил)-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (пример 360)
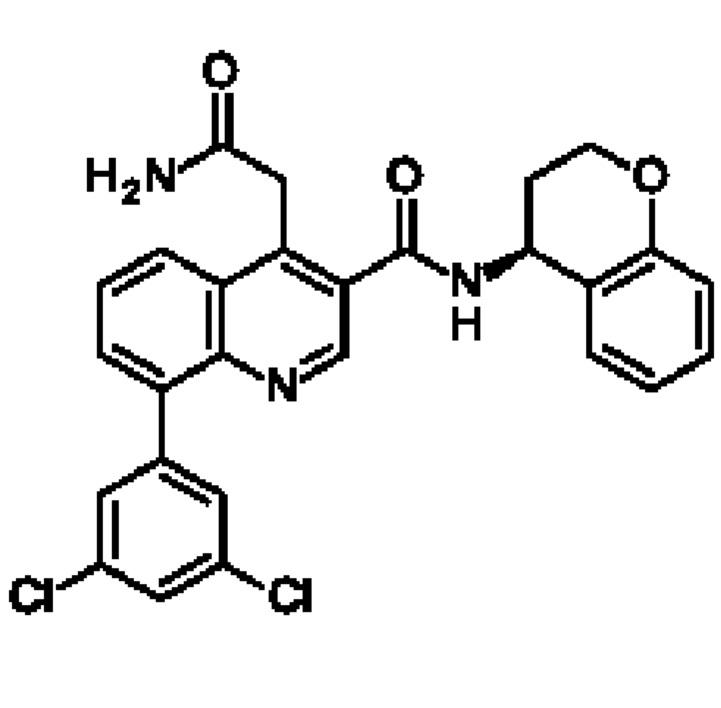
Суспензию 4-(цианометил)-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамида (пример 355) (150 мг, 307 мкмоль) в концентрированной соляной кислоте (0.77 мл, 37%) и диоксане (0.5 мл) перемешивали 3 дня при температуре окружающей среды. Твердое вещество отфильтровали, промыли диоксаном и высушили в вакууме.
Выход: 90 мг (92% чистота, 53% от теоретического выхода)
LC-MS (Способ L1): Rt=1.13 мин; MS (ESIpos): m/z=506 [M+H]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.149 (0.40), 0.008 (3.42), 2.068 (0.55), 2.085 (0.61), 2.095 (0.80), 2.208 (0.74), 2.220 (0.70), 2.229 (0.68), 2.242 (0.51), 2.327 (0.61), 2.366 (0.61), 2.670 (0.57), 2.710 (0.54), 2.794 (0.77), 3.568 (2.60), 4.179 (0.56), 4.197 (0.56), 4.216 (3.94), 4.225 (3.86), 4.238 (1.19), 4.264 (1.32), 4.283 (1.00), 5.270 (0.46), 5.285 (1.06), 5.304 (1.07), 5.319 (0.51), 6.779 (1.94), 6.800 (2.15), 6.883 (0.98), 6.899 (2.02), 6.918 (1.20), 7.147 (1.02), 7.164 (1.67), 7.185 (0.81), 7.349 (2.28), 7.369 (1.67), 7.659 (16.00), 7.764 (1.23), 7.782 (1.93), 7.803 (1.67), 7.894 (2.35), 7.910 (1.74), 7.989 (1.55), 8.349 (1.83), 8.368 (1.68), 8.949 (6.32), 9.468 (1.76), 9.488 (1.75).
Фильтрат довели до рН 6 посредством добавления водного бикарбоната натрия (7 мл, 1.5 М) и экстрагировали этилацетатом. Объединенные органические фазы высушили, выпарили, и остаток очистили посредством препаративной ВЭЖХ (С 18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил) с получением второго выхода (40 мг, 100% чистота, 26% от теоретического выхода)
Синтез 4-циано-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-кар бокс амида (пример 362)
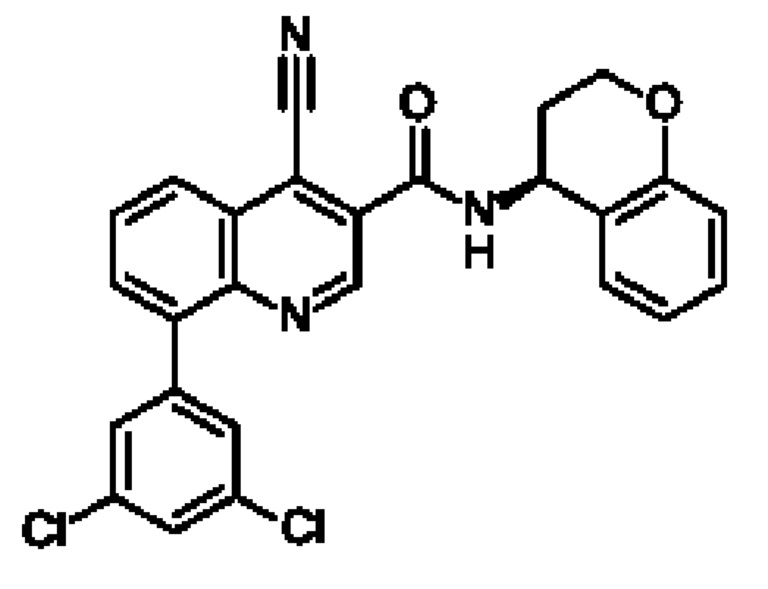
В атмосфере аргона в толстостенный сосуд, подходящий для обработки микроволнами, загрузил и 4-хлор-8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]хинолин-3-карбоксамид (1.00 г, 2.07 ммоль), цианид меди (I) (185 мг, 2.07 ммоль), карбонат натрия (219 мг, 2.07 ммоль), 1,1'-бнс(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (169 мг, 0.21 ммоль) н N-метилпирролидон (7.2 мл), закрыли и нагревали всю ночь при перемешивании при 120°С. Реакционную смесь добавили к 3:1 смеси насыщенного водного хлорида аммония / концентрированного водного аммиака (120 мл) и этил ацетата, перемешивали в течение 30 мин и отфильтровали через целит. Фазы разделили, органическую фазу промыли три раза 3:1 смесью насыщенного водного хлорида аммония / концентрированного водного аммиака, затем соляным раствором и высушили. Остаток (1.06 г) очистили посредством колоночной хроматографии на силикагеле (100 г) с циклогексаном / этил ацетатом (3-30%).
Выход: 760 мг (93% чистота, 72% от теоретического выхода)
LC-MS (Способ L1): Rt=1.44 мин; MS (ESIpos): m/z=474 [М+Н]+
1H-ЯМР Перечень пиков (400 МГц, ДМСО-d6) δ [ppm]: -0.008 (0.70), 0.008 (0.49), 1.398 (16.00), 1.988 (0.45), 2.519 (0.43), 6.790 (0.48), 6.849 (0.44), 6.851 (0.45), 6.870 (0.51), 6.872 (0.48), 6.966 (0.40), 7.673 (0.41), 7.696 (4.12), 7.933 (0.43), 7.951 (0.60), 7.953 (0.54), 7.972 (0.53), 8.054 (0.67), 8.057 (0.62), 8.071 (0.49), 8.075 (0.41), 9.279 (0.96), 9.311 (0.50).
Синтез 8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-2-метилхинолин-3-карбоксамида (пример 481).
Стадия 1
трет-бутил 8-бром-4-гидрокси-2-метилхинолин-3-карбоксилат
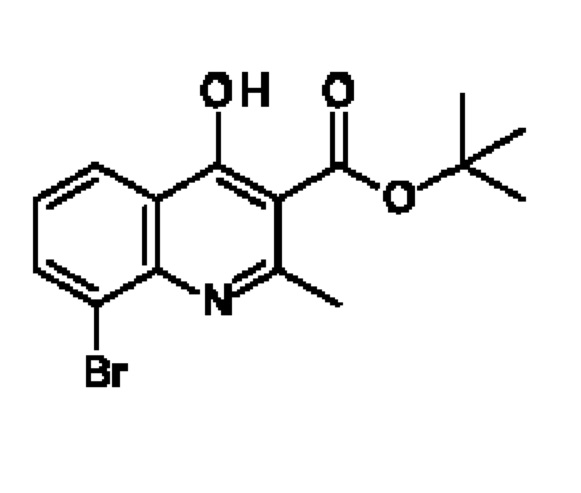
В трехгорловую колбу загрузили гидрид натрия (910 мг, 22.7 ммоль, 60% дисперсия в минеральном масле) и сухой DMF (50 мл). 3-Бромизтоевый ангидрид (5 г, 20.6 ммоль) добавили медленно (0.42 г, 4 ммоль), а затем по каплям добавили трет-бутил 3-оксобутаноат (3.6 г, 22.7 ммоль), растворенный в 50 мл DMF при комнатной температуре. Реакционную смесь нагрели до 120°С в течение 10 минут. Затем растворитель удалили при пониженном давлении, и оставшееся вещество диспергировали в воде и дважды экстрагировали дихлорметаном. Объединенные органические слои высушили над сульфатом натрия, отфильтровали и концентрировали в вакууме. Полученный осадок очистили посредством флэш-хроматографии на силикагеле (элюент циклогексан/этилацетат градиент).
Выход: 1.05 г (2.96 ммоль, 15% от теоретического выхода)
1Н-ЯМР (400 МГц, ДМСО-d6) δ 10.48 (s, 1Н), 8.10-8.08 (d, 1Н), 8.02-7.99 (d, 1Н), 7.31-7.27 (t, 1Н), метил синглет под ДМСО сигналом, 1.51 (s, 9Н).
Стадия 2
8-бром-4-хлор-2-метилхинолин-3-карбонил хлорид
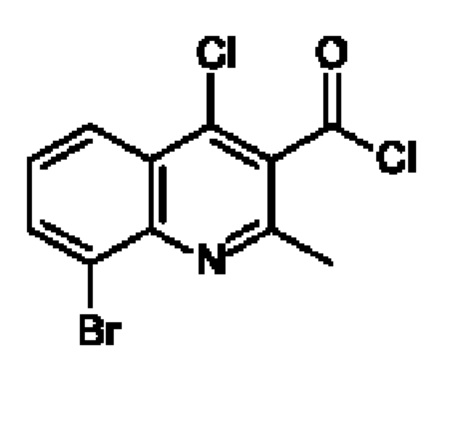
В трехгорловую колбу загрузили трет-бутил 8-бром-4-гидрокси-2-метилхинолин-3-карбоксилат (1.2 г, 3,54 ммоль)) и оксихлорид фосфора (42 г, 274 ммоль) и нагрели до возврата флегмы в течение 16 ч. Реакционную смесь концентрировали в вакууме и применяли в таком виде на следующей стадии.
Стадии 3
8-фом-4-хлор-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-2-метилхинолин-3-карбоксамнд
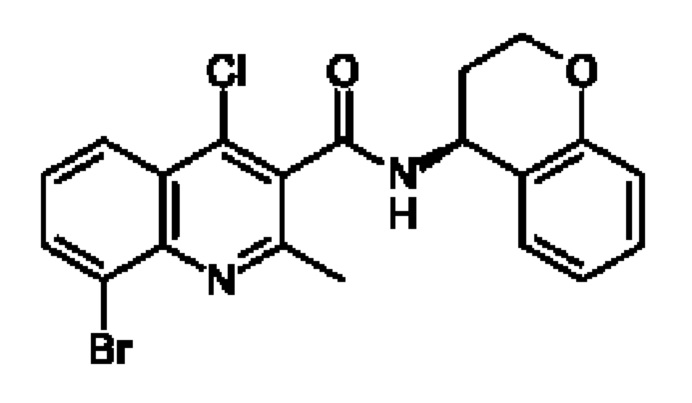
8-Бром-4-хлор-2-метилхинолин-3-карбонил хлорид (неочищенный продукт со стадии 2) (1 г, 3,13 ммоль) растворили в 60 мл ацетонитрила и смешали с (4S)-хроман-4-амин гидрохлоридом (582 мг, 3,13 ммоль) и триэтиламином (951 мг, 9,4 ммоль) при 0°С. Реакционной смеси позволили нагреться до комнатной температуры и перемешивали до завершения превращения Растворитель удалили при пониженном давлении; оставшийся раствор дважды экстрагировали дихлорметаном. Объединенные органические слои высушили над сульфатом натрия, отфильтровали и концентрировали в вакууме. Полученный осадок очистили посредством флэш-хроматографии на силикагеле (элюент циклогексан/этил ацетат градиент).
Выход: 766 мг (1.77 ммоль, 55% от теоретического выхода)
1Н-ЯМР (400 МГц, ДМСО-d6) δ 9.29 (d, 1H, NH), 8.26-8.22 (t, 2Н), 7.66-7.62 (dd, 1Н), 7.38-7.36 (d, 1Н), 7.20-7.16 (t, 1Н), 6.97-6.93 (t, 1Н), 6.82-6.80 (d, 1Н), 5.32-5.28 (m, 1Н), 4.34-4.29 (m, 1Н), 4.23-4.17 (m, 1Н),2.71 (s, 3Н), 2.28-2.22 (m, 1Н), 2.10-2.03 (m, 1H).
Стадия 4
8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-нл]-4-(диметиламино)-2-метилхинолин-3-карбоксамид
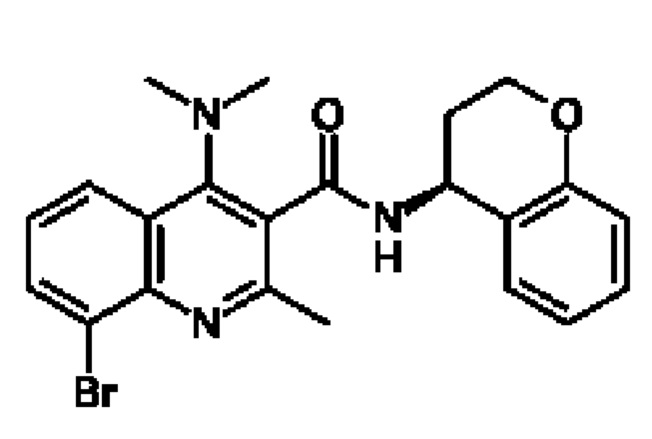
8-Бром-4-хлор-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-2-метилхинолин-3-кар6оксамид (стадия 3) (766 мг, 1.77 ммоль) в 30 мл диоксана распределили по трем колбам, подходящим для обработки микроволнами (20 мл объем). В каждую загрузили 3.7 мл водного раствора диметиламина (40%, объединенные 8.87 ммоль). Реакционные смеси нагревали в микроволновой печи (Anton Paars Monowave 400) до 100°С в течение 40 минут. Реакционные смеси объединили, и растворитель удалили при пониженном давлении. Полученный осадок очистили посредством флэш-хроматографии на силикагеле (элюент циклогексан/этилацетат градиент).
Выход: 625 мг (1.42 ммоль, 73% от теоретического выхода)
1H-ЯМР (400 МГц, ДМСО-d6) δ 9.07 (d, 1H, NH), 8.08-8.02 (2d, 2Н), 7.41-7.37 (t, 1Н),7.32-7.31 (d, 1Н), 7.20-7.16 (t, 1Н), 6.96-6.92 (t, 1Н), 6.82-6.79 (d, 1Н), 5.28-5.26 (m, 1Н), 4.35-4.27 (m, 1Н), 4.23-4.16 (m, 1Н), 3.01 (s, 6Н), 2.61 (s, 3Н), 2.28-2.19 (m, 1Н), 2.10-2.02 (m, 1H).
Стадия 5
8-(2,3-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-2-метилхинолин-3-карбоксамид (Пример 481)
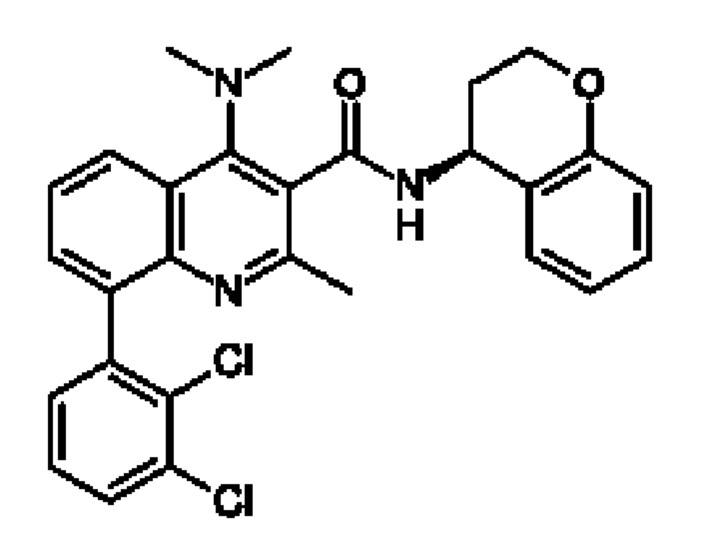
К дегазированной (1 мин, аргон) смеси 8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(диметиламино)-2-метилхинолин-3-кар6оксамида (стадия 4) (200 мг, 0.45 ммоль), (2,3-дихлорфенил)бороновой кислоты (130 мг, 0.68 ммоль), карбоната калия (125.5 мг, 0.90 ммоль), воды (3,5 мл) и диоксана (12 мл) добавили 1,1'-бис(дифенилфосфино)ферроценпалладия(II) дихлорид (18.5 мг, 0.02 ммоль). Реакционную смесь перемешивали в течение 16 ч при 85°С, затем охладили до комнатной температуры, разбавили водой и дважды экстрагировали дихлорметаном. Объединенные органические слои высушили над сульфатом натрия, отфильтровали и концентрировали в вакууме. Полученный осадок очистили посредством флэш-хроматографии на силикагеле (элюент циклогексан/этилацетат градиент) с получением указанного в названии соединения.
Выход: 159 мг(0.31 ммоль, 66% от теоретического выхода)
1Н-ЯМР (400 МГц, ДМСО-d6) δ 9.06 (d, 1H, NH), 8.17-8.15 (d, 1Н), 7.68-7.66 (d, 1Н), 7.58-7.55 (m, 2Н), 7.42-7.42 (m, 1Н), 7.32-7.30 (m, 2Н), 7.17-7.15 (t, 1Н), 6.93-6.91 (t, 1Н), 6.80-6.78 (d, 1Н), 5.28-5.24 (m, 1Н), 4.32-4.27 (m, 1Н),4.23-4.17 (m, 1Н), 3.04 (s, 6Н), метил синглет под ДМСО сигналом, 2.24-2.18 (m, 1Н), 2.08-2.02 (m, 1H).
Синтез 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(тетрагидро-2Н-пиран-4-ил)хинолин-3-карбоксамида (Пример 539).
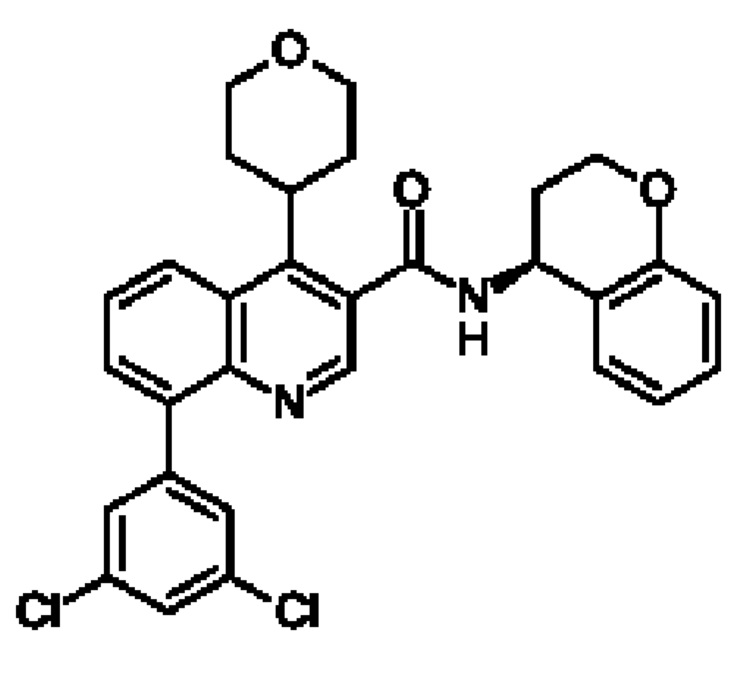
В атмосфере аргона 8-(3,5-дихлорфенил)-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(3,6-дигидро-2Н-пиран-4-ил)хинолин-3-карбоксамид (60.0 мг, 113 мкмоль) растворили в этилацетат/этаноле (2:1, 6 мл). Катализатор, 10% палладия на активированном угле (20 мг), добавили, аргон заменили на водород, и смесь перемешивали в атмосферном давлении водорода в течение 4.5 ч. Еще 10% палладия на активированном угле (20 мг) добавили в атмосфере аргона и гидратирование продолжали при атмосферном давлении в течение 6 часов. Реакционную смесь отфильтровали через целит, промыли этилацетатом и концентрировали в вакууме. Остаток (66 мг) очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил).
Выход: 11 мг (18% от теоретического выхода)
LC-MS (Способ L1): Rt=1.28 мин; MS (ESIpos): m/z=533 [М+Н]+
1H-ЯМР (400 МГц, ДМСО-d6) δ [ppm]: 0.008 (2.51), 1.235 (0.43), 1.676 (1.54), 1.713 (2.60), 1.751 (1.67), 2.057 (0.97), 2.072 (1.11), 2.085 (1.87), 2.218 (1.33), 2.231 (1.31), 2.240 (1.26), 2.252 (0.92), 2.327 (0.56), 2.366 (0.60), 2.429 (2.14), 2.460 (2.25), 2.670 (0.69), 2.710 (0.67), 3.464 (1.07), 3.493 (1.97), 3.520 (2.14), 3.546 (2.15), 3.575 (1.18), 3.738 (1.26), 4.010 (3.17), 4.023 (2.81), 4.038 (2.85), 4.219 (0.82), 4.240 (2.21), 4.247 (1.78), 4.260 (2.15), 4.268 (2.70), 4.279 (2.21), 4.295 (1.97), 5.293 (0.94), 5.307 (2.08), 5.327 (2.08), 5.342 (0.90), 5.754 (5.00), 6.785 (3.97), 6.804 (4.38), 6.918 (1.97), 6.937 (4.07), 6.956 (2.40), 7.158 (2.10), 7.176 (3.37), 7.193 (1.61), 7.405 (3.52), 7.423 (3.20), 7.613 (13.15), 7.617 (16.00), 7.648 (4.20), 7.653 (5.68), 7.748 (2.29), 7.766 (3.65), 7.787 (3.20), 7.856 (4.95), 7.874 (3.52), 8.510 (3.43), 8.531 (3.17), 8.777(12.63), 9.140 (3.54), 9.161 (3.54).
Синтез N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(метоксиметил)-8-(2,3,5-трифторфенил)хинолин-3-карбоксамида (Пример 686).
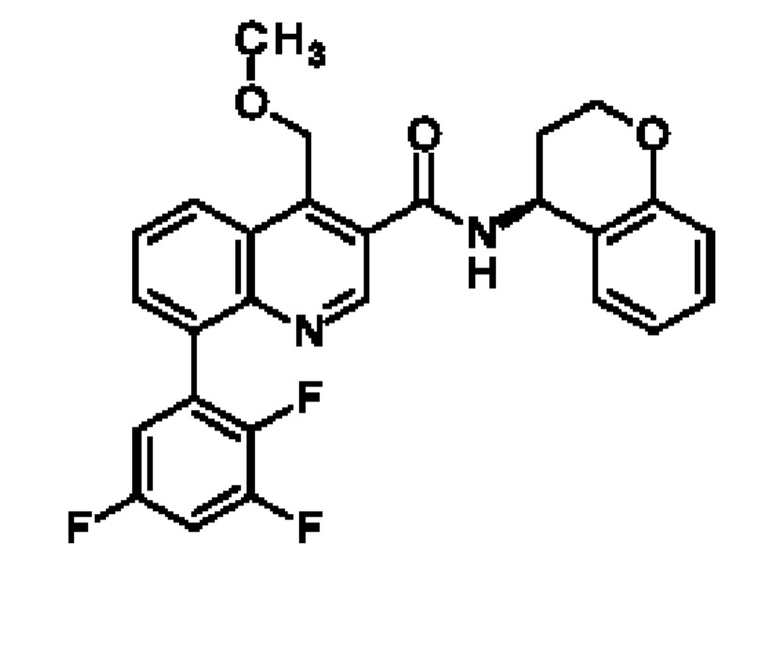
Стадия 1
этил 8-бром-4-метилхинолин-3-кар6оксилат
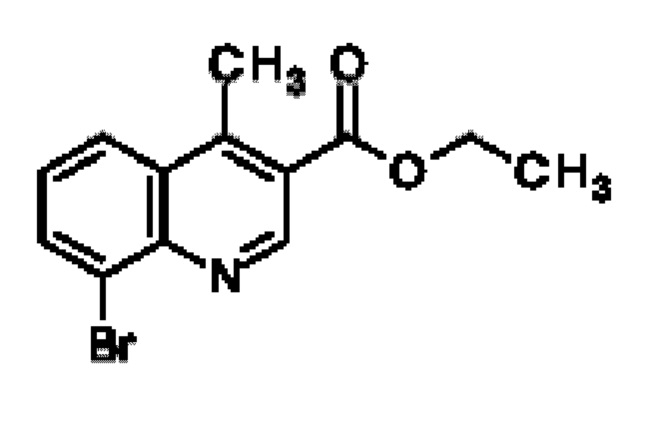
К раствору этил 8-бром-4-гидрокси-хинолин-3-карбоксилата (3.00 г, 9.54 ммоль) (Gharat, al., WO 2013/118071) в THF (45 мл) добавили в атмосфере аргона кобальта(II)ацетилацетонат (2.45 г, 9.54 ммоль). Смесь нагрели на масляной бане 60°С, диметилцинк (раствор в толуоле, 1.9 мл, 2.0 М, 3.8 ммоль) добавили по каплям и перемешивали при этой температуре в течение 1 часа. В течение периода времени 4.5 часа еще диметилцинк (раствор в толуоле, 6.2 мл, 2.0 М, 12.4 ммоль) добавили при этой температуре в несколько порций, пока почти весь исходный материал не был израсходован (ВЭЖХ мониторинг). Смесь перепилив воду (250 мл), содержащую уксусную кислоту (1.8 мл), органические растворители в основном выпарили при пониженном давлении и водную фазу экстрагировали этилацетатом. Объединенные органические фазы выпарили и выпарили до сухости. Остаток (3.1 г) очистили посредством колоночной хроматографии на силикагеле (100 г), элюент: циклогексан / этилацетат (3-10%) с получением соединения, указанного в названии (1.25 г, 45% от теоретического выхода)
LC-MS (Способ L4): Rt=3.06 мин; MS (ESIpos): m/z=294 [M+H]+
1H-ЯМР (400 МГц, ДМСО-d6) δ [ppm]: 1.369 (4.76), 1.387 (9.98), 1.405 (4.89), 2.934 (16.00), 4.393 (1.57), 4.411 (4.77), 4.429 (4.71), 4.447 (1.51), 7.615 (1.30), 7.634 (2.23), 7.655 (1.46), 8.253 (1.85), 8.271 (1.76), 8.340 (2.09), 8.361 (1.99), 9.185 (3.32).
Стадия 2
этил 8-бром-4-(бромметил)хинолин-3-карбоксилат
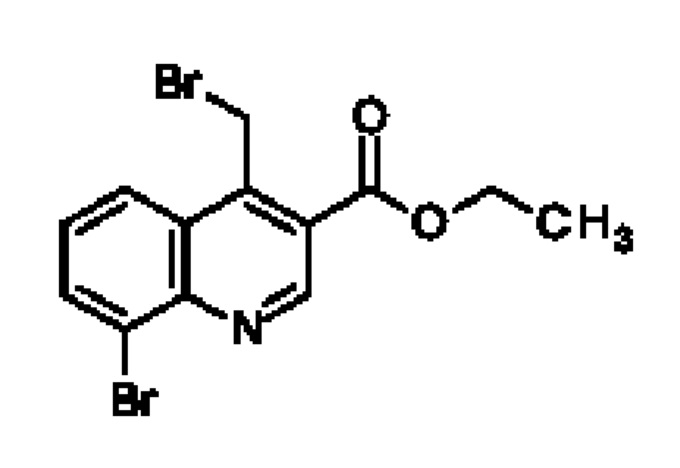
Этил-8-бром-4-метилхинолин-3-карбоксилат (1.50 г, 5.10 ммоль) растворили в THF (23 мл). Фенилтриметиламмония трибромид (3.07 г, 8.16 ммоль,) и уксусную кислоту(1.5 мл, 25 ммоль) добавили и смесь при перемешивании при температуре окружающей среды.
Еще фенилтриметиламмония трибромид (0.96 г, 2.5 ммоль) добавили и перемешивали в течение 3 дней при температуре окружающей среды. Другую порцию фенилтриметиламмония трибромида (0.96 г, 2.5 ммоль) и уксусной кислоты (0.9 мл, 15,3 ммоль) добавили и перемешивание продолжали всю ночь. Реакционную смесь разбавили водой и дихлорметаном. Водную фазу экстрагировали дихлорметаном, и объединенные органические слои промыли водным раствором гидрокарбоната натрия, высушили и концентрировали в вакууме при 30°С.
Остаток перемешивали в течение 1 часа в МТВЕ (80 мл). Твердое вещество отфильтровали, промыли МТВЕ и высушили в вакууме. Неочищенное вещество (3.23 г) очистили посредством колоночной хроматографии, элюент циклогексан/этилацетат (3-22%).
Выход: 985 мг (90.5% чистота, 47% от теоретического выхода)
LC-MS (Способ L1): Rt=1.11 мин; MS (ESIpos): m/z=371 [М+Н]+
1H-ЯМР (500 МГц, ДМСО-d6) δ [ppm]: 1.401 (7.41), 1.415 (16.00), 1.429 (7.42), 1.435 (0.41), 4.441 (2.26), 4.455 (7.12), 4.470 (6.98), 4.484 (2.13), 5.479 (11.96), 5.758 (1.31), 7.721 (2.28), 7.736 (2.76), 7.738 (2.62), 7.753 (2.43), 8.311 (2.94), 8.314 (3.02), 8.326 (2.85), 8.329 (2.69), 8.446 (2.62), 8.448 (2.54), 8.463 (2.57), 8.465 (2.29), 9.311 (8.57).
Стадия 3
8-бром-4-(метоксиметил)хинолин-3-карбоновая кислота
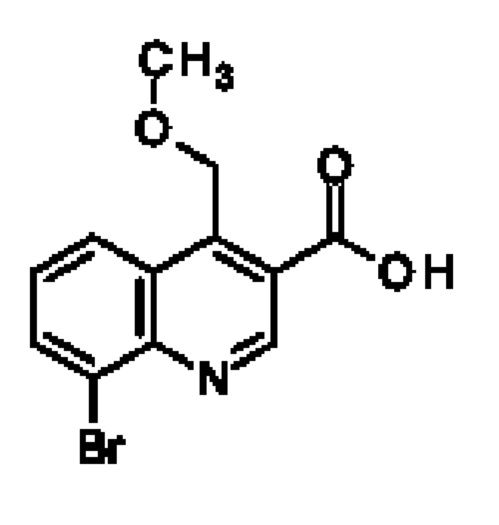
Суспензию этил 8-6ром-4-(бромметил)хинолин-3-кар6оксилата (1.14 г, 3.06 ммоль) в метаноле (15 мл) обработали по каплям метоксидом натрия (раствор в метаноле, 5.4 М) при температуре окружающей среды, в ходе чего происходило растворение, а затем осаждалось твердое вещество. Через 1,5 ч THF (5 мл) и воду (3 мл) добавляли и перемешивали в течение ночи при температуре окружающей среды. Затем раствор разбавляли 20 мл воды и рН доводили до 4 добавлением уксусной кислоты (5 М). После концентрирования в вакууме для удаления большей части органических растворителей оставшаяся смесь распределялась между этилацетатом и водой. Водный слой экстрагировали несколько раз этилацетатом, и объединенные органические слои высушили и концентрировали в вакууме. Это вещество (363 мг, 91% чистота, 37% от теоретического выхода) было подходящим для дальнейшего использования. Водную фазу концентрировали до небольшого объема при пониженном давлении, разбавили ДМСО и очистили посредством препаративной ВЭЖХ (С18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил) с получение второго выхода (270 мг, 100%) чистота, 30% от теоретического выхода).
LC-MS (Способ L1): Rt=0.69 мин; MS (ESIpos): m/z=296 [М+Н]+
1H-ЯМР (500 МГц, ДМСО-d6) δ [ppm]: 1.221 (0.47), 3.184 (0.52), 5.199 (16.00), 7.611 (3.54), 7.627 (5.28), 7.643 (3.76), 8.238 (4.81), 8.252 (4.56), 8.351 (4.61), 8.367 (4.38), 9.215 (10.02).
Стадия 4
8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(метоксиметил)хинолин-3-карбоксамид
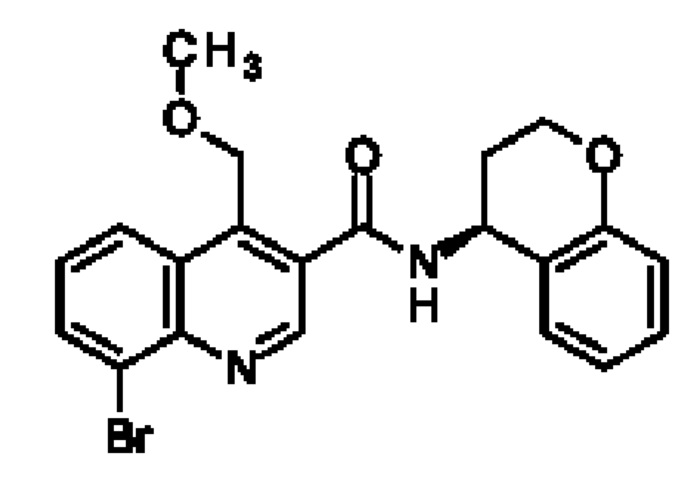
Раствор 8-бром-4-(метоксиметил)хинолин-3-карбоновой кислоты (360 мг, 1.22 ммоль) в THF (6 мл) обработали (4S)-хроман-4-амин гидрохлоридом (1:1) и триметиламином (680 мкмл, 4.9 ммоль). Смесь нагрели до 45°С, 2,4,6-трипропил-1,3,5,2,4,6-триоксатрифосфинан 2,4,6-триоксид (раствор в этилацетате, 23 мл, 50% содержание, 39 ммоль) добавили, нагревание прекратили, и смесь перемешивали при температуре окружающей среды всю ночь. После добавления воды (рН 8-9) THF удалили в вакууме. Осадок отфильтровали и растворили в около 10 мл теплого ацетона. Теплую воду добавили (10 мл), и смеси позволили охладиться до комнатной температуры. Твердое вещество отфильтровали, промыли ацетоном/водой (1:2) и высушили в вакууме.
Выход: 391 мг (95% чистота, 72% от теоретического выхода)
LC-MS (Способ L1): Rt=0.96 мин; MS (ESIpos): m/z=427 [М+Н]+
1H-ЯМР (600 МГц, ДМСО-d6) δ [ppm]: 1.235 (0.52), 2.090 (2.20), 2.230 (2.15), 3.287 (16.00), 4.241 (2.66), 4.293 (2.83), 4.998 (8.92), 5.314 (2.68), 6.800 (2.83), 6.811 (3.13), 6.943 (3.04), 7.183 (3.03), 7.397 (3.01), 7.612 (3.03), 8.211 (2.99), 8.221 (3.08), 8.311 (2.87), 8.324 (2.94), 8.998 (4.49), 9.207 (2.80).
Стадия 5
N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(метоксиметил)-8-(2,3,5-трифторфенил)хинолин-3-карбоксамид (Пример 686)
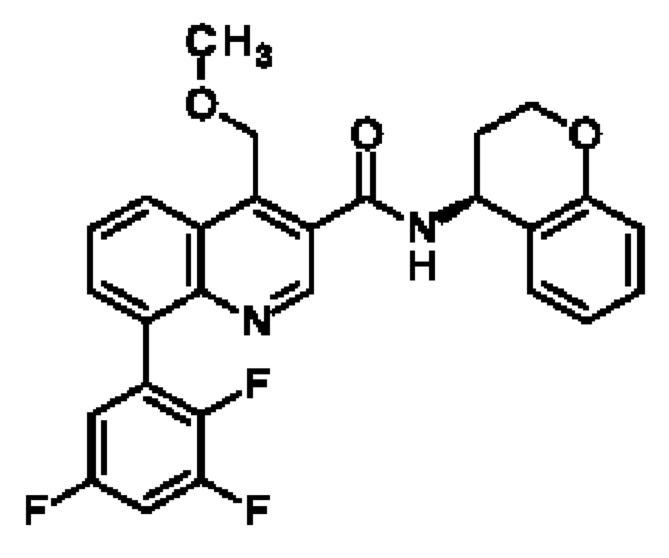
В атмосфере аргона в сосуд загрузили 8-бром-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(метоксиметил)хинолин-3-карбоксамид (90 мг, 211 мкмоль), 2,3,5-трифторбензолбороновую кислоту (55.6 мг, 316 мкмоль), 1,1'-бис(дифенилфосфино)ферроцен-палладия(II)дихлорид дихлорметан комплекс (8.60 мг, 10.5 мкмоль), карбонат калия (58.2 мг, 421 мкмоль) и дегазированную 5:1 смесь диоксана и воды (0.73 мл). Смесь перемешивали всю ночь при 70°С. Разбавили этилацетатом, отфильтровали через слой сульфата натрия и концентрировали в вакууме. Неочищенное вещество очистили посредством препаративной ВЭЖХ (С 18, градиент: 0.1% вод. муравьиная кислота/ацетонитрил.
Выход: 31 мг (31% от теоретического выхода)
LC-MS (Способ L1): Rt=1.14 мин; MS (ESIpos): m/z=479 [М+Н]+
1H-ЯМР (600 МГц, ДMCO-d6) δ [ppm]: 0.005 (1.04), 2.043 (0.47), 2.048 (0.60), 2.053 (0.96), 2.058 (1.04), 2.065 (1.12), 2.069 (1.07), 2.077 (1.37), 2.081 (1.20), 2.087 (2.11), 2.092 (0.63), 2.193 (0.58), 2.199 (0.86), 2.202 (0.81), 2.207 (1.32), 2.213 (0.97), 2.216 (1.31), 2.221 (1.32), 2.230 (0.99), 2.236 (0.64), 2.239 (0.62), 2.244 (0.46), 2.793 (0.55), 3.345 (8.00), 4.220 (0.71), 4.225 (0.87), 4.234 (0.90), 4.239 (2.32), 4.244 (1.61), 4.253 (1.77), 4.258 (1.47), 4.268 (1.42), 4.273 (1.80), 4.279 (1.58), 4.285 (1.91), 4.292 (0.78), 4.298 (0.84), 4.303 (0.65), 5.037 (16.00), 5.287 (0.91), 5.297 (1.95), 5.310 (1.96), 5.320 (0.92), 6.790 (3.66), 6.791 (3.76), 6.803 (4.00), 6.804 (3.99), 6.917 (1.85), 6.918 (1.84), 6.929 (3.75), 6.931 (3.68), 6.942 (2.14), 6.943 (2.05), 7.159 (1.78), 7.161 (1.80), 7.173 (3.01), 7.184 (1.56), 7.187 (1.49), 7.259 (1.51), 7.267 (1.49), 7.274 (1.49), 7.376 (3.08), 7.388 (2.95), 7.609 (0.49), 7.614 (0.63), 7.619 (0.75), 7.624 (1.18), 7.628 (1.14), 7.633 (1.23), 7.638 (1.18), 7.642 (1.18), 7.646 (0.74), 7.651 (0.65), 7.657 (0.56), 7.800 (2.66), 7.812 (3.85), 7.814 (3.18), 7.826 (3.61), 7.873 (4.17), 7.875 (4.29), 7.885 (3.06), 7.887 (2.94), 8.416 (3.61), 8.418 (3.65), 8.430 (3.48), 8.432 (3.27), 8.890 (12.74), 9.184 (3.52), 9.197 (3.43).
Синтез N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-4-(оксетан-3-ил)-8-(2,3,5-трифторфенил)хинолин-3-карбоксамида (пример 660).
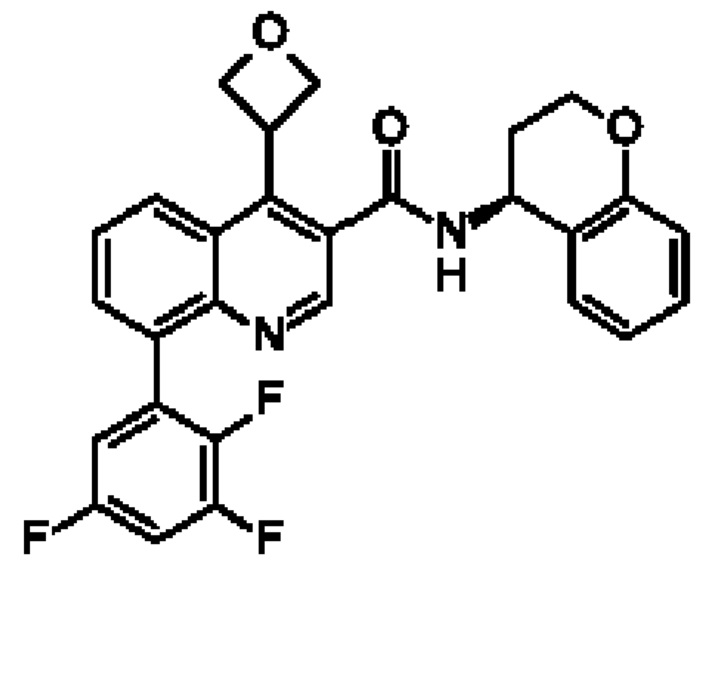
В круглодонной колбе, объемом 100 мл, смесь 4-хлор-N-[(4S)-3,4-дигидро-2Н-хромен-4-ил]-8-(2,3,5-трифторфенил)хинолин-3-карбоксамида (500 мг, 1.066 ммоль), безводного гидроксида лития (51 мг, 2.133 ммоль), 3-бромоксетана (0.133 мл, 1.600 ммоль), [4,4'-бис(1,1-диметилэтил)-2,2'-бипиридин-N1,N']бис[3,5-дифтор-2-[5-(трифторметил)-2-пиридинил-N]фенил-С] иридия(III) гексафторфосфата (24 мг, 0.021 ммоль) и трис(триметилсилил)силана (0.329 мл, 1.066 ммоль) в 1,2-диметоксиэтане (20 мл) дегазировали посредством продувания аргоном. В круглодонной колбе, объемом 50 мл, смесь комплекса диметилового простого эфира этиленгликоля и хлорида никеля (II) (14 мг, 0.064 ммоль) и 4,4'-ди-трет-бутил-2,2'-бипиридина (17 мг, 0.064 ммоль) в 1,2-диметоксиэтана (10 мл) бережно нагревали с помощью тепловой пушки, продули аргоном и перемешивали в течение пяти минут. С помощью шприца половину этой никель-каталитической смеси (5 мл) добавили к реакционной смеси. Полученную суспензию продували аргоном в течение пяти минут и затем перемешивали при облучении синим светодиодом в течение 18 часов при охлаждении вентилятором. Реакционную смесь разбавляли дихлорметаном (30 мл). Воду (10 мл) добавили, и слои разделили. Водный слой экстрагировали дихлорметаном (2×10 мл). Объединенные органические слои высушили над сульфатом натрия, и растворители удалили в вакууме. Очистка посредством колоночной флэш-хроматографии (80 г; гептан, 10%-60% этилацетат) и препаративной ВЭЖХ (Способ 11) позволила получить 0,054 г (0,110 ммоль; 10% от теоретического выхода) указанного в названии соединения.
LC-MS (Способ 2): Rt=3.65 мин; m/z=491 (М+Н)+
1H-ЯМР (400 МГц, ДМСО-d6) δ 9.26 (d, J=8.1 Гц, 1Н), 8.87 (s, 1Н), 7.91-7.87 (m, 1Н), 7.84-7.73 (m, 2Н), 7.70-7.57 (m, 1Н), 7.35 (d, J=7.8 Гц, 1Н), 7.30-7.23 (m, 1Н), 7.19 (t, J=7.8 Гц, 1Н), 6.93 (t, J=7.5 Гц, 1Н), 6.81 (d, J=8.2 Гц, 1Н), 5.31-5.11 (m, 4Н), 4.84-4.70 (m, 2Н), 4.34-4.21 (m, 2Н), 2.25-2.15 (m, 1Н), 2.08-2.01 (m, 1H).
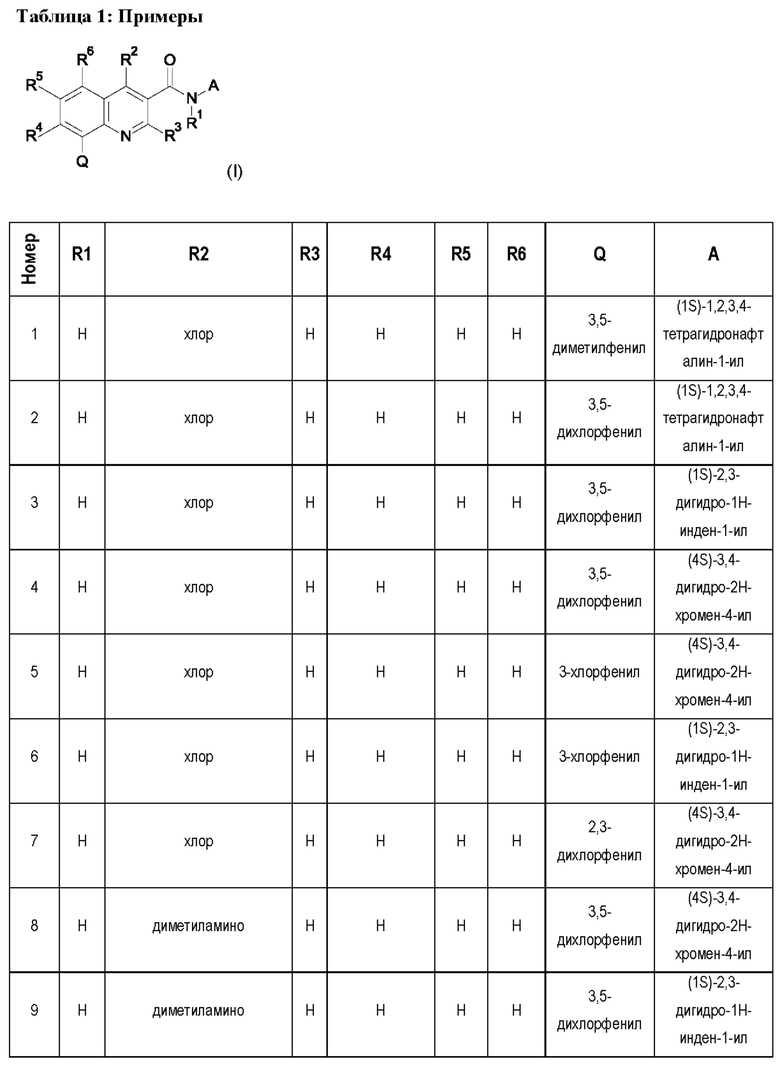
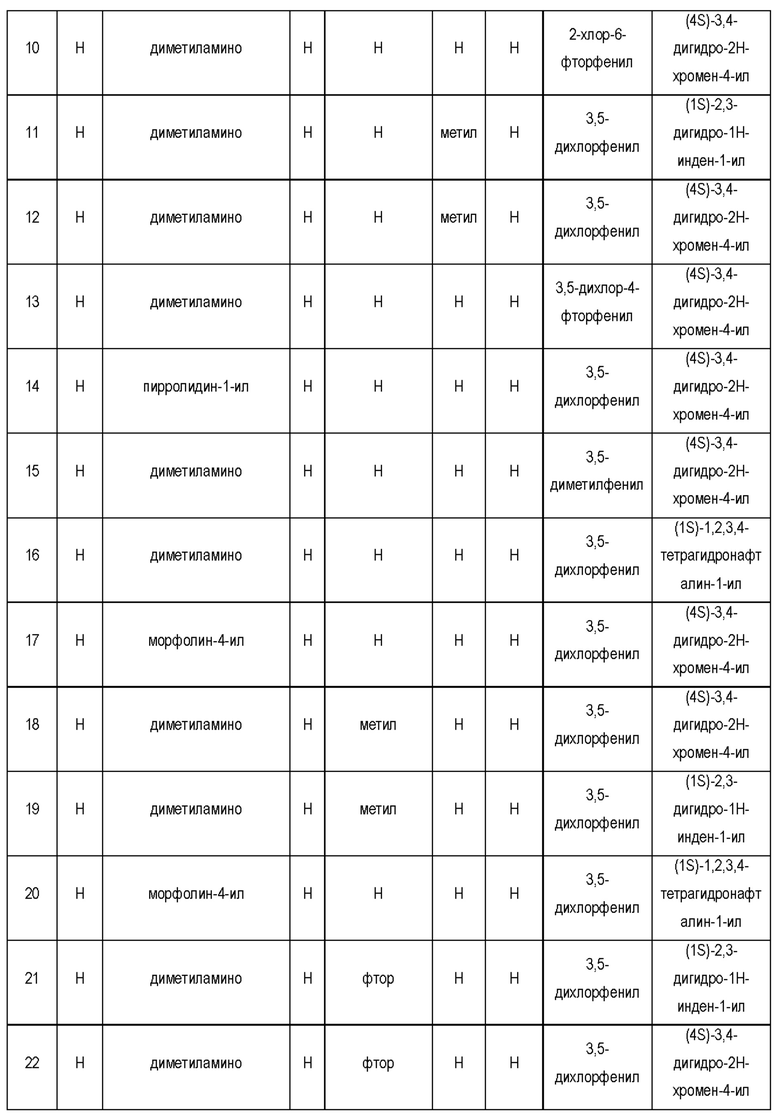
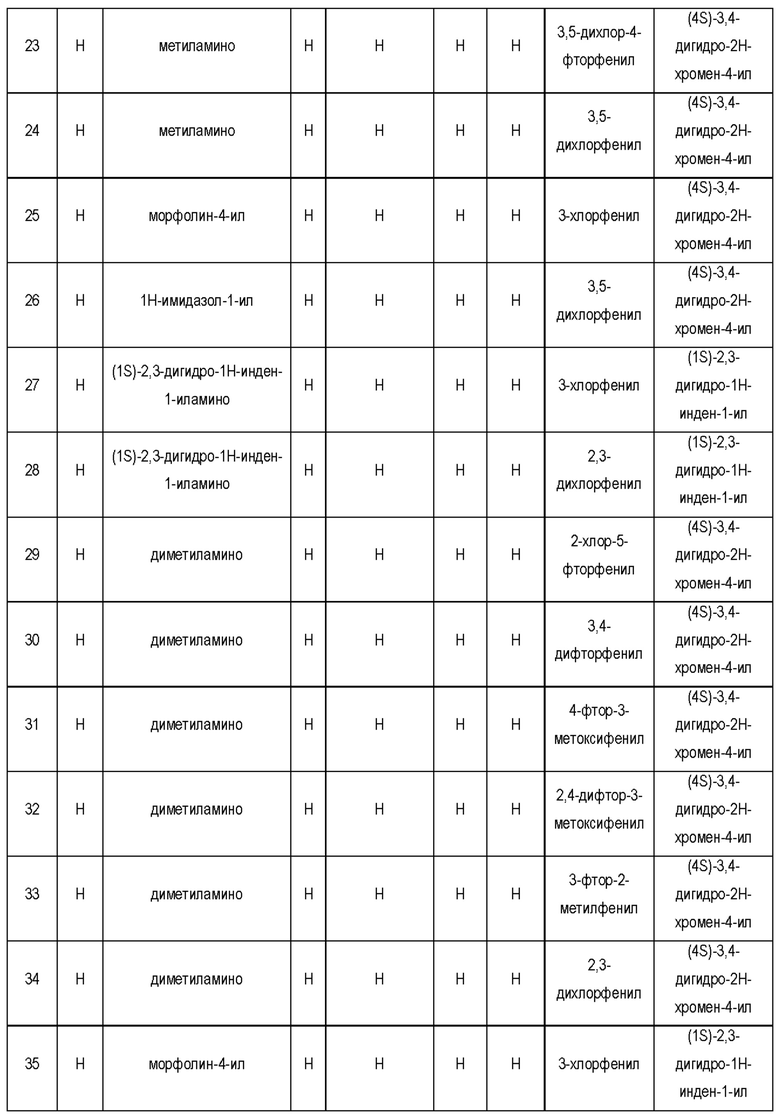
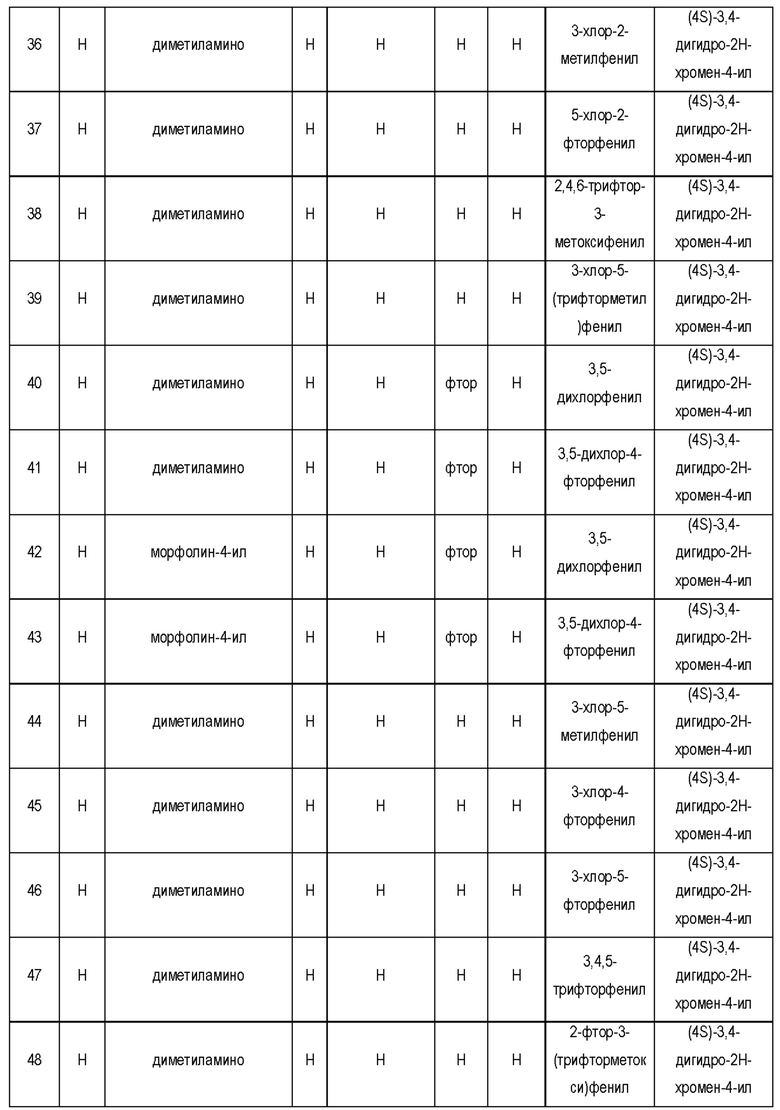
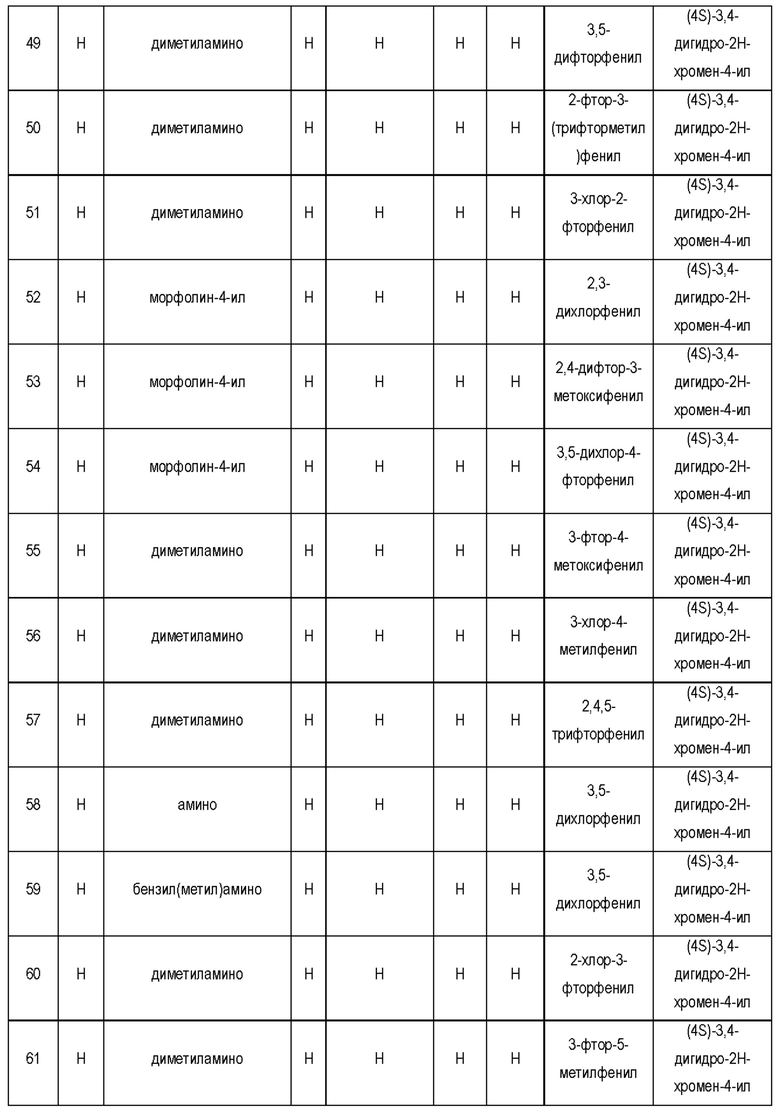
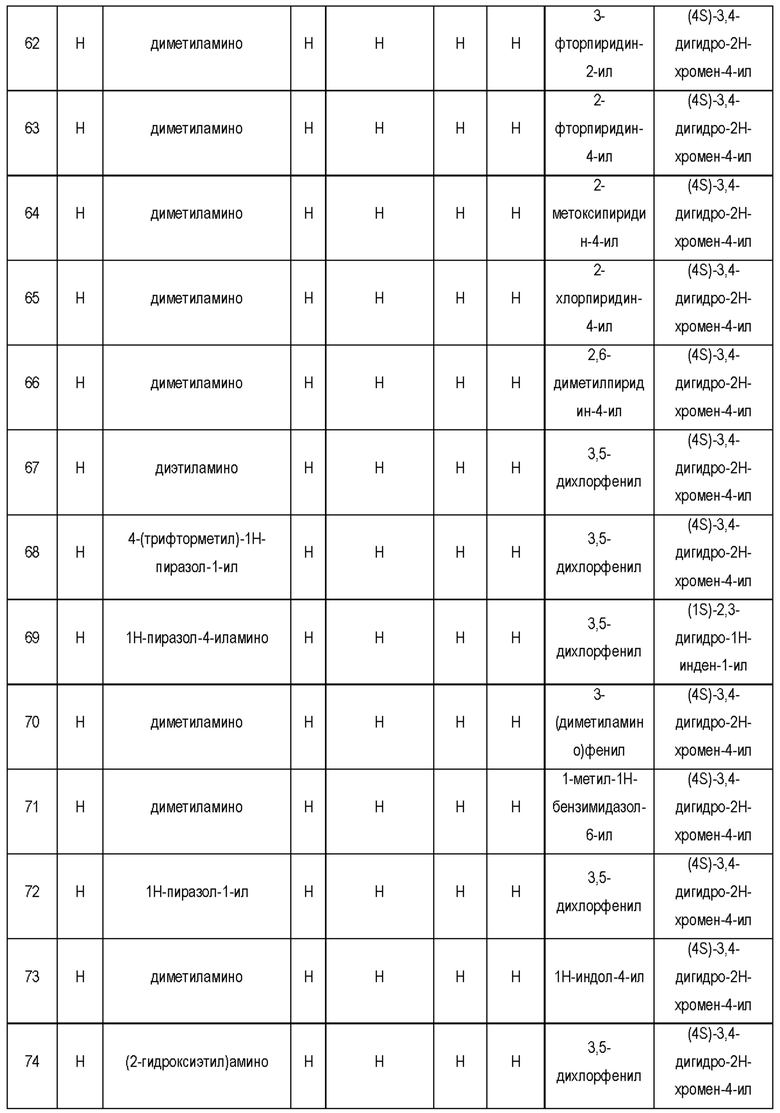
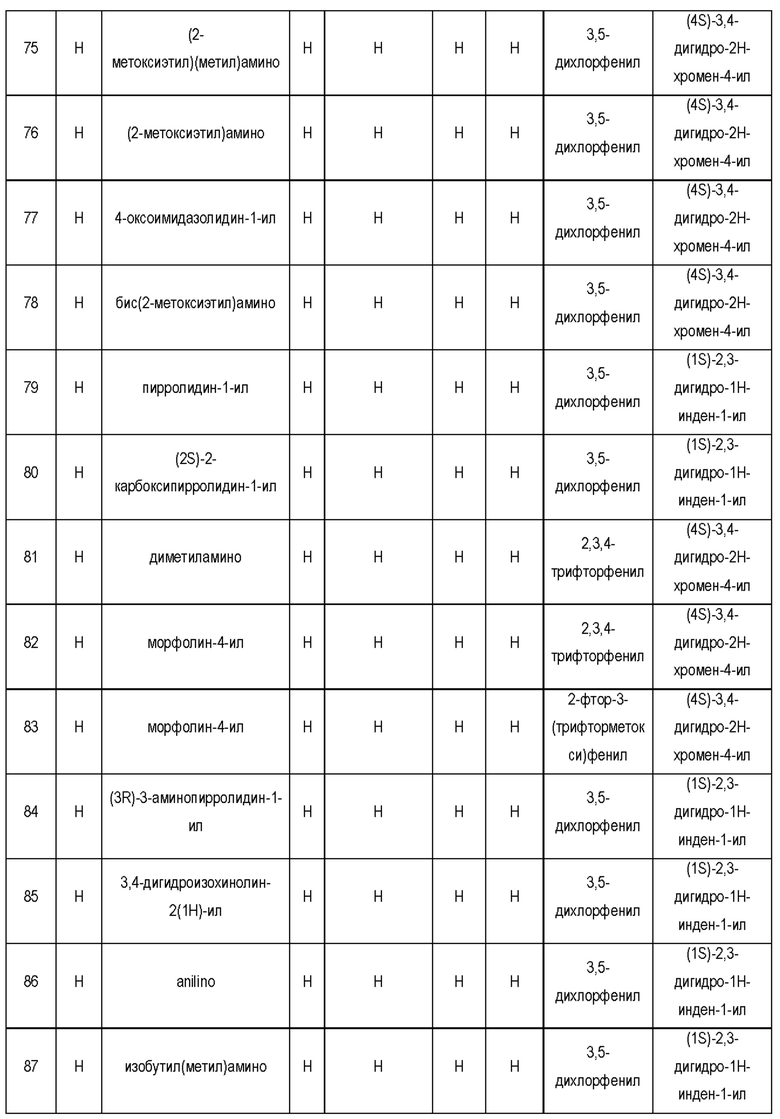
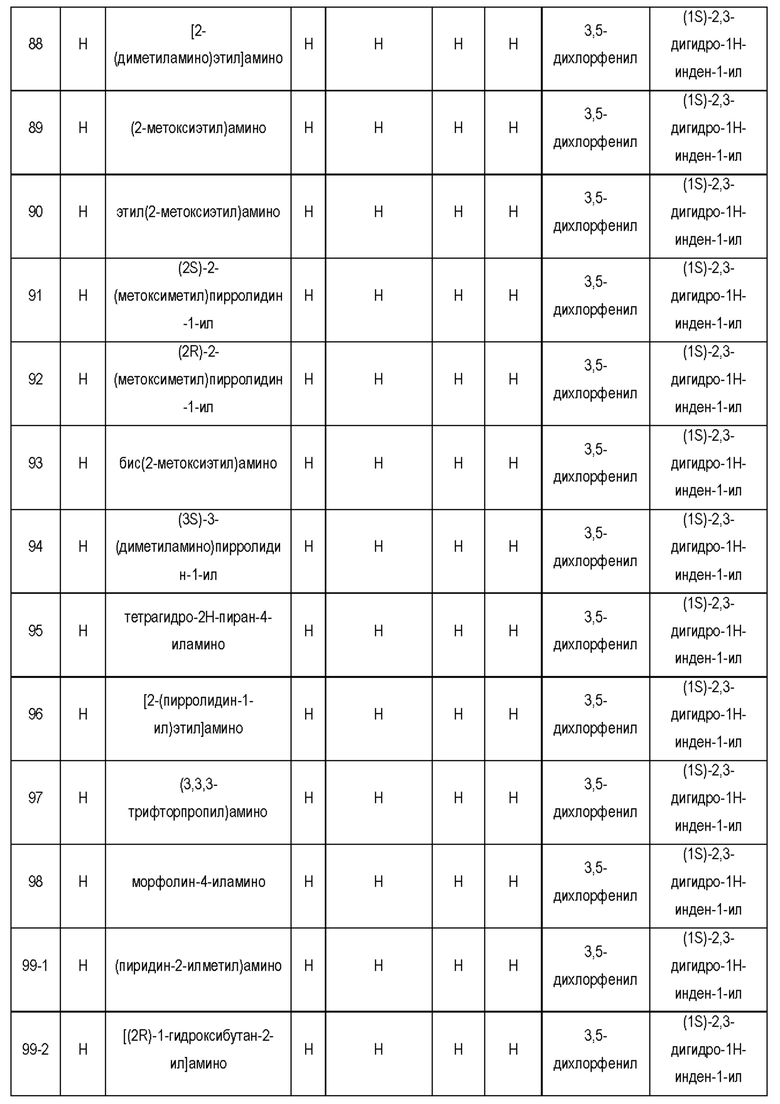
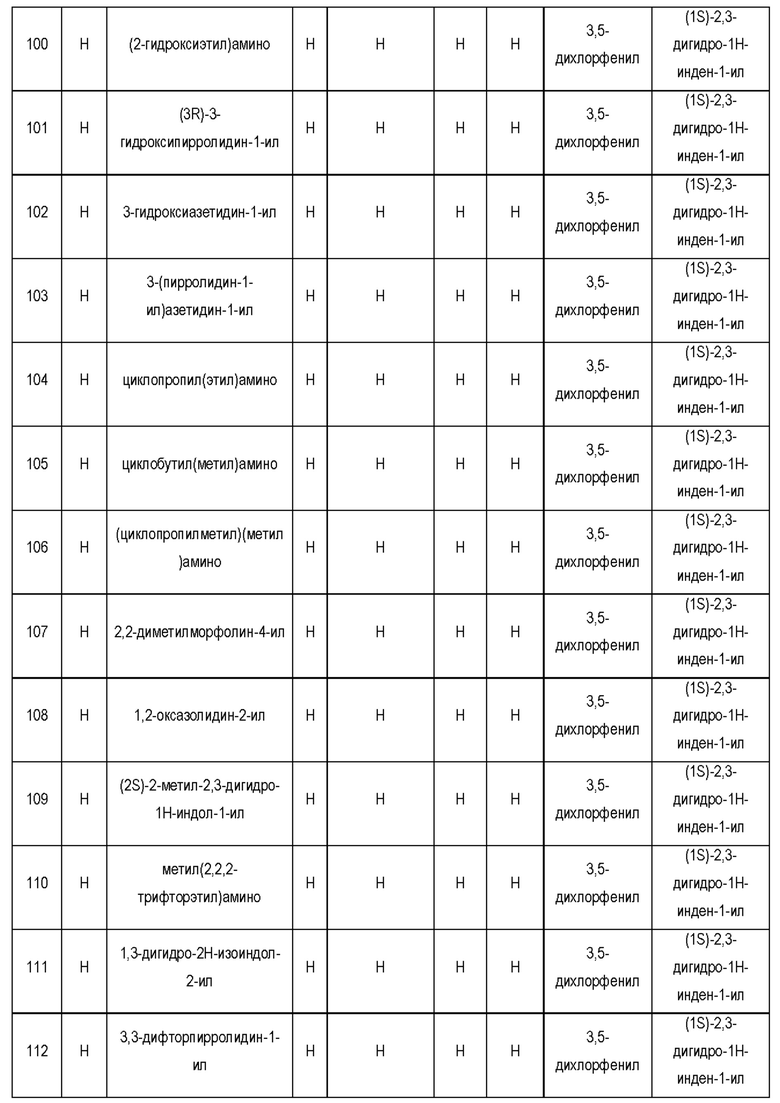
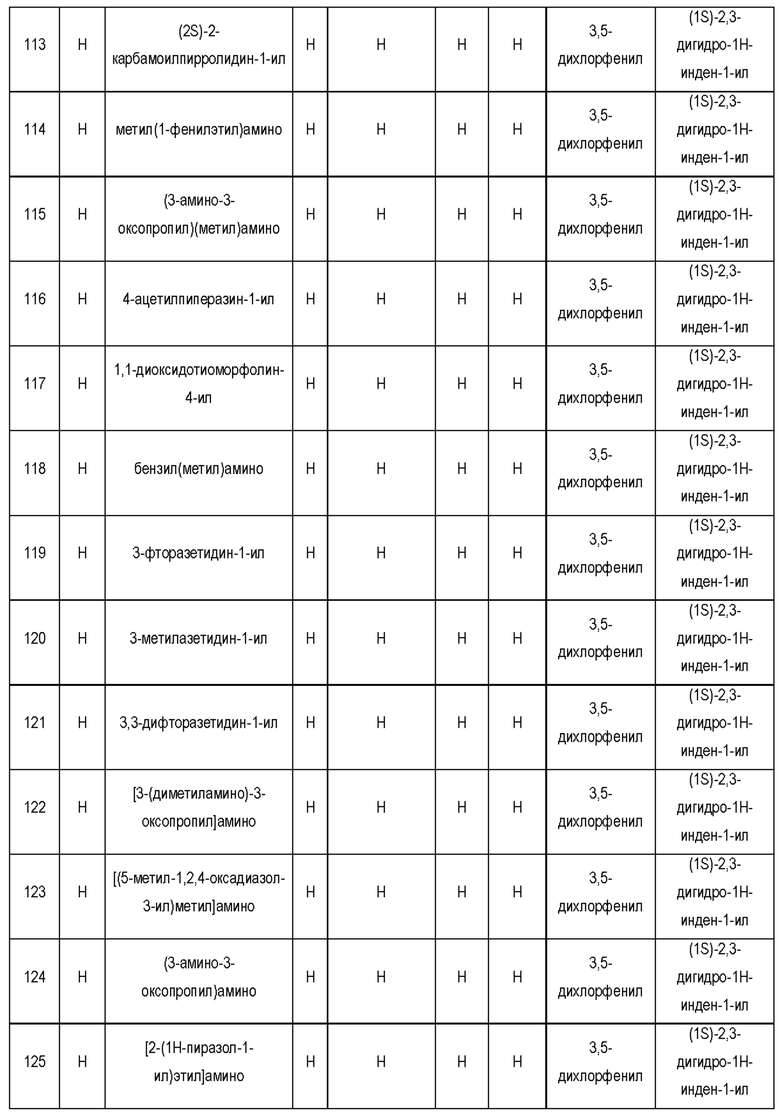
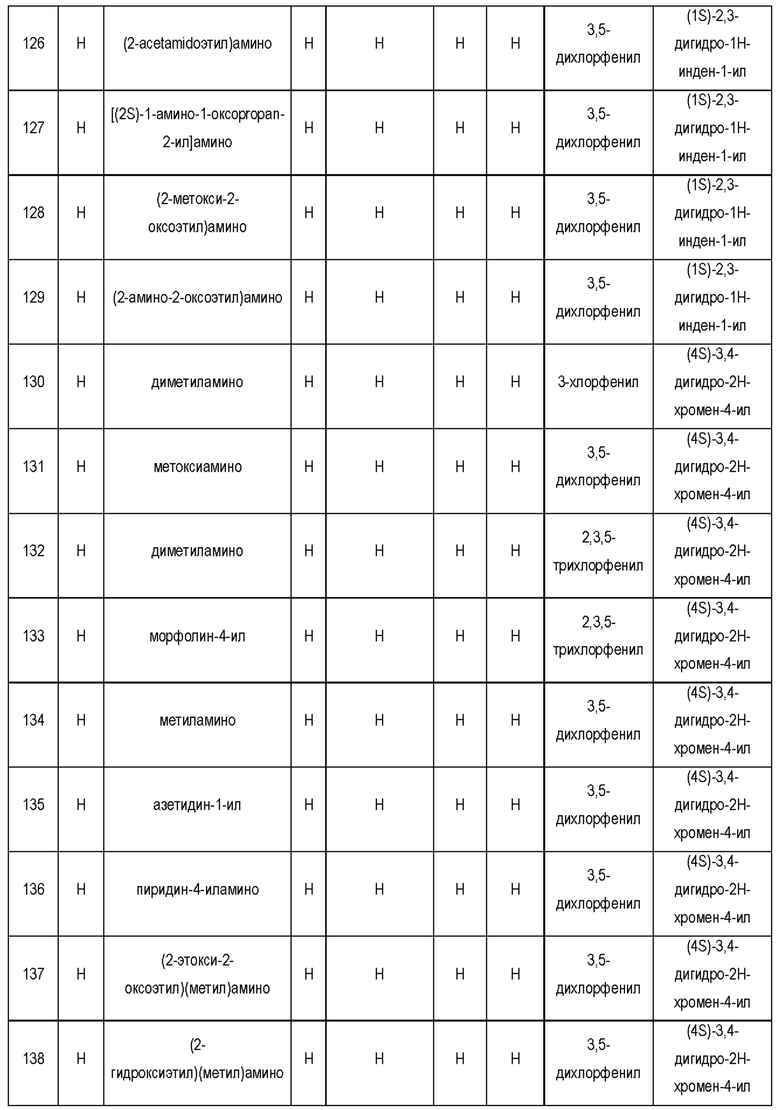
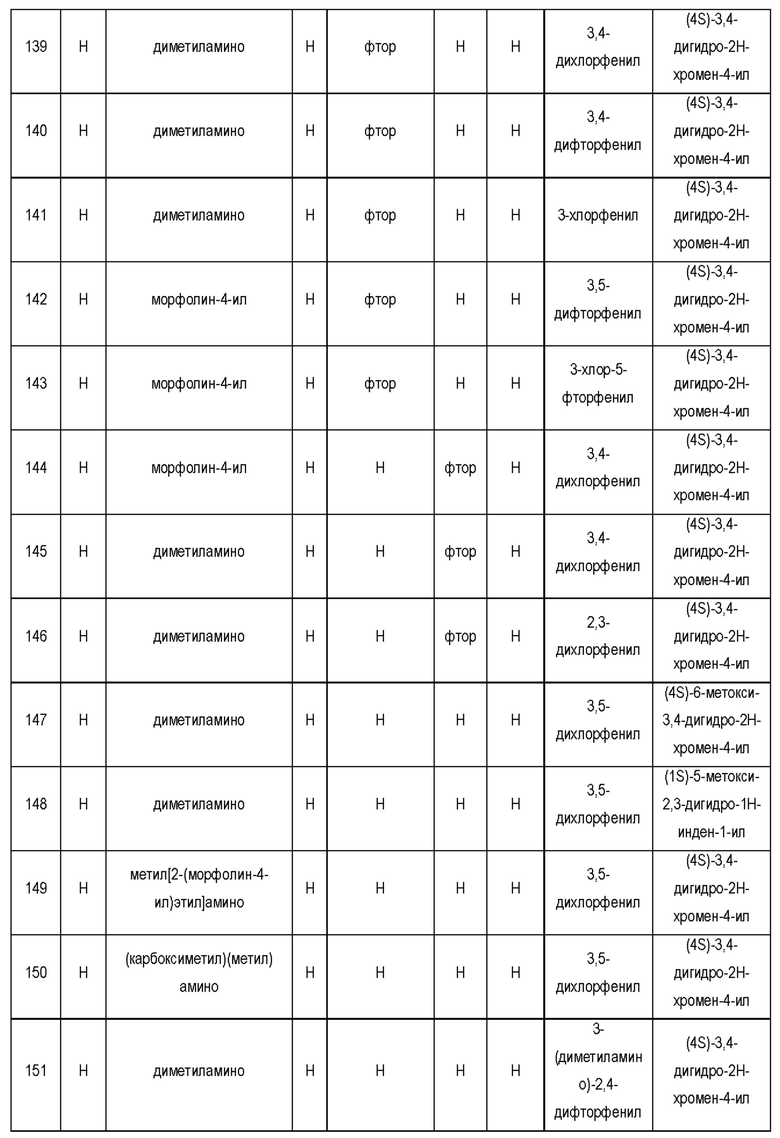
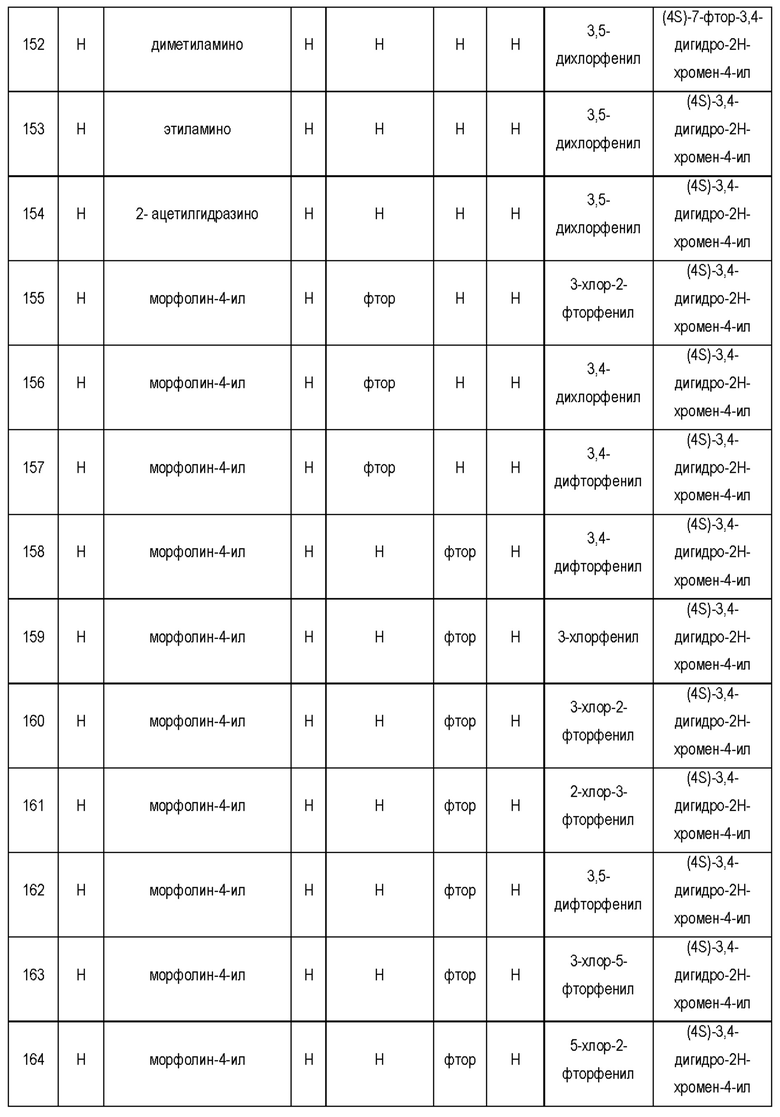
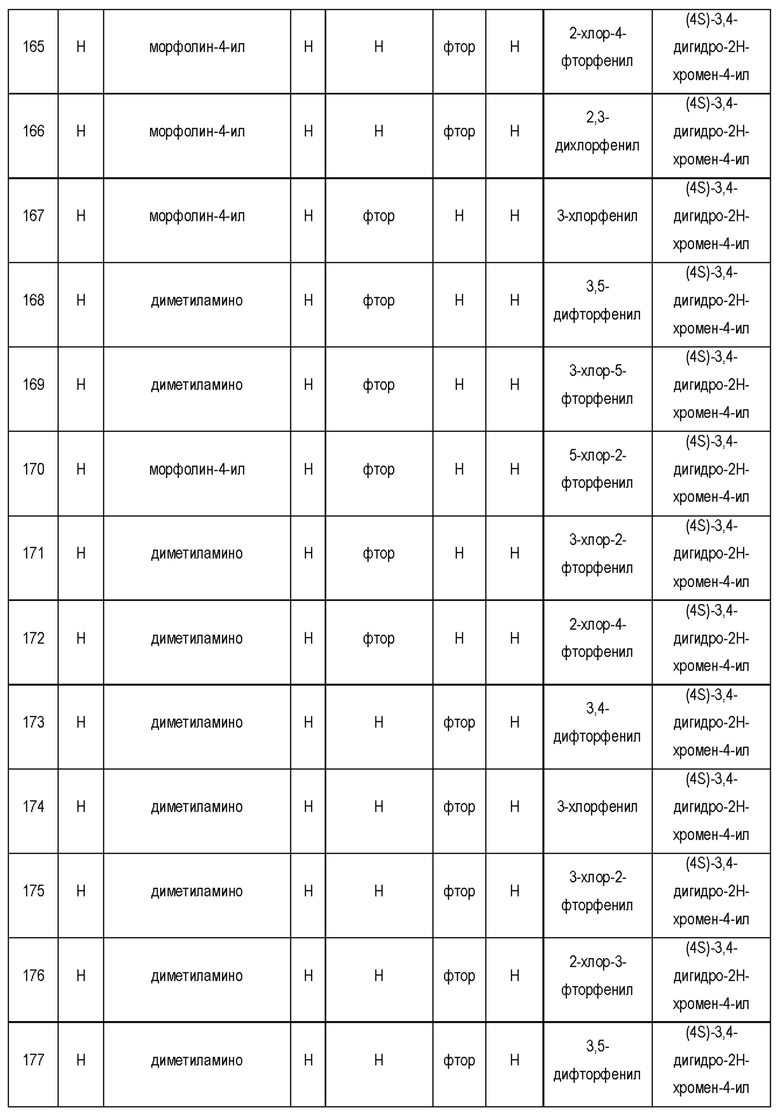
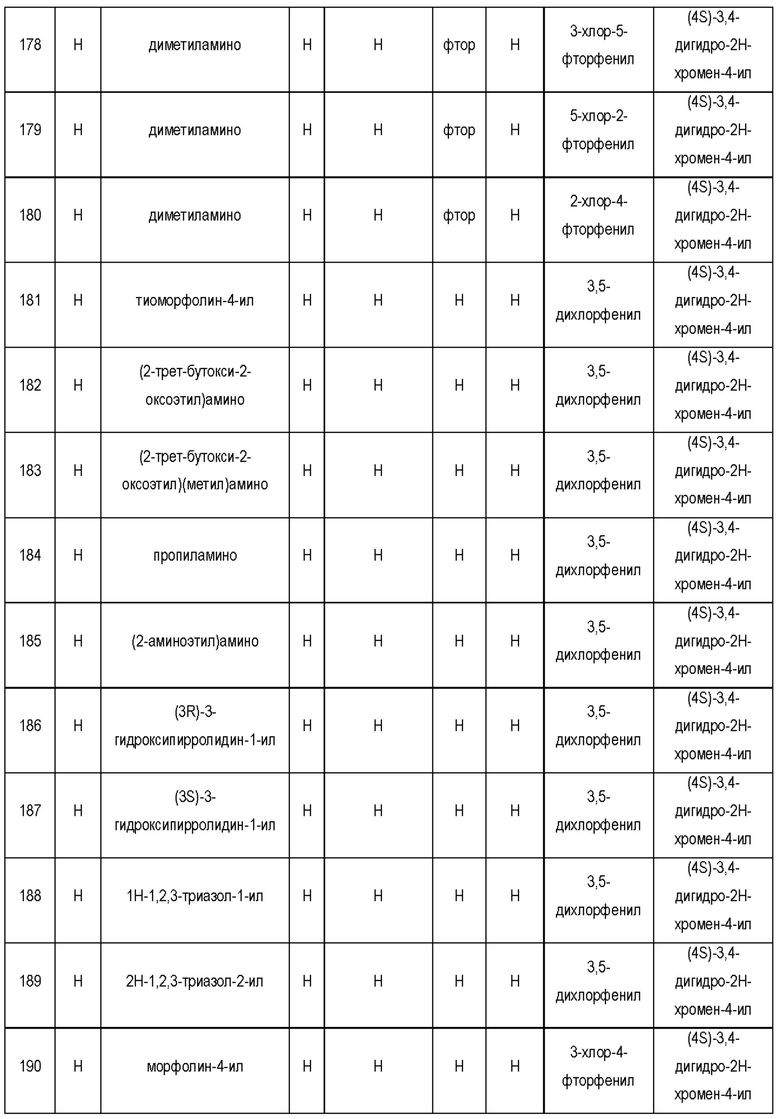
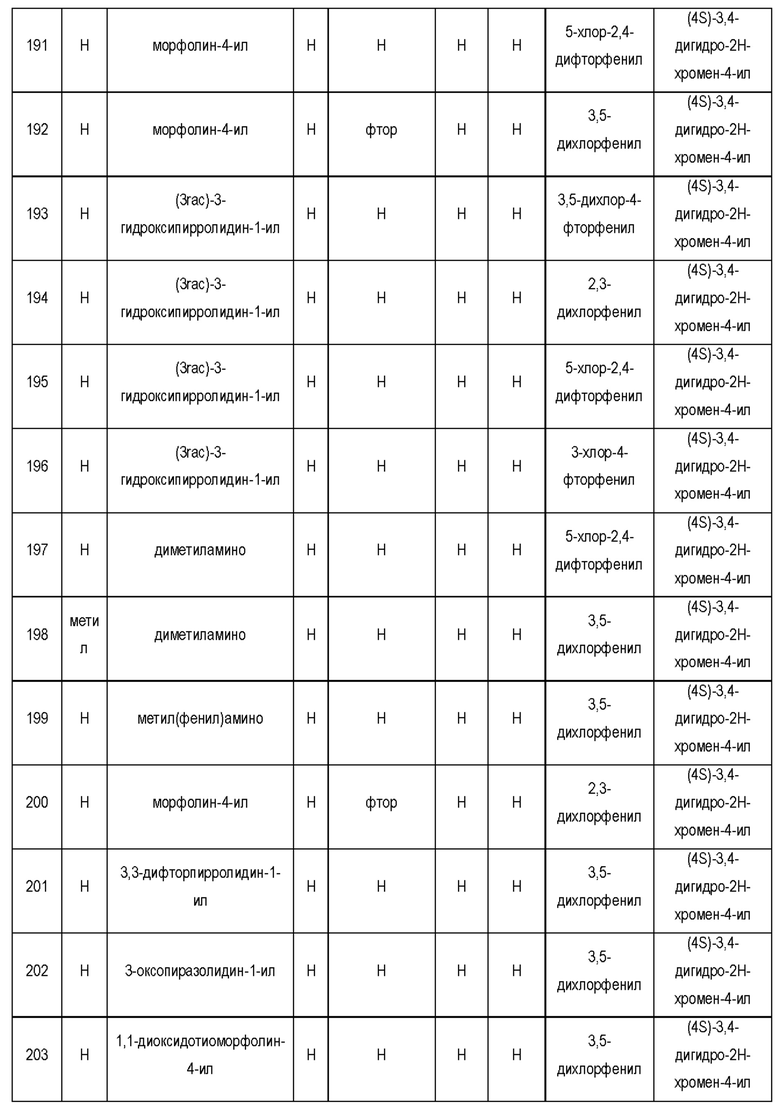
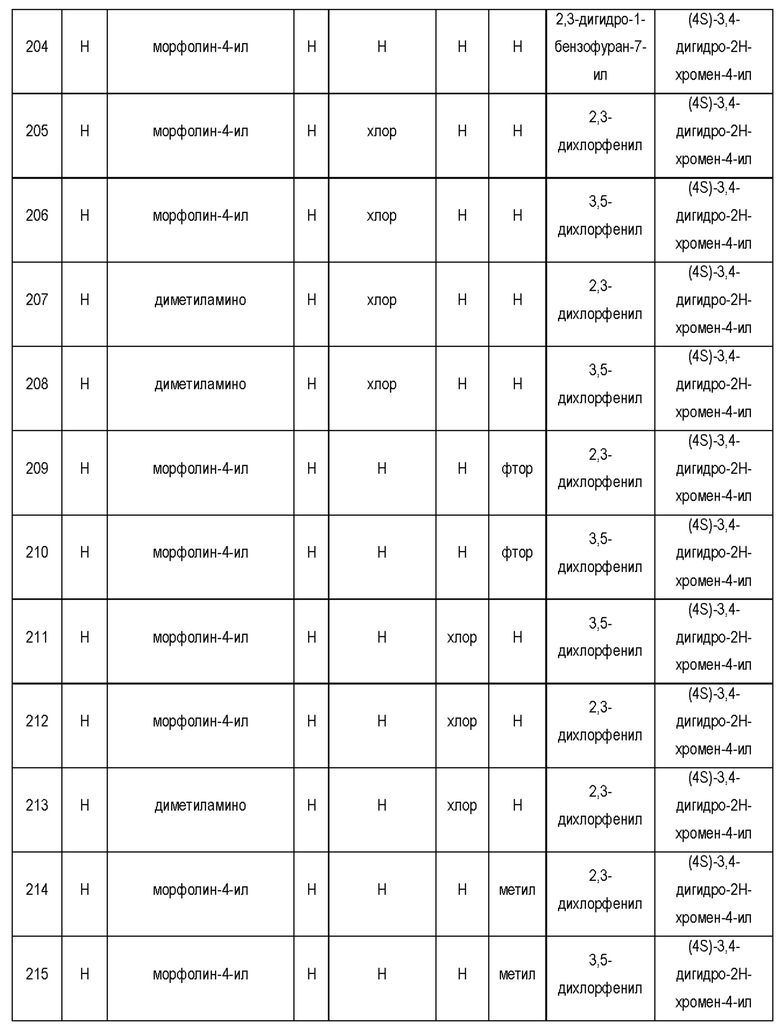
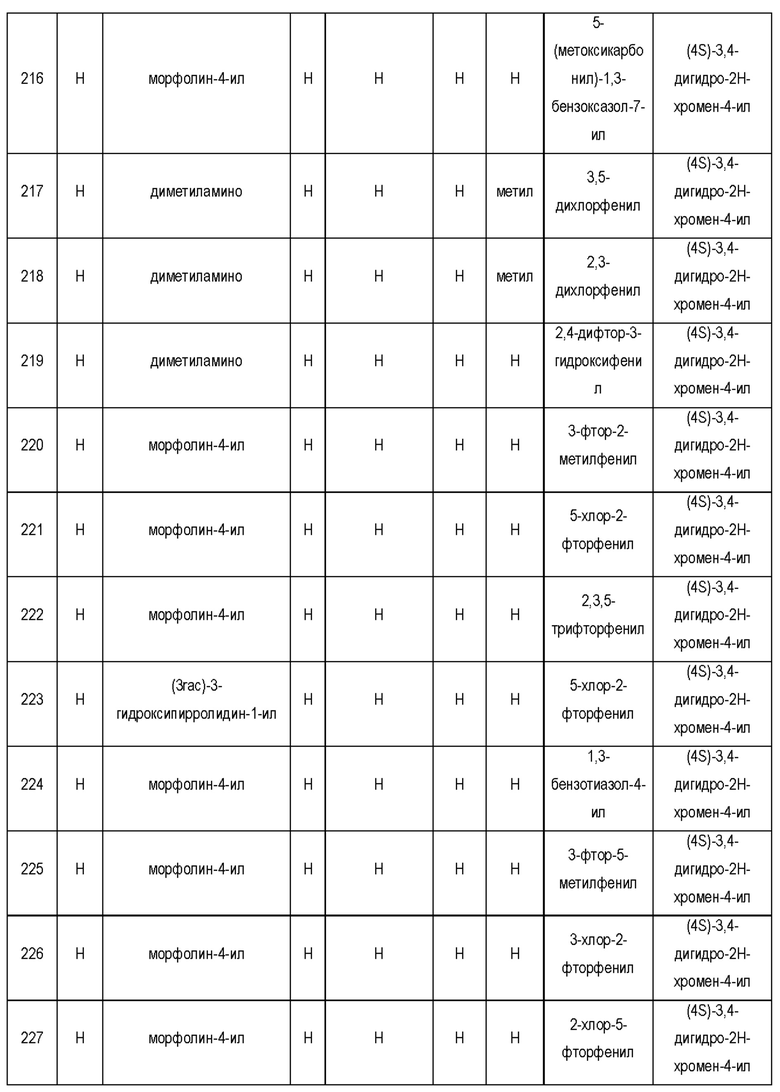
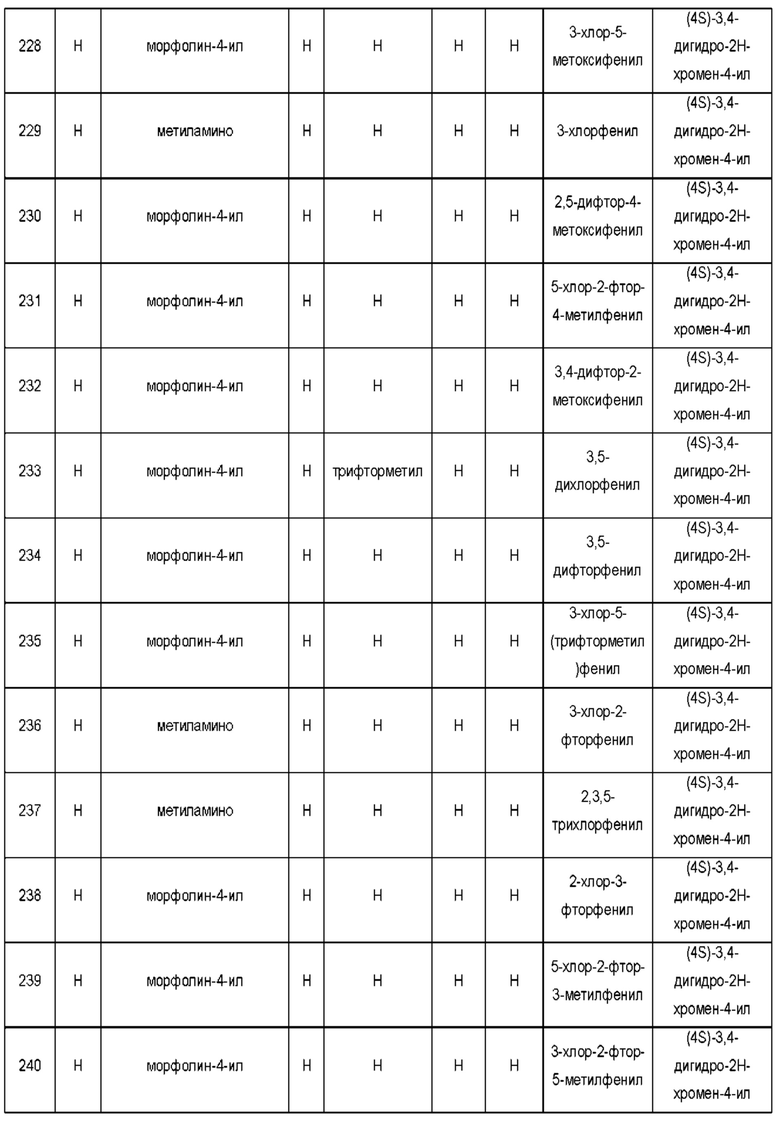
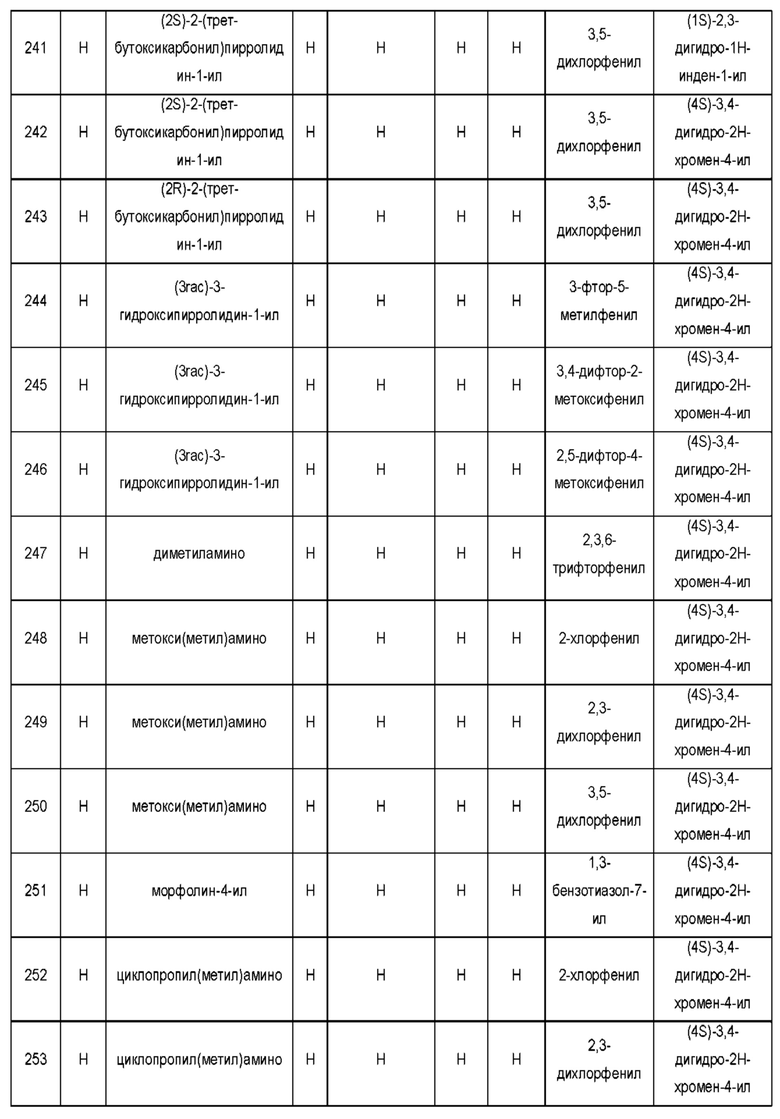
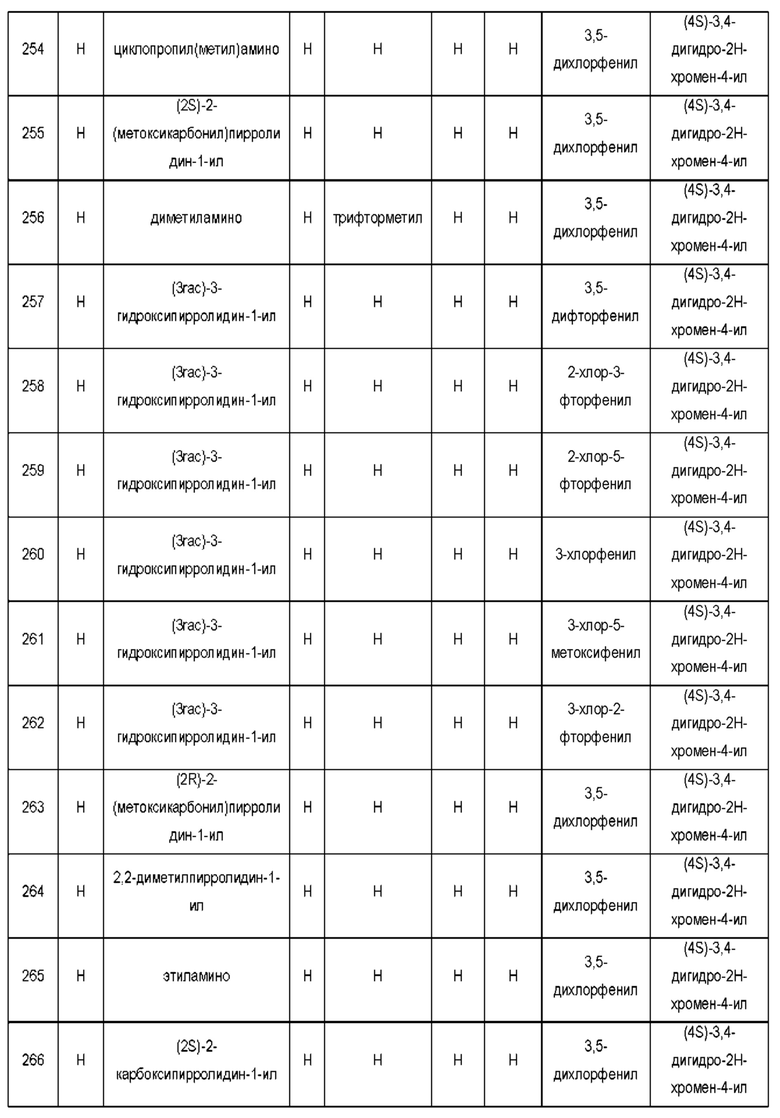
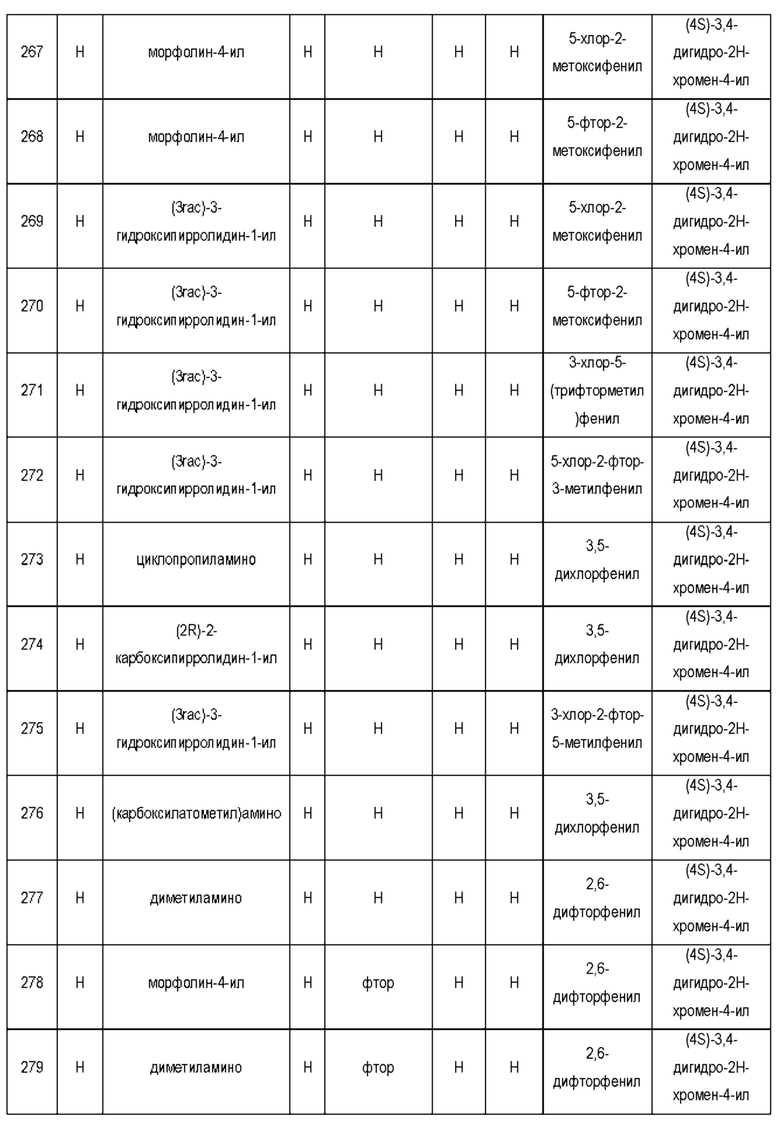
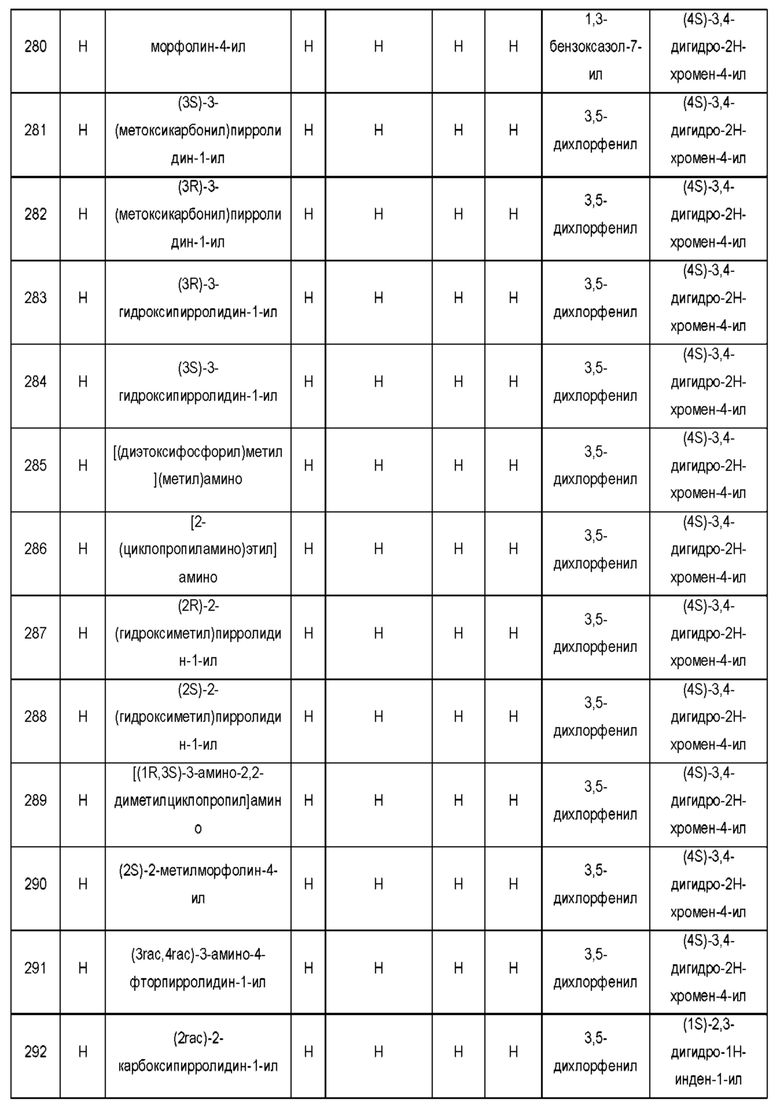
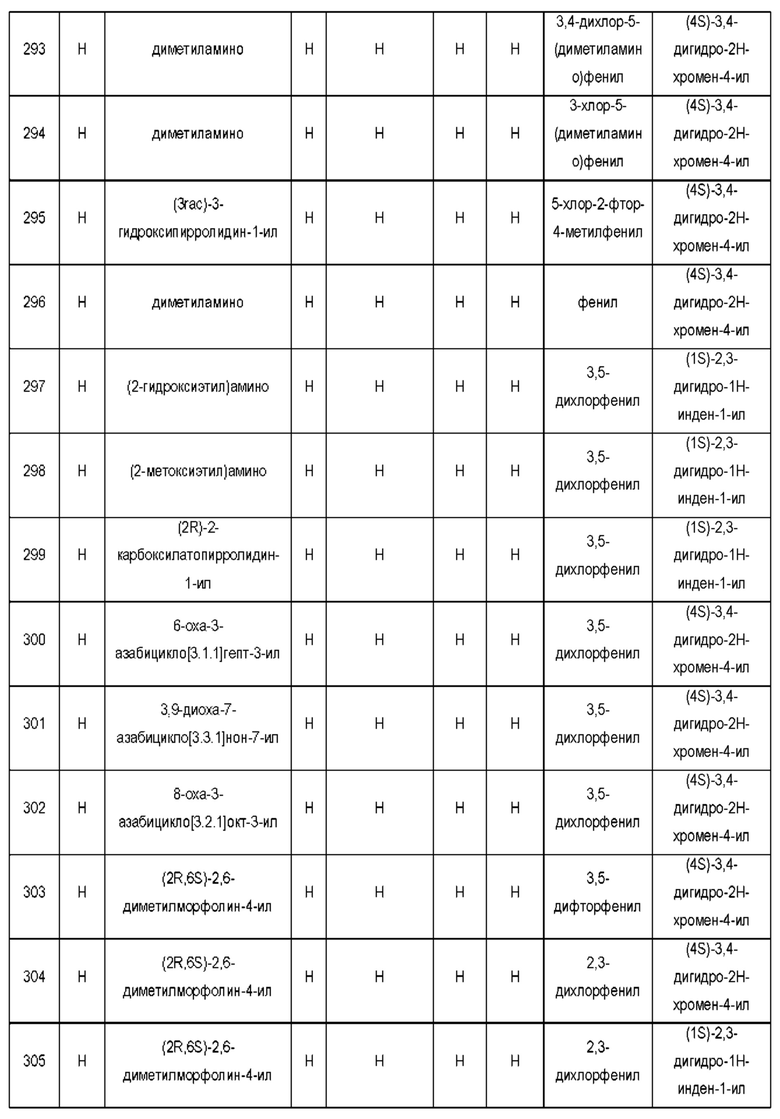
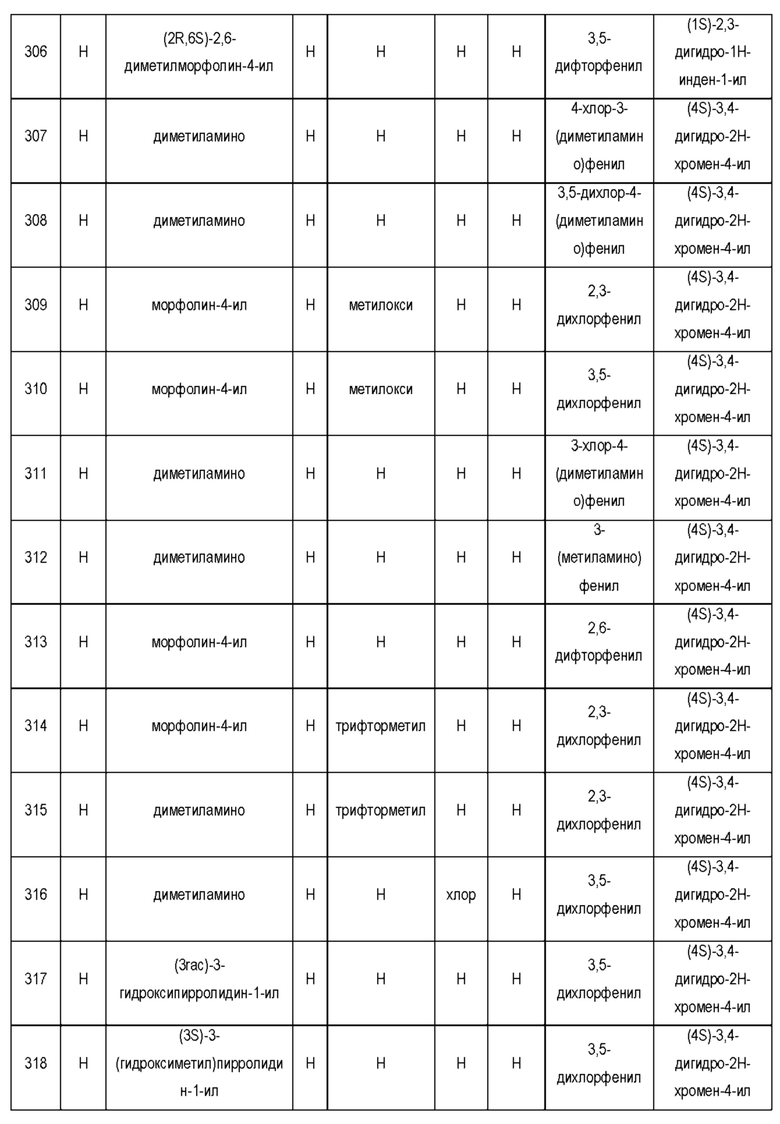
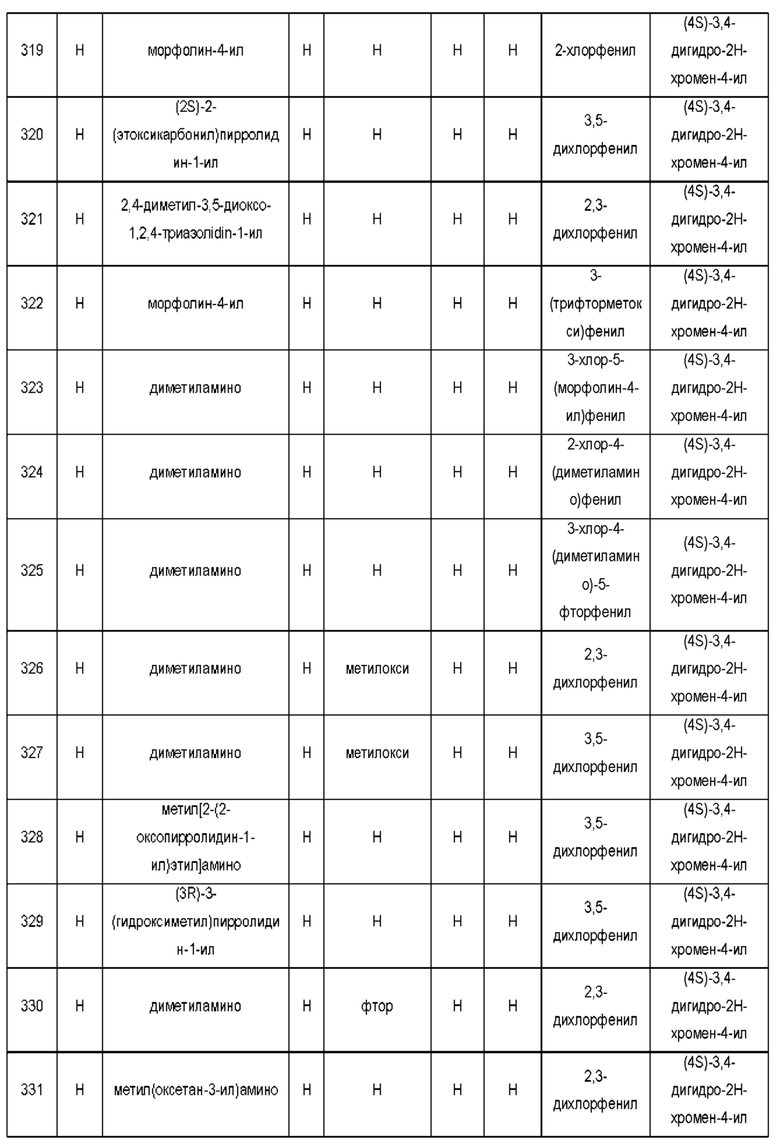
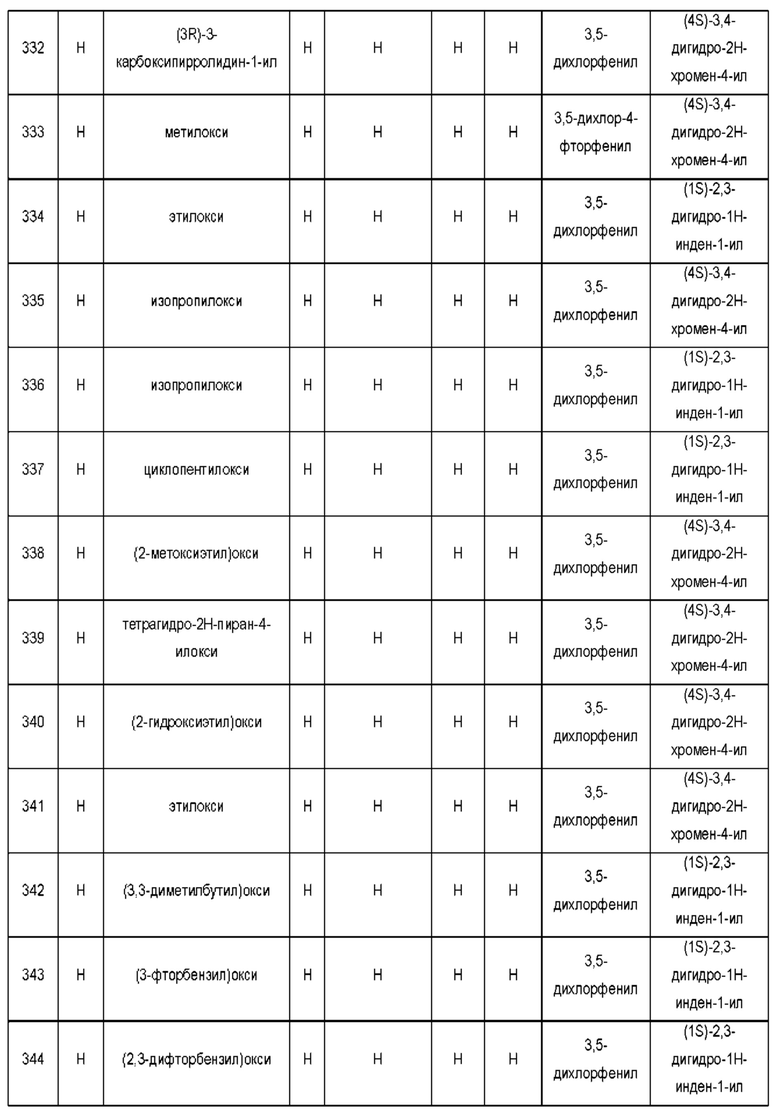
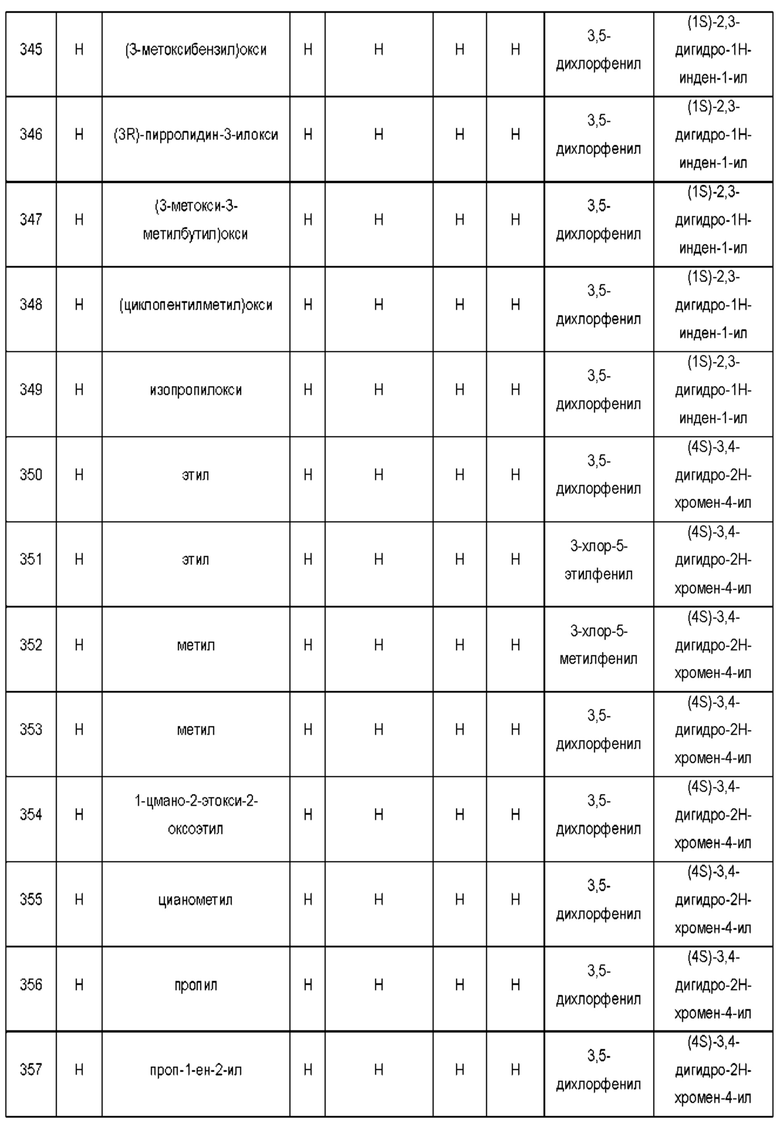
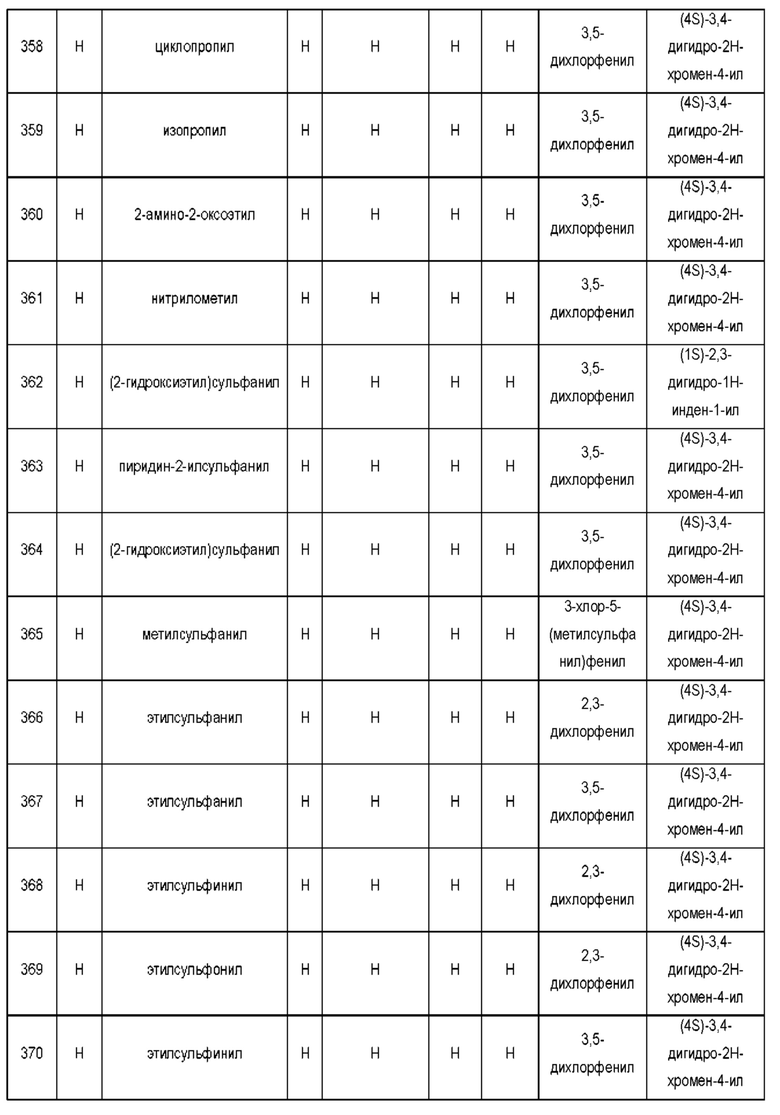
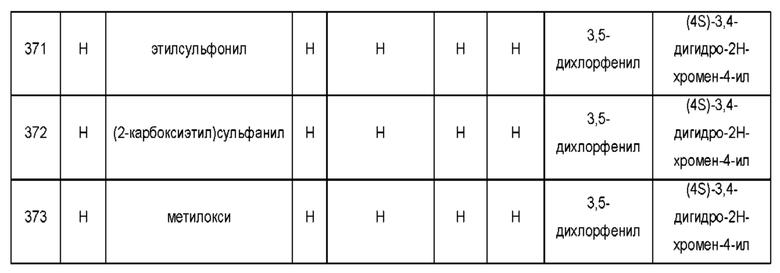
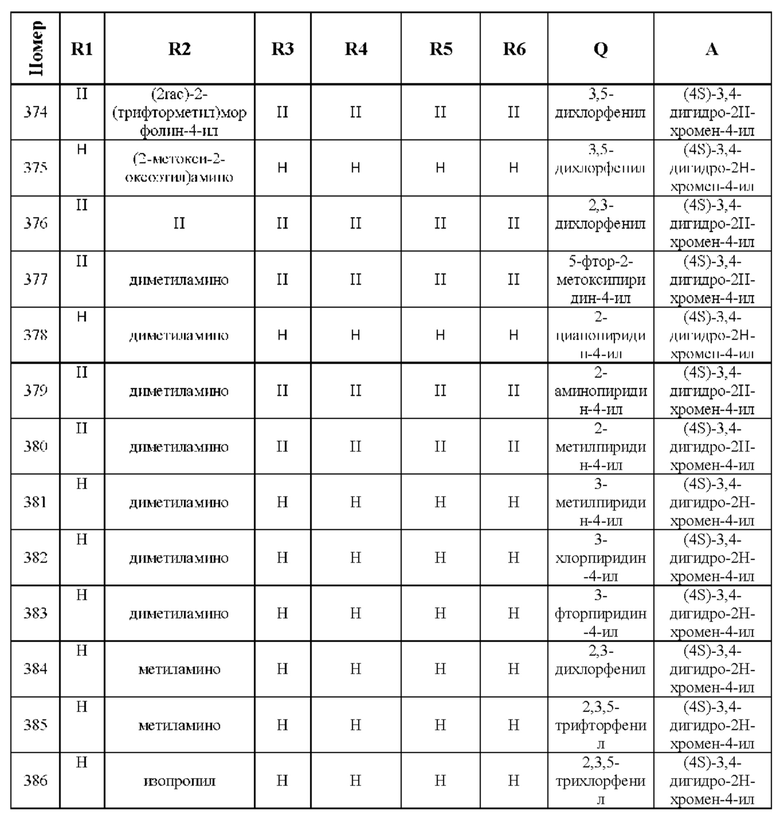
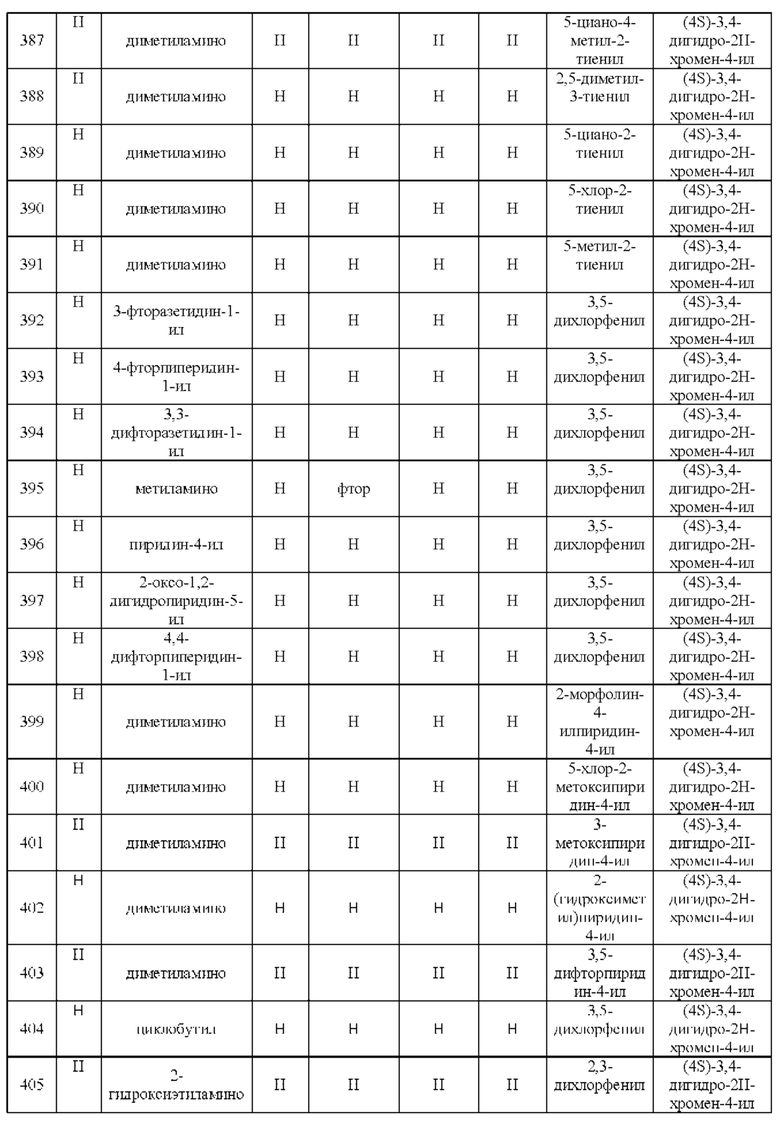
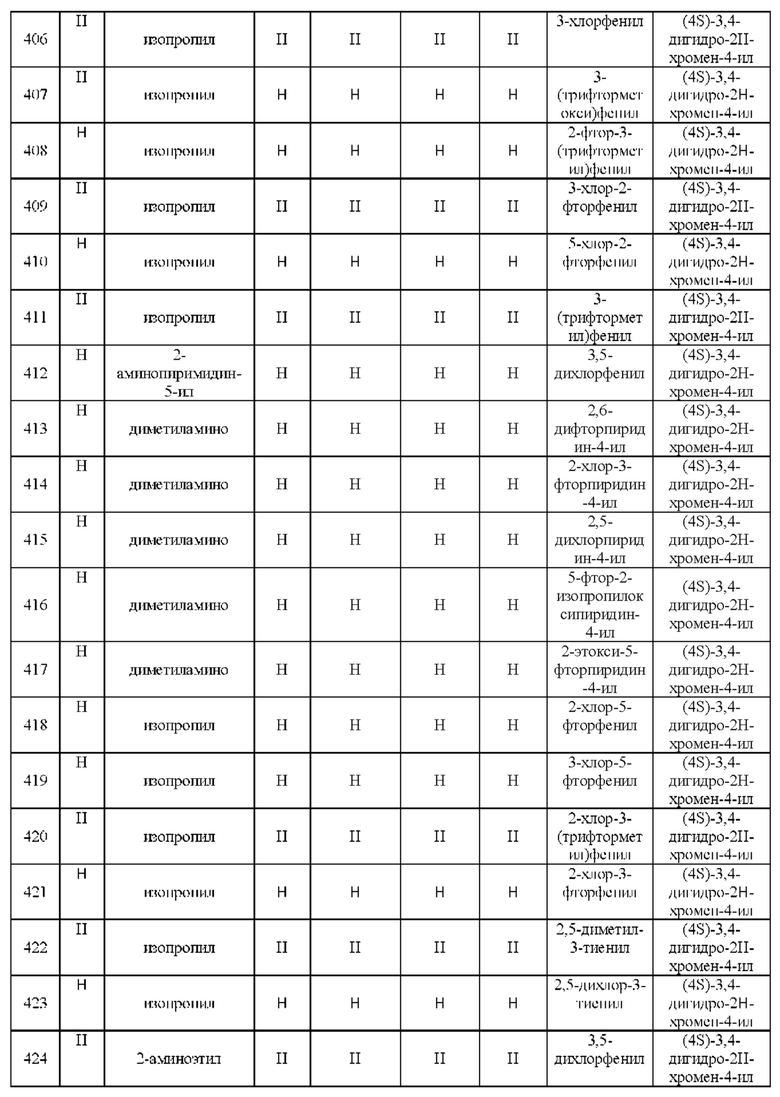
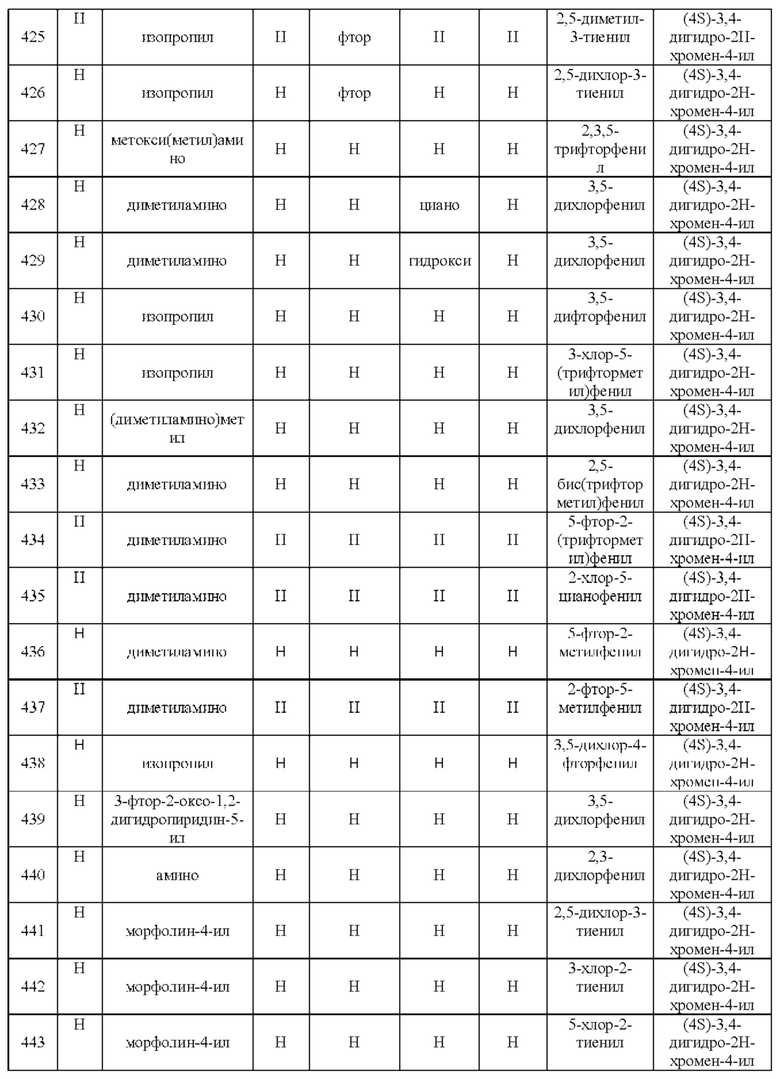
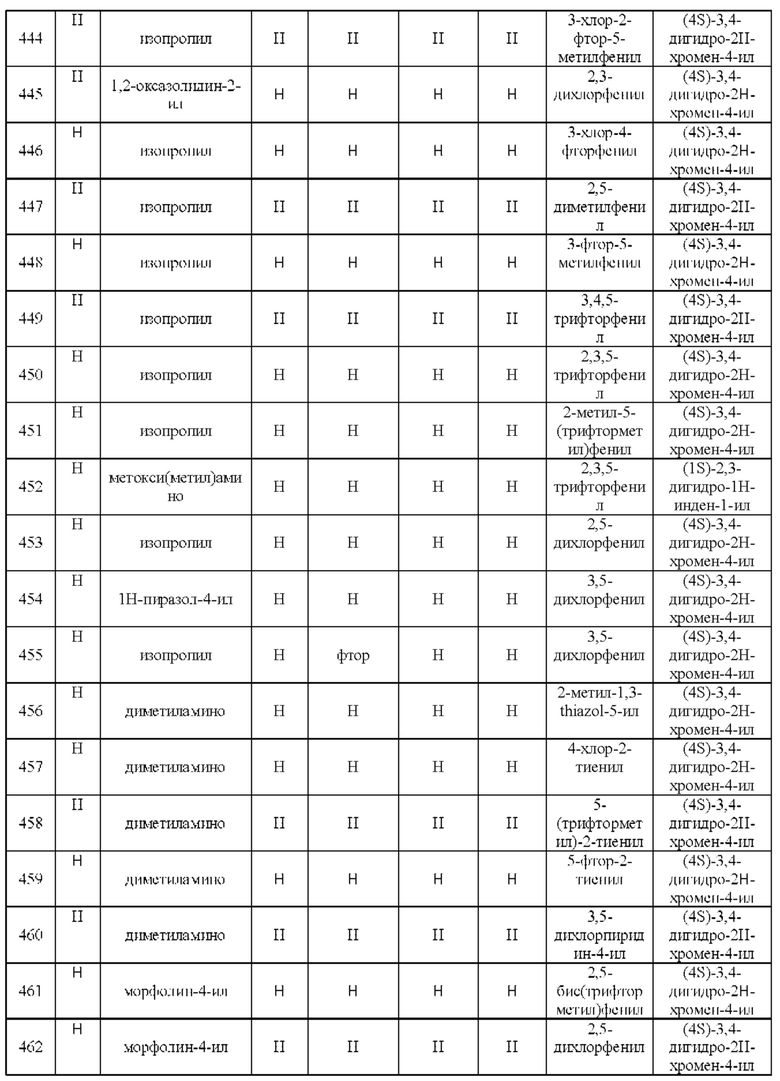
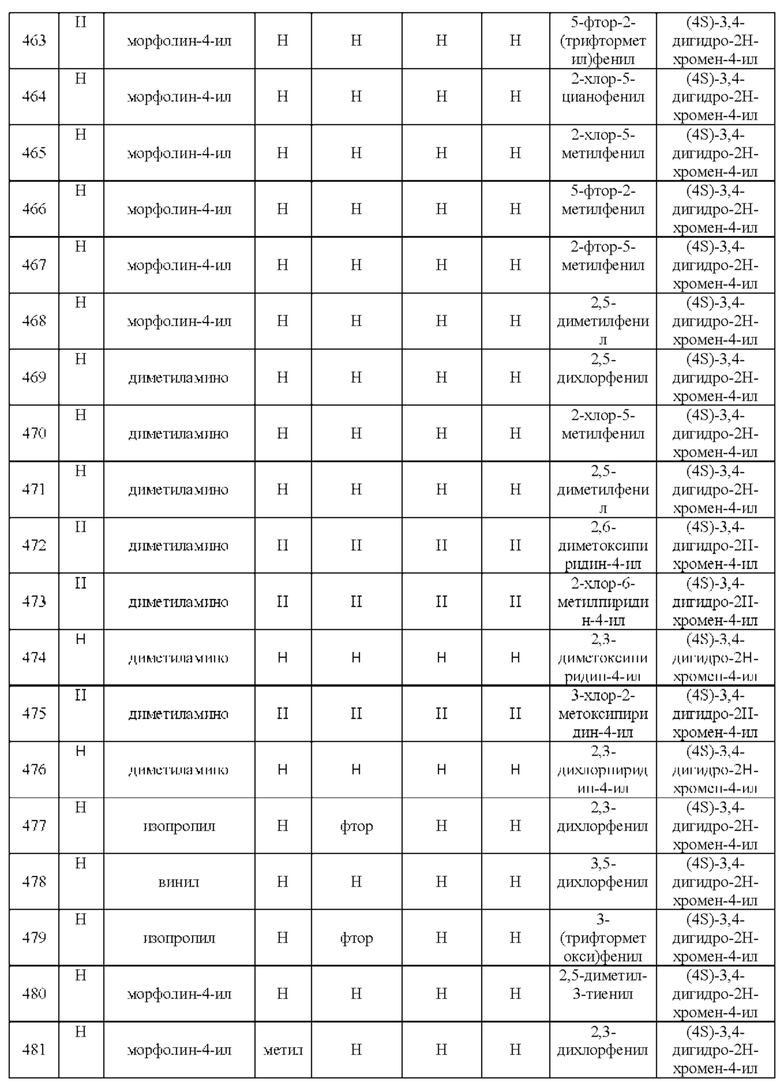
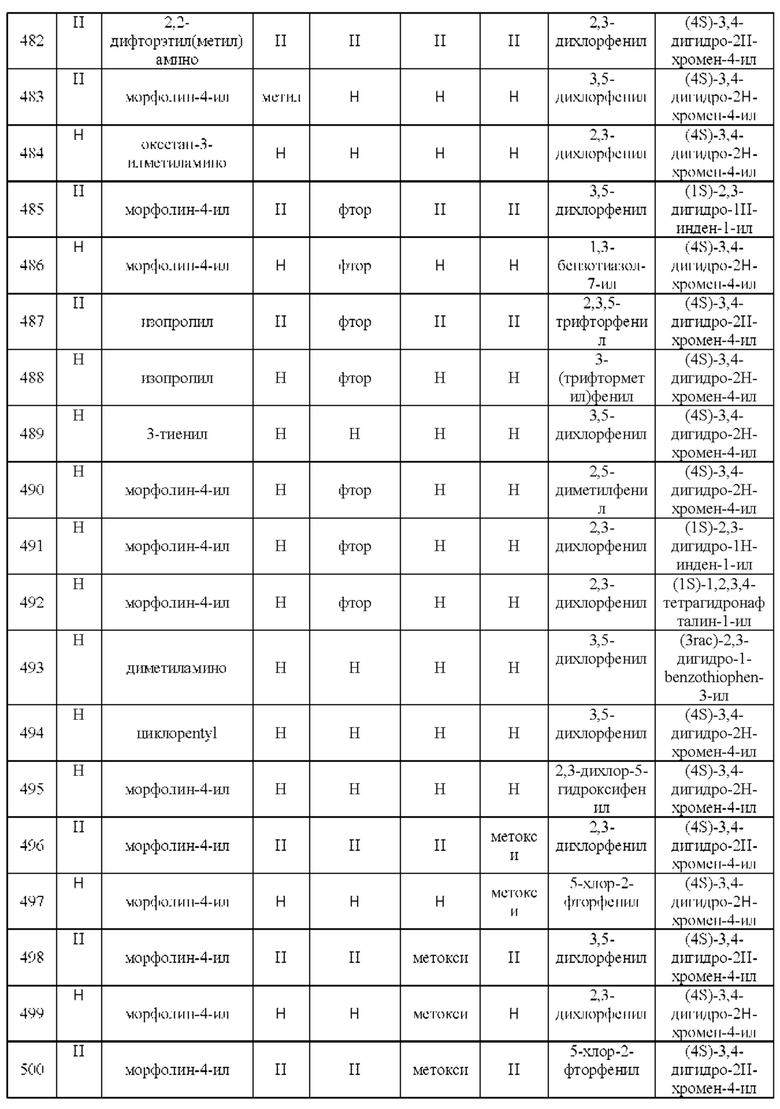
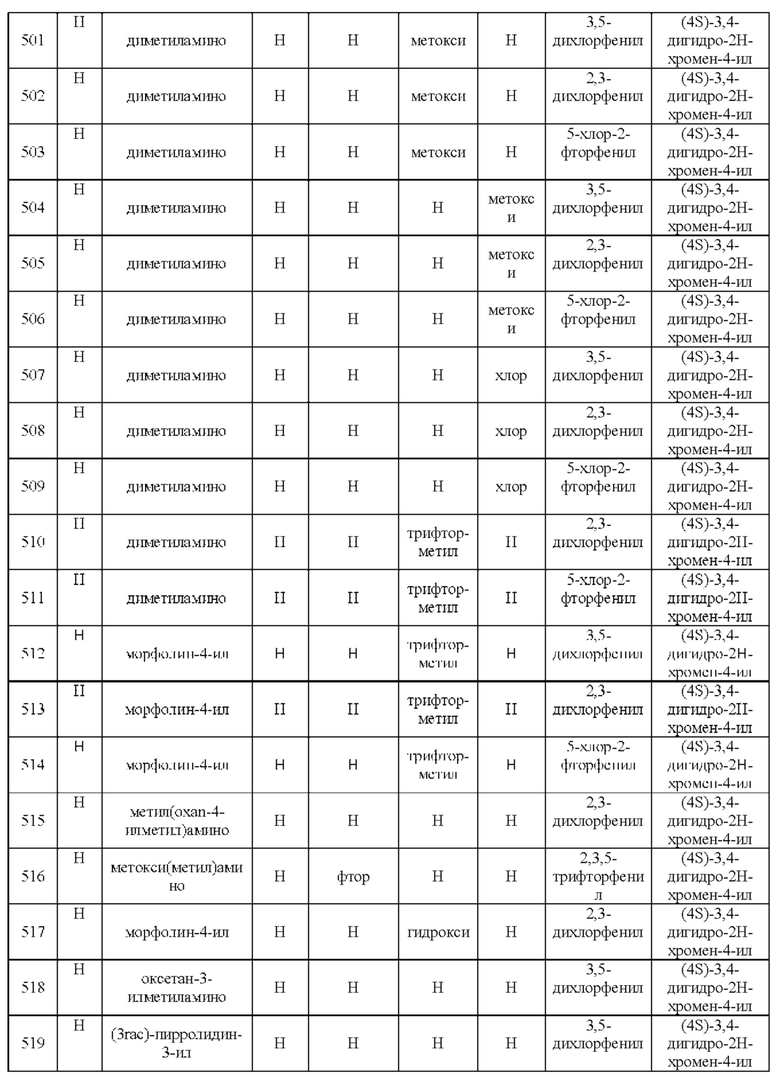
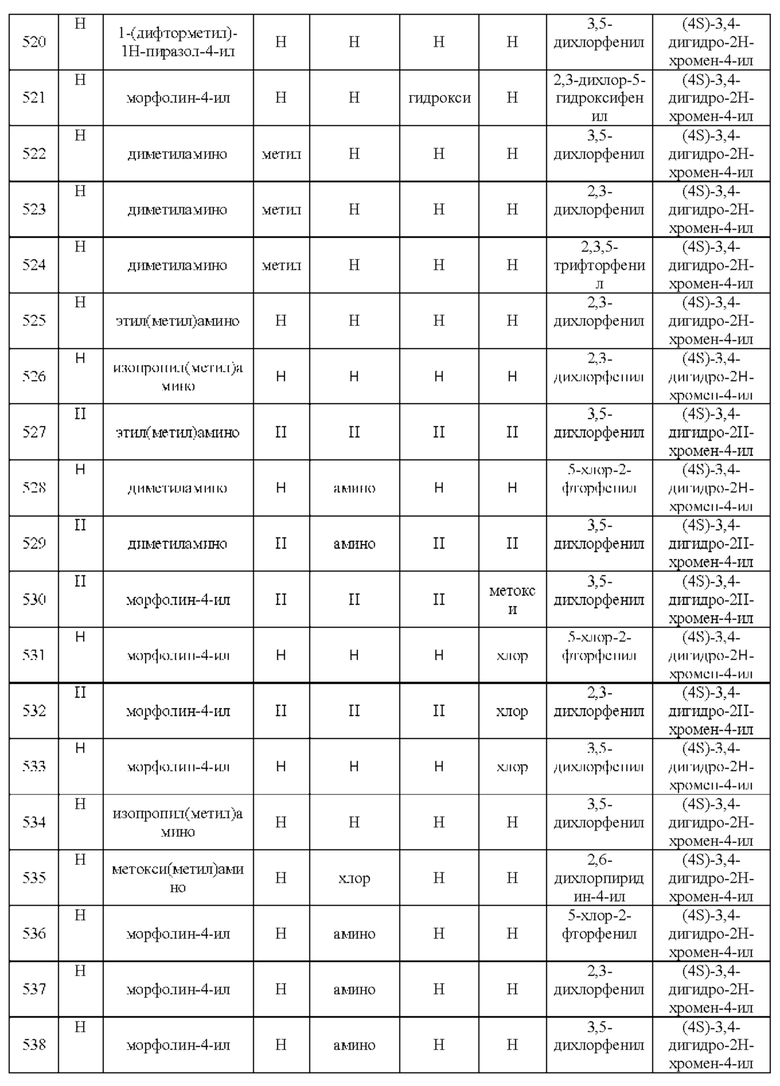
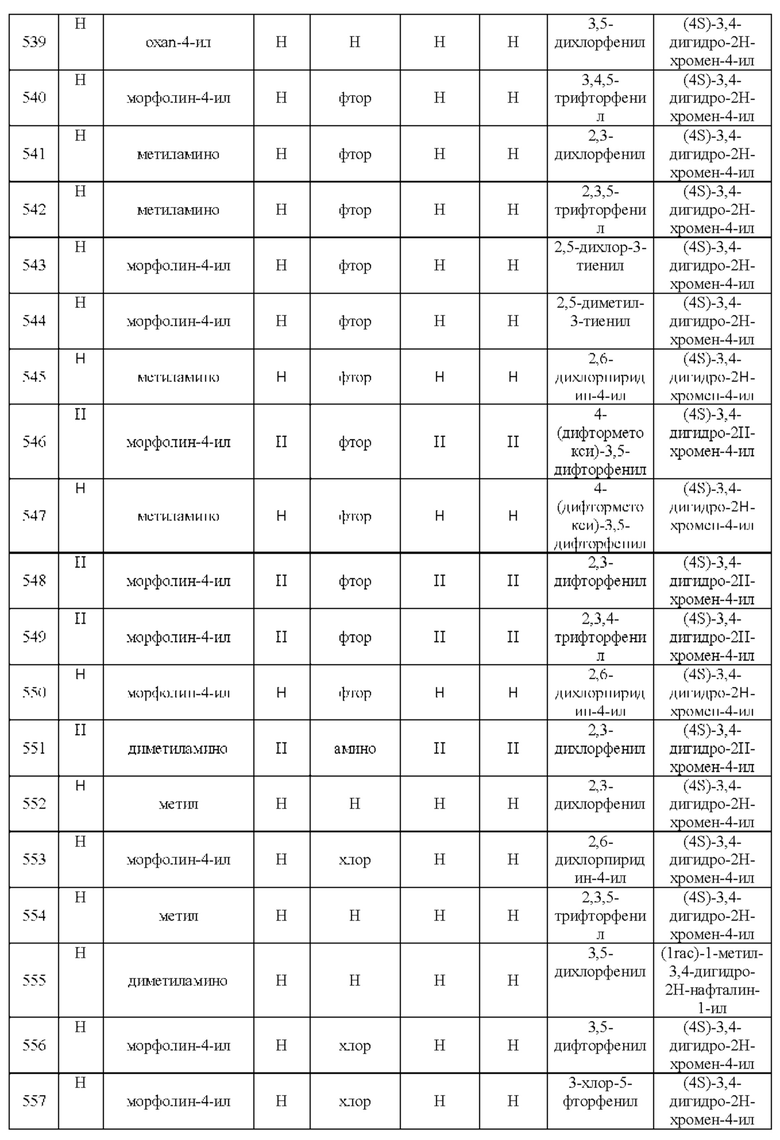
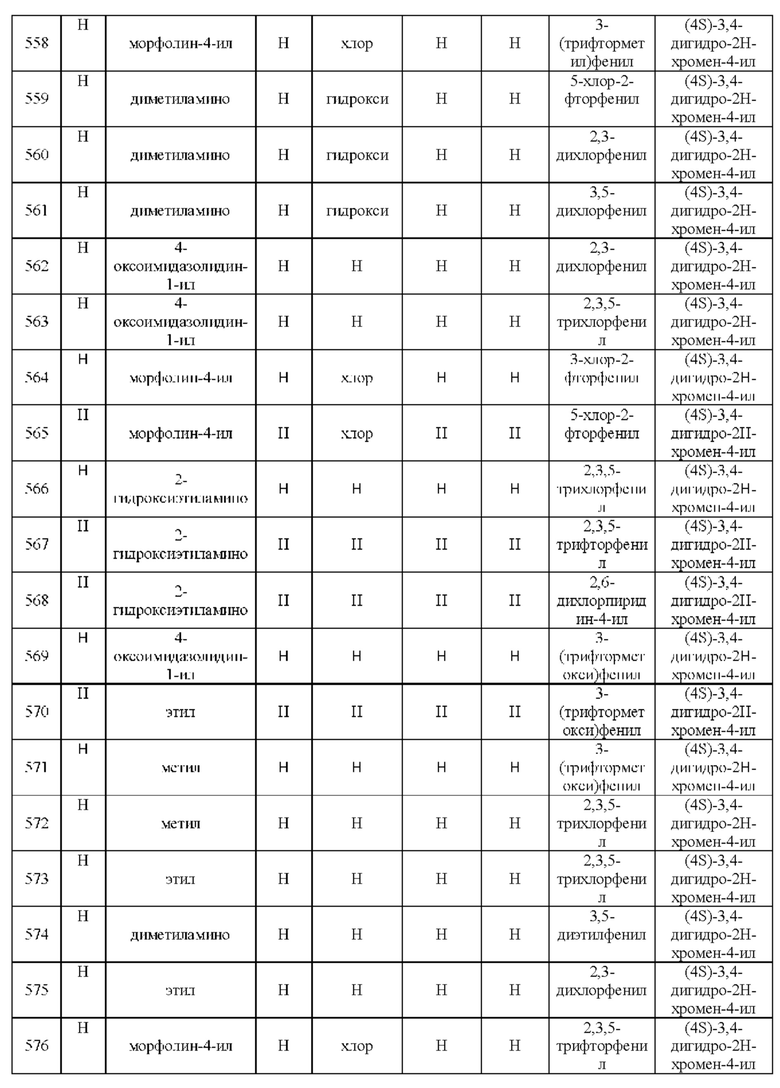
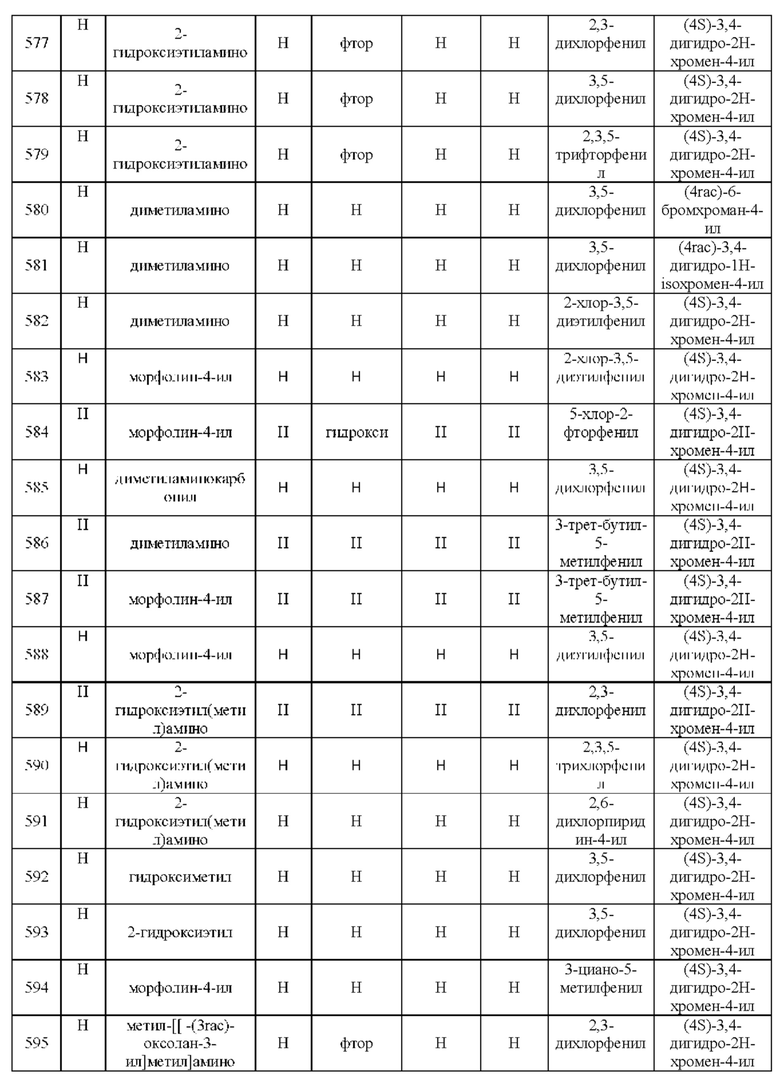
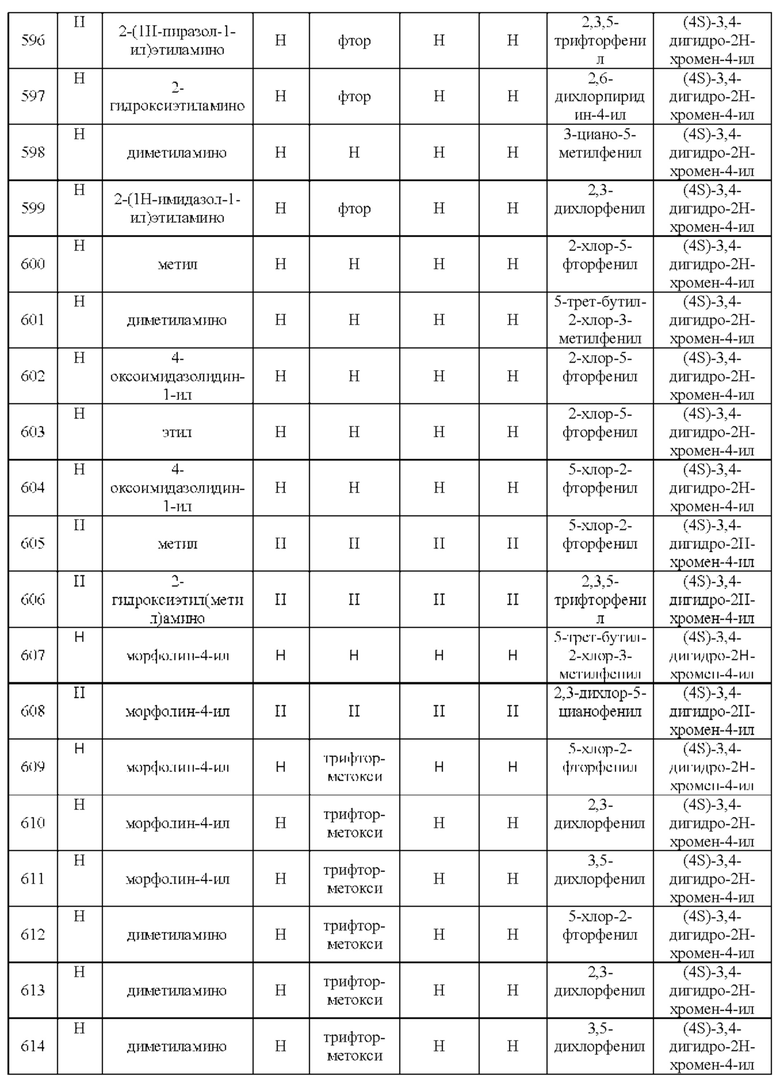
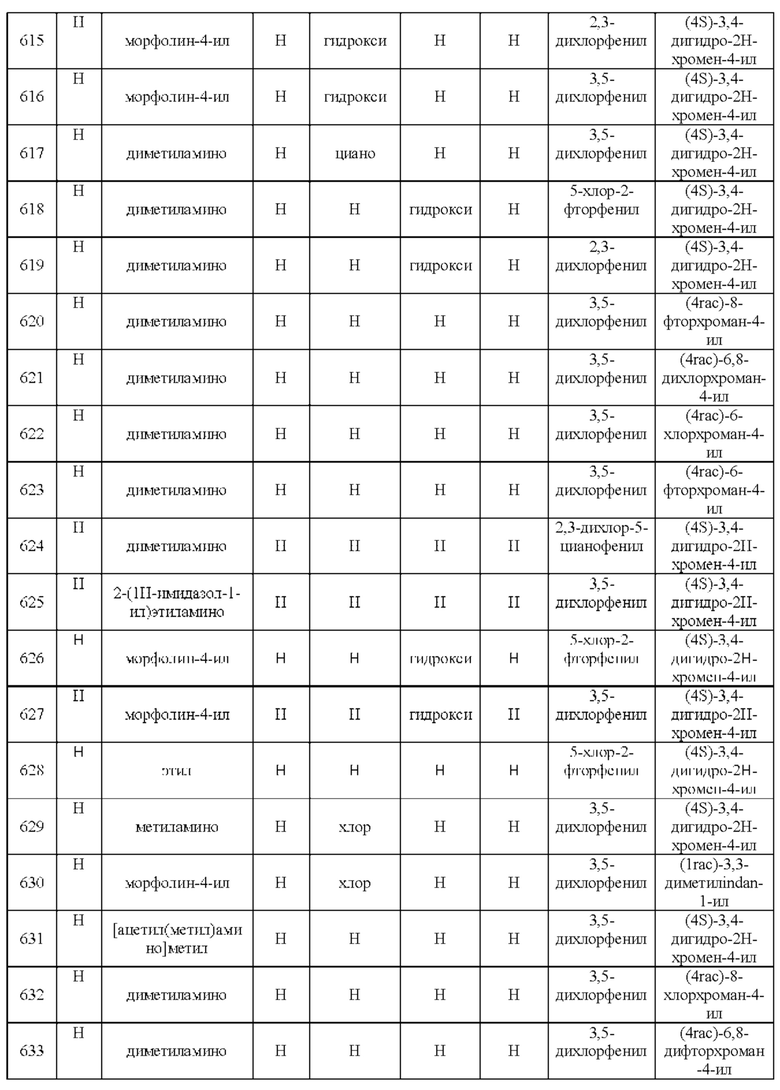
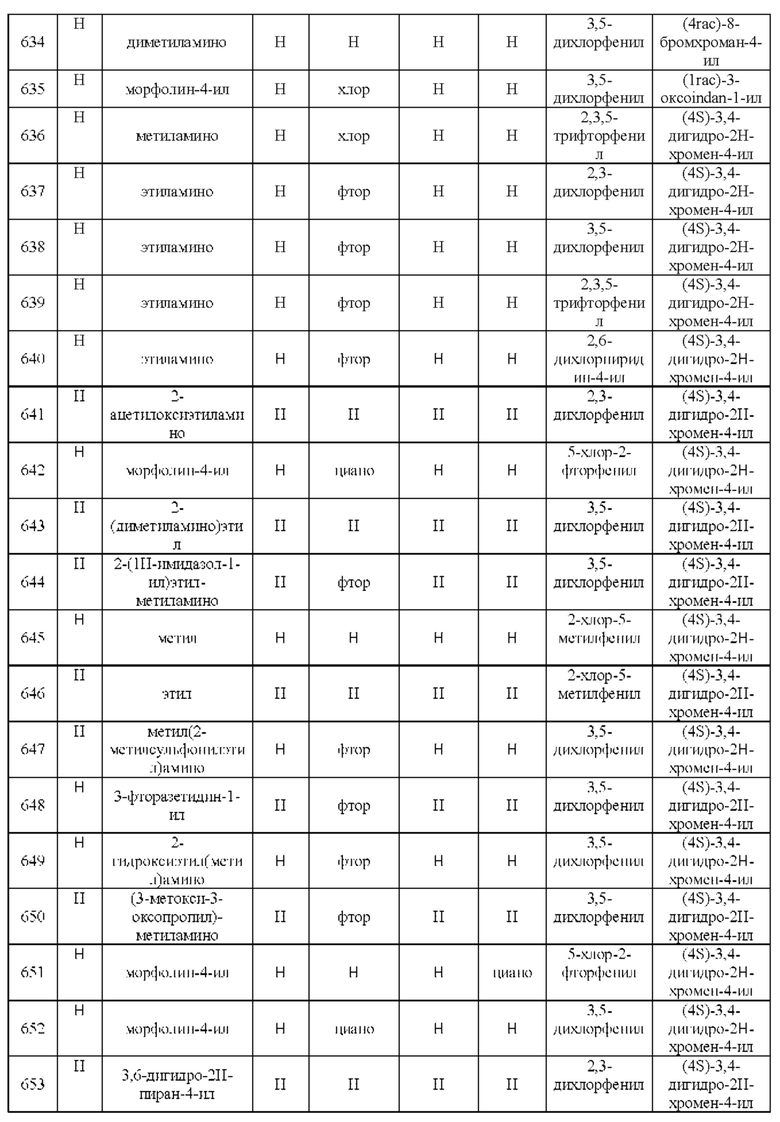
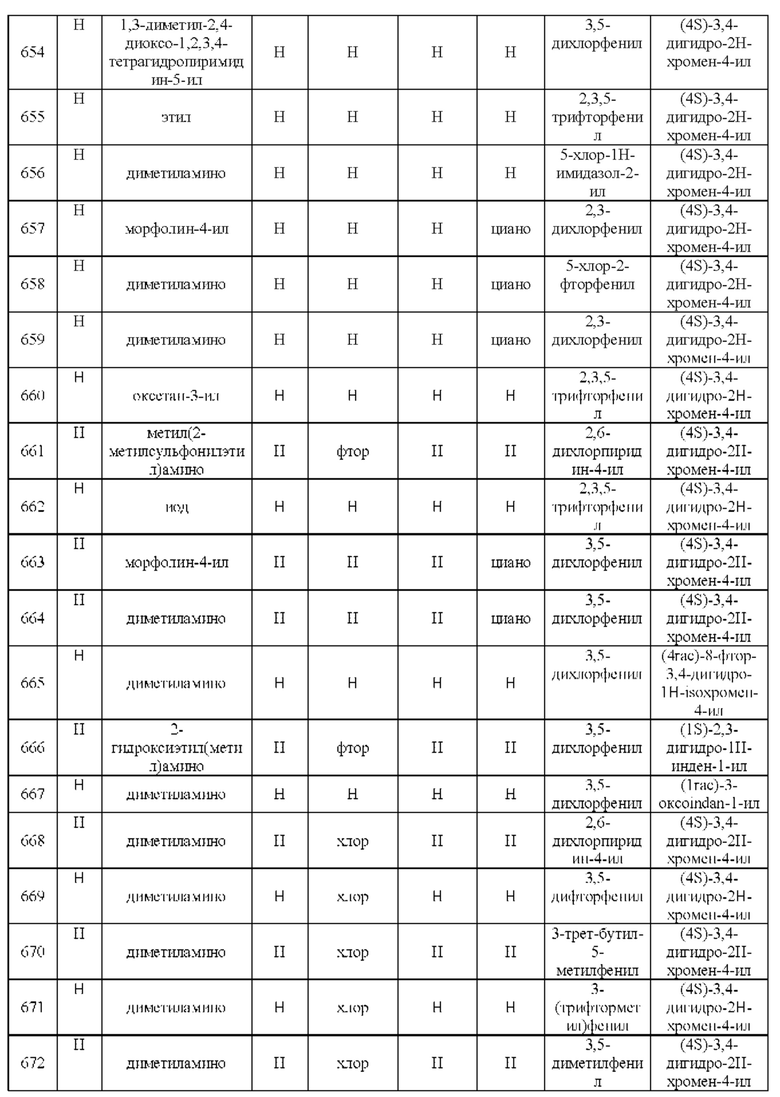
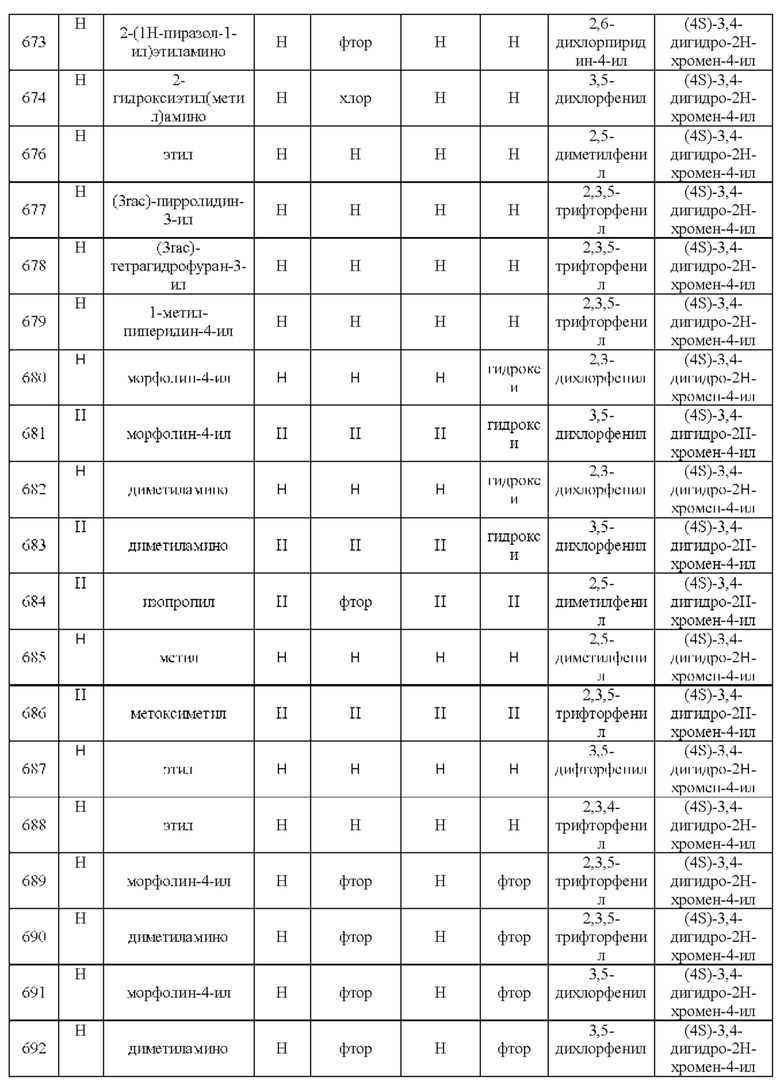
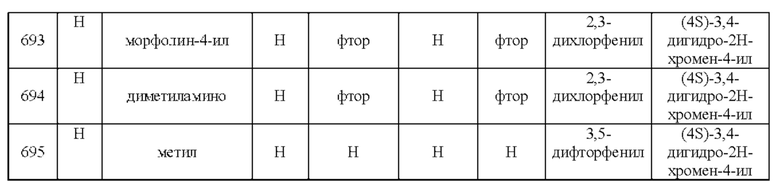
Таблица 2: LC-MS и ЯМР данные
Формы пиков ЯМР указаны по мере их появления в спектрах, возможные эффекты более высокого порядка не рассматривались.
Перечень ЯМР пиков
Данные 1H-ЯМР выбранных примеров записаны в виде списков сигналов 1H-ЯМР. Для каждого сигнала, перечислены δ-значение в ppm и интенсивность сигнала в круглых скобках. Между парами δ-значений и значений интенсивности стоят точка с запятой в качестве разделителей.
Пример списка сигналов имеет поэтому вид:
δ1 (интенсивность1); δ2 (интенсивность2); …; δi (интенсивностьi); …; δn (интенсивностьn) или
δ1 (интенсивность1), δ2 (интенсивность2), …; δi (интенсивностьi), …, δn (интенсивностьn)
Интенсивность узких сигналов коррелирует с высотой сигналов в печатном примере ЯМР-спектра в см и показывает реальные отношения интенсивностей сигналов. Из широких сигналов несколько пиков или середина сигнала и их относительная интенсивность в сравнении с наиболее интенсивным сигналом могут быть показаны.
Для калибровки химического сдвига для спектров 1Н, мы использовали тетраметилсилан и/или химический сдвиг растворителя, используемого, в частности, в случае спектров, измеренных в ДМСО. Поэтому в списки сигналов ЯМР может входить пик тетраметилсилана, но не обязательно.
Списки сигналов 1H-ЯМР аналогичны классическим 1Н-ЯМР и содержат поэтому, как правило, все пики, которые перечислены в классической ЯМР-интерпретации.
Кроме того, они могут показать аналогичные классическим 1H-ЯМР сигналам растворителей, стереоизомеров целевых соединений, которые также являются объектом настоящего изобретения, и/или пики примесей.
Для того, чтобы показать сигналы в дельта-диапазоне растворителей и/или воды, обычные пики растворителей, например, пики ДМСО в ДМСО-D6 и пик воды показаны в наших списках сигналов 1H-ЯМР и имеют, как правило, в среднем высокую интенсивность.
Пики стереоизомеров целевых соединений и/или пики примесей обычно имеют в среднем более низкую интенсивность, чем пики целевых соединений (например, с чистотой >90%).
Такие стереоизомеры и/или примеси могут быть типичными для конкретного процесса получения. Поэтому их пики могут помочь идентифицировать воспроизводимость нашего процесса получения с помощью "отпечатков пальцев побочных продуктов".
Эксперт, который рассчитывает пики целевых соединений с помощью известных способов (MestreC, ACD-моделирования, но также и с эмпирически оцененных средних значений) может выделить пики целевых соединений при необходимости, используя дополнительные фильтры интенсивности. Такое выделение будет аналогично соответствующему пику классической интерпретации 1H-ЯМР.
Дальнейшие подробности описания ЯМР-данных со списками пиков можно найти в публикации "Citation of NMR Peaklist Data within Patent Applications" в Research Disclosure Database Number 564025.
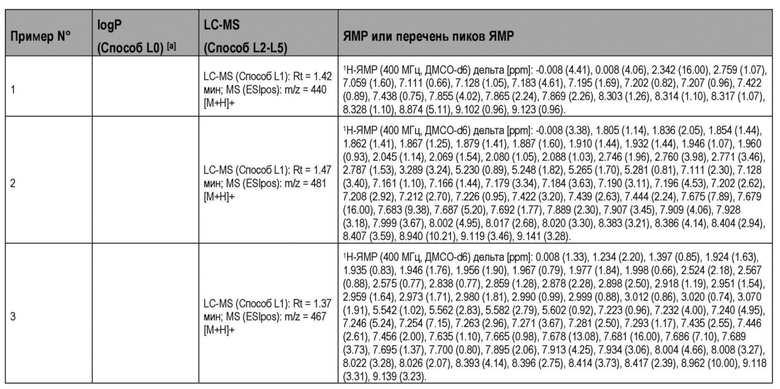
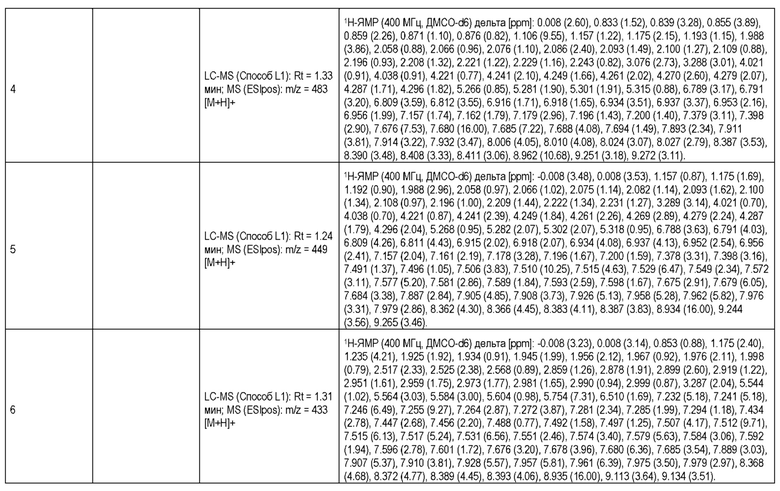
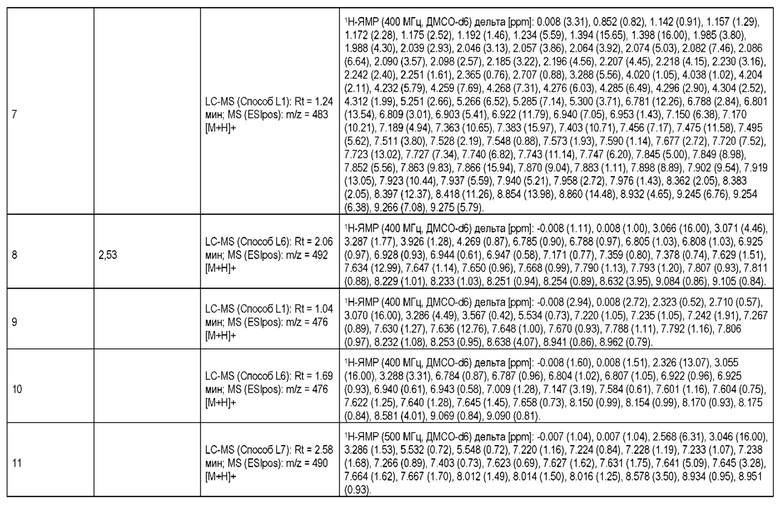
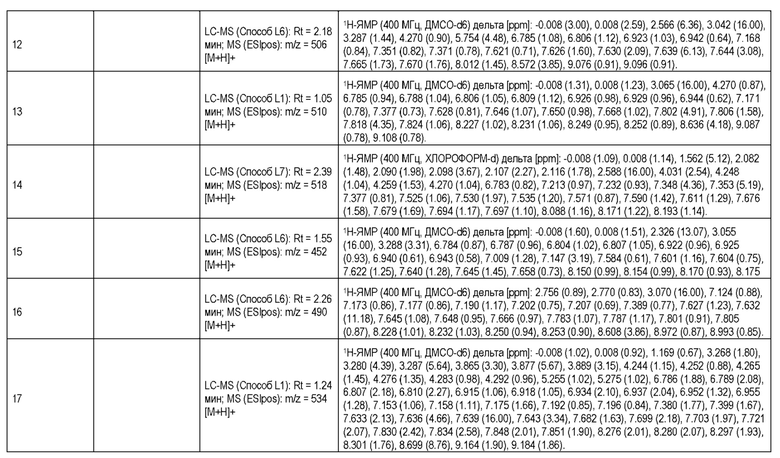
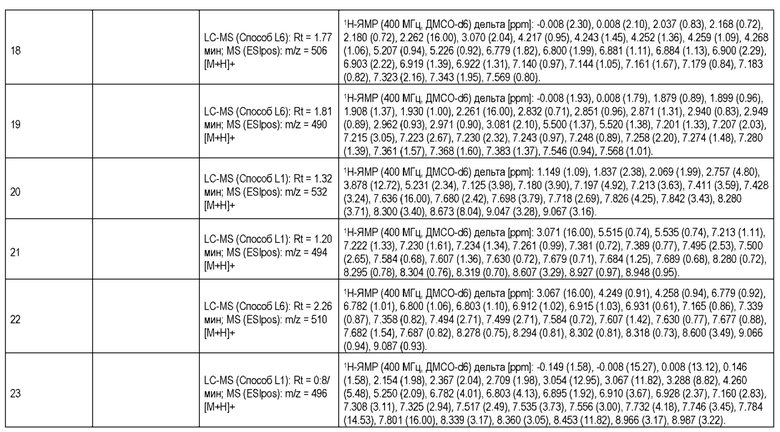
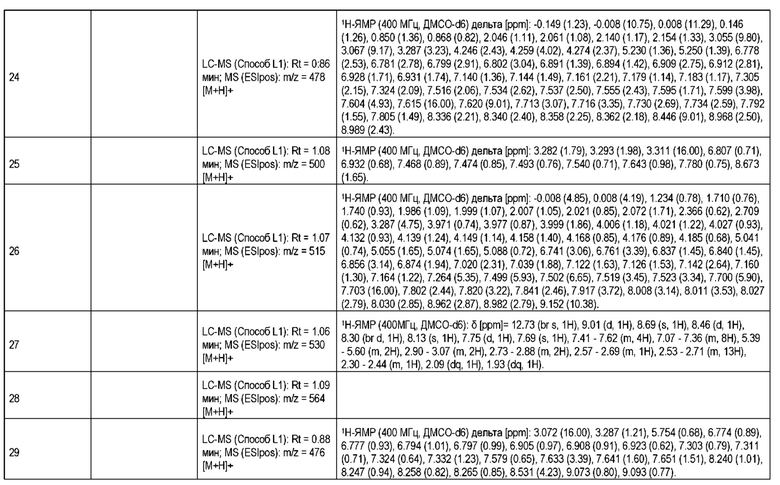
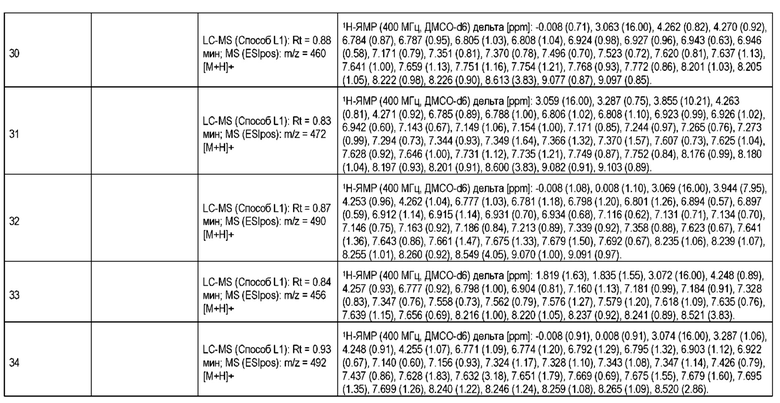
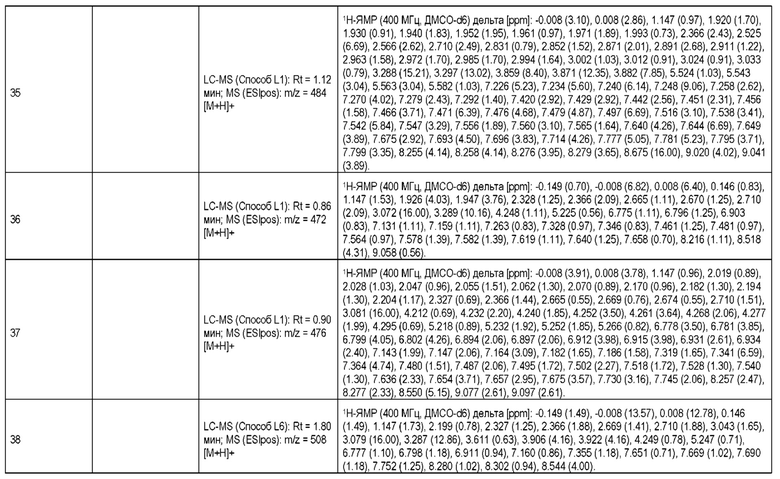
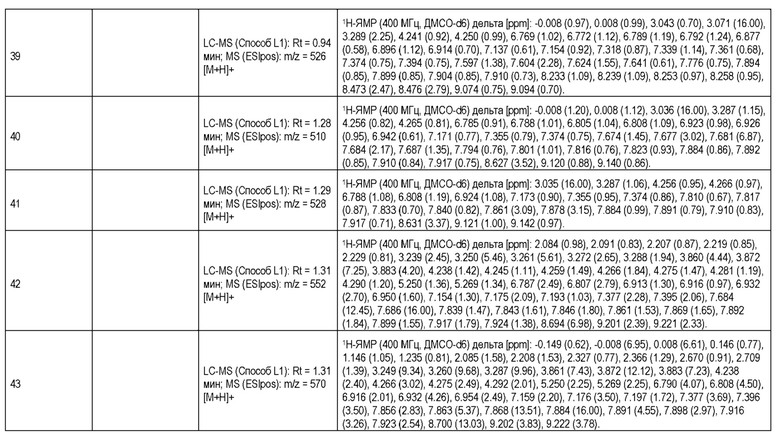
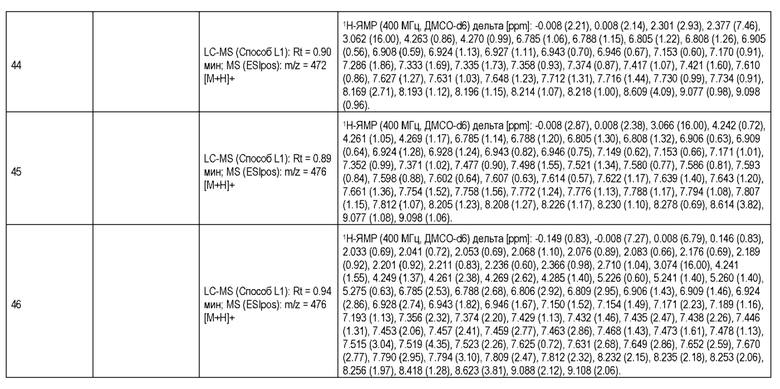
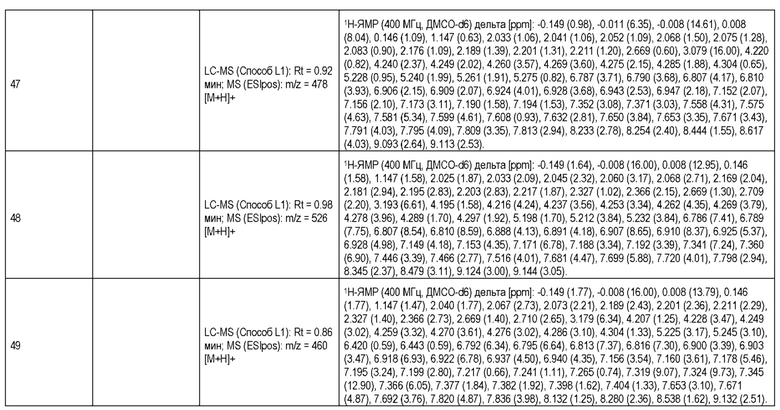
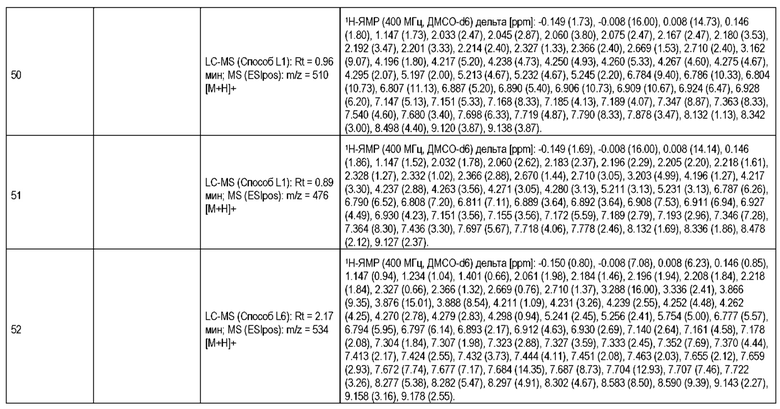
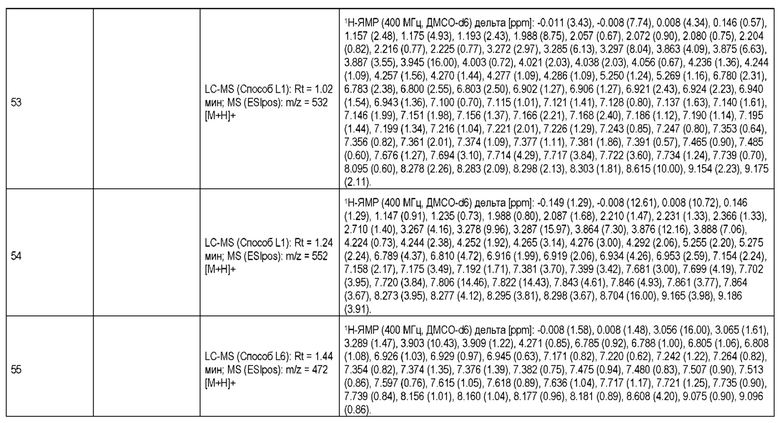
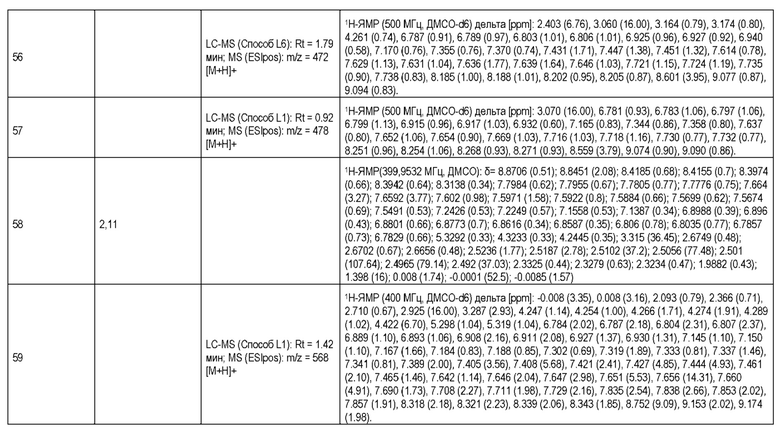
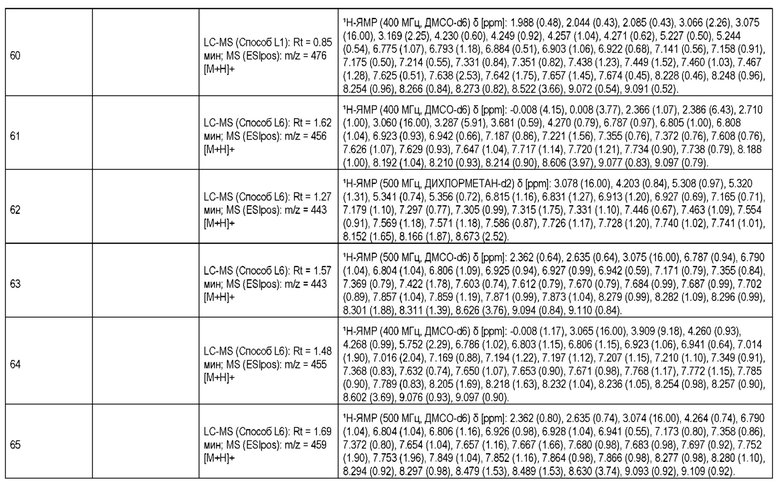
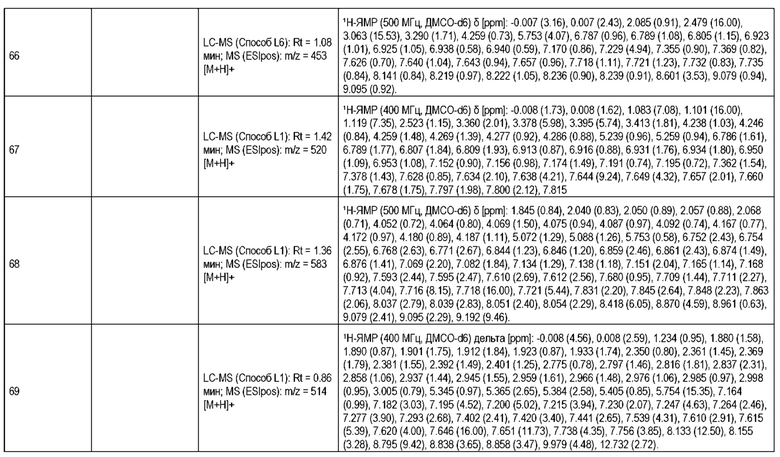
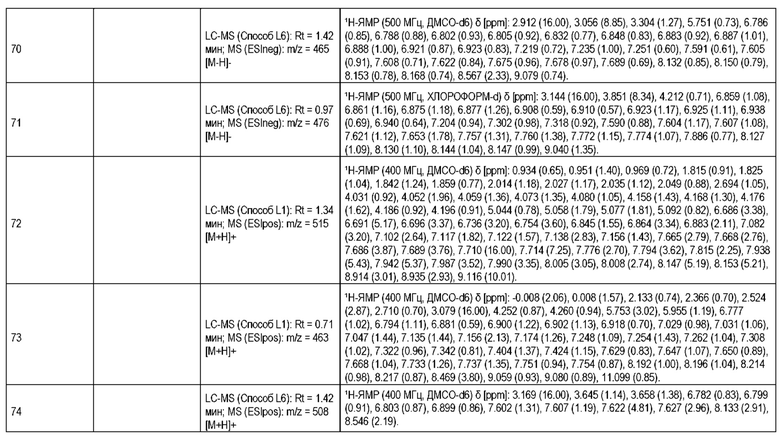
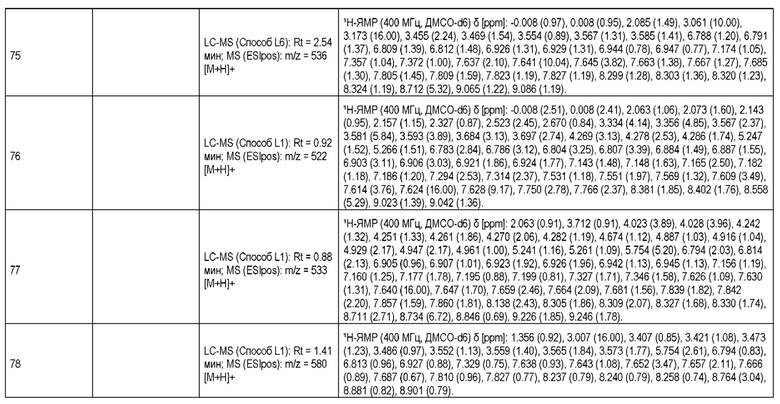
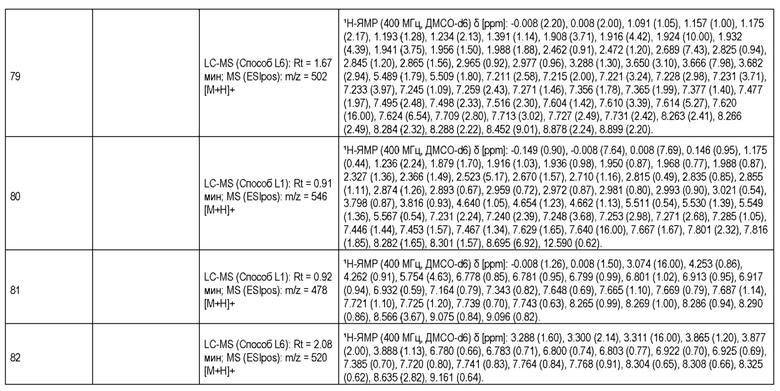
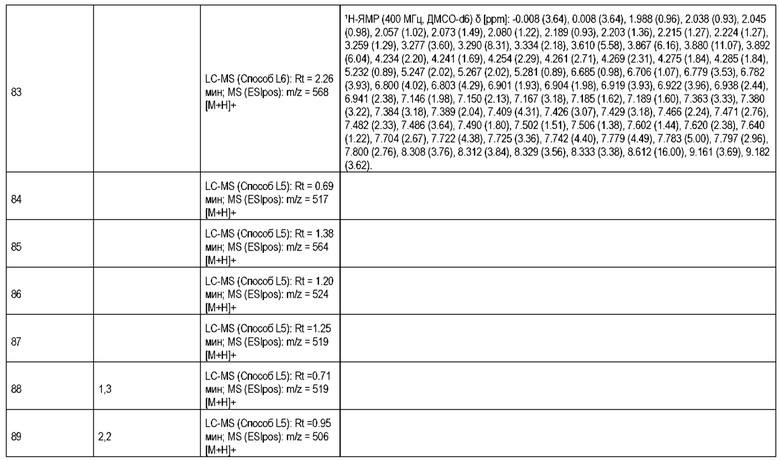
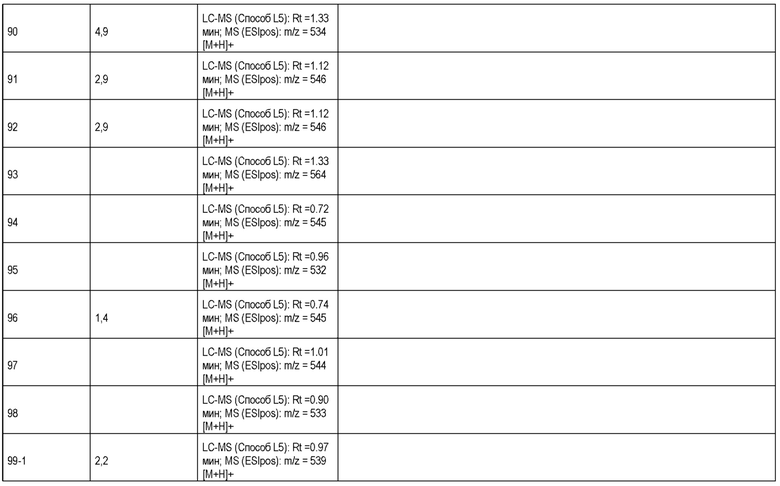
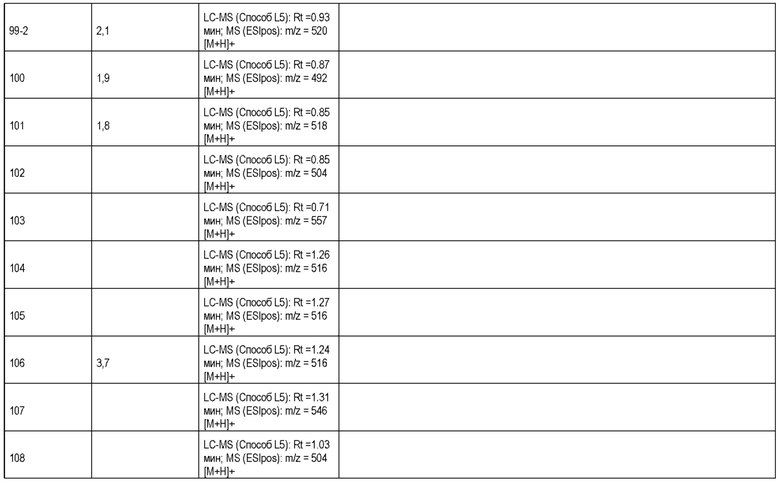
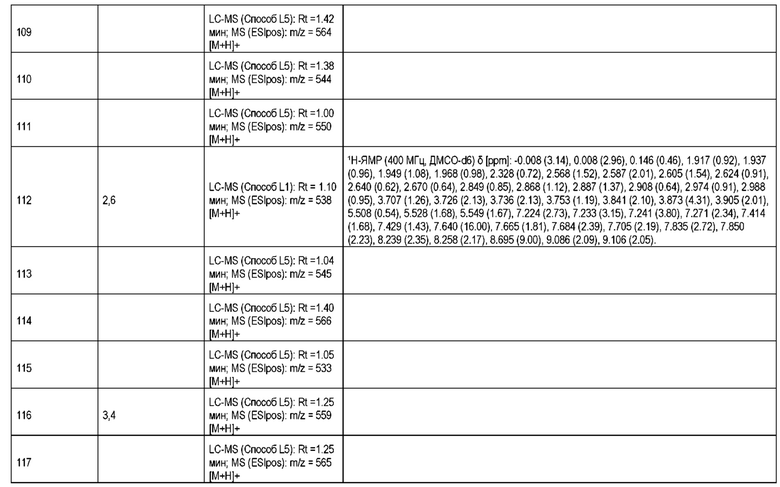
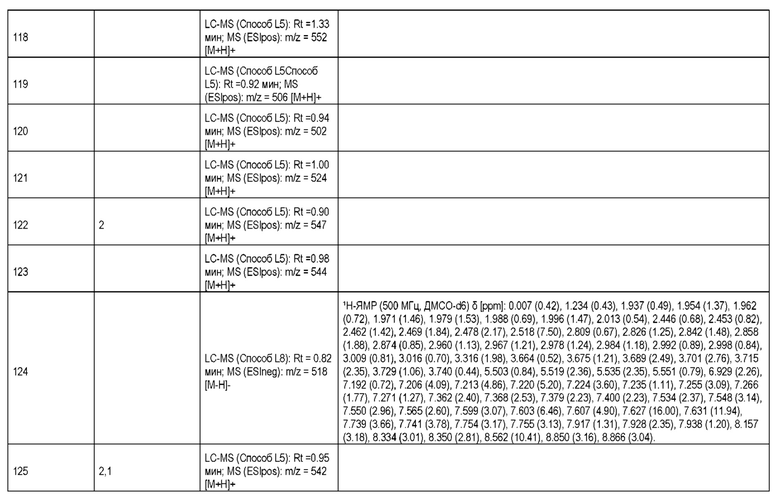
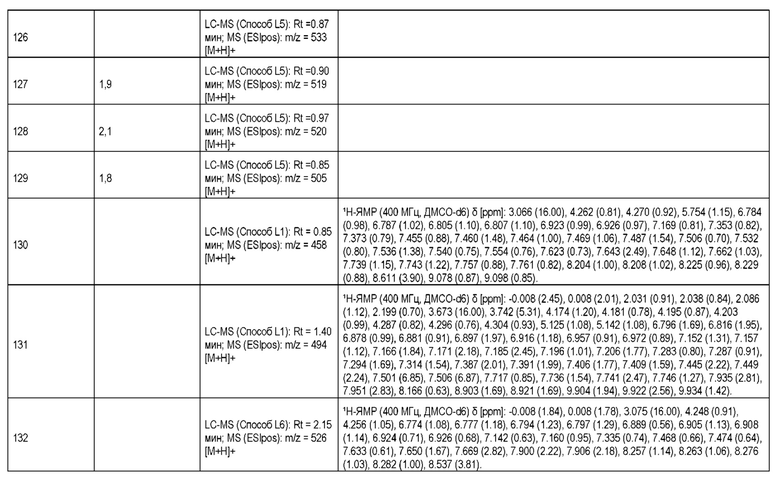
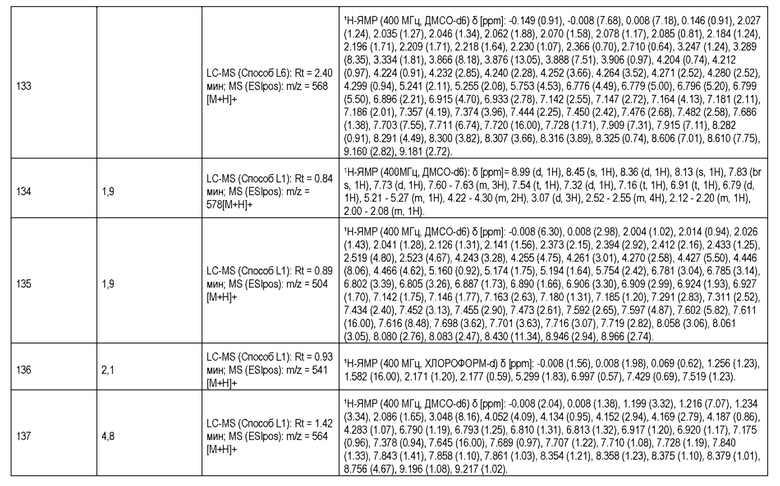
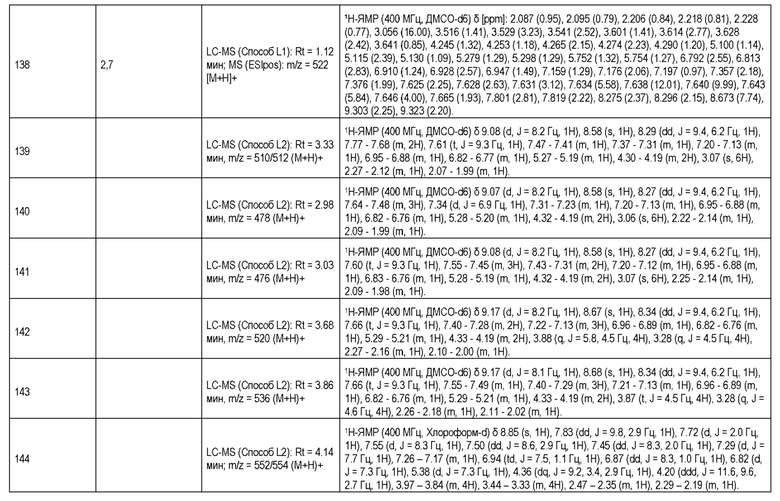
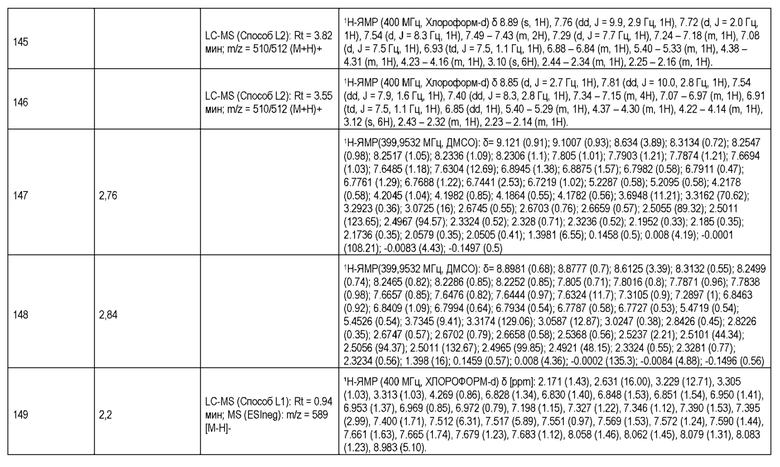
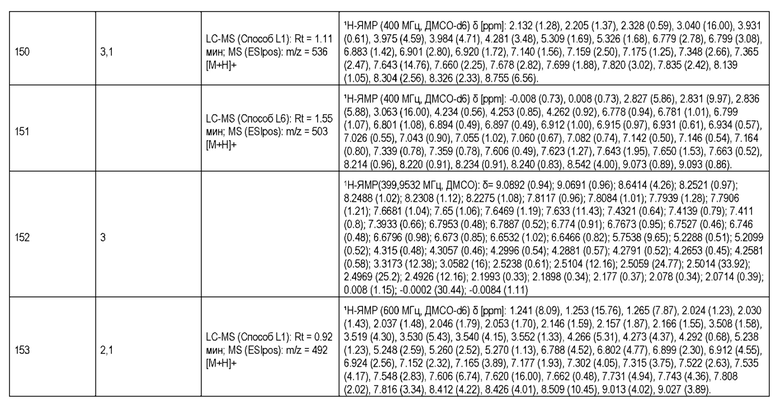
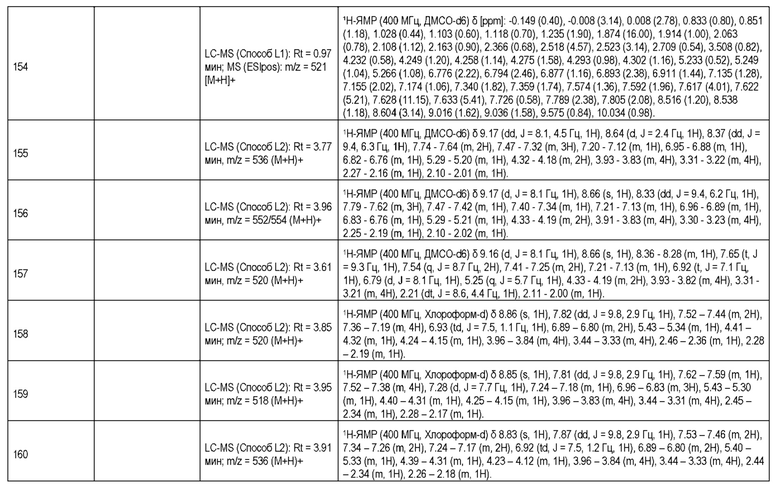
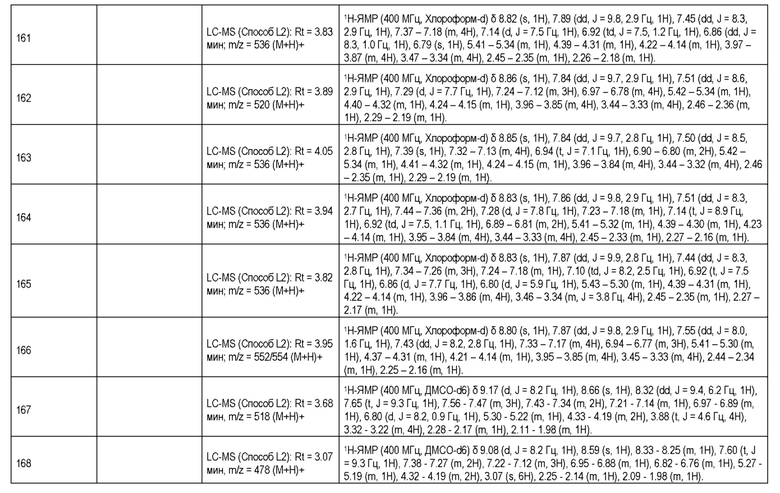
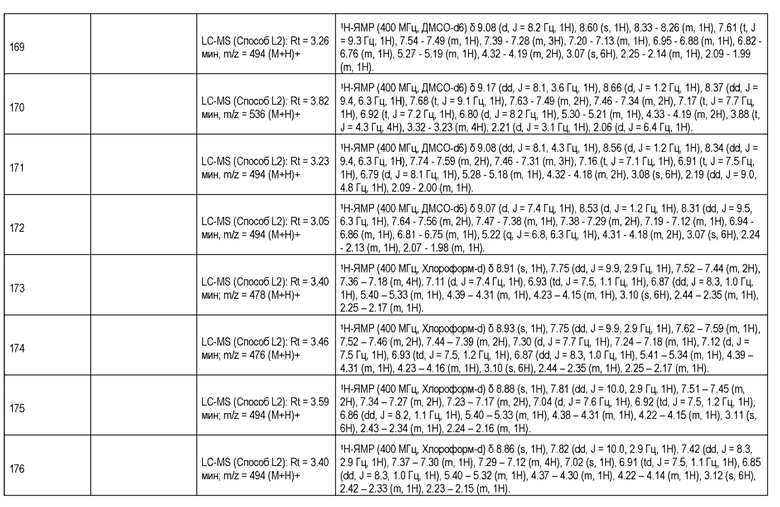
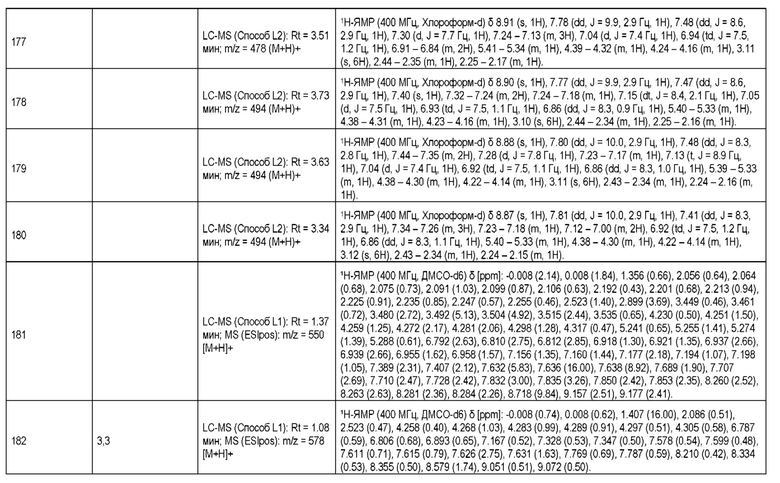
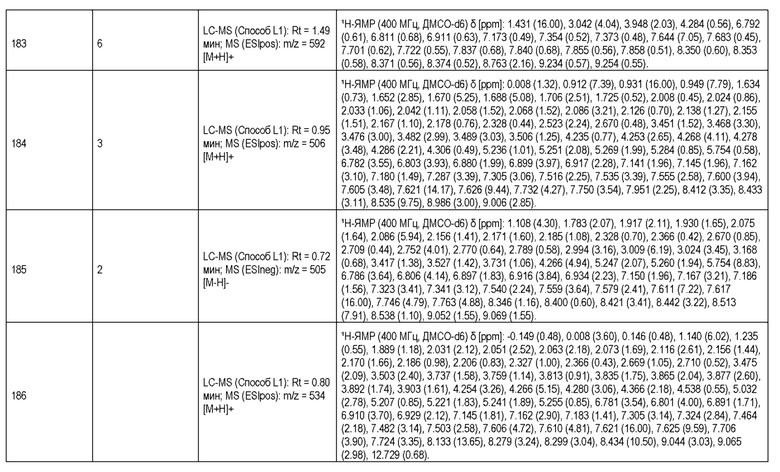
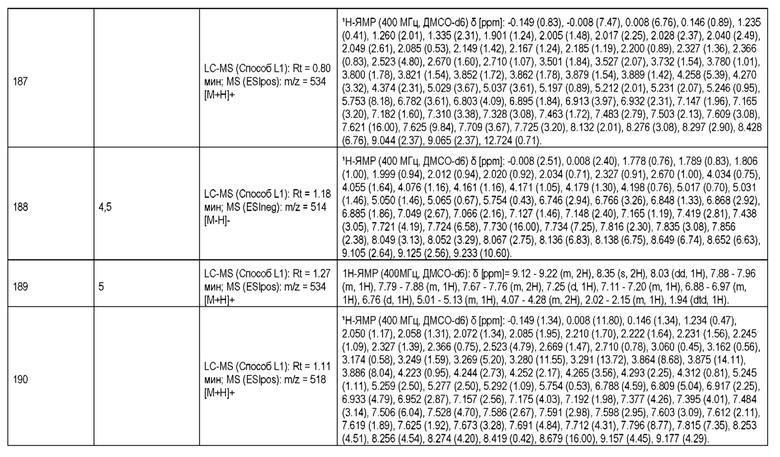
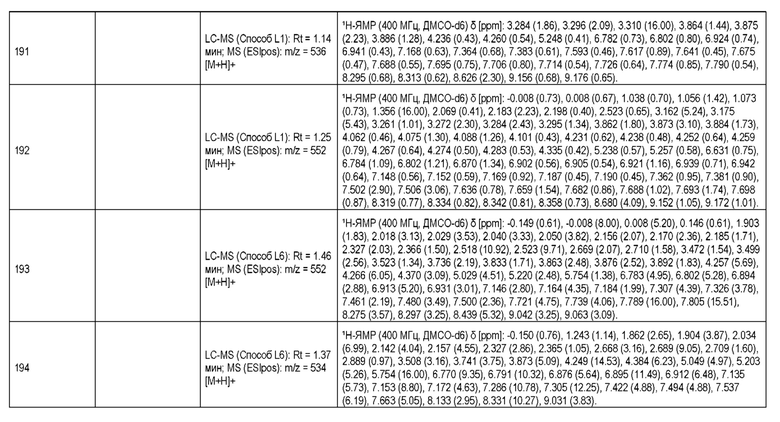
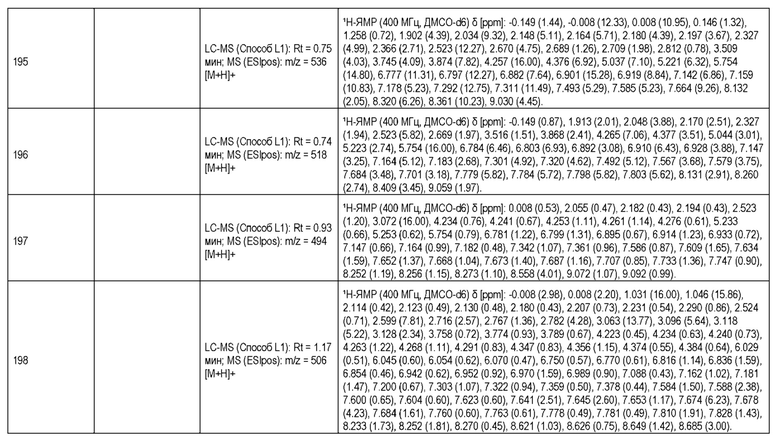
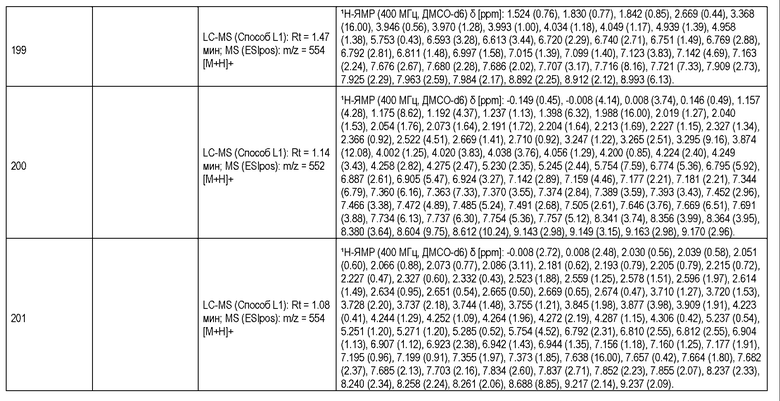
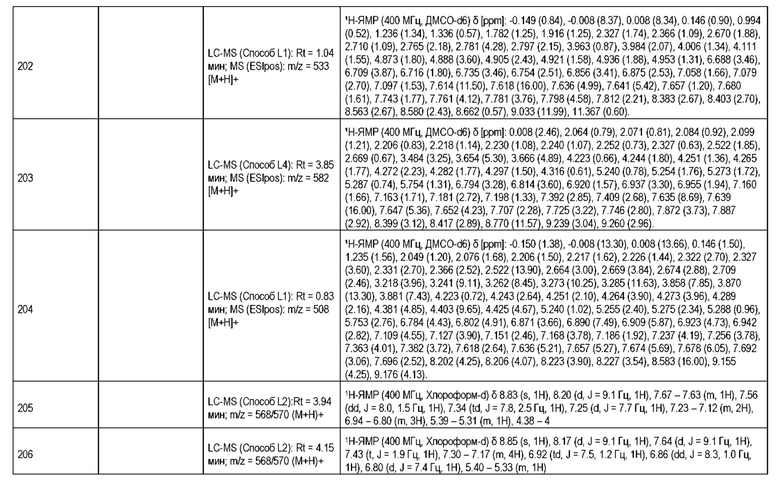
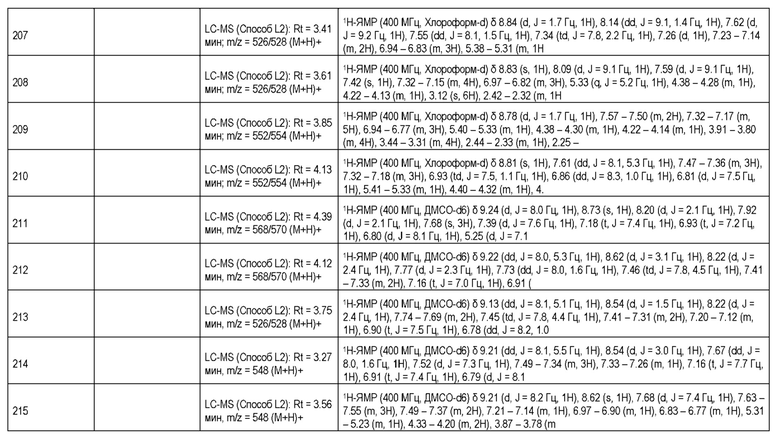
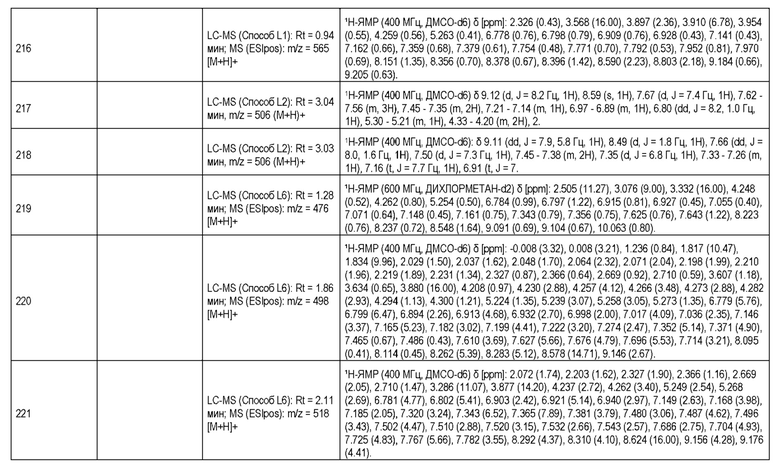
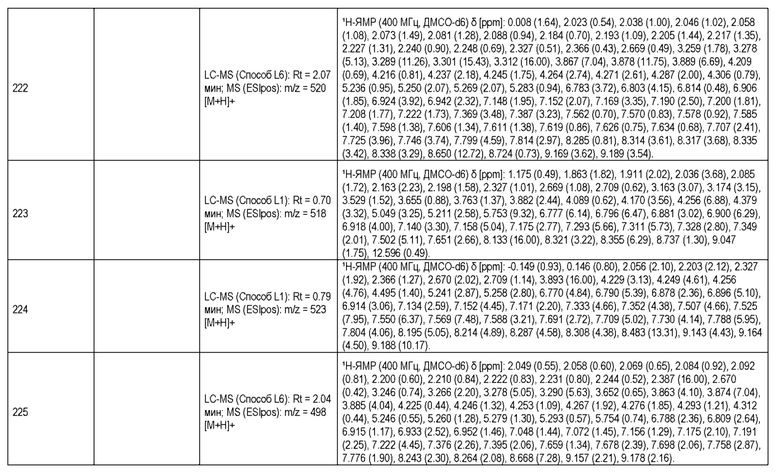
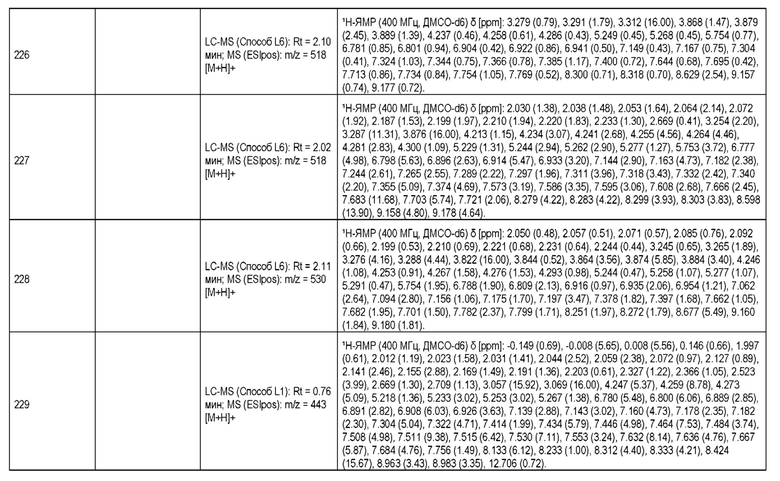
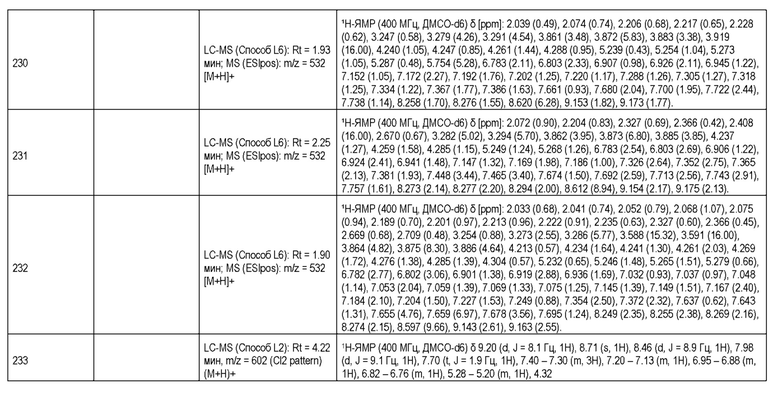
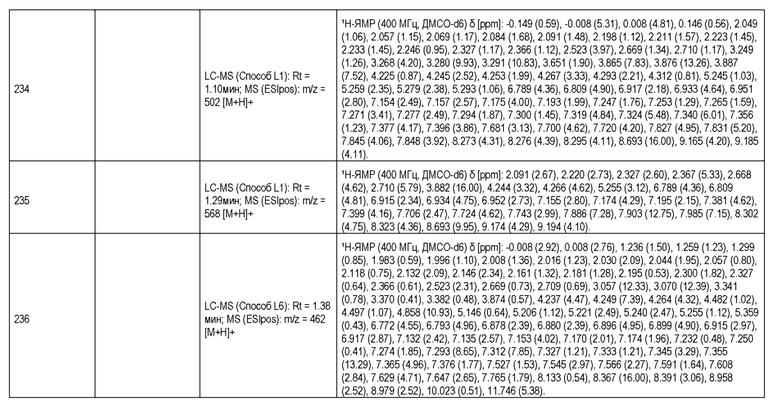
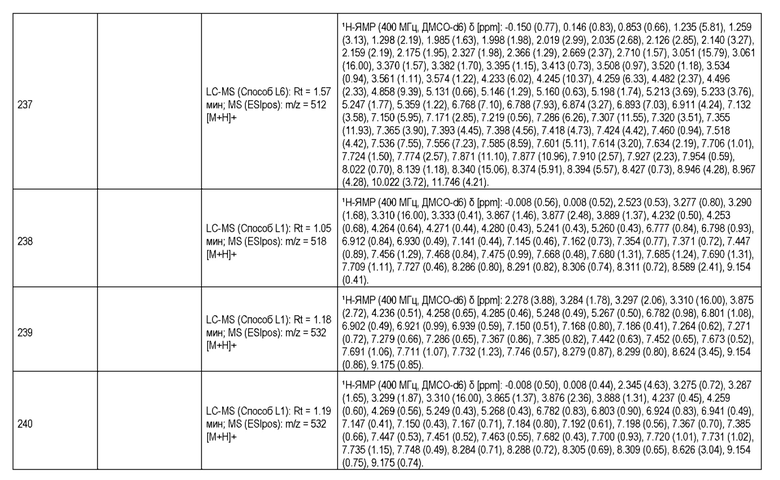
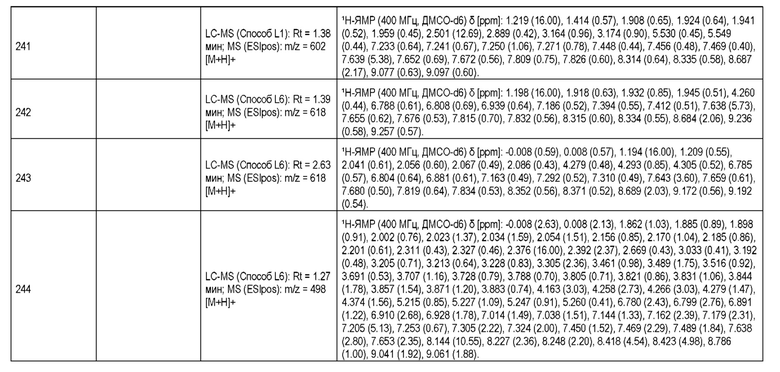
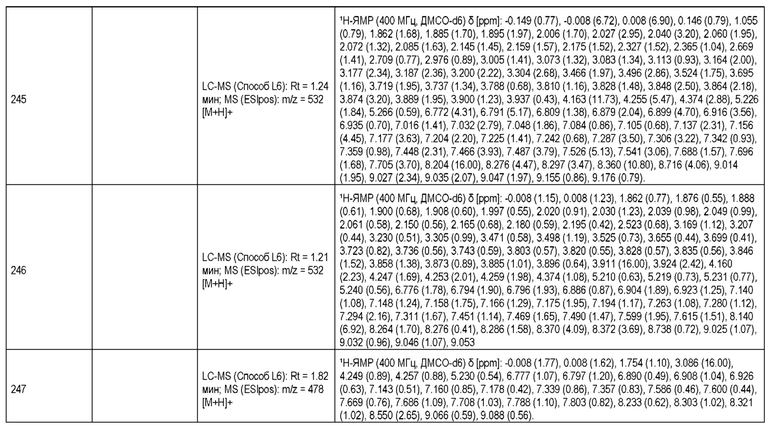
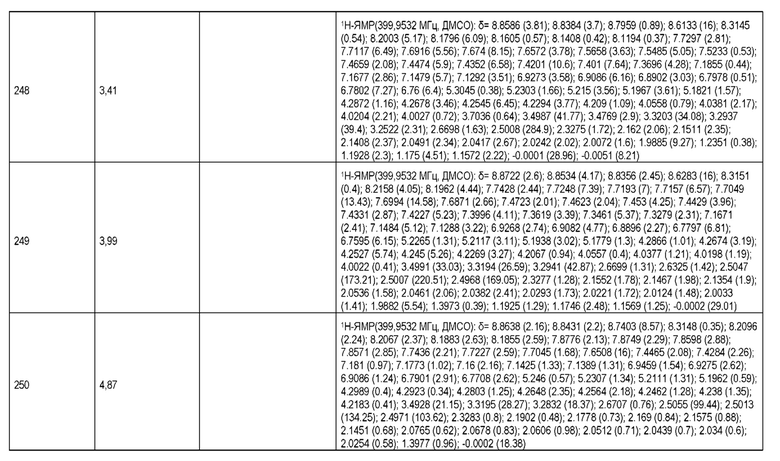
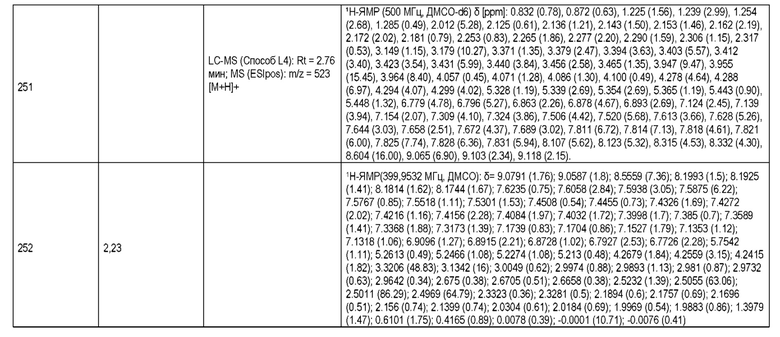
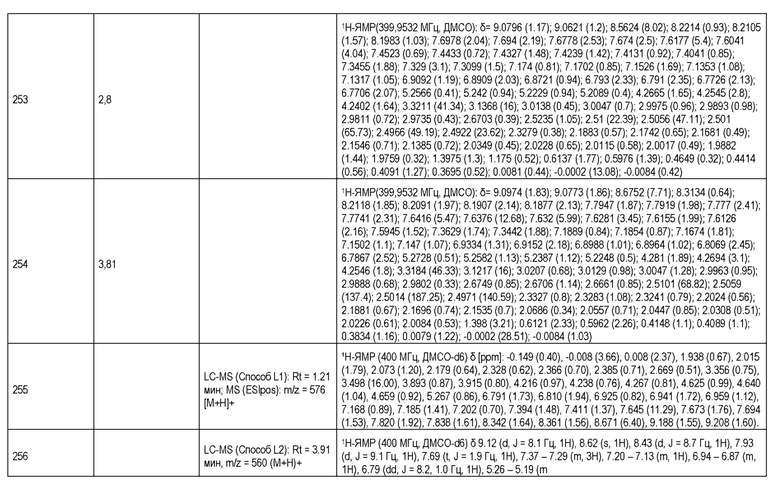
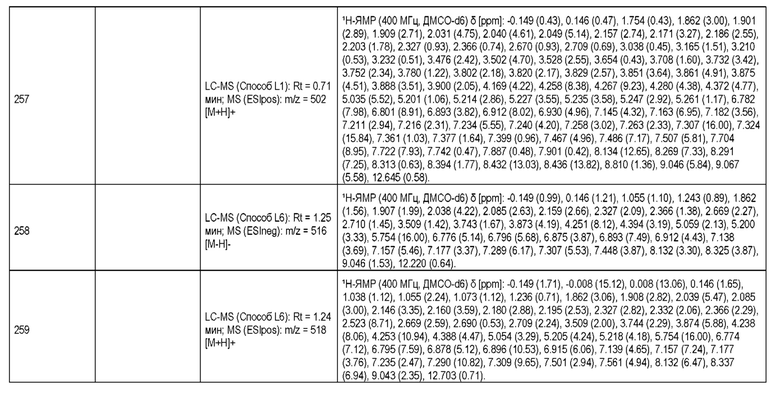
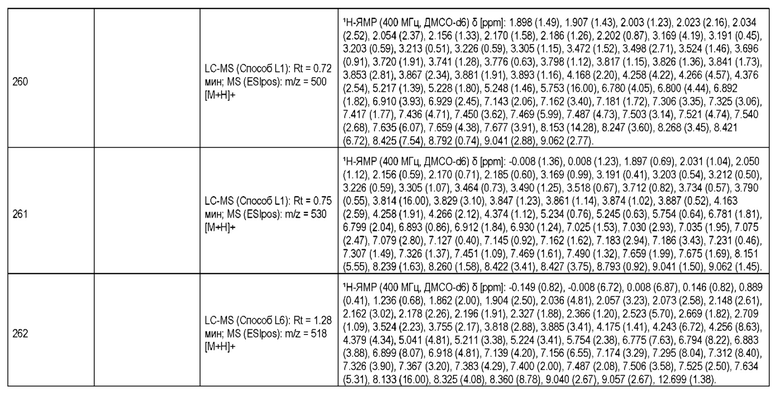
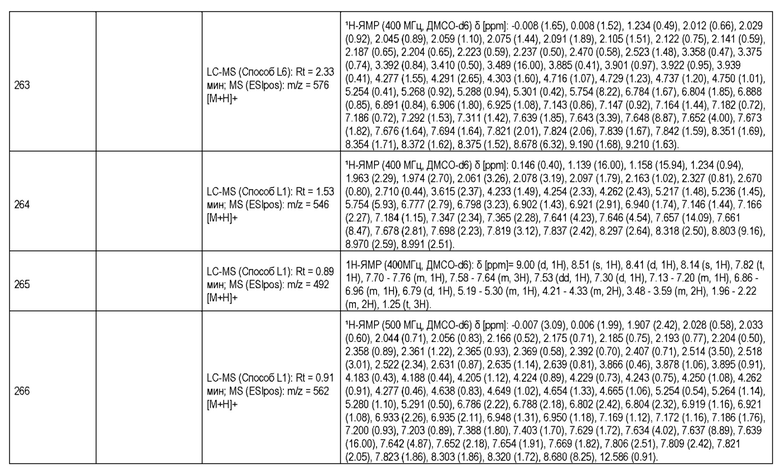
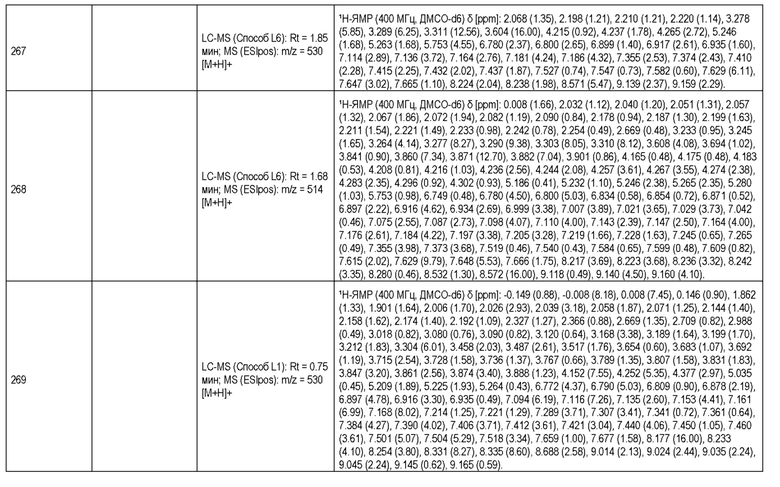
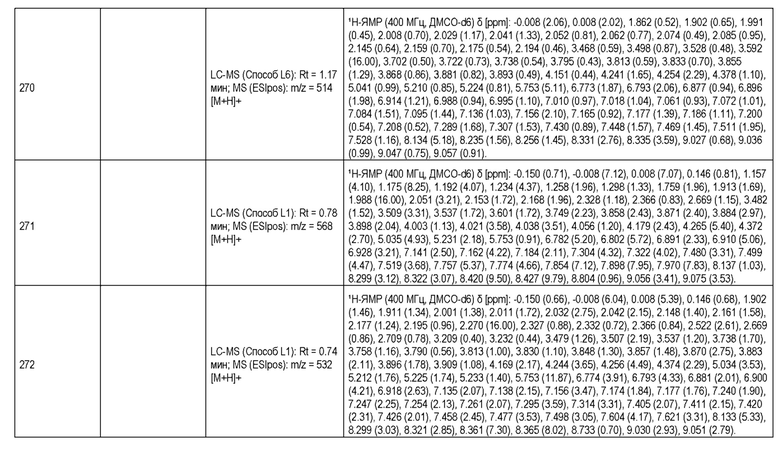
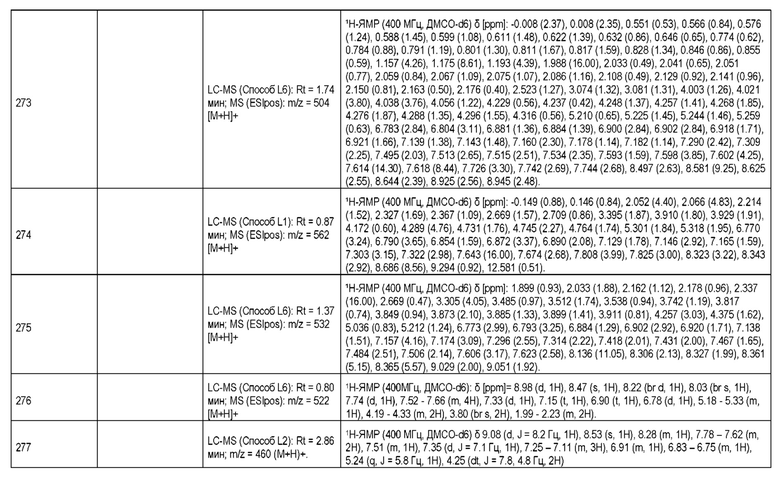
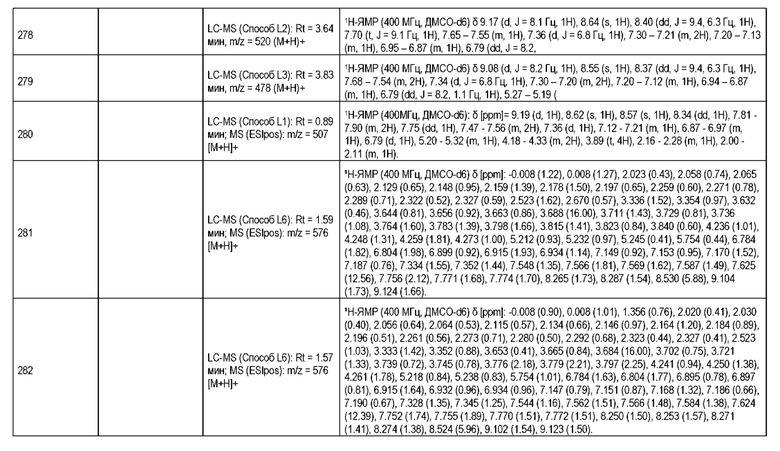
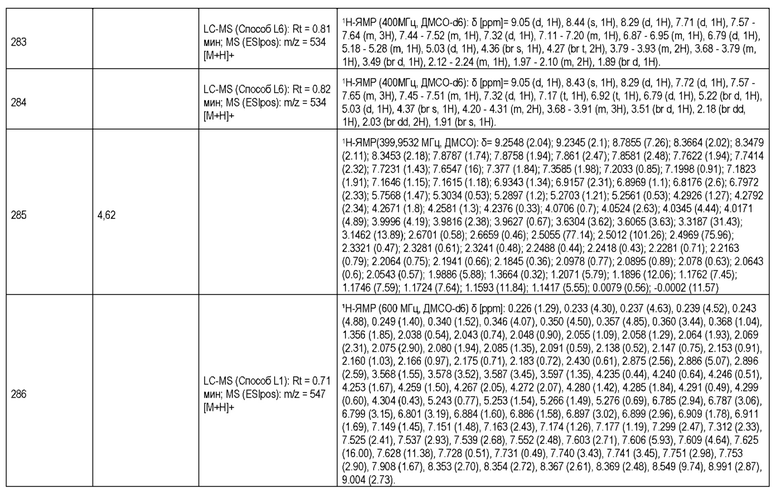
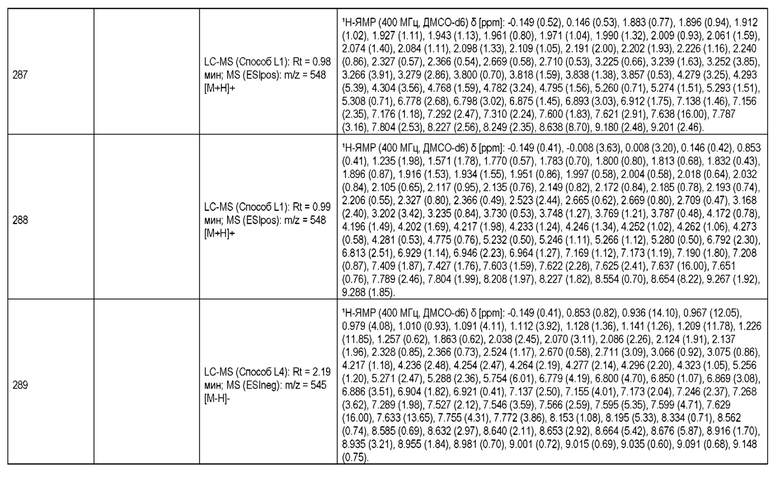
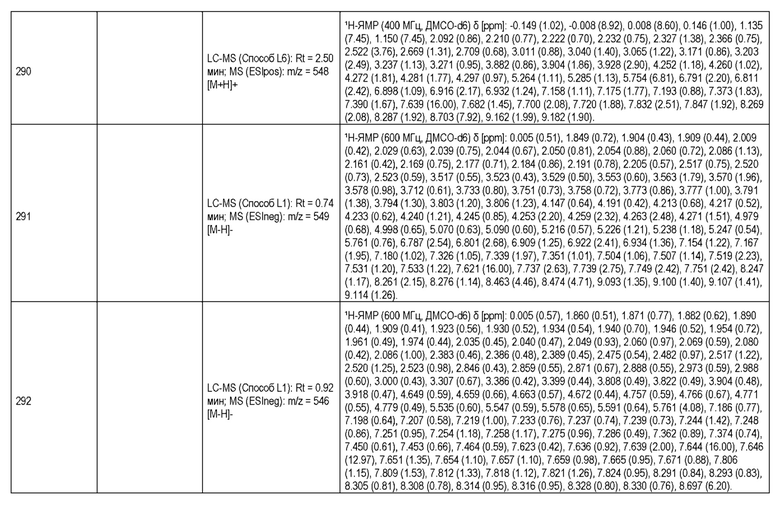
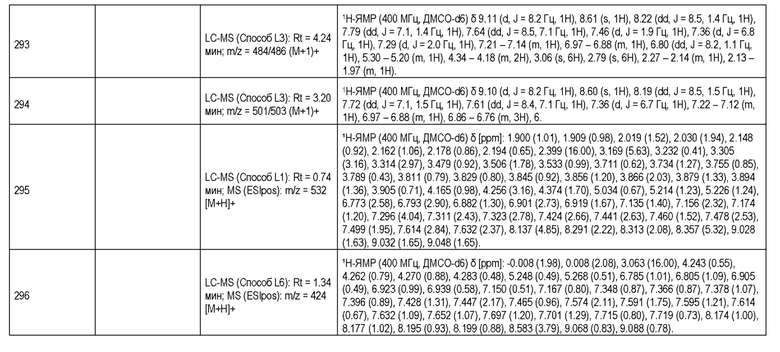
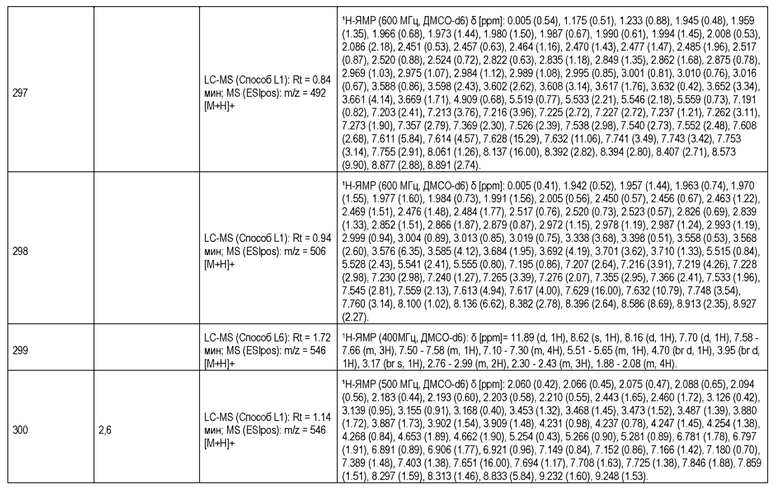
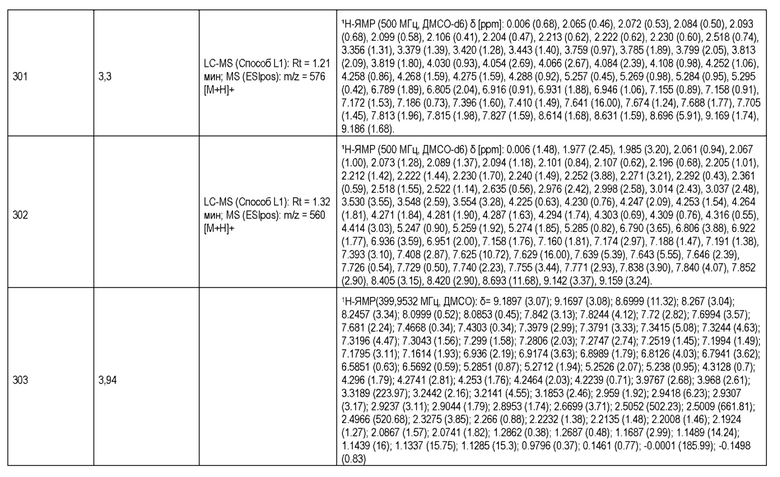
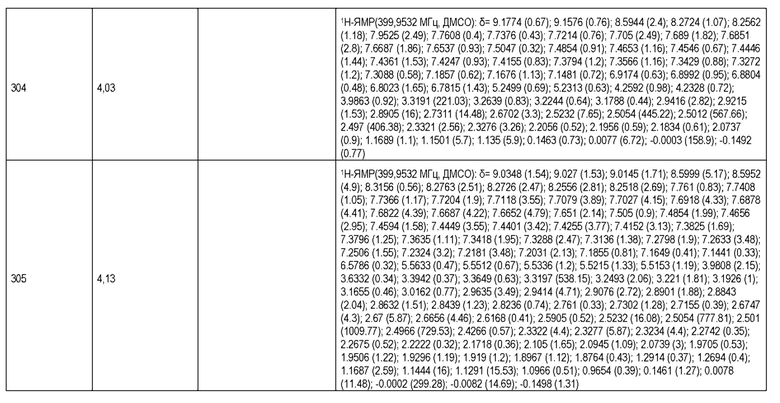
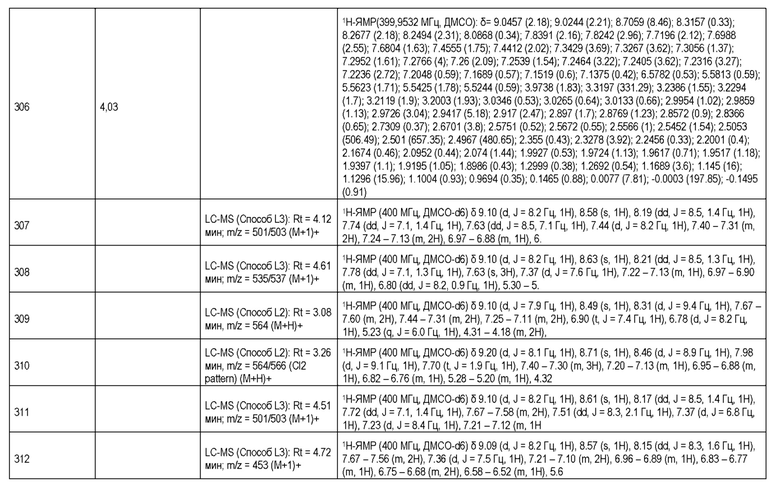
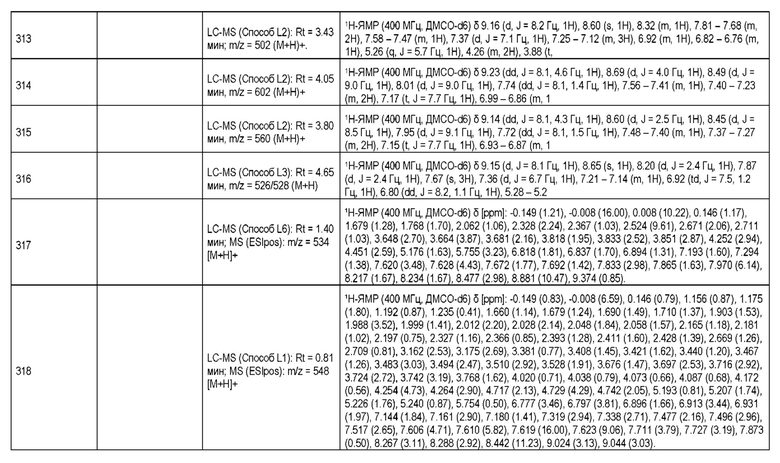
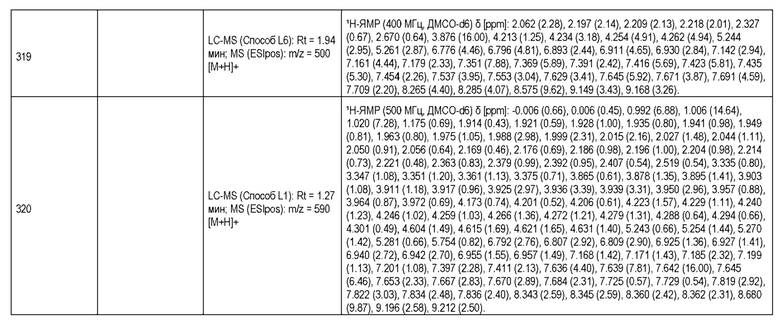
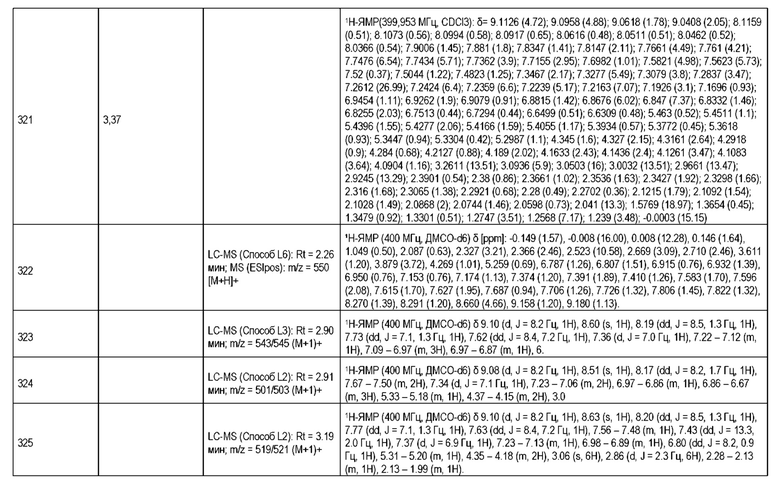
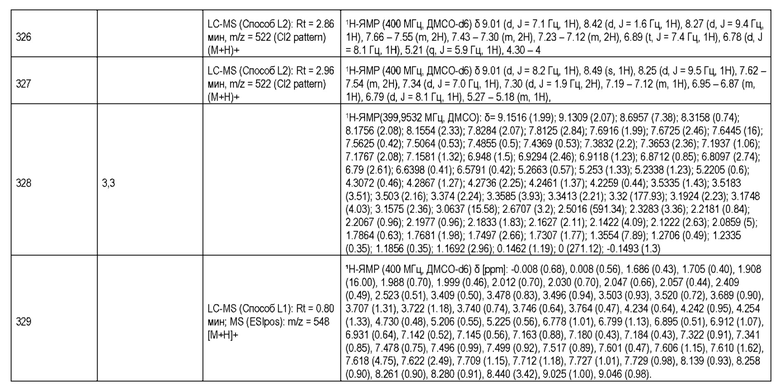
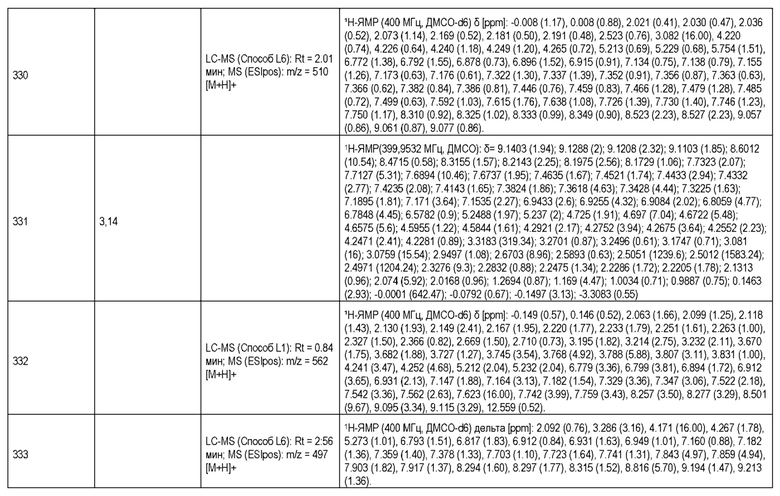
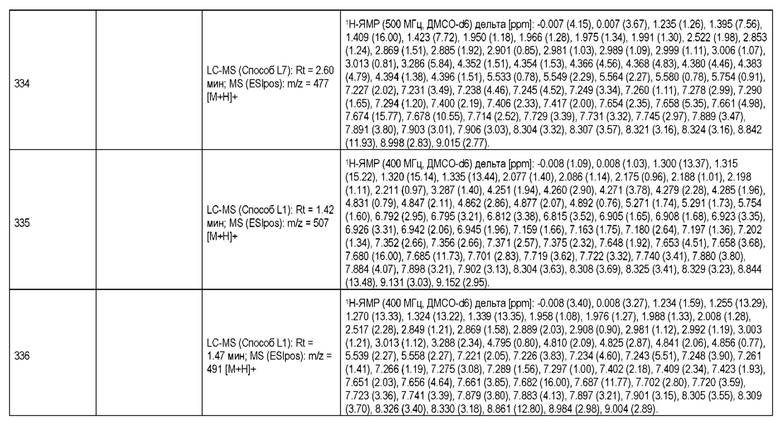
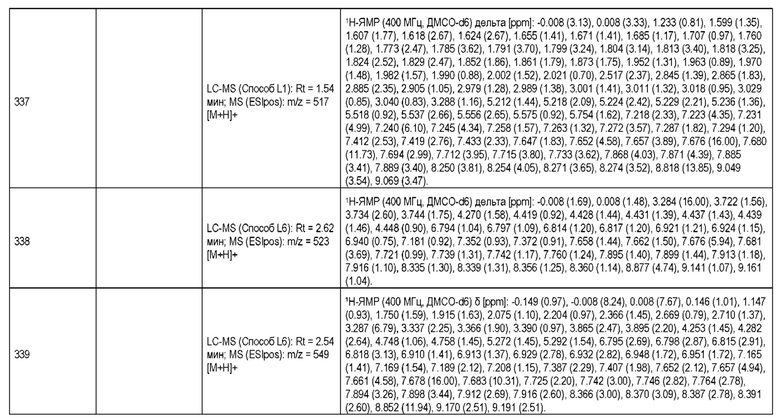
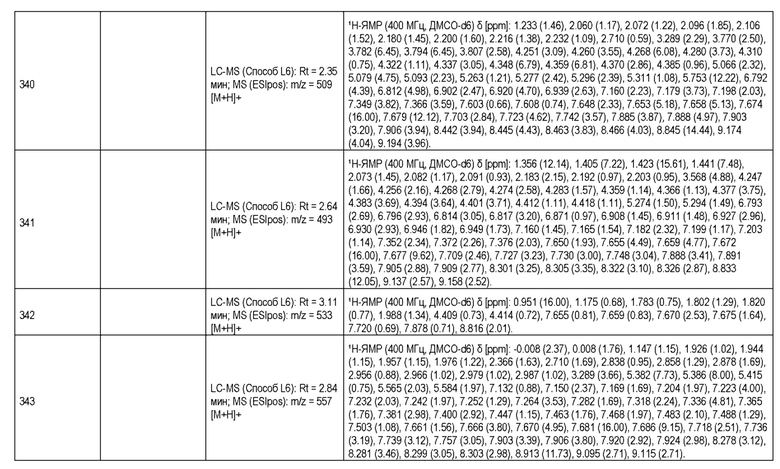
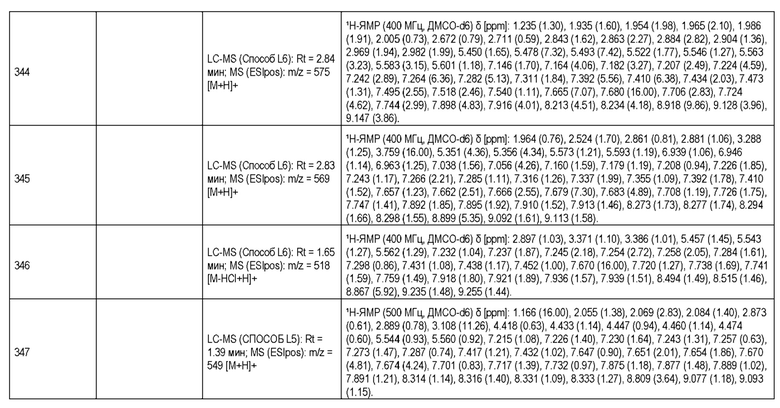
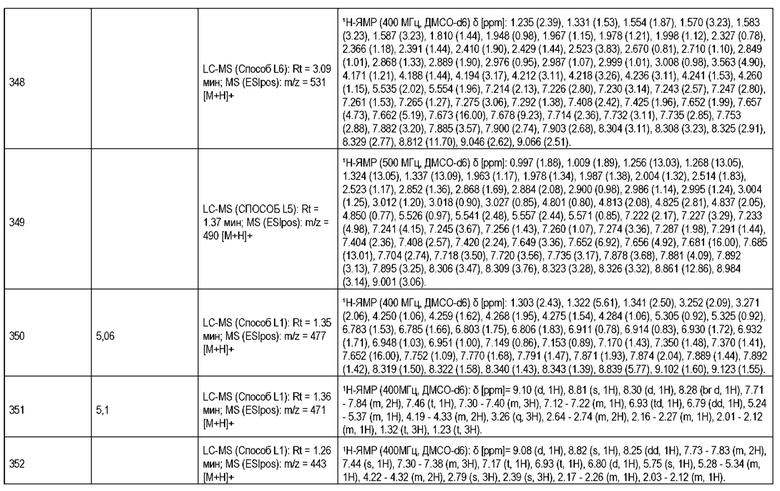
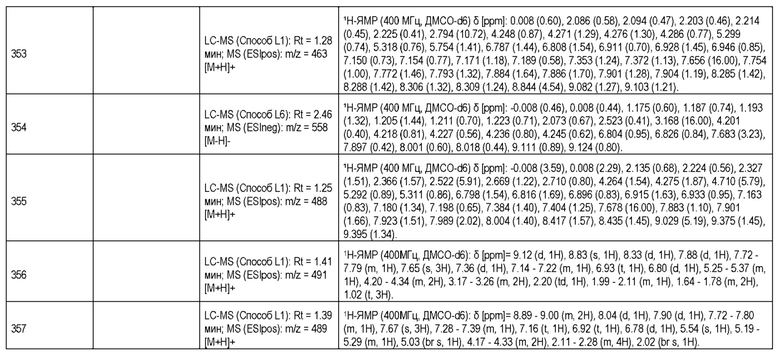
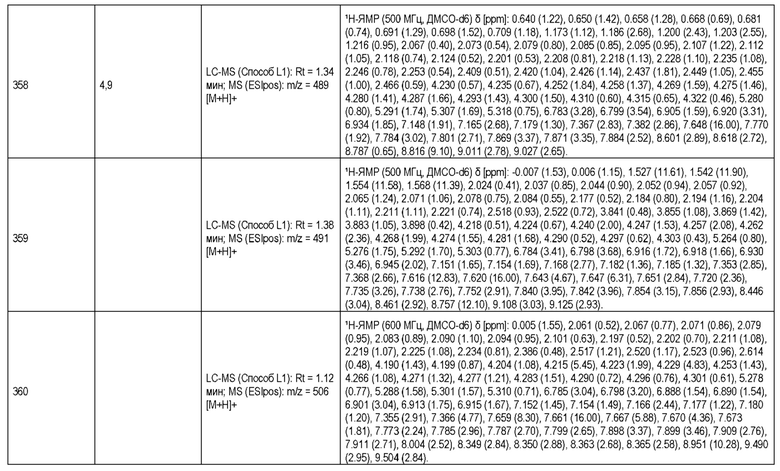
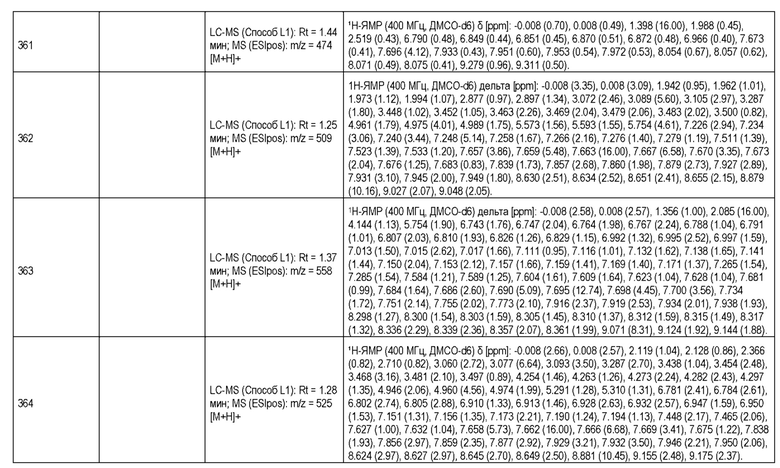
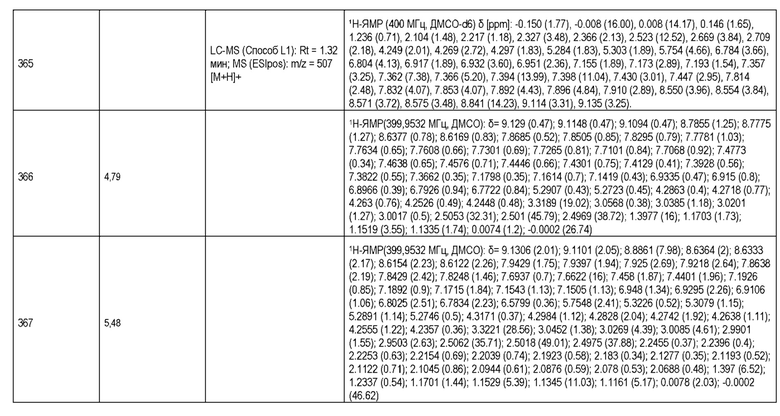
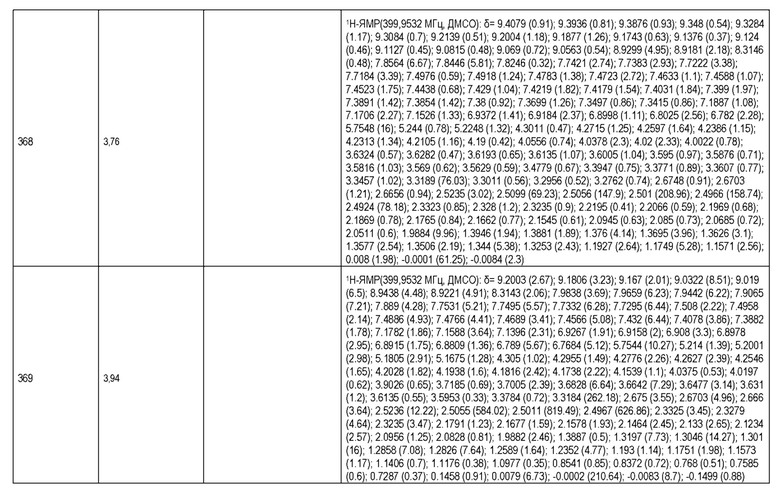
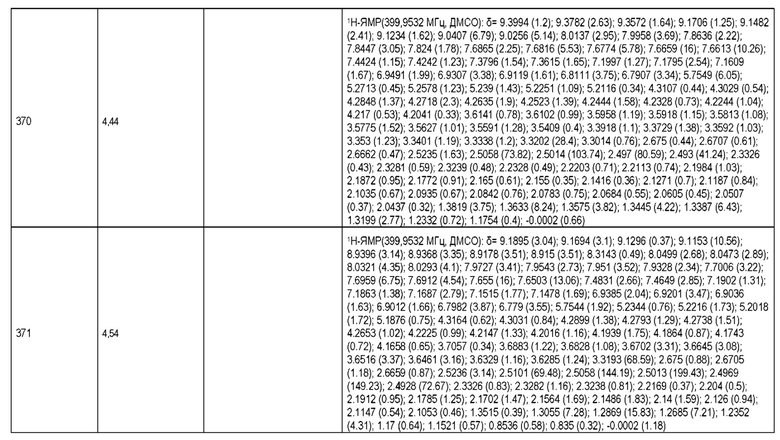
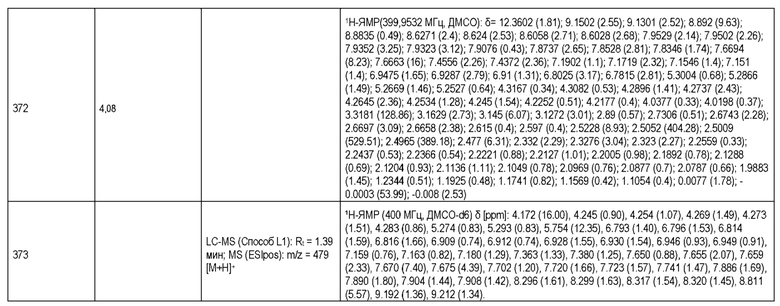


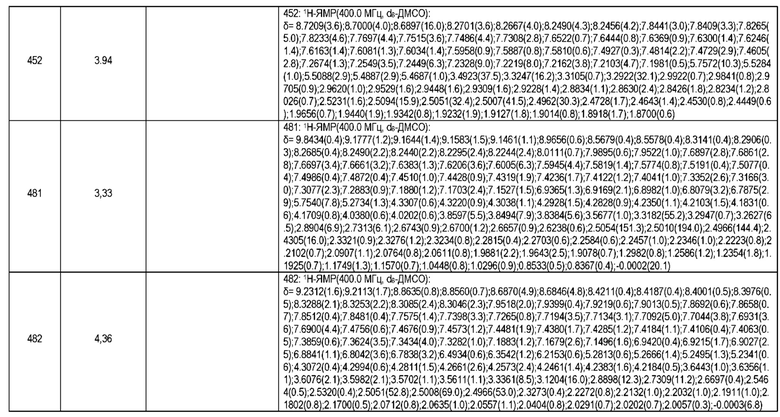

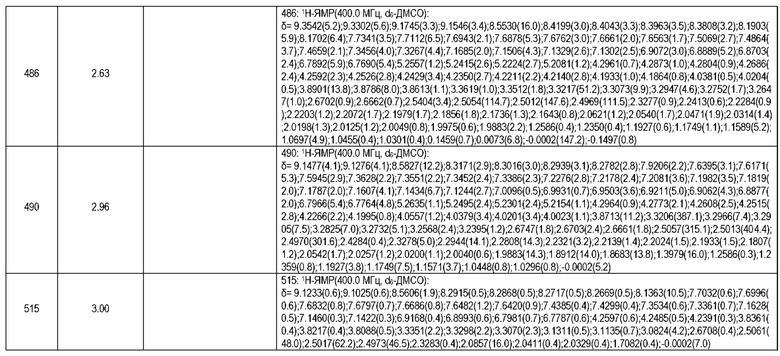

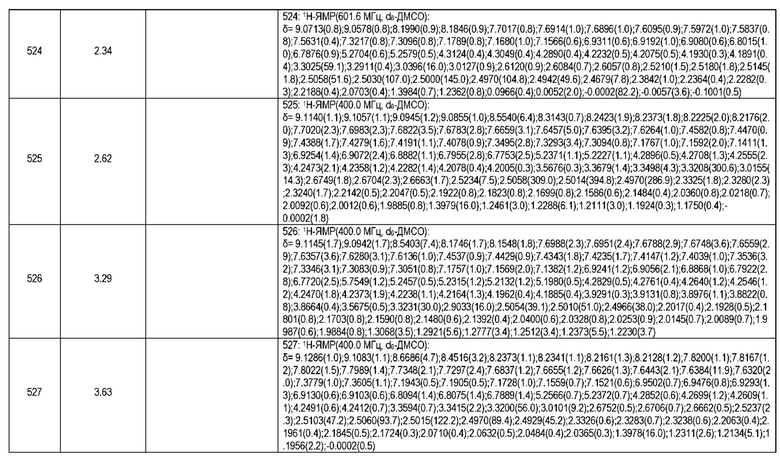

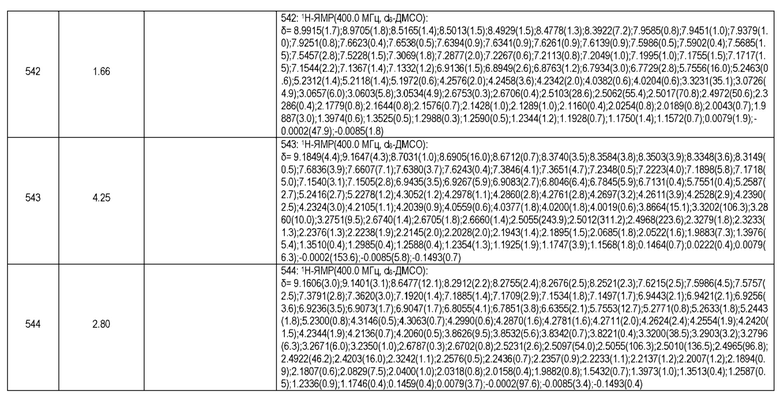
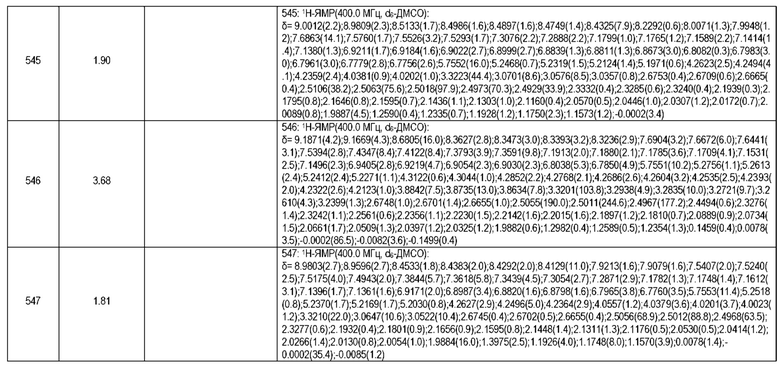
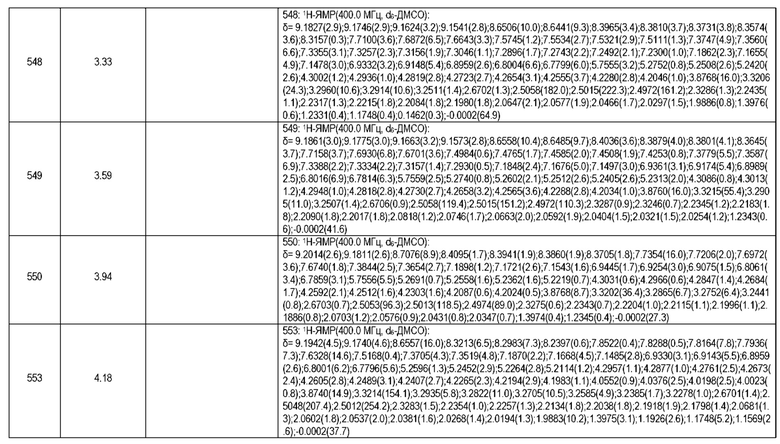
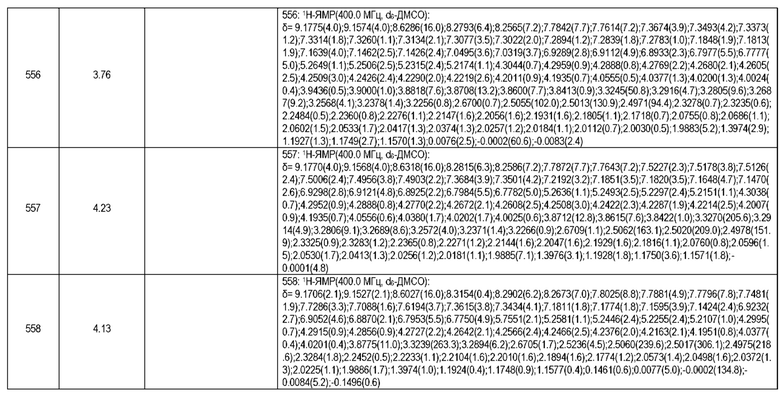
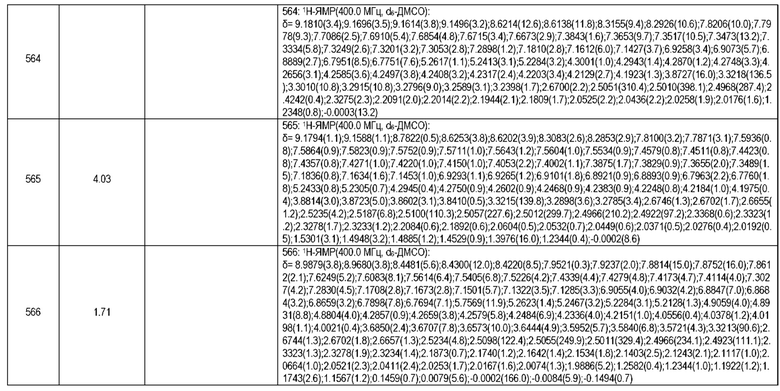
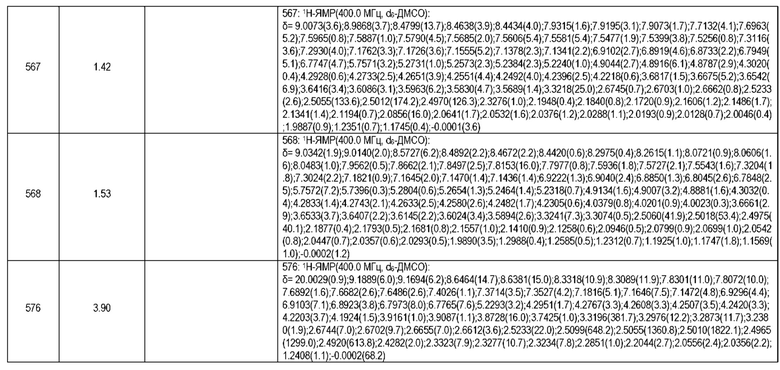

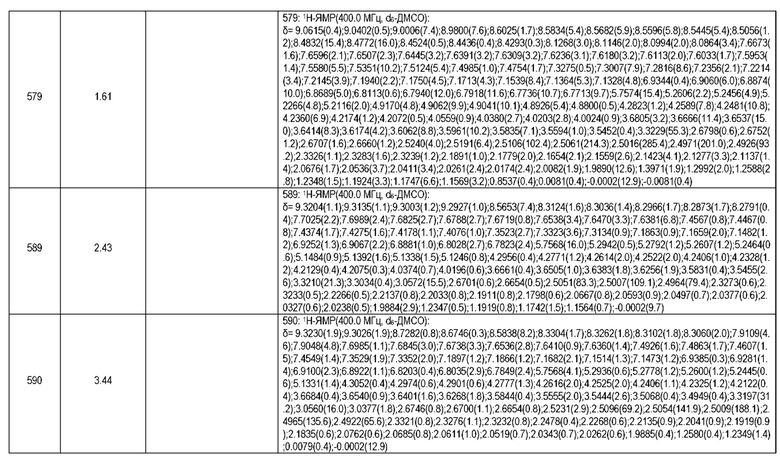

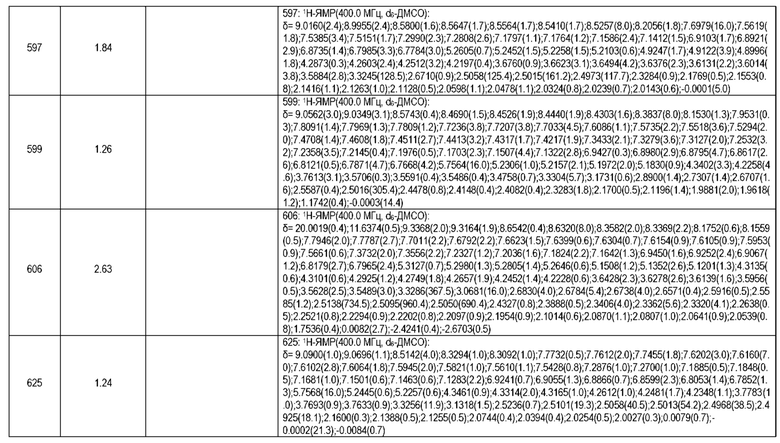

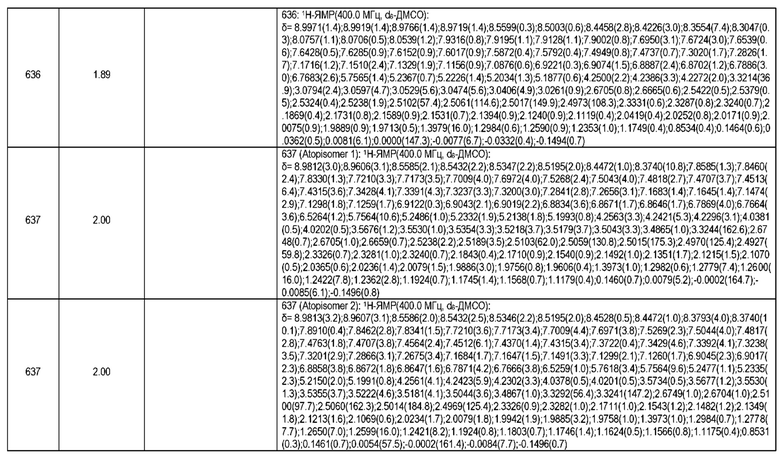

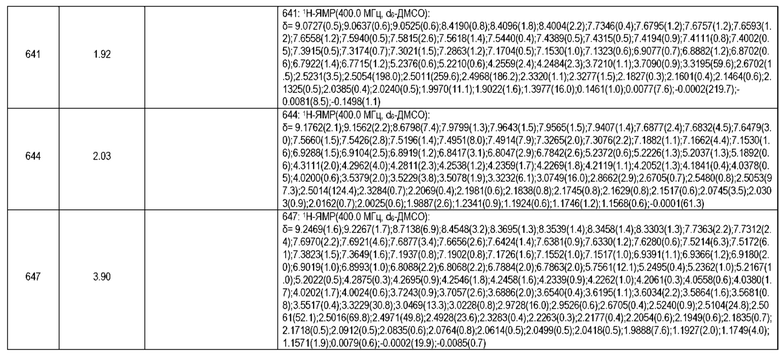
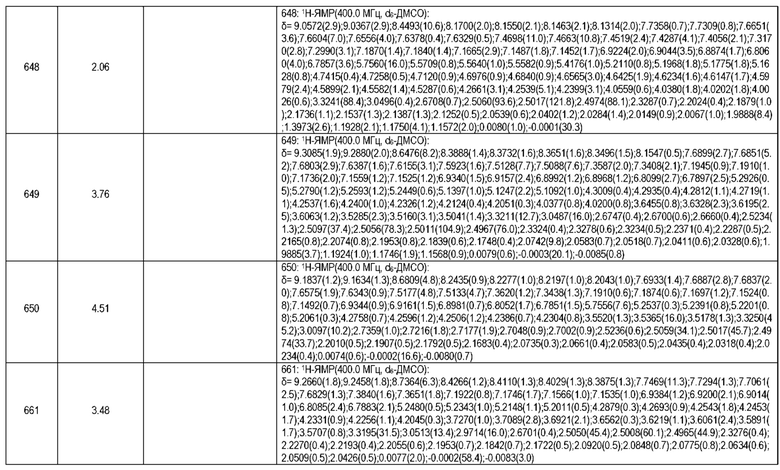
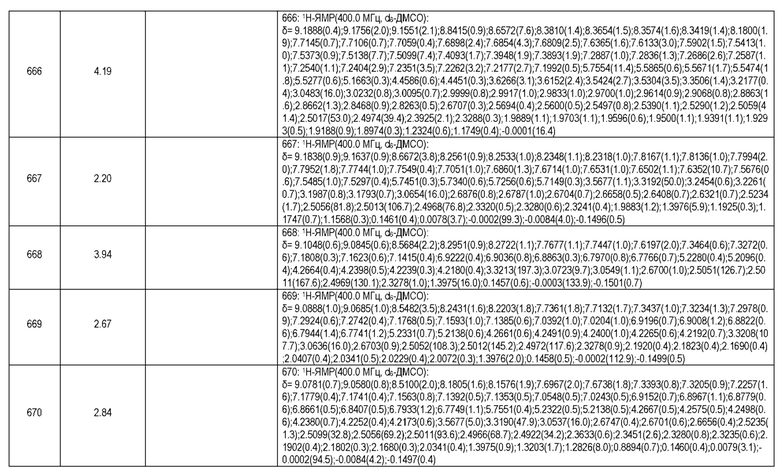
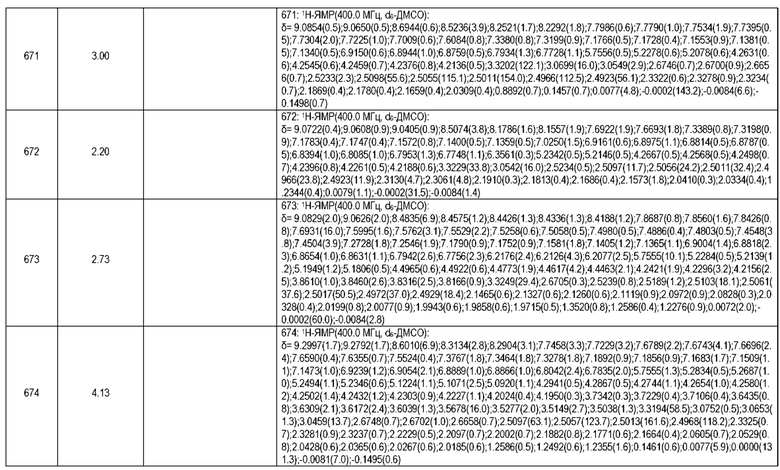
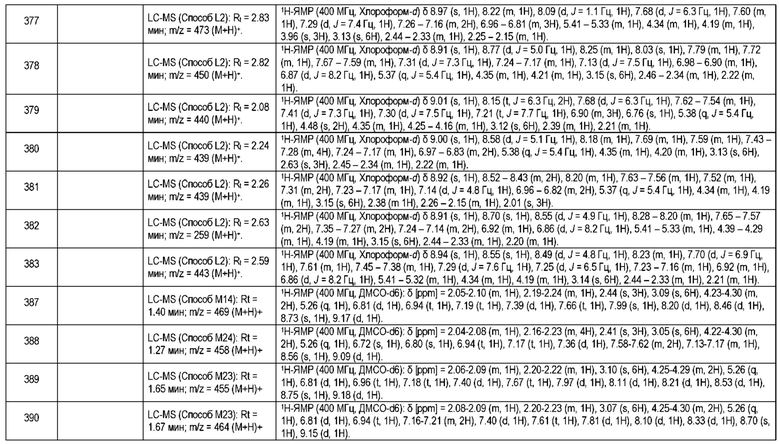
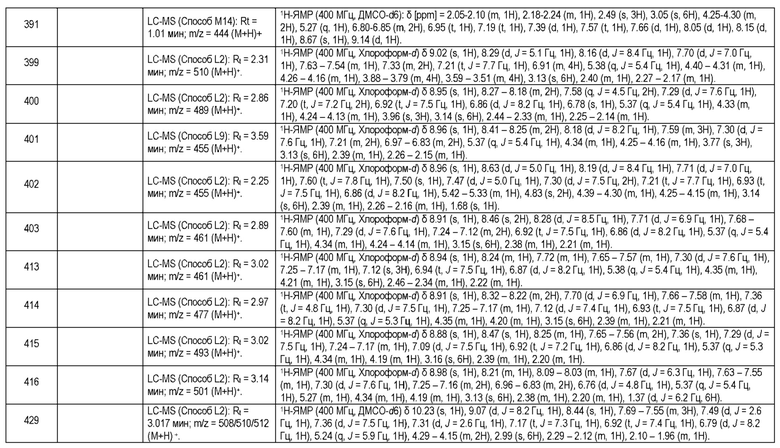
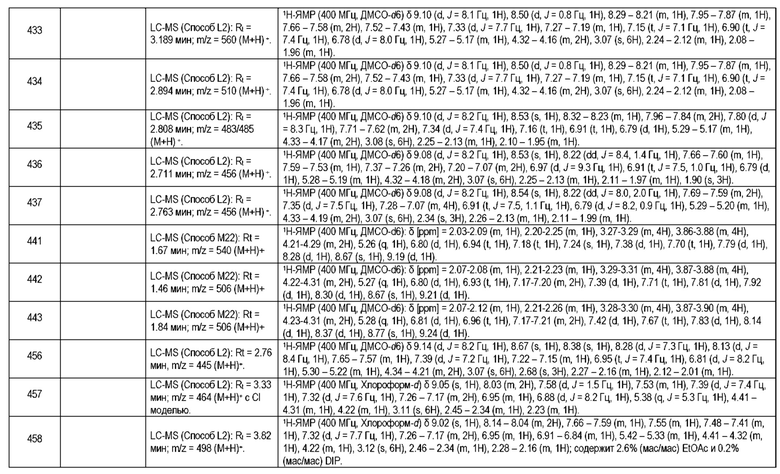
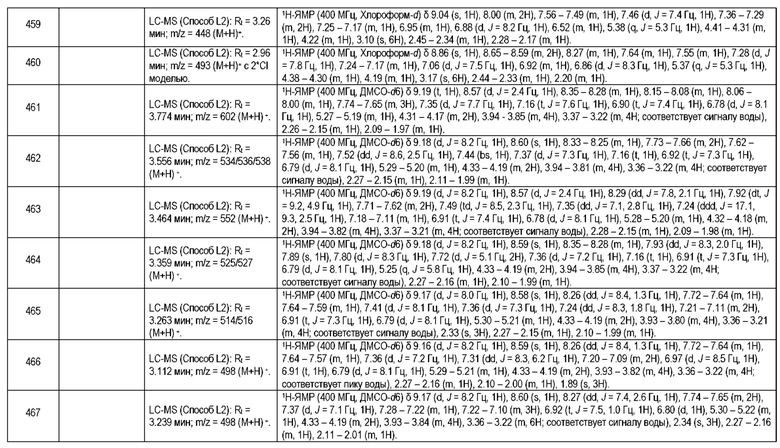
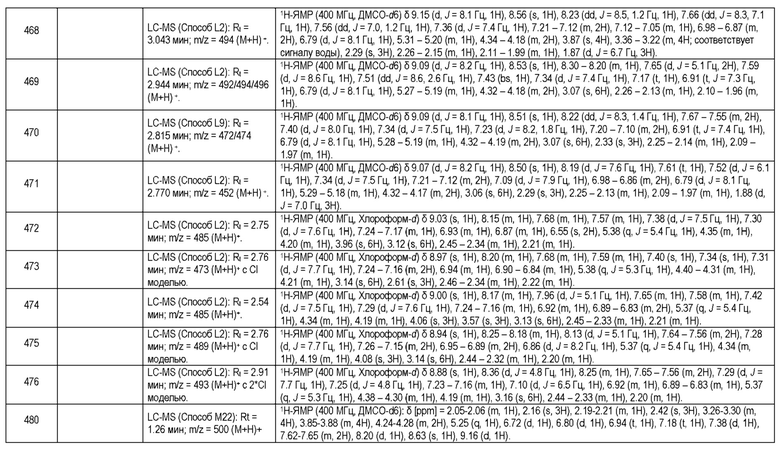
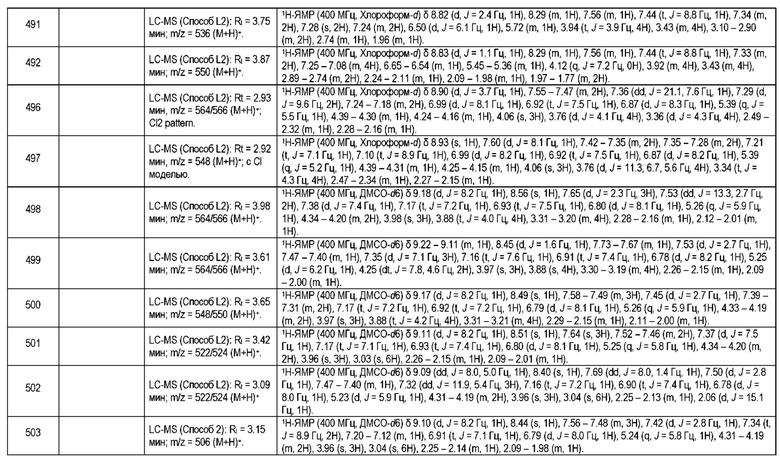
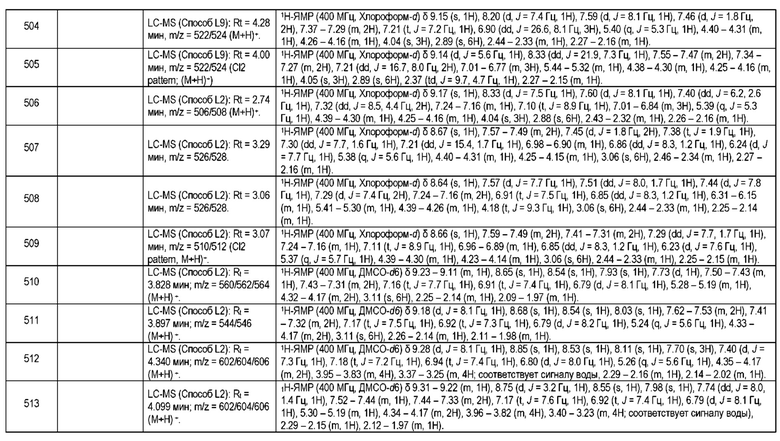
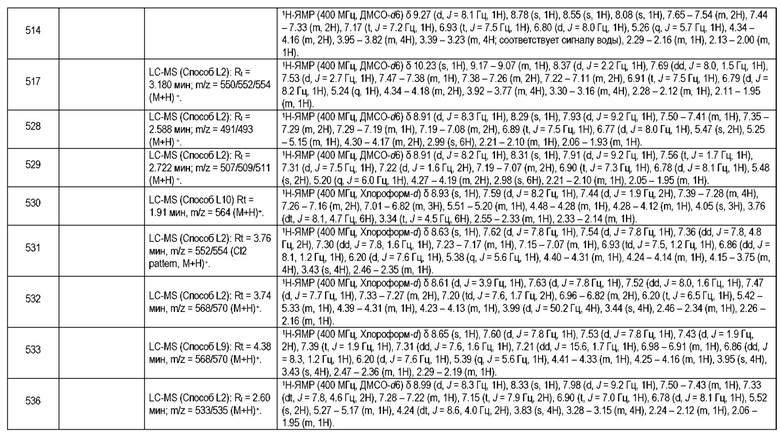
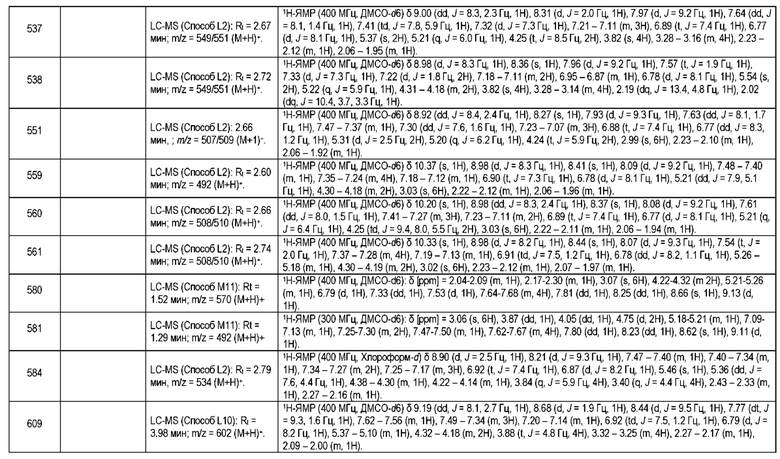
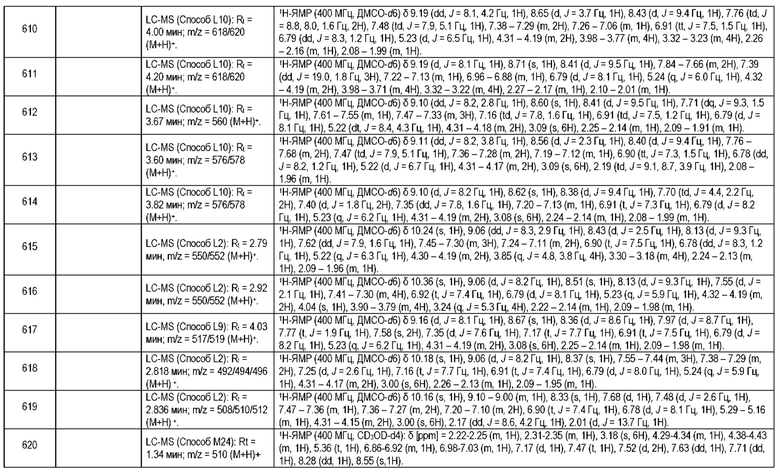
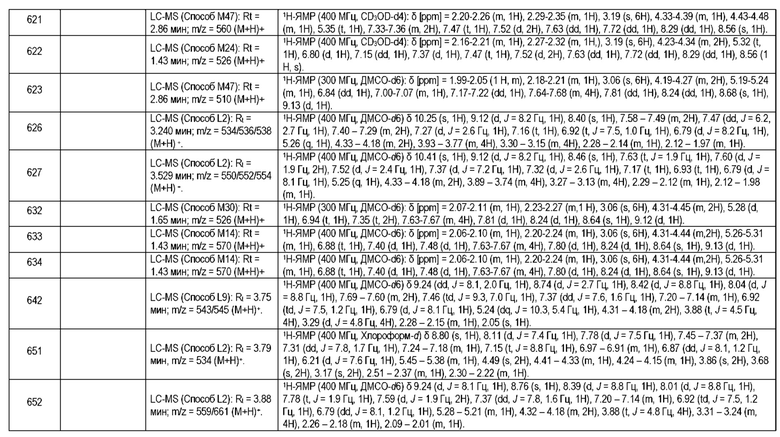
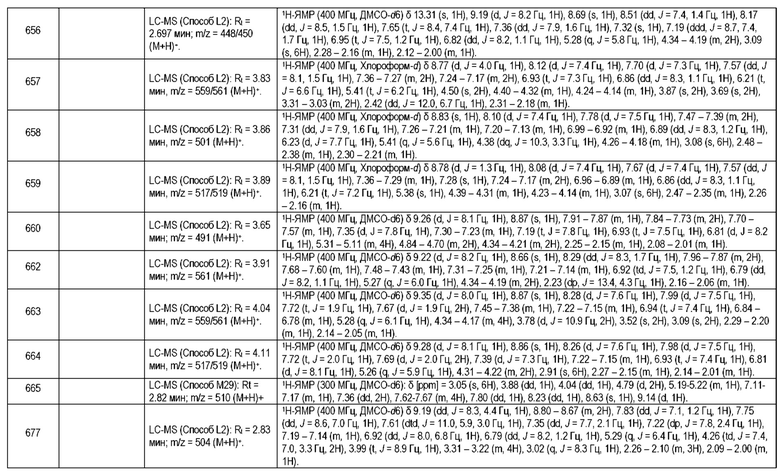
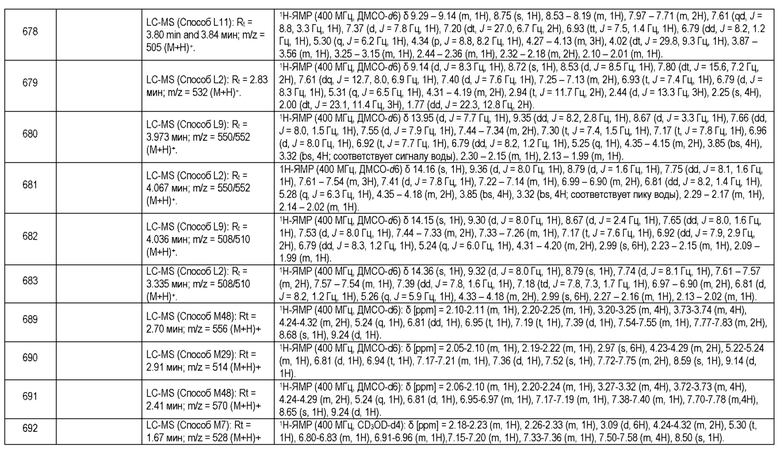
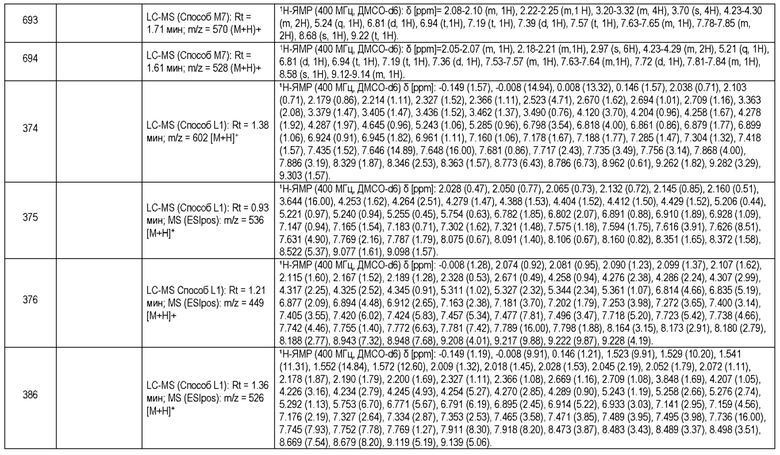
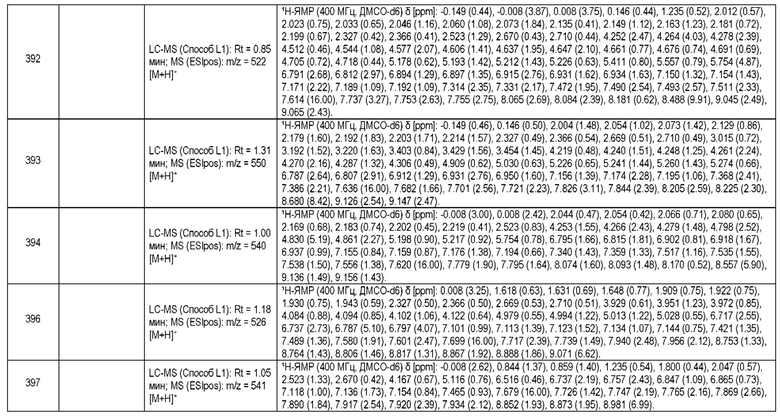
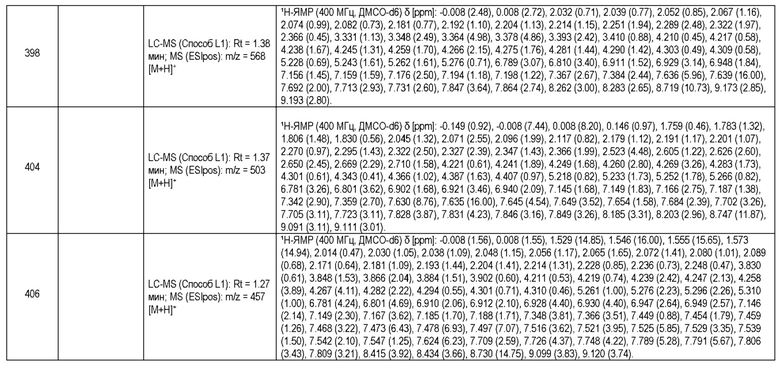
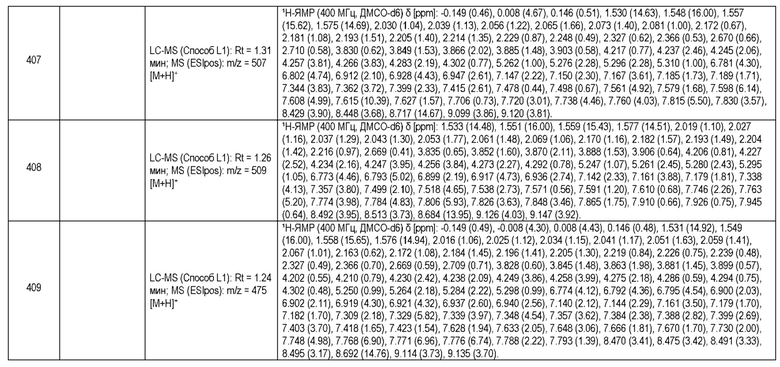
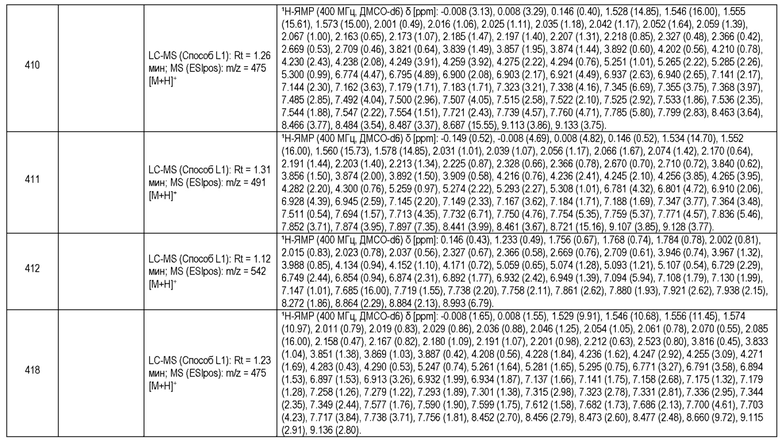
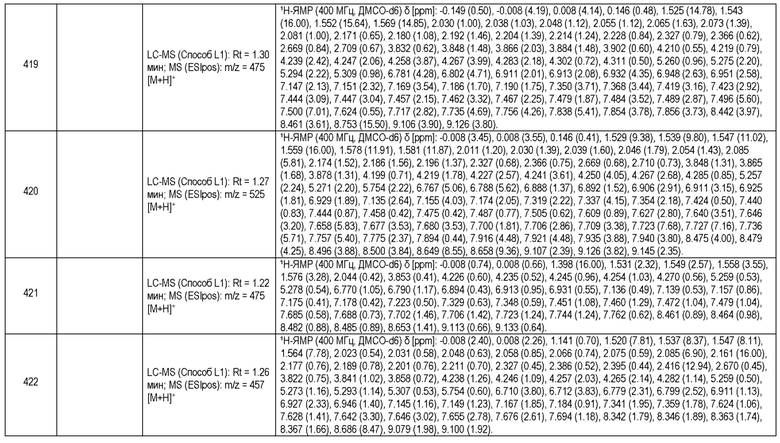
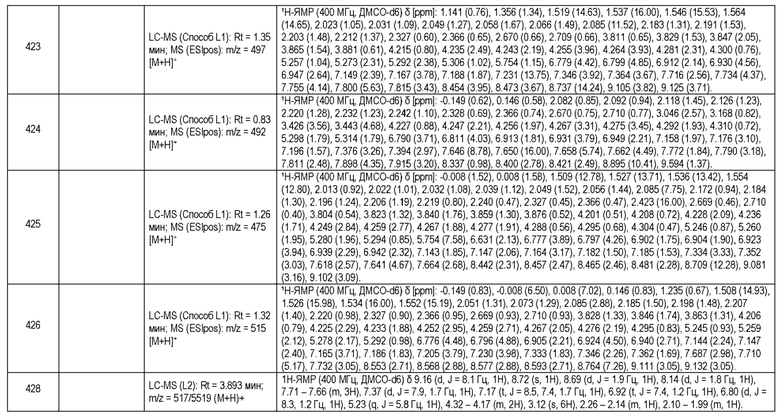
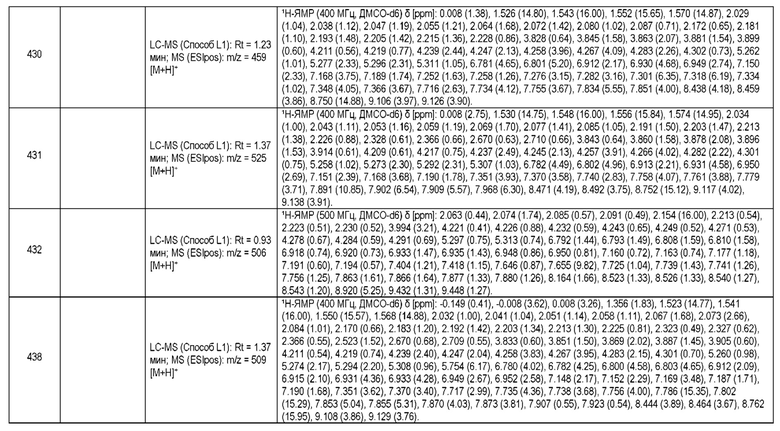
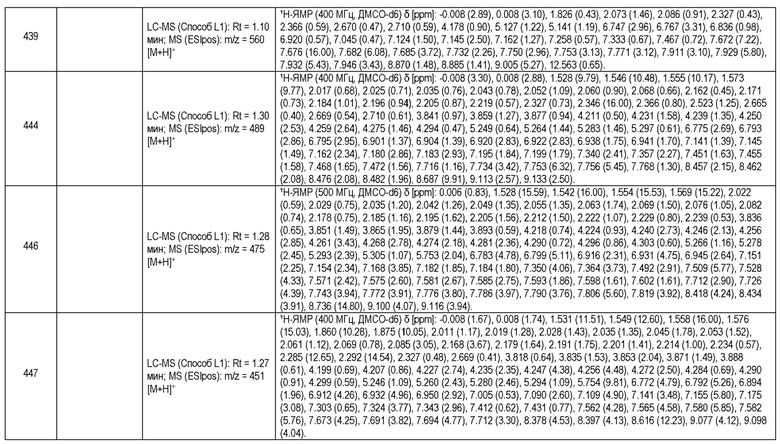
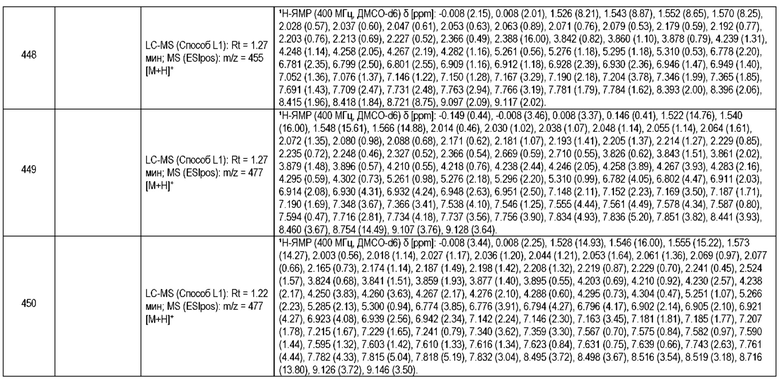
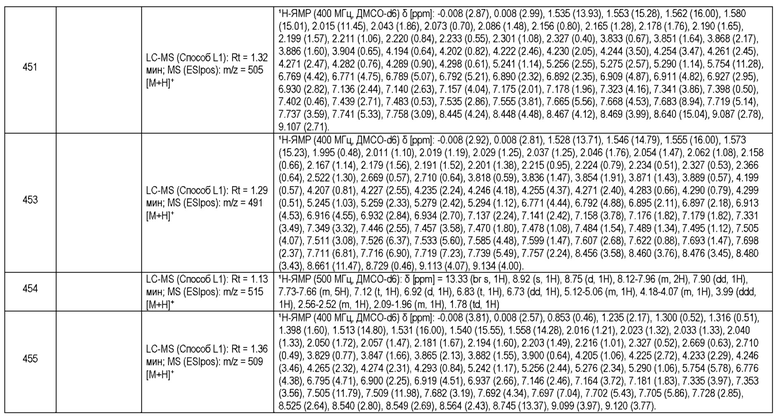
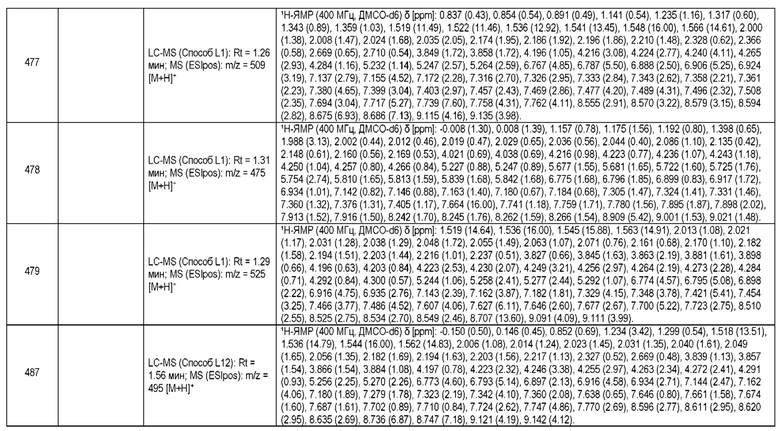
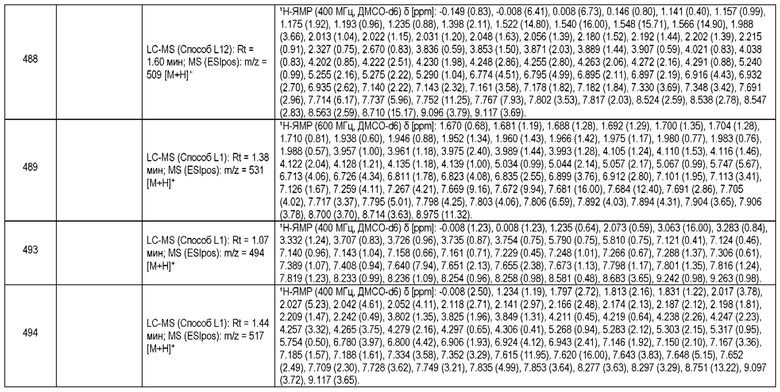
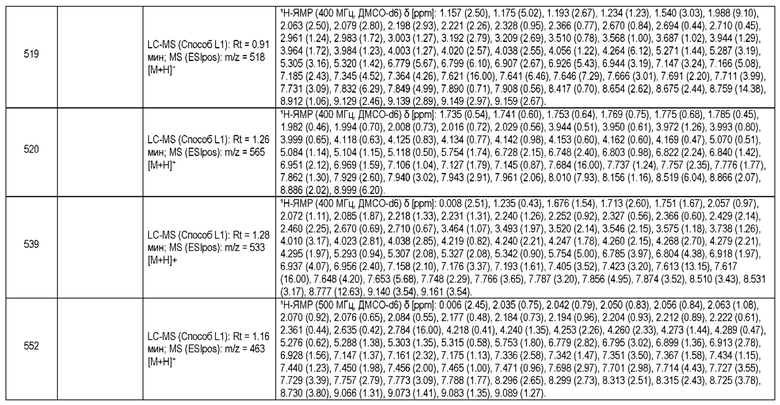
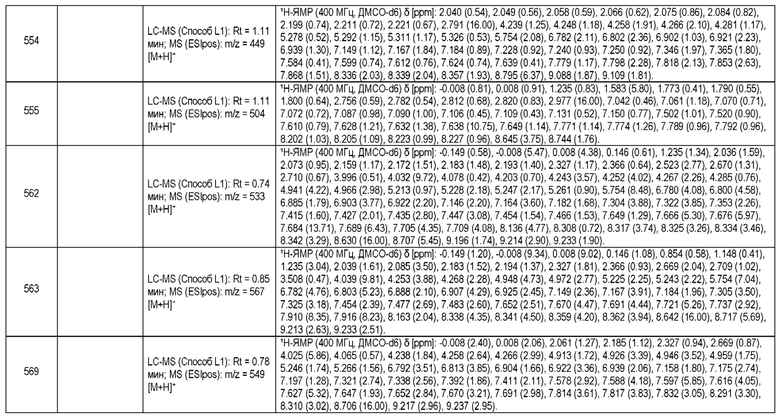
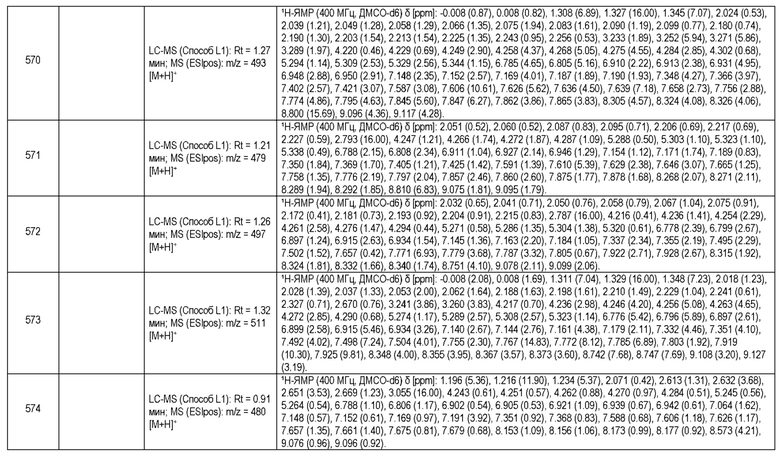
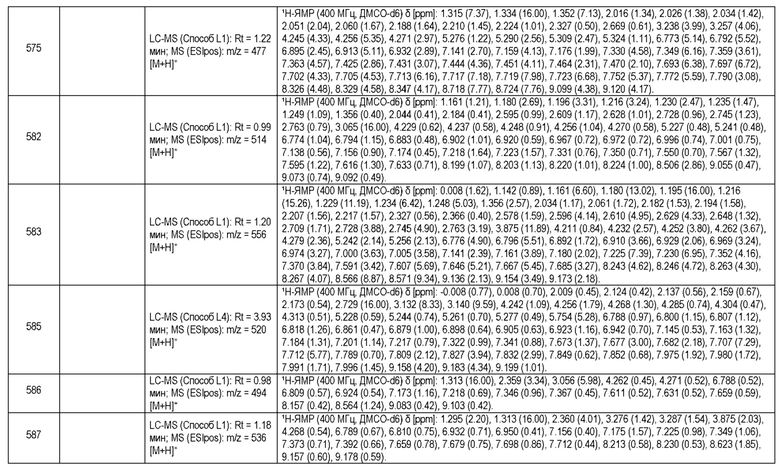
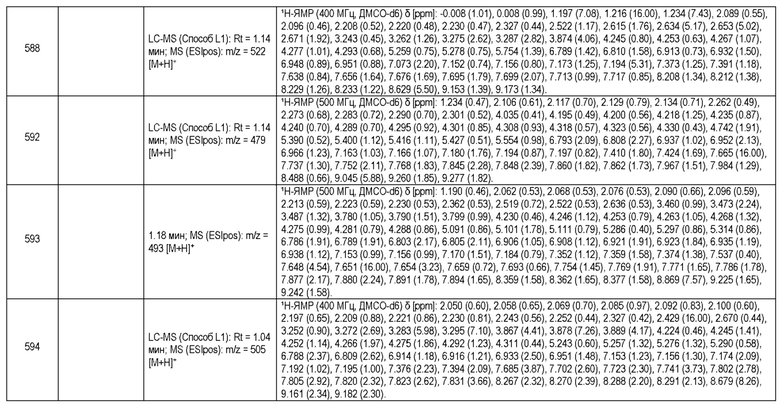
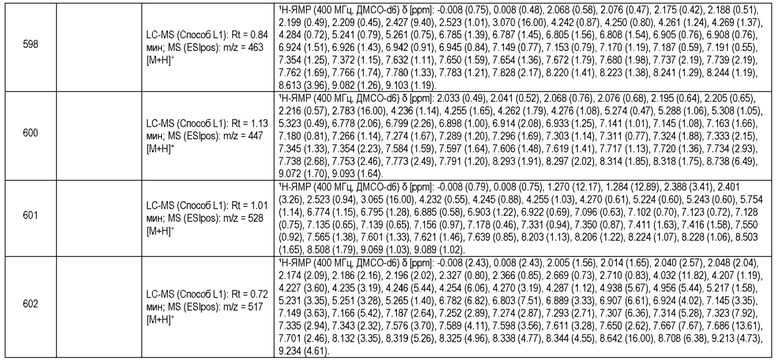
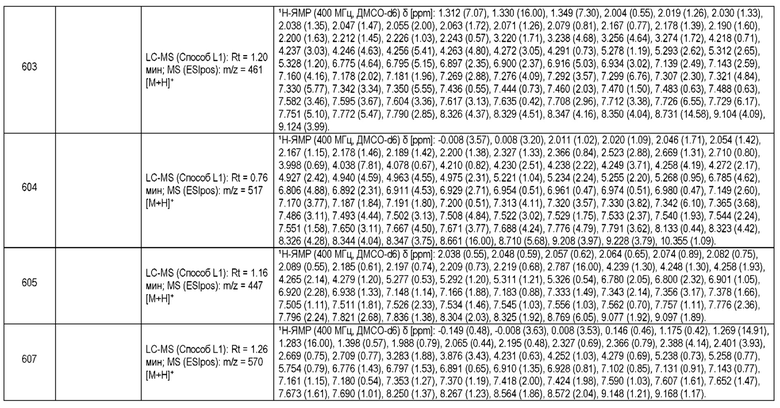
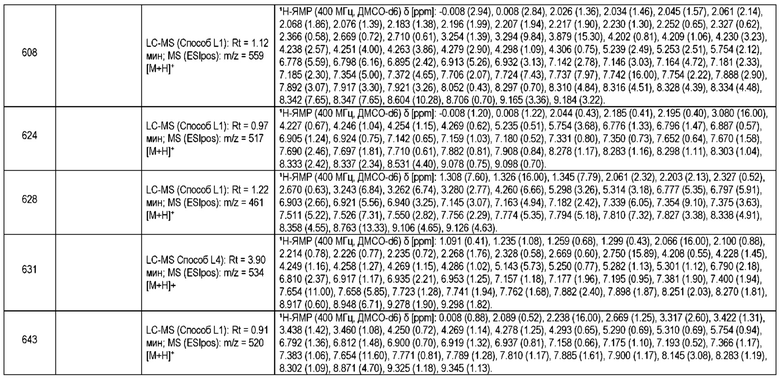
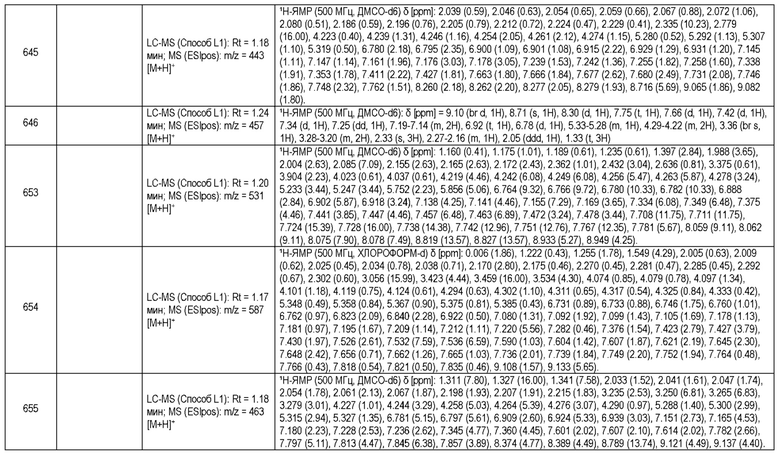
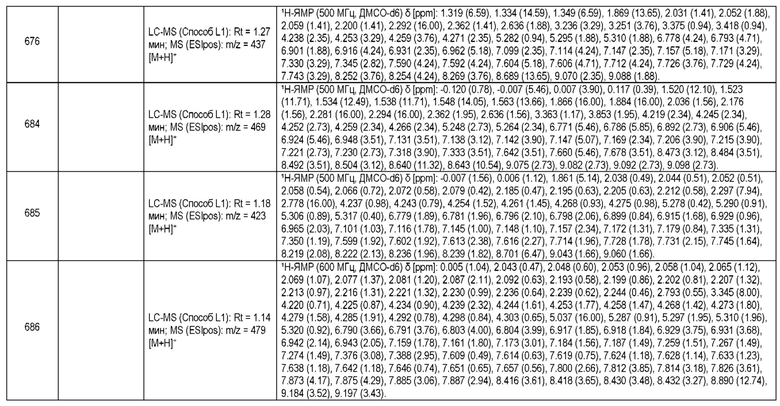
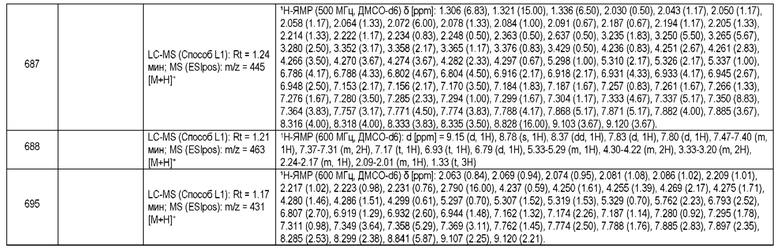
Таблицы 3a-3e: промежуточные соединения
Таблица 3a
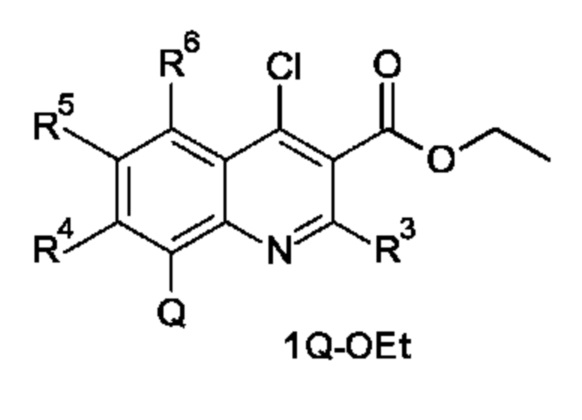
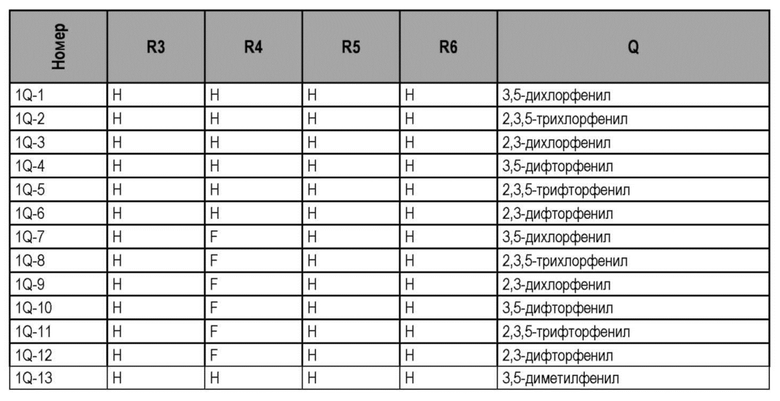
Таблица 3b
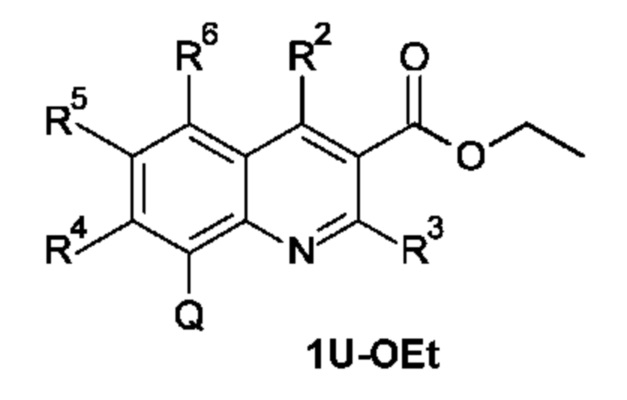
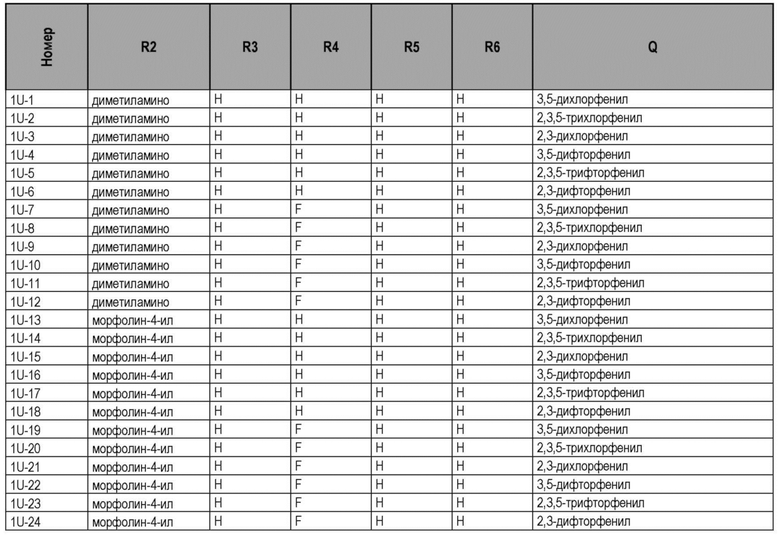
Таблица 3c
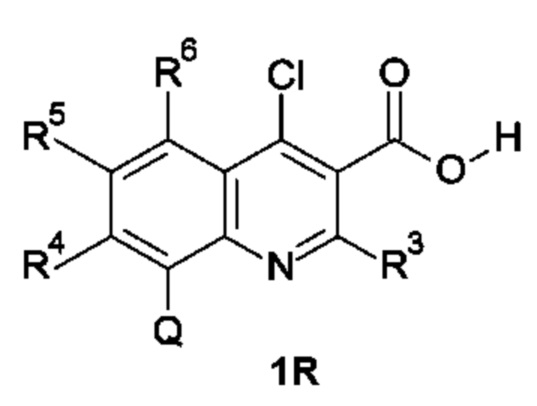
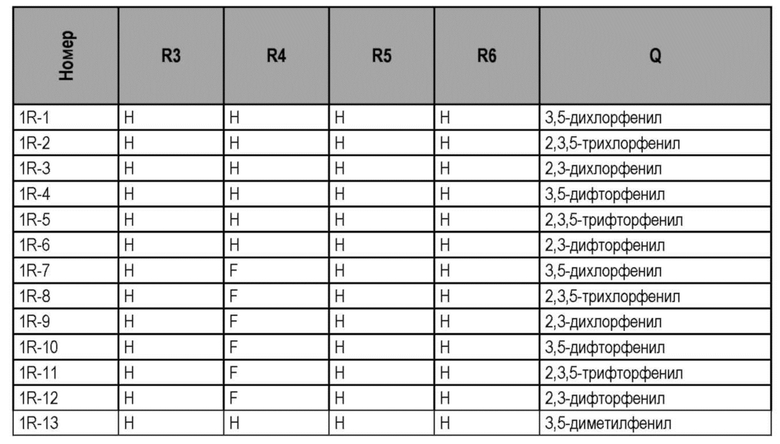
Таблица 3d
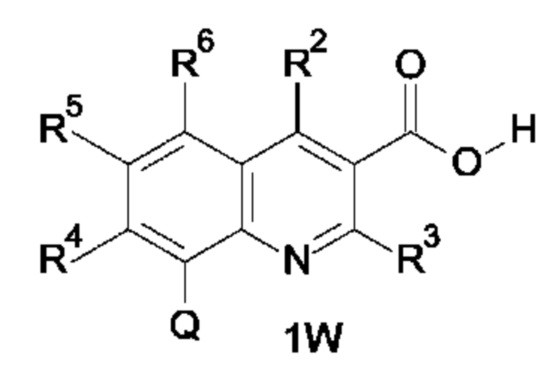
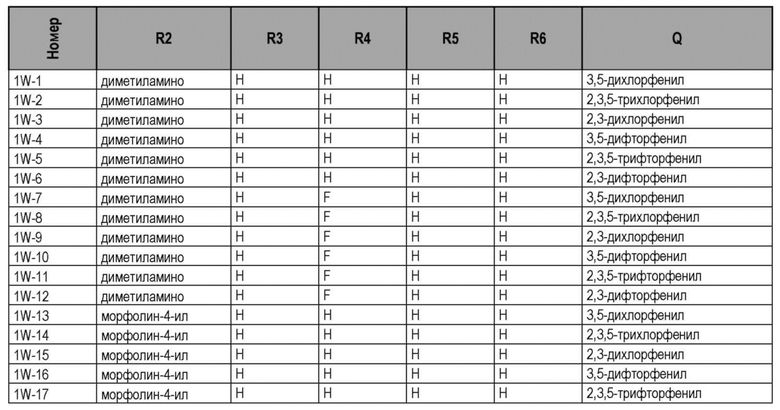
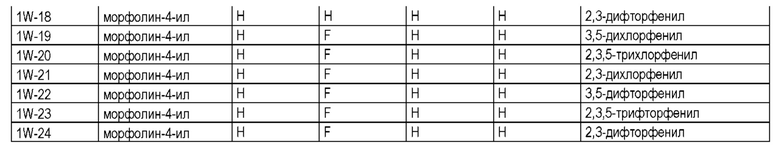
Таблица 3e
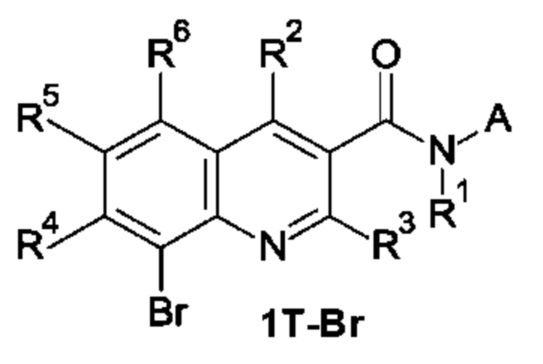
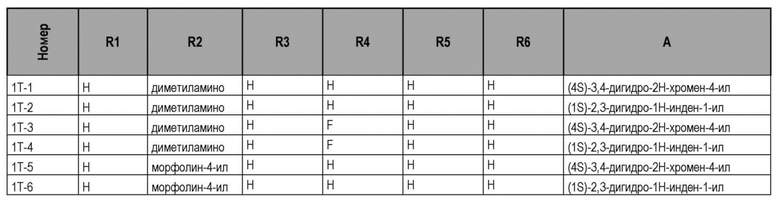

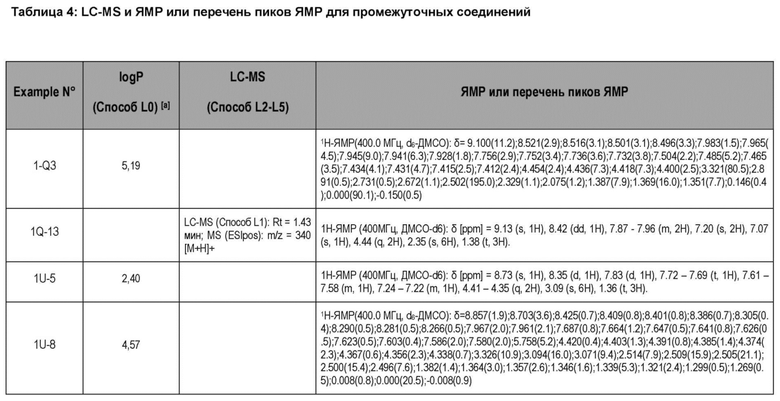
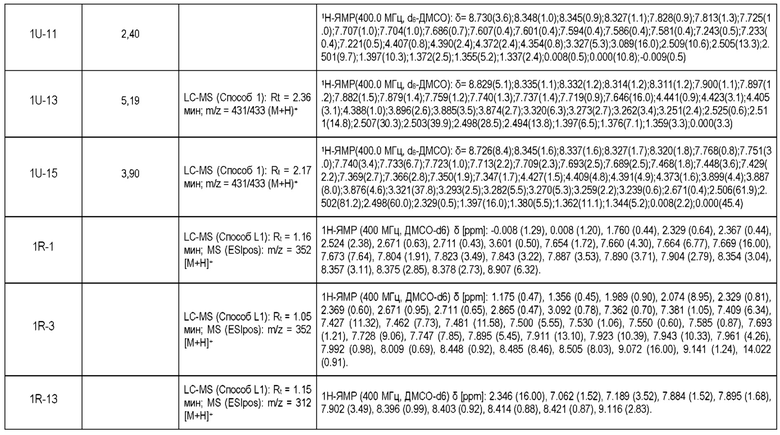
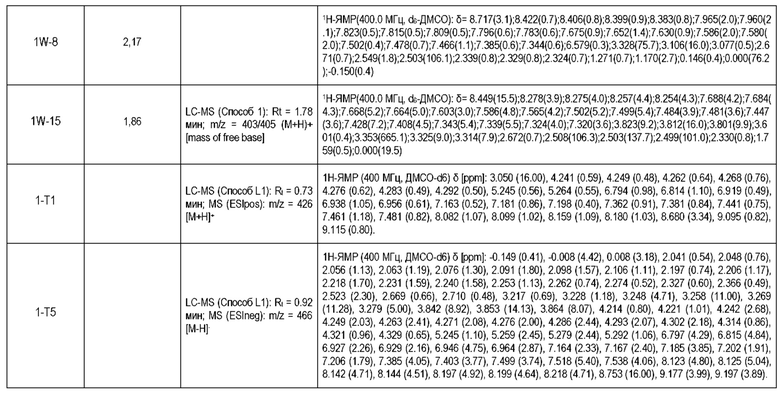

Экспериментальная часть - биологические анализы
Примеры тестировали в отдельных биологических анализах один или более раз.
При тестировании более одного раза данные сообщаются как средние значения, и как медианные значения, где
 среднее значение, также называемое средним арифметическим значением, представляет собой сумму полученных значений, поделенное на количество повторений тестирования, и
среднее значение, также называемое средним арифметическим значением, представляет собой сумму полученных значений, поделенное на количество повторений тестирования, и
 медианное значение представляет собой среднее число группы значений при ранжировании в порядке возрастания или убывания. Если число значений в наборе данных нечетное, медианным является среднее значение. Если число значений в наборе данных четное, медианное значение является средним арифметическим для двух средних значений.
медианное значение представляет собой среднее число группы значений при ранжировании в порядке возрастания или убывания. Если число значений в наборе данных нечетное, медианным является среднее значение. Если число значений в наборе данных четное, медианное значение является средним арифметическим для двух средних значений.
Примеры были синтезированы один или более раз. При синтезе более одного раза данные биологических анализов представляют в виде средних значений или медианных значений, вычисленных с использованием наборов данных, полученных при тестировании одной или более синтетических партий.
in vitro активность соединений согласно настоящему изобретению может быть продемонстрирована в следующих значения:
In vitro анализ 1: C. elegans Slo-1a - действие в отношении рекомбинантной клеточной линии C. elegans
Получение стабильной клеточной линии C. elegans CHO
CHO клеточную линию получили из ATCC, код ATCC CRL-9096. Для трансфекции плазмидной ДНК, чтобы экспрессировать C. elegans Slo-1a (номер доступа AAL28102) Клетки CHO пассировали до 40% конфлюэнции перед добавлением трансфекционного раствора в культуру клеток. Трансфекционный раствор включал 300 мкмл OptiMEM (Life Technologies, Nr.: 31985), 2 мкмл (=6 мкмг) плазмидной ДНК, содержащей ген C. elegans Slo 1 и 9 мкмл FugeneHD (Promega, Nr.: E2311), и его добавили к клеткам перед инкубацией в течение 48 часов при 37°C, 5% CO2. Трансфекционную среду заменили на среду отбора, которая содержала дополнительный G418 (2 мг/мл, Invitrogen, Nr.: 10131), и клетки высеяли в 384-луночный планшет (300 клеток/лунка). Через несколько недель оставшиеся выжившие клетки были протестированы с помощью чувствительного к напряжению красителя (Membrane Potential Analysis Kit, Molecular Devices Nr.: R8034) на экспрессии K+ канала. Клоны положительных клеток очищали методом ограниченного разбавления. Для этого клон с самым высоким и самым надежным сигналом в анализе с чувствительным к напряжению красителем дополнительно субклонировали (инкубировали) в 384-луночном планшете (0,7 клеток/лунка) для получения клональной чистоты. Это создает конечную стабильную клеточную линию СНО, экспрессирующую C. elegans Slo-1a.
Условия клеточной культуры
Клетки культивировали при 37°С и 5% CO2 в MEMalpha с Gutamax I (Invitrogen, Nr.: 32571), с добавкой 10% (об./об.) инактивированной теплом фетальной бычьей сывороткой (Invitrogen, Nr.: 10500), G418 (1 мг/мл, Invitrogen, Nr.: 10131). Клетки отделяли с использованием Accutase (Sigma, Nr.: A6964).
Измерения мембранного потенциала
Лабораторное тестирование соединений проводили на 384-луночных микротитровальных планшетах (MTPs, Greiner, Nr.: 781092). 8000 клеток/лунка высеевали на 384-луночные MTP и культивировали в течение 20-24 часов при 37°C и 5% CO2. После удаления клеточной культуральной среды клетки промывали один раз тиродом (150 мМ NaCl, 0.3 мМ KCl, 2 мМ CaCl2, 1 мМ MgCl2, 0.8 мМ NaH2PO4, 5 мМ глюкозы, 28 мМ Hepes, pH 7.4), а затем загружали чувствительный к напряжению краситель набора Membrane Potential Assay, разбавленный в тироде в течение 1 часа при комнатной температуре.
После начала измерения флуоресценции с использованием FLIPR Tetra (Molecular Devices, Exc. 510-545 нм, ЕмМ. 565-625 нм) тестируемые соединения добавили с последующим добавлением KCl тирода (конечная концентрация анализа: 70 мМ KCl, 2 мМ CaCl2, 1 мМ MgCl2, 0.8 мМ NaH2PO4, 5 мМ глюкоза, 28 мМ Hepes, pH 7.4, включая чувствительный к напряжению краситель). Измерение было завершено через 7 минут.
Статистика
Данные оценивались с использованием программного обеспечения ActivityBase XLfit (IDBS) для подгонки кривой и расчета полумаксимальной эффективной концентрации (EC50) и сообщаются как отрицательный десятичный логарифм (pE50).
Для следующих примеров, pE50>5,3-6,5 было обнаружено для: 27, 28, 85, 87, 88, 109, 131, 182, 183, 243, 345, 361, 363, 402, 424, 440, 510, 511, 521, 534, 547, 555, 580, 592, 599, 656.
Для следующих примеров, pE50>6,5-7,5 было обнаружено для: 1, 62, 68, 69, 71, 95, 114, 120, 122, 125, 129, 136, 148, 185, 216, 230, 241, 242, 246, 264, 276, 289, 299, 324, 346, 354, 372, 379, 389, 390, 399, 401, 424, 432, 439, 456, 459, 474, 512, 513, 514, 519, 546, 560, 568, 578, 581, 584, 625, 632, 634, 654, 665.
Для следующих примеров, pE50>7,5-8,5 было обнаружено для: 2, 3, 4, 5, 6, 23, 55, 58, 63, 64, 65, 66, 73, 74, 90, 93, 98, 102, 110, 117, 119, 124, 127, 128, 144, 145, 147, 150, 152, 154, 158, 159, 163, 173, 180, 188, 195, 196, 203, 204, 212, 213, 218, 219, 224, 229, 231, 232, 236, 245, 252, 253, 255, 257, 258, 259, 263, 266, 268, 269, 270, 273, 280, 284, 287, 288, 291, 295, 297, 301, 304, 308, 311, 312, 317, 319, 320, 321, 323, 325, 342, 343, 344, 348, 360, 370, 375, 378, 380, 381, 383, 384, 385, 386, 391, 392, 393, 394, 397, 403, 405, 412, 429, 433, 434, 443, 447, 454, 457, 458, 460, 461, 463, 464, 466, 471, 472, 473, 475, 476, 480, 481, 482, 483, 484, 486, 493, 494, 495, 499, 500, 501, 502, 503, 507, 508, 509, 515, 517, 518, 522, 523, 524, 525, 526, 527, 528, 529, 530, 531, 532, 533, 535, 536, 537, 538, 541, 545, 550, 551, 559, 561, 562, 563, 566, 567, 569, 570, 571, 572, 573, 574, 575, 577, 579, 585, 590, 593, 595, 597, 602, 615, 619, 620, 621, 622, 623, 626, 630, 633, 635, 640, 643, 661.
Для следующих примеров, pE50>8,5 было обнаружено для: 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 24, 25, 26, 29, 30, 31, 32, 33, 34, 35, 36, 37, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 56, 57, 60, 61, 70, 72, 75, 76, 77, 80, 81, 82, 83, 89, 100, 101, 108, 112, 115, 121, 130, 132, 133, 134, 135, 137, 138, 139, 140, 141, 142, 143, 146, 151, 153, 155, 156, 157, 160, 161, 162, 164, 165, 166, 167, 168, 169, 170, 171, 172, 174, 175, 176, 177, 178, 179, 181, 184, 186, 187, 189, 190, 191, 192, 193, 194, 197, 200, 201, 205, 206, 207, 208, 209, 210, 211, 214, 215, 217, 220, 221, 222, 223, 225, 226, 227, 228, 233, 234, 235, 237, 238, 239, 240, 244, 247, 248, 249, 250, 251, 254, 256, 260, 261, 262, 265, 267, 271, 272, 274, 275, 277, 278, 279, 281, 282, 283, 290, 292, 293, 294, 296, 298, 300, 302, 305, 307, 309, 310, 313, 314, 315, 316, 318, 322, 326, 327, 328, 329, 330, 331, 332, 333, 334, 335, 338, 339, 340, 341, 349, 350, 351, 352, 353, 355, 356, 357, 358, 359, 362, 364, 365, 366, 367, 368, 369, 371, 373, 374, 376, 377, 382, 387, 388, 395, 396, 398, 400, 404, 406, 407, 408, 409, 410, 411, 413, 414, 415, 416, 417, 418, 419, 420, 421, 422, 423, 425, 426, 427, 428, 429, 430, 431, 435, 436, 437, 438, 441, 442, 444, 445, 446, 448, 449, 450, 451, 452, 453, 455, 462, 465, 467, 468, 469, 470, 477, 478, 479, 485, 487, 488, 489, 490, 491, 492, 496, 497, 498, 504, 505, 506, 516, 517, 520, 539, 540, 542, 543, 544, 548, 549, 552, 553, 554, 556, 557, 558, 564, 565, 576, 582, 583, 586, 587, 588, 589, 591, 594, 596, 598, 600, 601, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 616, 617, 618, 624, 627, 628, 629, 631, 636, 637, 638, 639, 641, 642, 644, 645, 646, 647, 648, 649, 650, 651, 652, 653, 655, 657, 658, 659, 660, 662, 663, 664, 666.
In vitro анализ 2: Nippostrongylus brasiliensis (NIPOBR)
Взрослые Nippostrongylus brasiliensis промыли солевым буфером, содержащим 100 Ед/мл пенициллина, 0.1 мг/мл стрептомицина и 2.5 мкмкг/мл амфотерицина B. Тестируемые соединения растворили в DMSO, и червеобразных животных инкубировали в среде при конечной концентрации 10 мкмкг/мл (10 частей на миллион) соответственно 1 мкг/мл (1 частей на миллион). Аликвоту среды использовали для определения активности ацетилхолинэстеразы по сравнению с отрицательным контролем. Принцип измерения ацетилхолинэстеразы как показания для антигельминтной активности был описан в Rapson et al (1986) и Rapson et al (1987).
Для следующих примеров, активность (уменьшение AChE по сравнению с отрицательным контролем) составляла более 80% при 10 мкг/мл: 8, 9, 11, 12, 13, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 29, 31, 32, 33, 34, 35, 36, 37, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 57, 58, 59, 60, 61, 62, 64, 65, 66, 67, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 81, 82, 83, 87, 89, 95, 100, 101, 104, 108, 112, 115, 116, 119, 122, 123, 127, 128, 130, 132, 133, 134, 135, 136, 137, 138, 139, 141, 142, 143, 144, 146, 147, 148, 333, 334, 336, 338, 339, 340, 341, 349, 362, 363, 364, 373, 609, 610, 611, 612, 613, 614, 615, 617, 618, 619, 620, 623, 630.
Для следующих примеров, активность (уменьшение AChE по сравнению с отрицательным контролем) составляла более 80% при 1 мкг/мл: 8, 9, 12, 13, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 29, 31, 32, 33, 34, 35, 36, 37, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 57, 58, 60, 61, 65, 67, 69, 70, 73, 74, 75, 76, 77, 80, 81, 82, 83, 84, 89, 92, 93, 95, 100, 101, 108, 112, 114, 115, 116, 117, 118, 119, 122, 124, 125, 126, 127, 128, 129, 130, 132, 133, 134, 135, 136, 137, 138, 139, 142, 143, 144, 146, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 160, 161, 162, 163, 165, 166, 167, 168, 169, 170, 171, 172, 176, 178, 181, 182, 185, 186, 187, 189, 190, 191, 192, 193, 194, 195, 197, 198, 200, 201, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 214, 215, 217, 218, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 247, 249, 250, 251, 254, 256, 257, 260, 261, 262, 263, 265, 266, 268, 271, 272, 273, 274, 275, 276, 277, 279, 280, 281, 282, 283, 284, 285, 287, 288, 289, 290, 291, 292, 293, 294, 301, 302, 307, 308, 309, 310, 311, 313, 314, 315, 318, 319, 321, 322, 326, 327, 328, 329, 330, 331, 332, 333, 334, 336, 338, 339, 340, 341, 342, 347, 349, 350, 352, 353, 355, 356, 357, 358, 359, 360, 362, 364, 365, 367, 369, 370, 373, 374, 375, 377, 382, 384, 385, 386, 388, 392, 394, 395, 396, 397, 400, 403, 404, 406, 407, 408, 409, 410, 411, 413, 414, 415, 417, 418, 419, 420, 421, 422, 424, 425, 426, 427, 428, 429, 430, 431, 432, 433, 434, 435, 436, 437, 441, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 458, 460, 461, 462, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 476, 477, 478, 479, 482, 485, 486, 487, 488, 490, 491, 492, 495, 496, 497, 498, 499, 500, 501, 504, 505, 506, 507, 508, 509, 516, 517, 520, 527, 528, 529, 530, 531, 532, 533, 535, 536, 537, 538, 540, 541, 542, 543, 544, 545, 548, 549, 550, 551, 552, 553, 554, 556, 557, 558, 561, 562, 563, 564, 565, 566, 569, 570, 571, 572, 573, 574, 575, 576, 577, 578, 579, 581, 582, 583, 585, 586, 587, 588, 590, 594, 596, 597, 598, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 617, 618, 619, 620, 623, 624, 626, 627, 628, 629, 631, 632, 633, 634, 635, 636, 637, 638, 639, 640, 641, 642, 645, 646, 647, 648, 649, 650, 651, 652, 653, 655, 657, 658, 660.
In vitro анализ 3: Dirofilaria immitis microfilariae (DIROIM L1)
≥ 250 Dirofilaria immitis microfilariae, которые были свеже очищены от крови, добавили в лунки микротитровального планшета, содержащего питательную среду и тестируемое соединение в DMSO. Соединения протестировали в анализе зависимости от концентрации дважды. Личинки, подвергнутые воздействию DMSO, но не тестируемых соединений, применяли в качестве отрицательных контролей. Личинки оценивали через 72 часа инкубации с соединением. Эффективность определили как уменьшение подвижности по сравнению с отрицательным контролем. На основе оценки широкого диапазона концентраций, кривые концентрация-ответ, а также EC50-значения вычисляли.
Для следующих примеров EC50 составляла <0.1 частей на миллион: 1, 4, 5, 6, 7, 8, 9, 10, 12, 13, 15, 16, 17, 22, 23, 24, 25, 26, 29, 30, 31, 32, 33, 34, 35, 36, 37, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 50, 51, 52, 53, 54, 56, 57, 58, 60, 61, 64, 65, 69, 73, 74, 76, 77, 80, 81, 82, 83, 84, 89, 101, 103, 108, 111, 112, 115, 117, 119, 124, 125, 127, 128, 129, 130, 132, 133, 134, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 185, 186, 187, 188, 189, 190, 191, 192, 194, 196, 197, 200, 201, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 214, 215, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 244, 247, 248, 249, 250, 251, 253, 255, 256, 257, 258, 259, 260, 261, 262, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 283, 290, 292, 293, 296, 300, 303, 304, 305, 306, 307, 308, 309, 310, 311, 312, 313, 314, 315, 317, 319, 322, 326, 327, 329, 330, 331, 332, 333, 334, 338, 339, 340, 340, 341, 342, 344, 350, 351, 352, 353, 355, 356, 357, 358, 359, 360, 362, 364, 365, 366, 367, 368, 369, 373, 374, 375, 376, 377, 381, 382, 383, 384, 385, 386, 388, 390, 391, 392, 394, 395, 396, 400, 403, 404, 405, 406, 407, 408, 409, 410, 411, 413, 414, 415, 417, 418, 419, 420, 421, 422, 423, 425, 426, 427, 428, 429, 430, 431, 433, 434, 435, 436, 437, 438, 441, 442, 443, 444, 445, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 457, 458, 459, 460, 461, 462, 463, 464, 465, 466, 467, 468, 469, 470, 471, 472, 473, 474, 475, 476, 477, 478, 479, 480, 482, 483, 485, 486, 487, 488, 490, 491, 492, 493, 495, 497, 498, 499, 500, 501, 503, 504, 505, 506, 507, 508, 509, 516, 517, 521, 522, 523, 524, 525, 527, 528, 529, 530, 531, 532, 533, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 546, 547, 548, 549, 550, 551, 552, 553, 554, 556, 557, 558, 559, 560, 561, 562, 563, 564, 565, 566, 567, 568, 569, 570, 571, 572, 573, 574, 575, 576, 577, 578, 579, 581, 582, 583, 584, 586, 587, 588, 589, 590, 591,594, 596, 597, 598, 600, 601, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 616, 617, 618, 619, 620, 622, 623, 624, 626, 627, 628, 629, 632, 633, 634, 635, 636, 638, 639, 641, 642, 645, 646, 647, 648, 649, 650, 651, 652, 653, 655, 657, 658, 660.
Для следующих примеров EC50 составляла <1 частей на миллион: 3, 11, 19, 49, 55, 62, 63, 66, 67, 70, 71, 72, 75, 86, 90, 93, 94, 95, 99-1, 100, 102, 104, 105, 116, 135, 136, 137, 148, 182, 183, 184, 193, 195, 199, 213, 216, 230, 241, 242, 243, 245, 246, 252, 254, 263, 282, 288, 289, 291, 292, 294, 295, 299, 316, 320, 321, 323, 325, 343, 345, 348, 354, 361, 370, 371, 372, 373, 378, 379, 380, 401, 416, 424, 440, 456, 580, 585, 621, 630, 654.
Для следующих примеров EC50 составляла <10 частей на миллион: 2, 9, 13, 14, 18, 20, 21, 27, 28, 59, 67, 68, 78, 87, 88, 91, 92, 96, 99-2, 106, 113, 114, 118, 120, 122, 123, 126, 131, 149, 198, 202, 264, 284, 285, 286, 287, 288, 301, 302, 318, 324, 328, 335, 336, 337, 346, 347, 349, 363, 387, 389, 393, 397, 398, 399, 402, 412, 432, 439, 481, 484, 485, 489, 491, 492, 494, 510, 511, 512, 513, 514, 515, 518, 519, 520, 526, 534, 535, 555, 595, 599, 625, 631, 637, 640, 643, 644, 656, 659.
In vitro анализ 4: Dirofilaria immitis (DIROIM L4)
10 личинок третьей стадии Dirofilaria immitis, которые только выделили из их вектора (промежуточный хозяин), добавили в лунки микротитровального планшета, содержащего питательную среду и тестовое соединение в DMSO. Соединения протестировали в анализе зависимости от концентрации дважды. Личинки, подвергнутые воздействию DMSO, но не тестируемых соединений, применяли в качестве отрицательных контролей. Личинки оценивали через 72 часа инкубации с соединением. В течение этих 72 часов инкубации большинство личинок отрицательного контроля перешли в личинки четвертой стадии. Эффективность определили как уменьшение подвижности по сравнению с отрицательным контролем. На основе оценки широкого диапазона концентраций, кривые концентрация-ответ, а также EC50-значения вычисляли.
Для следующих примеров EC50<0.1 части на миллион: 7, 8, 9, 10, 11, 12, 13, 15, 16, 17, 18, 19, 21, 22, 23, 24, 25, 26, 29, 30, 31, 32, 33, 34, 35, 36, 37, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 69, 73, 74, 75, 76, 77, 81, 82, 83, 89, 101, 108, 112, 117, 119, 124, 125, 127, 130, 132, 133, 134, 138, 139, 140, 141, 142, 143, 144, 146, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 174, 175, 176, 177, 178, 179, 181, 186, 190, 191, 192, 194, 196, 197, 200, 203, 204, 205, 206, 207, 208, 209, 210, 211, 212, 214, 215, 217, 218, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229, 231, 232, 233, 234, 235, 236, 237, 238, 239, 240, 247, 248, 249, 250, 251, 253, 256, 257, 258, 259, 260, 261, 262, 265, 267, 268, 271, 272, 275, 277, 278, 279, 280, 281, 283, 290, 300, 304, 309, 310, 313, 314, 315, 319, 322, 326, 327, 330, 331, 332, 333, 334, 336, 338, 339, 340, 341, 350, 351, 352, 353, 355, 356, 357, 358, 359, 360, 362, 365, 366, 367, 374, 376, 377, 382, 384, 385, 386, 388, 390, 392, 394, 395, 396, 400, 403, 404, 405, 406, 407, 408, 409, 410, 411, 413, 414, 415, 417, 418, 419, 420, 421, 422, 423, 425, 426, 427, 429, 430, 431, 433, 434, 436, 437, 438, 441, 442, 443, 444, 446, 447, 448, 449, 450, 451, 452, 453, 454, 455, 457, 462, 463, 465, 466, 467, 468, 469, 470, 476, 477, 478, 479, 480, 482, 485, 486, 487, 488, 490, 491, 492, 493, 495, 496, 497, 498, 499, 504, 505, 506, 507, 516, 517, 523, 525, 527, 528, 529, 530, 531, 532, 533, 536, 537, 538, 539, 540, 541, 542, 543, 544, 545, 548, 549, 550, 551, 552, 553, 554, 556, 557, 558, 559, 561, 562, 563, 564, 565, 566, 567, 568, 570, 571, 572, 573, 575, 576, 577, 578, 579, 582, 583, 584, 587, 589, 590, 591, 596, 597, 600, 602, 603, 604, 605, 606, 607, 608, 609, 610, 611, 612, 613, 614, 615, 617, 618, 619, 628, 629, 635, 638, 660.
Для следующих примеров EC50<1 части на миллион: 1, 2, 3, 14, 20, 54, 80, 115, 150, 201, 244, 266, 364, 373.
Для следующих примеров EC50<10 частей на миллион: 133, 187
In vitro анализ 5: Litomosoides sigmodontis (LTMOSI L3)
10 личинок третьей стадии Litomosoides sigmodontis, которые только выделили из плевральной полости инфицированного грызуна, добавили в лунки микротитровального планшета, содержащего питательную среду и тестовое соединение в ДМСО. Соединения протестировали в анализе зависимости от концентрации дважды. Личинки, подвергнутые воздействию ДМСО, но не тестируемых соединений, применяли в качестве отрицательных контролей. Личинки оценивали через 72 часа инкубации с соединением. Эффективность определили как уменьшение подвижности по сравнению с отрицательным контролем. На основе оценки широкого диапазона концентраций, кривые концентрация-ответ, а также EC50-значения вычисляли.
Для следующих примеров EC50<0.1 части на миллион: 8, 9, 10, 12, 13, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 29, 32, 33, 34, 35, 36, 37, 45, 46, 48, 52, 53, 54, 74, 76, 77, 112, 133, 134, 141, 143, 339, 341, 350, 376, 382, 384, 385, 386, 394, 395, 396.
Для следующих примеров EC50<1 части на миллион: 3, 15, 44, 73, 373.
In vitro анализ 6: Cooperia curticei (COOPCU L3)
Растворитель: диметилсульфоксид
Для получения подходящего препарата активного соединения, 10 мг активного соединения растворили в 0.5 мл растворителя, и концентрат разбавили с помощью "раствора Рингера" до желаемой концентрации.
Около 40 личинок нематод (Cooperia curticei) перенесли в тестовую пробирку, содержащую раствор соединения.
Через 5 дней вычислили смертность личинок. 100% эффективность означает, что все личинки погибли; 0% эффективность означает, что ни одна личинка не погибла.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 100% при норме применения 20 частей на миллион: 8, 9, 10, 13, 17, 22, 23, 24, 29, 32, 33, 34, 36, 37, 45, 46, 52, 53, 57, 76, 77, 81, 83, 132, 133, 134, 139, 143, 150, 153, 155, 156, 157, 166, 167, 169, 170, 172, 191, 192, 193, 194, 195, 196, 197, 200, 204, 205, 206, 207, 208, 209, 210, 214, 215, 217, 218, 221, 222, 224, 226, 235, 236, 237, 247, 265, 266, 274, 280, 300, 309, 326, 327, 329, 332, 341, 350, 353, 356, 357, 359, 373, 377, 384, 385, 386, 395, 396, 407, 408, 410, 411, 415, 419, 420, 421, 426, 431, 438, 445, 449, 450, 451, 453, 454, 455, 464, 477, 479, 486, 487, 488, 496, 497, 504, 505, 506, 507, 516, 528, 529, 530, 531, 532, 533, 536, 537, 538, 539, 541, 542, 545, 551, 554, 557, 558, 562, 563, 564, 565, 569, 572, 573, 575, 576, 596, 600, 603, 604, 605, 607, 608, 624, 628, 631, 637, 638, 639, 642, 647, 651, 652, 655, 657, 658, 659, 660.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 90% при норме применения 20 частей на миллион: 16, 31, 40, 48, 50, 54, 60, 80, 108, 125, 142, 152, 176, 178, 179, 191, 201, 203, 220, 223, 229, 240, 251, 257, 259, 260, 271, 275, 276, 281, 292, 314, 330, 331, 333, 338, 339, 358, 382, 400, 406, 435, 444, 446, 462, 465, 467, 469, 473, 476, 491, 500, 509, 540, 543, 548, 552, 553, 601, 602, 615, 640, 648.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 80% при норме применения 20 частей на миллион: 15, 21, 30, 41, 42, 44, 47, 49, 51, 58, 65, 70, 75, 89, 135, 146, 154, 162, 163, 181, 211, 212, 228, 238, 239, 250, 272, 294, 298, 307, 310, 315, 318, 322, 328, 367, 394, 404, 409, 418, 424, 432, 460, 471, 482, 485, 490, 492, 495, 508, 556, 583, 587, 614, 650.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 100% при норме применения 4 части на миллион: 8, 13, 17, 22, 23, 24, 32, 33, 34, 36, 37, 45, 46, 52, 53, 57, 76, 77, 81, 83, 132, 133, 134, 143, 151, 153, 155, 167, 169, 170, 172, 192, 194, 195, 197, 200, 205, 207, 209, 210, 214, 215, 217, 222, 226, 237, 265, 266, 273,274, 300, 309, 327, 329, 332, 350, 353, 359, 373, 384, 385, 386, 395, 395, 396, 407, 408, 410, 411, 415, 420, 421, 426, 431, 438, 445, 449, 450, 451, 453, 455, 477, 479, 487, 488, 496, 497, 499, 504, 505, 529, 530, 531, 532, 533, 536, 539, 541, 542, 545, 554, 557, 558, 562, 563, 564, 565, 569, 572, 573, 575, 576, 596, 600, 604, 607, 608, 628, 631, 637, 638, 639, 642, 647, 651, 652, 655, 657, 658, 659, 660.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 90% при норме применения 4 части на миллион: 9, 29, 31, 40, 54, 60, 125, 139, 142, 152, 156, 157, 166, 191, 193, 196, 208, 218, 221, 223, 229, 235, 236, 247, 271, 275, 292, 326, 330, 338, 341, 356, 357, 358, 419, 435, 446, 462, 464, 469, 476, 500, 506, 507, 540, 551, 552, 601, 603, 605, 648.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 80% при норме применения 4 части на миллион: 10, 16, 39, 42, 44, 47, 48, 50, 51, 58, 80, 108, 146, 163, 171, 178, 201, 203, 206, 211, 212, 224, 240, 258, 260, 280, 281, 286, 318, 333, 339, 400, 406, 409, 430, 437, 444, 465, 467, 486, 491, 508, 509, 516, 528, 537, 548, 583, 602, 614, 624, 640.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 80% при норме применения 0.8 частей на миллион: 190, 549.
In vitro анализ 7: Haemonchus contortus (HAEMCO L3)
Растворитель: диметилсульфоксид
Для получения подходящего препарата активного соединения, 10 мг активного соединения растворили в 0.5 мл растворителя, и концентрат разбавили с помощью "Раствора Рингера" до желаемой концентрации.
Около 40 личинки красного желудочного червя (Haemonchus contortus) перенесли в тестовую пробирку, содержащую раствор соединения.
Через 5 дней вычисляли процент смертности личинок. 100% эффективность означает, что все личинки погибли, 0% эффективность означает, что ни одна личинка не погибла.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 100% при норме применения 20 частей на миллион: 8, 13, 15, 17, 22, 23, 24, 29, 32, 33, 34, 36, 37, 46, 47, 48, 50, 52, 53, 57, 60, 76, 77, 81, 83, 132, 133, 134, 135, 139, 142, 143, 153, 155, 166, 167, 169, 170, 172, 192, 194, 197, 200, 205, 206, 207, 214, 215, 218, 221, 222, 224, 226, 235, 237, 247, 265, 266, 274, 275, 280, 300, 309, 312, 326, 329, 330, 331, 332, 350, 353, 359, 373, 377, 384, 385, 386, 395, 396, 407, 410, 411, 415, 450, 455, 477, 486, 487, 488, 496, 497, 504, 505, 506, 509, 528, 529, 530, 531, 533, 537, 538, 539, 541, 542, 545, 551, 552, 554, 558, 562, 563, 564, 565, 569, 572, 573, 575, 576, 596, 604, 605, 608, 628, 631, 637, 638, 647, 651, 652, 655, 658, 659, 660.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 90% при норме применения 20 частей на миллион: 10, 31, 44, 45, 51, 74, 75, 136, 146, 150, 156, 179, 191, 203, 204, 209, 210, 217, 220, 223, 229, 236, 249, 250, 251, 258, 260, 271, 272, 327, 356, 357, 358, 400, 408, 421, 435, 438, 444, 445, 449, 451, 453, 460, 469, 476, 508, 532, 540, 548, 553, 557, 600, 602, 603, 615, 640, 642, 648, 657.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 80% при норме применения 20 частей на миллион: 12, 16, 39, 40, 42, 70, 125, 137, 138, 152, 157, 176, 178, 180, 208, 257, 259, 273, 276, 281, 292, 307, 310, 333, 341, 388, 392, 394, 419, 420, 432, 434, 446, 464, 473, 479, 491, 499, 500, 507, 516, 535, 543, 619, 624, 645, 646, 650.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 100% при норме применения 4 части на миллион: 8, 9, 13, 17, 22, 23, 24, 29, 32, 34, 36, 37, 40, 46, 52, 57, 60, 76, 77, 81, 132, 133, 134, 139, 142, 143, 153, 155, 170, 192, 197, 200, 205, 214, 222, 237, 247, 265, 266, 274, 309, 330, 332, 339, 350, 359, 373, 384, 385, 386, 395, 410, 411, 455, 477, 488, 496, 497, 504, 509, 530, 531, 539, 541, 542, 545, 554, 558, 562, 563, 564, 565, 569, 572, 573, 575, 576, 596, 605, 608, 628, 631, 637, 639, 647, 651, 652, 655, 658, 659, 660.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 90% при норме применения 4 части на миллион: 10, 15, 31, 33, 45, 47, 50, 83, 135, 146, 151, 166, 167, 169, 191, 194, 207, 209, 221, 226, 229, 235, 236, 271, 272, 275, 300, 326, 329, 353, 357, 358, 396, 400, 407, 408, 415, 421, 435, 436, 438, 445, 450, 451, 476, 487, 505, 508, 528, 529, 533, 536, 537, 540, 552, 600, 603, 604, 638, 640, 648.
В этом тесте, например, следующие соединения из примеров получения показали хорошую активность 80% при норме применения 4 части на миллион: 42, 44, 48, 51, 53, 74, 75, 150, 156, 172, 195, 206, 210, 215, 217, 218, 223, 232, 260, 281, 307, 327, 341, 356, 377, 392, 394, 403, 419, 42, 426, 444, 449, 453, 469, 470, 471, 479, 486, 500, 506, 507, 551, 557, 642, 645, 650, 657.
Примеры композиции
Примерные композиции состояли из активного вещества в 10% Transcutol, 10% Cremophor EL и 80% изотоническом солевом растворе. Сначала активное вещество растворяли в Transcutol. После растворения в Transcutol добавляли Cremophor и изотонический солевой раствор. Эти композиции использовались в качестве рабочих композиций в следующем анализе in vivo.
Примером композиции согласно настоящему изобретению является следующая примерная композиция F1. Активное вещество растворили в Transcutol с образованием сток-раствора A. Затем 0.100 мл этого сток-раствора A взяли, и 0.100 мл Cremophor EL и 0.800 мл изотонического солевого раствора добавили. Полученная жидкая композиция (пример композиции F1) имела объем 1 мл.
Сток-раствор A:
4.0 мг соединения примера 8,
0.100 мл Transcutol.
Пример композиции F1:
0.100 мл сток-раствора A,
0.100 мл Cremophor EL, и
0.800 мл изотонического солевого раствора.
In vivo анализ
Haemonchus contortus / Trichostrongylus colubriformis / песчанка
Песчанок, экспериментально зараженных Haemonchus и/или Trichostrongylus, обрабатывали один раз во время поздней препотентности. Тестируемые соединения получали в виде растворов или суспензий и применяли перорально или интраперитонеально. Для обоих применений использовалась одна и та же форма применения. Объем применения обычно составлял максимум 20 мл/кг. В качестве примера, песчанку с массой тела 40 г обрабатывали 0,200 мл композиции примера F1. Это соответствовало обработке 20 мг/кг массы тела.
Эффективность определяли для каждой группы как уменьшение количества червей в желудке и тонкой кишке, соответственно, после вскрытия по сравнению с количеством червей в контрольной группе, инфицированной и получавшей плацебо.
Следующие примеры были протестированы и имели активность ≥70% или выше при данной обработке:
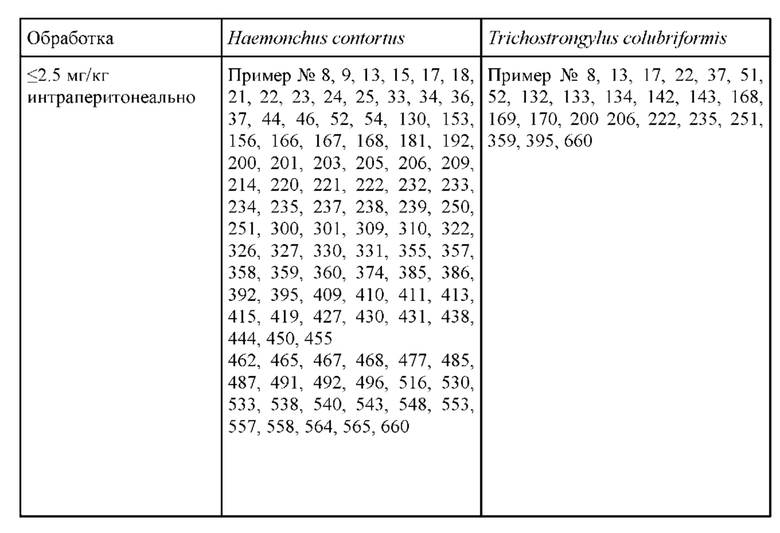
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА | 2020 |
|
RU2839897C2 |
| НОВЫЕ АНТИГЕЛЬМИНТНЫЕ СОЕДИНЕНИЯ | 2019 |
|
RU2828007C2 |
| НОВЫЕ ХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2792933C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ПИРАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ | 2018 |
|
RU2781426C2 |
| НОВЫЕ ПИРАЗОЛПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2017 |
|
RU2769448C2 |
| N-(2-ФТОР-2-ФЕНЭТИЛ)КАРБОКСАМИДЫ В КАЧЕСТВЕ НЕМАТИЦИДОВ И ЭНДОПАРАЗИТИЦИДОВ | 2014 |
|
RU2667779C2 |
| НОВЫЕ АЗАХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2018 |
|
RU2773290C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2830113C2 |
| ПРИМЕНЕНИЕ АРИЛЬНЫХ И ГЕТАРИЛЬНЫХ КАРБОКСАМИДОВ В КАЧЕСТВЕ ЭНДОПАРАЗИТИЦИДОВ | 2012 |
|
RU2638830C2 |
| СОСТАВЫ ДЛЯ МЕСТНОГО НАНЕСЕНИЯ, ВКЛЮЧАЮЩИЕ ПРОИЗВОДНОЕ 1-N-АРИЛПИРАЗОЛА И ФОРМАМИДИН | 2004 |
|
RU2361401C2 |
Изобретение относится к области органической химии, а именно к производному хинолин-амиду общей формулы (I) или к его фармацевтически приемлемой соли, где R1, R3 представляют собой водород или метил, R4 выбирают из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, метокси, трифторметила, трифторметокси и NH2, R5 выбирают из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, метокси, трифторметила и трифторметокси, R6 выбирают из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила и метокси, значения радикалов A, R2 и Q являются такими, как это определено в формуле изобретения. Также изобретения относится к промежуточным соединениям общих формул (II), (III), где значения радикалов имеют указанные в формуле изобретения значения; фармацевтической композиции на основе соединения формулы (I); применению соединения формулы (I); способу контроля гельминтных инфекций у людей и/или животных. Технический результат: получены новые гетероциклические соединения, полезные при гельминтных инфекциях у людей и/или животных. 7 н. и 5 з.п. ф-лы, 10 табл., 695 пр.
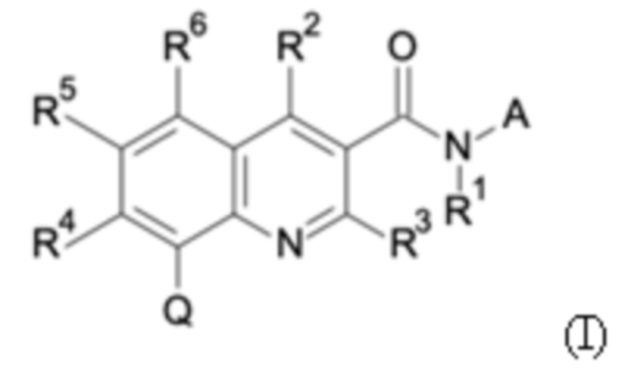 ,
, 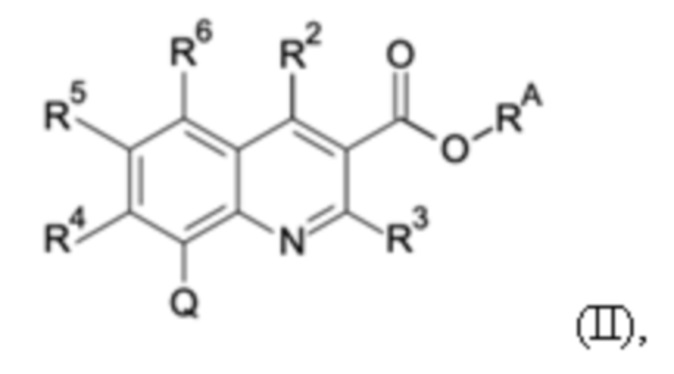
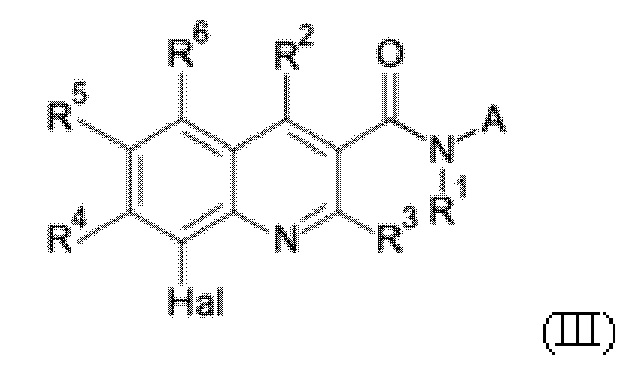
1. Соединение общей формулы (I):
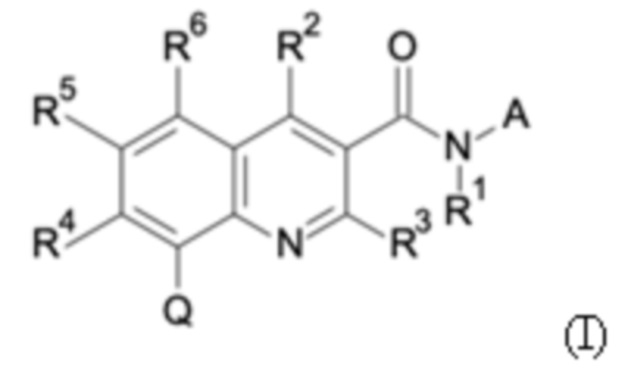 ,
,
в которой:
A выбран из группы, состоящей из:
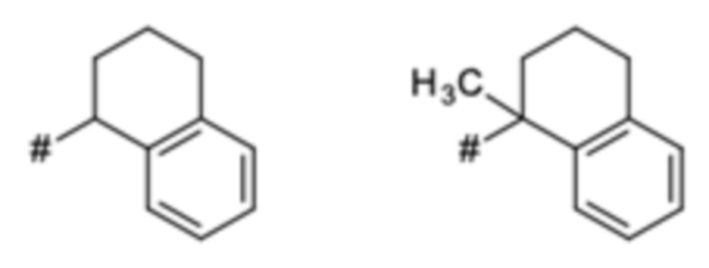
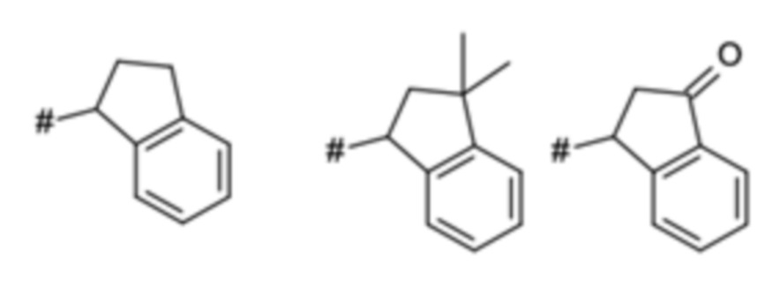
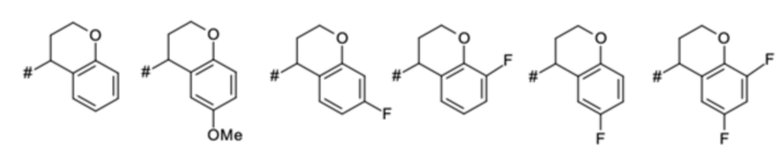
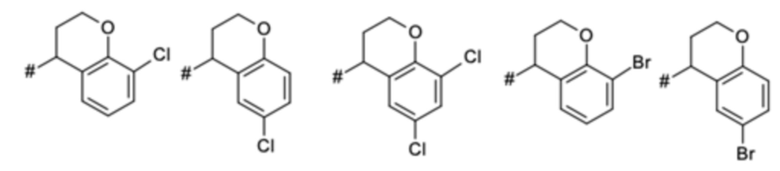
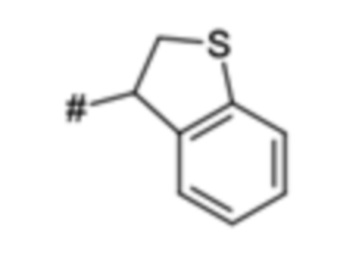
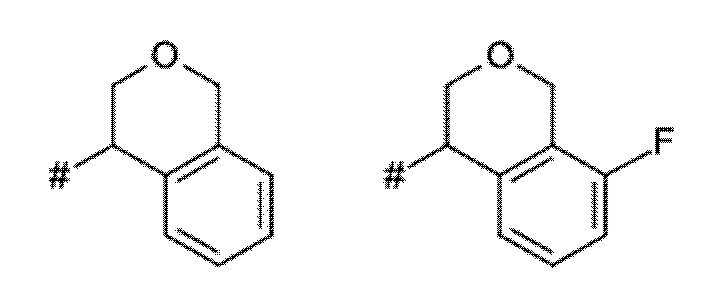 ,
,
R1 представляет собой водород или метил,
R2 выбран из группы, состоящей из:
водорода, хлора, иода, -C(O)-N(CH3)2,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклобутила, этенила, пропенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из галогена, -OH, циано, этокси-C(O)-, -C(O)-NH2, метокси, N(CH3)2, N(CH3)(C(O)CH3); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, оксетана, пирролидина, тетрагидрофурана, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропирана, дигидро-2H-пирана, 1,2-оксазолидина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидроиндола, 1,3-дигидроизоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло[3.1.1]гептана, 8-окса-3-азабицикло[3.2.1]октана, имидазола, пиразола, 1,2,3-триазола, пиридина, дигидропиридина, пиримидина, тетрагидропиримидина, каждый из которых необязательно замещен 1, 2 заместителями, независимо выбранными из группы, состоящей из фтора, -OH, оксо, -COOH, метокси-C(O)-, этокси-C(O)-, трет-бутокси-C(O)-, -C(O)-NH2, метила, метил-C(O)-, дифторметила, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R3 представляет собой водород или метил,
R4 выбран из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, метокси, трифторметила, трифторметокси и NH2,
R5 выбран из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, метокси, трифторметила и трифторметокси,
R6 выбран из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила и метокси,
R12 и R13 независимо друг от друга выбраны из группы, состоящей из:
водорода, -NH(-C(O)-метила), метокси;
метила, этила, пропила, изопропила, бутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, -OH, -COOH, метокси-C(O)-, этокси-C(O)-, трет-бутокси-C(O)-, -C(O)-NH2, -NH-C(O)-метила, метила, метокси, -NH2, NMe2, SO2-метила и (EtO)2P(=O)-;
гетероциклилметила, гетероциклилэтила, где гетероциклильный заместитель выбран из группы, состоящей из оксетана, тетрагидрофурана, тетрагидропирана, пирролидина, морфолина, пиразола, имидазола, пиридина, каждый из которых необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, хлора, -OH, оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического гетероцикла, выбранного из группы оксетана, морфолина, тетрагидропирана, пиридина и пиразола;
R14 выбран из группы, состоящей из:
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -OH, метила, метокси и циклопентила; и
моноциклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбран из группы, состоящей из:
метила и этила, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -OH и -COOH; и
пиридина,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
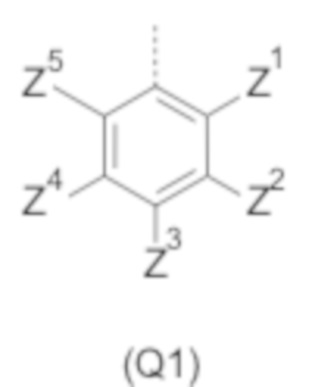 ,
,
в которой:
Z1 и Z5 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, метила, трифторметила и метокси,
Z2 и Z4 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и –NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
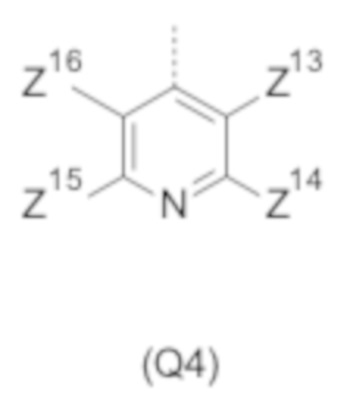 ,
,
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, изопропокси, гидроксиметила, NH2, морфолинила, или
Q представляет собой пиридиновое кольцо формулы (Q5)
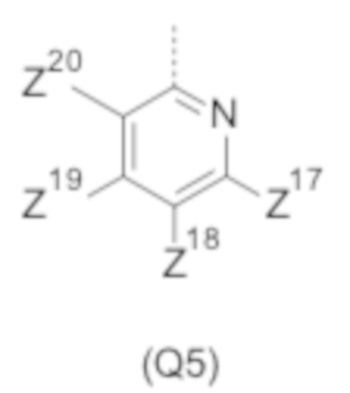 ,
,
в которой:
Z17, Z18, и Z19 представляют собой водород, и
Z20 представляет собой фтор, или
Q выбран из группы, состоящей из:
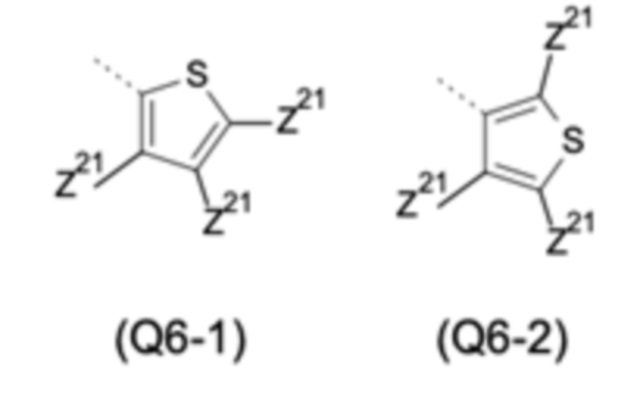
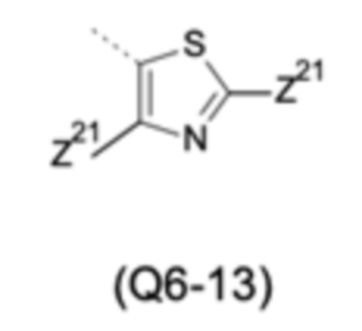 ,
, 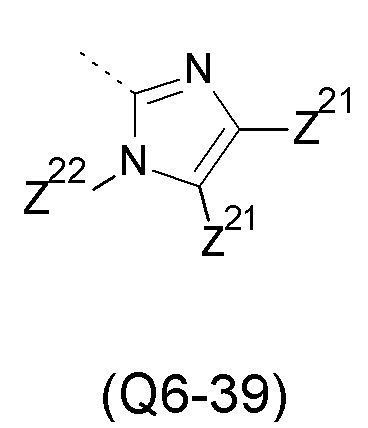
в которой:
каждый Z21 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила и
Z22 представляет собой водород, метил, или
Q выбран из группы, состоящей из:
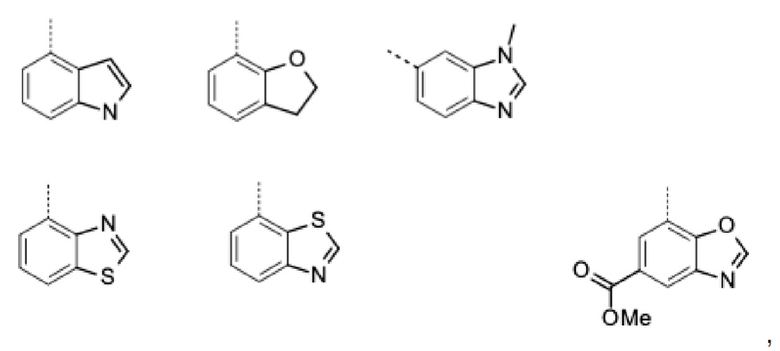
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, где:
A выбран из группы, состоящей из:
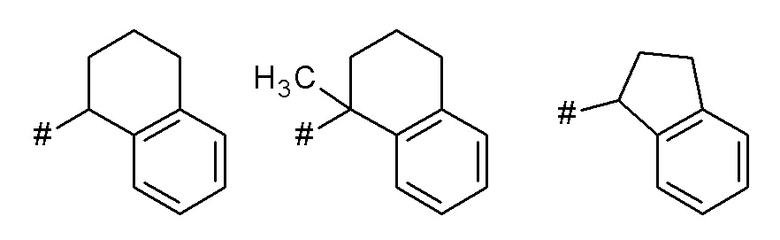 ,
,
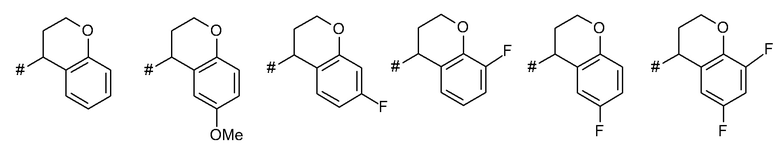
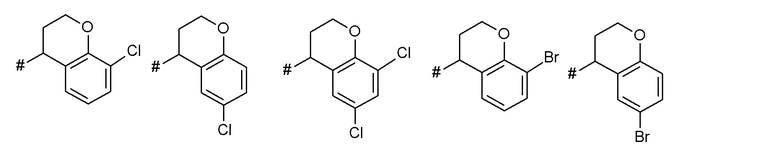
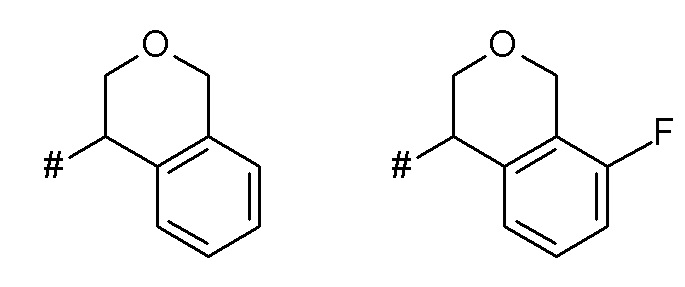 ,
,
R1 представляет собой водород или метил,
R2 выбран из группы, состоящей из:
хлора, иода, -C(O)-N(CH3)2,
-NR12R13;
-OR14;
-SR15, -S(O)R15, -SO2R15;
метила, этила, пропила, изопропила, циклопропила, циклобутила, этенила, пропенила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -OH, циано, этокси-C(O)-, -C(O)-NH2, метокси, N(CH3)2, N(CH3)(C(O)CH3); и
моноциклического или бициклического гетероцикла, выбранного из группы, состоящей из азетидина, оксетана, пирролидина, тетрагидрофурана, пиразолидина, имидазолидина, 1,2,4-триазолидина, пиперидина, пиперазина, тетрагидропирана, дигидро-2H-пирана, 1,2-оксазолидина, морфолина, тиоморфолина, 3,4-дигидроизохинолина, 2,3-дигидроиндола, 1,3-дигидроизоиндола, 3,9-диокса-7-азабицикло[3.3.1]нонана, 6-окса-3-азабицикло[3.1.1]гептана, 8-окса-3-азабицикло[3.2.1]октана, имидазола, пиразола, пиридина, дигидропиридина, пиримидина, тетрагидропиримидина, каждый из которых необязательно замещен 1, 2 заместителями, независимо выбранными из группы, состоящей из фтора, -OH, оксо, -COOH, метокси-C(O)-, этокси-C(O)-, трет-бутокси-C(O)-, -C(O)-NH2, метила, метил-C(O)-, дифторметила, трифторметила, гидроксиметила-, метоксиметила-, -NH2, -NMe2, пирролидина,
R3 представляет собой водород или метил,
R4 выбран из группы, состоящей из водорода, хлора, фтора, метила, метокси и трифторметила,
R5 выбран из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, метокси, трифторметила и трифторметокси,
R6 выбран из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила и метокси,
R12 и R13 независимо друг от друга выбраны из группы, состоящей из:
водорода, -NH(-C(O)-метила), метокси;
метила, этила, пропила, изопропила, бутила, циклопропила, циклобутила, бензила, 1-фенилэтила, каждый из которых необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из фтора, -OH, -COOH, метокси-C(O)-, этокси-C(O)-, трет-бутокси-C(O)-, -C(O)-NH2, -NH-C(O)-метила, метила, метокси, -NH2, -NMe2, SO2-метила и (EtO)2P(=O)-;
гетероциклилметила, гетероциклилэтила, где гетероциклильный заместитель выбран из группы, состоящей из оксетана, тетрагидрофурана, тетрагидропирана, пирролидина, пиразола, имидазола, морфолина, пиридина, каждый из которых необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из оксо и метила;
фенила;
2,3-дигидро-1H-индена, и
моноциклического гетероцикла, выбранного из группы оксетана, морфолина, тетрагидропирана, пиридина и пиразола;
R14 выбран из группы, состоящей из:
метила, этила, изопропила, бутила, циклопентила, бензила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из группы, состоящей из фтора, -OH, метила, метокси и циклопентила; и
моноциклического гетероцикла, выбранного из группы, состоящей из пирролидина и тетрагидропирана,
R15 выбран из группы, состоящей из:
метила и этила, каждый из который необязательно замещен 1 заместителем, независимо выбранным из группы, состоящей из -OH и -COOH; и
пиридина,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
 ,
,
в которой:
Z1 и Z5 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, метила, метокси и трифторметила,
Z2 и Z4 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2, или
Q представляет собой пиридиновое кольцо формулы (Q4)
 ,
,
в которой:
Z14 и Z15 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, изопропокси, гидроксиметила, NH2, морфолинила, и
Z13 и Z16 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, метила, метокси, или
Q представляет собой пиридиновое кольцо формулы (Q5)
 ,
,
в которой:
Z17, Z18 и Z19 представляют собой водород, и
Z20 представляет собой фтор, или
Q выбран из группы, состоящей из:
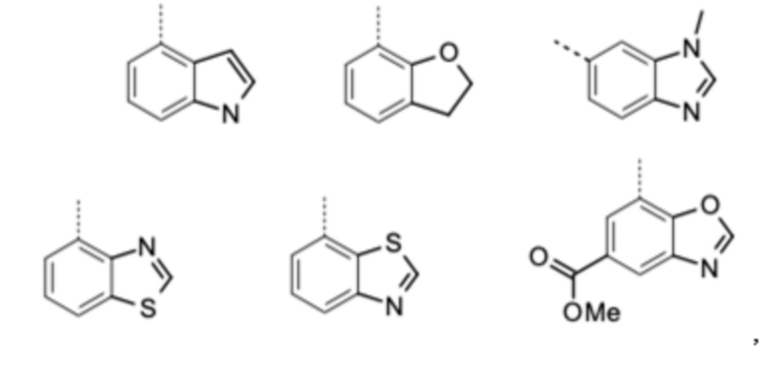
или его фармацевтически приемлемая соль.
3. Соединение общей формулы (II):
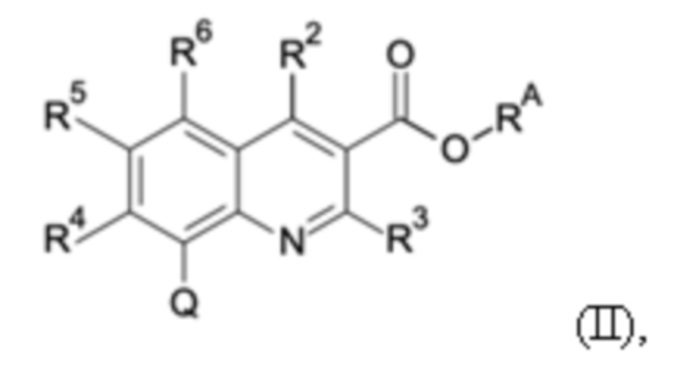
в которой:
R2 представляет собой -OH или как определено для соединения общей формулы (I) по любому из пп. 1, 2,
R3, R4, R5, R6 имеют значения, как определено для соединения общей формулы (I) по любому из пп. 1, 2,
Q представляет собой замещенное фенильное кольцо формулы (Q1)
 ,
,
в которой:
Z1 и Z5 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, метила и трифторметила,
Z2 и Z4 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, -OH, циано, метила, этила, трет-бутила, -NHMe, -NMe2, трифторметила, метокси, трифторметокси, -SMe и морфолинила, и
Z3 независимо выбран из группы, состоящей из водорода, фтора, хлора, метила, метокси, дифторметокси и -NMe2,
где по меньшей мере один из Z1, Z2, Z3, Z4 или Z5 не является водородом,
или
Q представляет собой пиридиновое кольцо формулы (Q4)
 ,
,
в которой:
Z13, Z14, Z15 и Z16 независимо друг от друга выбраны из группы, состоящей из водорода, фтора, хлора, циано, метила, метокси, изопропокси, гидроксиметила, NH2, морфолинила, или
Q выбран из группы, состоящей из:
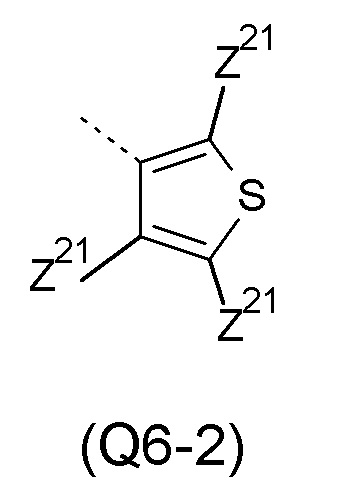 ,
,
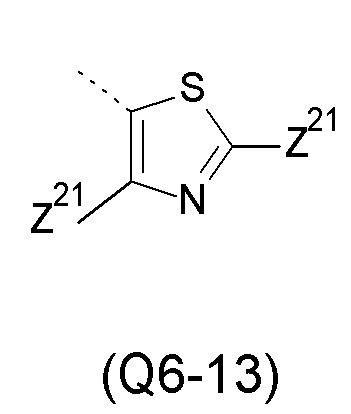 или
или  ,
,
в которой
каждый Z21 независимо выбран из группы, состоящей из водорода, фтора, хлора, циано, метила, трифторметила, и
Q выбран из группы, состоящей из
 ,
,
и
RA представляет собой H или C1-C4-алкил,
или его фармацевтически приемлемая соль.
4. Соединение общей формулы (III)
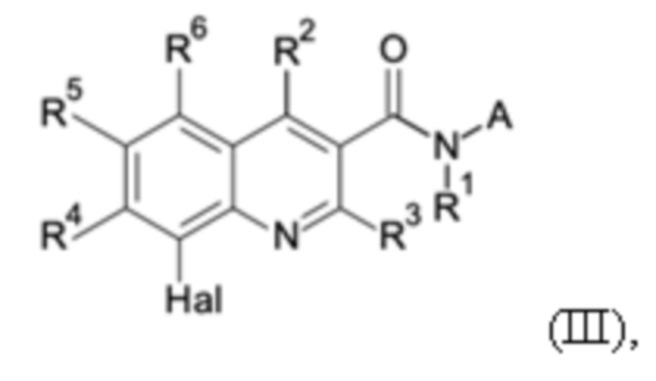
в которой:
R2 представляет собой -OH или как определено для соединения общей формулы (I) по любому из пп. 1, 2,
A, R1, R3, R4, R5 и R6 имеют значения, как определено для соединения общей формулы (I) по любому из пп. 1, 2, и
Hal представляет собой галоген,
или его фармацевтически приемлемая соль.
5. Фармацевтическая композиция для контроля, лечения и/или профилактики гельминтной инфекции, содержащая соединение общей формулы (I) по любому из пп. 1, 2 в эффективном количестве и один или более фармацевтически приемлемых вспомогательных веществ.
6. Применение соединения общей формулы (I) по любому из пп. 1, 2 для контроля, лечения и/или профилактики гельминтной инфекции.
7. Применение соединения общей формулы (I) по любому из пп. 1, 2 для получения лекарственного средства для контроля, лечения и/или профилактики гельминтной инфекции.
8. Способ контроля гельминтных инфекций у людей и/или животных посредством введения антигельминтно эффективного количества по меньшей мере одного соединения общей формулы (I) по любому из пп. 1, 2 человеку или животному, нуждающемуся в этом.
9. Соединение общей формулы (I) по любому из пп. 1, 2, где соединение является соединением формулы (I-a)
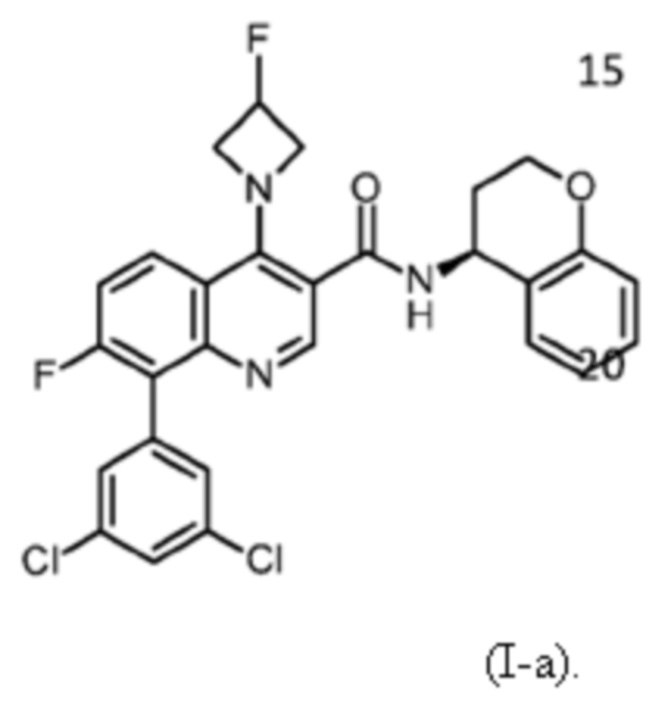
10. Соединение общей формулы (I) по любому из пп. 1, 2, где соединение является соединением формулы (I-b)
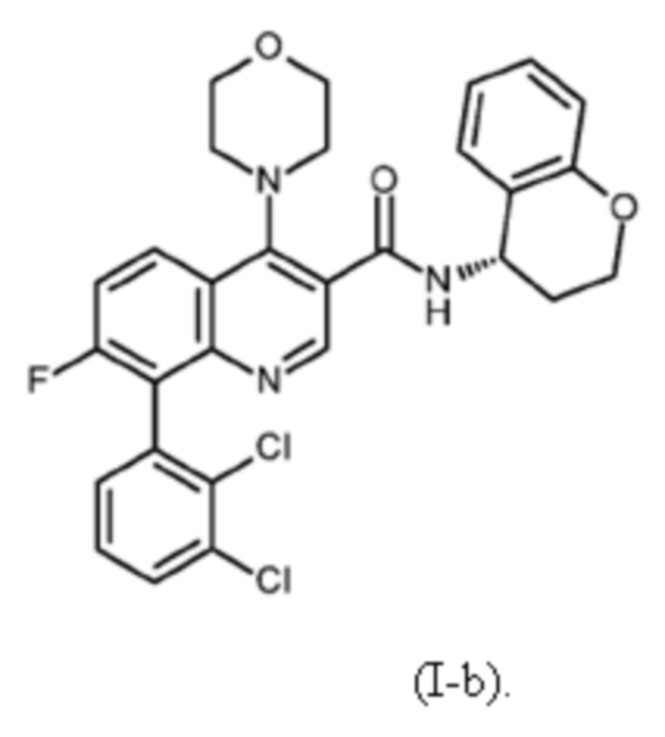
11. Соединение общей формулы (I) по любому из пп. 1, 2, где соединение является соединением формулы (I-c)
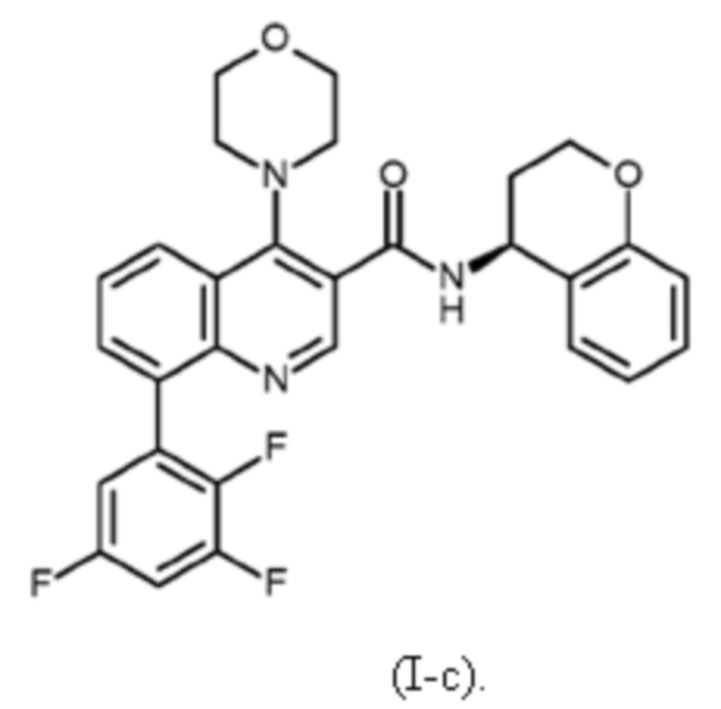
12. Соединение общей формулы (I) по любому из пп. 1, 2, где соединение является соединением формулы (I-d)
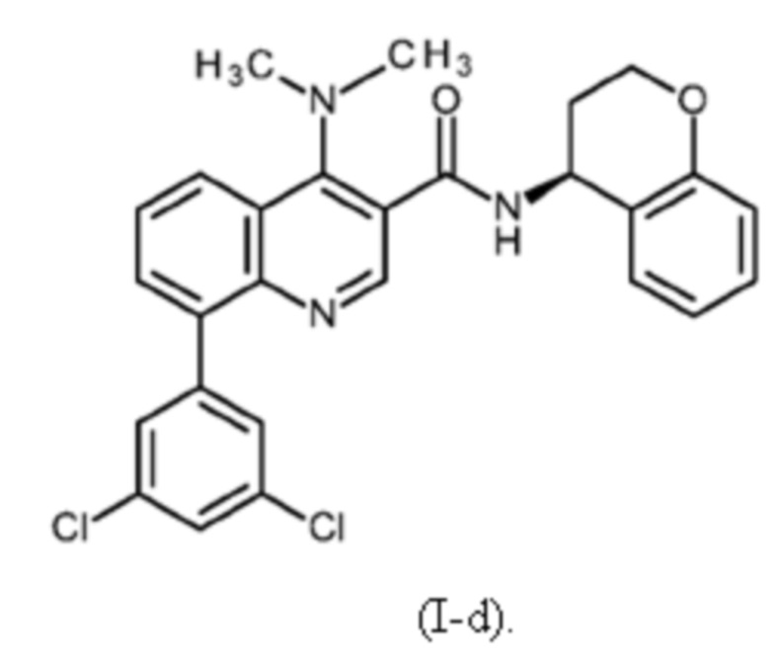
| Wilkinson, J | |||
| H | |||
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Lutz, R | |||
| E | |||
| и др | |||
| "Antimalarials | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| E.Schröder и др | |||
| "Nichtsteroidale | |||
Авторы
Даты
2022-05-18—Публикация
2017-11-06—Подача