ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США 62/858465, поданной 7 июня 2019 года, и предварительной заявке на патент США 62/947852, поданной 13 декабря 2019 года, полное содержание каждой из которых включено в настоящее описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области медицинской химии, фармакологии, ветеринарии и медицины. Конкретнее, настоящее изобретение относится к соединениям формулы (I) и их применению для подавления эндопаразитов, например, сердечных червей, у теплокровных животных.
УРОВЕНЬ ТЕХНИКИ
Сердечный червь (Dirofilaria immitis) - это паразитический круглый червь, который распространяется от хозяина к хозяину через укусы комаров. Жизненный цикл начинается, когда самка комара питается кровью зараженного хозяина. Комар поглощает незрелых сердечных червей, которые затем линяют до стадии инвазионных личинок и мигрируют в ротовые части комаров. Затем комар кормится на восприимчивом хозяине, таком как собака или кошка, оставляя инвазионные личинки. Затем личинки линяют, переходя на следующую личиночную стадию, в организме нового хозяина, а затем мигрируют по телу, в конечном итоге оказываясь в кровеносных сосудах. По мере того, как личинки мигрируют через ткани, они линяют, превращаясь в неполовозрелых взрослых особей. Неполовозрелые взрослые особи в конечном итоге мигрируют в кровеносные сосуды легких, где они созревают и превращаются в половозрелых взрослых особей. Взрослые сердечные черви затем размножаются и производят незрелых сердечных червей, завершая цикл. Инфицирование сердечным червем может привести к серьезному заболеванию хозяина.
Инфицрование взрослыми сердечными червями можно лечить соединениями на основе мышьяка; лечение занимает много времени, является затруднительным и часто только частично успешным. Соответственно, лечение сосредоточено на борьбе с инфицированием сердечным червем. В настоящее время подавление сердечного червя осуществляют исключительно путем круглогодичного периодического введения лекарственных препаратов. Типичные способы лечения включают макроциклические лактоны, такие как ивермектин, моксидектин и оксим милбемицина. К сожалению, наблюдается развитие резистентности Diroftlaria immitis к макроциклическим лактонам. Соответственно, существует потребность в новых соединениях, которые эффективно подавляют инфицирование сердечным червем либо путем профилактики, либо путем непосредственного уничтожения сердечных червей. Некоторые способы лечения эндопаразитов описаны в WO 2017/178416, WO 2018/087036, WO 2018/197401, WO 2019/025341 и WO 2019/002132.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложены соединения формулы (I), которые эффективно лечат и/или подавляют эндопаразитов (например, сердечного червя) у теплокровных животных.
В одном из вариантов реализации настоящего изобретения предложены соединения формулы (I):

где
n равен 0 или 1;
X1 выбран из группы, состоящей из N и CR1;
Х2 выбран из группы, состоящей из N и CR2;
Х3 выбран из группы, состоящей из N и CR3;
Х4 выбран из группы, состоящей из N и CR4;
Х5 выбран из группы, состоящей из N и CR5;
Х6 выбран из группы, состоящей из N и CR6;
G выбран из группы, состоящей из

М выбран из группы, состоящей из N-R13, О и S;
Y1 выбран из группы, состоящей из CR8R9, О, S и NR10;
Y2 выбран из группы, состоящей из CR8R9, О, S и NR10;
при этом по меньшей мере одна из групп Y1 или Y2 представляет собой CR8R9;
Z1 выбран из группы, состоящей из N, О, S и CR11;
Z2 выбран из группы, состоящей из отсутствия фрагмента, N и CR11;
Z3 выбран из группы, состоящей из отсутствия фрагмента, N и CR11;
Z4 выбран из группы, состоящей из N, О, S и CR11;
при этом не более 2 из Z1, Z2, Z3 и Z4 представляют собой N, и при этом только один из Z1 и Z4 представляет собой О или S, Z2 представляет собой отсутствие фрагмента только тогда, когда Z1 представляет собой О или S, и Z3 представляет собой отсутствие фрагмента только тогда, когда Z4 представляет собой О или S;
R1 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, -SC1-С4 алкила, -S(O)(C1-C4 алкила), -S(O)2(C1-C4 алкила), циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
R2 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, -SC1-С4 алкила, -S(O)(C1-C4 алкила), -S(O)2(C1-C4 алкила), циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
R3 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, -SC1-С4 алкила, -S(O)(C1-C4 алкила), -S(O)2(C1-C4 алкила), циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
R4 выбран из группы, состоящей из галогена, циано, -СНО, гидроксила, С1-С4 алкила, С2-С4 алкенила, С2-С4 алкинила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4-алкоксизамещенного-С1-С4 алкила, бензила, необязательно замещенного 1-5 атомами галогена, С1-С4 алкокси, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(C3-C6 циклоалкила), -N(C1-C4 алкила)(С3-С6-циклоалкила), -N(C1-C4 алкила)(4-7-членного гетероциклоалкила), -NH(4-7-членного гетероциклоалкила), -N(C1-C4 алкил)(С1-С4 алкокси), -C(O)NH(C1-C4 алкила), -C(O)N(C1-C4 алкила)2, -C(O)N(C1-C4 алкил)(4-7-членного гетероциклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; 6- или 10-членный арил; моноциклический гетероцикл, выбранный из группы, состоящей из 4-7-членного гетероциклоалкила, 5-членного гетероарила, содержащего по меньшей мере один атом азота, через который 5-членное гетероарильное кольцо соединено с остальной частью молекулы, и 6-членный гетероарил, содержащий по меньшей мере один атом азота; каждое из арильного, гетероциклоалкильного и гетероарильного колец в R4 необязательно замещено 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеналкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(С3-С6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкил, -S(O)C1-C4 алкил, -SO2C1-C4 алкил, -S(O)С1-С4-галогеноалкил и -SO2 С1-С4 галогеноалкил; где С3-С6 циклоалкил и гетероциклоалкильные кольца в R4 необязательно замещены спирогруппой, где указанная спирогруппа представляет собой 3-6-членный циклоалкил или 4-6-членный гетероциклоалкил, содержащий 1, 2 или 3 гетероатома, независимо выбранных из N, S или О, где указанная спирогруппа необязательно замещена 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(С3-С6 циклоалкила), -N(C1-C4 алкила)(С3-С6-циклоалкила), -NHSO2(C1-C4 алкила), -SC1-С4 алкила, -S(O)С1-С4 алкила, -SO2C1-C4 алкила, -S(O)С1-С4-галогеноалкила и -SO2C1-C4 галогеноалкила; и где каждый С1-С4 алкил, С3-С6 циклоалкил и С1-С4 алкокси в R4 может быть необязательно замещен 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, гидрокси, -NH2, -NH(С1-С4 алкил), -N(C1-C4 алкил)2, циано, карбокси, карбамоила, С1-С4 алкоксикарбонила, -C(O)NH(C1-C4 алкил), -C(O)N(С1-С4 алкил)2 и С1-С4 алкокси;
R5 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, -SC1-С4 алкила, -S(O)(С1-С4 алкила), -S(O)2(C1-C4 алкила), циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
R6 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, -SC1-С4 алкила, -S(O)(C1-C4 алкила), -S(O)2(C1-C4 алкила), циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 группами С1-С4 алкил; -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
R7 выбран из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила, необязательно замещенного 1-5 атомами галогена, группами -С(Н)O, С2-С4 алкенил, С2-С4 алкинил, С1-С4 галогеноалкил и С1-С4-алкокси;
R8 каждый раз независимо выбран из группы, состоящей из водорода, фтора и С1-С4 алкила;
R9 каждый раз независимо выбран из группы, состоящей из водорода, фтора и С1-С4 алкила;
R10 выбран из группы, состоящей из водорода и С1-С4 алкила;
R11 каждый раз независимо выбран из группы, состоящей из водорода, галогена, гидроксила, циано, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4-алкокси, С3-С6 циклоалкила, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2; и
Q выбран из группы, состоящей из
(i) 6- или 10-членного арила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4 алкокси, С3-С6 циклоалкила, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(С3-С6 циклоалкила), -N(C1-C4 алкила)(С3-С6 циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)С1-С4-галогеноалкила и -SO2C1-C4 галогеноалкила, где 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы О, S и N, и где атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, если позволяет валентность, замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила;
(ii) 5-10-членного гетероарила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из группы О, S и N, и при этом атомы углерода 5-10-членного гетероарила необязательно замещены 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, бензилокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -SC1-C4 алкила, -S(O)С1-С4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеналкила и -SO2C1-C4 галогеноалкила, и любой N в гетероариле, если это допускает валентность, необязательно замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила, С3-С6 циклоалкила;
(iii) 4-7-членного гетероциклоалкила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из группы О, S, N, при этом гетероциклоалкил необязательно является бензоконденсированным, при этом атомы углерода 4-7-членного гетероциклоалкила или необязательно бензоконденсированного 4-7-членного гетероциклоалкила необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(С1-С4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле необязательно замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила;
(iv) 6- или 10-членного арилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(С3-С6 циклоалкил), -N(C1-C4 алкил)(С3-С6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-С4-галогеноалкила и -SO2C1-C4 галогеноалкила;
(v) 6- или 10-членного арилтиоокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(C3-C6 циклоалкила), -N(C1-C4 алкила)(С3-С6-циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеноалкила и -SO2C1-C4 гало геналкила; и
(vi) 5-10-членного гетероарилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеналкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(С3-С6 циклоалкила), -N(C1-C4 алкила)(С3-С6-циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеналкила и -SO2C1-C4 галогеналкила;
R13 выбран из группы, состоящей из гидрокси, С1-С4 алкокси и -NH2; и
R14 каждый раз независимо выбран из группы, состоящей из водорода, галогена, циано, нитро, гидроксила, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеналкила, С1-С4 алкокси, С1-С4 галогеналкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2;
или соль указанного соединения.
В одном из вариантов реализации настоящего изобретения также предложены композиции, содержащие: соединение формулы (I) или его соль и приемлемое вспомогательное вещество, причем композиция необязательно дополнительно содержит по меньшей мере одно дополнительное активное соединение.
В одном из вариантов реализации настоящего изобретения также предложен способ лечения паразитов, включающий: введение нуждающемуся в этом субъекту эффективного количества соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
В одном из вариантов реализации настоящего изобретения также предложен способ подавления паразитов, включающий: введение нуждающемуся в этом субъекту эффективного количества соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
В одном из вариантов реализации настоящего изобретения также предложен способ лечения или подавления паразитов, включающий: приведение в контакт среды субъекта с эффективным количеством соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
Таким образом, изобретение обеспечивает применение соединений согласно настоящему изобретению в качестве лекарственного средства, в том числе для получения лекарственного средства. В одном из вариантов реализации настоящего изобретения предложено получение лекарственного средства, содержащего соединение формулы (I) или его соль, для лечения паразитов. В одном из вариантов реализации настоящего изобретения предложено получение лекарственного средства, содержащего соединение формулы (I) или его соль, для подавления паразитов.
В настоящем изобретении также предложены способы получения соединений согласно настоящему изобретению и их промежуточных соединений.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Термин «С1-С4 алкил» относится к линейной или разветвленной алкильной цепи, содержащей от одного до четырех атомов углерода, и включает метил, этил, пропил, изопропил, бутил и тому подобное.
Термин «галогеноалкил С1-С4» относится к прямой или разветвленной алкильной цепи, содержащей от одного до четырех атомов углерода и от 1 до 5 атомов галогена, и включает фторметил, дифторметил, трифторметил, 2,2,2-трифторэтил, 1,2,2-трифторэтил, 3,3,3-трифторпропил и тому подобное.
Термин «алкенил С2-С4» относится к прямой или разветвленной алкенильной цепи, содержащей от двух до четырех атомов углерода и одну двойную углерод-углеродную связь, и включает этилен, пропилен, изо-пропилен, бутилен, изо-бутилен, втор-бутилен и тому подобное.
Термин «С2-С4 алкинил» относится к прямой или разветвленной алкинильной цепи, содержащей от двух до четырех атомов углерода и одну тройную углерод-углеродную связь, и включает ацетилен, пропаргил и тому подобное.
Термин «С1-С4 алкокси» относится к С1-С4 алкилу, присоединенному через атом кислорода, и включает метокси, этокси, пропокси, изопропокси, бутокси и тому подобное.
Термин «С3-С6 циклоалкил» относится к алкильному кольцу из трех-шести атомов углерода и включает циклопропил, циклобутил, циклопентил и циклогексил.
Термины «галоген» и «галогено» относятся к атому хлора, фтора, брома или йода.
Термин «С6- или С10-членный арил» относится к фенилу или нафтилу.
Термин «С6- или С10-членный арилокси» относится к фенилу или нафтилу, присоединенному через атом кислорода, и включает фенокси и нафтилокси.
Термин «С6- или С10-членный арилтио-окси» относится к фенилу или нафтилу, присоединенному через атом серы, и включает фентио-окси и нафтилтио-окси. Кроме того, следует понимать, что термин «С6- или С10- членный арилтио-окси» также охватывает случай, в котором сера представляет собой -SO2- и -S(O)-.
Термин «4-7-членный гетероциклоалкил» относится к 4-7-членному моноциклическому насыщенному или частично (но не полностью) ненасыщенному кольцу, содержащему один или более гетероатомов, предпочтительно один, два или три гетероатома, выбранных из группы, состоящей из азота, кислорода и серы, и кольцо необязательно содержит карбонил с образованием лактама или лактона. Следует понимать, что если включена сера, то сера может представлять собой -S-, -SO- или -SO2-. Например, но не ограничиваясь этим, термин включает азетидинил, пирролидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, оксетанил, диоксоланил, тетрагидропиранил, тетрагидротиопиранил, тетрагидрофурил, гексагидропиримидинил, тетрагидропиримидинил, дигидроимидазолил и тому подобное.
Термин «5-членный гетероарил» относится к пятичленному, моноциклическому, полностью ненасыщенному кольцу, содержащему от одного до четырех атомов углерода и от одного до четырех гетероатомов, выбранных из группы, состоящей из азота, кислорода и серы. Например, без ограничения, термин включает фурил, тиенил, пирролил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, тиазолил, тиадиазолил, триазолил, тетразолил и тому подобное. Следует понимать, что 5-членный гетероарил может быть присоединен в качестве заместителя через кольцевой атом углерода или кольцевой атом азота, где такой режим присоединения доступен, например, для пирролила, имидазолила, пиразолила, триазолила и тому подобного.
Термин «6-членный гетероарил» относится к шестичленному моноциклическому полностью ненасыщенному кольцу, содержащему от одного до пяти атомов углерода и с одним или более, обычно от одного до четырех, гетероатомами, выбранными из группы, состоящей из азота, кислорода и серы. Например, без ограничения, указанный термин включает пиразинил, пиразолил, пиридазинил, пиридил, пиримидил и тому подобное. Следует понимать, что 6-членный гетероарил может быть присоединен в качестве заместителя через кольцевой атом углерода или кольцевой атом азота, если такой режим присоединения доступен.
Термин «5-10-членный гетероарил» относится к 5-10-членному, моноциклическому или полициклическому полностью ненасыщеннму кольцу или кольцевой системе, содержащей от одного до девяти атомов углерода и один или более гетероатомов, предпочтительно один, два или три гетероатома, выбранных из группы, состоящей из азота, кислорода и серы. Например, без ограничения, этот термин включает фурил, тиенил, пирролил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, тиазолил, пиразинил, пиразолил, пиридазинил, пиримидил, азепинил, диазепинил, бензофурил, бензотиенил, индолил, изоиндолил, бензимидазолил, бензизотиазолил, бензизоксазолил, бензоксазолил, бензопиразинил, бензопиразолил, хиназолил, тиенопиридил, хинолил, изохинолил, бензотиазолил и тому подобное. Следует понимать, что 5-10-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы О, S и N, может быть присоединен в качестве заместителя через кольцевой атом углерода или кольцевой атом азота, если такой режим присоединения доступен.
Термин «5-10-членный гетероарилокси» относится к 5-10-членному гетероарилу, содержащему один или более гетероатомов, предпочтительно 1, 2 или 3 гетероатома, выбранных из группы О, S и N, присоединенных через атом кислорода и включающих имидазолилокси, пиразолилокси, пиридилокси, пиримидилокси, хинолилокси и тому подобное.
Термин «оксо» относится к атому кислорода, связанному с углеродом, к которому он присоединен, посредством двойной связи, с образованием карбонила кетона или альдегида. Например, пиридоновый радикал рассматривается как оксозамещенный 6-членный гетероарил.
Термин «карбоксил» относится к группе ниже:

Термин «карбамоил» относится к группе ниже:

Термин «С1-С4 алкоксикарбонил» относится к группе ниже:

где R представляет собой С1-С4 алкил.
Термин «отсутствие фрагмента» в контексте настоящего описания в отношении группы, заместителя, фрагмента или тому подобного указывает на то, что эта группа, заместитель или фрагмент отсутствует. При этом группа, заместитель или фрагмент обычно связаны с двумя или более другими группами, заместителями или фрагментами, которые связаны вместе вместо группы, заместителя или фрагмента, который отсутствует. Например, в соединении, имеющем структуру А-В-С; если В представляет собой отсутствие фрагмента, то А непосредственно связан с С, и соединение представляет собой А-С. В качестве другого примера, в соединении, имеющем структуру А-В-С; если С представляет собой отсутствие фрагмента, то соединение представляет собой А-В.
Термин «соль» относится к солям ветеринарно или фармацевтически приемлемых органических кислот и оснований или неорганических кислот и оснований. Такие соли хорошо известны в данной области техники и включают соли, описанные в Journal of Pharmaceutical Science, 66,2-19 (1977). Примером является гидрохлоридная соль.
Термин «замещенный», в том числе при использовании в «необязательно замещенный», относится к одному или более водородным радикалам группы, замещенным неводородными радикалами (заместителем (заместителями)). Следует понимать, что заместители могут быть одинаковыми или различными в каждом замещенном положении. Комбинации групп и заместителей, предусмотренных в настоящем изобретении, представляют собой комбинации, которые являются стабильными или химически осуществимыми. Для соединений, описанных в настоящем документе, их группы и заместители могут быть выбраны в соответствии с разрешенной валентностью атомов и заместителей, так что выборы и замещения приводят к стабильному соединению, например, которое не подвергается спонтанному превращению, например, путем перегруппировки, циклизации, элиминации и т.д.
Понятно, что когда циклоалкильное или гетероциклоалкильное кольцо замещено спирогруппой, спирогруппа может быть присоединена, если позволяет валентность, к любому положению циклоалкила или гетероциклоалкила, образуя дополнительное кольцо, так что спирогруппа присоединена к циклоалкильному или гетероциклоалкильному кольцу через общий атом. Примеры таких спирозамещенных колец включают 2-окса-6-азаспиро[3.3]гептан, 2-азаспиро[3.3]гептан, 2-азаспиро[3.4]октан, 6-окса-2-азаспиро[3.4]октан и тому подобное.
Термин «стабильный» относится к соединениям, которые по существу не изменяются под воздействием условий для обеспечения их получения. В неограничивающем примере стабильное соединение или химически осуществимое соединение представляет собой соединение, которое по существу не изменяется при хранении при температуре 40°С или менее в отсутствие влаги или других химически активных условий в течение примерно недели.
Следует понимать, что в тех случаях, когда термины, определенные в настоящем документе, упоминают число атомов углерода, указанное число относится к указанной группе и не включает никаких атомов углерода, которые могут присутствовать в любом необязательном заместителе (заместителях) на них, или любых атомов углерода, которые могут присутствовать в виде части конденсированного кольца, включая бензоконденсированное кольцо.
Специалисту в данной области техники будет известно, что некоторые соединения согласно настоящему изобретению существуют в виде изомеров. Предполагается, что все стереоизомеры соединений согласно настоящему изобретению, включая геометрические изомеры, энантиомеры и диастереомеры, в любом соотношении, входят в объем настоящего изобретения.
Специалисту в данной области техники также будет известно, что некоторые соединения согласно настоящему изобретению существуют в виде таутомеров. Предполагается, что все таутомерные формы соединений согласно настоящему изобретению входят в объем настоящего изобретения.
Соединения согласно настоящему изобретению также включают все изотопные вариации, в которых по меньшей мере один атом преобладающей атомной массы заменен атомом, имеющим одинаковый атомный номер, но имеющим атомную массу, отличную от преобладающей атомной массы. Применение изотопных вариаций (например, дейтерия, 2Н) может обеспечить более высокую метаболическую стабильность. Кроме того, некоторые изотопные вариации соединений согласно настоящему изобретению могут включать радиоактивный изотоп (например, тритий, 3Н или 14С), который может быть полезен в исследованиях распределения лекарственного средства и/или субстрата в ткани. Замена изотопами, излучающими позитроны, такими как 11С, 18F, 15O и 13N, может применяться в исследованиях позитронной эмиссионной топографии (ПЭТ).
Термины «соединения согласно изобретению» и «соединение согласно изобретению» и «соединения согласно настоящему изобретению» и т.п. включают вариант реализации формулы (I) и другие более конкретные варианты реализации, охватываемые формулой (I), описанной в настоящем документе, и приведенные в качестве примера соединения, описанные в настоящем документе, и соль каждого из этих вариантов реализации.
Соединение формулы (I) с G, как определено, имеет формулы:



Дополнительные варианты реализации соединений согласно настоящему изобретению представлены ниже:
(a) Один из вариантов реализации относится к соединению формулы (Ia).
(b) Один из вариантов реализации относится к соединению формулы (Ib).
(1) Один из вариантов реализации относится к соединению формулы (Ic).
(2) Один из вариантов реализации относится к соединению формулы (I), вариантам реализации (а), варианту реализации (b) и (1), где по меньшей мере один из X1, Х2, Х3 и Х5 представляет собой N.
(c) Один из вариантов реализации относится к соединениям формулы (I), формулы (Ia), формулы (Ib) или формулы (Ic), где X1 представляет собой CR1; Х2 представляет собой CR2; Х3 представляет собой CR3; Х4 представляет собой CR4; Х5 представляет собой CR5; и Х6 представляет собой N; или соли указанных соединений.
(d) Один из вариантов реализации относится к соединениям формулы (I), формулы (Ia), формулы (Ib) или формулы (Ic), где X1 представляет собой CR1; Х2 представляет собой CR2; Х3 представляет собой CR3; Х4 представляет собой CR4; Х5 представляет собой N; и Х6 представляет собой N; или соли указанных соединений.
(e) Один из вариантов реализации относится к соединениям формулы (I), формулы (Ia) или формулы (Ib)), где X1 представляет собой CR1; Х2 представляет собой CR2; Х3 представляет собой CR3; Х4 представляет собой CR4; Х5 представляет собой N; и Х6 представляет собой CR6; или соли указанных соединений.
(f) Один из вариантов реализации относится к соединениям формулы (I), формулы (Ia), формулы (Ib) или формулы (Ic), где X1 представляет собой CR1; Х2 представляет собой CR2; Х3 представляет собой CR3; Х4 представляет собой N; Х5 представляет собой N; и Х6 представляет собой N; или соли указанных соединений.
(g) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), где Q представляет собой 6- или 10-членный арил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4 алкокси, С3-С6 циклоалкила, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(С3-С6 циклоалкила), -N(C1-C4 алкила)(С3-С6-циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила,
-S(O)С1-С4-галогеноалкила и -SO2C1-C4 галогеноалкила; или соли указанных соединений.
(h) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), где Q представляет собой 6-членный арил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4 алкокси, С3-С6 циклоалкила, -NH2,
-NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(С3-С6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)С1-С4-галогеноалкила и -SO2C1-C4 галогеноалкила, при этом 6-членный арил конденсирован с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы О, S и N, и при этом атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-С4 алкил) и -N(C1-С4 алкил)2, и любой N в гетероциклоалкиле замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила; или соли указанного соединения.
(i) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), где Q представляет собой 5-10-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из группы О, S и N, и где атомы углерода гетероарила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -ОН, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-С4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероариле необязательно замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила; или соли указанного соединения.
(j) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), где Q представляет собой 4-7-членный гетероциклоалкил, содержащий 1 или 2 гетероатома, выбранных из группы О, S, N, при этом гетероциклоалкил необязательно является бензо-конденсированным, при этом атомы углерода гетероциклоалкила или необязательно бензоконденсированного гетероциклоалкила необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, C1-С4 алкокси, -NH2, -NH(C1-C4 алкил) и
-N(С1-С4 алкил)2, и любой N в гетероциклоалкиле необязательно замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила; или соли указанного соединения.
(k) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), где Q представляет собой 6- или 10-членный арилокси, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(С3-С6 циклоалкил), -NSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеналкила и -SO2C1-C4 галогеналкила; или соли указанного соединения.
(l) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (1), (2), (а), (b), (с), (d), (е) и (f), где Q представляет собой и 5-10-членный гетероарилокси, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, С1-С4 алкокси, -NH2, -NH(C1-С4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(С3-С6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)С1-С4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеноалкила и -SO2C1-C4 галогеноалкила; или соли указанных соединений.
(m) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) (f), (g), (h), (i), (j), (k) и (l), где n равен 1; или соли указанных соединений.
(n) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) и (f), (g), (h), (i), (j), (k), (l) и (m), где Y1 представляет собой CR8R9, и Y2 представляет собой О; или соли указанных соединений;
(о) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е) (f), (g), (h), (i), (j), (k), (l), (m) и (n), где R4 выбран из группы, состоящей из С1-С4 алкила, С3-С6 циклоалкила, -N(C1-C4 алкил)2 и 4-7-членного гетероциклоалкила; или соли указанных соединений.
(р) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е), (f), (1), (2), (g), (h), (i), (j), (k), (l), (m) и (n), где R4 представляет собой -N(C1-C4 алкил)2; или соли указанных соединений.
(q) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е), (f), (g), (h), (i), (j), (k), (l), (m), (n), (о) и (p), где M представляет собой О; или соли указанных соединений.
(r) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е), (f), (g), (h), (i), (j), (k), (l), (m), (n), (о) и (p), где M представляет собой NR13; или соли указанных соединений.
(s) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е), (f), (g), (h), (i), (j), (k), (l), (m), (n), (о) и (p), где M представляет собой S; или соли указанных соединений.
(t) Один из вариантов реализации относится к соединению формулы (I) и вариантам реализации (a), (b), (1), (2), (с), (d), (е), (f), (g), (h), (i), (j), (k), (l), (m), (n), (o), (p), (q), (r) и (s), где Z1 представляет собой CR11, Z2 представляет собой CR11, Z3 представляет собой отсутствие группы, и Z4 представляет собой S; или соли указанных соединений.
(u) Другой вариант реализации относится к соли каждого из приведенных в качестве примера соединений.
В другом варианте реализации предложены соединения формул:



или соль любого из вышеуказанных соединений;
где X1, Х2, Х3, Х4, Х5, Х6, R1, R4, R5, R7 и Q являются такими, как определено в кратком описании.
В другом варианте реализации формулы (Ia-1) - (Ia-8а) [то есть, формулы (Ia-1), (Ia-2), (Ia-3), (Ia-4), (Ia-5), (Ia-6), (Ia-7), (Ia-8), (Ia-1a), (Ia-2a), (Ia-3a), (Ia-4a), (Ia-5a), (Ia-6а), (Ia-7а) и (Ia-8a)], R1, при его наличии [то есть, когда конкретно изображен в формуле], выбран из водорода, галогена и циано. В другом варианте реализации формулы (Ia-1) - (Ia-8a) R1, при его наличии, выбран из водорода, фтора и циано. В другом варианте реализации формулы (Ia-1) - (Ia-8a), R1, при его наличии, представляет собой водород или фтор. В другом варианте реализации формулы (Ia-1) - (Ia-8a) R1, при его наличии, представляет собой водород. В другом варианте реализации формулы (Ia-1) - (Ia-8a) R1, при его наличии, представляет собой фтор.
В другом варианте реализации формулы (Ia-1) - (Ia-8a) R4, при его наличии, выбран из:

В другом варианте реализации формулы (Ia-1) - (Ia-8a) R4, при его наличии, выбран из:

В другом варианте реализации формулы (Ia-1) - (Ia-8a) R4, при его наличии, выбран из:

В другом варианте реализации формулы (Ia-1) - (Ia-8a) R5, при его наличии, представляет собой водород, галоген, С1-С4 алкил или С1-С4 галогеноалкил. В другом варианте реализации формулы (Ia-1) - (Ia-8a) R5, при его наличии, представляет собой водород, С1-С4 алкил или С1-С4 галогеноалкил. В другом варианте реализации формулы (Ia-1) - (Ia-8a), R5, при его наличии, представляет собой водород, метил или трифторметил.
В другом варианте реализации формулы (Ia-1) - (Ia-8a) R7, при его наличии, представляет собой водород.
В другом варианте реализации формулы (Ia-1) - (Ia-8a) Q выбран из 6-членного арила и 5- или 6-членного гетероарила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из N, О и S, при этом арил и гетероарил необязательно замещены 1, 2, 3, 4 или 5 заместителями, независимо выбранными из галогена, С1-С4 галогеналкила и С1-С4 алкокси. В другом варианте реализации формулы (Ia-1) - (Ia-8a) Q выбран из 6-членного арила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из галогена.
В другом варианте реализации формулы (Ia-1) - (Ia-8a) Q выбран из:


В другом варианте реализации формулы (Ia-1) - (Ia-8a) Q выбран из:
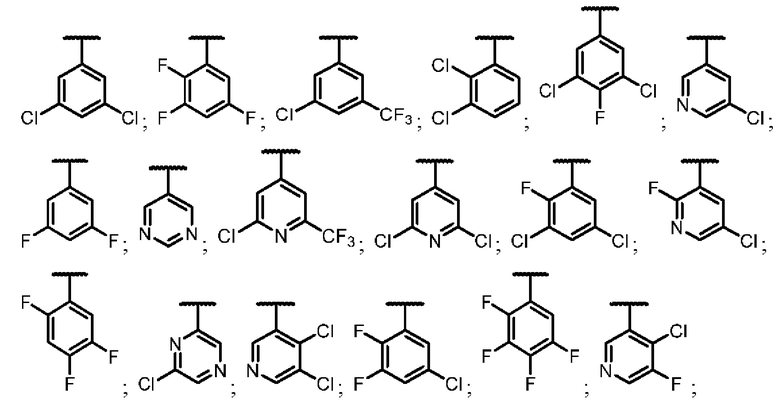

В другом варианте реализации формулы (Ia-1) - (Ia-8а),
X1, Х2, Х3, Х4, Х5, Х6, при их наличии, являются такими, как определено i кратком описании;
R1, при его наличии, выбран из водорода, галогена и циано;
R4, при его наличии, выбран из:

R5, при его наличии, выбран из водорода, метила и трифторметила;
R7, при его наличии, представляет собой водород; и
Q выбран из:


или соль указанного соединения.
В другом варианте реализации формулы (Ia-1) - (Ia-8а),
X1, Х2, Х3, Х4, Х5, Х6, при их наличии, являются такими, как определено в кратком описании;
R1, при его наличии, выбран из водорода, галогена и циано;
R4, при его наличии, выбран из:

R5, при его наличии, выбран из водорода;
R7, при его наличии, представляет собой водород; и
Q выбран из:

или соль указанного соединения.
В другом варианте реализации соединение формулы (I) или его соль имеет формулу (Ia-5),

где R1, R4 и Q являются такими, как определено в кратком описании. Предпочтительно R1 представляет собой водород, галоген или циано. Более предпочтительно, R1 представляет собой водород или фтор. Предпочтительно, R4 представляет собой 4-морфолино или диметиламино. Предпочтительно, Q представляет собой 6-членный арил, необязательно замещенный 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, С1-С4 алкила, С1-С4 галогеноалкила, С1-С4 алкокси, С3-С6 циклоалкила, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(С3-С6 циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)С1-С4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеноалкила и -SO2C1-C4 галогеноалкила, при этом 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы О, S и N, и при этом атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, С1-С4 алкила, С3-С6 циклоалкила, С1-С4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(С1-С4 алкил), и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, если позволяет валентность, замещен заместителем, выбранным из группы, состоящей из водорода, С1-С4 алкила и С3-С6 циклоалкила. Предпочтительно, Q представляет собой 6-членный арил, замещенный 1, 2, 3, 4 или 5 заместителями, независимо выбранными из галогена, С1-С4 алкила, С1-С4 галогеноалкила и циано. Предпочтительно, Q выбран из:

Соединения согласно настоящему изобретению могут быть получены различными способами, некоторые из которых описаны ниже. Все заместители, если не указано иное, являются такими, как определено ранее.
Продукты на каждой стадии могут быть выделены обычными способами, включая экстракцию, выпаривание, осаждение, хроматографию, фильтрацию, растирание, кристаллизацию и тому подобное. Процедуры могут требовать защиты определенных групп, например гидроксильных, тиольных, амино или карбоксильных групп, для минимизации нежелательных реакций. Выбор, применение и удаление защитных групп хорошо известны и оценены как стандартная практика, например, T.W. Greene and P.G.M. Wuts in Protective Groups in Organic Chemistry (John Wiley and Sons, 1991).
В контексте настоящего описания: АсОН обозначает уксусную кислоту; водн. обозначает водный раствор, уш. обозначает уширенный, CH3CN обозначает ацетонитрил, CH2Cl2 обозначает метиленхлорид, д обозначает дублет, дд обозначает дублет дублетов, DIPEA обозначает N-диизопропилэтиламин, ДМАА обозначает N,N-диметилацетамид, ДМФА обозначает N,N-диметилформамид, ДМСО обозначает диметилсульфоксид, эи обозначает энантиомерный избыток, экв. обозначает эквивалент, ES обозначает электрораспылительную ионизацию, EtOAc обозначает EtOAc, EtOH обозначает EtOH, HATU обозначает 1-[бис(диметиламино)-метилен]-1H-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфат, ВЭЖХ обозначает высокоэффективную жидкостную хроматографию, iPrOH обозначает изопропанол, J обозначает константу связывания, KOAc обозначает ацетат калия, K2CO3 обозначает карбонат калия, ЖХМС обозначает жидкостную хроматографию - масс-спектрометрию, m/z обозначает соотношение массы к заряду, М обозначает молярность, м обозначает мультиплет, МеОН обозначает mEtOH, мин обозначает минуты, NaHCO3 обозначает бикарбонат натрия, Na2CO3 обозначает карбонат натрия, NEt3 обозначает триэтиламин, ЯМР обозначает ядерный магнитный резонанс, НМП обозначает N-метилпирролидон, ПЭГ обозначает полетиленгликоль, кв обозначает квартет, квинт обозначает квинтет, кт обозначает комнатную температуру, Rt обозначает время удержания, с обозначает синглет, насыщ. обозначает насыщенный, Т обозначает температуру, т обозначает триплет, тд обозначает триплет дублетов, ТГФ обозначает тетрагидрофуран, масс. обозначает массу, и δ обозначает химический сдвиг.
Схема А

Схема А иллюстрирует реакцию соединения формулы (1) и соединения формулы (2) с получением соединения формулы (Ia). Изображенное соединение формулы (1) представляет собой соединение, в котором группа A1 представляет собой гидроксильную группу или активирующие группы, как описано ниже, a Q, М, X1, Х2, Х3, Х4, Х5 и Х6 являются такими, как требуется в конечном соединении формулы (Ia) или группой, которая приводит к Q, М, X1, Х2, Х3, Х4, Х5 и Х6, как требуется в конечном соединении формулы (Ia). Например, соединение формулы (1) может представлять собой соединение, в котором изображенная группа «Q» представляет собой галоген, который дополнительно преобразован на последующей стадии, не показанной, с получением соединения, в котором Q является таким, как определено в формуле (Ia). Кроме того, например, соединение, в котором М представляет собой О, может быть дополнительно преобразовано до соединения, в котором М представляет собой S или в котором М представляет собой NR13. Получение таких соединений формулы (1) хорошо известно в данной области техники. Соединение формулы (2) представляет собой соединение, в котором R7, n, Y1, Y2, Z1, Z2, Z3 и Z4 являются такими, как требуется в конечном продукте формулы (Ia), или группой, которая приводит к R7, Y1, Y2, Z1, Z2, Z3 и Z4, как требуется в конечном продукте формулы (Ia). Получение таких соединений формулы (2) хорошо известно в данной области техники.
Как упоминалось выше, схема А иллюстрирует реакцию соединения формулы (1) с использованием соединения формулы (2) для получения соединения формулы (Ia). Типичные группы A1 представляют собой гидроксил или уходящую группу, такую как хлор, бром или имидазолил, активирующий фрагмент, смешанный ангидрид другой карбоновой кислоты, такой как муравьиная кислота, уксусная кислота, или представляет собой другую часть симметричного ангидрида, образованного из двух соединений формулы (1). Например, могут быть использованы стандартные условия образования амидов, такие как условия использования связывающих агентов, включая те, которые используются в пептидных связях, такие как 2-(1Н-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат метанаминий (HATU), дициклогексилкарбодиимид (DCC) и 1-(3-диметиламинопропил)-3-этилкарбодиимид HCl. При необходимости или желании, для облегчения реакции может быть использована добавка, такая как 4-(диметиламино)-пиридин, 1-гидроксибензотриазол и тому подобное. Такие реакции, как правило, проводят с использованием основания, такого как N-метилморфолин или NEt3, в широком спектре подходящих растворителей, таких как CH2Cl2, ДМФА, НМП, ДМАА, ТГФ и тому подобное. Такие реакции хорошо изучены и известны в данной области техники.
Специалисту в данной области техники будет очевидно, что соединение формулы (Ia) может быть преобразовано различными способами для получения других соединений формулы (Ia). Такие реакции включают гидролиз, окисление, восстановление, алкилирование, арилирование (включая гетероарильные группы), амидирование, сульфирование и тому подобное.
Кроме того, на необязательной стадии, не показанной, соединения формулы (Ia) могут быть превращены в соли способами, хорошо изученными и известными из уровня техники.
Схема В

На схеме В показана реакция соединения формулы (3) и соединения формулы (4) с получением соединения формулы (Ib). Изображенные соединения формулы (3) Q, R7, X1, Х2, Х3, Х4, Х5 и Х6 являются такими, как требуется в конечном соединении формулы (I) или группой, которая приводит к Q, R7, X1, Х2, Х3, Х4, Х5 и Х6, как требуется в конечном соединении формулы (Ib). Например, соединение формулы (3) может представлять собой соединение, в котором изображенная группа «Q» представляет собой галоген, который дополнительно преобразован на последующей стадии, не показанной, с получением соединения, в котором Q является таким, как определено в формуле (Ib). Получение таких соединений формулы (3) хорошо известно в данной области техники. Соединение формулы (4) представляет собой соединение, в котором группа А2 представляет собой карбоксильную группу или активирующие группы, как описано ниже, и n, Y1, Y2, Z1, Z2, Z3 и Z4 являются такими, как требуется в конечном продукте формулы (Ib), или группой, которая приводит к Y1, Y2, Z1, Z2, Z3 и Z4, как требуется в конечном продукте формулы (Ib). Получение таких соединений формулы (4) хорошо известно в данной области техники.
Как упоминалось выше, схема В иллюстрирует реакцию соединения формулы (3), в которой с использованием соединения формулы (4) получается соединение формулы (Ib). Типичные группы А2 представляют собой карбокси или хлорид кислоты или бромид кислоты, или имидазид, активирующий фрагмент, смешанный ангидрид другой карбоновой кислоты, такой как муравьиная кислота, уксусная кислота, или представляет собой другую часть симметричного ангидрида, образованного из двух соединений формулы (4), в которых А2 представляет собой карбоксильное производное или другой активированный фрагмент. Такие реакции, как правило, проводят с использованием основания, такого как N-метилморфолин или триэтиламин, в широком спектре подходящих растворителей, таких как CH2Cl2, ДМФА, N-метилпирролидон (НМП), ДМАА, ТГФ и тому подобное. Как хорошо известно, соединение (Ib), в котором М представляет собой О, может быть дополнительно превращено в соединение, в котором М представляет собой S или в котором М представляет собой NR13.
Схема С

На схеме С изображена реакция соединения формулы (5) и соединения формулы (6) с получением соединения формулы (Ib). Изображенное соединение формулы (5) является таким же, как и соединение формулы (3), описанное на Схеме В. Соединение формулы (6) представляет собой соединение, в котором изображенные R7 и n, Y1, Y2, Z1, Z2, Z3 и Z4 являются такими, как требуется в конечном продукте формулы (Ib), или группой, которая приводит к изображенному R7, и Y1, Y2, Z1, Z2, Z3 и Z4, как требуется в конечном продукте формулы (Ib). Получение таких соединений формулы (6) хорошо известно в данной области техники. Образование несимметричных мочевин хорошо известно с использованием фосгена, карбонилдиимидазола, изопропенилкарбаматов и необязательно замещенных феноксикарбонилгалогенидов, таких как п-нитрофеноксикарбонилхлорид.
Такие реакции, как правило, проводят последовательно путем добавления фосгена, карбонилдиимидазола, изопропенилкарбаматов и необязательно замещенных феноксикарбонилгалогенидов к соединению формулы (5) или соединению формулы (6) с использованием основания, такого как N-метилморфолин или триэтиламин, в широком спектре подходящих растворителей, таких как CH2Cl2, ДМФА, N-метилпирролидон (НМП), ДМАА, ТГФ и тому подобное. Затем добавляют другое соединение (5) или соединение (6).
Специалисту в данной области техники будет известно, что на схемах В и С соединение формулы (Ib) может быть преобразовано различными способами для получения других соединений формулы (Ib). Такие реакции включают гидролиз, окисление, восстановление, алкилирование, арилирование (включая гетероарильные группы), амидирование, сульфирование и тому подобное. Как хорошо известно, соединение (Ib), в котором М представляет собой О, может быть дополнительно превращено в соединение, в котором М представляет собой S или в котором М представляет собой NR13.
Кроме того, на необязательной стадии, не показанной, соединения формулы (Ib) могут быть превращены в соли способами, хорошо изученными и известными из уровня техники.
Следующие примеры являются иллюстративными и неограничивающими и представляют собой конкретные варианты реализации настоящего изобретения.
Методы анализа А и В проводили с использованием системы жидкостной хроматографии Agilent 1200 Infinity Series (ЖХ), состоящей из дегазатора 1260 HiP (G4225A), бинарного насоса 1260 (G1312B), автоматического пробоотборника 1290 (G4226A), термостатированного отсека колонки 1290 (G1316C) и диодно-матричного детектора 1260 (G4212B), соединенного с детектором одноквадрупольной масс-спектрометрии (МС) Agilent 6150. По умолчанию объем вводимой пробы был установлен на 1 мкл. Получение УФ-излучения (ДМД) проводили при 40 Гц, с диапазоном сканирования 190-400 нм (с шагом 5 нм). Перед МС-детектором использовали разделение потока 1:1. МС работал с источником ионизации электрораспылением (ПЭР) как в режиме положительных, так и отрицательных ионов. Давление в небулайзере было установлено на 50 фунтов/кв. дюйм, температура сушильного газа и расход до 350°С и 12 л/мин соответственно. Используемые капиллярные напряжения составляли 4000 В в положительном режиме и 3500 В в отрицательном режиме. Диапазон сбора данных МС был установлен на 100-800 m/z с размером шага 0,2 m/z в обоих режимах полярности. Напряжение фрагментатора было установлено на 70 (ИЭР+) или 120 (ИЭР-), коэффициент усиления - на 0,40 (ИЭР+) или 1,00 (ИЭР-), а пороговое значение количества ионов - на 4000 (ИЭР+) или 1000 (ИЭР-). Общее время цикла сканирования МС составило 0,15 с/цикл. Получение данных проводили с помощью программного обеспечения Agilent Chemstation.
Метод А: Анализы проводили на колонке Phenomenex Gemini-NX С18 длиной 50 мм, внутренним диаметром 2,1 мм и размером частиц 3 мкм. В качестве подвижной фазы использовали: А1 = вода с 0,1% муравьиной кислоты / B1=CH3CN с 0,1% муравьиной кислоты. Рабочий цикл проводили при температуре 50°С и расходе 1,2 мл/мин с градиентным элюированием от 5% до 95% (В1) в течение 1,5 мин с последующей выдержкой 0,5 мин при 95% (В1).
Метод В: Анализы проводили на колонке Waters XBridge С18 длиной 50 мм, внутренним диаметром 2,1 мм и размером частиц 3,5 мкм. Используемая подвижная фаза представляла собой: А2 = вода с 10 мМ бикарбоната аммония, доведенная до рН 9 с помощью гидроксида аммония / В2=CH3CN. Рабочий цикл проводили при температуре 50°С и расходе 1,2 мл/мин с градиентным элюированием от 5% до 95% (В2) в течение 1,5 мин с последующей выдержкой 0,5 мин при 95% (В2).
Анализы методов С и D проводили с использованием системы жидкостной хроматографии (ЖХ) Waters Acquity СВЭЖХ, соединенной с детектором Waters SQ Detector 2 одноквадрупольной масс-спектрометрии (МС). Получение УФ-излучения (ДМД) проводили с диапазоном сканирования 200-400 нм (с разрешением 1,2 нм). МС работал с источником ионизации электрораспылением (ИЭР) как в режиме положительных, так и отрицательных ионов. Капиллярное напряжение 3,50 (кВ), напряжение конуса 35 (В) и температура десольватации 550°С. Поток газа десольватации 1000 (л/ч), поток конусного газа 50 (л/ч). Диапазон сбора данных МС был установлен на уровне 100-1500 m/z. Время цикла сканирования МС составляло 0,5 сек. Сбор данных выполнялся с помощью программного обеспечения Waters Masslynx.
Метод С: Анализы проводили на колонке Acquity СВЭЖХ ВЕН С18 длиной 50 мм, внутренним диаметром 2,1 мм и размером частиц 1,7 мкм. В качестве подвижной фазы использовали: А1 = вода с 0,1% муравьиной кислоты / B1=CH3CN с 0,1% муравьиной кислоты. Объем вводимой пробы составлял 0,1 мкл. Рабочий цикл проводили при температуре 40°С и расходе 0,6 мл/мин с градиентным элюированием. Информация о методе (время (мин) и В %): 0-5; 0,3-5; 2,5-95; 3,7-95; 4-5; 4,6-5.
Метод D: Анализы проводили на колонке Acquity СВЭЖХ ВЕН С18 длиной 50 мм, внутренним диаметром 2,1 мм и размером частиц 1,7 мкм. В качестве подвижной фазы использовали: А1 = вода с 10 мМ ацетата аммония / B1=CH3CN с 0,1% муравьиной кислоты. Объем вводимой пробы составлял 0,1 мкл. Рабочий цикл проводили при температуре 45°С и расходе 0,5 мл/мин с градиентным элюированием. Информация о методе (время (мин) и А %): 0-98; 0,3-98; 3,2-2; 4,4-2; 4,7-98.
Пример 1.1
N-[8-(3,5-дихлорфенил)-4-(диметиламино)-3-хинолил]-2,3-дигидро-1,4-бензоксазин-4-карбоксамид

К перемешиваемому раствору 8-бромхинолин-4-ола (2 г, 8,82 ммоль) в пропионовой кислоте (20 мл, 265 ммоль) при 100°С медленно добавляли азотную кислоту (1 мл, 16 ммоль) в течение 5 минут. Реакционную смесь нагревали до 125°С и оставляли при перемешивании в течение 45 мин. Затем реакционной смеси давали остыть до комнатной температуры, вызывая осаждение продукта. Твердое вещество собирали фильтрованием и промывали водой (3×10 мл), iPrOH (10 мл), изогексаном (10 мл) и затем сушили в вакуумной печи в течение 1 часа с получением 8-бром-3-нитро-хинолин-4-ола. ЖХ-МС (Метод В): Rt=0,54 мин, m/z=269 [М+Н]+.
К раствору 8-бром-3-нитро-хинолин-4-ола (1,52 г, 5,37 ммоль) добавляли POCl3 (10 мл, 107 ммоль). Суспензию нагревали с обратным холодильником и перемешивали в течение 2 часов. Реакционной смеси давали остыть до комнатной температуры и оставляли стоять в течение ночи. Реакционную смесь концентрировали в вакууме (азеотропная отгонка с толуолом) с получением 8-бром-4-хлор-3-нитро-хинолина, который непосредственно применяли на следующей стадии без дополнительной очистки.
К раствору 8-бром-4-хлор-3-нитрохинолина (2,32 г, 5,38 ммоль) в ТГФ (30 мл) медленно добавляли диметиламин (2 M в ТГФ, 7 мл, 14 ммоль). Реакционную смесь оставляли при перемешивании при комнатной температуре в течение 1,5 часов. Реакционную смесь разделяли между EtOAc и насыщенным водн. NaHCO3 (по 50 мл каждого). Добавляли солевой раствор (50 мл). Слои разделяли и водный слой экстрагировали EtOAc (2×50 мл). Объединенные органические слои концентрировали в вакууме, в результате чего получали 8-бром-N,N-диметил-3-нитро-хинолин-4-амин. ЖХ-МС (Метод В): Rt=1,13 мин, m/z=296 [М+Н]+.
К раствору 8-бром-N, N-диметил-3-нитро-хинолин-4-амина (505 мг, 1,62 ммоль) добавляли (3,5-дихлорфенил)-бороновую кислоту (314 мг, 1,61 ммоль), тетракис-(трифенилфосфин)-палладий(0) (92 мг, 0,08 ммоль) и Na2CO3 (351 мг, 3,28 ммоль). Сосуд герметично закрывали, затем вакуумировали и трижды заполняли N2. Добавляли 1,4-диоксан (9 мл), затем воду (3 мл), и реакционную смесь нагревали до 100°С в микроволновой печи в течение 1 часа. Реакционную смесь разделяли между EtOAc и насыщ. водн. NaHCO3 (по 50 мл каждого). Слои разделяли и водный слой экстрагировали EtOAc (2×25 мл). Объединенные органические слои концентрировали в вакууме, а остаток очищали с помощью колоночной хроматографии, в результате чего получали 8-(3,5-дихлорфенил)-N,N-диметил-3-нитро-хинолин-4-амин. ЖХ-МС (Метод В): Rt=1,57 мин, m/z=362 [М+Н]+.
К перемешиваемой суспензии 8-(3,5-дихлорфенил)-N, N-диметил-3-нитро-хинолин-4-амина (401 мг, 1,05 ммоль) в ТГФ (5 мл), EtOH (5 мл) и воде (2,5 мл) добавляли железо (184 мг, 3,23 ммоль) и NH4Cl (168 мг, 3,13 ммоль). Реакционную смесь нагревали до 75°С и оставляли при перемешивании в течение 45 мин. Реакционной смеси давали остыть до комнатной температуры, затем разделяли между насыщ. водн. NaHCO3 и EtOAc (25 мл каждого). Смесь фильтровали через Celite® (промывая EtOAc), и разделяли слои фильтрата. Водный слой подвергали экстракции EtOAc (2×25 мл), и объединенные органические слои концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии, в результате чего получали 8-(3,5-дихлорфенил)-N4,N4-диметилхинолин-3,4-диамин. ЖХ-МС (Метод В): Rt=1,48 мин, m/z=363,2 [М+Н]+.
К перемешиваемому раствору 4-нитрофенилхлорформиата (88 мг, 0,42 ммоль) в ТГФ (2 мл) при 0°С в атмосфере N2 по каплям добавляли раствор 8-(3,5-дихлорфенил)-N4,N4-диметилхинолин-3,4-диамина (148 мг, 0,42 ммоль) в ТГФ (2,5 мл) в течение 2 мин. Реакционную смесь оставляли при перемешивании при 0°С в течение 30 мин. Реакционный раствор непосредственно использовали на следующей стадии.
К реакционной смеси добавляли 3,4-дигидро-2Н-1,4-бензоксазин (71 мг, 0,51 ммоль) и NEt3 (132 мкл, 0,94 ммоль) в ТГФ (0,5 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь разделяли между насыщ. водн. NaHCO3 и CH2Cl2 (по 20 мл каждого). Слои разделяли и водный слой экстрагировали CH2Cl2 (2×20 мл). Объединенные органические слои пропускали через Celite® и концентрировали в вакууме. Неочищенный продукт очищали с помощью колоночной хроматографии с получением целевого соединения. ЖХ-МС (Метод В): Rt=1,62 мин, m/z=493,0 [М+Н]+. 1Н ЯМР (400 МГц, CDCl3) δ [м.д.]: 9,95 (с, 1Н), 9,13 (с, 1Н), 7,91 (квинт, J=4,8 Гц, 1Н), 7,55 (д, J=2 Гц, 1Н), 7,53 (д, J=5,2 Гц, 1Н), 7,43 (дд, J=1,6, 8,4 Гц, 1Н), 7,38 (т, J=2 Гц, 1Н), 7,17 (м, 1Н), 7,01 (м, 2Н), 4,36 (т, J=4,4 Гц, 2Н), 4,02 (т, J=4,8 Гц, 2Н), 2,9 (с, 6Н).
Пример 2.1
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-1,7-нафтиридин-3-карбоксамид

Смесь 2-хлор-3-фтор-пиридин-4-карбоновой кислоты (10,1 г, 56,3 ммоль) и SOCl2 (40 мл, 547 ммоль) нагревали при 80°С в течение 2 часов. Реакционной смеси давали остыть до комнатной температуры и концентрировали в вакууме. Ее непосредственно использовали на следующей стадии: добавляли толуол (145 мл) и NEt3 (9,8 мл, 70 ммоль), а затем этил-3-(диметиламино)-проп-2-еноат (10,2 г, 69,6 ммоль). Реакционную смесь нагревали при 80°С и перемешивали в течение 45 мин. Смеси давали остыть до комнатной температуры и фильтровали через Celite® (промывка EtOAc). Фильтрат концентрировали в вакууме и остаток распределяли между EtOAc и водн. 2М HCl (150 мл каждого). Слои разделяли и водный слой экстрагировали EtOAc (150 мл). Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, в результате чего получали этил-2-(2-хлор-3-фтор-пиридин-4-карбонил)-3-(диметиламино)-проп-2-еноат. ЖХ-МС (Метод В): Rt=0,86 мин, m/z=301,00 [М+Н]+.
К раствору этил-2-(2-хлор-3-фтор-пиридин-4-карбонил)-3-(диметиламино)-проп-2-еноата (188 мг, 0,59 ммоль) в диэтиловом эфире (2,4 мл) и EtOH (0,6 мл) добавляли 4-метоксибензиламин (94 мкл, 0,71 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 15 мин, получая осадок. Реакционную смесь концентрировали в вакууме, в результате чего получали остаток. Указанный остаток растирали с циклогексаном с получением этил-2-(2-хлор-3-фторпиридин-4-карбонил)-3-[(4-метоксифенил)-метиламино]-проп-2-еноата. ЖХ-МС (Метод В): Rt=1,21 мин, m/z=393 [М+Н]+.
К раствору этил-2-(2-хлор-3-фтор-пиридин-4-карбонил)-3-[(4-метоксифенил)-метиламино]-проп-2-еноата (214 мг, 518 мкмоль) в ДМФА (2,6 мл) добавляли K2CO3 (230 мг, 1,66 ммоль) при комнатной температуре. Реакционную смесь нагревали при 40°С и оставляли при перемешивании в течение 2 часов. После охлаждения до кт реакционную смесь вливали в ледяную воду (20 мл), с образованием мелкого осадка. Осадок растворяли в EtOAc (20 мл) и разделяли слои. Водный слой экстрагировали EtOAc (2×10 мл), а объединенные органические слои промывали водой (20 мл), сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, получая этил 8-хлор-1-[(4-метоксифенил)-метил]-4-оксо-1,7-нафтиридин-3-карбоксилат. ЖХ-МС (Метод В): Rt = 1,01 мин, m/z = 373 [М+Н]+.
(3,5-дихлорфенил)-бороновую кислоту (110 мг, 0,56 ммоль) смешивали с комплексом 1,1'-бис-(дифенилфосфино)-ферроцен-Pd (II)⋅CH2Cl2 и Na2CO3 (100 мг, 0,93 ммоль). Флакон закрывали, затем вакуумировали и заполняли N2. Затем добавляли этил-8-хлор-1-[(4-метоксифенил)-метил]-4-оксо-1,7-нафтиридин-3-карбоксилат (186 мг, 0,47 ммоль) в 1,4-диоксане (2,4 мл, 28 ммоль), затем воду (0,8 мл) и реакционную смесь нагревали при 100°С в микроволновой печи в течение 1 часа. Реакционную смесь фильтровали через слой Celite® (промывая EtOAc). Фильтрат промывали водой (20 мл), сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, затем очищали с помощью колоночной хроматографии, в результате чего получали этил-8-(3,5-дихлорфенил)-1-[(4-метоксифенил)-метил]-4-оксо-1,7-нафтиридин-3-карбоксилат. ЖХ-МС (Метод В): Rt = 1,30 мин, m/z = 483 [М+Н]+.
К раствору этил-8-(3,5-дихлорфенил)-1-[(4-метоксифенил)-метил]-4-оксо-1,7-нафтиридин-3-карбоксилата (877 мг, 1,72 ммоль) в CH2Cl2 (9 мл) добавляли анизол (1 мл, 1,74 ммоль), затем ТФУК (2,5 мл, 33 ммоль). Полученную реакционную смесь перемешивали при комнатной температуре в течение 1 часа, затем концентрировали в вакууме. К неочищенному продукту добавляли смесь насыщ. водн. NaHCO3 и EtOAc (25 мл каждого), и полученную суспензию интенсивно перемешивали в течение 15 мин. Выделяли осадок фильтрованием (промывали водой, затем EtOAc) и сушили в вакуумной печи, получая этил-8- (3,5-дихлорфенил)-4-гидрокси-1,7-нафтиридин-3-карбоксилат. ЖХ-МС (Метод В): Rt = 0,9 мин, m/z = 363 [М+Н]+.
К перемешиваемой суспензии этил-8-(3,5-дихлорфенил)-4-гидрокси-1,7-нафтиридин-3-карбоксилата (61 мг, 0,13 ммоль) в CH2Cl2 (2 мл) добавляли оксалилхлорид (17 мкл, 192 мкмоль), затем ДМФА (1 мкл, 13 мкмоль) и полученную смесь оставляли перемешиваться при комнатной температуре в течение 45 мин.
Реакцию гасили путем добавления насыщ. водн. раствора NaHCO3 (5 мл), и смесь разделяли между водой и CH2Cl2 (по 10 мл каждого). Слои разделяли и водный слой экстрагировали CH2Cl2. Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, в результате чего получали этил-4-хлор-8-(3,5-дихлорфенил)-1,7-нафтиридин-3-карбоксилат. ЖХ-МС (Метод В): Rt = 1,6 мин, m/z = 381 [М+Н]+.
В микроволновую пробирку добавляли этил-4-хлор-8-(3,5-дихлорфенил)-1,7-нафтиридин-3-карбоксилат (59 мг, 0,12 ммоль) и диметиламин⋅HCl (17 мг, 0,2 ммоль) в 1,4-диоксане (0,5 мл). Флакон закрывали, добавляли DIPEA (73 мкл, 0,41 ммоль) и реакционную смесь нагревали в микроволновой печи при 100°С в течение 30 минут. Смесь разбавляли EtOAc (10 мл), промывали насыщ. водн. раствором NaHCO3 (10 мл) и солевым раствором (10 мл), сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, получая этил-8-(3,5-дихлорфенил)-4-(диметиламино)-1,7-нафтиридин-3-карбоксилат.ЖХ-МС (Метод В): Rt = 1,5 мин, m/z = 390 [М+Н]+. К раствору этил-8-(3,5-дихлорфенил)-4-(диметиламино) -1,7-нафтиридин-3-карбоксилата (556 мг, 1,35 ммоль) в ТГФ (14 мл) при перемешивании добавляли раствор гидроксида лития (99 мг, 4,05 ммоль) в воде (4,5 мл) и МеОН (4,5 мл). Реакционную смесь нагревали при 40°С в течение 2 часов и оставляли при перемешивании при комнатной температуре в течение ночи. Затем смесь концентрировали в вакууме, и остаток помещали в воду (25 мл). Водный слой промывали EtOAc (25 мл), затем доводили рН до 4 путем добавления водн. 2 М HCl, получая суспензию. Осадок выделяли путем фильтрации и сушили в вакуумной печи в течение ночи, в результате чего получали 8-(3,5-дихлорфенил)-4-(диметиламино) -1,7-нафтиридин-3-карбоновую кислоту в виде твердого вещества. ЖХ-МС (Метод В): Rt = 0,78 мин, m/z = 362 [М+Н]+.
При кт в атмосфере N2 к раствору 3,4-дигидро-2H-1,4-бензоксазина (504 мг, 3,73 ммоль) в EtOH (4 мл) добавляли нитрит натрия (309 мг, 4,48 ммоль) в воде (1,6 мл). Затем смесь охлаждали до 0°С. К реакции по каплям добавляли концентрированную HCl (0,39 мл, 4,7 ммоль) при 0°С. Затем реакционную смесь перемешивали при 0°С в течение 15 мин.
Добавляли раствор гидроксида натрия (1,43 г, 35,87 ммоль) в воде (3,7 мл) при 0°С с последующим добавлением гидросульфита натрия (2,40 г, 11,75 ммоль).
Полученную в результате суспензию нагревали до 90°С в течение 2 часов, затем охлаждали до комнатной температуры.
Реакционную смесь разбавляли водой (30 мл) и затем экстрагировали толуолом (30 мл) и EtOAc (15 мл). Объединенные органические слои разделяли и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии с получением 2,3-дигидро-1,4-бензоксазин-4-амина в виде бледно-желтого масла (354 мг). ЖХ-МС (метод В) Rt = 0,63 мин, m/z = 151 [М+Н]+. К перемешиваемой суспензии 8-(3,5-дихлорфенил)-4-(диметиламино) -1,7-нафтиридин-3-карбоновой кислоты (158 мг, 0,41 ммоль) в ДМ ФА (5 мл) добавляли NEt3 (0,25 мл, 1,8 ммоль), затем 2,3-дигидро-1,4-бензоксазин-4-амин (79 мг, 0,501 ммоль) и РуВОР (341 мг, 0,64 ммоль). Реакционную смесь оставляли при перемешивании при кт в атмосфере N2 в течение 48 часов. Реакционную смесь разбавляли солевым раствором (25 мл) и экстрагировали CH2Cl2 (3×15 мл). Объединенные органические слои разделяли и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии, в результате чего получали целевое соединение. ЖХ-МС (метод В) Rt = 1,35 мин, m/z = 494 [М+Н]+. 1H ЯМР (400 МГц, ДМСО-d6) δ [м.д.]: 10,7 (с, 1H), 8,90 (с, 1H), 8,67 (д, J=4,4 Гц, 1H), 8,1 (м, 2H), 7,75 (т, J=2 Гц, 1H), 7,03 (дд, J=8, 1,2 Гц, 1H), 6,85 (тд, J=2, 8 Гц, 1H), 6,69-6,78 (м, 2H), 4,38 (т, J=4,4 Гц, 2H), 3,68 (с, 2H), 3,13 (с, 6Н).



Пример 3.1
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-1,5-нафтиридин-3-карбоксамид

Тионилхлорид (15 мл, 205 ммоль) добавляли к 3,4-дихлорпиридин-2-карбоновой кислоте (3,96 г, 20,6 ммоль) и реакционную смесь нагревали до 80°С в течение 1 часа. Реакционной смеси давали остыть до кт и концентрировали в вакууме, в результате чего получали 3,4-дихлорпиридин-2-карбонилхлорид, который применяли на следующей стадии без дополнительной очистки.
К перемешиваемому раствору 3,4-дихлорпиридин-2-карбонилхлорида (20,6 ммоль, 4,76 г) в толуоле (50 мл) добавляли NEt3 (3,5 мл, 25 ммоль), а затем этил-3-(диметиламино)-проп-2-еноат (3,6 мл, 25 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь фильтровали через слой Celite® (промывая EtOAc). Фильтрат концентрировали в вакууме и остаток распределяли между EtOAc и водн. 1 М HCl (по 100 мл каждого). Слои разделяли, и водный слой экстрагировали EtOAc (50 мл). Объединенные органические слои концентрировали в вакууме, в результате чего получали этил-2-(3,4-дихлорпиридин-2-карбонил)-3-(диметиламино)проп-2-еноат. ЖХ-МС (метод В) Rt = 0,88 мин, m/z = 317,0 [М+Н]+.
К перемешиваемому раствору этил-2-(3,4-дихлорпиридин-2-карбонил)-3-(диметиламино)-проп-2-еноата (5,58 г, 12,7 ммоль) в диэтиловом эфире (50 мл) и EtOH (12 мл) добавляли 4-метоксибензиламин (1,9 мл, 14 ммоль). Реакционную смесь оставляли при перемешивании при кт в течение 2 часов. Реакционную смесь разбавляли водой (100 мл). Слои разделяли и водный слой экстрагировали CH2Cl2 (3×50 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме, в результате чего получали этил-2-(3,4-дихлорпиридин-2-карбонил)-3-[(4-метоксифенил)-метиламино]-проп-2-еноат. Этил-2-(3,4-дихлорпиридин-2-карбонил)-3-[(4-метоксифенил)-метиламино]-проп-2-еноат (5,92 г, 9,40 ммоль) растворяли в ДМФА (24 мл). Добавляли K2CO3 (4,0 г, 28,9 ммоль), и смесь перемешивали при 90°С в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры, гасили путем добавления воды (250 мл) и разбавляли CH2Cl2 (100 мл). Слои разделяли и водный слой экстрагировали CH2Cl2 (2×50 мл). Объединенные органические слои фильтровали через Celite®, а затем промывали солевым раствором (100 мл), сушили над безводным Na2SO4, фильтровали и концентрировали до сухого состояния в вакууме. Неочищенный материал очищали с помощью хроматографии (0-6% МеОН в CH2Cl2), получая этил-8-гидрокси-1-[(4-метоксифенил)-метил]-4-оксо-1,5-нафтиридин-3-карбоксилат. Этил-8-гидрокси-1-[(4-метоксифенил)-метил]-4-оксо-1,5-нафтиридин-3-карбоксилат (840 мг, 1,09 ммоль) растворяли в CH2Cl2 (11 мл) и ДМФА (0,05 мл). К этой смеси добавляли оксалилхлорид (0,48 мл, 5,5 ммоль), и смесь нагревали с обратным холодильником в течение 3 часов. Реакционную смесь охлаждали и гасили путем добавления насыщ. водн. раствора NaHCO3 (50 мл). Слои разделяли и водный слой экстрагировали CH2Cl2 (2×25 мл). Объединенные органические слои концентрировали в вакууме, в результате чего получали этил-4,8-дихлор-1,5-нафтиридин-3-карбоксилат.
Этил-4,8-дихлор-1,5-нафтиридин-3-карбоксилат (950 мг, 2,21 ммоль) растворяли в ТГФ (5 мл). К полученному раствору по каплям добавляли диметиламин (2 моль/л) в ТГФ (1,1 мл, 2,2 ммоль, 2 М) и смесь перемешивали при комнатной температуре в течение 30 мин. Неочищенную реакционную смесь концентрировали, а остаток очищали с помощью колоночной хроматографии (20-50% EtOAc в циклогексане), в результате чего получали этил-8-хлор-4-(диметиламино)-1,5-нафтиридин-3-карбоксилат. ЖХ-МС (метод В) Rt = 1,07 мин, m/z = 280,0 [М+Н]+. Этил-8-хлор-4-(диметиламино)-1,5-нафтиридин-3-карбоксилат (315 мг, 0,93 ммоль) растворяли в 1,4-диоксане (3 мл) и воде (1 мл). К указанной смеси добавляли 1,Г-бис(дифенилфосфино)-ферроцен]-дихлорпалладий(II) (40 мг, 0,048 ммоль), (3,5-дихлорфенил)-бороновую кислоту (215 мг, 1,13 ммоль) и Na2CO3 (300 мг, 2,83 ммоль). Смесь подвергали микроволновому облучению в течение 1 часа при 100°С. Неочищенную реакционную смесь концентрировали и остаток очищали с помощью колоночной хроматографии (5-40% EtOAc в циклогексане), в результате чего получали этил-8-(3,5-дихлорфенил)-4-(диметиламино)-1,5-нафтиридин-3-карбоксилат. ЖХ-МС (метод В) Rt = 1,56 мин, m/z = 390,0 [М+Н]+. К перемешиваемому раствору этил-8-(3,5-дихлорфенил)-4-(диметиламино)-1,5-нафтиридин-3-карбоксилата (272 мг, 0,65 ммоль) в 1,4-диоксане (2 мл) добавляли гидроксид лития (32 мг, 1,34 ммоль) в воде (2 мл). Реакционную смесь нагревали до 100°С в течение ночи. Затем реакционную смесь охлаждали до комнатной температуры. Реакционную смесь гасили путем добавления воды (50 мл) и EtOAc (50 мл). рН доводили до значения, равного 4, с помощью 2 М HCl. Слои разделяли и водный слой экстрагировали EtOAc (2×50 мл). Объединенные органические слои промывали солевым раствором, сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме, получая 8-(3,5-дихлорфенил)-4-(диметиламино)-1,5-нафтиридин-3-карбоновую кислоту. ЖХ-МС (метод В) Rt = 0,82 мин, m/z = 362,0 [М+Н]+.
Смесь 2,3-дигидро-1,4-бензоксазин-4-амина (0,115 г, 0,73 ммоль) и РуВОР (0,63 г, 1,21 ммоль) помещали в атмосферу N2 и обрабатывали раствором 8-(3,5-дихлорфенил)-4-(диметиламино)-1,5-нафтиридин-3-карбоновой кислоты (0,24 г, 0,67 ммоль) в ТГФ (3 мл), а затем NEt3 (0,42 мл, 3 ммоль). Полученную реакционную смесь оставляли при перемешивании при кт в течение 48 часов. Реакционную смесь гасили путем добавления насыщ. водн. раствора NaHCO3 (100 мл) и разбавляли CH2Cl2 (50 мл). Слои разделяли и водный слой экстрагировали CH2Cl2 (2×25 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и затем концентрировали в вакууме. Неочищенный продукт очищали с помощью колоночной хроматографии (10-50% EtOAc в циклогексане), в результате чего получали целевое соединение. ЖХ-МС (метод В) Rt = 1,39 мин, m/z = 494,0 [М+Н]+. 1Н ЯМР (400 МГц, CDCl3) δ [м.д.]: 9,62 (с, 1H), 9,24 (с, 1H), 8,96 (д, J=4,4 Гц, 1H), 7,59 (м, 3Н), 7,47 (т, J=2 Гц, 1H), 6,79-6,95 (м, 4Н), 4,50 (т, J=4,4 Гц, 2H), 3,74 (т, J=4,8 Гц, 2H), 3,35 (с, 6Н).

Пример 4.1
5-(3,5-дихлорфенил)-К-(2,3-дигидро-1,4-бензоксазин-4-ил)-1-(диметиламино)нафталин-2-карбоксамид

Круглодонную колбу, содержащую смесь 1-бром-5-нитронафталина (1,04 г, 4,13 ммоль), (3,5-дихлорфенил)-бороновой кислоты (0,7 г, 3,6 ммоль), Na2CO3 (0,86 г, 8,10 ммоль) и [1,1''-бис-(дифенилфосфино)-ферроцен]-дихлорпалладия(II) (156 мг, 0,20 ммоль), вакуумировали и трижды повторно заполняли N2. Реакционную смесь обрабатывали 1,4-диоксаном (20 мл) и дегазированной водой (6 мл), нагревали до 80°С и оставляли при перемешивании в течение 45 мин. Затем смеси давали остыть до кт, после чего разбавляли водой (40 мл) и экстрагировали CH2Cl2 (3×30 мл). Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью колоночной хроматографии, и соответствующие фракции объединяли и концентрировали в вакууме, получая 1-(3,5-дихлорфенил)-5-нитро-нафталин. Смесь 1-(3,5-дихлорфенил)-5-нитронафталина (928 мг, 2,77 ммоль), NH4Cl (0,47 г, 8,72 ммоль) и железа (0,47 г, 8,28 ммоль) помещали в атмосферу N2 перед обработкой ТГФ (14 мл), EtOH (14 мл) и водой (7 мл). Полученную смесь нагревали до 75°С и оставляли при перемешивании в течение 45 мин. Затем смеси давали остыть до комнатной температуры, после чего фильтровали через Celite® (промывая CH2Cl2). Фильтрат концентрировали в вакууме, обрабатывали насыщ. водн. NaHCO3 (50 мл) и экстрагировали CH2Cl2 (3×25 мл). Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, в результате чего получали 5-(3,5-дихлорфенил)-нафталин-1-амин. ЖХ-МС (метод В) Rt = 1,49 мин, m/z = 288,0 [М+Н]+.
Раствор 5-(3,5-дихлорфенил)-нафталин-1-амина (881 мг, 2,60 ммоль) в ДМФА (10 мл) помещали в атмосферу N2, охлаждали на ледяной/солевой бане до примерно -5°С и обрабатывали N-бромсукцинимидом (474 мг, 2,58 ммоль). Полученную реакционную смесь затем обрабатывали насыщ. водн. раствором NaHCO3 (50 мл) с образованием бледно-коричневого осадка. Смесь экстрагировали CH2Cl2 (3×30 мл), и объединенные органические слои концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии с получением 2-бром-5-(3,5-дихлорфенил)-нафталин-1-амина. ЖХ-МС (метод В) Rt = 1,64 мин, m/z = 365,8 [М+Н]+. Суспензию 2-бром-5-(3,5-дихлорфенил)-нафталин-1-амина (0,73 г, 1,79 ммоль) в муравьиной кислоте (6 мл, 160 ммоль) помещали в атмосферу N2 и обрабатывали раствором формальдегида (37 масс. % в воде; 110 ммоль, 8 мл). Полученную суспензию нагревали до 100°С и оставляли при перемешивании в течение 1 часа. Реакционной смеси давали остыть до комнатной температуры перед гашением путем осторожного добавления насыщ. водн. раствора NaHCO3 (60 мл). Затем смесь экстрагировали CH2Cl2 (3×20 мл), а объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии с получением 2-бром-5-(3,5-дихлорфенил)-N,N-диметил-нафталин-1-амина. ЖХ-МС (метод В) Rt = 1,93 мин, m/z = 393,8 [М+Н]+. Раствор 2-бром-5-(3,5-дихлорфенил)-N, N-диметил-нафталин-1-амина (532 мг, 1,28 ммоль) в 1,4-диоксане (10 мл) в сосуде под давлением обрабатывали МеОН (10 мл), NEt3 (0,54 мл, 3,9 ммоль) и [1,1'-бис-(дифенилфосфино)-ферроцен]-дихлорпалладием (II) (103 мг, 134 мкмоль) перед перемешиванием при 100°С в атмосфере СО (50 psi) в течение 16 часов. Затем реакционной смеси давали остыть до комнатной температуры, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии, в результате чего получали метил-5-(3,5-дихлорфенил)-1-(диметиламино)-нафталин-2-карбоксилат.ЖХ-МС (метод В) Rt = 1,75 мин, m/z = 374,0 [М+Н]+.
Раствор метил-5-(3,5-дихлорфенил)-1-(диметиламино)-нафталин-2-карбоксилата (421 мг, 1,01 ммоль) в 1,4-диоксане (15 мл), воде (5 мл) и гидроксиде лития (512 мг, 20,3 ммоль) перемешивали при 80°С в течение 48 часов. Реакционной смеси давали остыть до комнатной температуры перед обработкой 2 М HCl (17,5 мл - делали смесь слабоосновной). Водный слой экстрагировали CH2Cl2 (3×25 мл). Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме, в результате чего получали 5-(3,5-дихлорфенил)-1-(диметиламино)-нафталин-2-карбоновую кислоту. ЖХ/МС (метод В) Rt = 1,10 мин, m/z = 358,0 [М-Н]-.
Смесь 2,3-дигидро-1,4-бензоксазин-4-амина (0,082 г, 519 мкмоль) и РуВОР (452 мг, 869 мкмоль) помещали в атмосферу N2 и обрабатывали раствором 5-(3,5-дихлорфенил)-1-(диметиламино)-нафталин-2-карбоновой кислотой (192 мг, 426 мкмоль) в ТГФ (3 мл), а затем NEt3 (0,30 мл, 2,2 ммоль). Полученную реакционную смесь оставляли при перемешивании при комнатной температуре в течение ночи. Реакционную смесь разбавляли водой (15 мл) и экстрагировали CH2Cl2 (3×15 мл). Объединенные органические слои сушили над безводным MgSO4, фильтровали и концентрировали в вакууме. Неочищенный продукт очищали с помощью колоночной хроматографии, в результате чего получали целевое соединение. ЖХ-МС (метод В) Rt = 1,61 мин, m/z = 492,2 [М+Н]+. 1Н ЯМР (400 МГц, ДМСО) δ [м.д.]: 10,5 (с, 1H), 8,36 (д, J=8,6 Гц, 1H), 7,75 (т, J=2 Гц, 1H), 7,64-7,68 (м, 1H), 7,60-7,48 (м, 5 Н), 6,98 (дд, J=8, 1,4 Гц, 1H), 6,86-6,80 (м, 1H), 6,77 (дд, J=8, 1,6 Гц, 1H), 6,73-6,67 (м, 1H), 4,38 (т, J=4,3 Гц, 2H), 3,70-3,63 (м, 2H), 2,99 (с, 6 Н).
Пример 5.1
8-(3,5-дихлорфенил)-N-(2,3-дигидро-4Н-бензо[b][1,4]оксазин-4-ил)-4-(диметиламино)-хинолин-3-карбоксамид

Раствор 2-броманилина (7,96 г, 44,9 ммоль) и диэтил-2-(этоксиметилен)-пропандиоата (11 мл, 53,8 ммоль) нагревали до 125°С в течение 1 часа. ЖХ-МС (метод В) Rt = 1,28 мин, m/z = 342,0 [М+Н]+. Добавляли дифениловый эфир (100 мл), реакционную смесь нагревали до 250°С и оставляли при перемешивании в течение 48 часов. Реакционной смеси давали остыть до комнатной температуры с образованием осадка. Добавляли диэтиловый эфир (100 мл), выделяли осадок фильтрованием (промывая диэтиловым эфиром) и сушили в вакууме, получая этил-8-бром-4-гидрокси-хинолин-3-карбоксилат.ЖХ/МС (метод В) Rt = 0,69, m/z = 296,0 [М+Н]+.
Суспензию этил-8-бром-4-гидрокси-хинолин-3-карбоксилата (2,0 г, 6,42 ммоль) в CH2Cl2 (20 мл) помещали в атмосферу N2 и обрабатывали оксалилхлоридом (0,60 мл, 6,8 ммоль) и ДМФА (0,02 мл). Реакционную смесь нагревали до 50°С и оставляли при перемешивании в течение 45 мин. Реакционной смеси давали остыть до комнатной температуры, затем ее концентрировали в вакууме, получая этил-8-бром-4-хлор-хинолин-3-карбоксилат. ЖХ-МС (метод В) Rt = 1,28 мин, m/z = 314,0 [М+Н]+. Диметиламин (2 М) в ТГФ (13 мл) добавляли к этил-8-бром-4-хлор-хинолин-3-карбоксилату (2,13 г, 6,42 ммоль) в атмосфере N2. Полученную смесь нагревали до 60°С и оставляли при перемешивании в течение 15 мин. Реакционную смесь концентрировали в вакууме перед обработкой насыщ. водн. NaHCO3 (40 мл) и экстрагировали EtOAc (3×30 мл). Объединенные органические слои сушили над безводным MgSO4 и концентрировали в вакууме. Остаток подвергали колоночной хроматографии (20-60% EtOAc в циклогексане), в результате чего получали этил-8-бром-4-(диметиламино)-хинолин-3-карбоксилат.ЖХ-МС (метод В) Rt = 1,23 мин, m/z = 323,0 [М+Н]+.
В атмосфере N2 реакционную смесь этил-8-бром-4- (диметиламино)-хинолин-3-карбоксилата (2,22 г, 6,54 ммоль), (3,5-дихлорфенил)-бороновой кислоты (1,26 г, 6,61 ммоль), комплекса бис-(дифенилфосфино)-ферроцен-Pd (II)⋅CH2Cl2 (0,27 г, 0,33 ммоль) и Na2CO3 (1,43 г, 13,5 ммоль) в 1,4-диоксане (20 мл) и воде (10 мл) нагревали до 80°С и оставляли при перемешивании в течение 30 мин. Реакционной смеси давали остыть до кт, после чего разбавляли водой (70 мл) и экстрагировали CH2Cl2 (3×50 мл). Объединенные органические слои фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (0-30% EtOAc в циклогексане), в результате чего получали этил-8-(3,5-дихлорфенил)-4-(диметиламино)-хинолин-3-карбоксилат. ЖХ-МС (метод В) Rt = 1,67 мин, m/z = 389,0 [М+Н]+.
Раствор этил-8-(3,5-дихлорфенил)-4-(диметиламино)-хинолин-3-карбоксилата (2,82 г, 6,17 ммоль) в 1,4-диоксане (20 мл) обрабатывали водой (10 мл) и гидроксидом лития (0,44 г, 18,5 ммоль). Полученную реакционную смесь нагревали до 100°С и перемешивали в течение ночи. Реакционной смеси давали остыть до комнатной температуры, затем подкисляли до рН 2 с помощью 2 М HCl и экстрагировали EtOAc (3×30 мл). Водную фазу подщелачивали до рН 6 и экстрагировали 10% МеОН в CH2Cl2 (3×30 мл). Органические фазы объединяли и концентрировали в вакууме, получая 8-(3,5-дихлорфенил)-4-(диметиламино)-хинолин-3-карбоновую кислоту. ЖХ-МС (метод В) Rt = 0,94 мин, m/z = 361,0 [М+Н]+.
К перемешиваемой суспензии 8-(3,5-дихлорфенил)-4-(диметиламино)-хинолин-3-карбоновой кислоты (160 мг, 0,35 ммоль) в ДМФА (3,5 мл) добавляли NEt3 (200 мкл, 1,42 ммоль), затем 2,3-дигидро-1,4-бензоксазин-4-амин (67 мг, 0,42 ммоль) и РуВОР (282 мг, 0,53 ммоль). Реакционную смесь оставляли при перемешивании при кт в атмосфере N2 в течение ночи. Реакционную смесь разбавляли солевым раствором и дважды экстрагировали CH2Cl2. Неочищенный продукт очищали с помощью колоночной хроматографии, элюируя циклогексаном: EtOAc (0-40% EtOAc), в результате чего получали целевое соединение. ЖХ-МС (метод В) Rt = 1,47 мин, m/z = 493,0 [М+Н]+. 1Н ЯМР (400 МГц, ДМСО) δ [м.д.]: 9,04 (с, 1H), 8,4 (с, 1H), 8,20 (дд, J=1,6 Гц, J=8,8 Гц, 1H), 7,69-7,71 (м, 1H), 7,58-7,62 (м, 1H), 7,52 (д, J=2 Гц, 2H), 7,4 (т, J=1,6 Гц, 1H), 6,79-6,97 (м, 4H), 4,49 (т, J=4,4 Гц, 2H), 3,74 (т, J=4,4 Гц, 2H), 3,19 (с, 6Н).

















Пример 6.1
4-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-морфолино-пиридо[3,2-с1]пиримидин-7-карбоксамид

К суспензии этил-6-гидроксипиримидин-4-карбоксилата (5,03 г, 28,74 ммоль) в ДМФА (25 мл) в атмосфере N2 добавляли 1,3-дихлор-5,5-диметилгидантоин (3,48 г, 17,3 ммоль). Смесь перемешивали в течение ночи при кт. Реакционную смесь распределяли между водой (200 мл) и EtOAc (100 мл), затем экстрагировали EtOAc (2×75 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме, в результате чего получали этил-5-хлор-6-гидрокси-пиримидин-4-карбоксилат. ЖХ-МС (метод A) Rt = 0,54 мин, m/z = 203,0 [М+Н]+.
К суспензии этил-5-хлор-6-гидрокси-пиримидин-4-карбоксилата (8,74 г, 28,1 ммоль) в CH3CN (100 мл) при комнатной температуре в атмосфере N2 добавляли DIPEA (6,4 мл, 36 ммоль), затем добавляли оксибромид фосфора (9,44 г, 31,28 ммоль). Полученную смесь перемешивали при кт. Реакционную смесь разбавляли CH2Cl2 (100 мл) и медленно вливали в воду (100 мл). Затем смесь экстрагировали CH2Cl2 (3×100 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме. Масло очищали с помощью колоночной хроматографии (0-10% EtOAc в циклогексане), в результате чего получали этил-6-бром-5-хлорпиримидин-4-карбоксилат. ЖХ-МС (метод A) Rt = 0,98 мин, m/z = 265,0 [М+Н]+.
К раствору этил-6-бром-5-хлор-пиримидин-4-карбоксилата (4,31 г, 14,9 ммоль) и (3,5-дихлорфенил)-бороновой кислоты (2,71 г, 14,20 ммоль) в 1,4-диоксане (55 мл) при перемешивании в атмосфере N2 добавляли K2CO3 (8,69 г, 62,9 ммоль), а затем тетракис-(трифенилфосфин)-палладий(0) (732 мг, 0,63 ммоль). Реакционную смесь дегазировали и помещали в атмосферу N2, затем нагревали до 90°С в течение 16 часов. Смесь разбавляли EtOAc (50 мл) и пропускали через Celite®. Объединенные органические фильтраты концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (0-20% EtOAc в циклогексане), в результате чего получали этил-5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбоксилат.ЖХ-МС (метод В) Rt = 1,43 мин, m/z = 331,0 [М+Н]+.
К смеси этил-5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбоксилата (2,90 г, 8,75 ммоль) в ТГФ (85 мл) и воды (30 мл) при комнатной температуре в атмосфере N2 добавляли гидроксид лития (624 мг, 25,6 ммоль). Полученную смесь нагревали до 50°С в течение 1 часа. Реакционную смесь охлаждали до кт и затем концентрировали при пониженном давлении с удалением ТГФ. Полученный раствор разбавляли водой (50 мл), затем подкисляли 2 М раствором HCl до тех пор, пока рН не становился равен 1, вызывая осаждение твердого вещества. Указанный осадок отфильтровывали и промывали водой (25 мл). Затем осадок сушили в вакууме при 50°С с получением 5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбоновой кислоты. ЖХ-МС (метод В) Rt = 0,72 мин, m/z = 303,0 [М+Н]+.
Суспензию 5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбоновой кислоты (2,49 г, 7,82 ммоль) в тионилхлориде (30 мл, 411 ммоль) нагревали до 80°С в атмосфере N2. Добавляли ДМФА (0,5 мл, 6 ммоль) и реакционную смесь полностью растворяли. Затем реакционную смесь концентрировали в вакууме, помещали в толуол (20 мл) и подвергали азеотропной перегонке (3 раза) с получением 5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонилхлорида, который использовали без дополнительной очистки.
К раствору 5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонилхлорида (2,65 г, 7,82 ммоль) в толуоле (20 мл) при комнатной температуре в атмосфере N2 добавляли NEt3 (2 мл, 14 ммоль), а затем этил-3-(диметиламино)-проп-2-еноат (1,4 мл, 9,7 ммоль). Реакционную смесь перемешивали при кт в атмосфере N2. Реакционную смесь разбавляли EtOAc (125 мл) и фильтровали через Celite®. Celite® промывали EtOAc (125 мл). Объединенные органические фильтраты концентрировали в вакууме. Остаток помещали в EtOAc (250 мл) и 2М HCl (водн., 100 мл). Водный слой экстрагировали EtOAC (125 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме, в результате чего получали этил-2-[5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонил]-3-(диметиламино)-проп-2-еноат.ЖХ-МС (метод В) Rt = 1,24 мин, m/z = 428,0 [М+Н]+. 4-метоксибензиламин (1,20 мл, 9,09 ммоль) добавляли к раствору этил-2-[5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонил]-3-(диметиламино)-проп-2-еноата (3,59 г, 6,29 ммоль) в диэтиловом эфире (25 мл) и EtOH (6 мл) при комнатной температуре в атмосфере N2 в течение 1 часа. Реакционную смесь разбавляли водой (150 мл) и экстрагировали CH2Cl2 (4×75 мл). Объединенные органические слои промывали солевым раствором, сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме, получая этил-2-[5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонил]-3-[(4-метоксифенил)-метиламино]-проп-2-еноат.Полученный материал брали без дополнительной очистки. ЖХ-МС (метод В) Rt = 1,49 мин, m/z = 520,0 [М+Н]+.
К раствору этил-2-[5-хлор-6-(3,5-дихлорфенил)-пиримидин-4-карбонил]-3-[(4-метоксифенил)-метиламино]-проп-2-еноата (4,4 г, 5,66 ммоль) в ДМФА (15 мл) при комнатной температуре в атмосфере N2 добавляли K2CO3 (2,37 г, 17,1 ммоль). Полученную смесь нагревали до 90°С в течение 24 часов. Реакционную смесь охлаждали до кт, затем вливали в воду (300 мл) и экстрагировали CH2Cl2 (3×100 мл). Объединенные органические слои промывали солевым раствором (200 мл), сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (0-5% МеОН в CH2Cl2), в результате чего получали этил-4-(3,5-дихлорфенил)-5-[(4-метоксифенил)-метил]-8-оксо-пиридо[3,2-d]пиримидин-7-карбоксилат.ЖХ-МС (метод В) Rt = 1,17 мин, m/z = 484,0 [М+Н]+.
К раствору этил-4-(3,5-дихлорфенил)-5-[(4-метоксифенил)-метил] -8-оксо-пиридо[3,2-с1]пиримидин-7-карбоксилата (1,89 г, 3,70 ммоль) в CH2Cl2 (75 мл) и ДМФА (0,5 мл) при кт в атмосфере N2 медленно добавляли оксалилхлорид (2 мл, 23,1 ммоль). Реакционную смесь нагревали с обратным холодильником при 60°С в течение 1 часа. Смесь охлаждали до кт, затем гасили добавлением насыщ. водн. раствора NaHCO3 (200 мл) и экстрагировали CH2Cl2 (3×100 мл). Объединенные органические слои объединяли, а затем концентрировали в вакууме, получая этил-8-хлор-4-(3,5-дихлорфенил)-пиридо[3,2-d]пиримидин-7-карбоксилат. ЖХ-МС (метод В) Rt = 1,52 мин, m/z = 382,0 [М+Н]+.
К раствору этил-8-хлор-4- (3,5-дихлорфенил)-пиридо[3,2-d]пиримидин-7-карбоксилата (502 мг, 0,93 ммоль) в ТГФ (10 мл, 123 ммоль) при кт в атмосфере N2 по каплям добавляли морфолин (0,17 мл, 1,9 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Затем реакционную смесь гасили насыщ. водн. раствором NaHCO3 (50 мл) и экстрагировали CH2Cl2 (3×25 мл). Объединенные органические слои сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (10-25% EtOAc в циклогексане), в результате чего получали этил-4-(3,5-дихлорфенил)-8-морфолино-пиридо[3,2-d]пиримидин-7-карбоксилат. ЖХ-МС (метод В) Rt = 1,56 мин, m/z = 433,0 [М+Н]+. К смеси этил-4-(3,5-дихлорфенил)-8-морфолино-пиридо[3,2-с1]пиримидин-7-карбоксилата (337,5 мг, 0,717 ммоль) в 1,4-диоксане (15 мл) и воде (5 мл) при кт в атмосфере N2 добавляли гидроксид лития (61,6 мг, 2,52 ммоль). Полученную смесь нагревали до 80°С. Реакционную смесь концентрировали в вакууме, а остаток помещали в воду (20 мл) и подкисляли 2 М раствором HCl. Полученный осадок отфильтровывали и промывали водой (20 мл), затем сушили в вакууме при 45°С в течение ночи, получая 4-(3,5-дихлорфенил)-8-морфолино-пиридо[3,2-с1]пиримидин-7-карбоновую кислоту. ЖХ-МС (метод В) Rt = 0,80 мин, m/z = 405,0 [М+Н]+. К суспензии 4-(3,5-дихлорфенил)-8-морфолин-пиридо[3,2-d]пиримидин-7-карбоновой кислоты (125,1 мг, 0,31 ммоль) в ТГФ (3 мл) добавляли NEt3 (0,18 мл, 1,3 ммоль), затем РуВОР (259 мг, 0,49 ммоль). Реакционную смесь перемешивали при кт в атмосфере N2. Затем к реакции добавляли 2,3-дигидро-1,4-бензоксазин-4-амин (60,5 мг, 0,40 ммоль) в ТГФ (1 мл). Смесь перемешивали в течение 22 часов при комнатной температуре. Затем смесь разбавляли солевым раствором (25 мл) и экстрагировали CH2Cl2 (3×15 мл). Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (5-40% EtOAc в циклогексане), в результате чего получали целевое соединение. ЖХ-МС (метод В) Rt = 1,38 мин, m/z = 537,0 [М+Н]+. 1H ЯМР (400 МГц, ДМСО-d6) δ [м.д.]: 10,75 (с, 1H), 9,38 (с, 1H), 8,92 (с, 1H), 8,31 (д, J=2 Гц, 2H), 7,87 (т, J=2 Гц, 1H), 7,01 (дд, J=1,2, 8 Гц, 1H), 6,85 (тд, J=1,6, 8,4 Гц, 1H), 6,69-6,78 (м, 2H), 4,38 (т, J=4,4 Гц, 2H), 3,86 (т, J=4 Гц, 4H), 3,63-3,73 (м, 6Н).
Пример 7.1
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,6-нафтиридин-3-карбоксамид

К перемешиваемому раствору 3,4-дигидро-2Н-1,4-бензоксазина в EtOH (8 мл) по каплям добавляли нитрит натрия (612 мг, 8,87 ммоль) в воде (3,2 мл) при О°С. Через 5 мин по каплям добавляли HCl (0,8 мл) и реакционную смесь оставляли при перемешивании при 0°С в течение 2 часов. К реакционной смеси по каплям добавляли NaOH (2,96 г, 74 ммоль) в воде (7,5 мл), затем дитионат натрия (4,4 г, 22,2 ммоль) при 0°С. Полученную реакционную смесь нагревали до 90°С в течение 4 часов. Реакционную смесь растворяли в EtOAc (20 мл), промывали водой (10 мл) и насыщенным солевым раствором (10 мл). Органический слой сушили над безводным Na2SO4 и концентрировали в вакууме. Неочищенное соединение очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире. ЖХ-МС (метод С) Rt = 0,89 мин, m/z = 152,36 [М+Н]+.
Смесь 3-бромпиридин-4-амина (10,0 г, 57,8 ммоль) и диэтил-2-(этоксиметилен)-пропандиоата (32,8 мл, 173 ммоль) нагревали до 120°С в течение 16 часов. Реакционную смесь оставляли при комнатной температуре, концентрировали до сухого состояния в вакууме и очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире с получением диэтил-2-[[(3-бром-4-пиридил)-амино]-метилен]-пропандиоата. ЖХ-МС (метод С) Rt = 1,71 мин, m/z = 343,19 [М+Н]+.
Раствор 2-[[(3-бром-4-пиридил)-амино]-метилен]-пропандиоата (2,8 г, 8,12 ммоль) помещали в дифениловый эфир (42 мл) и нагревали до 250°С в течение 30 мин. Реакционной смеси давали остыть до кт и добавляли петролейный эфир (50 мл). Полученное твердое соединение фильтровали, промывали петролейным эфиром (50 мл) и сушили в вакууме с получением этил-8-бром-4-гидрокси-1,6-нафтиридин-3-карбоксилата. ЖХ-МС (метод С) Rt = 1,16 мин, m/z = 297,11 [М+Н]+.
Этил-8-бром-4-гидрокси-1,6-нафтиридин-3-карбоксилат (4,3 г, 14,5 ммоль) добавляли к POCl3 (43 мл) и нагревали до 90°С в течение 6 часов. Реакционной смеси давали остыть до кт и концентрировали при пониженном давлении. Остаток разбавляли EtOAc (100 мл), промывали насыщ. водн. раствором NaHCO3 (3×30 мл) и солевым раствором (20 мл). Органический слой сушили над безводным Na2SO4 и концентрировали при пониженном давлении. Неочищенный продукт очищали с помощью колоночной хроматографии, элюируя 0-20% EtOAc в петролейном эфире. ЖХ-МС (метод С) Rt = 2,30 мин, m/z = 315,09 [М+Н]+.
К перемешиваемому раствору этил-8-бром-4-хлор-1,6-нафтиридин-3-карбоксилата (3 г, 9,5 ммоль) в ТГФ (60 мл) добавляли морфолин (4,1 г, 47,5 ммоль) при кт и перемешивали в течение 30 мин. Реакционную смесь концентрировали досуха при пониженном давлении. Сырой продукт очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире, с получением этил-8-бром-4-морфолино-1,6-нафтиридин-3-карбоксилата. ЖХ-МС (метод С) Rt = 1,65 мин, m/z = 366,24 [М+Н]+.
К перемешиваемому раствору этил-8-бром-4-морфолино-1,6-нафтиридин-3-карбоксилата (0,8 г, 2,18 ммоль) и (3,5-дихлорфенил)-бороновой кислоты (1,04 г, 5,46 ммоль) в 1,4-диоксане/воде (16/4 мл) добавляли Cs2CO3 (2,13 г, 6,55 ммоль), затем тетрафторбораттри-трет-бутилфосфония (0,127 г, 0,43 ммоль), и дегазировали при помощи N2 в течение 10 мин. PdCl2(dppf) (0,16 г, 0,21 ммоль) добавляли к реакционной смеси и нагревали до 90°С в течение 16 часов. Реакционную смесь растворяли в EtOAc (30 мл), промывали водой (15 мл) и солевым раствором (10 мл). Органический слой сушили над безводным Na2SO4 и концентрировали досуха. Неочищенный продукт очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире. ЖХ-МС (метод С) Rt = 2,33 мин, m/z = 432,30 [М+Н]+.
К перемешиваемому раствору этил-8-(3,5-дихлорфенил) -4-морфолино-1,6-нафтиридин-3-карбоксилата (0,55 г, 1,27 ммоль) в EtOH : ТГФ : воде (1:1:1, 9 мл) добавляли LiOH⋅H2O (0,16 г, 3,81 ммоль) при кт и нагревали до 70°С в течение 4 часов. Реакционной смеси давали остыть до кт, а затем концентрировали с удалением растворителей. рН доводили до 6-7 с использованием 0,5 М водного раствора HCl в условиях охлаждения (0°С) и экстрагировали EtOAc (3×30 мл). Объединенные органические слои сушили над безводным Na2SO4 и концентрировали досуха. ЖХ-МС (метод С) Rt = 2,15 мин, m/z = 403,9 [М+Н]+.
К перемешиваемому раствору 8-(3,5-дихлорфенил) -4-морфолино-1,6-нафтиридин-3-карбоновой кислоты (0,3 г, 0,74 ммоль) и 2,3-дигидро-1,4-бензоксазин-4-амина (134 мг, 0,89 ммоль) в ДМФА (5 мл) добавляли HATU (0,34 г, 0,89 ммоль) и DIPEA (0,38 г, 2,2 ммоль) при кт. Полученную реакционную смесь нагревали до 60°С в течение 16 часов. Реакционную смесь гасили путем добавления воды (5 мл) и экстрагировали EtOAc (3×15 мл). Объединенные органические слои промывали солевым раствором, сушили над безводным Na2SO4 и концентрировали при пониженном давлении. Сырой продукт очищали с помощью колоночной хроматографии, элюируя 0-100% EtOAc в петролейном эфире с получением целевого соединения. ЖХ-МС (метод D) Rt = 2,12 мин, m/z = 536,24 [М+Н]+. 1Н ЯМР (400 МГц, ДМСО-d6) δ [м.д.]: 10,75 (с, 1H), 9,03 (с, 1H), 8,84 (с, 1H), 7,77 (д, J=2 Hz, 2H), 7,72 (т, J=2 Hz, 1H), 7,03 (м, 1H), 6,85 (тд, J=2, 7,2 Hz, 1H), 6,72-6,78 (м, 2H), 4,38 (т, J=4,4 Hz, 2H), 3,92 (т, J=3,6 Hz, 4H), 3,69 (уш. с, 2H), 3,39 (т, J=4 Hz, 4Н).
Пример 8.1
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-4-морфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамид

К перемешиваемому раствору 8-бром-1Н-3,1-бензоксазин-2,4-диона (0,8 г, 3,3 ммоль) и этил-3-оксобутаноата (0,86 г, 6,61 ммоль) в ДМАА (5 мл) добавляли NaOH (0,132 г, 3,3 ммоль). Полученную реакционную смесь перемешивали в течение 12 ч при 100°С. Смесь гасили путем добавления воды (200 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический слой промывали солевым раствором (50 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение растирали с н-пентаном (30 мл) с получением этил-8-бром-4-гидрокси-2-метил-хинолин-3-карбоксилата. ЖХ-МС (метод С) Rt = 1,54 мин, m/z = 310,22 [М+Н]+.
К перемешиваемому раствору этил-8-бром-4-гидрокси-2-метил-хинолин-3-карбоксилата (0,3 г, 0,96 ммоль) в EtOH (5 мл) добавляли KOH (0,814 г, 14,5 ммоль) при кт и нагревали до 80°С в течение 24 ч. Реакционной смеси давали остыть до кт и концентрировали. рН остатка доводили до 1-2 с использованием водного раствора 2Н HCl и осажденное твердое вещество фильтровали, промывали водой (10 мл) и сушили с получением 8-бром-4-гидрокси-2-метил-хинолин-3-карбоновой кислоты. ЖХ-МС (метод С) Rt = 1,46 мин, m/z = 280,05 [М-Н]-.
Смесь 8-бром-4-гидрокси-2-метил-хинолин-3-карбоновой кислоты (0,2 г, 0,7 ммоль) и POCl3 (10 мл) нагревали до 90°С в течение 2 ч. Реакционной смеси давали остыть до кт и концентрировали при пониженном давлении с получением 8-бром-4-хлор-2-метил-хинолин-3-карбонилхлорида.
К перемешиваемому раствору 2,3-дигидро-1,4-бензоксазин-4-амина (0,188 г, 1,25 ммоль) в ТГФ (3 мл) добавляли DIPEA (0,342 г, 2,5 ммоль) и охлаждали до 0-5°С. К реакционной смеси добавляли раствор 8-бром-4-хлор-2-метил-хинолин-3-карбонил хлорид а (0,2 г, 0,62 ммоль) в 2 мл ТГФ и оставляли при перемешивании при кт. Реакционную смесь гасили добавлением воды (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический слой промывали солевым раствором (50 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии с получением 8-бром-4-хлор-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-хинолин-3-карбоксамида. ЖХ-МС (метод С) Rt = 2,12 мин, m/z = 432,06 [М+Н]+. К перемешиваемому раствору 8-бром-4-хлор-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-хинолин-3-карбоксамида (0,25 г, 0,57 ммоль) и морфолина (0,5 г, 5,77 ммоль) в ТГФ (5 мл) добавляли Et3N (0,116 г, 1,15 ммоль). Реакционную смесь перемешивали при кт в течение 16 ч. Реакционную смесь гасили добавлением воды (100 мл) и экстрагировали EtOAc (2×50 мл). Объединенный органический слой промывали солевым раствором, сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение растирали с диэтиловым эфиром (30 мл) с получением 8-бром-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-4-морфолино-хинолин-3-карбоксамида. ЖХ-МС (метод С) Rt = 2,25 мин, m/z = 483,49 [М+Н]+.
К перемешиваемому раствору 8-бром-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-4-морфолино-хинолин-3-карбоксамида (0,3 г, 0,62 ммоль) и (2,3,5-трифторфенил)-бороновой кислоты (0,656 г, 3,72 ммоль) в 1,4-диоксане (12 мл):воде (3 мл), добавляли Cs2CO3, реакционную смесь дегазировали N2 в течение 10 мин с последующим добавлением [(t-Bu)3PH]BF4 (0,036 г, 0,12 ммоль) и PdCl2(dppf) (0,045 г, 0,06 ммоль) и нагревали до 90°С в течение 16 ч. Реакционную смесь гасили путем добавления воды (200 мл) и экстрагировали EtOAc (2×100 мл). Объединенный органический слой промывали солевым раствором (50 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии и элюировали 10% EtOAc в петролейном эфире, получая Пример 8.1. ЖХ-МС (метод С) Rt = 2,29 мин, m/z = 535,22 [М+Н]+. 1H ЯМР (400 МГц, ДМСО) δ [м.д.]: 10,57 (с, 1H), 8,31 (д, J=7,6 Гц, 2H), 7,79 (д, J=6,4 Гц, 2H), 7,69 (т, J=8,4 Гц, 1H), 7,59-7,61 (м, 1H), 7,20-7,21 (м, 1H), 6,99 (д, J=6,8 Гц, 1H), 6,85 (тд, J=1,6, 6,8 Гц, 1H), 6,74-6,79 (м, 2H), 4,39 (т, J=4 Гц, 2H), 3,87 (т, J=4 Гц, 4H), 3,72 (уш. с, 2H), 3,32 (уш. с, 4H), 2,55 (с, 3 Н).
Пример 8.2
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-2-(трифторметил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамид

Стадия 1: К перемешиваемому раствору 7-броминдолин-2,3-диона (2,5 г, 11,06 ммоль) и этил-4,4,4-трифторбут-2-иноата (1,83 г, 11,06 ммоль) в ДМФА (15 мл) добавляли Na2CO3 (2,34 г, 22,12 ммоль), а затем трет-бутилгидропероксид (ТБГП, 0,99 г, 11,06 ммоль). Реакционную смесь перемешивали в течение 2 ч при кт. Реакционную смесь гасили путем добавления воды (20 мл) и экстрагировали этилом (2×30 мл). Объединенный органический слой промывали солевым раствором (3×30 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире с получением этил-8-бром-4-гидрокси-2-(трифторметил)-хинолин-3-карбоксилата. ЖХ-МС (метод С) Rt = 2,29 мин, m/z = 364,14 [М+Н]+.
Стадия 2: К перемешиваемому раствору этил-8-бром-4-гидрокси-2-(трифторметил)-хинолин-3-карбоксилата (1,75 г, 4,80 ммоль) в EtOH (10 мл) добавляли KOH (5,39 г, 96,12 ммоль) при комнатной температуре и нагревали до 90°С в течение 24 ч. Реакционной смеси давали остыть до кт и концентрировали. рН остатка доводили до 1-2 с использованием водного раствора 2H HCl и осажденного твердого вещества фильтровали, промывали водой (10 мл), диэтиловым эфиром (20 мл) и сушили с получением 8-бром-4-гидрокси-2- (трифторметил)-хинолин-3-карбоновой кислоты. ЖХ-МС (метод С) Rt = 1,79 мин, m/z = 335,99 [М+Н]+.
Стадия 3: Смесь 8-бром-4-гидрокси-2- (трифторметил)-хинолин-3-карбоновой кислоты (1 г, 2,97 ммоль) и POCl3 (10 мл) нагревали до 90°С в течение 2 ч. Реакционной смеси давали остыть до кт и концентрировали при пониженном давлении с получением 8-бром-4-хлор-2-(трифторметил)-хинолин-3-карбонилхлорида.
Стадия 4: К перемешиваемому раствору 2,3-дигидро-1,4-бензоксазин-4-амина (0,8 г, 5,36 ммоль) в ТГФ (5 мл) добавляли DIPEA и охлаждали до 0-5°С. К реакционной смеси добавляли раствор 8-бром-4-хлор-2- (трифторметил)-хинолин-3-карбонилхлорида (1 г, 2,68 ммоль) в 4 мл ТГФ и оставляли при перемешивании при кт в течение 16 ч. Реакцию гасили добавлением воды (20 мл) и экстрагировали EtOAc (2×30 мл). Объединенные органические слои промывали солевым раствором (20 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии, элюируя 0-100% EtOAc в петролейном эфире, с получением 8-бром-4-хлор-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-(трифторметил)-хинолин-3-карбоксамида. ЖХ-МС (метод С) Rt = 2,23 мин, m/z = 486,04 [М+Н]+.
Стадия 5: К перемешиваемому раствору 8-бром-4-хлор-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-(трифторметил)-хинолин-3-карбоксамида (0,844 г, 1,73 ммоль) в ТГФ (6 мл) добавляли мор фол ин (1,5 мл, 17,34 ммоль) при комнатной температуре и перемешивали в течение 16 ч. Реакционную смесь концентрировали досуха. Неочищенный продукт очищали с помощью колоночной хроматографии, элюируя 0-50% EtOAc в петролейном эфире, в результате чего получали 8-бром-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-2-(трифторметил)-хинолин-3-карбоксамид. ЖХ-МС (метод С) Rt = 2,18 мин, m/z = 537,08 [М+Н]+.
Стадия 6: К перемешиваемому раствору 8-бром-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-2-(трифторметил)-хинолин-3-карбоксамида и (2,3,5-трифторфенил)-бороновой кислоты (0,687 г, 3,91 ммоль) в 1,4-диоксане (15 мл) : воде (5 мл) добавляли Cs2CO3 (0,636 г, 1,95 нмоль). Реакционную смесь дегазировали с помощью N2 в течение 10 минут с последующим добавлением [(t-Bu)3PH]BF4 (0,075 г, 0,26 ммоль) и PdCl2(dppf) (0,095, 0,13 ммоль). Реакционную смесь нагревали до 90°С в течение 16 ч. Реакционную смесь гасили путем добавления воды (150 мл) и экстрагировали EtOAc (3×50 мл). Объединенный органический слой промывали солевым раствором (30 мл), сушили над Na2SO4 и концентрировали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии, элюируя 0-14% EtOAc в петролейном эфире, в результате чего получали Пример 8.2 в виде твердого вещества белого цвета. ЖХ-МС (метод С) Rt=2,27 мин, m/z=589,39 [М+Н]+. 1H ЯМР (400 МГц, ДМСО) δ [м.д.]: 10,62 (с, 1Н), 8,45 (д, J=8,4 Гц, 2Н), 8,03 (д, J=7,2 Гц, 2Н), 7,94 (т, J=8,4 Гц, 1Н), 7,65-7,67 (м, 1Н), 7,29-7,31 (м, 1Н), 7,03 (д, J=7,6 Гц, 1Н), 6,83-6,87 (м, 1Н), 6,76-6,80 (м, 2Н), 4,39 (т, J=3,6 Гц, 2Н), 3,87 (уш. с, 4Н), 3,64 (уш. с, 2Н), 3,43 (уш. с, 4Н).
Экспериментальные данные по соединениям в таблицах:












Соединения формулы (I) согласно настоящему изобретению пригодны для лечения и/или подавления, в частности, гельминтов, при которых эндопаразитарные нематоды и трематоды могут быть причиной серьезных заболеваний млекопитающих и птицы. Типичными нематодами для данного показания являются: Filariidae, Setariidae, Haemonchus, Trichostrongylus, Ostertagia, Nematodirus, Cooperia, Ascaris, Bunostonum, Oesophagostonum, Charbertia, Trichuris, Strongylus, Trichonema, Dictyocaulus, Capillaria, Heterakis, Toxocara, Ascaridia, Oxyuris, Ancylostoma, Uncinaria, Toxascaris и Parascaris. Трематоды включают, в частности, семейство Fasciolideae, особенно Fasciola hepatica.
Некоторые паразиты видов Nematodirus, Cooperia и Oesophagostonum заражают кишечный тракт животного-хозяина, в то время как другие виды Haemonchus и Ostertagia паразитирует в желудке, а Dictyocaulus паразитируют в легочной ткани. Паразиты семейств могут быть обнаружены во внутренней клеточной ткани ив органах, например, в сердце, кровеносных сосудах, лимфатических сосудах и подкожной ткани. Особенно заметным паразитом является сердечный червь собак, Dirofilaria iminitis.
Паразиты, которых можно лечить и/или подавлять при помощи соединений формулы (I), также включают паразитов из класса Cestoda (ленточные черви), например, семейств Mesocestoidae, особенно рода Mesocestoides, в частности М. lineatus; Dipylidiidae, особенно Dipylidium caninum, Joyeuxiella spp., в частности Joyeuxiella pasquali, и Diplopylidium spp., и Taeniidae, особенно Taenia pisformis, Taenia cervi, Taenia ovis, Taeneia hydatigena, Taenia multiceps, Taenia taeniaeformis, Taeniaserialis и Echinococcus spp., особенно Taneia hydatigena, Taenia ovis, Taenia multiceps, Taenia serialis; Echinococcus grulosus и Echinococcus multocilularis.
Кроме того, соединения формулы (I) подходят для лечения и/или подавления патогенных паразитов человека. Из них типичными представителями, которые появляются в пищеварительном тракте, являются представители рода Ancylostoma, Necator, Ascaris, Strongyloides, Trichinella, Capillaria, Trichuris и Enterobius. Соединения согласно настоящему изобретению также направлены против паразитов рода Wuchereria, Brugia, Onchocerca и Loa из семейства Dracunculus и паразитов рода Strongyloides и Trichinella, которые, в частности, инфицируют желудочно-кишечный тракт.
Конкретным паразитом, подлежащим лечению и/или подавлению с помощью соединений согласно настоящему изобретению, является сердечный червь (Dirofilaria immitis). Конкретными субъектами такого лечения являются собаки и кошки.
Соединения согласно настоящему изобретению можно вводить отдельно или в форме композиции. На практике соединения согласно настоящему изобретению обычно вводят в форме композиций, то есть в смеси по меньшей мере с одним приемлемым вспомогательным веществом. Пропорции и характер любого приемлемого вспомогательного вещества (веществ) определяются свойствами выбранного соединения согласно настоящему изобретению, выбранным путем введения и стандартной практикой в области ветеринарии и фармацевтики.
В одном из вариантов реализации настоящего изобретения предложены композиции, содержащие: соединение согласно настоящему изобретению и по меньшей мере одно приемлемое вспомогательное вещество.
При осуществлении такого лечения и/или подавления соединение согласно настоящему изобретению можно вводить в любой форме и путем, которые делают соединение биодоступным. Соединения согласно настоящему изобретению можно вводить различными способами, в том числе перорально, в частности, в виде таблеток и капсул. Соединения согласно настоящему изобретению можно вводить парентеральными путями, в частности, путем ингаляции, подкожно, внутримышечно, внутривенно, внутриартериально, трансдермально, интраназально, ректально, вагинально, окклюзионно, местно, сублингвально и буккально, внутрибрюшинно, внутриадипозально, интратекально и путем местной доставки, например, с помощью катетера или стента.
Специалист в данной области техники может легко выбрать подходящую форму и способ введения в зависимости от конкретных характеристик выбранного соединения, расстройства или состояния, подлежащего лечению, стадии расстройства или состояния и других соответствующих обстоятельств. Фармацевтические композиции согласно настоящему изобретению могут быть введены субъекту, например, в форме таблеток, капсул, облаток, пакетов, пастилок, лепешек, эликсиров, мазей, трансдермальных пластырей, аэрозолей, ингалянтов, суппозиториев, жидких пероральных форм, растворов и суспензий.
Термин «приемлемое вспомогательное вещество» относится к веществам, обычно применяемым при получении ветеринарных и фармацевтических композиций, и должен быть чистым и нетоксичным в применяемых количествах. Как правило, они представляют собой твердый, полутвердый или жидкий материал, который в совокупности может служить носителем или средой для активного ингредиента. Некоторые примеры приемлемых вспомогательных веществ содержатся в Remington's Pharmaceutical Sciences и Handbook of Pharmaceutical Excipients и включают разбавители, носители, носители, мазевые основания, связующие вещества, дезинтеграты, смазывающие вещества, скользящие агенты, подсластители, ароматизаторы, гелевые основания, матрицы с замедленным высвобождением, стабилизирующие средства, консерванты, растворители, суспендирующие средства, буферные агенты, эмульгаторы, красители, пропелленты, покрывающие средства и другие.
В одном из вариантов реализации композиция адаптирована для перорального введения, такая как таблетка, капсула или жидкий состав, например, раствор или суспензия, адаптированные для перорального введения. В одном из вариантов реализации композиция адаптирована для перорального введения, например, жевательный состав, адаптированный для перорального введения. В еще одном варианте реализации композиция представляет собой жидкий или полутвердый состав, например, раствор, суспензию или пасту, адаптированный для парентерального введения.
Конкретные композиции для применения у субъектов при лечении и/или подавлении нематод/гельминтов включают растворы; эмульсии, включая классические эмульсии, микроэмульсии и самоэмульгирующиеся композиции, которые являются безводными органическими, предпочтительно масляными, композициями, которые образуют эмульсии, вместе с биологическими жидкостями, при добавлении в организм субъекта; суспензии (жидкие пероральные формы); наливные составы; пищевые добавки; порошки; таблетки, включая шипучие таблетки; болюсы; капсулы, включая микрокапсулы; и жевательные лакомства. В частности, формы композиции представляют собой таблетки, капсулы, пищевые добавки или жевательные лакомства.
Композиции согласно настоящему изобретению получают способом, хорошо известным в области ветеринарии и фармацевтики, и они включают по меньшей мере одно из соединений согласно настоящему изобретению в качестве активного ингредиента. Количества соединения согласно настоящему изобретению могут варьироваться в зависимости от его конкретной формы и могут удобно составлять от 1% до около 50% от массы единичной дозированной формы. Настоящие фармацевтические композиции предпочтительно составлены в виде единичной дозированной формы, каждая доза, как правило, содержит от примерно 0,5 мг до примерно 100 мг соединений согласно настоящему изобретению. Для влияния на дозировку лечения можно принимать одну или более единичных дозированных форм.
В одном из вариантов реализации настоящего изобретения также предложен способ лечения паразитов, включающий: введение нуждающемуся в этом субъекту эффективного количества соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
В одном из вариантов реализации настоящего изобретения также предложен способ подавления паразитов, включающий: введение нуждающемуся в этом субъекту эффективного количества соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
В одном из вариантов реализации настоящего изобретения также предложен способ лечения или подавления паразитов, включающий: приведение в контакт среды субъекта с эффективным количеством соединения формулы (I) или его соли, причем способ необязательно дополнительно содержит эффективное количество по меньшей мере одного дополнительного активного соединения.
Таким образом, изобретение обеспечивает применение соединений согласно настоящему изобретению в качестве лекарственного средства, в том числе для получения лекарственного средства. В одном из вариантов реализации настоящего изобретения предложено получение лекарственного средства, содержащего соединение формулы (I) или его соль, для лечения паразитов. В одном из вариантов реализации настоящего изобретения предложено производство лекарственного средства, содержащего соединение согласно настоящему изобретению или его соль, для подавления паразитов.
Термины «лечащий», «лечить» или «лечение» включают, без ограничения, ограничение, замедление, остановку, уменьшение, облегчение, обращение вспять прогрессирования или тяжести существующего симптома или предотвращение расстройства, патологического состояния или заболевания. Например, инфицирование взрослым сердечным червем можно лечить путем введения соединения согласно настоящему изобретению. Лечение может быть применено или введено терапевтически.
Термины «подавление», «подавляющий» или «подавляемый» относятся, без ограничения, к уменьшению, снижению или уменьшению риска возникновения симптома, расстройства, патологического состояния или заболевания и защите животного от симптома, расстройства, патологического состояния или заболевания. Подавление может относиться к терапевтическому, профилактическому или превентивному введению. Хорошо известно, что инфицирование личинкой или незрелым сердечным червем могут быть бессимптомными, а инфицирование зрелыми паразитами является симптоматическим и/или изнурительным. Следовательно, например, инфицирование сердечным червем можно было бы подавлять путем воздействия на личинок или незрелого паразита, предотвращая развитие инфекции до стадии инфицирования зрелыми паразитами.
Таким образом, применение соединений согласно настоящему изобретению для лечения и/или подавления паразитов, в частности гельминтов, в числе которых эндопаразитарные нематоды и трематоды, относится к применению соединений согласно настоящему изобретению для воздействия на различные формы паразитов на протяжении всего их жизненного цикла, независимо от того, проявляется ли у субъекта симптом, включая заболеваемость или смертность, и независимо от фазы (фаз) паразитарного заражения.
В настоящем документе термин «введение субъекту» включает, но не ограничивается перечисленным, кожное, подкожное, внутримышечное, слизистое, подслизистое, трансдермальное, пероральное или интраназальное введение. Введение может включать инъекцию или местное введение.
Термины «субъект» и «пациент» включают людей и животных, млекопитающих, не являющихся людьми, таких как собаки, кошки, мыши, крысы, морские свинки, кролики, хорьки, коровы, лошади, овцы, козы и свиньи. Следует понимать, что более конкретным субъектом является человек. Кроме того, более конкретным субъектом являются домашние млекопитающие питомцы или животные-компаньоны, такие как собаки и кошки, а также мыши, морские свинки, хорьки и кролики.
Термин «эффективное количество» относится к количеству, которое дает желаемую пользу субъекту и включает введение как для лечения, так и для подавления. Количество будет варьироваться от индивидуума к индивидууму и будет зависеть от ряда факторов, включая общее физическое состояние индивидуума и тяжесть основной причины состояния, подлежащего лечению, сопутствующее лечение и количество соединения согласно изобретению, применяемого для поддержания желаемого ответа на благоприятном уровне.
Эффективное количество может быть легко определено лечащим врачом, как специалистом в данной области техники, с использованием известных методик и путем наблюдения за результатами, полученными в аналогичных обстоятельствах. При определении эффективного количества, дозы, лечащий врач учитывает ряд факторов, включая, без ограничения: вид пациента; его размер, возраст и общее состояние здоровья; конкретное состояние, расстройство, инфекцию или заболевание; степень или поражение или тяжесть состояния, расстройства или заболевания, ответ отдельного пациента; конкретное вводимое соединение; способ введения; характеристики биодоступности вводимого препарата; выбранный режим дозирования; применение сопутствующего лекарственного средства; и другие соответствующие обстоятельства. Ожидается, что эффективное количество согласно настоящему изобретению, лекарственная доза, будет находиться в диапазоне от 0,5 мг до 100 мг. Конкретные количества могут быть определены специалистом в данной области техники. Хотя эти дозы основаны на массе субъекта, имеющего массу от около 1 кг до около 20 кг, диагност сможет определить подходящую дозу для субъекта, масса которого выходит за пределы этого диапазона массы. Ожидается, что эффективное количество согласно настоящему изобретению, лекарственная доза, будет находиться в диапазоне от 0,1 мг/кг до 10 мг/кг субъекта. Ожидается, что режим дозирования будет ежедневным, еженедельным или ежемесячным.
Соединения согласно настоящему изобретению могут быть объединены с одним или более другими активными соединениями или терапиями для лечения одного или более расстройств, заболеваний или состояний, включая лечение паразитов, для лечения которых они показаны. Соединения согласно настоящему изобретению можно вводить одновременно, последовательно или по отдельности в комбинации с одним или более соединениями или способами лечения паразитов и других расстройств.
Например, при применении для лечения паразитов, включая сердечного червя, соединение согласно настоящему изобретению может быть объединено с макроциклическим лактоном, таким как ивермектин, моксидектин или оксим милбемицина, или с имидаклопридом. Конкретные комбинации для лечения паразитов включают соединение согласно настоящему изобретению и ивермектин. Другая конкретная комбинация для лечения паразитов включает соединение согласно настоящему изобретению и оксим милбемицина.
Таким образом, следует понимать, что композиции и способы согласно настоящему изобретению, необязательно, содержат эффективное количество по меньшей мере одного дополнительного активного соединения.
Активность соединений как антипаразитических средств может быть определена различными способами, включая способы in vitro и in vivo.
Пример А
Микрофилярии сердечных червей собак
Микрофилярии D. immitis выделяли путем фильтрования из крови инфицированного донора и оставляли для инкубации в соответствующих средах. Исследуемые соединения разбавляли в ДМСО и добавляли в 96-луночный планшет, содержащий паразитов. Планшеты инкубировалии в течение требуемого времени, а подвижность оценивали с помощью системы визуализации с ЖК-камерой. Влияние сыворотки проверяли путем добавления в испытание до 20% фетальной бычьей сыворотки. Процентные значения ингибирования подвижности получали относительно среднего значения для лунок, содержащих только ДМСО.
В этом испытании, например, следующие соединения из примеров синтеза показали ЕС50<0,1 μг/мл: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 3.1, 3.2, 3.3, 3.4, 4.1, 5.1, 5.2, 5.3, 5.4, 5.6, 5.7, 5.8, 5.10, 5.11, 5.12, 5.13, 5.14, 5.15, 5.16, 5.17, 5.18, 5.19, 5.20, 5.21, 5.22, 5.23, 5.23, 5.24, 6.1 и 7.1.
Пример В1
Желудочно-кишечный тракт жвачных животных (испытание на развитие личинок Н. contortus (Hc LDA)):
Яйца Н.с., выделенные из фекалий ягнят, оставляли для выведения в течение ночи. Испытуемые соединения разбавляли в ДМСО и добавляли в 96-луночный планшет, содержащий соответствующую среду. Личинки Н.с. добавляли в каждую лунку и инкубировали планшеты в течение желаемого времени. Подвижность оценивали с помощью системы визуализации с помощью ЖК-камеры. Процентные значения ингибирования подвижности получали относительно среднего значения для лунок, содержащих только ДМСО.
В этом испытании, например, следующие соединения из примеров синтеза показали ЕС50<1 μг/мл: 2.1, 2.2, 2.3, 2.4, 2.5, 2.6, 2.8, 3.1, 3.2, 3.3, 3.4, 4.1, 5.1, 5.2, 5.3, 5.4, 5.6, 5.7, 5.8, 5.11, 5.12, 5.13, 5.14, 5.15, 5.16, 5.17, 5.18, 5.19, 5.20, 5.21, 5.22, 5.23, 5.23, 5.24, 6.1 и 7.1.
Пример В2
Другие нематоды in vitro
Caenorhabditis elegans (Се): Анализ развития С. elegans (Се DA) измеряет влияние соединений на развитие нематод. Яйца С. elegans помещали в 384-луночный планшет вместе с пищей (Е. coli) и обработкой, приготовленной в ДМСО. Планшеты инкубировали при 25°С в течение 48 часов, чтобы обеспечить развитие нематод вплоть до стадии L4. Эффект соединений измеряли как снижение подвижности. Эффективность выражали в % снижения подвижности по сравнению с отрицательными контролями.
В этом испытании, например, следующие соединения из примеров синтеза показали ЕС90<1 μг/мл: 5.23, 5.35, 5.36, 5.41, 5.45, 5.47, 5.48, 5.49, 5.54, 5.55, 5.56, 5.57, 5.58, 5.59, 5.60, 5.61, 5.62, 5.63.
Пример С
Желудочно-кишечные нематоды
Песчанок (Meriones unguiculatus), искусственно заражали через желудочный зонд личинками третьего возраста Т. colubriformis и Н. contortus. Затем перорально обрабатывали исследуемым соединением, приготовленным, например, в ДМСО/ПЭГ 2/1, на 6-й день после инфицирования в дозе в диапазоне от 1×3 мг/кг до 1×32 мг/кг. Через три дня после обработки проводили эвтаназию и вскрытие песчанок для выделения H. contortus из желудка и Т. colubriformis из тонкой кишки. Эффективность выражали в % снижения количества червей по сравнению с группой, получавшей плацебо, с использованием формулы Эббота.
Соединения из примеров 3.3, 5.2, 5.3, 5.4, 5.19, 5.23 и 5.47 были на > 80% эффективными против Hc и Тс. Соединения из примеров 3.1, 2.3 и 5.6 были на > 80% эффективным против Hc.
Пример D
Филяриальные нематоды
Модель Av: Птиц, которым подкожно вводили инфицированные личинки A. viteae, впоследствии обрабатывали исследуемым препаратом, составленным, например, в ДМСО/ПЭГ 2/1, путем перорального введения через желудочный зонд в дозе от 1×3 мг/кг до 5×32 мг/кг (одна доза в день в течение 5 последовательных дней). При вскрытии через 12 недель после инфицирования эффективность выражали в виде % снижения количества червей по сравнению с группой, получавшей плацебо, с использованием формулы Эббота.
Соединения из примеров 2.6, 3.4, 5.4, 5.6, 5.7, 5.8, 5.19 и 5.20 были на > 80% эффективным против Av.
Пример Е
Модель L.s.
Мышей (BALB/c) экспериментально инфицировали личинками 3-й стадии L. sigmodontis либо путем подкожной инъекции, либо путем воздействия инфицированных клещей. Обработку проводили исследуемым препаратом, приготовленным в ДМСО/ПЭГ в соотношении 2/1, путем перорального введения через желудочный зонд или подкожной инъекции в дозе в диапазоне от 1×3 мг/кг (однократная доза) до 5×32 мг/кг (одна доза в день в течение 5 последовательных дней). При вскрытии через 35-37 дней после инфицирования производили подсчет червей в брюшине и плевральной полости. Эффективность выражали в % снижения количества червей по сравнению с группой, получавшей плацебо, с использованием формулы Эббота. Соединения из примеров 3.3, 5.3, 5.41, 5.47, 5.48 и 5.56 были на > 80% эффективными против L.s.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ АНТИГЕЛЬМИНТНЫЕ ХИНОЛИН-3-КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ | 2017 |
|
RU2772283C2 |
| НОВЫЕ АЗАХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2018 |
|
RU2773290C2 |
| НОВЫЕ АНТИГЕЛЬМИНТНЫЕ СОЕДИНЕНИЯ | 2019 |
|
RU2828007C2 |
| СОЕДИНЕНИЯ С НЕМАТОЦИДНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2608217C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА | 2020 |
|
RU2839897C2 |
| НОВЫЕ ПИРАЗОЛПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2017 |
|
RU2769448C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2794894C2 |
| ПРОИЗВОДНЫЕ ИНДОЛ-3-ИЛ-КАРБОНИЛ-СПИРО-ПИПЕРИДИНА | 2006 |
|
RU2420529C2 |
| БИЦИКЛИЧЕСКИЕ ПИРИДИНЫ И АНАЛОГИ В КАЧЕСТВЕ МОДУЛЯТОРОВ СИРТУИНА | 2010 |
|
RU2550821C2 |
| НОВЫЕ ХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2019 |
|
RU2792933C2 |
Изобретение относится к области химии и фармацевтики и раскрывает соединение формулы (I) или его ветеринарно или фармацевтически приемлемую соль, композиции на их основе для лечения и/или подавления эндопаразитов, а также относится к их применению при получении лекарственного средства для лечения эндопаразитов, для лечения или подавления сердечного червя. В общей формуле (I) G выбран из группы, состоящей из  ; и
; и  ; Q выбран из группы, состоящей из (i) 6- или 10-членного арила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C1-C4 галогеноалкила, C1-C4 алкокси, C3-C6 циклоалкила, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(C3-C6 циклоалкила), -N(C1-C4 алкила)(C3-C6 циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила, где 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы O, S и N, и где атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, если позволяет валентность, замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила; (ii) 5-10-членного гетероарила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из группы O, S и N, и при этом атомы углерода 5-10-членного гетероарила необязательно замещены 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, бензилокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеноалкила и -SO2C1-C4 галогеноалкила, и любой N в гетероариле, если это допускает валентность, необязательно замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила, C3-C6 циклоалкила; (iv) 6- или 10-членного арилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила; (v) 6- или 10-членного арилтиоокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила; и (vi) 5-10-членного гетероарилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6 циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила. Остальные значения радикалов указаны в п. 1 формулы изобретения. 5 н. и 21 з.п. ф-лы, 15 пр.
; Q выбран из группы, состоящей из (i) 6- или 10-членного арила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C1-C4 галогеноалкила, C1-C4 алкокси, C3-C6 циклоалкила, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(C3-C6 циклоалкила), -N(C1-C4 алкила)(C3-C6 циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила, где 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы O, S и N, и где атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, если позволяет валентность, замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила; (ii) 5-10-членного гетероарила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из группы O, S и N, и при этом атомы углерода 5-10-членного гетероарила необязательно замещены 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, бензилокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеноалкила и -SO2C1-C4 галогеноалкила, и любой N в гетероариле, если это допускает валентность, необязательно замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила, C3-C6 циклоалкила; (iv) 6- или 10-членного арилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила; (v) 6- или 10-членного арилтиоокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила; и (vi) 5-10-членного гетероарилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6 циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила. Остальные значения радикалов указаны в п. 1 формулы изобретения. 5 н. и 21 з.п. ф-лы, 15 пр.

1. Соединение формулы (I)

где n равен 0 или 1;
X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой CR6;
X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N;
X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой N; и X6 представляет собой CR6;
X1 представляет собой N; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N;
X1 представляет собой CR1; X2 представляет собой N; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N;
X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой N; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N;
X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой N; и X6 представляет собой N; или
X1 представляет собой N; X2 представляет собой CR2; X3 представляет собой N; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N;
G выбран из группы, состоящей из
 ; и
; и  ;
;
M представляет собой O;
Y1 выбран из группы, состоящей из CR8R9, O и S;
Y2 выбран из группы, состоящей из CR8R9, O и S;
где по меньшей мере одна из групп Y1 или Y2 представляет собой CR8R9;
Z1 представляет собой CR11;
Z2 представляет собой CR11;
Z3 представляет собой CR11;
Z4 представляет собой CR11;
R1 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH и циано;
R2 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH и циано;
R3 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH и циано;
R4 выбран из группы, состоящей из галогена, циано, -CHO, гидроксила, C1-C4 алкила, C2 -C4 алкенила, C2-C4 алкинила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкоксизамещенного-C1-C4 алкила, бензила, необязательно замещенного 1-5 атомами галогена, C 1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -N(C1-C4 алкил)(4-7-членный гетероциклоалкил), где 4-7-членный гетероциклоалкил содержит 1, 2 или 3 гетероатома, выбранных из группы, состоящей из N, O и S, и необязательно содержит карбонил с образованием лактама или лактона, -NH(4-7-членный гетероциклоалкил), где 4-7-членный гетероциклоалкил содержит 1, 2 или 3 гетероатома, выбранных из группы, состоящей из N, O и S, и необязательно содержит карбонил с образованием лактама или лактона, -N(C1-C4 алкил)(C1-C4 алкокси), -C(O)NH(C1-C4 алкил), -C(O)N(C1-C4 алкил)2, -C(O)N(C1-C4 алкил)(4-7-членный гетероциклоалкил), где 4-7-членный гетероциклоалкил содержит 1, 2 или 3 гетероатома, выбранных из группы, состоящей из N, O и S, и необязательно содержит карбонил с образованием лактама или лактона, -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -B(OR15)(OR16), где R15 каждый раз выбран из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила, R16 каждый раз выбран из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила, или R15 и R16 вместе с атомами кислорода, к которым они присоединены, образуют 5-7-членное кольцо, которое необязательно замещено 1-4 C1-C4 алкилом; 6- или 10-членного арила; моноциклического гетероцикла, выбранного из группы 4-7-членного гетероциклоалкила, где 4-7-членный гетероциклоалкил содержит 1, 2 или 3 гетероатома, выбранных из группы, состоящей из N, O и S, и необязательно содержит карбонил с образованием лактама или лактона, 5-членного гетероарила, содержащего по меньшей мере один атом азота, посредством которого 5-членное гетероарильное кольцо соединено с остальной частью молекулы, и 6-членного гетероарила, содержащего по меньшей мере один атом азота; каждое из арильного, гетероциклоалкильного и гетероарильного колец в R4 необязательно замещено 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси и -NH2;
при этом C3-C6 циклоалкильные и гетероциклоалкильные кольца в R4 необязательно замещены спирогруппой, при этом указанная спирогруппа представляет собой 3-6-членный циклоалкил или 4-6-членный гетероциклоалкил, содержащий 1, 2 или 3 гетероатома, независимо выбранных из N, S или O, при этом указанная спирогруппа необязательно замещена 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси и -NH2;
R5 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH, циано, C1-C4 алкила и C1-C4 галогеноалкила;
R6 выбран из группы, состоящей из водорода, галогена, гидроксила, -SH и циано;
R7 выбран из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила;
R8 каждый раз независимо выбран из группы, состоящей из водорода, фтора и C1-C4 алкила;
R9 каждый раз независимо выбран из группы, состоящей из водорода, фтора и C1-C4 алкила;
R11 каждый раз независимо выбран из группы, состоящей из водорода, галогена, гидроксила, циано и -NH2;
Q выбран из группы, состоящей из
(i) 6- или 10-членного арила, необязательно замещенного 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C1-C4 галогеноалкила, C1-C4 алкокси, C3-C6 циклоалкила, -NH2, -NH(C1-C4 алкила), -N(C1-C4 алкила)2, -NH(C3-C6 циклоалкила), -N(C1-C4 алкила)(C3-C6 циклоалкила), -NHSO2(C1-C4 алкила), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеноалкила и -SO2C1-C4 галогеноалкила, где 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы O, S и N, и где атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, если позволяет валентность, замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила;
(ii) 5-10-членного гетероарила, содержащего 1, 2 или 3 гетероатома, независимо выбранных из группы O, S и N, и при этом атомы углерода 5-10-членного гетероарила необязательно замещены 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, бензилокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеноалкила и -SO2C1-C4 галогеноалкила, и любой N в гетероариле, если это допускает валентность, необязательно замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила, C3-C6 циклоалкила;
(iv) 6- или 10-членного арилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 -галогеноалкила и -SO2C1-C4 галогеноалкила;
(v) 6- или 10-членного арилтиоокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6 циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила; и
(vi) 5-10-членного гетероарилокси, необязательно замещенного 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
2. Соединение по п. 1, где X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой CR5; и X6 представляет собой N; или его ветеринарно или фармацевтически приемлемая соль.
3. Соединение по п. 1, где X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой N; и X6 представляет собой N; или его ветеринарно или фармацевтически приемлемая соль.
4. Соединение по п. 1, где X1 представляет собой CR1; X2 представляет собой CR2; X3 представляет собой CR3; X4 представляет собой CR4; X5 представляет собой N; и X6 представляет собой CR6; или его ветеринарно или фармацевтически приемлемая соль.
5. Соединение по любому из пп. 1-4, где
Q представляет собой 6- или 10-членный арил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, C1-C4 алкила, C1-C4 галогеноалкила, C1-C4 алкокси, C3-C6 циклоалкила, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4 галогеноалкила и -SO2C1-C4 галогеноалкила;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
6. Соединение по любому из пп. 1-4, где
Q представляет собой 6-членный арил, необязательно замещенный 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, C1-C4 алкила, C1-C4 галогеноалкила, C1 -C4 алкокси, C3-C6 циклоалкила, -NH2, -NH (C1-C4 алкил), -N(C1-C 4 алкил) 2, -NH(C3-C 6 циклоалкил), -N(C1-C4 алкил)(C3-C 6 циклоалкил), -NHSO2 (C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеноалкила и -SO2C1-C4 галогеноалкила, при этом 6-членный арил конденсирован с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы O, S и N, при этом атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2 и любой N в гетероциклоалкиле замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
7. Соединение по любому из пп. 1-4, где
Q представляет собой 5-10-членный гетероарил, содержащий 1 или 2 гетероатома, выбранных из группы O, S и N, и при этом атомы углерода гетероарила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, -OH, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероариле необязательно замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
8. Соединение по любому из пп. 1-4, где
Q представляет собой 4-7-членный гетероциклоалкил, содержащий 1 или 2 гетероатома, выбранных из группы O, S, N, при этом гетероциклоалкил необязательно бензоконденсирован, при этом атомы углерода гетероциклоалкила или необязательно бензоконденсированного гетероциклоалкила необязательно замещены 1, 2, 3 или 4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидрокси, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкила, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле необязательно замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
9. Соединение по любому из пп. 1-8, где n равно 1; или его ветеринарно или фармацевтически приемлемая соль.
10. Соединение по любому из пп. 1-9, где Y1 представляет собой CR8R9 и Y2 представляет собой O; или его ветеринарно или фармацевтически приемлемая соль.
11. Соединение по любому из пп. 1-10, где R4 выбран из группы, состоящей из C1-C4 алкила, C3-C6 циклоалкила, -N(C1-C4 алкил)2 и 4-7-членного гетероциклоалкила, где 4-7-членный гетероциклоалкил содержит 1, 2 или 3 гетероатома, выбранных из группы, состоящей из N, O и S, и необязательно содержит карбонил с образованием лактама или лактона; или его ветеринарно или фармацевтически приемлемая соль.
12. Соединение по любому из пп. 1-11, где
G представляет собой
 ; и
; и
M представляет собой O;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
13. Соединение по любому из пп. 1-11, где
G представляет собой
 ; и
; и
M представляет собой O;
или ветеринарно или фармацевтически приемлемая соль указанного соединения.
14. Соединение формулы (I) по п. 1 или его ветеринарно или фармацевтически приемлемая соль, имеющее формулу (Ia-5)

где R1, R4 и Q являются такими, как определено в п. 1.
15. Соединение формулы (Ia-5) по п. 14 или его ветеринарно или фармацевтически приемлемая соль, где R1 представляет собой водород, галоген или циано.
16. Соединение формулы (Ia-5) по п. 14 или 15, или его ветеринарно или фармацевтически приемлемая соль, где R1 представляет собой водород или фтор.
17. Соединение формулы (Ia-5) по любому из пп. 14-16 или его ветеринарно или фармацевтически приемлемая соль, где R4 представляет собой 4-морфолино или диметиламино.
18. Соединение формулы (Ia-5) по любому из пп. 14-17 или его ветеринарно или фармацевтически приемлемая соль, где Q представляет собой 6-членный арил, необязательно замещенный 1, 2, 3, 4 или 5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, гидроксила, C1-C4 алкила, C1-C4 галогеноалкила, C1-C4 алкокси, C3-C6 циклоалкила, -NH2, -NH(C1-C4 алкил), -N(C1-C4 алкил)2, -NH(C3-C6 циклоалкил), -N(C1-C4 алкил)(C3-C6-циклоалкил), -NHSO2(C1-C4 алкил), -SC1-C4 алкила, -S(O)C1-C4 алкила, -SO2C1-C4 алкила, -S(O)C1-C4-галогеноалкила и -SO2C1-C4 галогеноалкила, при этом 6- или 10-членный арил необязательно слит с 4-7-членным гетероциклоалкилом, содержащим 1 или 2 гетероатома, выбранных из группы O, S и N, и при этом атомы углерода гетероциклоалкила необязательно замещены 1, 2 или 3 заместителями, независимо выбранными из группы галогена, циано, нитро, гидроксила, оксо, C1-C4 алкила, C3-C6 циклоалкила, C1-C4 галогеноалкил, C1-C4 алкокси, -NH2, -NH(C1-C4 алкил) и -N(C1-C4 алкил)2, и любой N в гетероциклоалкиле, при наличии валентности, замещен заместителем, выбранным из группы, состоящей из водорода, C1-C4 алкила и C3-C6 циклоалкила.
19. Соединение формулы (Ia-5) по любому из пп. 14-18 или его ветеринарно или фармацевтически приемлемая соль, где Q выбран из:


20. Соединение по п. 1, выбранное из группы, состоящей из:
N-[8-(3,5-дихлорфенил)-4-(диметиламино)-3-хинолил]-2,3-дигидро-1,4-бензоксазин-4-карбоксамида (Пример 1.1);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-1,7-нафтиридин-3-карбоксамида (Пример 2.1);
8-(3,5-дихлорфенил)-N-(3,4-дигидро-2H-хинолин-1-ил)-4-(диметиламино)-1,7-нафтиридин-3-карбоксамида (Пример 2.2);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,7-нафтиридин-3-карбоксамида (Пример 2.3);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-1,5-нафтиридин-3-карбоксамида (Пример 3.1);
5-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-1-(диметиламино)-нафталин-2-карбоксамида (Пример 4.1); и
8-(3,5-дихлорфенил)-N-(2,3-дигидро-4H-бензо[b][1,4]оксазин-4-ил)-4-(диметиламино)-хинолин-3-карбоксамида; (Пример 5.1);
или ветеринарно или фармацевтически приемлемая соль любого из вышеуказанных соединений.
21. Соединение по п. 1, выбранное из группы, состоящей из:
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,5-трифторфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.4);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-[метокси-(метил)-амино]-8-(2,3,5-трифторфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.5);
8-[3-хлор-5-(трифторметил)-фенил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,7-нафтиридин-3-карбоксамида (Пример 2.6);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3-дихлорфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.7);
8-(3,5-дихлор-4-фтор-фенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,7-нафтиридин-3-карбоксамида (Пример 2.8);
8-(5-хлор-3-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,7-нафтиридин-3-карбоксамида (Пример 2.9);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-тиоморфолино-8-(2,3,5-трифторфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.10);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(1,1-диоксо-1,4-тиазинан-4-ил)-8-(2,3,5-трифторфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.11);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(3,4,5-трифторфенил)-1,7-нафтиридин-3-карбоксамида (Пример 2.12);
8-(2,3-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-1,5-нафтиридин-3-карбоксамида (Пример 3.2);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,5-нафтиридин-3-карбоксамида (Пример 3.3);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,5-трифторфенил)-1,5-нафтиридин-3-карбоксамида (Пример 3.4);
8-(2,3-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.2);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.3);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.4);
8-(5-хлор-3-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.5);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида; (Пример 5.6);
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.7);
8-(3,5-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.8);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-пиримидин-5-ил-хинолин-3-карбоксамида (Пример 5.9);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-тиоморфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.10);
8-[2-хлор-6-(трифторметил)-4-пиридил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.11);
8-(2,6-дихлор-4-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.12);
8-(3,5-дихлор-2-фторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.13);
8-(5-хлор-2-фтор-3-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.14);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(1,1-диоксо-1,4-тиазинан-4-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.15);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,4,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.16);
8-(6-хлорпиразин-2-ил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.17);
8-(4,5-дихлор-3-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.18);
8-(5-хлор-2,3-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.19);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,4,5-тетрафторфенил)-хинолин-3-карбоксамида (Пример 5.20);
8-(4-хлор-5-фтор-3-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.21);
8-[4-хлор-6-(трифторметил)-2-пиридил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.22);
8-(3,5-дихлор-2,4-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.23);
N-индолин-1-ил-4-морфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.24);
8-(4,6-дихлор-2-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.25);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(6-фторпиразин-2-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.26);
8-[2-хлор-6-(трифторметил)-пиримидин-4-ил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.27);
8-(6-хлор-5-фтор-2-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.28);
8-(6-хлор-3-фтор-2-пиридил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.29);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(6-этоксипиразин-2-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.30);
4-(азетидин-1-ил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.31);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-пирролидин-1-ил-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.32);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-[2-метоксиэтил-(метил)-амино]-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.33);
4-[бис-(2-метоксиэтил)-амино]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.34);
7-циано-8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.35);
4-циклопропил-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.36);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(3-фторазетидин-1-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.37);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(3-гидроксиазетидин-1-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.38);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-оксазолидин-3-ил-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.39);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(2-окса-6-азаспиро[3.3]гептан-6-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.40);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-8-(3,4,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.41);
4-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-морфолино-пиридо[3,2-d]пиримидин-7-карбоксамида (Пример 6.1); и
8-(3,5-дихлорфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-1,6-нафтиридин-3-карбоксамида (Пример 7.1);
или ветеринарно или фармацевтически приемлемая соль любого из вышеуказанных соединений.
22. Соединение по п. 1, выбранное из группы, состоящей из:
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-изоксазолидин-2-ил-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.42);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-[1-(2,2,2-трифторэтил)-пиразол-4-ил]-хинолин-3-карбоксамида (Пример 5.43);
8-(2,6-дихлорпиримидин-4-ил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.44);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-тетрагидропиран-4-ил-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.45);
4-[ацетил-(метил)-амино]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.46);
8-(3,5-дихлор-2-фтор-фенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.47);
8-(3,5-дихлор-2,4-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.48);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,6-трифтор-4-пиридил)-хинолин-3-карбоксамида (Пример 5.49);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-(4-фтор-2,6-диметил-фенил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.50);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-8-[4-этилсульфанил-6-(трифторметил)-пиримидин-2-ил]-4-морфолино-хинолин-3-карбоксамида (Пример 5.51);
8-[4-бензилокси-6-(трифторметил)-пиримидин-2-ил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.52);
[3-(2,3-дигидро-1,4-бензоксазин-4-илкарбамоил)-8-(2,3,5-трифторфенил)-4-хинолил]-бороновой кислоты (Пример 5.53);
8-(3,5-дихлор-2,4-дифтор-фенил)-7-фтор-N-индолин-1-ил-4-морфолино-хинолин-3-карбоксамида (Пример 5.54);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(1-метоксиэтил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.55);
8-(3,5-дихлор-2,4-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(диметиламино)-7-фтор-хинолин-3-карбоксамида (Пример 5.56);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-(2,3,5,6-тетрафторфенил)-хинолин-3-карбоксамида (Пример 5.57);
4-циклопропил-8-(3,5-дихлор-2,4-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-хинолин-3-карбоксамида (Пример 5.58);
8-[3,5-бис-(трифторметил)-фенил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.59);
8-(5-хлор-2,3-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.60);
8-[3-хлор-5-(трифторметил)-фенил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.61);
8-(3,5-дихлор-2,4-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-[метокси-(метил)-амино]-хинолин-3-карбоксамида (Пример 5.62);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-8-[4-(трифторметил)-фенил]-хинолин-3-карбоксамида (Пример 5.63);
8-[3,5-дихлор-4-(трифторметил)-фенил]-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.64);
8-(3-хлор-2,5,6-трифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-7-фтор-4-морфолино-хинолин-3-карбоксамида (Пример 5.65);
8-(3-хлор-5-циано-фенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.66);
8-(3-циано-2,5-дифторфенил)-N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-хинолин-3-карбоксамида (Пример 5.67);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-(2,2,2-трифтор-1-метил-этил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 5.68);
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-2-метил-4-морфолино-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 8.1); и
N-(2,3-дигидро-1,4-бензоксазин-4-ил)-4-морфолино-2-(трифторметил)-8-(2,3,5-трифторфенил)-хинолин-3-карбоксамида (Пример 8.2);
или ветеринарно или фармацевтически приемлемая соль любого из вышеуказанных соединений.
23. Композиция для лечения и/или подавления эндопаразитов, содержащая терапевтически эффективное количество соединения по любому из пп. 1-22 или его ветеринарно или фармацевтически приемлемой соли и по меньшей мере один приемлемый носитель.
24. Применение соединения по любому из пп. 1-22 или его ветеринарно или фармацевтически приемлемой соли при получении лекарственного средства для лечения эндопаразитов.
25. Применение соединения по любому из пп. 1-22 или его ветеринарно или фармацевтически приемлемой соли при получении лекарственного средства для лечения сердечного червя.
26. Применение соединения по любому из пп. 1-22 или его ветеринарно или фармацевтически приемлемой соли при получении лекарственного средства для подавления сердечного червя.
| WO 2017178416 A1, 19.10.2017 | |||
| WO 2019002132 A1, 03.01.2019 | |||
| WO 2018087036 A1, 17.05.2018 | |||
| WO 1999029318 A1, 17.06.1999 | |||
| ПРОИЗВОДНЫЕ ХИНОЛОН- И НАФТИРИДОН-КАРБОНОВОЙ КИСЛОТЫ В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫХ ИЗОМЕРОВ, ИХ СОЛИ | 1994 |
|
RU2114832C1 |
Авторы
Даты
2024-11-13—Публикация
2020-06-05—Подача