Изобретение относится к остеоиндуктивным костно-пластическим материалам на основе термотропного хитозан-глицерофосфатного гидрогеля, наполненного высокопористыми частицами из хитозана или полилактида, с импрегнированным rhBMP-2, для использования в регенеративной медицине, стоматологии, челюстно-лицевой хирургии, пластической хирургии и прочих областях медицины, где существует потребность в восполнении дефектов костной ткани или увеличении объема костей.
В стоматологии, челюстно-лицевой хирургии, ортопедии и травматологии при проведении костных пластик существует потребность в материалах, способных эффективно восполнять утраченную костную ткань. Помимо высокой биологической эффективности, важным требованием является удобство при работе с материалом: превосходные манипуляционные свойства, отсутствие необходимости применения вспомогательных конструкций типа титановых сеток, фиксирующих винтов и барьерных мембран (Кузнецова и др, 2017).
Существующие костно-пластические препараты можно разделить на две большие группы: ординарные и активированные (Деев и др., 2015). Ординарные костно-пластические материалы представляют собой матрицу алло-, ксеногенного или синтетического происхождения, состав которой обуславливает форму препарата: костная крошка, цемент, пластилин, паста, губка. Каждая форма имеет свои преимущества и недостатки. Так, пластилин является наиболее удобной для моделирования субстанцией. Однородная плотная структура и способность к прилипанию позволяет использовать его без дополнительных армирующих конструкций, таких как титановые сетки, винты или мембраны, для обеспечения направленной костной регенерации (Deshmukh et al., 2014; Lakshmiganthan et al., 2012; Uehara et al., 2015). Однако пластилин проигрывает цементам по способности отверждаться в ране и не обеспечивает надлежащую стабильность смоделированной формы (Педаченко и Кущаев, 2001). Кроме того, в отличие от костной крошки у зарегистрированных препаратов в форме пластилина поверхность представляет собой сплошную структуру, что не позволяет сосудам врастать в толщу материала и обеспечивать его резорбцию и миграцию остеогенных клеток-предшественников с образованием костной ткани во всем его объеме (Verneetal., 2015).
Активированные материалы представляют собой сочетание ординарных матриц и остеоиндукторов, в качестве которых могут применяться генетические конструкции (вирусы и плазмиды) и вещества с белково-пептидной структурой (факторы роста), действие которых направлено на рецепторы, активирующие сигнальные пути остеогенной дифференцировки клеток. Генетические конструкции в современных препаратах не используются в связи с определенными трудностями: плазмиды являются малоэффективными, а использование вирусных векторов для доставки гена сопровождается рядом проблем, которые пока не решены в этой отрасли науки в целом, например, риск инсерционного мутагенеза. В связи с этим наиболее безопасным и эффективным на настоящий момент следует считать использование факторов роста (Triplett et al., 2009; van Hout et al., 2011).
К настоящему времени существует ряд зарегистрированных и разрешенных для клинического применения материалов, содержащих остеоиндуктивные рекомбинантные белковые факторы, - это INFUSE Bonegraft («Medtronic», США) с ВМР-2; ОР-1 («StrykerBiotech», США) с ВМР-7; GEM21S и Augmentbonegraft («BioMimeticTherapeuticsInc.», США) с PDGF-BB; i-FactorPutty («Cerapedics», США) с белком Р-15, являющимся лигандом для интегринов α2β1, экспрессируемых клетками остеобластического дифферона и др. (DuscherandShiffman, 2020; Деев и др., 2015). Данные препараты являются более эффективными по сравнению с ординарными материалами, но их стоимость слишком высока. Кроме того, они не обладают способностью своевременно создавать пик концентрации остеоиндуктора к началу фазы активной дифференцировки клеток-предшественников остеобластов. В связи с этим большая часть дорогостоящего остеоиндуктора расходуется впустую. Для эффективной регенерации костной ткани своевременная доставка факторов роста к прогениторным и камбиальным клеткам является одной из важнейших задач (Leknes et al., 2008; Whang et al., 2000). Среди изученных белков-остеоиндукторов наибольшим остеогенным потенциалом обладает ВМР-2 - инъекция даже его малых доз под кожу способна индуцировать эктопический неоостеогенез (Carragee et al., 2011). Однако внесение чистого ВМР-2 в костную рану не имеет высокой эффективности: в первые сутки после операции происходит воспаление, которое препятствует его действию, после чего последовательно развиваются процессы миграции и пролиферации остеогенных клеток-предшественников, и только затем возникает необходимость воздействия на них белка для индуцирования остеогенной дифференцировки.
Проблема своевременной доставки остеоиндуктора может быть решена разными способами. Один из подходов заключается в инкапсулировании остеоиндуктора в костно-пластическом материале. Для этой задачи лучше всего подходят биоразлагаемые полимеры. Их синтетическая природа подразумевает полный контроль над процессом их получения, что позволяет добиться прогнозируемой динамики биодеградации и, как следствие, высвобождения, заключенных в них веществ (Boyan et al., 1999; Shue et al., 2012). Однако белковые структуры не переносят нагревания и воздействия агрессивных химических агентов, в связи с чем существует сложность сохранения активности факторов роста при включении их в полимер, а ряд технологических ограничений позволяет использовать только узкую группу полимеров для инкапсулирования белков (El Bialy et al., 2017). Так, существует апробированная в нашей стране технология включения rhBMP-2 в частицы у полилактида/полигликолида (Minaeva et al., 2019; А.V. Vasilyev et al., 2019). Однако в процессе биодеградации полилактиды и полигликолиды закисляют среду, что негативно сказывается на процессе неоостеогенеза из-за возникающего в зоне их имплантации воспаления (Hutmacher, 2000; Shueetal., 2012; Vogesetal., 2002). Для решения этой задачи можно использовать композицию из различных полимеров, которая позволит усиливать положительные свойства одного полимера и нивелировать негативные эффекты другого. Для придания матрице материала уникальных манипуляционных свойств и способности к термоотверждению с образованием пор наилучшим образом подходит хитозановый гель, представляющий собой смесь хитозана и β-глицерофосфата. Применение компонентов в определенном соотношении позволяет добиться термоотверждения гидрогеля после внесения в рану при 37°C (Cho et al., 2005). Отвержденный хитозановый гель имеет пористую структуру, что обеспечивает врастание в него сосудов и миграцию клеток. Однако биодеградация хитозанового геля в слабощелочной среде организма вызывает определенные сложности - для повышения ее эффективности хитозановому гелю требуется акцепция протонов. В связи с этим использование композиции на основе полилактидов/полигликолидов и хитозанового гидрогеля является перспективным (Yaretal., 2015; Кузнецова и др., 2017).
Композиция из полилактида/полигликолида и хитозана позволила бы создать матрицу материала, обладающую способностью к термоотверждению с образованием пор, биодеградацией без воспаления и программируемым высвобождением остеоиндукторов. Коммерческие аналоги материала с такими свойствами в настоящее время не существуют, в связи с чем его разработка является перспективным направлением, позволяющим решить актуальные проблемы практической медицины.
Известны композиционные материалы для заполнения костных дефектов в виде губок на основе хитозана с добавлением карбоната аммония (RU 2356581 С1, дата публикации 27.05.2009), трикальций фосфата (патент RU 2376019 С2, дата публикации 20.12.2009) и хитозан-желатина с добавлением порошка или гранул октакальциевого фосфата (патент RU 2412711 С1, дата публикации 27.02.2011). Недостатками подобных материалов являются отсутствие остеоиндуктивных свойств, неудобные манипуляционные свойства и деформируемость, которые ограничивают применение материалов в области дефектов сложной анатомической формы.
Известна инъекционная смесь на основе хитозанов с разной степенью деацетилирования, образующая в условиях физиологического рН и температуры 37°С гидрогель (US 8153612 В2, дата публикации 10.04.2012). Недостатком данной композиции являются низкие прочностные свойства композиции, что препятствует ее применению в качестве материала для дефектов костной ткани, подвергающихся механическим нагрузкам в послеоперационном периоде.
Известны композиционные материалы для заполнения костных дефектов на основе хитозан-альгинатного комплекса в виде геля с добавлением хондроитинсерной кислоты, гиалуроновой кислоты, гепарина, сывороточного фактора роста крупного рогатого скота (патент RU 2494721 С1, дата публикации 10.10.2013) или гидроксиапатита и порошка фосфата магния с добавлением водной суспензии 2-амино-5-гуанидиновалериановой кислоты (RU 2494721 С1, дата публикации 10.10.2013). Несмотря на лучшую по сравнению с губками способность к заполнению костных полостей, материал характеризуется способностью к набуханию и отсутствием выраженных остеоиндуктивных свойств (Jin et al., 2012; Li et al., 2005). Также по данным исследований, ксеногенный гидроксиапатит, входящий в состав второй композиции, зачастую не подвергается полной резорбции в организме (Hallman et al., 2001; Yildirim et al., 2000).
Известна композиция, содержащая сополимер хитозана и полиэтиленгликоля, которая представляет собой жидкость при температуре ниже 25°С и гель при температуре выше 35°C (Huang et al., 2014).Однако данная композиция характеризуется быстрым лавинообразным высвобождением белка в объеме 10-67% в первые пять часов. Через 70 часов высвобождение полностью прекращается. В связи с этим использование данного материала для доставки белка-остеоиндуктора в зону регенерации костной ткани невозможно из-за короткого периода высвобождения белка во время фазы острого воспаления, что может приводить к существенному снижению его эффективности (Huang et al., 2014).
Наиболее близким к изобретению являются композиции на основе: (1) веществ, вызывающих ангиогенез, таких как FGF, VEGF, TGF, хитозана, PDGF, PGF, ангиогенина, ИЛ-8, GCSF и кондиционированных сред клеточных культур, (2) материала, состоящего из деминерализованного костного матрикса, недекальцинированного костного матрикса с добавлением или без добавления гиалуроновой кислоты, (3) матрицы выбранной из группы материалов, представленной губчатой костью, хитозаном, соединением хитозан-белок или хитин-белковых волокон, (4) материала в виде геля, выбранного из группы: хитозан, производного хитозана и имидазола или метилпиролидинона, или карбодиимида, или глутаральдегида, альгинат, альгинат-хитозан, смесь альгината с хитозаном или его производными, гиалуроновая кислота, смесь гиалуроновой кислоты с хитозаном или его производными (патент US 8563040 В2, дата публикации 22.10.2013). К недостатку данного изобретения следует отнести использование большого количества компонентов, что не позволяет контролировать в достаточной мере физико-механические и биологические свойства композиции, а также сроки ее резорбции.
Основные недостатки костно-пластических материалов из хитозана связаны, во-первых, с неудовлетворительными физико-механическими свойствами, которые не позволяют материалу сопротивляться напряжению мягких тканей и сохранять свою форму после имплантации. Во-вторых, аналоги не стимулируют эффективной неоостеогенез в связи с отсутствием в их составе остеоиндукторов.
Материалы в виде губок и гидрогелей обладают низкими прочностными свойствами и подвергаются деформации под давлением окружающих тканей. Это препятствует сохранению формы и матриксных свойств в послеоперационном периоде. В связи с этим материалы в виде губок, и частиц требуют применения дополнительных армирующих конструкций в виде сеток или мембран, что создает дополнительные сложности при их применении в клинической практике.
Аналоги костно-пластических материалов из хитозанане содержат высокоактивных остеоиндукторов в виде белков или генных конструкций, что обуславливает заживление дефектов в неполном объеме и в течение длительного периода времени.
Преодолеть физико-механические недостатки материалов можно за счет сочетаний компонентов, обладающих различными свойствами. Так, использование в качестве основы материала гидрогеля позволит обеспечить материалу пластичность и способность к in situ моделированию. Использование наполнителя в виде губок или частиц может обеспечить прочностные и вязко-упругие свойства материала.
Для придания материалам остеоиндуктивных свойств могут быть использованы генные конструкции или остеоиндуктивные факторы. Так как на настоящем этапе применение генетических конструкций затруднено в связи с проблемами их безопасности и эффективности, то оптимальным является использование остеоиндуктивных факторов белковой природы, которые показали свою эффективность (Деев и др., 2015). Однако следует учитывать, что в послеоперационный период в результате посттравматического воспаления активность таких факторов снижается, что приводит к необходимости применения повышенных концентраций остеоиндукторов, что может провоцировать осложнения в виде гиперостоза или опухолей (Carragee et al., 2011). В связи с этим для повышения эффективности в состав материала должен входить носитель, обладающий пролонгированной кинетикой высвобождения остеоиндуктивных факторов.
В настоящем изобретении в качестве основы использован хитозановый гидрогель, полученный с помощью β-глицерофосфата, с температурой отверждения 37°С (патент СА 221300 А1, дата публикации 04.02.1999), способный заполнять анатомические пространства различной формы. Для улучшения прочностных и манипуляционных характеристик в составе композиции использованы высокопористые полилактидные частицы, которые обладают высокими показателями модуля упругости и позволяют моделировать материал. Остеоиндуктивные свойства достигаются за счет контролируемого медленного высвобождения из частиц полилактида высокоэффективного белка-остеоиндуктора rhBMP-2 (Vasilyev et al., 2019). После 3 суток, соответствующих фазе острого воспаления, частицы полилактида продолжают высвобождать импрегнированный в них белок, который воздействует на приходящие в область вмешательства клетки-предшественники остеобластов и стимулирует неоостеогенез. Кроме того, структура материала способствует его своевременному замещению костной тканью. Отвержденный наполненный хитозановый гидрогель обладает пористой структурой и характеризуется быстрой резорбцией, что способствует его замещению коллагеновыми волокнами и проникновению микрососудов в толщу материала. Полилактидные частицы различного размера (рис. 1) характеризуются высокой пористостью, их структура поверхности и диаметр пор способствуют прикреплению и пролиферации клеток. Полилактидные частицы обладают контролируемым сроком резорбции, который соответствует периоду новообразования костной ткани.
Технической задачей изобретения является разработка активированного отверждаемого костно-пластического материала на основе хитозанового гидрогеля и частиц наполнителя, обладающего выраженными остеоиндуктивными свойствами и биосовместимостью.
Техническим результатом изобретения является создание композиционного костно-пластического материала, имеющего в составе:
1. Отверждаемую композиция на основе хитозанового гидрогеля, полученного смешиванием в пропорции 2:1 раствора хитозана с концентрацией 2,2 масс. % в 0,1 М уксусной кислоте и водного раствора β-глицерофосфата с концентрацией 35 масс. % и высокопористыми полилактидными частицами с rhBMP-2 с концентрацией частиц относительно гидрогелевой матрицы 6-16 масс. %;
2. Отверждаемую композиция на основе хитозанового гидрогеля, полученная смешиванием в пропорции 2:1 раствора хитозанас концентрацией 2,2 масс. % в 0,1 М уксусной кислоте и водного раствора β-глицерофосфата с концентрацией 35 масс. % с хитозановыми частицами с rhBMP-2 с концентрацией частиц относительно гидрогелевой матрицы 6-16 масс. %.
Технический результат, достигается следующим способом изготовления, включающим в себя этапы:
1) (вариант 1) Импрегнация rhBMP-2 в высокопористые полилактидные частицы размером 50-200 мкм (рис. 1), путем промачивания частиц раствором в буфере rhBMP-2 и поочередным набором и сбросом вакуума, с последующей заморозкой и лиофилизацией;
2) (вариант 2) изготовление хитозановых частиц, сшитых глутаровым альдегидом, диаметром 0,9-4 мм с включенным в структуру rhBMP-2, полученных заморозкой капель раствора хитозана с глутаровым альдегидом и rhBMP-2 в жидком азоте с дальнейшей сублимационной сушкой. Получение хитозанового гидрогеля смешением в пропорции 2:1 раствора хитозана с концентрацией 2,2 масс. % в 0,1 М уксусной кислоте и водного раствора β-глицерофосфата с концентрацией 50 масс. %; 3) соединение компонентов материала.
Для импрегнации rhBMP-2 используют высокопористые (98%) частицы полилактида со средним диаметром 50-200 мкм (фиг. 1), полученные методом сублимационной сушки. Импрегнация проводится путем промачивания частиц раствором в буфере rhBMP-2 и пятикратным набором до 10-2 бар и сбросом вакуума, с последующим замораживанием и лиофилизацией. Замораживание и лиофилизация приводят к адсорбции белка на поверхности и в порах полилактидных частиц.
Хитозан - производное линейного полисахарида, макромолекулы которого состоят из случайно связанных β-(1-4)-D-глюкозаминовых звеньев и N-ацетил-D-глюкозамина. Для изготовления частиц и гидрогеля используют порошки хитозана с молекулярной массой от 80 кг/моль и степенью деацетилирования до 85%. Из литературы известно, что снижение степени деацетилирования хитозана приводит к улучшению биологических свойств композиции (Huang et al., 2004; Younes et al., 2016), поэтому рекомендуется использовать материалы с низкой степенью деацетилирования.
Частицы хитозана, сшитые глутаровым альдегидом (1 масс. % от сухого остатка полимера), получают сублимационной сушкой 2 масс. % водного раствора хитозана в 0,3 М уксусной кислоте с добавлением rhBMP-2. Диаметр хитозановых частиц составляет 0,9-4 мм (фиг. 2).
Изготовление хитозанового гидрогеля проводится в стерильных условиях в ламинарном боксе. В раствор хитозана с концентрацией 2,2 масс. %) в 0,1 М уксусной кислоте, при температуре 4°С каплям добавляют стерильный охлажденный 35 масс. % водный раствор β-глицерофосфата (SigmaAldrichcat. 50020) при постоянном перемешивании. Отверждение гидрогелей происходит при температуре 37-40°С в течение 2 часов (фиг. 3)
Полученные компоненты смешивают. Для этого в хитозановый гидрогель добавляют высокопористые полилактидные или хитозановые частицы импрегнированные rhBMP-2. Массовая доля частиц составляет - 6-16%.
Термоотверждаемый и остеоиндуктивный костно-пластический материал на основе композиции хитозанового гидрогеля и частиц из полилактида или хитозана с импрегнированным костным морфогенетическим белком-2 (ВМР-2) (фиг. 4).
Композиция моделируемого и отверждаемого резорбируемого материала для замещения дефектов костей скелета на основе наполнителя в виде высокопористых полилактидных или хитозановых частиц, импрегнированных rhBMP-2, и хитозанового гидрогеля, состоящего из раствора хитозана в уксусной кислоте и водного раствора β-глицерофосфата может быть использована для восстановления дефектов костей. При этом, охлажденную до плюс 4 °С композицию, вносят в костный дефект с последующим его отверждением до 4-15 минут, дальнейшим ушиванием раны и экспозицией в зоне имплантации не менее одного месяца.
Техническим результатом заявленного способа применения является то, что при имплантации охлажденной композиции удается достичь её равномерного распределения с последующим отверждением в ране, что в дальнейшем обеспечивает контролируемое полное восстановление дефекта за счет формирования новообразованной костной ткани. Способ позволяет добиться контролируемого отверждения материала, обеспечить последующее заполнение критического дефекта новообразованной костной тканью и может быть применим в ветеринарной и медицинской практике.
Пример 1. Физико-механические свойства композиционного материала
Морфология поверхности полилактидных частиц была изучена с помощью сканирующего электронно-ионного микроскопа Versa 3D DualBeam (FEI, США) в режиме высокого вакуума с использованием IСЕ-детектора вторичных электронов. Результаты СЭМ анализа поверхности частиц, позволили подтвердить наличие многочисленных пор в структуре частиц. Пористость материала достигала 98%. Размер пор составлял от 2 до 20 мкм (фиг. 5).
Для установления влияния наполнителя и степени деацетилирования на реологическое поведение материалов получали суспензии и исследовали на ротационном вискозиметре Physica MCR 501 (AntonPaar, Австрия). В качестве измерительной системы были выбраны плоскость-плоскость с зазором от 1 до 1,1 мм. Измерения проводили в режиме амплитудной развертки для установления линейного диапазона вязкоупругих свойств, в режимах частотной и температурной развертки, а также в изотермическом режиме при 37°С.
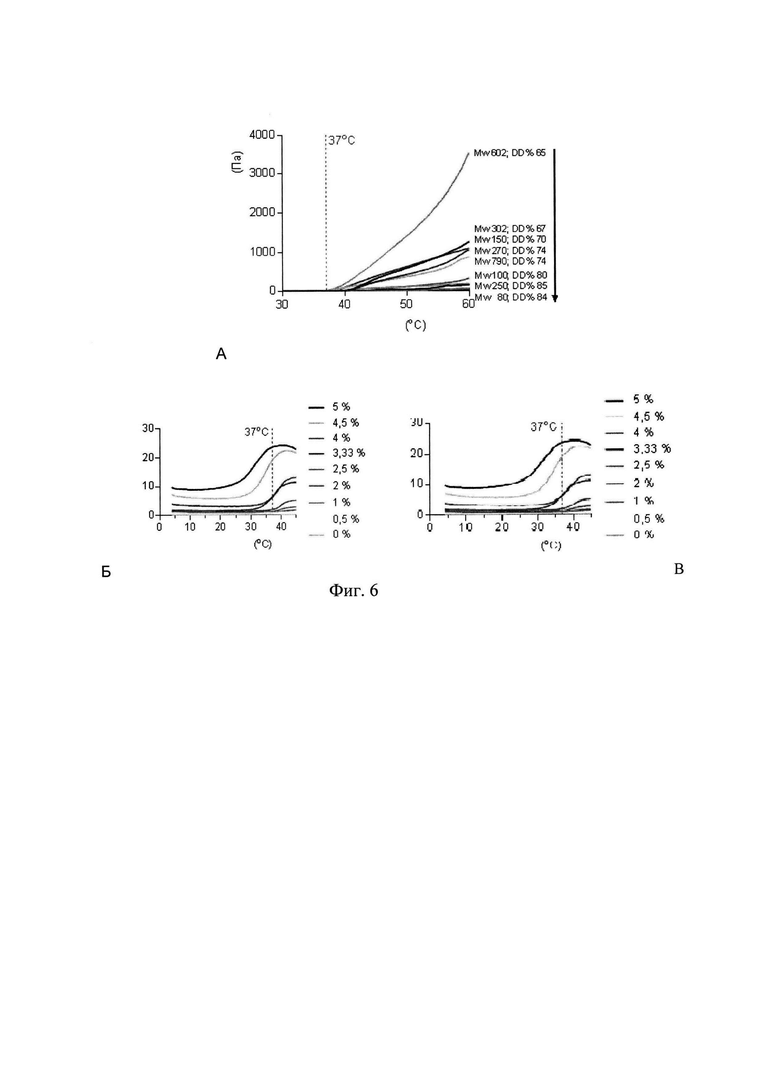
На амплитудной развертке для всех образцов наблюдается линейный участок вязкоупругих свойств (фиг. (А)). Для получения достоверных данных в последующих экспериментах была выбрана амплитуда 0,1%.
Как можно заметить, при 37°С для хитозана со степенью деацетилирования около 80% наблюдается значительное снижение модулей упругости по сравнению с ранее исследованными системами, несмотря на сохранение высокой молекулярной массы (фиг. (А)). Дальнейшее понижение степени деацетилирования хитозана приводит к драматическому снижению прочности гидрогелей и способности к гелеобразованию в системе хитозан-глицерофосфат (фиг. 6 (А)). Тем не менее, наполнение пористыми частицами даже до достаточно невысоких степеней позволяет значительно улучшить прочностные характеристики низкомодульных гидрогелей (Фиг. (Б, В)).
Пример 2. Определение динамики высвобождения rhBMP-2 из полилактидных и хитозановых частиц в условиях invitro
Для оценки динамики высвобождения rhBMP-2 из полилактидных и хитозановых частиц использовали набор для иммуноферментного анализа (ИФА) ELISA-BMP-2 (Sigma-Aldrich, США). 0,5 см3 полилактидных и хитозановых частиц помещали в полипропиленовые пробирки и добавляли к ним раствор фосфатно-солевого буфера (рН 7.4) (ПанЭко, Россия). Инкубацию проводили при плюс 37°С в течение 5 суток. После каждого срока соответствующие пробирки центрифугировали на 800 об/мин в течение 30 минут и собирали водный экстракт, который хранили при температуре минус 80°С. После окончания эксперимента производилось размораживание ранее собранных образцов. Работа набора ELISA-BMP-2 основана на твердофазном «сэндвич» - варианте ИФА. Моноклональные антитела к ВМР-2 адсорбированы на поверхности лунок микропланшета и при добавлении анализируемых образцов происходит связывание белка с иммобилизированными антителами.
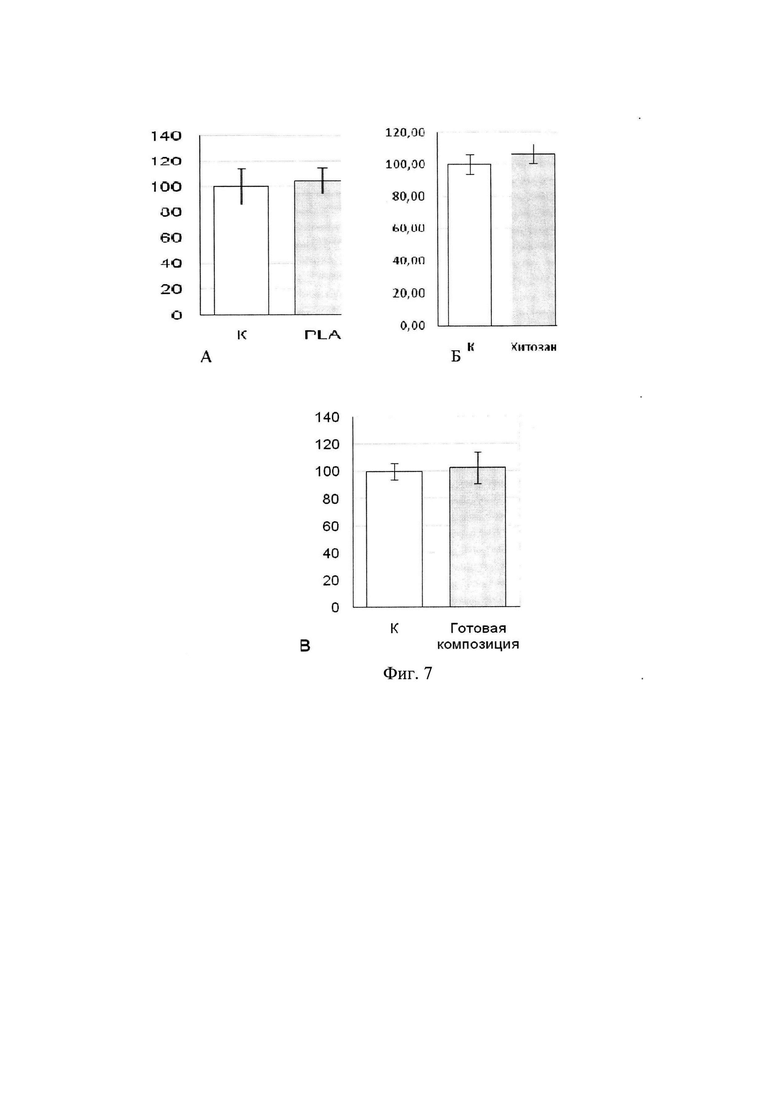
После вымывания несвязавшихся реагентов в лунки добавляли моноклональные антитела, специфичные к ВМР-2 и связанные с ферментом (пероксидазой хрена). После повторной промывки в лунки добавляли раствор субстрата пероксидазы хрена - тетраметилбензидина, что приводило к развитию цветной реакции. Реакцию останавливали стоп-реагентом (H2SO4). Оптическую плотность суспензии в лунках оценивали при длине волны 570 нм. Измерения проводили на планшетном ридере «AnthosReader 2020» («AnthosLabtec», Австрия). Для получения статистически значимой выборки эксперимент повторяли трижды. Частицы полилактида обеспечивали плавную кинетику высвобождения белка к окончанию 5 суток эксперимента, в то время как хитозановые частицы обладали слабой способностью к удержанию белка и высвобождали основной объем к третьим суткам эксперимента (фиг. 7).
Пример 3. Исследование цитотоксичности материала invitro
Исследование цитотоксических свойств компонентов материала проводили с помощью колориметрического МТТ-теста. К ММСК жировой ткани, культивируемым в лунках 24-луночного планшета, добавляли высокопористые полилактидные частицы (фиг. 7 (А)), хитозановые частицы массой 5 мг (фиг. 7 (Б)), губки хитозана с различной степенью деацетилирования массой 5 мг и композиционные материалы на основе хитозанового гидрогеля со степенью наполненности высокопористыми полилактидными частицами 12 масс. % объемом 1 мл (фиг. 7 (В)).
После инкубации в течение 1, 3 или 7 суток материалы удаляли, из лунок планшетов и вносили МТТ (Sigma-Aldrich, США) до конечной концентрации 0,5 мг/мл и инкубировали в течение 2 часов при 37°С. Кристаллы формазана экстрагировали из клеток с помощью диметилсульфоксида (ПанЭко, Россия). Поглощение формазана оценивали, измеряя оптическую плотность элюата при длине волны 570 нм на планшетном ридере «AnthosReader2020» (AnthosLabtec, Австрия). Результаты МТТ-теста показали, что как полилактидные, так и хитозановые частицы не оказывают значимого цитотоксического влияния на клетки на протяжение всего срока исследования. (оценка «О - нецитотоксичен» по шкале цитотоксичности в соответствии с ГОСТ Р ИСО 10993-5-2009).
Пример 4. Оценка биосовместимости материалов invivo
Исследование проводили на половозрелых самках крыс Wistar массой 300-350 г. Для наркотизации лабораторных животных использовали внутрибрюшинное введение Золетила (Virbac, Франция). Наркоз осуществляли путем внутрибрюшинного введения препаратов Золетил (Virbac, Франция) и Ксилазин (InterchemieWerken «deAdelaar» BV, Нидерланды) в дозировке 30 мг/кг и 5 мг/кг соответственно. Крысам сбривали шерсть в области холки, проводили антисептическую обработку, в стерильных условиях выполняли продольный разрез кожи и имплантировали исследуемые материалы после формирования тупым путем подкожных карманов. После рану ушивали узловыми швами.
Выведение животных из эксперимента проводили на 14 сут после операции. Область имплантации материала с окружающими мягкими тканями забирали с помощью ножниц. Полученные образцы фиксировали в 10% нейтральном растворе формалина и подвергали гистологическому исследованию.
Исследование хитозанов с различной степенью деацетилирования показало, что хитозаны со степенью деацетилирования 19% и 35% обладали минимальным воспалительным ответом на их имплантацию.
Композиция, состоящая из хитозанового гидрогеля с добавлением β-глицерофосфата и высокопористыми полилактидными частицами без rhBMP-2, при подкожной имплантации не вызывала воспалительный ответ, что свидетельствует о высокой биосовместимости разработанного материала.
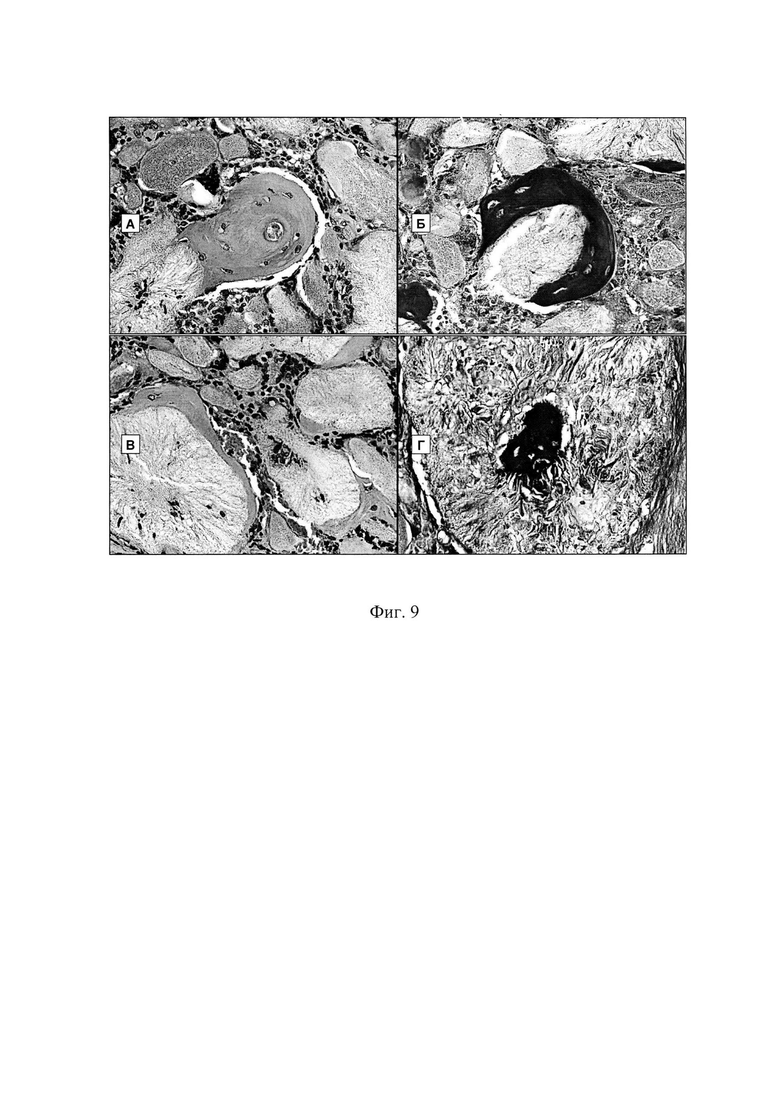
Основной объем хитозанового гидрогеля сохранялся на протяжение 7 суток, а затем к 14 суткам происходило существенное его снижение. Объем полилактидных частиц сохранялся в неизменном виде вплоть до 14 суток (фиг. 8 (А, Б, В, Г)). Кроме того, наблюдались очаги новообразованной костной ткани в области подкожной имплантации композиции на основе хитозанового гидрогеля и полилактидных частиц, импрегнированных rhBMP-2 (фиг. 9 (А, Б, В, Г)).
Пример 5. Оценка остеоиндуктивных свойств композиций
Оценку остеоиндуктивных свойств материалов проводили на моделях подкожной и внутрикостной имплантации, где оценивали регенерацию костной ткани в области критического дефекта теменных костей крыс.
Для наркотизации лабораторных животных использовали внутрибрюшинное введение Золетила (Virbac, Франция) Наркоз осуществляли путем внутрибрюшинного введения препаратов Золетил (Virbac, Франция) и Ксилазин (InterchemieWerken «deAdelaar» BV, Нидерланды) в дозировке 30 мг/кг и 5 мг/кг соответственно.
Подкожную имплантацию материала, содержащего хитозановый гидрогель и высокопористые полилактидныечастицы, импрегнированные rhBMP-2, проводили по ранее описанной методике.
Для внутрикостной имплантации крысам сбривали шерсть на голове, производили поперечный и вертикальный латерально-смещенный разрез кожи головы, формируя треугольный лоскут и последовательно тупым и острым путем обнажали теменные кости. Посередине сагиттального шва на теменных костях формировали круглое отверстие с помощью трепана C-reamer диаметром 5,5 мм и высотой 1,5 мм из набора Neobiotech SLA (Корея), избегая перфорации сагиттального венозного синуса. После этого в сформированный костный дефект вносили исследуемые материалы. Рану послойно ушивали. В экспериментальной группе животным имплантировали хитозановый гидрогель с высокопористыми полилактидными частицами, импрегнированными rhBMP-2, в группе контроля применяли композицию, не содержащую rhBMP-2. Животные были выведены из эксперимента с помощью передозировки Золетила на 28 сутки с целью выявления очагов первичного неоостеогенеза.
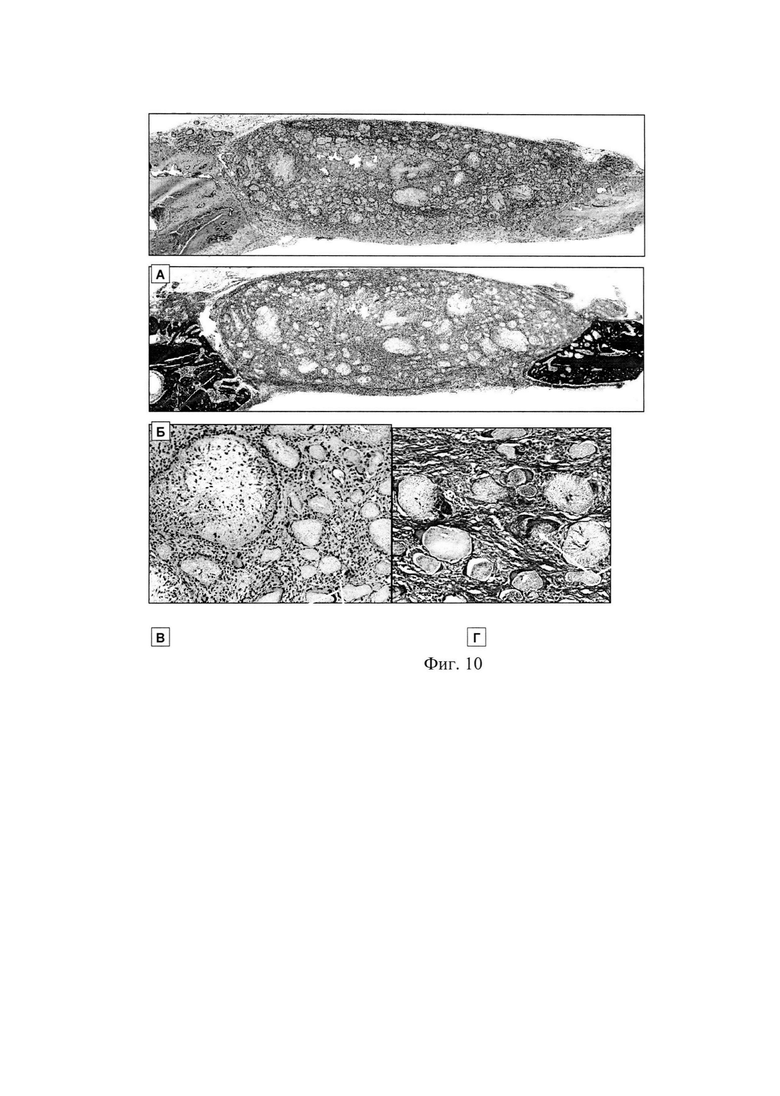
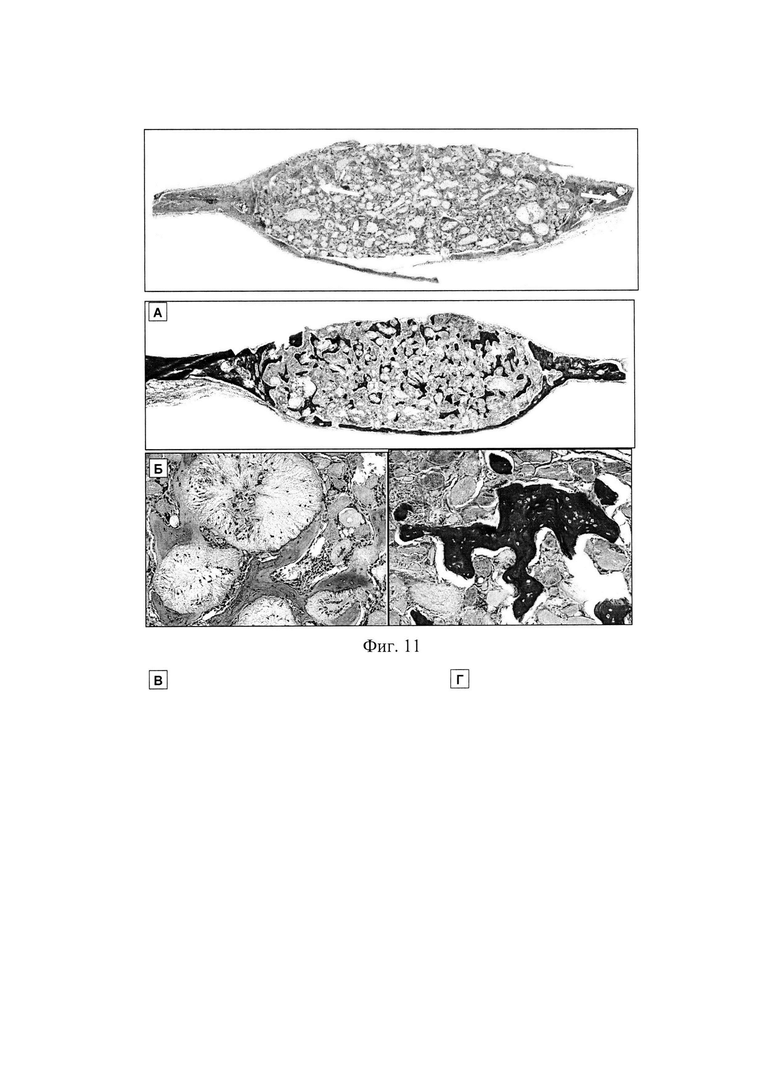
К 28 суткам во всех группах в области имплантации отсутствовали признаки воспалительной реакции (фиг. 10 (А, Б, В, Г), 11 (А, Б, В, Г)).
Хитозановый гидрогель подвергся резорбции, а его место занимали коллагеновые волокна. В контрольной группе очаги неоостеогенеза выявлены не были (фиг. 11 (А, Б, В, Г)). В экспериментальных группах, где была проведена подкожная и внутрикостная имплантация материалов, содержащих rhBMP-2, полилактидные частицы под действием гигантских клеток инородных тел резорбировались и замещались новообразованной костной тканью. Очаги неоостеогенеза были представлены в виде пластин, окружающих остатки частиц. Таким образом, можно заключить, что динамика резорбциии материала соответствовала скорости неоостеогенеза, что не должно приводить к существенному снижению объема материала после его замещения костью.
| название | год | авторы | номер документа |
|---|---|---|---|
| Композиция для восстановления дефектов костной ткани на основе аденовирусных конструкций, несущих кДНК ВМР-2, фибринового геля и синтетического β-трикальцийфосфата и способ ее получения | 2016 |
|
RU2620962C1 |
| ИМПЛАНТАТ ДЛЯ ЗАМЕЩЕНИЯ КОСТНОЙ ТКАНИ | 2019 |
|
RU2712701C1 |
| Жидкостный ин виво биореактор для выращивания костной ткани | 2021 |
|
RU2777947C1 |
| КОМПОЗИЦИЯ - ОСТЕОИНДУКТОР И ОСТЕОКОНДУКТОР, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ, И СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ - ОСТЕОИНДУКТОРА И ОСТЕОКОНДУКТОРА, ПРИ ЛЕЧЕНИИ КОСТНОЙ ПАТОЛОГИИ В СТОМАТОЛОГИИ И ЧЕЛЮСТНО-ЛИЦЕВОЙ ХИРУРГИИ | 2008 |
|
RU2383564C1 |
| ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ ИМПЛАНТАТА ДЛЯ ЗАМЕЩЕНИЯ КОСТНОЙ ТКАНИ | 2019 |
|
RU2708639C1 |
| ХИТОЗАНОВАЯ КОМПОЗИЦИЯ | 2008 |
|
RU2482133C2 |
| Способ получения средства для регенерации кости, содержащего рекомбинантный белок ВМР-2, и его применение | 2022 |
|
RU2781921C1 |
| СИСТЕМА И СПОСОБ МНОГОФАЗНОГО ВЫСВОБОЖДЕНИЯ ФАКТОРОВ РОСТА | 2012 |
|
RU2633057C2 |
| ИНЪЕЦИРУЕМЫЕ СТЕРЖНИ ИЗ ФОСФАТА КАЛЬЦИЯ ДЛЯ ДОСТАВКИ ОСТЕОГЕННЫХ БЕЛКОВ | 2004 |
|
RU2363478C2 |
| БИОРЕЗОРБИРУЕМЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ ДЛЯ РЕКОНСТРУКЦИИ КОСТНОЙ ТКАНИ | 2024 |
|
RU2834481C1 |






Настоящее изобретение относится к области медицины, а именно к способу применения композиции термоотверждаемого и остеоиндуктивного костно-пластического материала на основе композиции хитозанового гидрогеля и частиц из полилактида или хитозана с импрегнированным костным морфогенетическим белком-2 для замещения дефектов костей скелета, согласно изобретению заявленную композицию охлаждают до плюс 4°С и вносят в костный дефект, с экспозицией до 4-15 мин, после отверждения композиции рану послойно ушивают, для стимулирования первичного остеогенеза осуществляют экспозицию в зоне имплантации не менее 1 мес. Настоящее изобретение обеспечивает достижение равномерного распределения с последующим отверждением в ране, что в дальнейшем обеспечивает контролируемое полное восстановление дефекта за счет формирования новообразованной костной ткани. 11 ил., 5 пр.
Способ применения композиции термоотверждаемого и остеоиндуктивного костно-пластического материала на основе композиции хитозанового гидрогеля и частиц из полилактида или хитозана с импрегнированным костным морфогенетическим белком-2 для замещения дефектов костей скелета, отличающийся тем, что заявленную композицию охлаждают до плюс 4°С и вносят в костный дефект, с экспозицией до 4-15 мин, после отверждения композиции рану послойно ушивают, для стимулирования первичного остеогенеза осуществляют экспозицию в зоне имплантации не менее 1 мес.
| Кузнецова Валерия Сергеевна, Применение композиционного материала на основе хитозанового геля и полилактидов с импрегнированным rhBMP-2 для регенерации костной ткани (экспериментальное исследование), Дисс | |||
| канд | |||
| мед | |||
| наук | |||
| Москва, дата поступления в библиотеку: 14.04.2020 | |||
| A | |||
| V | |||
| Vasilyev et al., Comparison of Impregnated Bone Morphogenetic |
Авторы
Даты
2022-09-09—Публикация
2021-05-31—Подача